Определение авидности антител IgG к Toxoplasma gondii в лаборатории Lab4U со скидкой 50% в Москве
Описание анализа
Определение авидности антител IgG к Toxoplasma gondii проводится в случае положительных результатов исследования на IgM- и IgG-антител к Toxoplasma gondii для диагностики первичной (недавней) инфекции или реактивации инфекции.
В период до 18-20 недели после появления первых симптомов инфекции выявляется низкая авидность антител Ig G.
Исследование особенно показано беременным женщинам, у которых обнаружены Ig M и Ig G антитела к токсоплазме.
Метод исследования — Иммунохемилюминесцентный анализ (ИХЛА)
Материал для исследования — Сыворотка крови
Срок исполнения
Анализ будет готов в
течение 6 дней, исключая субботу, воскресенье и день забора. Срок может быть увеличен на 1 день в случае необходимости.
Вы получите результаты на эл. почту сразу по готовности.
Срок может быть увеличен на 1 день в случае необходимости.
Вы получите результаты на эл. почту сразу по готовности.
Как подготовиться
Заранее
Не сдавайте анализ крови сразу после рентгенографии, флюорографии, УЗИ, физиопроцедур.
Накануне
За 24 часа до взятия крови:
- Ограничьте жирную и жареную пищу, не принимайте алкоголь.
- Исключите тяжёлые физические нагрузки.
Не менее 8 часов до сдачи крови не принимайте пищу, пейте только чистую негазированную воду.
В день сдачи
Перед забором крови
- 60 минут не курить,
- 15-30 минут находиться в спокойном состоянии.

Результат
Пример результата анализа.pdfРасшифровка
Интерпретация результатов анализов носит информационный характер, не является диагнозом и не заменяет консультации врача. Референсные значения могут отличаться от указанных в зависимости от используемого оборудования, актуальные значения будут указаны на бланке результатов.
- индекс авидности менее 45% – низкая авидность (низкоавидные антитела)
- индекс авидности 45-50% — неопределённые значения
- индекс авидности более 50% – высокая авидность (высокоавидные антитела)
Низкий индекс авидности свидетельствует о первичной (недавней) инфекции.
Неопределённые значения авидности могут свидетельствовать о поздней стадии первичной инфекции или недавно перенесенной инфекции.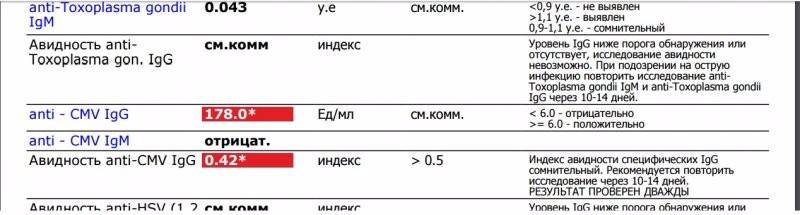 Исследование рекомендуется повторить (вместе с исследованием IgM- и IgG-антител) через 2-3 недели.
Исследование рекомендуется повторить (вместе с исследованием IgM- и IgG-антител) через 2-3 недели.
Высокий индекс авидности исключает первичную инфекцию, свидетельствует о вторичном иммунном ответе при реинфекции или обострении латентной инфекции.
Единица измерения: %
Гарантия качества
Исследование выполняет Иммунохимический анализатор Architect i2000sr фирмы Abbott Laboratories, США
Модульный анализатор, обеспечивающий превосходное качество анализов, выполняя анализы в любом порядке, в том числе одновременно, снижая общее время тестирования
Определение авидности антител IgG к Toxoplasma gondii
Токсоплазмоз – паразитарное заболевание человека и животных часто протекает бессимптомно. Источником инфекции являются домашние кошки, реже сырые или плохо обработанные мясо, молоко и яйца животных и птиц.
Токсоплазмоз представляет собой серьезнейшую опасность при первичном заражении женщины во время беременности. Врожденный токсоплазмоз у ребенка проявляется тяжелым поражением нервной системы, выраженной умственной отсталостью, патологией глаз и других органов.
В связи с этим женщинам, планирующим беременность, а также беременным при их первичном обращении к врачу необходимо провести исследование на токсоплазмоз. IgM-антитела выявляются у женщин, недавно перенёсших инфекцию, однако IgM-антитела могут выявляться в крови в течение 18 месяцев после перенесённой инфекции. В случаях когда одновременно в крови обнаруживаются IgM- и IgG-антитела, необходимо отличить первичную инфекцию и обострение, так как первичная инфекция ведёт к тяжёлым последствиям для плода.
IgG-антитела в процессе развития иммунного ответа постепенно увеличивают прочность связывания с инфекционным агентом. Эту прочность связывания называют авидностью. В самом начале заболевания связывание IgG-антителами возбудителя достаточно слабое. Выявление низкоавидных IgG-антител свидетельствует о первичной (недавней) инфекции, наличие же высокоавидных IgG-антител говорит о вторичном иммунном ответе в случае реинфицирования или реактивации инфекции.
Эту прочность связывания называют авидностью. В самом начале заболевания связывание IgG-антителами возбудителя достаточно слабое. Выявление низкоавидных IgG-антител свидетельствует о первичной (недавней) инфекции, наличие же высокоавидных IgG-антител говорит о вторичном иммунном ответе в случае реинфицирования или реактивации инфекции.
Определение авидности IgG к Toxoplasma gondii (токсоплазмоз) в сыворотке крови методом иммунохемилюминисценции
Toxoplasma gondii (T. gondii) один из представителей внутриклеточных паразитов. Токсоплазмоз – это заболевание, характеризующееся хроническим или острым течением с поражением нервной системы, печени, селезенки, лимфатических узлов, скелетных мышц, миокарда. Как известно, токсоплазмоз входит в группу TORCH-инфекций, являющихся потенциально опасными для развития плода и вызывающих тяжелые поражения органов у новорожденных детей.
Авидность (лат. — avidity) — это степень прочности связывания молекулы антитела с молекулой антигена.
Первичный иммунный ответ на ранее не встречаемые организмом антигены начинается с продукции IgM. IgG — это поздние антитела, при первичном иммунном ответе они сменяют ранние антитела IgM и накапливаются в организме в значительно больших количествах. IgG обладают наиболее высокой авидностью.
Анализ крови включает в себя определение антител, образующихся в организме в ответ на проникновение токсоплазмы. Об острой фазе заболевания говорит наличие антител IgM. Но срок их присутствия в организме длится от нескольких недель до месяцев. Нарастание уровня IgG происходит в течение нескольких недель. При этом вначале образуются низкоафинные (с низкой степенью сродства) антитела, образующиеся в начале иммунного ответа при размножении вируса в организме и сохраняющиеся в течение 1-1,5 мес. от начала заболевания. Позже, в процессе созревания иммунного ответа, в организме появляются высокоафинные IgG антитела. Высокоафинные антитела остаются в организме длительное время. За счет этих антител развивается быстрый вторичный иммунный ответ в случае повторного попадания возбудителя в организм. В случае латентной инфекции в крови обнаруживаются IgM при обострении или реактивации инфекционного процесса.
За счет этих антител развивается быстрый вторичный иммунный ответ в случае повторного попадания возбудителя в организм. В случае латентной инфекции в крови обнаруживаются IgM при обострении или реактивации инфекционного процесса.
В случаях, когда обнаруживаются IgM в крови, необходимо разделять первичную инфекцию и обострение, так как первичная инфекция у беременных женщин ведет к тяжелым последствиям для плода. Кроме того, различаются схемы лечения первичной и латентной инфекций. Для этого рекомендуется определять авидность антител IgG. Если в крови при наличии IgM обнаруживаются IgG с низкой авидностью, то это свидетельствует о первичной (недавней) инфекции. Наличие же высокоавидных антител IgG (в присутствии IgM) говорит о вторичном иммунном ответе в случае попадания возбудителя в организм или обострения (реактивации).
Таким образом, определение авидности антител к данному возбудителю позволяет выделить первичную инфекцию, дифференцировать ее от периода реактивации или вторичного проникновения антигена в организм.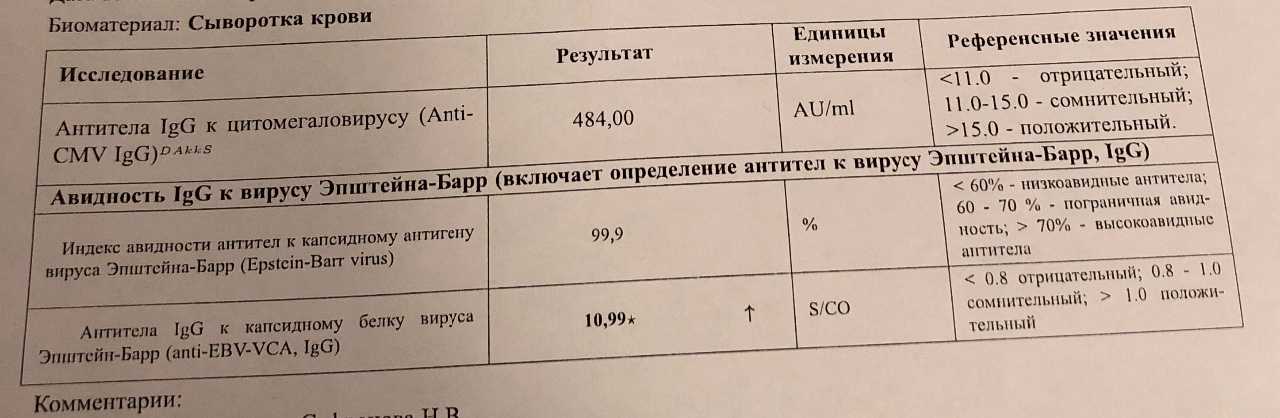
Использование авидности IgG-антител в качестве индикатора срока первичного инфицирования, впервые предложенное финскими исследователями (Hedman K. M. с соавт.,1989).
Выявление в сыворотке присутствия одновременно IgG- и IgM-антител к инфекционному агенту можно трактовать как свидетельство недавнего первичного инфицирования, поскольку, как известно, срок исчезновения Ig M-антител обычно составляет около 3 месяцев от начала инфекционного процесса. Но период циркуляции Ig M антител может значительно варьировать в зависимости от инфекционного возбудителя и индивидуальных особенностей иммунного ответа организма. При инфицировании Toxoplasma gondii, следовые количества IgM-антител к этим инфекционным агентам в некоторых случаях выявляются в течение 1 — 2 и более лет.
CDC — Токсоплазмоз — Ресурсы для медицинских работников
- Диагностика
- Лечение
Диагноз токсоплазмоза обычно ставится путем обнаружения Toxoplasma -специфических антител IgG, IgM, IgA или IgE. Существует несколько доступных тестов, которые обнаруживают эти иммуноглобулиновые антитела в течение нескольких недель после заражения:
Существует несколько доступных тестов, которые обнаруживают эти иммуноглобулиновые антитела в течение нескольких недель после заражения:
- Тест с красителем (DT)
- Непрямой флуоресцентный тест на антитела (IFA)
- Иммуноферментные анализы (ИФА, иммуноблоты)
- Реакция агглютинации
- Тест на авидность
При подозрении на острую инфекцию сыворотку пациента следует проверить на наличие специфических антител IgG и IgM Toxoplasma . Некоторые серологические тесты доступны в коммерческих лабораториях. Однако из-за трудностей, присущих диагностике острого токсоплазмоза, врачам рекомендуется пройти подтверждающее тестирование в справочной лаборатории Медицинского фонда Пало-Альто / Лаборатории специальной диагностики Джека С. Ремингтона.
Для получения дополнительной информации: http://www.pamf.org/serology/
Серологические тесты иногда ненадежны у пациентов с иммуносупрессией. Из-за персистенции цист Toxoplasma и антител при бессимптомных хронических латентных инфекциях у лиц с иммунодефицитом и положительными результатами ПЦР и серологических исследований результаты диагностических тестов следует интерпретировать в связи с клиническими признаками активной инфекции. Отрицательный ПЦР не исключает активной инфекции. ПЦР также можно проводить на амниотической жидкости, что может помочь в определении инфекции плода после острой приобретенной инфекции у матери.
Отрицательный ПЦР не исключает активной инфекции. ПЦР также можно проводить на амниотической жидкости, что может помочь в определении инфекции плода после острой приобретенной инфекции у матери.
Диагноз можно поставить путем непосредственного обнаружения паразита в окрашенных срезах тканей, спинномозговой жидкости (ЦСЖ) или другом материале биопсии. Эти методы используются реже из-за сложности получения этих образцов. Паразитов также можно выделить из крови или других жидкостей организма (например, ЦСЖ), но этот процесс может быть сложным и требует значительного времени.
Болезнь глаз диагностируется главным образом при осмотре глаз.
Рекомендуемые в настоящее время препараты для лечения токсоплазмоза нацелены на тахизоитную стадию паразита и не уничтожают инцистированных паразитов в тканях. Пириметамин, считающийся наиболее эффективным препаратом против токсоплазмоза, является стандартным компонентом терапии. Пириметамин является антагонистом фолиевой кислоты и может вызывать дозозависимую супрессию костного мозга, которая смягчается одновременным введением фолиновой кислоты (лейковорин).
Лечение иммунокомпетентных взрослых с лимфоаденопатическим токсоплазмозом показано редко; эта форма заболевания обычно самокупируется. Если заболевание внутренних органов клинически очевидно или симптомы тяжелые или стойкие, может быть показано лечение в течение 2–4 недель.
Лечение заболеваний глаз должно основываться на полном офтальмологическом обследовании.
- Взрослые: пириметамин 100 мг в течение 1 дня в качестве ударной дозы, затем 25–50 мг в день плюс сульфадиазин 2–4 г в день в течение 2 дней, затем от 500 мг до 1 г четыре раза в день плюс фолиновая кислота (лейковорин) 5-25 мг с каждой дозой пириметамина;
- Детская доза: пириметамин 2 мг/кг в первый день, затем 1 мг/кг каждый день плюс сульфадиазин 50 мг/кг два раза в день плюс фолиновая кислота (лейковорин) 7,5 мг в день)
- Терапию следует проводить в течение 4–6 недель с последующей повторной оценкой состояния пациента. (См.: de-la-Torre A, Stanford M, Curi A, Jaffe GJ, Gomez-Marin JE. Терапия глазного токсоплазмоза. Ocul Immunol Inflamm. 2011; 19:314-20.) Кортикостероиды иногда назначают в дополнение к противопаразитарным препаратам.
 агенты.
агенты.
Лечение инфекций матери и плода зависит от лечебного центра. В целом, спирамицин рекомендуется женщинам, у которых инфекция была приобретена и диагностирована до 18 недель беременности, а инфекция плода не документирована или не подозревается. Спирамицин уменьшает передачу инфекции плоду и наиболее эффективен, если его начать в течение 8 недель после сероконверсии. Спирамицин можно получить в Управлении по санитарному надзору за качеством пищевых продуктов и медикаментов США по телефону 301-796-1400. Пириметамин, сульфадиазин и лейковорин рекомендуются при инфекциях, приобретенных на 18-й неделе беременности или после нее, или при подтвержденной или предполагаемой инфекции у плода. ПЦР часто проводят на амниотической жидкости на 18-й неделе беременности, чтобы определить, инфицирован ли ребенок.
Для получения дополнительной информации о лечении токсоплазмоза у беременных см. Montoya JG, Remington JS. Лечение инфекции Toxoplasma gondii во время беременности. Clin Infect Dis 2008; 47:554-566 и Maldonado YA, Read JS, Комитет AAP по инфекционным заболеваниям. Диагностика, лечение и профилактика врожденного токсоплазмоза в США. Педиатрия . 2017;139(2):e20163860.
Clin Infect Dis 2008; 47:554-566 и Maldonado YA, Read JS, Комитет AAP по инфекционным заболеваниям. Диагностика, лечение и профилактика врожденного токсоплазмоза в США. Педиатрия . 2017;139(2):e20163860.
Новорожденных с врожденной инфекцией обычно лечат пириметамином, сульфонамидом и лейковорином в течение 12 месяцев. Рекомендации Национальной референс-лаборатории токсоплазмоза (PAMF-TSL) и Центра токсоплазмоза Чикагского университета по лечению врожденно инфицированных детей:
- Пириметамин: 2 мг/кг в день перорально, два раза в день в течение первых 2 дней; затем с 3-го дня до 2-х месяцев (или 6 месяцев при наличии симптомов) по 1 мг/кг в день, перорально, каждый день; затем по 1 мг/кг в день внутрь 3 раза в неделю
- Сульфадиазин: 100 мг/кг в день, перорально, два раза в день
- Фолиновая кислота (лейковорин): 10 мг 3 раза в неделю
- См. Maldonado YA, Read JS, Комитет AAP по инфекционным заболеваниям. Диагностика, лечение и профилактика врожденного токсоплазмоза в США.
 Педиатрия . 2017;139(2):e20163860.
Педиатрия . 2017;139(2):e20163860.
Токсоплазмоз у пациентов с иммунодефицитом часто приводит к летальному исходу, если его не лечить. Лечение рекомендуется в течение как минимум 4-6 недель после исчезновения всех клинических признаков и симптомов, но может потребоваться и в течение 6 месяцев или дольше. Известно, что у больных СПИДом случаются рецидивы, поэтому рекомендуется поддерживающая терапия до тех пор, пока не будет достигнуто значительное иммунологическое улучшение в ответ на антиретровирусную терапию. Пириметамин, фолиновая кислота (лейковорин) и сульфадиазин являются стандартами терапии для пациентов с иммунодефицитом. Для получения дополнительной информации см. Рекомендации по профилактике и лечению оппортунистических инфекций у ВИЧ-инфицированных взрослых и подростков и Рекомендации по профилактике и лечению оппортунистических инфекций среди ВИЧ-инфицированных и ВИЧ-инфицированных детей.
Ссылки по теме
- CDC MMWR : Профилактика врожденного токсоплазмоза
- Maldonado YA, Read JS, Комитет AAP по инфекционным заболеваниям.
 Диагностика, лечение и профилактика врожденного токсоплазмоза в США. Педиатрия . 2017;139(2):e20163860
Диагностика, лечение и профилактика врожденного токсоплазмоза в США. Педиатрия . 2017;139(2):e20163860 - Монтойя Дж. Г., Лизенфельд О. Токсоплазмоз. Ланцет . 2004 г., 12 июня; 363: 1965–1976.
Чтобы получить доступ к этой статье в Интернете через Lancet, вы должны либо быть подписчиком, либо выбрать вариант с оплатой за просмотр. - CDC: Информационные бюллетени по токсоплазмозу
Эта информация предоставляется в качестве информационного ресурса для лицензированных поставщиков медицинских услуг только в качестве руководства. Он не предназначен для замены профессионального суждения.
Триметоприм-сульфаметоксазол
Триметоприм-сульфаметоксазол (TMP-SMX) относится к категории беременности C. TMP-SMX следует использовать во время беременности, только если потенциальная польза оправдывает потенциальный риск для плода. TMP-SMX следует избегать в ближайшее время из-за возможности гипербилирубинемии и ядерной желтухи у новорожденных.
Беременность Категория C: Либо исследования на животных выявили неблагоприятное воздействие на плод (тератогенное, эмбриоцидное или другое), и отсутствуют контролируемые исследования на женщинах, либо исследования на женщинах и животных недоступны. Лекарства следует назначать только в том случае, если потенциальная польза оправдывает потенциальный риск для плода.
Триметоприм-сульфаметоксазол (TMP-SMX) выделяется с грудным молоком. TMP-SMX обычно совместима с грудным вскармливанием здоровых доношенных детей после периода новорожденности. Тем не менее, женщины обычно должны избегать приема TMP-SMX при кормлении недоношенных детей, детей с желтухой, больных или находящихся в состоянии стресса, или с дефицитом глюкозо-6-фосфатдегидрогеназы.
Безопасность триметоприма-сульфаметоксазола (ТМП-СМХ) у детей систематически не оценивалась. Использование у детей младше 2 месяцев, как правило, не рекомендуется.
ПАТОГЕНЕЗ, ДИАГНОСТИКА И ЛЕЧЕНИЕ ТОКСОПЛАЗМОЗА | Юлиавати
Чахая (2003). Эпидемиология «Toxoplasma Gondii». Bagian kesehatan lingkungan FakultasKesehatan Masyarakat Universitas Sumatera Utara, hlm 1–13.
Эпидемиология «Toxoplasma Gondii». Bagian kesehatan lingkungan FakultasKesehatan Masyarakat Universitas Sumatera Utara, hlm 1–13.
Хокелек М (2009 г.). токсоплазмоз. Доступно по адресу: http://www. emedicine.medscape.com/article/229969. Дата обращения: 6 февраля 2010 г.
Николь К. и Мансо Л. (1908). Sur une инфекции корпус де Лейшман (или организмы voisins) дю Гонди. CR Seances Acad. наук, 147: 763–766.
Йеллита (2004 г.). Mekanisme interaksi Toxoplasma gondii dengan sel host. Pengantar falsafah sains Institut Pertanian Bogor, зал 1–12
Демар М., Айзенберг Д., Мобон Д., Джоссу Ф., Панчо Д., Пунваси Д. (2007). Эпидемиологические, клинические и паразитологические аспекты фатальной вспышки токсопламоза человека вдоль реки Махони. Клин Инфект Дис, 45: e88–95.
Уэри П. (2008 г.). Патогенез токсопламоза и иммунный ответ. Медицинский журнал Таммасат, 8: 487–95.
Беккер Дж., Сингх Д., Синерт Р.Х. (2010). токсоплазмоз. Доступно по адресу: http://www. emedicine.medscape.com/article/787505. По состоянию на 28 октября 2010 г.
emedicine.medscape.com/article/787505. По состоянию на 28 октября 2010 г.
Subauste C (2006 г.). Токсоплазмоз и ВИЧ в главе базы знаний HIV inSite. UCSF HIV inSite, стр. 1–13.
Монтойя Дж. Г. (2002 г.). Лабораторная диагностика инфекции Toxoplasma gondii и токсоплазмоза. J Infect Dis, 185: S73–82.
Mechain B, Garin YJ, Camel JD, Gangneun FR, Derouin F (2000). Недостаточная полезность авидности специфических антител иммуноглобулина G для серодиагностики реактивированного токсоплазмоза у пациентов с ослабленным иммунитетом. Clin Diagn Lab Immunol, 7: 703–05.
Монтойя Дж. Г., Лизенфельд О. (2004 г.). токсоплазмоз. Ланцет, 363:
–76.
Марколино П., Сильва Д.А., Лезер П.Г., Камарго М.Е., Минео Дж.Р. (2000). Молекулярные маркеры острой и хронической фаз токсопламоза человека: определение авидности иммуноглобулина G методом вестерн-блоттинга. Clin Diagn Lab Immunol, 7: 384–89.
Жарро П. (2010 г.). Серологический ответ на паразитарные и грибковые инфекции в клинической иммунологии, серология с лабораторной точки зрения, под ред. Stevens CD, FA Davis Company USA, стр. 328–40.
Stevens CD, FA Davis Company USA, стр. 328–40.
Уилсон М., Шанц П.М., Натман П., Цанг В.К. (2002). Клиническая иммунопаразитология в Руководстве по клинической лабораторной иммунологии 6-е изд. Эдс Роуз Н.Р., Гамильтон Р.Г., ASM Press, Вашингтон, округ Колумбия, стр. 547–57.
Уокер М., Зунт-младший (2005 г.). Паразитарные инфекции центральной нервной системы у хозяев с ослабленным иммунитетом. Clin infect Dis, 40: 1005–15.
Идальго Х.Ф., Булабуа К.Е., Пинчарт М.П., Хамидфар Р., Гарбан Ф. (2008).
Диагностика токсоплазмоза после аллогенной трансплантации стволовых клеток: результаты обнаружения ДНК и серологические методы. Clin Infect Dis, 49: e9–15
Беланже Ф., Деруин Ф., Керос Л.Г., Мейер Л. (1999). Заболеваемость и фактор риска токсоплазмоза в когорте пациентов, инфицированных вирусом иммунодефицита человека, 1988-1995 гг. Clin Infect Dis, 575–81.
Антинори А., Ларусса Д., Чинголани А., Лоренцини П., Боссоласко С., Финацци М.Г. (2004). Распространенность, ассоциированные факторы и прогностические детерминанты токсоплазматического энцефалита, связанного со СПИДом, в эпоху передовой высокоактивной антиретровирусной терапии. Клин заражает Диса, 39 лет: 1681–91.
Распространенность, ассоциированные факторы и прогностические детерминанты токсоплазматического энцефалита, связанного со СПИДом, в эпоху передовой высокоактивной антиретровирусной терапии. Клин заражает Диса, 39 лет: 1681–91.
Рибера Э., Сола А.Ф., Жюст К., Ровира А., Ромеро Ф.Дж., Гил Л.А., Руис И. (1999). Сравнение высоких и низких доз триметопримсульфаметоксазола для первичной профилактики токсоплазматического энцефалита у пациентов, инфицированных вирусом иммунодефицита человека. Clin infect Dis, 29: 1461–1466.
Дьякович О.Д., Миленкович В., Николич А., Бобич Б., Груйич Дж. (2002). Эффективность атоваквона в сочетании с клиндамицином против инфицирования мышей цистогенным (Me49) штаммом Toxoplasma gondii. Дж. Антимикроб Chemother, 50:981–987.
Каплан Дж. Э., Холмс К. Х., Мазур Х. (2002). Руководство по профилактике оппортунистических инфекций среди ВИЧ-инфицированных, рекомендация Службы общественного здравоохранения США и Американского общества инфекционистов.


 агенты.
агенты. Педиатрия . 2017;139(2):e20163860.
Педиатрия . 2017;139(2):e20163860. Диагностика, лечение и профилактика врожденного токсоплазмоза в США. Педиатрия . 2017;139(2):e20163860
Диагностика, лечение и профилактика врожденного токсоплазмоза в США. Педиатрия . 2017;139(2):e20163860