Механизм действия бактериофагов, как это работает. Фагочувствительность
открытие пенициллина – первого антибиотика природного происхождения, воспринималось поначалу как шанс раз и навсегда победить инфекционные заболевания, уносившие миллионы жизней. Однако во второй половине прошлого века первоначальная эйфория пошла на убыль: выяснилось, что бактерии благодаря мутациям могут приобретать устойчивость к любому антибиотику и даже обмениваться между собой этими генами. Так началась «гонка вооружений» человека и бактерий.
Между препаратами бактериофагов и химическими антибиотиками существует принципиальное различие: антибиотик, в отличие от фагового препарата, убивает всё на своем пути, включая содружество полезных микроскопических обитателей организма.
Cовместная эволюция бактерий и фагов за последние 3 миллиарда лет привела к тому, что практически для любой болезнетворной бактерии имеется соответствующий вирус-«убийца».
В отличие от обычных антибиотиков, бактериофаги модифицируют свои генетические программы сами, что снимает проблему устойчивости.
Процесс уничтожения бактериальной клетки бактериофагом включает в себя несколько строго запрограммированных шагов.
Действие бактериофагов
Очень важным является то, что бактериофаги не трогают не «свои» бактерии, поэтому не вызывают гибель «хорошей» микрофлоры и, конечно, абсолютно безопасны для клеток высших организмов, включая человека.
При фаготерапии отсутствуют побочные эффекты, такие как аллергия, дисбактериоз, вторичные инфекции (например, грибковые), что нередко наблюдается при приеме антибиотиков. Бактериофаги могут применяться в комбинированной терапии с любыми лекарственными препаратами, включая антибиотики.
Препараты бактериофагов представляют собой раствор, используют их либо местно (например, на кожу или слизистые), либо принимают внутрь. В организме бактериофаги концентрируются в местах наибольшего поражения и размножаются до тех пор, пока находят бактерии-«мишени». После того, как бактерии-«мишени» закончились, фаги выводятся из организма.
После того, как бактерии-«мишени» закончились, фаги выводятся из организма.
Главная цель фаготерапии – остановить и повернуть вспять инфекционный процесс, чтобы дать иммунной системе организма возможность справиться с болезнью.
С помощью бактериофагов лечат
| |
| |
| |
| Гнойно-воспалительные заболевания кожи и слизистых | Внутрибольничные инфекции |
В идеальном случае перед началом лечения у конкретного больного следует выделить болезнетворную бактерию в культуру и подобрать бактериофаг из «коллекции» уже известных бактериальных вирусов.
Препараты бактериофагов трудно поддаются стандартизации из-за специфики производства. Даже опытный специалист не всегда может заранее предсказать эффективность того или иного препарата у конкретного пациента, так как разные бактериальные штаммы бактерий могут вызывать схожие проявления болезни. Выход – производство «коктейлей» из фагов, способных убивать разные штаммы и даже виды возбудителей. И такие препараты уже существуют — это комплексные, или поливалентные препараты бактериофагов
6 этапов работы бактериофагов
Условные обозначения
Бактерия
ДНК бактерии
Бактериофаг
ДНК фага
Адсорбция бактериофагов на бактериальных клетках
Специальные элементы фага, расположенные на поверхности в виде фибрилл или шипов, связываются со специфичными поверхностными молекулами — рецепторами на своей жертве — бактерии. Пока бактериофаг достаточно плотно не закрепится на поверхности бактерии, следующей стадии не происходит. Так как существует специальная система блокировки.
Пока бактериофаг достаточно плотно не закрепится на поверхности бактерии, следующей стадии не происходит. Так как существует специальная система блокировки.
Инъекция нуклеиновой кислоты бактериофага внутрь клетки
После плотного прикрепления фага (адсорбции) происходит внедрение генетического материала бактериофага в тело бактерии. Для этого в структуре фага природа предусмотрела наличие специальных структур, которые действуют по типу шприца. Именно за счет этого фаг как бы делает инъекцию, растворяет оболочку и вводит свой генетический материал в бактерию. Для этого у фага есть агрессивный фермент для прокалывания бактерии.
Сборка фаговых частиц
Сборка молодых фагов начинается с упаковывания генетического материала в икосаэдрические белковые оболочки. Далее к фагам присоединяется хвост, на головке фага появляются различные, необходимые для его жизнедеятельности белки. Количество молодых фагов внутри бактерии возрастает. Новое поколение готовится к выходу из бактериальной клетки.
Репликация копий нуклеиновой кислоты бактериофага
Когда ДНК фага попадает в бактерию она может раствориться ферментами бактерии. Однако фаг защищает свою ДНК специальными липкими белками, которые замыкают молекулу в кольцо, делая ее неуязвимой. Далее происходит тиражирование генетического материала (ДНК) фага прямо в клетке бактерии.
Синтез белковых и нуклеиновых частиц
После заражения бактерии начинается перестройка клеточного метаболизма под нужды фага: разрушаются некоторые клеточные белки. Далее происходит включение генетического материала фага в метаболизм бактерии и начинается сборка новых, молодых фагов.
Выход зрелых фагов и смерть бактерии
Финал жизненного цикла фага — клеточный лизис. Молодые фаги используют для разрушения бактериальной клетки набор ферментов, которые расщепляют оболочки бактерий (лизины), и белков, создающих поры во внутренней мембране бактерии и обеспечивающих ускорение действия фермента лизина.
Противопоказания
Только индивидуальная непереносимость.
С клинической точки зрения фаги достаточно безопасны, поскольку люди с рождения встречаться с ними. Фаги – это постоянные спутники организма, они были обнаружены в желудочно кишечном тракте, коже, моче, во рту, где они содержаться в слюне. Бактериофаги являются безопасной альтернативой антибиотикам.
Сравнение профилактического и терапевтического использования фагов и антибиотиков
Бактериофаги
Антибиотики
Воздействие на бактерии
Фаги эффективно убивают чувствительные клетки бактерий (их действие бактерицидное).
Некоторые антибиотики (например, хлорамфеникол) бактериостатические; они скорее ингибируют рост бактерий, чем убивают клетки.
Селективность действия
Высокая селективность бактериофагов позволяет нацеливаться на специфичных патогенов, не затрагивая нормальную бактериальную флору (например, маловероятно, что фаги будут враждебны по отношению к нормофлоре пациентов).
Антибиотики атакуют не только бактерий – возбудителей заболеваний, но также все чувствительные микроорганизмы, включая нормальную – и часто полезную – микрофлору хозяина. Поэтому их неселективное действие нарушает микробный баланс в организме пациента, что может привести к различным побочным эффектам.
Побочные эффекты
Незначительные побочные эффекты при применении лечебных фагов (могут быть вызваны высвобождением эндотоксинов из бактерий, лизированных in vivo фагами).
Для антибиотиков характерно множество побочных эффектов, включая кишечные расстройства, аллергии и вторичные инфекции (например, грибковые инфекции).
Разработка новых препаратов
Естественная коэволюция бактерий и фагов может облегчить получение новых литических фагов против фагоустойчивых бактерий, появляющихся в результате действия других фагов или естественных изменений в бактериальных популяциях.
Создание новых антибиотиков (например, против антибиотикоустойчивых бактерий) требует временных затрат и может занять много лет.
Устойчивость бактерий к действию препарата
Из-за специфичности фагов маловероятно появление устойчивости у других бактериальных видов, не являющихся мишенями терапии.
Из-за широкого спектра активности антибиотики могут приводить к отбору устойчивых мутантов многих видов бактерий, а не только у штаммов мишени.
Применение препарата
Из-за специфичности фагов их успешное использование для предупреждения и лечения бактериальных инфекций требует идентификации этиологического агента и определения его фагочувствительности к препарату in vivo перед началом фагового лечения.
Эмпирически назначенные до идентификации этиологического агента антибиотики с большей вероятностью будут эффективны нежели фаговые препараты.
Бактериофаги. Безопасные антибактериальные препараты. Эффективная альтернатива антибиотикам
Бактериофаги. Безопасные антибактериальные препараты. Эффективная альтернатива антибиотикамsection-container news-container
что такое бактериофаги
Бактериофаги — современные антимикробные препараты природного происхождения. Это микроорганизмы, способные точечно уничтожать только болезнетворные бактерии. Бактериофаги используются в профилактике и антибактериальной терапии заболеваний, возбудителями которых являются патогенные бактерии.
Это микроорганизмы, способные точечно уничтожать только болезнетворные бактерии. Бактериофаги используются в профилактике и антибактериальной терапии заболеваний, возбудителями которых являются патогенные бактерии.
в природе
- Присутствуют повсюду в нашем мире — в океане, почве, глубоководных источниках, питьевой воде и пище.
- Самая распространённая форма жизни на Земле; в биосфере содержится от 1030 до 1032 фаговых частиц.
- Старейшие из известных микроорганизмов — их возраст оценивают примерно в 3 миллиарда лет.
- Играют ключевую роль в поддержании баланса всех исследованных человеком экосистем.
- Контролируют количество микробной флоры и сдерживают её патологический рост.
- История применения бактериофагов насчитывает более 100 лет. Мировое врачебное и научное сообщество активно исследует фаги в качестве антимикробных агентов.

- Биотехнологи научились создавать медицинские антибактериальные препараты на основе бактериофагов и применять их для лечения пациентов.
- Современная медицина позволяет использовать бактериофаговую терапию против большинства бактериальных инфекций.
12345678
Строение бактериофага
Ниже расположен хвостовой отросток , состоящий из внутреннего стержня и сократительного чехла.
Передвигается бактериофаг с помощью ножек-фибрилл, скреплённых в центре базальной пластиной. Размер бактериофага в сотни и тысячи раз меньше микробных клеток.
Факты о бактериофагах
Бактериофаги – антибактериальные агенты и природные антисептики
Безопасны и нетоксичны, побочные эффекты редки, применяются у новорождённых детей, беременных и кормящих женщин
Действие бактериофагов не затрагивает полезную микрофлору организма, в отличие от антибиотиков
Бактериофаги совместимы со всеми лекарственными препаратами. Применение бактериофагов не ограничивает использование других лекарств и не влияет на их эффективность
Применение бактериофагов не ограничивает использование других лекарств и не влияет на их эффективность
Воздействует лишь на чувствительные к ним болезнетворные бактерии, вызывающие инфекционное заболевание, разрушая их изнутри
Бактериофаги выводятся из организма естественным путем
Как работают бактериофаги
Бактериофаги (от лат. phagos — пожирающий бактерии) — особые вирусы, которые способны размножаться только в присутствии определенного вида болезнетворных бактерий. Бактериофаги воспроизводят себе подобных только за счёт бактерий. Но человеку эта особенность только на руку: бактериофаг питается клетками вредных бактерий и полностью разрушает их.
6
этаповработы
бактериофагов
1
Прикрепление бактериофагов
на бактериальных клетках
2
Инъекция нуклеиновой кислоты бактериофага внутрь бактерии
3
Синтез белковых и нуклеиновых компонентов бактериофагов
4
Соединение белковых и нуклеиновых компонентов фагов
5
Сборка новых фаговых частиц
6
Выход зрелых фагов и гибель бактерии
Условные обозначения
Бактерия
ДНК бактерии
Бактериофаг
ДНК фага
Что лечат бактериофагами
Препараты бактериофагами применяются для лечения и профилактики инфекционных заболеваний в следующих областях: гастроэнтерология, урология, гинекология, хирургия, оториноларингология, пульмонология, инфекционные заболевания желудочно-кишечного тракта (ЖКТ), гнойно-воспалительные заболевания кожи и слизистых.
Гастроэнтерология
Холецистит, гастроэнтероколит, дисбактериоз кишечника
Урогинекология
Цистит, пиелонефрит, кольпит, уретрит, эндометрит
Хирургия
Абсцесс, панариций, парапроктит, остеомиелит, мастит, перитонит, фурункулы, ожоги, гнойные раны, профилактика внутрибольничных инфекций
Оториноларингология
Синусит, тонзиллит, фарингит, ларингит, бронхит, ангина, гайморит, отит
Пульмонология
Трахеит, плеврит, ларингит, бронхит, пневмония
Инфекционные заболевания ЖКТ
Бактериальная дизентерия, дисбактериоз, энтероколит, колит, диспепсия
Гнойно-воспалительные заболевания кожи и слизистых
Омфалит, пиодермия, конъюнктивит, кератоконъюнктивит, сепсис, пемфигус и другие
ПРОИЗВОДСТВО БАКТЕРИОФАГОВ
Опыт применения бактериофагов насчитывает более 80 лет. Единственным в России производителем лекарственных препаратов бактериофагов является АО «НПО «Микроген» , выпускающее более 11 уникальных разновидностей препаратов данного вида. Для удобства пользователя препараты производятся в виде раствора. В разработке новые лекарственные формы — капсулы, спрей, гель, раневые губки, суппозитории.
Для удобства пользователя препараты производятся в виде раствора. В разработке новые лекарственные формы — капсулы, спрей, гель, раневые губки, суппозитории.
На предприятии разрабатываются первый в мире мире универсальный бактериофаг против бактерий рода энтеробактер. Ведутся работы по созданию новых фаговых коктейлей, включая препарат, который действует на синегнойную палочку и бактерии рода ацинетобактер баумани.
Регистрационные удостоверения
Лекарственные препараты бактериофаги сертифицированы в соответствии с государственными стандартами Российской Федерации.
Бактериофаги и антибиотики
Сравнение профилактического и терапевтического эффекта фагов и антибиотиков
Бактериофаги
антибиотики
Селективность действия
Предельно селективны. Уничтожают специфичных патогенов, не затрагивая нормальную бактериальную флору. Сохраняют микробный баланс организма.
Атакуют не только возбудителей заболеваний, но также все чувствительные микроорганизмы, включая нормальную микрофлору хозяина.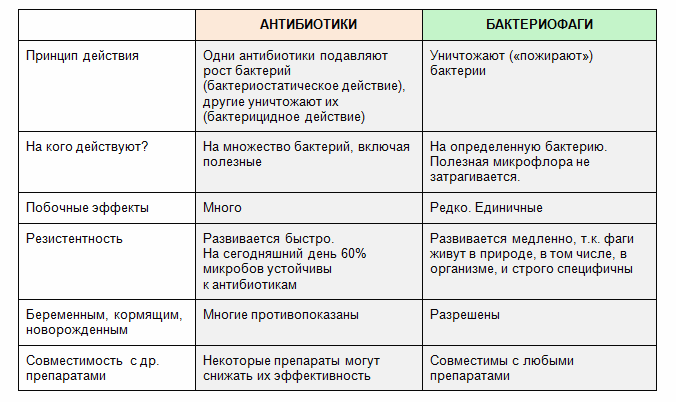
Побочные эффекты
Индивидуальная непереносимость. С клинической точки зрения фаги безопасны, поскольку люди с рождения встречаются с ними. Фаги – постоянные спутники организма, они были обнаружены в желудочно-кишечном тракте, на коже, в моче, во рту. Благодаря этому препараты можно назначать даже новорождённым детям.
Кишечные расстройства, аллергии, вторичные инфекции, подавление иммунитета, токсическое воздействие на печень и почки.
Разработка новых лекарств
Получение новых литических фагов происходит быстро благодаря естественной эволюции бактерий и фагов.
Создание новых антибиотиков (например, против антибиотикоустойчивых бактерий) требует временных затрат и может занять много лет.
Новости
«Микроген» провел научно-практическую конференцию по бактериофагам
С 20 по 21 октября 2022 года на уфимском предприятии НПО «Микроген» состоялась двухдневная научно-практическая конференция «Бактериофаги: биология, производство и применение в клинической практике», посвященная различным фундаментальным и прикладным аспектам изучения биологии бактериофагов, а также технологиям производства препаратов на их основе.
Подробнее
Эксперт НПО «Микроген» рассказал читателям «Комсомольской правды» о преимуществах бактериофагов
Руководитель проектного офиса «Развитие бактериофагов» НПО «Микроген», дочерней организации холдинга «Нацимбио» (Госкорпорация Ростех), Александр Жарников принял участие в обсуждении перспектив преодоления антибиотикорезистентности в России в рамках еженедельного мероприятия «Деловая пятница» издательского дома «Комсомольская правда».
Подробнее
Препараты бактериофагов включены в Федеральные Клинические рекомендации по острому синуситу
Лекарственные препараты бактериофагов рекомендованы в качестве консервативной терапии острого синусита в Федеральных Клинических рекомендациях – Острый синусит – 2021-2022-2023 (01.09.2021). Разработчик клинических рекомендаций — Национальная медицинская ассоциация оториноларингологов. Рекомендации одобрены Научно-практическим Советом Минздрава РФ.
Подробнее
Все новости
Странная история фаговой терапии
Со времен просветления ученые наслаждались представлением о себе как о рациональных актерах, руководствующихся только разумом, доказательствами и логикой. Когда Лондонское Королевское общество было основано в 1660 году, оно выбрало своим девизом «nullius in verba» (часто переводимое как «никто не говорит»), отсылку к Посланиям Горация «Nullius Addictus iurare in verba magistri…» (не будучи обязан присягнуть любому хозяину). Подобно нашим современникам 21-го века, которые принимают «новую доказательную медицину», «виртуозы» Королевского общества провозгласили новую эру в науке, основанную только на наблюдениях и непосредственном опыте.
Когда Лондонское Королевское общество было основано в 1660 году, оно выбрало своим девизом «nullius in verba» (часто переводимое как «никто не говорит»), отсылку к Посланиям Горация «Nullius Addictus iurare in verba magistri…» (не будучи обязан присягнуть любому хозяину). Подобно нашим современникам 21-го века, которые принимают «новую доказательную медицину», «виртуозы» Королевского общества провозгласили новую эру в науке, основанную только на наблюдениях и непосредственном опыте.
Ключевые слова: фаговая терапия, Феликс д’Эрель, Гюнтер Стент, Фредерик Туорт, литический принцип любопытна история терапии бактериофагами? История фаготерапии, начиная с открытия фагов столетие назад, полна противоречивых наблюдений, неправильных интерпретаций и неполного понимания, которые являются частью обычной науки. Но это еще не все: история фаговой терапии богата политикой, личными распрями и непризнанными конфликтами. Понимание этих вненаучных аспектов его истории может помочь объяснить мучительный курс фаговой терапии в прошлом столетии.
Вскоре после того, как Феликс д’Эрель обнаружил связь бактериофагов с диарейными заболеваниями, он предположил, что фаги ответственны за обычное выздоровление от таких болезней благодаря их антибактериальному действию in vivo. 1 Кроме того, он предложил активно использовать фаги лабораторного производства в качестве как профилактических, так и терапевтических средств против бактериальных инфекций. После первых полевых испытаний в качестве средства профилактики птичьего тифа ( Salmonella gallinarum ) в сельских районах Франции в 1919 г.19 до его широкого применения у людей в 1930-х годах, когда еще не было антибиотиков, фаготерапия вызывала споры. Некоторые видели в нем панацею от всех инфекционных болезней, в то время как другие считали его перепроданным и, вероятно, бесполезным. 2 , 3
Хотя несомненно верно, что открытие и широкое распространение антибиотиков сразу после мировой войны подорвали энтузиазм в отношении фаготерапии, это еще не все.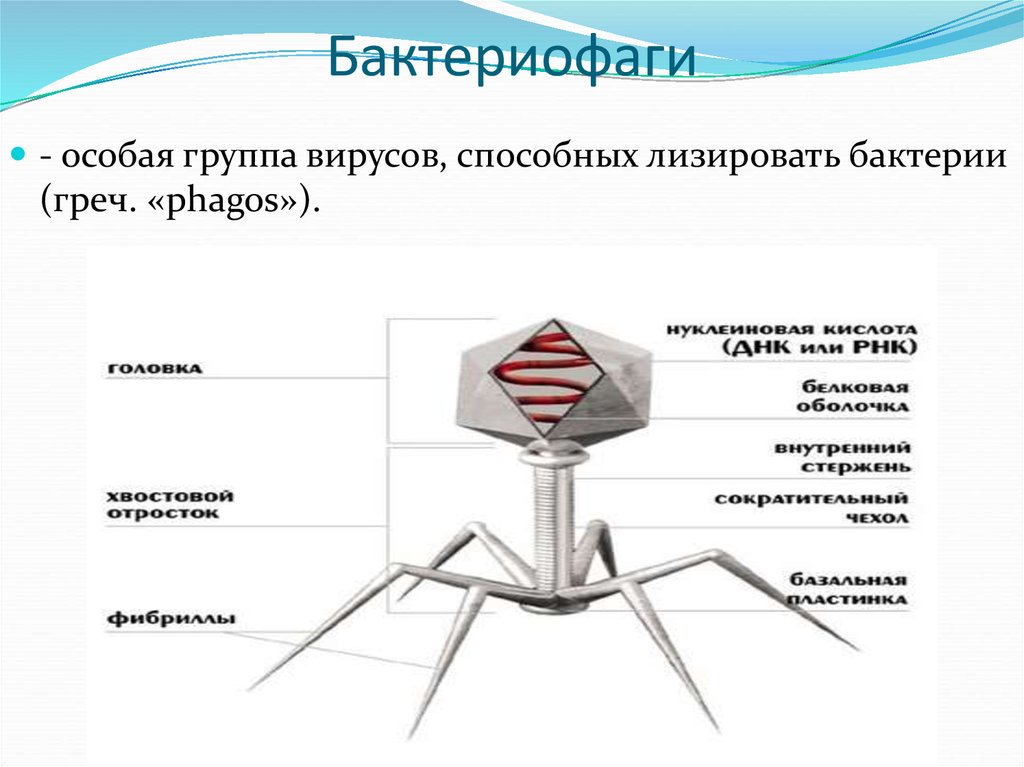 Действительно верно, что фаговые препараты не имели удобства антибиотиков, не были «широкого спектра действия» и сильно пострадали от научных споров о биологической природе фагов, разыгравшихся в XIX веке.20-х и 30-х годов. Это, конечно, рациональные объяснения упадка фаготерапии, начавшегося в 1940-х годах. Но как насчет других, более тонких причин этого упадка?
Действительно верно, что фаговые препараты не имели удобства антибиотиков, не были «широкого спектра действия» и сильно пострадали от научных споров о биологической природе фагов, разыгравшихся в XIX веке.20-х и 30-х годов. Это, конечно, рациональные объяснения упадка фаготерапии, начавшегося в 1940-х годах. Но как насчет других, более тонких причин этого упадка?
Возможно, самым показательным, наиболее подробным и наиболее влиятельным гвоздем в крышку гроба фаготерапии стал отрывок из вводной главы очень влиятельной монографии 1963 года Гюнтера Стента, одного из помощников Макса Дельбрюка «Церковь фагов». ” Стент обсудил использование фаготерапии против эпидемии чумы в романе Arrowsmith автора Нобелевской премии Синклера Льюиса следующим образом:
«Хотя Льюис написал Arrowsmith еще в 1924 году, он позволил своему герою прийти к тому, что последующие события показали как наиболее разумное решение: несмотря на двадцать лет» интенсивной работы, бактериофаги так и не стали успешным медицинским инструментом.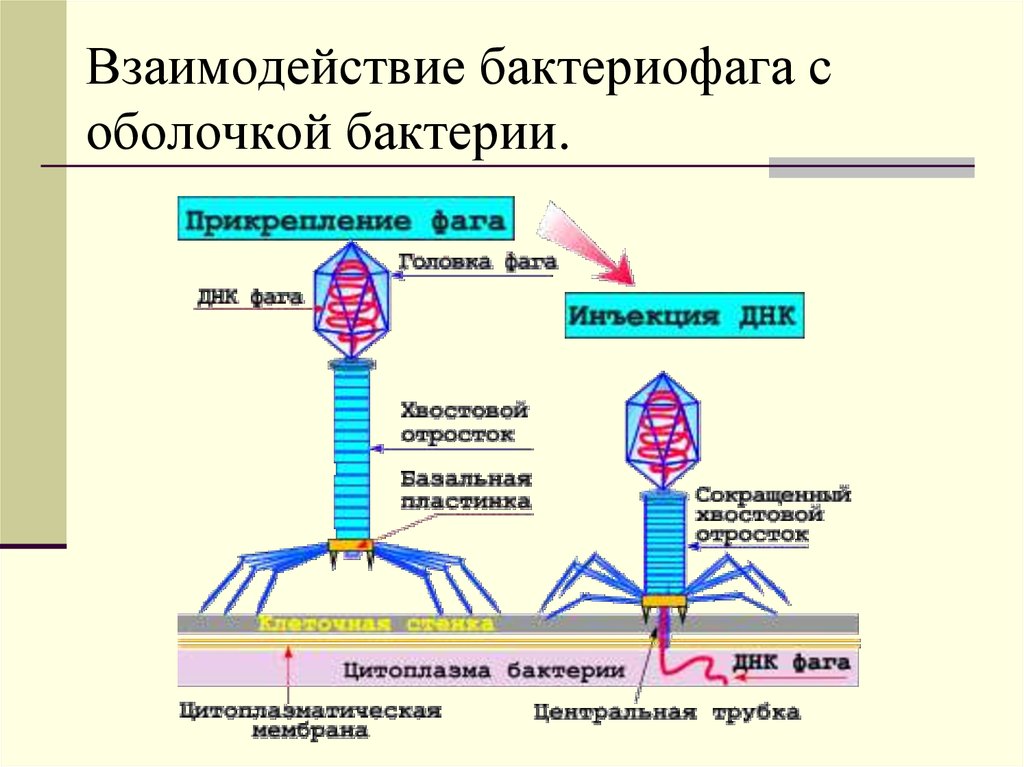 Правда, многим врачам удалось убедиться в эффективности терапии бактериофагами, особенно в борьбе с холерой, но такие новообращенные везде оставались в меньшинстве. Тем не менее, уже во время Второй мировой войны бактериофаги, как говорят, нашли применение в медицинских службах немецкой и японской армий, и даже сегодня медицинское использование бактериофагов все еще сохраняется в некоторых отдаленных местах. Но с тех пор, как антибиотики показали себя гораздо более эффективными в борьбе с бактериальными заболеваниями, чем самые ярые сторонники терапии бактериофагами когда-либо осмеливались надеяться на их панацею, странная глава истории медицины, посвященная терапии бактериофагами, теперь может справедливо рассматриваться как закрыто. Почему бактериофаги, столь вирулентные в своем антибактериальном действии in vitro, оказались столь бессильными in vivo, так и не были должным образом объяснены. Возможно, немедленный ответ антител пациента против фагового белка при подкожной инъекции, чувствительность фага к инактивации желудочным соком при пероральном введении и легкость, с которой (как мы сейчас увидим) бактерии приобретают иммунитет или проявляют резистентность к фагам.
Правда, многим врачам удалось убедиться в эффективности терапии бактериофагами, особенно в борьбе с холерой, но такие новообращенные везде оставались в меньшинстве. Тем не менее, уже во время Второй мировой войны бактериофаги, как говорят, нашли применение в медицинских службах немецкой и японской армий, и даже сегодня медицинское использование бактериофагов все еще сохраняется в некоторых отдаленных местах. Но с тех пор, как антибиотики показали себя гораздо более эффективными в борьбе с бактериальными заболеваниями, чем самые ярые сторонники терапии бактериофагами когда-либо осмеливались надеяться на их панацею, странная глава истории медицины, посвященная терапии бактериофагами, теперь может справедливо рассматриваться как закрыто. Почему бактериофаги, столь вирулентные в своем антибактериальном действии in vitro, оказались столь бессильными in vivo, так и не были должным образом объяснены. Возможно, немедленный ответ антител пациента против фагового белка при подкожной инъекции, чувствительность фага к инактивации желудочным соком при пероральном введении и легкость, с которой (как мы сейчас увидим) бактерии приобретают иммунитет или проявляют резистентность к фагам. все препятствовало успеху фаготерапии». 4
все препятствовало успеху фаготерапии». 4
В этом отрывке, который в то время читал почти каждый фаговый биолог, Стенту удается подорвать фаговую терапию тремя ключевыми способами, совершенно не связанными с научными данными. Во-первых, он предполагает, что ее защитники были небрежны с научной точки зрения: фраза «многим врачам удалось убедить себя» ясно подразумевает, что эти врачи, даже называемые «новообращенными», предполагая религиозную веру, а не рациональный анализ, были виновны в принятии желаемого за действительное, а не в ясности. объективное научное суждение. Во-вторых, Стент связывает фаготерапию с медициной врагов Америки во Второй мировой войне, немцев и японцев. В первые после Маккарти дни холодной войны фаговая терапия была как-то не по-американски. В-третьих, «даже сегодня» фаготерапия сохраняется, предполагая устаревшую технологию, которую можно найти только «в отдаленных местах». Фаготерапия предназначалась для отсталых и примитивных регионов земного шара. Тот факт, что стент относится к «странной главе о терапии бактериофагами» в истории медицины, ставит его за рамки нарратива о прогрессе и научном триумфе, который обычно рассказывается о западной медицине. Авторитетно и без капли высокомерия Стент заявляет, что эту главу «по праву можно считать закрытой». Ненадолго, так сказать, сняв шляпу перед научной респектабельностью, он задается вопросом: «Почему бактериофаги, столь опасные в своем антибактериальном действии in vitro, оказались столь бессильными in vivo…», а затем предлагает ответы, апеллирующие к современным биологическим знаниям.
Тот факт, что стент относится к «странной главе о терапии бактериофагами» в истории медицины, ставит его за рамки нарратива о прогрессе и научном триумфе, который обычно рассказывается о западной медицине. Авторитетно и без капли высокомерия Стент заявляет, что эту главу «по праву можно считать закрытой». Ненадолго, так сказать, сняв шляпу перед научной респектабельностью, он задается вопросом: «Почему бактериофаги, столь опасные в своем антибактериальном действии in vitro, оказались столь бессильными in vivo…», а затем предлагает ответы, апеллирующие к современным биологическим знаниям.
Вердикт Стента в отношении фаговой терапии уходит своими корнями в ранние разногласия в исследованиях фагов, отсутствие понимания биологии фагов и неотъемлемые трудности оценки методов лечения в клинических испытаниях на людях. Эта история столь же личная, сколь и научная. С самого открытия фага в этой области наблюдались личные нападки, споры о приоритетах, массовое эго и международная политика. Все это — часть непростой истории фаготерапии.
Все это — часть непростой истории фаготерапии.
Само открытие фага стало предметом длительного спора между двумя лагерями: на одной стороне был Феликс д’Эрель, 9 лет.0011 5 франко-канадский самоучка, который первым распознал фаг в соответствии с нашей нынешней концепцией бактериального вируса; с другой стороны были сторонники Фредерика Туорта, 6 , причудливого британского микробиолога, который наблюдал «трансмиссивное стекловидное превращение» бактерий, но не смог развить свои первоначальные наблюдения. Туорт был представлен в этих ранних спорах маловероятным суррогатом, лауреатом Нобелевской премии Жюлем Борде. Этот спор, на первый взгляд, о приоритете открытия и о биологической природе бактериофага, однако, коренился в обиде и личных амбициях. Д’Эрель был бесплатным волонтером в Институте Пастера в 1919 г.16, когда он обнаружил основные факты о бактериофагах, которые он наблюдал в фильтратах дизентерийных жидкостей. Он был странствующим микробиологом в поисках открытия, которое, по его собственной характеристике, позволило бы ему пойти по стопам Пастера. Открытие фага предоставило ему такую возможность: он сразу связал лизис фага in vitro с действием фага in vivo, чтобы объяснить выздоровление больных дизентерией. Фаг стал агентом естественного эндогенного иммунитета. Однако с этой новой теорией была одна проблема. В 1919 Жюль Борде был удостоен Нобелевской премии за свою работу об иммунитете, основанном на лизисе бактерий антителами, а не фагами. Неустрашимый бунтарь д’Эрель в своей второй монографии о фагах смело бросил вызов знаменитому Борде, директору Института Пастера в Брюсселе, назвав работу Борде «историей ошибки». 7 Это оскорбление не осталось незамеченным. Борде и его протеже Андре Грация ответили почти десятилетней критикой д’Эреля и его работы, бросив вызов как его концепции фага как вируса (они думали, что это индуцированный литический фермент), так и его приоритету, утверждая, что Творт был там первым. Д’Эрель яростно сопротивлялся, но не имея ни реальной институциональной базы, ни Нобелевской премии, ни тонкой натуры, в 1919 г.
Открытие фага предоставило ему такую возможность: он сразу связал лизис фага in vitro с действием фага in vivo, чтобы объяснить выздоровление больных дизентерией. Фаг стал агентом естественного эндогенного иммунитета. Однако с этой новой теорией была одна проблема. В 1919 Жюль Борде был удостоен Нобелевской премии за свою работу об иммунитете, основанном на лизисе бактерий антителами, а не фагами. Неустрашимый бунтарь д’Эрель в своей второй монографии о фагах смело бросил вызов знаменитому Борде, директору Института Пастера в Брюсселе, назвав работу Борде «историей ошибки». 7 Это оскорбление не осталось незамеченным. Борде и его протеже Андре Грация ответили почти десятилетней критикой д’Эреля и его работы, бросив вызов как его концепции фага как вируса (они думали, что это индуцированный литический фермент), так и его приоритету, утверждая, что Творт был там первым. Д’Эрель яростно сопротивлялся, но не имея ни реальной институциональной базы, ни Нобелевской премии, ни тонкой натуры, в 1919 г. 31 г. он, наконец, обратился в парижские суды, чтобы заставить редактора «Анналов Пастеровского института» опубликовать свой вызов научной дуэли между ним и Борде. Как ни странно это может показаться нам сегодня, большая часть научного сообщества, включая все стандартные учебники, поддержала концепцию Борде о фаге как о самовоспроизводящемся литическом ферменте.
31 г. он, наконец, обратился в парижские суды, чтобы заставить редактора «Анналов Пастеровского института» опубликовать свой вызов научной дуэли между ним и Борде. Как ни странно это может показаться нам сегодня, большая часть научного сообщества, включая все стандартные учебники, поддержала концепцию Борде о фаге как о самовоспроизводящемся литическом ферменте.
Этот взгляд на фаг как литический фермент был подкреплен поддержкой другого лауреата Нобелевской премии, который занялся исследованиями фагов в 1930 с. Джон Нортроп из Рокфеллеровского института и лауреат Нобелевской премии за работу по пищеварительным ферментам, таким как трипсин и пепсин, поддержал идею о том, что фаг является еще одним примером автокаталитической самоактивации, подобной трипсиногену/трипсину и системы пепсиноген/пепсин. Только после применения электронной микроскопии для визуализации бактериофагов в конце 1930-х годов вирусная концепция фага д’Эреля была подтверждена. 8 Даже тогда это свидетельство медленно проникало в научное сообщество по вненаучной причине: Вторая мировая война. Электронный микроскоп был разработан в довоенной Германии и первые изображения фага были получены там в 1939 и опубликована в немецкой литературе в 1940 г. Однако с началом войны распространение научной литературы было серьезно затруднено. Американские библиотеки, например, отправляли свои подписки по почте в Швейцарию, чтобы хранить их там до окончания войны. В разгар войны немецкая литература, показывающая ЭМ-изображения фага, попала во Францию, где эти изображения были переизданы (с указанием) во французской прессе. 9
Электронный микроскоп был разработан в довоенной Германии и первые изображения фага были получены там в 1939 и опубликована в немецкой литературе в 1940 г. Однако с началом войны распространение научной литературы было серьезно затруднено. Американские библиотеки, например, отправляли свои подписки по почте в Швейцарию, чтобы хранить их там до окончания войны. В разгар войны немецкая литература, показывающая ЭМ-изображения фага, попала во Францию, где эти изображения были переизданы (с указанием) во французской прессе. 9
В то время как споры, некоторые научные, а некоторые более личные, бушевали о природе фага, в медицинской литературе разыгрывались другие дебаты о пригодности фага как терапевтического и профилактического средства против бактериальных инфекций. И снова в этих дебатах фигурировали личности главных героев. При самых благоприятных обстоятельствах трудно оценить эффективность лечения, а показать ценность профилактики еще труднее. В то время о стандартизированных методах и материалах, статистически контролируемых испытаниях и двойных слепых исследованиях почти ничего не было слышно. Вместо этого нормой были небольшие испытания, отдельные отчеты, исторический контроль и клинические впечатления. Неудивительно, что возник спор. Один из подходов к разрешению двусмысленности был предпринят Американской медицинской ассоциацией, когда она учредила Совет по фармации и химии, который, помимо прочего, регулярно заказывал научные обзоры литературы для публикации в журнале Ассоциации. Эти обзоры, своего рода предшественник нынешнего «метаанализа», были предназначены для уравновешивания конфликтов, оценки конкурирующих и противоречивых утверждений и получения выводов. Было опубликовано три таких отчета о терапии бактериофагами, первый за 19 лет.34, 10 , второй в 1941 г. 11 и третий в 1945 г. 12 Все трое согласились с тем, что литература по фаготерапии и профилактике была запутанной и противоречивой. Все три отражали развитие исследований фагов того времени. Все трое содержали сильные личные предубеждения.
Вместо этого нормой были небольшие испытания, отдельные отчеты, исторический контроль и клинические впечатления. Неудивительно, что возник спор. Один из подходов к разрешению двусмысленности был предпринят Американской медицинской ассоциацией, когда она учредила Совет по фармации и химии, который, помимо прочего, регулярно заказывал научные обзоры литературы для публикации в журнале Ассоциации. Эти обзоры, своего рода предшественник нынешнего «метаанализа», были предназначены для уравновешивания конфликтов, оценки конкурирующих и противоречивых утверждений и получения выводов. Было опубликовано три таких отчета о терапии бактериофагами, первый за 19 лет.34, 10 , второй в 1941 г. 11 и третий в 1945 г. 12 Все трое согласились с тем, что литература по фаготерапии и профилактике была запутанной и противоречивой. Все три отражали развитие исследований фагов того времени. Все трое содержали сильные личные предубеждения.
Первый отчет АМА по терапии бактериофагами был подготовлен двумя профессорами Йельского университета Монро Итон, молодым специалистом по инфекционным заболеваниям, и Стэнхоупом Бейн-Джонсом, который вскоре стал деканом Йельской школы медицины и выдающимся бактериологом. 10 Интересно, что Бейн-Джонс только что был принят на работу в Йельский университет из Рочестерского университета, чтобы заполнить вакансию по бактериологии, оставшуюся после бурного отъезда д’Эреля в Тбилиси.
10 Интересно, что Бейн-Джонс только что был принят на работу в Йельский университет из Рочестерского университета, чтобы заполнить вакансию по бактериологии, оставшуюся после бурного отъезда д’Эреля в Тбилиси.
Второй отчет АМА был опубликован в 1941 г. Его авторами были Альберт Крюгер, сторонник дебатов о биологической природе фагов и протеже Джона Нортропа, и молодой коллега Э. Джейн Скрибнер. Они решительно поддержали концепцию Борде о фаге как автокаталитически активируемом «литическом принципе» в противовес концепции вируса д’Эреля. 11 Крюгер, кроме того, распространял эту полемику на следующее поколение фаговых работников в своих спорах с Эмори Эллисом и Максом Дельбрюком, сторонниками позиции д’Эреля (Эллис, личное сообщение).
Третий и, по-видимому, последний отчет АМА о бактериофагах был опубликован в 1945 году Гарри Э. Мортоном и Фрэнком Б. Энгли-младшим, которые всего через четыре года после Крюгера и Скрибнера, полностью изменив предшествующую догму, полностью приняли вирусная природа фага. 12 Действительно, несколько картинок ЭМ стоили многих тысяч слов.
12 Действительно, несколько картинок ЭМ стоили многих тысяч слов.
Во всех трех отчетах показана напряженность между лабораторными исследованиями фаговой терапии и ее клиническими применениями, а также между действием фагов in vitro и in vivo на бактерии. Задачу всех рецензентов не облегчало отсутствие стандартизации методов и материалов: некоторые испытания были проведены с недавними специфическими для пациента фаговыми изолятами, а некоторые — с тем или иным коммерчески доступным препаратом. Коммерческие препараты фагов, часто продаваемые в виде поливалентных смесей, иногда содержали так много консерванта, что фаги химически инактивировались. Состав препаратов был неясен: один из первых сотрудников рассказал, что, хотя изначально они готовили много разных препаратов фагов по отдельности, а затем смешивали их для получения поливалентного продукта, в конце концов им стало легче сначала смешать фаги, а затем выращивать их последовательно все вместе. Этот процесс, конечно, гарантировал, что в конечном продукте будут обнаружены только самые вирулентные и быстро размножающиеся фаги (Макс Дельбрюк, личное сообщение). С такой неопределенностью противоречивые и противоречивые результаты были почти гарантированы. Различие между терапевтическим и профилактическим применением фага было важным, но иногда также упускалось из виду.
С такой неопределенностью противоречивые и противоречивые результаты были почти гарантированы. Различие между терапевтическим и профилактическим применением фага было важным, но иногда также упускалось из виду.
Помимо сложностей и неопределенностей клинических испытаний, в общественном сознании бактериофаги заняли темное положение, как и все вирусы в конце 1930-х годов, «на границе жизни». Их статус не совсем живых организмов и не совсем простых химических веществ интересовал как ученых, так и неспециалистов. 13 Тот факт, что вирусы могут кристаллизоваться, золотой стандарт органической химии, предполагал, что они были «всего лишь» химическими веществами, но их способность размножаться и мутировать говорила о том, что они каким-то образом выходят за рамки химии, что добавляло их таинственного характера. Примитивное понимание фагов как биологических объектов было недостаточным для прояснения этих противоречий. Напротив, новые сульфаниламидные препараты XIX в.30s, простые и хорошо охарактеризованные органические соединения, были просты в использовании, достаточно однородны и чрезвычайно эффективны против важных инфекций и широко доступны. Антимикробная химиотерапия достигла совершеннолетия и стала вызовом для фагов в качестве ответа на инфекционные заболевания. Сульфаты проложили путь к внедрению антибиотиков, потенциально проблематичных из-за их биологического происхождения и сложной химии, но с готовностью принятых специалистами, все более знакомыми с химиотерапией.
Антимикробная химиотерапия достигла совершеннолетия и стала вызовом для фагов в качестве ответа на инфекционные заболевания. Сульфаты проложили путь к внедрению антибиотиков, потенциально проблематичных из-за их биологического происхождения и сложной химии, но с готовностью принятых специалистами, все более знакомыми с химиотерапией.
В медицинской практике в США в этот период преобладали врачи общей практики, не имеющие рутинного доступа к бактериологическим лабораторным ресурсам, даже для диагностики, не говоря уже о комплексной поддержке, необходимой для эффективной фаготерапии. Готовые лекарства и простые местные составы были основой общей практики, а фаговые препараты плохо себя чувствовали в этой среде по сравнению со стабильными сульфатами или даже новыми антибиотиками, которые требовали только охлаждения для долгосрочной стабильности. Фаготерапия, даже если бы она была однозначно эффективной, была слишком сложна для состояния американской медицины в XIX веке.40с. Терапевтическую нишу фага заняли более «подходящие» антибиотики.
А еще был политический аспект фага. Д’Эрель уехал из США в 1934 году и вместе с Джорджем Элиавой, бывшим коллегой из Института Пастера, помог основать институт по изучению фагов и фаговой терапии в Тбилиси в Грузинской Советской Республике. Фаговая терапия была разработана, продвигалась и широко применялась как в Советском Союзе, так и, по крайней мере, в некоторых случаях, в немецкой армии во время Второй мировой войны. Такое применение не было удивительным, поскольку первые антибиотики были доступны только союзникам и, по крайней мере, вначале, в очень ограниченных количествах. Сразу после Второй мировой войны прежнее сотрудничество между США и СССР вскоре испортилось, и все «коммунистическое» стало подозрительным на Западе; в том числе и советское научное знание. 14 Хотя для такого отношения были некоторые причины, такие как неприятие менделевской генетики школой Лысенко и дискредитированное лечение рака Клюевой и Роскиным, большая часть тотального отказа от советской науки (по крайней мере, до спутника) была политической. в природе. Выдающегося генетика Трейси Соннеборна, например, заподозрили в «коммунистических симпатиях» из-за его интереса к цитоплазматической наследственности парамеций, предположительно «розовой» идее. 15 Любая наука, хорошая или плохая, которую осваивали «коммуняки», была опасна. Как заметил Гюнтер Стент, фаговая терапия была отнесена к «удаленным местам» (в то время все понимали, что это Советский Союз) и, как следствие, была несостоятельной с научной точки зрения, потому что она была несостоятельной с политической.
в природе. Выдающегося генетика Трейси Соннеборна, например, заподозрили в «коммунистических симпатиях» из-за его интереса к цитоплазматической наследственности парамеций, предположительно «розовой» идее. 15 Любая наука, хорошая или плохая, которую осваивали «коммуняки», была опасна. Как заметил Гюнтер Стент, фаговая терапия была отнесена к «удаленным местам» (в то время все понимали, что это Советский Союз) и, как следствие, была несостоятельной с научной точки зрения, потому что она была несостоятельной с политической.
Рост фармацевтической промышленности в послевоенный период также сыграл роль в экономической маргинализации фаготерапии. «Большая фармацевтика» получила огромную прибыль от новых антибиотиков, «чудо-лекарств». Простые в массовом производстве, простые в применении и довольно стабильные, а также действительно эффективные антибиотики рассматривались как путь вперед в борьбе с бактериальными инфекциями. Последние коммерческие фаговые препараты исчезли с основных фармацевтических рынков в начале XIX в. 70-е годы. Однако постепенно, по мере того как устойчивость к антибиотикам стала как клинической проблемой, так и проблемой общественного здравоохранения, особенно в связи со взрывным ростом бактериальных штаммов, устойчивых к основным пенициллинам (таких штаммов, как устойчивые к метициллину Staphylococcus aureus , MRSA), стали искать новые подходы. . Неотъемлемо переплетенные проблемы развития устойчивости к антибиотикам с широким использованием, противодействующие неспособности окупить инвестиции в НИОКР в условиях ограниченного использования, сделали эти проблемы еще более насущными. Кажется, что в отчаянии старые предрассудки могут рухнуть и появиться новые подходы. Фаговая терапия, потенциально используемая в отдельных контекстах, пересматривается. Тем не менее, дискуссия продолжается. 16 , 17
70-е годы. Однако постепенно, по мере того как устойчивость к антибиотикам стала как клинической проблемой, так и проблемой общественного здравоохранения, особенно в связи со взрывным ростом бактериальных штаммов, устойчивых к основным пенициллинам (таких штаммов, как устойчивые к метициллину Staphylococcus aureus , MRSA), стали искать новые подходы. . Неотъемлемо переплетенные проблемы развития устойчивости к антибиотикам с широким использованием, противодействующие неспособности окупить инвестиции в НИОКР в условиях ограниченного использования, сделали эти проблемы еще более насущными. Кажется, что в отчаянии старые предрассудки могут рухнуть и появиться новые подходы. Фаговая терапия, потенциально используемая в отдельных контекстах, пересматривается. Тем не менее, дискуссия продолжается. 16 , 17
Ранее опубликовано на сайте: www.landesbioscience.com/journals/bacteriophage/article/20757
Comptes rendus Acad Sci Paris 1917; 165:373-5.
2. Редакция. Ограничения терапии бактериофагами. ДЖАМА. 1931; 96: 693. doi: 10.1001/jama.1931.02720350045014. [CrossRef] [Google Scholar]
3. От редакции. Коммерческие аспекты бактериофаговой терапии. ДЖАМА. 1933;100:1603–4. doi: 10.1001/jama.1933.02740200037014. [CrossRef] [Google Scholar]
4. Стент GS. Молекулярная биология бактериальных вирусов. Сан-Франциско и Лондон: WH Freeman, 1963:8-9. [Google Scholar]
5. Летний туалет. Феликс д’Эрель и истоки молекулярной биологии. New Haven: Yale Univ Press, 1999. [Google Scholar]
6. Туорт А. В фокусе, не в ногу. Биография Фредерика Уильяма Туорта, FRS 1877-1950 гг. Довер, Нью-Хэмпшир: Alan Sutton Publishing, 1993. [Google Scholar]
7. d’Herelle F. Иммунитет при естественных инфекционных заболеваниях. Балтимор: Уильямс и Уилкинс, 1924: 162. [Google Scholar]
8. Ruska H. Die Sichtbarmachung der bakteriophagen Lyse im Ubermikroskop. Натурвиссен. 1940; 28: 45–46. doi: 10.1007/BF01486931. [CrossRef] [Google Scholar]
[CrossRef] [Google Scholar]
9. Levaditi C, Bonet-Maury P. Ультравирус: Рассмотрение результатов электронного микроскопа. Ла Пресс мед 1942; 17:203-207.
10. Eaton MD, Bayne-Jones S. Бактериофаговая терапия. ДЖАМА 1934; 103:1769-76; 1847-53; 1934-9.
11. Крюгер А.П., Скрибнер Э.Дж. Бактериофаг. ДЖАМА. 1941; 116:2160–7, 2269–77. doi: 10.1001/jama.1941.628201010. [CrossRef] [Google Scholar]
12. Morton HE, Engley FB., Jr Dysentery Bacteriophage. ДЖАМА. 1945; 127: 584–91. [Google Scholar]
13. Ньюман Б.М. Плавное скольжение к жизни. Редакционный комментарий. наук Ам. 1937; 156: 304–6. doi: 10.1038/scientificamerican0537-304. [CrossRef] [Google Scholar]
14. Кременцов Н. Сталинская наука. Принстон, Нью-Джерси: Princeton Univ Press, 19.97. [Google Scholar]
15. Сапп Дж. Глава 6. Холодная война в генетике. В: За пределами гена: цитоплазматическое наследование и борьба за авторитет в генетике. Нью-Йорк: Oxford Univ Press, 1987. [Google Scholar]
16. Проян С. Антибиотики, вдохновленные фагами? Нац биотехнолог. 2004; 22: 167–8. doi: 10.1038/nbt0204-167. [PubMed] [CrossRef] [Google Scholar]
Проян С. Антибиотики, вдохновленные фагами? Нац биотехнолог. 2004; 22: 167–8. doi: 10.1038/nbt0204-167. [PubMed] [CrossRef] [Google Scholar]
17. Schoolnik GK, Summers WC, Watson JD. Phage предлагают реальную альтернативу. Нац биотехнолог. 2004; 22: 505–6, ответ автора 506–7. doi: 10.1038/nbt0504-505. [PubMed] [CrossRef] [Академия Google]
Решение нашей проблемы с антибиотиками? Как мы можем использовать вирус для борьбы с бактериальной инфекцией
Veerasak «Jeep» Srisuknimit
цифры Jovana Andrejevic
Наше время с антибиотиками истекает. В 2016 году женщина в Неваде умерла от бактериальной инфекции, вызванной Klebsiella pneumoniae , устойчивой ко всем доступным антибиотикам. Бактерии, устойчивые к колистину, антибиотику последней инстанции, были обнаружены на свинофермах в Китае. Бактерии эволюционировали, чтобы противостоять антибиотикам быстрее, чем когда-либо.
Тем временем ученым требуется десять или более лет, чтобы разработать новый антибиотик и получить одобрение FDA. Наша медленная реакция означает, что мы проигрываем в этой гонке вооружений с применением антибиотиков. Нам срочно нужен альтернативный метод борьбы с бактериальной инфекцией. Одним из многообещающих методов уничтожения бактерий является использование бактериофагов: вирусов, которые заражают и убивают бактерии.
Наша медленная реакция означает, что мы проигрываем в этой гонке вооружений с применением антибиотиков. Нам срочно нужен альтернативный метод борьбы с бактериальной инфекцией. Одним из многообещающих методов уничтожения бактерий является использование бактериофагов: вирусов, которые заражают и убивают бактерии.
Бактериофаги, для краткости называемые фагами, были независимо открыты Фредериком Туортом в 1915 и Феликсом д’Эрелем в 1917 году, более чем за десять лет до появления пенициллина, самого известного антибиотика. В последующие годы фаги с успехом применялись для лечения дизентерии и холеры. Эти фаги были выделены из стула пациентов, неожиданно выздоровевших от болезни. Ученые предположили, что в этих счастливых пациентах было что-то, что помогало удалять вредные бактерии из их кишечника. Они выделили фаги из стула, очистили их и дали фаги другим пациентам. В одном исследовании 63% нелеченых людей, страдающих холерой в Пенджабе, Индия, умерли, в то время как только 8% тех, кто лечился фагами, умерли. Несмотря на ранний успех, фаговую терапию затмило открытие пенициллина и появление антибиотиков.
Несмотря на ранний успех, фаговую терапию затмило открытие пенициллина и появление антибиотиков.
В то время, когда фаги впервые использовались для лечения холеры, ученые только начали изучать вирусы и размышлять о том, как работают фаги. Лишь в 1940 г. были получены первые изображения фагов с помощью электронного микроскопа. Теперь мы знаем, что фаги — это вирусы, поражающие только бактерии. Как тип вируса, фаги не могут жить и размножаться в одиночку. Вирусам необходимо вторгнуться в клетку-хозяин, потреблять питательные вещества хозяина, чтобы сделать больше копий себя, и, наконец, выбраться из клетки-хозяина — часто убивая хозяина в процессе.
Как правило, фаги начинают убивать первыми, распознавая бактерии и приземляясь на них. Каждый тип фагов имеет определенную посадочную площадку. Затем фаг вводит свою ДНК в бактерии. Эта ДНК копирует себя, создает большую часть оболочки фага и упаковывает только что созданную ДНК в новую оболочку. Наконец, фаг вырабатывает токсичные химические вещества, которые разрывают бактерию-хозяина изнутри, выпуская своих новоиспеченных потомков наружу, чтобы заразить еще больше бактерий (рис. 1).
1).
Антибиотик — это химическое вещество, убивающее бактерии. Он делает это, нарушая один или несколько важных процессов, необходимых бактериям для выживания. Поскольку эти процессы характерны для многих бактерий, один антибиотик «широкого спектра действия» потенциально может убить сразу несколько видов бактерий. Хотя антибиотики произвели революцию в медицине и часто очень эффективны в борьбе с бактериальной инфекцией, хорошо развитые фаги могут иметь несколько преимуществ перед антибиотиками.
Во-первых, фаги специфичны для одного вида бактерий и, следовательно, вряд ли потревожат полезные микробы, живущие в нашем кишечнике. Человеческое тело населено более чем тысячей видов микробов, которые, по оценкам, составляют около 3-5 фунтов от общей массы нашего тела. Эти микробы выполняют для нас важную работу, например, помогают нам производить питательные вещества, которые мы не можем производить сами. Поскольку многие антибиотики убивают бактерии без разбора, лечение инфекции антибиотиком также приводит к уничтожению этих полезных кишечных бактерий. С другой стороны, каждый фаг эволюционировал, чтобы убивать только определенный набор бактерий. Поскольку фаг убивает в узком диапазоне, его можно использовать для лечения инфекции, не нарушая сообщества полезных бактерий в нашем организме.
Человеческое тело населено более чем тысячей видов микробов, которые, по оценкам, составляют около 3-5 фунтов от общей массы нашего тела. Эти микробы выполняют для нас важную работу, например, помогают нам производить питательные вещества, которые мы не можем производить сами. Поскольку многие антибиотики убивают бактерии без разбора, лечение инфекции антибиотиком также приводит к уничтожению этих полезных кишечных бактерий. С другой стороны, каждый фаг эволюционировал, чтобы убивать только определенный набор бактерий. Поскольку фаг убивает в узком диапазоне, его можно использовать для лечения инфекции, не нарушая сообщества полезных бактерий в нашем организме.
Во-вторых, фаги способны убивать устойчивые к антибиотикам бактерии. Способ, которым фаги убивают бактерии, бактериям труднее выработать устойчивость по сравнению с тем, как антибиотики убивают бактерии. Вместо того, чтобы мешать бактериям выполнять один конкретный процесс, как в случае с антибиотиками, фаги активно разрушают клеточную стенку и клеточную мембрану бактерий и убивают бактерии, проделывая множество отверстий изнутри наружу. Кроме того, у многих бактерий образуется биопленка — толстый слой вязких материалов, защищающих их от антибиотиков. Многие фаги оснащены инструментами, способными переваривать эту биопленку.
Кроме того, у многих бактерий образуется биопленка — толстый слой вязких материалов, защищающих их от антибиотиков. Многие фаги оснащены инструментами, способными переваривать эту биопленку.
За исключением вариантов лечения, доступных в нескольких странах, от фагов в основном отказались как от бактериальных инфекций. Одна из основных причин заключается в том, что антибиотики работали достаточно хорошо в течение последних 50 лет, поэтому в большинстве стран не было возобновлено исследование клинического применения фагов. Но другая причина заключается в том, что существуют некоторые ограничения на использование фагов в качестве лечения.
Во-первых, фаги труднее подготовить чисто. Чтобы произвести фаги, сначала ученые должны вырастить большое количество бактерий, которые являются естественным хозяином фага. Затем бактерии заражаются фагами, а фаги, в свою очередь, размножаются и убивают все бактерии. Трудность начинается с выделения живых фагов из множества мертвых трупов бактерий. Если их не удалить из последнего лекарства, которое дали пациенту, тела мертвых бактерий могут вызвать смертельный иммунный ответ, называемый сепсисом. Еще одна проблема заключается в том, чтобы получить правильную концентрацию фагов, поскольку ее концентрацию нельзя измерить напрямую. Если концентрация слишком низкая, фаговая терапия будет неэффективной. Многие из первых коммерческих фаговых продуктов были низкого качества и не могли лечить инфекционные заболевания, что привело к дискредитации фаговой терапии.
Если их не удалить из последнего лекарства, которое дали пациенту, тела мертвых бактерий могут вызвать смертельный иммунный ответ, называемый сепсисом. Еще одна проблема заключается в том, чтобы получить правильную концентрацию фагов, поскольку ее концентрацию нельзя измерить напрямую. Если концентрация слишком низкая, фаговая терапия будет неэффективной. Многие из первых коммерческих фаговых продуктов были низкого качества и не могли лечить инфекционные заболевания, что привело к дискредитации фаговой терапии.
Во-вторых, фагам требуется больше времени для лечения, чем антибиотикам. Поскольку один тип фага может инфицировать только несколько видов бактерий, выбор фага должен проводиться с осторожностью. Во-первых, врачи должны выяснить, какие именно бактерии вызывают заболевание. Затем они должны проверить, могут ли имеющиеся фаги убить этот штамм бактерий. Если нет, им приходится искать новые фаги, которые могли бы выполнить эту работу. Этот процесс требует времени, которого у пациентов может не быть, особенно когда фаги используются только в крайнем случае у очень больных пациентов. С другой стороны, поскольку антибиотики убивают без разбора, врачи могут назначать антибиотики для лечения пациента без необходимости предварительно идентифицировать конкретный тип бактерий.
С другой стороны, поскольку антибиотики убивают без разбора, врачи могут назначать антибиотики для лечения пациента без необходимости предварительно идентифицировать конкретный тип бактерий.
Другие опасения по поводу фаготерапии связаны с ее безопасностью и эффективностью. Поскольку западный мир отказался от фаготерапии много десятилетий назад, данных по этим темам мало. Однако исследования в области фаготерапии продолжаются и процветают во Франции и странах Восточной Европы, особенно в Грузии. Согласно их исследованиям, фаготерапия не вызывает серьезных проблем с безопасностью.
Рисунок 2: Фаги можно использовать двумя способами: для защиты или для лечения. Вот два примера. Фаги можно использовать для обожженных жертв, чтобы защитить их кожу от бактериальной инфекции. Фаг также можно использовать для лечения пациентов, пораженных устойчивыми к антибиотикам бактериальными инфекциями. Где мы сейчас? Теперь, когда все больше и больше бактерий вырабатывают устойчивость к антибиотикам, ученые всего мира вновь проявляют интерес к фагам. Европейский Союз инвестировал 5 миллионов евро в проект Phagoburn, который изучает использование фагов для предотвращения кожных инфекций у пострадавших от ожогов (рис. 2). В США FDA одобрило ListshieldTM, пищевую добавку, содержащую фаги, которая убивает Listeria monocytogenes, один из наиболее вирулентных патогенов пищевого происхождения и одну из причин менингита. В настоящее время проводится множество клинических испытаний с использованием фагов для лечения или профилактики бактериальных инфекций, таких как туберкулез и MRSA.
Европейский Союз инвестировал 5 миллионов евро в проект Phagoburn, который изучает использование фагов для предотвращения кожных инфекций у пострадавших от ожогов (рис. 2). В США FDA одобрило ListshieldTM, пищевую добавку, содержащую фаги, которая убивает Listeria monocytogenes, один из наиболее вирулентных патогенов пищевого происхождения и одну из причин менингита. В настоящее время проводится множество клинических испытаний с использованием фагов для лечения или профилактики бактериальных инфекций, таких как туберкулез и MRSA.
Несмотря на то, что фаговая терапия еще не одобрена FDA, фаги уже использовались для спасения жизней в экспериментальных методах лечения. В Сан-Диего сообщалось о чудесном выздоровлении пациента, который страдал от устойчивых к антибиотикам бактерий. Во время отпуска в Египте Том Паттерсон заразился полирезистентным штаммом Acinetobacter baumannii . Его доставили обратно в Калифорнию и лечили антибиотиками более 100 дней, но Паттерсону не стало лучше, и он впал в кому.

