Иммунитет попутал. Названа прививка с необычными побочными эффектами
https://ria.ru/20210818/privivka-1746129943.html
Иммунитет попутал. Названа прививка с необычными побочными эффектами
Иммунитет попутал. Названа прививка с необычными побочными эффектами — РИА Новости, 03.09.2021
Иммунитет попутал. Названа прививка с необычными побочными эффектами
В самом начале пандемии появлялись сообщения о том, что в странах, где население массово привито противотуберкулезной вакциной, люди реже заболевают ковидом и… РИА Новости, 03.09.2021
2021-08-18T08:00
2021-08-18T08:00
2021-09-03T13:25
наука
туберкулез
вакцинация
прививки
сша
пенсильвания
санкт-петербургский государственный университет
воз
/html/head/meta[@name=’og:title’]/@content
/html/head/meta[@name=’og:description’]/@content
https://cdnn21.img.ria.ru/images/07e5/08/0b/1745365698_0:49:1306:784_1920x0_80_0_0_8ef3215ad5a0caf352bc9e168396e531. jpg
jpg
МОСКВА, 18 авг — РИА Новости, Альфия Еникеева. В самом начале пандемии появлялись сообщения о том, что в странах, где население массово привито противотуберкулезной вакциной, люди реже заболевают ковидом и меньше от него умирают. Позже информацию опровергли, однако недавно ученые выяснили: БЦЖ все-таки полезна при терапии от коронавируса, поскольку способствует снижению в крови уровня провоспалительных цитокинов — они часто становятся причиной так называемого цитокинового шторма. Это не первые данные о неожиданных побочных эффектах этой вакцины. Среди них — защита от лепры, некоторых видов рака и диабета. От чего еще помогает БЦЖ, разбиралось РИА Новости.Призрачная защитаВ марте 2020-го группа ученых из Нью-Йорка, проанализировав данные по заболеваемости ковидом в разных частях света, обнаружила: там, где детей массово прививают противотуберкулезной вакциной, эпидемия разворачивается медленнее, а смертность от болезни в несколько раз ниже. Исследователи выложили наблюдения в виде препринта на сайте medRxiv, где публикуют медицинские статьи, которые пока не прошли рецензирование и не появились в научном журнале. Уже через несколько недель похожую информацию опубликовали — тоже в виде препринта — эпидемиологи из Техасского университета (США). Собрали сведения о заболеваемости на тот момент в 178 странах, и по их подсчетам получилось: количество инфицированных на душу населения в государствах с обязательной вакцинацией от туберкулеза ниже примерно в десять раз, чем там, где БЦЖ больше не делают. При этом разница в количестве погибших от ковида — почти в 20 раз. По мнению ученых из СПбГУ, объясняется это тем, что прививка против туберкулеза в младенчестве способна серьезно повлиять на только на складывающийся иммунитет: «Раннее и продолжительное воздействие штамма вакцины на формирующуюся иммунную систему обеспечивает адъювантный эффект — усиливает иммунный ответ организма на различные, в том числе многие инфекционные антигены». Таким образом, страны, где до сих пор активно прививают от туберкулеза, должны были значительно меньше пострадать от нового коронавируса. Однако этого не произошло. В частности, Россию, где каждому новорожденному на третий день жизни делают БЦЖ, накрыло уже тремя волнами эпидемии.
Уже через несколько недель похожую информацию опубликовали — тоже в виде препринта — эпидемиологи из Техасского университета (США). Собрали сведения о заболеваемости на тот момент в 178 странах, и по их подсчетам получилось: количество инфицированных на душу населения в государствах с обязательной вакцинацией от туберкулеза ниже примерно в десять раз, чем там, где БЦЖ больше не делают. При этом разница в количестве погибших от ковида — почти в 20 раз. По мнению ученых из СПбГУ, объясняется это тем, что прививка против туберкулеза в младенчестве способна серьезно повлиять на только на складывающийся иммунитет: «Раннее и продолжительное воздействие штамма вакцины на формирующуюся иммунную систему обеспечивает адъювантный эффект — усиливает иммунный ответ организма на различные, в том числе многие инфекционные антигены». Таким образом, страны, где до сих пор активно прививают от туберкулеза, должны были значительно меньше пострадать от нового коронавируса. Однако этого не произошло. В частности, Россию, где каждому новорожденному на третий день жизни делают БЦЖ, накрыло уже тремя волнами эпидемии. Статьи о защите от ковида, которую якобы дает противотуберкулезная прививка, подверглись серьезной критике научного сообщества. Последний гвоздь в крышку гроба гипотезы вбили ученые из Университета Пенсильвании (США). В апрельской статье в Nature они заявили: на ранних этапах пандемии разница в заболеваемости между странами, где делают и не делают БЦЖ, действительно была. Но теперь она полностью исчезла, и на распространение коронавирусной инфекции сейчас влияют антиковидные вакцины. Нет дыма без огняОднако предположения исследователей о неожиданном побочном эффекте противотуберкулезной вакцины возникли не на пустом месте.Во-первых, БЦЖ точно защищает от лепры (ее еще называют проказой). Дело в том, что эту болезнь, как и туберкулез, вызывают микобактерии, правда, другого рода: Mycobacterium leprae. Они и палочки Коха — возбудители туберкулеза — обладают сходными белками на поверхности клеток. Именно поэтому антитела, которые организм научился производить против туберкулезных палочек, реагируют на их родственниц и запускают иммунный ответ.
Статьи о защите от ковида, которую якобы дает противотуберкулезная прививка, подверглись серьезной критике научного сообщества. Последний гвоздь в крышку гроба гипотезы вбили ученые из Университета Пенсильвании (США). В апрельской статье в Nature они заявили: на ранних этапах пандемии разница в заболеваемости между странами, где делают и не делают БЦЖ, действительно была. Но теперь она полностью исчезла, и на распространение коронавирусной инфекции сейчас влияют антиковидные вакцины. Нет дыма без огняОднако предположения исследователей о неожиданном побочном эффекте противотуберкулезной вакцины возникли не на пустом месте.Во-первых, БЦЖ точно защищает от лепры (ее еще называют проказой). Дело в том, что эту болезнь, как и туберкулез, вызывают микобактерии, правда, другого рода: Mycobacterium leprae. Они и палочки Коха — возбудители туберкулеза — обладают сходными белками на поверхности клеток. Именно поэтому антитела, которые организм научился производить против туберкулезных палочек, реагируют на их родственниц и запускают иммунный ответ. Такое явление называют кросс-реактивностью. Во-вторых, еще в 2013-м датские, нидерландские и американские ученые обнаружили, что БЦЖ снижает детскую смертность вообще от всех причин в два-три раза. Тогда исследователи предположили: дело не в защите от туберкулеза, ведь младенцы им практически не болеют. Кроме того, от самой болезни вакцина как раз предохраняет не всегда. А значит, срабатывает неизвестный ранее механизм иммунологической памяти, благодаря которому БЦЖ тренирует врожденный иммунитет против огромного количества патогенов — неважно, вирусов, бактерий или грибков.Скорее всего, после встречи с ослабленной бычьей туберкулезной палочкой — именно она входит в состав вакцины — в организме остаются не только специфические Т- и В-лимфоциты, но и клетки врожденного иммунитета с измененным обменом веществ. Они генерируют больше сигнальных молекул, из-за чего происходят эпигенетические сдвиги: одни гены перестают работать, другие, наоборот, становятся активнее. Как следствие, меняется и набор выделяемых этими клетками веществ, что, в свою очередь, помогает иммунитету справляться не только со знакомыми, но и с неизвестными ему патогенами.
Такое явление называют кросс-реактивностью. Во-вторых, еще в 2013-м датские, нидерландские и американские ученые обнаружили, что БЦЖ снижает детскую смертность вообще от всех причин в два-три раза. Тогда исследователи предположили: дело не в защите от туберкулеза, ведь младенцы им практически не болеют. Кроме того, от самой болезни вакцина как раз предохраняет не всегда. А значит, срабатывает неизвестный ранее механизм иммунологической памяти, благодаря которому БЦЖ тренирует врожденный иммунитет против огромного количества патогенов — неважно, вирусов, бактерий или грибков.Скорее всего, после встречи с ослабленной бычьей туберкулезной палочкой — именно она входит в состав вакцины — в организме остаются не только специфические Т- и В-лимфоциты, но и клетки врожденного иммунитета с измененным обменом веществ. Они генерируют больше сигнальных молекул, из-за чего происходят эпигенетические сдвиги: одни гены перестают работать, другие, наоборот, становятся активнее. Как следствие, меняется и набор выделяемых этими клетками веществ, что, в свою очередь, помогает иммунитету справляться не только со знакомыми, но и с неизвестными ему патогенами. Впрочем, научное сообщество к работам этой команды относится прохладно. Их публикации не раз критиковали за неточности методологии. Эксперты ВОЗ и вовсе заключили: дополнительные преимущества БЦЖ настолько малы, что их не стоит принимать в расчет. Кто, если не БЦЖТем не менее положительные побочные эффекты БЦЖ могут быть связаны не только с вакцинацией во младенчестве. Некоторые исследователи предлагают использовать этот препарат в терапии рассеянного склероза. Как показали испытания на пациентах, введение вакцины сразу после первых проявлений болезни значительно тормозит ее развитие. Инъекции БЦЖ помогают и против диабета первого типа. Главная проблема при этом аутоиммунном заболевании — разрушение поджелудочной железы, которая синтезирует инсулин. В результате из-за нехватки гормона глюкоза перестает поступать в клетки, а ее уровень в крови повышается. Поэтому медики вводят больным инсулин, однако такое лечение никак не влияет на саму поджелудочную железу — она продолжает деградировать.
Впрочем, научное сообщество к работам этой команды относится прохладно. Их публикации не раз критиковали за неточности методологии. Эксперты ВОЗ и вовсе заключили: дополнительные преимущества БЦЖ настолько малы, что их не стоит принимать в расчет. Кто, если не БЦЖТем не менее положительные побочные эффекты БЦЖ могут быть связаны не только с вакцинацией во младенчестве. Некоторые исследователи предлагают использовать этот препарат в терапии рассеянного склероза. Как показали испытания на пациентах, введение вакцины сразу после первых проявлений болезни значительно тормозит ее развитие. Инъекции БЦЖ помогают и против диабета первого типа. Главная проблема при этом аутоиммунном заболевании — разрушение поджелудочной железы, которая синтезирует инсулин. В результате из-за нехватки гормона глюкоза перестает поступать в клетки, а ее уровень в крови повышается. Поэтому медики вводят больным инсулин, однако такое лечение никак не влияет на саму поджелудочную железу — она продолжает деградировать. А вот инъекции БЦЖ, как выяснилось, эту проблему решают. Во-первых, приглушают аутоиммунную атаку организма на железу. Во-вторых, нормализуют глюкозный метаболизм лимфоцитов: глюкоза из плазмы крови начинает поступать в клетки, и ее концентрация в крови снижается. Кроме того, есть сразу несколько работ, показывающих эффективность БЦЖ в терапии рака мочевого пузыря, лейкемии, лимфомы и меланомы. При этих заболеваниях вакцина усиливает иммунный ответ и помогает организму вовремя распознать раковые клетки, которые маскируются под нормальные. Впрочем, эксперты Кокрейнского общества пока относятся к таким работам скептически и считают приведенные доказательства недостаточными. Палочка от ковидаИ вот совсем недавно появились данные, что БЦЖ все-таки может быть полезна в лечении ковида. В начале августа индийские ученые выдвинули гипотезу, что прививка снижает циркуляцию в крови пациентов провоспалительных цитокинов, которые вызывают цитокиновый шторм. При этом состоянии собственные лейкоциты больного, охотясь на зараженные клетки, разрушают ткань легкого и приводят к гипервоспалению, с которым организм не в силах справиться.
А вот инъекции БЦЖ, как выяснилось, эту проблему решают. Во-первых, приглушают аутоиммунную атаку организма на железу. Во-вторых, нормализуют глюкозный метаболизм лимфоцитов: глюкоза из плазмы крови начинает поступать в клетки, и ее концентрация в крови снижается. Кроме того, есть сразу несколько работ, показывающих эффективность БЦЖ в терапии рака мочевого пузыря, лейкемии, лимфомы и меланомы. При этих заболеваниях вакцина усиливает иммунный ответ и помогает организму вовремя распознать раковые клетки, которые маскируются под нормальные. Впрочем, эксперты Кокрейнского общества пока относятся к таким работам скептически и считают приведенные доказательства недостаточными. Палочка от ковидаИ вот совсем недавно появились данные, что БЦЖ все-таки может быть полезна в лечении ковида. В начале августа индийские ученые выдвинули гипотезу, что прививка снижает циркуляцию в крови пациентов провоспалительных цитокинов, которые вызывают цитокиновый шторм. При этом состоянии собственные лейкоциты больного, охотясь на зараженные клетки, разрушают ткань легкого и приводят к гипервоспалению, с которым организм не в силах справиться. В ходе эксперимента исследователи ввели БЦЖ 82 добровольцам в возрасте от 60 до 80 лет. Антител к коронавирусу у них не было. Еще 55 их ровесников вошли в контрольную группу. Через месяц после вакцинации уровень провоспалительных цитокинов в крови привитых оказался значительно ниже, чем у остальных. Кроме того, в их плазме уменьшилась концентрация хемокинов — цитокинов, стимулирующих миграцию лейкоцитов из крови в ткани.Основываясь на этих результатах, авторы работы предположили: вовремя проведенная вакцинация БЦЖ сможет предотвратить развитие гипериммунного ответа при коронавирусной инфекции, а значит, спасти многие жизни.
В ходе эксперимента исследователи ввели БЦЖ 82 добровольцам в возрасте от 60 до 80 лет. Антител к коронавирусу у них не было. Еще 55 их ровесников вошли в контрольную группу. Через месяц после вакцинации уровень провоспалительных цитокинов в крови привитых оказался значительно ниже, чем у остальных. Кроме того, в их плазме уменьшилась концентрация хемокинов — цитокинов, стимулирующих миграцию лейкоцитов из крови в ткани.Основываясь на этих результатах, авторы работы предположили: вовремя проведенная вакцинация БЦЖ сможет предотвратить развитие гипериммунного ответа при коронавирусной инфекции, а значит, спасти многие жизни.
https://ria.ru/20200403/1569536977.html
https://ria.ru/20200330/1569372986.html
https://ria.ru/20210726/tuberkulez-1742850449.html
https://ria.ru/20210331/epidemiya-1603505952.html
сша
пенсильвания
россия
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og. xn--p1ai/awards/
xn--p1ai/awards/
2021
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
Новости
ru-RU
https://ria.ru/docs/about/copyright.html
https://xn--c1acbl2abdlkab1og.xn--p1ai/
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
https://cdnn21.img.ria.ru/images/07e5/08/0b/1745365698_164:54:1253:871_1920x0_80_0_0_f9deb476273c46e15e926bd8fcd3c040.jpgРИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
туберкулез, вакцинация, прививки, сша, пенсильвания, санкт-петербургский государственный университет, воз, здоровье, диабет, рак, биология, вакцины, россия, коронавирус covid-19, рассеянный склероз
МОСКВА, 18 авг — РИА Новости, Альфия Еникеева. В самом начале пандемии появлялись сообщения о том, что в странах, где население массово привито противотуберкулезной вакциной, люди реже заболевают ковидом и меньше от него умирают. Позже информацию опровергли, однако недавно ученые выяснили: БЦЖ все-таки полезна при терапии от коронавируса, поскольку способствует снижению в крови уровня провоспалительных цитокинов — они часто становятся причиной так называемого цитокинового шторма. Это не первые данные о неожиданных побочных эффектах этой вакцины. Среди них — защита от лепры, некоторых видов рака и диабета. От чего еще помогает БЦЖ, разбиралось РИА Новости.
В самом начале пандемии появлялись сообщения о том, что в странах, где население массово привито противотуберкулезной вакциной, люди реже заболевают ковидом и меньше от него умирают. Позже информацию опровергли, однако недавно ученые выяснили: БЦЖ все-таки полезна при терапии от коронавируса, поскольку способствует снижению в крови уровня провоспалительных цитокинов — они часто становятся причиной так называемого цитокинового шторма. Это не первые данные о неожиданных побочных эффектах этой вакцины. Среди них — защита от лепры, некоторых видов рака и диабета. От чего еще помогает БЦЖ, разбиралось РИА Новости.
Призрачная защита
В марте 2020-го группа ученых из Нью-Йорка, проанализировав данные по заболеваемости ковидом в разных частях света, обнаружила: там, где детей массово прививают противотуберкулезной вакциной, эпидемия разворачивается медленнее, а смертность от болезни в несколько раз ниже. Исследователи выложили наблюдения в виде препринта на сайте medRxiv, где публикуют медицинские статьи, которые пока не прошли рецензирование и не появились в научном журнале. Уже через несколько недель похожую информацию опубликовали — тоже в виде препринта — эпидемиологи из Техасского университета (США). Собрали сведения о заболеваемости на тот момент в 178 странах, и по их подсчетам получилось: количество инфицированных на душу населения в государствах с обязательной вакцинацией от туберкулеза ниже примерно в десять раз, чем там, где БЦЖ больше не делают. При этом разница в количестве погибших от ковида — почти в 20 раз. По мнению ученых из СПбГУ, объясняется это тем, что прививка против туберкулеза в младенчестве способна серьезно повлиять на только на складывающийся иммунитет: «Раннее и продолжительное воздействие штамма вакцины на формирующуюся иммунную систему обеспечивает адъювантный эффект — усиливает иммунный ответ организма на различные, в том числе многие инфекционные антигены». Таким образом, страны, где до сих пор активно прививают от туберкулеза, должны были значительно меньше пострадать от нового коронавируса. Однако этого не произошло. В частности, Россию, где каждому новорожденному на третий день жизни делают БЦЖ, накрыло уже тремя волнами эпидемии.
Уже через несколько недель похожую информацию опубликовали — тоже в виде препринта — эпидемиологи из Техасского университета (США). Собрали сведения о заболеваемости на тот момент в 178 странах, и по их подсчетам получилось: количество инфицированных на душу населения в государствах с обязательной вакцинацией от туберкулеза ниже примерно в десять раз, чем там, где БЦЖ больше не делают. При этом разница в количестве погибших от ковида — почти в 20 раз. По мнению ученых из СПбГУ, объясняется это тем, что прививка против туберкулеза в младенчестве способна серьезно повлиять на только на складывающийся иммунитет: «Раннее и продолжительное воздействие штамма вакцины на формирующуюся иммунную систему обеспечивает адъювантный эффект — усиливает иммунный ответ организма на различные, в том числе многие инфекционные антигены». Таким образом, страны, где до сих пор активно прививают от туберкулеза, должны были значительно меньше пострадать от нового коронавируса. Однако этого не произошло. В частности, Россию, где каждому новорожденному на третий день жизни делают БЦЖ, накрыло уже тремя волнами эпидемии. Статьи о защите от ковида, которую якобы дает противотуберкулезная прививка, подверглись серьезной критике научного сообщества. Последний гвоздь в крышку гроба гипотезы вбили ученые из Университета Пенсильвании (США). В апрельской статье в Nature они заявили: на ранних этапах пандемии разница в заболеваемости между странами, где делают и не делают БЦЖ, действительно была. Но теперь она полностью исчезла, и на распространение коронавирусной инфекции сейчас влияют антиковидные вакцины. 3 апреля 2020, 13:31Распространение коронавирусаВрач оценил влияние прививки от туберкулеза на течение коронавируса
Статьи о защите от ковида, которую якобы дает противотуберкулезная прививка, подверглись серьезной критике научного сообщества. Последний гвоздь в крышку гроба гипотезы вбили ученые из Университета Пенсильвании (США). В апрельской статье в Nature они заявили: на ранних этапах пандемии разница в заболеваемости между странами, где делают и не делают БЦЖ, действительно была. Но теперь она полностью исчезла, и на распространение коронавирусной инфекции сейчас влияют антиковидные вакцины. 3 апреля 2020, 13:31Распространение коронавирусаВрач оценил влияние прививки от туберкулеза на течение коронавирусаНет дыма без огня
Однако предположения исследователей о неожиданном побочном эффекте противотуберкулезной вакцины возникли не на пустом месте.
Во-первых, БЦЖ точно защищает от лепры (ее еще называют проказой). Дело в том, что эту болезнь, как и туберкулез, вызывают микобактерии, правда, другого рода: Mycobacterium leprae. Они и палочки Коха — возбудители туберкулеза — обладают сходными белками на поверхности клеток. Именно поэтому антитела, которые организм научился производить против туберкулезных палочек, реагируют на их родственниц и запускают иммунный ответ. Такое явление называют кросс-реактивностью.
Именно поэтому антитела, которые организм научился производить против туберкулезных палочек, реагируют на их родственниц и запускают иммунный ответ. Такое явление называют кросс-реактивностью.
А значит, срабатывает неизвестный ранее механизм иммунологической памяти, благодаря которому БЦЖ тренирует врожденный иммунитет против огромного количества патогенов — неважно, вирусов, бактерий или грибков.
Скорее всего, после встречи с ослабленной бычьей туберкулезной палочкой — именно она входит в состав вакцины — в организме остаются не только специфические Т- и В-лимфоциты, но и клетки врожденного иммунитета с измененным обменом веществ. Они генерируют больше сигнальных молекул, из-за чего происходят эпигенетические сдвиги: одни гены перестают работать, другие, наоборот, становятся активнее. Как следствие, меняется и набор выделяемых этими клетками веществ, что, в свою очередь, помогает иммунитету справляться не только со знакомыми, но и с неизвестными ему патогенами.
Они генерируют больше сигнальных молекул, из-за чего происходят эпигенетические сдвиги: одни гены перестают работать, другие, наоборот, становятся активнее. Как следствие, меняется и набор выделяемых этими клетками веществ, что, в свою очередь, помогает иммунитету справляться не только со знакомыми, но и с неизвестными ему патогенами.
26 июля 2021, 06:05
В России снизилась заболеваемость туберкулезомКто, если не БЦЖ
Тем не менее положительные побочные эффекты БЦЖ могут быть связаны не только с вакцинацией во младенчестве. Некоторые исследователи предлагают использовать этот препарат в терапии рассеянного склероза. Как показали испытания на пациентах, введение вакцины сразу после первых проявлений болезни значительно тормозит ее развитие. Инъекции БЦЖ помогают и против диабета первого типа. Главная проблема при этом аутоиммунном заболевании — разрушение поджелудочной железы, которая синтезирует инсулин. В результате из-за нехватки гормона глюкоза перестает поступать в клетки, а ее уровень в крови повышается. Поэтому медики вводят больным инсулин, однако такое лечение никак не влияет на саму поджелудочную железу — она продолжает деградировать.
Инъекции БЦЖ помогают и против диабета первого типа. Главная проблема при этом аутоиммунном заболевании — разрушение поджелудочной железы, которая синтезирует инсулин. В результате из-за нехватки гормона глюкоза перестает поступать в клетки, а ее уровень в крови повышается. Поэтому медики вводят больным инсулин, однако такое лечение никак не влияет на саму поджелудочную железу — она продолжает деградировать.А вот инъекции БЦЖ, как выяснилось, эту проблему решают. Во-первых, приглушают аутоиммунную атаку организма на железу. Во-вторых, нормализуют глюкозный метаболизм лимфоцитов: глюкоза из плазмы крови начинает поступать в клетки, и ее концентрация в крови снижается.
Кроме того, есть сразу несколько работ, показывающих эффективность БЦЖ в терапии рака мочевого пузыря, лейкемии, лимфомы и меланомы. При этих заболеваниях вакцина усиливает иммунный ответ и помогает организму вовремя распознать раковые клетки, которые маскируются под нормальные. Впрочем, эксперты Кокрейнского общества пока относятся к таким работам скептически и считают приведенные доказательства недостаточными. 31 марта 2021, 08:00НаукаВыжили сильнейшие. Во что человека превратили смертельные эпидемии
31 марта 2021, 08:00НаукаВыжили сильнейшие. Во что человека превратили смертельные эпидемииПалочка от ковида
И вот совсем недавно появились данные, что БЦЖ все-таки может быть полезна в лечении ковида. В начале августа индийские ученые выдвинули гипотезу, что прививка снижает циркуляцию в крови пациентов провоспалительных цитокинов, которые вызывают цитокиновый шторм. При этом состоянии собственные лейкоциты больного, охотясь на зараженные клетки, разрушают ткань легкого и приводят к гипервоспалению, с которым организм не в силах справиться.В ходе эксперимента исследователи ввели БЦЖ 82 добровольцам в возрасте от 60 до 80 лет. Антител к коронавирусу у них не было. Еще 55 их ровесников вошли в контрольную группу. Через месяц после вакцинации уровень провоспалительных цитокинов в крови привитых оказался значительно ниже, чем у остальных. Кроме того, в их плазме уменьшилась концентрация хемокинов — цитокинов, стимулирующих миграцию лейкоцитов из крови в ткани.
Основываясь на этих результатах, авторы работы предположили: вовремя проведенная вакцинация БЦЖ сможет предотвратить развитие гипериммунного ответа при коронавирусной инфекции, а значит, спасти многие жизни.
Развитие вакцинопрофилактики | ГОБУЗ «Кольская ЦРБ»
24 марта 1882 года, когда Роберт Кох объявил о том, что сумел выделить бактерию, вызывающую туберкулёз, ученый достиг величайшего за всю свою жизнь триумфа.
Почему все же именно открытие возбудителя туберкулеза называют научным подвигом?
Дело в том, что возбудители болезни туберкулеза – чрезвычайно трудный объект для исследования. В первых препаратах для микроскопии, сделанных Кохом из легочной ткани молодого рабочего, умершего от скоротечной чахотки, ни одного микроба обнаружить не удалось. Не теряя надежды, ученый провел окраску препаратов по собственной методике и впервые под микроскопом увидел неуловимого возбудителя туберкулеза.
На следующем этапе необходимо было получить пресловутые микробактерии в чистой культуре. Еще несколько лет назад Кох нашел способ культивирования микробов не только на подопытных животных, но и в искусственной среде, например, на разрезе сваренного картофеля или в мясном бульоне.
Желая создать питательную среду, подобную живым тканям, Кох решил применить сыворотку животной крови, которую ему удалось раздобыть на бойне. И действительно, в этой среде бактерии быстро размножались. Полученными таким образом чистыми культурами бактерий Кох заразил несколько сотен подопытных животных разных видов, и все они заболели туберкулезом. Ученому было ясно, что возбудитель заболевания найден. В это время мир был возбужден открытым Пастером методом предупреждения заразных болезней с помощью прививок ослабленных культур бактерий, вызывающих данную болезнь. Поэтому Кох считал, что ему удастся тем же способом спасти человечество от туберкулеза.
Он приготовил вакцину из ослабленных бактерий туберкулеза, но предупредить заболевание с помощью этой вакцины ему не удалось. Вакцина эта под названием «туберкулина» до сих пор применяется как вспомогательное средство при диагностике туберкулеза. Кроме этого, Кох открыл бациллу сибирской язвы, холерный вибрион. В 1905 году за «исследования и открытия, касающиеся лечения туберкулеза» ученый был удостоен Нобелевской премии по физиологии и медицине.
26 декабря 1891 года Эмиль фон Беринг спас жизнь больному ребенку, сделав ему первую прививку от дифтерии.
До начала XX века дифтерия ежегодно уносила тысячи детских жизней, а медицина была бессильна облегчить их страдания и спасти от тяжелой агонии.
Немецкий бактериолог Фридрих Лёффлер в 1884 году сумел открыть бактерии, вызывающие дифтерию — палочки Corynebacterium diphtheriae. А ученик Пастера Пьер Эмиль Ру показал, как действуют палочки дифтерии и доказал, что все общие явления дифтерии — упадок сердечной деятельности, параличи и прочие смертельные последствия – вызваны не самой бактерией, а вырабатываемым ею ядовитым веществом (токсином), и что вещество это, введенное в организм, вызывает эти явления само по себе, при полном отсутствии в организме дифтерийных микробов.
Но Ру не умел обезвредить яд и не мог найти способ спасения больных детей. В этом ему помог ассистент Коха Беринг. В поисках средства, которое убивало бы бактерии дифтерии, Беринг делал прививки зараженным животным из разных веществ, но животные погибали. Однажды для прививки он использовал трихлорид йода. Правда, и на этот раз морские свинки тяжело заболели, но ни одна из них не погибла.
Воодушевленный первой удачей, Беринг, дождавшись выздоровления подопытных свинок, сделал им прививку, содержавшую дифтерийный токсин. Животные превосходно выдержали прививку, несмотря на то, что получили огромную дозу токсина. Затем ученый выяснил, что если сыворотку крови перенесших дифтерию и выздоровевших морских свинок ввести заболевшим животным, те выздоравливают. Значит, в крови переболевших появляется какой-то антитоксин, который нейтрализует токсин дифтерийной палочки.
В конце 1891 года в клинике детских болезней в Берлине, переполненной детьми, умирающими от дифтерии, была сделана прививка с антитоксином – и ребенок выздоровел.
В 1894 году усовершенствованная сыворотка была успешно опробована на 220 больных детях. За спасение детей Берингу в 1901 году была присуждена первая Нобелевская премия по физиологии и медицине «за работу по сывороточной терапии, главным образом, за её применение при лечении дифтерии, что открыло новые пути в медицинской науке и дало в руки врачам победоносное оружие против болезни и смерти».
Уже позже, в 1913 году, Беринг предложил введение смеси токсина и антитоксина для выработки у детей активного иммунитета. И это оказалось наиболее действенным средством защиты (пассивный иммунитет, возникающий после введения одного только антитоксина, недолговечен). Профилактическая сыворотка, которая употребляется теперь против дифтерии, была найдена
Профилактическая сыворотка, которая употребляется теперь против дифтерии, была найдена
В конце XIX в. немецкий ученый Пауль Эрлих (1854-1915) положил начало учению об антителах как факторах гуморального иммунитета. Бурная полемика и многочисленные исследования, предпринятые после этого открытия, привели к весьма плодотворным результатам: было установлено, что иммунитет определяется как клеточными, так и гуморальными факторами. Таким образом, было создано учение об иммунитете. П. Эрлих в 1908 г. был удостоен Нобелевской премии по физиологии за создание клеточной теории иммунитета, которую он разделил с Ильей Ильичом Мечниковым.
1892 год считается годом открытия новых организмов — вирусов.
Впервые существование вируса (как нового типа возбудителя болезней) доказал русский учёный Дмитрий Иосифович Ивановский. Дмитрий Иосифович обнаружил вирусы в результате изучения заболевания табачных растений.
Дмитрий Иосифович обнаружил вирусы в результате изучения заболевания табачных растений.
Пытаясь найти возбудителя опасной болезни – табачной мозаики (проявляется на многих, особенно тепличных растениях в виде скручивающихся трубочкой, желтеющих и опадающих листьев, в некрозе плодов, нарастающих боковых почек), Ивановский несколько лет занимался исследованиями в Никитском ботаническом саду под Ялтой и в ботанической лаборатории АН.
Зная из работ голландского ботаника А.Д. Майера о том, что мозаичную болезнь табака можно вызвать переносом сока больных растений здоровым, ученый растирал листья больных растений, процеживал сок через полотняный фильтр и впрыскивал его в жилки здоровых листьев табака. Как правило, инфицированные растения перенимали болезнь.
Ботаник тщательно изучал под микроскопом больные листья, но не обнаружил ни бактерий, ни еще каких-либо микроорганизмов, что неудивительно, так как вирусы размером от 20 до 300 нм (1 нм = 109 м) на два порядка меньше бактерий, и их в оптический микроскоп увидеть нельзя.
Попытка вырастить возбудителя мозаики на обычных питательных средах, как это делается с теми же бактериями, не увенчалась успехом. Обнаружив в клетках инфицированных растений кристаллические включения (кристаллы «И»), ученый пришел к выводу, что возбудителем мозаичной болезни является твердое инфекционное начало – либо фильтрующиеся бактерии, не способные расти на искусственных субстратах, либо неведомые и невидимые микроорганизмы, выделяющие токсины.
О своих наблюдениях Ивановский доложил в 1892 г. на заседании Императорской АН. Исследования Ивановского подхватили ученые во всем мире. Использовав метод фильтрации русского ученого, немецкие врачи Ф. Лефлер и П. Фрош в 1897 г. обнаружили возбудителя ящура крупного рогатого скота. Затем последовал бум открытий вирусов – желтой лихорадки, чумы, бешенства, натуральной оспы, полиомиелита и т. д. В 1917 году были открыты бактериофаги – вирусы, разрушающие бактерии. Естественно, каждое открытие не было задачей «чистой» науки, за ним тут же следовало приготовление противоядия – вакцины, лечение и профилактика заболевания.
обнаружили возбудителя ящура крупного рогатого скота. Затем последовал бум открытий вирусов – желтой лихорадки, чумы, бешенства, натуральной оспы, полиомиелита и т. д. В 1917 году были открыты бактериофаги – вирусы, разрушающие бактерии. Естественно, каждое открытие не было задачей «чистой» науки, за ним тут же следовало приготовление противоядия – вакцины, лечение и профилактика заболевания.
1921 год ознаменовался изобретением живой бактериальной вакцины против туберкулеза (БЦЖ).
Туберкулез перестал считаться смертельно опасным заболеванием, когда микробиолог Альбер Кальметт и ветеринар Камиль Герен разработали во Франции в 1908-1921 годах первую вакцину для человека на основе штамма ослабленной живой коровьей туберкулезной бациллы.
В 1908 году они работали в Институте Пастера в Лилле. Их деятельность охватывала получение культур туберкулёзной палочки и исследования различных питательных сред. При этом ученые выяснили, что на питательной среде на основе глицерина, жёлчи и картофеля вырастают туберкулёзные палочки наименьшей вирулентности (от лат. virulentus— ядовитый, сумма свойств микроба, определяющая его болезнетворное действие).
virulentus— ядовитый, сумма свойств микроба, определяющая его болезнетворное действие).
С этого момента они изменили ход исследования, чтобы выяснить, нельзя ли посредством повторяющегося культивирования вырастить ослабленный штамм для производства вакцины. Исследования продлились до 1919 года, когда вакцина с невирулентными (ослабленными) бактериями не вызвала туберкулёз у подопытных животных. В 1921 году ученые создали вакцину БЦЖ (BCG – Bacille bilie’ Calmette-Gue’rin) для применения на людях.
Общественное признание вакцины проходило с трудом, в частности, из-за случавшихся трагедий. В Любеке 240 новорождённых были привиты в 10-дневном возрасте. Все они заболели туберкулёзом, 77 из них умерли. Расследование показало, что вакцина была заражена вирулентным (неослабленным) штаммом, который хранился в том же инкубаторе. Вина была возложена на директора больницы, которого приговорили к 2 годам лишения свободы за халатность, повлёкшую смерть.
Многие страны, получившие от Кальметта и Герена штамм БЦЖ (1924-1925 гг. ), подтвердили его эффективность и вскоре перешли к ограниченной, а затем и к массовой вакцинации против туберкулеза. В СССР штамм БЦЖ был привезен Л.А. Тарасевичем в 1925 году и обозначен BCG-I.
), подтвердили его эффективность и вскоре перешли к ограниченной, а затем и к массовой вакцинации против туберкулеза. В СССР штамм БЦЖ был привезен Л.А. Тарасевичем в 1925 году и обозначен BCG-I.
Вакцина БЦЖ выдержала испытание временем, ее эффективность проверена и доказана практикой. В наши дни вакцина БЦЖ является основным препаратом для специфической профилактики туберкулеза, признанным и используемым во всем мире. Попытки приготовления противотуберкулезной вакцины из других ослабленных штаммов или отдельных фракций микробных клеток пока не дали значимых практических результатов.
В 1923 году французский иммунолог Г. Рамон получил столбнячный анатоксин, который стал применяться для профилактики заболевания. Научное изучение столбняка началось во второй половине XIX века. Возбудитель столбняка был открыт почти одновременно русским хирургом Н. Д. Монастырским (в 1883 году) и немецким ученым А. Николайером (в 1884 году). Чистую культуру микроорганизма выделил в 1887 г. японский микробиолог С. Китазато, он же в 1890 г. получил столбнячный токсин и (совместно с немецким бактериологом Э. Берингом) создал противостолбнячную сыворотку.
Николайером (в 1884 году). Чистую культуру микроорганизма выделил в 1887 г. японский микробиолог С. Китазато, он же в 1890 г. получил столбнячный токсин и (совместно с немецким бактериологом Э. Берингом) создал противостолбнячную сыворотку.
12 апреля 1955 г. в США успешно завершилось крупномасштабное исследование, подтвердившее эффективность вакцины Джонаса Солка – первой вакцины против полиомиелита. Эксперименты по созданию противополиомиелитной вакцины Солк начал в 1947 году. Вакцина из предварительно умерщвленных формалином полиовирусов была испытана Американским национальным фондом по борьбе с полиомиелитом. Впервые вакцина, созданная из предварительно умерщвленных формалином полиовирусов, прошла испытание в 1953-54 гг. (тогда ее тестировали добровольцы), а с 1955 года она получила уже широкое применение.
В исследовании приняло участие около 1 млн детей в возрасте 6-9 лет, из которых 440 тыс. получили вакцину Солка. По свидетельству очевидцев, родители с воодушевлением делали пожертвования на исследование и охотно записывали своих детей в ряды его участников. Сейчас это трудно представить, но в то время полиомиелит был самой грозной детской инфекцией, и родители со страхом ожидали прихода лета, когда регистрировался сезонный пик инфекции.
По свидетельству очевидцев, родители с воодушевлением делали пожертвования на исследование и охотно записывали своих детей в ряды его участников. Сейчас это трудно представить, но в то время полиомиелит был самой грозной детской инфекцией, и родители со страхом ожидали прихода лета, когда регистрировался сезонный пик инфекции.
Результаты пятилетнего, с 1956 по 1961 год, массового применения вакцины превзошли все ожидания: среди детей в возрастных группах, особенно подверженных инфекции, заболеваемость снизилась на 96%.
В 1954 г. в США было зарегистрировано более 38 тыс. случаев полиомиелита, а спустя 10-летие применения вакцины Солка, в 1965 г., количество случаев полиомиелита в этой стране составило всего 61.
В 1991 году Всемирная организация здравоохранения объявила, что в Западном полушарии полиомиелит побежден. В странах Азии и Африки, благодаря массовым вакцинациям, заболеваемость также резко снизилась. Позже вакцина Солка была заменена на более совершенную, разработанную Альбертом Сэйбином. Однако вклад Джонаса Солка в борьбу с полиомиелитом это ничуть не приуменьшило: в этой области он по сей день считается первопроходцем.
Однако вклад Джонаса Солка в борьбу с полиомиелитом это ничуть не приуменьшило: в этой области он по сей день считается первопроходцем.
В 1981-82 гг. стала доступной первая вакцина против гепатита В. Тогда в Китае приступили к использованию вакцины, приготовленной из плазмы крови, полученной от доноров из числа больных, которые имели продолжительную инфекцию вирусного гепатита В. В том же году она стала доступна и в США. Пик её применения пришёлся на 1982-88 гг. Вакцинацию проводили в виде курса из трёх прививок с временным интервалом. При постмаркетинговом наблюдении после введения такой вакцины отметили возникновение нескольких случаев побочных заболеваний центральной и периферической нервной системы. В исследовании привитых вакциной лиц, проведённом через 15 лет, подтверждена высокая иммуногенность вакцины, приготовленной из плазмы крови.
С 1987 г. на смену плазменной вакцине пришло следующее поколение вакцины против вируса гепатита В, в которой использована технология генной модификации рекомбинантной ДНК в клетках дрожжевого микроорганизма. Её иногда называют генно-инженерной вакциной. Синтезированный таким способом HBsAg выделяли из разрушаемых дрожжевых клеток. Ни один способ очистки не позволял избавляться от следов дрожжевых белков. Новая технология отличалась высокой производительностью, позволила удешевить производство и уменьшить риск, происходящий из плазменной вакцины.
Её иногда называют генно-инженерной вакциной. Синтезированный таким способом HBsAg выделяли из разрушаемых дрожжевых клеток. Ни один способ очистки не позволял избавляться от следов дрожжевых белков. Новая технология отличалась высокой производительностью, позволила удешевить производство и уменьшить риск, происходящий из плазменной вакцины.
В 1983 году Харальд цур Хаузен ему обнаружил ДНК папилломавируса в биопсии рака шейки матки, и это событие можно считать открытием онкогенного вируса ВПЧ-16.
Еще в 1976 году была выдвинута гипотеза о взаимосвязи вирусов папилломы человека (ВПЧ) с раком шейки матки. Некоторые разновидности ВПЧ безвредны, некоторые вызывают образование бородавок на коже, некоторые поражают половые органы (передаваясь половым путем). В середине семидесятых Харальд цур Хаузен обнаружил, что женщины, страдающие раком шейки матки, неизменно заражены ВПЧ.
В то время многие специалисты полагали, что рак шейки матки вызывается вирусом простого герпеса, но цур Хаузен нашел в раковых клетках не вирусы герпеса, а вирусы папилломы и предположил, что развитие рака происходит в результате заражения именно вирусом папилломы. Впоследствии ему и его коллегам удалось подтвердить эту гипотезу и установить, что большинство случаев рака шейки матки вызваны одним из двух типов этих вирусов: ВПЧ-16 и ВПЧ-18. Эти типы вируса обнаруживаются примерно в 70% случаях рака шейки матки. Зараженные такими вирусами клетки с довольно большой вероятностью рано или поздно становятся раковыми, и из них развивается злокачественная опухоль.
Впоследствии ему и его коллегам удалось подтвердить эту гипотезу и установить, что большинство случаев рака шейки матки вызваны одним из двух типов этих вирусов: ВПЧ-16 и ВПЧ-18. Эти типы вируса обнаруживаются примерно в 70% случаях рака шейки матки. Зараженные такими вирусами клетки с довольно большой вероятностью рано или поздно становятся раковыми, и из них развивается злокачественная опухоль.
Исследования Харальда цур Хаузена в области ВПЧ-инфекции легли в основу понимания механизмов канцерогенеза, индуцированного вирусом папилломы. Впоследствии были разработаны вакцины, которые позволяют предотвратить инфекцию вирусами ВПЧ-16 и ВПЧ-18. Это лечение позволяет сократить объем хирургического вмешательства и в целом снизить угрозу, представляемую раком шейки матки.
В 2008 году Нобелевский комитет присудил Нобелевскую премию в области физиологии и медицины Харальду цур Хаузену за открытие того, что вирус папилломы может вызывать рак шейки матки.
Прививки: быть или не быть?
Вопрос, ставить ли ребенку прививки, беспокоит многих родителей. Эта тема связана со множеством страхов, мифов и сомнений. Мы задали самые волнующие вопросы педиатру «ЕвроМед клиники» Елене Сергеевне Кочетковой.
— Елена Сергеевна, может ли быть два мнения по вопросу того, ставить ли прививки ребенку?
— Однозначно нет! Вакцинация – это единственный способ уберечь ребенка от множества опасных (и порой смертельно опасных) инфекций. Многие родители боятся осложнений после прививок, но уверяю вас, риск осложнений от перенесенных инфекций в разы выше. Если говорить про осложнения после прививок, то для начала надо различать нежелательные побочные эффекты и действительно реальные осложнения. Побочные эффекты обычно легко переносятся ребенком и быстро проходят. Что касается серьезных осложнений после прививок, то могу сказать, что за свою более чем 30-летнюю практику я всего два раза сталкивалась с действительно непредсказуемыми и серьезными осложнениями у детей. Да и то нельзя сказать, что они были совсем уж криминальными.
Да и то нельзя сказать, что они были совсем уж криминальными.
Обычно же осложнений можно избежать, подготовить ребенка к вакцинации с учетом его анамнеза, имеющихся у него заболеваний, аллергий.
— В каких случаях прививку не ставят по медицинским показаниям?
— Большинство наших медотводов – чисто российская перестраховка, уступка тревожным родителям. Заграницей основанием к временному отказу от прививки будет считаться, например, высокая температура, а у нас даже насморк, который был три дня назад для многих является поводом отложить прививку. В большинстве случаев прививка не влияет на выздоровление, так же, как выздоровление не влияет на прививку. Но у нас принято всё, что происходит с ребенком в течение длительного времени после введения вакцины, списывать на прививку. Мы забываем золотое правило: «после» не значит «вследствие».
Разумеется, есть случаи, когда вакцинацию лучше отложить. Это острое состояние при аллергии (в период ремиссии вакцинация аллергикам не просто можно, а нужно делать), высокая температура, ОРВИ, некоторые неврологические заболевания.Отдельный случай, когда вакцинацию рекомендуется отложить – наличие у ребенка до года доброкачественной нейтропении. Это состояние связано с адаптацией ребенка к нашим городским условиям, современным нагрузкам; проявляется тем, что в анализе крови наблюдается недостаточное количество нейтрофилов. Причем это количество не укладывается ни в норму, ни в состояние при болезни, а находится в среднем значении. В такой ситуации лучше не нагружать организм дополнительно, его иммунные силы сейчас и так ослаблены, и все силы направлены на то, чтобы адаптироваться к окружающей среде.
— Можно ли ставить прививки детям, склонным к аллергии, часто болеющим?
— В первую очередь! Конечно, в остром состоянии прививки не ставят. Но в состоянии ремиссии прививаться обязательно. Сами посудите, если ребенок часто болеющий, ослабленный, заразится какой-то серьезной инфекцией, то как он будет болеть? С высокой долей вероятности – очень тяжело, скорее всего, с осложнениями. Что касается аллергиков, то с ними дополнительно возникнет проблема – как их лечить, как он среагирует на заболевание, на лекарственные препараты. Опять же велик риск того, что заболевание будет протекать в тяжелой форме.
Что касается аллергиков, то с ними дополнительно возникнет проблема – как их лечить, как он среагирует на заболевание, на лекарственные препараты. Опять же велик риск того, что заболевание будет протекать в тяжелой форме.
Поэтому аллергикам, часто болеющим детям, пациентам с пороком сердца вакцинация нужна обязательно.
— Есть мнение, что вакцинация может спровоцировать развитие аллергии у ребенка. Это так?
— Прямой связи здесь, конечно, нет. Но если у ребенка есть предрасположенность к аллергии, введение вакцины может послужить толчком к развитию заболевания. В данной ситуации сложно предположить, что опаснее, потому что сама инфекция или лекарственные препараты так же могут спровоцировать развитие аллергии.
— Многие родители задаются вопросом, стоит ли ставить прививки от гепатита В и туберкулеза сразу в роддоме – ведь новорожденный малыш еще так слаб. Может быть, разумнее дать ему время адаптироваться, а эти прививки поставить позже – допустим, в 3-6 месяцев?
— Ребенок сразу после рождения (да и еще находясь в утробе матери!) сталкивается с сотней микроорганизмов, и успешно их обрабатывает. Так что дополнительные пара антигенов, которые ему введут во время вакцинации не играют уже особой роди на фоне этого.
Так что дополнительные пара антигенов, которые ему введут во время вакцинации не играют уже особой роди на фоне этого.
Иммунный ответ на БЦЖ (прививку от туберкулеза) развивается в течение 2-3 месяцев. Учитывая, что туберкулез встречается абсолютно во всех социальных слоях, в том числе среди весьма благополучных и обеспеченных людей, то когда же прививать ребенка, чтобы обеспечить ему надежную защиту?
Гепатит В – это такая болезнь, у которой в детском возрасте нет понятия «выздоровление». Если взрослый человек заболеет гепатитом В, то он имеет шанс взять его под контроль – при помощи соответствующего образа жизни и лекарственных препаратов. У детей же это невозможно. Они растут и поэтому гепатит у них может только активно прогрессировать.
В детском возрасте основной путь заражения гепатитом В – во время медицинских процедур. И никто не может знать, когда ребенку понадобиться медицинская помощь: неотложная операция, переливание крови после травмы, ДТП. Девочкам сейчас очень рано прокалывают уши – и это тоже риск заражения гепатитом.
Девочкам сейчас очень рано прокалывают уши – и это тоже риск заражения гепатитом.
Прививку от гепатита В неслучайно ставят в первые сутки после рождения – именно потому, что никто не застрахован от срочного медицинского вмешательства.
— Какие еще прививки, помимо тех, которые перечислены в календаре вакцинации, можно порекомендовать поставить ребенку?
— Прививку против ротавирусной инфекции. Ротавирус очень опасен в первые годы жизни ребенка. Более 90% детей с ротавирусной инфекцией госпитализируется в инфекционную больницу. Вообще, по статистике, более половины госпитализаций детей с острыми кишечными заболеваниями связаны с ротавирусной инфекцией. Болезнь сопровождается высокой температурой, сильной рвотой и диареей (поносом), что приводит к обезвоживанию, а для маленьких детей это может быть весьма опасно. Кроме того, дети могут болеть этой инфекцией неоднократно, так как у нее масса разновидностей. Вакцина защищает от ротавируса и значительно облегчает течение заболевания при смежных вирусах (норовирус, астровирус и др. ).
).
Курс вакцинации включает в себя три прививки с интервалом в 4-10 недель, вакцина вводится перорально (то есть капли в рот). Первая прививка ставится в возрасте от 6 до 12 недель (не позже!), последняя прививка должна быть поставлена не позже 8 месяцев. После полного курса вакцинации у ребенка вырабатывается иммунитет к ротавирусной инфекции, который сохраняется до 5 лет. Ревакцинация не требуется.
Прививку против ветряной оспы. Эта прививка не входит в российский календарь прививок, в отличие от многих зарубежных стран, но я рекомендую ее делать. Ставить прививку от ветряной оспы можно, начиная с года ребенка.
Многие родители задаются вопросом: зачем она нужна, ведь если ребенок переболеет в детстве ветрянкой, то у него и так появится иммунитет на всю жизнь? Все так просто. В детском возрасте ветряная оспа действительно обычно переносится достаточно легко, особенно в случае, если мама ребенка имеет иммунитет к этой инфекции, и, соответственно, у маленького ребенка еще сохраняются материнские антитела. В более взрослом возрасте ветрянка, чаще всего, протекает достаточно тяжело и с большим количеством осложнений.
В более взрослом возрасте ветрянка, чаще всего, протекает достаточно тяжело и с большим количеством осложнений.
Многолетний опыт работы позволяет сделать следующие наблюдения: сейчас ветрянка достаточно сильно мутирует. Еще 15 лет назад большинство врачей относились к ветрянке достаточно спокойно, рассуждая так же: переболел с достаточно предсказуемыми последствиями, и иммунитет сформирован. Сейчас же вирус становится более агрессивным, каждый год фиксируются летальные исходы и серьезные осложнения! Высыпания появляются не только на коже, но и на слизистых, на внутренних органах: поверхности кишечника, бронхов, и это может привести к развитию тяжелых осложнений.
Кроме того, важно учитывать, что ветрянка вызывается генерализованной герпетической инфекцией. И герпес после этого из организма не уходит. Зачастую после 40 лет вирус просыпается и проявляется в виде неврологической реакции: опоясывающем лишае в межреберных промежутках. Это обычно связано со стрессами, со снижением иммунитета.
Это обычно связано со стрессами, со снижением иммунитета.
Таким образом, актуальность вакцинации против ветряной оспы уже не вызывает сомнений.
Вакцинация против ВПЧ. Вирус папилломы человека (ВПЧ) является основной причиной развития рака шейки матки. Соответственно, своевременная вакцинация девочек от ВПЧ является надежной защитой от развития рака. Иммунопрофилактика против ВПЧ рекомендована девушкам и молодым женщинам, которые еще не инфицированы ВПЧ. Желательно провести вакцинацию до начала половой жизни, обычно ее рекомендуют девочкам-подросткам в 12 лет. Стандартный курс вакцинации состоит из 3 доз и проводится по схеме (0-2-6 мес.): вторая доза – через 2 месяца после первой; третья доза – через 6 месяцев после первой.
Эту вакцину можно рекомендовать поставить всем девочкам. Но если есть семейный анамнез (онкология у кого-то из близких родственников, особенно – рак шейки матки, вульвы, влагалища), тогда эта прививка особенно нужна!
Мальчиков тоже рекомендуем прививать. Во-первых, с целью защитить их будущих любимых женщин, так как мальчики могут являться переносчиками ВПЧ. Во-вторых, ВПЧ может являться одним из факторов развития онкологии половой системы и у мужчин, хотя это и проявляется значительно реже.
Во-первых, с целью защитить их будущих любимых женщин, так как мальчики могут являться переносчиками ВПЧ. Во-вторых, ВПЧ может являться одним из факторов развития онкологии половой системы и у мужчин, хотя это и проявляется значительно реже.
Таким образом, повторим еще раз: только вакцинация является надежной защитой от множества тяжелых инфекций. Давайте не будем ставить эксперименты на своих детях, проверяя их устойчивость к инфекциям и играя в русскую рулетку: легко они переболеют или получат тяжелейшие осложнения от заболевания, от которого мы легко могли их защитить всего лишь поставив прививку.
Справка
- Вакцинация
- – это самое эффективное средство защиты вашего ребенка от инфекционных заболеваний. При помощи прививок успешно борются с вирусами кори, краснухи, паротита (свинки), ветряной оспы, полиомиелита, гепатита В, ротавирусной инфекции и с бактериями, вызывающими туберкулез, дифтерию, коклюш, столбняк, гемофильную инфекцию.
Суть вакцинации заключается в том, что ребенку прививается ослабленный или убитый болезнетворный агент (или искусственно синтезированный, аналогичный настоящему) с целью стимулировать выработку организмом антител к нему.
- Календарь прививок
- – это перечень вакцин и схема их введения, утвержденная Министерством здравоохранения РФ. В календаре прививок регламентируются плановые прививки и прививки, которые делают по эпидемиологическим показаниям.
Плановые прививки ставятся от массовых инфекций, которые протекают тяжело, имеют высокую вероятность неблагоприятных последствий или летального исхода. Их проводят, начиная с рождения ребенка, по специальному графику. Кроме утвержденных в календаре прививок вы можете отдельно поставить по желанию прививки от некоторых тяжелых инфекций: ветряной оспы, вируса папилломы человека, ротавирусной инфекции и др.
Прививки по эпидемическим показаниям ставятся в случае возникновения вспышек некоторых инфекций; людям, живущим или посещающим эпидемиологически неблагополучные районы; работникам определенных специальностей (медицинские работники, учителя и др.
). Например, всем жителям Новосибирской области рекомендуется ставить прививку от клещевого энцефалита – опасной инфекции, которой можно заразиться при укусе клеща.
| Категории и возраст граждан, подлежащих профилактическим прививкам | Наименование прививки | Примечания |
|---|---|---|
| Новорожденные в первые 24 часа жизни | Первая вакцинация против вирусного гепатита В | |
| Новорожденные на 3-7 день жизни | Вакцинация против туберкулеза | |
| Дети в 1 месяц | Вторая вакцинация против вирусного гепатита В | |
| Дети в 2 месяца | Третья вакцинация против вирусного гепатита В |
По показаниям, только если ребенок находится в группе риска.
|
| Первая вакцинация от пневмококковой инфекции (дает защиту от пневмоний, бронхитов, отитов и ОРВИ средней степени) | ||
| Дети в 3 месяца | Первая вакцинация против дифтерии, коклюша, столбняка | |
| Первая вакцинация против гемофильной инфекции (гнойные отиты, менингиты) | Курс вакцинации против гемофильной инфекции для детей в возрасте от 3 до 6 месяцев состоит из 3 инъекций по 0,5 мл с интервалом 1-1,5 месяца. | |
| Первая вакцинация против полиомиелита | ||
| Дети в 4, 5 месяцев | Вторая вакцинация против дифтерии, коклюша, столбняка | Проводится детям, получившим первую вакцинацию в 3 месяца |
| Вторая вакцинация против гемофильной инфекции | Проводится детям, получившим первую вакцинацию в 3 месяца | |
| Вторая вакцинация против полиомиелита | Проводится детям, получившим первую вакцинацию в 3 месяца | |
| Дети в 6 месяцев | Третья вакцинация против дифтерии, коклюша, столбняка | Проводится детям, получившим первую и вторую вакцинацию в 3 и 4,5 месяца соответственно |
| Третья вакцинация против вирусного гепатита В | Проводится детям, не относящимся к группам риска, получившим первую и вторую вакцинацию в 0 и 1 месяц соответственно | |
| Третья вакцинация против гемофильной инфекции | Проводится детям, получившим первую и вторую вакцинацию в 3 и 4,5 месяца соответственно | |
| Третья вакцинация против полиомиелита | ||
| Дети в 12 месяцев | Вакцинация против кори, краснухи, эпидемического паротита | |
| Четвертая вакцинация против вирусного гепатита В | Проводится детям из групп риска | |
| Дети в 18 месяцев | Первая ревакцинация против дифтерии, коклюша, столбняка | |
| Первая ревакцинация против полиомиелита | ||
| Ревакцинация против гемофильной инфекции |
Ревакцинации проводят однократно детям, привитым на первом году жизни.
|
|
| Дети в 20 месяцев | Вторая ревакцинация против полиомиелита | |
| Дети в 6 лет | Ревакцинация против кори, краснухи, эпидемического паротита | Проводится детям, получившим вакцинацию против кори, краснухи, эпидемического паротита |
| Дети в 6-7 лет | Вторая ревакцинация против дифтерии, столбняка | |
| Дети в 7 лет | Ревакцинация против туберкулеза | |
| Третья ревакцинация против дифтерии, столбняка | ||
| Третья ревакцинация против полиомиелита | ||
| Ревакцинация против туберкулеза | ||
| Взрослые от 18 лет | Ревакцинация против дифтерии, столбняка | Проводится в соответствии с инструкциями по применению анатоксинов с уменьшенным содержанием антигенов взрослым от 18 лет каждые 10 лет с момента последней ревакцинации |
Вакцинация детей
Вакцинация – профилактическая мера, которая исключает возможность заразиться тяжелыми инфекционными болезнями, а,
значит, и предотвратить непоправимые последствия утраты здоровья и дееспособности.
Принцип работы вакцины основан на формировании иммунитета ребенка. Это происходит благодаря тому, что в организм вводится препарат – специально подготовленная культура возбудителя (инактивированные клетки болезнетворных микроорганизмов). В ходе естественной борьбы организма формируются антитела, которые на всю жизнь обеспечивают ребенка эффективным механизмом защиты.
Видео-интервью с врачом Лазаревой О.В.
«Вакцинация за и против»
Какие прививки делают детям
Прививки детям, направленны на формирование иммунитета в самом детстве, это:
- БЦЖ – вакцина от туберкулеза. Последствия этого заболевания выражены в тяжелейших поражениях легких, костной и
нервной ткани. Лечение занимает очень много времени и проходит по строгой схеме приема большого списка
антибиотиков, что сильно разрушает весь иммунитет.
 Поэтому вовремя пройденная вакцинация ребенком – гарант его
крепкого здоровья;
Поэтому вовремя пройденная вакцинация ребенком – гарант его
крепкого здоровья; - АКДС – вакцина, которая формирует иммунитет от трех заболеваний: Коклюш, Дифтерия, Столбняк:
- Коклюш – инфекционное заболевание, которое распространяется воздушно-капельным путем. Переносится крайне тяжело человеком. Обнаруживает себя в спазматическом кашле в приступах, в результате чего возникает гипоксия – кислородное голодание всего организма и мозга, в частности. Заболевание может привести к остановке заболевания. Поэтому крайне необходимо сформировать механизмы защиты у детей.
- Дифтерия – также заболевание, которое относится к инфекционным. Проявляется это заболевание в тяжелых осложнениях по типу инфекционного-токсического шока (отравление всего организма и его недееспособность), сложными болезнями сердца, легких, почек, вялый паралич.
- Столбняк – проявление этой болезни выражено в непоправимых повреждениях нервной системы, которые
сопровождаются сильными множественными судорогами, приводящие к летальному исходу.

- Вакцина против Полиомиелита – заболевание, распространение которого в организме происходит очень быстро. В случае несформированных внутренних резервов борьбы, заболевание приводит к параличу. Проставленные во время прививки формируют иммунитет, который предотвращает саму возможность болезни.
- Прививка от Краснухи – заболевание, которое может привести к гибели плода у беременной женщины.
- Вакцина от Гепатита В – болезнь, мишенью которой является печень. Поражение главного кроветворного органа выливается в такие патологии как цирроз и рак.
Если у вас возникают сомнения на счет того, а стоит ли вообще прививаться – проводить вакцинацию детей, задайтесь вопросом: «Готовы ли вы рисковать здоровьем и жизнью ребенка?»
Ребенок после прививки
В ходе диалога с врачом-педиатром высшей квалификационной категории Лазаревой Ольгой Викторовной, были прояснены такие важные аспекты процесса
вакцинации детей как: что такое календарь вакцинации, как ребенок переживает прививку, в чем разница между
российскими и зарубежными препаратами и многие другие вопросы.
Календарь прививок
Календарь прививок детей создан с учетом особенностей физиологического и иммунного развития организма. В нем зафиксированы периоды, в которые необходимо пройти вакцинацию.
Прививки детям:
- БЦЖ ставится ребенку – на 3-7 день жизни ребенка;
- АКДС – ставится в три подхода: в 3 месяца, 4,5 и 6 месяцев – процесс прививания разбивается, чтобы организм смог формировать защитные механизмы без перегрузки;
- Полиомиелит – ставится совместно с АКДС, также на 3ий месяц, в 4,5 и 6 месяцев;
- Гепатит В – вакцинация проходит в несколько этапов, растянутых во времени: I прививка делается в первые 24 жизни малыша. II – 1 месяц. III – 2 месяц
Другие прививки и сроки проведения вакцинации детям узнавайте у врача-педиатра.
Что делать, если пропустили прививку?
Ольга Викторовна Лазарева отмечает, что ничего катастрофического в том, что пропустили прививку нет. Обратившись к
педиатру, и под его присмотром, вы всегда можете построить Индивидуальный график прививок для ребенка! Это актуально
не только в тех случаях, когда была пропущена процедура, но, в первую очередь, для аллергиков.
Обратившись к
педиатру, и под его присмотром, вы всегда можете построить Индивидуальный график прививок для ребенка! Это актуально
не только в тех случаях, когда была пропущена процедура, но, в первую очередь, для аллергиков.
Детям
страдающим аллергией важно подобрать период стойкой ремиссии – когда аллергия себя не проявляет.
Есть ли разница между российскими и зарубежными препаратами?
Разницы между препаратами нет. Все препараты проходят сертификацию и контроль качества на уровне МинЗдрава. Только после разрешения, препараты доступны к использованию. Существуют особенности: к примеру, некоторые препараты России основаны на белке перепелиного эмбриона (яйца), в то время как зарубежные – куриного. Это крайне важно для детей, страдающих аллергией и непереносимостью.
Ребенок после прививки
После введения препарата организм начинает строить иммунитет, а, значит, бороться с агентами болезни. Поэтому
могут проявляться такие признаки:
Поэтому
могут проявляться такие признаки:
- Повышение температуры;
- Небольшое покраснение места введения препарата;
- Беспокойство;
- Отсутствие аппетита у ребенка.
Таким образом, вакцинация – необходимая мера для повышения качества жизни ребенка, вашего спокойствия и здоровья
всей семьи!
Мы предлагаем вам изучить мнение эксперта – Лазаревой О.В. по теме: «Вакцинация: За и Против», и
получить ответы на все интересующие вас вопросы, обратившись в детский медицинский центр «M+clinic» в Невском районе
СПб.
Запишитесь на консультацию по телефону: +7 (812) 303-07-03
+7 (921) 961-85-00 или через форму на
сайте.
Городская поликлиника №24 — ДЕЛАТЬ ЛИ РЕБЕНКУ ПРИВИВКИ?
В последние годы у родителей частовозникает сомнение по поводу того,нужно ли вообще делать прививки детям. Обращаясь к различным источникам информации, родителиищут ответы на волнующие их вопросы: не станут ли прививки причиной тяжелых болезней в дальнейшем, каковы риски получить поствакцинальное осложнение.
По большому счету страх родителей перед прививками совершенно иррационален, зато во многом спровоцирован навязываемыми со стороны суждениями и грамотно направляемым потоком негативной информации, с которыми врачам просто нет сил бороться.
Попробуем вместе разобраться в том, что такое вакцинация и почему это важно.
ЧТО ТАКОЕ ПРИВИВКА?
В ответ на инфекцию организм вырабатывает иммунитет, который будет препятствовать повторному заражению. На этом основана вакцинация: подкожно, накожно, внутримышечно или орально вводится доза препарата, содержащего минимальное количество штаммов заразных и опасных инфекций. Это и есть прививка.
Полученный эффект сравним с легкой формой течения заболеваний: имитируется естественный процесс заражения, на который иммунная система дает ответ и формирует дальнейшую невосприимчивость в случае полноценного инфицирования.
Иными словами, привитый ребенок либо вовсе не заболевает, когда вокруг бушует эпидемия, либо переносит атаку инфекции очень легко и без осложнений.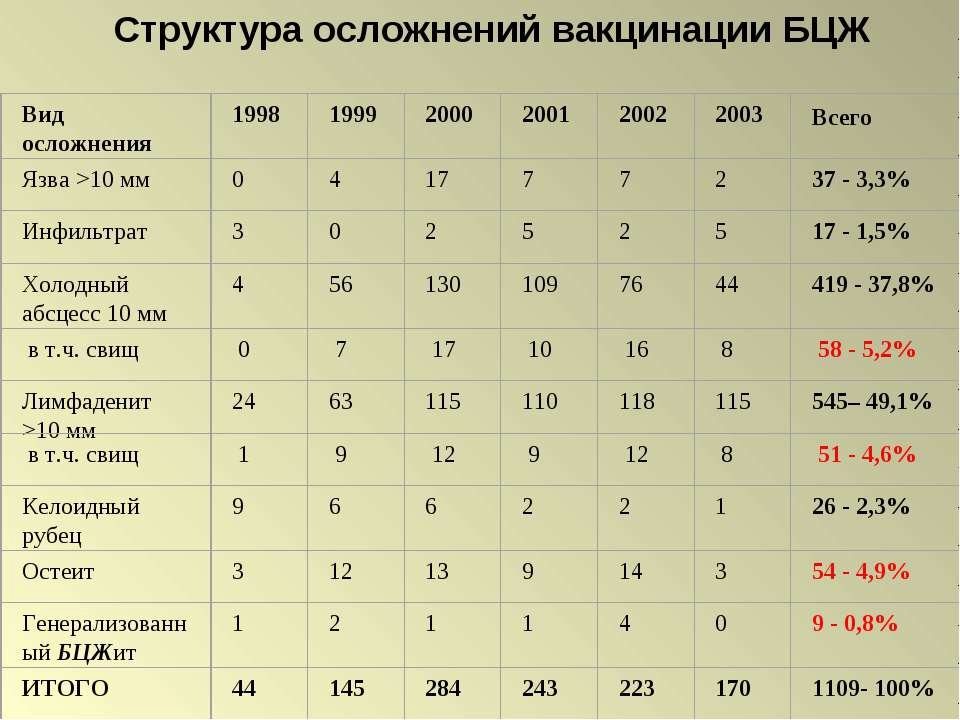
ЗАЧЕМ НУЖНЫ ПРИВИВКИ?
До появления первых вакцин человечество несколько раз подходило к грани вымирания. Пандемия чумы в XIV веке унесла 60 миллионов жизней, пандемии холерыв общей сложности убили порядка пяти миллионов человек. От «Испанки» — тяжелейшей формы гриппа в 1918-1919 годах умерли от 50 до 100 миллионов жителей Земли.
Дифтерия, скарлатина, коклюш, корь, полиомиелит, туберкулез, столбняк – эти болезни уносили сотни тысяч человеческих жизней. Инфекционные заболевания еще в начале прошлого века становились причиной до 40% в Санкт-Петербурге и Москве, а в воспитательных учреждениях – до 80% всех случаев детской смертности.
С появлением вакцин и программ тотальной вакцинации ситуацию удалось преодолеть, но мы должны постоянно помнить, что эти инфекции никуда не делись, и, если ослабить контроль, они вновь вырвутся на свободу.
ЧТО ГОВОРЯТ ПРОТИВНИКИ ПРИВИВОК?
Доводы противников прививок всегда основаны на слабом знании и плохом понимании сути проблемы. Основные тезисы противников звучат так:
Основные тезисы противников звучат так:
- Качество вакцин сомнительно, правил хранения и транспортировки никто не придерживается, детям колют просроченные препараты.
- Опасность заражения – абсолютно гипотетическая и не грозит человеку, живущему в современном обществе.
- Многие врачи выступают против прививок и не вакцинируют своих детей.
- Грудному ребенку вакцины не нужны.
Попытаемся ответить на эти заявления.
КАЧЕСТВО ВАКЦИН
Если в фармкомпаниях никто не контролирует качество прививочных материалов, то и вся остальная их продукция тоже опасна. Однако это не так, и даже самые завзятые противники прививок принимают те или иные медицинские препараты. А это значит, что контролем качества все в порядке.
Что касается правил хранения и транспортировки. Действительно, вакцины – материал капризный и склонный к быстрой порче из-за перепадов температур. Поэтому медицинские работники не только проходят специальное обучение и хорошо представляют себе последствия неправильного хранения этих препаратов, но и несут личную ответственность за все, что будет происходить с привитыми ими людьми после введения некачественной вакцины.
НЕВОЗМОЖНОСТЬ ЗАРАЖЕНИЯ
В эпидемиологии принято такое соотношение: для того чтобы не дать возникнуть эпидемии, привитыми должны быть не менее 95 процентов детей и взрослых: при таких цифрах социум надежно защищен от вспышек инфекций. Однако рост числа противников прививок и снижение числа привитых ниже этой нормы ведет к рискам возникновения эпидемии.
ВРАЧИ ПРОТИВ ПРИВИВОК
Нет и еще раз нет. Врач получает специальное образование и как никто другой знает опасность отказа от вакцинации. Тех, кто не только сам отказывается от прививок, но еще и детей своих не хочет прививать– единицы.Но даже эти единицы знают об эпидемических порогах и условиях, при которых возникает эпидемия, поэтому даже те врачи, которые по какой-то причине отказываются от прививок, никогда не станутраспространять вокруг себя недостоверную информацию. Более того, именно отношение к прививкам может стать для пациента отличным маркером профессиональной пригодности его лечащего врача.
ЗАЧЕМ делать ПРИВИВки младенцам?
На первые три года жизни здорового ребенка приходится самое большое количество плановых прививок: первую из них – против гепатита В – малыш получает уже через 12 часов после рождения, потом наступает черед БЦЖ, которую делают через несколько дней.
Далее обязательны вакцинации против полиомиелита, АКДС, кори, краснухи, паротита, после которых через определенное время полагается ребенка ревакцинировать.
Эти прививки совершенно необходимы, потому что в этом возрасте дети наиболее уязвимы для атак инфекций, а детский иммунитет еще слишком хрупок, чтобы в одиночку справляться с тяжелыми болезнями.
В первый годидет интенсивное доразвитие органов и систем малыша, поэтому вопрос о том, нужно ли делать прививки, вообще не должен даже подниматься.
Посмотрим, какие прививки первого года особенно важны.
ПРИВИВКА ОТ ГЕПАТИТА В
Самая первая вакцина, которую получает ребенок. Она предохраняет малышей от тяжелого вирусного поражения печени, которое часто в дальнейшем приводит к циррозу. Заразиться гепатитом В маленький ребенок может при любой случайности: не следует забывать о том, что носители гепатита B часто даже не подозревают о своем статусе.
Заразиться гепатитом В маленький ребенок может при любой случайности: не следует забывать о том, что носители гепатита B часто даже не подозревают о своем статусе.
ПРИВИВКА БЦЖ
Все знают, что туберкулез – опаснейшее заболевание, поэтому даже те, кто сознательно уклоняется от вакцинации, редко отказываются от прививки БЦЖ.
ПРИВИВКА ОТ ПОЛИОМИЕЛИТА
Противники этой вакцины указывают на большую редкость заболевания. Это не так. Условно «благополучные» страны действительно преодолели эту болезнь. Но там, где процветает нищета и практически отсутствует система здравоохранения, полиомиелит весьма распространен. Современные миграционные процессы делают уязвимыми любого не привитого человека, поэтому прививку от полиомиелита нужно делать обязательно.
КОРЬ, КРАСНУХА, ДИФТЕРИЯ, ПАРОТИТ
Эти болезни унесли больше детских жизней, чем войны и голод вместе взятые. Даже перенеся эти тяжелые заболевания, ребенок рискует на всю жизнь остаться инвалидом.
ПРИВИВКА ОТ ГРИППА
Еще один вид вакцинации, который не понятен многим родителям. Резон противников не лишен логики: вакцины от гриппа нацелены на борьбу только с каким-то одним штаммом, а гарантии, что именно он придет зимой, нет. То есть прививка может получиться бессмысленной. Вопрос остается открытым до сих пор: ни одной стороне не удается собрать достаточно доводов в пользу своей точки зрения.
О КАЛЕНДАРЕ ПРИВИВОК
Каждая прививка привязана к конкретным срокам. Объясняется это клинической доказанностью наибольшей эффективности введения вакцин именно в том или ином возрасте.
Конечно, жизнь вносит в Национальный календарь прививок свои изменения: например, ребенку пора делать прививку, а он как раз болеет, поэтому сроки вакцинации приходится сдвигать до полного выздоровления. Однако лучше все-таки придерживаться рекомендаций, внесенных в прививочный календарь, чтобы эффект от вакцинации был максимальным.
Надеемся, что наши публикации помогут колеблющимся или отрицающим пользу прививок родителям пересмотреть свои взгляды, а тем, кто всегда был «за», еще больше укрепиться в своей поддержке вакцинирования детей.
Подробнее: http://pro-privivku.ru/nuzhno-li-delat-privivki
ПРОХОДИТЕ ВАКЦИНАЦИЮ СВОЕВРЕМЕННО
Жители Адмиралтейского района могут пройти вакцинацию в поликлинике по месту жительства. Для этого нужно прийти в поликлинику с паспортом и полисом ОМС.
Как работают прививочные кабинеты районных поликлиник:
СПб ГБУЗ «Городская поликлиника № 24» (наб. Обводного канала, 140; тел.: 252-33-06), кабинет 214:
- по рабочим дням с 11.00 до 19.30.
СПб ГБУЗ «Городская поликлиника № 27» (Вознесенский пр., 27; тел.: 314-16-92), кабинет 415:
- понедельник, вторник, среда, четверг – с 11:00-15:00,
- пятница – с 11:00-13:00.
СПб ГБУЗ «Поликлиника № 28» (Подъездной пер., 2; тел.: 764-72-29), кабинет 2:
- понедельник, среда, четверг – с 14.00 до 19.00,
- вторник, пятница – с 9.00 до 15.00.
Обратите внимание: детям прививки можно делать только по направлению участкового врача – педиатра!
%d0%b1%d1%86%d0%b6 — со всех языков на все языки
Все языкиРусскийАнглийскийИспанский────────Айнский языкАканАлбанскийАлтайскийАрабскийАрагонскийАрмянскийАрумынскийАстурийскийАфрикаансБагобоБаскскийБашкирскийБелорусскийБолгарскийБурятскийВаллийскийВарайскийВенгерскийВепсскийВерхнелужицкийВьетнамскийГаитянскийГреческийГрузинскийГуараниГэльскийДатскийДолганскийДревнерусский языкИвритИдишИнгушскийИндонезийскийИнупиакИрландскийИсландскийИтальянскийЙорубаКазахскийКарачаевскийКаталанскийКвеньяКечуаКиргизскийКитайскийКлингонскийКомиКомиКорейскийКриКрымскотатарскийКумыкскийКурдскийКхмерскийЛатинскийЛатышскийЛингалаЛитовскийЛюксембургскийМайяМакедонскийМалайскийМаньчжурскийМаориМарийскийМикенскийМокшанскийМонгольскийНауатльНемецкийНидерландскийНогайскийНорвежскийОрокскийОсетинскийОсманскийПалиПапьяментоПенджабскийПерсидскийПольскийПортугальскийРумынский, МолдавскийСанскритСеверносаамскийСербскийСефардскийСилезскийСловацкийСловенскийСуахилиТагальскийТаджикскийТайскийТатарскийТвиТибетскийТофаларскийТувинскийТурецкийТуркменскийУдмуртскийУзбекскийУйгурскийУкраинскийУрдуУрумскийФарерскийФинскийФранцузскийХиндиХорватскийЦерковнославянский (Старославянский)ЧеркесскийЧерокиЧеченскийЧешскийЧувашскийШайенскогоШведскийШорскийШумерскийЭвенкийскийЭльзасскийЭрзянскийЭсперантоЭстонскийЮпийскийЯкутскийЯпонский
Все языкиРусскийАнглийскийИспанский────────АймараАйнский языкАлбанскийАлтайскийАрабскийАрмянскийАфрикаансБаскскийБашкирскийБелорусскийБолгарскийВенгерскийВепсскийВодскийВьетнамскийГаитянскийГалисийскийГреческийГрузинскийДатскийДревнерусский языкИвритИдишИжорскийИнгушскийИндонезийскийИрландскийИсландскийИтальянскийЙорубаКазахскийКарачаевскийКаталанскийКвеньяКечуаКитайскийКлингонскийКорейскийКрымскотатарскийКумыкскийКурдскийКхмерскийЛатинскийЛатышскийЛингалаЛитовскийЛожбанМайяМакедонскийМалайскийМальтийскийМаориМарийскийМокшанскийМонгольскийНемецкийНидерландскийНорвежскийОсетинскийПалиПапьяментоПенджабскийПерсидскийПольскийПортугальскийПуштуРумынский, МолдавскийСербскийСловацкийСловенскийСуахилиТагальскийТаджикскийТайскийТамильскийТатарскийТурецкийТуркменскийУдмуртскийУзбекскийУйгурскийУкраинскийУрдуУрумскийФарерскийФинскийФранцузскийХиндиХорватскийЦерковнославянский (Старославянский)ЧаморроЧерокиЧеченскийЧешскийЧувашскийШведскийШорскийЭвенкийскийЭльзасскийЭрзянскийЭсперантоЭстонскийЯкутскийЯпонский
Отказ родителей от вакцинации БЦЖ стал темой конференции врачей-фтизиатров, педиатров и неонатологов в Махачкале
Отказ родителей от вакцинации БЦЖ стал темой конференции с участием более 150 врачей-фтизиатров, педиатров и неонатологов, которая прошла сегодня в министерстве здравоохранения Дагестана.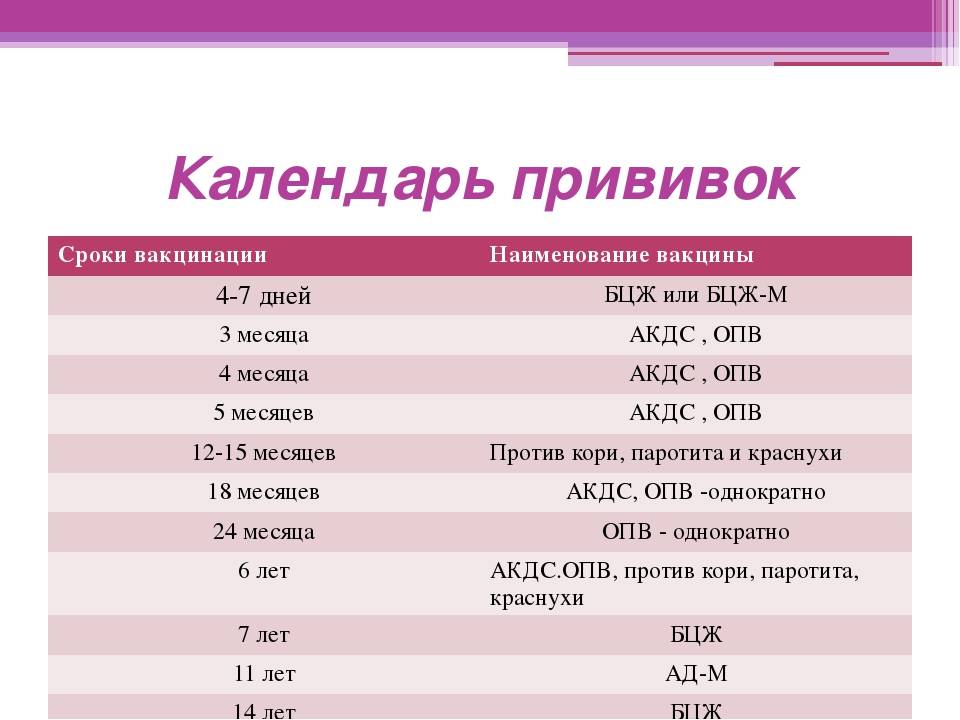 Она проводится с целью повышения знаний врачей по вопросам вакцинации БЦЖ от туберкулеза. Были обсуждены такие актуальные вопросы, как эпидемиологическая ситуация по заболеваемости в республике, вакцинопрофилактика туберкулеза, методика проведения, показания, противопоказания и осложнения, раннее выявление туберкулеза среди детей и подростков.
Она проводится с целью повышения знаний врачей по вопросам вакцинации БЦЖ от туберкулеза. Были обсуждены такие актуальные вопросы, как эпидемиологическая ситуация по заболеваемости в республике, вакцинопрофилактика туберкулеза, методика проведения, показания, противопоказания и осложнения, раннее выявление туберкулеза среди детей и подростков.
Начальник отдела организации медицинской помощи женщинам и детям Минздрава Дагестана Раиса Шахсинова в своем выступлении отметила, что на сегодняшний день в сети Интернет идет сильная антипропаганда вакцинации, говорится о том, какой вред наносят новорожденным детям прививки. «Мы приходим к выводам, что проводим недостаточную санитарно-профилактическую работу среди населения. Нужно объяснять будущим родителям, насколько важна своевременная вакцинация, к каким осложнениям может привести не сделанная вовремя прививка», – обратилась она к присутствующим.
Отмечено, что в последнее время появилась такая тенденция, что родители отказываются от прививок новорожденным детям, а врачи, выписывая детей и мам, говорят, что это их право. Вакцинация БЦЖ-М против туберкулеза проводится детям после 3-7 дней со дня рождения. Ревакцинацию БЦЖ проводят в 6-7-летнем возрасте. По статистике, в махачкалинских роддомах от вакцинации БЦЖ-М в 2015 году отказались мамы 2 тыс. 138 детей. Медицинский отвод получили 2 тыс. 191 ребенок. Это значит, что у ребенка неподходящие для укола показатели. В этом случае врачам необходимо подождать до 2 недель и провести вакцинацию. Если по каким-то причинам укол не сделали в роддоме, его необходимо сделать в срочном порядке в детской поликлинике, пока ребенку 2-3 месяца.
Вакцинация БЦЖ-М против туберкулеза проводится детям после 3-7 дней со дня рождения. Ревакцинацию БЦЖ проводят в 6-7-летнем возрасте. По статистике, в махачкалинских роддомах от вакцинации БЦЖ-М в 2015 году отказались мамы 2 тыс. 138 детей. Медицинский отвод получили 2 тыс. 191 ребенок. Это значит, что у ребенка неподходящие для укола показатели. В этом случае врачам необходимо подождать до 2 недель и провести вакцинацию. Если по каким-то причинам укол не сделали в роддоме, его необходимо сделать в срочном порядке в детской поликлинике, пока ребенку 2-3 месяца.
Следует отличать тубинфицированных людей от больных туберкулезом. Тубинфицированный – не значит, что больной, это значит, что в крови человека существует инфекция, которая может перерасти в болезнь, если не провести должного лечения. Предпринятые меры защищают ребенка от тубинфицированности, которая является прямой дорогой к возникновению локального туберкулеза.
Врачи отметили, что по сравнению с прошлыми годами уровень заболеваемости и смертности от туберкулеза в республике значительно снизился. Однако, как отметил главный врач Республиканского противотуберкулезного диспансера Абдуразак Адзиев, называть ситуацию с туберкулезом однозначно благополучной нельзя. «Это не только инфекционное заболевание, но и социально обусловленное, которое зависит от уровня жизни населения, условий проживания, образа жизни людей и качества питания. При хороших условиях уровень заболеваемости значительно снижается. Эта болезнь не лечится за месяц, порой на это уходят годы. В таком случае человек должен ежедневно принимать лекарства. Но тут проблема заключается в том, что после курса медикаментозного лечения человек отказывается принимать таблетки, потому что чувствует себя лучше. Нельзя делать перерыв, нужно объяснять это людям», – заявил Адзиев.
Однако, как отметил главный врач Республиканского противотуберкулезного диспансера Абдуразак Адзиев, называть ситуацию с туберкулезом однозначно благополучной нельзя. «Это не только инфекционное заболевание, но и социально обусловленное, которое зависит от уровня жизни населения, условий проживания, образа жизни людей и качества питания. При хороших условиях уровень заболеваемости значительно снижается. Эта болезнь не лечится за месяц, порой на это уходят годы. В таком случае человек должен ежедневно принимать лекарства. Но тут проблема заключается в том, что после курса медикаментозного лечения человек отказывается принимать таблетки, потому что чувствует себя лучше. Нельзя делать перерыв, нужно объяснять это людям», – заявил Адзиев.
Заведующая детско-подростковым отделением Республиканского противотуберкулезного диспансера Зулхижат Ахмеддибирова рассказала собравшимся о противопоказаниях, осложнениях и правилах вакцинопрофилактики туберкулеза: «Прежде чем делать укол, вы должны удостовериться, в порядке ли ампулы, шприцы, набрано ли нужное количество препарата, читать инструкцию. Но это человеческий фактор, то, как вы сами сделали укол. Ни в коем случае нельзя делать укол пациенту на дому».
Но это человеческий фактор, то, как вы сами сделали укол. Ни в коем случае нельзя делать укол пациенту на дому».
Бывают редкие случаи осложнения после того, как новорожденному ребенку провели БЦЖ-М. Из 100 тысяч новорожденных может быть один случай. Если правильно оценить состояние ребенка, проводить вакцинацию технически правильно, в отдельной стерильной комнате, то осложнений можно избежать. В случае возникновения осложнений педиатр должен отправить ребенка к врачу-фтизиатру, который по результатам обследования дает заключение. Отталкиваясь от него, нужно проводить соответствующее лечение.
О методах выявления заболеваемости туберкулезом среди детей и подростков рассказала врач-фтизиатр и педиатр Джамиля Забирова. Это подкожный диаскинтест и квантифероновый тест, который позволяет выявить наличие иммунной реакции в крови на заболевание. Эти процедуры, по словам врача, должны проводить всем детям без исключения.
Специалисты порекомендовали своим коллегам тщательнее подходить к вопросам вакцинации и проводить с новоиспеченными мамами просветительскую работу. Медработники должны объяснять, насколько важно сделать своему ребенку БЦЖ-М и БЦЖ-вакцинацию, так как в дальнейшем она убережет его от такого заболевания, как туберкулез.
Медработники должны объяснять, насколько важно сделать своему ребенку БЦЖ-М и БЦЖ-вакцинацию, так как в дальнейшем она убережет его от такого заболевания, как туберкулез.
История вакцины БЦЖ
РЕЗЮМЕ
Туберкулез (ТБ) по-прежнему является причиной 2 миллионов смертей каждый год, несмотря на то, что он является излечимым инфекционным заболеванием, передающимся воздушно-капельным путем. Термины «чахотка» и «туберкулез» исторически использовались для описания туберкулеза, который был причиной каждой четвертой смерти в 19 веке. Из-за своей инфекционной природы, хронического течения и длительного лечения туберкулез является тяжелым бременем для общества. Более того, появление ТБ с множественной лекарственной устойчивостью и текущая эпидемия ТБ-ВИЧ вызывают еще большую озабоченность.Лечение и профилактика туберкулеза стали постоянной проблемой с древних времен. Бацилла Кальметта-Герена (БЦЖ) — единственная доступная на сегодняшний день вакцина, которая используется уже более 90 лет с поразительными показателями безопасности. Однако его эффективность остается спорной. Не существует универсальной политики вакцинации БЦЖ, при этом некоторые страны просто рекомендуют ее использование, а другие внедрили программы иммунизации. В этой статье мы рассмотрим несколько важных вех разработки вакцины БЦЖ с момента открытия до сегодняшнего дня.
Однако его эффективность остается спорной. Не существует универсальной политики вакцинации БЦЖ, при этом некоторые страны просто рекомендуют ее использование, а другие внедрили программы иммунизации. В этой статье мы рассмотрим несколько важных вех разработки вакцины БЦЖ с момента открытия до сегодняшнего дня.
Ключевые слова: Туберкулез, БЦЖ, вакцина, история, обзор
ВВЕДЕНИЕ
Люди были инфицированы M.tuberculosis (Mtb) на протяжении тысячелетий. Туберкулезная инфекция характеризуется сложным иммунологическим ответом, который приводит к уникальному взаимодействию хозяина и патогена, что затрудняет лечение и контроль. Кроме того, ТБ является болезнью, связанной с бедностью, и имеет серьезные социальные последствия. Внедрение бациллы Кальметта-Герена (БЦЖ) и химиотерапии в прошлом столетии знаменует собой важный прогресс в истории туберкулеза (ТБ), который объясняет оптимизм в борьбе с болезнью, особенно в эндемичных районах.На сегодняшний день БЦЖ остается наиболее широко используемой вакциной во всем мире, она была введена более чем 4 миллиардам человек с поразительными показателями безопасности (1,2). Помимо БЦЖ, нет других доступных вакцин для лечения туберкулеза, и из многих новых кандидатов, находящихся в стадии разработки, ни одна не близка к использованию на рынке. В этом обзоре мы обсудим основные вехи в истории ТБ и БЦЖ.
Помимо БЦЖ, нет других доступных вакцин для лечения туберкулеза, и из многих новых кандидатов, находящихся в стадии разработки, ни одна не близка к использованию на рынке. В этом обзоре мы обсудим основные вехи в истории ТБ и БЦЖ.
Ранняя история туберкулеза
Mtb, внутриклеточный патоген, вызывающий туберкулез, был открыт в 1882 г. Робертом Кохом и сегодня является причиной большего числа смертей среди людей, чем любой другой отдельный патоген (3-5).В начале прошлого века существовала надежда, что ТБ можно победить с помощью вакцинации недавно разработанной вакциной M. bovis БЦЖ, выделенной и названной в честь Кальметта и Герена в Лилле, Франция (6). Эти надежды были еще больше подкреплены разработкой первых противотуберкулезных препаратов во время Второй мировой войны Сельманом Ваксманом, который обнаружил бактериостатическую активность стрептомицина в отношении Mtb (7). Первоначально лечение стрептомицином казалось очень эффективным, но ситуация изменилась, когда быстро развилась лекарственная устойчивость, что является ранним свидетельством способности Mtb приобретать лекарственную устойчивость при лечении одним антибиотиком. Несмотря на эту раннюю запись на стене, ошибочное представление о том, что туберкулез можно победить с помощью антибиотиков и вакцинации БЦЖ, привело к самоуспокоенности на несколько десятилетий. Эта ситуация резко изменилась только в начале 1990-х годов, когда Всемирная организация здравоохранения (ВОЗ) объявила туберкулез глобальной чрезвычайной ситуацией (8). С этого времени ученые-фтизиатры, которые сосредоточили большую часть своих усилий на других областях исследований и разработок из-за отсутствия интереса к ТБ и финансирования, смогли переориентировать усилия и инициировать значительные мероприятия по изучению ТБ (9). ).Появление туберкулеза с множественной лекарственной устойчивостью (МЛУ-ТБ), вызванного эпидемией ВИЧ, стало причиной такого смещения интереса. Вскоре исследователи определили последовательность генома Mtb и начали анализировать иммунологию туберкулеза и клеточную биологию (10).
Несмотря на эту раннюю запись на стене, ошибочное представление о том, что туберкулез можно победить с помощью антибиотиков и вакцинации БЦЖ, привело к самоуспокоенности на несколько десятилетий. Эта ситуация резко изменилась только в начале 1990-х годов, когда Всемирная организация здравоохранения (ВОЗ) объявила туберкулез глобальной чрезвычайной ситуацией (8). С этого времени ученые-фтизиатры, которые сосредоточили большую часть своих усилий на других областях исследований и разработок из-за отсутствия интереса к ТБ и финансирования, смогли переориентировать усилия и инициировать значительные мероприятия по изучению ТБ (9). ).Появление туберкулеза с множественной лекарственной устойчивостью (МЛУ-ТБ), вызванного эпидемией ВИЧ, стало причиной такого смещения интереса. Вскоре исследователи определили последовательность генома Mtb и начали анализировать иммунологию туберкулеза и клеточную биологию (10).
2012 — 91 год вакцинации БЦЖ
В 1900 году Альберт Кальметт и Камиль Герен начали свои исследования противотуберкулезной вакцины в Институте Пастера в Лилле. Они культивировали бациллы туберкулеза на глицериновой и картофельной среде, но им было трудно получить гомогенную суспензию бацилл.Пытаясь противодействовать их склонности к слипанию, они попытались добавить в среду бычью желчь и, к своему удивлению, отметили, что пересев приводит к снижению вирулентности организма. Именно это случайное наблюдение привело их к осуществлению долгосрочного проекта по производству вакцины из этой аттенуированной туберкулезной палочки (11).
Они культивировали бациллы туберкулеза на глицериновой и картофельной среде, но им было трудно получить гомогенную суспензию бацилл.Пытаясь противодействовать их склонности к слипанию, они попытались добавить в среду бычью желчь и, к своему удивлению, отметили, что пересев приводит к снижению вирулентности организма. Именно это случайное наблюдение привело их к осуществлению долгосрочного проекта по производству вакцины из этой аттенуированной туберкулезной палочки (11).
В 1908 г., начав с вирулентного бычьего штамма туберкулезной палочки, предоставленного Нокардом (первоначально выделенного им в 1902 г. из вымени туберкулезной коровы), они культивировали его на своей желчной, глицериновой и картофельной среде, а затем приступили к пересеву в примерно три недельных интервала.К 1913 году они были готовы начать испытание вакцины на крупном рогатом скоте, которое было прервано началом Первой мировой войны. Субкультивирование продолжалось на протяжении всей немецкой оккупации Лилля, несмотря на значительно возросшую стоимость картофеля и трудности с получением подходящей бычьей желчи на скотобойне. . Тем не менее, им удалось получить это по милости ветеринаров немецких оккупационных войск. К 1919 году, после примерно 230 субкультур, проведенных в течение предыдущих 11 лет, у них была туберкулезная палочка, которая не вызывала прогрессирующего туберкулеза при введении морским свинкам, кроликам, крупному рогатому скоту или лошадям.По предложению Герена они назвали его Bacille Bilie Calmette-Guerin; позже они опустили «Bilie», и так родилась БЦЖ (11).
. Тем не менее, им удалось получить это по милости ветеринаров немецких оккупационных войск. К 1919 году, после примерно 230 субкультур, проведенных в течение предыдущих 11 лет, у них была туберкулезная палочка, которая не вызывала прогрессирующего туберкулеза при введении морским свинкам, кроликам, крупному рогатому скоту или лошадям.По предложению Герена они назвали его Bacille Bilie Calmette-Guerin; позже они опустили «Bilie», и так родилась БЦЖ (11).
В 1921 году Кальметт решил, что пришло время испытать вакцину на людях. Первое введение БЦЖ человеку было осуществлено Бенджамином Вайль-Халле (1875-1958) при содействии Раймонда Турпина (1895-1988) в больнице Шарите в Париже. Женщина умерла от туберкулеза через несколько часов после рождения здорового ребенка. 18 июля 1921 года Вайль-Халле и Терпин дали младенцу перорально дозу БЦЖ.Нежелательных последствий не было. Оральный путь был выбран, поскольку Кальметт считал желудочно-кишечный тракт обычным путем естественного заражения туберкулезной палочкой. Затем Weill-Halle попробовал подкожный и накожный пути введения другим младенцам, но родители возражали против местных реакций, поэтому пероральный метод был продолжен с использованием эмульсии БЦЖ, приготовленной Боке и Негре. К 1924 г. они смогли сообщить о серии из 664 пероральных прививок БЦЖ младенцам (12).Институт Пастера в Лилле начал массовое производство вакцины БЦЖ для медицинских работников. С 1924 по 1928 год 114 000 младенцев были вакцинированы без серьезных осложнений (13). В 1928 году Кальметт позвал Герена присоединиться к нему в Париже, поскольку не считал необходимым, чтобы Герен продолжал эксперименты с БЦЖ на животных в Лилле. К 1931 году появилась специальная лаборатория по приготовлению БЦЖ, заведующей которой был назначен Герен.
Затем Weill-Halle попробовал подкожный и накожный пути введения другим младенцам, но родители возражали против местных реакций, поэтому пероральный метод был продолжен с использованием эмульсии БЦЖ, приготовленной Боке и Негре. К 1924 г. они смогли сообщить о серии из 664 пероральных прививок БЦЖ младенцам (12).Институт Пастера в Лилле начал массовое производство вакцины БЦЖ для медицинских работников. С 1924 по 1928 год 114 000 младенцев были вакцинированы без серьезных осложнений (13). В 1928 году Кальметт позвал Герена присоединиться к нему в Париже, поскольку не считал необходимым, чтобы Герен продолжал эксперименты с БЦЖ на животных в Лилле. К 1931 году появилась специальная лаборатория по приготовлению БЦЖ, заведующей которой был назначен Герен.
Таким образом, метод вакцинации БЦЖ оказался безопасным.Но не менее важным был вопрос о его эффективности. Статистика Calmette и Guerin показала снижение смертности от туберкулеза среди восприимчивых детей, привитых БЦЖ. За пределами Франции вакцинация БЦЖ также применялась, особенно в Барселоне Луисом Сайе; а в скандинавских странах Арвид Валлгрен в Гётеборге (14) и Йоханнес Хеймбек в Осло (15) первыми применили кожное введение БЦЖ. Однако в Великобритании по-прежнему сохранялся значительный скептицизм, и статистика Кальметта и Герена подверглась резкой критике в 1928 г. со стороны профессора М. Гринвуда (16).Более того, в Соединенных Штатах Петрофф и его коллеги из санатория Трюдо сообщили в 1929 г., что в образце БЦЖ, предоставленном Кальметтом, были выделены вирулентные туберкулезные бациллы, что поставило под серьезное сомнение утверждение Кальметта о том, что БЦЖ является «вирусным лекарством» (17). . Несмотря на эти тревожные сообщения, Кальметт и Герен были уверены, что BCG безопасна, пока не произошла «катастрофа в Любеке».
Однако в Великобритании по-прежнему сохранялся значительный скептицизм, и статистика Кальметта и Герена подверглась резкой критике в 1928 г. со стороны профессора М. Гринвуда (16).Более того, в Соединенных Штатах Петрофф и его коллеги из санатория Трюдо сообщили в 1929 г., что в образце БЦЖ, предоставленном Кальметтом, были выделены вирулентные туберкулезные бациллы, что поставило под серьезное сомнение утверждение Кальметта о том, что БЦЖ является «вирусным лекарством» (17). . Несмотря на эти тревожные сообщения, Кальметт и Герен были уверены, что BCG безопасна, пока не произошла «катастрофа в Любеке».
Любекская катастрофа (1930 г.)
В 1930 г. трагическая катастрофа в Любеке подорвала доверие к BCG.В этом городе на севере Германии профессор Дейке, директор больницы общего профиля Любека, и доктор Альштедт, главный врач департамента здравоохранения Любека, разработали схему вакцинации новорожденных. БЦЖ поставлялась из Института Пастера в Париже, но была подготовлена для введения в туберкулезной лаборатории в Любеке, и использовался пероральный путь введения. Через четыре-шесть недель у большого числа детей развился туберкулез. Из 250 вакцинированных 73 человека умерли в первый год и еще 135 были инфицированы, но выздоровели.Правительство Германии организовало расследование, которое возглавили профессор Бруно Ланге из Института Роберта Коха в Берлине и профессор Людвиг Ланге из Министерства здравоохранения Германии. Через 20 месяцев в их отчете БЦЖ была оправдана как причина катастрофы, которую они приписали небрежному заражению вакцины вирулентными туберкулезными бациллами в лабораториях Любека (18). Двое из пострадавших врачей были приговорены к тюремному заключению.
Через четыре-шесть недель у большого числа детей развился туберкулез. Из 250 вакцинированных 73 человека умерли в первый год и еще 135 были инфицированы, но выздоровели.Правительство Германии организовало расследование, которое возглавили профессор Бруно Ланге из Института Роберта Коха в Берлине и профессор Людвиг Ланге из Министерства здравоохранения Германии. Через 20 месяцев в их отчете БЦЖ была оправдана как причина катастрофы, которую они приписали небрежному заражению вакцины вирулентными туберкулезными бациллами в лабораториях Любека (18). Двое из пострадавших врачей были приговорены к тюремному заключению.
Когда известие о катастрофе в Любеке распространилось по всему миру, Кальметт и Герен стали объектами серьезной критики, и оба мужчины испытали сильное напряжение.В августе 1930 года на собрании Международного союза борьбы с туберкулезом в Осло Кальметт защищался и получил бурные овации. Хотя отчет немецкого расследования реабилитировал БЦЖ как причину катастрофы, доверие к вакцине было подорвано.
Первые исследования БЦЖ
К концу 1940-х годов появилось несколько исследований, доказывающих полезность БЦЖ для защиты от туберкулеза. Туберкулез стал серьезной проблемой после Второй мировой войны, и использование БЦЖ поощрялось, в частности, ЮНИСЕФ, недавно созданной Всемирной организацией здравоохранения (ВОЗ) и Скандинавскими обществами Красного Креста.В течение следующего десятилетия кампании распространились на развивающиеся страны. Также в 1950-х годах Совет по медицинским исследованиям в Соединенном Королевстве и Служба общественного здравоохранения США организовали крупные испытания. Вскоре стало очевидно, что процедура, используемая в Соединенном Королевстве (копенгагенский штамм БЦЖ, вводимый туберкулин-отрицательным 13-летним детям), очень эффективна против туберкулеза (19), в то время как в Соединенных Штатах (штамм Tice, вводимый туберкулин-отрицательным разного возраста) практически не обеспечивали защиты (20).На основании этих результатов соответствующие органы общественного здравоохранения рекомендовали БЦЖ в качестве рутинной процедуры для туберкулин-негативных подростков в Соединенном Королевстве, тогда как БЦЖ не рекомендовалась для рутинного использования в Соединенных Штатах, но ограничивалась определенными группами высокого риска. Большинство стран мира последовали примеру Европы и ВОЗ и ввели рутинную вакцинацию БЦЖ по различным графикам (например, при рождении, поступлении в школу, выпуске из школы), в то время как Нидерланды и США отказались от рутинного использования БЦЖ и основывали свои стратегия борьбы с туберкулезом при отслеживании контактов и использовании туберкулина для выявления лиц для профилактического лечения.
Большинство стран мира последовали примеру Европы и ВОЗ и ввели рутинную вакцинацию БЦЖ по различным графикам (например, при рождении, поступлении в школу, выпуске из школы), в то время как Нидерланды и США отказались от рутинного использования БЦЖ и основывали свои стратегия борьбы с туберкулезом при отслеживании контактов и использовании туберкулина для выявления лиц для профилактического лечения.
Эффективность БЦЖ
Две гипотезы появились ранее как объяснение несопоставимых результатов, наблюдаемых между различными оценками БЦЖ. Один объяснил различия различиями между штаммами БЦЖ (21). На самом деле БЦЖ никогда не клонировали и пассировали в разных условиях, в разных лабораториях с момента ее первоначального получения в 1920-х годах. Было признано, что штаммы, произведенные разными производителями, различаются по микробиологическим свойствам (22), и поэтому вполне разумно предположить, что это может отражаться в различиях в иммуногенности (23).Альтернативная гипотеза возникла вокруг испытаний USPHS, в которых отмечалось, что плохие результаты наблюдались в Алабаме, Джорджии и Пуэрто-Рико среди населения, которое, как известно, подвергалось воздействию многих различных «экологических» микобактерий. Таким образом, изначально Палмер и его коллеги предположили, что воздействие различных микобактерий из окружающей среды может само по себе обеспечивать некоторую защиту от туберкулеза и различными способами влиять на иммунную систему, и что БЦЖ не может значительно улучшиться на этом фоне (24).
Таким образом, изначально Палмер и его коллеги предположили, что воздействие различных микобактерий из окружающей среды может само по себе обеспечивать некоторую защиту от туберкулеза и различными способами влиять на иммунную систему, и что БЦЖ не может значительно улучшиться на этом фоне (24).
Чтобы сделать выбор между этими точками зрения, в районе Чинглпут в Южной Индии, начиная с 1968 г., было организовано большое исследование при содействии Индийского совета медицинских исследований, ВОЗ и Службы общественного здравоохранения США (25). . План состоял в том, чтобы сравнить два разных штамма БЦЖ (парижский/пастеровский против датского), каждый в двух дозах, в районе, который, как известно, имеет очень высокую распространенность воздействия микобактерий из окружающей среды. Сопутствующее испытание планировалось провести в районе на севере Индии с небольшим воздействием микобактерий из окружающей среды, но, к сожалению, отчасти из-за политических волнений, оно так и не было начато. Результаты испытания Chingleput были обнародованы в 1979 г., и они показали, что ни одна из вакцин не обеспечивает никакой защиты от легочного туберкулеза (25). Подробные результаты этого испытания странны по нескольким причинам. Риск заболевания среди лиц, считавшихся «туберкулинотрицательными» в начале, был намного ниже, чем предсказывалось вначале, и оказалось, что на самом деле было больше случаев среди вакцинированных, чем среди контрольной группы, в течение короткого времени после вакцинации (хотя статистическая значимость это наблюдение сомнительно).Хотя два семинара, организованных ВОЗ, рассмотрели исследование и пришли к выводу, что его результаты не могут быть объяснены методологической ошибкой (26), полностью подробное представление результатов этого масштабного исследования никогда не появлялось, а без подробных данных трудно точно понять что случилось. Неожиданные результаты исследования Chingleput привели к серии обсервационных исследований, направленных на оценку использования БЦЖ в различных популяциях мира (27).
Результаты испытания Chingleput были обнародованы в 1979 г., и они показали, что ни одна из вакцин не обеспечивает никакой защиты от легочного туберкулеза (25). Подробные результаты этого испытания странны по нескольким причинам. Риск заболевания среди лиц, считавшихся «туберкулинотрицательными» в начале, был намного ниже, чем предсказывалось вначале, и оказалось, что на самом деле было больше случаев среди вакцинированных, чем среди контрольной группы, в течение короткого времени после вакцинации (хотя статистическая значимость это наблюдение сомнительно).Хотя два семинара, организованных ВОЗ, рассмотрели исследование и пришли к выводу, что его результаты не могут быть объяснены методологической ошибкой (26), полностью подробное представление результатов этого масштабного исследования никогда не появлялось, а без подробных данных трудно точно понять что случилось. Неожиданные результаты исследования Chingleput привели к серии обсервационных исследований, направленных на оценку использования БЦЖ в различных популяциях мира (27). Хотя большинство исследований показали некоторую степень защиты, общее впечатление состоит в большом разнообразии, для которого до сих пор нет общепризнанного объяснения.
Хотя большинство исследований показали некоторую степень защиты, общее впечатление состоит в большом разнообразии, для которого до сих пор нет общепризнанного объяснения.
ВАКЦИНЫ БЦЖ сегодня
В настоящее время используется несколько вакцин БЦЖ. Основными производителями для международного рынка являются Pasteur-Merieux-Connaught, Датский институт сывороток Statens, Evans Medeva (который взял на себя старую вакцину Glaxo) и Японская лаборатория БЦЖ в Токио. Каждая из этих вакцин БЦЖ производится по-своему, и признано, что они различаются по различным качествам, таким как доля жизнеспособных клеток на дозу (22). Штаммы БЦЖ, полученные из исходного парижского штамма после 1925 г.g., нынешние штаммы Pasteur, Copenhagen, Glaxo-Evans) не имеют области генома, известной как RD-2, которая все еще присутствует в штаммах, полученных ранее этой даты [представлена нынешними бразильскими (Moreau), японскими и японскими Русские штаммы] (28,29).
Фенотипические различия между этими вакцинными штаммами БЦЖ были впервые обнаружены в 1920-х годах, а совсем недавно молекулярные исследования определили их геномные различия. Хотя несколько исследований на животных и людях предполагают, что конкретный вакцинный штамм БЦЖ, используемый для иммунизации, влияет на микобактериальный специфический иммунный ответ, в настоящее время недостаточно данных, чтобы отдавать предпочтение или рекомендовать один вакцинный штамм БЦЖ.
Хотя несколько исследований на животных и людях предполагают, что конкретный вакцинный штамм БЦЖ, используемый для иммунизации, влияет на микобактериальный специфический иммунный ответ, в настоящее время недостаточно данных, чтобы отдавать предпочтение или рекомендовать один вакцинный штамм БЦЖ.
Тем не менее, большинство населения мира получает вакцину БЦЖ, которую закупает ЮНИСЕФ (Детский фонд Организации Объединенных Наций) от имени Глобального альянса по вакцинам и иммунизации. ЮНИСЕФ использует только четырех поставщиков вакцины БЦЖ, которые производят только три различных вакцинных штамма БЦЖ: БЦЖ-Дания, производимая Государственным институтом сывороток в Дании, БЦЖ-Россия (генетически идентичная БЦЖ-Болгария) производства Bulbio (BB-NCIPD) в Болгарии и Институтом сыворотки в Индии и БЦЖ-Япония, произведенная Японской лабораторией БЦЖ.
На людях было проведено три исследования защитной эффективности, вызванной различными вакцинными штаммами БЦЖ (вставка ref). В двух исследованиях (с последующим наблюдением от 4 до 50 лет) БЦЖ Пастера была связана со статистически значимо более высокой защитной эффективностью, чем БЦЖ-Фиппс или БЦЖ-Глаксо (30). В третьем исследовании (с последующим наблюдением в течение 15 лет) вакцина БЦЖ-Дания показала большую защитную эффективность, чем БЦЖ-Пастер (25 и 17% соответственно) (31).
В третьем исследовании (с последующим наблюдением в течение 15 лет) вакцина БЦЖ-Дания показала большую защитную эффективность, чем БЦЖ-Пастер (25 и 17% соответственно) (31).
Эти исследования дают лишь ограниченную информацию о защитной эффективности вакцинных штаммов БЦЖ, наиболее часто используемых в настоящее время, поскольку БЦЖ-Фиппс и БЦЖ-Глаксо больше не используются, а БЦЖ-Пастер используется в очень немногих странах, в которых определяется оптимальный вакцинный штамм БЦЖ имеет серьезные последствия.
Во-первых, принимая во внимание большое количество младенцев, ежегодно получающих вакцину БЦЖ, даже небольшое повышение защитного иммунитета в результате использования определенного штамма БЦЖ приведет к усилению защиты от ТБ для большого числа детей. Во-вторых, разрабатывается ряд новых противотуберкулезных вакцин, в том числе вакцины, предназначенные для замены БЦЖ, и вакцины, предназначенные для бустерной вакцинации БЦЖ (5). Наиболее продвинутыми являются бустерные вакцины на основе субъединиц или живых векторов, предназначенные для использования после введения примирующей дозы существующей вакцины БЦЖ. Поэтому по-прежнему важно определить, какой штамм вакцины БЦЖ индуцирует наилучший первичный иммунный ответ против туберкулеза для последующей бустерной вакцинации.
Поэтому по-прежнему важно определить, какой штамм вакцины БЦЖ индуцирует наилучший первичный иммунный ответ против туберкулеза для последующей бустерной вакцинации.
Одно из недавних исследований Н. Ритц и Ко. (32) пришли к выводу, что существуют значительные различия в иммунном ответе, индуцированном различными вакцинными штаммами БЦЖ у новорожденных. Иммунизация БЦЖ-Дания или БЦЖ-Япония индуцировала более высокие частоты микобактериально-специфических полифункциональных и цитотоксических Т-клеток и более высокие концентрации цитокинов Th2, чем иммунизация БЦЖ-Россия.Эти результаты могут иметь важные последствия для глобальной политики противотуберкулезной иммунизации и будущих испытаний противотуберкулезной вакцины. ❑
вакцина БЦЖ — Перевод на японский — примеры английский
Эти примеры могут содержать нецензурные слова, основанные на вашем поиске.
Эти примеры могут содержать разговорные слова на основе вашего поиска.
К сожалению, текущая эффективность вакцины БЦЖ ограничена, и в разработке находится очень мало новых антибиотиков.
残念なことに現状の BCGワクチン の効果は限定的であり、また、ほんのわずかな新規抗生物質しか開発パイプラインに乗っていない。The BCG vaccine is a weakened strain of Mycobacteria, which sufficiently immunogeny but in healthy children do not cause infection.
BCG ワクチン は抗酸菌を十分に immunogeny の弱体化ひずみが、健康な小児では感染症を引き起こさない。NOVEL RECOMBINANT BCG VACCINE
BCG vaccine should be given intradermally.
DAR-901 will be administered to 13-15-year-old participants who received the standard TB vaccine at birth, known as the Bacillus Calmette-Guérin or BCG vaccine .
Before the BCG be sure to discuss this issue with the BCG vaccine is injected intracutaneously, ensuring the development of a local, non-threatening tuberculous process for general health.
前に BCG は、小児科医とこの問題を議論してください。 BCG ワクチン は一般的な健康のためのローカル、非脅迫的結核性プロセスの開発を確保する、皮内に注入されます。It is anticipated that this rhPIV2 platform will work as a booster for BCG vaccine .
このワクチン候補は、 BCG接種後 のブースターとして機能すると期待されている。 These techniques allowed researchers to develop reliable and effective vaccines- first for smallpox, and again in 1921, when scientists developed the BCG vaccine to battle TB.
Since babies are able to receive the BCG vaccine within three(3) months after birth (to be intended for babies less than 6 months of age), it is advisable to receive the vaccination as earlier a possible…
BCG は生後3か月過ぎたら受けられますので(6か月未満対象)早めに接種しましょう。This recombinant BCG vaccine excels in the amount of antigenic protein expressed, so that even with the same dosage as employed for conventional BCG vaccines, the recombinant BCG vaccine can induce satisfactory immune response to target infectious diseases, cancer, etc.
この組換え BCGワクチン は、抗原性タンパク質の発現量に優れ、その結果として通常のBCGワクチンと同程度の使用量によっても、標的とする感染症や癌等に対して十分な免疫応答を誘導することができる。 A recombinant BCG vaccine obtained by transformation with an expression vector carrying a polynucleotide coding for an ecdemic antigenic protein, which recombinant BCG vaccine consists of a modified type polynucleotide comprising a polynucleotide having the third base of each of the codons thereof substituted with G or C without changing of the type of amino acid.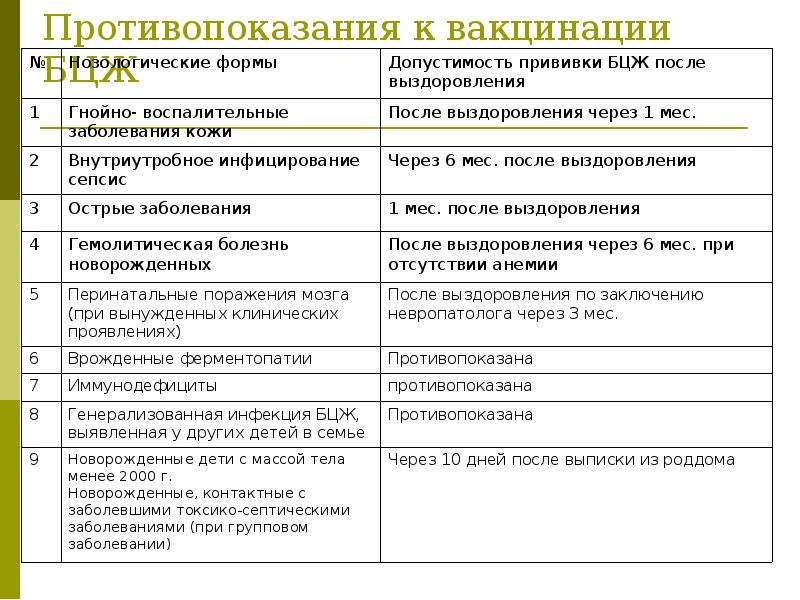
Suggest an example
Other results
BCG vaccines are able to protect babies from tuberculosis.Once babies are attacked by tubercle bacillus, there is a danger that conditions will get serious immediately.
BCGワクチン は結核から赤ちゃんを守ってくれる 赤ちゃんが結核菌に襲われると一気に重症化することもあります。This is in comparison to the 22% average of children in Latin America.Only 7.2% of the children demonstrated a lower than average Vitamin A presence.A control record for the amount of BCG vaccines was taken.
ビタミン B12 の血中濃度が正常 値 を下回っていたのは、12. 6 % の子供たちでした。この数字と比較すると、ラテンアメリカでは、平均して 22 % の子供たちとなっています。ビタミン A の血中濃度が平均値を下回っていたのは、わずか7.2 % の子供たちにすぎませんでした。
6 % の子供たちでした。この数字と比較すると、ラテンアメリカでは、平均して 22 % の子供たちとなっています。ビタミン A の血中濃度が平均値を下回っていたのは、わずか7.2 % の子供たちにすぎませんでした。In mice, the vaccine added protection to BCG , the current vaccine against tuberculosis.
Importantly, this protective effect was much stronger than that produced when the animals were vaccinated with BCG , the only vaccine currently used against tuberculosis.
重要な点は、この防御効果がマカクザルにBCGを接種した場合よりも相当に強力だったことだ。 BCG は、現在唯一使用されている結核 ワクチン だ。The CD4+ T cell-dependent immunity against subsequent exposure to Mtb was as good as or better than that induced by BCG , the only vaccine against Mtb in current use.
その後の結核菌感染に対するCD4+T細胞依存性の免疫は、現在使われている唯一の結核菌 ワクチン である BCG によって誘導される免疫と同等かそれ以上の強さだった。 BCG , the only vaccine against TB, is not effective in preventing infection and transmission of the disease. The development of new generation vaccines against TB is therefore urgently needed. Most developmental approaches use the parenteral route of administration.
The development of new generation vaccines against TB is therefore urgently needed. Most developmental approaches use the parenteral route of administration.
Provided is a vaccine against tuberculosis in which the active ingredient is a recombinant BCG bacterium capable of promoting cytokine production.
Prof. Yasutomi, Director of Tsukuba Primate Center, NIBIO, has found that recombinant human parainfluenza type2 virus (rhPIV2) vector vaccine candidate expressing TB antigen Ag85B is more potent than BCG in reducing TB disease in the mouse model of TB.
医薬基盤研究所・霊長類医科学研究センター長の保富教授は、結核抗原Ag85Bを発現する組み換えヒトパラインフルエンザ2型ウイルスをベクターとする ワクチン 候補が、マウスで BCG よりも結核防御に有効であることを明らかにしました。 In mice, the vaccine increased the level of protection conferred by protection to BCG (Bacillus Calmette-Guérin) alone, the current vaccine against tuberculosis.
Universal BCG vaccination and protection against COVID-19: critique of an ecological study
While there is no specific treatment or vaccine for COVID-19, a recent study has suggested the potential effectiveness of an existing vaccine, the Bacille Calmette-Guérin (BCG) vaccine, against COVID-19.
Вакцина БЦЖ используется в некоторых странах для профилактики туберкулеза (ТБ), бактериального инфекционного заболевания, вызываемого Mycobacterium tuberculosis (Mtb), от которого в 2018 году во всем мире погибло 1,5 миллиона человек. Национальная политика вакцинации БЦЖ различается в разных странах. , при этом всеобщая вакцинация БЦЖ при рождении все еще проводится в странах с высоким бременем туберкулеза, таких как Индия и Эфиопия, в то время как страны с более низкой общей заболеваемостью туберкулезом в значительной степени прекратили всеобщую вакцинацию БЦЖ в пользу целевой вакцинации определенных групп риска туберкулеза (например, детей из семей). иммигрантов из стран с высоким бременем туберкулеза).Всемирный атлас BCG, созданный Международным противотуберкулезным центром McGill, содержит данные о политике и практике BCG во всем мире.
иммигрантов из стран с высоким бременем туберкулеза).Всемирный атлас BCG, созданный Международным противотуберкулезным центром McGill, содержит данные о политике и практике BCG во всем мире.
Кабинет
Для исследования, проведенного Miller et al., политика вакцинации БЦЖ в разных странах была собрана из Атласа мира БЦЖ. Данные о случаях COVID-19 и смертности по странам были получены 21 марта 2020 г. с https://google.org/crisisresponse/covid19-map. Экологический анализ выявил связь между уровнем смертности от COVID-19 и политикой всеобщей вакцинации БЦЖ в странах со средним и высоким уровнем дохода.Авторы также наблюдали связь между случаями COVID-19 на душу населения и политикой вакцинации БЦЖ, при этом страны с политикой всеобщей вакцинации БЦЖ имели более низкие показатели заболеваемости на душу населения и смертности. Основываясь на анализе, авторы заявляют: «Корреляция между началом всеобщей вакцинации БЦЖ и защитой от COVID-19 предполагает, что БЦЖ может обеспечить длительную защиту от текущего штамма коронавируса».
Критика
Дизайн исследования
Основная проблема этого исследования заключается в его дизайне.Экологические исследования часто объединяют воздействия на уровне населения, такие как общенациональные политики, с воздействиями на индивидуальном уровне, такими как влияние вакцины БЦЖ на организм человека. То, что может иметь место на агрегированном уровне, не обязательно будет верным, если принять во внимание разнородность индивидуумов. В этом исследовании доказательства низкого качества, наблюдаемые на уровне популяции, используются для того, чтобы сделать широкие выводы об эффективности БЦЖ на индивидуальном уровне. Методы экологического анализа просто не могут напрямую информировать об этиологии взаимосвязей между воздействием и заболеванием; скорее, они хорошо служат нам как строго генерирующие гипотезы запросы, и их не следует расширять за пределы этой цели.
Время имеет значение
С момента проведения анализа (данные о COVID-19 были загружены 21 марта 2020 г. ) пандемия обострилась во многих странах, в том числе в странах с низким и средним уровнем дохода (СНСД), где БЦЖ вводится при рождении. Например, число случаев COVID-19 в Индии увеличилось со 195 на 21 марта до 1071 на 31 марта. В Южной Африке число случаев увеличилось с 205 на 21 марта до 1326 на 31 марта. страны улучшают свои эпидемические сроки (и расширяют диагностический потенциал).Например, как только мы увидим все последствия передачи вируса в сообществе в крупных густонаселенных странах, таких как Индия, где большое количество поденщиков теперь покидают города после того, как их уволили из-за общенационального карантина. Это подчеркивает, что делать преждевременные выводы на основе быстро меняющихся данных во время пандемии проблематично.
) пандемия обострилась во многих странах, в том числе в странах с низким и средним уровнем дохода (СНСД), где БЦЖ вводится при рождении. Например, число случаев COVID-19 в Индии увеличилось со 195 на 21 марта до 1071 на 31 марта. В Южной Африке число случаев увеличилось с 205 на 21 марта до 1326 на 31 марта. страны улучшают свои эпидемические сроки (и расширяют диагностический потенциал).Например, как только мы увидим все последствия передачи вируса в сообществе в крупных густонаселенных странах, таких как Индия, где большое количество поденщиков теперь покидают города после того, как их уволили из-за общенационального карантина. Это подчеркивает, что делать преждевременные выводы на основе быстро меняющихся данных во время пандемии проблематично.
Отсутствие испытаний
Точный анализ зависит от точных данных, и мы знаем, что текущее число случаев коронавируса во всем мире сильно занижено из-за нехватки диагностических тестов.Количество тестов, проводимых на душу населения, сильно различается в зависимости от страны. Недооценка числа случаев в странах с низким уровнем дохода может полностью объяснить наблюдаемые авторами результаты. Например, в Индии один из самых низких показателей тестирования на COVID-19 в мире. Кроме того, каждая страна применяет собственный алгоритм для определения того, кто будет проходить тестирование. Таким образом, количество и состав известных случаев сильно зависят от стратегии тестирования. Авторы этого документа признают опасения, связанные с текущими оценками случаев COVID-19, а также используют смертность от COVID-19 в качестве меры серьезности вспышки в каждой стране.К сожалению, даже текущие данные о смертности от COVID-19 в некоторых частях мира ненадежны. В богатых странах верно то, что большинство смертей из-за COVID-19 происходит в больнице после того, как им поставили диагноз COVID-19. Однако мы знаем, что в СНСД даже до нынешней пандемии большинство смертей происходило дома без медицинской помощи. Люди, умирающие дома в странах с низким и средним доходом, вряд ли получат подтвержденный диагноз COVID-19, и их смерть может не быть учтена в государственных отчетах.
Недооценка числа случаев в странах с низким уровнем дохода может полностью объяснить наблюдаемые авторами результаты. Например, в Индии один из самых низких показателей тестирования на COVID-19 в мире. Кроме того, каждая страна применяет собственный алгоритм для определения того, кто будет проходить тестирование. Таким образом, количество и состав известных случаев сильно зависят от стратегии тестирования. Авторы этого документа признают опасения, связанные с текущими оценками случаев COVID-19, а также используют смертность от COVID-19 в качестве меры серьезности вспышки в каждой стране.К сожалению, даже текущие данные о смертности от COVID-19 в некоторых частях мира ненадежны. В богатых странах верно то, что большинство смертей из-за COVID-19 происходит в больнице после того, как им поставили диагноз COVID-19. Однако мы знаем, что в СНСД даже до нынешней пандемии большинство смертей происходило дома без медицинской помощи. Люди, умирающие дома в странах с низким и средним доходом, вряд ли получат подтвержденный диагноз COVID-19, и их смерть может не быть учтена в государственных отчетах. Смертность от коронавируса также может быть пропущена в странах с высоким уровнем дохода, которые были поражены вирусом, например, в Италии. Очень сложно делать выводы о каком-либо потенциальном воздействии вакцинации БЦЖ, когда данные столь ошибочны.
Смертность от коронавируса также может быть пропущена в странах с высоким уровнем дохода, которые были поражены вирусом, например, в Италии. Очень сложно делать выводы о каком-либо потенциальном воздействии вакцинации БЦЖ, когда данные столь ошибочны.
Корреляция не является причинно-следственной связью
Серьезный недостаток методологии этого исследования очевиден в том факте, что воспринимаемая связь между воздействием и результатом не означает, что одно вызывает другое — концепция, часто выражаемая в хорошо известной поговорке «корреляция не подразумевает причинно-следственную связь.Это может произойти в ситуациях, когда другие основные факторы влияют как на воздействие, так и на результат и тем самым создают ложную связь между ними (в эпидемиологии такая ситуация называется смешанной). В частности, в случае взаимосвязи между всеобщей вакцинацией БЦЖ и очевидным более низким числом случаев заболевания COVID-19 и смертей, связанных с COVID-19, играет роль множество основных факторов. Важный вывод здесь заключается в том, что если бы эти факторы можно было бы должным образом учесть, мы, скорее всего, , а не , увидели бы связь между вакцинацией БЦЖ и защитой от COVID-19, предложенную в этой статье.Обеспокоенность по поводу качества данных теперь становится потенциальным источником путаницы в отношениях между вакцинацией БЦЖ и меньшим числом случаев COVID-19. Вполне вероятно, что недостаточно финансируемые системы здравоохранения в (СНСУД) имеют низкий потенциал тестирования на COVID-19 и в то же время с большей вероятностью сохранят политику универсальной вакцинации БЦЖ, учитывая, что бремя ТБ является самым высоким в СНСД. Таким образом, исследование на самом деле не демонстрирует, что население в странах с универсальной политикой вакцинации БЦЖ каким-то образом более защищено от COVID-19, потому что более низкие показатели заболеваемости и смертности могут быть в большей степени связаны с низкими возможностями тестирования, чем с какой-либо предполагаемой защитной способностью БЦЖ.
Важный вывод здесь заключается в том, что если бы эти факторы можно было бы должным образом учесть, мы, скорее всего, , а не , увидели бы связь между вакцинацией БЦЖ и защитой от COVID-19, предложенную в этой статье.Обеспокоенность по поводу качества данных теперь становится потенциальным источником путаницы в отношениях между вакцинацией БЦЖ и меньшим числом случаев COVID-19. Вполне вероятно, что недостаточно финансируемые системы здравоохранения в (СНСУД) имеют низкий потенциал тестирования на COVID-19 и в то же время с большей вероятностью сохранят политику универсальной вакцинации БЦЖ, учитывая, что бремя ТБ является самым высоким в СНСД. Таким образом, исследование на самом деле не демонстрирует, что население в странах с универсальной политикой вакцинации БЦЖ каким-то образом более защищено от COVID-19, потому что более низкие показатели заболеваемости и смертности могут быть в большей степени связаны с низкими возможностями тестирования, чем с какой-либо предполагаемой защитной способностью БЦЖ. Таким образом, заявления в документе, которые подразумевают причинно-следственную связь, такие как заявление о том, что «вакцинация БЦЖ также снизила количество зарегистрированных случаев COVID-19 в стране», вводят в опасное заблуждение, особенно в контексте, когда количество зарегистрированных случаев в значительной степени является функцией возможностей тестирования и стратегии тестирования, а не фактической относительной нагрузки.
Таким образом, заявления в документе, которые подразумевают причинно-следственную связь, такие как заявление о том, что «вакцинация БЦЖ также снизила количество зарегистрированных случаев COVID-19 в стране», вводят в опасное заблуждение, особенно в контексте, когда количество зарегистрированных случаев в значительной степени является функцией возможностей тестирования и стратегии тестирования, а не фактической относительной нагрузки.
Еще одним важным соображением является то, что трудно сделать выводы о причинно-следственных связях в широком диапазоне стран с различными базовыми демографическими характеристиками, такими как различия в возрастном распределении изучаемого населения.Особенно это касается заболеваний, тяжесть которых зависит от возраста. Как показано в недавнем исследовании, проведенном в Ухане, Китай, пожилые люди подвергаются более высокому риску тяжелого течения COVID-19, поэтому различия в возрастном распределении населения могут существенно влиять на показатели смертности, наблюдаемые в разных странах (например, регионы ВОЗ Юго-Восточной Азии). В Азии и Африке средний возраст составляет 27,0 и 18,7 лет соответственно, в то время как население европейского региона намного старше (медиана 38,6 лет), что может отчасти способствовать более высокому уровню смертности, наблюдаемому в Европе).В свете этих соображений, учитывая, что в исследовании Miller et al. не использовался метод стандартизации возраста. необходимо подчеркнуть сильные ограничения сделанных выводов.
В Азии и Африке средний возраст составляет 27,0 и 18,7 лет соответственно, в то время как население европейского региона намного старше (медиана 38,6 лет), что может отчасти способствовать более высокому уровню смертности, наблюдаемому в Европе).В свете этих соображений, учитывая, что в исследовании Miller et al. не использовался метод стандартизации возраста. необходимо подчеркнуть сильные ограничения сделанных выводов.
Биологическое правдоподобие
Наконец, некоторая «здравомыслящая» привлекательность утверждения этой статьи основана на несколько ложной эквивалентности. Авторы дважды упоминают, что БЦЖ в целом защищает от респираторных заболеваний. Идея о том, что вакцина против инфекционного заболевания легких может также защитить от других инфекционных заболеваний легких, кажется несколько последовательной и, следовательно, приемлемой.Однако это становится загвоздкой, когда мы смотрим на тип туберкулеза, от которого БЦЖ защищает наиболее эффективно. Из-за неудачного естественного эксперимента, в ходе которого с 2013 по 2015 год наблюдалась глобальная нехватка вакцины БЦЖ, ретроспективные данные показывают, что произошел всплеск случаев туберкулезного менингита, то есть туберкулеза центральной нервной системы. Аккуратная идея вакцины от болезни легких, защищающей от другой болезни легких, то есть от COVID-19, не совсем проста, поскольку БЦЖ, по-видимому, обеспечивает наиболее значительную защиту от туберкулезного менингита.Кроме того, в области борьбы с туберкулезом хорошо известно, что вакцина БЦЖ обеспечивает защиту от туберкулеза только у детей младшего возраста, и эта защита почти полностью ослабевает к 12 годам. помочь расширить эту противотуберкулезную защиту. Важным выводом является то, что защитный эффект БЦЖ со временем ослабевает. Поэтому неясно, как вакцина, которая обеспечивает защиту на ранних этапах жизни человека, защитит людей от COVID-19, когда они достигнут преклонного возраста.
Из-за неудачного естественного эксперимента, в ходе которого с 2013 по 2015 год наблюдалась глобальная нехватка вакцины БЦЖ, ретроспективные данные показывают, что произошел всплеск случаев туберкулезного менингита, то есть туберкулеза центральной нервной системы. Аккуратная идея вакцины от болезни легких, защищающей от другой болезни легких, то есть от COVID-19, не совсем проста, поскольку БЦЖ, по-видимому, обеспечивает наиболее значительную защиту от туберкулезного менингита.Кроме того, в области борьбы с туберкулезом хорошо известно, что вакцина БЦЖ обеспечивает защиту от туберкулеза только у детей младшего возраста, и эта защита почти полностью ослабевает к 12 годам. помочь расширить эту противотуберкулезную защиту. Важным выводом является то, что защитный эффект БЦЖ со временем ослабевает. Поэтому неясно, как вакцина, которая обеспечивает защиту на ранних этапах жизни человека, защитит людей от COVID-19, когда они достигнут преклонного возраста.
Выводы
От последней статьи в Forbes до Bloomberg — результаты исследования набирают все большую популярность. Опасно ссылаться на то, что существуют доказательства того, что вакцина вековой давности может повышать иммунитет у людей, обеспечивая неспецифическую защиту от других заболеваний и, следовательно, защищая от COVID-19 или уменьшая тяжесть его проявления на основе только этого анализа. Принятие этих выводов за чистую монету может привести к самоуспокоенности в ответ на пандемию, особенно в СНСД.Достаточно только взглянуть на то, как это уже было представлено в новостных агентствах нескольких СНСД; опасность такого изображения, дезинформирующего общественность, не следует недооценивать, например, в таких странах, как Индия, широкий охват БЦЖ, предлагаемый их политикой всеобщей вакцинации, может создать ложное чувство безопасности и привести к бездействию. Если подобные утверждения, основанные на недостаточных доказательствах, будут мешать ответным мерам на пандемию, наиболее уязвимые группы населения больше всего пострадают от последствий.
Опасно ссылаться на то, что существуют доказательства того, что вакцина вековой давности может повышать иммунитет у людей, обеспечивая неспецифическую защиту от других заболеваний и, следовательно, защищая от COVID-19 или уменьшая тяжесть его проявления на основе только этого анализа. Принятие этих выводов за чистую монету может привести к самоуспокоенности в ответ на пандемию, особенно в СНСД.Достаточно только взглянуть на то, как это уже было представлено в новостных агентствах нескольких СНСД; опасность такого изображения, дезинформирующего общественность, не следует недооценивать, например, в таких странах, как Индия, широкий охват БЦЖ, предлагаемый их политикой всеобщей вакцинации, может создать ложное чувство безопасности и привести к бездействию. Если подобные утверждения, основанные на недостаточных доказательствах, будут мешать ответным мерам на пандемию, наиболее уязвимые группы населения больше всего пострадают от последствий.
Дальнейшие исследования могут показать, что вакцина БЦЖ обеспечивает защиту от COVID-19; однако при нынешнем состоянии знаний мы не можем утверждать это с какой-либо степенью уверенности, а экологическое исследование не дает достаточных доказательств. Чтобы проанализировать эту взаимосвязь, необходимы дополнительные фундаментальные научные исследования и надлежащим образом спланированные испытания. Австралийские испытания должны начаться в ближайшее время, чтобы выяснить, защищает ли вакцинация БЦЖ от COVID-19 или снижает тяжесть течения COVID-19 у австралийских медицинских работников.Если в хорошо проведенном испытании мы действительно увидим пользу от перепрофилирования этой вакцины, доказательства будут гораздо более убедительными.
Чтобы проанализировать эту взаимосвязь, необходимы дополнительные фундаментальные научные исследования и надлежащим образом спланированные испытания. Австралийские испытания должны начаться в ближайшее время, чтобы выяснить, защищает ли вакцинация БЦЖ от COVID-19 или снижает тяжесть течения COVID-19 у австралийских медицинских работников.Если в хорошо проведенном испытании мы действительно увидим пользу от перепрофилирования этой вакцины, доказательства будут гораздо более убедительными.
Внутривенное введение повышает эффективность противотуберкулезной вакцины
01.01.2020
PITTSBURGH – Во всем мире от туберкулеза (ТБ) умирает больше людей, чем от любой другой инфекционной болезни, несмотря на то, что подавляющее большинство из них были привиты. Вакцина просто не настолько надежна. Но новое исследование Nature показало, что простое изменение способа введения вакцины может значительно повысить ее защитную силу.
«Эффекты поразительны», — сказала старший автор Джоэнн Флинн, доктор философии, профессор микробиологии и молекулярной генетики в Центре исследований вакцин Питта.
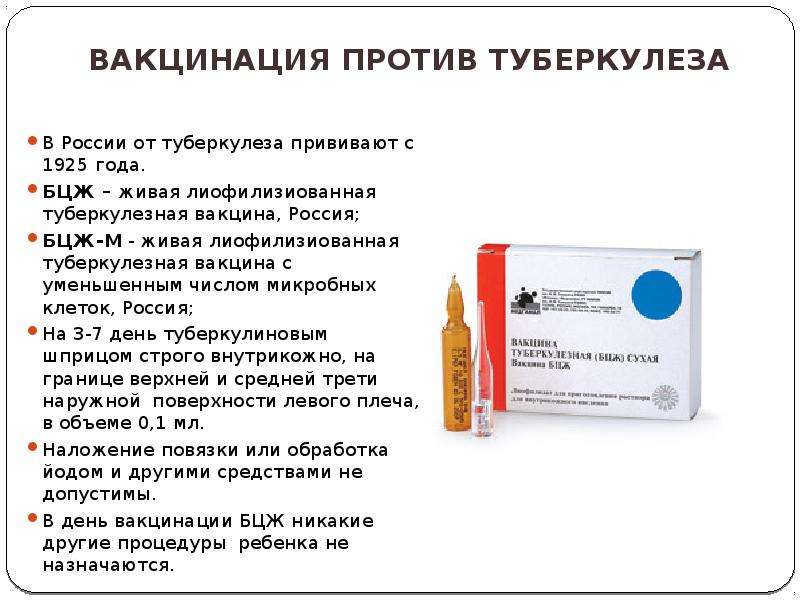 «Когда мы сравнили легкие животных, получавших вакцину внутривенно, со стандартным путем, мы увидели снижение бактериальной нагрузки в 100 000 раз. У девяти из 10 животных не было воспаления в легких».
«Когда мы сравнили легкие животных, получавших вакцину внутривенно, со стандартным путем, мы увидели снижение бактериальной нагрузки в 100 000 раз. У девяти из 10 животных не было воспаления в легких».Команда Флинна протестировала несколько способов и доз единственной коммерчески доступной противотуберкулезной вакцины для человека, бациллы Кальметта-Герена (БЦЖ), которая состоит из живой ослабленной формы туберкулезных бактерий, обнаруженных у крупного рогатого скота.
Вакцина БЦЖ существует уже 100 лет и является одной из наиболее широко используемых вакцин в мире, но ее эффективность сильно различается.
Чтобы проверить, имеет ли значение метод введения при туберкулезе, Флинн и его коллеги разделили свою колонию обезьян на шесть групп: невакцинированные, стандартная человеческая инъекция, более сильная доза, но тот же путь инъекции, аэрозоль, инъекция плюс аэрозоль и, наконец, более сильная доза вакцины. БЦЖ вводят однократно прямо в вену.
Шесть месяцев спустя исследователи заразили животных туберкулезом и наблюдали за ними на наличие признаков инфекции.
Обезьяны чрезвычайно восприимчивы к туберкулезу. У всех животных, получивших стандартную человеческую дозу, наблюдалось стойкое воспаление легких, а среднее количество туберкулезных бактерий в их легких было лишь немного меньше, чем у обезьян, которые вообще не получали вакцину. Другие инъекционные и ингаляционные вакцины обеспечивали столь же скромную защиту от туберкулеза.
С другой стороны, внутривенная вакцина обеспечивала почти полную защиту. В легких этих животных бактерий туберкулеза практически не было, и только у одной обезьяны из этой группы развилось воспаление легких.
«Причина, по которой внутривенный путь настолько эффективен, — объяснил Флинн, — заключается в том, что вакцина быстро проходит через кровоток в легкие, лимфатические узлы и селезенку и активирует Т-клетки, прежде чем погибнет».
Команда Флинна обнаружила БЦЖ и активированные Т-клетки в легких всех внутривенно вакцинированных животных.В других группах БЦЖ не обнаруживалась в легочной ткани, а Т-клеточный ответ был относительно скудным.
Затем исследователи планируют проверить, могут ли более низкие дозы внутривенного введения БЦЖ обеспечить такой же уровень защиты без побочных эффектов, которые в основном состоят из временного воспаления в легких.
Но прежде чем этот метод можно будет применить к людям, исследователи должны знать, что он не только безопасен, но и практичен. Внутривенная вакцина требует больше навыков для введения и сопряжена с более высоким риском заражения.
«Мы далеки от реализации переводческого потенциала этой работы, — сказал Флинн. «Но в конечном итоге мы надеемся провести испытания на людях».
Дополнительные авторы исследования включают Патрисию Дарра, доктора философии, Джошуа Хакни, Суприю Поккали, доктора философии, Филиппа Суонсона, доктора медицины, Мегху Камат и Марио Редерера, доктора философии, из NIAID; Джозеф Зеппа, доктор философии, Полин Майелло, Николь Грант, Марк Роджерс, магистр наук, Челси Косгроув, Эдвин Кляйн, доктор медицинских наук, Александр Уайт и Чарльз Скэнга, доктор философии.Д., Питта; Марк Уодсворт, Трэвис Хьюз, магистр здравоохранения, и Алекс Шалек, доктор философии, из Массачусетского технологического института и Гарвардского университета; Доминик Лэдди, доктор философии, и Данило Касимиро, доктор философии, Aeras; Аурелио Бонавиа, доктор философии, компания Vir Biotechnology; и Филана Лин Лин, доктор медицинских наук, Детская больница UPMC в Питтсбурге.
ИНФОРМАЦИЯ О ФОТО: (щелкните изображение, чтобы увеличить его)
ПРЕДОСТАВЛЕНИЕ: Джоэнн Флинн, доктор философии, Александр Уайт, Полин Майелло и Марио Рёдерер, доктор философии.
НАЗВАНИЕ: Путь доставки имеет значение для вакцинации против туберкулеза
ЗАГОЛОВОК: 3D-сканы ПЭТ-КТ легких обезьян, показывающие воспаление (красный и желтый) от туберкулезной инфекции.Верхний ряд был вакцинирован обычным способом с инъекцией в кожу. Нижний ряд получил вакцину внутривенно.
Длительные эффекты вакцинации БЦЖ как на гетерологичные ответы Th2 / Th27, так и на врожденный тренированный иммунитет — Полный текст — Journal of Innate Immunity 2014, Vol. 6, № 2
Аннотация
Недавно мы показали, что вакцинация БЦЖ (бацилла Кальметта-Герена) у здоровых добровольцев вызывает эпигенетическое перепрограммирование моноцитов, приводящее к увеличению продукции цитокинов в ответ на неродственные патогены в течение 3 месяцев после вакцинации.Это явление получило название «тренированный иммунитет». В настоящем исследовании мы оценили, способна ли БЦЖ вызывать длительные эффекты как на тренированный иммунитет, так и на гетерологичные Т-хелперы 1 (Th2) и Th27 иммунные ответы через 1 год после вакцинации. Продукция TNFα и IL-1β микобактериями или неродственными патогенами была выше через 2 недели и 3 месяца после вакцинации, но эти эффекты были менее выражены через 1 год после вакцинации. Однако моноциты, восстановленные через 1 год после вакцинации, имели повышенную экспрессию рецепторов распознавания образов, таких как CD14, Toll-подобный рецептор 4 (TLR4) и рецептор маннозы, и это коррелировало с увеличением продукции провоспалительных цитокинов после стимуляции лигандом TLR4 липополисахаридом.Гетерологичная продукция Th2 (IFN-γ) и Th27 (IL-17 и IL-22) иммунных ответов на немикобактериальную стимуляцию оставалась сильно повышенной даже через 1 год после вакцинации БЦЖ. Таким образом, БЦЖ вызывает стойкие изменения в иммунной системе, связанные с неспецифическим ответом на инфекции как на уровне врожденного тренированного иммунитета, так и на уровне гетерологичных Th2/Th27-ответов.
© 2013 S. Karger AG, Базель
Введение
Неспецифические полезные эффекты БЦЖ (бациллы Кальметта-Герена) описаны на протяжении многих десятилетий.Вскоре после ее появления в 1920-х годах эпидемиологические исследования неожиданно показали, что БЦЖ защищает от младенческой смертности независимо от ее влияния на туберкулез (ТБ) [1,2,3,4,5]. Недавние исследования подтвердили эти выводы и предложили снижение бремени инфекций, отличных от туберкулеза [6,7,8,9,10]. Например, БЦЖ снизила наполовину неонатальную смертность детей в нескольких недавних исследованиях в Западной Африке [8, 9, 11, 12, 13, 14], в то время как в исследовании случай-контроль в Бразилии БЦЖ снизила риск смерти от пневмонии на 50% у детей в возрасте до 1 года [7].В свете этих данных возникает вопрос, какие механизмы опосредуют эти неспецифические иммунные эффекты БЦЖ и как долго они длятся?
Два возможных иммунологических механизма были предложены для объяснения неспецифических положительных эффектов вакцинации. Первым таким механизмом является гетерологичный иммунитет, при котором перекрестная защита опосредуется ответами памяти гетерологичных Т-клеток [15]. Однако для развития гетерологичного иммунитета требуется как минимум пара недель, и, таким образом, маловероятно, что он отвечает за очень быстрое воздействие, наблюдаемое на перинатальный иммунитет [14].Недавно был предложен второй механизм защиты в виде эпигенетического перепрограммирования иммунных клеток, явления, придающего неспецифическую иммунную память врожденным иммунным ответам и получившего название «тренированный иммунитет» [16]. Многие виды организмов, лишенные адаптивного иммунитета, такие как растения [17] или насекомые [18, 19], проявляют сильную иммунную память после предшествующего воздействия инфекций или определенных микробных компонентов, а адаптивные черты врожденного иммунитета также были продемонстрированы у мышей, лишенных функциональные адаптивные иммунные реакции [20,21].Выдающимися микробными компонентами, способными усиливать эффекторную функцию клеток врожденного иммунитета и защищать от инфекций, являются микобактериальные стимулы, такие как БЦЖ, полный адъювант Фрейнда и мурамилдипептид [22,23,24,25]. Недавно мы показали, что вакцинация БЦЖ у здоровых добровольцев приводила к NOD2-зависимому эпигенетическому репрограммированию моноцитов, что приводило к усилению экспрессии клеточных рецепторов на моноцитах, что сопровождалось повышенной продукцией цитокинов в ответ на неродственные патогены [26].Этот недавно описанный механизм может служить объяснением быстрых неспецифических защитных эффектов, вызываемых вакцинацией БЦЖ. Однако неизвестно, как долго сохраняется сформированный иммунитет и/или гетерологичный иммунитет после вакцинации БЦЖ. Поэтому в настоящем исследовании мы исследовали долгосрочные неспецифические эффекты вакцинации БЦЖ у здоровых добровольцев, оценивая реакцию как врожденных, так и адаптивных иммунных клеток на немикобактериальную стимуляцию в период до 1 года после вакцинации.
Материалы и методы
Субъекты
Людей (в возрасте от 20 до 36 лет), которым планировалось сделать прививку БЦЖ в службе общественного здравоохранения в связи с поездками или работой в эндемичных по ТБ странах, было предложено принять участие в этом испытании. Двадцать здоровых людей были включены в период с августа по ноябрь 2010 года. Кровь брали до и через 2 недели, 3 месяца и 1 год после вакцинации БЦЖ. Два участника были потеряны для последующего наблюдения через 3 месяца. Исследование было одобрено Этическим комитетом Арнема-Неймегена.
Анализы стимуляции РВМС
Для анализов стимуляции РВМС фракцию мононуклеарных клеток выделяли центрифугированием плотности из крови, разбавленной 1:1 в апирогенном физиологическом растворе над Ficoll-Paque (Pharmacia Biotech, Uppsala, Sweden). Клетки дважды промывали физиологическим раствором и ресуспендировали в культуральной среде (RPMI, Invitrogen, Карлсбад, Калифорния, США) с добавлением 10 мкг/мл гентамицина, 10 мМ L-глутамина и 10 мМ пирувата. Клетки подсчитывали на счетчике Коултера (Coulter Electronics) и количество доводили до 5×10 6 клеток/мл.Всего 5 × 10 5 мононуклеарных клеток в объеме 100 мкл добавляли в круглодонные 96-луночные планшеты (Greiner) с RPMI или обработанными ультразвуком Mycobacterium tuberculosis (MTB) h47Rv (1 мкг/мл). конечная концентрация белка), убитые нагреванием Candida albicans (1 × 10 6 микроорганизмов/мл, штамм UC820), Staphylococcus aureus (1 × 10 6 микроорганизмов/мл, клинический изолят) или Escher coli липополисахарид (ЛПС; 1 нг/мл; Sigma-Aldrich, St.Луис, штат Миссури, США). Через 24, 48 ч или 7 сут супернатанты хранили при -20°С. Концентрацию цитокинов в супернатантах оценивали с помощью твердофазного иммуноферментного анализа (ELISA).
Измерение цитокинов
Циркулирующие IFN-γ, IL-17 и IL-22 измеряли в плазме с помощью наборов Sanquin Pelikine ELISA (IFN-γ) или наборов R&D Quantikine ELISA (IL-17 и IL-22; R&D Systems, Minneapolis , Миннесота, США) соответственно по описанию производителя. Измерения цитокинов TNFα, IL-1β, IFN-γ, IL-17 и IL-22 после стимуляции PBMC проводили в супернатантах с использованием коммерческих наборов ELISA от R&D Systems (TNFα, IL-1β, IL-17 и IL-22). или Sanquin (IFN-γ; Амстердам, Нидерланды).В небольшой части исходных образцов, в которых концентрации цитокинов превышали предел обнаружения, эти выбросы были исключены из анализа.
Анализ FACS
Фенотип клеток анализировали с помощью десятицветной и пятицветной проточной цитометрии с использованием Coulter Navios и Coulter Cytomics FC 500 соответственно (Beckman Coulter, Fullerton, FL, USA) и оценивали с использованием программного обеспечения Kaluza 1.1 (Beckman Коултер). Чтобы гарантировать надежные результаты, проточная цитометрия была откалибрована с помощью шариков Flow Set Pro (Beckman Coulter).Клетки промывали в PBS с 1% бычьим сывороточным альбумином перед мечением mAb, конъюгированными с флуорохромом. После инкубации в течение 30 мин при 4°С в темноте клетки дважды отмывали от несвязавшихся антител и анализировали. Для окрашивания клеточной поверхности использовали следующие mAb: CD3-PECy7 (737657), CD4-PB (A82789), CD8-APC-A700 (A66332), CD45-PO (A96416), CD11b-PE (IM25814), CD14- ECD (IM2707U), CD45-PC7 (IM3548; все от Beckman Coulter Corporation), CD284-PE (TLR4; 312806) и CD206-PE (321106; оба образуют Biolegend), CD16-FITC (335035) и CD282-APC (TLR2). ; 558319; оба от BD biosciences) и декстин-1-APC (FAB1859A; R&D Systems).
Статистический анализ
Различия анализировали с использованием знакового рангового критерия Уилкоксона или критерия Фридмана для парных выборок. p < 0,05 считали статистически значимым. Если не указано иное, данные представлены как совокупные результаты данных, полученных у всех добровольцев (среднее значение + стандартная ошибка среднего).
Результаты
Влияние вакцинации БЦЖ на гетерологичные ответы Th2 и Th27
FACS-анализ субпопуляций Т-клеток не показал значительных сдвигов в лимфоцитах CD4 и CD8 (онлайн-приложение.инжир. 1; для всех онлайн доп. материал см. на сайте www.karger.com/doi/10.1159/000355628). Циркулирующие концентрации цитокинов Т-клеточного происхождения IFN-γ, IL-17 и IL-22 были ниже предела обнаружения во все моменты времени (данные не показаны). Напротив, через 2 недели и 3 месяца после вакцинации БЦЖ продукция IFN-γ, индуцированная MTB , была в 7 раз выше, чем до вакцинации, о чем также сообщалось ранее [26]. Интересно, что этот эффект сохранялся не менее 1 года (рис. 1а).Аналогичное увеличение продукции цитокинов через 2 недели и 3 месяца наблюдалось при стимуляции клеток неродственными патогенами ( C. albicans или S. aureus ; рис. 1b, c). Увеличение производства сохранялось до 1 года после вакцинации в случае S. aureus , в то время как оно в значительной степени возвращалось к уровням до вакцинации после стимуляции C. albicans .
Рис. 1
Вакцинация БЦЖ повышала гетерологичные ответы Th2. РВМС, выделенные от 18 добровольцев до и после (2 недели, 3 месяца и 1 год) вакцинации, стимулировали in vitro обработанным ультразвуком MTB ( a ), убитым нагреванием C.albicans ( b ) и S. aureus ( c ). Продукцию IFN-γ оценивали в супернатантах с помощью ELISA. * р < 0,05; ** р < 0,01.
В дополнение к ее влиянию на ответы Th2, мы стремились исследовать влияние вакцинации БЦЖ на выработку цитокинов, происходящих из Th27, а именно IL-17 и IL-22. MTB -стимулированная продукция IL-17 была значительно выше в клетках, извлеченных после вакцинации БЦЖ (рис. 2а). Более того, этот эффект не зависел от стимулирующего патогена, так как при стимуляции C также наблюдалось стойкое увеличение продукции IL-17.albicans (рис. 2б) и S. aureus (рис. 2в). Повышение гетерологичного Th27-иммунитета также отражалось в потенцировании продукции IL-22 после вакцинации БЦЖ. Это было очевидно после стимуляции клеток MTB, C. albicans или S. aureus (рис. 2d-f).
Рис. 2
БЦЖ вызывает длительные гетерологичные ответы Th27. РВМС, выделенные от 18 добровольцев до и после (2 недели, 3 месяца и 1 год) вакцинации, стимулировали in vitro обработанным ультразвуком MTB ( a , d ), убитым нагреванием C.albicans дрожжей ( b , e ) и S. aureus ( c , f ). Продукцию IL-17 ( a-c ) и IL-22 ( d-f ) оценивали с помощью ELISA в супернатантах. * р < 0,05; ** р < 0,01; *** р < 0,005.
Влияние вакцинации БЦЖ на тренированный иммунитет
Ранее мы сообщали, что БЦЖ влияет на выработку провоспалительных цитокинов, продуцируемых моноцитами, прототипом популяции клеток врожденного иммунитета [26].В то время как продукция TNFα и IL-1β была выше через 2 недели и 3 месяца после вакцинации, она в значительной степени вернулась к норме через 1 год после вакцинации БЦЖ. Этот уменьшающийся эффект на высвобождение TNFα и IL-1β наблюдался при стимуляции клеток MTB , а также неродственным патогеном C. albicans (рис. 3а, б) или S. aureus (не показано). ). Аналогичные данные были получены по продукции IL-1β (данные не показаны). Однако индуцированная ЛПС продукция TNFα (рис. 3c) и IL-1β (рис. 3d) через 1 год после вакцинации оставалась значительно выше по сравнению с уровнями до вакцинации.
Рис. 3
Влияние БЦЖ на цитокины врожденного иммунитета. РВМС, выделенные от 18 добровольцев до и после (2 недели, 3 месяца и 1 год) вакцинации, стимулировали in vitro обработанными ультразвуком MTB ( a ), убитыми нагреванием дрожжами C. albicans ( b ) и LPS. ( в , д ). Продукцию TNFα ( а-с ) и IL-1β ( d ) оценивали с помощью ELISA в супернатантах. * р < 0,05; ** р < 0,01.
Влияние вакцинации БЦЖ на экспрессию рецепторов на моноцитах
Экспрессия нескольких рецепторов распознавания образов и маркеров активации на моноцитах демонстрировала устойчивый рост экспрессии с течением времени.На рис. 4 представлены средние флуоресцентные индексы (MFI) маркеров активности моноцитов (CD14 и CD11b; рис. 4а, б), Toll-подобного рецептора 4 (TLR4) и TLR2 (рис. 4в, г) и С-типа. лектины (рецептор маннозы, MR и dectin-1; рис. 4д, е). Увеличение MFI было специфичным для рецептора, так как не на все TLR или лектины С-типа влияла вакцинация. Маркеры активности CD14 и CD11b демонстрировали стойкие более высокие уровни экспрессии на моноцитах, которые сохранялись не менее 1 года. Также экспрессия TLR4 и MR на моноцитах увеличивалась после вакцинации БЦЖ через 1 год после вакцинации.Никакого влияния на экспрессию TLR2 или dectin-1 не наблюдалось (рис. 4d, f). На дополнительном онлайн-рисунке 2 показана стратегия гейтирования моноцитов, использованная на рис. 4. Кроме того, на дополнительном онлайн-рисунке 3 представлены репрезентативные гистограммы всех рецепторов, показанных на рис. 4.
Рис. 4
БЦЖ изменяет фенотип циркулирующих моноцитов у здоровых волонтеры. Средние уровни поверхностной экспрессии маркеров активации CD14+ ( a ) и CD11b ( b ), TLR4 ( c ) и TLR2 ( d ), рецепторов лектина С-типа MR ( e ) и дектин- 1 ( f ) в популяции моноцитов CD14+, выделенных от 18 добровольцев до и после вакцинации БЦЖ.* р < 0,05; ** р < 0,01; *** р < 0,005.
Обсуждение
БЦЖ благотворно влияет на инфекции, отличные от туберкулеза, однако иммунологические механизмы, ответственные за эти эффекты, остаются неясными. Недавно было предложено два иммунологических механизма, опосредующих эти эффекты: краткосрочные эффекты, скорее всего, опосредованы эпигенетическим перепрограммированием врожденных иммунных клеток, процесс, называемый «тренированным иммунитетом» [26], в то время как долгосрочные эффекты могут быть опосредованы гетерологичный Th2/Th27-иммунитет [15], возможно, в сочетании с остаточными эффектами тренированного иммунитета.В настоящем исследовании мы показываем, что вакцинация БЦЖ вызывает неспецифические потенцирующие эффекты как врожденного тренированного иммунитета, так и гетерологичных Т-хелперных ответов, которые явно присутствуют в течение по крайней мере 1 года после вакцинации.
Долгосрочные эффекты после вакцинации БЦЖ наиболее заметны при гетерологичных ответах Th2 и Th27. Объяснением этого может быть процесс «перекрестной защиты», описанный 5 десятилетий назад [27] или позже названный «гетерологичным иммунитетом» [15,28]. Классическая форма перекрестной защиты опосредована лимфоцитами, которые высвобождают IFN-γ после стимуляции первым встреченным патогеном и впоследствии активируют макрофаги-наблюдатели, вызывая состояние временного повышенного врожденного иммунитета против вторичной инфекции, который быстро ослабевает после поражения первичным патогеном. устраняется [29].Вторая форма является долгоживущей и поэтому, возможно, более сопоставима с нашими выводами: Berg et al. [30] описали, что как эффекторные клетки, так и клетки памяти CD8+ способны секретировать IFN-γ в ответ на IL-12 и IL-18 в отсутствие родственного антигена. IL-12 и IL-18 вырабатываются на начальных стадиях вторичной инфекции. Еще одним возможным объяснением может быть совместное использование эпитопа, как описано ранее, хотя это вряд ли сыграет важную роль в объяснении повышенного ответа на C.albicans или S. aureus после вакцинации БЦЖ.
Можно предположить, что повышенная реактивность клеток Th27 происходит аналогичным образом. Общий принцип индукции Th27-ответов подобен принципу Th2-иммунитета, с той разницей, что IL-1β и IL-23 (а не IL-12 и IL-18) являются цитокинами, ответственными за дифференцировку Th27. Повышенная экспрессия рецепторов распознавания образов, которые, как известно, вызывают ответы Th27, такие как MR [31], и провоспалительные цитокины, такие как IL-1β [32], могут, по крайней мере, частично объяснять индукцию гетерологичного иммунитета Th27.Таким образом, увеличение этих типичных врожденных иммунных ответов во время индукции тренированного иммунитета может способствовать гетерологичным ответам Т-хелперов, но эта прямая связь еще предстоит формально продемонстрировать в будущих исследованиях. Кроме того, можно также предположить о потенциальных вредных эффектах гетерологичного иммунитета, индуцированного БЦЖ, при аутоиммунных процессах. Важное различие между вакцинацией БЦЖ и аутоиммунными заболеваниями заключается в том, что в то время как аутоиммунитет индуцирует спонтанную выработку ИЛ-17 с аутоиммунным повреждением тканей, вакцинация БЦЖ лишь индуцирует примированное состояние клеток, чтобы они более сильно реагировали на вторичную микробную стимуляцию.Без стимуляции более высокой продукции этих цитокинов не наблюдалось. В соответствии с этим в одном исследовании даже сообщалось о положительном влиянии вакцинации БЦЖ на сахарный диабет 1 типа [33], а также сообщалось о положительном влиянии на астму и аллергии [34].
Помимо воздействия на гетерологичный иммунитет, вакцинация БЦЖ также оказывает долгосрочное воздействие на врожденный тренированный иммунитет. Это проявляется стойким увеличением продукции провоспалительных цитокинов, опосредованной ЛПС, и экспрессией рецепторов распознавания образов и маркеров активации моноцитов.Можно предположить, что эти два эффекта связаны, так как именно экспрессия рецепторов ЛПС TLR4 и CD14 [35], оставшаяся высокой через 1 год после введения БЦЖ, ответственна за усиленный цитокиновый ответ после стимуляции ЛПС. В отличие от этого, вакцинация БЦЖ не влияла на экспрессию других рецепторов распознавания образов, таких как dectin-1 и TLR2. В то время как изменения в опосредованной S. aureus и C. albicans продукции цитокинов явно присутствовали через 2 недели и 3 месяца после вакцинации, эти эффекты уменьшались через 1 год.Это говорит о том, что, по крайней мере, для некоторых врожденных иммунных путей эпигенетическое перепрограммирование, ответственное за эффекты тренированного иммунитета [26], относительно короткоживущее и присутствует в течение месяцев, а не лет.
В заключение, в настоящем исследовании мы охарактеризовали долгосрочные неспецифические иммунологические эффекты вакцинации БЦЖ. Ранее мы показали, что врожденный иммунитет имеет адаптивные черты, называемые тренированным иммунитетом [16]. Несмотря на то, что на сегодняшний день сообщается о максимальной продолжительности эффектов тренированного иммунитета в 3 месяца [26], в настоящем исследовании мы показали, что неспецифические тренировочные эффекты вакцинации БЦЖ на экспрессию рецепторов и LPS-индуцированные провоспалительные цитокины являются давними и присутствуют. не менее 1 года.Кроме того, через 1 год после вакцинации наблюдалось сильное усиление гетерологичных ответов Th2 и Th27. Эти двойные эффекты вакцинации БЦЖ как на тренированный иммунитет, так и на ответы гетерологичных Т-клеток обеспечивают вероятное объяснение как краткосрочных, так и долгосрочных неспецифических эффектов БЦЖ, которые были известны на протяжении десятилетий и могут иметь важные последствия для разработки вакцин и политики здравоохранения. .
Благодарности
J.Q. и М.Г.Н. были поддержаны грантом Vici от Нидерландской организации научных исследований (М.Г. Н.). Р.В.К. был поддержан грантом Види Нидерландской организации научных исследований. R.J.X. был поддержан грантами (AI 062773, DK 043351, DK 83756) Национальных институтов здравоохранения США и Фонда Хелмсли. CVIVA поддерживается Датским национальным исследовательским фондом (DNRF108). CSB финансировался за счет стартового гранта ERC (через грант ERC-2009-StG -243149).
Ссылки
- Левин М.И., Сакетт М.Ф.: Результаты иммунизации БЦЖ в Нью-Йорке.Am Rev Tuberc 1946; 53: 517-532.
- Аронсон Д.Д.: Защитная вакцинация против туберкулеза с особым упором на вакцину БЦЖ. Минн Мед 1948; 31:1336.
- Фергюсон Р.Г., Саймс А.Б.: Вакцинация БЦЖ индийских младенцев в Саскачеване.Туберкул 1949;30:5-11.
- Розенталь С.Р., Лоуинсон Э., Грэм М.Л., Ливерит Д., Торн М.Г., Джонсон В.: Вакцинация БЦЖ в семьях, больных туберкулезом. Am Rev Respir Dis 1961; 84: 690-704.
- Naeslund C: Опыт вакцинации БЦЖ в провинции Норрботтен (Замша).Преподобный Туберк 1931; 12:617-636.
- Velema JP, Alihonou EM, Gandaho T, Hounye FH: Детская смертность среди пользователей и не пользователей первичной медико-санитарной помощи в сельской западноафриканской общине. Int J Epidemiol 1991; 20:474-479.
- Niobey FM, Duchiade MP, Vasconcelos AG, de Carvalho ML, Leal MC, Valente JG: Факторы риска смерти от пневмонии у детей в возрасте до 1 года в столичном регионе на юго-востоке Бразилии: исследование случай-контроль (на португальском языке) .Rev Saude Publica 1992; 26:229-238.
- Кристенсен И., Ааби П., Дженсен Х.: Обычные прививки и выживание детей: последующее исследование в Гвинее-Бисау, Западная Африка. BMJ 2000;321:1435-1438.
- Гарли М.Л., Мартинс С.Л., Бэйл С., Бальде М.А., Хедегаард К.Л., Густафсон П., Лиссе И.М., Уиттл Х.К., Ааби П.: рубец БЦЖ и положительная реакция на туберкулин, связанные со снижением детской смертности в Западной Африке: неспецифический положительный эффект БЦЖ ? Вакцина 2003; 21:2782-2790.
- Vaugelade J, Pinchinat S, Guiella G, Elguero E, Simondon F: Неспецифические эффекты вакцинации на выживаемость детей: проспективное когортное исследование в Буркина-Фасо. BMJ 2004; 329:1309.
- Рот А., Гарли М.Л., Дженсен Х., Нильсен Дж., Ааби П.: Вакцинация Bacillus calette-guerin и детская смертность.Expert Rev Vaccines 2006; 5:277-293.
- Stensballe LG, Nante E, Jensen IP, Kofoed PE, Poulsen A, Jensen H, Newport M, Marchant A, Aaby P: Острые инфекции нижних дыхательных путей и респираторно-синцитиальный вирус у младенцев в Гвинее-Бисау: положительный эффект вакцинации БЦЖ для исследование методом случай-контроль среди девочек.Вакцина 2005; 23:1251-1257.
- Aaby P, Roth A, Ravn H, Napirna BM, Rodrigues A, Lisse IM, Stensballe L, Diness BR, Lausch KR, Lund N, Biering-Sorensen S, Whittle H, Benn CS: Рандомизированное исследование вакцинации БЦЖ от рождения до низкого -дети с массой тела при рождении: благоприятные неспецифические эффекты в неонатальном периоде? J Infect Dis 2011; 204: 245-252.
- Biering-Sorensen S, Aaby P, Napirna BM, Roth A, Ravn H, Rodrigues A, Whittle H, Benn CS: Небольшое рандомизированное исследование среди детей с низкой массой тела при рождении, вакцинированных бациллой Кальметта-Герена при первом обращении в медицинский центр. Pediatr Infect Dis J 2012;31:306-308.
- Уэлш Р.М., Селин Л.К.: Никто не наивен: значение гетерологичного Т-клеточного иммунитета.Nat Rev Immunol 2002;2:417-426.
- Netea MG, Quintin J, van der Meer JW: Тренированный иммунитет: память для врожденной защиты хозяина. Клеточный микроб-хозяин 2011; 9: 355-361.
- Durrant WE, Dong X: системная приобретенная резистентность.Энн Рев Фитопатол 2004; 42:185-209.
- Pham LN, Dionne MS, Shirasu-Hiza M, Schneider DS: Специфический первичный иммунный ответ у Drosophila зависит от фагоцитов. PLoS Pathog 2007; 3:e26.
- Rodrigues J, Brayner FA, Alves LC, Dixit R, Barillas-Mury C: Дифференцировка гемоцитов опосредует врожденную иммунную память у комаров Anopheles gambiae .Наука 2010;329:1353-1355.
- Sun JC, Beilke JN, Lanier LL: Адаптивные иммунные свойства естественных клеток-киллеров. Природа 2009;457:557-561.
- Квинтин Дж., Саид С., Мартенс Дж. Х., Джамареллос-Бурбулис Э. Дж., Ифрим Д. С., Логи С., Джейкобс Л., Янсен Т., Куллберг Б. Дж., Вийменга С., Юстен Л. А., Ксавье Р. Дж., Ван дер Меер Дж. В., Станненберг Х. Г., Нетеа М. Г.: Инфекция Candida albicans обеспечивает защиту от повторного заражения за счет функционального перепрограммирования моноцитов.Микроб-хозяин клетки 2012; 12: 223-232.
- Gorhe DS: Ингибирование размножения вируса ящура у взрослых мышей, предварительно обработанных полным адъювантом Фрейнда. Природа 1967; 216:1242-1244.
- Chedid L, Parant M, Parant F, Lefrancher P, Choay J, Lederer E: Повышение неспецифического иммунитета к инфекции klebsiella pneumoniae синтетическим иммуноадъювантом (N-ацетилмурамил-L-аланил-D-изоглутамин) и несколькими аналогами.Proc Natl Acad Sci USA 1977;74:2089-2093.
- van ‘t Wout JW, Poell R, van FR: Роль макрофагов, активированных БЦЖ/ППД, в устойчивости к системному кандидозу у мышей. Scand J Immunol 1992; 36:713-719.
- Сакума Т., Суэнага Т., Йошида И., Адзума М.: Механизмы повышенной устойчивости мышей, получавших Mycobacterium bovis БЦЖ, к вирусной инфекции эктромелии.Infect Immun 1983;42:567-573.
- Kleinnijenhuis J, Quintin J, Preijers F, Joosten LA, Ifrim DC, Saeed S, Jacobs C, van Loenhout J, de Jong D, Stunnenberg HG, Xavier RJ, van der Meer JW, van Crevel R, Netea MG: Bacille Calmette- Герен индуцирует NOD2-зависимую неспецифическую защиту от повторного заражения посредством эпигенетического перепрограммирования моноцитов.Proc Natl Acad Sci USA 2012;109:17537-17542.
- Маканесс Г.Б.: Иммунологическая основа приобретенной клеточной резистентности. J Exp Med 1964; 120:105-120.
- Селин Л.К., Варга С.М., Вонг И.К., Уэлш Р.М.: Защитный гетерологичный противовирусный иммунитет и усиленный иммунопатогенез, опосредуемый популяциями Т-клеток памяти.J Exp Med 1998;188:1705-1715.
- Маканесс Г.Б.: Влияние иммунологически детерминированных лимфоидных клеток на активность макрофагов in vivo. J Exp Med 1969; 129:973-992.
- Берг Р.Е., Кроссли Э., Мюррей С., Форман Дж.: CD8+ Т-клетки памяти обеспечивают врожденную иммунную защиту от листерии моноцитогенной в отсутствие родственного антигена.J Exp Med 2003; 198:1583-1593.
- ван де Вердонк Ф.Л., Марийниссен Р.Дж., Куллберг Б.Дж., Коенен Х.Дж., Ченг С.К., Йостен И., ван ден Берг В.Б., Уильямс Д.Л., ван дер Меер Дж.В., Йостен Л.А., Нетеа М.Г.: Рецептор маннозы макрофагов индуцирует IL-17 в ответ на Candida albicans .Клеточный микроб-хозяин 2009; 5:329-340.
- Кричек И., Вей С., Ватан Л., Эскара-Вилке Дж., Шелига В., Келлер Э.Т., Зоу В.: Передний край: противоположные эффекты ИЛ-1 и ИЛ-2 на регуляцию ИЛ-17+ пула Т-клеток ИЛ-1 разрушает опосредованную IL-2 супрессию. Дж. Иммунол 2007; 179:1423-1426.
- Faustman DL, Wang L, Okubo Y, Burger D, Ban L, Man G, Zheng H, Schoenfeld D, Pompei R, Avruch J, Nathan DM: Proof-of-concept, рандомизированное, контролируемое клиническое исследование Bacillus-Calmette-Guerin для лечения длительного диабета 1 типа.PLoS One 2012;7:e41756.
- Rousseau MC, Parent ME, St-Pierre Y: Возможные последствия для здоровья от неспецифической стимуляции иммунной функции в раннем возрасте: пример вакцинации БЦЖ. Pediatr Allergy Immunol 2008;19:438-448.
- Акаши-Такамура С., Мияке К.: Вспомогательные молекулы TLR.Curr Opin Immunol 2008;20:420-425.
Автор Контакты
Dr. Mihai G. Netea
Медицинский факультет (463), Медицинский центр Университета Радбауд в Неймегене
Geert Grooteplein Zuid 8
NL-6525 GA Nijmegen (Нидерланды)
Электронная почта [email protected]
Информация о статье / публикации
Предварительный просмотр первой страницы
Получено: 03 мая 2013 г.
Принято: 03 сентября 2013 г.
Опубликовано онлайн: 30 октября 2013 г.
Дата выпуска выпуска: февраль 2014 г.
Количество печатных страниц: 7
Количество фигурок: 4
Количество столов: 0
ISSN: 1662-811X (печать)
eISSN: 1662-8128 (онлайн)
Для получения дополнительной информации: https://www.karger.com/ДЖИН
Авторское право / Дозировка препарата / Отказ от ответственности
Авторское право: Все права защищены. Никакая часть данной публикации не может быть переведена на другие языки, воспроизведена или использована в любой форме и любыми средствами, электронными или механическими, включая фотокопирование, запись, микрокопирование или любую систему хранения и поиска информации, без письменного разрешения издателя. .
Дозировка препарата: авторы и издатель приложили все усилия, чтобы гарантировать, что выбор препарата и дозировка, указанные в этом тексте, соответствуют текущим рекомендациям и практике на момент публикации.Тем не менее, в связи с продолжающимися исследованиями, изменениями в правительственных постановлениях и постоянным потоком информации, касающейся лекарственной терапии и реакций на лекарства, читателю настоятельно рекомендуется проверять вкладыш в упаковке для каждого лекарства на предмет любых изменений в показаниях и дозировке, а также для дополнительных предупреждений. и меры предосторожности. Это особенно важно, когда рекомендуемый агент является новым и/или редко используемым лекарственным средством.
Отказ от ответственности: заявления, мнения и данные, содержащиеся в этой публикации, принадлежат исключительно отдельным авторам и участникам, а не издателям и редакторам.Появление рекламы и/или ссылок на продукты в публикации не является гарантией, одобрением или одобрением рекламируемых продуктов или услуг или их эффективности, качества или безопасности. Издатель и редактор(ы) отказываются от ответственности за любой ущерб людям или имуществу в результате любых идей, методов, инструкций или продуктов, упомянутых в содержании или рекламе.
Перевести прививку БЦЖ на польский с примерами
Компьютерный перевод
Пытаюсь научиться переводить на примерах человеческого перевода.
Человеческий вклад
От профессиональных переводчиков, предприятий, веб-страниц и свободно доступных репозиториев переводов.
Добавить перевод
Последнее обновление: 06.04.2017
Частота использования: 1
Качество:
Последнее обновление: 06.04.2017
Частота использования: 1
Качество:
Последнее обновление: 2017-04-26
Частота использования: 1
Качество:
Последнее обновление: 2017-04-26
Частота использования: 1
Качество:
Последнее обновление: 2019-02-08
Частота использования: 1
Качество:
Последнее обновление: 2019-02-08
Частота использования: 1
Качество:
Последнее обновление: 2019-02-08
Частота использования: 1
Качество:
Последнее обновление: 2019-02-08
Частота использования: 1
Качество:
Последнее обновление: 2019-02-08
Частота использования: 1
Качество:
Последнее обновление: 2019-02-08
Частота использования: 1
Качество:
Последнее обновление: 2019-02-08
Частота использования: 1
Качество:
Последнее обновление: 2019-02-08
Частота использования: 1
Качество:
Последнее обновление: 2019-02-08
Частота использования: 1
Качество:
Последнее обновление: 2019-02-08
Частота использования: 1
Качество:
Последнее обновление: 2019-02-08
Частота использования: 1
Качество:
Последнее обновление: 2019-03-04
Частота использования: 1
Качество:
Последнее обновление: 2014-12-09
Частота использования: 1
Качество:
Предупреждение: Это выравнивание может быть неверным.
Пожалуйста, удалите это, если так считаете.
Последнее обновление: 2014-12-09
Частота использования: 1
Качество:
Предупреждение: Это выравнивание может быть неверным.
Пожалуйста, удалите это, если так считаете.
Последнее обновление: 2014-12-09
Частота использования: 1
Качество:
Предупреждение: Это выравнивание может быть неверным.
Пожалуйста, удалите это, если так считаете.
Последнее обновление: 2014-12-09
Частота использования: 1
Качество:
Предупреждение: Это выравнивание может быть неверным.
Пожалуйста, удалите это, если так считаете.
Получите лучший перевод с
4 401 923 520 человеческий вклад
Пользователи теперь просят о помощи:
Мы используем файлы cookie, чтобы улучшить ваш опыт.Продолжая посещать этот сайт, вы соглашаетесь на использование нами файлов cookie. Выучить больше. В ПОРЯДКЕ
Уроки прошлого Превращение в будущие возможности
Разработка вакцин против инфекционных заболеваний прошла долгий путь благодаря недавним достижениям в разработке адъювантов и открытию новых антигенов, способных вызывать сильные иммунологические реакции для бесплодной ликвидации болезни. Туберкулез (ТБ), от которого ежегодно умирает почти 2 миллиона человек, также является одним из основных моментов последних событий.Наличие или отсутствие методов диагностики инфекции имеет значение для борьбы с болезнью системами здравоохранения, но не связано с иммунным надзором, явлением, возникающим в результате взаимодействия между бактериями и их хозяином. Здесь мы рассмотрим иммунологию ТБ и текущие вакцины-кандидаты для ТБ. Текущие стратегии разработки новых противотуберкулезных вакцин также будут рассмотрены для дальнейшего обсуждения нового понимания иммунотерапевтических подходов с использованием комбинаций адъювантов и антигенов, которые могут иметь потенциал для борьбы с ТБ.
1. Введение
Т-клеточная вакцинация представляет собой введение антигенного материала для выработки Т-клеточного иммунитета против определенных заболеваний. Антигены, используемые в вакцинациях, варьируются от живых вирусов или бактерий до пептидов белков, связанных с мишенью заболевания. Эдвард Дженнер положил начало современной вакцинации, применив коровью оспу для защиты людей от оспы в 1796 году. Введя безвредную форму болезнетворного организма, Дженнер использовал специфичность и память приобретенного иммунного ответа, чтобы заложить основу для современных стратегий вакцинации. 1].Основными целями борьбы с инфекционными заболеваниями являются профилактика и лечение. Первоначальным приоритетом разработки вакцин всегда была профилактика, но разработка и оценка терапевтических вакцин, в основном для хронических инфекционных заболеваний и рака, набирают обороты. Терапевтические вакцины представляют собой гораздо более сложную задачу, поскольку такие заболевания, как рак или хронические инфекционные заболевания, долгое время сосуществовали бы с иммунной системой и, наконец, ускользали от иммунного надзора, когда симптомы были видны.На этом этапе почти по определению должна была бы индуцироваться толерантность [2, 3]. Воздействие Mycobacterium tuberculosis ( M. tb ) дает несколько результатов: отсутствие инфекции, латентная инфекция или активное заболевание [4, 5]. В течение латентного периода M. tb переходит в спящее состояние и будет контролироваться иммунитетом хозяина. Однако этот контроль будет медленно останавливать иммунную систему за счет блокады преобразования регуляторных Т-клеток (Treg) в клетки, блокады клеток, обеспечивающих стимуляцию Т-клеток памяти (), и блокады костимулирующих лигандов, чтобы избежать активации эффекторных клеток. Т-клетки () [5].В этом контексте иммунная система теряет способность сдерживать реактивацию M. tb , что приводит к явному клиническому заболеванию, которое проявляется почти 8 миллионами новых случаев ТБ каждый год. Эта ситуация усугубляется растущим числом случаев ТБ с множественной лекарственной устойчивостью (МЛУ-ТБ), ТБ с широкой устойчивостью (ШЛУ-ТБ) и ТБ с полной устойчивостью (ТБ-ТБ). При МЛУ-ТБ и ШЛУ-ТБ терапия требует альтернативных, длительных, дорогих и токсичных методов лечения с низким уровнем успеха, в то время как МЛУ-ТБ не поддается лечению.Эта ужасная ситуация в настоящее время вызывает потребность в иммунотерапии с особым интересом к вакцинам на основе Т-клеток для реактивации цитотоксических Т-клеток, способных излечивать заболевание [6].
2. Обзор
Mycobacterium tuberculosis и иммунитетаТуберкулез – это заболевание дыхательных путей, передающееся воздушно-капельным путем M. tb . Заражение M. tb начинается с отложения в альвеолярных пространствах легких при вдыхании воздуха с воздушно-капельным путем M.тб . Здесь M. tb будут фагоцитироваться альвеолярными макрофагами (АМ) и разрушаться с помощью активации комплемента [7–9]. Клетки, такие как дендритные клетки, также играют роль в этом процессе [10–12], но некоторые из M. tb смогут избежать процесса внутриклеточного разрушения врожденным иммунитетом, что приведет к размножению инфекции и разрушению. AM. Затем клеточный дебрис разрушенного АМ поглощается другими моноцитами, которые в норме дифференцируются в другие макрофаги, готовые фагоцитировать другие M.tb , но не разрушает интернализированный M. tb из клеточного дебриса AM.
При развитии приобретенного иммунитета (ответ Т/В-клеток) ранние инфицированные клетки будут подвергаться цитотоксичности. Другие AM, которые были вторичными по отношению к первоначальной инфекции, затем будут демонстрировать заторможенный логарифмический бациллярный рост, где инфекция теперь переходит в латентное состояние [13]. Во время покоящегося/латентного состояния M. tb избегает иммунного надзора с помощью нескольких стратегий. Он способен ингибировать как созревание фагосом, так и аутофагию, а также перемещаться из фаголизосом в цитозоль АМ [14, 15]. M. tb также способен снижать уровень провоспалительных цитокинов, гамма-интерферона (IFN-gamma) и рецептора гамма-интерферона (IFN-gammaR), что имеет решающее значение для ответа T/B-клеток [16]. С другой стороны, продукция противовоспалительных цитокинов, таких как IL-10, IL-1Ra и IL-4, и трансформирующий фактор роста бета (TGF- β ), противодействует защитным реакциям IFN-gamma и IL-1 β. , а также индуцирующие регуляторные Т-клетки (Tregs) [16–20].
Развитие механизмов ускользания от иммунного надзора не останавливается на уровне цитокинов.Было также обнаружено, что пути процессинга главного комплекса гистосовместимости (MHC) класса I, MHC класса II и молекулы CD1, которая представляет антиген, ингибируются M. tb . Механизм, с помощью которого молекула MHC класса I ингибируется, еще предстоит четко понять, но данные показывают возможность ассоциированных с патогенами молекулярных паттернов [21], особенно липопротеинового антигена 19 kDa, известного как LpqH из M. tb , для ингибирования созревания фагосом и тем самым ограничить доступность антигенных пептидов из М.tb должен быть представлен на молекулах MHC класса I [22–24]. Молекулы MHC класса II, которые важны для стимуляции CD4 + T-клеток с целью их выработки против болезней, более четко наблюдались как ослабленные LpqH из M. tb . Он действует как PAMP и запускает активацию макрофагов через толл-подобный рецептор (TLR) 2. Однако это хроническое воздействие LpqH и инфекции M. tb вызывает ингибирование индуцированных IFN-gamma генов регуляции (46%), которые играют важную роль в презентации антигена на молекулах МНС класса II [25, 26].В конечном итоге это приводит к подавлению презентации антигена и снижению активации Т-клеток CD4 + [27, 28].
При сочетании этих механизмов M. tb обычно успешно уклоняется от иммунной системы хозяина и находится в состоянии покоя или медленно размножается в некротической гранулеме инфицированных легких (состоящей из нерегулируемого оборота гранулемы, разжижающего некроза и патологического рубцевания). ). Пораженные образования в гранулеме гетерологически инфицированы M.tuberculosis , приводя к образованию клеток CD4 + и CD8 + . Микроокружение поражений человека определяет различные ответы, вызываемые клетками M. tb , в зависимости от локализации бактерий во внешней стенке поражения [29]. Состояние внутри этих гранулем не только обеспечивает прекрасную питательную среду для размножения M. tb , но также служит средой распространения из-за доступа к дыхательным путям легких [30].Таким образом, иммунитет, вырабатываемый на ранних стадиях инфекции, будет служить только смутным предупреждающим знаком для пациента, и в большинстве случаев многие больные туберкулезом остаются недиагностированными до тех пор, пока не достигают активного состояния, когда иммунная система уже не в состоянии принять ответные меры против болезни. Эта проблема усугубляется тем, что для латентного ТБ не существует золотого стандарта диагностики: то есть около 10% этих чисел переходят в состояние активного ТБ [5]. Хотя новые анализы высвобождения гамма-интерферона (IGRA), обнаруживающие M.tb , специфический антиген высвобождения IFN-gamma способны давать более точные результаты, чем реакция Манту, все еще существуют проблемы с ложноположительными результатами теста [31]. Таким образом, современное лечение ТБ имеет плохой прогноз, так как лечение затягивается из-за отсутствия диагностики и невозможности стимулировать иммунологический ответ при переходе ТБ в активное состояние. Этот факт также усиливает необходимость в разработке улучшенных вакцин, которые будут генерировать более сильные и устойчивые иммунологические реакции против ТБ, будь то для профилактики или лечения.
Современные тенденции понимания ТБ также продвинулись вперед в отношении вовлечения других нетрадиционных Т-клеток (iNKT, CD1-рестриктированные Т-клетки, γδ Т-клетки, клетки Th27 и др. [32]), презентации пептидов молекулами HLA-E [33, 34] и распознавание гликолипидов/гликопротеинов CD1-рестриктированными Т-клетками [35]. Все они были подробно рассмотрены в цитируемых публикациях и показывают, что иммунитет, генерируемый в результате инфекции M. tb , не только придает иммунитет CD4, CD8 и B-клеткам, но также распространяется на другие части иммунитета. из-за его способности избегать иммунного надзора.
3. Современные противотуберкулезные вакцины и их разработки
Исторически противотуберкулезная вакцина предназначалась для профилактической/защитной иммунизации бациллой де Кальметта и Герена (БЦЖ), которая была впервые признана в 1931 году [36, 37]. БЦЖ, вакцина, изготовленная из живых аттенуированных Mycobacterium bovis (штамм микобактерий, вызывающий ТБ у крупного рогатого скота), используется во всем мире, но в настоящее время показано, что она не может защитить взрослых с легочным ТБ и подростков, несмотря на то, что демонстрирует эффективную защиту у детей [38].Увеличение числа случаев активного ТБ также обусловлено коинфекцией ВИЧ [39–43]. ВИЧ нацелен на Т-клетки CD4 + , которые играют важную роль в защите от туберкулеза, как обсуждалось в предыдущей главе. Из-за этой коинфекции ВИЧ нарушает иммунитет на основе Т-клеток, выработанный против ТБ, что приводит к ускоренной реактивации латентного ТБ [44].
Для решения таких проблем по всему миру появляются новые вакцины-кандидаты. Эти вакцины-кандидаты предназначены не только для обеспечения более сильных иммунологических ответов против M.tb , но также и длительные ответы, которые потребуют стимуляции ответов Т- и В-клеток памяти [38].
Одним из многих примеров новых противотуберкулезных вакцин является вакцина MVA85A, которая основана на антигене Ag85A, экспрессируемом модифицированным вирусом Vaccinia Ankara в виде субъединичной вакцины. Ag85A представляет собой миколилтрансферазу, обнаруженную у M. M. tb на стадии покоя, которая опосредует переэтерификацию диацилглицерола в качестве донора ацила с образованием запасных тел липидов, вызывающих персистенцию инфекции [45].Вакцина MVA, которая была разработана как противооспенная вакцина в 1983 г., впервые была использована на нескольких моделях животных, что вызывало иммуногенный ответ и обеспечивало защиту от вакцинированных БЦЖ животных. Исследования безопасности, проведенные на пациентах, получавших БЦЖ, также показали положительные результаты в клиническом испытании I фазы [46]. Протокол вакцинации на тот момент представлял собой вакцинацию БЦЖ, за которой следовала вакцинация MVA85A, а затем вакцинация против оспы птиц, экспрессирующая Ag85A (FP85A) в стратегии первичной бустерной вакцинации. Эта стратегия показала заметное увеличение Ag85A-специфических CD8 + Т-клеток после вакцинации FP85A [47].Хотя исследования фазы I были успешными, дальнейшие клинические исследования рандомизированного исследования фазы IIb не показали эффективности по сравнению с плацебо [48]. В исследование было включено большое количество пациентов (2797 детей грудного возраста, 1399 детей, получавших MVA85A, и 1398 пациентов, получавших плацебо) в Кейптауне, Южная Африка, но авторы обнаружили только, что вакцина была безопасной и вызывала умеренные иммунологические реакции. Однако эффективность отсутствовала, и в настоящее время продолжаются дальнейшие исследования, чтобы проанализировать результаты.
Хотя MVAg85A фаза IIb не показала улучшенной эффективности, усилия по разработке вакцин против туберкулеза должны быть активизированы, а клинические испытания должны быть спланированы таким образом, чтобы учесть современные знания, такие как нетрадиционные Т-клетки и представление гликолипидов/гликопротеинов CD1 ограниченным Т-клетки. Это связано с тем, что в фазе IIb испытания MVAg85A защитная эффективность была показана вакцинацией БЦЖ, и, таким образом, повышения эффективности не наблюдалось за такой короткий период.Отсутствие группы, не вакцинированной БЦЖ, также указывает на необходимость улучшения дизайна клинических испытаний [38].
Другие профилактические вакцины, которые в настоящее время находятся на стадии разработки, перечислены в Таблице 1. Одна из многих интересных вакцин включает рекомбинантную БЦЖ (рБЦЖ), предназначенную для экспрессии лизина из Listeria monocytogenes , что будет способствовать представлению доставляемых антигенов на хост с именем VPM1002 [49]. Эта вакцина была специально разработана для повышения способности вакцины БЦЖ стимулировать ответы Т-клеток CD8 + .Листериолизин действует внутри инфицированных макрофагов, вызывая апоптоз, а также транслокацию антигенов в цитоплазму, тем самым увеличивая количество доступных антигенов, которые будут представлены молекулой МНС класса I. VPM1002 с тех пор завершил свою первую фазу испытаний, показавшую безопасность, иммуногенность и стимуляцию ответов как В-, так и Т-клеток против антигенов из вакцины [50]. Тем не менее, исследования как таковые потребуют дальнейшего изучения, и исследователи должны будут извлечь уроки из результатов, полученных в ходе клинических испытаний MV85A.
До сих пор мы обсуждали примеры не- M.tb вакцины, которые использовались при вакцинации против туберкулеза. Идея иммунизации аттенуированным живым M. tb также использовалась несколькими группами для разработки новых вакцин против ТБ. Несмотря на опасения, что аттенуированный M. tb является жизнеспособным микроорганизмом, которому присущ потенциальный риск вызвать активное заболевание, этот тип вакцины имеет большой потенциал. По понятным причинам использование живой аттенуированной M. tb обеспечило бы все необходимые антигены, а сама микобактерия действовала бы как адъювант, поскольку присутствие многочисленных типов липосахаридов способно запускать врожденный иммунитет, увеличивая тем самым образование провоспалительные цитокины, такие как TNF- α , IL-2 и IFN-gamma. Одним из таких примеров является вакцина SO2, мутантный штамм M. tb MT103 с нарушенным геном phoP [51, 52]. Было показано, что ген phoP играет важную роль в вирулентности штамма M. tb MT103, и это нарушение значительно снижает потенциал репликации [53]. Вакцина SO2 содержит несколько ключевых антигенов из M. tb , которые, как было показано, играют решающую роль в обеспечении защиты по сравнению с БЦЖ. Например, было показано, что антиген ESAT-6 обладает высокой иммунодоминантностью в штамме M.исследование заражения tb , проведенное на морских свинках, которое не было обнаружено при вакцинации БЦЖ [54–56]. Таким образом, использование живой аттенуированной M. tb в качестве вакцины представляет собой потенциальную альтернативу. Другой известной вакциной является слитый белок HyVac4 (h5), состоящий из микобактериальных антигенов Ag85B и TB10.4, который вводят с адъювантом IC31 или DDA/MPL больным с БЦЖ-индуцированной инфекцией. В доклиническом исследовании скрещивания инбредных самцов мышей C57BL/6 и самок мышей Balb/c в возрасте от 6 до 8 недель было показано, что h5 эффективно повышает и продлевает иммунитет, индуцированный БЦЖ, с преобладанием иммунного ответа IFN γ . /TNF α /IL-2 или TNF α /IL2, продуцирующие CD4 Т-клетки [57].Клинические испытания фазы II были объявлены компанией Aeras в марте 2014 года, в них примут участие 990 подростков. H56, представляющая собой гибридную белковую вакцину, состоящую из Ag85B и ESAT-6, очень похожа на h5, так как она также усиливает иммунный ответ, генерируемый БЦЖ. В доклиническом исследовании яванских макак, привитых БЦЖ, ревакцинация H56/IC31 привела к эффективному сдерживанию инфекции M.tuberculosis и снижению показателей клинического заболевания. Это измерялось клиническими параметрами, воспалительными маркерами и улучшенной выживаемостью животных по сравнению с одной БЦЖ [58].H56 разработан Statens Serum Institut (SSI) и с тех пор сотрудничает с AERAS для проведения клинических испытаний. Другие известные вакцины, которые продемонстрировали большой потенциал, включены в Таблицу 1 выше. 4. Текущие терапевтические противотуберкулезные вакцины и их разработкиПрофилактические противотуберкулезные вакцины, как обсуждалось ранее, показали, что только БЦЖ способна обеспечить защиту, но это неполный результат. В связи с тем, что обеспечиваемая защита является неполной, реактивация ТБ у пациентов с латентной инфекцией представляет большой риск, а ликвидация заболевания все еще остается сложной задачей [59].С открытием штаммов M. tb M. tb MDR, XDR и TDR лечение активного ТБ остается одним из главных приоритетов, которое будет дополнять профилактические прививки для искоренения ТБ. Без лекарств, способных бороться с этими штаммами M. tb , ежегодно погибает около 2 миллионов человек в мире, а некоторые пациенты даже не получают никакого лечения [60]. Новые возможности и комбинации препаратов в клинических испытаниях показали определенные положительные результаты, такие как меропенем-клавуланат в сочетании со схемами, содержащими линезолид, для лечения ШЛУ-ТБ [61].Однако с появлением нескольких различных кандидатов возникло новое направление в использовании терапевтических вакцин. В настоящее время в разработке находится лишь несколько терапевтических вакцин. Примером таких вакцин является инактивированная цельноклеточная Mycobacterium vaccae ( M. vaccae ). Эта вакцина была впервые представлена в 1985 г. для усиления вакцинации БЦЖ вместо того, чтобы использоваться для лечения лепры [62, 63]. Инактивированный M. vaccae обладает иммунодоминантными антигенами, сходными с M.tb , таким образом демонстрируя улучшенную генерацию ответов антиген-специфических лимфоцитов, особенно у ВИЧ-пациентов с ТБ. Несмотря на демонстрацию эффективности, вызывающей ответы, у этих вакцинированных пациентов также было показано, что ответы антител, особенно IgG против антигенов микобактерий, усиливаются [64]. Когда одна доза инактивированного 10 9 M. vaccae вводилась в сочетании с химиотерапией, в клинических испытаниях, проведенных в Уганде, наблюдались значительные клинические улучшения у пациентов без ВИЧ [65].Другое исследование с тремя дозами M. vaccae также показало клинические улучшения у не-ВИЧ пациентов, получавших химиотерапию [66]. Однако этот прогресс означал, что лечение химиотерапией по-прежнему имеет решающее значение. Другие потенциальные терапевтические вакцины также находятся в стадии разработки, но одно сходство между вакцинами заключается в том, что они усиливают реакцию, вызванную химиотерапией, или используются для контроля латентной инфекции после химиотерапии (таблица 2). Терапевтические вакцины, такие как CSU-F36, которая представляет собой слияние агониста TLR-2 и антигена ESAT-6, действуют как самостоятельная вакцина, которая потенциально может генерировать ответы цитотоксических Т-лимфоцитов, поскольку был выработан сильный уровень IL-12 [67]. .Однако эта вакцина выдержала только слабую дозу аэрозоля M. tb .
RUTI представляет собой новую форму иммунотерапии, включающую использование детоксицированных и липосомных фрагментов клеток Mycobacterium tuberculosis (табл. 2 в схеме вакцинации).Доклинические исследования показали, что лечение РИМП имеет тенденцию улучшать химиотерапию с повышенной эффективностью в отношении хронических заболеваний, вызванных моделью Mycobacterium tuberculosis на мышах (штаммы C57BL/6 и DBA/2) и морских свинках [68]. Эта месячная стратегия вакцинации использует бактерицидный эффект, обеспечиваемый химиотерапией, для синергетического уничтожения активного роста бацилл и подавления местных воспалительных реакций. Прививку РИМП можно проводить после химиотерапии, чтобы предотвратить реактивацию латентных микобактерий.Интраназальное введение вакцины RUTI мышам способствует снижению числа бациллярных клеток и сбалансированным ответам Th2/Th3/Th4 без токсичности. RUTI имеет преимущество перед другими противотуберкулезными вакцинами благодаря защитным свойствам, придаваемым специфическими Т-клетками CD8, и гуморальным ответам, индуцируемым во время лечения. Это позволяет иммунной системе бороться с широким спектром антигенов с образованием антиген-специфических антител после вакцинации против РИМП [69]. Экстракт РИТИ успешно вызывал выраженные иммунные ответы, вызванные рекомбинантными микобактериальными антигенами [70].Значительная защита была продемонстрирована в сыворотке мышей, получавших режим RUTI у мышей SCID [71]. Вакцина РУТИ показала профилактическое действие как лечебная вакцина против туберкулеза. В мышиной модели C57BL количество жизнеспособных бацилл было значительно снижено как в легких, так и в селезенке через 4 недели после вакцинации. Более сильная защита наблюдалась для клеток легкого по сравнению с клетками селезенки после 9-месячной вакцинации. Кроме того, морские свинки выживали дольше, если им была сделана 5-недельная вакцинация перед контрольным заражением.Вакцинация против РИМП потенциально может быть профилактическим средством для снижения риска заражения туберкулезом [72]. Во время фазы II клинических испытаний рандомизированное плацебо-контролируемое исследование показало достаточно безопасную вакцину, которая хорошо переносится и является иммуногенной для людей с латентным туберкулезом [69, 72]. Разработка эффективной противотуберкулезной вакцины была сложной задачей на пути лицензирования терапевтического продукта с доказанной безопасностью и эффективностью. Для разработки эффективной профилактической вакцины во время разработки вакцины широко использовались животные модели.Тем не менее, необходимы успешные клинические испытания для изучения иммунного ответа, возникающего в реальных условиях туберкулезной инфекции. Необходимы дальнейшие исследования, чтобы понять иммунные реакции, которые возникают естественным образом при инфекции. Чтобы обойти эту проблему, важно отслеживать глобальную разработку противотуберкулезной вакцины, и этого можно добиться путем поощрения партнерства «Остановить ТБ» для сбора конвейеров вакцин, чтобы признать текущий профиль вакцины-кандидата и новые терапевтические стратегии.Комбинация примирующих, бустерных и терапевтических вакцин может обеспечить защиту до и после воздействия ТБ-антигена во время ТБ-инфекции, которая может быть дополнительно усилена быстрым диагностическим подходом и дополнительным лекарственным лечением против ТБ с множественной лекарственной устойчивостью [73, 74]. 5. Будущие направления развития противотуберкулезных вакцинТекущие вакцины, находящиеся в разработке, сильно перекошены в сторону защитной вакцинации и терапии в сочетании с химиотерапией. Эта текущая тенденция весьма правдоподобна, и в свете полученных результатов, будь они положительными или отрицательными, она лишь указывает на возможную борьбу с ТБ.Однако мы все еще далеки от бесплодной ликвидации туберкулеза. Чтобы улучшить уже сделанные открытия, мы хотели бы подчеркнуть несколько ключевых факторов, которые, по нашему мнению, помогут в разработке вакцин с повышенной эффективностью. Одним из ключевых факторов, который, по нашему мнению и другим, будет иметь решающее значение для создания лучшей вакцины, является роль В-клеток и антител [5]. Как и все вакцины против инфекционного заболевания, то есть вируса гепатита В, антитела играют доминирующую роль в обеспечении начальной защиты от поступающей инфекции.Антитела являются связывающими агентами, которые не только специфичны по отношению к своим мишеням, но и привлекают многие ответвления иммунной системы (NK-клетки, нейтрофилы и т. д.) к очагу инфекции, тем самым увеличивая вероятность бесплодной эрадикации. Хотя мы обсуждали способность M. tb уклоняться от этого способа эрадикации, мы считаем, что введение вакцины, способной вызывать Th3-ответы, и соответствующего антигена, особенно на латентной стадии, может генерировать антитела, направленные против легочных M. .тб . Открытие подавленных инвариантных Т-клеток естественных киллеров (iNKT-клеток) в периферической крови больных туберкулезом [75] также указывает на возможность использования антител в качестве способа нацеливания на латентную инфекцию и активацию iNKT-клеток через α -галактозилцерамид ( α -GalCer) [32, 76] могли бы приводить к гибели латентно инфицированных клеток. Однако, как упоминалось Nunes-Alves et al., использование α -GalCer еще предстоит изучить. Однако его можно заменить другим активатором iNKT-клеток, таким как минорные виды липидов, которые совместно очищаются с β -GlcCer у млекопитающих [77].Помимо индуцирования ответов антител, использование соответствующего антигена является ключом к образованию цитотоксических антиген-специфических CD4 + и CD8 + Т-клеток. Как мы наблюдали в разрабатываемых в настоящее время вакцинах, они в основном были нацелены против Ag85A, Ag85B и ESAT-6. Все эти мишени являются очень иммунодоминантными, и если это так, при латентном туберкулезе, постоянно стимулирующем аналогичные клоны Т-клеток, и результатах, показывающих активацию Treg у пациентов, также будут Tregs, которые специально нацелены на подавление ответов T-клеток против этих антигенов.Эта ситуация часто наблюдается при хронических заболеваниях, а также при раке, когда антиген-специфические Treg часто обладают превосходной супрессорной способностью, что приводит к подавлению Т-клеточного ответа [78]. Мы предполагаем, что это может быть одной из причин, по которой результаты, полученные в ходе клинических испытаний, уступают результатам, полученным в исследованиях на животных. Генерация Т-клеточного ответа против М. tb , который еще предстоит подавить, потребует поиска новых антигенов, которые конститутивно экспрессируются, но менее иммунодоминантны.Одним из примеров такого возможного антигена является Mtb32, который, несмотря на то, что он менее изучен, показал себя многообещающим антигеном для генерации CD4 + и CD8 + Т-клеточных ответов до и после воздействия на моделях мышей M. tb . [79, 80]. Другим ключевым фактором при разработке потенциальной вакцины будет использование адъюванта, который будет обеспечивать эффекты депо, стимулировать врожденный иммунитет для создания провоспалительной среды и искажать ответы Th [81]. Комбинация эмульсии сквален/твин-80, 2-агониста TLR, пептида-мишени МНС класса I, хелперного пептида МНС класса II и IFN-гамма недавно показала образование высоких уровней антиген-специфических CD8 + T- клетки, которые не только являются цитотоксическими, но и, как было показано, генерируют Т-клетки памяти.Ответы, вызванные этой комбинацией (адъювант CASAC), были не только против чужеродных антигенов (овальбумин), но также были способны усиливать ответы против собственного антигена (белок 2, родственный тирозиназе). Полученные ответы были способны устранить заражение мышиной меланомой B16. Сгенерированные ответы также можно было вспомнить после 50-дневного периода отдыха [82]. Последний ключевой фактор, который мы должны учитывать, — это использование антител, которые истощают или блокируют подавляющие сигналы, такие как запрограммированная смерть 1 (PD-1), цитотоксический Т-лимфоцитарный антиген 4 (CTLA-4) и, в конечном счете, Treg.PD-1, CTLA-4 и Treg коррелируют в подавлении ответов Т-клеток. В недавнем исследовании по разработке противораковых вакцин было показано, что PD-1 и CTLA-4 присутствуют на инфильтрирующих опухоль лимфоцитах (TIL), антиген-специфических CD8 + T-клетках. Это присутствие регулировалось Treg, что в конце концов вызывало дисфункцию цитотоксических Т-клеток, инфильтрирующих опухоли. В сравнительном исследовании двойная блокада PD-1 и CTLA-4 восстанавливала дисфункцию этих TIL и вызывала 100% отторжение опухоли [83].Это может быть очень интересным направлением для возможного восстановления функций реактивных Т-клеток, которые могли быть сгенерированы на начальной стадии инфекции ТБ, как описано ранее. Основываясь на этом направлении мыслей, мы предлагаем возможность разработки новых вакцин на основе использования адъюванта, такого как CASAC, в сочетании с новыми антигенами, обладающими меньшей иммунодоминантностью, и предварительной обработки антителами, которые истощают или блокируют супрессивные реакции, такие как антигены. -PD-1 и анти-CTLA-4. При таком же ходе мыслей мы считаем, что использование белков теплового шока (HSP) в качестве иммуногенного носителя может иметь потенциальную пользу [84–86]. HSP представляют собой группу белков, которые распознаются иммунной системой человека и экспрессируются во время воспаления. Иммунная система человека обладает естественным аутоиммунитетом по отношению к HSP, в частности к HSP60, в результате чего будут генерироваться ответы Т-клеток CD4 + . | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 Отдельный случай, когда вакцинацию рекомендуется отложить – наличие у ребенка до года доброкачественной нейтропении. Это состояние связано с адаптацией ребенка к нашим городским условиям, современным нагрузкам; проявляется тем, что в анализе крови наблюдается недостаточное количество нейтрофилов. Причем это количество не укладывается ни в норму, ни в состояние при болезни, а находится в среднем значении. В такой ситуации лучше не нагружать организм дополнительно, его иммунные силы сейчас и так ослаблены, и все силы направлены на то, чтобы адаптироваться к окружающей среде.
Отдельный случай, когда вакцинацию рекомендуется отложить – наличие у ребенка до года доброкачественной нейтропении. Это состояние связано с адаптацией ребенка к нашим городским условиям, современным нагрузкам; проявляется тем, что в анализе крови наблюдается недостаточное количество нейтрофилов. Причем это количество не укладывается ни в норму, ни в состояние при болезни, а находится в среднем значении. В такой ситуации лучше не нагружать организм дополнительно, его иммунные силы сейчас и так ослаблены, и все силы направлены на то, чтобы адаптироваться к окружающей среде.

 ). Например, всем жителям Новосибирской области рекомендуется ставить прививку от клещевого энцефалита – опасной инфекции, которой можно заразиться при укусе клеща.
). Например, всем жителям Новосибирской области рекомендуется ставить прививку от клещевого энцефалита – опасной инфекции, которой можно заразиться при укусе клеща. Поэтому вовремя пройденная вакцинация ребенком – гарант его
крепкого здоровья;
Поэтому вовремя пройденная вакцинация ребенком – гарант его
крепкого здоровья;