Мифы о прививках
Миф: В состав вакцин входят опасные для здоровья ребенка вещества, такие как ртуть. Они вызывают необратимые последствия, вплоть до развития аутизма у привитого.
Факт: Непонимание вопроса приводит к ложным выводам и необоснованным страхам. В некоторых вакцинах для взрослого населения в качестве консерванта содержится органическое соединение ртути, которое имеет период полувыведения до 3,5–4 дней. Важно понимать, что консервант в небольшом количестве совершенно безопасен для здоровья человека. Его объем в одной дозе вакцины меньше того, что мы потребляем в течение дня с пищей, или вдыхая городской воздух. Многочисленные исследования нейрохимического развития подтверждают, что зависимости между вакцинацией содержащими мертиолят препаратами и нарушениями в развитии, в том числе в нейропсихическом, не существует. Слухи о том, что консервант или компоненты вакцин могут провоцировать аутизм, были инициированы работой английского доктора Эндрю Уэйкфилда.
Миф: Вакцинация сопровождается реакцией организма, которая сравнима с симптомами самой болезни или ее осложнениями.
Факт: Как мы ранее выяснили, в отличие от «естественной» инфекции, которая наносит мощный удар по организму и характеризуется попаданием в него живых патогенных микроорганизмов и их активным размножением,
Миф: У детей есть природный иммунитет, который может пострадать, если его «нагружать» многочисленными прививками.
Факт: Иммунную систему невозможно «перегрузить» вакцинами, а пренебрежение ими может, напротив, причинить серьезный вред здоровью, поскольку у ребенка нет природного «врожденного» иммунитета от опасных инфекций.
Миф: Организму легче справляться с вирусной нагрузкой, если вводить вакцины по одной, а не несколько одновременно.
Факт: У иммунитета не существует определенного предела, дальше которого защита начинает ослабевать из-за слишком большой нагрузки. Он постоянно реагирует на многочисленные бактерии, которыми наполнена окружающая нас среда. Давно доказано, что введение многокомпонентных (пяти- и шестикомпонентных) вакцин воспринимается организмом так же, как и профилактика моновакцинами, и иммунная реакция проявляется в равной степени – накопительного эффекта, который рисует наше сознание, нет – иммунитет работает совершенно иначе. При этом ребенку гораздо легче переносить один укол, а родителям не приходится испытывать стресс из-за частых походов в поликлинику.
При этом ребенку гораздо легче переносить один укол, а родителям не приходится испытывать стресс из-за частых походов в поликлинику.
Миф: Многие люди не прививают своих детей и не делают вакцинацию сами и при этом не болеют.
Факт: Официальная статистика однозначна – среди привитых людей случаев заболеваний намного меньше, чем среди невакцинированного населения. Чтобы сделать корректное заключение о пользе вакцинации, необходимо сравнивать сопоставимые случаи – пол, возраст, социальные обстоятельства, что недоступно обычному человеку. Кроме того, необходимо принимать во внимание такой феномен, как коллективный иммунитет – в обществе с широким охватом уровня вакцинации населения болезнь распространяется не столь активно и без вспышек, такая массовая защита помогает сохранять здоровье и отдельному индивиду. Случается и так, что привитый человек заболевает, например, гриппом. В таком случае можно говорить об изменчивости некоторых вирусов, быстрые мутации которого могут быть незнакомы организму.
Миф: Поствакцинальная реакция на АКДС опаснее, чем болезни, от которых она защищает.
Факт: Действительно, более 70% поствакцинальных реакций приходится на вакцину, содержащую коклюшный компонент, именно поэтому она вызывает больше всего опасений у родителей. У детей после прививки повышается температура, они могут проявлять беспокойство или впадать в сонливое состояние, становиться плаксивыми, плохо спать, нередки и аллергические реакции. Все эти проявления ожидаемы и проходят в течение суток.

Миф: Люди с аллергией, хроническими заболеваниями не должны прививаться, так как у них ослабленный иммунитет.
Факт: Именно ослабленный иммунитет – виновник того, что инфекционные заболевания протекают намного тяжелее, чем у здоровых людей. Как мы уже выяснили, в основе механизма действия вакцины лежит способность организма создавать иммунную память, для выработки которой ему нужно минимальное количество антигенов. Без предварительной подготовки, не имея специфического иммунитета, при встрече с настоящей инфекцией ослабленные основным заболеванием защитные механизмы человека могут не сработать. Так, коклюш или ветряная оспа могут сильно отягощать течение хронических недугов, иногда они становятся причиной смерти.
Миф: Вакцинироваться от гриппа не имеет смысла, так как все равно заболеешь.
Факт: Грипп ошибочно воспринимают как легкое недомогание, которое излечивается народными средствами. Он тяжело переносится организмом, ежегодно в мире из-за заболевания и его осложнений умирают сотни тысяч людей. Вакцинация обеспечивает иммунитет против трех наиболее распространенных штаммов, циркулирующих в любой сезон, поэтому шансы заразиться после прививки снижаются, но не исчезают полностью. Действительно
Миф: Вакцинация намного опаснее, чем признает официальная медицина. Количество осложнений после прививок замалчивается.
Количество осложнений после прививок замалчивается.
Факт: Все случаи серьезных осложнений тщательно расследуются и фиксируются Росздравнадзором. Каждое заявление подлежит статистическому учету, на основании которого принимается решение об изъятии партии той или иной вакцины. Практически все реакции на иммунобиологические препараты известны медицине, поэтому врачи могут оказать адекватную и оперативную помощь в случае появления поствакцинальных или нежелательных реакций.
«Вся правда о прививках» или чего на самом деле стоит бояться родителям, отказывающимся от вакцинации? (+видео!)
 Как врач, она должна была бы рассказать, к какому заключению о причинах смерти в конце концов пришла комиссия. Ведь все случаи побочных явлений после прививок тщательно рассматриваются комиссионно, так что ни один из них не остается не расследованным – особенно в наше время, когда противники вакцинации ищут любого повода очернить прививки.
Как врач, она должна была бы рассказать, к какому заключению о причинах смерти в конце концов пришла комиссия. Ведь все случаи побочных явлений после прививок тщательно рассматриваются комиссионно, так что ни один из них не остается не расследованным – особенно в наше время, когда противники вакцинации ищут любого повода очернить прививки.Так вот, внезапная смерть младенцев – это устоявшийся диагноз. В возрасте 2-4 месяцев жизни внезапно умирают дети, как получившие, так, чаще не получившие прививку. Педиатр, тем более со стажем, должен знать, что внезапная смерть младенцев – это вторая по частоте причина постнеонатальной младенческой смертности. А также и то, что из известных причин на первом месте стоят курение родителей, сон младенца на животе, сон в одной постели с матерью. Вот об этом стоит предупредить родителей. А от введения АКДС умереть просто невозможно, за 3 дня эта инактивированная вакцина даже еще не начнет действовать на иммунную систему.
— Помимо голословности заявлений, отсутствия фактов, какие особенности материала Вы бы еще отметили?
Это некомпетентность. Автор не пишет, где и сколько она училась на невропатолога, после того как прекратила работать в детском саду. Не думаю, что подготовка была серьезной. Она, например, указывает: «Известно, что скрытая или явная патология нервной системы после вакцинации может манифестировать в виде судорожной готовности. То есть, вакцинация может провоцировать эпилепсию (описанное осложнение на вакцинацию)».
Автор не пишет, где и сколько она училась на невропатолога, после того как прекратила работать в детском саду. Не думаю, что подготовка была серьезной. Она, например, указывает: «Известно, что скрытая или явная патология нервной системы после вакцинации может манифестировать в виде судорожной готовности. То есть, вакцинация может провоцировать эпилепсию (описанное осложнение на вакцинацию)».
Я напомню, что эпилептический припадок у больного эпилепсией гораздо чаще вызывает мелькание экрана телевизора, чем болевые ощущения, связанные с прививкой. Может запретить телевизор? Да, у небольшой части детей повышение температуры после введения вакцины может вызвать фебрильные судороги. Но ведь и они у 99 детей из 100 бывают при развитии инфекции. К тому же, врач-невропатолог должен не распалять родителей по этому поводу, а объяснить, что фебрильные судороги доброкачественные и ничем ребенку не грозят.
Также автор указывает: «Однажды на консультации был особенно тяжелый ребенок, угрожаемый по ДЦП (на самом деле-то уже с ДЦП, но такой диагноз ему поставят после года), я запретила делать ему вакцинацию, потому что на ее фоне ДЦП резко прогрессирует».
Это ее утверждение выглядит совсем дико — ДЦП – врожденное заболевание, ребенок рождается с теми или иными повреждениями, которые могут позже проявиться двигательными или иными расстройствами по мере роста ребенка (например, неспособность сидеть до 6-8 месяцев выявить нельзя, как и неспособность ходить до возраста 1 года), но никак не прогрессировать.
Противники вакцинации чаще всего связывают с прививкой поражения нервной системы. Я хотел бы предложить автору покопаться в книгах по неврологии и найти там – среди причин нервных болезней – прививки, и рассказать родителям, какие это болезни. Да, еще 10 лет назад у детей с врожденным иммунодефицитом живая полиомиелитная вакцина вызывала параличи (5-8 детей в год на всю Россию) – но сейчас прививают инактивированной вакциной, так что эти осложнения исчезли.
Что касается причитаний о том, что прививка «является серьезной иммунобиологической операцией», это говорилось задолго до г. Онищенко; думаю, доктор Емельянова согласится со мной, что, например, употребление в пищу многих продуктов, вызывающих аллергию, — гораздо более частая, чем прививки и более «серьезная иммунобиологическая операция», поскольку вызывает подчас тяжелые поражения, вплоть до анафилактического шока, с летальным исходом. Вот бы ей разъяснить родителям, какие виды пищи лучше не давать маленькому ребенку.
Вот бы ей разъяснить родителям, какие виды пищи лучше не давать маленькому ребенку.
— А как Вы могли бы прокомментировать такое утверждение: «все современные вакцинирующие препараты получают методами биотехнологии с использованием сывороток и клеток животных. У животных, как становится известно нам чем дальше, тем больше, есть чрезвычайно опасные для человека инфекции типа прионных и ретровирусных. Очистить вакцину от примесей, потенциально содержащих эти инфекции, принципиально невозможно?
Действительно, есть опасения передачи ретровирусов и прионов через вакцины – это, конечно проблема, но с ней пока что успешно справляются изготовители вакцин. Фактов подобных заболеваний не могут привести даже ярые противники вакцинации.
— Действительно ли вакцины могут спровоцировать серьезные аутоиммунные заболевания?
Причина их вообще не совсем ясна, так что их легко нарочно привязать к теме прививок. Но и это не получается – в ряде стран подсчитана частота этих болезней до проведения прививок (например, против папилломавирусной инфекции) и после – цифры сходятся, указывая на непричастность вакцин к их развитию. Вообще, противники вакцинации любят ссылаться на отдельные случаи, обычно недостаточно обследованные, и не приводят цифры. А они интересны.
Вообще, противники вакцинации любят ссылаться на отдельные случаи, обычно недостаточно обследованные, и не приводят цифры. А они интересны.
Так, в 80-е годы пошел вниз охват прививками АКДС – и с 90-х годов в странах бывшего СССР разразилась эпидемия дифтерии – 120 000 случаев при 6000 умерших. Плюс к этому рост коклюша и кори. Тогда Минздрав спросил инфекционистов – что делать? Единственный выход – массовые прививки – и привиты были все 150 000 000 россиян, некоторые повторно. И, знаете, каких-то особых неприятностей это не принесло. И после 1995 г. массовые прививки детей от полиомиелита погасили вспышку, привили всех, так что при заносе этой инфекции в 2010 г. из Таджикистана в России заболели полиомиелитом всего 8 детей – и все не привитые (6 из них с фиктивными справками о прививках).
А кто болеет корью в наше время? Дети, чьи родители слушают «всю правду о прививках». И с коклюшем мы пока справиться как следует не можем из-за большого числа отказавшихся от прививок. Зайдите в нашу клинику, поговорите с родителями не привитого ребенка с коклюшем – а это 15-20 приступов кашля в день со рвотой, и так в течение 3-4 недель. Из-за низкого охвата заражаются дети первых месяцев, еще не привитые – они болеют очень тяжело, и нередко дело кончается летальным исходом.
Зайдите в нашу клинику, поговорите с родителями не привитого ребенка с коклюшем – а это 15-20 приступов кашля в день со рвотой, и так в течение 3-4 недель. Из-за низкого охвата заражаются дети первых месяцев, еще не привитые – они болеют очень тяжело, и нередко дело кончается летальным исходом.
Мой совет докторам, устроившим антипрививочную пропаганду, повернитесь лицом к действительным проблемам и не дурите голову 20 миллионам родителей в России, прививающих детей от всех инфекций. Ведь предсказывали люди вашего круга в конце 18 века, что прививки Дженнера против оспы приведут к появлению рогов и вымени у привитых. Сейчас эти страсти Вы заменили на аутоиммунные болезни, диабет, рак. Уже много поколений человечества выросло с прививками (уверен, и авторы статей против прививок), прививки не только не мешали, но и способствовали, как никакие другие меры медицинского характера, улучшению показателей физического развития человека, его способностей, снижению смертности и увеличению продолжительности жизни – и в дальнейшем они будут способствовать укреплению здоровья, нравится это противникам прививок или нет.
Я, например, сделал всем своим детям, внукам и правнукам все необходимые прививки, и сам ежегодно прививаюсь от гриппа.
Подготовлено по материалам портала:
Использованы иллюстрации комикса Maki Naro.
Переводчик: irvitzer.
Отсроченные последствия вакцин: стоит ли их опасаться?
Под словами «побочный эффект» часто понимают очень разные вещи. С одной стороны, это вполне ожидаемые спутники прививки вроде повышенной температуры, слабости и ломоты в мышцах. Они связаны с активацией иммунных процессов и даже могут служить подсказкой, что вакцина сработала. С другой стороны, к побочкам относят и те проявления, которые создатели вакцины не прогнозировали.
Но и с последними все не так просто. Даже качественная вакцина, которую проверяли годами, все равно не будет застрахована от форс-мажоров. Особенно если ее производят в огромных масштабах. Например, если на производстве нарушены меры безопасности, в партию может попасть инфекция. Проблемы могут возникнуть и на этапе введения вакцины — из-за ошибки медработника. К примеру, если игла попадет не в мышцу, а в кровеносный сосуд, эффекты от вакцины могут быть другими (на этом остановимся чуть позже).
Проблемы могут возникнуть и на этапе введения вакцины — из-за ошибки медработника. К примеру, если игла попадет не в мышцу, а в кровеносный сосуд, эффекты от вакцины могут быть другими (на этом остановимся чуть позже).
Еще один фактор — особенности здоровья конкретного пациента. Во время испытаний разработчики стараются подбирать не только здоровых добровольцев, но и тех, у кого есть хронические болезни, аллергические реакции и другие нарушения иммунитета. Но учесть все варианты просто невозможно. А на риск побочек могут «работать», например, комбинированные нарушения и редкие генетические варианты. Поэтому до сих пор нет ни одного лекарства, у которого в инструкции не было бы списка побочных эффектов.
Наконец, у каждого типа вакцин свои риски. Большая часть из них пока связана с ослабленными живыми вакцинами — к ним относится, например, комбинированная вакцина против кори, паротита и краснухи (КПК), противотуберкулезная БЦЖ и оральная вакцина против полиомиелита. Причины понятны: там содержится настоящий патоген, способный заражать клетки. С другой стороны, полностью обезвреженная (или даже состоящая из отдельных частей патогена) вакцина может не «заинтересовать» иммунную систему так, как это сделала бы живая.
С другой стороны, полностью обезвреженная (или даже состоящая из отдельных частей патогена) вакцина может не «заинтересовать» иммунную систему так, как это сделала бы живая.
Поэтому фармакологи постоянно ищут способы убить двух зайцев: имитировать процесс заражения, но при этом обойтись без присутствия патогена. А медицинские регуляторные органы ищут способы «отлавливать» побочные явления как можно быстрее, чтобы меньше людей столкнулись с ними в будущем.
Отделить «сигнал» от «шума»
Сбором информации о «побочках» занимаются прежде всего контролирующие органы в странах, где проводится вакцинация. Например, в ЕС это Европейское агентство по контролю качества лекарственных средств (EMEA), а в США — Управление по контролю качества продуктов питания и лекарственных средств в США (FDA). Данные, собранные национальными службами, затем передаются во Всемирную организацию здравоохранения. Но окончательное решение — продолжать вакцинацию или приостановить — остается за конкретными странами.
Например, в США начиная с 1990-х годов работает система VAERS (Vaccine Adverse Event Report System). Любой человек — в том числе сами пациенты, их родители и медицинские работники — может подать сообщение о нежелательном эффекте в систему. Обратная сторона такой оперативности в том, что данные в системе сырые, а их вольная интерпретация чревата ошибками. При этом доступ к информации открытый, его может получить получить кто угодно — в том числе непрофессионалы.
В мае 2021 года в США разразился скандал, поводом для которого послужила как раз неверная интерпретация данных VAERS. Ведущий канала Fox News Такер Карлсон сообщил в эфире, что в Соединенных Штатах после вакцинации от COVID-19 умерли 3362 человека. Эту новость перепечатал ряд консервативных и конспирологических сайтов. Авторы заголовков соревновались в сенсационности: «Число смертей от антиковидных вакцин больше, чем от всех вакцин за последние 20 лет вместе взятых».
Но специалисты возразили, что журналисты просто не разобрались в том, как работает система отчетности. Поскольку вакцины получили разрешение в экстренном порядке, врачи — согласно протоколу — должны были самым тщательным образом документировать все проблемы со здоровьем у привитых. Учитывая, что счет шел на десятки миллионов людей, в базу попадало много случайных событий. Часть из них неизбежно накладывались на период после прививки.
Поскольку вакцины получили разрешение в экстренном порядке, врачи — согласно протоколу — должны были самым тщательным образом документировать все проблемы со здоровьем у привитых. Учитывая, что счет шел на десятки миллионов людей, в базу попадало много случайных событий. Часть из них неизбежно накладывались на период после прививки.
Именно так работает статистическая связь: когда у вас есть большие данные, частота одних событий может случайным образом совпадать с частотой других. Возникает соблазн найти в этом совпадении закономерность. Например, в США каждые четыре минуты регистрируется смерть от инсульта. Большинство умерших за неделю до этого хотя бы раз принимали душ. Или пили кофе. Значит ли это, что для снижения числа инсультов нужно запретить кофе и гигиенические процедуры?
В статистике есть понятия «шум» и «сигнал». Чтобы услышать голос проблемы («сигнал») за «шумом» данных, сотрудники медицинских регуляторов строят гипотезы, а затем тестируют их. Они запрашивают медицинскую карту пациента, относящуюся к серьезному нежелательному явлению, чтобы узнать больше о том, что произошло. Они просматривают эти медицинские записи и определяют, вызвано ли указанное нежелательное явление именно вакциной. И в большинстве случаев связь оказывается ложной. Хотя и не всегда.
Они просматривают эти медицинские записи и определяют, вызвано ли указанное нежелательное явление именно вакциной. И в большинстве случаев связь оказывается ложной. Хотя и не всегда.
Ротавирусная дилемма
Ротавирусная инфекция — частая проблема у младенцев и детей раннего возраста и одна из причин тяжелой диареи во всем мире. У взрослых и детей старшего возраста инфекция проходит обычно без серьезных последствий. А подавляющее большинство смертей приходится на детей младше трех лет. Поэтому разработка вакцин против ротавируса была приоритетом исследовательского сообщества с начала 1970-х годов, в течение нескольких лет после открытия самого вируса.
Вакцина RotaShield стала первой, одобренной для использования в Соединенных Штатах в августе 1998 года. Результаты исследований вакцины показали эффективность 69–91% против тяжелой диареи, которая с наибольшей вероятностью может привести к госпитализации или смерти. Эти уровни были сопоставимы с таковыми у большинства других вакцин в США. Профиль безопасности вакцины был положительным, самым частым побочным явлением было умеренное повышение температуры.
Профиль безопасности вакцины был положительным, самым частым побочным явлением было умеренное повышение температуры.
Вакцинация стартовала в начале весны 1999 года, и уже к середине марта VAERS получила 62 отчета о побочных эффектах, потенциально связанных с RotaShield. Среди них были и три случая инвагинации кишечника. Это неотложное состояние, при котором один участок кишки, как телескоп, «складывается» в другую часть. Это вызывает боль, рвоту и кишечную непроходимость. Если не начать лечение вовремя, может начаться перитонит — воспаление кишечника.
РНК-вирус, ответственный за доброкачественный инфекционный гастроэнтерит у детей
© BSIP/UIG Via Getty ImagesК 17 июня было выявлено еще девять случаев инвагинации — на эту дату было назначено заседание Консультативного комитета по методикам иммунизации. Было решено провести экстренное расследование связи между инвагинацией и вакциной RotaShield, чтобы определить, действительно ли существует связь, и если да, с чем она может быть связана.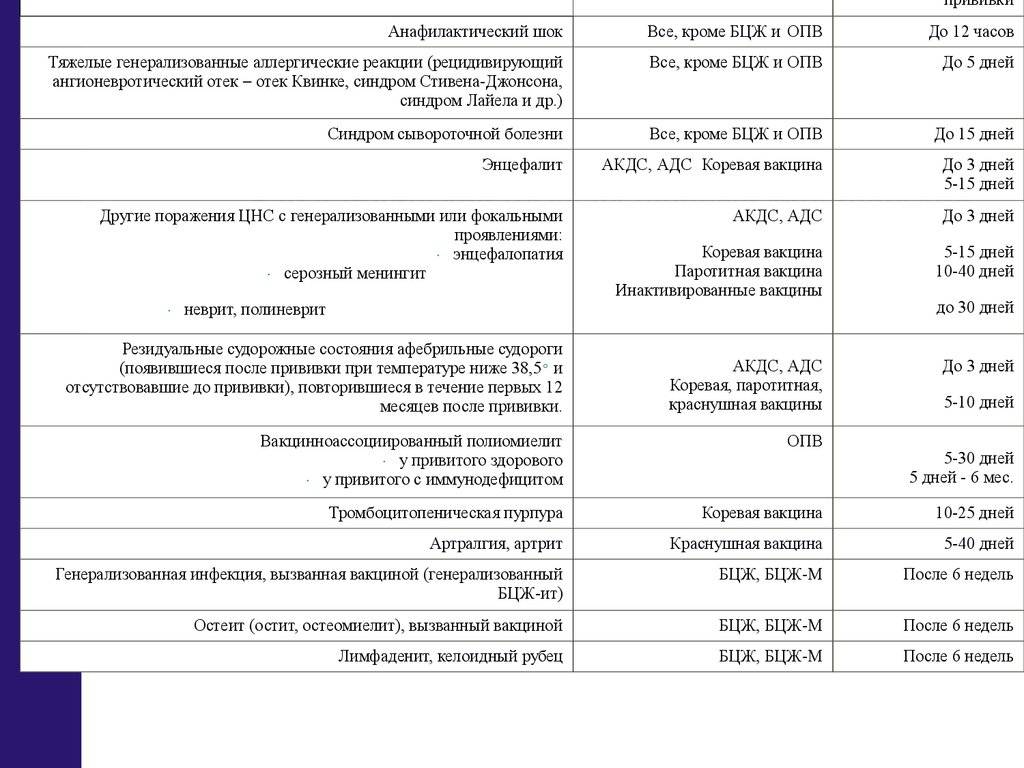 Уже 13 июля Центр по контролю за заболеваниями временно приостановил использование вакцины. К тому времени дозу получили около 900 тыс. детей.
Уже 13 июля Центр по контролю за заболеваниями временно приостановил использование вакцины. К тому времени дозу получили около 900 тыс. детей.
Расследование показало, что статистически риск инвагинации у вакцинированных был выше в 20–30 раз по сравнению с обычным риском у детей этой возрастной группы в течение двух недель после первой дозы. Риск также увеличился в три — семь раз после второй дозы. При этом не было отмечено повышение риска после трех недель с момента введения любой дозы. В итоге в октябре 1999-го на заседании Консультативного комитета вакцину запретили к использованию. С ним согласились и эксперты ВОЗ.
Самое любопытное, что случаи инвагинации встречались и в ходе клинических испытаний: у пяти детей из 10 тыс., получивших вакцину, и у одного из 4,6 тыс. в контрольной группе. Никто не скрывал этот факт, данные были упомянуты в публикации по результатам испытаний наравне с другими. Но разработчики, опираясь на среднюю распространенность таких случаев, не посчитали различие статистически значимым.
Это фиаско поставило фармакологов в трудное положение. Ведь точный механизм появления «избыточных» случаев инвагинации установить не удалось. А значит, непонятно, куда двигаться дальше. Разработчикам приходилось действовать, меняя подходы практически вслепую. И хотя новые препараты оказались более безопасными (сейчас они есть в Национальных календарях прививок), часть врачей и исследователей до сих пор критикуют решение властей по RotaShield.
Ведь даже с учетом редких (один случай на 12 тыс. детей) случаев инвагинации прививки все равно предотвращали несоизмеримо больше проблем, чем вызывали сами. Особенно это касалось детей в развивающихся странах, где более полумиллиона умирают от ротавируса каждый год. Останься RotaShield на международном рынке, вероятно, она спасла бы многих из них.
Загадка нарколепсии
Связь между вакцинами и их последствиями выявить тем труднее, чем больше проходит времени и чем менее очевидна эта связь. Именно так и произошло во время вспышки свиного гриппа (подтип h2N1) в 2009 году.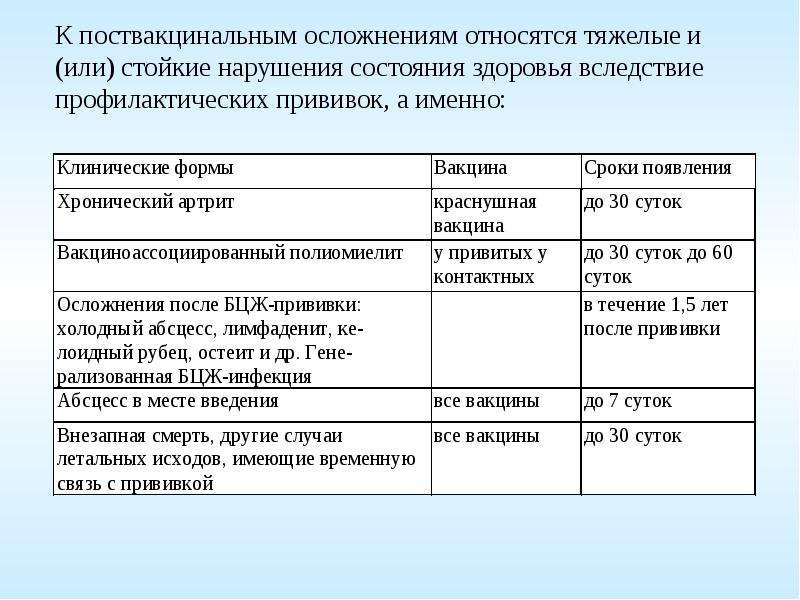 Тогда, как и в случае с нынешней пандемией, в особом порядке была зарегистрирована вакцина Pandemrix. Она была сделана быстро благодаря макетной технологии: в составе уже опробованной вакцины от другого гриппа просто заменяли штамм, не проводя дополнительных испытаний.
Тогда, как и в случае с нынешней пандемией, в особом порядке была зарегистрирована вакцина Pandemrix. Она была сделана быстро благодаря макетной технологии: в составе уже опробованной вакцины от другого гриппа просто заменяли штамм, не проводя дополнительных испытаний.
Вакцина Pandemrix компании GlaxoSmithKline
© Andreas Rentz/Getty ImagesНо в течение полугода из разных стран начали поступать сообщения о случаях нарколепсии у вакцинированных детей. Заболевание обычно регистрировали через месяц или два после укола, но бывали и случаи, когда проходило полгода. Причем преимущественно эти случаи были выявлены в Северной Европе, где один заболевший приходился на каждые 15–16 тыс. вакцинированных. В Великобритании, Ирландии и Нидерландах были лишь отдельные случаи на миллионы людей, а в других странах их не было вовсе.
Нарколепсия — это тяжелое неврологическое расстройство сна. У больного нарушается регуляция химических процессов, в результате чего у него могут возникать внезапные приступы сонливости, а общее время бодрствования резко сокращается. Кроме того, у людей с нарколепсией возникают галлюцинации после пробуждения и другие неудобства. Природа нарколепсии до последнего времени была не вполне ясна, и это затрудняло поиск ответов на вопрос — может ли она быть вызвана действием вакцины.
Кроме того, у людей с нарколепсией возникают галлюцинации после пробуждения и другие неудобства. Природа нарколепсии до последнего времени была не вполне ясна, и это затрудняло поиск ответов на вопрос — может ли она быть вызвана действием вакцины.
Проведенное Всемирной организацией здравоохранения расследование показало, что у всех заболевших имелась генетическая предрасположенность к заболеванию. При этом эксперты пришли к выводу, что вакцина не вызывала болезнь напрямую. Нарколепсия проявлялась только при взаимодействии вакцины с «другим, пока неизвестным фактором». В 2010 году Европейское агентство лекарственных средств рекомендовало воздержаться от вакцинации до получения результатов. Несколько стран (Финляндия и Эстония) полностью приостановили прививочную кампанию.
В ряде государств заболевшие нарколепсией, считавшие, что причина в вакцине, обращались в суд (правда, с переменным успехом). В других странах решения о компенсациях заболевшим были приняты на уровне правительств (например, в Швеции). Сомнения отчасти разрешились в 2013 году, когда группа ученых выяснила, что у некоторых людей после вакцинации Pandemrix вырабатываются антитела, которые атакуют их собственный нейромедиатор гипокретин. Снижение его количества и приводит к развитию нарколепсии. Работа, кстати, была проспонсирована самой компанией-производителем.
Сомнения отчасти разрешились в 2013 году, когда группа ученых выяснила, что у некоторых людей после вакцинации Pandemrix вырабатываются антитела, которые атакуют их собственный нейромедиатор гипокретин. Снижение его количества и приводит к развитию нарколепсии. Работа, кстати, была проспонсирована самой компанией-производителем.
При этом в выводах статьи авторы указали, что их открытие не до конца проясняет ситуацию. Например, почему случаи нарколепсии были связаны именно с этой вакциной против гриппа h2N1 (а не с какой-либо другой)? И почему эти случаи встречались с такой неравномерностью? Загадка вакцинной нарколепсии не разгадана полностью до сих пор, однако в процессе ученые узнали больше о природе болезни. В каком-то смысле побочки Pandemrix подстегнули развитие науки.
Худший вариант, за исключением остальных
Если сравнивать нежелательные последствия вакцин именно по степени отдаленности, рекордсменом будет вакцина БЦЖ от туберкулеза. Осложнения могут поражать разные органы. Например, хроническую инфекцию в костной ткани (остит и остеомиелит) выявляли через 12 месяцев с момента вакцинации и более. При этом вероятность таких последствий зависит от многих факторов — штамма, который используется в вакцине, числа жизнеспособных бацилл в партии, техники введения и иммунного статуса человека.
Например, хроническую инфекцию в костной ткани (остит и остеомиелит) выявляли через 12 месяцев с момента вакцинации и более. При этом вероятность таких последствий зависит от многих факторов — штамма, который используется в вакцине, числа жизнеспособных бацилл в партии, техники введения и иммунного статуса человека.
Альберт Кальмет (в центре)
© Bettmann/Getty imagesБЦЖ была разработана еще в начале прошлого века во Франции из болезнетворного штамма микобактерий туберкулеза бычьего вида (Mycobacterium bovis). Название как раз и происходит от сокращения слов «бацилла Кальмета (во французском начальная буква имени читается как Ц) — Герена». Вирусологи Кальмет и Герен обнаружили, что выращенные в особой среде туберкулезные палочки почти не способны заражать организм, но все еще вызывают иммунный ответ.
Стоит сказать, что БЦЖ — единственная в мире противотуберкулезная вакцина. Она вводится в обязательном порядке в 64 странах мира и официально рекомендована в 118 странах. С 1945 года эту прививку сделали более чем 3 млрд человек. Такой огромный массив данных дал медикам прекрасную возможность изучить и описать почти все побочные эффекты — а также их частоту и условия, в которых они возникают. И составить протоколы для их раннего выявления.
С 1945 года эту прививку сделали более чем 3 млрд человек. Такой огромный массив данных дал медикам прекрасную возможность изучить и описать почти все побочные эффекты — а также их частоту и условия, в которых они возникают. И составить протоколы для их раннего выявления.
Самым опасным последствием считается диссеминированная БЦЖ-инфекция — одновременное поражение множества органов. Она часто приводит к смерти. Однако во всем мире регистрируют всего по два — четыре таких случая на миллион введенных доз. Почти все жертвы имели серьезные сбои в работе иммунной системы, и вакцину им вводили по ошибке или незнанию. Риск смерти от любых инфекций у таких детей гораздо выше, чем у большинства людей.
БЦЖ вакцина компании AJ Vaccines
© Paul Kane/Getty ImagesВызванные вакциной остит или остеомиелит, которые обычно поражают длинные кости рук и ног, наблюдают еще реже — например, в России это 0,3 случая на миллион (но в целом для некоторых партий препарата число может доходить и до 30 на миллион), и при их возникновении прогноз хороший. Сегодня такие инфекции успешно лечатся антибиотиками, и большинство детей выздоравливают и живут нормальной жизнью.
Сегодня такие инфекции успешно лечатся антибиотиками, и большинство детей выздоравливают и живут нормальной жизнью.
Поголовная БЦЖ-вакцинация — пример прагматичного подхода, которому следует медицина. Как сказал однажды Черчиль: «Демократия — худшая из форм правления, за исключением всех остальных». Введение живого микроба в организм — это всегда риск, независимо от того, насколько он ослаблен. Лучше всего было бы не вводить ничего. Но тогда риск заболеть туберкулезом тоже должен быть нулевым, так как его последствия во много раз страшнее. Так что с несовершенством вакцины нам придется мириться до тех пор, пока не найдется более технологичного способа познакомить организм с патогеном.
Вектор неопределенности
Сегодня векторные вакцины претендуют (наряду с мРНК-вакцинами) на роль лидеров по соотношению безопасности и эффективности. Они не содержат живого возбудителя, а только инструкцию для сборки его ключевого белка. Антитела к нему лучше всего нейтрализуют инфекцию. При этом содержащийся в вакцине вектор (доставщик) — технически тоже вирус, но гораздо более безопасный. Во-первых, он лишен генов, отвечающих за размножение (репликацию), — а значит, он заразит лишь небольшое число клеток. Во-вторых, даже в природе он вызывает лишь легкую простуду.
При этом содержащийся в вакцине вектор (доставщик) — технически тоже вирус, но гораздо более безопасный. Во-первых, он лишен генов, отвечающих за размножение (репликацию), — а значит, он заразит лишь небольшое число клеток. Во-вторых, даже в природе он вызывает лишь легкую простуду.
Здесь есть своя ложка дегтя. Сегодня почти достоверно можно сказать, что у очень небольшого числа вакцинированных повышается риск образования тромбов — таких случаев приблизительно один на 100 тыс. человек (0,001% от всех, получивших прививку). Шанс летального исхода еще ниже: один на 1 млн (0,0001%). Причины таких осложнений до сих пор точно не установлены. Главное, до конца не ясно, на чьей стороне «мяч». Стоит ли доработать вакцины или, скажем, изменить инструкции по их применению.
По основной версии, в организме у некоторых привитых образуются антитела к собственным тромбоцитам, которые и вызывают слипание этих клеток и образование тромбов. Но почему появляются эти странные антитела? Одна из гипотез говорит о том, что векторы из вакцины случайно попадают в кровь (хотя в норме они должны попасть в мышечную ткань) и связываются там с тромбоцитами. Иммунные клетки распознают эти необычные образования как чужеродные и создают против них антитела, которые и атакуют нормальные тромбоциты. Причиной может быть, например, ошибка медработника.
Иммунные клетки распознают эти необычные образования как чужеродные и создают против них антитела, которые и атакуют нормальные тромбоциты. Причиной может быть, например, ошибка медработника.
Но случаи тромбозов регистрируют в первые неделю-две. Никаких отдаленных последствий, которые могли бы серьезно нарушить работу организма, у векторных вакцин до сих пор не выявлено. А могут ли они все же наступить? Точнее, насколько велика вероятность, что они наступят? Одно дело, когда ученые разводят руками и говорят: не знаем, давайте смотреть. И совсем другое — когда есть уверенность, основанная на знаниях. Скажем, перед запуском Большого адронного коллайдера многие опасались, что из-за столкновения частиц возникнет черная дыра, которая поглотит Землю. Но ученые объяснили на основе выводов теории относительности, что этот вариант невозможен.
Но вернемся к вакцинам. Один из главных страхов связан с тем, что вакцинные антитела каким-то образом вступят в реакцию с тканями нашего тела — с непредсказуемым результатом. И выяснится это только спустя годы — скажем, когда нас накроет «эпидемия» бесплодия. Например, исследователи заметили, что один из белков-шипов вируса по структуре якобы похож на белок синцитин-1, который участвует в развитии плаценты — важной части зародыша. Антитела к белку-шипу якобы должны ударить и по синцитину-1, а значит, привести к прерыванию беременности. Однако исследования не выявили способность антител связываться с этим белком.
И выяснится это только спустя годы — скажем, когда нас накроет «эпидемия» бесплодия. Например, исследователи заметили, что один из белков-шипов вируса по структуре якобы похож на белок синцитин-1, который участвует в развитии плаценты — важной части зародыша. Антитела к белку-шипу якобы должны ударить и по синцитину-1, а значит, привести к прерыванию беременности. Однако исследования не выявили способность антител связываться с этим белком.
Еще менее вероятно встраивание векторных частиц в геном клеток. Для этого вирусу необходимо иметь определенное «программное обеспечение», которое есть, например, у ретровирусов (а это другое вирусное семейство). Теоретически даже векторная частица может получить такую способность — благодаря способности вирусов «одалживать» гены у других организмов. Но исследования показали, что на практике этого не происходит. Векторы живут в организме 5-10 суток, а затем их уничтожают и переваривают иммунные клетки.
Так есть ли смысл бояться?
Стоит признать: в медицине действительно были случаи, когда у прививок находили неожиданные неприятные последствия — и даже через много месяцев. Но среди всех получивших прививку это, без преувеличения, капля в море. И даже в отношении этих случаев расследование иногда тянулось годы. А в ситуации пандемии приходится взвешивать риски здесь и сейчас — какой вариант сохранит больше жизней. Ведь в число жертв попадают не только зараженные коронавирусом, но и другие больные, которые не получили помощь из-за перегрузки больниц.
Но среди всех получивших прививку это, без преувеличения, капля в море. И даже в отношении этих случаев расследование иногда тянулось годы. А в ситуации пандемии приходится взвешивать риски здесь и сейчас — какой вариант сохранит больше жизней. Ведь в число жертв попадают не только зараженные коронавирусом, но и другие больные, которые не получили помощь из-за перегрузки больниц.
На эту тему
Самый честный ответ на вопрос, ждут ли нас роковые сюрпризы из-за вакцинации через год или даже два, звучит так: «Мы не знаем на 100%, но мы уже знаем достаточно много, чтобы действовать без оглядки на эту вероятность». Именно так мы действуем каждый день. Мы сталкиваемся с огромным количеством рисков — погибнуть, заболеть, получить травму или заразиться инфекцией. Наши маленькие, незаметные решения могут привести к серьезным последствиям. Но мы выбираем жить, несмотря на риски.
Мы не можем сидеть дома, хотя в этом случае риск погибнуть из-за падения самолета падает в 100 раз. Мы не отказываемся от электротехники, чтобы снизить до минимума риск погибнуть от удара током. Мы соглашаемся на плановые операции, чтобы поправить свое здоровье, хотя есть случаи, когда люди гибнут из-за действия наркоза. И да, мы загораем летом, хотя ни один солнцезащитный крем не дает 100% защиты от ультрафиолета.
Мы не отказываемся от электротехники, чтобы снизить до минимума риск погибнуть от удара током. Мы соглашаемся на плановые операции, чтобы поправить свое здоровье, хотя есть случаи, когда люди гибнут из-за действия наркоза. И да, мы загораем летом, хотя ни один солнцезащитный крем не дает 100% защиты от ультрафиолета.
Не существует жизненных решений, которые не несут в себе рисков. Во многих случаях нам приходится выбирать, и не всегда мы делаем выбор рационально. Например, многие боятся летать на самолете, потому что ассоциируют огромную высоту с риском упасть, и поэтому выбирают машину. Но статистически риск погибнуть в авиакатастрофе во много раз меньше, чем попасть в смертельную аварию на дороге. В случае с вакцинацией разница еще больше.
Мы можем быть уверены в одном: каждый день приносит новые знания. Каждый день добавляет еще один кусочек в пазл под названием «вакцины». Мы уже можем угадать — хотя бы в общих чертах — какой будет картина целиком. И теперь, после миллионов случаев, обработанных и занесенных в статистику, эта картина уже вряд ли поменяется радикально.
Антон Солдатов
Вакцина против туберкулеза связана с более низким риском заражения COVID-19
Согласно новому исследованию Cedars-Sinai, широко используемая противотуберкулезная вакцина снижает вероятность заражения COVID-19 (коронавирусом). Полученные данные повышают вероятность того, что вакцина, уже одобренная Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США, может помочь предотвратить коронавирусные инфекции или снизить тяжесть заболевания.
Вакцина, известная как Бацилла Кальметта-Герена (БЦЖ), была разработана в период с 1908 по 1921 год и ежегодно вводится более чем 100 миллионам детей во всем мире.В США он одобрен FDA как препарат для лечения рака мочевого пузыря и как вакцина для людей с высоким риском заражения туберкулезом. Вакцина БЦЖ в настоящее время проходит многочисленные клинические испытания по всему миру на предмет эффективности против COVID-19.
В новом исследовании, опубликованном 19 ноября в The Journal of Clinical Investigation , исследователи проверили кровь более 6000 медицинских работников в системе здравоохранения Cedars-Sinai на наличие антител к SARS-CoV-2, вирус, вызывающий COVID-19, а также расспросил их об их истории болезни и прививках.
Они обнаружили, что работники, получившие вакцинацию БЦЖ в прошлом — почти 30% обследованных, — значительно реже имели положительный результат теста на антитела к SARS-CoV-2 в своей крови или сообщали об инфицировании коронавирусом или коронавирусом. сопутствующих симптомов в течение предыдущих шести месяцев, чем у тех, кто не получал БЦЖ. Эти эффекты не зависели от того, получали ли работники прививки от менингококка, пневмококка или гриппа.
Причины более низких уровней антител к SARS-CoV-2 в группе БЦЖ не были ясны, по словам Моше Ардити, доктора медицинских наук, директора отделения педиатрии, инфекционных заболеваний и иммунологии в Cedars-Sinai и со-старшего автора исследования. учиться.
учиться.
«Похоже, что люди, вакцинированные БЦЖ, либо меньше болели и, следовательно, производили меньше антител против SARS-CoV-2, либо у них мог развиться более эффективный клеточный иммунный ответ против вируса», — сказал Ардити, профессор Педиатрия и биомедицинские науки. «Мы были заинтересованы в изучении вакцины БЦЖ, потому что давно известно, что она обладает общим защитным действием против ряда бактериальных и вирусных заболеваний, помимо туберкулеза, включая сепсис новорожденных и респираторные инфекции.
В новом исследовании более низкие уровни антител в группе БЦЖ сохранялись, несмотря на то, что у этих людей была более высокая частота гипертонии, диабета, сердечно-сосудистых заболеваний и ХОБЛ, которые являются известными факторами риска для большей восприимчивости к SARS-CoV- 2 и развитие более тяжелых форм болезни COVID-19.
Отметив, что никто не верит, что БЦЖ будет более эффективной, чем конкретная вакцина против COVID-19, Ардити пояснил, что ее можно было бы быстрее утвердить и сделать доступной, учитывая, что он имеет сильный профиль безопасности, продемонстрированный многолетним использованием. «Это потенциально важный мост, который может принести некоторую пользу, пока мы не получим широко доступные наиболее эффективные и безопасные вакцины против COVID-19», — сказал он.
«Это потенциально важный мост, который может принести некоторую пользу, пока мы не получим широко доступные наиболее эффективные и безопасные вакцины против COVID-19», — сказал он.
«Учитывая наши результаты, мы считаем, что срочно необходимы крупные рандомизированные клинические испытания, чтобы подтвердить, может ли вакцинация БЦЖ оказывать защитный эффект против инфекции SARS-CoV2», — сказала Сьюзан Ченг, доктор медицинских наук, магистр здравоохранения, MMSc, доцент кафедры кардиологии и директор по исследованиям в области общественного здравоохранения в Институте сердца Смидта в Сидарс-Синай.Она была другим со-старшим автором исследования. Первым автором был Магали Новаль Ривас, доктор философии, доцент кафедры педиатрии Cedars-Sinai.
Фактически, был начат ряд рандомизированных клинических испытаний для изучения потенциальных защитных эффектов вакцинации БЦЖ против COVID-19. Наряду с Техасским университетом A&M, Медицинским колледжем Бэйлора и Онкологическим центром им. доктора медицины Андерсона Техасского университета, Cedars Sinai является площадкой для американского отделения этого продолжающегося испытания, в котором участвуют сотни медицинских работников.Ардити выступает в качестве главного исследователя этого клинического испытания в Cedars-Sinai.
доктора медицины Андерсона Техасского университета, Cedars Sinai является площадкой для американского отделения этого продолжающегося испытания, в котором участвуют сотни медицинских работников.Ардити выступает в качестве главного исследователя этого клинического испытания в Cedars-Sinai.
«Было бы замечательно, если бы одна из самых старых вакцин, которые у нас есть, могла помочь победить новейшую пандемию в мире», — сказал Ардити. Национальный институт здравоохранения под номером U54 CA26059 и Семейный фонд Эрики Дж. Глейзер .
Подробнее читайте в журнале Discoveries: On the Front Lines of COVID-19
Реактивация шрамов от прививки БЦЖ после вакцинации мРНК-Covid-вакциной: два клинических случая | BMC Infectious Diseases
После введения вакцин мРНК Covid-19 у двух медработников, которые недавно были вакцинированы БЦЖ в рамках исследования БЦЖ-ДАНИЯ-COVID, произошла реактивация в месте введения пробной вакцины БЦЖ, введенной 6–8 месяцами ранее. Реактивации шрамов от БЦЖ у детей не было. Участник, который наиболее сильно реагировал после вакцинации БЦЖ как в детстве, так и при включении в исследование БЦЖ-ДАНИЯ-COVID, испытывал симптомы на месте пробного рубца БЦЖ уже после первой вакцинации против Covid-19, тогда как участник, у которого были только умеренные симптомы после прививки БЦЖ 6 мес. ранее отмечали реактивацию только после второй инъекции.
Реактивации шрамов от БЦЖ у детей не было. Участник, который наиболее сильно реагировал после вакцинации БЦЖ как в детстве, так и при включении в исследование БЦЖ-ДАНИЯ-COVID, испытывал симптомы на месте пробного рубца БЦЖ уже после первой вакцинации против Covid-19, тогда как участник, у которого были только умеренные симптомы после прививки БЦЖ 6 мес. ранее отмечали реактивацию только после второй инъекции.
Ранее сообщалось о реактивации рубцов БЦЖ после вакцинации против гриппа [7, 8], но у участника, получившего вакцину против гриппа за 2 месяца до вакцинации против Covid-19, таких реакций не наблюдалось.
В двух недавних сообщениях описывались сходные реакции в рубцах после вакцинации БЦЖ у новорожденных у четырех медицинских работников в возрасте от 28 до 45 лет после вакцинации мРНК Covid-19 [9, 10]. Реактивация рубцов БЦЖ описана также при вирусных инфекциях у детей, например, при кори и вирусе герпеса человека 6 типа [11,12,13]. Однако реактивация рубцов БЦЖ в основном была связана с болезнью Кавасаки (БК), а местные реакции, такие как эритема и уплотнение в месте рубца БЦЖ, даже предлагались в качестве диагностического инструмента при диагностике БК [14]. В исследовании, проведенном в Сингапуре, где всем новорожденным вводят БЦЖ, сообщается, что у 43% пациентов с БК развилась реактивация в месте рубца БЦЖ, чаще всего у самых маленьких детей [13]. Исследование показало, что более высокая распространенность среди самых маленьких детей была связана с более коротким периодом времени между прививкой БЦЖ и началом БК, а не с возрастом как таковым [13]. Это может объяснить, почему мы наблюдали реактивацию только в самых последних шрамах БЦЖ.
В исследовании, проведенном в Сингапуре, где всем новорожденным вводят БЦЖ, сообщается, что у 43% пациентов с БК развилась реактивация в месте рубца БЦЖ, чаще всего у самых маленьких детей [13]. Исследование показало, что более высокая распространенность среди самых маленьких детей была связана с более коротким периодом времени между прививкой БЦЖ и началом БК, а не с возрастом как таковым [13]. Это может объяснить, почему мы наблюдали реактивацию только в самых последних шрамах БЦЖ.
Интересно, что было выявлено новое педиатрическое заболевание, связанное с Covid-19, называемое мультисистемным воспалительным синдромом у детей (MIS-C), с патогенезом и клиническими проявлениями, сходными с БК [15].Тот факт, что COVID-19 может вызывать MIS-C, что MIS-C напоминает KD, а KD связан с реактивацией БЦЖ, указывает на некоторую степень общей этиологии. Патофизиология MIS-C до сих пор неизвестна [15]. MIS-C в основном был диагностирован в странах с высоким уровнем дохода, где БЦЖ не используется широко, и, насколько нам известно, у детей, страдающих MIS-C, не было зарегистрировано реактивации рубцов БЦЖ. Однако это, вероятно, связано с редкостью MIS-C и низкой эпидемиологической вероятностью того, что это произойдет у ребенка, вакцинированного БЦЖ.С другой стороны, на основании имеющихся данных можно ожидать реактивации рубца БЦЖ у детей с MIS-C в странах, где БЦЖ используется рутинно.
Однако это, вероятно, связано с редкостью MIS-C и низкой эпидемиологической вероятностью того, что это произойдет у ребенка, вакцинированного БЦЖ.С другой стороны, на основании имеющихся данных можно ожидать реактивации рубца БЦЖ у детей с MIS-C в странах, где БЦЖ используется рутинно.
Было показано, что живые организмы БЦЖ остаются у мышей, вакцинированных БЦЖ, до 5 месяцев [16] и были выделены из детей, рожденных от ВИЧ-позитивных матерей, через 9 лет после введения БЦЖ при рождении [17]. Однако маловероятно, что изменения, наблюдаемые в двух случаях, связаны с живыми бактериями БЦЖ. Таким образом, более вероятно, что местная реакция была вызвана перекрестной реактивностью между микробными компонентами БЦЖ, сохраняющимися в месте вакцинации, и вакцинами против SARS-CoV-2.Анализ in silico показал, что вакцина БЦЖ может генерировать перекрестно-реактивные Т-клетки против SARS-CoV-2 [18]. В подтверждение этого вывода недавно были идентифицированы восемь пептидов, полученных из БЦЖ, со значительной гомологией последовательностей с пептидами, полученными либо из неструктурного белка 3 (NSP3), либо из неструктурного белка 13 (NSP13) SARS-CoV-2 [19]. Интересно, что человеческие CD4+ и CD8+ T-клетки, примированные пептидом, полученным из БЦЖ, проявляли повышенную реактивность по отношению к соответствующему пептиду, полученному из SARS-CoV-2, что подтверждает гипотезу о том, что вакцинация БЦЖ индуцирует перекрестно-реактивные Т-клеточные ответы, специфичные для SARS-CoV-2 [19]. ].Кроме того, высокая гомология белка оболочки SARS-CoV-2 с консенсусным белком LytR C, уникальным для Mycobacteria , указывает на то, что вакцинация БЦЖ индуцирует специфический иммунитет против SARS CoV-2, который нацелен на белок оболочки вируса, необходимый для инфекционности. 20]. Таким образом, реактивация рубца БЦЖ у двух медработников после введения мРНК-вакцины могла быть вызвана иммунологической реакцией из-за перекрестной реактивности между БЦЖ и SARS-CoV-2.
Интересно, что человеческие CD4+ и CD8+ T-клетки, примированные пептидом, полученным из БЦЖ, проявляли повышенную реактивность по отношению к соответствующему пептиду, полученному из SARS-CoV-2, что подтверждает гипотезу о том, что вакцинация БЦЖ индуцирует перекрестно-реактивные Т-клеточные ответы, специфичные для SARS-CoV-2 [19]. ].Кроме того, высокая гомология белка оболочки SARS-CoV-2 с консенсусным белком LytR C, уникальным для Mycobacteria , указывает на то, что вакцинация БЦЖ индуцирует специфический иммунитет против SARS CoV-2, который нацелен на белок оболочки вируса, необходимый для инфекционности. 20]. Таким образом, реактивация рубца БЦЖ у двух медработников после введения мРНК-вакцины могла быть вызвана иммунологической реакцией из-за перекрестной реактивности между БЦЖ и SARS-CoV-2.
В исследовании BCG-DENMARK-COVID 614 медработников были рандомизированы для получения БЦЖ.Два участника сообщили о реактивации рубца БЦЖ после вакцинации против Covid-19. В обоих случаях симптомы были раздражающими, но самоограничивающимися и не оставляли последствий. Оба участника были рады внести свой вклад в испытание и были бы рады участвовать в подобных испытаниях в будущем. В нашем случае один участник почувствовал, что ее общее состояние здоровья улучшилось по сравнению с состоянием до испытания, тогда как участник из второго случая почувствовал, что ее общее состояние не изменилось.
Оба участника были рады внести свой вклад в испытание и были бы рады участвовать в подобных испытаниях в будущем. В нашем случае один участник почувствовал, что ее общее состояние здоровья улучшилось по сравнению с состоянием до испытания, тогда как участник из второго случая почувствовал, что ее общее состояние не изменилось.
Ограничение зарегистрированных случаев заключается в том, что не проводилось никаких тестов для выяснения патогенеза, вызывающего симптомы.Тем не менее, два участника испытали симптомы до такой степени, что они спонтанно сообщили о них, поэтому для клиницистов важно знать о возможности наблюдения подобных реакций, а также представляется целесообразным предупредить врачей о том факте, что реактивация рубца БЦЖ может быть индикатор МИС-Ц. Тем не менее, нет причин избегать вакцинации любой из мРНК-вакцин Covid-19.
Вакцинация БЦЖ. Побочные эффекты противотуберкулезной вакцины и информация.
Живой аттенуированный штамм Mycobacterium bovis , известный как бацилла Кальметта-Герена (БЦЖ), использует общие антигены для стимуляции развития перекрестного иммунитета к Mycobacterium tuberculosis и Mycobacterium leprae .
Вакцина БЦЖ также используется в качестве внутрипузырного иммуномодулятора при лечении рака мочевого пузыря (см. отдельную статью о раке мочевого пузыря).
Программа иммунизации БЦЖ была введена в Великобритании в 1953 году. Первоначально программа была нацелена на детей школьного возраста (тогда 14 лет), поскольку пик заболеваемости туберкулезом (ТБ) приходился на молодых людей трудоспособного возраста.
В 2005 г. в связи с продолжающимся снижением заболеваемости туберкулезом среди коренного населения Великобритании школьная программа была остановлена.Программа иммунизации БЦЖ в настоящее время является программой, основанной на оценке рисков, ключевой частью которой является неонатальная программа, направленная на защиту детей, подвергающихся наибольшему риску заражения туберкулезом, особенно от более серьезных детских форм заболевания.
Вакцина БЦЖ содержит живой аттенуированный штамм, полученный из M. bovis . Исследования эффективности вакцины БЦЖ варьируются от отсутствия защиты до 70-80% защиты. Однако вакцина на 70-80% эффективна против наиболее тяжелых форм заболевания, таких как туберкулезный менингит у детей.Он менее эффективен для профилактики респираторных заболеваний, которые чаще встречаются у взрослых. [1]
Однако вакцина на 70-80% эффективна против наиболее тяжелых форм заболевания, таких как туберкулезный менингит у детей.Он менее эффективен для профилактики респираторных заболеваний, которые чаще встречаются у взрослых. [1]
Срок действия защиты от 10 до 15 лет. Данные о продолжительности защиты по истечении этого времени ограничены, но со временем защита может ослабевать. Хотя защита, обеспечиваемая вакциной БЦЖ, может со временем ослабевать, нет никаких доказательств того, что повторная вакцинация обеспечивает значительную дополнительную защиту, и повторная вакцинация БЦЖ не рекомендуется. [1]
Имеется мало данных о защите, обеспечиваемой вакциной БЦЖ при введении ее взрослым (в возрасте 16 лет и старше), и нет данных о лицах в возрасте 35 лет и старше.БЦЖ обычно не рекомендуется людям старше 16 лет, за исключением случаев, когда риск заражения велик (например, работники здравоохранения или лабораторий, подвергающиеся профессиональному риску). [1]
[1]
Введение
[1]Вакцину БЦЖ следует вводить внутрикожно, обычно в латеральную часть левого плеча на уровне прикрепления дельтовидной мышцы. Левая рука рекомендована Всемирной организацией здравоохранения (ВОЗ).
Не следует проводить дальнейшую иммунизацию в той группе, которая используется для иммунизации БЦЖ, в течение по крайней мере трех месяцев из-за риска регионарного лимфаденита.В идеале БЦЖ следует вводить одновременно с другими живыми вакцинами, например, против кори, эпидемического паротита и краснухи (MMR). Если живые вакцины нельзя вводить одновременно, рекомендуется четырехнедельный интервал.
Однократно следует вводить:
- 0,05 мл для детей младше 12 месяцев.
- 0,1 мл для детей в возрасте 12 месяцев и старше и взрослых.
Показания
[1]Иммунизация БЦЖ должна быть предложена:
- Всем младенцам (в возрасте от 0 до 12 месяцев), проживающим в районах Великобритании, где ежегодная заболеваемость ТБ составляет 40/100 000 или выше.

- Все младенцы (в возрасте от 0 до 12 месяцев) с одним из родителей или бабушек и дедушек, которые родились в стране, где ежегодная заболеваемость ТБ составляет 40/100 000 или выше.
- Ранее не привитые дети в возрасте от 1 до 5 лет, родители или дедушки и бабушки, родившиеся в стране, где ежегодная заболеваемость ТБ составляет 40/100 000 или выше.
- Ранее не вакцинированные, туберкулин-отрицательные дети в возрасте от 6 до 16 лет, чьи родители или дедушки и бабушки родились в стране, где ежегодная заболеваемость ТБ составляет 40/100 000 или выше.
- Ранее невакцинированные туберкулинотрицательные лица в возрасте до 16 лет, контактировавшие с больными туберкулезом органов дыхания.
- Ранее не вакцинированные, туберкулин-отрицательные лица в возрасте до 16 лет, родившиеся или проживающие в течение длительного периода (не менее трех месяцев) в стране с годовой заболеваемостью туберкулезом 40/100 000 или выше.
Пробу Манту не следует проводить рутинно перед вакцинацией БЦЖ у детей в возрасте до 6 лет, за исключением случаев проживания или длительного пребывания (более одного месяца) в стране с высокой заболеваемостью туберкулезом. [2]
[2]
Лица, подвергающиеся профессиональному риску
Люди из следующих профессиональных групп чаще, чем население в целом, вступают в контакт с больными туберкулезом:
- Медицинские работники, которые будут контактировать с пациентами или клиническими материалами.
- Лабораторный персонал, который будет контактировать с пациентами, клиническими материалами или производными изолятами.
- Ветеринары и персонал, например работники скотобоен, работающие с видами животных, о которых известно, что они восприимчивы к туберкулезу.
- Тюремный персонал, работающий непосредственно с заключенными.
- Персонал домов престарелых.
- Персонал общежитий для бездомных и учреждений для размещения беженцев и лиц, ищущих убежища.
Невакцинированным туберкулинотрицательным лицам в возрасте до 35 лет, работающим в этих профессиях, рекомендуется введение БЦЖ. Нет данных о защите, обеспечиваемой вакциной БЦЖ при введении ее взрослым в возрасте 35 лет и старше.
Не все работники здравоохранения подвержены одинаковому риску заболеть туберкулезом.Вероятно, существуют категории медицинских работников, подвергающихся особому риску заболевания туберкулезом, и они должны быть частью клинической оценки риска, когда рассматривается возможность использования БЦЖ медицинским работником старше 35 лет.
Путешественники и те, кто собирается жить за границей
БЦЖ может потребоваться ранее не вакцинированным, туберкулин-отрицательным лицам в зависимости от пункта назначения и характера поездки. Вакцина рекомендуется для лиц моложе 16 лет, которые собираются жить или работать с местными жителями более трех месяцев в стране, где ежегодная заболеваемость туберкулезом составляет 40/100 000 или выше.
Противопоказания
[1]Вакцину нельзя вводить:
- Тем, кто уже был вакцинирован БЦЖ.
- Те, у кого в прошлом был туберкулез.
- Имеющие уплотнение 6 мм и более после кожной пробы с туберкулином Манту.

- Те, у кого была подтвержденная анафилактическая реакция на компонент вакцины.
- Новорожденные в домохозяйстве, где подозревается или подтвержден активный случай туберкулеза.
- Люди с ослабленным иммунитетом в результате болезни или лечения, например:
- Пациенты, получающие кортикостероиды или другие иммунодепрессанты, включая общее облучение.Ингаляционные стероиды не являются противопоказанием.
- Те, кто страдает злокачественными заболеваниями, такими как лимфома, лейкемия, болезнь Ходжкина или другие опухоли ретикуло-эндотелиальной системы.
БЦЖ противопоказана ВИЧ-инфицированным с симптомами. В таких странах, как Великобритания, где риск заболевания туберкулезом низок, рекомендуется также воздерживаться от введения вакцины БЦЖ всем тем, у кого известно о наличии или подозрении на ВИЧ, независимо от клинического статуса.
Меры предосторожности
[1]- Легкие заболевания без лихорадки или системных нарушений не являются уважительной причиной для отсрочки иммунизации.

- Если человек остро болен, иммунизацию следует отложить до полного выздоровления. Это делается для того, чтобы избежать путаницы при дифференциальной диагностике любого острого заболевания, ошибочно приписывая любые признаки или симптомы побочным эффектам вакцины.
- Лица с генерализованным септическим кожным заболеванием не должны быть вакцинированы. При наличии экземы следует выбрать место для иммунизации, свободное от кожных поражений.
Не было выявлено вредного воздействия БЦЖ на плод во время беременности; однако целесообразно избегать вакцинации, особенно в первом триместре, и по возможности откладывать вакцинацию до родов.Грудное вскармливание не является противопоказанием для БЦЖ.
Реакция на иммунизацию и уход за местом иммунизации
[1] Обычной реакцией на успешную вакцинацию БЦЖ является уплотнение в месте инъекции с последующим местным поражением, которое начинается в виде папулы через две или более недель после вакцинации. Он может изъязвляться, а затем медленно исчезать в течение нескольких недель или месяцев до заживления, оставляя небольшой плоский шрам. Это может также включать увеличение регионарного лимфатического узла менее чем на 1 см.
Он может изъязвляться, а затем медленно исчезать в течение нескольких недель или месяцев до заживления, оставляя небольшой плоский шрам. Это может также включать увеличение регионарного лимфатического узла менее чем на 1 см.
Нет необходимости защищать место от намокания во время мытья и купания. Временная сухая повязка может использоваться до тех пор, пока не образуется струп, если происходит просачивание.
Тяжелые реакции в месте инъекции, большие местные язвы, абсцессы и келоидные рубцы чаще всего вызываются неправильной техникой инъекции, чрезмерной дозировкой или вакцинацией туберкулин-положительных лиц.
Другие побочные реакции на вакцину включают головную боль, лихорадку и увеличение регионарного лимфатического узла более чем на 1 см, который может изъязвляться.Аллергические реакции (включая анафилактические реакции), более тяжелые местные реакции, такие как образование абсцесса, и диссеминированные осложнения БЦЖ (такие как остит или остеомиелит) встречаются редко.
Все серьезные или необычные побочные реакции, которые могут быть связаны с вакцинацией БЦЖ (включая абсцессы и келоидные рубцы), должны регистрироваться и сообщаться в Комиссию по лекарственным средствам для человека через систему желтой карточки, а протоколы и методы вакцинации должны быть пересмотрены. Необходимо приложить все усилия для восстановления и идентификации возбудителя из любого поражения, представляющего собой серьезное осложнение.
Лечение побочных реакций
[1]Лица с тяжелыми местными реакциями (изъязвление более 1 см, казеозные поражения, абсцессы или выделения в месте инъекции) или с регионарным гнойным лимфаденитом с дренированием синусов после вакцинации БЦЖ должны быть направлены к пульмонологу или педиатру для обследования и лечения.
Приросший, нагнаивающийся или свищевой лимфатический узел может потребовать разреза и дренирования.
При диссеминированной БЦЖ-инфекции следует обратиться к пульмонологу или педиатру для консультации специалиста, и обычно требуется системное противотуберкулезное лечение в соответствии с текущими рекомендациями по лечению M. Бовис инфекции. Тестирование in vitro показало, что и изониазид, и рифампицин эффективны. Однако неясно, эффективны ли пероральные антибиотики (изониазид, эритромицин или комбинация изониазида и рифампицина) для разрешения БЦЖ-индуцированного заболевания. [3]
Бовис инфекции. Тестирование in vitro показало, что и изониазид, и рифампицин эффективны. Однако неясно, эффективны ли пероральные антибиотики (изониазид, эритромицин или комбинация изониазида и рифампицина) для разрешения БЦЖ-индуцированного заболевания. [3]
Будущие разработки
БЦЖ неэффективна для защиты от туберкулеза легких у взрослых в тех частях мира, где больше всего нужна хорошая вакцина. [4] Многие новые вакцины находятся в разработке. [5] Новые кандидаты включают живую аттенуированную M.tuberculosis , рекомбинантную БЦЖ, ДНК-вакцины и гибридные белки с новыми адъювантами, и все они направлены на обеспечение более сильного и продолжительного иммунного ответа в гетерогенных популяциях.
Может ли вакцина БЦЖ защитить от COVID-19?
Почти 100-летняя вакцина Bacillus Calmette-Guérin (BCG) защищает от некоторых из самых смертельных форм туберкулеза (ТБ), бактериальной инфекции, которая была причиной 1. Только в 2018 году во всем мире погибло 5 миллионов человек.
Только в 2018 году во всем мире погибло 5 миллионов человек.
Вакцина БЦЖ была впервые введена людям в начале 1920-х годов, но ее использование не получило широкого распространения в течение десятилетий после продолжающихся исследований ее безопасности и эффективности в 1940-х и 1950-х годах.
Обзор данных, проведенный в начале 1990-х годов, пришел к выводу, что вакцина БЦЖ ненадежна в защите от туберкулеза легких, наиболее распространенной и заразной формы заболевания. Это привело к тому, что несколько стран прекратили его включение в плановую иммунизацию.
Несмотря на это, вакцина по-прежнему спасает жизни. Исследования показывают, что он на 70–80% эффективен для защиты от наиболее тяжелых форм туберкулеза, таких как туберкулезный менингит у детей. Сегодня одну дозу вакцины вводят новорожденным, проживающим в странах с высоким уровнем заболеваемости туберкулезом, таких как Индия и Эфиопия, или тем, кто может подвергаться воздействию возбудителя, включая медицинских работников.
Так почему же вакцина БЦЖ вызывает такой ажиотаж на фоне пандемии COVID-19?
Иммуностимулирующие свойства
За время своего долгого существования появилось множество данных, свидетельствующих о том, что вакцина БЦЖ может также оказывать положительное нецелевое действие, обеспечивая некоторую защиту не только от некоторых форм туберкулеза, но и от других заболеваний.Это потому, что он помогает укрепить иммунную систему. Учитывая, что организации здравоохранения во всем мире срочно ищут способы лечения и предотвращения распространения COVID-19, пока не будет разработана вакцина, некоторое внимание сейчас обращено на вакцину БЦЖ.
Теоретически это был бы очень привлекательный вариант, так как его безопасность давно доказана. Это означает, что если будет показано, что он оказывает какое-либо профилактическое действие на COVID-19, его потенциально можно будет давать большому количеству людей, которые еще не заразились этой болезнью, чтобы уменьшить ее распространение и количество людей, которые переходят на коронавирус. развиваются тяжелые симптомы.Тем не менее, по-прежнему недостаточно доказательств, чтобы делать какие-либо выводы.
развиваются тяжелые симптомы.Тем не менее, по-прежнему недостаточно доказательств, чтобы делать какие-либо выводы.
Что мы знаем, так это то, что реакция вакцины БЦЖ на иммунную систему человека позволяет предположить, что она может оказывать общее иммуностимулирующее действие. Когда ученые сравнили иммунную систему людей, получивших вакцину БЦЖ, с теми, у кого ее не было, они обнаружили, что иммунные клетки, которые первыми реагируют на заболевание у людей, вакцинированных БЦЖ, более бдительны и готовы действовать в ответ на потенциальную угрозу.
Активная иммунная система означает, что организм лучше подготовлен к борьбе с болезнями.Эта идея была подтверждена исследованиями, проведенными на младенцах, рожденных в Гвинее-Бисау. Они предположили, что вакцина может помочь снизить детскую смертность сверх того, что можно было бы ожидать, предотвратив только туберкулез.
Отчеты о контролируемых медицинских испытаниях также предполагают, что это может снизить вероятность заражения людей другими респираторными инфекциями, некоторые из которых вызваны вирусами, форма которых очень похожа на COVID-19. Даже если это не может остановить людей, заражающихся этой болезнью, некоторые данные свидетельствуют о том, что есть шанс, что это может оказаться полезным для снижения тяжести симптомов, ответственных за число погибших от пандемии.
Даже если это не может остановить людей, заражающихся этой болезнью, некоторые данные свидетельствуют о том, что есть шанс, что это может оказаться полезным для снижения тяжести симптомов, ответственных за число погибших от пандемии.
Какие исследования проводятся?
Ряд исследовательских групп внимательно изучают вопрос о том, может ли получение дозы вакцины БЦЖ предотвратить или помочь людям бороться с инфекцией COVID-19 и снизить число смертей, связанных с COVID-19.
Исследование, изучающее глобальную связь между БЦЖ и COVID-19, показало, что существует значительная обратная корреляция между «индексом БЦЖ» или тем, насколько хорошо вакцина БЦЖ была развернута в стране, и смертностью от COVID-19.Исследователи смотрели только на смертность, потому что, хотя во многих странах есть много противоречивых данных о случаях и смертях, подсчет смертей, скорее всего, будет точным. Они обнаружили, что каждые 10% увеличения индекса БЦЖ были связаны со снижением смертности от COVID-19 на 10,4%. Они наблюдали более высокий уровень смертности во Франции и Великобритании, чем в Германии или Скандинавии, и предположили, что там, где вакцинация БЦЖ была сделана детям старшего возраста (как в Великобритании), она могла пропустить «критическое окно» в раннем возрасте, когда вакцинация БЦЖ могла иметь значение. привели к пожизненному усилению иммунитета.
Они наблюдали более высокий уровень смертности во Франции и Великобритании, чем в Германии или Скандинавии, и предположили, что там, где вакцинация БЦЖ была сделана детям старшего возраста (как в Великобритании), она могла пропустить «критическое окно» в раннем возрасте, когда вакцинация БЦЖ могла иметь значение. привели к пожизненному усилению иммунитета.
Группа нигерийских исследователей провела аналогичное сравнение на уровне нескольких стран политики вакцинации БЦЖ, случаев и смертей от COVID-19. Они обнаружили поразительную связь между странами с очень высокой смертностью и отсутствием политики вакцинации БЦЖ, в первую очередь Италией и США.
Обе группы исследователей признают основные переменные, участвующие в реагировании на пандемию, которые могут повлиять на количество смертей, такие как качество системы здравоохранения по странам, системы эпиднадзора и возможности тестирования.
Это означает, что мы узнаем наверняка, работает ли вакцина БЦЖ против COVID-19, только после тщательного изучения результатов ряда клинических испытаний. Из-за срочности ученые из четырех разных стран уже собрали и начали ряд исследований, чтобы выяснить, может ли вакцина помочь защитить тех, кто находится на переднем крае пандемии.
Из-за срочности ученые из четырех разных стран уже собрали и начали ряд исследований, чтобы выяснить, может ли вакцина помочь защитить тех, кто находится на переднем крае пандемии.
Команда из Нидерландов добилась успехов в наборе 1000 медицинских работников в восемь голландских больниц, чтобы выяснить, повлияет ли это на количество взятых отпусков по болезни.Медсестры, врачи и другой ключевой персонал больницы получат либо вакцину, либо фиктивный препарат (плацебо). Сравнение количества дней болезни между группами — хороший способ оценить, может ли вакцина БЦЖ снизить тяжесть побочных эффектов COVID-19 и обеспечить некоторую защиту от болезни.
Исследователи в Австралии также начали очень похожее испытание и надеются изучить более 10 000 медицинских работников, отслеживая их прогресс с помощью опросов по электронной почте и текстовых сообщений.
Еще одним интересным кандидатом является новый экспериментальный тип вакцины БЦЖ под названием VPM1002.Исследование в Германии проверяет, может ли он защитить медицинских работников и пожилых пациентов от COVID-19, после исследований на мышах, которые показали, что он может защитить от других вирусных инфекций легких. У мышей, зараженных гриппом, также было обнаружено более низкое содержание вирусов гриппа в крови, если им заранее была сделана вакцина БЦЖ, намекая на то, что вакцина может помочь иммунной системе уничтожить вирус.
У мышей, зараженных гриппом, также было обнаружено более низкое содержание вирусов гриппа в крови, если им заранее была сделана вакцина БЦЖ, намекая на то, что вакцина может помочь иммунной системе уничтожить вирус.
Почему мы не можем начать вакцинацию БЦЖ от COVID-19 сейчас?
Дело в том, что мы еще не знаем, переносятся ли задокументированные положительные побочные эффекты вакцины БЦЖ на COVID-19.С точки зрения лечения туберкулеза действующая вакцина действительно оказывает благотворное влияние только на детей, поэтому возникает большой вопрос, окажет ли она какое-либо положительное влияние на взрослых, подверженных риску заражения COVID-19. Есть также вопросы, какая форма вакцины будет наиболее подходящей.
На данный момент, хотя мы не знаем, действительно ли вакцина имеет какие-либо положительные эффекты, ресурсы следует зарезервировать для тех, кто может получить наибольшую пользу. Несмотря на то, что вакцина БЦЖ не так эффективна против туберкулеза, как хотелось бы, она по-прежнему остается наилучшей формой профилактики. И запасы не безграничны.
И запасы не безграничны.
В прошлом производство вакцины было проблематичным, и временами возникала глобальная нехватка, а это означало, что многие дети подвергались риску заражения туберкулезом, которые в противном случае могли бы быть защищены.
В конечном счете, необходимы дополнительные исследования, прежде чем мы расширим масштабы вакцинации БЦЖ для защиты людей от COVID-19.
Натренированный иммунитет, индуцированный вакциной БЦЖ, и COVID-19: Protective or Bysta
Введение
Коронавирусы (CoV) известны с 1930-х годов и вызывают широкий спектр заболеваний как у животных, так и у людей.С 1960-х годов было идентифицировано семь человеческих альфа- и бета-КоВ. Однако в конце 2002 года опасные для жизни патогенные штаммы начали передаваться от животных человеку, вызывая тяжелые респираторные заболевания. 1–4 Эти штаммы представляют собой бета-CoV, такие как коронавирус тяжелого острого респираторного синдрома (SARS-CoV), появившийся в 2002/2003 гг. в Китае, и десять лет спустя коронавирус ближневосточного респираторного синдрома (MERS-CoV), появившийся в регион Ближнего Востока. 1–3,5–7 В конце 2019 г. в Ухане/Китай появился новый штамм коронавируса, который в феврале 2020 г. был назван коронавирусом тяжелого острого респираторного синдрома-2 (SARS-CoV-2) из-за филогенетического сходства ( 79.5%) с SARS-CoV. 8 Этот вирус быстро распространился между другими странами и внутри них, вызвав коронавирусную болезнь-2019 (COVID-19) и создав чрезвычайную ситуацию в области общественного здравоохранения. В марте 2020 года Всемирная организация здравоохранения (ВОЗ) объявила вспышку COVID-19 глобальной пандемией. 9 По состоянию на 14 февраля 2021 года ВОЗ заявляет, что эта глобальная вспышка COVID-19 привела к примерно 108 246 992 подтвержденным случаям заболевания и более 2 386 717 смертям во всем мире. 10 Чтобы быстро сдержать эту вспышку, последовательность генома SARS-CoV-2 была раскрыта в течение нескольких недель после появления вируса.
в Китае, и десять лет спустя коронавирус ближневосточного респираторного синдрома (MERS-CoV), появившийся в регион Ближнего Востока. 1–3,5–7 В конце 2019 г. в Ухане/Китай появился новый штамм коронавируса, который в феврале 2020 г. был назван коронавирусом тяжелого острого респираторного синдрома-2 (SARS-CoV-2) из-за филогенетического сходства ( 79.5%) с SARS-CoV. 8 Этот вирус быстро распространился между другими странами и внутри них, вызвав коронавирусную болезнь-2019 (COVID-19) и создав чрезвычайную ситуацию в области общественного здравоохранения. В марте 2020 года Всемирная организация здравоохранения (ВОЗ) объявила вспышку COVID-19 глобальной пандемией. 9 По состоянию на 14 февраля 2021 года ВОЗ заявляет, что эта глобальная вспышка COVID-19 привела к примерно 108 246 992 подтвержденным случаям заболевания и более 2 386 717 смертям во всем мире. 10 Чтобы быстро сдержать эту вспышку, последовательность генома SARS-CoV-2 была раскрыта в течение нескольких недель после появления вируса. Параллельно с несколькими перепозиционированными противовирусными препаратами (такими как ремдесивир) 11–28 несколько многообещающих вакцин-кандидатов (такие как Ad5-nCoV, 29 мРНК-1273, 30 PiCoVacc и INO-4800 31 ) проходят клинические испытания. изучал. В настоящее время доступны вакцины против COVID-19, такие как вакцина Pfizer-BioNTech COVID-19, вакцина Moderna COVID-19, вакцина Janssen (Johnson & Johnson) COVID-19 и вакцина AstraZeneca/Oxford COVID-19. 32
Параллельно с несколькими перепозиционированными противовирусными препаратами (такими как ремдесивир) 11–28 несколько многообещающих вакцин-кандидатов (такие как Ad5-nCoV, 29 мРНК-1273, 30 PiCoVacc и INO-4800 31 ) проходят клинические испытания. изучал. В настоящее время доступны вакцины против COVID-19, такие как вакцина Pfizer-BioNTech COVID-19, вакцина Moderna COVID-19, вакцина Janssen (Johnson & Johnson) COVID-19 и вакцина AstraZeneca/Oxford COVID-19. 32
Учитывая настоятельную необходимость усиления иммунного ответа населения и борьбы с быстро распространяющейся пандемией COVID-19, 33,34 индукция тренированного иммунитета может быть потенциальным защитным подходом против инфекций до разработки эффективной терапии. 35 Тренированный иммунитет означает длительную гиперактивацию врожденной иммунной системы (моноцитов, макрофагов и естественных киллеров (NK-клеток)) по отношению к неродственным инфекциям. Вакцина Bacillus Calmette-Guérin (BCG), которая десятилетиями использовалась против туберкулеза (ТБ), является одним из наиболее ярких примеров индукции тренированного иммунитета. БЦЖ демонстрирует снижение восприимчивости к неродственным инфекционным агентам, особенно инфекциям дыхательных путей, таким как вирус гриппа А, респираторно-синцитиальный вирус (РСВ) и вирус простого герпеса типа 2 (ВПГ2). 36–41 Интересно, что страны с обязательной вакцинацией БЦЖ коррелируют с низким числом подтвержденных случаев COVID-19, а также снижением смертности. 42–46 Эта обратная корреляция может быть связана с длительным усилением механизмов врожденного иммунитета (вызванный БЦЖ тренированным иммунитетом). Однако на сравнение стран, где вакцина БЦЖ используется, со странами, где она не используется, могут влиять различные факторы, включая демографические характеристики, социально-экономический статус, частоту тестирования на COVID-19, стадию пандемии в каждой стране, клиническую помощь, профилактику инфекции.
Вакцина Bacillus Calmette-Guérin (BCG), которая десятилетиями использовалась против туберкулеза (ТБ), является одним из наиболее ярких примеров индукции тренированного иммунитета. БЦЖ демонстрирует снижение восприимчивости к неродственным инфекционным агентам, особенно инфекциям дыхательных путей, таким как вирус гриппа А, респираторно-синцитиальный вирус (РСВ) и вирус простого герпеса типа 2 (ВПГ2). 36–41 Интересно, что страны с обязательной вакцинацией БЦЖ коррелируют с низким числом подтвержденных случаев COVID-19, а также снижением смертности. 42–46 Эта обратная корреляция может быть связана с длительным усилением механизмов врожденного иммунитета (вызванный БЦЖ тренированным иммунитетом). Однако на сравнение стран, где вакцина БЦЖ используется, со странами, где она не используется, могут влиять различные факторы, включая демографические характеристики, социально-экономический статус, частоту тестирования на COVID-19, стадию пандемии в каждой стране, клиническую помощь, профилактику инфекции. и политики контроля.Кроме того, климатические и городские различия между странами влияют на подтвержденные случаи COVID-19. 47,48 Более того, поскольку пандемия COVID-19 все еще находится в разгаре, а количество случаев заболевания все еще растет даже в странах с вакцинами БЦЖ, считается, что слишком рано делать незрелые выводы, основанные только на экологических исследованиях. Поэтому, чтобы сделать выводы относительно вакцины БЦЖ и COVID-19, необходимы клинические исследования в поддержку экологических исследований. В ВОЗ заявили, что нет доказательств того, что вакцина БЦЖ может защитить от COVID-19, и все еще ждут результатов клинических испытаний. 49 В обзоре использован сборник опубликованных статей о CoV и вакцинации БЦЖ. В этом обзоре основное внимание уделяется перекрестной защите, индуцированной БЦЖ, и приобретению тренированного иммунитета, а также корреляции между тренированным иммунитетом, индуцированным вакциной БЦЖ, на COVID-19.
и политики контроля.Кроме того, климатические и городские различия между странами влияют на подтвержденные случаи COVID-19. 47,48 Более того, поскольку пандемия COVID-19 все еще находится в разгаре, а количество случаев заболевания все еще растет даже в странах с вакцинами БЦЖ, считается, что слишком рано делать незрелые выводы, основанные только на экологических исследованиях. Поэтому, чтобы сделать выводы относительно вакцины БЦЖ и COVID-19, необходимы клинические исследования в поддержку экологических исследований. В ВОЗ заявили, что нет доказательств того, что вакцина БЦЖ может защитить от COVID-19, и все еще ждут результатов клинических испытаний. 49 В обзоре использован сборник опубликованных статей о CoV и вакцинации БЦЖ. В этом обзоре основное внимание уделяется перекрестной защите, индуцированной БЦЖ, и приобретению тренированного иммунитета, а также корреляции между тренированным иммунитетом, индуцированным вакциной БЦЖ, на COVID-19.
Коронавирусы, симптомы и прогноз COVID-19
Коронавирусы (CoV) представляют собой группу вирусов, поражающих людей и животных. Существует четыре CoV (229E, NL63, OC43 и HKU1), которые характеризуются низкой патогенностью.Более патогенными CoV, вызывающими смертельные заболевания, являются SARS-CoV, появившийся в Китае, и MERS-CoV, возникший в ближневосточном регионе. 1–3,5–7,50,51 В настоящее время мы переживаем глобальный кризис из-за SARS-CoV-2. 50,52–54 В декабре 2019 года ВОЗ зафиксировала первые случаи заболевания COVID-19 на рынке морепродуктов в городе Ухань, провинция Хубэй, Китай. 8 В течение месяца вирус распространился из Ухани в другие районы Китая и за его пределы.
Существует четыре CoV (229E, NL63, OC43 и HKU1), которые характеризуются низкой патогенностью.Более патогенными CoV, вызывающими смертельные заболевания, являются SARS-CoV, появившийся в Китае, и MERS-CoV, возникший в ближневосточном регионе. 1–3,5–7,50,51 В настоящее время мы переживаем глобальный кризис из-за SARS-CoV-2. 50,52–54 В декабре 2019 года ВОЗ зафиксировала первые случаи заболевания COVID-19 на рынке морепродуктов в городе Ухань, провинция Хубэй, Китай. 8 В течение месяца вирус распространился из Ухани в другие районы Китая и за его пределы.
Передача от человека к человеку часто происходит при тесном контакте. 55 Первоначально передача происходит воздушно-капельным путем при чихании, кашле или даже при разговоре. Загрязненные капли оседают в различных частях тела, таких как нос, рот, легкие и глаза. 56,57 Кроме того, вирус может распространяться при прикосновении к зараженным поверхностям или предметам. 56,58 SARS-CoV-2 может инфицировать желудочно-кишечный тракт и был выделен из фекальных мазков. 26 Таким образом, вирус может распространяться фекально-оральным путем. 26,59,60 Возможна передача воздушно-капельным путем при определенных условиях.
56,58 SARS-CoV-2 может инфицировать желудочно-кишечный тракт и был выделен из фекальных мазков. 26 Таким образом, вирус может распространяться фекально-оральным путем. 26,59,60 Возможна передача воздушно-капельным путем при определенных условиях.
Симптомы COVID-19 различаются у разных людей: от бессимптомной инфекции до серьезной дыхательной недостаточности. 61 Лихорадка, кашель, утомляемость, легкая одышка, боль в горле, головная боль и конъюнктивит являются частыми симптомами заболевания. 62–64 Вовлечение желудочно-кишечного тракта с диареей, тошнотой и рвотой отмечалось в более низком проценте случаев. Ли и др. 65 предположили, что SARS-CoV-2 может обладать нейроинвазивным потенциалом, поскольку попадание вируса в центральную нервную систему у некоторых пациентов может способствовать развитию дыхательной недостаточности.Сообщаемые гипосмия и гипогевзия, испытываемые людьми с COVID-19, также могут указывать на потенциальный нейротропизм этого вируса. 66 Нейроинвазивная способность SARS-CoV-2 остается малоизученной. 67 Смертность от COVID-19 ниже, чем от SARS-CoV (10%) и MERS-CoV (35%). 58,68 Однако пока рано оценивать реальную смертность от заболевания, учитывая быстрое распространение COVID-19. Пожилой возраст, ишемическая болезнь сердца, гипертония, сахарный диабет, хронические заболевания легких, рак и пациенты, получающие иммунодепрессанты, являются основными факторами риска неблагоприятных исходов. 59
66 Нейроинвазивная способность SARS-CoV-2 остается малоизученной. 67 Смертность от COVID-19 ниже, чем от SARS-CoV (10%) и MERS-CoV (35%). 58,68 Однако пока рано оценивать реальную смертность от заболевания, учитывая быстрое распространение COVID-19. Пожилой возраст, ишемическая болезнь сердца, гипертония, сахарный диабет, хронические заболевания легких, рак и пациенты, получающие иммунодепрессанты, являются основными факторами риска неблагоприятных исходов. 59
Вакцина БЦЖ и ее влияние на вирусные инфекции
Живая аттенуированная вакцина БЦЖ против ТБ была разработана из вирулентного штамма Mycobacterium bovis ( M. bovis ) в Институте Пастера в Париже. В 1950-х годах клинические испытания вакцины БЦЖ были начаты как в Великобритании, так и в США, и, соответственно, использование вакцины БЦЖ было рекомендовано в Великобритании, но в США оно было ограничено только группами населения с высоким риском. С тех пор большинство стран придерживаются политики вакцинации БЦЖ.Распространение вакцины БЦЖ во многих лабораториях мира и повторные пересева в разных странах привели к появлению фенотипически различных вакцинных штаммов. 69 Продолжающиеся исследования направлены на определение эффекта геномного разнообразия среди вакцинных штаммов БЦЖ.
С тех пор большинство стран придерживаются политики вакцинации БЦЖ.Распространение вакцины БЦЖ во многих лабораториях мира и повторные пересева в разных странах привели к появлению фенотипически различных вакцинных штаммов. 69 Продолжающиеся исследования направлены на определение эффекта геномного разнообразия среди вакцинных штаммов БЦЖ.
Существует доступная база данных о политике и практике BCG во всем мире, BCG World Atlas. 70 Вакцина БЦЖ никогда не использовалась в национальной программе вакцинации Италии.Испания, Германия и Великобритания прекратили систематическую вакцинацию БЦЖ в 1981, 1998 и 2005 годах соответственно. 71 В настоящее время обязательные полисы BCG действуют в Аргентине, Бразилии, Болгарии, Чили, Китае, Египте, Эстонии, Иране, Ирландии, Японии, Мексике, Польше, Сингапуре, Южной Африке, Тайване, Таиланде и Турции. 70,71 Для получения информации о текущих и прошлых политиках и практиках вакцинации БЦЖ в более чем 180 странах используются Всемирный атлас БЦЖ и интерактивная карта. 70 БЦЖ вводят новорожденным с высоким защитным эффектом против туберкулезного менингита и милиарного туберкулеза, но этот эффект значительно ниже при туберкулезе легких. В случае взрослых вакцинация БЦЖ не полностью защищает от туберкулеза легких, что может объяснить, почему туберкулез является одной из основных причин смерти во всем мире.
70 БЦЖ вводят новорожденным с высоким защитным эффектом против туберкулезного менингита и милиарного туберкулеза, но этот эффект значительно ниже при туберкулезе легких. В случае взрослых вакцинация БЦЖ не полностью защищает от туберкулеза легких, что может объяснить, почему туберкулез является одной из основных причин смерти во всем мире.
Интересно, что БЦЖ также снижает младенческую смертность, что может быть связано с неспецифической перекрестной защитой от других, неродственных патогенов. 72 Вакцина БЦЖ снижает риск развития инфекций дыхательных путей, таких как вирус гриппа А, RSV и HSV2. 36–41 Кроме того, благодаря вакцинации БЦЖ исследования в Западной Африке показали значительное снижение смертности от малярии, сепсиса, респираторных инфекций и лепры. В целом во многих странах наблюдается снижение младенческой смертности благодаря вакцинации БЦЖ. 73 Кроме того, БЦЖ можно использовать для лечения других заболеваний, таких как рак мочевого пузыря, бородавки, лейшманиоз, кандидоз и астма. 74 В таблице 1 показаны неспецифические эффекты вакцины БЦЖ на различные вирусные инфекции.Более того, вакцина БЦЖ помогает в производстве других вакцин против болезнетворных бактерий и вирусов. Это связано с ее безопасностью в течение длительного времени у вакцинированных новорожденных, детей и взрослых, а также с тем, что антигены БЦЖ могут действовать как адъюванты, индуцируя врожденные и адаптивные иммунные ответы. 73 Ограниченные клинические данные свидетельствуют о том, что вакцинация БЦЖ может оказывать нецелевое защитное действие против вирусных инфекций у людей. Было проведено множество исследований, чтобы объяснить механизмы, лежащие в основе этих нецелевых защитных эффектов БЦЖ. 37,75,76
74 В таблице 1 показаны неспецифические эффекты вакцины БЦЖ на различные вирусные инфекции.Более того, вакцина БЦЖ помогает в производстве других вакцин против болезнетворных бактерий и вирусов. Это связано с ее безопасностью в течение длительного времени у вакцинированных новорожденных, детей и взрослых, а также с тем, что антигены БЦЖ могут действовать как адъюванты, индуцируя врожденные и адаптивные иммунные ответы. 73 Ограниченные клинические данные свидетельствуют о том, что вакцинация БЦЖ может оказывать нецелевое защитное действие против вирусных инфекций у людей. Было проведено множество исследований, чтобы объяснить механизмы, лежащие в основе этих нецелевых защитных эффектов БЦЖ. 37,75,76
Таблица 1 Обзор неспецифических эффектов вакцины БЦЖ, описанных при различных вирусных инфекциях (адаптировано из Moorlag et al. 77 ) |
Иммунный ответ на вакцину БЦЖ
Как правило, действие вакцин основано на активации адаптивного иммунного ответа и формировании иммунологической памяти антиген-специфических Т- и В-клеток для нацеливания на патогены. 95 После вакцинации БЦЖ бациллы распознаются и идентифицируются в месте прививки нейтрофилами, макрофагами и дендритными клетками (ДК), чтобы запустить иммунный ответ (рис. 1), где патоген-ассоциированные молекулярные паттерны (ПАМП), экспрессируемые микобактериями (такие как пептидогликан, арабиногалактан и миколовые кислоты) взаимодействуют с рецепторами распознавания образов (PRR), экспрессированными на клетках врожденного иммунитета, стимулируя макрофаги, созревание DC и высвобождение провоспалительных цитокинов. 96–99
95 После вакцинации БЦЖ бациллы распознаются и идентифицируются в месте прививки нейтрофилами, макрофагами и дендритными клетками (ДК), чтобы запустить иммунный ответ (рис. 1), где патоген-ассоциированные молекулярные паттерны (ПАМП), экспрессируемые микобактериями (такие как пептидогликан, арабиногалактан и миколовые кислоты) взаимодействуют с рецепторами распознавания образов (PRR), экспрессированными на клетках врожденного иммунитета, стимулируя макрофаги, созревание DC и высвобождение провоспалительных цитокинов. 96–99
Рисунок 1 Схематическое изображение иммунного ответа, вызванного вакцинацией БЦЖ. Примечания: Во-первых, нейтрофилы, макрофаги и дендритные клетки распознают БЦЖ в месте инокуляции. Затем активированные дендритные клетки мигрируют в лимфатические узлы, активируя адаптивные иммунные клетки. CD4 + и CD8 + Т-клетки активируются, высвобождая IFN-γ и гранзимы. |
PRR, которые участвуют в распознавании и интернализации БЦЖ, включают толл-подобные рецепторы (TLR), рецепторы, подобные домену олигомеризации нуклеотидов (NOD), рецепторы комплемента (CR3 и CR4), рецепторы CD14 и C-типа. лектины, такие как молекула межклеточной адгезии, специфичная для дендритных клеток, захватывающая нонинтегрин (DC-SIGN). 96,99 Созревание и миграция ДК в ближайшие вторичные лимфоидные ткани или селезенку связаны с повышенной экспрессией костимулирующих молекул (CD40, CD80, CD83 и CD86). 100 Антиген (Ag) 85, обнаруженный в клеточной стенке БЦЖ и M.tuberculosis , запускает продукцию фактора некроза опухоли-альфа (TNF-α), интерлейкина 1-бета (IL-1β) и IL-6, что приводит к провоспалительному состоянию для активации иммунных клеток. 101
Адаптивный иммунный ответ развивается, когда антигенпрезентирующие клетки (ДК, макрофаги и В-клетки) представляют антигенные пептиды на МНС и первичных Т-клетках в лимфатических узлах. 102 В лимфатических узлах инфицированные БЦЖ ДК выделяют ИЛ-6, ИЛ-12 и ФНО-α, а также вызывают активацию CD4 + и CD8 + Т-клеток с высокой продукцией IFN-γ. 103 Через десять недель после вакцинации в крови микобактерии-специфические CD8 + Т-клетки пролиферируют, высвобождают IFN-γ и экспрессируют гранзимы. 104 Кроме того, IFN-γ, TNF-α и IL-2 высвобождаются активированными Th2 CD4 + Т-клетками. 105 Кроме того, БЦЖ-инфицированные нейтрофилы объединяются с ДК (БЦЖ-инфицированными), стимулируя ответ антиген-специфических Т-клеток. 106 Высвобожденный IFN-γ активирует В-клетки и приводит к образованию клеток памяти и плазматических клеток, высвобождающих антиген-специфические антитела, способные опсонизировать БЦЖ и М.tuberculosis , ингибирующий внутриклеточный рост бактерий. 107
102 В лимфатических узлах инфицированные БЦЖ ДК выделяют ИЛ-6, ИЛ-12 и ФНО-α, а также вызывают активацию CD4 + и CD8 + Т-клеток с высокой продукцией IFN-γ. 103 Через десять недель после вакцинации в крови микобактерии-специфические CD8 + Т-клетки пролиферируют, высвобождают IFN-γ и экспрессируют гранзимы. 104 Кроме того, IFN-γ, TNF-α и IL-2 высвобождаются активированными Th2 CD4 + Т-клетками. 105 Кроме того, БЦЖ-инфицированные нейтрофилы объединяются с ДК (БЦЖ-инфицированными), стимулируя ответ антиген-специфических Т-клеток. 106 Высвобожденный IFN-γ активирует В-клетки и приводит к образованию клеток памяти и плазматических клеток, высвобождающих антиген-специфические антитела, способные опсонизировать БЦЖ и М.tuberculosis , ингибирующий внутриклеточный рост бактерий. 107
Вакцина БЦЖ перепрограммирует врожденный иммунитет (тренированный иммунитет)
В результате вакцинации БЦЖ повышенный неспецифический ответ на неродственные патогены опосредуется индукцией клеток врожденного иммунитета, включая моноциты/макрофаги и NK-клетки, и не зависит от ответов Т- и В-клеток (тренированный иммунитет) (рис. 2). Тренированный иммунитет после вакцинации БЦЖ связан с повышенной продукцией провоспалительных цитокинов (например,г. TNF-α, IL-1β и IL-6), обеспечивающие значительную защиту от различных вирусных инфекций. 108 109
2). Тренированный иммунитет после вакцинации БЦЖ связан с повышенной продукцией провоспалительных цитокинов (например,г. TNF-α, IL-1β и IL-6), обеспечивающие значительную защиту от различных вирусных инфекций. 108 109
Рисунок 2 Тренированный иммунитет, опосредованный эпигенетическим перепрограммированием моноцитов. |
Одним из молекулярных механизмов тренированного иммунитета является эпигенетическое перепрограммирование моноцитов посредством модификаций гистонов (метилирование и ацетилирование гистонов) в регуляторных элементах определенных генов (таких как TNF-α, IL-6 и IL-1β). ). 43,109,110 Эта модификация гистонов приводит к повышению доступности хроматина и облегчению транскрипции генов, которые связаны с усиленным антимикробным ответом и улучшенной функцией клеток. 110 Соответственно, когда эпигенетически обученные БЦЖ моноциты подвергаются воздействию другого патогена (вирусы и бактерии как патоген-ассоциированные молекулярные структуры), PPR легко и быстро распознают его, что приводит к увеличению продукции цитокинов (например, TNF-α, IL-1β и Ил-6). 95 Кроме того, метаболическое перепрограммирование приводит к избирательному накоплению или истощению некоторых метаболитов, которые регулируют эпигенетические изменения.
95 Кроме того, метаболическое перепрограммирование приводит к избирательному накоплению или истощению некоторых метаболитов, которые регулируют эпигенетические изменения.
Вакцина БЦЖ как средство против COVID-19
SARS-CoV-2 представляет собой вирус с одноцепочечной РНК. Жизненно важным структурным белком, кодируемым в его цепи РНК, является гликопротеин Spike (S), который состоит из трех гетеродимеров S1-S2, которые связываются с рецептором пневмоцитов типа II ангиотензинпревращающего фермента 2 (ACE2). SARS-CoV-2 проникает в клетки-хозяева путем эндоцитоза, а затем размножается в цитоплазме, что приводит к апоптозу клеток из-за высокого стресса, связанного с производством белка. Коронавирусная РНК сама по себе работает как PAMP и распознается PRR или TLR, что приводит к хемокинетическому всплеску, вызывающему миграцию и активацию нейтрофилов, что приводит к разрушению альвеолярно-капиллярных стенок.На микроскопическом уровне это приводит к потере интерфейса между внутриальвеолярным пространством и окружающей стромой, а затем к утечке жидкости и заполнению альвеолярных мешочков. 111 Натренированный иммунитет может оказывать потенциальное защитное действие против COVID-19.
111 Натренированный иммунитет может оказывать потенциальное защитное действие против COVID-19.
Была изучена связь некоторых вакцин (таких как БЦЖ, взрослая пневмококковая вакцина и сезонный грипп взрослых) со смертностью от COVID-19, что позволяет предположить, что у лиц, вакцинированных БЦЖ, снизился уровень смертности. 43,112 БЦЖ, как наиболее яркий пример индукции тренированного иммунитета, демонстрирует широкий спектр защиты не только от туберкулеза, но и от неродственных инфекций, особенно от инфекций дыхательных путей. 36–41,72 Интересно, что в нескольких экологических исследованиях была обнаружена обратная корреляция между вакцинацией БЦЖ и распространенностью и смертностью от COVID-19, что свидетельствует о потенциальном защитном эффекте БЦЖ против COVID-19. 42–46,113–116
Взаимодействие врожденной и адаптивной иммунной систем играет решающую роль в защите от вирусных инфекций.Хотя текущий обзор посвящен тренированному иммунитету, связанному с вакциной БЦЖ, с точки зрения COVID-19, недавно сообщалось о другом механизме перекрестной защиты, поскольку вакцина БЦЖ может генерировать перекрестно-реактивные Т-клетки против SARS-CoV-2, поскольку было показано, что БЦЖ содержат сходные последовательности из 9 аминокислот с SARS-CoV-2, и эти близкородственные пептиды имеют аффинность связывания от средней до высокой с обычными молекулами HLA класса I. 117
117
Кроме того, вакцинация БЦЖ может модулировать противовоспалительные реакции цитокинов и хемокинов, предотвращая госпитализацию и приводя к менее тяжелым случаям COVID-19. 118,119 Это может быть связано с предположением, что вакцина БЦЖ модулирует врожденную иммунную систему.
На основании этих исследований страны, в которых БЦЖ участвует в своих национальных программах вакцинации (страны БЦЖ), демонстрируют меньшее количество подтвержденных случаев COVID-19 на миллион жителей, чем страны, в которых политика вакцинации БЦЖ отсутствует (страны, не применяющие БЦЖ) (рис. 3). 43 116 120 Кроме того, количество смертей на миллион жителей в странах БКЖ ниже, чем в странах, не входящих в БКЖ (рис. 3C и D). 43 116 120 Escobar et al. 8 показали, что каждые 10% увеличения индекса БЦЖ были связаны со снижением смертности от COVID-19 на 10,4%. Кроме того, Галлахер и др. 112 обнаружили, что снижение log (10) смертности на 64% на 10 миллионов населения связано с вакцинацией БЦЖ.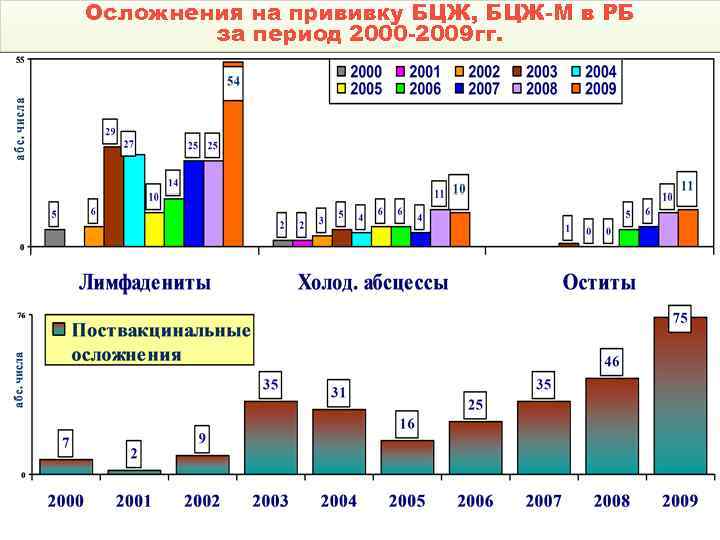 Более того, наблюдалась отрицательная корреляция между случаями и смертями от COVID-19 и годами после введения БЦЖ. 121 Исследование (опубликованное в октябре 2020 г.) также выявило меньшее количество случаев COVID-19 в странах БЦЖ, включая Афганистан, Индию, Бангладеш, Непал и Японию, по сравнению со странами, не входящими в БЦЖ, включая США, Великобританию, Канаду, Италию и Испанию. 122
Более того, наблюдалась отрицательная корреляция между случаями и смертями от COVID-19 и годами после введения БЦЖ. 121 Исследование (опубликованное в октябре 2020 г.) также выявило меньшее количество случаев COVID-19 в странах БЦЖ, включая Афганистан, Индию, Бангладеш, Непал и Японию, по сравнению со странами, не входящими в БЦЖ, включая США, Великобританию, Канаду, Италию и Испанию. 122
Рисунок 3 Защитный эффект вакцины БЦЖ против COVID-19. Примечания: ( A ) случаев COVID-19 в разных странах, начиная со дня, когда число случаев превысило 2 случая на миллион, до нескольких месяцев пандемии (апрель 2020 г.). Кривые стран без программы вакцинации БЦЖ выделены желтым фоном, а кривые стран с программой вакцинации БЦЖ при рождении выделены розовым фоном, ( B ) Подтвержденные случаи на миллион жителей в странах с БЦЖ и без БЦЖ, ( C ) смертей на миллион жителей и ( D ) коэффициенты смертности в странах, где действует БЦЖ, и в странах, не входящих в БЦЖ. |
Отрицательная корреляция между плановой вакцинацией младенцев БЦЖ и распространением COVID-19 среди молодежи была зафиксирована в разных странах в нескольких исследованиях. 123–125 Вакцинация БЦЖ в возрасте до 25 лет показала защитный эффект против COVID-19. 121 123 125 В 27 странах БЦЖ (либо при рождении, либо в детстве) смертность была ниже, чем в 23 странах, где БЦЖ не применялась (P < 0,001). 123
Большинство этих корреляционных экологических исследований были проведены в течение первых нескольких месяцев пандемии COVID-19. 42–46,126 Как и в любом обсервационном эпидемиологическом исследовании, собранные данные (например, данные на рис. 3) интерпретируются только как гипотеза, для подтверждения которой требуются дальнейшие детальные исследования.Таким образом, необходимы дальнейшие исследования с учетом различий между странами, включая демографию, социально-экономический статус, климат, частоту тестирования, стадию пандемии и протоколы профилактики инфекций.
42–46,126 Как и в любом обсервационном эпидемиологическом исследовании, собранные данные (например, данные на рис. 3) интерпретируются только как гипотеза, для подтверждения которой требуются дальнейшие детальные исследования.Таким образом, необходимы дальнейшие исследования с учетом различий между странами, включая демографию, социально-экономический статус, климат, частоту тестирования, стадию пандемии и протоколы профилактики инфекций.
Важно отметить, что клинические исследования также необходимы для того, чтобы сделать вывод о роли вакцины БЦЖ против COVID-19. 49 Соответственно, некоторые страны начали клинические исследования, чтобы подтвердить, способна ли вакцина БЦЖ защитить медицинских работников от инфекции SARS-CoV-2, и начался набор в эти клинические испытания (таблица 2). 127 128 В таблице 2 показаны различные клинические испытания по всему миру, в которых планируется рандомизировать более 10 000 медицинских работников, прошедших вакцинацию БЦЖ. В каждом исследовании измеряются различные первичные исходы. В случае с австралийским и американским дизайном они оценивают заболеваемость COVID-19 и симптомы заболевания; однако голландская группа рассматривает в первую очередь невыходы на работу медицинских работников. Четвертое обсервационное исследование случай-контроль в Египте начало набор положительных случаев COVID-19 и сравнивает тяжесть заболевания у пациентов с грудной клеткой. 129 Еще одно исследование в Германии проводится для проверки того, может ли VPM1002 (рекомбинантный вакцинный штамм, полученный из БЦЖ), защитить медицинских работников или пожилых пациентов от COVID-19. 130
В каждом исследовании измеряются различные первичные исходы. В случае с австралийским и американским дизайном они оценивают заболеваемость COVID-19 и симптомы заболевания; однако голландская группа рассматривает в первую очередь невыходы на работу медицинских работников. Четвертое обсервационное исследование случай-контроль в Египте начало набор положительных случаев COVID-19 и сравнивает тяжесть заболевания у пациентов с грудной клеткой. 129 Еще одно исследование в Германии проводится для проверки того, может ли VPM1002 (рекомбинантный вакцинный штамм, полученный из БЦЖ), защитить медицинских работников или пожилых пациентов от COVID-19. 130
Таблица 2 Характеристики текущих клинических испытаний вакцины БЦЖ в качестве средства профилактики COVID-19. |
На основании результатов этих клинических исследований мы можем подтвердить наличие защитного эффекта вакцинации БЦЖ против COVID-19. Однако для ответа на многие вопросы об этой защите потребуются дальнейшие исследования. Во-первых, как долго сохраняется гетерологичный иммунитет, вызванный БЦЖ, после прививки БЦЖ? И если этот натренированный иммунитет продержится несколько месяцев после прививки, то постепенно снизится. Во-вторых, когда лучше делать прививку БЦЖ? И если вакцинация БЦЖ в раннем возрасте (в возрасте до девяти месяцев) приводит к лучшему воздействию на респираторные инфекции и COVID-19, чем более поздние вакцинации? 43,131 Важно, чтобы эти вопросы были тщательно изучены, чтобы ответить на все высказанные опасения относительно недостаточности доказательств между вакцинацией БЦЖ и защитой от COVID-19. 132 Кроме того, для расшифровки механизмов, лежащих в основе корреляции между тренированным иммунитетом, индуцированным БЦЖ, и COVID-19, по-прежнему необходимы механистические исследования.
Однако для ответа на многие вопросы об этой защите потребуются дальнейшие исследования. Во-первых, как долго сохраняется гетерологичный иммунитет, вызванный БЦЖ, после прививки БЦЖ? И если этот натренированный иммунитет продержится несколько месяцев после прививки, то постепенно снизится. Во-вторых, когда лучше делать прививку БЦЖ? И если вакцинация БЦЖ в раннем возрасте (в возрасте до девяти месяцев) приводит к лучшему воздействию на респираторные инфекции и COVID-19, чем более поздние вакцинации? 43,131 Важно, чтобы эти вопросы были тщательно изучены, чтобы ответить на все высказанные опасения относительно недостаточности доказательств между вакцинацией БЦЖ и защитой от COVID-19. 132 Кроме того, для расшифровки механизмов, лежащих в основе корреляции между тренированным иммунитетом, индуцированным БЦЖ, и COVID-19, по-прежнему необходимы механистические исследования.
До сих пор ВОЗ по-прежнему рекомендует использовать вакцину БЦЖ против COVID-19 только в рандомизированных контролируемых исследованиях по ряду причин, а) неуверенная способность БЦЖ защищать от COVID-19, б) нехватка вакцины БЦЖ, в ) ложное чувство безопасности, d) на вакцину БЦЖ может повлиять последующее введение другой вакцины и e) усиление иммунитета с помощью БЦЖ может ухудшить течение COVID-19 у некоторых пациентов в критическом состоянии. 133,134 Еще один важный аспект связан с усилением врожденного иммунного ответа БЦЖ и осложнениями у пациентов с COVID-19 из-за преувеличенного цитокинового ответа. Эта гипотеза требует дальнейшего уточнения, поскольку было замечено, что у здоровых людей, вакцинированных БЦЖ, индуцировался тренированный иммунитет, что усиливало антимикробные свойства и снижало вирусную нагрузку, что приводило к уменьшению воспаления и симптомов. 44,135 Напротив, пожилые люди, как группа высокого риска, имеют дефектный противовирусный ответ, что приводит к высокой вирусной нагрузке и системному воспалению.Предположение о том, что индукция тренированного иммунитета БЦЖ может обеспечить защиту от COVID-19, должно быть оценено в ходе рандомизированных клинических испытаний.
133,134 Еще один важный аспект связан с усилением врожденного иммунного ответа БЦЖ и осложнениями у пациентов с COVID-19 из-за преувеличенного цитокинового ответа. Эта гипотеза требует дальнейшего уточнения, поскольку было замечено, что у здоровых людей, вакцинированных БЦЖ, индуцировался тренированный иммунитет, что усиливало антимикробные свойства и снижало вирусную нагрузку, что приводило к уменьшению воспаления и симптомов. 44,135 Напротив, пожилые люди, как группа высокого риска, имеют дефектный противовирусный ответ, что приводит к высокой вирусной нагрузке и системному воспалению.Предположение о том, что индукция тренированного иммунитета БЦЖ может обеспечить защиту от COVID-19, должно быть оценено в ходе рандомизированных клинических испытаний.
Интересно, что индукция квалифицированного иммунитета против COVID-19 может не ограничиваться БЦЖ, поскольку предполагается, что оральные вакцины против полиомиелита защищают от несвязанных вирусных инфекций, а рекомбинантная вакцина на основе БЦЖ (VPM1002) также может быть рассмотрена для клинических испытаний. 136 Таким образом, вакцина БЦЖ или другие обученные индукторы иммунитета, которые обеспечивают неспецифическую защиту, могут стать важным инструментом в ответ на COVID-19 и будущие пандемии.
136 Таким образом, вакцина БЦЖ или другие обученные индукторы иммунитета, которые обеспечивают неспецифическую защиту, могут стать важным инструментом в ответ на COVID-19 и будущие пандемии.
Заключение
В настоящее время пандемия COVID-19 поставила весь земной шар в беспрецедентный кризис, который требует быстрой разработки эффективной вакцины или лечения. БЦЖ, как живая аттенуированная вакцина, снижает младенческую смертность благодаря неспецифической перекрестной защите от других неродственных патогенов, включая инфекции дыхательных путей. В первые месяцы пандемии несколько эпидемиологических исследований выявили обратную зависимость между вакцинацией БЦЖ и заболеваемостью и смертностью от COVID-19.Поскольку вокруг неспецифической защиты БЦЖ ведутся споры, ожидается, что результаты нескольких текущих клинических испытаний в разных странах подтвердят корреляцию между вакцинацией БЦЖ и COVID-19, и следует соблюдать осторожность при интерпретации соответствующих результатов. Прежде чем размышлять о практике и политике вакцинации, следует собрать убедительные доказательства любой защитной роли вакцинации БЦЖ.
Прежде чем размышлять о практике и политике вакцинации, следует собрать убедительные доказательства любой защитной роли вакцинации БЦЖ.
Благодарности
Все фигурки созданы с помощью BioRender.ком. Работа KM поддерживается грантом стартапа Университета ОАЭ № G3347 и грантом UAEU-UPAR-Grant № G3458.
Вклад авторов
Все авторы внесли существенный вклад в концепцию и дизайн, сбор данных, анализ и интерпретацию данных; принимал участие в составлении статьи или ее критическом редактировании на предмет важного интеллектуального содержания; согласился подать в текущий журнал; дал окончательное одобрение версии для публикации; и соглашаетесь нести ответственность за все аспекты работы.
Раскрытие информации
Авторы заявляют об отсутствии конфликта интересов в отношении этой работы.
Ссылки
1. Коулман С.М., Фриман М.Б. Коронавирусы: важные новые патогены человека. Дж Вирол . 2014;88(10):5209–5212. doi:10.1128/ОВИ.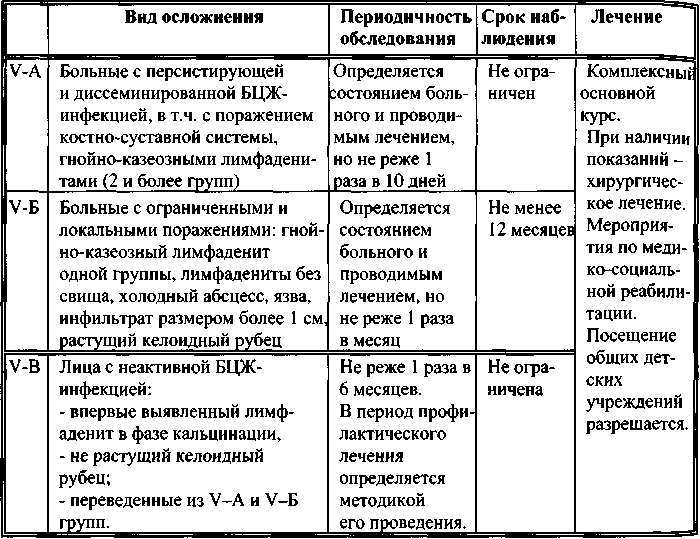 03488-13
03488-13
2. Lau SKP, Woo PCY, Li KSM и др. Вирус, подобный коронавирусу тяжелого острого респираторного синдрома, у китайских подковоносов. Proc Natl Acad Sci U S A . 2005;102(39):14040–14045. doi: 10.1073 / pnas.0506735102
3. Dar HA, Waheed Y, Najmi MH, et al. Дизайн мультиэпитопной субъединичной вакцины против COVID-19 на основе шиповидного белка SARS-CoV-2: анализ in silico. J Иммунол Рез . 2020;2020:1–15. дои: 10.1155/2020/8893483
4. Абид С.А., Сухейл А., Аль-Кадми И.М. и др. Биосенсоры как будущий подход к диагностике COVID-19. Науки о жизни . 2021;273:119117. doi:10.1016/j.lfs.2021.119117
5. Corman VM, Ithete NL, Richards LR, et al. Укоренение филогенетического древа коронавируса ближневосточного респираторного синдрома путем характеристики конспецифического вируса африканской летучей мыши. Дж Вирол . 2014;88(19):11297–11303. doi:10.1128/ОВИ.01498-14
6. ван Бохемен С., де Грааф М., Лаубер С. и соавт. Геномная характеристика недавно открытого коронавируса, связанного с острым респираторным дистресс-синдромом у людей. мБио . 2012;3(6):e00473. doi:10.1128/mBio.00473-12
и соавт. Геномная характеристика недавно открытого коронавируса, связанного с острым респираторным дистресс-синдромом у людей. мБио . 2012;3(6):e00473. doi:10.1128/mBio.00473-12
7. Заки А.М., ван Бохемен С., Бестеброер ТМ, Остерхаус АДМЕ, Фушье РАМ. Выделение нового коронавируса от мужчины с пневмонией в Саудовской Аравии. N Eng J Med .2012;367(19):1814–1820. дои: 10.1056/NEJMoa1211721
8. Escobar LE, Molina-Cruz A, Barillas-Mury C, Вакцина БЦЖ. Защита от тяжелой коронавирусной болезни 2019 (COVID19). medRxiv . 2020. doi:10.1101/2020.05.05.20091975
9. ВОЗ. ВОЗ объявляет вспышку COVID-19 пандемией; 2020 г. Доступно по адресу: http://www.euro.who.int/en/health-topics/health-emergencies/coronavirus-covid-19/news/news/2020/3/who-announces-covid-19-outbreak. -пандемия. По состоянию на 4 марта 2021 г.
10.ВОЗ. Коронавирусная болезнь, Еженедельное эпидемиологическое обновление — февраль 2021 г.; 2021 г. Доступно по адресу: https://www. who.int/publications/m/item/weekly-epidemiological-update—16-february-2021. По состоянию на 4 марта 2021 г.
who.int/publications/m/item/weekly-epidemiological-update—16-february-2021. По состоянию на 4 марта 2021 г.
11. Ван М., Цао Р., Чжан Л. и др. Ремдесивир и хлорохин эффективно ингибируют недавно появившийся новый коронавирус (2019-nCoV) in vitro. Сотовые Res . 2020;30(3):269–271. дои: 10.1038/s41422-020-0282-0
12. Holshue ML, DeBolt C, Lindquist S, et al. Первый случай нового коронавируса 2019 года в США. N Eng J Med . 2020;382(10):929–936. дои: 10.1056/NEJMoa2001191
13. Рейна Дж. Ремдесивир, противовирусная надежда против SARS-CoV-2. Rev Espanola de Quimioterapia . 2020;33(3):176–179. doi: 10.37201/req/028.2020
14. Sheahan TP, Sims AC, Leist SR, et al. Сравнительная терапевтическая эффективность ремдесивира и комбинации лопинавира, ритонавира и бета-интерферона против БВРС-КоВ. Нац Коммуна . 2020;11(1):222. дои: 10.1038/s41467-019-13940-6
15.Крузе РЛ. Терапевтические стратегии в сценарии вспышки для лечения нового коронавируса, возникшего в Ухане, Китай. F1000Res . 2020;9:72. doi:10.12688/f1000research.22211.2
F1000Res . 2020;9:72. doi:10.12688/f1000research.22211.2
16. Cascella M, Rajnik M, Cuomo A, Dulebohn SC, Di Napoli R. Особенности, оценка и лечение коронавируса (COVID-19) . StatPearls [Интернет]: StatPearls Publishing; 2020.
17. Zumla A, Chan JFW, Azhar EI, Hui DSC, Yuen K-Y. Коронавирусы — открытие лекарств и терапевтические возможности. Nat Rev Drug Discov . 2016;15(5):327–347.
18. Аль-Тауфик Дж.А., Моматтин Х., Диб Дж., Мемиш З.А. Терапия рибавирином и интерфероном у пациентов, инфицированных коронавирусом ближневосточного респираторного синдрома: обсервационное исследование. Int J Infect Dis . 2014;20:42–46. doi:10.1016/j.ijid.2013.12.003
19. Wu C-Y, Jan J-T, Ma S-H, et al. Небольшие молекулы, нацеленные на тяжелый острый респираторный синдром, коронавирус человека. Proc Natl Acad Sci U S A . 2004;101(27):10012.doi:10.1073/pnas.0403596101
20. Chu CM, Cheng VCC, Hung IFN и соавт. Роль лопинавира/ритонавира в лечении атипичной пневмонии: первоначальные вирусологические и клинические данные. Грудная клетка . 2004;59(3):252–256. doi:10.1136/грудная клетка.2003.012658
Грудная клетка . 2004;59(3):252–256. doi:10.1136/грудная клетка.2003.012658
21. Cao B, Wang Y, Wen D, et al. Испытание лопинавира-ритонавира у взрослых, госпитализированных с тяжелой формой Covid-19. N Eng J Med . 2020;382(19):1787–1799. дои: 10.1056/NEJMoa2001282
22. Саварино А., Ди Трани Л., Донателли И., Кауда Р., Кассоне А.Новое понимание противовирусных эффектов хлорохина. Ланцет Infect Dis . 2006;6(2):67–69. дои: 10.1016/S1473-3099(06)70361-9
23. Ян Ю., Цзоу З., Сунь Ю. и др. Противомалярийный препарат хлорохин высокоэффективен при лечении инфекции, вызванной вирусом птичьего гриппа A H5N1, на животных моделях. Сотовые Res . 2013;23(2):300–302. doi:10.1038/cr.2012.165
24. Vincent MJ, Bergeron E, Benjannet S, et al. Хлорохин является мощным ингибитором коронавирусной инфекции SARS и ее распространения. Вирол Дж . 2005;2(1):69. дои: 10.1186/1743-422X-2-69
25. Ролен Дж. М., Колсон П. , Рауль Д. Переработка хлорохина и его гидроксильного аналога для борьбы с бактериальными, грибковыми и вирусными инфекциями в 21 веке. Противомикробные агенты Int J . 2007;30(4):297–308. doi:10.1016/j.ijantimicag.2007.05.015
, Рауль Д. Переработка хлорохина и его гидроксильного аналога для борьбы с бактериальными, грибковыми и вирусными инфекциями в 21 веке. Противомикробные агенты Int J . 2007;30(4):297–308. doi:10.1016/j.ijantimicag.2007.05.015
26. Zhang Y, Chen C, Zhu S, et al. Выделение 2019-nCoV из образца стула лабораторно подтвержденного случая коронавирусной болезни 2019 (COVID-19). Еженедельный номер CCDC .2020;2(8):123–124. дои: 10.46234/ccdcw2020.033
27. Gao J, Tian Z, Yang X. Прорыв: хлорохина фосфат продемонстрировал очевидную эффективность при лечении пневмонии, связанной с COVID-19, в клинических исследованиях. Тенденции Biosci . 2020;14(1):72–73. doi: 10.5582/bst.2020.01047
28. Колсон П., Ролен Дж. М., Рауль Д. Хлорохин для нового коронавируса 2019 года. Противомикробные агенты Int J . 2020;55(3):105923. doi:10.1016/j.ijantimicag.2020.105923
29. Zhu F-C, Li Y-H, Guan X-H, et al.Безопасность, переносимость и иммуногенность рекомбинантной аденовирусной векторной вакцины против COVID-19 типа 5: открытое, нерандомизированное, первое испытание на людях с повышением дозы. Ланцет . 2020:395(10240):1845.
Ланцет . 2020:395(10240):1845.
30. Ван Ф., Крим Р.М., Стефано Г.Б. Доказательная точка зрения на разработку вакцины мРНК-SARS-CoV-2. Медицинский научный монитор . 2020; 26:e924700–e924700. doi:10.12659/MSM.924700
31. Smith TRF, Patel A, Ramos S, et al. Иммуногенность ДНК-вакцины-кандидата против COVID-19. Нац Коммуна . 2020;11(1):2601. дои: 10.1038/s41467-020-16505-0
32. Всемирная организация здравоохранения. Коронавирусная болезнь (COVID-19): вакцины; 2020 г. Доступно по адресу: https://www.who.int/news-room/q-a-detail/coronavirus-disease-(covid-19)-vaccines.
33. Kasozi KI, Niedbała G, Alqarni M, et al. Пчелиный яд — потенциальный кандидат в дополнительные лекарства для лечения инфекций SARS-CoV-2. Фронт общественного здравоохранения . 2020;8:755. doi:10.3389/fpubh.2020.594458
34.Махмуд З., Альрефаи Х., Хетта Х.Ф. и др. Изучение вирусологических, иммунологических и патологических путей для выявления потенциальных целей для разработки стратегий лечения и профилактики COVID-19. Вакцины . 2020;8(3):443. doi:10.3390/вакцин8030443
Вакцины . 2020;8(3):443. doi:10.3390/вакцин8030443
35. Абд Элла Н.Х., Гад С.Ф., Мухаммад К., Хетта Г.Э.Б. Наномедицина как перспективный подход к диагностике, лечению и профилактике COVID-19. Наномедицина . 2020;15(21):2085–2102. doi:10.2217/nnm-2020-0247
36.Спенсер Дж. К., Гангули Р., Уолдман Р. Х. Неспецифическая защита мышей от заражения вирусом гриппа путем местной или системной иммунизации бациллой Кальметта-Герена. J Заразить Dis . 1977;136(2):171–175.
37. Starr SE, Visintine AM, Tomeh MO, Nahmias AJ. Влияние иммуностимуляторов на устойчивость новорожденных мышей к инфекции простого герпеса 2 типа. Proc Soc Exp Biol Med . 1976;152(1):57–60. дои: 10.3181/00379727-152-39327
38. Вардхана Д.Э., Султана А., Манданг В., Джим Э.Эффективность прививки бациллой Кальметта-Герена для профилактики острых инфекций верхних дыхательных путей у пожилых людей. Acta Med Indones . 2011;43(3):185–190.
39. Nemes E, Geldenhuys H, Rozot V, et al. Профилактика инфекции M.tuberculosis с помощью вакцины h5: IC31 или ревакцинации БЦЖ. N Eng J Med . 2018;379(2):138–149. дои: 10.1056/NEJMoa1714021
Nemes E, Geldenhuys H, Rozot V, et al. Профилактика инфекции M.tuberculosis с помощью вакцины h5: IC31 или ревакцинации БЦЖ. N Eng J Med . 2018;379(2):138–149. дои: 10.1056/NEJMoa1714021
40. Ohrui T, Nakayama K, Fukushima T, Chiba H, Sasaki H. Профилактика пневмонии у пожилых людей с помощью вакцин против пневмококка, гриппа и БЦЖ. Нихон Ронен Игаккай Засси . 2005;42(1):34–36. doi:10.3143/гериатрия.42.34
41. Stensballe LG, Nante E, Jensen IP, et al. Острые инфекции нижних дыхательных путей и респираторно-синцитиальный вирус у младенцев в Гвинее-Бисау: положительный эффект вакцинации БЦЖ для девочек в исследовании методом случай-контроль. Вакцина . 2005;23(10):1251–1257. doi:10.1016/j.vaccine.2004.09.006
42. Миллер А., Реанделар М.Дж., Фаскильоне К., Руменова В., Ли Ю., Отазу Г.Х.Корреляция между политикой всеобщей вакцинации БЦЖ и снижением заболеваемости и смертности от COVID-19: эпидемиологическое исследование. MedRxiv . 2020.
2020.
43. Ковиан С., Ретамаль-Диас А., Буэно С.М., Калергис А.М. Может ли вакцинация БЦЖ вызвать защитный тренированный иммунитет против SARS-CoV-2? Фронт Иммунол . 2020;11:970. doi:10.3389/fimmu.2020.00970
44. Гурсель М., Гурсель И. Имеет ли значение глобальный тренированный иммунитет, вызванный вакцинацией БЦЖ, для прогрессирования пандемии SARS-CoV-2? Аллергия .2020;69(1):1–4. doi:10.15036/arerugi.69.1
45. Weng C, Saal A, Butt WW, et al. Вакцинация против бациллы Кальметта-Герена, клинические характеристики и исходы COVID-19 в Род-Айленде, США: когортное исследование. Эпидемиол Инфекция . 2020;1–9.
46. Берг М.К., Ю К., Сальвадор К.Э., Мелани И., Китаема С. Обязательная вакцинация бациллой Кальметта-Герена (БЦЖ) предсказывает сглаженные кривые распространения COVID-19. Медрхив . 2020.
47. Пироуз Б., Шаффи Хагшенас С., Шаффи Хагшенас С., Пиро П.Исследование серьезной проблемы в процессе устойчивого развития: анализ подтвержденных случаев COVID-19 (новый тип коронавируса) посредством бинарной классификации с использованием искусственного интеллекта и регрессионного анализа. Устойчивое развитие . 2020;12(6):2427. дои: 10.3390/su12062427
Устойчивое развитие . 2020;12(6):2427. дои: 10.3390/su12062427
48. Шаффи Хагшенас С., Пироуз Б., Шаффи Хагшенас С. и соавт. Приоритизация и анализ роли климатических и городских параметров в подтвержденных случаях COVID-19 на основе приложений искусственного интеллекта. Int J Environ Res Общественное здравоохранение . 2020;17(10):3730. doi:10.3390/ijerph27103730
49. Всемирная организация здравоохранения. вакцинация против бациллы Кальметта-Герена (БЦЖ) и COVID-19; 2020 г. Доступно по адресу: https://www.who.int/news-room/commentaries/detail/bacille-calmette-guérin-(bcg)-vaccination-and-covid-19. По состоянию на 4 марта 2021 г.
50. НБИК+. Обзор патентов в области нанотехнологий, посвященных коронавирусам. НБИК+. Доступно по адресу: https://statnano.com/news/67513/An-Overview-of-Nanotechnology-Patents-Focusing-on-Coronaviruses.По состоянию на 4 марта 2021 г.
51. Poon LLM, Chu DKW, Chan KH, et al. Идентификация нового коронавируса у летучих мышей. Дж Вирол . 2005;79(4):2001–2009. doi:10.1128/ОВИ.79.4.2001-2009.2005
Дж Вирол . 2005;79(4):2001–2009. doi:10.1128/ОВИ.79.4.2001-2009.2005
52. Ливингстон Э., Бухер К., Рекито А. Коронавирусная болезнь 2019 г. и грипп 2019-2020 гг. ЯМА . 2020;323(12):1122. дои: 10.1001/jama.2020.2633
53. Xu Z, Shi L, Wang Y, et al. Патологические проявления COVID-19, связанные с острым респираторным дистресс-синдромом. Ланцет Респир Мед . 2020;8(4):420–422. дои: 10.1016/S2213-2600(20)30076-X
54. Udugama B, Kadhiresan P, Kozlowski HN, et al. Диагностика COVID-19: болезнь и инструменты для обнаружения. АКС Нано . 2020;14(4):3822–3835. дои: 10.1021/acsnano.0c02624
55. Zhou P, Yang X-L, Wang X-G и др. Вспышка пневмонии, связанная с новым коронавирусом вероятного происхождения от летучих мышей. Природа . 2020;579(7798):270–273. doi: 10.1038/s41586-020-2012-7
56.Шахин А.Р., Эрдоган А., Агаоглу П.М. и др. Вспышка нового коронавируса (COVID-19) в 2019 году: обзор современной литературы. ЭЙМО . 2020;4(1):1–7.
ЭЙМО . 2020;4(1):1–7.
57. Гох ГК-М, Дункер А.К., Фостер Дж.А., Уверский В.Н. Жесткость внешней оболочки, предсказанная моделью внутреннего расстройства белка, проливает свет на инфекционность COVID-19 (Wuhan-2019-Ncov) . Многопрофильный институт цифровых публикаций; 2020.
58. Ан Д-Г, Шин Х-Дж, Ким М-Х и др. Текущее состояние эпидемиологии, диагностики, терапии и вакцин против новой коронавирусной болезни 2019 г. (COVID-19). Дж Микробиол Биотехнолог . 2020;30(3):313–324. дои: 10.4014/jmb.2003.03011
59. Xiao F, Tang M, Zheng X, Liu Y, Li X, Shan H. Доказательства желудочно-кишечной инфекции SARS-CoV-2. Гастроэнтерология . 2020; 158(6):1831–1833. е1833. doi:10.1053/j.gastro.2020.02.055
60. Hindson J. COVID-19: фекально-оральная передача? Nat Rev Гастроэнтерол Гепатол . 2020;17(5):259. дои: 10.1038/s41575-020-0295-7
61. He F, Deng Y, Li W. Коронавирусная болезнь 2019: что мы знаем? Дж Мед Вирол . 2020;92(7):719–725. дои: 10.1002/jmv.25766
2020;92(7):719–725. дои: 10.1002/jmv.25766
62. Chen N, Zhou M, Dong X, et al. Эпидемиологические и клинические характеристики 99 случаев новой коронавирусной пневмонии 2019 года в Ухане, Китай: описательное исследование. Ланцет . 2020;395(10223):507–513.
63. Yang X, Yu Y, Xu J, et al. Клиническое течение и исходы тяжелобольных пациентов с пневмонией SARS-CoV-2 в Ухане, Китай: одноцентровое ретроспективное обсервационное исследование. Ланцет Респир Мед .2020;8(5):475–481. дои: 10.1016/S2213-2600(20)30079-5
64. Магди Бешбиши А., Хетта Х.Ф., Хусейн Д.Э. и соавт. Факторы, связанные с повышенной заболеваемостью и смертностью пациентов с ожирением и избыточной массой тела при COVID-19. Биология . 2020;9(9):280. doi:10.3390/biology90
65. Li YC, Bai WZ, Hashikawa T. Нейроинвазивный потенциал SARS-CoV2 может играть роль в развитии дыхательной недостаточности у пациентов с COVID-19. Дж Мед Вирол . 2020;92(6):552–555. дои: 10.1002/jmv.25728
66. Desforges M, Le Coupanec A, Dubeau P, et al. Коронавирусы человека и другие респираторные вирусы: недооцененные условно-патогенные микроорганизмы центральной нервной системы? Вирусы . 2020;12(1):14. дои: 10.3390/v12010014
67. Сунь Т., Гуан Дж. Новый коронавирус и центральная нервная система. март . 2020:27(9):e52.
68. Петросильо Н., Вицеконте Г., Эргонул О., Ипполито Г., Петерсен Э. COVID-19, SARS и MERS: они тесно связаны? Clin Microbiol Infect .2020;26(6):729–734. doi:10.1016/j.cmi.2020.03.026
69. Махаирас Г.Г., Сабо П.Дж., Хики М.Дж., Сингх Д.К., Стовер К.К. Молекулярный анализ генетических различий между Mycobacterium bovis BCG и вирулентным M. bovis. J Бактериол . 1996;178(5):1274–1282. дои: 10.1128/JB.178.5.1274-1282.1996
70. Издание TBWAn. База данных о глобальной политике и практике вакцинации БЦЖ; 2017. Доступно по адресу: http://www.bcgatlas.org. По состоянию на 4 марта 2021 г.
71. Цверлинг А., Бер М.А., Верма А., Брюэр Т.Ф., Мензис Д., Пай М.Всемирный атлас БЦЖ: база данных о глобальной политике и практике вакцинации БЦЖ. ПЛОС Мед . 2011;8(3):3. doi:10.1371/journal.pmed.1001012
72. Ааби П., Рот А., Равн Х. и др. Рандомизированное исследование вакцинации БЦЖ при рождении детей с низкой массой тела при рождении: положительный неспецифический эффект в неонатальном периоде? J Заразить Dis . 2011;204(2):245–252. doi: 10.1093/infdis/jir240
73. Covián C, Fernández-Fierro A, Retamal-Díaz A, et al. Индуцированная БЦЖ перекрестная защита и развитие тренированного иммунитета.Значение для дизайна вакцины. Фронт Иммунол . 2019;10:2806. doi:10.3389/fimmu.2019.02806
74. Arts RJ, Carvalho A, La Rocca C, et al. Иммунометаболические пути в тренированном иммунитете, индуцированном БЦЖ. Представитель ячейки . 2016;17(10):2562–2571. doi:10.1016/j.celrep.2016.11.011
75. Ikeda S, Negishi T, Nishimura C. Повышение неспецифической устойчивости к вирусной инфекции с помощью мурамилдипептида и его аналогов. Противовирусный рез . 1985;5(4):207–215. дои: 10.1016/0166-3542(85)
-776. Спенсер Дж. К., Гангули Р., Вальдман Р. Х. Неспецифическая защита мышей от заражения вирусом гриппа путем местной или системной иммунизации бациллой Кальметта-Герена. J Заразить Dis . 1977;136(2):171–175. doi: 10.1093/infdis/136.2.171
77. Мурлаг С., Arts RJW, ван Кревел Р., Netea MG. Неспецифические эффекты вакцины БЦЖ при вирусных инфекциях. Clin Microbiol Infect . 2019;25(12):1473–1478. doi:10.1016/j.cmi.2019.04.020
78.Arts RJ, Moorlag SJ, Novakovic B, et al. Вакцинация БЦЖ защищает человека от экспериментальной вирусной инфекции за счет индукции цитокинов, связанных с тренированным иммунитетом. Микроб-хозяин клетки . 2018;23(1):89–100. е105.
79. Салем А., Нофал А., Хосни Д. Лечение обыкновенных и плоских бородавок у детей местной жизнеспособной бациллой Кальметта-Герена. Педиатр Дерматол . 2013;30(1):60–63. doi:10.1111/j.1525-1470.2012.01848.x
80. Podder I, Bhattacharya S, Mishra V, et al.Иммунотерапия вирусных бородавок внутрикожной вакциной Bacillus Calmette-Guerin по сравнению с внутрикожным туберкулиновым очищенным белковым производным: двойное слепое рандомизированное контролируемое исследование, сравнивающее эффективность и безопасность в центре третичной медицинской помощи в Восточной Индии. Indian J Dermatol Venereol Leprol . 2017;83(3):411.
81. Даулатабад Д., Панди Д., Сингал А. Вакцина БЦЖ для иммунотерапии бородавок: действительно ли она безопасна в эндемичных по туберкулезу районах? Дерматол Тер . 2016;29(3):168–172.doi:10.1111/dth.12336
82. Leentjens J, Kox M, Stokman R, et al. Вакцинация БЦЖ повышает иммуногенность последующей вакцинации против гриппа у здоровых добровольцев: рандомизированное плацебо-контролируемое пилотное исследование. J Заразить Dis . 2015; 212(12):1930–1938. дои: 10.1093/infdis/jiv332
83. Андерсон Ф.Д., Усидзима Р.Н., Ларсон С.Л. Рецидивирующий генитальный герпес: лечение Mycobacterium bovis (БЦЖ). Акушерство Гинекол . 1974;43(6):797–805.
84. Хиппманн Г., Веккели М., Розенкранц А.Р., Яриш Р., Гётц М.Неспецифическая иммунная стимуляция БЦЖ при рецидиве простого герпеса. Наблюдение через 5–10 лет после вакцинации БЦЖ. Вена Клин Вохеншр . 1992;104(7):200–204. [Статья на немецком языке].
85. Floc’h F, Werner G Повышенная устойчивость к вирусным инфекциям у мышей, привитых БЦЖ (Bacillus calette-guérin). Документ представлен в: Анналы иммунологии. 1976.
86. Мукерджи С., Субраманиам Р., Чен Х., Смит А., Кешава С., Шамс Х. Повышение эффероцитоза в альвеолярном пространстве с использованием вакцины БЦЖ для защиты хозяина от гриппозной пневмонии. PLoS One . 2017;12(7):7. doi:10.1371/journal.pone.0180143
87. de Bree LCJ, Marijnissen RJ, Kel JM, et al. Натренированный иммунитет, индуцированный Bacillus calette-guérin, не защищает от экспериментальной инфекции гриппа a/anhui/1/2013 (h7n9) у мышей. Фронт Иммунол . 2018;9:869. doi:10.3389/fimmu.2018.00869
88. Scheid A, Borriello F, Pietrasanta C, et al. Адъювантный эффект бациллы Кальметта-Герена на иммуногенность вакцины против гепатита В у недоношенных и доношенных новорожденных. Фронт Иммунол . 2018;9:29. doi:10.3389/fimmu.2018.00029
89. Кулкарни С., Мукерджи С., Пандей А., Дахаке Р., Падманабхан У., Чоудхари А.С. Бацилла Кальметта-Герена обеспечивает нейропротекцию в мышиной модели японского энцефалита. Нейроиммуномодуляция . 2016;23(5–6):278–286. дои: 10.1159/000452171
90. Лодмелл Д.Л., Эвальт Л.С. Повышенная устойчивость к инфекции вируса энцефаломиокардита у мышей, индуцированная масляно-капельной вакциной нежизнеспособных микобактерий туберкулеза. Заразить Иммуном . 1978;19(1):225–230. doi: 10.1128/IAI.19.1.225-230.1978
91. Лодмелл Д.Л., Эвальт Л.С. Индукция повышенной резистентности мышей к заражению вирусом энцефаломиокардита нежизнеспособными микобактериями туберкулеза: механизмы защиты. Заразить Иммуном . 1978;22(3):740–745. doi: 10.1128/IAI.22.3.740-745.1978
92. Suenaga T, Okuyama T, Yoshida I, Azuma M. Влияние инфекции Mycobacterium tuberculosis BCG на устойчивость мышей к инфекции вирусом эктромелии: участие интерферона в повышении устойчивости. Заразить Иммуном . 1978;20(1):312–314. doi:10.1128/IAI.20.1.312-314.1978
93. Sakuma T, Suenaga T, Yoshida I, Azuma M. Механизмы повышенной устойчивости мышей, обработанных Mycobacterium bovis БЦЖ, к вирусной инфекции эктромелии. Заразить Иммуном . 1983;42(2):567–573. doi:10.1128/IAI.42.2.567-573.1983
94. Матурин К.С., Мартенс Г.В., Корнфельд Х., Уэльс Р.М. Гетерологичный иммунитет, опосредованный Т-клетками CD4, между микобактериями и поксвирусами. Дж Вирол . 2009;83(8):3528–3539.дои: 10.1128/ОВИ.02393-08
95. Пулендран Б., Ахмед Р. Иммунологические механизмы вакцинации. Нат Иммунол . 2011;12(6):509. дои: 10.1038/ni.2039
96. Kumar S, Sunagar R, Gosselin E. Агонисты толл-подобных рецепторов бактериального белка: новый взгляд на вакцинные адъюванты. Фронт Иммунол . 2019;10:1144. doi:10.3389/fimmu.2019.01144
97. Молива Дж.И., Тернер Дж., Торреллес Дж.Б. Иммунный ответ на вакцинацию бациллами Кальметта-Герена: почему они не защищают от микобактерий туберкулеза? Фронт Иммунол .2017;8:407.
98. Докрелл Х.М., Смит С.Г. Что мы узнали о вакцинации БЦЖ за последние 20 лет? Фронт Иммунол . 2017;8:1134. doi:10.3389/fimmu.2017.01134
99. Гальярди М.С., Телони Р., Джаннони Ф. и соавт. Mycobacterium bovis Bacillus Calmette-Guérin инфицирует дендритную клетку DC-SIGN и вызывает ингибирование IL-12 и усиление продукции IL-10. J Лейкок Биол . 2005;78(1):106–113. doi:10.1189/jlb.0105037
100. Tsuji S, Matsumoto M, Takeuchi O, et al.Созревание дендритных клеток человека скелетом клеточной стенки Mycobacterium bovis бациллы Кальметта-Герена: участие толл-подобных рецепторов. Заразить Иммуном . 2000;68(12):6883–6890. doi:10.1128/IAI.68.12.6883-6890.2000
101. Joosten SA, van Meijgaarden KE, Arend SM, et al. Ингибирование роста микобактерий связано с тренированным врожденным иммунитетом. Дж Клин Инвест . 2018; 128(5):1837–1851. дои: 10.1172/JCI97508
102. Кауфманн С.Х. Противотуберкулезные вакцины: время подумать о следующем поколении.Документ представлен на: Семинары по иммунологии. 2013.
103. Bertholet S, Ireton GC, Kahn M, et al. Идентификация антигенов Т-клеток человека для разработки вакцин против микобактерий туберкулеза. Дж Иммунол . 2008;181(11):7948–7957. doi:10.4049/jиммунол.181.11.7948
104. Ханеком В.А. Иммунный ответ новорожденных на вакцинацию БЦЖ. Ann NY Acad Sci . 2005;1062(1):69–78. дои: 10.1196/анналы.1358.010
105. Soares AP, Kwong Chung CK, Choice T, et al.Продольные изменения ответов CD4(+) T-клеток памяти, индуцированных вакцинацией новорожденных БЦЖ. J Заразить Dis . 2013;207(7):1084–1094. дои: 10.1093/infdis/jis941
106. Морел С., Баделл Э., Абади В. и соавт. Mycobacterium bovis БЦЖ-инфицированные нейтрофилы и дендритные клетки взаимодействуют, вызывая специфические Т-клеточные ответы у людей и мышей. Евро J Иммунол . 2008;38(2):437–447. дои: 10.1002/эджи.200737905
107. Силва К.Л., Бонато В.Л., Лима В.М., Фаччоли Л.Х., Леао С.К.Характеристика памяти/активированных Т-клеток, которые опосредуют долгоживущий ответ хозяина против туберкулеза после вакцинации бациллой Кальметта-Герена или ДНК. Иммунология . 1999;97(4):573–581. doi:10.1046/j.1365-2567.1999.00840.x
108. Kleinnijenhuis J, Quintin J, Preijers F, et al. Бацилла Кальметта-Герена индуцирует NOD2-зависимую неспецифическую защиту от повторного заражения путем эпигенетического перепрограммирования моноцитов. Proc Nat Acad Sci . 2012;109(43):17537–17542.doi:10.1073/pnas.1202870109
109. Kleinnijenhuis J, van Crevel R, Netea MG. Тренированный иммунитет: последствия гетерологичных эффектов вакцинации БЦЖ. Trans R Soc Trop Med Hyg . 2015;109(1):29–35. дои: 10.1093/trstmh/tru168
110. Netea MG, Joosten LA, Latz E, et al. Тренированный иммунитет: программа врожденной иммунной памяти в норме и при болезни. Наука . 2016;352(6284):6284. doi:10.1126/science.aaf1098
111. Какодкар П., Кака Н., Байг М.Всесторонний обзор литературы по клинической картине и лечению пандемического коронавирусного заболевания 2019 г. (COVID-19). Куреус . 2020;12:4.
112. Галлахер Дж., Уотсон С., Ледвидж М. Ассоциация бацилл Кальметта-Герена (БЦЖ), пневмококковая вакцина для взрослых и вакцина против сезонного гриппа для взрослых со скорректированными показателями смертности от covid-19 в европейских странах уровня 4. medRxiv . 2020.
113. Хегарти П.К., Сфакианос Дж.П., Джаннарини Г., ДиНардо А.Р., Камат А.М.COVID-19 и бацилла Кальметта-Герена: какая связь? Евр Урол Онкол . 2020;3(3):259–261. doi:10.1016/j.euo.2020.04.001
114. Акияма Ю., Исида Т. Взаимосвязь между временем удвоения числа смертей от COVID-19 и национальной политикой вакцинации БЦЖ. medRxiv . 2020.
115. Дайал Д., Гупта С. Связь вакцинации БЦЖ и COVID-19: дополнительные данные. Медрхив . 2020.
116. Куратани Н. Ассоциация национальной политики вакцинации против Бациллы Кальметта-Герена с эпидемиологией COVID-19: экологическое исследование в 78 странах. medRxiv . 2020.
117. Томита Ю., Сато Р., Икеда Т., Сакагами Т. Вакцина БЦЖ может генерировать перекрестно-реактивные Т-клетки против SARS-CoV-2: анализ in silico и гипотеза. Вакцина . 2020;38(41):6352–6356. doi:10.1016/j.vaccine.2020.08.045
118. Freyne B, Donath S, Germano S, et al. Неонатальная вакцинация БЦЖ влияет на цитокиновый ответ на лиганды толл-подобных рецепторов и гетерологичные антигены. J Заразить Dis . 2018; 217(11):1798–1808. дои: 10.1093/infdis/jiy069
119. Weng C, Saal A, Butt WW, et al. Вакцинация против бациллы Кальметта-Герена, клинические характеристики и исходы COVID-19 в Род-Айленде, США: когортное исследование. Эпидемиол Инфекция . 2020;148.
120. Green CM, Fanucchi S, Fok ET, et al. COVID-19: модель, связывающая вакцинацию БЦЖ с защитой от смертности, подразумевает тренированный иммунитет. MedRxiv . 2020.
121. Клингер Д., Бласс И., Раппопорт Н., Линиал М.Значительно улучшенные результаты COVID-19 в странах с более высоким охватом вакцинацией БЦЖ: многопараметрический анализ. medRxiv . 2020.
122. Шарма А.Р., Батра Г., Кумар М. и соавт. БЦЖ как средство, меняющее правила игры, для предотвращения заражения и тяжести пандемии COVID-19? Аллергология и иммунопатология (Мард) . сент.-окт. 2020;48(5):507–517.
123. Эбина-Шибуя Р., Хорита Н., Намкунг Х., Канеко Т. Национальная политика универсальной детской вакцинации БЦЖ была связана со снижением смертности от COVID-19. Респирология . 2020;25(8):898–899. дои: 10.1111/соотв. 13885
124. Киношита М., Танака М. Влияние плановой вакцинации младенцев БЦЖ на COVID-19. J Заразить . 2020;81(4):625–633. doi:10.1016/j.jinf.2020.08.013
125. Шарма А., Шарма С.К., Ши Ю. и др. Политика вакцинации БЦЖ и профилактическое использование хлорохина: влияют ли они на пандемию COVID-19? Смерть клеток Dis . 2020;11(7):1–10. дои: 10.1038/s41419-020-2720-9
126. Урасима М., Отани К., Хасэгава Ю., Акуцу Т. Вакцинация БЦЖ.Смертность от COVID-19 в 173 странах: экологическое исследование. Int J Environ Res Общественное здравоохранение . 2020;17:15. дои: 10.3390/ijerph27155589
127. Миясака М. Связана ли вакцинация БЦЖ со снижением смертности от COVID-19? ЭМБО Мол Мед . 2020;12(6):e12661. дои: 10.15252/эммм.202012661
128. Санчес-Мостиеро Д., Меликор А.Ф. Следует ли использовать вакцину Bacillus Calmette-Guérin (BCG) для профилактики COVID-19? АктаМедика Филиппина . 2020; 54 (Специальный выпуск о коронавирусной болезни (COVID19)).
129. O’Connor E, Teh J, Kamat AM, Lawrentschuk N. Использование вакцины Bacillus Calmette Guérin (BCG) в борьбе с COVID-19 – что из старого в новом? Медицина будущего . 2020.
130. De Vrieze J. Может ли противотуберкулезная вакцина столетней давности укрепить иммунную систему против нового коронавируса. Наука . 2020;370(6519):895–897. doi:10.1126/наука.370.6519.895
131. Холлм-Дельгадо М.-Г., Стюарт Э.А., Блэк Р.Э. Острая инфекция нижних дыхательных путей у детей, привитых бациллой Кальметта-Герена (БЦЖ). Педиатрия . 2014;133(1):e73–e81. doi:10.1542/пед.2013-2218
132. Hamiel U, Kozer E, Youngster I. Показатели SARS-CoV-2 у вакцинированных БЦЖ и невакцинированных молодых людей. ЯМА . 2020;323(22):2340. дои: 10.1001/jama.2020.8189
133. Фауст Л., Хаддарт С., Маклин Э., Свадзян А. Универсальная вакцинация БЦЖ и защита от COVID-19: критика экологического исследования. Джей Клуб . 2020;1.
134. Поллард А.Дж., Финн А., Кертис Н. Неспецифические эффекты вакцин: вероятные и потенциально важные, но последствия неясны. Арч Ди Чайлд . 2017;102(11):1077–1081. doi: 10.1136 / archdischild-2015-310282
135. Arts RJW, Moorlag SJCFM, Novakovic B, et al. Вакцинация БЦЖ защищает человека от экспериментальной вирусной инфекции за счет индукции цитокинов, связанных с тренированным иммунитетом. Микроб-хозяин клетки . 2018;23(1):89–100.e105. doi:10.1016/j.chom.2017.12.010
136. Сингх Б.Р., Гандхарва Р. Являются ли вакцинация БЦЖ, плотность населения, средний возраст и бедность важными детерминантами распространения пандемии COVID-19, заболеваемости и смертности? Заболеваемость Смертность .2020;10.
Оценка детей с осложнениями после вакцинации БЦЖ на севере Ирана
Авторы
1 Доцент Исследовательского центра инфекционных заболеваний с упором на внутрибольничные инфекции Мазандаранского университета медицинских наук, Сари, Иран.
2 Аспирант в области медицинской микологии, Исследовательский центр устойчивости к противомикробным препаратам, Студенческий исследовательский комитет, Мазандаранский университет медицинских наук, Сари, Иран
3 Резидент кафедры педиатрии, Исследовательский центр инфекционных заболеваний с упором на внутрибольничные инфекции, Университет медицинских наук Мазандаран, Сари, Иран.
4 Доцент, Исследовательский центр талассемии, Институт гемоглобинопатии, Мазандаранский университет медицинских наук, Сари, Иран.
Реферат
Справочная информация: Хотя эффективность вакцины Bacillus Calmette-Guerin (BCG) в профилактике туберкулеза неоднократно отмечалась, использование вакцины BCG не лишено риска.В этом исследовании мы стремились провести иммунологическую оценку детей с осложнениями после вакцинации БЦЖ на севере Ирана.
Материалы и методы: Это исследование методом «случай-контроль» началось 30 января 2013 г. и завершилось 2 июля 2015 г. В группу наблюдения было включено 35 пациентов с умеренными и тяжелыми осложнениями вакцинации БЦЖ против туберкулеза (ТБ). В контрольную группу вошли 35 пациентов с легкими осложнениями и без осложнений, связанных с вакциной БЦЖ. Были проведены рутинные и специфические тесты для оценки иммунологической функции.
Результаты: Из общего числа 35 пациентов в группе наблюдения у 3 (8,6%) пациентов было тяжелое осложнение, также им был поставлен диагноз БЦЖ-оз; 32 (91,42%) случая имели умеренную симптоматику. В контрольной группе у 25 (71,4%) больных были легкие осложнения и у 10 (28,57%) больных осложнений не было. Средний уровень IL-23 в двух группах имел значительную разницу (P = 0,027). Выявлена достоверная взаимосвязь дефицита интерлейкина и интерферона у пациентов с тяжелыми осложнениями.Пациенты с легкими и среднетяжелыми осложнениями вакцины БЦЖ не были связаны с иммунодефицитом. Пациенты с тяжелыми осложнениями вакцины БЦЖ были связаны с менделевской восприимчивостью к микобактериальной болезни (MSMD) и первичным иммунодефицитом (PID).
Заключение: Тяжелые осложнения вакцины БЦЖ могут быть вызваны MSMD и могут быть связаны с иммунодефицитом IL 12/23. Вакцинация БЦЖ должна быть отложена у новорожденных в семьях с историей смерти после предполагаемой вакцинации БЦЖ или ранняя смерть, или рецидивирующая инфекция, пока соответствующие скрининговые иммунологические тесты не исключат ВЗОМТ.
Ключевые слова
Туберкулез | История вакцин
Симптомы и возбудитель
Туберкулез – заболевание, вызываемое бактериями туберкулеза, Mycobacterium tuberculosis.
Симптомы активной туберкулезной инфекции включают кашель, длящийся несколько недель, отхаркивание мокроты (слизи) или крови, лихорадку, ночную потливость и боль в груди.
Некоторые люди могут быть инфицированы бактериями туберкулеза, но не иметь симптомов. Это называется латентным туберкулезом. Латентный туберкулез может привести к активному заболеванию. Некоторые люди с латентным туберкулезом могут никогда не заболеть.
Трансмиссия
Туберкулезные бактерии передаются через инфицированные респираторные капли, такие как те, которые распространяются, когда больные люди кашляют, чихают или даже разговаривают. Неинфицированный человек может вдохнуть инфицированные капли в легкие и заразиться.
Люди с латентной туберкулезной инфекцией не передают бактерии туберкулеза окружающим.
Лечение и уход
Большинство случаев туберкулеза можно успешно лечить. Людей с активным туберкулезом лечат антибиотиками и другими препаратами, которые убивают или контролируют бактерии туберкулеза. Лечение обычно длится несколько месяцев.
Людей с латентным туберкулезом можно лечить антибиотиками, чтобы они впоследствии не заболели активным туберкулезом.
В последние годы некоторые штаммы туберкулеза стали устойчивыми к антибиотикам. Эти случаи сложнее и дороже лечить, и лечение может иметь серьезные побочные эффекты. Поскольку лекарственно-устойчивый туберкулез крайне сложно поддается лечению, важно предотвратить заболевание. Меры профилактики включают в себя обеспечение того, чтобы больные туберкулезом принимали все прописанные им лекарства и лечились правильными лекарствами.
Осложнения и смертность
Несмотря на то, что путь заражения туберкулезом – респираторный, а основные симптомы обычно респираторные, туберкулезные бактерии могут распространяться и инфицировать другие части тела, такие как кости и головной мозг.
Активный туберкулез без лечения может привести к летальному исходу. Около 3% людей с невылеченным туберкулезом умирают. Однако эта цифра намного выше, когда человек также инфицирован вирусом иммунодефицита человека (ВИЧ). Около 18% людей с активной формой туберкулеза и ВИЧ-инфекцией могут умереть.
Заражение активным туберкулезом также более опасно для очень маленьких детей. У них больше шансов получить серьезные осложнения от туберкулеза, такие как туберкулезный менингит (инфекция оболочек, окружающих мозг).
В 2014 г., 9.6 миллионов человек заболели туберкулезом. От туберкулеза умерло около 1,5 млн человек, в том числе около 140 тыс. детей. Около трети населения земного шара больны латентным туберкулезом.
Доступные вакцины и кампании по вакцинации
Вакцина против бациллы Кальметта-Герена (БЦЖ) используется в рамках национальных программ вакцинации в странах с большим количеством случаев туберкулеза. Вакцина не защищает детей от легочных заболеваний, вызванных бактериями ТБ, и не предотвращает прогрессирование латентной инфекции ТБ в активную форму заболевания.Однако он предотвращает некоторые серьезные осложнения туберкулеза у детей, такие как туберкулезный менингит. Вакцина, как правило, не используется у взрослых, а вакцинация детей не предотвращает распространение болезни.
Вакцина БЦЖ используется с 1921 года. Многие исследователи работают над созданием более эффективной противотуберкулезной вакцины. Надежда состоит в том, чтобы разработать вакцину, которая предотвращает заражение туберкулезом, что уменьшит серьезное бремя болезней во всем мире, а также уменьшит передачу бактерий туберкулеза.
Рекомендации по вакцинацииВ странах со многими случаями туберкулеза вакцина БЦЖ вводится младенцам вскоре после их рождения. Младенцам с ВИЧ-инфекцией не рекомендуется делать прививку.
В странах с очень небольшим числом случаев ТБ младенцам может быть рекомендована вакцинация, если они могут заразиться ТБ, например, если они проживают в доме со взрослым, инфицированным активным ТБ.
Источники
Центры по контролю и профилактике заболеваний.Основные факты о туберкулезе. Дата обращения 25.01.2018.
Straetemans, M., Glaziou, P., Bierrenbach, A.L., Sismanidis, C., & van der Werf, M.J. Оценка коэффициента смертности от туберкулеза: метаанализ. PLoS One, 2011;6(6), e20755.
Всемирная организация здравоохранения. Детский туберкулез. Дата обращения 25.01.2018.
ВОЗ. Документ с изложением позиции по вакцине БЦЖ. № 4, 2004. С. 79. С. 25-40. Дата обращения 25.01.2018.
ВОЗ. Пересмотренные рекомендации по вакцинации БЦЖ для младенцев с риском заражения ВИЧ.Дата обращения 25.01.2018.
ВОЗ. Информационный бюллетень по туберкулезу.




 Активация В-клеток приводит к образованию клеток памяти и плазматических клеток с высвобождением антиген-специфических антител.
Активация В-клеток приводит к образованию клеток памяти и плазматических клеток с высвобождением антиген-специфических антител. Эта цифра основана на собранных данных до апреля 2020 года. ** Статистически значимые различия между группами. Воспроизведено из Covián C, Retamal-Díaz A, Bueno SM, Kalergis AM. Может ли вакцинация БЦЖ вызвать защитный тренированный иммунитет против SARS-CoV-2? Границы иммунологии . 2020;11:970. Авторское право © 2020 Covián, Retamal-Díaz, Bueno and Kalergis. Лицензия Creative Commons с указанием авторства (CC BY). 43
Эта цифра основана на собранных данных до апреля 2020 года. ** Статистически значимые различия между группами. Воспроизведено из Covián C, Retamal-Díaz A, Bueno SM, Kalergis AM. Может ли вакцинация БЦЖ вызвать защитный тренированный иммунитет против SARS-CoV-2? Границы иммунологии . 2020;11:970. Авторское право © 2020 Covián, Retamal-Díaz, Bueno and Kalergis. Лицензия Creative Commons с указанием авторства (CC BY). 43