МУКОЛИТИКИ В ЛЕЧЕНИИ БОЛЕЗНЕЙ ОРГАНОВ ДЫХАНИЯ: ФОКУС НА БЕЗОПАСНОСТЬ
Статті06/04/2015
Продолжение. Начало в журнале «Фармацевт Практик» № 2, 2015: Муколитики в лечении болезней органов дыхания: фокус на безопасность
Муколитики и мукорегуляторы являются наиболее востребованными при лечении продуктивного кашля, сходны по фармакологическим свойствам и показаниям к применению, но в то же время имеют некоторые особенности
К муколитикам относятся препараты, которые разжижают мокроту, практически без увеличения ее объема, и облегчают ее выведение из легких.
Амброксол обладает секретолитическим и секретокинетическим действием, восстанавливает мукоцилиарный транспорт (МЦТ), увеличивает проникновение антибиотиков в легочную ткань. Он стимулирует образование трахеобронхиального секрета пониженной вязкости. Амброксол восстанавливает МЦТ путем стимуляции двигательной активности ресничек мерцательного эпителия.
Амброксол не рекомендовано применять в І триместре беременности и в период кормления грудью. При применении амброксола побочные явления наблюдаются редко и проявляются в виде растройств желудочно-кишечного тракта (изжоги, диспепсии, тошноты, рвоты, поноса, аллергических реакций, сухости во рту и носоглотке). Препарат не следует применять совместно с противокашлевыми средствами, так как это приводит к накоплению бронхиального секрета в дыхательных путях.
Бромгексин при приеме внутрь превращается в активный метаболит — амброксол.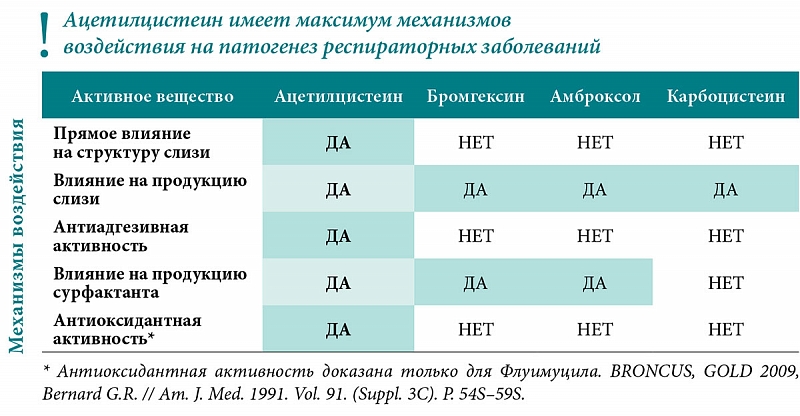 Действие его аналогично таковому амброксола, хотя и менее выражено. Бромгексин применяют внутрь в суточной дозе 32–48 мг, разделенной на 2–3 приема. В отличие от амброксола, при тяжелой печеночной недостаточности клиренс бромгексина снижается, так как он является пролекарством, поэтому необходима коррекция дозы и режима дозирования. Препарат при многократном применении может кумулировать. Его не следует принимать в I триместр беременности [1].
Действие его аналогично таковому амброксола, хотя и менее выражено. Бромгексин применяют внутрь в суточной дозе 32–48 мг, разделенной на 2–3 приема. В отличие от амброксола, при тяжелой печеночной недостаточности клиренс бромгексина снижается, так как он является пролекарством, поэтому необходима коррекция дозы и режима дозирования. Препарат при многократном применении может кумулировать. Его не следует принимать в I триместр беременности [1].
Ацетилцистеин характеризуется прямым действием на молекулярную структуру слизи. К разжижению мокроты приводит также стимуляция мукозных клеток, секрет которых обладает способностью лизировать фибрин и кровяные сгустки. Препарат эффективен как при гнойной, так и при слизистой мокроте. Данные о влиянии ацетилцистеина на МЦТ противоречивы [2, 3]. Важное свойство ацетилцистеина — влияние на процессы детоксикации [1]. Он способствует повышению синтеза глутатиона — важного фактора химической детоксикации. Эта особенность ацетилцистеина дает возможность эффективно применять его при отравлениях парацетамолом и другими токсическими веществами (альдегидами, фенолами и др.
Ацетилцистеин назначают внутрь по 200 мг 3 раза в сутки (максимальная суточная доза — 1200 мг) в течение 5–7 дней, при хронических заболеваниях возможно увеличение продолжительности его применения до 6 мес. Ацетилцистеин можно также использовать в виде внутрибронхиальных инстилляций по 1 мл 10% раствора и промывания бронхов во время проведения лечебной бронхоскопии. Имеются данные о том, что длительное применение ацетилцистеина при хронической обструктивной болезни легких (ХОБЛ) приводит к снижению частоты, тяжести и уменьшению длительности обострений [5].
Мукорегуляторы — лекарственные препараты, увеличивающие синтез сиаломуцинов (мукорегулирующий эффект) и изменяющие вязкость бронхиального секрета (муколитический эффект). Представителем мукорегуляторов является карбоцистеин. Он обладает одновременно как муколитическим, так и мукорегулирующим эффектом. Карбоцистеин стимулирует активность сиалилтрансферазы, увеличивает синтез сиаломуцинов, оптимизируя баланс сиаломуцинов и фукомуцинов [7], восстанавливает эластичные (вязкоупругие) свойства слизи [8]. Карбоцистеин не действует непосредственно на структуру слизи, в отличие от прямого муколитика ацетилцистеина. Карбоцистеин обладает не только муколитическим эффектом, но и восстанавливает нормальную активность секреторных (бокаловидных) клеток слизистой оболочки дыхательных путей, повышает продукцию sIgA [9–11], что особенно важно у детей с рецидивирующими респираторными инфекциями. Это позволяет отнести карбоцистеин к наиболее современным и перспективным мукоактивным лекарственным средством [12, 5]. Кроме мукорегулирующего действия, карбоцистеин оказывает противовоспалительный и иммуномодулирующий эффект [10, 13]. В доклинических и клинических исследованиях доказано, что карбоцистеин уменьшает инфильтрацию нейтрофильных гранулоцитов в просвет дыхательных путей [14], снижает уровень интерлейкина (ИЛ)-8, ИЛ-6, уровень цитокинов и 8-изопростана при ХОБЛ [15].
Карбоцистеин стимулирует активность сиалилтрансферазы, увеличивает синтез сиаломуцинов, оптимизируя баланс сиаломуцинов и фукомуцинов [7], восстанавливает эластичные (вязкоупругие) свойства слизи [8]. Карбоцистеин не действует непосредственно на структуру слизи, в отличие от прямого муколитика ацетилцистеина. Карбоцистеин обладает не только муколитическим эффектом, но и восстанавливает нормальную активность секреторных (бокаловидных) клеток слизистой оболочки дыхательных путей, повышает продукцию sIgA [9–11], что особенно важно у детей с рецидивирующими респираторными инфекциями. Это позволяет отнести карбоцистеин к наиболее современным и перспективным мукоактивным лекарственным средством [12, 5]. Кроме мукорегулирующего действия, карбоцистеин оказывает противовоспалительный и иммуномодулирующий эффект [10, 13]. В доклинических и клинических исследованиях доказано, что карбоцистеин уменьшает инфильтрацию нейтрофильных гранулоцитов в просвет дыхательных путей [14], снижает уровень интерлейкина (ИЛ)-8, ИЛ-6, уровень цитокинов и 8-изопростана при ХОБЛ [15].
В числе побочных эффектов очень редко можно выделить нарушения пищеварения, тошноту, рвоту, боль в желудке, в единичных случаях могут возникнуть аллергические реакции.
Нецелесообразно одновременно применять препараты, подавляющие секреторную функцию бронхов, и средства от кашля. Препараты карбоцистеина в форме сиропа не следует назначать больным сахарным диабетом, так как они содержат сахарозу.
Карбоцистеин противопоказан в І триместре беременности.
Препараты карбоцистеина выпускаются только для приема внутрь. Наиболее комплаентными препаратами карбоцистеина являются лекарственные средства в форме сиропа, выпускаемые в двух дозировках: для взрослых — 5% и детей — 2%.
Результаты недавно проведенных исследований свидетельствуют о потенциальных свойствах карбоцистеина предотвращать патологические процессы в бронхиальных эпителиальных клетках, вызванных воздействием табачного дыма [20–22].
По данным систематического обзора по исследованию эффективности карбоцистеина у детей с инфекционными заболеваниями верхних и нижних отделов дыхательных путей без хронических бронхолегочных заболеваний была доказана способность карбоцистеина уменьшать выраженность кашля. При этом отмечена хорошая переносимость препарата [23]. Кроме того, карбоцистеин оказался эффективным и безопасным при лечении пациентов с ХОБЛ, что доказано в ряде рандомизированных клинических испытаний [2, 24–27]. Препарат снижает частоту обострений и улучшает качество жизни пациентов. Также была установлена способность карбоцистеина ингибировать окислительный стресс и воспаление при хронических заболеваниях, как самостоятельно, так и в сочетании с другими антиоксидантными препаратами [28–30].
Продолжение следует
Анна Зайченко д-р мед. наук, профессор, зав. кафедрой,
Оксана Мищенко, д-р фарм. наук, профессор,
Кафедра клинической фармакологии Института повышения квалификации специалистов фармации, Национальный фармацевтический университет
Список литературы находится в редакции
Референтный препарат карбоцистеина в Украине Флюдитек («Иннотек Интернасиональ», Франция) занимает сегодня
лидирующие позиции по назначениям врачей и рекомендациям фармацевтов. Препарат разрешен к безрецептурному отпуску и включен в протоколы провизоров (фармацевтов) [31]. С целью повышения комплаентности Флюдитек выпускается в 2 формах: сироп 2% — для детей и 5% — для взрослых, по 125 мл во флаконе. Успешный 20-летний опыт клинического применения свидетельствует о эффективности, безопасности и хорошей переносимости препарата Флюдитек. Этот мукорегулятор широко используют у пациентов разных возрастных групп в комплексной терапии воспалительных заболеваний верхних и нижних дыхательных путей. Флюдитек можно применять у детей старше 2 лет при респираторных заболеваниях, сопровождающихся нарушением бронхиальной секреции и выведения мокроты из дыхательных путей, особенно при острых бронхолегочных заболеваниях (остром бронхите, обострении хронических заболеваний дыхательной системы)
Флюдитек можно применять у детей старше 2 лет при респираторных заболеваниях, сопровождающихся нарушением бронхиальной секреции и выведения мокроты из дыхательных путей, особенно при острых бронхолегочных заболеваниях (остром бронхите, обострении хронических заболеваний дыхательной системы)
Для детей от 2 до 15 лет применяют 2% сироп в дозе: 2–5 лет — по 5 мл 2 раза в сутки; 5–15 лет — по 5 мл 3 раза в сутки. Детям старше 15 лет и взрослым назначают 5% сироп в дозе 15 мл 3 раза в сутки, при достижении терапевтического эффекта дозу снижают до 10 мл 3 раза в сутки. Курс лечения составляет 8–10 дней [19]
Информация для специалистов в сфере здравоохранения. Полная информация содержится в инструкции по применению препарата.
Р.С. МЗ Украины № UA/8082/02 от 12.07.2013 № 593. Инструкция по медицинскому применению препарата Флюдитек 2%, сироп, и Флюдитек 5%, сироп
“Фармацевт Практик” #03′ 2015
Поділіться цим з друзями!
Вам також буде цікаво це:
АЦЦ® О кашле.
 Что такое кашель – сухой, влажный, мокрота и как лечить. Муколитики и отхаркивающие – амброксол, карбоцистеин, бромгексин. Кашель при ОРЗ (ОРВИ), бронхите, пневмония, синусит, ларинготрахеит, бронхиолит, ХОБЛ, отите.
Что такое кашель – сухой, влажный, мокрота и как лечить. Муколитики и отхаркивающие – амброксол, карбоцистеин, бромгексин. Кашель при ОРЗ (ОРВИ), бронхите, пневмония, синусит, ларинготрахеит, бронхиолит, ХОБЛ, отите.Кашель — это защитный рефлекс организма, который позволяет освободить дыхательные пути от слизи, пыли и инородных тел. Каждый день в клетках, выстилающих дыхательные пути, образуется небольшое количество слизи. Эта слизь увлажняет дыхательные пути и поглощает мелкие частицы, вдыхаемые с воздухом, чтобы они не попали в легкие. Кашель нужен организму, ведь он удаляет скопление слизи и помогает очистить дыхательные пути.
Вместе с тем кашель — основной симптом, сопровождающий различные инфекции дыхательной системы, такие как ОРВИ («простуда») и грипп. При воспалительных заболеваниях дыхательных путей характерно изменение вязкости бронхиальной слизи (вязкая слизь называется мокротой).
Можно условно выделить следующие стадии развития кашля при заболеваниях нижних дыхательных путей:
Непродуктивный или малопродуктивный кашель (ощущается как «сухой» и мокрота еще не откашливается).

Непродуктивный или малопродуктивный кашель, как правило, возникает в самом начале острых респираторных инфекций. Отделение мокроты при этом еще не происходит, т.к. она очень густая и вязкая, её трудно откашлять.
Для того, чтобы помочь избавиться от мокроты и от кашля при ОРИ рекомендовано применение муколитиков – например, АЦЦ®. Это позволит перевести непродуктивный кашель в продуктивный, и тем самым, поможет выздоровлению11.
Течение многих респираторных заболеваний предполагает переход от непродуктивного или малопродуктивного кашля к продуктивному кашлю с отхождением мокроты.
Важно! Малопродуктивный кашель при простуде не рекомендуется лечить противокашлевыми средствами, это может только усугубить болезнь, из-за застоя мокроты в бронхах.
Продуктивный кашель (ощущается как «влажный», с отхождением мокроты).

В отличие от непродуктивного, этот кашель характеризуется отделением мокроты и обычно возникает на более поздних стадиях заболевания. Как правило, он безболезненный, более частый, иногда с хрипами. Продуктивный кашель помогает очистить бронхи и легкие от скопившейся мокроты.11 Муколитический препарат АЦЦ® помогает разжижать и выводить мокроту.
Непродуктивный кашель (мокрота есть, но не отделяется)
Малопродуктивный кашель (мокроты мало, отделяется плохо)
Продуктивный кашель (мокрота отделяется)
Продолжайте принимать АЦЦ®
Выздоровление
Важно помнить, что продуктивность кашля зависит как от фазы воспалительного процесса, так и от характера заболевания. При заболеваниях верхних дыхательных путей мокрота может не образовываться, и кашель может остаться сухим.
При заболеваниях верхних дыхательных путей мокрота может не образовываться, и кашель может остаться сухим.
Данная рекомендация не заменяет консультацию специалиста.
Лечение кашля
Целью лечения кашля с мокротой является, прежде всего, разжижение мокроты. Чтобы превратить «сухой» непродуктивный кашель в «мокрый» продуктивный, рекомендуется начать прием муколитиков, которые уменьшают вязкость слизи и облегчают ее выведение из дыхательных путей.
Активное вещество препарата АЦЦ® – ацетилцистеин – разжижает вязкую мокроту и повышает эффективность кашля12, способствуя выздоровлению. При простудных заболеваниях, сопровождающихся образованием вязкой мокроты, прием муколитиков рекомендуется начинать в самом начале появления непродуктивного кашля, когда образующуюся мокроту трудно самостоятельно откашлять12.
Чем нас лечат: АЦЦ. Борется с мокротой и парацетамолом
Еще один обзор посвящен сравнению действия двух лекарств, ацетилцистеина и карбоцистеина, против острых инфекций дыхательных путей у детей. Авторы рассмотрели 34 научные работы, посвященные безопасности препаратов, и шесть научных работ, где исследовалась эффективность препарата. В целом ацетилцистеин оказался безопасным для детей старше двух лет. Эффективность препаратов была ограниченной – к седьмому дню лечения кашель явно снижался, но было не совсем понятно, какую роль в этом играет естественное выздоровление. Не самыми убедительными оказались и данные о применении ацетилцистеина при бронхоэктазе (расширении участка бронхов при их поражении).
Авторы рассмотрели 34 научные работы, посвященные безопасности препаратов, и шесть научных работ, где исследовалась эффективность препарата. В целом ацетилцистеин оказался безопасным для детей старше двух лет. Эффективность препаратов была ограниченной – к седьмому дню лечения кашель явно снижался, но было не совсем понятно, какую роль в этом играет естественное выздоровление. Не самыми убедительными оказались и данные о применении ацетилцистеина при бронхоэктазе (расширении участка бронхов при их поражении).
Однако есть множество клинических испытаний, доказывающих пользу ацетилцистеина при хроническом бронхите (но не бронхите с осложнениями). А вот ингаляции с ацетилцистеином от бронхита не помогли. При обструкции легких, как показали многочисленные систематические обзоры рандомизированных двойных слепых сравнительных испытаний, ацетилцистеин способствует отделению мокроты и предотвращает дальнейшие осложнения.
Indicator.Ru рекомендует: применять при комплексном лечении респираторных заболеваний
Эффективность ацетилцистеина – действующего вещества препарата АЦЦ – против сухого кашля подтвердила доказательная медицина. Также ацетилцистеин входит в список незаменимых препаратов с точки зрения Всемирной организации здравоохранения как специфический антидот (противоядие), которое используют при передозировке парацетамолом. При этом от муковисцидоза АЦЦ, скорее всего, не поможет, хотя его и включили в федеральные рекомендации по борьбе с симптомами этого заболевания. Также дело обстоит и с травмами легких.
Также ацетилцистеин входит в список незаменимых препаратов с точки зрения Всемирной организации здравоохранения как специфический антидот (противоядие), которое используют при передозировке парацетамолом. При этом от муковисцидоза АЦЦ, скорее всего, не поможет, хотя его и включили в федеральные рекомендации по борьбе с симптомами этого заболевания. Также дело обстоит и с травмами легких.
Нужно понимать, что несмотря на его эффективность против кашля, АЦЦ самого по себе далеко не всегда достаточно, чтобы справиться с инфекцией – причиной заболевания. Поэтому в случае пневмонии, например, вам понадобятся антибиотики, а для борьбы с другими симптомами – болью, слабостью, повышенной температурой – могут пригодиться жаропонижающие и обезболивающие препараты. Если у вас еще и заложен нос, может потребоваться лекарство от насморка.
Правильно подобрать комбинацию препаратов и решить, нужен ли антибиотик, можно, только поставив верный диагноз. Иногда для этого нужен лабораторный анализ (например, чтобы найти каких-то определенных бактерий), поэтому лучше посетить врача.
Наши рекомендации нельзя приравнивать к назначению врача. Перед тем, как начать принимать тот или иной препарат, обязательно посоветуйтесь со специалистом.
Подписывайтесь на Indicator.Ru в соцсетях: Facebook, ВКонтакте, Twitter, Telegram, Одноклассники.
Ни следа от болезни. Как пережить зиму в Башкирии здоровым и активным | ЗДОРОВЬЕ: Медицина | ЗДОРОВЬЕ
В уходящем 2020 году список респираторных заболеваний и уже привычного гриппа пополнился новым инфекционным COVID-19. Его сложнее лечить, а последствия инфицирования этим коронавирусом для организма серьезнее. UFA.AUF.RU обратился к врачам за советом, какие препараты помогут встретить наступающий год без лишних хлопот о здоровье.
Дыхание – это жизньБороться с обычными симптомами простуды врачи научились давно, температура легко сбивается парацетомолом или ибупрофеном, против насморка есть спреи. Сложнее дела обстоят с кашлем. По статистике, каждый пятый пациент на приеме у терапевта жалуется именно на этот симптом, и примерно у 15% заболевших кашель остается хроническим на протяжении более двух месяцев. Конечно, самолечение может привести к еще более тяжким последствиям, принимать следует только те препараты, которые назначает лечащий врач.
Конечно, самолечение может привести к еще более тяжким последствиям, принимать следует только те препараты, которые назначает лечащий врач.
«Это перспективный препарат с точки зрения клинической практики, – считает доцент кафедры детской оториноларингологии Российской медицинской академии непрерывного профобразования Минздрава России Денис Тулупов. – У карбоцистеина имеется доказательная база, он хорошо переносится пациентами. У препарата интересный механизм действия, особенно при лечении хронических заболеваний».
Восстановительный эффектКарбоцистеин не просто делает мокроту менее вязкой, но активирует защитные ресурсы организма, помогая устранять воспалительные процессы. То есть способствует естественной очистке органов дыхания и снижает риск развития осложнений.
То есть способствует естественной очистке органов дыхания и снижает риск развития осложнений.
По словам Тулупова, «Флуифорт» препятствует проникновению вируса в клетки организма человека, что важно при таких осложнениях как острый вирусный бронхит. Кроме того, препарат снижает вероятность развития бактериальной инфекции за счет уменьшения адгезии бактерий к эпителию дыхательных путей.
«Флуифорт» неспроста выписывают не только на стадии заболевания, но и в период восстановления организма после перенесенной вирусной инфекции. Карбоцистеин, по словам профессора кафедры фтизиатрии и пульмонологии Уральского государственного медицинского университета Игоря Лещенко, обладает противовоспалительным эффектом, то есть способствует восстановлению легких – орган, наиболее подверженный разрушению при коронавирусе.
«Препарат „Флуифорт“ дополнительно обладает антиоксидантными свойствами, то есть снижает уровень так называемого окислительного стресса», – объяснил Лещенко.
Напомним, что при любом заболевании правильный препарат может выбрать только лечащий врач. При этом следует строго следовать инструкции доктора, ведь каждый организм имеет свои индивидуальные особенности, которые зависят в том числе и от возраста.
КомментарийЗаслуженный врач России, доктор медицинских наук, профессор Андрей Зайцев:
«Приём карбоцистеина сопровождается не только улучшением с точки зрения уменьшения мокроты, но регенеративным действием слизистой бронхов. Кроме того, для карбоцистеина зарегистрировано антиоксидантное действие. Всё это позволяет использовать препараты с этим действующим веществом при таких патологиях, как хронический бронхит и хроническая обструктивная болезнь лёгких, а также в ситуациях, когда у пациентов наблюдается постоянный продуктивный кашель, приводящий к частым обострениям».
Лангес: инструкция, цена, аналоги | раствор оральный Сперко Украина
фармакодинамика. Карбоцистеин влияет на гелевую фазу слизи дыхательных путей: путем разрыва дисульфидных мостиков гликопротеинов вызывает разжижение чрезмерно вязкого секрета бронхов, способствует выведению мокроты.
Карбоцистеин влияет на гелевую фазу слизи дыхательных путей: путем разрыва дисульфидных мостиков гликопротеинов вызывает разжижение чрезмерно вязкого секрета бронхов, способствует выведению мокроты.
Мукорегуляторный эффект карбоцистеина связан с активацией сиаловой трансферазы — фермента бокаловидных клеток слизистой оболочки бронхов. Действующее вещество препарата Лангес — карбоцистеин — нормализует количественное соотношение кислых и нейтральных сиаломуцинов бронхиального секрета, восстанавливает его вязкость и эластичность. Активизирует деятельность мерцательного эпителия и улучшает мукоцилиарный клиренс. Способствует регенерации слизистой оболочки дыхательных путей, нормализует ее структуру, уменьшает гиперплазию бокаловидных клеток и, как следствие, уменьшает выработку слизи. Восстанавливает секрецию иммунологически активного IgA (специфическая защита) и количество сульфгидрильных групп компонентов слизи (неспецифическая защита). Проявляет противовоспалительный эффект за счет кининингибирующей активности сиаломуцинов, что приводит к уменьшению отека и бронхообструкции.
Фармакокинетика. После приема внутрь препарат быстро всасывается в ЖКТ. Cmax в плазме крови достигается через 2 ч. Биодоступность карбоцистеина низкая (около 10% принятой дозы) из-за интенсивного метаболизма в ЖКТ и эффекта первого прохождения через печень. T½ составляет около 2 ч. Карбоцистеин и его метаболиты выводятся в основном с мочой.
лечение симптомов нарушений бронхиальной секреции и выведения мокроты, особенно при острых бронхолегочных заболеваниях, например при остром бронхите; при обострениях хронических заболеваний дыхательной системы.
Лангес назначают внутрь. Дозировка препарата в зависимости от возраста пациента приведена в таблице.
| Возраст, лет | Форма выпуска | Дозировка |
|---|---|---|
| 2—5 | Контейнер 60 мл | 2 мл 2 раза в сутки |
| 5—12 | Контейнер 60 мл | 2 мл 3 раза в сутки |
| >15 лет и взрослые | Контейнер 200 мл или пакетики | 15 мл или содержимое 1 пакетика 3 раза в сутки |
Максимальная разовая доза для детей в возрасте до 15 лет не должна превышать 100 мг (2 мл).
Продолжительность лечения не должна превышать 8–10 дней.
Длительность применения карбоцистеина у детей должна быть короткой, не более 5 дней.
Взрослым и детям в возрасте старше 15 лет назначать р-р в контейнерах по 200 мл или в пакетиках, детям в возрасте от 2 до 15 лет — в контейнерах по 60 мл. Для точности дозирования при применении р-ра в контейнерах по 200 мл использовать мерный стаканчик, а в контейнерах по 60 мл — дозирующий шприц.
Дети. Препарат применять у детей в возрасте от 2 лет. Лечение детей следует проводить под наблюдением врача.
повышенная чувствительность к карбоцистеину или каким-либо компонентам препарата (особенно к метилпарагидроксибензоату или другим солям парагидроксибензоата), язвенная болезнь желудка и двенадцатиперстной кишки в фазе обострения.
со стороны пищеварительной системы: нарушения пищеварения, тошнота, рвота, боль в желудке, диарея.
Со стороны ЦНС: головокружение, слабость, недомогание.
Аллергические реакции: в единичных случаях — зуд, крапивница, экзантема, ангионевротический отек (могут быть отдаленными по времени).
В случае возникновения побочных реакций рекомендуется снизить дозу или отменить препарат и обязательно обратиться к врачу.
продуктивный кашель — это фундаментальный механизм защиты бронхолегочной системы и в основном его не следует подавлять. Нерациональной является комбинация лекарственных средств, которые модифицируют бронхиальную секрецию, со средствами, угнетающими кашель (противокашлевыми средствами), и/или веществами, снижающими секрецию (например группа атропина).
Применение муколитических средств (в том числе и карбоцистеина) может привести к нарушению бронхиальной проходимости у новорожденных. У детей первого года жизни возможность очистки дыхательных путей от бронхиального секрета ограничена из-за возрастных анатомо-физиологических особенностей. Любые муколитические средства не следует применять у младенцев.
Лечение необходимо пересмотреть в случае отсутствия эффекта или усиления симптомов заболевания.
Не следует превышать рекомендованные дозы препарата. Необходим тщательный врачебный контроль при выделении гнойной мокроты и высокой температуре тела.
Препарат следует применять с осторожностью у пациентов с язвенной болезнью желудка или двенадцатиперстной кишки в анамнезе.
Лекарственное средство содержит метилпарагидроксибензоат, который может вызвать аллергические реакции (возможно замедленные).
Применение в период беременности или кормления грудью. Применение препарата в I триместр беременности противопоказано. Во II–III триместр беременности или в период кормления грудью препарат применять только под наблюдением врача, если ожидаемая польза для матери превышает потенциальный риск для плода/ребенка.
Способность влиять на скорость реакции при управлении транспортными средствами или другими механизмами. Не влияет.
в период лечения препаратом не следует применять противокашлевые средства и средства, подавляющие бронхиальную секрецию. Повышает эффективность глюкокортикоидной (взаимно) и антибактериальной терапии.
Повышает эффективность глюкокортикоидной (взаимно) и антибактериальной терапии.
при передозировке могут отмечаться боль в желудке, тошнота, диарея. Рекомендуется обратиться к врачу. Лечение симптоматическое.
при температуре не выше 25 °C. Срок годности р-ра после вскрытия контейнера — 12 мес.
Препарат Лангес согласно АТС-классификации относится к препаратам, действующим на респираторную систему, муколитикам. Действующим веществом Лангеса является карбоцистеин. У карбоцистеина в химической структуре содержатся сульфгидрильные группы, которые разрывают дисульфидные связи в слизи и снижают ее вязкость, тем самым происходит выведение мокроты.
Лангес показан для лечения симптомов нарушений бронхиальной секреции и выведения мокроты, особенно при острых бронхолегочных заболеваниях, например при остром бронхите; при обострениях хронических заболеваний дыхательной системы (инструкция МЗ Украины).
Механизм действия, терапевтическое действие
Карбоцистеин (S-карбоксиметилцистеин или S-CMC), обладающий мукоактивными, антиоксидантными и противовоспалительными свойствами, является тиоловым производным аминокислоты L-цистеина. Сегодня доступны препараты для приема внутрь карбоцистеина как в виде S-CMC, так и его соли лизина (S-CMC-lys). Остаток лизина в S-CMC-lys расщепляется в ЖКТ с получением активного лекарственного средства S-CMC. Мукоактивное действие карбоцистеина отличается от такового других тиоловых муколитиков, поскольку он увеличивает содержание сиаломуцина, который влияет на реологические свойства слизи посредством ингибирования кининов. Карбоцистеин также способствует увеличению скорости слизисто-реснитчатого клиренса, особенно у пациентов с хроническим бронхитом, у которых до лечения клиренс медленный.
В доклинических исследованиях было установлено, что карбоцистеин защищает от эмфиземы, вызванной сигаретным дымом у крыс. Лечение S-CMC-Lys больных ХОБЛ в течение 6 мес значительно снизило уровни продукта перекисного окисления липидов 8-изопростана и провоспалительного цитокина IL-6, что указывает на наличие у препарата как антиоксидантных, так и противовоспалительных свойств. Из-за его способности снижать бактериальные нагрузки в дыхательных путях при ХОБЛ было высказано предположение, что карбоцистеин может действовать через ингибирование присоединения патогенных микроорганизмов к клеткам. Это подтверждается исследованиями in vitro, в которых было установлено, что лечение карбоцистеином снижает прилипание Moraxella catarrhalis (бактерии, обычно выявляемые при обострении ХОБЛ) к эпителиальным клеткам глотки как у здоровых людей, так и у пациентов с хроническим бронхитом, по сравнению с группой, получавшей плацебо. Точно так же карбоцистеин может значительно снизить прикрепление Streptococcus pneumoniae к эпителиальным клеткам глотки. Карбоцистеин также может снижать частоту простудных заболеваний и связанных с ними обострений у пациентов с ХОБЛ, что связано с его способностью снижать экспрессию ICAM-1 в дыхательных путях (Rahman I., MacNee W., 2012).
Из-за его способности снижать бактериальные нагрузки в дыхательных путях при ХОБЛ было высказано предположение, что карбоцистеин может действовать через ингибирование присоединения патогенных микроорганизмов к клеткам. Это подтверждается исследованиями in vitro, в которых было установлено, что лечение карбоцистеином снижает прилипание Moraxella catarrhalis (бактерии, обычно выявляемые при обострении ХОБЛ) к эпителиальным клеткам глотки как у здоровых людей, так и у пациентов с хроническим бронхитом, по сравнению с группой, получавшей плацебо. Точно так же карбоцистеин может значительно снизить прикрепление Streptococcus pneumoniae к эпителиальным клеткам глотки. Карбоцистеин также может снижать частоту простудных заболеваний и связанных с ними обострений у пациентов с ХОБЛ, что связано с его способностью снижать экспрессию ICAM-1 в дыхательных путях (Rahman I., MacNee W., 2012).
В результате некоторых исследований было доказано, что карбоцистеин может уменьшить выраженность обострения за счет непосредственного выведения активных форм кислорода и защитить от развития эмфиземы, вызванной экстрактом сигаретного дыма. В исследованиях на животных карбоцистеин продемонстрировал преимущества снижения нагрузки Haemophilus influenzae на дыхательные пути за счет отхаркивающего действия. В других исследованиях также было установлено, что карбоцистеин ингибирует инфекцию риновируса и вируса сезонного гриппа (Zheng Zeng et al., 2017). Показано, что ведущая роль в формировании воспалительного процесса при ХОБЛ принадлежит цитокинам интерлейкина-6 (IL-6) и интерлейкина-8 (IL-8). Установлено, что у пациентов наблюдалось значимое повышение как спонтанной, так и индуцированной продукции IL-6, IL-8 (p<0,05). Индуцированная продукция цитокинов в большей степени отражает резервные возможности иммунокомпетентных клеток в ответ на действие патогенного фактора. С IL6, IL-8 в первую очередь связано формирование нейтрофильного типа воспаления, выражающегося в активации гранулоцитов, прежде всего нейтрофилов, в ответ на токсические (в частности курение) и бактериальные патогены (Трущина Е.Ю. и соавт., 2019).
В исследованиях на животных карбоцистеин продемонстрировал преимущества снижения нагрузки Haemophilus influenzae на дыхательные пути за счет отхаркивающего действия. В других исследованиях также было установлено, что карбоцистеин ингибирует инфекцию риновируса и вируса сезонного гриппа (Zheng Zeng et al., 2017). Показано, что ведущая роль в формировании воспалительного процесса при ХОБЛ принадлежит цитокинам интерлейкина-6 (IL-6) и интерлейкина-8 (IL-8). Установлено, что у пациентов наблюдалось значимое повышение как спонтанной, так и индуцированной продукции IL-6, IL-8 (p<0,05). Индуцированная продукция цитокинов в большей степени отражает резервные возможности иммунокомпетентных клеток в ответ на действие патогенного фактора. С IL6, IL-8 в первую очередь связано формирование нейтрофильного типа воспаления, выражающегося в активации гранулоцитов, прежде всего нейтрофилов, в ответ на токсические (в частности курение) и бактериальные патогены (Трущина Е.Ю. и соавт., 2019).
Актуальность проблемы
ХОБЛ является одной из основных причин заболеваемости и смертности во всем мире и представляет собой одну из наиболее важных проблем общественного здравоохранения. Частые обострения приводят к более быстрому ухудшению функции легких и ухудшению качества жизни, повышению смертности. В результате клинических исследований оценивали влияние муколитиков при ХОБЛ и пришли к выводу, что длительный прием карбоцистеина сочетанно с бронходилататорами, антихолинергическими препаратами и стероидами снижает частоту обострений и улучшает качество жизни пациента (Paone G. et al., 2019).
ХОБЛ, четвертая по значимости причина смерти в мире, является распространенным прогрессирующим излечимым и предотвратимым заболеванием. Согласно исследованиям, проведенным ранее, распространенность ХОБЛ составляла около 7–11%. Распространенность среди мужчин выше, чем у женщин. Характеризуется преимущественно фиксированной обструкцией дыхательных путей посредством различных процессов. Патогенез включает множество компонентов, включая гиперсекрецию слизи, оксидативный стресс и воспаление в дыхательных путях и легких. ХОБЛ оказывает влияние не только на легкие, но и на другие органы. На более позднем этапе прогрессирования болезни у пациентов обычно отмечали уменьшение массы тела, плохой аппетит и депрессию. Болезнь обусловливает возникновение заболеваний сердца легочного происхождения (хроническое легочное сердце — легочная гипертензия вследствие патологии легких и/или гипоксии), легочной энцефалопатии. ХОБЛ приводит ко многим медицинским и финансовым проблемам, поэтому важно разработать соответствующие стратегии по профилактике и лечению ХОБЛ (Zeng Z. еt al., 2017).
Патогенез включает множество компонентов, включая гиперсекрецию слизи, оксидативный стресс и воспаление в дыхательных путях и легких. ХОБЛ оказывает влияние не только на легкие, но и на другие органы. На более позднем этапе прогрессирования болезни у пациентов обычно отмечали уменьшение массы тела, плохой аппетит и депрессию. Болезнь обусловливает возникновение заболеваний сердца легочного происхождения (хроническое легочное сердце — легочная гипертензия вследствие патологии легких и/или гипоксии), легочной энцефалопатии. ХОБЛ приводит ко многим медицинским и финансовым проблемам, поэтому важно разработать соответствующие стратегии по профилактике и лечению ХОБЛ (Zeng Z. еt al., 2017).
Актуальные факты назначений
Карбоцистеин (S-карбоксиметилцистеин или SCMC) — это мукоактивный препарат, который широко применяется в Европе и Азии. Период полураспада карбоцистеина составляет 1,33 ч. Доза карбоцистеина при ХОБЛ различна: от 750 мг 2 р/сут до 4,5 г 1 р/сут. Карбоцистеин оказывает антиоксидантное, противовоспалительное и муколитическое действие. Антиокислительные и противовоспалительные свойства карбоцистеина актуальны для сохранения активности α1-антитрипсина, главная функция которого — защита легких от эластазы, он инактивируется оксидативным стрессом. Инактивация α1-антитрипсина связана с обширным повреждением ткани, которое можно наблюдать при хронической эмфиземе. Антиоксидантное и противовоспалительное действие карбоцистеина может играть важную роль при длительном применении препарата при ХОБЛ.
Антиокислительные и противовоспалительные свойства карбоцистеина актуальны для сохранения активности α1-антитрипсина, главная функция которого — защита легких от эластазы, он инактивируется оксидативным стрессом. Инактивация α1-антитрипсина связана с обширным повреждением ткани, которое можно наблюдать при хронической эмфиземе. Антиоксидантное и противовоспалительное действие карбоцистеина может играть важную роль при длительном применении препарата при ХОБЛ.
Острые инфекции верхних и нижних дыхательных путей являются наиболее частыми инфекциями у детей, в частности у детей школьного возраста — 7–10 раз в год (Chang A. B. et al., 2006; Shields M. D. et al., 2008). Их основной симптом — острый кашель. Кашель может длиться более 10 дней (50% всех заболеваний) и более 3 нед (10% всех заболеваний). Кашель оказывает серьезное влияние на сон ребенка и других членов семьи (Shields M.D. et al., 2008). Конечно же, изначально необходимо выяснить причину кашля и начать этиотропную терапию, которая направлена на устранение причины возникновения заболевания. Из муколитических препаратов, доступных для лечения, производные цистеина (это ацетилцистеин и карбоцистеин) наиболее часто назначаются во многих европейских (Duijvestijn Y.C. et al., 1997; Chalumeau M. et al., 2000; Sen E.F. et al., 2011; Cano Garcinuño A. et al., 2013), африканских странах (Mourdi N. et al., 2010 ) и в Бразилии (Bricks L.F. et al., 1996). Доступны различные системные (пероральные, в/м или в/в) или ингаляционные формы лекарственных средств. Например, в Нидерландах 30% врачей общей практики назначают ацетилцистеин при астматическом бронхите, остром бронхите или продуктивном или сухом кашле (Duijvestijn Y.C. et al., 1997; Sen E.F. et al., 2011). Во Франции в результате 3 исследований было зафиксировано, что ацетилцистеин и карбоцистеин являются одними из наиболее рекомендуемых препаратов для детей, особенно для детей в возрасте младше 2 лет (Collet J.P. et al., 1991; Chalumeau M. et al., 2000; Horen B., 2002). В одном из этих исследований доля производных цистеина составила 18–25% назначений лекарств для лечения острого ринофарингита, острого кашля и острого бронхита (Chalumeau M.
Из муколитических препаратов, доступных для лечения, производные цистеина (это ацетилцистеин и карбоцистеин) наиболее часто назначаются во многих европейских (Duijvestijn Y.C. et al., 1997; Chalumeau M. et al., 2000; Sen E.F. et al., 2011; Cano Garcinuño A. et al., 2013), африканских странах (Mourdi N. et al., 2010 ) и в Бразилии (Bricks L.F. et al., 1996). Доступны различные системные (пероральные, в/м или в/в) или ингаляционные формы лекарственных средств. Например, в Нидерландах 30% врачей общей практики назначают ацетилцистеин при астматическом бронхите, остром бронхите или продуктивном или сухом кашле (Duijvestijn Y.C. et al., 1997; Sen E.F. et al., 2011). Во Франции в результате 3 исследований было зафиксировано, что ацетилцистеин и карбоцистеин являются одними из наиболее рекомендуемых препаратов для детей, особенно для детей в возрасте младше 2 лет (Collet J.P. et al., 1991; Chalumeau M. et al., 2000; Horen B., 2002). В одном из этих исследований доля производных цистеина составила 18–25% назначений лекарств для лечения острого ринофарингита, острого кашля и острого бронхита (Chalumeau M. et al., 2000). Установлено, что высокий показатель назначения производных цистеина для лечения острой инфекции верхних и нижних дыхательных путей у детей в последние десятилетия не изменился во Франции (Halna M. et al., 2005). В Италии карбоцистеин является одним из 20 препаратов, которые чаще всего назначают семейные врачи и педиатры (Cazzato N. et al., 2001; Sen E.F. et al., 2011). В Испании муколитики — это препараты, которые чаще всего назначают педиатры и врачи общей практики для лечения острого бронхита, и они являются второй наиболее распространенной фармакологической группой, назначаемой детям в возрасте до 2 лет (Sanz E.J. et al., 1988; Cano Garcinuño A. et al., 2013). В Германии ацетилцистеин входит в пятерку препаратов, назначаемых педиатрическим пациентам в возрасте до 1 года (Bücheler R. et al., 2002; Chalumeau M., Duijvestijn Y.C., 2013).
et al., 2000). Установлено, что высокий показатель назначения производных цистеина для лечения острой инфекции верхних и нижних дыхательных путей у детей в последние десятилетия не изменился во Франции (Halna M. et al., 2005). В Италии карбоцистеин является одним из 20 препаратов, которые чаще всего назначают семейные врачи и педиатры (Cazzato N. et al., 2001; Sen E.F. et al., 2011). В Испании муколитики — это препараты, которые чаще всего назначают педиатры и врачи общей практики для лечения острого бронхита, и они являются второй наиболее распространенной фармакологической группой, назначаемой детям в возрасте до 2 лет (Sanz E.J. et al., 1988; Cano Garcinuño A. et al., 2013). В Германии ацетилцистеин входит в пятерку препаратов, назначаемых педиатрическим пациентам в возрасте до 1 года (Bücheler R. et al., 2002; Chalumeau M., Duijvestijn Y.C., 2013).
В нашей же стране карбоцистеин в составе препарата Лангес назначают детям в возрасте старше 2 лет. При этом кратность дозирования препарата отличается для детей разных возрастных групп: детям в возрасте 2–5 лет — по 2 мл 2 р/сут; в возрасте 5–12 лет по 2 мл 3 р/сут (инструкция МЗ Украины).
А это интересно
Одним из наиболее интересных классов мукоактивных средств являются препараты на основе карбоцистеина, регулирующие выработку секрета железистыми клетками (мукорегуляторы), действующие непосредственно на железистую клетку и нормализующие ее секреторную функцию независимо от исходного состояния. Добавление лизина к молекуле карбоцистеина (флуифорт) улучшает переносимость препарата, так как повышается его pH и, следовательно, минимизируются нежелательные явления со стороны ЖКТ. Исходя из результатов проведенного исследования, можно сделать вывод, что применение препарата карбоцистеина лизиновой соли (флуифорт) в терапии экссудативного среднего отита у детей с рецидивирующим и хроническим аденоидитом является более эффективным методом лечения по сравнению с выжидательной тактикой, что согласуется с имеющимися данными литературы. Применение препарата карбоцистеина лизиновой соли в комбинации с назальным спреем мометазона фуроата позволяет достичь более быстрого купирования симптомов аденоидита и значительно ускоряет разрешение экссудативного среднего отита по сравнению с монотерапевтическим подходом. Применение препарата карбоцистеина лизиновой соли является безопасным методом лечения, имеющим крайне низкий риск развития нежелательных побочных эффектов (Карпова Е.П. и соавт., 2018).
Применение препарата карбоцистеина лизиновой соли является безопасным методом лечения, имеющим крайне низкий риск развития нежелательных побочных эффектов (Карпова Е.П. и соавт., 2018).
Заключение
Карбоцистеин признан эффективным и безопасным лекарственным средством для длительного лечения ХОБЛ, способным снизить частоту обострений и улучшить качество жизни пациентов. Кроме того, карбоцистеин является эффективным в противодействии некоторым симптомам, связанным с раковой кахексией. В результате доклинических и клинических исследований при подтверждении его терапевтической эффективности было установлено, что антиоксидантные и противовоспалительные свойства карбоцистеина являются более важными, чем сам муколиз. Поэтому карбоцистеин может быть способен предотвратить оксидативный стресс, связанный с некоторыми хроническими воспалительными заболеваниями, такими как сердечно-сосудистые заболевания и нейродегенеративные нарушения. Требуются контролируемые рандомизированные исследования на людях (Macciò A. et al., 2009).
et al., 2009).
Горло свело | Статьи | Известия
— Относиться к кашлю нужно осторожно, — советует Владимир Ноников, известный пульмонолог, профессор и заведующий кафедрой терапии лечебного факультета МГУ. — За этим симптомом могут скрываться серьезные заболевания. Лечить кашель самостоятельно можно только при легкой простуде. В остальных случаях лучше обратиться к врачу, чтобы не пропустить какую-то более опасную болезнь. Справиться с кашлем даже при банальной простуде совсем непросто. И прежде чем заглотнуть какую-нибудь пилюлю, нужно определить природу этого симптома: разные виды кашля лечатся по-разному. Медики выделяют два основных вида кашля: продуктивный и непродуктивный. Под «продуктом» они подразумевают мокроту, которая образуется в воспаленных бронхах и трахее. Наш организм воспринимает этот «продукт» как инородное тело и спешит от него избавиться… с помощью кашля. Как это происходит? Кашель можно сравнить с взрывной волной или ураганом: с бешеной скорость воздух проносится по дыхательным путям, сметая все на своем пути, в том числе и мокроту. Но нередко она бывает столь густой, что «сдуть» ее с поверхности бронхов бывает непросто. И в таких случаях мы долго и натужно кашляем, пытаясь избавиться от нее. Тут могут помочь лекарства, которые делают мокроту более жидкой — так она легче изгоняется взрывной волной, вызванной кашлем. Освобождение бронхов и трахеи от мокроты очень важно. Этот «продукт» служит хорошей пищей для бактерий. Когда его скапливается много, бактерии очень активно плодятся на таком корме, и болезнь прогрессирует. Сделать «продукт» более жидким помогают препараты, содержащие в качестве активных компонентов бромгексин, амброксол, ацетилцистеин и карбоцистеин. Они выпускаются под самыми разными названиями (см. таблицу). Кроме них, есть масса препаратов, сделанных из термопсиса, алтея, подорожника, истода и других лечебных трав. Из них делают мукалтин, таблетки от кашля, глицирам и массу микстур, сиропов и грудных сборов. Неплохо помогают ингаляции даже обычным теплым паром. Но еще лучше сделать ингаляции с бронхикумом, эвкабалом, ментокларом и прочими препаратами, содержащими эфирные масла эвкалипта, аниса, хвойных деревьев, тимьяна и других лекарственных растений.
Но нередко она бывает столь густой, что «сдуть» ее с поверхности бронхов бывает непросто. И в таких случаях мы долго и натужно кашляем, пытаясь избавиться от нее. Тут могут помочь лекарства, которые делают мокроту более жидкой — так она легче изгоняется взрывной волной, вызванной кашлем. Освобождение бронхов и трахеи от мокроты очень важно. Этот «продукт» служит хорошей пищей для бактерий. Когда его скапливается много, бактерии очень активно плодятся на таком корме, и болезнь прогрессирует. Сделать «продукт» более жидким помогают препараты, содержащие в качестве активных компонентов бромгексин, амброксол, ацетилцистеин и карбоцистеин. Они выпускаются под самыми разными названиями (см. таблицу). Кроме них, есть масса препаратов, сделанных из термопсиса, алтея, подорожника, истода и других лечебных трав. Из них делают мукалтин, таблетки от кашля, глицирам и массу микстур, сиропов и грудных сборов. Неплохо помогают ингаляции даже обычным теплым паром. Но еще лучше сделать ингаляции с бронхикумом, эвкабалом, ментокларом и прочими препаратами, содержащими эфирные масла эвкалипта, аниса, хвойных деревьев, тимьяна и других лекарственных растений. Непродуктивный кашель похож на самообман: «продукта» в дыхательных путях нет, но организму кажется, что он есть. В результате мы натужно кашляем впустую. Обман возникает из-за того, что кашлевые рецепторы возбуждаются не инородным телом, а воспалением. Чаще всего это бывает при поражении глотки, которое обычно встречается при ОРВИ (острой респираторной вирусной инфекции). Разжижать мокроту при таком кашле бессмысленно — ее нет. Поэтому лечить его надо теми средствами, которые угнетают кашлевой центр в головном мозге или успокаивают воспаленные рецепторы в глотке. В мозгу лучше работают декстрометорфан и кодеин. Но поскольку эти вещества относятся к наркотикам, лекарства с ними лучше использовать как можно реже. Даже несмотря на то что многие из них продаются без рецепта. Несколько слабее подавляют кашлевой центр препараты с бутамиратом, глауцином и окселадинолом. Но поскольку они не являются наркотиками, лучше пользоваться ими. При сухом кашле могут помочь и препараты, успокаивающие кашлевые рецепторы в глотке, — либексин, фалиминт и многочисленные спреи, леденцы и пастилки с ментолом и эфирными маслами.
Непродуктивный кашель похож на самообман: «продукта» в дыхательных путях нет, но организму кажется, что он есть. В результате мы натужно кашляем впустую. Обман возникает из-за того, что кашлевые рецепторы возбуждаются не инородным телом, а воспалением. Чаще всего это бывает при поражении глотки, которое обычно встречается при ОРВИ (острой респираторной вирусной инфекции). Разжижать мокроту при таком кашле бессмысленно — ее нет. Поэтому лечить его надо теми средствами, которые угнетают кашлевой центр в головном мозге или успокаивают воспаленные рецепторы в глотке. В мозгу лучше работают декстрометорфан и кодеин. Но поскольку эти вещества относятся к наркотикам, лекарства с ними лучше использовать как можно реже. Даже несмотря на то что многие из них продаются без рецепта. Несколько слабее подавляют кашлевой центр препараты с бутамиратом, глауцином и окселадинолом. Но поскольку они не являются наркотиками, лучше пользоваться ими. При сухом кашле могут помочь и препараты, успокаивающие кашлевые рецепторы в глотке, — либексин, фалиминт и многочисленные спреи, леденцы и пастилки с ментолом и эфирными маслами. В числе средств, продающихся без рецепта, есть группа препаратов, пытающихся совместить несовместимое: одни их компоненты делают мокроту жидкой, другие же, подавляя кашлевой рефлекс, мешают ее эвакуации из дыхательных путей. Чем грозит скопление мокроты, вы уже читали выше. «Комбинации таких средств научно не обоснованы», — считают известные английские фармакологи Дж. Лоуренс и Питер Бенитт. И к их словам могут присоединиться большинство врачей, вынужденных гасить кашель такими «парадоксальными» лекарствами. Кстати Вот несколько ситуаций, при которых профессор Владимир Ноников настоятельно советует не заниматься самолечением, а обязательно обратиться к врачу, чтобы не пропустить какую-то более опасную болезнь: — Мокрота становится желтовато-зеленой, это часто бывает при пневмонии или серьезном воспалении органов дыхания. — Количество мокроты увеличивается, и ее становится много. Это признак серьезного воспалительного процесса в дыхательных путях. — Появляется кровь в мокроте. Даже при минимальной примеси крови надо обратиться к врачу.
В числе средств, продающихся без рецепта, есть группа препаратов, пытающихся совместить несовместимое: одни их компоненты делают мокроту жидкой, другие же, подавляя кашлевой рефлекс, мешают ее эвакуации из дыхательных путей. Чем грозит скопление мокроты, вы уже читали выше. «Комбинации таких средств научно не обоснованы», — считают известные английские фармакологи Дж. Лоуренс и Питер Бенитт. И к их словам могут присоединиться большинство врачей, вынужденных гасить кашель такими «парадоксальными» лекарствами. Кстати Вот несколько ситуаций, при которых профессор Владимир Ноников настоятельно советует не заниматься самолечением, а обязательно обратиться к врачу, чтобы не пропустить какую-то более опасную болезнь: — Мокрота становится желтовато-зеленой, это часто бывает при пневмонии или серьезном воспалении органов дыхания. — Количество мокроты увеличивается, и ее становится много. Это признак серьезного воспалительного процесса в дыхательных путях. — Появляется кровь в мокроте. Даже при минимальной примеси крови надо обратиться к врачу. — При сухом и длительном кашле, даже если отсутствуют какие-либо другие симптомы, и вы чувствуете себя удовлетворительно. — При приступах сухого кашля, сопровождающихся затруднением дыхания. Больные в такой ситуации не могут сделать вдох, у них возникает «как будто заслонка в груди». Иногда во время приступа они даже теряют сознание. Это типичные признаки трахеобронхиальной дискинезии, при которой стенки трахеи или бронхов спадаются и их просвет становится очень узким. Чаще всего это бывает после парагриппа и микоплазменной инфекции. Таблица Препараты, помогающие откашливать мокроту Препараты с ацетилцистеином (АЦЦ, экзомюк), карбоцистеином (флюдитек, дрилл отхаркивающий, мукодин, мукопронт, флювик), амброксолом (амброксол, амбробене, амброгексал, амбролан, бронховерн, лазолван, медовент, халиксол), бромгексином (бромгексин, бронхотил, паксиразол, солвин, флегамин) Фитопрепараты, сделанные из термопсиса, алтея, подорожника, истода, плюща и других лечебных трав — мукалтин, таблетки от кашля, глицирам, геделикс и множество различных микстур, сиропов и грудных сборов Препараты, содержащие гвайфенезин (колдрекс бронхо, туссин, робитуссин от кашля) Препараты для ингаляций, содержащие эфирные масла эвкалипта, хвойных деревьев, тимьяна и других лекарственных растений — эвкабал, бронхикум, ментоклар и др.
— При сухом и длительном кашле, даже если отсутствуют какие-либо другие симптомы, и вы чувствуете себя удовлетворительно. — При приступах сухого кашля, сопровождающихся затруднением дыхания. Больные в такой ситуации не могут сделать вдох, у них возникает «как будто заслонка в груди». Иногда во время приступа они даже теряют сознание. Это типичные признаки трахеобронхиальной дискинезии, при которой стенки трахеи или бронхов спадаются и их просвет становится очень узким. Чаще всего это бывает после парагриппа и микоплазменной инфекции. Таблица Препараты, помогающие откашливать мокроту Препараты с ацетилцистеином (АЦЦ, экзомюк), карбоцистеином (флюдитек, дрилл отхаркивающий, мукодин, мукопронт, флювик), амброксолом (амброксол, амбробене, амброгексал, амбролан, бронховерн, лазолван, медовент, халиксол), бромгексином (бромгексин, бронхотил, паксиразол, солвин, флегамин) Фитопрепараты, сделанные из термопсиса, алтея, подорожника, истода, плюща и других лечебных трав — мукалтин, таблетки от кашля, глицирам, геделикс и множество различных микстур, сиропов и грудных сборов Препараты, содержащие гвайфенезин (колдрекс бронхо, туссин, робитуссин от кашля) Препараты для ингаляций, содержащие эфирные масла эвкалипта, хвойных деревьев, тимьяна и других лекарственных растений — эвкабал, бронхикум, ментоклар и др. Препараты, угнетающие кашлевой центр в головном мозге Препараты с бутамиратом (синекод), с глауцином (глаувент, тусидил), с окселадином (тусупрекс, пакселадин) Препараты, угнетающие кашлевые рецепторы Препараты с феноксдиазином (либексин), фалиминт и многочисленные спреи, леденцы и пастилки с ментолом и эфирными маслами Комбинированные препараты, сочетающие в себе отхаркивающие компоненты с противокашевыми Туссин плюс и гликодин — содержат наркотический декстрометорфан
Неокодион, терпинкод и коделак — содержат наркотический кодеин
Стоптуссин — содержит ненаркотический бутамират в комплексе с гвайфенезином
Препараты, угнетающие кашлевой центр в головном мозге Препараты с бутамиратом (синекод), с глауцином (глаувент, тусидил), с окселадином (тусупрекс, пакселадин) Препараты, угнетающие кашлевые рецепторы Препараты с феноксдиазином (либексин), фалиминт и многочисленные спреи, леденцы и пастилки с ментолом и эфирными маслами Комбинированные препараты, сочетающие в себе отхаркивающие компоненты с противокашевыми Туссин плюс и гликодин — содержат наркотический декстрометорфан
Неокодион, терпинкод и коделак — содержат наркотический кодеин
Стоптуссин — содержит ненаркотический бутамират в комплексе с гвайфенезином
какие бывают и как действуют?
Помимо коронавируса, нас донимают еще и ОРВИ с гриппом – с их невыносимыми симптомами в виде ринита, боли в горле и, конечно же, кашлем. Естественно, категория препаратов для лечения кашля растет.
Тут у нас есть хорошие новости для пациентов, чей кашель не связан с Covid-19: скоро появятся на рынке новые таблетки от хронического кашля. Производителю лекарства, компании Merck, осталось только завершить последние исследования. Пока же, в ожидании инновационного препарата от хронического кашля, пересмотрим, чем лечить острый и хронический кашель сейчас. Ведь часто фармопека обычно сводится к вопросу: «Кашель сухой или мокрый?», на основе ответа на который и отпускается определенный препарат. При этом далеко не всегда посетитель может правильно расценить характер кашля (сухой или влажный) и к тому же этот подход несколько устарел. Как понять, какое лекарство от кашля порекомендовать?
Производителю лекарства, компании Merck, осталось только завершить последние исследования. Пока же, в ожидании инновационного препарата от хронического кашля, пересмотрим, чем лечить острый и хронический кашель сейчас. Ведь часто фармопека обычно сводится к вопросу: «Кашель сухой или мокрый?», на основе ответа на который и отпускается определенный препарат. При этом далеко не всегда посетитель может правильно расценить характер кашля (сухой или влажный) и к тому же этот подход несколько устарел. Как понять, какое лекарство от кашля порекомендовать?
Так «мокрый» или «сухой»?
Деление кашля на мокрый (продуктивный) и сухой (непродуктивный) – краеугольный камень назначения препаратов от кашля. Фармацевты всего мира получали образование в соответствии с этой парадигмой в течение многих десятилетий, однако такой подход к лечению кашля предназначался скорее для контроля таких заболеваний, как туберкулез, которые сопровождались значительным выделением бронхиальной слизи.
В наше время эта парадигма, как считают специалисты, привела к путанице, несмотря на кажущуюся простоту: больным трудно понять, какой ОТС-препарат является для них наиболее подходящим. К тому же, по мнению ряда международных экспертов, есть небольшое различие между симптомом «сухой кашель» и «кашель, который производит минимальное количество мокроты». Так что признанная классификация кашля – его деление на «сухой» или «мокрый» – на сегодня устарела, в наши дни разрабатывается новая модель классификации подвидов этого симптома.
К тому же, по мнению ряда международных экспертов, есть небольшое различие между симптомом «сухой кашель» и «кашель, который производит минимальное количество мокроты». Так что признанная классификация кашля – его деление на «сухой» или «мокрый» – на сегодня устарела, в наши дни разрабатывается новая модель классификации подвидов этого симптома.
Новая парадигма
Более правильно (и намного безопаснее!) рекомендовать препараты «для кашля», чем «от кашля». Да и пульмонологи считают, что более глубокое понимание физиологии кашля должно привести к переоценке классификации лекарственных средств для контроля этого распространенного симптома. По сути, все средства, направленные на устранение или облегчения этого симптомов можно разделить на препараты «для кашля», то есть те, что увеличивают секрецию слизи, и препараты «от кашля», призванные снизить частоту изнурительных приступов (как правило, ночью). Первые необходимы, когда мокроты мало, и нужно увеличить ее количество или же она присутствует, но слишком густая, поэтому необходимо облегчить ее отхождение. Вторые уже необходимы при частом мучительном кашле, который нарушает общее самочувствие, сказывается на продолжительности и качестве сна больного.
Вторые уже необходимы при частом мучительном кашле, который нарушает общее самочувствие, сказывается на продолжительности и качестве сна больного.
Основной задачей при остром кашле является уже не увеличить нормальное количество мокроты, а нормализовать кашлевой рефлекс, а также снизить проявление этого симптома в ночное время. И при рассмотрении существующих методов лечения кашля отмечается «значительная неудовлетворенная клиническая потребность». Хотя понимание кашлевого рефлекса и факторов, приводящих к повышенной чувствительности кашлевого центра, увеличилось, особенно за последнее десятилетие, эта информация лишь недавно начала использоваться для разработки новых препаратов от кашля. Однако их ожидает еще этап хорошо спланированных клинических исследований и одобрение регуляторов. Пока что фармацевтам приходится довольствоваться имеющимися в аптечном ассортименте таблетками и сиропами. И ставить правильные вопросы:
- Если просят дать что-нибудь от кашля, выясните, не болит ли горло, нет ли осиплости, першения в горле.
 Если ответ утвердительный, нужны не препараты «от кашля», а антисептики, смягчающие и противовоспалительные средства для горла, например, те же леденцы.
Если ответ утвердительный, нужны не препараты «от кашля», а антисептики, смягчающие и противовоспалительные средства для горла, например, те же леденцы. - Если вы рекомендуете посетителю средства на основе карбоцистеина или ацетилцистеина, спросите, нет ли у больного язвенной болезни.
- Противокашлевые средства для детей отпускайте только по назначению врача! Не берите на себя ответственность и не рекомендуйте ничего от кашля детям до 6 лет.
- Пожилым людям, учитывая противопоказания и риск полипрагмазии, лучше рекомендовать препараты из группы отхаркивающих средств на растительной основе.
Изнуряющий кашель: укрощая симптом
Уменьшают дискомфорт при кашле две группы препаратов, воздействующие на объем и качество мокроты.
- 1. Отхаркивающие средства. Они раздражают слизистую оболочку желудка и рефлекторно повышают секрецию слизи в бронхах. Это увеличивает объем мокроты и уменьшает ее вязкость. Она раздражает рецепторы слизистой нижних дыхательных путей, активизируется работа ресничек, и вот мокрота уже пошла наружу, куда ей и дорога.
 По такому принципу действуют средства на основе растительных экстрактов (тимьяна, плюща, аниса, мать-и-мачехи, подорожника, солодки и др.), например, Геделикс, Бронхикум, Линкас. Внимание! Детям младшего возраста опасно использовать эти препараты, так как они увеличивают объем мокроты, а их дыхательная мускулатура еще недостаточно развита, поэтому ребенок не сможет все откашлять. Тем временем, в сгустке мокроты размножаются болезнетворные бактерии.
По такому принципу действуют средства на основе растительных экстрактов (тимьяна, плюща, аниса, мать-и-мачехи, подорожника, солодки и др.), например, Геделикс, Бронхикум, Линкас. Внимание! Детям младшего возраста опасно использовать эти препараты, так как они увеличивают объем мокроты, а их дыхательная мускулатура еще недостаточно развита, поэтому ребенок не сможет все откашлять. Тем временем, в сгустке мокроты размножаются болезнетворные бактерии. - 2. Муколитики. Эта группа препаратов изменяет уже качество мокроты: отделяемое разжижается и легче откашливается. К муколитикам относятся препараты на основе амброксола, снижающие вязкость мокроты и благоприятно воздействующие на нижний отдел дыхательных путей. В эту группу входят также препараты на основе ацетилцистеина, разжижающие мокроту, а также снижающие прилипание адгезию к слизистой оболочке дыхательных путей. Но они имеют серьезный недостаток – снижают активность некоторых антибиотиков (пенициллинов, тетрациклинов), поэтому промежуток между приемом таких средств должен составлять не менее 2 часов.
 К тому же препараты на основе ацетилцистеина способны усиливать бронхоспазм, поэтому часто врачи выписывают их вместе с бронхолитиками. Также учтите, что и карбоцистеин, и ацетилцистеин противопоказаны при язвенной болезни желудка (в стадии обострения).
К тому же препараты на основе ацетилцистеина способны усиливать бронхоспазм, поэтому часто врачи выписывают их вместе с бронхолитиками. Также учтите, что и карбоцистеин, и ацетилцистеин противопоказаны при язвенной болезни желудка (в стадии обострения).
Категория препаратов «от кашля»
Выбор средств из группы «от кашля» несколько уже. Это препараты центрального действия, которые влияют непосредственно на кашлевой центр, уменьшая его возбудимость и, соответственно, частоту симптома. Формулы таких лекарств могут дополняться растительными компонентами.
Их альтернатива – препараты периферического действия, оказывающие локальное анестезирующее действие на слизистую оболочку дыхательных путей, тем самым снижая чувствительность местных рецепторов к различным факторам, провоцирующим кашель. Некоторые из них дополнительно уменьшают воспаление и проявляют спазмолитический эффект.
Профиль безопасности и эффективности муколитиков/антиоксидантов при хронической обструктивной болезни легких: сравнительный анализ эрдостеина, карбоцистеина и N-ацетилцистеина | Респираторные исследования
Стратегия поиска
Этот метаанализ был зарегистрирован в международной базе данных проспективно зарегистрированных систематических обзоров (регистрационный номер PROSPERO: CRD42016053762) и выполнен в соответствии с PRISMA-P [11] с представленной блок-схемой на рис. 1А. Этот количественный синтез удовлетворил всем рекомендуемым пунктам, указанным в контрольном списке PRISMA-P [11].
1А. Этот количественный синтез удовлетворил всем рекомендуемым пунктам, указанным в контрольном списке PRISMA-P [11].
Блок-схема PRISMA для идентификации исследований, включенных в метаанализ ( a ), и диаграмма, отображающая сеть по видам лечения; связи между узлами указывают на прямое сравнение между парами обработок; числа, показанные вдоль линий связи, указывают на количество пациентов, сравнивающих пары методов лечения в прямом порядке ( b )
Два обозревателя провели всесторонний литературный поиск РКИ, оценивающих влияние муколитических и антиоксидантных препаратов на пациентов с ХОБЛ.Структура PICO (проблема пациента, вмешательство, сравнение и результат) использовалась для разработки стратегии поиска литературы, как описано ранее [12]. А именно, «Проблема пациента» включала субъекта, страдающего ХОБЛ; «Вмешательство» касалось введения муколитических и антиоксидантных средств; «Сравнение» проводилось в отношении плацебо и каждого активного лечения; «Исходами» были продолжительность обострения ХОБЛ, госпитализации из-за обострения ХОБЛ и нежелательные явления (НЯ).
Поиск по терминам «эрдостеин» ИЛИ «карбоцистеин» ИЛИ «NAC» И «ХОБЛ» И «клиническое исследование» был проведен в Кокрановском центральном регистре контролируемых исследований (CENTRAL), MEDLINE, Embase, Scopus, Web of Science, ClinicalTrials.gov и базы данных Регистра клинических испытаний ЕС, чтобы предоставить соответствующие исследования, доступные до 26 ноября 2018 г. Никаких языковых ограничений не применялось. Был использован следующий перевод запроса: «((«эрдостеин» [дополнительная концепция] ИЛИ «эрдостеин» [все поля]) ИЛИ («карбоцистеин» [термины MeSH] ИЛИ «карбоцистеин» [все поля]) ИЛИ («ацетилцистеин»[ Термины MeSH] ИЛИ «ацетилцистеин» [Все поля] ИЛИ «н-ацетилцистеин» [Все поля])) И («легочное заболевание, хроническая обструктивная» [Термины MeSH] ИЛИ («легочное» [Все поля] И «заболевание» [Все поля Поля] И «хронический» [Все поля] И «обструктивный» [Все поля]) ИЛИ «хроническая обструктивная болезнь легких» [Все поля] ИЛИ «ХОБЛ» [Все поля]) И Клинические испытания [ptyp]».
Цитаты из ранее опубликованных мета-анализов и соответствующих обзоров были изучены для определения дальнейших соответствующих исследований, если таковые имеются [3, 5, 13,14,15].
Выбор исследования
В этот метаанализ были включены опубликованные РКИ с участием пациентов с ХОБЛ, получавших пероральные препараты эрдостеина в дозе 600 мг/сутки, карбоцистеина 1500 мг/сутки и NAC 1200 мг/сутки в течение более 6 месяцев.
Два обозревателя независимо друг от друга проверили релевантные исследования, найденные в результате поиска литературы, полученной из уже упомянутых баз данных.Исследования были отобраны в соответствии с вышеупомянутыми критериями, и любые разногласия во мнениях о приемлемости разрешались на основе общего консенсуса.
Конечные точки
Первичной конечной точкой этого мета-анализа было влияние эрдостеина 600 мг/сут, карбоцистеина 1500 мг/сут и NAC 1200 мг/сут на снижение риска обострения ХОБЛ по сравнению с плацебо и для каждого активное лечение.
Вторичными конечными точками были влияние эрдостеина в дозе 600 мг/сут, карбоцистеина 1500 мг/сут и NAC 1200 мг/сут на риск возникновения, по крайней мере, обострения ХОБЛ, продолжительность обострения ХОБЛ и риск госпитализации по поводу обострения ХОБЛ. , по сравнению с плацебо.Частота НЯ была еще одной вторичной конечной точкой.
Оценка качества, риск систематической ошибки и профиль доказательств
Шкала Джадада со шкалой от 1 до 5 (5 баллов — наилучшее качество) использовалась для оценки качества РКИ в отношении вероятности систематической ошибки, связанной с рандомизация, двойное ослепление, изъятие и выбывание [16]. Оценка Jadad ≥ 3 была определена для определения высокого качества исследований. Два рецензента независимо друг от друга оценивали качество отдельных исследований, и любые расхождения во мнениях относительно показателя качества разрешались на основе консенсуса.
В попарном метаанализе уровни гетерогенности между исследованиями от умеренного до высокого рассматривались для I 2 > 50%; риск систематической ошибки публикации оценивался для первичных конечных точек с помощью воронкообразного графика и теста Эггера, как описано ранее [16]. Свидетельство асимметрии по тесту Эггера считалось значимым при P < 0,1, и было представлено графическое представление 90% доверительных полос [16]. Риск систематической ошибки в сетевом метаанализе был проверен с помощью анализа согласованности/несогласованности, чтобы оценить, адекватно ли результаты, полученные в результате использования моделей согласованности и несогласованности, соответствуют линии равенства, как описано ранее [5].
Свидетельство асимметрии по тесту Эггера считалось значимым при P < 0,1, и было представлено графическое представление 90% доверительных полос [16]. Риск систематической ошибки в сетевом метаанализе был проверен с помощью анализа согласованности/несогласованности, чтобы оценить, адекватно ли результаты, полученные в результате использования моделей согласованности и несогласованности, соответствуют линии равенства, как описано ранее [5].
Качество доказательств было оценено для первичной конечной точки в соответствии с системой классификации рекомендаций, разработки и оценки (GRADE), где ++++ соответствует высокому качеству доказательств, +++ — среднему качеству доказательств. , ++ для низкого качества доказательств и + для очень низкого качества доказательств [17].
Извлечение данных
Данные из включенных РКИ были извлечены и проверены на предмет характеристик и продолжительности исследования, включенных пациентов, препаратов и суточных доз, характеристик заболевания, определения обострения ХОБЛ, истории и частоты обострений ХОБЛ, возраста, пола, привычки курения, функции легких, и оценка Джадада. Из-за сложности этого метаанализа данные были извлечены в соответствии с рекомендациями DECiMAL [18].
Из-за сложности этого метаанализа данные были извлечены в соответствии с рекомендациями DECiMAL [18].
Анализ данных
Был проведен попарный метаанализ для количественной оценки влияния эрдостеина в дозе 600 мг/сут, карбоцистеина 1500 мг/сут и NAC 1200 мг/сут на первичные и вторичные конечные точки по сравнению с плацебо.
Продолжительность наблюдения могла быть непостоянной в РКИ, включенных в этот метаанализ. Поэтому данные, касающиеся оценки риска, нормированы как функция человеко-времени (а именно человеко-сезон), где один сезон длится три месяца [19].Этот метод включает преобразование мер в общую метрику (события на человека-время) перед метаанализом данных, что приводит к повышению оценки эффекта, точности и клинической интерпретируемости результатов [20, 21]. В частности, числитель представляет общее количество событий, а знаменатель представляет заданную продолжительность времени, умноженную на количество пациентов [22]. Такой метод был поддержан Cochrane Collaboration и успешно использовался в недавних мета-анализах [20, 21, 23, 24].
Результаты попарного метаанализа выражены в виде относительного риска (RR) или разности средних (MD) и 95% доверительного интервала (95% CI). Поскольку данные были отобраны из серии исследований, проведенных исследователями, работающими независимо, и невозможно предположить общую величину эффекта, была использована модель бинарных случайных эффектов, чтобы сбалансировать веса исследования и адекватно оценить 95% ДИ среднего распределения влияние препаратов на исследуемые переменные [16].
Также был проведен сетевой метаанализ для сравнения исследуемых препаратов с точки зрения первичной конечной точки и ранжирования их эффективности в снижении риска обострения ХОБЛ.Сетевой метаанализ был проведен путем включения исключительно высококачественных РКИ, которые не вносили ни гетерогенности, ни систематической ошибки в оценку общего эффекта первичной конечной точки. Поскольку неоднородность и предвзятость могут распространяться через сеть РКИ и, таким образом, по-разному влиять на оценки в разных регионах сети, этот подход позволил выявить те исследования, которые могут изменить правильные результаты сетевого метаанализа [25].
В сетевом метаанализе использовалась полная байесовская сеть доказательств (цепи: 4; масштабирование начальных значений: 2.5; итерации настройки: 20 000; итерации моделирования: 50 000; интервал настройки: 10). Диагностику конвергенции на согласованность и несогласованность оценивали с помощью метода Брукса-Гельмана-Рубина, как описано ранее [26]. Результаты сетевого метаанализа выражены в виде относительного эффекта (RE) и 95% достоверного интервала (95% CrI). Вероятность того, что каждая группа вмешательства была наиболее эффективной, рассчитывалась путем подсчета доли итераций цепочки, в которой каждая группа вмешательства имела наибольшую среднюю разницу, и поверхности под кумулятивной кривой ранжирования (SUCRA), представляющей собой сводку этих вероятностей. , также был рассчитан.SUCRA равен 1, когда лечение определенно будет лучшим, и 0, когда лечение определенно будет худшим [27].
Анализ чувствительности был проведен для выявления исследований, которые внесли неоднородность и погрешность в оценку эффекта первичной конечной точки.
Анализ числа пациентов, нуждающихся в лечении (NNT), был выполнен для первичной конечной точки. NNT является обратной величиной абсолютного снижения риска, связанного с вмешательством в течение фиксированного периода времени [28, 29, 30]. Значения NNT представлены в этом исследовании как индивидуальные и рассчитываются путем анализа кривых Каплана-Мейера или с использованием необработанных данных, представленных в первичных публикациях, как описано ранее [31, 32].Относительный вес каждого исследования, полученный в результате попарного метаанализа, использовался для расчета средневзвешенной частоты исследуемых групп и для правильного предоставления значений NNT.
Профиль безопасности исследованных препаратов был исследован с помощью объединенного анализа частоты нежелательных явлений, которые были ранжированы в соответствии с рекомендациями Европейского медицинского агентства (EMA): очень часто ≥1/10, часто ≥1/100 до < 1 /10, нечасто от ≥1/1000 до < 1/100, частота неизвестна, если ее нельзя рассчитать на основе извлеченных данных. Программное обеспечение
Программное обеспечение
OpenMetaAnalyst [33] и GeMTC [34] использовалось для выполнения метаанализа, программное обеспечение GraphPad Prism (Калифорния, США) для графического отображения данных и GRADEpro GDT для оценки качества доказательств [17]. Статистическая значимость оценок эффекта, полученных в результате парного и сетевого метаанализа, оценивалась для P < 0,05.
Эрдостеин признан более эффективным по сравнению с другими муколитическими агентами при ХОБЛ
По общему профилю эффективности и безопасности эрдостеин превосходит другие широко используемые муколитические агенты для лечения хронической обструктивной болезни легких (ХОБЛ), как показывает новое исследование.
Исследование « Профиль эффективности и безопасности муколитических/антиоксидантных средств при хронической обструктивной болезни легких: сравнительный анализ эрдостеина, карбоцистеина и N-ацетилцистеина » было опубликовано в журнале Respiratory Research .
Стандартное лечение ХОБЛ включает муколитические препараты, которые помогают снизить вязкость (густоту) бронхиального и легочного секрета за счет расщепления слизи, улучшая функцию легких.
Исследования показали, что муколитики снижают риск обострений (внезапного ухудшения симптомов ХОБЛ) и приводят к улучшению общего состояния больных ХОБЛ.
Общие муколитические препараты для лечения ХОБЛ включают эрдостеин, карбоцистеин и N-ацетилцистеин (NAC). Но исследований, сравнивающих эффективность этих муколитических средств, не проводилось. Таким образом, нет данных в поддержку использования одного агента над другим при лечении ХОБЛ.
Чтобы решить эту проблему, исследователи провели метаанализ (CRD42016053762), чтобы сравнить эффективность и безопасность 600 мг/день эрдостеина, 1500 мг/день карбоцистеина и 1200 мг/день NAC при лечении ХОБЛ. .
Исследователи оценили эффективность этих муколитических средств в отношении количества острых обострений ХОБЛ (ОХОБЛ), продолжительности обострения ХОБЛ и частоты госпитализаций по поводу ХОБЛ. Исследователи также изучили безопасность терапии, изучив частоту зарегистрированных нежелательных явлений (НЯ).
Команда проанализировала данные 2753 пациентов с ХОБЛ, включенных в семь клинических испытаний, опубликованных в период с 2004 по 2017 год.![]()
Исследователи обнаружили, что наиболее эффективным оказался эрдостеин, за ним следует карбоцистеин, а затем NAC.
Следует отметить, что эрдостеин был единственной терапией, которая ассоциировалась со снижением риска развития по крайней мере одного обострения ХОБЛ, а также снижением риска госпитализации по поводу обострения ХОБЛ.
Кроме того, эрдостеин и NAC, но не карбоцистеин, значительно снижали продолжительность ХОБЛ.
НЯ, вызванные эрдостеином, карбоцистеином и NAC, были легкими и в основном хорошо переносились.
Основываясь на результатах, команда пришла к выводу, что «общий профиль эффективности/безопасности эрдостеина превосходит профиль как карбоцистеина, так и NAC».
Исследователи, однако, подчеркнули, что «для окончательного подтверждения результатов этого метаанализа необходимы будущие непосредственные исследования, проведенные на тех же популяциях ХОБЛ».
Муколитические препараты Статья
Непрерывное образование
Муколитики — это препараты, используемые для лечения гиперсекреции слизи и ее последствий, таких как рецидивирующие инфекции у пациентов с ХОБЛ, кистозным фиброзом и бронхоэктазами. Они принадлежат к группе агентов, называемых мукоактивными агентами. В этом упражнении описываются различные варианты и их соответствующие механизмы действия, показания и противопоказания, относящиеся к членам медицинской бригады, поскольку они являются ценными средствами для лечения продуктивного кашля и связанных с ним слизисто-обструктивных респираторных заболеваний.
Они принадлежат к группе агентов, называемых мукоактивными агентами. В этом упражнении описываются различные варианты и их соответствующие механизмы действия, показания и противопоказания, относящиеся к членам медицинской бригады, поскольку они являются ценными средствами для лечения продуктивного кашля и связанных с ним слизисто-обструктивных респираторных заболеваний.
Цели:
- Определить механизмы действия различных классов муколитических средств.
- Опишите побочные эффекты муколитических средств.
- Рассмотрите соответствующий мониторинг для пациентов, получающих муколитические средства.
- Объясните важность улучшения межпрофессиональных командных стратегий для улучшения коммуникации и координации для улучшения результатов у пациентов, страдающих слизисто-обструктивными расстройствами, которые получают муколитические препараты.

Показания
Муколитики — препараты, относящиеся к классу мукоактивных средств.Они оказывают влияние на слизистый слой, выстилающий дыхательные пути, с целью повышения его клиренса. Слизь является первой линией защиты различных эпителиев внутри нашего тела от вредных патогенов. Его работа также влечет за собой защиту эпителия от раздражающих раздражителей, обнаруженных в желудочно-кишечном тракте. В нем находится набор белков, таких как иммуноглобулины, различные гликопротеины и даже некоторые антимикробные ферменты, такие как лизоцим. Сшивание полимерных гелеобразующих муцинов в основном определяет биофизические свойства слизи.Этот слой очень хорошо защищает от бактерий благодаря ингибированию роста бактерий и предотвращению образования биопленки. Слой слизи также работает как физический барьер против респираторных раздражителей и предотвращает потерю жидкости. Отхаркиваемая слизь называется мокротой.
Количество слизи в нашем организме регулируется главным образом двумя механизмами: клетками, секретирующими слизь, и мукоцилиарным эскалаторным механизмом. Бокаловидные клетки слизистых оболочек и подслизистых желез дыхательной, желудочно-кишечной и репродуктивной систем отвечают за секрецию слизи, а слизисто-цилиарный эскалатор отвечает за отхождение слизи по направлению к глотке, откуда она в конечном итоге отхаркивается. кашлевой рефлекс.Однако есть некоторые условия, при которых это правило нарушается.
Бокаловидные клетки слизистых оболочек и подслизистых желез дыхательной, желудочно-кишечной и репродуктивной систем отвечают за секрецию слизи, а слизисто-цилиарный эскалатор отвечает за отхождение слизи по направлению к глотке, откуда она в конечном итоге отхаркивается. кашлевой рефлекс.Однако есть некоторые условия, при которых это правило нарушается.
При таких состояниях, как ХОБЛ и астма, хроническое раздражение дыхательных путей приводит к гиперсекреции слизи. Чрезмерное образование слизи подавляет механизмы мукоцилиарного клиренса, что приводит к накоплению этой избыточной слизи. Это приводит к образованию слизистых пробок, которые еще больше уменьшают клиренс. Дыхательные пути реагируют выделением избытка медиаторов воспаления в попытке устранить обструкцию.К сожалению, это только ухудшает состояние по мере увеличения вязкости слизи, что приводит к дальнейшему снижению клиренса, а также к возникновению воспаления и фиброза. Это состояние только ухудшается, потому что эта статическая слизь заражена бактериями, такими как Pseudomonas aeruginosa и Staphylococcus aureus. Таким образом запускается порочный круг, который неизменно заканчивается острым обострением состояния. Классические муколитики, такие как N-ацетилцистеин, показаны при таких состояниях, поскольку они снижают вязкость слизи и повышают ее текучесть, тем самым улучшая ее клиренс.[1]
Это состояние только ухудшается, потому что эта статическая слизь заражена бактериями, такими как Pseudomonas aeruginosa и Staphylococcus aureus. Таким образом запускается порочный круг, который неизменно заканчивается острым обострением состояния. Классические муколитики, такие как N-ацетилцистеин, показаны при таких состояниях, поскольку они снижают вязкость слизи и повышают ее текучесть, тем самым улучшая ее клиренс.[1]
При таких состояниях, как кистозный фиброз, секреция слизи нарушена, поэтому секрет дыхательных путей в основном включает нитевидные полимеры актина и ДНК, полученную из воспалительных клеток. Эти выделения также густые и вязкие и часто становятся мишенью для бактерий. Здесь полезен другой класс муколитиков, нацеленный на полимеры ДНК.
Механизм действия
Муколитики делят на две подгруппы:
1.Классические муколитики
2. Пептидные муколитики
Классические муколитики:
Дисульфидные связи являются строительными блоками многих сложных белков, включая слизь. N-ацетил-L-цистеин (NAC), прототип препарата этого класса, сохраняет восстанавливающую способность и работает по механизму обмена тиол-дисульфид. Муциновые полимеры имеют остатки цистеина по всей своей структуре. Дисульфидные связи закрепляются на этих остатках, что приводит к сшиванию полимера. Свободная тиольная группа в структуре NAC гидролизует дисульфидные связи, присоединенные к цистеиновым остаткам.Эта реакция нарушает трехмерную структуру слизи, восстанавливая связь S-S до связи S-H (сульфгидрила), что делает ее неспособной закреплять сложную структуру белка.[1] В эту подгруппу входят
N-ацетил-L-цистеин (NAC), прототип препарата этого класса, сохраняет восстанавливающую способность и работает по механизму обмена тиол-дисульфид. Муциновые полимеры имеют остатки цистеина по всей своей структуре. Дисульфидные связи закрепляются на этих остатках, что приводит к сшиванию полимера. Свободная тиольная группа в структуре NAC гидролизует дисульфидные связи, присоединенные к цистеиновым остаткам.Эта реакция нарушает трехмерную структуру слизи, восстанавливая связь S-S до связи S-H (сульфгидрила), что делает ее неспособной закреплять сложную структуру белка.[1] В эту подгруппу входят
N-ацетилцистеин
Наряду с вышеупомянутым муколитическим действием N-ацетилцистеин также обладает противовоспалительными и антиоксидантными свойствами. Эти агенты помогают уменьшить количество активных форм кислорода и медиаторов воспаления, которые вызывают поражение дыхательных путей.
Карбоцистеин
Карбоцистеин также увеличивает объем мокроты, вызывая, таким образом, дополнительный отхаркивающий эффект. Он очень безопасен и эффективен для астматиков, так как не раздражает дыхательные пути.[2] Он может быть показан для снижения острого ХОБЛ (острого обострения хронической обструктивной болезни легких) из-за его свойства значительно снижать бактериальную нагрузку в дыхательных путях таких пациентов.[3] Легочные инфекции вызывают до 70% всех обострений ХОБЛ.
Он очень безопасен и эффективен для астматиков, так как не раздражает дыхательные пути.[2] Он может быть показан для снижения острого ХОБЛ (острого обострения хронической обструктивной болезни легких) из-за его свойства значительно снижать бактериальную нагрузку в дыхательных путях таких пациентов.[3] Легочные инфекции вызывают до 70% всех обострений ХОБЛ.
Эрдостеин и Фудостеин
Это более новые препараты, которые являются производными тиолов и обладают дополнительным антиоксидантным и противокашлевым действием. У них есть сульфгидрильная группа в их активном метаболите, называемом Met-1, который действует во время респираторного взрыва нейтрофилов. Эрдостеин также продемонстрировал значительный антибиотикопотенциирующий эффект. В отчетах также указывается, что он защищает от альфа-1-антитрипсина.
Пептидные муколитики
В отличие от классических муколитиков пептидные муколитики сохраняют защитные муцины. Пептидные муколитики воздействуют на ДНК-полимеры и звенья F-актина, которые имеют тенденцию к увеличению при гнойных выделениях. Таким образом, пептидные муколитики, предназначенные для снижения вязкости слизи за счет деполимеризации полимеров ДНК или сети F-актина, которые часто присутствуют в гнойных выделениях, очень полезны при таких состояниях, как муковисцидоз.
Пептидные муколитики воздействуют на ДНК-полимеры и звенья F-актина, которые имеют тенденцию к увеличению при гнойных выделениях. Таким образом, пептидные муколитики, предназначенные для снижения вязкости слизи за счет деполимеризации полимеров ДНК или сети F-актина, которые часто присутствуют в гнойных выделениях, очень полезны при таких состояниях, как муковисцидоз.
Дорназа альфа
Дорназа альфа оказывает муколитическое действие за счет деполимеризации полимеров ДНК. Он вызывает умеренное увеличение ОФВ1 (объем форсированного выдоха через 1 секунду) у пациентов с муковисцидозом.[6]
Тимозин β4
Муколитический эффект тимозина β4 обусловлен его действием на F-актин. F-актин вырабатывается в большом количестве в гнойных выделениях и повышает вязкость из-за своей нитевидной природы. Таким образом, тимозин может иметь значение для разрушения гноя в дыхательных путях посредством деполимеризации этих нитей.[7]
Администрация
N-ацетилцистеин можно вводить перорально, внутривенно и местно в форме небулайзера. Хотя местный путь имел преимущество в активации механизма мукоцилиарного клиренса наряду с индукцией кашлевого рефлекса, пероральный путь предлагает гораздо лучшую переносимость. Это обсуждается далее в разделе о побочных реакциях. Пероральная доза от 200 до 600 мг в день рекомендуется для лечения слизисто-обструктивных заболеваний.[9] Безопасность для беременных женщин и детей хорошо известна.[10]
Хотя местный путь имел преимущество в активации механизма мукоцилиарного клиренса наряду с индукцией кашлевого рефлекса, пероральный путь предлагает гораздо лучшую переносимость. Это обсуждается далее в разделе о побочных реакциях. Пероральная доза от 200 до 600 мг в день рекомендуется для лечения слизисто-обструктивных заболеваний.[9] Безопасность для беременных женщин и детей хорошо известна.[10]
Рекомендуемая доза дорназы альфа составляет 2,5 мг, которую вводят через небулайзер 1–2 раза в день пациентам с муковисцидозом.[6] Данные свидетельствуют об улучшении ФЖЕЛ и ОФВ1 уже через три дня после начала терапии. Стандартные методы лечения муковисцидоза, такие как антибиотики и физиотерапия органов грудной клетки, следует продолжать вместе с препаратом. Аналогичная доза и способ введения рекомендованы для детей всех возрастных групп и подростков. Раннее введение у младенцев и детей младшего возраста с диагнозом муковисцидоз, даже при отсутствии клинических признаков или симптомов заболевания, показало пользу. [11] Хотя данные о безопасности дорназы альфа при беременности ограничены, в моделях на животных, получавших дозы, намного превышающие максимальную рекомендуемую дозу для человека, не сообщалось о влиянии на исход плода.
[11] Хотя данные о безопасности дорназы альфа при беременности ограничены, в моделях на животных, получавших дозы, намного превышающие максимальную рекомендуемую дозу для человека, не сообщалось о влиянии на исход плода.
Карбоцистеин вводят перорально в дозах от 750 мг два раза в день до 4,5 г один раз в день. Имеющиеся данные свидетельствуют о том, что более высокая концентрация активных соединений была достигнута за счет ночного приема препарата.[2]
Эрдостеин вводят перорально, и дозы могут варьироваться от 600 до 900 мг.Тем не менее, дозу следует тщательно титровать у пожилых пациентов с хроническим заболеванием печени, поскольку в этих случаях сообщалось о повышении концентрации в плазме и периоде полувыведения [5].
Побочные эффекты
- Наиболее частыми побочными эффектами перорального приема N-ацетилцистеина являются рвота и диарея. После 16-18 дней использования N-ацетилцистеина частота рвоты и диареи увеличилась на 50 % и 43.
 5 % соответственно.[9][12] Сообщается, что повышение артериального давления, респираторный дистресс, боль в груди, лихорадка, ректальное кровотечение, головная боль, гипотония, вялость и кожная аллергия встречаются менее чем в 5% случаев. Аэрозольный N-ацетилцистеин плохо переносится из-за его раздражающего действия и очень неприятного запаха, который может вызвать рвоту. Высокая частота анафилактических реакций наблюдается у пациентов, получающих внутривенно N-ацетилцистеин.[13]
5 % соответственно.[9][12] Сообщается, что повышение артериального давления, респираторный дистресс, боль в груди, лихорадка, ректальное кровотечение, головная боль, гипотония, вялость и кожная аллергия встречаются менее чем в 5% случаев. Аэрозольный N-ацетилцистеин плохо переносится из-за его раздражающего действия и очень неприятного запаха, который может вызвать рвоту. Высокая частота анафилактических реакций наблюдается у пациентов, получающих внутривенно N-ацетилцистеин.[13] - Наиболее часто сообщаемыми побочными реакциями при приеме Дорназы альфа являются ларингит, изменение голоса и сыпь по сравнению с плацебо.Другими менее значительными побочными эффектами были фарингит, боль в груди и конъюнктивит. Эти побочные эффекты были в основном преходящими и, как сообщалось, не были достаточно серьезными, чтобы вызвать отмену лечения или потребовать изменения дозировки. На сегодняшний день не было сообщений об анафилактической реакции на дорназу альфа. Во всех исследованиях примерно у 2 – 4% пациентов, получавших дорназу альфа, вырабатывались сывороточные антитела к препарату, клиническое значение которых еще предстоит выяснить.
 [6]
[6] - При применении карбоцистеина сообщалось о легком дискомфорте в желудке, язве желудка и фиксированной лекарственной сыпи.[2]
- У пациентов, получавших эрдостеин, были зарегистрированы эпигастралгия, головная боль, эритема и тошнота, последние два из которых привели к прекращению лечения.[5]
Противопоказания
- Из-за склонности вызывать рвоту N-ацетилцистеин противопоказан пациентам с язвенной болезнью. Он также противопоказан пациентам с варикозным расширением вен пищевода и разрывами Мэллори-Вейса по тем же причинам. Его следует строго избегать у пациентов, у которых в прошлом была анафилактическая реакция на препарат.
- Единственным противопоказанием для дорназы альфа является известная гиперчувствительность к препарату в прошлом или гиперчувствительность пациента к клеточным продуктам яичника китайского хомяка (CHO).[14]
- Карбоцистеин противопоказан пациентам с активной язвой желудка.
 [2]
[2]
Мониторинг
После перорального приема 400 мг N-ацетилцистеина максимальная концентрация в плазме составила 3,47 мг/л, для ее достижения потребовалось 30 минут.Объем распределения N-ацетилцистеина колеблется от 0,33 до 0,47 л/кг. Через 4 часа после внутривенного введения 50% препарата связывается с белками плазмы. N-ацетилцистеин подвергается экстенсивному метаболизму при первом прохождении в стенке кишечника и печени при пероральном введении, что приводит к биодоступности примерно от 6 до 10%. Большая часть элиминации этого препарата не связана с почками, а почками выводится только 30%.[9]
Исследования на животных показали минимальную системную абсорбцию после аэрозольного вдыхания дорназы альфа.Вдыхание даже очень высоких доз (10 мг три раза в день) не приводило к значительному увеличению концентрации ДНКазы в сыворотке [15]. Считается, что какая бы небольшая системная абсорбция ни происходила, она связана с белком и выводится из организма без значительного накопления в тканях. Это означает, что для пациентов, получающих этот препарат, необходим минимальный мониторинг или его отсутствие. После вдыхания дозы 2,5 мг дорназы альфа средняя концентрация в мокроте 2 мкг/мл была обнаружена в течение первых 15 минут, а через 2 часа концентрация упала до 0.6 мкг/мл. Расчетный период полувыведения из легких в моделях животных составил около 11 часов. У приматов биодоступность была менее 2%.[17]
Это означает, что для пациентов, получающих этот препарат, необходим минимальный мониторинг или его отсутствие. После вдыхания дозы 2,5 мг дорназы альфа средняя концентрация в мокроте 2 мкг/мл была обнаружена в течение первых 15 минут, а через 2 часа концентрация упала до 0.6 мкг/мл. Расчетный период полувыведения из легких в моделях животных составил около 11 часов. У приматов биодоступность была менее 2%.[17]
Карбоцистеин демонстрирует кинетику открытой модели с одним отделением после абсорбции и достигает своей максимальной концентрации в плазме через 1–1,7 часа. Препарат подвергается частичному метаболизму в печени, и до 60% препарата выводится почками в неизмененном виде.[2]
После перорального приема эрдостеин достигает максимальной концентрации в плазме через 1.4 часа и имеет аналогичный период полувыведения. Он содержит две заблокированные сульфгидрильные группы. Они высвобождаются только после метаболизма в печени, что придает ценное свойство не воздействовать на слизь, выстилающую желудок. О значительном накоплении препарата не сообщалось.[5]
О значительном накоплении препарата не сообщалось.[5]
Лекарственное взаимодействие
- Пероральный N-ацетилцистеин нельзя назначать с активированным углем, так как препарат массой 3 г адсорбирует 54,6% препарата, а препарат массой 6 г адсорбирует 96%.2% препарата, что заметно снижает его эффективность.[9]
- N-ацетилцистеин обеспечивает местную защиту уретры, мочевого пузыря, мочеточников и почек от токсичных метаболитов внутривенного циклофосфамида при пероральном введении вместе с ним.[18]
- Имеющиеся данные свидетельствуют о том, что N-ацетилцистеин может предотвращать доксорубицин-индуцированную кардиомиопатию на животных моделях при совместном применении. Было показано, что
- Дорназа альфа значительно усиливает антибиотический эффект тобрамицина и амикацина в отношении нескольких штаммов Pseudomonas aeruginosa и Staphylococcus aureus. [6]
- Введение эрдостеина с амоксициллином у пациентов с острым инфекционным обострением хронического бронхита приводило к более высоким концентрациям антибиотика в мокроте, что приводило к более раннему и более выраженному улучшению клинических симптомов по сравнению с плацебо.

- Сообщалось о более высокой концентрации амоксициллина в мокроте пациентов, страдающих острым инфекционным обострением хронического бронхита, при одновременном применении с эрдостеином.[5]
Токсичность
N-ацетилцистеин имеет широкий терапевтический индекс. Однако ошибки дозирования привели к случаям токсичности. Они чаще встречаются при внутривенном введении препарата. Сообщается о случае, когда 23-летней женщине была введена десятикратная рекомендуемая нагрузочная доза.[13] Эта доза привела к тромбоцитопении, гемолизу, острой почечной недостаточности и, в конечном итоге, к смерти. Другое исследование, однако, показало, что пероральное введение N-ацетилцистеина, которое обычно используется у пациентов с слизисто-обструктивными заболеваниями, безопаснее, чем внутривенное введение, а ошибки дозирования гораздо менее вероятны.[19] Исследования показали, что пероральные дозы до 30 г/день в течение трех дней очень хорошо переносятся с незначительными побочными эффектами, такими как рвота и диарея. [12]
[12]
Из-за короткого периода полувыведения и плохой системной абсорбции дорназа альфа является относительно хорошо переносимым препаратом. Токсичность дорназы альфа не приводила к тому, что животные модели подвергались воздействию доз, в 180 раз превышающих максимальную рекомендуемую дозу для человека в исследованиях однократной ингаляционной дозы [14].
В моделях на животных не было обнаружено какой-либо клинически значимой токсичности эрдостеина даже после введения очень больших доз препарата.[5]
Улучшение результатов команды здравоохранения
По прогнозам ВОЗ, глобальная распространенность ХОБЛ составляет около 250 миллионов человек, при этом ежегодно умирает около 3 миллионов человек. К сожалению, ожидается, что в ближайшие годы эта цифра возрастет, что будет означать существенное социально-экономическое воздействие. Поэтому, пока продолжаются исследования по окончательному лечению ХОБЛ, крайне важно отвлечь внимание на методы лечения, которые могли бы улучшить образ жизни и уменьшить количество острых обострений, пребывание в стационаре и смертность у таких пациентов. Именно в этой области муколитики демонстрируют огромный потенциал.
Именно в этой области муколитики демонстрируют огромный потенциал.
Требуется хорошо скоординированная межпрофессиональная команда пульмонологов, физиотерапевтов, семейных врачей (MD, DO, NPs, PA), медсестер и фармацевтов для совместной работы над лечением случая ХОБЛ. Прежде всего, пациент должен быть проинструктирован о важности изменения образа жизни. Врач должен тщательно проинструктировать пациента о пользе прописанных лекарств, правильной дозировке, ожидаемых побочных реакциях и научить их правильной процедуре использования небулайзера.Такой подход поможет добиться максимальной комплаентности пациента. Пациенты также должны быть осведомлены о важности регулярных контрольных посещений. Важную роль также играют клинические психологи, группы поддержки и центры избавления от зависимости, так как это поможет отсрочить прогрессирование заболевания у курящих пациентов. Такой межпрофессиональный подход к лечению пациентов муколитиками, где это уместно, может привести к улучшению исходов с меньшим количеством побочных эффектов. [Уровень 5]
[Уровень 5]
За последние 30 лет в лечении муковисцидоза достигнуты большие успехи.Сегодня средний возраст выживания пациента составляет почти 40 лет. Частично это может быть связано с развитием таких методов лечения, как муколитики. Этим усилиям можно способствовать, привлекая к управлению хорошо организованную межпрофессиональную команду. Хотя муколитики, назначенные врачом, являются важной частью этого, роль медсестер, физиотерапевтов грудной клетки, диетологов и детских психиатров также важна.[20]
Хотя в последнее время эффективность муколитиков подвергалась сомнению, данные, представленные в крупномасштабных исследованиях, проведенных для N-ацетилцистеина [уровень 2], дорназы альфа [уровень 1], карбоцистеина [уровень 1] и эрдостеина [уровень 2 ] нельзя игнорировать.[21][22][23][24]
Карбоцистеин – обзор | ScienceDirect Topics
4.2 Антиоксиданты
Учитывая основную роль окислительного стресса в патогенезе ХОБЛ и резистентности к кортикостероидам, в настоящее время изучается несколько стратегий использования антиоксидантов с потенциальными терапевтическими эффектами. Например, было протестировано лечение муколитическими препаратами на основе тиолов с признанным антиоксидантным действием, такими как N -ацетилцистеин (NAC), карбоцистеин и эрдостеин.В целом, лечение этими препаратами снижает частоту обострений заболевания, но не оказывает существенного влияния на улучшение функции легких или качества жизни. Точно так же нет доказательств того, что эти антиоксиданты повышают чувствительность пациентов к кортикостероидам (Rogliani et al., 2019; Poole et al., 2019; Zheng et al., 2014). Возможное объяснение состоит в том, что высокий уровень окислительного стресса в легких при ХОБЛ может спровоцировать быструю инактивацию этого класса молекул. Следовательно, это увеличило исследовательские усилия по поиску более эффективных антиоксидантных молекул для лечения ХОБЛ.
Например, было протестировано лечение муколитическими препаратами на основе тиолов с признанным антиоксидантным действием, такими как N -ацетилцистеин (NAC), карбоцистеин и эрдостеин.В целом, лечение этими препаратами снижает частоту обострений заболевания, но не оказывает существенного влияния на улучшение функции легких или качества жизни. Точно так же нет доказательств того, что эти антиоксиданты повышают чувствительность пациентов к кортикостероидам (Rogliani et al., 2019; Poole et al., 2019; Zheng et al., 2014). Возможное объяснение состоит в том, что высокий уровень окислительного стресса в легких при ХОБЛ может спровоцировать быструю инактивацию этого класса молекул. Следовательно, это увеличило исследовательские усилия по поиску более эффективных антиоксидантных молекул для лечения ХОБЛ.
НАДФН (никотинамидадениндинуклеотидфосфат) оксидаза (NOX) представляет собой многокомпонентный фермент, связывающийся с цитоплазматической мембраной и опосредующий перенос электронов от никотинамидадениндинуклеотидфосфата (НАДФ) к молекулярному кислороду, что приводит к образованию супероксидных анионов. Этот белковый комплекс является основным источником эндогенных АФК при ХОБЛ. Было разработано несколько ингибиторов NOX для ослабления повреждения тканей, вызванного окислительным стрессом (Cifuentes-Pagano et al., 2012). Апоцинин является неселективным ингибитором NOX, который уменьшал воспаление легких у мышей с моделью обострения ХОБЛ, вызванного сочетанием сигаретного дыма и вирусной инфекции (Oostwoud et al., 2016). Распыляемый апоцинин, вводимый пациентам с ХОБЛ, снижал концентрации H 2 O 2 и нитритов в конденсате выдыхаемого воздуха, но о клинических параметрах не сообщалось (Stefanska et al., 2012). Несмотря на то, что NOX представляет собой интересную лекарственную мишень для лечения воспалительных заболеваний легких, разработка селективных ингибиторов оказалась сложной задачей. Недавно были разработаны некоторые сильнодействующие и специфические ингибиторы, но большинство этих соединений были проверены только на моделях in vitro или на мышах (Chocry and Leloup, 2020).
Этот белковый комплекс является основным источником эндогенных АФК при ХОБЛ. Было разработано несколько ингибиторов NOX для ослабления повреждения тканей, вызванного окислительным стрессом (Cifuentes-Pagano et al., 2012). Апоцинин является неселективным ингибитором NOX, который уменьшал воспаление легких у мышей с моделью обострения ХОБЛ, вызванного сочетанием сигаретного дыма и вирусной инфекции (Oostwoud et al., 2016). Распыляемый апоцинин, вводимый пациентам с ХОБЛ, снижал концентрации H 2 O 2 и нитритов в конденсате выдыхаемого воздуха, но о клинических параметрах не сообщалось (Stefanska et al., 2012). Несмотря на то, что NOX представляет собой интересную лекарственную мишень для лечения воспалительных заболеваний легких, разработка селективных ингибиторов оказалась сложной задачей. Недавно были разработаны некоторые сильнодействующие и специфические ингибиторы, но большинство этих соединений были проверены только на моделях in vitro или на мышах (Chocry and Leloup, 2020).
Миелопероксидазы (МПО) являются другими важными источниками окислительных радикалов. В дополнение к перекиси водорода (H 2 O 2 ) эти ферменты производят большое количество аниона хлорида (Cl — ) и хлорноватистой кислоты (HOCl), оба из которых являются значительно агрессивными окислителями. Гранулы нейтрофилов содержат большое количество МПО, поэтому активность МПО заметно повышается при ХОБЛ (Keatings and Barnes, 1997). Лечение селективным необратимым ингибитором МПО, 2-тиоксантином AZD5904, у морских свинок, подвергавшихся воздействию сигаретного дыма в течение 6 месяцев, уменьшало ремоделирование дыхательных путей и эмфизему.Лечение также ингибировало окислительное повреждение легких и улучшало функцию легких (Churg et al., 2012). Однако, несмотря на хорошую переносимость этого препарата у добровольцев, клинические исследования этого препарата были прекращены по неизвестным причинам (Barnes, 2020).
Другие антиоксидантные стратегии включают антиоксидантные миметики, которые предназначены для восстановления активности антиоксидантов, тем самым снижая влияние окислительного стресса на ткани. Было показано, что эбселен, миметик GPx, уменьшает воспаление дыхательных путей на модели обострения ХОБЛ, вызванного сочетанием сигаретного дыма и вирусной инфекции (Oostwoud et al., 2016). Как и эбселен, другие препараты эффективны на животных моделях окислительного стресса, хотя о клинических исследованиях с использованием антиоксидантных миметиков при ХОБЛ не сообщалось (Smith et al., 2002; Barnes, 2020). Оксид азота способствует окислительному стрессу при ХОБЛ за счет образования высокореактивных ионов пероксинитрита (Osoata et al., 2009; Smith et al., 2002). Распыляемый аминогуанидин, относительно селективный ингибитор индуцибельной синтазы оксида азота (iNOS), не смог снизить уровень 8-изопростана, маркера окислительного стресса, в конденсате выдыхаемого воздуха (КВВ) и мокроте пациентов с ХОБЛ (Brindicci et al., 2009).
Было показано, что эбселен, миметик GPx, уменьшает воспаление дыхательных путей на модели обострения ХОБЛ, вызванного сочетанием сигаретного дыма и вирусной инфекции (Oostwoud et al., 2016). Как и эбселен, другие препараты эффективны на животных моделях окислительного стресса, хотя о клинических исследованиях с использованием антиоксидантных миметиков при ХОБЛ не сообщалось (Smith et al., 2002; Barnes, 2020). Оксид азота способствует окислительному стрессу при ХОБЛ за счет образования высокореактивных ионов пероксинитрита (Osoata et al., 2009; Smith et al., 2002). Распыляемый аминогуанидин, относительно селективный ингибитор индуцибельной синтазы оксида азота (iNOS), не смог снизить уровень 8-изопростана, маркера окислительного стресса, в конденсате выдыхаемого воздуха (КВВ) и мокроте пациентов с ХОБЛ (Brindicci et al., 2009).
Фактор транскрипции Nrf2 регулирует экспрессию нескольких генов антиоксидантов. Снижение активности Nrf2 было связано с чрезмерным окислительным повреждением при ХОБЛ, а также с резистентностью к кортикостероидам (Zhao et al. , 2017; Barnes, 2013). Клиническое испытание с сульфорафаном, естественным активатором Nrf2, в течение 4 недель не привело к увеличению мишеней антиоксидантного гена Nrf2 или уменьшению окислительного стресса и воспаления у пациентов с ХОБЛ (Wise et al., 2016). Кроме того, синтетические активаторы Nrf2, такие как противовоспалительный препарат бардоксолон метил или диметилфумарат, продемонстрировали несколько побочных эффектов в клинических испытаниях (Gold et al., 2012; Россинг, 2013). Несмотря на то, что активаторы Nrf2 представляют собой привлекательный терапевтический подход, разработка сильнодействующих и специфических активаторов Nrf2 затруднена.
, 2017; Barnes, 2013). Клиническое испытание с сульфорафаном, естественным активатором Nrf2, в течение 4 недель не привело к увеличению мишеней антиоксидантного гена Nrf2 или уменьшению окислительного стресса и воспаления у пациентов с ХОБЛ (Wise et al., 2016). Кроме того, синтетические активаторы Nrf2, такие как противовоспалительный препарат бардоксолон метил или диметилфумарат, продемонстрировали несколько побочных эффектов в клинических испытаниях (Gold et al., 2012; Россинг, 2013). Несмотря на то, что активаторы Nrf2 представляют собой привлекательный терапевтический подход, разработка сильнодействующих и специфических активаторов Nrf2 затруднена.
Респираторные парадоксальные побочные реакции, связанные с системным применением ацетилцистеина и карбоцистеина у детей: национальное исследование.
Mallet P, Mourdi N, Dubus JC, Bavoux F, Boyer-Gervoise MJ, Jean-Pastor MJ, Chalumeau M
Респираторные парадоксальные побочные реакции, связанные с системным применением ацетилцистеина и карбоцистеина у детей: национальное исследование .
PLoS Один. 2011;6(7):e22792. doi: 10.1371/journal.pone.0022792. Epub 2011 Jul 27.
ЦЕЛЬ: Сообщить о педиатрических случаях парадоксальных побочных реакций со стороны органов дыхания (НЛР) после воздействия пероральных муколитических препаратов (карбоцистеин, ацетилцистеин), которые привели к отзыву лицензий на эти препараты для младенцев во Франции, а затем Италия. ДИЗАЙН. Исследование проводилось в соответствии с рекомендациями Европейского руководства по фармаконадзору за лекарственными средствами, используемыми в педиатрической популяции.ОБСТАНОВКА: Случаи, добровольно зарегистрированные врачами в период с 1989 по 2008 год, были выявлены в общедоступной базе данных национального французского фармаконадзора и в базах данных фармацевтических компаний. ПАЦИЕНТЫ: Определение парадоксальных респираторных нежелательных реакций было основано на литературных данных. Воздействие муколитических препаратов было условно определено как прием муколитических препаратов в течение не менее 2 дней (> 200 мг) и, по крайней мере, до дня, предшествовавшего появлению первых признаков подозрения на НР. Результаты. Неэксклюзивные парадоксальные респираторные нежелательные реакции, зарегистрированные у 59 детей (средний возраст 5 месяцев, диапазон от 3 недель до 34 месяцев, 98% моложе 2 лет), включали усиление бронхореи или рвоту слизью (n = 27), ухудшение респираторных дистресс при инфекции дыхательных путей (n = 35), одышка (n = 18), усиление или пролонгация кашля (n = 11) и бронхоспазм (n = 1).51 (86%) ребенку потребовалась госпитализация или длительная госпитализация из-за НДР; один больной умер от отека легких после слизистой рвоты. ЗАКЛЮЧЕНИЕ: Родители, врачи, фармацевты и органы регулирования лекарственных средств должны знать, что, согласно имеющимся данным, соотношение пользы и риска муколитических препаратов у младенцев по крайней мере равно нулю и, скорее всего, отрицательно.
Результаты. Неэксклюзивные парадоксальные респираторные нежелательные реакции, зарегистрированные у 59 детей (средний возраст 5 месяцев, диапазон от 3 недель до 34 месяцев, 98% моложе 2 лет), включали усиление бронхореи или рвоту слизью (n = 27), ухудшение респираторных дистресс при инфекции дыхательных путей (n = 35), одышка (n = 18), усиление или пролонгация кашля (n = 11) и бронхоспазм (n = 1).51 (86%) ребенку потребовалась госпитализация или длительная госпитализация из-за НДР; один больной умер от отека легких после слизистой рвоты. ЗАКЛЮЧЕНИЕ: Родители, врачи, фармацевты и органы регулирования лекарственных средств должны знать, что, согласно имеющимся данным, соотношение пользы и риска муколитических препаратов у младенцев по крайней мере равно нулю и, скорее всего, отрицательно.
Ацетилцистеин | Memorial Sloan Kettering Cancer Center
N-ацетилцистеин (NAC) — это антиоксидант, который используется как лекарство, отпускаемое по рецепту, и как пищевая добавка.В качестве лекарственного средства его назначают парентерально или перорально для лечения передозировки ацетаминофена. Формы раствора для ингаляций и приема внутрь обладают муколитическим действием и используются для устранения обструкции при заболеваниях бронхов и при процедурах трахеотомии. Пероральная капсула продается как пищевая добавка из-за ее защитных свойств для печени и поддержки здорового функционирования иммунной системы.
Формы раствора для ингаляций и приема внутрь обладают муколитическим действием и используются для устранения обструкции при заболеваниях бронхов и при процедурах трахеотомии. Пероральная капсула продается как пищевая добавка из-за ее защитных свойств для печени и поддержки здорового функционирования иммунной системы.
Клинические исследования показывают, что NAC может лечить лекарственную гепатотоксичность (1) (2) . Предварительные данные свидетельствуют о том, что он также может повышать уровень антиоксидантов у пациентов с ВИЧ/СПИДом (3) и сохранять функцию почек у пациентов, находящихся на гемодиализе (40) (41) .
Результаты применения NAC при хроническом заболевании легких неоднозначны. Некоторые исследования показывают, что он может уменьшать обострения (5) (44) , воспаления (45) и помогать улучшать или поддерживать функцию легких (6) (38) , но такие были. в других испытаниях не наблюдалось (7) (8) (37) (39) . Кроме того, метаанализ показывает, что это не самый эффективный муколитический агент при хронической обструктивной болезни легких (ХОБЛ) (46) .
в других испытаниях не наблюдалось (7) (8) (37) (39) . Кроме того, метаанализ показывает, что это не самый эффективный муколитический агент при хронической обструктивной болезни легких (ХОБЛ) (46) .
Также был интерес к NAC для улучшения психиатрических состояний, с предварительным эффектом, показанным при зависимости, злоупотреблении психоактивными веществами и компульсивных расстройствах дополнительные NAC при симптомах депрессии смешанные (47) (48) (49) .
Хотя небольшие исследования предполагают, что NAC может ингибировать развитие биомаркеров рака (15) (16) , крупное исследование показало, что он не ингибирует образование вторичных опухолей головы и шеи или легких (17) .Предварительные результаты предполагают возможную пользу NAC в отношении токсичности при лечении рака, такой как снижение токсичности для печени (4) , невропатия (18) и мукозит (43) (50) , хотя он не уменьшал окислительный стресс. (42) или токсичность цисплатина (51) .
(42) или токсичность цисплатина (51) .
Сообщалось о побочных эффектах со стороны желудочно-кишечного тракта после применения NAC (19) . Благодаря своей антиоксидантной активности он также может ускорять прогрессирование некоторых видов рака, о чем свидетельствует ускоренный рост рака легких на животной модели (36) .Поэтому необходимы дополнительные исследования для определения безопасности и эффективности.
Список применений муколитиков, распространенные торговые марки и информация о безопасности
Муколитики — это рецептурные препараты, используемые для лечения хронических респираторных заболеваний, таких как ХОБЛ, кистозный фиброз и бронхоэктазы
. Муколитики — это класс препаратов, которые используются для разжижения слизи в дыхательных путях. Чрезмерное выделение слизи может быть признаком острого обострения или ухудшения, хронического или кратковременного респираторного заболевания.Муколитики могут сделать слизь в дыхательных путях более жидкой и менее липкой, особенно когда слизь густая и трудно откашливается. Эти лекарства помогают лечить застой в груди и продуктивный кашель, связанные с респираторными заболеваниями, такими как ХОБЛ, кистозный фиброз и бронхоэктазы.
Эти лекарства помогают лечить застой в груди и продуктивный кашель, связанные с респираторными заболеваниями, такими как ХОБЛ, кистозный фиброз и бронхоэктазы.
Продолжайте читать, чтобы узнать больше о муколитиках, их применении и побочных эффектах.
Прочие муколитики
- Мукомист (ацетилцистеин)
- Ацис-5 (ацетилцистеин)
- Ацетадот (ацетилцистеин)
- Availnex (карбоцистеин)
- N-ацетилцистеин (NAC)
- Эрдотин (эрдостеин)
- Клинал (фудостеин)
- Пульмозим (дорназа альфа)
- Тимозин бета-4
Что такое муколитики?
Муколитики входят в группу препаратов, называемых мукоактивными агентами, и используются для управления образованием слизи, вызванным хроническими респираторными заболеваниями.В эту группу препаратов входят разные лекарства, которые могут работать по-разному и использоваться для разных целей. Некоторые муколитики могут оказывать антиоксидантное и противовоспалительное действие, тогда как другие обладают дополнительным отхаркивающим или противокашлевым действием. Хотя они могут действовать по-разному, муколитики обычно назначают для одной и той же цели: разжижения избыточной слизи, чтобы вывести ее из легких.
Некоторые муколитики могут оказывать антиоксидантное и противовоспалительное действие, тогда как другие обладают дополнительным отхаркивающим или противокашлевым действием. Хотя они могут действовать по-разному, муколитики обычно назначают для одной и той же цели: разжижения избыточной слизи, чтобы вывести ее из легких.
Большинство муколитиков вводят перорально, хотя их также можно вводить внутривенно или через небулайзер.Например, N-ацетилцистеин, карбоцистеин и эрдостеин назначают перорально при респираторных заболеваниях. Дорназу альфа вводят через небулайзер пациентам с муковисцидозом.
Муколитики также можно назначать вместе с другими лекарствами, в зависимости от состояния, которое лечат. Дорназу альфа обычно назначают вместе с антибиотиками при муковисцидозе. Муколитики можно вводить в сочетании с другим мукоактивным средством, таким как отхаркивающее средство, для лечения продуктивного кашля.Муцинекс (гвайфенезин) — отхаркивающее средство, помогающее увеличить объем воды и секрета в дыхательных путях. Комбинация мукоактивных агентов может помочь контролировать секрецию дыхательных путей и способствовать очищению от слизи.
Комбинация мукоактивных агентов может помочь контролировать секрецию дыхательных путей и способствовать очищению от слизи.
Как действуют муколитики?
Слизь обычно вырабатывается в легких и дыхательных путях, выступая в качестве смазки и защитного барьера против патогенов. Слизь — это первая линия защиты организма от вредных патогенов, таких как бактерии и вирусы, вызывающие инфекцию. Он образуется путем перекрестного связывания гелеобразующих белков, называемых муцинами.Эти белки создают слизистый слой, который предотвращает рост бактерий, а также обеспечивает физический барьер против раздражителей дыхательных путей и потери жидкости.
Мокрота, или мокрота, представляет собой слизь, которая вырабатывается в дыхательных путях, и она может быть густой, липкой и трудно откашляемой. Большое количество слизи также может снизить функцию легких и затруднить дыхание.
Муколитики разжижают слизь в легких и дыхательных путях, разрушая ее структуру. В частности, они работают, чтобы разрушить связи, которые удерживают мукопротеины вместе. Когда эти связи разрываются, слизь разжижается и легче удаляется из дыхательных путей.
Когда эти связи разрываются, слизь разжижается и легче удаляется из дыхательных путей.
Для чего используются муколитики?
Муколитики обычно используются для лечения хронических респираторных заболеваний, которые характеризуются периодами избыточного образования слизи или гиперсекреции слизи. Однако их также можно использовать для очистки от слизи, вызванной кратковременным ухудшением респираторных заболеваний, таких как обострение ХОБЛ. Кроме того, некоторые муколитики могут быть показаны по другим причинам, включая передозировку ацетаминофена и диагностические исследования бронхов.
Типы муколитиков
Существует два типа муколитических средств: классические и пептидные муколитики.
Классические муколитики
Классические муколитики работают, разрушая муциновую сеть, которая изначально формирует слизистый слой. Разрушая структуры, удерживающие слизь, классические муколитики облегчают удаление мокроты из дыхательных путей. Классические муколитики включают ацетилцистеин, карбоцистеин, эрдостеин и фудостеин.
Пептидные муколитики
Пептидные муколитики не воздействуют на муциновую сеть, обнаруженную в слизистом слое.Вместо этого они нацелены на белки и связи ДНК, которые обычно находятся в гное. Пептидные муколитики полезны при густой гнойной слизи, характерной для муковисцидоза, который часто связан с респираторными инфекциями. Пептидные муколитики включают дорназу альфа и тимозин бета-4.
Кому можно принимать муколитики?
Взрослые
Муколитики могут назначаться взрослым с хроническими респираторными заболеваниями, такими как ХОБЛ и хронический бронхит. Клинические испытания показали, что применение муколитических препаратов может привести к меньшему количеству обострений у пациентов с ХОБЛ или хроническим бронхитом по сравнению с плацебо.У тех, кто принимал муколитические препараты, было мало побочных эффектов. Более ранние исследования также предполагали, что муколитики также могут улучшать качество жизни.
Муколитики работают лучше всего при регулярном приеме, и может потребоваться прием нескольких доз в течение дня. Муколитики доступны в виде растворов для ингаляций, растворов для внутривенного введения, пероральных шипучих таблеток, пероральных таблеток, капсул и пероральных растворов. Если муколитические средства вводят в виде раствора для ингаляций, используют небулайзер.Перед введением ингаляционного раствора может быть рекомендовано применение аэрозольных бронхолитиков для повышения эффективности муколитика.
Муколитики доступны в виде растворов для ингаляций, растворов для внутривенного введения, пероральных шипучих таблеток, пероральных таблеток, капсул и пероральных растворов. Если муколитические средства вводят в виде раствора для ингаляций, используют небулайзер.Перед введением ингаляционного раствора может быть рекомендовано применение аэрозольных бронхолитиков для повышения эффективности муколитика.
При передозировке тайленола ацетилцистеин следует вводить как можно ближе к моменту передозировки и в течение восьми часов после приема тайленола.
Дети
Младенцы, дети и подростки могут безопасно принимать муколитики. Дорназа альфа используется для лечения муковисцидоза и вводится с помощью распыляемого раствора для ингаляций.Было показано, что у маленьких детей и младенцев дорназа альфа полезна при муковисцидозе, даже у тех, у кого проявляются только ранние признаки или симптомы заболевания.
Ацетилцистеин можно вводить детям через небулайзер или клизму. В случае передозировки тайленола доза ацетилцистеина рассчитывается в зависимости от веса ребенка.
В случае передозировки тайленола доза ацетилцистеина рассчитывается в зависимости от веса ребенка.
Пожилые люди
Пожилые люди могут безопасно принимать муколитики. Дозирование такое же, как для взрослых, и не требует коррекции.
Можно ли принимать муколитики во время беременности или кормления грудью?
Муколитики, как правило, безопасны для использования во время беременности. Некоторые муколитические средства, такие как ацетилцистеин, могут быть предпочтительнее других во время беременности. Хотя риск причинения вреда при применении муколитиков в период грудного вскармливания низок, муколитики следует применять только в случае необходимости или если польза превышает потенциальный риск. Проконсультируйтесь с врачом перед использованием муколитического препарата во время беременности или кормления грудью.
Безопасны ли муколитики?
В целом муколитики безопасны и хорошо переносятся. Токсичность муколитиков встречается редко и чаще всего связана с внутривенным введением препаратов. Некоторым группам людей следует избегать муколитиков или наблюдать за побочными эффектами во время лечения.
Некоторым группам людей следует избегать муколитиков или наблюдать за побочными эффектами во время лечения.
Прежде чем принимать муколитик, сообщите своему лечащему врачу, если у вас есть какие-либо из следующих симптомов:
- Язвенная болезнь
- Варикоз пищевода
- Слезы Мэллори-Вайс
- Язвы желудка
- Использование других лекарств
- Аллергические реакции на муколитические средства
- Аллергические реакции на клеточные продукты яичника китайского хомячка (СНО)
Отзыв муколитика
В настоящее время отзывов муколитических препаратов нет.
Муколитические ограничения
Взрослым и детям с аллергией на хомяков следует избегать применения Пульмозима (дорназа альфа).
Муколитики не рекомендуется использовать у пациентов с пептической язвой, варикозным расширением вен пищевода, синдромом Мэллори-Вейса или подобными состояниями. Муколитики могут вызвать рвоту, которая может ухудшить эти состояния.
Муколитики могут вызвать рвоту, которая может ухудшить эти состояния.
Поговорите с поставщиком медицинских услуг, чтобы определить другие потенциальные ограничения, связанные с муколитиками.
Являются ли муколитики контролируемыми веществами?
Нет, муколитики не являются контролируемыми веществами.
Распространенные побочные эффекты муколитиков
Побочные эффекты муколитиков могут различаться в зависимости от препарата и состава. Наиболее распространенные побочные эффекты муколитиков могут включать:
- Тошнота
- Рвота
- Диарея
- Головная боль
- Лихорадка
- Насморк
- Боль в горле
- Сонливость
- Сыпь
Более тяжелые, но редкие побочные эффекты включают:
- Натяжение груди
- Проблемы с дыханием
- Желудочные кровотечения или язвы
В редких случаях муколитики могут вызывать реакции гиперчувствительности или аллергические реакции. Немедленно обратитесь за медицинской помощью, если у вас появились признаки аллергической реакции, такие как сильная сыпь или отек лица или горла.
Немедленно обратитесь за медицинской помощью, если у вас появились признаки аллергической реакции, такие как сильная сыпь или отек лица или горла.
В редких случаях N-ацетилцистеин может вызывать боль в груди, высокое или низкое кровяное давление или кожную сыпь. Риск аллергической реакции может увеличиваться при внутривенном введении N-ацетилцистеина. N-ацетилцистеин может действовать как раздражитель при введении в виде аэрозоля.
Другие менее распространенные побочные эффекты дорназы альфа включают боль в груди и конъюнктивит.Аллергические реакции на дорназу альфа возникают редко.
Этот список побочных эффектов не является исчерпывающим. Побочные эффекты, как правило, слабо выражены и проходят сами по себе, а муколитики считаются безопасными для применения у взрослых и детей всех возрастов. Поговорите со своим врачом, если вы испытываете побочные эффекты, которые особенно беспокоят во время лечения.
Перед началом лечения муколитиками проконсультируйтесь с врачом для получения полного списка побочных эффектов, предупреждений и мер предосторожности.

/93.jpg)
 Если ответ утвердительный, нужны не препараты «от кашля», а антисептики, смягчающие и противовоспалительные средства для горла, например, те же леденцы.
Если ответ утвердительный, нужны не препараты «от кашля», а антисептики, смягчающие и противовоспалительные средства для горла, например, те же леденцы. По такому принципу действуют средства на основе растительных экстрактов (тимьяна, плюща, аниса, мать-и-мачехи, подорожника, солодки и др.), например, Геделикс, Бронхикум, Линкас. Внимание! Детям младшего возраста опасно использовать эти препараты, так как они увеличивают объем мокроты, а их дыхательная мускулатура еще недостаточно развита, поэтому ребенок не сможет все откашлять. Тем временем, в сгустке мокроты размножаются болезнетворные бактерии.
По такому принципу действуют средства на основе растительных экстрактов (тимьяна, плюща, аниса, мать-и-мачехи, подорожника, солодки и др.), например, Геделикс, Бронхикум, Линкас. Внимание! Детям младшего возраста опасно использовать эти препараты, так как они увеличивают объем мокроты, а их дыхательная мускулатура еще недостаточно развита, поэтому ребенок не сможет все откашлять. Тем временем, в сгустке мокроты размножаются болезнетворные бактерии. К тому же препараты на основе ацетилцистеина способны усиливать бронхоспазм, поэтому часто врачи выписывают их вместе с бронхолитиками. Также учтите, что и карбоцистеин, и ацетилцистеин противопоказаны при язвенной болезни желудка (в стадии обострения).
К тому же препараты на основе ацетилцистеина способны усиливать бронхоспазм, поэтому часто врачи выписывают их вместе с бронхолитиками. Также учтите, что и карбоцистеин, и ацетилцистеин противопоказаны при язвенной болезни желудка (в стадии обострения).
 5 % соответственно.[9][12] Сообщается, что повышение артериального давления, респираторный дистресс, боль в груди, лихорадка, ректальное кровотечение, головная боль, гипотония, вялость и кожная аллергия встречаются менее чем в 5% случаев. Аэрозольный N-ацетилцистеин плохо переносится из-за его раздражающего действия и очень неприятного запаха, который может вызвать рвоту. Высокая частота анафилактических реакций наблюдается у пациентов, получающих внутривенно N-ацетилцистеин.[13]
5 % соответственно.[9][12] Сообщается, что повышение артериального давления, респираторный дистресс, боль в груди, лихорадка, ректальное кровотечение, головная боль, гипотония, вялость и кожная аллергия встречаются менее чем в 5% случаев. Аэрозольный N-ацетилцистеин плохо переносится из-за его раздражающего действия и очень неприятного запаха, который может вызвать рвоту. Высокая частота анафилактических реакций наблюдается у пациентов, получающих внутривенно N-ацетилцистеин.[13] [6]
[6] [2]
[2]