Цитомегаловирус у новорожденных: лечение инфекции
Цитомегаловирус у новорожденных встречается достаточно часто. Инфицирование происходит во время внутриутробного развития или после родов. Только в 10–15% случаев признаки заболевания проявляются у малышей непосредственно после появления на свет. Дети с бессимптомным течением цитомегаловирусного синдромома рождаются клинически здоровыми. Обнаружить у них активную форму цитомегаловирусной инфекции можно только после лабораторного исследования. Чем раньше предпринять лечебные меры против врожденной формы болезни, тем лучше будет результат.

Что такое цитомегаловирусная инфекция
Цитомегаловирусная инфекция (цитомегалия) — это вирусное заболевание, возбудителем которого является цитомегаловирус (ЦМВ) человека из семейства герпесвирусов. В основном он поражает слюнные железы (особенно околоушную). При самой тяжелой форме патологический процесс распространяется на другие органы — легкие, печень, почки, надпочечники, кишечник, пищевод, поджелудочную железу, сетчатку глаз, и даже на головной мозг. У слабых и недоношенных грудничков бывают внутренние кровотечения и омертвление клеток в организме.
Под действием вируса происходит рост клеток, которые увеличиваются до гигантских размеров (в 30–40 раз). Внутри них появляется плотное крупное внутриядерное включение. Оно делает клетку похожей на совиный глаз.
Наиболее опасен вирус для плода на стадии эмбрионального развития, если беременная женщина была впервые инфицирована цитомегаловирусом. Вследствие отсутствия у будущей матери антител к возбудителю заболевания, неослабленный вирус поражает эмбрион и нарушает его формирование. Вирус представляет серьезную опасность и для плода на более поздней стадии развития. Цитомегаловирус способен преодолевать плацентарный барьер и влиять на здоровье ребенка. При первичном заражении беременной инфицирование плода происходит в 40–50% случаев.
- Если женщина инфицирована вирусом не впервые, ее антитела ослабляют возбудителей заболевания и снижают их агрессивное воздействие на плод. В таких случаях риск заражения ребенка составляет не более 1–2 %.
- Вероятность инфицирования увеличивают постоянные стрессы, неполноценное питание, малоподвижный образ жизни и хронические заболевания.
- Коварство цитомегаловирусной инфекции заключается в ее способности протекать скрыто или маскироваться под острую респираторно-вирусную инфекцию. По этой причине заболевание у беременных часто не диагностируют.
Обнаружение антител к ЦМВ у новорожденных не свидетельствует об их инфицировании. Передача антител может осуществляться через плаценту от мамы к плоду при беременности . Диагноз цитомегаловирусной инфекции ставится при выявлении возбудителей заболевания в моче, крови и слюне.
Врожденная цитомегаловирусная инфекция
Если женщина была заражена вирусом в первые двенадцать недель беременности, возбудители заболевания могут спровоцировать самопроизвольный аборт или гибель плода. У эмбриона возникают серьезные нарушения развития, несовместимые с жизнью. Если плоду удается выжить, вирус вызывает у него тяжелые пороки. Некоторые из них относят к генетическим (синдром Денди-Уокера).
Наиболее серьезные пороки развития возникают у детей, если у беременной обнаружили цитомегалию впервые. В результате поражения инфекцией у детей развивается микроцефалия (уменьшение головного мозга), гепатоспленомегалия (увеличение селезенки и печени), тромбоцитопения (уменьшение количества тромбоцитов, вызывающее снижение свертываемости крови) и затянувшаяся желтуха (гипербилирубинемия).
Инфекция поражает нервную систему плода, провоцируя тяжелые заболевания (дебют эписиндрома и устойчивую к терапии эпилепсию, неокклюзивные гидроцефалии, детский церебральный паралич, аутизм). В отдельных случаях цитомегаловирусная инфекция у новорожденных может стать причиной глухоты, ухудшения зрения и умственной отсталости.
Но чаще всего инфекция вызывает поражения мозга. У детей с врожденной формой цитомегаловирусной инфекции диагностируют менингоэнцефалит (воспаление оболочек и вещества головного мозга), патологию желудочков мозга, кальцификаты (отложения солей в мягких тканях) и «кальцинацию» мозговых сосудов (минерализационная васкулопатия). Все эти патологии сопровождаются нарушениями неврологического характера (церебральными изменениями, гипертензионно-гидроцефальным синдромом). Минерализационная васкулопатия часто становится причиной судорожного синдрома у новорожденного.
- Распространенным проявлением цитомегаловирусной инфекции является блокада ликвороносных путей.
- Она диагностируется в 7% случаев при повреждении мозга вирусной инфекцией.
- Вирус поражает сосудистое сплетение желудочков мозга и вызывает появление в нем кист.
Если заражение произошло во втором и третьем триместре беременности, вирус может спровоцировать геморрагический синдром, гемолитическую анемию, цирроз печени, интерстициальную пневмонию, энтерит, колит, поликистоз поджелудочной железы и нефрит.
Приобретенная форма цитомегаловирусной инфекции
Сразу после появления на свет новорожденный в 30% случаев инфицируется цитомегаловирусом от своей матери через биологические жидкости, содержащие вирус (слюну, грудное молоко, мочу, выделения из гениталий, кровь). Малыш также может заразиться от других людей.
Как считает педиатр Евгений Комаровский, если у ребенка хорошо развита иммунная система, возбудители заболевания неспособны вызвать у него серьезные заболевания. Перед вирусом уязвимы недоношенные детки, а также малыши с иммунодефицитом. У них может возникнуть продуктивный перибронхит или затяжная пневмония.
Иногда после заражения цитомегаловирусом у слабых младенцев увеличиваются лимфатические узлы, развивается гепатит. В почках могут появиться цитомегалические изменения канальцевого эпителия. Вирус способен вызвать язвенное поражение в кишечнике ребенка. Такие дети тяжело и долго излечиваются. Они часто отстают в развитии.
У малышей с приобретенной формой цитомегаловирусной инфекции не возникают поражения мозга.
Острая форма врожденного заболевания
Врожденная цитомегаловирусная инфекция может протекать в острой и хронической формах. При остром течении заболевания первые признаки заболевания проявляются сразу после рождения ребенка или на протяжении первых 24 часов.
У младенца поднимается температура тела. На лице, теле и на конечностях становятся заметными пятна синюшно-фиолетового цвета. У младенца могут появиться кровоизлияния в слизистые оболочки и кровь в кале (гемоколит). Иногда из пупочной ранки продолжает сочиться кровь. О развивающемся гепатите будет свидетельствовать желтизна кожного покрова.
Если у новорожденных поражен мозг, у них с первых часов жизни может возникнуть судорожный синдром. Он продолжается до 5 дней и больше. Дрожание верхних конечностей происходит на фоне повышенной сонливости.
Острая врожденная цитомегаловирусная инфекция может проявляться в виде нарушений координации, слуха и зрения. Иногда она вызывает слепоту. У малыша нередко развивается пневмония. Слабый иммунитет и присоединение другой острой инфекции могут привести к смерти новорожденного.
Хроническая форма врожденного заболевания
Хроническая форма цитомегаловирусной инфекции может протекать манифестно и бессимптомно. Симптомы манифестного течения заболевания проявляются в виде нарушений зрения. Помутнение хрусталика и стекловидного тела становятся причиной ухудшения или полной потери зрительного восприятия. У грудного ребенка обнаруживают гидроцефалию, эпилепсию, микрогирию (структурные нарушения в коре головного мозга), микроцефалию или признаки детского церебрального паралича.
Малыш с хронической формой цитомегаловирусной инфекции отстает в развитии и плохо набирает вес. В старшем возрасте обнаруживаются речевые дефекты и задержка умственного развития.
Хроническая цитомегаловирусная инфекция не всегда диагностируется в первые недели после рождения малыша. Поэтому лечение заболевания начинают иногда слишком поздно. Ранняя диагностика и своевременная терапия позволяют не допустить ухудшение зрения, остановить прогрессирование эпилепсии, гидроцефального синдрома и других патологий. В большинстве случаев удается избежать отставания в развитии. Дети с аутизмом, получившие адекватное лечение, способны обучаться в обычных общеобразовательных школах.
Труднее всего обнаружить скрытую форму хронической цитомегаловирусной инфекции у новорожденного. Такие младенцы не имеют видимых признаков заболевания. Если после рождения ребенка не были проведены лабораторные исследования, инфицирование не будет обнаружено длительное время.
Характерным признаком поражения цитомегаловирусом является склонность к бактериальным инфекциям. Нередко на первом году жизни ребенка одолевают заболевания бактериального происхождения. У него диагностируют пиодермию (гнойное поражение кожи), рецидивирующие стоматиты, отиты, гаймориты, бронхиты, пневмонии, циститы, пиелонефриты. В некоторых случаях симптомы цитомегаловирусной инфекции обнаруживают только в школьном возрасте.
Таким детям противопоказаны прививки. Вакцинация может спровоцировать у них аутизм, эпилепсию, детский церебральный паралич или умственную отсталость.
Лечение вирусного заболевания
В настоящее время при цитомегаловирусной инфекции у новорожденных назначаются инъекции иммуноглобулина в вену. Сразу после рождения младенцу вводят гипериммунный иммуноглобулин «Цитотект». Препарат содержит в 10 раз больше антител к цитомегаловирусу, чем другие иммуноглобулины. Он изготавливается из крови доноров, имеющих большое количество выработанных организмом антител. «Цитотект» содержит и антитела к микробным возбудителям заболеваний, чаще всего поражающих новорожденных в послеродовом периоде.
Значительное улучшение состояния младенца наблюдается через 7–8 дней после введения препарата «Цитотект». В крови активно вырабатываются собственные противоцитомегаловирусные и противогерпетические антитела.
Для лечения заболеваний, вызванных бактериями, применяются антибиотики. Чаще всего назначается новорожденным комбинированный препарат с широким спектром бактерицидного действия «Сульперазон». Он содержит цефалоспорины 3 поколения (цефоперазон и сульбактам). «Сульперазон» вводят сначала внутривенно, а затем и внутримышечно. Курс лечения составляет 8–14 дней. Чтобы малыш быстрее излечился, его оберегают и от других инфекций.
venerologia03.ru
Цитомегаловирус у новорожденных: последствия и лечение
Цитомегаловирус у новорожденных детей бывает врожденным и приобретенным. В первом случае наблюдаются тяжелые пороки развития. При данной патологии высока вероятность летального исхода.
Цитомегаловирусная инфекция у детей
Цитомегалией называется инфекционное заболевание вирусной этиологии. Первичное заражение чаще всего не приводит к проявлению болезни. Внутриутробным (трансплацентарным) способом заражается 5-7% детей инфицированных матерей. Данная патология относится к группе TORCH-инфекций. Это означает, что инфицирование во время беременности представляет опасность для будущего малыша.
Данная проблема очень актуальна, так как в 20-30% случаев первичной (врожденной) инфекции наблюдается летальный исход. Остальные же дети отстают от своих сверстников в развитии. Часто инфицирование младенца происходит во время родов при прохождении через родовые пути. Иногда новорожденные заражаются от матерей в постнатальном периоде. Возбудителем заболевания является вирус герпеса.
Клинические проявления инфекции
При врожденном цитомегаловирусе симптомы разнообразны. Признаки заболевания появляются в течение 21 дня с момента рождения. При данной патологии наблюдаются:
- микроцефалия;
- менингит;
- гидроцефалия;
- энцефалит;
- увеличение сердца;
- миокардит;
- хориоретинит;
- кератоконъюнктивит;
- помутнение хрусталика;
- врожденная глухота;
- аномалии развития челюсти;
- лихорадка;
- низкий вес;
- обильная экзантема;
- нарушение зрения вплоть до полной слепоты;
- головная боль;
- судороги;
- увеличение печени и селезенки;
- желтуха;
- параличи;
- синдром Денди-Уокера.

Основные признаки цитомегаловируса у новорожденных детей — низкая/экстремально низкая масса тела и поражения внутренних органов.
У ребенка с врожденной ЦМВИ возможно недоразвитие головного мозга и черепа. Данное состояние называется микроцефалией. Это тяжелый порок развития центральной нервной системы. В норме окружность черепа новорожденных малышей составляет 35-37 см. При микроцефалии она равна 25-27 см. При этом вес мозга составляет всего около 250 г.
При микроцефалии у грудничка возможны следующие признаки:
- преобладание лицевого отдела черепа;
- узкий лоб;
- крупные уши;
- выступающие надбровные дуги;
- диспропорциональное телосложение;
- мышечная дистония;
- косоглазие;
- судороги;
- нарушение координации движений.
У таких малышей наблюдается задержка умственного и физического развития. Они позже других детей начинают ходить, нередко развивается олигофрения. Такие дети требуют постоянного ухода. Наряду с микроцефалией при цитомегаловирусной инфекции возможно развитие гидроцефалии. Это менее опасное состояние, характеризующееся накоплением в головном мозге цереброспинальной жидкости.
Основными признаками гидроцефалии являются:
- большая голова;
- выбухание вен;
- отек диска зрительного нерва;
- истончение кожи в области головы;
- расхождение швов в области родничка;
- снижение зрения;
- гипертонус мышц нижних конечностей;
- ограничение подвижности глазных яблок.
У новорожденного малыша, страдающего цитомегаловирусной инфекцией, часто выявляется менингит. При нем воспаляются мозговые оболочки. Основными симптомами являются отказ от еды, лихорадка, вялость, бледность кожи лица, плаксивость, сонливость, повышенная пульсация сосудов в области родничка и судороги.
Поражения кожи и глаз
Наличие цитомегаловируса у грудничка чревато развитием хориоретинита и катаракты. В тяжелых случаях наблюдается полная слепота. Частым признаком цитомегаловирусной инфекции является хориоретинит. Это воспаление сетчатки и сосудистой оболочки глаза. Основными признаками хориоретинита являются:
- искажение зрительных образов;
- нечеткость предметов;
- световые вспышки;
- нарушение темновой адаптации;
- снижение остроты зрения;
- нарушение восприятия цветов.
Реже при цитомегаловирусной инфекции у новорожденных выявляется кератоконъюнктивит. Он проявляется сухостью, болью, слезотечением и повышенной чувствительностью глаз к яркому свету. Очень опасно для инфицированных детей помутнение хрусталика. Это тоже проявление зрительных расстройств на фоне ЦМВИ. Врожденная катаракта характеризуется наличием белого пятна, косоглазием, нистагмом и дрожанием глазного яблока.
При цитомегаловирусной инфекции у новорожденных изменяется цвет кожи. Он приобретает желтоватый оттенок. Причина — желтуха. Нередко в процесс вовлекаются видимые слизистые. Специфическим признаком врожденной цитомегалии является петехиальная сыпь. Она обильная и локализуется на разных участках тела. Экзантема при данной патологии напоминает краснуху. Петехиальные высыпания в виде кровоизлияний встречаются в 60-80% случаев врожденной инфекции.
Другие проявления инфекции
При цитомегалии иногда развивается синдром Денди-Уокера. Это тяжелый порок развития, характеризующийся аномалией 4 желудочка, образованием ликворной кисты в области задней черепной ямки и отсутствием червя мозжечка. Частота встречаемости этой патологии у новорожденных составляет 1:25000.
Основными клиническими проявлениями синдрома Денди-Уокера являются:
- замедленное моторное развитие ребенка;
- расширение черепа;
- увеличение объема головы;
- нистагм.
В будущем у таких детей появляются зрительные расстройства, тошнота, раздражительность, мозжечковая атаксия и признаки поражения черепных нервов. Синдром Денди-Уокера нередко сочетается с иными аномалиями.
Часто инфицирование младенца происходит во время родов при прохождении через родовые пути. Иногда новорожденные заражаются от матерей в постнатальном периоде.
Другие последствия цитомегаловирусной инфекции у новорожденных включают миокардит. При нем наблюдаются такие симптомы, как одышка, боль в области сердца, артериальная гипотензия, увеличение в объеме сердца, частый пульс, бледность кожных покровов ребенка и нарушение сердечного ритма.
План обследования малышей
Лечение больных детей проводится после комплексного обследования. Понадобятся следующие исследования:
- иммунологический анализ;
- общий и биохимический анализ крови;
- анализ мочи;
- полимеразная цепная реакция;
- неврологический осмотр;
- физикальное исследование;
- магнитно-резонансная томография;
- неврологический осмотр.
Наиболее информативны выделение вируса путем посева крови малыша на питательную среду, полимеразная цепная реакция и иммуноферментный анализ. ПЦР-исследование позволяет обнаружить геном цитомегаловируса. Материалом могут быть моча, кровь, слюна и спинномозговая жидкость ребенка. Очень информативна серодиагностика. С ее помощью можно обнаружить специфические антитела (IgG и IgM) в крови малыша.
Лечение и профилактические меры
При обнаружении цитомегаловируса у новорожденных детей необходимы:
- иммуноглобулины;
- интерфероны;
- иммуномодуляторы;
- витамины;
- симптоматические лекарства;
- полноценное питание.

Своевременная диагностика цитомегаловируса у будущей мамы — залог рождения здорового малыша.
Больным детям назначаются интерферон и иммуноглобулин человеческий. Очень эффективен против цитомегаловируса Неоцитотект. Это иммунологический препарат, выпускаемый в форме раствора для инфузий. Он содержит антитела к возбудителю инфекции. При тяжелой форме цитомегалии могут назначаться противовирусные препараты.
При данной патологии проводится симптоматическая терапия. В случае развития миокардита могут назначаться лекарства, улучшающие обменные процессы в сердечной мышце, а также системные кортикостероиды. При низком давлении применяются препараты, которые его повышают. Если же у ребенка выявлена гидроцефалия, то может понадобиться хирургическое вмешательство. Применение диуретиков малоэффективно.
В случае развития у новорожденного синдрома Денди-Уокера лечение является только симптоматическим. Нередко требуется шунтирование. В дальнейшем такие дети нуждаются в постоянном уходе. Устранить интеллектуальные нарушения при данной патологии невозможно. Самолечение новорожденных недопустимо.
В настоящее время экспериментально применяется вакцина против цитомегаловируса. Она показала свою эффективность, но пока не нашла широкого применения. Прогноз при цитомегалии у новорожденных относительно неблагоприятный. Возможен летальный исход. Основными мерами профилактики заболевания у новорожденных малышей являются:
- исключение незащищенных половых контактов у женщины до беременности;
- своевременное лечение инфекции у будущей мамы;
- планирование беременности;
- применение противовирусных препаратов людям из групп риска;
- плановое обследование во время беременности.
Таким образом, цитомегаловирус легко проникает через плаценту и поражает плод. Чтобы избежать заражения малыша, следует своевременно обращаться к врачу и проходить курс терапии.
Еще по этой теме:
herpesdoc.ru
Цитомегаловирус у новорожденных: причины, симптомы, осложнения
Содержание статьи
Цитомегаловирусная инфекция у новорожденных – это распространенное заболевание, которое вызывается вирусом герпеса. У больных детей часто диагностируется поражение головного мозга, почек, нарушение физического развития. В тяжелых случаях инфекция может привести к летальному исходу. Цитомегаловирус у новорожденных длительное время может протекать скрыто, не проявляя никаких симптомов.

Ребенок часто болеет?
Ваш ребенок постоянно болеет?
Неделю в садике (школе), две недели дома на больничном?
В этом виновато много факторов. От плохой экологии, до ослабления иммунитета ПРОТИВОВИРУСНЫМИ ПРЕПАРАТАМИ!
Да-да, вы не ослышались! Пичкая своего ребенка мощными синтетическими препаратами вы, порой, наносите больше вреда маленькому организму.
Чтобы в корне изменить ситуацию, необходимо не губить иммунитет, а ПОМОГАТЬ ЕМУ…
Читать подробнее
Проявляется цитомегалия, когда младенец ослаблен и у него есть иммунодефицит. Грудничок с ЦМВИ внешне отличается малым весом, у него может быть сыпь на коже, он малоактивен.
При цитомегаловирусной инфекции у новорожденного симптомы будут отличаться зависимо от состояния иммунной системы. При нормальной защите у ребенка могут проявляться легкие симптомы схожие с простудой.
Для грудничков с ослабленным иммунитетом характерны такие признаки:
- синюшность кожи на фоне отека легких и бронхов;
- генерализованная сыпь на теле, которую дифференцируют с диатезом;
- воспалительный процесс в носоглотке и гортани;
- высокая температура тела до 39 градусов.
При наличии подобной симптоматики новорожденного осматривает специалист, забираются анализы на выявление вируса. При подтверждении диагноза ребенку назначается симптоматическая терапия. Незначительные проявления схожие с простудой уходят уже через 2 недели. Осложненное течение при цитомегаловирусной инфекции будет характеризоваться наличием лихорадки, мононуклеоза и ангины длительное время.
Причины
Заражается ребенок в период внутриутробного развития или во время родов. Такой исход возможен в случае приобретенного заболевания матери во время беременности. На развитие заболевания и выраженность клинических симптомов будет влиять период заражения и механизмы передачи вируса.
Заражение ребенка происходит следующими путями:
- антенатальным – при внутриутробном формировании вирус проникает через плаценту;
- интранатальным – ребенок заражается во время родов;
- постнатальным – у ребенка диагностируется приобретенная инфекция, он заряжается с молоком матери или при контакте с больным.

Наиболее тяжелые последствия для ребенка возможны в случае внутриутробного заражения. Тогда вирус в большом количестве находится в околоплодных водах, попадая в пищеварительную систему, легкие и другие органы плода. В 50% случаев вирус проникает в плаценту при первичном заражении матери в период беременности.
Почему иммунитет моего ребенка ослаблен?
Многим знакомы эти ситуации:
Читать статью
Также причиной может быть обострение скрытого цитомегаловируса у женщины. Но в таком случае у беременной уже есть антитела, которые снижают риск заражения ребенка и защищают его от тяжелых последствий.
Еще лучше, когда у женщины есть антитела и отсутствуют признаки заболевания, тогда риск заражения ребенка практически отсутствует.
Наибольшую угрозу для плода представляет инфицирование матери в первый и второй триместр. В таком случае заболевание может привести к выкидышу, так как плод не способен выделять антитела для своей защиты. Уже в третьем триместре у него появляются антитела, и тогда риск заражения и осложнений минимален. Вероятность заражения во время родов не превышает 5%, даже когда у матери в организме присутствует активный вирус. Уже после рождения заражение происходит с молоком матери или при тесном контакте с больным.
Во время вскармливания больной матерью заражение происходит в 60% случаев. Если в это время заражения не произошло, первый контакт с вирусом будет ждать ребенка в возрасте от 2 до 6 лет, когда он посещает детский сад и школу. Цитомегаловирус может передаваться от вирусоносителя воздушно-капельным, контактным, бытовым путем. У здорового ребенка с крепким иммунитетом симптомы заболевания не будут проявляться, но после попадания вируса, он будет выделять его в течение 2 лет.
Клиническая картина
Симптомы отличаются зависимо от того, врожденная это или приобретенная инфекция. При врожденной форме наблюдается желтуха новорожденных, нарушение глотания, недоношенность, кожная сыпь. У ребенка может быть увеличена селезенка и другие органы. Нередко диагностируется глухота, слепота, гидроцефалия, микроцефалия, косоглазие. Реже появляются патологии сердечно-сосудистой и пищеварительной системы, а также опорно-двигательного аппарата.

Отсутствие этих нарушений еще не говорит о полном здоровье ребенка и отсутствии вируса. Проявиться заболевание может не сразу, отсроченные симптомы можно наблюдать даже спустя 10 лет.
Это может быть нарушение интеллектуального и физического развития, отсутствие некоторых зубов, ухудшение слуха и зрения.
При заражении во время родов первые симптомы проявляются в течение 2 месяцев жизни. Уже тогда можно увидеть нарушение физического и умственного развития, снижение активности, патологии слюнных желез, судороги, нарушение зрения, мелкие подкожные кровоизлияния. При наличии вируса, но отсутствии симптомов, заболевание переходит в латентную форму, и может никогда не проявиться.
Здоровый организм ребенка хорошо справляется с вирусом без внешних проявлений, но в определенные моменты могут появляться некоторые симптомы.
Мононуклеозоподобный синдром при цитомегаловирусе:
- мышечные боли и быстрая утомляемость;
- озноб, высокая температура тела;
- увеличение лимфатических узлов;
- насморк, белый налет на языке и деснах.
Симптомы могут продолжаться до 2 недель и даже нескольких месяцев. Но при этом ребенок не нуждается в специфическом лечении, показаны только симптоматические препараты для улучшения его самочувствия.
Острый цитомегаловирус
Острая фаза заболевания продолжается от 2 недель до 3 месяцев. Для этого периода будут характерны признаки общей интоксикации организма. Под действием вируса перестраивается иммунная система, она готовится к вторжению чужеродного микроорганизмы. Острые проявления говорят о нормальной работе иммунной системы и борьбе с вирусом, но когда защитных сил не хватает, ЦМВИ переходит в скрытую форму. Тогда появляются заболевания внутренних органов, сосудисто-вегетативные нарушения.
Есть 3 варианта течения цитомегаловирусной инфекции:
- С признаками острой респираторной вирусной инфекции. У ребенка будут отмечаться все симптомы ОРВИ. Это общее недомогание, головные боли, насморк, слабость, быстрая утомляемость, высокая температура тела, увеличение слюнных желез, белый налет на деснах и языке, реже воспаляются небные миндалины.
- Генерализованная форма. Вирус поражает внутренние органы, включая надпочечники, селезенку, поджелудочную железу, почки. Инфекция может стать причиной воспаления легких, бронхита. Поражается желудочно-кишечный тракт, нарушается питание глазного яблока, проявляется дисфункция нервной системы и головного мозга. Из внешних признаков можно наблюдать кожную сыпь и увеличение слюнных желез.
- С признаками поражения органов мочеполовой системы. Проявляется периодическим воспалением мочевыводящей системы, которое плохо поддается лечению.
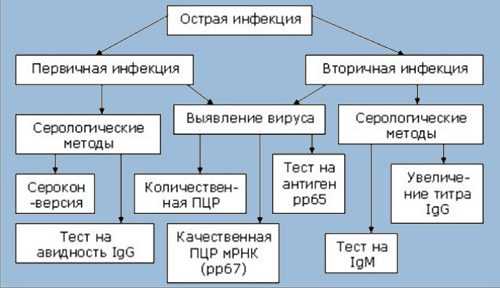
Диагностика
Для выявления цитомегаловируса применяются следующие методики:
- полимеразная цепная реакция;
- выявление антител в сыворотке крови или иммуноферментный анализ;
- выявление возбудителя инфекции в биологических жидкостях;
- культуральный посев.

При осложненном течении инфекции ребенку может потребоваться ультразвуковая диагностика, МРТ головного мозга.
Лечение
Специфического лечения цитомегаловирусной инфекции нет. Проводится симптоматическая терапия и укрепление иммунной системы для способности организма самостоятельно справляться с признаками инфекции.
Назначаются противовирусные препараты против герпеса – это Валацикловир, Ганцикловир, Валганцикловир. При сопутствующей бактериальной инфекции назначаются антибиотики. Эти препараты вместе с иммуномодуляторами позволяют вывести заболевания в неактивную форму.
Профилактика
Профилактика цитомегаловируса у новорожденного начинается еще в период планирования беременности. Женщина должна сдать анализы на выявление вируса. Если он присутствует в организме, риск заражения есть, но незначительный, так как у беременной будут антитела, защищающие плод.

При отсутствии цитомегаловируса у женщины до зачатия следует руководствоваться общей профилактикой заражения вирусными инфекциями в период беременности.
Применяется также вакцинация, но она оказывается малоэффективной, и защищает только половину женщин.
Последствия ЦМВИ
При первичном заражении матери во время беременности возможны такие последствия для плода:
- нарушение формирования перегородок сердца;
- аномалии легочного ствола и строения почек;
- увеличение легких;
- микрогирия и макрогерия;
- микроцефалия.
Заражение беременной на позднем сроке приводят к желтухе у новорожденного, воспалению легких, нефриту, гидроцефалии, колиту, энтериту, менингоэнцефалиту, анемии.
До сих пор не разработано эффективных профилактических средства для лечения и профилактики вируса, и единственной защитой будет соблюдение гигиены и регулярное обследование у врача.
Это может быть интересно:
Если ребенок постоянно болеет — его иммунитет НЕ РАБОТАЕТ!
 Иммунная система человека создана для того, чтобы противостоять вирусам и бактериям. У малышей она еще сформирована не полностью и работает не во всю силу. А тут еще родители «добивают» иммунитет противовирусными средствами, приучая его к расслабленному состоянию. Свою лепту вносит плохая экология и широкое распространение разных штаммов вируса гриппа. Необходимо закалять и прокачивать иммунную систему и делать это нужно НЕМЕДЛЕННО!
Иммунная система человека создана для того, чтобы противостоять вирусам и бактериям. У малышей она еще сформирована не полностью и работает не во всю силу. А тут еще родители «добивают» иммунитет противовирусными средствами, приучая его к расслабленному состоянию. Свою лепту вносит плохая экология и широкое распространение разных штаммов вируса гриппа. Необходимо закалять и прокачивать иммунную систему и делать это нужно НЕМЕДЛЕННО!Читайте статью: Как избавиться от ЧАСТЫХ ПРОСТУД ребёнка и наконец-то перестать его «лечить» вредными и дорогими таблетками
infectium.ru
врождённая и хроническая ЦМВИ, как лечить, последствия
Цитомегаловирус – болезнь, которая передаётся грудничку от матери. Цитомегаловирус у новорождённых протекает по-разному, но всегда несёт тяжёлые последствия для здоровья. Несвоевременная диагностика приводит к задержкам в развитии и патологиям внутренних органов у грудничка.
Как происходит заражение
У грудничка герпес 5 типа, которым и является цитомегаловирус, «селится» в организме через контакт с матерью. Инфицирование с разной долей вероятности происходит на любом этапе вынашивания ребёнка.
Основной путь заражения женщины во время беременности – через орогенитальный половой контакт. Цитомегаловирус начинает свою деятельность незаметно. Женщины чаще всего думают, что болеют простудой или гриппом. Плод в это время уже может быть глубоко поражён ЦМВИ.
Проникнуть в организм матери цитомегаловирус способен и через процедуру переливания крови или трансплантацию внутренних органов. Диагностировать его сложно, что в ряде случаев приводит к отторжению пересаженного органа.
Слабое состояние иммунитета – подкрепление для цитомегаловируса. Беременность забирает много сил, поэтому организм теряет устойчивость ко многим заболеваниям. Если у женщины проблемы с иммунной защитой организма, ЦМВИ легко заразит околоплодные воды. Оттуда инфекция быстро попадёт к плоду. Новорождённый в трети случаев заражается при контактах с выделениями матери: грудным молоком, слюной, кровью при прохождении родовых путей во время родов.
Цитомегаловирус при беременности: последствия для плода, диагностика (анализы)
Клинические проявления ЦМВИ у новорождённых
Узнают о заражении в 21 день жизни грудничка. ЦМВ проявляется у новорождённых в виде различных симптомов, иногда прямо противоположных. Факт их наличия даёт врачам повод для проверки на цитомегаловирус. К наиболее характерной симптоматике относят:
- микро- или гидроцефалию;
- увеличенный размер сердца, печени, селезёнки;
- глухоту;
- мутный хрусталик глаза;
- неправильно развитую челюсть;
- судороги и параличи;
- нарушение координации;
- сильно сниженную массу тела.
У младенцев в первый месяц жизни берут пробы крови. Цитомегаловирус диагностируется безошибочно, если показатель специфического антигена IgG выше нормы в 4 раза. Таким образом врачи не только отсеивают другие причины болезней, но и определяют, был ли грудничок заражён внутриутробно, или это произошло после появления на свет.
Врождённая цитомегаловирусная инфекция
У новорождённых врождённую цитомегаловирусную инфекцию часто видно по неправильному строению черепа. Впоследствии страдает головной мозг, что отрицательно сказывается на развитии грудничка.
Первый порок называется микроцефалией. Это последствие цитомегаловируса проявляется у новорождённых в виде непропорционально маленького черепа. Окружность головы грудничка при измерении меньше нормы на 10 сантиметров. Мозгу новорождённого становится тесно в черепной коробке, в итоге он лишается части функций.
Фото 1 — нормальная форма черепа, фото 2 — микроцефалия.
1 2
К прочим признакам микроцефалии у грудного ребёнка относят увеличенные уши и надбровные дуги, косое расположение глаз, плохие пропорции других частей тела – к примеру, ручки разного размера. Впоследствии таким детям сложно научиться ходить и говорить, а по мере взросления – адаптироваться к социальной жизни. Задержки умственного развития грудничка приводят к психическим заболеваниям.
Среди других проявлений инфекции – гидроцефалия с прямо противоположными симптомами. У страдающих этим заболеванием новорождённых череп непропорционально увеличен в связи с накапливанием внутри спинномозговой жидкости. Гидроцефалия гораздо менее опасна, и её возможно излечить.
Фото 1 — циркуляция линквора нарушена, фото 2 — патология отсутствует.
1 2
У новорождённых гидроцефалов не ущемляется работа мозга, но большая голова становится причиной физического дискомфорта. Глазные диски увеличены, из-за чего снижается зрение. Вены на голове набухают, а швы у родничка часто расходятся. Кроме того, новорождённому сложно двигать глазами.
Основная опасность гидроцефалии кроется в возможности менингита. Он поражает мозговые оболочки и способен привести к смертельному исходу. Первоначально диагностируется по плохому аппетиту новорождённого, вялости, бледности и сильной пульсации сосудиков у родничка.
Острая форма врождённой ЦМВИ
Иммунная система грудничка работает плохо. А под действием цитомегаловируса и вовсе начинает перестраиваться конкретно под эту болезнь. Мобилизуя все силы для борьбы с инфекцией, организм новорождённого вызывает вспышки острых проявлений ЦМВ. Они длятся от 2 до 12 недель.
Врачи выделяют три типа систем, чаще и сильнее всего страдающих при острой форме врождённой цитомегаловирусной инфекции:
- Дыхательные пути. У грудничка резко поднимается температура, возникает насморк, снижается активность. Симптомы очень напоминают ОРВИ. Однако миндалины воспаляются редко, чаще грудничок испытывает головные боли. На языке появляется много белого налёта, нехарактерного для новорождённых.
- Внутренние органы. Поражению подвержены любые органы: сердце, лёгкие и бронхи, желудочно-кишечный тракт и даже глазные яблоки. Нервная система даёт сбой в дополнение к другим нарушениям работы организма. Внешне подобные отрицательные процессы выражаются в виде сыпи по всей коже грудничка.
- Мочеполовая система. Почти не поддаётся лечению. Органы периодически воспаляются, доставляя новорождённому дискомфорт при испражнениях. Дополнительно поражаются слюнные железы.
Острые проявления цитомегалии младенца свидетельствуют о том, что организм не сдаётся. Но их не следует пускать на самотёк, ведь с каждым днём силы грудничка истощаются.
Хроническая форма врождённой ЦМВИ
Выделяют две формы протекания хронической ЦМВИ. В клинически манифестной груднички испытывают проблемы со зрением вплоть до слепоты; подвергаются болезням нервной системы – от не поддающейся лечению эпилесии до аутизма.
Во втором случае цитомегаловирус является скрытым. Он не вызывает клинических признаков болезни, внешне грудничок кажется здоровым, а его внутренние органы в порядке. Спустя несколько месяцев цитомегаловирус «взрывается», приводя к немедленной глухоте или слепоте, нарушениям умственного развития новорождённого.
Возникновение этих форм зависит от срока, на котором у плода начала развиваться инфекция.
Приобретённая форма цитомегаловирусной инфекции у грудничков
В организм новорождённого цитомегаловирус проникает через контакт с заражённой матерью. Размножается возбудитель в этом случае бессимптомно. Впервые цитомегаловирус у грудничка становятся заметным только когда он переходит в хроническую форму.
Заразиться младенец может ещё в утробе. В ранний период беременности это чаще всего приводит к выкидышу. Если плод удалось сохранить, его здоровье будет безнадёжно подорвано.
При родах инфицирование происходит случайным образом, уследить за этим врачи не в состоянии. Новорождённый может случайно вдохнуть околоплодные воды, контактировать с кровью матери. Однако первое кормление находится в ведении доктора. Если у матери было подозрение на ЦМВИ, нельзя давать ей кормить новорождённого грудью.
Методы лечения
В разработке находятся новые превентивные методы во избежание ЦМВИ у новорождённых. Хорошие результаты показывает новая вакцина против данной болезни. Позаботиться о профилактике будущая мама может и лично:
- своевременно обращаясь к врачам при первых признаках болезни, даже если это простуда;
- избегая возможных иммуносупрессивных воздействий с помощью укрепления иммунитета;
- не пропуская плановые обследования;
- занимаясь защищённым сексом;
- до беременности сдать анализы на выявление вируса.
Лечением заражённых грудничков занимаются иммунологи. Детям прописывают интерферон и иммуноглобулин для внутривенных инъекций. Дополнительно вводятся антитела класса IgG к цитомегаловирусу. Они содержатся в препарате «Неоцитотект».
Остальное лечение проводится симптоматически. Если у новорождённого диагностирован миокардит, ему назначат лекарства для укрепления мозга и сердца. Дыхательные пути лечатся аналогично бронхиту. Однако при гидроцефалии у грудничков часто рекомендуют операцию, поскольку череп не способен уменьшиться сам собой.
К сожалению, любые интеллектуальные патологии лечению не поддаются. Аутизм нельзя купировать минимальной социальной адаптацией. Задержка в развитии останется на протяжении жизни новорождённого.
Полностью избавиться от цитомегаловируса невозможно. Все методы лечения направлены лишь на подавление активного течения болезни. Поэтому своевременная диагностика матери на наличие вируса крайне важна для здоровья грудничка.
Профилактика и лечение цитомегаловируса при беременности. Бесплодие и цитомегаловирус
herpes.center
Цитомегаловирусная инфекция у новорожденных: диагностика и лечение | #03/06
Цитомегаловирусная инфекция (ЦМВИ) относится к числу хрестоматийно латентных. Цитомегаловирус (ЦМВ) содержит ДНК, обладает способностью реактивироваться, тропностью к железистой ткани, где персистирует, оказывает цитопатическое действие, в результате которого образуются гигантские клетки, похожие на «совиный глаз».
В Западной Европе (Франция, ФРГ, Испания) от 50 до 70 % всего населения инфицированы ЦМВ. Точных статистических данных частоты распространения инфицированности по России и даже по Москве нет.
Большой толчок для изучения ЦМВИ дали успехи трансплантологии. Есть веские основания полагать, что причиной отторжения трансплантата является активация ЦМВИ. Частота инфицирования (наличие антител класса иммуноглобулина (Ig) G к ЦМВ) ЦМВ зависит от социально-экономических условий, степени повреждения иммунной системы и др. ЦМВ относятся к разряду «слабых антигенов». Изучение этих вирусов, их воздействия, например, на эндотелий сосудов, ряд других органов, кроме слюнных желез, продолжается.
Нами проводились многолетние систематические исследования (И. В. Орловская, А. В. Александровский, В. В. Зубков) различных аспектов развития этой инфекции. Было установлено, что это типичная социально значимая инфекция. Данные свидетельствуют о том, что в Москве за последние 15 лет ЦМВИ претерпела существенную эволюцию.
Так с 1988 по 1993 г. антитела класса IgG к ЦМВ у матерей и их новорожденных больных детей выявлялись лишь в 40–50 % случаев.
Выявлена зависимость от социальной принадлежности пациентов и ряда дополнительных факторов: наиболее часто (от 86 до 96 % случаев) инфекция выявляется у больных, перенесших пересадку почек, гомосексуалистов и больных СПИДом (Западная Европа, США).
По нашим данным, полученным на основании сероэпидемиологических исследований, проводившихся в 1995–1999 гг. и в 2000–2002 гг. у женщин репродуктивного возраста, родивших детей с внутриутробной инфекцией, частота циркуляции антител к ЦМВ класса IgG достигает высокого уровня (90 % от общего числа обследуемых) и не имеет тенденции к снижению.
Это свидетельствует об отсутствии и неэффективности контроля за инфекциями у женщин, передающимися половым путем, в том числе ЦМВИ. Установлено, что в 60 % случаев у больных имеются одновременно специфические антитела к нескольким перинатальным патогенам. Наиболее распространенными являются вирус простого герпеса (ВПГ), ЦМВ, хламидии и уреаплазма. Доля смешанных инфекций значительна и продолжает расти. Выявить лидирующего возбудителя сложно, это требует дополнительных исследований.
ЦМВИ — это инфекция плода. Эта инфекция особенно опасна для беременных женщин. Проявления ЦМВИ большей частью стертые, особенно часто у беременных женщин она протекает в виде острой респираторно-вирусной инфекции.
ЦМВИ после пубертатного периода распространяется в основном половым путем. У беременных женщин она проявляется чаще «под маской» другого заболевания. Поэтому своевременная диагностика заболевания затруднена. Специфически не проявляясь у женщины, у плода ЦМВИ вызывает врожденные нарушения центральной нервной системы, пороки развития сердца, почек.
Доказано, что ЦМВ являются причиной многоводия и одновременно развития водянки плода (A. Breinl, Lebmanu), угрозы и спонтанного прерывания беременности, фетоплацентарной недостаточности. Выявление ЦМВ у мертворожденных варьирует от 9 до 33 % (ФРГ, Франция). Инфекцию трудно выявить из-за несовершенства диагностики. Все проявления ЦМВИ у женщин и у плода развиваются на фоне иммунодефицита.
Одним из главных способов распространения инфекции является половой путь передачи. Об этом свидетельствует одновременное наличие у больных антител к ВПГ и ЦМВ.
Большое число беременных женщин, особенно в последних триместрах беременности, заражаются при орогенитальных контактах (до 20 % и более).
Заражение ЦМВИ может происходить после трансфузий инфицированной крови. В Западной Европе и США 15–70 % образцов крови содержат ЦМВ. Кроме того, проникновение в организм ЦМВ может иметь место при трансплантации инфицированных почек, костного мозга, сердца и других органов. В 20 % случаев причина реакции отторжения — активация ЦМВ (ФРГ, США). Несовершенство диагностики ЦМВИ зачастую не позволяет доказать значимость вирусной агрессии при формировании того или иного патологического процесса.
Как было сказано выше, все проявления ЦМВИ у женщин и плода развиваются на фоне иммунодефицита. Результаты многолетних исследований, проведенных в НЦАГиП РАМН, показали, что одной из ведущих причин реализации внутриутробной инфекции является состояние иммуносупрессии у матери в период беременности. Особенно четко это проявляется у женщин с гиперандрогенией, миастенией, лимфогранулематозом и др., которые получают стероидную терапию до и во время беременности.
ЦМВИ является эндемичной во всех популяциях человека. Пути заражения плода, новорожденного, взрослого человека различны.
Заражение плода может осуществляться гематогенно-трансплацентарным путем, особенно при наличии первичной инфекции у женщины и при повреждении плаценты с нарушением ее барьерной функции. В 10–15 % случаев у плода признаки ЦМВИ проявляются сразу после рождения. Гематогенно-трансплацентарный путь инфицирования плода ЦМВ является основным.
Восходящим путем заражение происходит при наличии ЦМВ в цервикальном и вагинальном секретах, а также через инфицированные околоплодные воды.
Интранатально заражаются до 5–7 % новорожденных, как путем непосредственного контакта с инфицированным материалом, так и при аспирации околоплодных вод, содержащих ЦМВ.
В постнатальном периоде новорожденный заражается в 30 % случаев (данные ВОЗ) от выделений матери, содержащих вирус: слюну, мочу, выделений из гениталий, грудное молоко, кровь. Наши исследования показали, что антиген ЦМВ можно выявить и в ликворе, особенно при наличии у ребенка генерализованной формы инфекции с церебральными повреждениями.
По данным Clive Smeet, гематогенным путем ЦМВ распространяется в различные органы, включая почки, печень, селезенку, сердце, мозг, сетчатку глаза, пищевод, внутреннее ухо, легкие, кишечник.
В период вирусемии ДНК ЦМВ можно обнаружить в моноцитах, лимфоцитах, нейтрофилах. Лейкоциты играют важную роль в диссеминации вируса по всему организму. ЦМВ более тропен к полинуклеарным фагоцитам, чем к мононуклеарным клеткам. Можно считать доказанным факт поражения эндотелия сосудов, сердца, желудочков мозга.
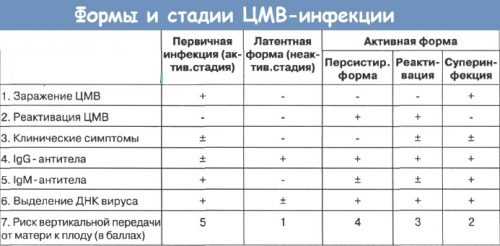
ЦМВИ может протекать в виде первичной (острой) инфекции с появлением и ростом специфических антител к ЦМВ класса IgM, а в дальнейшем и IgG. Эта форма инфекции характеризуется наличием вирусоспецифического антигена в крови, моче и ликворе. Первичная инфекция у беременных женщин особенно опасна. В этом случае очень легко происходит вертикальная трансмиссия (трансплацентарным путем) вируса плоду.
Эта инфекция может вызвать серьезные изменения у плода: микроцефалию, гепатоспленомегалию, тромбоцитопению, затянувшуюся желтуху, реже — потерю слуха, умственную отсталость и др. В этой ситуации у плода могут возникать вирусный интерстициальный пневмонит, ретинит, энцефалит, болезни желудочно-кишечного тракта.
При более раннем заражении ЦМВ могут иметь место пороки развития желудочно-кишечного тракта. Заражение плода при первичной инфекции во всех случаях происходит при отсутствии у беременной специфических IgG-антител, что является причиной тяжелого поражения плода.
Первичной формой ЦМВИ беременные женщины часто заражаются в результате орогенитальных контактов. Эта форма инфекции представляет наибольшую опасность для беременной женщины и плода, так как она развивается на фоне полного отсутствия специфических антител.
Под реактивацией понимают форму ЦМВИ, которая ранее протекала латентно, бессимптомно. Реактивация вируса происходит под влиянием терапии стероидными гормонами у беременных женщин (плода), иммуноскомпрометированных больных (реципиентов трансплантатов, лиц больных СПИДом). Так, у новорожденных, родившихся от женщин, в отношении которых применялись репродуктивные технологии, а также у самих женщин нами в 100 % случаев были выявлены антицитомегаловирусные IgG-антитела.
При реактивации ЦМВИ у беременной женщины может происходить подъем титров антител как класса IgG, так и IgM к ЦМВ. Однако у ряда пациентов нового появления антител IgM не происходит в связи с формированием вторичного иммунологического ответа, характеризующегося гиперпродукцией специфических IgG-антител. Именно этим объясняется то обстоятельство, что в этом случае может родиться как здоровый ребенок, так и новорожденный с серьезными проявлениями ЦМВИ.
ЦМВИ (первичная) может переходить в хроническую или латентную формы, которые могут реактивироваться.
Реинфекция — заражение пациента новым экзогенным вирусом — может сопровождаться иммунологическими сдвигами, повторным нарастанием титра специфических IgM, а в дальнейшем и IgG или (реже) только повышением титра специфических антител класса IgG. Серологических тестов, помогающих отличить первичную инфекцию от вторичной в таких ситуациях не существует.
У больных с иммунодефицитом, СПИДом и у новорожденных детей антитела при реактивации могут не выявляться. У них в процессе диагностики должно использоваться одновременно несколько методов.
Одновременного наличия антител класса IgG и положительного анализа (полимеразная цепная реакция — ПЦР) достаточно для подтверждения клинического диагноза.
По клиническим проявлениям врожденная ЦМВ и герпетическая инфекции имеют как сходные черты, так и значимые различия. Оба заболевания имеют склонность к хронизации процесса.
Частота внутриутробных повреждений различных органов и систем ЦМВ, по данным различных авторов, не одинакова. По уточненным патогистологическим данным, наиболее часто наблюдаются (в порядке их частоты выявления) поражения мозга (менингоэнцефалит, поражения желудочков мозга, кальцификаты, «кальцинация» мозговых сосудов). Все эти морфологические изменения сопровождаются различными неврологическими проявлениями: от легких церебральных изменений до серьезного судорожного, гипертензионно-гидроцефального синдромов и др.
Одним из распространенных проявлений ЦМВИ является блокада ликвороносных путей (до 7 % из числа перинатальных повреждений мозга вирусной этиологии). Другой «точкой приложения» ЦМВ часто является сосудистое сплетение с последующим образованием кист.
Наши наблюдения показали, что минерализационная васкулопатия («кальцификация» — по терминологии зарубежных авторов) мозговых сосудов, сопровождающая ЦМВИ, может быть причиной судорожного синдрома у новорожденного. Судорожный синдром в этом случае возникает с первых часов после родов и продолжается до 5 дней и больше. Это состояние требует тщательного специфического лечения цитотектом, антиконвульсантами и др. Изменения сосудов мозга, вызываемые ЦМВ, требуют дальнейшего изучения.
В этих случаях требуется исключить герпетическую инфекцию новорожденного ребенка. Внутриутробная гидроцефалия у плода часто связывается с ЦМВ (ФРГ, Австрия).
Довольно распространенным проявлением ЦМВИ является пневмония. Среди общего числа пневмоний (больше 1/3 всех больных, поступающих в отделение патологии новорожденных НЦАГиП) примерно в 10 % случаев этиологическим фактором является ЦМВ, что подтверждено при оценке эпидемиологического анамнеза матери: наличие эндоцервицита, кольпита, иммуносупрессивных факторов, носительство ВПГ и ЦМВ, а также обязательное наличие IgG и IgM и (реже) — положительная ПЦР у новорожденного.
Следует заметить, что рентгенологически при этом определялись очаговые воспалительные инфильтраты, реже — сегментарные тени. При гематологическом исследовании выявлялись лейкоцитоз с нейтрофильным сдвигом влево, реже — тромбоцитопения. Нет сомнения, что в генезе этих пневмоний участвует вторичная бактериальная флора, активация последней наступает позже. Заражение новорожденного в этом случае происходит как аспирационным (чаще), так и гематогенным путем. Вторичный иммунодефицит в этих случаях приводит к более длительному течению заболевания и требует одновременного проведения иммунотерапии.
Как указывают J. Frank и H. Fridman, ЦМВИ в виде пневмонии часто приводит к смертельным исходам у больных СПИДом, у пациентов после трансплантации почек и костного мозга, сердца. Причина тяжелого течения пневмонии при ЦМВИ — угнетение иммунных реакций.
Нередко проявлением ЦМВИ у новорожденных являются гепатоспленомегалия, затянувшаяся желтуха (до 32%). За последние 5 лет повысилось число больных с гипербилирубинемией, с незначительным изменением уровня трансаминаз. Этот факт требует дальнейшего изучения вопроса о роли ЦМВ.
Тромбоцитопения нами отмечалась (до 2–3 %) в основном на фоне генерализованных форм инфекции.
В 30 % случаев ЦМВИ может протекать без локальных изменений и проявляться только ухудшением общего состояния пациентов, наличием специфических антител IgM. Эта форма в ряде случаев протекает легко, но всегда требует исключения генерализации процесса, проведения иммунотерапии.
ЦМВИ может служить причиной: миокардитов, кардиомегалии, утолщения миокарда, увеличения предсердия, гидроперикарда (до 15 %), а также водянки плода.
В отдельных случаях могут отмечаться и поздние поражения, которые регистрируются только в 6–7 мес жизни: слепота, глухота, отставание в развитии и др.
Диагностика этой инфекции сложна и должна проводиться с учетом ее клинических проявлений.
- Оценка эпиданамнеза матери (вирусоносительство), наличие у нее эндоцервицита, аднексита, кольпита, наличие возможных иммуносупрессивных воздействий на нее и на плод, обследование пациентки.
- Учет соответствующей клиники у ребенка: наличие кальцификатов в мозгу, васкулопатии сосудов мозга, вентрикуломегалии, энцефалита, а также выявление пневмонии, гепатоспленомегалии, затянувшейся гипербилирубинемии и др.
- Эхоэнцефалография и УЗИ внутренних органов.
- Определение антител классов IgM и IgG к ЦМВ (метод иммуноферментного анализа — ИФА). Классический метод с использованием детекции нарастания в 4 и более раз специфических IgG-антител вначале и спустя 12–14 дней у новорожденных не применяется, хотя у взрослых он является наиболее достоверным и точным. У беременных этот серологический метод вполне может быть использован. Иммунная система новорожденного не способна синтезировать антитела класса IgG; последние переходят трансплацентарно от матери плоду.
- Выявление вирус-специфических антигенов (частей вирусов) в культуре клеток не применяется даже для научных целей из-за дороговизны методики. Вирус-специфический антиген можно выявить путем экспресс-метода иммунофлюоресценции; последний является точным, но, к сожалению, в последние годы почти не используется.
Широко применяются биотехнологические методы: ДНК-гибридизации и особенно ПЦР. Однако гибридизационная техника требует совершенствования, наличия качественных тест-систем и квалифицированных лаборантов.
Метод ПЦР, к сожалению, возложенных на него надежд не оправдал. По нашим данным, подтвердить диагноз этим методом можно не больше чем в 50 % случаев. Хотя за рубежом (ФРГ) многие авторы считают, что положительной ПЦР и наличия специфических IgG-антител достаточно для окончательной постановки диагноза.
Во всех случаях при выявлении антигена ЦМВ в моче, крови, ликворе новорожденного, в том числе при положительной ПЦР необходимо подтвердить инфицирование выявлением специфических противовирусных антител (IgG и IgM).
Следует упомянуть, что определение наличия в крови IgM-специфических антител является наиболее надежным и быстрым методом диагностики.
- Для выявления антигена применяются электронная микроскопия (ФРГ) и иммуногистология.
- Окончательная интерпретация иммуновирусологических результатов должна осуществляться с одновременной оценкой эпиданамнеза матери, возможных иммуносупрессивных воздействий на нее, особенно при использовании репродуктивных технологий с учетом клинических проявлений инфекции у ребенка.
Большое научно-практическое значение имеют результаты проводившихся недавно исследований по выяснению защитной роли специфических противовирусных IgG к антигенам ЦМВ, передающихся трансплацентарно от матери плоду.
Исследования, проводимые одновременно в лабораториях трех институтов (НЦАГиП, НИИ вирусных препаратов им. О. Г. Анджапаридзе, ГНИИ биологического приборостроения), дали возможность сделать следующие научно-практические выводы.
- В основе развития внутриутробной инфекции лежат иммуносупрессивные факторы, влияющие на состояние матери, плода и новорожденного — развитие у них вторичных иммунодефицитных состояний. Уникальным аргументом в пользу защитной роли специфических противовирусных иммуноглобулинов является тот факт, что больные новорожденные, родившиеся от матерей с первичной формой генитального герпеса (при отсутствии у них антител), заражаются в 10 раз чаще. Инфекционный процесс у них в 86 % случаев протекает в тяжелой генерализованной форме (с повреждениями мозга, пневмониями и др.) и часто заканчивается летально.
Установлено, что в 12 % случаев специфические противовирусные антитела от больной матери новорожденному передаются не полностью. Очевидно, что причина этого явления — нарушение функции плаценты вследствие развития в ней инфекционного процесса.
Убедительно показана роль угнетения иммунологических факторов в генезе реактивации ЦМВ и возникновении инфекции у новорожденных.
Дефицит противовирусных IgG у плода и новорожденного приводит к диссеминации вируса, развитию генерализованной формы инфекции и к тяжелому повреждению мозга, легких, надпочечников и др.
Отмечаются повреждения клеточного звена иммунитета; при этом реальная возможность их компенсации уменьшается. Выявлен дефицит клеток, принадлежащих к субпопуляции Т-клеток, обладающих цитотоксической активностью против клеток, инфицированных вирусами.
- Углубленные исследования противовирусного иммунитета дали возможность выявить группу новорожденных, больных внутриутробной инфекцией, с «транзиторными иммуносупрессивными состояниями», в терапии которых следует использовать препараты, воздействующие на гуморальное звено иммунитета.
- Нарушения в гуморальном звене иммунитета компенсируются внутривенным введением препаратов иммуноглобулина. Разработана специальная технология их применения. Для больных с внутриутробными вирусными инфекциями эти препараты являются средством как заместительной, так и специфической терапии из-за содержания в них противовирусных антител. Существуют убедительные доказательства их позитивной роли. Применение иммуноглобулинов способствует не только улучшению состояния больных, но и повышению в их крови содержания IgG. Из-за наличия в препаратах иммуноглобулинов антител различной специфичности одновременное их введение с зовираксом и антибиотиками обеспечивает их синергидное действие.
Это дает возможность создать необходимый компонент «терапевтической технологии» — иммунотерапию.
Способы терапии ЦМВИ: химиотерапия (ганцикловир, фоскарнет), интерферонотерапия (достоверных сведений о действии на ЦМВ нет) и иммунотерапия специфическим антицитомегаловирусным иммуноглобулином (цитотект).
Ганцикловир (цимевен) — противовирусный препарат, сходный с ацикловиром, оказывает воздействие на все виды вируса герпеса. Ганцикловир в 50 раз превосходит ацикловир по эффективности воздействия на ЦМВ.
Препарат был синтезирован в 1982 г. Он угнетает репликацию вируса за счет конкурентного ингибирования вирусной ДНК-полимеразы и нарушения удлинения цепи ДНК. Ганцикловир выводится из организма через почки. По данным вирусологических исследований, применение ганцикловира приводит к подавлению вируса у 87 % больных, отмечается исчезновение ЦМВ в крови и моче. Ганцикловир применялся в основном в США у больных ретинитом, пневмонией, которые развились у пациентов, страдающих СПИДом; у реципиентов костного мозга, почек, а также у лиц с цитомегаловирусным колитом. Препарат используется в дозе 10–20 мг/кг в неделю внутривенно. Во всех случаях была доказана его клиническая и вирусологическая эффективность.
После лечения ганцикловиром, однако, отмечались и осложнения в виде нейтропении, тромбоцитопении. По этой причине мы отказались от применения ганцикловира.
Таким образом, можно отметить, что химиотерапия ЦМВИ делает лишь первые шаги. В этом направлении необходимы дальнейшие исследования.
Фоскарнет, применявшийся у больных с ЦМВ-пневмонией, нефротоксичен. Поиски эффективных и безопасных противовирусных препаратов продолжаются.
В настоящее время единственным действенным методом терапии и неотложной профилактики ЦМВИ у новорожденных является использование иммуноглобулина для внутривенных вливаний, содержащего антитела класса IgG к ЦМВ.
Имеются веские научные доводы в пользу данного лечебного подхода. Во-первых, существуют обширные научно-практические доказательства эффективности применения иммуноглобулинов при инфекциях; во-вторых, не вызывает сомнений необходимость коррекции гуморального звена иммунитета, особенно при вторичных иммунодефицитах. Таким образом, при ЦМВИ иммуноглобулины являются средством как иммунозаместительной, так и этиотропной терапии. В-третьих, в последние годы доказано модулирующее влияние иммуноглобулинов при внутривенном введении на клеточное звено иммунитета. В-четвертых, активация ЦМВИ происходит всегда на фоне иммунодефицитов. Введение антицитомегаловирусных иммуноглобулинов воздействует не только на этиологический фактор, но и дает возможность влиять на различные патогенетические звенья заболевания.
Показано, что клеточный иммунный ответ у пациентов, инфицированных ЦМВ, «распознает» минимум один протеин «очень ранней» вирусной репликационной фазы на поверхности инфицированной клетки. Это приводит к разрушению инфицированной клетки вирусоспецифическими цитотоксическими Т-лимфоцитами. У пациентов с иммунодефицитом это невозможно, так как вирусоспецифических цитотоксических Т-лимфоцитов у них нет, или их количество недостаточно. ЦМВ-нейтрализующие антитела являются в этом случае единственными иммунологическими компонентами, которые предотвращают инфицирование клетки.
Механизмы воздействия иммуноглобулинов и синтетических вирусостатиков различаются, так как последние не могут проникать в клетку. Противовирусное действие развивается вне клетки. В результате связывания с гликопротеинами на поверхности вируса иммуноглобулины предотвращают инфицирование других клеток-хозяев. Нейтрализован может быть как свободный вирус, так и вирус во время выхождения из инфицированной клетки после репликации. Свободные, нейтрализованные вирусы выводятся почками. Если для терапии и профилактики ЦМВИ у пациентов с подавленным иммунитетом применяют препараты человеческого иммуноглобулина, то выраженных побочных эффектов не возникает, в отличие от терапии вирусостатиками.
Одним из препаратов, используемых для терапии серьезных форм ЦМВИ у беременных и новорожденных, является цитотект. С началом его применения активизировалась разработка новых методов диагностики этой инфекции.
Цитотект представляет собой гипериммунный иммуноглобулин для внутривенных вливаний, содержащий в 10 раз больше антител к ЦМВ, чем обычные иммуноглобулины. Препарат готовится из крови специально отобранных доноров, которые имеют высокий титр противоцитомегаловирусных антител. В 1 мл цитотекта содержится не менее 50 единиц антител против ЦМВ (единицы эталонного препарата Института Пауля Эрлиха). Иммуноглобулин соответствует евростандарту качества. Контроль за содержанием антител осуществляет Федеральное ведомство по вакцинам и сывороткам Германии (Paul Ehrliсh Institut). Одновременно в препарате содержится повышенный титр антител к антигенам вируса Эпштейн–Барр и к антигену ВПГ 1-го и 2-го типа. Кроме того, в цитотект входит широкий спектр антител к микробным возбудителям — перинатальным патогенам, вызывающим серьезные инфекции у новорожденных и женщин в послеродовом периоде. Эти антитела усиливают опсонизацию микроорганизмов, имеют близкое к физиологической норме распределение субклассов IgG (IgGI — IgGIV).
Производство цитотекта контролируется в соответствии со стандартами, разработанными Институтом Пауля Эрлиха. Забор плазмы проводится после тщательного отбора и тестирования доноров.
Кроме того, под контролем находится весь пул плазмы. Многоступенчатая подготовка, проверка безопасности цитотекта исключает передачу гепатитов и других инфекций, включая пока еще не идентифицированные.
Нами проводилось клинико-иммунологическое изучение цитотекта (Н. И. Кудашов, О. В. Орловская) у 56 больных с ЦМВИ. Диагноз был подтвержден во всех случаях путем выявления у больного антицитомегаловирусных IgM.
Одновременно в препаратах, вводимых детям, определялось наличие не только антител IgG к ЦМВ, но и к ВПГ. Было установлено, что во всех сериях используемых препаратов содержались специфические антитела к антигенам ЦМВ и ВПГ 1-го типа, при этом антител к ВПГ 2-го типа содержалось в 2 раза меньше. Было убедительно доказано, что цитотект оказывает в комплексе с традиционной терапией выраженный клинико-иммунологический эффект. Происходило не только улучшение общего состояния больных: через 7–8 дней IgM исчезал из крови пациентов, кроме того, существенно повышалось содержание в крови противоцитомегаловирусных IgG, одновременно повышалось и содержание противогерпетических IgG. Таким образом, цитотект является практически единственным препаратом, который эффективен в борьбе с ЦМВИ.
Показания для применения цитотекта в ранние сроки беременности:
- первичная инфекция у беременной: циркуляция в крови антител к ЦМВ класса IgM;
- высокая степень вероятности трансмиссии вируса плоду. Дозы: на 28-й неделе — 2 мл/кг веса, на 31-й неделе — 1 мл/кг;
- у беременных-носительниц антител к ЦМВ класса IgG при многократных перинатальных потерях, особенно при сочетании с состояниями, сопровождающимися иммуносупрессией (гиперандрогения, миастения, использование репродуктивных технологий).
Цитотект вводится сразу же после родов матери и ребенку в следующих случаях:
- при первичной (острой) ЦМВИ у матери (циркуляция антител IgM в крови) в связи с высокой вероятностью передачи вируса плоду;
- при рецидиве инфекции (наличие антител IgG + симптомы инфекции) в конце беременности;
- матери с наличием антицитомегаловирусных антител IgG и ее ребенку (6–7 мес) при повышении у них титра антител в процессе наблюдения.
Дозы цитотекта для профилактики и терапии ЦМВИ для новорожденных — 2–4 мл/кг массы тела, при наличии энцефалита и серьезных невротических изменений введение повторяется многократно.
Для матерей с терапевтической целью используют следующие схемы лечения цитотектом:
- в легких случаях — в дозе 2 мл/кг массы тела, трансфузия цитотекта может быть повторена через 4 дня в зависимости от клинической картины;
- в тяжелых случаях — в дозе 4 мл/кг массы тела, трансфузия препарата может быть повторена через 4 дня, при ухудшении состояния возможно повторное многократное введение препарата.
С профилактической целью — в дозе 1 мл/кг массы тела. Препарат вводится только внутривенно, капельно (20 капель в 1 мин).
Дозы цитотекта для профилактики и терапии ЦМВИ у новорожденных составляют 2–4 мл/кг массы тела.
Постоянным компонентом лечения ЦМВИ у новорожденных является антибиотикотерапия. В этиологическом отношении почти все инфекционные болезни у новорожденных вызываются смешанной вирусно-бактериальной флорой. При ЦМВИ, особенно при наличии пневмонии, активация вторичной бактериальной флоры происходит очень быстро — с первых дней. Выбор антибактериальных препаратов производится эмпирически и основывается на большом опыте и знании спектра возможных возбудителей и особенностей действия антибиотика. Для эмпирической стартовой терапии целесообразно выбирать антибиотик с широким спектром бактерицидного действия, при генерализованной форме инфекции используется комбинированная антибактериальная терапия препаратами, обладающими активностью в отношении возможных в данном случае «перинатальных патогенов».
Одним из наиболее часто применяемых в последние годы антибиотиков является сульперазон. Он представляет собой комбинацию цефоперазона с ингибитором β-лактамаз сульбактамом (цефалоспорины 3-го поколения). Сульперазон используется внутривенно (в первые 3–4 дня) и внутримышечно дважды в день в дозе 80–100 мг/кг массы тела; курс терапии от 8 до 14 дней, в среднем — 10 дней.
Для усиления грамотрицательного действия сульперазона применяется обычно аминогликозид — нетромицин. Препарат назначался из расчета 7 мг/кг массы тела в сутки; курс терапии — не более 7 дней. Иммуноглобулины для внутривенного вливания и антибиотики (сульперазон + нетромицин) входят в стандарт терапии. Они являются эффективными, существенно сокращают длительность пребывания ребенка в стационаре (до 10–12 дней). Кроме того, следует отметить отсутствие внутрибольничных инфекций, рецидивов и случаев заболевания после выписки в домашних условиях.
Н. И. Кудашов, доктор медицинских наук, профессор
НЦАГиП, Москва
www.lvrach.ru
Врожденная цитомегаловирусная инфекция у новорожденных: признаки цитомегалии

Когда родители слышат от врачей после рождения, что у малыша обнаружена врожденная инфекция – это всегда тревожно. Особенно если название этой инфекции для них неизвестно, они ранее не слышали о подобном. Цитомегаловирусная инфекция среди взрослых встречается не очень часто, обычно имея вид бессимптомного носительства. Но в отношении детей, особенно новорожденных, наличие подобного вируса (а это именно вирусная инфекция), опасно тяжелыми поражениями внутренних органов.
Оглавление: Что это такое – цитомегалия? Как часто развивается врожденная цитомегалия Причина врожденной цитомегалии Как происходит заражение? Как проявляется цитомегалия у младенцев? Как поставить диагноз? Если ли лечение цитомегаловируса у новорожденных
Что это такое – цитомегалия?
Врожденная цитомегалия (а если правильнее – цитомегаловирусная инфекция) это одна из опасных инфекций, развивающихся еще внутриутробно или в период родов, если малыш инфицируется этим вирусом от матери.
Важно
Основной характеристикой этой патологии является формирование множественных грубых пороков развития (если кроха заразился в утробе) или поражениями внутренних органов и системными проявлениями инфекции (при заражении перед родами и в их течении).
 Нередко нет никаких симптомов болезни у матери, а затем и у крохи, помимо носительства вируса в крови, но могут выявляться и грубые поражения со стороны нервной системы – пороки мозга в виде гидроцефалии или микроцефалии, формирование энцефалопатии. Также поражаются внутренние органы с формированием желтухи, тяжелых пневмоний или нефритов, патологий со стороны органов чувств – слепоты или глухоты. Поставить диагноз подобной врожденной патологии можно по данным анализов, обнаружив антитела к вирусу в крови или моче, мазках с носоглотки и ликворе. Лечить подобную инфекцию трудно, спектр препаратов очень мал.
Нередко нет никаких симптомов болезни у матери, а затем и у крохи, помимо носительства вируса в крови, но могут выявляться и грубые поражения со стороны нервной системы – пороки мозга в виде гидроцефалии или микроцефалии, формирование энцефалопатии. Также поражаются внутренние органы с формированием желтухи, тяжелых пневмоний или нефритов, патологий со стороны органов чувств – слепоты или глухоты. Поставить диагноз подобной врожденной патологии можно по данным анализов, обнаружив антитела к вирусу в крови или моче, мазках с носоглотки и ликворе. Лечить подобную инфекцию трудно, спектр препаратов очень мал.
Как часто развивается врожденная цитомегалия
Считается, что среди всех врожденных инфекций именно цитомегалия относится к одной из лидирующих врожденных патологий. По данным разных авторов, она встречается с частотой от 0.2 до 3%, а если мать до беременности не была знакома с вирусом, и перенесла инфицирование, уже будучи в положении, риски для ребенка возрастают в десятки раз, достигая 30-50%. Это связано с отсутствием защитных антител. При вторичном инфицировании, то есть реактивации имевшейся у матери вирусной инфекции во время беременности, шансы на повреждения плода составляют около 1%.
Важно
Сегодня данная инфекция очень актуальная для неонатологии, так как заболеваемость цитомегалией и врожденными инфекциями возрастает, приходя на смену микробным инфекциям, с которыми уже частично научились бороться.
Нередко тяжелые последствия связаны с поздней диагностикой и отсутствием видимых клинических симптомов после того, как ребенок родился. Поэтому сегодня важно как можно раньше начинать профилактику подобных болезней, нужно прицельное и подробное обследование будущих мам на предмет обнаружения у них возбудителей скрытых инфекций, чтобы затем вести этих женщин по особым стандартам. Если своевременно начать лечение, можно снизить количество неблагоприятных исходов и инвалидности среди младенцев. Сегодня также врачи направляют усилия на то, чтобы разработать вакцины против этого вируса, чтобы защитить будущих матерей и их детей.
Причина врожденной цитомегалии
 Основная причина, приводящая к развитию врожденной цитомегалии – это заражение особым видом вируса, содержащим в себе ДНК-цепочку. Он относится к группе герпесных, и соответственно обладает свойством, как и его собратья, пожизненно храниться в организме после первичного инфицирования. Возбудитель хорошо сохранятся в условиях комнатной температуры, но не выносит воздействия дезинфицирующих веществ. Внутри пораженных клеток он может выживать на протяжении длительного периода, уходя из-под надзора иммунной системы.
Основная причина, приводящая к развитию врожденной цитомегалии – это заражение особым видом вируса, содержащим в себе ДНК-цепочку. Он относится к группе герпесных, и соответственно обладает свойством, как и его собратья, пожизненно храниться в организме после первичного инфицирования. Возбудитель хорошо сохранятся в условиях комнатной температуры, но не выносит воздействия дезинфицирующих веществ. Внутри пораженных клеток он может выживать на протяжении длительного периода, уходя из-под надзора иммунной системы.
Если женщина ранее не контактировала с вирусом, риск ее инфицирования повышается, если будучи беременной, она контактирует с больными данной инфекцией, по долгу службы посещает места скопления людей или медицинские учреждения, где могут находиться инфицированные. Немалую роль играет сила иммунного ответа у самой женщины, особенно в условиях носительства вируса и его реактивации в последующем.
Важно
При активации инфекции при беременности шансы на поражение ребенка невысоки, иммунная система уже знакома с инфекцией и сдерживает ее развитие. Если же женщина ослаблена, имеются проблемы с иммунитетом и патологии, возможен перенос вируса к плоду.
Как происходит заражение?
Малыш может заразиться двумя способами – еще внутриутробно (трансплацентарно) и в период родов (интранатально), проходя через родовые пути мамы, у которой имеется вирус. Именно второй вариант у младенцев отмечается чаще, из-за чего в первые дни после рождения, пока вирус разносится по органам и тканям, нет никаких проявлений. Прежде всего, инфекция обладает тропностью к ткани слюнных желез, в их клетки вирус проникает в первую очередь и фиксируется там. Особенно часто поражаются околоушные железы, а также подчелюстные. В области выводных протоков вирус активно размножается, не выходя за пределы тканей, изменяются клетки, их видно под микроскопом – они приобретают характер цитомегалов. Они значительно разрастаются, внутри них есть скопления вирусных частиц, видимые как патологические включения. По этим клеткам, если они обнаружены, можно точно поставить диагноз. Помимо слюнных желез могут поражаться печень и поджелудочная железа, почки и головной мозг.
По классификации различается две формы врожденной инфекции – локализованная и генерализованная. Но подобное деление относительно условное, так как малейшее подавление иммунитета у плода приводит к переходу из ограниченной формы в распространенные поражения.
По характеру течения инфекция может быть острой, затяжного и хронического течения. При острой и затяжной формах выявляются типичные симптомы, хроническую форму нередко можно обнаружить только по антителам и активности вируса в крови.
Также возможна классификация по преобладающему виду повреждений – со стороны печени и селезенки, легочная или мозговая, кишечная форма, но нередко они могут сочетаться между собой.
Как проявляется цитомегалия у младенцев?
Все зависит от срока заражения или реактивации инфекции. Если это ранний срок беременности, плод может быть инфицирован с тяжелыми пороками развития, что приводит к выкидышу или замиранию беременности. Возможно также заражение на протяжении второго и третьего триместра, что может завершаться внутриутробной гибелью малыша.
Обратите внимание
Если ребенок рождается инфицированным, у почти 90% младенцев врожденная инфекция протекает без симптомов, и только около 10% детей имеют определенные проявления поражения. Но именно эти дети имеют большой процент остаточных инвалидизирующих повреждений или гибели в первые недели жизни от тяжелых патологий внутренних органов.
Для классической внутриутробной цитомегалии типично три ведущих синдрома:
- Желтуха
- Увеличение печени с селезенкой
- Геморрагические проявления.
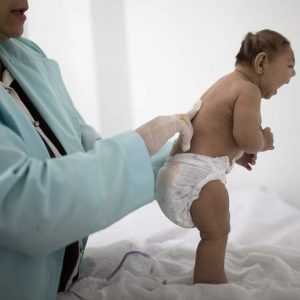 У новорожденных проявляется по телу сыпь в виде мелких кровоизлияний, точечных, как укол иголки, а также синяки и кровоподтеки по коже и слизистым. Возможно появление крови в фекалиях. Обычно подобное явление проходит в течение двух недель.
У новорожденных проявляется по телу сыпь в виде мелких кровоизлияний, точечных, как укол иголки, а также синяки и кровоподтеки по коже и слизистым. Возможно появление крови в фекалиях. Обычно подобное явление проходит в течение двух недель.
При врожденной цитомегалии типично также поражение головного мозга в виде гидроцефалии (скопление жидкости вокруг мозга), микроцефалии (уменьшен размер головки), энцефалопатии с судорогами, дрожанием конечностей, подбородка. Возможно также формирование острого энцефалита с последующими кальцификатами в ткани мозга. Наряду с этим нередко выявляется врожденная пневмония тяжелого течения, повреждения почек и гепатиты, воспалительный процесс в слюнных железах и поражение сетчатки глаз, слухового нерва с формированием сенсоневральной тугоухости. Реже при цитомегалии могут развиваться пороки сердца с дефектами перегородок между предсердиями либо желудочками, клапанные пороки на легочной артерии, аорте или в зоне митрального клапана.
Одним из характерных симптомов патологии может становиться снижение массы тела ребенка при рождении и около 30% случаев недоношенности. По мере роста формируется гипотрофия (дефицит массы тела), требующая специальной методики коррекции. Серьезные поражения мозга могут приводить в последующем к отставанию в психомоторном развитии и формированию умственной отсталости (олигофрения), возможна в последующем проблема с обучением и усвоением материала, памятью и мышлением. При тяжелом поражении печени может развиваться цирроз в периоде от полугода до года.
Как поставить диагноз?
Если беременная перенесла в период беременности первичное инфицирование цитомегаловирусом, показана подробная пренатальная диагностика. Она позволяет выявить у плода врожденные дефекты, которые могут сопутствовать активности вируса, но не саму инфекцию.
Важно
При подозрении на цитомегалию при беременности сразу после родов у младенца берется анализ крови для того, чтобы подтвердить или опровергнуть заражение. Это связано с тем, что симптомы при подобной патологии на начальном этапе отсутствуют.
Поэтому основа диагностики — лабораторные исследования.
Диагноз можно подтвердить при обнаружении в моче или крови самого вируса методом ПЦР или выявить антитела класса IgM и IgG к вирусу методом ИФА.
Сложность ранней диагностики в том, что антитела у новорожденного могут быть как собственными, так и материнскими, если женщина при беременности переносила инфекцию, а плод при этом не был заражен. Чтобы отличить материнские антитела от младенческих исследования проводят последовательно несколько раз, при возрастании титра антител в 4 раза и более при повторных исследованиях можно говорить об инфекции у младенца. Повторяют анализ спустя неделю от первого, и оценивают уровень антител.
Если же по данным ПЦР-анализа вирус выявили, это подтверждает диагноз стопроцентно. Но делается такой анализ длительно, а наличие вируса в крови еще не говорит об активности его и формировании инфекции. Поэтому проводят сразу два этих исследования, которые дополняют данные друг друга. Особенно тщательно нужно обследовать тех детей, чьи матери при беременности переносили острую инфекцию, и у них выявлялись антитела к цитомегалии.
Рекомендуем прочитать: Цитомегалия при беременности
Если ли лечение цитомегаловируса у новорожденных
Специфических препаратов против цитомегалии практически нет, после подтверждения диагноза у младенцев в стационаре применяют только специфический вид иммуноглобулина – анти-цитомегаловирусный. В нем содержатся готовые антитела против инфекции, которые связывают вирусные частицы в крови младенца. Дополняет лечение применение интерфероновых препаратов и его индукторов. При поражении определенных органов назначают специальное лечение, исходя из того, какие симптомы имеют место. Успех в лечении достигается тогда, когда вирус не выявляется в крови.
Парецкая Алена, педиатр, медицинский обозреватель
3,067 просмотров всего, 3 просмотров сегодня
Загрузка…okeydoc.ru
симптомы, причины, лечение, профилактика, осложнения
Причины
Заражение новорождённого цитомегаловирусом может произойти в период внутриутробного развития через плацентарный барьер. Также ребёнок может заразиться и в неонатальный период. Вирус проникает в организм через грудное молоко инфицированной матери или при переливании заражённой крови.
Если доношенный ребёнок находится на естественном вскармливании, вирус не представляет опасности для малыша, поскольку у него есть антитела к инфекции. Заболевание протекает бессимптомно.
Если ребёнок родился недоношенным, находится на грудном вскармливании у матери с цитомегаловирусной инфекцией, возможны тяжёлые последствия, представляющие угрозу для жизни малыша.
Передача вируса от человека человеку происходит путём:
- бытового контакта,
- воздушно-капельным,
- через переливание крови или трансплантацию органов,
- через плацентарный барьер или родовые пути,
- через материнское молоко.
Новорождённого малыша и ребёнка младшего детского возраста ежедневно окружают люди, заражённые вирусом, поэтому заражение происходит, как правило, на первом году жизни малыша. Если у ребёнка хороший иммунитет, то заболевание пройдёт в лёгкой форме, на всю жизнь будет выработан стойкий иммунитет.
Симптомы
Только малая часть детей, заражённых цитомегаловирусом внутриутробно, страдает самим заболеванием. Если женщина до беременности уже была заражена вирусом, то плоду ничего не грозит. Если будущая мама впервые заболела во время беременности, то вирус может отразиться серьёзными проблемами для развития плода.
Наиболее частыми проявлениями цитомегаловирусной инфекции у детей в первые дни жизни является:
- желтуха,
- цитомегаловирусный энцефалит,
- пневмония,
- нарушения работы пищеварительной системы,
- цитомегаловирусный ретинит.
Данные заболевания сопровождаются такими симптомами:
- лихорадкой,
- желтушностью кожных покровов,
- головной боли,
- нарушением подвижности конечностей,
- повышенной сонливостью,
- кашлем,
- тошнотой, рвотой,
- поносом,
- поражением сетчатки глаза.
Смотря на то, какое заболевание сопутствует инфекции, проявляются разные симптомы.
Диагностика цитомегаловирусной инфекции у новорождённых
Диагностирование цитомегаловируса, как правило, проводят в случае инфицирования людей с повышенным фактором риска – у беременных женщин и новорождённых.
У малышей в неонатальный период проявления инфицирования ярко выражены, поэтому диагностировать заболевание не составляет труда. С разницей в месяц у ребёнка проводятся пробы крови, необходимые для оценки титра IgG. Если значение превышает норму в четыре раза, ребёнок считается инфицированным. Если на первом месяце жизни малыша, в его крови обнаружены антитела, такой малыш считается заражённым внутриутробно.
Для диагностики цитомегаловируса также проводятся такие анализы:
- культуральный метод,
- анализ полимеразной цепной реакции,
- серологические исследования.
Осложнения
Наиболее распространёнными осложнениями, вызванными цитомегаловирусом, у новорождённых является гепатит, пневмония, энцефалит, который впоследствии приводит к некрозу тканей головного мозга и сбоям работы всей нервной системы. Энцефалитный ретинит через несколько месяцев жизни малыша приводит к полной слепоте.
Лечение
Что можете сделать вы
Если у новорождённого ребёнка появились признаки цитомегаловируса, следует обязательно обратиться к врачу для полного обследования и назначения адекватного лечения. Если заболевание протекает в осложнённой форме, его последствия могут обернуться серьёзными проблемами для здоровья ребёнка и даже его инвалидизацией.
Что делает врач
Лечение цитомегаловируса проводится только у людей, входящих в группу риска, то есть у новорождённых детей и беременных женщин. В качестве медикаментозной терапии цитомегаловирусной инфекции назначаются противовирусные средства и иммуноглобулины. Также проводится терапия, направленная на купирование симптомов – жаропонижающие, противовоспалительные средства.
Несмотря на то, что цитомегаловирус причисляется к группе вирусов герпеса, действие противогерпесных препаратов на него не распространяется. После лечения такими препаратами вирус всё равно останется в организме и будет размножаться. Поэтому ни в коем случае нельзя заниматься самолечением. Лучше обратиться к специалисту, который назначит адекватное лечение.
Профилактика
Основной мерой профилактики инфицирования цитомегаловирусом является элементарное соблюдение правил личной гигиены. Во время вынашивания ребёнка женщине лучше избегать мест большого скопления людей, детских учреждений. Чтобы предотвратить заражение цитомегаловирусом при беременности, необходимо пользоваться исключительно личной посудой и только своими предметами гигиены.
Профилактические меры против цитомегаловируса у новорождённых эффективны только пи сниженном иммунитете, недоношенности. Инфицирование здорового малыша обеспечит ему стойкий иммунитет на всю жизнь.
Для предупреждения возникновения осложнений должны приниматься общие меры, направленные на укрепление иммунитета:
- соблюдение правильного питания,
- активный образ жизни,
- отказ от вредных привычек,
- закаливание организма,
- излечивание инфекционных заболеваний.
Оцените материал:
спасибо, ваш голос принят
Статьи на тему
Показать всёПользователи пишут на эту тему:
Показать всёВооружайтесь знаниями и читайте полезную информативную статью о заболевании цитомегаловирусная инфекция у новорожденных детей. Ведь быть родителями – значит, изучать всё то, что поможет сохранять градус здоровья в семье на отметке «36,6».
Узнайте, что может вызвать недуг цитомегаловирусная инфекция у новорожденных детей, как его своевременно распознать. Найдите информацию о том, каковы признаки, по которым можно определить недомогание. И какие анализы помогут выявить болезнь и поставить верный диагноз.
В статье вы прочтёте всё о методах лечения такого заболевания, как цитомегаловирусная инфекция у новорожденных детей. Уточните, какой должна быть эффективная первая помощь. Чем лечить: выбрать лекарственные препараты или народные методы?
Также вы узнаете, чем может быть опасно несвоевременное лечение недуга цитомегаловирусная инфекция у новорожденных детей, и почему так важно избежать последствий. Всё о том, как предупредить цитомегаловирусная инфекция у новорожденных детей и не допустить осложнений. Будьте здоровы!
detstrana.ru
