Citrobacter freundii (цитробактер фреунди): в кале у ребенка и взрослого: лечение, симптомы, профилактика, сдать анализы
Цитробактер (в бланках результатов лабораторного исследования кала обозначается как C. amalonaticus, C. freundii, C. koseri) – относится к группе условно-патогенных бактерий, которые населяют кишечник и каловые массы человека. При адекватном функционировании иммунной системы не опасен для здоровья и жизни.
О заболевании, вызываемом цитробактером, можно говорить только в ситуации, когда снижен иммунитет, а количество нормальных представителей кишечной микрофлоры существенно ниже нормы.
Citrobacter freundii (цитробактер фреунди) является разновидностью микроорганизма.
Что такое Цитробактер фреунди (Citrobacter freundii)?
Штамм Цитробактер фреунди (Citrobacter freundii) можно обнаружить во всех отделах толстого кишечника человека. Тем не менее он способен покидать его пределы, когда наступает дисбаланс микрофлоры, вследствие этого начинают развиваться различные патологии, затрагивающие мочеполовую систему, желудочно-кишечный тракт, желчный пузырь и так далее.
Цитобактерии в кишечнике наиболее активно начинают свою деятельность при попадании в организм младенца. Их можно встретить у малышей в возрасте до 1 года. В этих случаях его проявления можно обнаружить уже через 2 часа после попадания в организм. Если ребенку больше года, то на процесс развития понадобится несколько часов.
Заподозрить, что ребенка поразили именно эти бактерии можно по следующим симптомам – быстро растущее недомогание, боли мигренозного характера, резкий подъем температуры, рвота и учащение процесса дефекации в среднем до 1 раза в час.
Как можно заразиться?
Citrobacter freundii (так выглядит тривиальное название бактерий) присутствуют в почве, воде и фекалиях человека и животных, поэтому инфекция передается, как правило, фекально-оральным путем.
Заражение человека может наступить вследствие употребления в пищу недостаточно пастеризованного молока, молочных продуктов и сливочного масла, выпущенных непроверенными производителями, а также в результате плохой прожарки мяса птиц и животных.
Бактерии живут целыми колониями, их количество исчисляется тысячами.
Дети, в особенности те, у которых ослаблен иммунитет, могут заразиться через грязные руки, игрушки, при контакте со взрослыми, являющимися носителями этих бактерий и прочими контактно-бытовыми способами.
Цитробактер фреунди у грудничка
Цитробактериоз – это очень опасное заболевание и многим родителям не помешает ознакомиться с его причинами и симптомами, которые могут возникнуть у ребенка.
Мы рассмотрим общее понятие о заболевании, способы передачи инфекции, источники заболевания и особенности течения цитробактериоза у детей грудного возраста. Рассмотрим также основные методы лечения.
Citrobacter – это небольшие подвижные палочки, которые присутствуют в микрофлоре каждого человека. В свою очередь цитробактериоз представляет собой заболевание, которое вызвано палочками Citrobacter.
Наиболее часто заболевание поражает ЖКТ и способно вовлекать в воспалительный процесс желчевыводящие и мочевыводящие пути, а также в ряде случаев центральную нервную систему.
Причины
Родителям приходилось неоднократно слышать об отравлениях детей в дошкольных и школьных учреждениях, а иногда и взрослых. Нередко цитробактер фреунди возникает у грудничков, особенно, во время введения прикорма при покупке некачественных продуктов.
Инфекция очень активна и легко передается оральным путем.
Цитробактер у грудничка может возникнуть при несоблюдении элементарных правил гигиены. Речь идет об игрушках и других контактных предметах. В наибольшей степени подвержены заболеванию грудные дети с ослабленным иммунитетом.
Иногда заболевание носит ярко выраженный характер отравления, но симптоматика схожа с гастритом. У детей старшего возраста заболевание проявляет себя через несколько часов, у грудничка цитробактер может заявить о себе уже спустя полтора-два часа.
Симптомы
Температура тела ребенка резко повышается до отметки в 38,5 градусов. Периодически наблюдается рвота и понос, которые могут усиливаться и спадать.
Взрослые дети отмечают боли в области эпигатсрала.
При появлении указанных симптомов следует немедленно обращаться к врачу. Диагноз цитробактер у грудного ребенка может быть подтвержден только после проведения соответствующих лабораторных исследований.
Несмотря на острое начало заболевания, стоит успокоить родителей, поскольку медицина при своевременном вмешательстве выставляет благоприятный прогноз. Течение болезни составляет в среднем 5 суток и после оперативного лечения, маленькому пациенту становится легче уже на второй день.
Заболевание у детей на первых месяцах жизни характеризуется острым началом и напоминает энтероколит и энтерит. Первый стул после инфицирования частый и жидкий, позже он становится обильным с примесями слизи. Иногда зеленого цвета.
Признаки беспокойства малыша носят кратковременный характер и могут повторяться даже на третий и четвертый день. Если вам дорого здоровье, то лечение цитробактера у грудничка должно проходить под обязательным наблюдением специалиста.
Лечение
Анализ, который выполняют специалисты лаборатории, позволяет установить количество циробактерий в микрофлоре кишечника. Но вместе с установлением количества этих бактерий, всегда выполняется комплексный анализ, определяющий состав других патогенных микроорганизмов, стафилококков, гемолитических отложений, лактонегативных бактерий и других.
Поэтому такой показатель цитробактера 10 в 7 степени у грудничка может быть обнаружен совершенно случайно и ребенок может вполне хорошо себя чувствовать. Это говорит о том, что не нужно спешить бежать в аптеку за лакто и бифидум препаратами. Их может назначать только специалист после комплексного лабораторного исследования.
Могут использоваться монобактамы — азтреонам или карбоксипенициллины – тикарциллин. При штамме фреунди у грудничков применяют левофлоксацин. Тяжелые формы заболевания требуют использования сильных препаратов: карбапенемы и фторхинолоны.
Заключение
Любые заболевания у детей грудного возраста, которые связаны с пищеварительным трактом, необходимо лечить в специализированных заведениях. Не допускается самолечение цитробактер у грудничка даже с применением дорогостоящих и разрекламированных препаратов.
Не допускается самолечение цитробактер у грудничка даже с применением дорогостоящих и разрекламированных препаратов.
Какова опасность заражения цитробактером
Citrobacter чаще всего поражает моче- и желчевыводящие, а также дыхательные пути. Также нередки случаи появления внутрибольничных антигенных инфекций. Разросшиеся колонии этих бактерий крайне опасны для здоровья человека, поскольку они могут вызвать развитие таких заболеваний, как:
- гастроэнтерит;
- менингит;
- токсикоинфекция;
- абсцесс мозга;
- урологические болезни;
- гнойные инфекции;
- сепсис.
Важно: в последние годы нередки случаи массовых отравлений в дошкольных учреждениях, а также школах. Их причиной служит отклонение от установленных норм и технологий приготовления пищи. Ну а непосредственным виновником является цитробактер фреунди, лечение которого должно начинаться незамедлительно.
Цитобактериоз: как он протекает и что нужно делать
Цитобактериоз способен протекать как любое заболевание желудочно-кишечного тракта.
Заболевание начинает развиваться с болей в эпигастральной области. Наряду с этим возникают тошнота и рвота, частота которой постепенно усиливается. Температура тела значительно повышается и может достигать 38,5 градусов. Острая фаза может продолжаться 1-2 дня. Все прочие симптомы цитобактериоза достаточно размыты и вполне могут квалифицироваться за признаки иного заболевания.
Самые первые признаки болезни – это:
- жидкий стул и частые позывы к нему;
- частая рвота (рефлекторные сокращения происходят даже тогда, когда в желудке нет пищи, в результате этого
- наружу начинает выходить соляная кислота).
- Наряду с этими симптомами начинает появляться боль. Она постепенно становится все более выраженного
- характера и поражает всю брюшную полость. При пальпации усиливается и отдает в тонкую кишку.

Важно: отличить цитробактериоз от любого иного заболевания сможет только специалист после проведения всех необходимых обследований и анализов, равно как и назначить соответствующее лечение.
Цитробактер у грудничка отличается тем, что очередность и интенсивность проявлений варьируется, при этом они могут обладать определенными особенностями:
- в самое первое время цитробактериоз практически сразу приобретает тяжелую форму. При этом резко повышается температура тела (вплоть до 40 градусов), начинается сильная рвота, ребенок становится вялым, неактивным. Он слабо или вовсе не реагирует на различные внешние раздражители. При этом показана экстренная госпитализация;
- кал становится жидким и скудным, в его составе можно обнаружить слизь зеленого цвета. По мере развития заболевания он становится более водянистым и обильным. На этом этапе возможна примесь крови – это станет следствием развития гемоколита.

Наряду с вышеперечисленными признаками начнется раздражение кожи и слизистых, появится аллергический синдром, сопровождающийся обильными высыпаниями по всей поверхности тела.
Цитробактериоз у ребенка – серьезное заболевание
Важно: при появлении этих признаков необходимо как можно быстрее показаться специалисту.
Цитробактер: как его обнаружить
Обнаружить бактерию цитробактер в анализе кале достаточно просто, достаточно лишь правильно провести исследование взятых образцов.
Наличие большого количества этих микроорганизмов можно считать главным лабораторным показателем того, почему у пациента нарушена микрофлора кишечника (за исключением случаев, когда есть злокачественные новообразования или ослаблен иммунитет).
В организме каждого человека есть цитробактер, норма его не превышает 10.000 колоний на 1 грамм кала. Если этот показатель превышен, то врач сразу же диагностирует цитробактериоз.
В случае с маленькими детьми анализ кала берут несколько раз и сравнивают количество колоний. Если оно неуклонно растет, то следует как можно быстрее принимать меры.
- выявить наличие патогенных микроорганизмов, отягчающих течение болезни;
- идентифицировать штамм citrobacter в кале (freundii или diversus), чтобы предупредить возможные негативные последствия и назначить соответствующее лечение.
Как лечить
Особых проблем избавление от бактерий не составит, если постановка диагноза была осуществлена своевременно. При лечении крайне важно не только вылечить пациента, но и гарантировать, что цитробактериоз не начнет развиваться в будущем.
Назначается диета, при которой следует полностью исключить жареную, перченую, жирную пищу, продукты, которые усиливают гнилостное брожение и образование газов в кишечнике.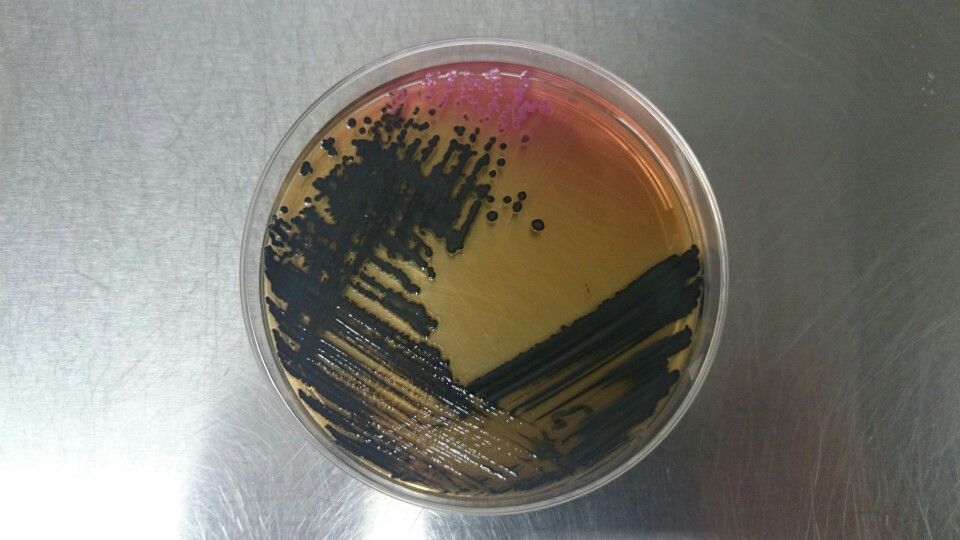 В рацион нужно добавить кисломолочную продукцию, свежие овощи и фрукты.
В рацион нужно добавить кисломолочную продукцию, свежие овощи и фрукты.
Медикаментозная терапия состоит из приема препаратов – это Нифуроксазид и Ципрофлоксацин. Если цитробактер у ребенка – оптимален Левофлоксацин. При необходимости может быть назначен Азтреонам.
Для исключения развития недуга вновь прописываются пробиотики – Лактобактерин, Бификол, Бифидумбактерин. Для того чтобы облегчить работу пищеварительной системы назначаются Панкреатин, Абомин, Фестал.
Важно знать, что самостоятельно ставить диагноз и назначать лечение цитробактера запрещено – это прерогатива специалиста. В этой статье информация дана исключительно в ознакомительных целях.
цитробактер у ребенка — 25 рекомендаций на Babyblog.ru
Как “читать” анализ на дисбактериоз
Копанев Ю.А. Соколов А.Л.
В бланке каждого анализа на дисбактериоз имеются показатели микрофлоры, которые мы расшифруем.
Патогенные энтеробактерии. Обычно этот показатель в бланке анализа идет первым. К этой группе микроорганизмов относятся такие бактерии, которые вызывают острую кишечную инфекцию (сальмонеллы, шигеллы – возбудители дизентерии, возбудители брюшного тифа). Выявление этих микроорганизмов является уже не показателем дисбактериоза, а показателем серьезного инфекционного заболевания кишечника.
Бифидобактерии. Это основные представители нормальной кишечной микрофлоры, количество которых в кишечнике должно быть 95 – 99%. Бифидобактерии выполняют важную работу по расщеплению, перевариванию и всасыванию различных компонентов пищи, например, углеводов; они сами синтезируют витамины, а также способствуют усвоению их из пищи; при участии бифидобактерий происходит всасывание в кишечнике железа, кальция и других важных микроэлементов; бифидобактерии стимулируют моторику кишечной стенки и способствуют нормальному опорожнению кишечника; бифидобактерии нейтрализуют разлчные токсические вещества, попадающие в кишечник извне или образовавшиеся в результате жизнедеятельности гнилостных микроорганизмов. 8). Снижение общего количества кишечной палочки может быть признаком присутствия в кишечнике небактериальных паразитов (глистов, простейших, которые также нуждаются в кислороде, обделяя им кишечную палочку).
8). Снижение общего количества кишечной палочки может быть признаком присутствия в кишечнике небактериальных паразитов (глистов, простейших, которые также нуждаются в кислороде, обделяя им кишечную палочку).
Следует отметить, что бактерии нормальной кишечной флоры живут, прикрепляясь к кишечной стенке и образуя пленку, покрывающую кишечник изнутри. Через эту пленку происходит все всасывание в кишечнике. Бактерии нормальной кишечной микрофлоры обеспечивают по совокупности 50 – 80% всего пищеварения, а также выполняют защитные (в том числе противоаллергические) функции, нейтрализуют действие чужеродных и гнилостных бактерий, способствуют опорожнению кишечника, обеспечивают адаптацию к питанию и к внешним воздействиям.
Кишечная палочка со сниженной ферментативной активностью. Это неполноценная кишечная палочка, которая не представляет никакого вреда, но при этом не выполняет своих полезных функций. Присутствие данного показателя в анализе является признаком начинающегося дисбактериоза, а также как и снижение общего количества кишечной палочки может быть косвенным признаком присутствия в кишечнике глистов или простейших.
В некоторых анализах описываются бактероиды, роль которых неясна, но известно, что это – не вредные бактерии, обычно их количество не имеет практического значения.
Все остальные показатели микрофлоры являются условно-патогенной флорой. В самом термине “условно-патогенный” обозначена суть данных микробов. Они становятся патогенными (нарушающими нормальные функции кишечника) при определенных условиях: повышение их абсолютного количества или процентного соотношения к нормальной флоре, при неэффективности защитных механизмов или снижении функции иммунной системы. Условно-патогенная флора – это лактозонегативные энтеробактерии (клебсиелла, протей, цитробактеры, энтеробактеры, гафнии, серрации), гемолизирующая кишечная палочка и различные кокки (энтерококки, эпидермальные или сапрофитные стафилококки, золотистый стафилококк). Кроме того, к условно-патогенным относятся клостридии, которые высеваются не во всех лабораториях. Условно-патогенная флора внедряется, конкурируя с полезными бактериями, в микрбную пленку кишечника, заселяет кишечную стенку и вызывает нарушения работы всего желудочно-кишечного тракта. 7), это чаще всего связано со снижением нормальной флоры. В редких случаях повышение количества энтерококков является главной причиной дисфункции, связанной с дисбактериозом.
7), это чаще всего связано со снижением нормальной флоры. В редких случаях повышение количества энтерококков является главной причиной дисфункции, связанной с дисбактериозом.
Эпидермальный (или сапрофитный) стафилококк (S. epidermidis, S. saprophyticus). Эти виды стафилококков могут вызывать нарушения, но их количество до 25% является допустимым.
Процент гемолизирующих кокков по отношению ко всем кокковым формам. Даже среди относительно безобидных кокков, названных выше, могут встречаться более патогенные, что и обозначается в этой позиции. Если общее количество кокков составляет, например, 16%, а процент гемолизирующих кокков – 50%, это значит, что половина из 16% — более вредоносные кокки, а их процент по отношению к нормальной флоре составляет 8%.
Золотистый стафилококк (S. aureus). Один из самых неприятных (наряду с гемолизирующей кишечной палочкой, протеем и клебсиеллой) представителей условно-патогенной флоры. Даже небольшие его количества могут вызвать выраженные клинические проявления, особенно у детей первых месяцев жизни. 3). Патогенность золотистого стафилококка напрямую зависит от состояния нормальной флоры: чем больше бифидобактерий, лактобактерий и нормальной кишечной палочки, тем меньше вреда от стафилококка. Присутствие его в кишечнике может приводить к аллергическим реакциям, гнойничковым кожным высыпаниям, дисфункции кишечника. Стафилококки являются распространенными микробами окружающей среды, в частности, они в больших количествах живут на коже и слизистых оболочках верхних дыхательных путей. Ребенку они могут попадать через грудное молоко. Наиболее подвержены заражению стафилококками ослабленные дети (проблемная беременность, недоношенность, кесарево сечение, искусственное вскармливание, применение антибиотиков – факторы риска ослабления функций иммунной системы). Важно понимать, что стафилококки как и другие условно-патогенные бактерии проявляют себя при определенных условиях, главным из которых является ослабление иммунитета, поэтому важным при лечении дисбактериоза, ассоциированного со стафилококком, является проведение иммунокоригирующей терапии.
3). Патогенность золотистого стафилококка напрямую зависит от состояния нормальной флоры: чем больше бифидобактерий, лактобактерий и нормальной кишечной палочки, тем меньше вреда от стафилококка. Присутствие его в кишечнике может приводить к аллергическим реакциям, гнойничковым кожным высыпаниям, дисфункции кишечника. Стафилококки являются распространенными микробами окружающей среды, в частности, они в больших количествах живут на коже и слизистых оболочках верхних дыхательных путей. Ребенку они могут попадать через грудное молоко. Наиболее подвержены заражению стафилококками ослабленные дети (проблемная беременность, недоношенность, кесарево сечение, искусственное вскармливание, применение антибиотиков – факторы риска ослабления функций иммунной системы). Важно понимать, что стафилококки как и другие условно-патогенные бактерии проявляют себя при определенных условиях, главным из которых является ослабление иммунитета, поэтому важным при лечении дисбактериоза, ассоциированного со стафилококком, является проведение иммунокоригирующей терапии.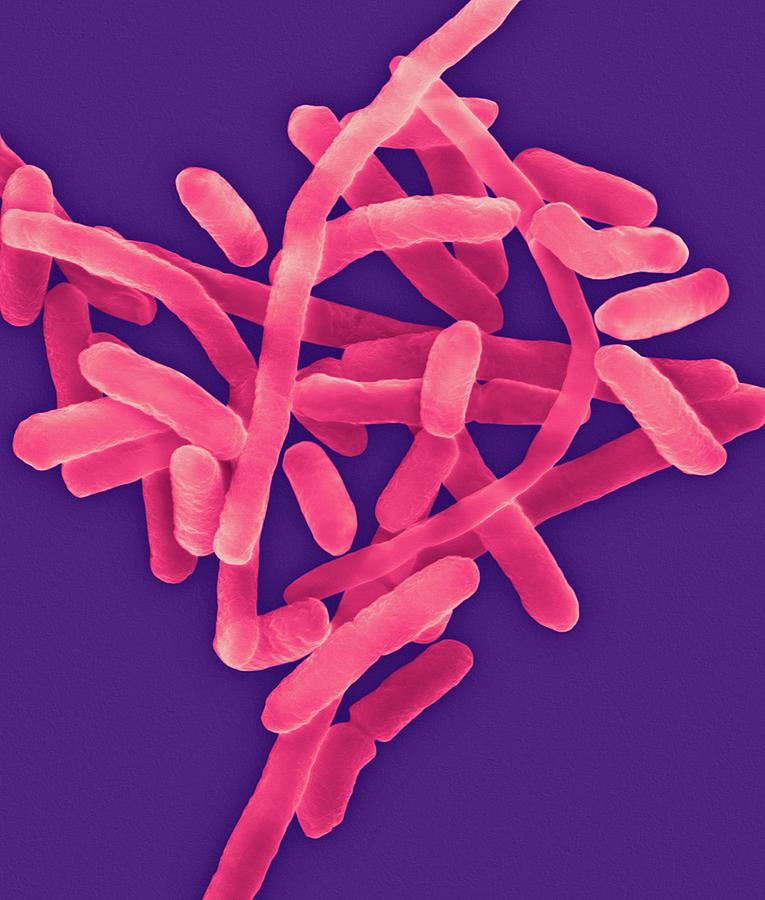
Гемолизирующая кишечная палочка. Является представителем лактозонегативных энтеробактерий, но выделяется отдельно в связи с распространенностью и значимостью. В норме должна отсутствовать. К данному микробу применимо практически все, сказанное про золотистый стафилококк. То есть, она может вызывать аллергические и кишечные проблемы, очень распространена в окружающей среде (правда, практически никогда не встречается в грудном молоке), вызывает проблемы у ослабленных детей, требует иммунокоррекции. Следует отметить, что термин “гемолизирующая” не означает, что имеется какое-то влияние на кровь. Условно-патогенная флора при дисбактериозе не должна преодолевать кишечную стенку и попадать в кровь. Это возможно только при крайне выраженных формах дисбактериоза у детей с выраженными иммунодефицитами, как правило, представляющих угрозу для жизни. К счастью, такие состояния встречаются нечасто.
Лактозонегативные энтеробактерии. Большая группа условно-патогенных бактерий большей или меньшей степени патогенности. 7. Проявляют патогенность обычно в комплексе с другой условно-патогенной флорой, редко изолированно вызывают проблемы (чаще всего – разжижение стула, понос). Их количество зависит от функции местного иммунитета кишечника.
7. Проявляют патогенность обычно в комплексе с другой условно-патогенной флорой, редко изолированно вызывают проблемы (чаще всего – разжижение стула, понос). Их количество зависит от функции местного иммунитета кишечника.
Прочие микроорганизмы. В данном параметре описываются редко встречающиеся виды бактерий, самым опасным из которых является синегнойная палочка (Pseudomonas aerugenosa). Чаще всего, микроорганизмы, описанные в этой позиции анализа не имеют практического значения.
Термин “abs” обозначает отсутствие данного микроорганизма, также употребляется “не обнаружено”.
Что такое Citrobacter Freundii? | Возбудитель месяца
Бактерии, возбудитель месяца
Автор Чандана Баласубраманян, 30 ноября 2021 г.
Содержание
Citrobacter freundii теперь вызывает озабоченность. Когда-то считавшиеся невирулентными, бактерии все чаще становятся полирезистентными к лекарственным препаратам (MDR) или устойчивыми к противомикробным препаратам (AMR).
Открытие пенициллина — первого антибиотика — стало революционным. Препарат был обнаружен Александром Флемингом в 1928 году и стал коммерчески доступным примерно в 1945 году благодаря исследованиям Говарда Флори и Эрнеста Чейн в Оксфорде. Пенициллин изменил курс современной медицины. Если раньше люди умирали от инфекций мочевыводящих путей, тонзиллита и пневмонии, то эволюция антибиотиков продолжает спасать миллионы жизней во всем мире [3].
Однако, как говорится, «с большой силой приходит и большая ответственность» (Стэн Ли, создатель вселенной Marvel).
К сожалению, основными причинами сегодняшнего кризиса УПП являются:
- чрезмерное использование антибиотиков,
- неправильное использование антибиотиков у животных и
- неправильное использование антибиотиков, которые не уничтожают возбудителя.

Чтобы помочь клиницистам бороться с УПП, Американское общество инфекционистов (IDSA) в ноябре 2021 года выпустило новые рекомендации по лечению трех наиболее устойчивых к лекарствам патогенов. К ним относятся семьи, которым Citrobacter spp. принадлежит [4].
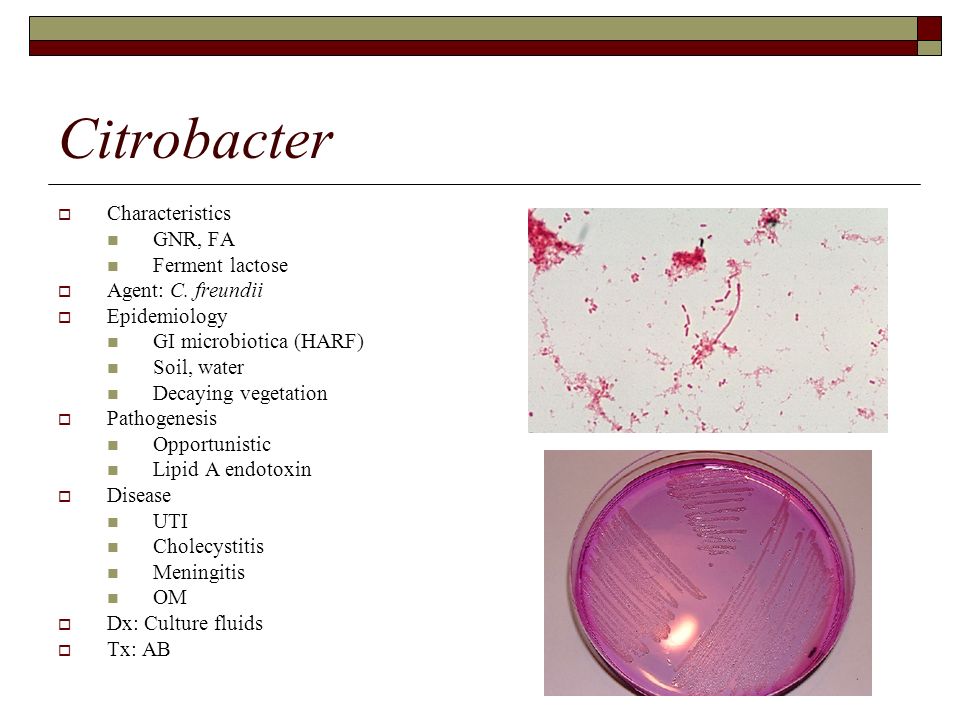
Что такое Citrobacter freundii?
Citrobacter freundii — это факультативная грамотрицательная анаэробная бактерия. Он имеет форму палочки и имеет длину около 1-5 мкм. Большинство клеток Citrobacter freundii имеют жгутики и подвижны, но некоторые нет.
Является членом семейства Enterobacteriaceae, включающего 15 геномных видов. Некоторыми из наиболее часто обсуждаемых являются Citrobacter amalonaticus и Цитробактер козери .
Поскольку они являются факультативными, они могут предпочитать аэробное дыхание в присутствии кислорода. Однако они могут перейти на анаэробное дыхание без кислорода и ферментировать углерод с помощью цитрата.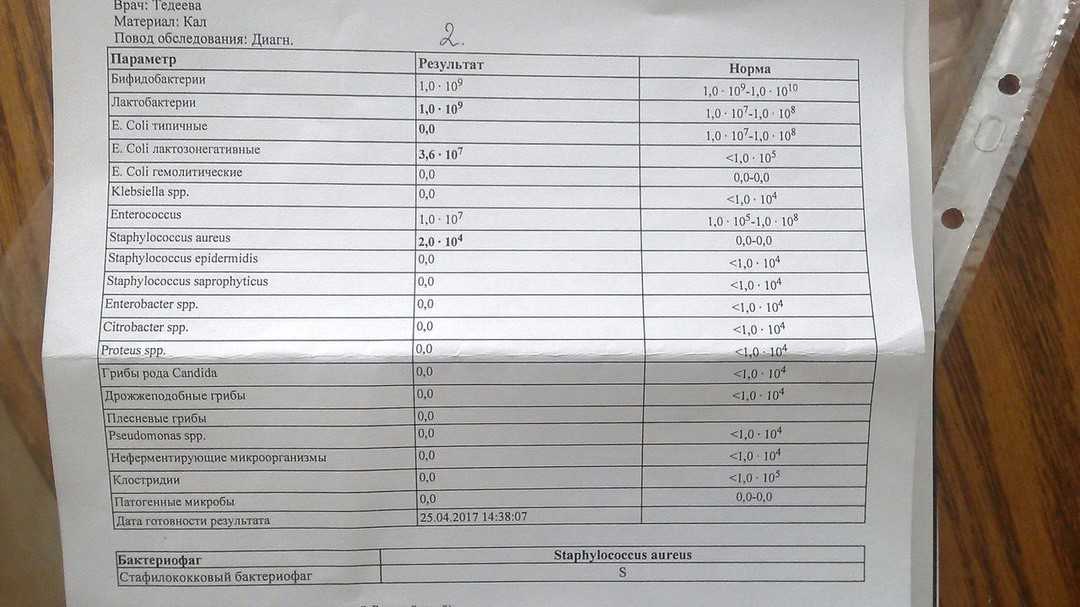 Кроме того, Citrobacter koseri также может ферментировать лактозу [5].
Кроме того, Citrobacter koseri также может ферментировать лактозу [5].
Где найти?
Citrobacter freundii обычно обнаруживается в воде, почве, пище и кишечнике людей и животных. Бактерии были впервые обнаружены в 1932 путем выделения чистой культуры из почвы [6].
Это обычный компонент нашей кишечной флоры, и многие штаммы считаются «хорошими кишечными бактериями» и полезны. Однако некоторые штаммы со временем трансформировались и выработали устойчивость к обычным антибиотикам (MDR). В результате инфекции могут быть трудно или даже невозможно лечить.
Какие заболевания вызывают бактерии Citrobacter freundii?
Citrobacter freundii может вызывать инфекции мочевыводящих путей, менингит, абсцессы головного мозга, сепсис, пневмонию, диарею, респираторные и раневые инфекции [7].
Как передается? Опасен ли этот тип цитробактеров?
Citrobacter freundii чаще всего является внутрибольничной инфекцией (ИСМП) и передается внутрибольничным путем. Больные приобретают их после госпитализации.
Больные приобретают их после госпитализации.
Инфекции, вызванные Citrobacter freundii , называются «оппортунистическими заболеваниями» (ОИ). Бактерия считается условно-патогенным микробом. Это связано с тем, что бактерии предпочитают заражать пациентов с ослабленным иммунитетом, пожилых людей, людей с множественными сопутствующими заболеваниями и тех, кто длительное время находился в отделении интенсивной терапии (ОИТ) или в стационаре [8].
Симптомы часто включают чувство жжения при мочеиспускании, более частые позывы к мочеиспусканию, неприятный запах мочи, кровь в моче. Другие симптомы включают высокую температуру, рвоту, судороги и многое другое.
Без обработки, Citrobacter spp. Инфекции могут быть опасными и даже смертельными. Инвазивные инфекции имеют высокий уровень смертности 33–48% [7].
Как диагностировать инфекцию Citrobacter freundii?
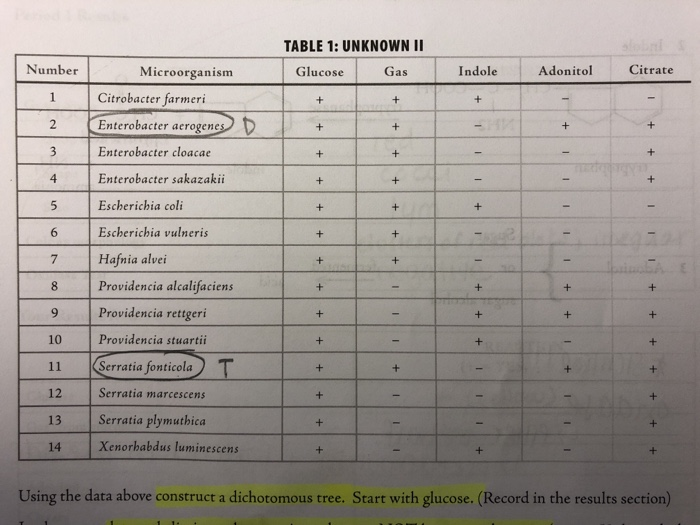
Единственный способ диагностировать 9Инфицирование 0009 Citrobacter freundii происходит через посев.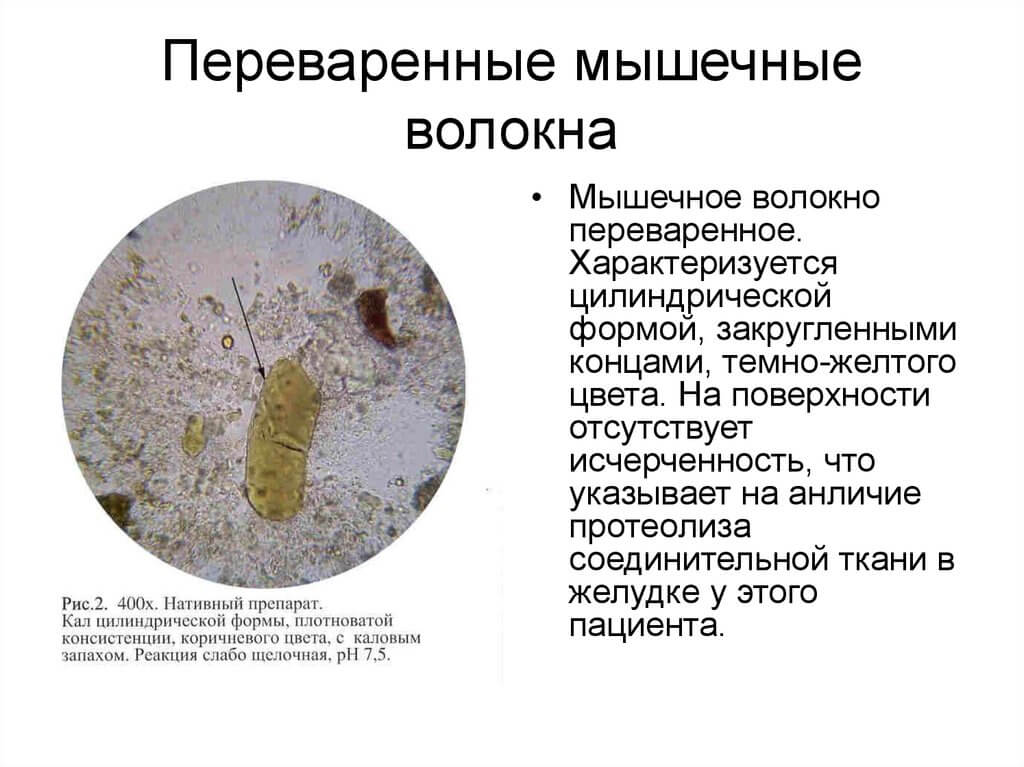 Citrobacter freundii ферментируют глюкозу, выделяют газ и потребляют цитрат. Большинство из них подвижны. В анаэробном режиме они ферментируют углерод.
Citrobacter freundii ферментируют глюкозу, выделяют газ и потребляют цитрат. Большинство из них подвижны. В анаэробном режиме они ферментируют углерод.
К каким препаратам он устойчив?
Изоляты Citrobacter freundii продемонстрировали устойчивость к традиционным агентам противомикробной химиотерапии. К ним относятся ампициллин, карбенициллин и цефалотин. Они также проявляют устойчивость к таким агентам, как цефалоспорины третьего поколения и монобактамы [9].] [10].
Многоцентровое исследование in vitro в Китае, проведенное в 2019 г. Zhou et al. обнаружили, что среди 20 штаммов Citrobacter, выделенных от животных, устойчивость была в основном к ампициллину, тетрациклину, стрептомицину, флорфениколу, хлорамфениколу и азтреонаму, в то время как все штаммы, обнаруженные в образцах окружающей среды, были устойчивы к нескольким антибиотикам [11].
В 2018 г. Yang et al. выделил штамм Citrobacter freundii (CWH001) с высокой множественной лекарственной устойчивостью, продуцирующий карбапенемазу, устойчивый ко всем протестированным противомикробным препаратам, кроме тетрациклина [12].
Эта ситуация вызывает тревогу, поскольку карбапенемы относятся к классу антибиотиков, используемых для лечения тяжелых инфекций. Резистентные к карбапенемам энтеробактерии становятся устойчивыми почти ко всем доступным антибиотикам. Эти бактерии производят карбапенемазы, ферменты, которые могут сделать большинство антибиотиков неэффективными. Существует три класса ферментов, которые вызывают резистентность к карбапенемам. Это:
- карбапенемазы класса А,
- металло-β-лактамазы класса В (MBL) и
- β-лактамазы класса D (OXA).
Фермент карбапенемаза под названием OXA-48 (класс D) вырабатывается растущим числом устойчивых к карбапенемам бактерий и быстро распространяется в Средиземноморском регионе и на Ближнем Востоке. Недавно даже европейские страны, такие как Нидерланды, Бельгия, Италия, Великобритания и Швейцария, обнаружили присутствие OXA-48. Обнаружено больше устойчивых к лекарствам ферментов OXA, включая OXA-181 и OXA-163.
Эти ферменты OXA могут ускользнуть от обычных диагностических тестов, что проблематично. Необходимы дополнительные исследования, чтобы помочь повысить точность и эффективность диагностических тестов и методов лечения Enterobacteriaceae, продуцирующих карбапенемазы [13].
Как лечить?
До недавнего времени карбапенемы были наиболее эффективными антибиотиками для лечения серьезных инфекций Citrobacter freundii . Однако из-за растущей резистентности к карбапенемам лечение этих инфекций с помощью карбапенемов стало затруднительным.
С бактериями МЛУ или УПП очень трудно бороться. Клиницистам, возможно, придется использовать более сильные антибиотики в качестве терапии этих инфекций. В этих случаях сильнодействующие препараты также могут быть токсичными для пациентов с ослабленным иммунитетом.
Клиницисты могут обратиться к недавно выпущенному руководству IDSA от ноября 2021 г. по лечению грамотрицательных инфекций УПП.
Эволюция борьбы с бактериями, вызывающими МЛУ и УПП
Устойчивость бактерий к лекарствам может проявляться двумя способами:
- Одна бактерия может иметь несколько генов, каждый из которых устойчив к определенному антибиотику, или
- Бактерия может использовать один механизм одновременное определение нескольких антибиотиков.

Гены устойчивости к антибиотикам у бактерий часто располагаются на плазмидах. Плазмиды представляют собой небольшие кольцевые нити ДНК, которые могут передавать и распространять устойчивость к антибиотикам между бактериями. Они даже могут передавать устойчивость сразу к нескольким антибиотикам. В медицинских учреждениях разновидности бактерий с МЛУ могут стать доминирующими штаммами и создать более тревожные супербактерии [14].
Плазмиды, содержащие гены MDR, часто являются конъюгативными, что означает, что они могут переносить себя и другие плазмиды. В настоящее время ученые и исследователи используют генно-инженерные плазмиды в качестве новой терапии на основе CRISPR для борьбы с УПП. Это достижение дает надежду на борьбу с УПП. Однако, хотя это может помочь атаковать гены лекарственной устойчивости, присутствующие на плазмидах, это не относится к бактериям, у которых лекарственная устойчивость закодирована в их хромосомной ДНК [15].
Основная проблема в борьбе с возбудителями УПП заключается в том, что они мутируют быстрее, чем позволяют наши исследования и технологии. В то время как ученые продолжают изучать эти мутации и разрабатывать новые методы лечения, клиницисты должны ограничивать использование антибиотиков только надлежащим и необходимым применением. В противном случае мы продолжим производить более сильные супербактерии, которые могут вызвать широкое распространение инфекции и даже смерть.
В то время как ученые продолжают изучать эти мутации и разрабатывать новые методы лечения, клиницисты должны ограничивать использование антибиотиков только надлежащим и необходимым применением. В противном случае мы продолжим производить более сильные супербактерии, которые могут вызвать широкое распространение инфекции и даже смерть.
Кроме того, все больше стран и учреждений общественного здравоохранения должны поддерживать основанные на данных научные исследования новых инфекционных заболеваний и патогенов. Например, более 200 научных публикаций использовали обширную базу данных по инфекционным заболеваниям GIDEON для исследования инфекционных заболеваний и патогенов. Повышение осведомленности научного сообщества о доступе к надежным онлайн-ресурсам, таким как обширная библиотека электронных книг GIDEON, может быть чрезвычайно полезным.
Отличие GIDEON
GIDEON — одна из самых известных и всеобъемлющих глобальных баз данных по инфекционным заболеваниям. Данные обновляются ежедневно, а GIDEON API предоставляет медицинским работникам и исследователям доступ к непрерывному потоку данных. Независимо от того, включает ли ваше исследование количественную оценку данных, изучение конкретных микробов или тестирование инструментов дифференциальной диагностики, GIDEON предоставит вам программу, соответствующую стандартам доступности. Вы также можете ознакомиться с нашими электронными книгами об австралийско-тихоокеанских арбовирусах, кожных мигрирующих личинках, вирусе герпеса человека 6 и многом другом. Или проверьте наши глобальные обновления статуса в таких странах, как Гибралтар, Венгрия, Иордания и других!
Данные обновляются ежедневно, а GIDEON API предоставляет медицинским работникам и исследователям доступ к непрерывному потоку данных. Независимо от того, включает ли ваше исследование количественную оценку данных, изучение конкретных микробов или тестирование инструментов дифференциальной диагностики, GIDEON предоставит вам программу, соответствующую стандартам доступности. Вы также можете ознакомиться с нашими электронными книгами об австралийско-тихоокеанских арбовирусах, кожных мигрирующих личинках, вирусе герпеса человека 6 и многом другом. Или проверьте наши глобальные обновления статуса в таких странах, как Гибралтар, Венгрия, Иордания и других!
Список литературы
| [1] | Всемирная организация здравоохранения (ВОЗ), «Антимикровиальное сопротивление», ВОЗ, 17 11 2021. [онлайн] [ВОЗ). |
| [2] | Центры по контролю и профилактике заболеваний (CDC), «Устойчивость к антибиотикам/противомикробным препаратам (AR/AMR)», CDC, 20 июля 2020 г. [Онлайн] [По состоянию на 30 ноября 2021 г.]. [Онлайн] [По состоянию на 30 ноября 2021 г.]. |
| [3] | Аминов Р.И. Краткая история эпохи антибиотиков: извлеченные уроки и задачи на будущее, Frontiers in Microbiology, vol. Опубликовано в Интернете, с. 1:134, 2010. |
| [4] | Т. Д. Пранита, С. Л. Эйткен, Р. А. Бономо, А. Дж. Мазерс, Д. Ван Дуин и К. Дж. Клэнси, «Руководство IDSA по лечению устойчивых к противомикробным препаратам грамотрицательных инфекций: Версия 2.0», Американское общество инфекционных заболеваний (IDSA), 22 ноября 2021 г. [Онлайн] [По состоянию на 30 ноября 2021 г.]. |
| [5] | K. P. Ranjan and N. Ranjan, «Citrobacter: новый патоген, связанный с оказанием медицинской помощи в моче», Анналы урологии, том. 5, нет. 4, с. 313–314, 2013. |
| [6] | J. T. Wang, S. C. Chang, Y. C. Chen и K. T. Luh, «Сравнение чувствительности изолята Citrobacter freundii к противомикробным препаратам в два разных периода времени», J Microbiol.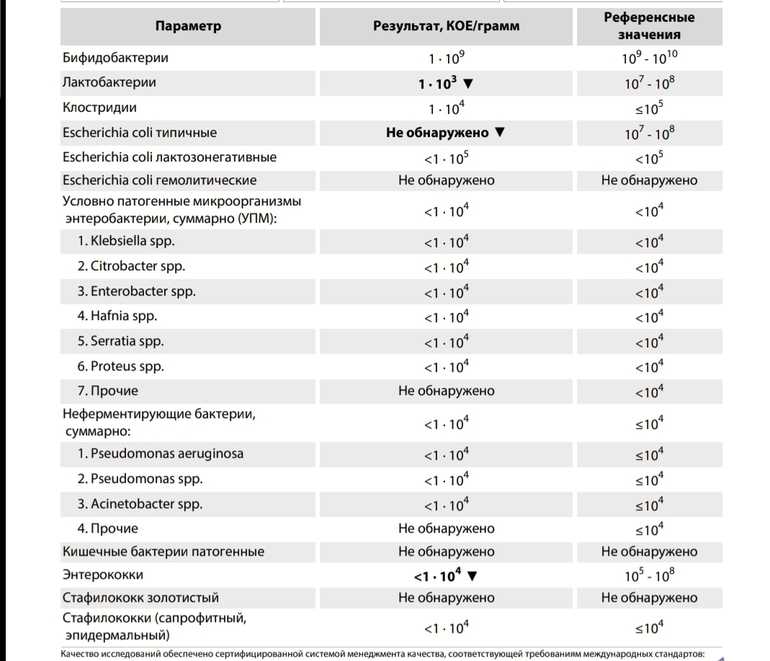 , Immunol Infect. том. 33, нет. 4, pp. 258-62, 2000. , Immunol Infect. том. 33, нет. 4, pp. 258-62, 2000. |
| [7] | C. Pepperell, JV Kus, M.A. Gardam, A. Humar and L.L. Burrows, «Low-Virulence Citrobacter Species Encode Resistance to Multiple Antimicrobials», Антимикробные агенты и химиотерапия, vol. 46, нет. 11, с. 3555–3560, 2002. |
| [8] | А. Ф. Монегро, В. Муппиди и Х. Регунат, «Больничные инфекции», StatPearls Publishing [Интернет], 30 августа 2021 г. [Онлайн] [Доступ 302 11 2021]. ]. |
| .0010 том. 25, нет. 5, pp. 591-5, 1984. | |
| [10] | P. Gaibani, S. Ambretti, P. Farruggia, G. Bua, A. Berlingeri, M.V. Tamburini, M. Cordovana, L. Guerra, M. Mazzetti, G. Roncarati, C. Tenace, M.L. Moro, C. Gagliotti, M.P. Landini и S. Vittorio, «Вспышка Citrobacter freundii, несущих VIM-1, в итальянской больнице, выявленная во время скрининга карбапенемаз, июнь 2012 г., Int J Infect Dis, vol. 17, нет. 2013. Т. 9. С. 714–7. 2013. Т. 9. С. 714–7. |
| [11] | В. Чжоу, К. Чен, К. Цянь, К. Шен, С. Чжу, Д. Чжоу, В. Лу, З. Сунь, Х. Лю, К. Ли, Т. Сюй , Q. Bao и J. Lu, «In Vitro Susceptibility and Florfenicol Resistance in Vitrobacter Isolates and Full-Genome Analysis of Multidrug-Resistant Citrobacter freundii», International Journal of Genomics, 2019. |
| [12] | Л. Ян, П. Ли, Б. Лян, С. Ху, Дж. Ли, Дж. Се, К. Ян, Р. Хао, Л. Ван, Л. Цзя, П. Ли, С. Цю и Х. Песня «Citrobacter freundii ST139 с множественной лекарственной устойчивостью».совместное производство NDM-1 и CMY-152 из Китая», Scientific Reports, vol. 10653, 2018. |
| [13] | А. Стюарт, П. Харрис, А. Хендерсон и Д. Патерсон, «Лечение инфекций с помощью OXA-48-продуцирующих энтеробактерий», Антимикробные агенты и химиотерапия, об. 62, нет. 11, 2018. |
| [14] | М. Розвандович, М.С.М. Брауэр, Дж. Фишер, Дж.А. Вагенаар, Б. Гонсалес-Зорн, Б. Герра, Д.Дж. гены Enterobacteriaceae», Журнал антимикробной химиотерапии, vol. 73, нет. 5, с. 1121–1137, 2018. Герра, Д.Дж. гены Enterobacteriaceae», Журнал антимикробной химиотерапии, vol. 73, нет. 5, с. 1121–1137, 2018. |
| [15] | M. Rodrigues, S. W. McBride, K. Hullahalli, K. L. Palmer и B. A. Duerkop, «Конъюгативная доставка CRISPR-Cas9 для селективного истощения Противомикробные агенты и химиотерапия, vol. 63, нет. 11, 2019. |
Статьи, которые вы не удалите.
Еженедельно в ваш почтовый ящик. Пожалуйста, оставьте это поле пустым. Пожалуйста, оставьте это поле пустым.
Нужны самые подробные и актуальные данные об инфекционных заболеваниях?
Генерируйте эпидемиологические диаграммы
Дифференциальный диагноз с вероятностью двигателя
Сравнение заболеваний
ДАБОЛОТАЯ ДОБАВИТЕЛЬНЫЕ ДОБАВИТЬ
Сценарий первого случая
. функция
Связанные статьи
Эпидемиология, инфекционные заболевания, вирусы
Гепатит В (HBV), «Тихая эпидемия»: эпидемиология, вакцинация, симптомы и лечение
Эпидемия, инфекционные диску.
Свинка: как она распространяется, вспышки, вакцина MMR и многое другое
Этот сайт использует файлы cookie. Если вы не возражаете, просто нажмите принять и продолжить просмотр. Принять
Управление согласием
Основы дисбактериоза и тесты — MyBioHack
Здесь вы можете найти самые сильные тактики, которые наука может предложить для преодоления и улучшения состояния при хронических заболеваниях.
Джейкоб Гордон
Каждый врач, которого я посещал, говорил мне, что у меня синдром раздраженного кишечника или все мои симптомы были только в моей голове.
СРК — это не настоящая вещь.
Это был не мозг моей головы.
Это был мой второй мозг который был испорчен.
Contents
Gut Biome Basics
SIBO
Dysbiosis
Intestinal Barrier Dysfunction
Tests
Eliminate Pathogens
Restore Beneficial Bacteria
More Research
Основы биома кишечника
Кишечник представляет собой интегрированную систему, состоящую из иммунных, эндокринных и нейронных компонентов. р
р
Second Brain
Когда кто-то говорит «иди с тобой» «внутреннее чувство», он может не знать, что на самом деле имеет в виду.
Микробиота в нашем кишечнике, которую иногда называют «вторым геномом» или «вторым мозгом», влияет на наше настроение. R
Кишечник и мозг тесно связаны в определенных эмоциональных состояниях и интуитивном принятии решений. R
Микробиом тесно связан с иммунной системой, которая влияет на настроение и поведение. р
Микробы в нашем кишечнике влияют на мозг с помощью множества механизмов. R
Кишечные бактерии производят нейротрансмиттеры, такие как серотонин, дофамин и ГАМК. R
Кишечные бактерии влияют на то, как люди метаболизируют соединения, влияя на кровь и мозг. R
Кишечные бактерии вырабатывают нейроактивные химические вещества, такие как бутират, который связан с уменьшением беспокойства и депрессии. R
Некоторые микробы активируют блуждающий нерв.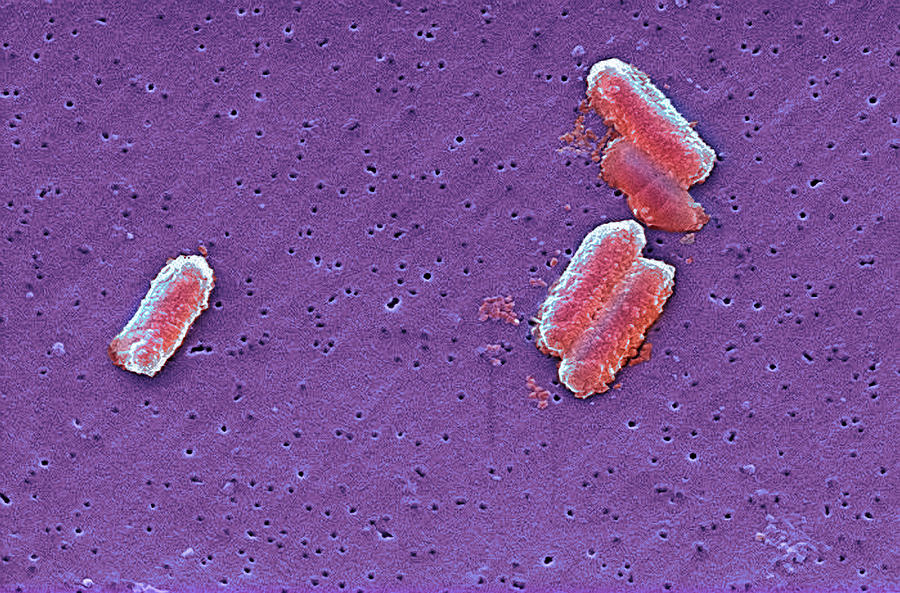 R
R
Узнайте все об оси мозг-кишка здесь.
Синдром раздраженного кишечника ненастоящий
Если кто-то сказал вам, что у него СРК, он ошибся. СРК имеет много причин.
Было показано, что одной из этих причин является уменьшение количества микробиоты, и обычно считается, что воспаление кишечника связано с уменьшением бактериального разнообразия. R R R
СРК обычно может быть вызван постинфекционной или еще не обнаруженной активной инфекцией. Р
Это я много лет назад. СИБР может заставить вас выглядеть и чувствовать себя беременной.
СИБР, или избыточный бактериальный рост в тонком кишечнике, представляет собой увеличение количества и/или изменение типа бактерий в верхних отделах желудочно-кишечного тракта. R
Пациенты с СИБР проявляются по-разному: у некоторых симптомы проявляются слабо, в то время как другие могут страдать хронической диареей, потерей веса и нарушением всасывания.
Антибиотики могут быть вредными. Они могут способствовать чрезмерному росту кишечника, убивая полезные бактерии.
Прием антибиотиков увеличивает риск развития СРК. R
Некоторые антибиотики, такие как рифаксамин, могут быть полезными. Вероятно, это связано с тем, что он нацелен на определенные бактерии и патогены.
При циррозе несколько факторов способствуют чрезмерному бактериальному росту кишечника.
К ним относятся нарушение перистальтики тонкого кишечника, уменьшение выделения желчи и изменение секреции иммуноглобулина А и противомикробных молекул. R
Это снижение сопровождается снижением противомикробной активности в отношении Enterobacteriaceae. р
Дисбактериоз
Стенка желудочно-кишечного тракта
Дисбактериоз — это нарушение баланса микробиоты. Это может быть вредным, если это происходит в вашем кишечнике.
Заболевания, связанные с дисбактериозом, включают:
воспалительные заболевания кишечника R
синдром раздраженного кишечника (СРК) R
глютеновая болезнь R
9002 аллергия0003asthma R
metabolic syndrome R
cardiovascular disease R
obesity R
Dysbiosis can cause changes in diet, obesity, immunologic, and neurological diseases that impact brain function and behavior . R
R
Также может вызывать гипертонию. R
Желчь (усугубляемая западной диетой) может увеличивать опухоль у лиц с дисбактериозом. R
Антибиотик рифампин помогает при некоторых симптомах СРК, вызванных дисбиозом, хотя может усугубить их. р
Другие исследователи сосредоточились на возможной нераспознанной протозойной инфекции, такой как бластоцистоз, как на причине СРК, поскольку некоторые протозойные инфекции чаще встречаются у пациентов с СРК. R
Таким образом, нарушенная защита кишечника хозяина может способствовать качественным и количественным изменениям кишечного микробиома, связанным с терминальной стадией заболевания печени. R
Дисфункция кишечного барьера
Проницаемость кишечника (также известная как проницаемость кишечника)
Проницаемость кишечника связана с массой тела, ожирением печени и резистентностью к инсулину у людей с ожирением, подвергающихся снижению веса. р
Щелкните здесь, чтобы узнать, как устранить протекающую кишку и устранить любые проблемы с ее проницаемостью.
Я использую тест зумера кишечника с моими клиентами для выявления дисбиотических патогенов и тест на органические кислоты для выявления скрытых инфекций, таких как клостридии и кандиды.
Уничтожение патогенов
СИБР
Существует два «традиционных» способа избавления от дисбиотических возбудителей при СИБР. Рифаксимин, или лечение травами. Рифаксмин столь же эффективен, как и лечение травами. R Я сделал и то, и другое.
Вот мой протокол:
Во время моего выздоровления я, к счастью, жил в Лос-Анджелесе, где у меня была связь с врачом, который был близким другом доктора Марка Пиментеля. Доктор Пиментел, автор книги «Новое решение СРК», рекомендует использовать рифаксамин. R
Большинство врачей придерживаются диеты с низким содержанием FODMAP. Это может быть проблематично, поскольку, когда у бактерий нет пищи, они могут впасть в спячку и спрятаться в биопленке .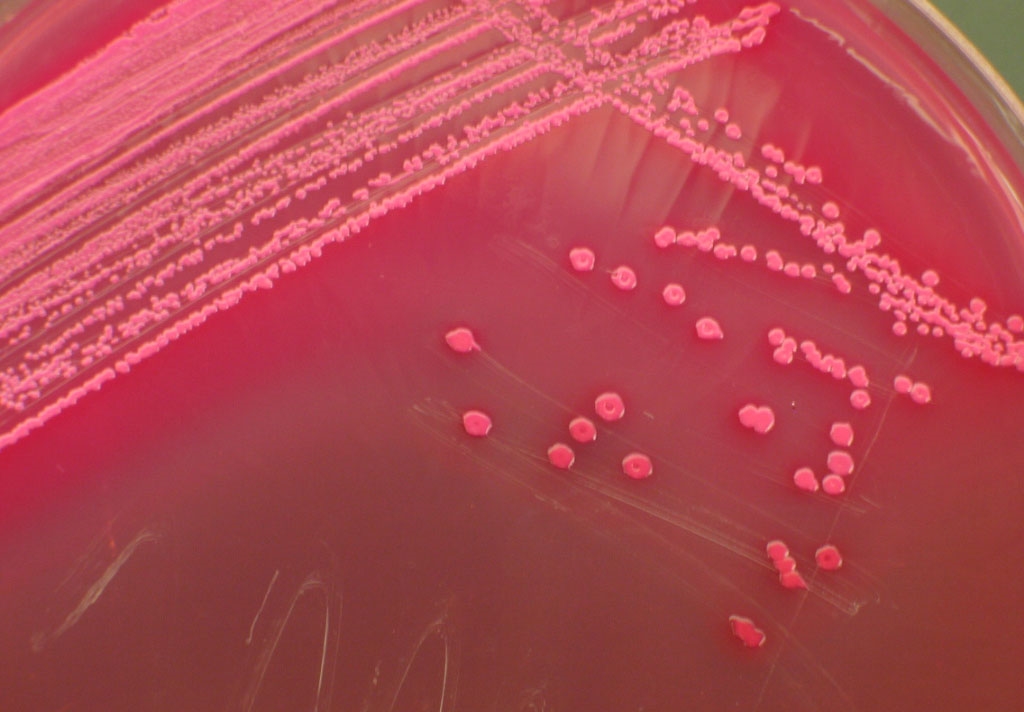 R
R
Добавление частично гидролизованной гуаровой камеди повышает эффективность лечения рифаксимином. R
Глина оказалась полезной из-за ее способности связываться с патогенами. R
Дисбактериоз
Я провел комплексный анализ стула , и результаты показали высокий уровень грамотрицательных бактерий Citrobacter Freundii. Я принял интенсивный протокол, чтобы убить его:
LightForce Pro (на мой кишечник 3-5 раз в неделю в течение 1 месяца)
Экстракт виноградных косточек
Коллоидное серебро
Последующее наблюдение Комплексный анализ стула показал, что этот протокол эффективен.
Восстановление полезных бактерий
Восстановление биома кишечника может быть сложной задачей.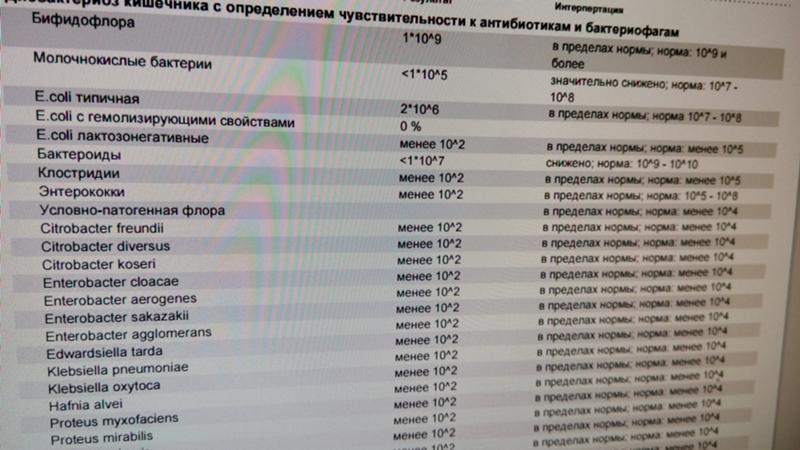
Биом вашего кишечника питается всем, что вы кладете в рот.
Патогены будут расти на плохих продуктах, в то время как хорошие бактерии будут процветать на здоровых продуктах.
Есть две вещи, которые мы хотим сделать, чтобы восстановить полезные бактерии.
Добавка с НАДЛЕЖАЩИМИ полезными бактериями
Поддержите эти бактерии ферментированными продуктами или пребиотиками
какие бактерии нужно восстановить).
Лучше всего для этого подходят данные врача или SmartGut/uBiome.
Кроме того, Я НАСТОЯТЕЛЬНО РЕКОМЕНДУЮ получить тест Spectracell Micronutrient test , так как после дисбактериоза высока вероятность мальабсорбции. R
Пробиотики
На рынке представлено множество видов пробиотических штаммов, которые можно использовать в качестве добавок. Я МНОГО пробовал и заметил, что штаммы Lactobacillus вызывают у меня тошноту и запоры.
Моим возбудителем был citrobacter freundii, который производит много гистамина .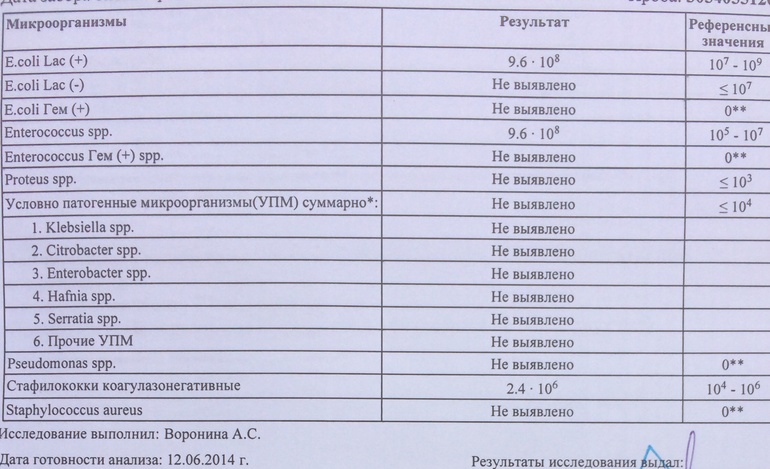 R
R
Некоторые штаммы молочнокислых бактерий также продуцируют гистамин. R R (L. Reuteri вырабатывает гистамин, но может быть полезным)
По сути, я добился непереносимости гистамина, принимая пробиотики.
Несколько штаммов бифидобактерий расщепляют гистамин , поэтому я обнаружил, что попытка только штаммов бифидобактерий (которые не производят d-лактат) помогла ( Lactobacillus plantarum также расщепляет гистамин). R
У вас может быть иначе.
Пребиотики
Ваши кишечные бактерии питаются пребиотиками. Обязательно сначала уничтожьте все болезнетворные микроорганизмы, чтобы не кормить их.
После уничтожения цитробактера я перешел на сыроедение на 6 месяцев, чтобы не отравлять свой кишечник и не кормить неправильными бактериями.
Волокно хорошее. Бактерии ферментируют клетчатку в бутират в толстой кишке, а затем бутират помогает питать клетки, выстилающие кишечник.