Цитомегаловирусная инфекция у детей. Что такое Цитомегаловирусная инфекция у детей?
ВАЖНО
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Цитомегаловирусная инфекция у детей — это инфекционное заболевание, которое вызвано цитомегаловирусом и поражает слюнные железы, внутренние органы, ЦНС. В детстве патология чаще возникает при трансплацентарном или интранатальном заражении. Локализованные формы проявляются сиаладенитом, гепатитом, нефритом и т. д., распространенный вариант инфекции характеризуется поражением головного мозга, легких, почек и органов ЖКТ. Диагностика предполагает идентификацию возбудителя цитологическими, гистологическими, серологическими и молекулярно-биологическими методами. Лечение цитомегаловирусной болезни проводится специфическим иммуноглобулином и противовирусными препаратами.
Лечение цитомегаловирусной болезни проводится специфическим иммуноглобулином и противовирусными препаратами.
МКБ-10
В25 Цитомегаловирусная болезнь
- Причины
- Патогенез
- Классификация
- Симптомы
- Врожденная ЦМВИ
- Приобретенная ЦМВИ
- Генерализованная ЦМВИ
- Осложнения
- Диагностика
- Лечение цитомегаловирусной инфекции у детей
- Прогноз и профилактика
- Цены на лечение
Общие сведения
Заражение цитомегаловирусной инфекцией (ЦМВИ) наблюдается у 20%‒60% всего детского населения, но в большинстве случаев оно протекает бессимптомно. Внутриутробное инфицирование вирусом от больной матери происходит в 30-50% случаев, при этом до 18% младенцев после рождения имеют клинические симптомы. Учитывая полиморфизм клинической картины, ранняя диагностика и лечение у детей затруднены. Цитомегаловирусная инфекция представляет серьезную опасность, особенно для плода и новорожденного, у которых заболевание, как правило, вызывает необратимые осложнения.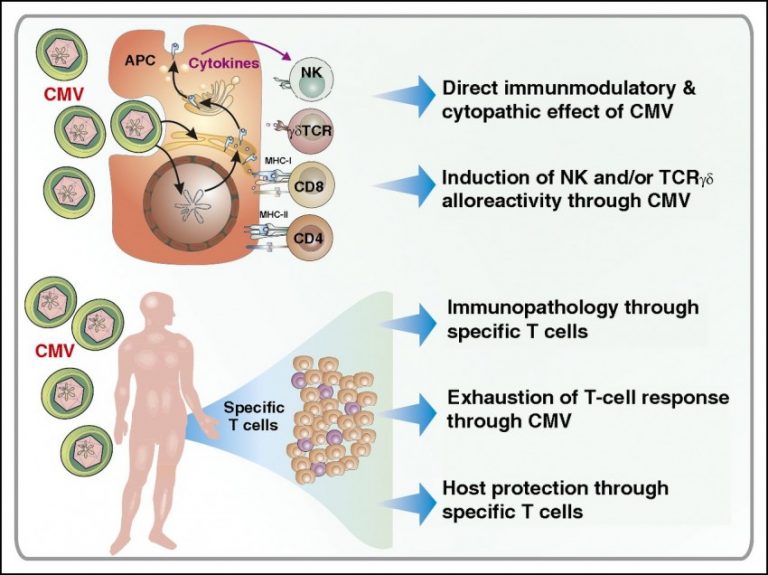
Цитомегаловирусная инфекция у детей
Причины
Болезнь вызвана герпесвирусом 5 типа — Cytomegalovirus hominis. Он имеет 6 штаммов: Davis, AD 169, Kerr, C-87, Esp, Towne, причем ребенок может быть инфицирован сразу несколькими подтипами возбудителя. Цитомегаловирус (ЦМВ) имеет ДНК-геном, отличается медленной репликацией и сравнительно низкой вирулентностью. Он термолабилен, уничтожается при температуре более 56°С, но длительно сохраняет жизнеспособность в комнатных условиях.
При врожденной ЦВМИ передача вируса к плоду происходит трансплацентарно, при перинатальной инфекции — путем контакта с вагинальными выделениями матери, грудным молоком или препаратами крови. Риск заражения увеличивается, если мать с острой формой болезни не получает специфическое лечение. В постнатальном периоде ребенок чаще всего заражается от ближайших родственников и сверстников воздушно-капельным или контактно-бытовым путем.
Патогенез
Попадая в кровь, вирус реплицируется в лейкоцитах, моноцитах и макрофагах и в дальнейшем он пожизненно сохраняется в лимфоцитарных органах. Зачастую процесс выражается в виде латентной инфекции, при которой у ребенка нет симптомов, и ему не требуется лечение. Активность цитомегаловируса зависит от состояния иммунитета: при физиологической иммунной недостаточности, которая наблюдается у детей раннего возраста, риск манифестной цитомегаловирусной инфекции возрастает в разы.
Классификация
В детской инфектологии различают врожденную (внутриутробную) и приобретенную формы патологии. По течению инфекция бывает острой (до 3 месяцев), подострой (3-6 месяцев), затяжной (6-12 месяцев) и хронической (более 1 года). По клиническим признакам выделяют локализованный (сиаладенит, нефрит, гепатит, энцефалит) и генерализованный вариант. С учетом тяжести течения цитомегаловирусную болезнь делят на 3 степени:
По течению инфекция бывает острой (до 3 месяцев), подострой (3-6 месяцев), затяжной (6-12 месяцев) и хронической (более 1 года). По клиническим признакам выделяют локализованный (сиаладенит, нефрит, гепатит, энцефалит) и генерализованный вариант. С учетом тяжести течения цитомегаловирусную болезнь делят на 3 степени:
- Легкая. Отличается незначительными патоморфологическими изменениями во внутренних органах, которые не сказываются на их функциональной активности.
- Среднетяжелая. Проявляется выраженными органическими поражениями в сочетании с клиническими симптомами и расстройством функции некоторых внутренних органов.
- Тяжелая. Манифестирует тяжелыми органическими патологиями, резко выраженной интоксикацией и генерализованным характером поражения.
Симптомы
Врожденная ЦМВИ
У пациентов с манифестной врожденной форме цитомегаловирусной болезни признаки наблюдаются с первых дней жизни. Типичный комплекс симптомов у новорожденных детей включает недоношенность и/или низкую массу тела, поражение гепатобилиарной системы (увеличение печени, желтуха, гепатиты и циррозы), лимфаденопатии и геморрагическую сыпь на коже. Если инфицирование произошло на ранних сроках беременности, ребенок рождается с аномалиями — микроцефалией, гипоплазией легких, атрезией пищевода.
Если инфицирование произошло на ранних сроках беременности, ребенок рождается с аномалиями — микроцефалией, гипоплазией легких, атрезией пищевода.
Приобретенная ЦМВИ
Приобретенная цитомегаловирусная болезнь обычно протекает в субклинической или латентной форме, когда у ребенка возникают гриппоподобные симптомы, субфебрильная температура без видимой причины. После заражения инфекция может длительное время себя не проявлять и давать обострения при снижении иммунного статуса, действии неблагоприятных эндо- или экзогенных факторов.
Течение манифестной приобретенной формы напоминает инфекционный мононуклеоз. У ребенка внезапно появляется слабость, повышается температура, беспокоят недомогание, головные боли, отсутствует аппетит. Позже присоединяются сильные боли в горле, увеличиваются подчелюстные и шейные лимфоузлы. Если цитомегаловирусная инфекция проявляется сиаладенитом, наблюдается резкое увеличение и болезненность слюнных желез на фоне фебрильной лихорадки.
Генерализованная ЦМВИ
При генерализованном варианте течения инфекции у детей поражается бронхолегочная система (пневмонии, дыхательная недостаточность), ЖКТ (энтероколит, мальабсорбция), печень (желтуха, цитомегаловирусный гепатит, билиарный цирроз). Особенно опасно вовлечение в процесс нервной системы, что проявляется судорожным синдромом, парезами и параличами, задержкой психомоторного развития.
Осложнения
Негативные последствия выявляются преимущественно у детей, страдающих врожденной цитомегаловирусной инфекцией. В 58% случаев после тяжелой формы заболевания остаются неврологические нарушения (парезы, соматосенсорная недостаточность), 28% детей отстают в умственном развитии. Для ЦМВИ характерно поражение слуха вплоть до глухоты (25% случаев) и необратимое снижение зрения (8-15%).
Поражение клеток при цитомегаловирусной болезни создает благоприятные условия для возникновения аутоиммунных поражений — системной красной волчанки, рассеянного склероза, гломерулонефрита. Иногда после малосимптомной врожденной цитомегаловирусной инфекции осложнения наблюдаются в отдаленном периоде (в возрасте ребенка 2-5 лет). В основном они проявляются неврологическими расстройствами и поражением органов чувств.
Иногда после малосимптомной врожденной цитомегаловирусной инфекции осложнения наблюдаются в отдаленном периоде (в возрасте ребенка 2-5 лет). В основном они проявляются неврологическими расстройствами и поражением органов чувств.
Диагностика
Цитомегаловирусная инфекция отличается многообразием клинических признаков и часто протекает под маской других патологий, что затрудняет работу детского инфекциониста. На первичном приеме, помимо стандартного физикального осмотра, врач собирает детальный акушерский анамнез, чтобы выявить факторы риска антенатального инфицирования. Диагноз ЦМВИ правомочен только при лабораторном подтверждении, для чего используют следующие методы:
- Цитологические анализы. Для исследования берут мочу, слюну, мокроту и другие биологические жидкости. При анализе специально окрашенных препаратов под микроскопом врач выявляет цитомегалы, которые являются патогномоничным признаком цитомегаловирусной инфекции. Метод обладает недостаточной чувствительностью, поэтому его повторяют многократно в течение 3-5 дней.

- Гистологические исследования. «Золотой стандарт» диагностики врожденной инфекции у детей предполагает исследование образцов плаценты. Важными критериями считают очаговые ишемические инфаркты, некроз базальной пластинки, признаки продуктивно-пролиферативного виллузита. Обычно анализ выявляет типичные клетки типа «совиный глаз».
- Молекулярно-биологические методы. Информативно проведение ПЦР-диагностики для обнаружения генетического материала вируса в биологическом материале (слюне, моче, спинномозговой жидкости). Метод дает врачу возможность следить за уровнем вирусной нагрузки, чтобы корректировать противовирусное лечение и оценивать его эффективность.
- Серологические реакции. ИФА требуется для выявляется IgM и низкоавидных IgG, что характерно для острой фазы инфекционного процесса. По мере выздоровления и формирования иммунитета в крови появляются иммуноглобулины G с высокой авидностью. С помощью РИФ выявляют антигены в клеточных культурах или клетках периферической крови.

Инструментальные методы подбираются соответственно форме заболевания. Для оценки структурно-функциональных особенностей печени и билиарного тракта назначают УЗИ органов брюшной полости. КТ и МРТ головного мозга информативны для выявления врожденных пороков и кальцификатов. Рентгенография ОГК необходима при симптомах дыхательных расстройств. По показаниям ребенка направляют на консультации к профильным специалистам— кардиологу, неврологу, отоларингологу.
Лечение цитомегаловирусной инфекции у детей
Препаратом выбора у новорожденных и детей первого года жизни является специфический антицитомегаловирусный иммуноглобулин, который имеет повышенную концентрацию IgG. Лечение начинают при манифестных формах заболевания и проводят по схеме: вначале вводится высокая доза препарата, а спустя 9-10 дней дозировку постепенно уменьшают, контролируя степень ответа на терапию и активность процесса.
В старшем возрасте перечень препаратов, применяемых при цитомегаловирусной инфекции, значительно расширяется. Лечение включает противовирусные средства из группы нуклеозидов и нуклеотидов (ганцикловир, валганцикловир), производные ортофосфорной кислоты (фоскарнет). При легкой и среднетяжелой формах назначают интерфероны, иммуностимуляторы.
Лечение включает противовирусные средства из группы нуклеозидов и нуклеотидов (ганцикловир, валганцикловир), производные ортофосфорной кислоты (фоскарнет). При легкой и среднетяжелой формах назначают интерфероны, иммуностимуляторы.
Для купирования интоксикации показано обильное питье (при легких формах), при среднетяжелых и тяжелых клинических вариантах рекомендована инфузионная терапия. Патогенетическая терапия подбирается в соответствии с характером течения болезни и может включать пищеварительные ферменты, ингибиторы протеиназ, гемостатики. Для предупреждения вторичных бактериальных осложнений используют антибиотики (макролиды, цефалоспорины, гликопептиды).
Прогноз и профилактика
При малосимптомных приобретенных вариантах цитомегаловирусная болезнь протекает без осложнений, зачастую у ребенка выявляется только латентное носительство. Угрозу для жизни и здоровья представляют тяжелые генерализованные инфекции, которые в 50-60% случаев сопровождаются осложнениями, несмотря на проводимое лечение. Особо опасно поражение цитомегаловирусом для детей с иммунодефицитными состояниями.
Особо опасно поражение цитомегаловирусом для детей с иммунодефицитными состояниями.
Основу профилактики врожденной ЦМВИ составляет обязательное лабораторное обследование женщин на носительство цитомегаловируса, которое проводится при планировании зачатия и во время беременности. Если в семье есть пациент с цитомегаловирусной инфекцией, необходимо ограничить его общение с ребенком и обеспечить лечение. Карантинно-изоляционные мероприятия в отношении заболевших и контактных лиц не производятся.
Вы можете поделиться своей историей болезни, что Вам помогло при лечении цитомегаловирусной инфекции у детей.
Источники
- Цитомегаловирусная инфекция у детей/ С.С. Кочкина, Е.П. Ситникова// Детские инфекции. — 2016.
- Клинические рекомендации (протокол лечения) оказания медицинской помощи детям больным цитомегаловирусной инфекцией. — 2015.
- Цитомегаловирусная инфекция у детей. Клинический протокол МЗ РК. — 2013.
- Детские инфекционные болезни/ Л.
 Г. Кузьменко, Д.Ю. Овсянников, Н.М. Киселева. — 2009.
Г. Кузьменко, Д.Ю. Овсянников, Н.М. Киселева. — 2009. - Настоящая статья подготовлена по материалам сайта: https://www.krasotaimedicina.ru/
ВАЖНО
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Цитомегаловирусная инфекция | Центр Дикуля
Цитомегаловирус является очень распространенным вирусом. К 40 годам у половины людей вирус присутствует в организме. ЦМВ легко также, как и вирус герпеса, передается через слюну инфицированного человека или другие биологические жидкости.
Если у человека крепкая иммунная система, которая может легко контролировать вирус, то никаких проблем со здоровьем не будет. Но при ослаблении иммунной системы у человека появляются различные патологические состояния.
У людей с развернутой формой ВИЧ ЦМВ может привести к глазной инфекции (ретиниту), которая может привести к слепоте. ЦМВ-ретинит — это характерная для СПИД оппортунистическая инфекция. Вирус может также приводить к проблемам в кишечнике пищеводе, легких, мозге и нервах.
Существуют несколько типов цитомегаловирусной инфекции.
- Врожденный – ребенок заражается от матери внутриутробно.
- Начальный – первичное заражение ЦМВ. Как правило, первичный контакт не приводит к появлению симптомов, но у некоторых людей могут симптомы, похожие на мононуклеоз.
- Реактивация- вирус, который находится в состоянии покоя, активируется на фоне ослабления иммунной системы. Активация вируса может возникнуть при запущенном ВИЧ или человек проходит курс лечения от рака или же принимает цитостатики после трансплантации.
Симптомы цитомегаловируса
Общие симптомы первичного ЦМВ.
Большинство здоровых людей, которые заражаются ЦМВ, не знают об этом.
 Если у человека есть симптомы первичного инфицирования ЦМВ, они легкие и включают:
Если у человека есть симптомы первичного инфицирования ЦМВ, они легкие и включают:- Усталость
- Опухшие лимфоузлы
- Жар
- Боли в горле
- Мышечные боли
Менее распространенные симптомы первичной инфекции ЦМВ.
В редких случаях ЦМВ также может вызывать:
- Изменения настроения
- Головные боли
- Проблемы с концентрацией внимания
- Одышка
- Сухой кашель
Симптомы врожденного ЦМВ.
У детей, рожденных с ЦМВ, могут быть:
- Недоношенность
- Маленький размер или низкий вес при рождении
- Петехиальная сыпь
- Желтушность кожи или склер глаз
- Гепатомегалия и спленомегалия
- Микроцефалия
- Судорожная готовность
- Глухота
- Воспаление легких (пневмония)
- Повреждение печени (гепатит)
Симптомы ЦМВ при ВИЧ.

Если у человека развернутая стадия ВИЧ, ЦМВ может поражать различные части тела. Могут быть следующие симптомы:
- Скотомы или движущиеся черные точки (мушки) перед глазами
- Нечеткость зрения
- Амавроз
- Диарея
- Боли в животе
- Нарушения глотания из-за наличия язв во рту или пищеводе.
- Оглушенное сознание
- Боли в поясничной области
- Снижение веса
- Утомленность
- Слабость в ногах
Если у человека ВИЧ, то вероятность активации ЦМВ возрастает, если количество лейкоцитов CD4 ниже 100.
Причины и пути передачи цитомегаловируса
Вероятность заражения ЦМВ от случайного контакта очень низкая. Но человек может заразиться при касании к глазам, носу или рту после контакта с зараженным человеком. Вирус может передаваться через:
- Слюну
- Сперму
- Вагинальные выделения
- Кровь
- Мочу
- Грудное молоко
Человек также может заразиться цитомегаловирусом:
- После сексуального контакта
- При переливании крови
- После пересадки органов
ЦМВ легко распространяется в местах с большим количеством маленьких детей, таких как детские сады, поэтому любой, кто там находится с ними вместе, подвержен высокому риску заражения. Человек также с большей вероятностью заразитесь вирусом, если его иммунная система ослаблена из-за приема лекарств или другого заболевания.
Человек также с большей вероятностью заразитесь вирусом, если его иммунная система ослаблена из-за приема лекарств или другого заболевания.
Диагностика
Врач может назначить такие анализы, как:
- Анализы крови и мочи. К ним относятся анализ крови на антиген ЦМВ, вирусная культура или ПЦР (молекулярный тест). Серологические тесты позволяют определить признаки реакции иммунной системы на инфекцию, такие как уровни антител IgM и IgG.
- Биопсия. При наличии клинических показаний может быть взят образец ткани из кишечника, пищевода или легкого и проведено его гистологическое исследование.
- Глазные тесты для выявления воспалений сетчатки.
- Визуализирующие исследования, такие как компьютерная томография, для выявления изменений в легком или головном мозге.
Лечение
Если у пациента ретинит из-за ЦМВ, врач может назначить сильнодействующие лекарства внутривенно в течение нескольких недель, этот метод называется индукционной терапией. Через некоторое время пациента могут перевести на прием таблеток.
Через некоторое время пациента могут перевести на прием таблеток.
При опасности развития слепоты лекарство могут вводить в глаз.
Врач может назначить следующие лекарства:
- Цидофовир (Вистид)
- Фоскарнет (Фоскавир)
- Ганцикловир (Цитовен)
- Марибавир (Ливтенсити)
- Валганцикловир (Вальцит)
Эти препараты, как правило, не могут уничтожить вирус, особенно если у пациента запущенный ВИЧ, но они могут контролировать инфекцию, пока он получает антиретровирусную терапию (АРТ) от ВИЧ-инфекции.
В зависимости от препарата у пациента могут быть побочные эффекты, в том числе:
- Низкий уровень лейкоцитов (нейтропения), который повышает риск других инфекций.
- Чувство усталости из-за низкого количества эритроцитов (анемия)
- Расстройство желудка или рвота
- Сыпь
- Нарушение функции почек
Цитомегаловирусные осложнения
Осложнения при ЦМВ возникают редко.
 Но могут быть следующие осложнения, в том числе:
Но могут быть следующие осложнения, в том числе:- Мононуклеоз
- Синдром Гийена-Барре
- Воспаление головного мозга (энцефалит)
- Воспаление сердца (миокардит)
У людей с ВИЧ осложнения включают:
- Ретинит
- Пневмония
- Кожная сыпь и поражения кожи
- Проблемы с нервами, пищеводом, легкими, толстой кишкой или слизистыми оболочками
- Отек мозга
Осложнения у детей, рожденных с ЦМВ, включают:
- Проблемы с обучением
- Церебральный паралич или проблемы с мышечным тонусом и координацией
- Судороги
Прогноз
Лекарства от ЦМВ нет. Вирус остается неактивным в организме и может вызвать проблемы со здоровьем через какое-то время. Эта реактивация вируса, чаще всего, встречается у людей, перенесших трансплантацию стволовых клеток и органов.
Прогноз зависит от общего состояния здоровья конкретного человека. У людей с сильной иммунной системой симптомы ЦМВ почти всегда проходят сами по себе.
У людей с сильной иммунной системой симптомы ЦМВ почти всегда проходят сами по себе.
Врожденный ЦМВ может иметь пожизненные последствия. Риски наиболее высоки, когда мать впервые заражается ЦМВ во время беременности.
Если у человека ослаблена иммунная система, ему может потребоваться лечение на всю оставшуюся жизнь, что позволит предотвратить осложнения.
Профилактика
Тщательная гигиена – лучшая профилактика ЦМВ. Можно принять следующие меры предосторожности:
- Часто мыть руки мылом в течение 15-20 секунд, особенно если есть контакт с маленькими детьми или их подгузниками, слюной или другими выделениями. Это особенно важно, если дети посещают детский сад.
- Избегать контакта со слезами и слюной ребенка. Это особенно важно для беременных.
- Не делиться едой или питьем из одного стакана с другими. Использование общих стаканов и кухонной утвари может привести к распространению ЦМВ.
- Необходима осторожность с одноразовыми предметами.
 При утилизации подгузников, салфеток и других предметов, загрязненных физиологическими жидкостями, необходимо тщательно мыть руки, прежде чем прикасаться к лицу.
При утилизации подгузников, салфеток и других предметов, загрязненных физиологическими жидкостями, необходимо тщательно мыть руки, прежде чем прикасаться к лицу. - Очищать любые поверхности, которые соприкасаются с детской мочой или слюной.
- Практиковать безопасный секс. Надевать презерватив во время каждого полового контакта, что позволит предотвратить распространение ЦМВ через сперму и вагинальные выделения.
Если у человека ослабленный иммунитет, ему может помочь прием противовирусных препаратов для предотвращения ЦМВ-инфекции.
Экспериментальные вакцины против ЦМВ уже испытываются на женщинах детородного возраста. Эти вакцины могут быть полезны для предотвращения ЦМВ-инфекции у матерей и младенцев, а также для снижения вероятности развития инвалидности у детей, рожденных женщинами, инфицированными во время беременности.
Цитомегаловирусные инфекции у детей с первичным и вторичным иммунодефицитом
1. Демарчи Дж.М., Бланкеншип М. Л., Браун Г.Д., Каплан А.С. Размер и сложность ДНК цитомегаловируса человека. Вирусология. 1978; 89: 643–646. doi: 10.1016/0042-6822(78)-X. [PubMed] [CrossRef] [Google Scholar]
Л., Браун Г.Д., Каплан А.С. Размер и сложность ДНК цитомегаловируса человека. Вирусология. 1978; 89: 643–646. doi: 10.1016/0042-6822(78)-X. [PubMed] [CrossRef] [Google Scholar]
2. Бове Д., Драмез Э., Блез Д., де Латур Р.П., Форкаде Э., Себаллос П., Юйтебрук А., Лабюссьер Х., Нгуен С., Бурхис Дж.-Х. и др. Система оценки клинически значимой ЦМВ-инфекции у серопозитивных реципиентов после аллогенной трансплантации гемопоэтических клеток: исследование SFGM-TC. Пересадка костного мозга. 2021;56:1305–1315. дои: 10.1038/s41409-020-01178-6. [PubMed] [CrossRef] [Google Scholar]
3. Дэвисон А.Дж., Долан А., Актер П., Аддисон С., Дарган Д.Дж., Альсендор Д.Дж., МакГеоч Д.Дж., Хейворд Г.С. Новый взгляд на геном цитомегаловируса человека: сравнение с шимпанзе геном цитомегаловируса FN1. Дж. Генерал Вирол. 2003; 84: 17–28. doi: 10.1099/vir.0.18606-0. [PubMed] [CrossRef] [Google Scholar]
4. McGeoch D.J., Rixon F.J., Davison A.J. Вопросы геномики и эволюции герпесвирусов. Вирус рез. 2006; 117: 90–104. doi: 10.1016/j.virusres.2006.01.002. [PubMed] [CrossRef] [Академия Google]
2006; 117: 90–104. doi: 10.1016/j.virusres.2006.01.002. [PubMed] [CrossRef] [Академия Google]
5. Stern L., Withers B., Avdic S., Gottlieb D., Abendroth A., Blyth E., Slobedman B. Латентность и реактивация цитомегаловируса человека у реципиентов аллогенной трансплантации гемопоэтических стволовых клеток. Фронт. микробиол. 2019;10:1186. doi: 10.3389/fmicb.2019.01186. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
6. Ривз М., МакЭри П.А., Ленер П.Дж., Сиссонс Дж.Г.П., Синклер Дж.Х. Латентность, ремоделирование хроматина и реактивация цитомегаловируса человека в дендритных клетках здоровых носителей. проц. Натл. акад. науч. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 2005; 102:4140–4145. doi: 10.1073/pnas.0408994102. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
7. Хайбуллина С.Ф., Мацеевский Дж.П., Крапнелл К., Спаллоне П.А., Сток А.Д., Пари Г.С., Занджани Э.Д., Джеор С.С. предшественников и передается миелоидному потомству в латентной форме. бр. Дж. Гематол. 2004; 126:410–417. doi: 10.1111/j.1365-2141.2004.05056.x. [PubMed] [CrossRef] [Google Scholar]
2004; 126:410–417. doi: 10.1111/j.1365-2141.2004.05056.x. [PubMed] [CrossRef] [Google Scholar]
8. Шнайдер М., Нахшон А., Кришна Б., Пул Э., Бошков А., Биньямин А., Маза И., Синклер Дж., Шварц М., Стерн-Гиноссар Н. Определение транскрипционного ландшафта во время латентности цитомегаловируса с помощью секвенирования одноклеточной РНК. мБио. 2018;9doi: 10.1128/mBio.00013-18. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
9. Лучин П., Махмутефендич Х., Загорац Г.Б., Томаш М.И. Уклонение цитомегаловируса от иммунитета за счет нарушения эндосомального транспорта. Клетка. Мол. Иммунол. 2014;12:154–169. doi: 10.1038/cmi.2014.85. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
10. Синклер Дж., Сиссонс П. Латентность и реактивация цитомегаловируса человека. Дж. Генерал Вирол. 2006; 87: 1763–1779. doi: 10.1099/vir.0.81891-0. [PubMed] [CrossRef] [Академия Google]
11. Ченг С., Кавинесс К., Бюлер Дж., Смити М., Николич-Жугич Дж., Гудрум Ф. Транскриптомная характеристика цитомегаловируса человека при естественной инфекции и экспериментальной латентности. проц. Натл. акад. науч. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 2017; 114:E10586–E10595. doi: 10.1073/pnas.1710522114. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Транскриптомная характеристика цитомегаловируса человека при естественной инфекции и экспериментальной латентности. проц. Натл. акад. науч. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 2017; 114:E10586–E10595. doi: 10.1073/pnas.1710522114. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
12. Берри Р., Уотсон Г.М., Йонджик С., Дегли-Эспости М.А., Россджон Дж. Модуляция врожденного и адаптивного иммунитета цитомегаловирусами. Нац. Преподобный Иммунол. 2019;20:113–127. doi: 10.1038/s41577-019-0225-5. [PubMed] [CrossRef] [Google Scholar]
13. Martins J.P., Andoniou C.E., Fleming P., Kuns R.D., Schuster I.S., Voigt V., Daly S., Varelias A., Tey S.-K., Degli -Эспости М.А. и др. Терапия штамм-специфическими антителами предотвращает реактивацию цитомегаловируса после трансплантации. Наука. 2019; 363: 288–293. doi: 10.1126/science.aat0066. [PubMed] [CrossRef] [Google Scholar]
14. Гриффитс П., Бараниак И., Ривз М. Патогенез цитомегаловируса человека. Дж. Патол. 2015; 235: 288–297. doi: 10.1002/путь.4437. [PubMed] [CrossRef] [Google Scholar]
doi: 10.1002/путь.4437. [PubMed] [CrossRef] [Google Scholar]
15. Киркпатрик П., Риминтон С. Первичные иммунодефицитные заболевания в Австралии и Новой Зеландии. Дж. Клин. Иммунол. 2007; 27: 517–524. doi: 10.1007/s10875-007-9105-z. [PubMed] [CrossRef] [Google Scholar]
16. Gunkel J., Wolfs T.F., De Vries L.S., Nijman J. Предикторы тяжести постнатальной цитомегаловирусной инфекции у недоношенных детей и их значение для лечения. Эксперт Преподобный Анти-Инфект. тер. 2014;12:1345–1355. дои: 10.1586/14787210.2014.966080. [PubMed] [CrossRef] [Google Scholar]
17. Hamprecht K., Maschmann J., Vochem M., Dietz K., Speer C.P., Jahn G. Эпидемиология передачи цитомегаловируса от матери недоношенному ребенку при грудном вскармливании. . Ланцет. 2001; 357: 513–518. doi: 10.1016/S0140-6736(00)04043-5. [PubMed] [CrossRef] [Google Scholar]
18. Биалас К.М., Вестрейх Д., Де Ла Роса Э.К., Нельсон К., Каувар Л.М., Фу Т.-М., Пермар С.Р. Реакции материнских антител и непервичная врожденная цитомегаловирусная инфекция младенцев, подвергшихся воздействию ВИЧ-1. Дж. Заразить. Дис. 2016;214:1916–1923. doi: 10.1093/infdis/jiw487. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Дж. Заразить. Дис. 2016;214:1916–1923. doi: 10.1093/infdis/jiw487. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
19. Ruffner M.A., Sullivan K.E., Henrickson S.E. Рецидивирующие и устойчивые вирусные инфекции при первичных иммунодефицитах. Фронт. Иммунол. 2017;8:665. doi: 10.3389/fimmu.2017.00665. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
20. Джозефсон К.Д., Калиендо А.М., Исли К.А., Кнежевич А., Шенви Н., Хинкс М.Т., Патель Р.М., Хиллиер К.Д., Робак Дж.Д. Передача цитомегаловируса через грудное молоко у младенцев с очень низкой массой тела при рождении: проспективное когортное исследование. JAMA Педиатр. 2014; 168:1054–1062. doi: 10.1001/jamapediatrics.2014.1360. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
21. Schleiss M.R. Цитомегаловирус у новорожденных: иммунные корреляты инфекции и защиты. клин. Дев. Иммунол. 2013;2013:1–14. дои: 10.1155/2013/501801. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
22. Yee A., De Ravin S.S., Elliott E., Ziegler J.B., сотрудники Австралийского отделения педиатрического надзора. Тяжелый комбинированный иммунодефицит: национальное эпиднадзорное исследование. Педиатр. Аллергия Иммунол. 2008; 19: 298–302. doi: 10.1111/j.1399-3038.2007.00646.x. [PubMed] [CrossRef] [Академия Google]
Yee A., De Ravin S.S., Elliott E., Ziegler J.B., сотрудники Австралийского отделения педиатрического надзора. Тяжелый комбинированный иммунодефицит: национальное эпиднадзорное исследование. Педиатр. Аллергия Иммунол. 2008; 19: 298–302. doi: 10.1111/j.1399-3038.2007.00646.x. [PubMed] [CrossRef] [Академия Google]
23. Van der Spek J., Groenwold R.H., van der Burg M., van Montfrans J.M. Скрининг новорожденных на тяжелый комбинированный иммунодефицит на основе Trec: систематический обзор. Дж. Клин. Иммунол. 2015; 35: 416–430. doi: 10.1007/s10875-015-0152-6. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
24. Пай С.-Ю., Логан Б.Р., Гриффит Л.М., Бакли Р.Х., Парротт Р.Э., Дворак С., Капур Н., Хэнсон И.С., Филипович AH, Jyonouchi S. и соавт. Результаты трансплантации при тяжелом комбинированном иммунодефиците, 2000–2009 гг.. Н. англ. Дж. Мед. 2014; 371:434–446. doi: 10.1056/NEJMoa1401177. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
25. Strand J., Gul K. A., Erichsen H.C., Lundman E., Berge M.C., Trømborg A.K., Sørgjerd L.K., Ytre-Arne M., Hogner S. ., Halsne R., et al. Секвенирование второго уровня нового поколения, интегрированное в общенациональный скрининг новорожденных, обеспечивает быструю молекулярную диагностику тяжелого комбинированного иммунодефицита. Фронт. Иммунол. 2020;11:1417. doi: 10.3389/fimmu.2020.01417. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
A., Erichsen H.C., Lundman E., Berge M.C., Trømborg A.K., Sørgjerd L.K., Ytre-Arne M., Hogner S. ., Halsne R., et al. Секвенирование второго уровня нового поколения, интегрированное в общенациональный скрининг новорожденных, обеспечивает быструю молекулярную диагностику тяжелого комбинированного иммунодефицита. Фронт. Иммунол. 2020;11:1417. doi: 10.3389/fimmu.2020.01417. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
26. Танье С.Г., Аль-Герц В., Бусфиха А., Чатила Т., Каннингем-Рандлс С., Эциони А., Франко Дж.Л., Холланд С.М., Кляйн С., Морио Т. и др. Врожденные нарушения иммунитета человека: обновление классификации 2019 г. от Экспертного комитета Международного союза иммунологических обществ. Дж. Клин. Иммунол. 2020;40:24–64. doi: 10.1007/s10875-019-00737-x. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
27. Wagstaff A.J., Bryson H.M. Фоскарнет. Переоценка его противовирусной активности, фармакокинетических свойств и терапевтического использования у пациентов с ослабленным иммунитетом с вирусными инфекциями. Наркотики. 1994;48:199–226. doi: 10.2165/00003495-199448020-00007. [PubMed] [CrossRef] [Google Scholar]
Наркотики. 1994;48:199–226. doi: 10.2165/00003495-199448020-00007. [PubMed] [CrossRef] [Google Scholar]
28. Лемберг К., Мошоус Д., Бут С. Трансплантация гемопоэтических стволовых клеток при первичном гемофагоцитарном лимфогистиоцитозе. Фронт. Педиатр. 2019;7:435. doi: 10.3389/fped.2019.00435. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
29. Gugliesi F., Pasquero S., Griffante G., Scutera S., Albano C., Pacheco S., Riva G., Dell’Oste В., Биолатти М. Цитомегаловирус человека и аутоиммунные заболевания: где мы? Вирусы. 2021;13:260. дои: 10.3390/v13020260. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
30. Kahan S.M., Wherry E.J., Zajac A.J. Истощение Т-клеток при персистирующих вирусных инфекциях. Вирусология. 2015; 479–480:180–193. doi: 10.1016/j.virol.2014.12.033. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
31. Друтман С.Б., Мансури Д., Махдавиани С.А., Нихус А.-Л., Хум Д., Брык Р., Эрнандес Н., Белкая С. ., Рапапорт Ф.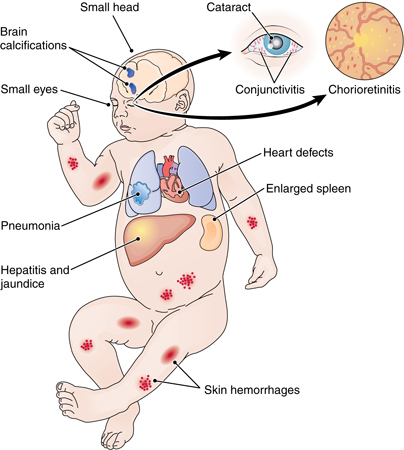 , Бигио Б. и др. Фатальная цитомегаловирусная инфекция у взрослого с наследственным дефицитом NOS2. Н. англ. Дж. Мед. 2020; 382: 437–445. дои: 10.1056/NEJMoa1910640. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
, Бигио Б. и др. Фатальная цитомегаловирусная инфекция у взрослого с наследственным дефицитом NOS2. Н. англ. Дж. Мед. 2020; 382: 437–445. дои: 10.1056/NEJMoa1910640. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
32. Hunger S.P., Mullighan C.G. Острый лимфобластный лейкоз у детей. Н. англ. Дж. Мед. 2015; 373:1541–1552. doi: 10.1056/NEJMra1400972. [PubMed] [CrossRef] [Google Scholar]
33. Pui C.-H., Yang J.J., Hunger S.P., Pieters R., Schrappe M., Biondi A., Vora A., Baruchel A., Silverman L.B., Шмигелов К. и др. Детский острый лимфобластный лейкоз: прогресс благодаря сотрудничеству. Дж. Клин. Онкол. 2015; 33: 2938–2948. doi: 10.1200/JCO.2014.59.1636. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
34. Рефф М.Е., Карнер К., Чемберс К.С., Чинн П.С., Леонард Дж.Э., Рааб Р., Ньюман А.Р., Ханна Н., Андерсон Д.Р. Истощение В-клеток in vivo химерным мышиным человеческим моноклональным антителом к CD20. Кровь. 1994; 83: 435–445. doi: 10.1182/кровь. V83.2.435.435. [PubMed] [CrossRef] [Google Scholar]
V83.2.435.435. [PubMed] [CrossRef] [Google Scholar]
35. Купер Т.М. Роль неларабина в лечении Т-клеточного острого лимфобластного лейкоза и Т-клеточной лимфобластной лимфомы. тер. клин. Управление рисками 2007;3:1135–1141. [Бесплатная статья PMC] [PubMed] [Google Scholar]
36. Шиллинг П.Дж., Вадхан-Радж С. Сопутствующая цитомегаловирусная и пневмоцистная пневмония после терапии флударабином при хроническом лимфоцитарном лейкозе. Н. англ. Дж. Мед. 1990;323:833–834. doi: 10.1056/nejm19
03231216. [PubMed] [CrossRef] [Google Scholar]
37. Bechman N., Maher J. Стратегии лимфодеплеции для усиления адоптивной Т-клеточной иммунотерапии — что мы делаем; куда мы идем? Мнение эксперта. биол. тер. 2021; 21: 627–637. doi: 10.1080/14712598.2021.1857361. [PubMed] [CrossRef] [Академия Google]
38. Минар-Колин В., Ауперин А., Пиллон М., Берк Г.А.А., Баркаускас Д.А., Уитли К., Дельгадо Р.Ф., Александр С., Юйтебрук А., Боллард С.М., и соавт. Ритуксимаб для лечения зрелой В-клеточной неходжкинской лимфомы высокого риска у детей. Н. англ. Дж. Мед. 2020;382:2207–2219. doi: 10.1056/NEJMoa1915315. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
Н. англ. Дж. Мед. 2020;382:2207–2219. doi: 10.1056/NEJMoa1915315. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
39. Held G., Pöschel V., Pfreundschuh M. Ритуксимаб для лечения диффузных крупноклеточных B-клеточных лимфом. Эксперт преподобный Anticancer Ther. 2006; 6: 1175–1186. дои: 10.1586/14737140.6.8.1175. [PubMed] [CrossRef] [Академия Google]
40. Келесидис Т., Дайкос Г., Бумпас Д., Циодрас С. Увеличивает ли ритуксимаб частоту инфекционных осложнений? Повествовательный обзор. Междунар. Дж. Заразить. Дис. 2011;15:e2–e16. doi: 10.1016/j.ijid.2010.03.025. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
41. Хилал Т. Фатальная цитомегаловирусная болезнь после комбинированной терапии кортикостероидами и ритуксимабом при гранулематозе с полиангиитом. Представитель дела Ревматол. 2015;2015:538137. doi: 10.1155/2015/538137. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
42. Аппельбаум Ф.Р., Бернштейн И.Д. Гемтузумаб озогамицин при остром миелоидном лейкозе. Кровь. 2017;130:2373–2376. doi: 10.1182/blood-2017-09-797712. [PubMed] [CrossRef] [Google Scholar]
Кровь. 2017;130:2373–2376. doi: 10.1182/blood-2017-09-797712. [PubMed] [CrossRef] [Google Scholar]
43. Hamann P.R., Hinman L.M., Hollander I., Beyer C.F., Lindh D., Holcomb R., Hallett W., Tsou H.-R., Upeslacis J., Шочат Д. и др. Гемтузумаб озогамицин, мощный и селективный конъюгат анти-CD33-антитело-калихеамицин для лечения острого миелоидного лейкоза. Биоконъюгат хим. 2002; 13:47–58. doi: 10.1021/bc010021y. [PubMed] [CrossRef] [Академия Google]
44. Fultang L., Panetti S., Ng M., Collins P., Graef S., Rizkalla N., Booth S., Lenton R., Noyvert B., Shannon-Lowe C., et al. Нацеливание на MDSC с помощью гемтузумаба озогамицина восстанавливает Т-клеточный иммунитет и иммунотерапию против рака. ЭБиоМедицина. 2019;47:235–246. doi: 10.1016/j.ebiom.2019.08.025. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
45. Zhang J., Jain A., Milhas S., Williamson D.J., Mysliwy J., Lodge A., Thirlway J., Al Nakeeb M. , Миллер А., Рэббитс Т.Х. Конъюгат антитело-лекарственное средство со свойствами внутриклеточного высвобождения лекарственного средства, демонстрирующий специфическую цитотоксичность в отношении CD7-позитивных клеток. Лейк. Рез. 2021;108:106626. doi: 10.1016/j.leukres.2021.106626. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Лейк. Рез. 2021;108:106626. doi: 10.1016/j.leukres.2021.106626. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
46. Hill J., Li D., Hay K., Green M.L., Cherian S., Chen X., Riddell S.R., Maloney D.G., Boeckh M., Turtle C.J. Инфекционные осложнения CD19-направленного химерного антигенного рецептора, модифицированного Т-клеточная иммунотерапия. Кровь. 2018; 131:121–130. doi: 10.1182/blood-2017-07-793760. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
47. Rastogi S., Ricci A., Jin Z., Bhatia M., George D., Garvin J.H., Hall M., Satwani P. Clinical и экономические последствия цитомегаловирусной инфекции среди детей, перенесших аллогенную трансплантацию гемопоэтических клеток. биол. Трансплантация костного мозга. 2019;25:1253–1259. doi: 10.1016/j.bbmt.2018.11.028. [PubMed] [CrossRef] [Google Scholar]
48. Boeckh M., Ljungman P. Как мы лечим цитомегаловирус у реципиентов трансплантата гемопоэтических клеток. Кровь. 2009;113:5711–5719. doi: 10. 1182/blood-2008-10-143560. [Статья PMC бесплатно] [PubMed] [CrossRef] [Google Scholar]
1182/blood-2008-10-143560. [Статья PMC бесплатно] [PubMed] [CrossRef] [Google Scholar]
49. Teira P., Battiwalla M., Ramanathan M., Barrett A.J., Ahn K.W., Chen M., Green J.S., Saad A., Antin J.H. , Савани Б.Н. и соавт. Ранняя реактивация цитомегаловируса по-прежнему связана с повышенной смертностью, связанной с трансплантацией, в нынешнюю эпоху: анализ CIBMTR. Кровь. 2016;127:2427–2438. doi: 10.1182/blod-2015-11-679639. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
50. Hiwarkar P., Gaspar H.B., Gilmour K.C., Jagani M., Chiesa R., Bennett-Rees N., Breuer J., Rao К., Кейл К., Гулден Н. и др. Влияние вирусной реактивации в эпоху превентивной противовирусной лекарственной терапии после аллогенной гемопоэтической ТСК у детей-реципиентов. Пересадка костного мозга. 2012; 48:803–808. doi: 10.1038/bmt.2012.221. [PubMed] [CrossRef] [Google Scholar]
51. Аль Язиди Л.С., Митчелл Р., Паласантиран П., О’Брайен Т.А., Макмаллан Б. Ведение и профилактика цитомегаловирусной инфекции у детей, перенесших трансплантацию гемопоэтических стволовых клеток (ТГСК). : Двунациональный опрос. Педиатр. Пересадка. 2019;23:e13458. doi: 10.1111/petr.13458. [PubMed] [CrossRef] [Google Scholar]
: Двунациональный опрос. Педиатр. Пересадка. 2019;23:e13458. doi: 10.1111/petr.13458. [PubMed] [CrossRef] [Google Scholar]
52. Marty F., Ljungman P., Chemaly R.F., Maertens J., Dadwal S.S., Duarte R.F., Haider S., Ullmann A.J., Katayama Y., Brown J., и другие. Летермовир для профилактики цитомегаловируса при трансплантации гемопоэтических клеток. Н. англ. Дж. Мед. 2017; 377: 2433–2444. doi: 10.1056/NEJMoa1706640. [PubMed] [CrossRef] [Google Scholar]
53. Миллер В., Флинн П., Маккалоу Дж., Бальфур Х.Х., Голдман А., Хааке Р., Макглэйв П., Рамзи Н., Керси Дж. Цитомегаловирусная инфекция после трансплантации костного мозга: связь с острой болезнью «трансплантат против хозяина». Кровь. 1986;67:1162–1167. doi: 10.1182/кровь.V67.4.1162.1162. [PubMed] [CrossRef] [Google Scholar]
54. Travi G., Pergam S.A., Xie H., Boeckh MJ Серостатус донора CMV не является предиктором рецидива при D-/R-детской HCT. биол. Трансплантация костного мозга. 2009; 15: 758–760. doi: 10.1016/j. bbmt.2009.03.025. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
bbmt.2009.03.025. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
55. Люнгман П., Бранд Р., Хук Дж., де ла Камара Р., Кордонье К., Эйнселе Х., Стычински Дж., Уорд К.Н., Чезаро С. Цитомегаловирусный статус донора влияет на исход аллогенной трансплантации стволовых клеток: исследование Европейской группы трансплантации крови и костного мозга. клин. Заразить. Дис. 2014;59: 473–481. doi: 10.1093/cid/ciu364. [PubMed] [CrossRef] [Google Scholar]
56. Lischka P., Zimmermann H. Противовирусные стратегии борьбы с цитомегаловирусными инфекциями у реципиентов трансплантатов. Курс. мнение Фармакол. 2008; 8: 541–548. doi: 10.1016/j.coph.2008.07.002. [PubMed] [CrossRef] [Google Scholar]
57. Лурейн Н.С., Чоу С. Устойчивость цитомегаловируса человека к противовирусным препаратам. клин. микробиол. 2010; 23:689–712. doi: 10.1128/CMR.00009-10. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
58. Чжоу С., Мароусек Г.И., Ван Вечел Л.С., Ли С., Вайнберг А. Фенотипы роста и лекарственной устойчивости, возникающие в результате мутаций области III ДНК-полимеразы цитомегаловируса, наблюдаемые в клинических образцах. Антимикроб. Агенты Чемотер. 2007; 51:4160–4162. doi: 10.1128/AAC.00736-07. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Фенотипы роста и лекарственной устойчивости, возникающие в результате мутаций области III ДНК-полимеразы цитомегаловируса, наблюдаемые в клинических образцах. Антимикроб. Агенты Чемотер. 2007; 51:4160–4162. doi: 10.1128/AAC.00736-07. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
59. Lea A.P., Bryson H.M. цидофовир. Наркотики. 1996;52:225–230; обсуждение 31. doi: 10.2165/00003495-199652020-00006. [PubMed] [CrossRef] [Академия Google]
60. Марти Ф.М., Уинстон Д.Дж., Роули С.Д., Вэнс Э., Папаниколау Г., Маллейн К.М., Брандейдж Т.М., Робертсон А.Т., Годкин С., Моммеха-Марин Х. и др. CMX001 для предотвращения цитомегаловирусной болезни при трансплантации гемопоэтических клеток. Н. англ. Дж. Мед. 2013; 369:1227–1236. doi: 10.1056/NEJMoa1303688. [PubMed] [CrossRef] [Google Scholar]
61. Marty F.M., Winston D.J., Chemaly R.F., Mullane K.M., Shore T.B., Papanicolaou G.A., Chittick G., Brundage TM, Wilson C., Morrison M.E., et al. Рандомизированное двойное слепое плацебо-контролируемое исследование фазы 3 перорального применения бринцидофовира для профилактики цитомегаловируса при аллогенной трансплантации гемопоэтических клеток. биол. Трансплантация костного мозга. 2019;25:369–381. doi: 10.1016/j.bbmt.2018.09.038. [Статья PMC бесплатно] [PubMed] [CrossRef] [Google Scholar]
биол. Трансплантация костного мозга. 2019;25:369–381. doi: 10.1016/j.bbmt.2018.09.038. [Статья PMC бесплатно] [PubMed] [CrossRef] [Google Scholar]
62. Ligat G., Cazal R., Hantz S., Alain S. Терминазный комплекс цитомегаловируса человека как противовирусная мишень: крупный план. ФЭМС микробиол. 2018; 42:137–145. doi: 10.1093/femsre/fuy004. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
63. Chemaly R.F., Ullmann A.J., Stoelben S., Richard M.P., Bornhäuser M., Groth C., Einsele H., Silverman M., Mullane K.M. , Браун Дж. и др. Летермовир для профилактики цитомегаловируса при трансплантации гемопоэтических клеток. Н. англ. Дж. Мед. 2014; 370:1781–1789. doi: 10.1056/NEJMoa1309533. [PubMed] [CrossRef] [Google Scholar]
64. Лин А., Флинн Дж., ДеРеспирис Л., Фиггинс Б., Гриффин М., Лау К., Проли А., Девлин С.М., Чо С., Тамари Р. и др. Летермовир для предотвращения реактивации цитомегаловируса при трансплантации гаплоидентичных и несовместимых аллогенных гемопоэтических клеток взрослого донора с посттрансплантационным циклофосфамидом для профилактики реакции «трансплантат против хозяина». Пересадка. Клетка. тер. 2021;27:85.e1–85.e6. doi: 10.1016/j.bbmt.2020.10.009. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Пересадка. Клетка. тер. 2021;27:85.e1–85.e6. doi: 10.1016/j.bbmt.2020.10.009. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
65. Лин А., Малой М., Су Ю., Бхатт В., ДеРеспирис Л., Гриффин М., Лау К., Проли А. , Баркер Дж., Шаффер Б. и др. Летермовир для первичной и вторичной профилактики цитомегаловируса у реципиентов аллогенных трансплантатов гемопоэтических клеток: реальный опыт. Транспл. Заразить. Дис. 2019;21:e13187. doi: 10.1111/tid.13187. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
66. Maertens J., Cordonnier C., Jaksch P., Poiré X., Uknis M., Wu J., Wijatyk A., Saliba F. , Витцке О., Виллано С. Марибавир для превентивного лечения реактивации цитомегаловируса. Н. англ. Дж. Мед. 2019;381:1136–1147. doi: 10.1056/NEJMoa1714656. [PubMed] [CrossRef] [Google Scholar]
67. Кришна Б., Уиллс М.Р., Синклер Дж.Х. Достижения в лечении цитомегаловируса. бр. Мед. Бык. 2019; 131:5–17. doi: 10.1093/bmb/ldz031. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
68. Бирон К.К., Харви Р.Дж., Чемберлен С.К., Гуд С.С., Смит А.А., 3-й, Дэвис М.Г., Таларико К.Л., Миллер У.Х., Феррис Р., Дорнсайф Р.Э. и др. Мощное и избирательное ингибирование репликации цитомегаловируса человека с помощью 1263w94, L-рибозид бензимидазола с уникальным механизмом действия. Антимикроб. Агенты Чемотер. 2002; 46: 2365–2372. doi: 10.1128/AAC.46.8.2365-2372.2002. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Бирон К.К., Харви Р.Дж., Чемберлен С.К., Гуд С.С., Смит А.А., 3-й, Дэвис М.Г., Таларико К.Л., Миллер У.Х., Феррис Р., Дорнсайф Р.Э. и др. Мощное и избирательное ингибирование репликации цитомегаловируса человека с помощью 1263w94, L-рибозид бензимидазола с уникальным механизмом действия. Антимикроб. Агенты Чемотер. 2002; 46: 2365–2372. doi: 10.1128/AAC.46.8.2365-2372.2002. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
69. Ревелло М.Г., Лаззаротто Т., Герра Б., Спинилло А., Феррацци Э., Кустерманн А., Гуаскино С., Вергани П., Тодрос Т., Фруска Т. и др. Рандомизированное исследование гипериммунного глобулина для предотвращения врожденного цитомегаловируса. Н. англ. Дж. Мед. 2014; 370:1316–1326. doi: 10.1056/NEJMoa1310214. [PubMed] [CrossRef] [Академия Google]
70. Rawlinson W. Международные рекомендации по врожденному ЦМВ необходимы для диагностики, профилактики и лечения. Акта Педиатр. 2017;106:1389–1390. doi: 10.1111/apa.13959. [PubMed] [CrossRef] [Google Scholar]
71. Hughes B.L., Clifton R.G., Rouse D.J., Saade G.R., Dinsmoor M.J., Reddy UM, Pass R., Allard D., Mallett G., Fette LM, et al. Испытание гипериммунного глобулина для предотвращения врожденной цитомегаловирусной инфекции. Н. англ. Дж. Мед. 2021; 385: 436–444. дои: 10.1056/NEJMoa1913569. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Hughes B.L., Clifton R.G., Rouse D.J., Saade G.R., Dinsmoor M.J., Reddy UM, Pass R., Allard D., Mallett G., Fette LM, et al. Испытание гипериммунного глобулина для предотвращения врожденной цитомегаловирусной инфекции. Н. англ. Дж. Мед. 2021; 385: 436–444. дои: 10.1056/NEJMoa1913569. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
72. Каган К.О., Эндерс М., Хоопманн М., Гейпель А., Симонини К., Берг К., Готтшалк И., Фашингбауэр Ф. ., Schneider M.O., Ganzenmueller T., et al. Исход беременностей с недавней первичной цитомегаловирусной инфекцией в первом триместре, получавших лечение гипериммуноглобулином: обсервационное исследование. УЗИ Акушерство. Гинекол. 2021; 57: 560–567. doi: 10.1002/uog.23596. [PubMed] [CrossRef] [Google Scholar]
73. Уолтер Э.А., Гринберг П.Д., Гилберт М.Дж., Финч Р.Дж., Ватанабэ К.С., Томас Э.Д., Ридделл С.Р. Восстановление клеточного иммунитета против цитомегаловируса у реципиентов аллогенного костного мозга путем переноса клонов Т-клеток от донора. Н. англ. Дж. Мед. 1995;333:1038–1044. doi: 10.1056/NEJM199510193331603. [PubMed] [CrossRef] [Google Scholar]
Н. англ. Дж. Мед. 1995;333:1038–1044. doi: 10.1056/NEJM199510193331603. [PubMed] [CrossRef] [Google Scholar]
74. Фостер А.Е., Готтлиб Д.Дж., Маранголо М., Бартлетт А., Ли Ю.-К., Бартон Г.В., Романьоли Дж.А., Брэдсток К.Ф. Быстрое крупномасштабное производство высокочистых цитомегаловирус-специфических цитотоксических Т-клеток для адоптивной иммунотерапии. J. Гематотерапия. 2003; 12:93–105. doi: 10.1089/152581603321210172. [PubMed] [CrossRef] [Google Scholar]
75. Gerdemann U., Keirnan J.M., Katari U.L., Yanagisawa R., Christin A.S., Huye L.E., Perna S.K., Ennamuri S., Gottschalk S., Brenner M.K., et al. . Быстро генерируемые мультивирус-специфические цитотоксические Т-лимфоциты для профилактики и лечения вирусных инфекций. Мол. тер. 2012;20:1622–1632. doi: 10.1038/mt.2012.130. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
76. Миклетвейт К., Хансен А., Фостер А., Снейп Э., Антоненас В., Сартор М., Шоу П., Брэдсток К., Готлиб Д. Распространение ex vivo и профилактическое введение пептида CMV-pp65 — Специфические цитотоксические Т-лимфоциты после аллогенной трансплантации гемопоэтических стволовых клеток. биол. Трансплантация костного мозга. 2007; 13: 707–714. doi: 10.1016/j.bbmt.2007.02.004. [PubMed] [CrossRef] [Google Scholar]
биол. Трансплантация костного мозга. 2007; 13: 707–714. doi: 10.1016/j.bbmt.2007.02.004. [PubMed] [CrossRef] [Google Scholar]
77. Миклетвейт К.П., Клэнси Л., Сандер У., Хансен А.М., Блит Э., Антоненас В., Сартор М.М., Брэдсток К.Ф., Готлиб Д.Дж. Профилактическая инфузия цитомегаловирус-специфических цитотоксических Т-лимфоцитов, стимулированных ген-модифицированными дендритными клетками Ad5f35pp65, после аллогенной трансплантации гемопоэтических стволовых клеток. Кровь. 2008;112:3974–3981. doi: 10.1182/blood-2008-06-161695. [PubMed] [CrossRef] [Google Scholar]
78. Блит Э., Клэнси Л., Симмс Р., Ма С.К.К., Берджесс Дж., Део С., Байт К., Дубоск М.-К., Шоу П.Дж. , Micklethwaite K.P., et al. ЦМВ-специфические Т-клетки донорского происхождения снижают потребность в фармакотерапии, направленной на ЦМВ, после аллогенной трансплантации стволовых клеток. Кровь. 2013; 121:3745–3758. doi: 10.1182/blood-2012-08-448977. [PubMed] [CrossRef] [Google Scholar]
79. Peggs K.S., Verfuerth S. , Pizzey A., Chow S.C., Thomson K., MacKinnon S. Цитомегаловирус-специфическая Т-клеточная иммунотерапия способствует восстановлению прочного функционального противовирусного иммунитета после аллогенной Трансплантация стволовых клеток. клин. Заразить. Дис. 2009 г.;49:1851–1860. дои: 10.1086/648422. [PubMed] [CrossRef] [Google Scholar]
, Pizzey A., Chow S.C., Thomson K., MacKinnon S. Цитомегаловирус-специфическая Т-клеточная иммунотерапия способствует восстановлению прочного функционального противовирусного иммунитета после аллогенной Трансплантация стволовых клеток. клин. Заразить. Дис. 2009 г.;49:1851–1860. дои: 10.1086/648422. [PubMed] [CrossRef] [Google Scholar]
80. Feuchtinger T., Opherk K., Bethge W.A., Topp M.S., Schuster F.R., Weissinger E.M., Mohty M., Or R., Maschan M., Schumm M., и другие. Адаптивный перенос pp65-специфических Т-клеток для лечения химиорезистентного цитомегаловирусного заболевания или реактивации после трансплантации гаплоидентичных и неродственных стволовых клеток. Кровь. 2010; 116:4360–4367. doi: 10.1182/blood-2010-01-262089. [PubMed] [CrossRef] [Академия Google]
81. Leen A.M., Myers G.D., Sili U., Huls M.H., Weiss H., Leung K.S., Carrum G., Krance R.A., Chang C.-C., Molldrem J.J., et al. Полученные из монокультуры Т-лимфоциты, специфичные для нескольких вирусов, размножаются и вызывают клинически значимые эффекты у лиц с ослабленным иммунитетом. Нац. Мед. 2006; 12:1160–1166. doi: 10.1038/nm1475. [PubMed] [CrossRef] [Google Scholar]
Нац. Мед. 2006; 12:1160–1166. doi: 10.1038/nm1475. [PubMed] [CrossRef] [Google Scholar]
82. Papadopoulou A., Gerdemann U., Katari U.L., Tzannou I., Liu H., Martinez C., Leung K., Carrum G., Gee A.P., Vera J.F. , и другие. Активность Т-клеток широкого спектра действия для лечения инфекций AdV, EBV, CMV, BKV и HHV6 после ТГСК. науч. Перевод Мед. 2014;6:242ra83. doi: 10.1126/scitranslmed.3008825. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
83. Уизерс Б., Блит Э., Клэнси Л.Е., Йонг А., Фрейзер С., Берджесс Дж., Симмс Р., Браун Р., Климан Д., Дубоск М.-К. и др. Долгосрочный контроль рецидивирующих или рефрактерных вирусных инфекций после аллогенной ТГСК с использованием сторонних вирус-специфических Т-клеток. Кровь Adv. 2017;1:2193–2205. doi: 10.1182/bloodadvances.2017010223. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
84. Уизерс Б., Клэнси Л., Берджесс Дж., Симмс Р., Браун Р., Миклетуэйт К., Блит Э., Готлиб Д. Создание и функционирование стороннего банка вирус-специфических Т-клеток в рамках программы трансплантации аллогенных стволовых клеток. биол. Трансплантация костного мозга. 2018;24:2433–2442. doi: 10.1016/j.bbmt.2018.08.024. [PubMed] [CrossRef] [Академия Google]
биол. Трансплантация костного мозга. 2018;24:2433–2442. doi: 10.1016/j.bbmt.2018.08.024. [PubMed] [CrossRef] [Академия Google]
85. O’Reilly R.J., Prockop S., Hasan A., Doubrovina E. Терапевтические преимущества, обеспечиваемые банком вирус-специфических Т-клеток с определенной HLA-рестрикцией. Пересадка костного мозга. 2019; 54: 759–764. doi: 10.1038/s41409-019-0614-1. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
86. Weekes M.P., Tan SYL, Poole E., Talbot S., Antrobus R., Smith DL, Montag C., Gygi S.P., Sinclair JH, Ленер П. Дж. Деградация переносчика лекарств MRP1, связанная с латентностью, во время латентной цитомегаловирусной инфекции человека. Наука. 2013;340:199–202. doi: 10.1126/science.1235047. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
Воздействие на латентный резервуар цитомегаловируса с помощью противовирусного слитого токсинного белка. Нац. коммун. 2017;8:14321. doi: 10.1038/ncomms14321. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
88. Плоткин С.А., Старр С.Е., Фридман Х.М., Брейман К., Харрис С., Джексон С., Тастин Н.Б., Гроссман Р., Дефо Д. , Баркер С. Влияние вакцины против живого вируса Таун на цитомегаловирусную болезнь после трансплантации почки. Анна. Стажер Мед. 1991;114:525–531. doi: 10.7326/0003-4819-114-7-525. [PubMed] [CrossRef] [Google Scholar]
Плоткин С.А., Старр С.Е., Фридман Х.М., Брейман К., Харрис С., Джексон С., Тастин Н.Б., Гроссман Р., Дефо Д. , Баркер С. Влияние вакцины против живого вируса Таун на цитомегаловирусную болезнь после трансплантации почки. Анна. Стажер Мед. 1991;114:525–531. doi: 10.7326/0003-4819-114-7-525. [PubMed] [CrossRef] [Google Scholar]
89. Adler S.P., Starr S.E., Plotkin S.A., Hempfling S.H., Buis J., Manning ML, Best A. Иммунитет, индуцированный первичной цитомегаловирусной инфекцией человека, защищает от вторичной инфекции среди женщин Детородный возраст. Дж. Заразить. Дис. 1995; 171: 26–32. doi: 10.1093/infdis/171.1.26. [PubMed] [CrossRef] [Google Scholar]
90. Sabbaj S., Pass R., Pichon S., Goepfert P.A. Вакцина на основе гликопротеина В способна усиливать реакцию антител и Т-клеток CD4 на цитомегаловирус у женщин с хронической инфекцией. Дж. Заразить. Дис. 2011; 203:1534–1541. дои: 10.1093/infdis/jir138. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
91. Pass RF, Zhang C., Evans A., Simpson T., Andrews W., Huang M.-L., Corey L., Hill Дж., Дэвис Э., Фланиган С. и соавт. Вакцинопрофилактика материнской цитомегаловирусной инфекции. Н. англ. Дж. Мед. 2009; 360:1191–1199. doi: 10.1056/NEJMoa0804749. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Pass RF, Zhang C., Evans A., Simpson T., Andrews W., Huang M.-L., Corey L., Hill Дж., Дэвис Э., Фланиган С. и соавт. Вакцинопрофилактика материнской цитомегаловирусной инфекции. Н. англ. Дж. Мед. 2009; 360:1191–1199. doi: 10.1056/NEJMoa0804749. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Симптоматическая врожденная цитомегаловирусная инфекция у детей серопозитивных женщин
Истории болезни
. 2017 9 июня; 5:134.
doi: 10.3389/fped.2017.00134. Электронная коллекция 2017.
Инес Мак 1 , Мари-Энн Буркхардт 2 3 , Ульрих Хайнингер 1 , Фридерике Прюфер 4 , Свен Шульцке 5 , Свен Веллманн 5
Принадлежности
- 1 Детские инфекционные заболевания, Детская больница Базельского университета (UKBB), Базель, Швейцария.

- 2 Отделение эндокринологии и диабета, Детская больница принцессы Маргарет, Перт, Вашингтон, Австралия.
- 3 Школа педиатрии и детского здоровья, Университет Западной Австралии, Перт, Вашингтон, Австралия.
- 4 Детская радиология, Детская больница Базельского университета (UKBB), Базель, Швейцария.
- 5 Неонатология, Детская больница Базельского университета (UKBB), Базель, Швейцария.
- PMID: 28649563
- PMCID: PMC5465240
- DOI:
10.
 3389/фпед.2017.00134
3389/фпед.2017.00134
Бесплатная статья ЧВК
Отчеты о клинических случаях
Инес Мак и др. Фронт Педиатр. .
Бесплатная статья ЧВК
. 2017 9 июня; 5:134.
doi: 10.3389/fped.2017.00134. Электронная коллекция 2017.
Авторы
Инес Мак 1 , Мари-Энн Буркхардт 2 3 , Ульрих Хайнингер 1 , Фридерике Прюфер 4 , Свен Шульцке 5 , Свен Веллманн 5
Принадлежности
- 1 Детские инфекционные заболевания, Детская больница Базельского университета (UKBB), Базель, Швейцария.

- 2 Отделение эндокринологии и диабета, Детская больница принцессы Маргарет, Перт, Вашингтон, Австралия.
- 3 Школа педиатрии и детского здоровья, Университет Западной Австралии, Перт, Вашингтон, Австралия.
- 4 Детская радиология, Детская больница Базельского университета (UKBB), Базель, Швейцария.
- 5 Неонатология, Детская больница Базельского университета (UKBB), Базель, Швейцария.
- PMID: 28649563
- PMCID: PMC5465240
- DOI:
10.
 3389/фпед.2017.00134
3389/фпед.2017.00134
Абстрактный
Цитомегаловирус (ЦМВ) является наиболее частой врожденной вирусной инфекцией во всем мире. Риск врожденной передачи ЦМВ (цЦМВ) наиболее высок у серонегативных женщин, которые заразились первичной ЦМВ-инфекцией во время беременности. Растущее количество данных указывает на то, что вторичные ЦМВ-инфекции у беременных женщин с предзачаточным иммунитетом (либо в результате реактивации латентного вируса, либо в результате повторного заражения новым штаммом ЦМВ) способствуют гораздо большей доле симптоматического ЦМВ, чем считалось ранее. Здесь мы описываем случай симптоматической инфекции cCMV у новорожденного женщины с доказанным иммунитетом до беременности. Диагноз был подтвержден с помощью ПЦР ЦМВ из амниотической жидкости и МРТ плода. У новорожденного были типичные симптомы ЦМВ, включая желтуху, гепатоспленомегалию, холестаз, петехии, маленькую окружность головы и нейросенсорную тугоухость, наиболее частые неврологические последствия. CMV был обнаружен в крови и моче младенцев с помощью ПЦР, и было начато внутривенное введение ганцикловира, которое продолжалось перорально в течение 6 недель. Помимо сохраняющейся правосторонней глухоты, у ребенка наблюдалось нормальное неврологическое развитие вплоть до последнего наблюдения в 4,5 года. На сегодняшний день наиболее эффективной стратегией профилактики вертикальной передачи ЦМВ является гигиеническое консультирование женщин детородного возраста, которое в нашем случае и в соответствии с последними литературными данными касается как серонегативных, так и серопозитивных женщин. Если у будущей матери обнаруживается сероконверсия или признаки активной ЦМВ-инфекции, не существует установленных процедур для снижения риска передачи или вариантов лечения плода с признаками инфекции. После рождения младенцев с симптомами можно лечить ганцикловиром для подавления репликации вируса и улучшения слуха и исходов развития нервной системы. Всесторонний обзор литературы, включая наше тематическое исследование, раскрывает самые современные и значимые доступные варианты диагностики и лечения.
CMV был обнаружен в крови и моче младенцев с помощью ПЦР, и было начато внутривенное введение ганцикловира, которое продолжалось перорально в течение 6 недель. Помимо сохраняющейся правосторонней глухоты, у ребенка наблюдалось нормальное неврологическое развитие вплоть до последнего наблюдения в 4,5 года. На сегодняшний день наиболее эффективной стратегией профилактики вертикальной передачи ЦМВ является гигиеническое консультирование женщин детородного возраста, которое в нашем случае и в соответствии с последними литературными данными касается как серонегативных, так и серопозитивных женщин. Если у будущей матери обнаруживается сероконверсия или признаки активной ЦМВ-инфекции, не существует установленных процедур для снижения риска передачи или вариантов лечения плода с признаками инфекции. После рождения младенцев с симптомами можно лечить ганцикловиром для подавления репликации вируса и улучшения слуха и исходов развития нервной системы. Всесторонний обзор литературы, включая наше тематическое исследование, раскрывает самые современные и значимые доступные варианты диагностики и лечения. В заключение, триада, состоящая из консультирования матери по гигиене, послеродового скрининга слуха всех новорожденных с последующей ПЦР на ЦМВ у младенцев с симптомами и противовирусной терапии младенцев с симптомами ЦМВ, представляет собой схему передовой практики для снижения бремени последствий передачи ЦМВ.
В заключение, триада, состоящая из консультирования матери по гигиене, послеродового скрининга слуха всех новорожденных с последующей ПЦР на ЦМВ у младенцев с симптомами и противовирусной терапии младенцев с симптомами ЦМВ, представляет собой схему передовой практики для снижения бремени последствий передачи ЦМВ.
Ключевые слова: черничный маффин; кальцификация; цитомегаловирусные инфекции; потеря слуха; магнитно-резонансная томография; нейровизуализация; беременность.
Цифры
Рисунок 1
Магнитно-резонансная томография (МРТ) плода…
Рисунок 1
Магнитно-резонансная томография (МРТ) плода. (A) 26-я неделя беременности, ускорение аксиального Т2…
фигура 1 Магнитно-резонансная томография (МРТ) плода. (A) 26-я неделя беременности, аксиальная Т2, взвешенная по ускорению. Красные стрелки указывают на внутрижелудочковые кисты в задних рогах слегка расширенных боковых желудочков. (B) 36-я неделя беременности, взвешенная по ускорению коронарная Т2. Красными стрелками показаны внутрижелудочковые кисты, желтой стрелкой отмечены диффузные поражения белого вещества с повышенной интенсивностью Т2.
(A) 26-я неделя беременности, аксиальная Т2, взвешенная по ускорению. Красные стрелки указывают на внутрижелудочковые кисты в задних рогах слегка расширенных боковых желудочков. (B) 36-я неделя беременности, взвешенная по ускорению коронарная Т2. Красными стрелками показаны внутрижелудочковые кисты, желтой стрелкой отмечены диффузные поражения белого вещества с повышенной интенсивностью Т2.
Рисунок 2
Послеродовая магнитно-резонансная томография (МРТ)…
Рисунок 2
Постнатальная магнитно-резонансная томография (МРТ) в день жизни 5. Аксиальная (A) и…
фигура 2 Постнатальная магнитно-резонансная томография (МРТ) в день жизни 5. Аксиальная (A) и коронарный (B) T2-взвешенные последовательности. Красными стрелками показаны перегородки внутрижелудочковых кист в области бывшего зародышевого матрикса (loco classico). Незначительное расширение обоих боковых желудочков. Желтые стрелки отмечают гиперинтенсивность белого вещества бифронтально и затылочно. Признаков кальцификации или полимикрогирии нет.
Красными стрелками показаны перегородки внутрижелудочковых кист в области бывшего зародышевого матрикса (loco classico). Незначительное расширение обоих боковых желудочков. Желтые стрелки отмечают гиперинтенсивность белого вещества бифронтально и затылочно. Признаков кальцификации или полимикрогирии нет.
Рисунок 3
Магнитно-резонансная томография (МРТ) в…
Рисунок 3
Магнитно-резонансная томография (МРТ) в возрасте 4 лет. (A) Осевая T2-взвешенная последовательность…
Рисунок 3 Магнитно-резонансная томография (МРТ) в возрасте 4 лет. (A) Аксиальная Т2-взвешенная последовательность. Остаточная гиперинтенсивность белого вещества (за счет демиелинизации и глиоза) с перивентрикулярной локализацией с обеих сторон (желтые стрелки) и персистирующими внутрижелудочковыми перегородками, преимущественно в затылочной области (красная стрелка). (B) Коронарная T2-взвешенная последовательность. Остаточное перивентрикулярное гиперинтенсивное поражение белого вещества (желтые стрелки).
(B) Коронарная T2-взвешенная последовательность. Остаточное перивентрикулярное гиперинтенсивное поражение белого вещества (желтые стрелки).
См. это изображение и информацию об авторских правах в PMC
Похожие статьи
Профилактика и лечение цитомегаловирусной инфекции плода цитомегаловирусным гипериммунным глобулином: многоцентровое исследование в Мадриде.
Бласкес-Гамеро Д., Галиндо Искьердо А., Дель Росаль Т., Бакеро-Артигао Ф., Искердо Мендес Н., Сориано-Рамос М., Рохо Конехо П., Гонсалес-Томе М.И., Гарсия-Бургильо А., Перес Перес Н., Санчес В., Рамос-Амадор Х.Т., Де ла Калье М. Бласкес-Гамеро Д. и др. J Matern Fetal Neonatal Med. 201932 февраля (4): 617-625. дои: 10.1080/14767058.2017.1387890. Epub 2017 26 октября. J Matern Fetal Neonatal Med. 2019. PMID: 28978246
[Современные подходы к диагностике и лечению врожденных цитомегаловирусных инфекций и ситуация в Турции].

Шахинер Ф. Шахинер Ф. Микробиол бул. 2020 Январь; 54 (1): 171-190. дои: 10.5578/mb.68978. Микробиол бул. 2020. PMID: 32050888 Обзор. Турецкий.
Исходы слуха у врожденно инфицированных ЦМВ детей в Финляндии – результаты наблюдения после трехлетнего возраста.
Пухакка Л., Лаппалайнен М., Лённквист Т., Ниеминен Т., Боппана С., Саксен Х., Нименсиву Р. Пухакка Л. и др. Int J Pediatr Оториноларингол. 2022 Май; 156:111099. doi: 10.1016/j.ijporl.2022.111099. Epub 2022 3 марта. Int J Pediatr Оториноларингол. 2022. PMID: 35276528
Использование цитомегаловирусного гипериммуноглобулина для профилактики врожденной цитомегаловирусной болезни: ретроспективный анализ.
Буксманн Х.
 , Штакельберг О.М., Шлёссер Р.Л., Эндерс Г., Гонсер М., Мейер-Виткопф М., Хампрехт К., Эндерс М.
Буксманн Х. и др.
J Перинат Мед. 2012 27 марта; 40 (4): 439-46. doi: 10.1515/jpm-2011-0257.
J Перинат Мед. 2012.
PMID: 22752777
, Штакельберг О.М., Шлёссер Р.Л., Эндерс Г., Гонсер М., Мейер-Виткопф М., Хампрехт К., Эндерс М.
Буксманн Х. и др.
J Перинат Мед. 2012 27 марта; 40 (4): 439-46. doi: 10.1515/jpm-2011-0257.
J Перинат Мед. 2012.
PMID: 22752777Естественная история врожденной цитомегаловирусной инфекции в высокосеропозитивных популяциях.
Мусси-Пинхата М.М., Ямамото А.Ю. Мусси-Пинхата М.М. и соавт. J заразить дис. 2020 5 марта; 221 (Приложение 1): S15-S22. doi: 10.1093/infdis/jiz443. J заразить дис. 2020. PMID: 32134482 Бесплатная статья ЧВК.
Посмотреть все похожие статьи
Цитируется
Влияние латентной инфекции Toxoplasma gondii на историю спонтанных абортов и исходы беременности: крупномасштабное исследование.

Мокану А.Г., Стоян Д.Л., Крачунеску Э.Л., Чохат И.М., Мотофеля А.С., Наволан Д.Б., Вилибич-Цавлек Т., Стеванович В., Немеску Д., Форга М., Данилук Р., Иоана А.М., Крайна М. Мокану АГ и др. Микроорганизмы. 2022 30 сентября; 10 (10): 1944. doi: 10.3390/microorganisms10101944. Микроорганизмы. 2022. PMID: 36296220 Бесплатная статья ЧВК.
Подводные камни в серологической оценке материнской цитомегаловирусной инфекции как потенциальной причины поражений плода и новорожденного: обзор описательной литературы.
Иидзима С. Иидзима С. Дж. Клин Мед. 2022 авг 26;11(17):5006. doi: 10.3390/jcm11175006. Дж. Клин Мед. 2022. PMID: 36078936 Бесплатная статья ЧВК. Обзор.
Повреждение головного мозга у плодов человека с врожденной цитомегаловирусной инфекцией: гистологические особенности и вирусный тропизм.

Piccirilli G, Gabrielli L, Bonasoni MP, Chiereghin A, Turello G, Borgatti EC, Simonazzi G, Felici S, Leone M, Salfi NCM, Santini D, Lazzarotto T. Piccirilli G, et al. Селл Мол Нейробиол. 7 августа 2022 г. doi: 10.1007/s10571-022-01258-9. Онлайн перед печатью. Селл Мол Нейробиол. 2022. PMID: 35933637
Бремя врожденной цитомегаловирусной инфекции и эпидемиологические факторы риска в странах с всеобщим скринингом: систематический обзор и метаанализ.
Ссентонго П., Хенли С., Бирунги П., Роуч М.А., Спади Дж., Фронтерре С., Ван М., Мюррей-Колб Л.Е., Аль-Шаар Л., Чинчилли В.М., Броуч Дж.Р., Эриксон Дж.Е., Шифф С.Дж. Сентонго П. и соавт. JAMA Сеть открыта. 2021 авг 2;4(8):e2120736. doi: 10.1001/jamanetworkopen.2021.20736. JAMA Сеть открыта. 2021. PMID: 34424308 Бесплатная статья ЧВК.
Врожденная цитомегаловирусная инфекция человека, вызывающая нейросенсорную потерю слуха.

Ся В., Ян Х., Чжан Ю., Ван С., Гао В., Ур. С., Ван В., Лю З. Ся В. и др. Фронт микробиол. 2021 14 апр;12:649690. doi: 10.3389/fmicb.2021.649690. Электронная коллекция 2021. Фронт микробиол. 2021. PMID: 33936007 Бесплатная статья ЧВК. Обзор.
Просмотреть все статьи «Цитируется по»
использованная литература
- Шарланд М. Цитомегаловирус. В: Майк С., Карина Б., Эндрю С., Рон Д., Грэм Д., Рональд де Г. и др., редакторы. Руководство по детским инфекциям/Синяя книга. Оксфорд, Великобритания: Издательство Оксфордского университета; (2016). п. 507–12, 945 и 965.
- Leruez-Ville M, Ville Y. Фетальная цитомегаловирусная инфекция. Best Pract Res Clin Obstet Gynaecol (2017) 38:97–107.10.1016/j.
 bpobgyn.2016.10.005
—
DOI
—
пабмед
bpobgyn.2016.10.005
—
DOI
—
пабмед
- Leruez-Ville M, Ville Y. Фетальная цитомегаловирусная инфекция. Best Pract Res Clin Obstet Gynaecol (2017) 38:97–107.10.1016/j.
- Наинг З.В., Скотт Г.М., Шанд А., Гамильтон С.Т., ван Зуйлен В.Дж., Баша Дж. и др. Врожденная цитомегаловирусная инфекция беременных: обзор распространенности, особенностей клиники, диагностики и профилактики. Aust NZ J Obstet Gynaecol (2016) 56 (1): 9–18.10.1111/аджо.12408 — DOI — пабмед
- Кимберлин Д.

- Кимберлин Д.



 Г. Кузьменко, Д.Ю. Овсянников, Н.М. Киселева. — 2009.
Г. Кузьменко, Д.Ю. Овсянников, Н.М. Киселева. — 2009. При утилизации подгузников, салфеток и других предметов, загрязненных физиологическими жидкостями, необходимо тщательно мыть руки, прежде чем прикасаться к лицу.
При утилизации подгузников, салфеток и других предметов, загрязненных физиологическими жидкостями, необходимо тщательно мыть руки, прежде чем прикасаться к лицу.
 3389/фпед.2017.00134
3389/фпед.2017.00134
 3389/фпед.2017.00134
3389/фпед.2017.00134
 , Штакельберг О.М., Шлёссер Р.Л., Эндерс Г., Гонсер М., Мейер-Виткопф М., Хампрехт К., Эндерс М.
Буксманн Х. и др.
J Перинат Мед. 2012 27 марта; 40 (4): 439-46. doi: 10.1515/jpm-2011-0257.
J Перинат Мед. 2012.
PMID: 22752777
, Штакельберг О.М., Шлёссер Р.Л., Эндерс Г., Гонсер М., Мейер-Виткопф М., Хампрехт К., Эндерс М.
Буксманн Х. и др.
J Перинат Мед. 2012 27 марта; 40 (4): 439-46. doi: 10.1515/jpm-2011-0257.
J Перинат Мед. 2012.
PMID: 22752777


 bpobgyn.2016.10.005
—
DOI
—
пабмед
bpobgyn.2016.10.005
—
DOI
—
пабмед