ЭНДОКРИННЫЕ ЗАБОЛЕВАНИЯ У ДЕТЕЙ — Педиатры РО
Ведущие специалисты в области педиатрии
 Дудникова Элеонора Васильевна, Профессор, Доктор медицинских наук, Заведующая кафедрой детских болезней №1
Дудникова Элеонора Васильевна, Профессор, Доктор медицинских наук, Заведующая кафедрой детских болезней №1
Прочитать о докторе подробнее
Симованьян Эмма Никитична, Профессор, Доктор медицинских наук, Заведующая кафедрой детских инфекционных болезней РостГМУ
Прочитать о докторе подробнее
Чепурная Мария Михайловна, Профессор, Доктор Медицинских наук, Заслуженный врач РФ, Заведующая пульмонологическим отделением
Прочитать о докторе подробнее
Карпов Владимир Владимирович, Профессор, врач — педиатр
Прочитать о докторе подробнее
 Андриященко Ирина Ивановна, Врач-педиатр высшей квалификационной категории
Андриященко Ирина Ивановна, Врач-педиатр высшей квалификационной категории
Прочитать о докторе подробнее
 Редактор страницы: Крючкова Оксана Александровна
Редактор страницы: Крючкова Оксана Александровна
Большинство эндокринных расстройств возникают вследствие ослабления или усиления функции какой-либо железы внутренней секреции. Причинами подобной дисфункции могут быть: врожденная аномалия, генетический дефект, травма, воспалительный или опухолевый процесс, аутоиммунная агрессия, нервно-психический стресс.
Поражения гипофиза и гипоталамуса приводят к развитию заболеваний, очень сходных по своим клиническим проявлениям. Продуцирующиеся в ядрах гипоталамуса гормоны (статины и либерины) регулируют количество гормонов, выделяемых гипофизом (тропинов), которые в свою очередь изменяют функциональное состояние другихэндокринных желез или уровень метаболических процессов. Отсюда становится понятной идентичность конечного эффекта первичного поражения гипофиза и вторичного, вследствие нарушения функции гипоталамуса. В то же время первичные гипофизарные заболевания характеризуются одновременным нарушением нескольких тройных функций, что связано со способностью каждой гормонально активной клетки гипофиза продуцировать несколько видов гормонов (V. Pantic, 1975). Гипоталамические поражения отличаются менее очерченной клиникой, частым сочетанием эндокринных расстройств с неврологическими и трофическими нарушениями, возможностью изолированного изменения одной тройной функции гипофиза из-за высокой избирательности действия гормонов гипоталамуса.
Усиленная или недостаточная продукция тиреоидных гормонов лежит в основе патогенеза тиреотоксикоза и гипотиреоза. Избыток тиреоидных гормонов приводит к интоксикации сердечно-сосудистой и нервной систем. При дефиците гормонов наблюдаются снижение уровня всех метаболических процессов, задержка физического и психомоторного развития, накопление мукополисахаридов и липидов в тканях.
При дефиците гормона паращитовидных желез (паратгормона) возникает гипопаратиреоз, характеризующийся снижением кальциемии и повышением фосфатемии, в результате чего усиливается нервно-мышечная возбудимость и развиваются судороги. Гиперпаратиреоз — следствие избыточной продукции паратгормона, сопровождается гиперкальциемией и гипофосфатемией, проявляется остеопорозом, переломами костей, нефролитиазом.
Сахарный диабет развивается при абсолютной или относительной недостаточности инсулина, что приводит к нарушению углеводного обмена с гипергликемией и глюкозурией. Из вторичных нарушении метаболизма наиболее существенное значение имеет ацидоз. Избыточная продукция инсулина вызывает гиперинсулинизм, сопровождающийся гипогликемией с вторичными нарушениями в центральной нервной системе (гипоксия мозга и пр.).
В патогенезе хронического (болезнь Аддисона) и острого (синдром Уотерхауза — Фридрихсена) гипокортицизма основное значение имеет недостаточная продукция глюко- и минералокортикоидов, приводящая к дегидратации, гипотонии, гипогликемии и т. д.
В патогенезе гипогонадизма ведущей является недостаточная выработка половых гормонов, которая нередко обусловлена хромосомными аномалиями, приводящими к нарушению формирования половых желез (синдромы гонадального дисгенеза). При интерсексуализме, кроме анатомических уродств развития половых органов, отмечается снижение инкреторной функции половых желез или несоответствие продуцируемых гормонов гено- или фенотипу больного.
Снижение андрогенной и гонадотропной функций — одно из основных патогенетических моментов развития крипторхизма. В свою очередь крипторхизм, особенно двусторонний, нередко сопровождается гипогонадизмом.
Ожирение у детей чаще рассматривается как проявление adiposus-генотипа, при котором отмечается избыточное потребление пищи и гиперинсулинизм. Возможны поражения пищевых центров гипоталамуса. Реже ожирение является симптомом других эндокринных заболеваний.
Гипофизарный нанизм. Патогенетической является заместительная терапия гормонами передней доли гипофиза. Тиреоидные гормоны, инсулин (в меньшей мере — андрогены) обладают пермиссивным и потенцирующим действием по отношению к соматотропному гормону, поэтому данный вид терапии необходимо комбинировать с введением других тропных гормонов или гормонов периферических эндокринных желез.
ЭНДОКРИННЫЕ ЗАБОЛЕВАНИЯ У ДЕТЕЙ
Соматотропин (син. сотропин) показан в любом возрасте при наличии открытых зон роста. Оказывает анаболическое действие с увеличением массы тела и роста. Назначается из расчета 2 мг/м2 в сутки. Практикуется внутримышечное введение в дозе 2—4 мг 2—3 раза в неделю в зависимости от антропометрических показателей. Лечение длительное (обычно в течение 1—2 лет), непрерывное. Эффективность наиболее высока в первые 6 мес, затем она прогрессивно снижается, что связывают с образованием антител к экзогенному гормону роста (Н А. Зарубина, 1970). После перерыва в лечении в течение 3—12 мес чувствительность к соматотропину у части больных восстанавливается и лечение можно продолжить.
Побочные явления: возможны аллергические реакции.
При симптомах гипотиреоза показан тиротропин, стимулирующий функцию щитовидной железы. Вводится по 5—10 ЕД ежедневно или через день, всего 10—15 инъекций. Рекомендуется ежегодно проводить 2—3 подобных курса. Побочные явления: аллергические реакции.
Больным мужского пола в препубертатном и более старшем возрасте назначают хорионический гонадотропин (сип. хориогонин, гонабион) по 500—1000 ЕД 2 раза в неделю. Всего 10 инъекций, 2—3 курса в год. Препарат стимулирует функцию половых желез. Побочные явления: возможны аллергические реакции.
Поскольку лечение больных гипофизарным нанизмом соматотропным и тиреотропным гормонами не всегда бывает возможным, используют препараты, стимулирующие обменные процессы, компенсирующие эндокринную недостаточность.
Наиболее широкое распространение получили анаболические стероиды, усиливающие синтез белка. У части больных, вероятно, при остаточной соматотропной функции они способны повышать уровень циркулирующего соматотропного гормона (Н. А. Зарубина, 1975).
Метандростенолон, (син. неробол, дианобол) назначают по 0,1 мг/кг массы тела натощак. Курс лечения 20—30 дней. В год проводят 8 курсов.
Метиландростендиол назначается по 1 мг/кг массы тела. Обладает несколько большей андрогенной активностью, чем неробол, поэтому предпочтительнее применять у мальчиков.
Феноболин (син. нероболил, дураболин) вводят внутримышечно по 1 мг/кг массы тела в месяц (в 2—4 приема).
Ретаболил (син. декадураболин) обладает длительностью действия до 1 мес. Расчет месячной дозы такой же, как для феноболина.
Лечение анаболическими стероидами проводится в течение многих лет. Во избежание привыкания рекомендуется периодическая смена препаратов. Побочные явления наблюдаются лишь при передозировке препарата и проявляются вирилизацией. Поэтому необходим строгий рентгенологический контроль за состоянием оссификации, так как значительное ускорение ее требует уменьшения дозировок, а при наступлении синостозов — отмены препаратов.
При вторичном гипотиреозе, наблюдаемом у больных гипофизарным нанизмом, применяются тиреоидин и трийодтиронин (см. с. 267).
При введении инсулина возникает гипогликемия, способствующая выбросу эндогенных контринсулярных гормонов, в первую очередь соматотропного, а также усилению аппетита, что дает возможность ввести в рацион больных количество белка, необходимое для проявления ростового действия анаболических стероидов. Кроме того, инсулин обладает анаболическими свойствами. Применяется подкожно 1 раз в день за 15—20 мин до обеда. Необходим второй прием пищи через 2—2,5 ч после введения инсулина. Начальная доза 2—4 ЕД. Затем через каждые 2—3 дня количество инсулина увеличивают на 1—2 ЕД, стремясь довести его до максимального, переносимого больным без выраженных гипогликемических проявлений. Максимальная доза: детям дошкольного возраста — 6— 8 ЕД; до 12—14 лет — 8—10 ЕД; старше 14 лет— 10—14 ЕД. В течение года проводят 1—2 курса лечения при длительности каждого в 2—3 мес. Наиболее частое осложнение — гипогликемия, возникающая при передозировке препарата или нарушении режима питания.
Лечение больных должно проводиться на фоне диеты, обогащенной белками и витаминами. Рекомендуется дополнительное введение витаминов, особенно ретинола ацетата и группы В.
При гипоталамическом нанизме также применяют соматотропный гормон и инсулин по схемам, изложенным выше. Другие тройные гормоны гипофиза и тиреоидин назначаются лишь при доказанном снижении соответствующих функций. Анаболические стероиды вызывают большее ускорение созревания костей скелета, чем роста. Это, вероятно, связано с удовлетворительной андрогенной функцией, особенно в период пубертации, и суммацией эндо- и экзогенных андрогенных влияний на оссификацию. Поэтому их можно применять только при выраженной задержке созревания костей скелета и в дозах, уменьшенных по сравнению с таковыми для больных гипофизарным нанизмом в 4—8 раз.
Рекомендуются также дегидратационная терапия, рассасывающие средства, витамины.
Адипозогенитальная дистрофия требует коррекции пораженных соматотропной и гонадотропной функций. Назначают соматотропный гормон и анаболические стероиды по схеме, изложенной выше. Гонадотропин хорионический вводят детям до 12 лет по 1000 ЕД на инъекцию; старше 12 лет— 1500 ЕД. Курс лечения 10 инъекций. В течение года проводят 4—5 кур сов. Лечение начинают в возрасте 10—11 лет и проводят настойчиво в течение 3—5 лет и более. Большинству больных начиная с 15—18 лет, ввиду неполного восстановления половой функции целесообразно дополнительно вводить половые гормоны (см. с. 276).
Наличие ожирения и несахарного диабета требует соответствующей симптоматической терапии.
При впервые диагностированном несахарном диабете, особенно если он возник после инфекционного заболевания или травмы, лечение должно быть направлено на восстановление нарушенных гипоталамо-гипофизарных функций. Назначают антибиотики в возрастных дозах на 7—10 дней, дегидратационную терапию (внутривенное введение гексаметилентетрамина с глюкозой или внутримышечное введение магния сульфата — 10 инъекций) и витамины (в первую очередь группы В). Десенсибилизация достигается внутрикожным (!) введением во внутреннюю поверхность предплечья 0,25% раствора кальция хлорида, начиная с 0,2 мл, ежедневно увеличивая дозу на 0,2 мл и доводя ее до 1,4—2 мл, с последующим снижением на 0,2 мл ежедневно. Показан также интраназальный электрофорез кальция хлорида или калия йодида. Курс лечения 10—20 сеансов. Из средств патогенетической терапии назначается адиурекрин в понюшках 2—4 раза в день по 0,01 — 0,05 г на прием в зависимости от возраста и тяжести заболевания. Побочные явления: местная аллергическая реакция, вазомоторный ринит. У маленьких детей активное вдыхание препарата или вдувание его в нос бывает затруднено. В этих случаях может быть назначена мазь, содержащая в 1 г 100 мг препарата. Применяется 2—4 раза в сутки по 0,1—0,5 г. Более целесообразно применение адиурекрина по 1—2 капли в нос 1—3 раза в сутки. Лечение постоянное. Противопоказания: поражение придаточных полостей носа и дыхательных путей. В последнем случае возможно назначение питуитрина подкожно или внутримышечно по 0,5—3 мл в сутки (1 — 2 инъекции). В случаях резистентности к питуитрину допустимо увеличение дозы до 4 мл на 2—3-е сутки; при отсутствии эффекта препарат отменяют. Побочные явления: тошнота, головокружение, боль в животе. Противопоказан при гипертензии.
Вместо гормонотерапии можно назначать дихлотиазид по 25—100 мг в день (в 1—2 приема) в сочетании с препаратами калия. Механизм действия неясен. Показан также хлорпрорамид, повышающий выработку антидиуретического гормона. Назначают по 250—750 мг в сутки в 1—3 приема. Более эффективно комбинированное лечение дихлотиазидом и хлорпропамидом. Возможна гипогликемия.
При гигантизме с целью достижения синостозирования костей скелета иногда применяют половые гормоны, особенно при сопутствующем гипогонадизме (см. с. 276). Однако сомнительный эффект и частые осложнения в виде нарушений половой функции делают подобное лечение малооправданным.
Болезнь Иценко—Кушинга требует комбинированного лечения: помимо хирургических и лучевых методов назначают хлодитан (см. с. 275).
При преждевременном половом развитии показаны седативные средства в возрастных дозах в связи с наблюдаемыми у больных гиперсексуальностью и невротичностью.
Гипоталамический синдром пубертатного периода. Для нормализации гипоталамо-гипофизарных функций необходимо проводить дегидратационную терапию: внутримышечно вводится 6—10 мл 25% раствора магния сульфата ежедневно. Курс лечения 10—15 инъекций. Затем на протяжении 2— 3 мес применяются диакарб по 0,25 г, дихлотиазид по 50 мг или фуросемид по 40 мг 1—2 раза в неделю. С целью десенсибилизации внутрикожно (!) вводится 0,25% раствор кальция хлорида (см. с. 265), затем на протяжении 1—2 мес внутрь применяются антигистаминные препараты. Показаны рассасывающая терапия и биогенные стимуляторы — экстракт алоэ по 1 мл, ФиБС или стекловидное тело в той же дозе. Курс лечения 20—25 инъекций. Вводят ежедневно или через день под кожу. Лечение необходимо проводить на фоне субкалорийной диеты и занятий ЛФК (см. с. 277). При упорной гипертензии, не снижающейся под влиянием описанной терапии, добавляют резерпин по 0,1—0,25 мг 1—2 раза в сутки с постепенным уменьшением дозы по достижении гипотензивного эффекта до минимальной поддерживающей, однако полная отмена препарата проводится лишь через 2—3 мес. Поскольку данное заболевание протекает хронически и склонно к обострениям, рекомендуется повторять подобные курсы 1—2 раза в год, лучше весной и осенью, на протяжении 2—3 лет.
Гипотиреоз. Всем больным как с первичным, так и вторичным гипотиреозом показаны тиреоидные гормоны, от которых во многом зависит биологическая зрелость клеточных структур. Поэтому поздно начатое лечение не восстанавливает некоторые дефекты, в первую очередь интеллектуальные.
Назначать тиреоидин после еды (в 1—3 приема) лучше в первую половину дня ввиду возбуждающего действия. Доза подбирается индивидуально, начиная с минимальной (0,01- 0,025 г в сутки), с постепенным повышением до оптимальной, обеспечивающей компенсацию патологического процесса.
Суточная потребность в тиреоидине варьирует в широких пределах в зависимости от тяжести заболевания, чувствительности организма к препарату и, в меньшей мере, от возраста больного. При легко протекающем вторичном гипотиреозе (например, при гипофизарном нанизме) потребность в тиреоидине составляет обычно 0,05—0,1 г в сутки. При более тяжелом первичном гипотиреозе соответствующая доза равна 0,1 — 0,3 г, в некоторых случаях — 0,5—0,7 г. Лечение пожизненное. Только при легко протекающем вторичном гипотиреозе допускаются перерывы в лечении на летние месяцы.
Передозировка препарата или повышенная чувствительность к нему проявляется возбуждением, потливостью, тахикардией и другими симптомами, аналогичными таковым при тиреотоксикозе. В подобных случаях рекомендуется уменьшение дозы или перерыв в лечении. Противопоказаний нет.
Трийодтиронина гидрохлорид назначается как самостоятельно, так и в комбинации с тиреоидином. Особенно целесообразна такая терапия при нарушении чувствительности к последнему, а также при гипотиреозе вследствие ферментативного дефекта, прекращающего синтез эндогенного трийодтиронина. Схема лечения, побочные явления такие же, как для тиреоидина, но доза препарата значительно меньше (5—25, редко 50 мкг в сутки).
Тиротропин показан при вторичном гипотиреозе.
Из средств симптоматической терапии внутрь назначают аминалон по 0,25 г 3—6 раз в сутки. Курс лечения 1—2 мес. В год проводят 2—3 курса. Церебролизин применяется по 1 мл внутримышечно ежедневно или через день. Курс лечения 20—30 инъекций. В год проводят 1—2 курса.
Кислота глютаминовая назначается внутрь по 0,05—0,1 г/кг массы тела. Детям младшего возраста, у которых прием таблеток затруднен, препарат целесообразно назначать внутрь в виде 1% раствора в 20% растворе глюкозы. Курс лечения до 6 мес. Для достижения лучшего эффекта рекомендуется чередовать курсы лечения аминалоном, церебролизином и кислотой глютаминовой, настойчиво повторяя их на протяжении многих лет.
При гипотиреозе показаны также общее ультрафиолетовое облучение ежедневно или через день (до 20 сеансов), хвойно-солевые ванны 2—3 раза в неделю (10 процедур), общий массаж.
При тиреотоксикозе используется мерказолил, тормозящий выработку тиреоидных гормонов. Назначается в комбинации с дийодтирозином и бетазином. Действие последних основано на снижении выделения тиреотропина и наиболее активных тиреоидных гормонов. Мерказолил используется в таблетках по 5 мг в 3—4 приема. Суточная доза колеблется в зависимости от тяжести процесса (15—60 мг). При достижении компенсации количество препарата медленно снижают. Перерывы в лечении или слишком быстрое уменьшение дозы вызывают рецидивы, плохо поддающиеся повторной компенсации. Излечения тиреотоксикоза удается добиться при длительности терапии не менее 2 лет. В случае отсутствия стойкого эффекта после 6 мес лечения больные подлежат оперативному вмешательству.
Мерказолил иногда вызывает лейко- и гранулопению, ввиду чего необходимо производить исследования крови. Реже отмечаются диспепсические и аллергические явления. В этих случаях отменяют препарат или уменьшают его дозы. Довольно постоянен зобогенный эффект мерказолила, однако он значительно ослабляется при назначении йодистых препаратов. Мерказолил противопоказан при выраженной лейко- и гранулопении. Следует избегать одновременного применения сульфаниламидных препаратов, амидопирина и других из-за повышенного риска поражения белой крови.
Дийодтирозин применяют по 0,05 г 2—3 раза в день после еды, запивая молоком. При достижении состояния компенсации доза постепенно снижается, однако, как и для мерказолила, общая длительность лечения не менее 2 лет. В случае развития побочных явлений (насморк, слезотечение, диспепсические расстройства, кожная сыпь) препарат отменяют.
Бетазин по действию близок к дийодтирозину. Отмечено лишь некоторое его преимущество при лечении больных с выраженным экзофтальмом.
В качестве симптоматической терапии, направленной на ликвидацию нервных проявлений тиреотоксикоза, применяется резерпин по 0,1—0,5 мг в сутки (в 1—2 приема). Курс лече- 1-1,5 Мес. При обострениях возможно повторное назначение препарата.
Для устранения вегетососудистых и неврологических симптомов показаны препараты валерианы, майского ландыша, горицвета, пустырника, бромиды и пр.
При тяжелых формах тиреотоксикоза, наличии сердечнососудистой недостаточности применяют препараты наперстянки и строфантина К в обычных возрастных дозах.
Больным тиреотоксикозом необходим постельный режим. В дальнейшем их переводят на полупостельный режим, а при достижении компенсации — на общий с исключением физических и психических нагрузок. Рекомендуется диета № 10. Всякие физиотерапевтические назначения противопоказаны.
Эутиреоидный зоб. При недостаточном поступлении йода в организм целесообразно введение его неорганических форм. Используют различные прописи, однако наиболее популярен раствор Люголя (йода 0,1 г, калия йодида 0,2 г, воды 10 мл). Назначается по 1—3 капли 2 раза в день после еды на молоке.
В обращении более удобен микройод, применяемый по 1 драже в неделю, или антиструмин — по 1 таблетке 2—3 раза в неделю. Лечение длительное (годами) без перерыва.
Побочные явления. Противопоказания: туберкулез, заболевания почек, угри и другие поражения кожи.
В последние годы для лечения зоба стали применять тиреоидин как блокатор тиреотропного гормона. Лечение начинают с 0,01—0,02 г в сутки. Постепенно дозу повышают до 0,05—0,2 г в сутки при условии, если она не вызывает симптомов тиреотоксикоза. Лечение длительное (не менее 3— 6 мес). Противопоказан при повышенной нервной возбудимости.
Диетические рекомендации касаются максимального введения в рацион продуктов, содержащих йод (морская рыба, морская капуста и пр.), и ограничение потребления репы, капусты, редиса, обладающих зобогенным эффектом.
В.ОК. 09.04.2016г.
ОПТ.ОК. 09.04.2016г.
pediatry-ro.ru
Лекции педиатрия — Стр 24
При исследовании костного мозга, которое является «золотым стандартом» диагностики лейкозов, выявляется почти полное замещение нормальных элементов кроветворения опухолевыми (лейкемическими) клетками.
Прогноз заболевания зависит от его типа и лучше при лимфобластном лейкозе, вызванным клетками-предшественницами В-лимфоцитов, которые выявляют по обнаружению их специфических рецепторов.
Эндокринная система у детей.
Понятие об эндокринной системе регуляций функции.
Под эндокринной системой регуляции подразумевают продукцию клетками эндокринных желез специальных веществ – гормонов, которые поступают в кровь, разносятся нею и осуществляют регуляцию функций органов и тканей мишеней (усиление или ослабление в зависимости от потребностей организма). Как правило, железы внутренней секреции значительно удалены от мест приложения действия их секретов – гормонов. Гормоны выступают своеобразными посланниками, командами, зашифрованными химическим путем. По своей составу они могут быть пептидной или стероидной (холестерол) природы. Пептидные гормоны реагируют со специфичными рецепторами на поверхности мембран клеток. Стероидные гормоны реагируют непосредственно с ДНК внутри клеток, высвобождая эффекты генов с достижением соответствующих эффектов.
Существует общая закономерность действия эндокринной системы –
чем больше выделяется гормонов, тем больше интенсивность выполнения функции органами и тканями. Отсутствие гормона ведет к остановке функции или ее очень низкому уровню. Организация гормонального управления в организме основывается на дублировании (несколько гормонов могут выполнять примерно сходные цели), и контррегулировании – противодействующие контргормоны. Кроме того, вся система функционирования эндокринной системы охвачена так называемой обратной связью – при исчезновении потребности в усилении функции автоматически снижается интенсивность выработки гормонов или включаются контргормоны.
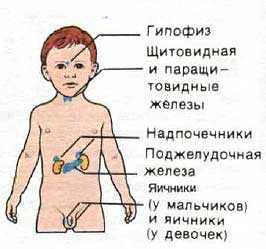
Эндокринные, то есть обладающие внутрисекреторной функцией, железы включают гипофиз, эпифиз, надпочечники, щитовидную, паращитовидные, вилочковую, поджелудочную и половые железы. Каждая из них обладает специфической функцией, но все они находятся в тесной взаимосвязи друг с другом и с ЦНС, обеспечивая единство регуляции функций организма, что отражается в часто используемом термине “нейроэндокринная
(нейрогуморальная) регуляция”. Главным организующим центром,
который обеспечивает регуляцию в условиях интенсивного потока нейроэндокринных импульсов и участвует в организации обратных связей, является гипоталамус. Эффективность его работы объясняется тем, что он является частью мозга и регулируется непосредственными связями с многочисленными нейронами ЦНС. В свою очередь гипоталамус обладает гормональной активностью, синтезирует релизинг-гормоны, которые стимулируют образование тропных к эндокринным железам гормонов гипофиза. Функциональное состояние эндокринных желез, особенно гипоталамо-гипофизарной «оси», имеет огромное значение для детей, так как определяет их рост и развитие.
Система эндокринной регуляции очень сильно зависит от состояния (восприимчивости) рецепторного аппарата клеток тканей к гормональным импульсам. В некоторых случаях отсутствуют не гормоны, а органы-мишени для действия гормонов или рецепторы клеток органов-мишеней. Например, ниже рассматривается клинический феномен, когда при врожденной аплазии щитовидной железы многочисленные стимулирующие «послания» гипофиза виде химических молекул – тиреотропных гормонов гипофиза остаются без ответа и функция щитовидной железы не нарастает.
Понятие о становлении эндокринной системы в различные периоды детства.
Органогенез большинства эндокринных желез и образование гипоталамического отдела промежуточного мозга начинается на 5 —6-й неделе эмбриональной фазы. Гормональный синтез начинается после завершения органогенеза — в І триместре беременности.
С позиций эмбриологии следует рассматривать гипоталамус, гипофиз и эпифиз как производные структуры головного мозга. Тимус (вилочковая железа), щитовидные и паращитовидные железы – производные жаберных карманов. Поджелудочная железа – образуется из выпячивания средней кишки эмбриона. Надпочечники образуются вместе с формированием коркового вещества почек.
Во II триместре участие системы гипоталамус — гипофиз-кора надпочечников в регуляторной деятельности уже выражено. К моменту рождения гипофиз обладает отчетливой секреторной активностью, что подтверждается наличием в пуповинной крови плода и новорожденного
высокого содержания АКТГ. Доказана также функциональная активность коры надпочечников во внутриутробном периоде.
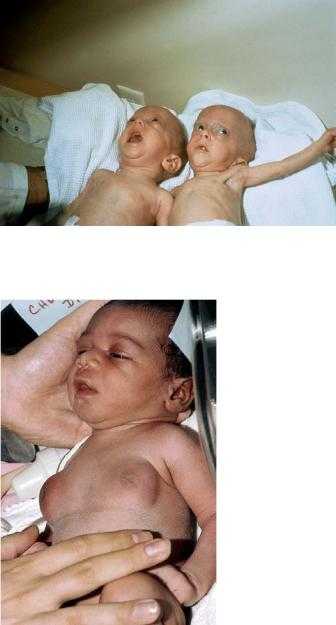
Неблагоприятное течение беременности, возраст матери и профессия могут способствовать отклонениям в процессах формирования нейроэндокринной системы плода. Развитие плода, особенно на раннем этапе, несомненно, находится под влиянием гормонов матери, которые ребенок получает с плацентарной кровью и затем продолжает получать с материнским молоком во внеутробном периоде. В любом случае, применение гормональных веществ беременным женщинам осуществляется по очень строгим показаниям. Эндокринные заболевания матери плода, сопровождающиеся высокими содержаниями гормонов в крови, могут вызвать аналогичные заболевания у плода и новорожденного (например, тиреотоксикоз и половой криз у новорожденных).
Два младенца-мальчика (близнецы) с врожденным неонатальным гипертиреозом. У обоих отмечается дефицит подкожно-жировой ткани. Дети постоянно лежат с широко раскрытыми глазами, которые «пристально за Вами наблюдают» и с «озабоченным» выражением лица.
Гинекомастия новорожденного, связанная с гиперэстрогенемией матери в последние недели беременности.
Подводя итог краткой характеристики онтогенеза эндокринной системы у человека можно отметить, что во внутриутробном периоде наибольшего анатомического совершенства и количественного развития достигают гипофиз и тимус, который является не только железой внутренней секреции, но все же больше относится к лимфоидным образованиям иммунной системы. После рождения быстро совершенствуются надпочечники, щитовидная и паращитовидные железы, панкреатическая железа, в то время как гормональная активность тимуса подвергается обратному развитию. В начале подросткового периода начинается бурное формирование половых желез, окончательное становление которых и знаменуют окончание детства, а возрастная инволюция
– старость.
Сущность эндокринной системы регуляции в организме.
Гормональная система регуляции организована обратными связями.
Например, тиреотропин-освобождающий гормон гипоталамуса способствует выработке тиреостимулирующего гормона передней доли гипофиза, который в свою очередь стимулирует выработку гормонов щитовидной железы – трийодтиронина и тироксина. Достаточное содержание тироксина тормозит гипоталамус и т.д.
Из всего перечисленного следует, что клинические исследования состояния эндокринной системы основываются на следующих принципах:
Принципы, на которых основывается клиническое исследование эндокринной системы.
1.Выявление признаков и синдромов, которые характерны для гиперили гипопродукции гормонов железами внутренней секреции у ребенка.
2.Определение содержания (концентрации) гормонов в сыворотке (плазме) крови, принимая во внимание принцип обратной связи – если содержание конечного эффекторного (тканевого) гормона недостаточно, должна выявляться повышенная концентрация тропного гормона гипофиза и релизинг-гормона гипоталамуса и наоборот.
3.Обнаружение ненормальной реакции органов и клетокмишеней для гормонов (феминизация мальчиков с развитием их по женскому типу при наличии яичек, которую называют еще тестикулярной феминизацией и др.).
4.Определение размеров эндокринных желез. Кстати, увеличение в размере эндокринной железы не обязательно сопровождается повышенной продукцией гормонов, например, как в случае эутиреоидного зоба – компенсаторного увеличения щитовидной железы при недостатке йода в пище, или при гормонально неактивной
234
аденоме (увеличение железы) гипофиза, которая проявляет себя только неврологическими симптомами в результате сдавления окружающих структур ЦНС. В редких случаях, когда возникает подозрение на отсутствие железы внутренней секреции (например, щитовидной) могут понадобиться методы определения (визуализации) ее возможного необычного перемещения (дислокации), например, язычная локализация щитовидной железы и др.
Характеристика желез внутренней секреции у детей, эффекты их гормонов на органы и клетки-мишени, семиотика недостаточности или избыточности деятельности
эндокринных желез.
Гипоталамус.
Гипоталамус – область ствола головного мозга и одновременно высший орган в системе прямых и обратных связей в системе эндокринной регуляции. Как часть нервной системы гипоталамус участвует в формировании важнейших вегетативных функций – чувства голода и жажды, поддержании температуры, артериального давления, потоотделения и многих других. Одновременно как орган эндокринной системы гипоталамус вырабатывает релизинг (освобождающие) гормоны, способные возбуждать продукцию гормонов гипофизом. То есть гормоны гипоталамуса в основном сосредоточены на органе-мишени – гипофизе.
Врожденные структурные изменения гипоталамуса, как правило, не совместимы с жизнью. Чаще во врачебной практике приходится иметь дело с приобретенными заболеваниями гипоталамической области – последствия перенесенных энцефалитов.
Семиотика поражений гипоталамуса
Гипоталамический синдром (дисфункция гипоталамуса) проявляет себя разнообразными вегетативными расстройствами (булимией — неукротимым аппетитом, немотивированной жаждой, колебаниями температуры тела так называемого «центрального» генеза, асимметрией потоотделения, повышением или понижением артериального давления). Закономерно возникают расстройства многих других эндокринных желез. Их деятельность может быть как усиленной, так и ослабленной в результате развития гипоталамического синдрома. Часто внешний вид больных соответствует ожирению значительных степеней тяжести с избыточной массой, достигающей 200% и более от нормы. Это так называемые гипоталамические формы ожирения. Развиваются они очень быстро после перенесенного вирусного заболевания ЦНС с поражением гипоталамической области.
Гипофиз (мозговой придаток).
Гипофиз также является производной частью головного мозга и его оболочек, однако имеет все атрибуты самостоятельной эндокринной железы, так как его секреты попадают в кровь и разносятся далеко, достигая других эндокринных желез. Анатомически гипофиз расположен в выемке на внутренней поверхности основания черепа, носящей название «турецкое седло». Гипофиз наиболее развит из всех эндокринных желез к моменту рождения. Его важнейшей функциональной особенностью является разносторонность действия.
Передняя доля гипофиза продуцирует несколько тропных пептидных гормонов. Это соматотропный гормон (СТГ) или гормон роста, адренокортикотропный гормон (АКТГ), стимулирующий выработку гормонов корой надпочечников, тиреотропный (ТТГ) и гонадотропные (ГТГ) гормоны. Все эти пептиды оказывают стимулирующее действие на другие железы внутренней секреции -щитовидную железу, надпочечники и гонады, заставляя их вырабатывать тканевые гормоны, которые и регулируют функции клеток тканей человеческого организма.
Физиологическое значение СТГ в период детства. В постнатальном периоде СТГ является основным метаболическим, влияющим на все виды обмена. Под его действием непосредственно во всех тканях образуется инсулиноподобный фактор роста, биологическое значение которого заключается в обеспечении роста тканей как биологического явления вообще. В настоящее время СТГ и фактор роста приобрели значение мощнейших спортивных допингов, позволяющих достичь исключительных физических возможностей у взрослых.
Задняя доля гипофиза, анатомически тесно связанная с гипоталамусом (гипоталамо-гипофизарная система), — основной продуцент окситоцина, усиливающего сокращения матки и молочных протоков у взрослых женщин, а также вазопрессина (антидиуретического гормона — АДГ), который принимает участие в регуляции водного баланса. Регуляция синтеза АДГ и его поступление в кровь контролируются гипоталамусом.
Семиотика поражений гипофиза Гиперфункция передней доли гипофиза
(аденома), которые бывают очень редко, проявляет себя высокими значения СТГ и влияет на рост и приводит к
гипофизарному гигантизму (не путать с семейной высокорослостью!).
Гипофизарный гигантизм у 8-летнего мальчика. Рост и костный возраст соответствовали 12 годам, IQ был 60. Обратите внимание на выступающие лоб и нижнюю челюсть, большие кисти и стопы. Половое
развитие соответствовало возрасту. Окончательный рост в возрасте 20 лет составил 208 см. Он носит размер 48 размер туфель.
Гормонально активная аденома передней доли гипофиза с высоким уровнем содержания СТГ в крови развивается чаще у подростков и взрослых лиц — по окончании периода их роста с исчезновением в костях ростковых зон. В клинической практике подобное явление ведет к формированию
акромегалии. Акромегалией обычно называют увеличение в размерах
дистальных частей конечностей и выступающих частей лица.
Гормонально активная аденома передней доли гипофиза, сопровождающаяся гиперпродукцией КТГ ведет к гипофизарной форме болезни Кушинга. Болезнь или синдром Кушинга складывается из признаков (симптомов), которые обусловлены повышенным содержанием в плазме глюко- и минералокортикоидов. Это гипергликемия, «буйволообразный» тип ожирения, гипертензия, гипернатриемия и пастозность тканей, гипокалиемия.
Гипофункция передней доли гипофиза обычно проявляется снижением по сравнению с нормой концентрации СТГ, инсулиноподобного фактора роста и гонадотропных гормонов (ГТГ) и вызывает гипофизарный пропорциональный нанизм с сохранной психикой, но задержкой или отсутствием полового созревания.
Функциональные нарушения в деятельности переднего гипофиза могут затрагивать все стороны деятельности железы. Этот синдром называется диспитуитаризмом и нередко возникает в подростковом возрасте.
Дисфункция задней доли гипофиза. При недостаточной выработке АДГ развивается синдром патологической полиурии и полидипсии (несахарный диабет) при отсутствии гипергликемии и глюкозурии.
Полное выпадение функции гипофиза (травма, уничтожение опухолью и др.) сопровождается клинической картиной прогрессирующей кахексии (истощения) и у детей наблюдается редко.
Увеличение в размерах гипофиза можно наблюдать косвенно по увеличению объема «турецкого седла» на боковых рентгенограммах черепа. Это один из визуализирующих методов определения размеров эндокринной железы и широко используется в эндокринологической практике.
А. Рентгенограмма черепа 9-летнего мальчика с полидипсией, полиурией, ноктурией и энурезом. Удельный вес мочи составил после пробы с сухоедением всего лишь 1.010. В течение последующих 6 месяцев симптомы мочеизнурения (диабета) уменьшились.
В. Вновь ребенок поступил в клинику в возрасте 14 лет с жалобами на задержку роста и полового созревания. Лабораторные исследования обнаружили недостаток гормона роста, гонадотропинов, кортикотропина и тиреотропина. Отмечено явное увеличение в размерах sella turcica. Неврологическое и офтальмологическое обследование не выявило патологических отклонений. После назначения с заместительной целью гидрокортизона и тироксина несахарный диабет у больного обострился. При хирургическом вмешательстве у больного была удалена большая краниофарингеома (аденома гипофиза).
Надпочечники
.
Корковый слой надпочечников вырабатывает более 60 биологически активных веществ и тканевых гормонов стероидной природы,
которые по своему воздействию на обменные процессы делятся на глюкокортикоиды (кортизон, кортизол), минералокортикоиды (альдостерон, 11- дезокси-кортикостерон), половые гормоны — андрогены (17-кетостероиды и тестостерон) и следовые концентрации женских половых гормонов — эстрогенов (эстрадиол).
Продукция кортико- и минералокортикостероидов находятся под контролем АКТГ гипофиза и взаимосвязана с ним. Эти гормоны обеспечивают катаболизирующие эффекты, высвобождая энергию, обладают антистрессорным, противовоспалительным и иммунорегулирующим действием. Кроме того, минералокортикоиды участвуют в регуляции водносолевого обмена (задерживают в организме натрий и выводят калий).
Роль половых гормонов надпочечников особенно велика во внутриутробном периоде. Она заключается в формировании первичных половых признаков – фенотипической дифференциации детей на мальчиков и девочек. При этом даже небольшие концентрации 17-кетостероидов, тестостерона и эстрадиола способны взаимодействовать с половыми
238
хромосомами клеток тканей, дающих начало формированию половых органов (гениталий), направляя их дифференциацию по мужскому или женскому типу в соответствии с генотипом — хромосомными наборами 46, ХY или 46, XX. В периоде жизни человека с момента рождения до начала его полового созревания нормальное, обычно небольшое, содержание половых гормонов надпочечников обладает лишь анаболическим действием и поддерживает потребности роста здорового организма. Тела детей до 8-9 лет по своему строению у мальчиков и девочек практически не отличаются. Исключение составляют гениталии, сформированные согласно генотипическим признакам. Они определяются как нормальные первичные половые признаки ребенка и соответствуют 1 стадии полового развития (по JM Tanner, см. фотографии). В начале пубертатного периода (примерно в 11 лет у девочек и 13 лет у мальчиков), повинуясь гормональным сигналам гипоталамуса и гипофиза, надпочечники кратковременно реагируют повышением продукции мужского полового гормона надпочечников – тестостерона как у мальчиков, так и у девочек. Запускается каскад реакций полового созревания. Первой из них является – пубархе — рост прямых светлых волос в виде пучка на лобке, а также рост и гормональная активность половых желез – яичек у мальчиков и яичников у девочек. В последующем только активность половых желез на все время полового созревания уже будет обеспечивать формирование вторичных половых признаков. Во время детородного периода эти же половые железы возьмут на себя обеспечение организма не только половыми гормонами, но и половыми клетками, что сделает возможным рождение потомства. И только лишь после возрастной инволюции половых желез надпочечники вновь, как и в детстве станут источником тестостерона, как гормона обладающего анаболическим действием.
Семиотика поражения коркового вещества надпочечников.
О состоянии функции коры надпочечников судят по содержанию в крови АКТГ, кортикостероидов, минералокортикоидов, по концентрация калия, натрия и хлора (косвенные признаки гипоили гиперальдостеронизма), по концентрации 17кетостероидов в моче, по типичным проявлением симптомокомплексов Кушинга, Аддисона, по правильности формирования наружных половых органов у девочек (генотип 46,ХХ), по возможным признакам преждевременного полового созревания у мальчиков и девочек.
Снижение функции коры надпочечников по выработке стероидов, а
нередко и поражение мозгового вещества надпочечников, возможно у детей, перенесших кровоизлияния в надпочечники в период родов, и в результате опухолевого процесса или менингококцемии в более старшем возрасте. Снижение функции надпочечников по выработке гормонов при этом бывает тотальным и заключается в дефиците всех видов стероидов, а, нередко, и прессорных аминов (адреналина, норадреналина). В клинической практике проявлением такой драматической дисфункции надпочечников является
синдром острой надпочечниковой недостаточности. В случаях его развития у детей независимо от возраста появляются признаки нарушения кровообращения: нитевидный учащенный пульс, падение артериального давления, гипогликемия, изменение окраски кожных покровов (ливедо). Методами визуализации увеличенных в результате кровоизлияния надпочечников являются ультразвуковое и рентгенологическое компьютерное сканирование. Более отдаленными симптомами перенесенного кровоизлияния является кальцификация надпочечников, которую можно обнаружить на обзорной рентгенограмме брюшной полости по специфичным плотным включениям солей кальция в ткань надпочечника.
Хроническая недостаточность надпочечников (болезнь Аддисона)
туберкулезного или аутоиммунного происхождения наблюдается преимущественно у школьников в виде похудения, мышечной слабости, своеобразной коричневатой окраски кожи на животе, в области гениталий и суставов, гипонатриемии и гиперкалиемии. И для острой и для хронической форм надпочечниковой недостаточности характерно снижение содержание глюкокортикоидов и минералокортикоидов в плазме крови. Кроме того, для хронической формы недостаточности характерна высокая концентрация АКТГ, как следствие безрезультатных сигналов гипофиза усилить продукцию тканевых гормонов.
Повышенная функция коры надпочечников с гиперсекрецией глюкокортикоидов, андрогенов и частично минералокортикоидов – надпочечниковая форма синдрома Кушинга — у детей развивается редко в основном в результате гормонально активной опухоли коркового слоя. Уровень АКТГ в плазме низкий.
Особый интерес с клинической точки зрения представляют генетически детерминированные нарушения синтеза стероидов коры надпочечников с повышением уровня в плазме крови пораженных детей гормонально активных метаболитов ряда 17-кетостероидов-тестостерона, возможно, с одновременным дефицитом минерало- и глюкокортикоидов. В этих случаях развивается так называемый адрено-генитальный синдром. Синдром наиболее рельефно с клинической точки зрения проявляет себя у носителей генотипа 46, ХХ, то есть у девочек. У детей может уже в период внутриутробного развития произойти вирилизация наружных половых органов, что означает «омужествление»: гипертрофируется клитор, большие половые губы, они становятся похожими на мошонку. Становится трудным определение пола у новорожденных. Как указано выше, некоторые формы адрено-генитального синдрома сопровождаются недостатком минералокортикоидов и развивается синдром потери солей натрия с мочой и неукротимой рвотой. Дети резко обезвоживаются и быстро погибают без оказания помощи. В более старшем возрасте (от 3 лет до 8 у девочек и от 3 лет до 11 лет у мальчиков) проявлениями адрено-генитального синдрома может быть все та же вирилизация у девочек и преждевременное половое созревание с
формированием вторичных половых признаков и преждевременным вступлением в работу половых желез как у девочек, так и у мальчиков.
studfiles.net
Заболевания эндокринной системы у детей
Кривая заболеваний эндокринной системы в 21 веке резко поползла вверх. И заболевания желез внутренней секреции у детей стали также встречаться все чаще.
К железам внутренней секреции относятся следующие органы
- гипофиз
- эпифиз
- щитовидная железа
- паращитовидные железы
- вилочковая железа
- надпочечники
- поджелудочная железа
- половые железы
Эндокринная система у детей закладывается в первые 3 месяца материнской беременности. Все эти органы и железы выделяют свои гормоны сразу в кровь и лимфу и действуют на все системы организма, так как находятся в тесной взаимосвязи с центральной нервной системой и друг с другом. Вот эта взаимосвязь и оказывается влияние на рост, умственное и физическое развитие ребенка, на все виды обмена.
Более подробно об анатомо-физиологических особенностях эндокринной системы у детей мы поговорим в другой статье. Но в разные периоды жизни происходит превалирование функций какой-то одной железы, в то время как другие железы продолжают совершенствоваться. Развитие эндокринных желез в детском возрасте могут быть причиной патологии у взрослого, если в растущем организме произойдут какие-либо расстройства.
Причины патологии эндокринных желез.
Общие причины – это наследственная предрасположенность, стрессы, инфекция, неправильное питание
В этом разделе мы рассмотрим наиболее часто встречающиеся заболевания эндокринной системы у детей, их причины, симптоматику и современные методы лечения.
Сахарный диабет
Несахарный диабет
Синдром Бабинского-Фрелиха
Синдром Русселя
Липодистрофическая мышечная дистрофия
Гипофизарный нанизм
Преждевременное половое развитие
Гипогонадизм
Болезнь Иценко-Кушинга
Аддисонова болезнь
Врожденный адреногенитальный синдром
Гипотиреоз
Гипертиреоз
Эндемический зоб
Тиреоидиты
Заболевания вилочковой железы
Лечение эндокринных болезней у ребенка.
Терапия эндокринных болезней очень сложная задача, ведь наряду с железами внутренней секреции будут поражаться и другие системы. Поэтому для лечения необходима консультация многих специалистов, помимо эндокринолога. Только комплексный подход способен оздоровить ребенка.
Большую роль играет диета, в современное время используют гормонотерапию, но ее должен назначать только знающий специалист. Осторожно надо подходить и лучевой терапии. Лечение эндокринной патологии должно проводиться в специализированных клиниках.
www.wp-german-pediatria.ru
Эндокринная система у детей — Med24info.com
Эндокринная система является основным регулятором роста и развития организма. К ней относятся гипофиз, эпифиз, щитовидная, паращитовидная, поджелудочная, вилочковая, надпочечники и половые железы. Часть из них функционирует уже внутриутробно. Огромное влияние на рост и развитие ребенка оказывают гормоны материнского организма, которые он получает внутриутробно и с молоком матери при грудном вскармливании.
Отмечается различное влияние определенных эндокринных желез в определенные возрастные периоды. Первой усиленно начинает функционировать в возрасте 5-6 месяцев щитовидная железа, ведущая роль которой отмечается до 2-2,5 лет. К 6-7 годам усиливается действие передней доли гипофиза. В препубертатном периоде отмечается повышенная деятельность щитовидной железы и гипофиза. В препубертатном и пубертатном периоде основное влияние на рост и развитие организма оказывают гормоны половых желез.
В основе заболеваний эндокринной системы лежит нарушение гормональной активности (гипер- или гипофункция) отдельных или нескольких эндокринных желез, что может быть обусловлено генетическими (в частности, хромосомными) нарушениями, воспалительными изменениями, расстройствами кровообращения, иммунными нарушениями и др.
Гипофиз является одной из основных желез эндокринной системы, которая влияет на структуру и функцию щитовидной железы, надпочечников и половых желез. Гипофиз делится натри доли, которые вырабатывают определенные гормоны.
В передней доле гипофиза образуются:
- соматотропный гормон — гормон роста, участвует в белковом обмене. Недостаток этого гормона приводит к карликовости, а переизбыток приводит к гигантизму;
- тиреотропный гормон стимулирует рост и функцию щитовидной железы, повышает ее
секреторную функцию, накопление железой йода, синтез и выделение ее гормонов; - адренокортикотропный гормон влияет на кору надпочечников, стимулирует выработку кортикостероидных гормонов, регулирует углеводный обмен;
- гонадотропные гормоны стимулируют функции половых желез;
- фолликулостимулирующий гормон стимулирует рост и созревание фолликулов у женщин, в мужском организме способствует росту и развитию семяобразующих канальцев и сперматогенезу;
- лютеинизирующий гормон стимулирует продукцию мужских гормонов (андрогенов) у мужчин, способствует образованию яйцеклетки и процессу ее выхода из яичников;
- лактогенный гормон у женщин воздействует на молочную железу, способствуя лактации, а у мужчин — росту предстательной железы;
- меланоформный гормон регулирует образование пигмента в коже;
- липотропный гормон стимулирует использование жира в энергетическом обмене организма.
В задней доле гипофиза образуются:
- антидиуретический гормон (вазопрессин) — регулирует водный обмен в организме.
Недостаток антидиуретического гормона приводит к развитию несахарного диабета.
- окситоцин влияет на уровень артериального давления, половое развитие, белковый и жировой обмен, сокращение мышцы матки в период родов.
Эпифиз вырабатывает гормоны, влияющие на половой цикл, лактацию, углеводный и водно-электролитный обмен.
Щитовидная железа закладывается уже на 1-м месяцев внутриутробного развития. К 4 месяцу внутриутробной жизни она вполне сформирована структурно и достаточно функционально активна, но ее рост, формирование и интенсивное увеличение массы идут до 5-6-летнего возраста. Новое нарастание размеров и массы наступает в период полового созревания.
Щитовидная железа — это самый крупный орган эндокринной системы человека. Гормоны, вырабатываемые в ней — трийодтиронин (Т ), тироксин (Т ),
тиреокальцитонин, — играют большую роль в регуляции различных обменных процессов в организме, влияя также на функции других систем организма — сердечно-сосудистой, пищеварительной и др.
При несвоевременном назначении заместительной терапии или отказе от ее приема заболевания щитовидной железы протекают тяжело.
Основными клиническими проявлениями заболеваний щитовидной железы являются нарушения со стороны нервно-психического состояния больных.
Тироксин и трийодтиронин являются универсальными стимуляторами обмена веществ, роста и нервно-психического развития. В то же время недостаточность щитовидной железы у плода не может сказаться существенно на его развитии, в связи с тем, что через плаценту к нему хорошо поступают тиреоидные гормоны, за исключением тиреостимулирующего.
Тиреокальцитонин регулирует нормальный уровень кальция в крови и процесс отложения его в костной ткани.
Паращитовидные железы синтезируют иаратгормон, который вместе с витамином D имеет большое значение в регуляции фосфорно-кальциевого обмена.
Вилочковая железа (тимус) активно функционирует до 2-х лет, а затем постепенно начинается ее обратное развитие (инволюция). Она располагается в передне-верхней части средостенья, сразу за грудиной. Тимус является центральным органом иммунитета, в котором образуются Т-лимфоциты, осущес вляющие защитную функцию организма от инфекционных агентов. В вилочковой железе вырабатываются гормоны тимозин, тимопоэтин, тимический фактор и др. Деятельность вилочковой железы тесно связана с деятельностью половых желез, надпочечников и щитовидной железы. Доказано участие вилочковой железы в контроле за деятельностью углеводного и кальциевого обмена, нервно-мышечной передачей импульсов.
Надпочечники
В надпочечниках различают два слоя, или вещества: корковое и мозговое. Их функции разнообразны.
В корковом веществе образуются кортикостероидные гормоны, среди которых наибольшее значение имеют:
- глюкокортикоиды (гидрокортизон, кортикостерон) регулируют углеводный, белковый, жировой обмен, обладают выраженным противовоспалительным, противоаллергическим и иммуносупрессивным действием, поддерживают на определенном уровне артериальное давление, стимулируют выработку соляной кислоты и пепсина в желудке;
- минералкортикоиды (альдостерон) участвуют в регуляции водно-солевого обмена и метаболизме углеводов, повышаюттонус сосудов;
- андрогены (мужские половые гормоны) влияют на формирование наружных половых органов и вторичных мужских половых признаков, усиливают синтез белка.
В мозговом слое надпочечников вырабатываются адреналин и норадреналин, которые оказывают влияние на повышение уровня артериального давления, регулируют тонус мышечных клеток сосудов и внутренних органов, передачу нервных импульсов, участвуют в белковом и углеводном обмене.
Кора надпочечников в функциональном отношении тесно связана с адренокортикотропным гормоном гипофиза, половыми и другими эндокринными железами.
Снижение функции надпочечников возможно при лимфатико-гипопластическом диатезе, кровоизлияниях, опухолевых процессах, туберкулезе, токсических воздействиях.
Поджелудочная железа
К моменту рождения ребенка гормональный аппарат развит анатомически и обладает достаточной секреторной функцией.
Внутрисекреторная функция осуществляется островками Лангерганса, содержащими секреторные клетки, продуцирующие гормоны:
- Р-клетки продуцируют инсулин, который способствует утилизации глюкозы в тканях, усиливает синтез белков, жиров, нуклеиновых кислот;
- а-клетки вырабатывают глюкагон, который стимулирует распад гликогена в печени, вызывая повышение уровня глюкозы в крови;
- D-клетки выделяют соматостатин, подавляющий секрецию основных гормонов
гипофиза (соматотропного и адренокортикотропного, щитовидной железы и др.
Эндокринная функция поджелудочной железы связана с действием гипофиза, щитовидной железы и надпочечников. Важная роль в ее деятельности принадлежит нервной системе.
Снижение продукции инсулина приводит к развитию сахарного диабета.
Внешнесекреторная функция поджелудочной железы обеспечивает выделение пищеварительных ферментов: трипсина, амилазы и липазы, которые принимают непосредственное участие в процессе пищеварения.
Половые железы
К половым железам относятся яичники и яички, в которых происходит выработка половых гормонов. Наиболее активно начинают функционировать к периоду полового созревания, они обладают выраженным действием на рост и развитие половых органов, вызывают формирование вторичных половых признаков.
www.med24info.com
Эндокринная система педиатрия. Особенности эндокринной системы у детей под эндокринной
Эндокринная система является основным регулятором роста и развития организма. К ней относятся гипофиз, эпифиз, щитовидная, паращитовидная, поджелудочная, вилочковая, надпочечники и половые железы. Часть из них функционирует уже внутриутробно. Огромное влияние на рост и развитие ребенка оказывают гормоны материнского организма, которые он получает внутриутробно и с молоком матери при грудном вскармливании.
Отмечается различное влияние определенных эндокринных желез в определенные возрастные периоды. Первой усиленно начинает функционировать в возрасте 5-6 месяцев щитовидная железа, ведущая роль которой отмечается до 2-2,5 лет. К 6-7 годам усиливается действие передней доли гипофиза. В препубертатном периоде отмечается повышенная деятельность щитовидной железы и гипофиза. В препубертатном и пубертатном периоде основное влияние на рост и развитие организма оказывают гормоны половых желез.
В основе заболеваний эндокринной системы лежит нарушение гормональной активности (гипер- или гипофункция) отдельных или нескольких эндокринных желез, что может быть обусловлено генетическими (в частности, хромосомными) нарушениями, воспалительными изменениями, расстройствами кровообращения, иммунными нарушениями и др.
Гипофиз является одной из основных желез эндокринной системы, которая влияет на структуру и функцию щитовидной железы, надпочечников и половых желез. Гипофиз делится натри доли, которые вырабатывают определенные гормоны.
В передней доле гипофиза образуются:
- соматотропный гормон — гормон роста, участвует в белковом обмене. Недостаток этого гормона приводит к карликовости, а переизбыток приводит к гигантизму;
- тиреотропный гормон стимулирует рост и функцию щитовидной железы, повышает ее
секреторную функцию, накопление железой йода, синтез и выделение ее гормонов; - адренокортикотропный гормон влияет на кору надпочечников, стимулирует выработку кортикостероидных гормонов, регулирует углеводный обмен;
- гонадотропные гормоны стимулируют функции половых желез;
- фолликулостимулирующий гормон стимулирует рост и созревание фолликулов у женщин, в мужском организме способствует росту и развитию семяобразующих канальцев и сперматогенезу;
- лютеинизирующий гормон стимулирует продукцию мужских гормонов (андрогенов) у мужчин, способствует образованию яйцеклетки и процессу ее выхода из яичников;
- лактогенный гормон у женщин воздействует на молочную железу, способствуя лактации, а у мужчин — росту предстательной железы;
- меланоформный гормон регулирует образование пигмента в коже;
- липотропный гормон стимулирует использование жира в энергетическом обмене организма.
- антидиуретический гормон (вазопрессин) — регулирует водный обмен в организме.
- окситоцин влияет на уровень артериального давления, половое развитие, белковый и жировой обмен, сокращение мышцы матки в период родов.
Щитовидная железа закладывается уже на 1-м месяцев внутриутробного развития. К 4 месяцу внутриутробной жизни она вполне сформирована структурно и достаточно функционально активна, но ее рост, формирование и интенсивное увеличение массы идут до 5-6-летнего возраста. Новое нарастание размеров и массы наступает в период полового созревания.
Щитовидная железа — это самый крупный орган эндокринной системы человека. Гормоны, вырабатываемые в ней — трийодтиронин (Т), тироксин (Т),
тиреокальцитонин, — играют большую роль в регуляции различных обменных процессов в организме, влияя также на функции других систем организма — сердечно-сосудистой, пищеварительной и др.
При несвоевременном назначении заместительной терапии или отказе от ее приема заболевания щитовидной железы протекают тяжело.
Основными клиническими проявлениями заболеваний щитовидной железы являются нарушения со стороны нервно-психического состояния больных.
Тироксин и трийодтиронин являются универсальными стимуляторами обмена веществ, роста и нервно-психического развития. В то же время недостаточность щитовидной железы у плода не может сказаться существенно на его развитии, в связи с тем, что через плаценту к нему хорошо поступают тиреоидные гормоны, за исключением тиреостимулирующего.
Тиреокальцитонин регулирует нормальный уровень кальция в крови и процесс отложения его в костной ткани.
Паращитовидные железы синтезируют иаратгормон, который вместе с витамином D имеет большое значение в регуляции фосфорно-кальциевого обмена.
Вилочковая железа (тимус) активно функционирует до 2-х лет, а затем постепенно начинается ее обратное развитие (инволюция). Она располагается в передне-верхней части средостенья, сразу за грудиной. Тимус является центральным органом иммунитета, в котором образуются Т-лимфоциты, осущес вляющие защитную функцию организма от инфекционных агентов. В вилочковой железе вырабатываются гормоны тимозин, тимопоэтин, тимический фактор и др. Деятельность вилочковой железы тесно связана с деятельностью половых желез, надпочечников и щитовидной железы. Доказано участие вилочковой железы в контроле за деятельностью углеводного и кальциевого обмена, нервно-мышечной передачей импульсов.
Надпочечники
В надпочечниках различают два слоя, или вещества: корковое и мозговое. Их функции разнообразны.
В корковом веществе образуются кортикостероидные гормоны, среди которых наибольшее значение имеют:
- глюкокортикоиды (гидрокортизон, кортикостерон) регулируют углеводный, белковый, жировой обмен, обладают выраженным противовоспалительным, противоаллергическим и иммуносупрессивным действием, поддерживают на определенном уровне артериальное давление, стимулируют выработку соляной кислоты и пепсина в желудке;
- минералкортикоиды (альдостерон) участвуют в регуляции водно-солевого обмена и метаболизме углеводов, повышаюттонус сосудов;
- андрогены (мужские половые гормоны) влияют на формирование наружных половых органов и вторичных мужских половых признаков, усиливают синтез белка.
Кора надпочечников в функциональном отношении тесно связана с адренокортикотропным гормоном гипофиза, половыми и другими эндокринными железами.
Снижение функции надпочечников возможно при лимфатико-ги
gcchili.ru
Педиатрия Болезни эндокринной системы у детей
Тема: Педиатрия Болезни эндокринной системы у детей[1]. Важнейший этиологический фактор сахарного диабета у детей
а) переохлаждение
б) перегревание
в) избыточный прием белков
+г) наследственная отягощенность
[2]. Клинические симптомы сахарного диабета у детей
+а) полифагия, полидипсия, полиурия
б) лихорадка, кашель с мокротой
в) боль в пояснице, отеки
г) тахикардия, тремор, экзофтальм
[3]. При сахарном диабете у детей в общем анализе мочи наблюдаются
а) высокая относительная плотность, гематурия
+б) высокая относительная плотность, глюкозурия
в) низкая относительная плотность, бактериурия
г) низкая относительная плотность, лейкоцитурия
[4]. Недиагностированный сахарный диабет у детей ведет к развитию комы
+а) гипергликемической (диабетической)
б) гипогликемической
в) печеночной
г) уремической
[5]. Передозировка инсулина при лечении сахарного диабета у детей ведет к развитию комы
а) гипергликемической (диабетической)
+б) гипогликемической
в) печеночной
г) уремической
[6]. Накрахмаленные пеленки у детей грудного возраста наблюдаются при
а) гломерулонефрите
б) пиелонефрите
+в) сахарном диабете
г) гипотиреозе
[7]. Накрахмаленные пеленки у детей грудного возраста определяются из-за отложения на них кристаллов
а) белка
+б) сахара
в) оксалатов
г) фосфатов
[8]. При сахарном диабете у детей на коже появляется
+а) фурункулез
б) желтуха
в) анулярная эритема
г) акроцианоз
[9]. Для выявления скрытого сахарного диабета у детей проводится
а) общий анализ мочи
б) общий анализ крови
в) анализ мочи по Нечипоренко
+г) тест толерантности к глюкозе
[10]. Гликемический и глюкозурический профиль исследуют детям при диагностике
а) болезни Дауна
б) пиелонефрита
+в) сахарного диабета
г) фенилкетонурии
[11]. Для диагностики диабетической ретинопатии у детей необходима консультация
а) гематолога
+б) окулиста
в) хирурга
г) фтизиатра
[12]. Для определения уровня глюкозы в крови ребенка следует направить в лабораторию
а) через 10 мин. после еды
б) через 20 мин. после еды
в) через 30 мин. после еды
+г) натощак
[13]. Гликемия натощак у детей в норме составляет (ммоль/л)
+а) 3,3-5,5
б) 5,5-7,7
в) 7,7-9,9
г) 9,9-11,11
[14]. Глюкотест используется для определения
а) ацетона в моче
б) ацетона в крови
+в) сахара в моче
г) сахара в крови
[15]. Диета № 9 назначается детям при
а) бронхиальной астме
б) ревматизме
в) пиелонефрите
+г) сахарном диабете
[16]. При лечении сахарного диабета у детей из питания исключают
а) нежирное мясо
б) кефир
в) гречневую крупу
+г) конфеты
[17]. При лечении сахарного диабета у детей в питании разрешается
а) банан
б) виноград
+в) свекла
г) хурма
[18]. При лечении сахарного диабета у детей сахар заменяют
+а) фруктозой
б) медом
в) вареньем
г) конфетами
[19]. При лечении сахарного диабета у детей используют инсулин короткого действия
+а) актрапид
б) инсулонг
в) ультраленте
г) ультралонг
[20]. При лечении сахарного диабета у детей используют инсулин длительного действия
а) актрапид
б) инсулрап
в) хоморап
+г) ультралонг
[21]. При лечении сахарного диабета у детей рекомендуется растение, усиливающее действие инсулина
а) алтей
б) валериана
в) пустырник
+г) черника
[22]. При проведении инсулинотерапии ребенок должен поесть через
а) 15-20 минут до инъекции
б) 30-40 минут до инъекции
+в) 15-20 минут после инъекции
г) 30-40 минут после инъекции
[23]. Инсулин необходимо хранить при температуре (?С)
+а) от +4 до +6
б) от -6 до -4
в) от +10 до +12
г) от -10 до +12
[24]. Липодистрофия развивается при подкожном введении
а) димедрола
б) кордиамина
в) гепарина
+г) инсулина
[25]. Запах ацетона в выдыхаемом воздухе появляется при коме
+а) гипергликемической
б) гипогликемической
в) печеночной
г) уремической
[26]. После инъекции инсулина у ребенка появились чувство голода, потливость, тремор. Это
а) гипергликемическая кома
+б) гипогликемическая кома
в) первый период лихорадки
г) третий период лихорадки
[27]. При гипотиреозе отмечается функциональная недостаточность железы
а) поджелудочной
+б) щитовидной
в) гипофиза
г) вилочковой
[28]. Йод необходим для выработки гормонов
а) инсулина
б) тестостерона
+в) тироксина, трийодтиронина
г) тиреотропного
[29]. Для врожденного гипотиреоза характерны
а) гипервозбудимость, тремор конечностей
б) опережение физического и нервно-психического развития
в) преждевременное половое развитие
+г) задержка физического и нервно-психического развития
[30]. Тест толерантности к глюкозе проводится при диагностике
+а) гипотиреоза
б) скрытого сахарного диабета
в) явного сахарного диабета
г) фенилкетонурии
[31]. Новорожденным проводят скрининг-тест для выявления
а) тиреотоксикоза
+б) врожденного гипотиреоза
в) сахарного диабета
г) адреногенитального синдрома
[32]. К группе риска по сахарному диабету относятся
+а) дети с наследственной отягощенностью
б) недоношенные
в) с аномалией конституции
г) с гипотрофией
[33]. Замедленные движения, одутловатость лица, гипотермия, запоры, ухудшение памяти и ухудшение успеваемо-сти в школе характерны для детей, страдающих
а) эутиреоидной гиперплазией щитовидной железы
б) диффузным токсическим зобом
+в) приобретенным гипотиреозом
г) гиповитаминозом В6
[34]. Сердцебиение, дрожь тела, повышенная потливость, эмоциональная лабильность, потеря массы тела при по-вышенном аппетите характерны для детей, страдающих
+а) диффузным токсическим зобом
б) гипотиреозом
в) гиповитаминозом В1
г) гиповитаминозом В6
[35]. При лечении сахарного диабета инсулин вводится
а) внутривенно
б) внутримышечно
+в) подкожно
г) внутрикожно
d.120-bal.ru
Педиатрия эндокринные заболевания у детей. Симптомы эндокринных нарушений. Диагностика эндокринных заболеваний у ребёнка
Большинство эндокринных органов недоступно для непосредственного обследования, за исключением щитовидной и половых желез, поэтому о состоянии желез внутренней секреции чаще приходится судить по клиническим синдромам, которые характерны для гипер- или гипофункции пораженной железы, и показателям гомеостаза.
Клиническое обследование эндокринной системы у детей состоит из изучения жалоб, анамнеза болезни и жизни ребенка, включая генетические особенности семьи, проведения объективного обследования всех органов и систем ребенка, оценки данных дополнительных методов исследования.
Общий осмотр больного
При внешнем осмотре ребенка обращается внимание на пропорциональность телосложения. Затем проводится оценка физического развития ребенка , на основании чего можно выявить расстройства роста. Оценка физического развития у детей:
Учитывая наблюдающееся варьирование различных показателей физического развития ребенка, нужно знать так называемое нормальное, или гаусс-лапласовское распределение. Характеристиками этого распределения являются средняя арифметическая величина признака или показателя (М) и величина среднего квадратического отклонения, или сигмы (δ). Величины, выходящие за пределы М ± 2δ стандарта для здоровых детей, как правило, свидетельствуют о патологии.
В практике сохраняют свое значение ориентировочные оценки, при которых следует использовать следующее эмпирическое правило: случайное варьирование признака, изменяющегося с возрастом, обычно не выходит за рамки одного возрастного интервала; значение признака, возможно, носит патологический характер в том случае, если его величина находится в интервале + 1-2 возрастных интервалов. Возрастные интервалы в таблицах стандартов обычно выбираются следующие: от рождения до одного года интервал равен месяцу, от 1 года до 3 лет — 3 месяцам, от 3 до 7 лет – 6 месяцам, от 7 до 12 лет — одному году.
Для точных определений показателей физического развития педиатр должен пользоваться таблицами (или кривыми) возрастного центильного распределения. Практическое использование этих таблиц (графиков) исключительно просто и удобно. Колонки центильных таблиц или кривые графикой показывают количественные границы признака у определенной доли или процента (центиля) детей данного возраста и пола. При этом за средние или условно нормальные величины принимаются значения, свойственные половине здоровых детей данного возраста и пола — в интервале от 25-го до 75-го центиля.
Для гипофизарного нанизма характерно замедление темпов роста без изменения пропорций тела. О карликовости можно думать, если рост ребенка отстает от долженствующего и выходит за пределы М-3δ (в сигмальном ряду), ниже границ 3-го центиля (в центильных таблицах) или SDS
При гипотиреозе имеет место отставание в росте с наруше
radzo.ru
