Субинволюция матки. Что такое Субинволюция матки?
ВАЖНО
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Субинволюция матки – послеродовое осложнение, характеризующееся замедлением восстановления нормальных (дородовых) размеров матки. Симптомами являются обильные кровянистые выделения бурого цвета, субфебрильная температура тела, отсутствие обычных схваткообразных болей при кормлении грудью. Наличие осложнения определяют посредством гинекологического осмотра, ультразвуковых исследований (УЗИ матки, трехмерная эхография). Лечение комплексное, включающееся в себя гормональные препараты – стимуляторы сокращения миометрия, антибиотики или противовирусные средства. Для стимуляции инволюции удаляют сгустки крови из матки, производят гинекологический массаж.
МКБ-10
N85.3 Субинволюция матки
- Причины субинволюции матки
- Патогенез
- Классификация
- Симптомы субинволюции матки
- Осложнения
- Диагностика
- Лечение субинволюции матки
- Прогноз и профилактика
- Цены на лечение
Общие сведения
Приставка «суб» в термине «субинволюция» обозначает неполную или частичную инволюцию (восстановление) матки после родов. Является достаточно частым послеродовым осложнением – оно регистрируется у 1-2% рожениц, а среди всех патологий после родов его доля составляет 30-50%. Существует научная дискуссия относительно того, считать ли это состояние отдельной нозологической единицей. Многие специалисты относят его к первым проявлениям послеродового эндометрита – к группе инфекционных осложнений после родов. Согласно иной точке зрения, субинволюция является самостоятельным заболеванием, вызывается бактериальной или вирусной инфекцией и практически всегда приводит к эндометриту.
Субинволюция матки
Причины субинволюции матки
Общепризнанная в акушерстве точка зрения непосредственной причиной развития патологии называет инфекционное воспаление бактериальной или вирусной природы. Но само наличие инфекции не гарантирует развитие осложнения, поэтому выделяют ряд предрасполагающих факторов. Степень их влияния различается у разных женщин, что затрудняет выявить четкую корреляцию. Выделяют следующие обстоятельства, способствующие развитию такого послеродового состояния:
- Задержка частей последа. Оставшиеся в полости матки фрагменты плаценты, плодного пузыря или сгустки крови практически всегда обнаруживают при субинволюции. Считается, что это состояние облегчает инфицирование половых органов с развитием эндометрита и замедлением восстановления матки.
- Патологии беременности. Многоводие, крупный плод, многоплодие являются предрасполагающими факторами к развитию такого осложнения.

- Аномалии родов. Затяжные или стремительные роды являются фактором риска возникновения данного осложнения в послеродовый период.
- Конституциональные особенности женщины. Существует мнение, что пониженная сократительная активность миометрия обусловлена генетическими и индивидуальными особенностями женского организма. У таких женщин вероятность появления этого послеродового осложнения в несколько раз выше.
Помимо вышеперечисленных предрасполагающих факторов, некоторыми исследователями отмечается повышенная частота развития субинволюции на фоне миомы матки, юного (менее 18 лет) или старшего репродуктивного (более 40 лет) возраста роженицы. Отсутствие кормления грудью на протяжении первых 4-5-ти дней после рождения ребенка увеличивает вероятность появления такого осложнения – это связано с отсутствием гормональной стимуляции при естественном вскармливании. Свою роль может сыграть неправильное расположение матки, нарушения ее связочного аппарата, анемия и системные заболевания.
Свою роль может сыграть неправильное расположение матки, нарушения ее связочного аппарата, анемия и системные заболевания.
Патогенез
Главную роль в патогенезе субинволюции матки играют несколько факторов – снижение сократительной активности миометрия, длительное сохранение послеродового отека тканей, замедление лизиса коллагеновых волокон. Сокращение мышечных волокон замедляется в результате их перерастяжения в процессе беременности или из-за слабой нейрогуморальной стимуляции. Такой механизм является ведущим при истинных формах осложнения. Снижение сократительной способности не только замедляет восстановление, но и косвенно облегчает проникновение инфекции на поврежденную поверхность эндометрия, приводя к эндометриту.
Обратное развитие внутренних половых органов в норме происходит не только за счет сокращения мышечного слоя, но и по причине снижения отека тканей. В первый период после родов поверхность эндометрия имеет раневой характер, однако в течение 4-10 суток происходит ее заживление со снижением отечности за счет спазма и «скручивания» кровеносных сосудов.
Классификация
В акушерской практике существует несколько типов классификации субинволюции, но большинство из них не получили широкого распространения. Сложность классификации обусловлена рядом обстоятельств – обилием механизмов развития состояния, отсутствием достоверных данных о роли сопутствующих патологий (поздних гестозов, воспалений органов мочеполовой системы). Поэтому используется лишь один тип классификации данного послеродового осложнения, в основе которого – непосредственные причины возникновения патологии:

- Миогенный подтип. Медленная инволюция обусловлена в основном перерастяжением или слабостью миометрия. Данное состояние наблюдается после беременности, протекавшей с многоводием, крупным плодом, при стремительных или затяжных родах.
- Микроциркуляторный подтип. Причина заболевания такого типа заключается в медленном восстановлении кровеносной сети матки и сохранении отечности тканей. При этом патологию может спровоцировать поздний гестоз, недостаточное опорожнение мочевого пузыря и прямой кишки перед родами.
- Эндокринный подтип. Возникает при недостаточной нейрогуморальной стимуляции половой системы после родов. Может быть обусловлен как эндокринными патологиями, так и отсутствием грудного вскармливания на протяжении первых нескольких суток жизни ребенка.
 Обусловлен воспалительными процессами, вызванными вирусными или бактериальными возбудителями, в том числе, условно-патогенной флорой. Риск развития осложнения повышается при наличии очагов инфекции в организме (пиелонефрит, цистит), задержке остатков последа в полости матки.
Обусловлен воспалительными процессами, вызванными вирусными или бактериальными возбудителями, в том числе, условно-патогенной флорой. Риск развития осложнения повышается при наличии очагов инфекции в организме (пиелонефрит, цистит), задержке остатков последа в полости матки.Симптомы субинволюции матки
Первым симптомом заболевания выступает наличие кровянистых выделений (лохий), нередко обильных, бурого цвета. Патогномоничным признаком является сохранение кровотечений вплоть до позднего послеродового периода (3-4 недели). Косвенным симптомом патологии акушеры признают отсутствие схваткообразных болей внизу живота при кормлении ребенка грудью. Иногда могут регистрироваться тянущие болевые ощущения, не связанные с режимом кормления или другими внешними факторами. Наличие этих проявлений в сочетании с предрасполагающими факторами в анамнезе указывает на наличие нарушения.
Инфекционный тип заболевания имеет черты послеродового эндометрита – развивается озноб (в тяжелых случаях — лихорадка), температура тела колеблется от субфебрильных до высоких (39-40°С) значений. Изменение характера лохий от кровянистого к гнойному указывает на развитие тяжелого воспаления внутренней оболочки матки. Наблюдается болезненность передней брюшной стенки, тахикардия, симптомы общей интоксикации – головные боли, слабость, тошнота. Выраженность симптомов в этом случае зависит от характера возбудителя, реактивности организма женщины и ряда других обстоятельств.
Изменение характера лохий от кровянистого к гнойному указывает на развитие тяжелого воспаления внутренней оболочки матки. Наблюдается болезненность передней брюшной стенки, тахикардия, симптомы общей интоксикации – головные боли, слабость, тошнота. Выраженность симптомов в этом случае зависит от характера возбудителя, реактивности организма женщины и ряда других обстоятельств.
Осложнения
Любой тип субинволюции матки без должного лечения рано или поздно приводит к инфекционным осложнениям – эндометриту или эндомиометриту. Даже при истинном типе осложнения признаки инфекционного воспаления отсутствуют только поначалу, но замедление восстановления органов репродуктивной системы делает их уязвимыми перед болезнетворной микрофлорой, в т. ч. и условно-патогенной. Эндометрит может осложняться сепсисом, перитонитом, септическим шоком и другими процессами инфекционного характера. Реже это состояние может приводить к метротромбофлебитам, эмболии сосудов внутренних половых органов, тяжелым маточным кровотечениям.
Диагностика
Акушеры-гинекологи уже на этапе беременности определяют среди женщин группу риска, у которой с большей вероятностью возможно развитие субинволюции. К ней относят беременных с многоводием, миомой, крупным плодом, инфекционными и воспалительными патологиями мочеполовой системы, выраженными признаками гестоза. Такие женщины нуждаются в особом контроле в послеродовом периоде для своевременного выявления осложнений и начала их лечения. Для диагностики состояния применяют спектр акушерских исследований и общеклинических анализов:
- Консультация врача-акушера. Специалист проводит расспрос, в его ходе определяет характер, объемы и длительность лохий, наличие или отсутствие субъективных симптомов. На основании полученных данных врач назначает ряд дополнительных диагностических процедур.
- Осмотр на кресле. Бимануальное исследование обнаруживает увеличение матки (не соответствие сроку после родов), грушевидно-шаровидную форму органа.
 Эластично-мягкая консистенция свидетельствует о наличии в родовых путях остатков последа. При осмотре зеркалами определяется отек и багровость шейки, цервикальный канал увеличен (легко проходят 1-2 пальца), в его полости выявляют сгустки крови.
Эластично-мягкая консистенция свидетельствует о наличии в родовых путях остатков последа. При осмотре зеркалами определяется отек и багровость шейки, цервикальный канал увеличен (легко проходят 1-2 пальца), в его полости выявляют сгустки крови. - Ультразвуковые исследования. Для диагностики осложнения применяют трансабдоминальное и трансвагинальное УЗИ органов малого таза, трехмерную эхографию. Определяется высокое стояние дна матки, не соответствующее послеродовому сроку, утолщение ее стенок. Эхография позволяет точно определить наличие инородных тел и остатков последа в маточной полости.
- Гистероскопия. Эндоскопическое изучение внутренней полости матки нередко позволяет выявить признаки субинволюции и эндометрита еще до разгара клинических проявлений. Помимо осмотра, методика делает возможным производить забор образцов эндометрия, лохий, остатков последа для более точной диагностики.
При инфекционной форме заболевания или присоединении осложнений в качестве диагностических процедур также назначают клинические анализы крови и мочи, иногда проводят посев микрофлоры влагалища или матки (при эндометрите) для определения возбудителя. В крови обнаруживают характерные для воспалительных процессов изменения – повышение СОЭ, лейкоцитоз, анемию. В последние годы для диагностики используют также томографический метод – МРТ органов малого таза. Он позволяет точно определить размеры и структуру матки и выявить даже мельчайшие патологические включения в ее полости.
В крови обнаруживают характерные для воспалительных процессов изменения – повышение СОЭ, лейкоцитоз, анемию. В последние годы для диагностики используют также томографический метод – МРТ органов малого таза. Он позволяет точно определить размеры и структуру матки и выявить даже мельчайшие патологические включения в ее полости.
Лечение субинволюции матки
Терапия состояния комплексная, включающая в себя медикаментозные, инструментальные и массажные процедуры. Большую роль в эффективности лечебных мер играет определение типа заболевания, а при его инфекционном характере — вида возбудителя. Длительность лечения зависит от выраженности симптомов патологии и наличия или отсутствия сопутствующих заболеваний, которые могут оказывать влияние на органы репродуктивной системы женщины. Эффективная терапия субинволюции включает в себя такие препараты и методы лечения:
- Гормональные средства. Сокращение матки после родов в норме происходит под воздействием гормона окситоцина.
 Поэтому для ускорения этого процесса применяют гормональные препараты, влияющие на миометрий и его сосуды – окситоцин, метилэргометрил и другие.
Поэтому для ускорения этого процесса применяют гормональные препараты, влияющие на миометрий и его сосуды – окситоцин, метилэргометрил и другие. - Антибактериальная терапия. Чаще всего причиной инфекции в послеродовом периоде выступает бактериальная микрофлора. Для ее устранения применяют антибиотики широкого спектра действия. Если в рамках диагностики удалось определить тип возбудителя – проводят антибиотикотерапию наиболее подходящим в этом случае препаратом.
- Удаление включений в матке. Остатки последа и сгустки крови облегчают инфицирование и сами по себе могут выступать причиной воспаления. Их устраняют методом вакуум-аспирации или посредством кюретажа полости матки.
- Гинекологический массаж. Способен улучшать сократительные свойства миометрия и ускорять восстановление репродуктивной системы после родов.
- Общережимные мероприятия. Женщине при субинволюции матки показан постельный режим, отсутствие физических нагрузок и эмоциональных стрессов.
 Регулярное прикладывание новорожденного к груди также способствует сокращению миометрия.
Регулярное прикладывание новорожденного к груди также способствует сокращению миометрия.
Прогноз и профилактика
Субинволюция матки до развития тяжелых инфекционных осложнений хорошо отзывается на лечебные мероприятия и устраняется на протяжении нескольких недель, поэтому имеет относительно благоприятный прогноз. Развитие на этом фоне эндометрита и других воспалительных состояний чревато более серьезными последствиями – возникновением сепсиса, инфицированием других органов и систем (брюшной полости, мочевыделительных путей). Акушеры рекомендуют проводить профилактические мероприятия женщинам, беременность и роды которых проходили с осложнениями (многоводие, стремительные роды). Они заключаются в назначении гормональных препаратов для ускорения инволюции в первые дни после рождения ребенка вне зависимости от наличия симптомов замедления восстановления матки.
Вы можете поделиться своей историей болезни, что Вам помогло при лечении субинволюции матки.
Источники
- Настоящая статья подготовлена по материалам сайта: https://www.krasotaimedicina.ru/
ВАЖНО
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Основные признаки субинволюции матки, лечение, профилактика и прогноз — клиника «Добробут»
Главная
Медицинская библиотека Добробут
Дата публикации: 2019-09-29
Дифференциальный диагноз и лечение субинволюции матки
Инволюция матки – физиологический процесс, во время которого происходит обратное развитие матки. Субинволюция – патология, сопровождающаяся замедлением восстановления нормальных размеров детородного органа. Основные признаки субинволюции матки – обильные выделения бурого цвета, субфебрильная температура, отсутствие схваткообразных болей при кормлении ребенка грудью. Специалисты считают это состояние самостоятельным заболеванием, причиной которого стала инфекция. Без надлежащего лечения субинволюция может осложниться эндометритом.
Специалисты считают это состояние самостоятельным заболеванием, причиной которого стала инфекция. Без надлежащего лечения субинволюция может осложниться эндометритом.
Причины послеродовой субинволюции матки:
- крупный плод, многоплодие;
- стремительные (затяжные) роды;
- миома матки;
- анатомические особенности;
- инфекция.
Кроме того, субинволюция матки после родов может быть обусловлена тяжелыми хроническими заболеваниями (туберкулез, сахарный диабет, патология щитовидной железы), возрастом женщины (старше 40 лет и младше 18), болезнями соединительной ткани, общим истощением организма.
Классификация
В зависимости от причины специалисты выделяют два типа патологического состояния: первичный и инфекционный.
Первичный встречается довольно редко и подразделяется на три подгруппы:
- миогенный – чаще всего встречается при многоводии и стремительных (затяжных) родах.
 Причина – слабость миометрия;
Причина – слабость миометрия; - микроциркулярный – диагностируется при позднем гестозе. Причина – отечность тканей и медленное восстановление кровеносной сетки матки;
- эндокринный подтип – обусловлен патологией эндокринной системы и отсутствием грудного вскармливания.
Инфекционный тип вызван вирусными (бактериальными) возбудителями, в том числе условно-патогенной флоры. Риск развития осложнений значительно повышается при наличии в организме очагов инфекции и задержке остатков последа в матке.
Во время консультации врач даст клинические рекомендации при субинволюции матки после кесарева и ответит на ваши вопросы. Запись на нашем сайте Добробут.ком и по телефону.
Симптомы субинволюции матки после родов
Основным симптомом считается наличие обильных кровянистых выделений бурого цвета на протяжении трех недель после родов. Также женщина может жаловаться на обильное потоотделение, озноб и субфебрильную температуру. Косвенным симптомом субинволюции матки после родов врачи считают отсутствие схваткообразных болей при кормлении грудью.
Инфекционный тип субинволюции матки протекает более тяжело. Клинические проявления – обильные гнойные выделения, тахикардия, озноб, повышенная температура, болезненность внизу живота, симптомы общей интоксикации.
Осложнения:
- эндометрит, эндомиометрит;
- перитонит;
- сепсис, септический шок;
- метротромбофлебит;
- маточные кровотечения.
Об особенностях субинволюции матки после аборта специалист расскажет в частной беседе.
Диагностика
Врачи изначально определяют группу риска, наиболее подверженных развитию субинволюции женщин. Особое внимание уделяется беременным с многоводием и крупным плодом, женщинам с миомой и поздним гестозом, а также пациенткам с инфекционными и воспалительными заболеваниями мочеполовой системы.
Диагноз ставится после осмотра женщины на кресле, УЗИ, МРТ органов малого таза и гистероскопии. При подозрении на инфекционный тип в обязательном порядке назначается общий анализ крови и мочи, а также посев микрофлоры для определения возбудителя. Крайне важно дифференцировать субинволюцию матки от пельвиоперитонита и аппендицита.
Крайне важно дифференцировать субинволюцию матки от пельвиоперитонита и аппендицита.
Так ли необходим окситоцин при субинволюции матки
Лечение патологии должно быть комплексным. Помимо лекарственных препаратов специалисты рекомендуют массаж и инструментальные методы.
Схема лечения:
- антибиотики и гормоны;
- общеукрепляющая терапия;
- гинекологический массаж;
- инструментальное удаление сгустков крови и отдельных включений.
Кроме того, женщине рекомендован постельный режим, отсутствие эмоциональных и физических нагрузок. Регулярное прикладывание малыша к груди также поможет сокращению миометрия.
Окситоцин при субинволюции матки играет важную роль, поскольку способствует более быстрому сокращению матки, останавливает кровотечение после родов и восстанавливает сократительную активность матки.
Профилактика и прогноз
Профилактика субинволюции матки заключается в выполнении специальных упражнений во время беременности, способствующих хорошему сокращению матки, в своевременном лечении хронических заболеваний мочеполовой системы, рациональном питании и контроле за весом. Женщинам, входящим в группу риска, акушеры-гинекологи в целях профилактики в первые дни после родов назначают гормональные препараты для ускорения инволюции.
Женщинам, входящим в группу риска, акушеры-гинекологи в целях профилактики в первые дни после родов назначают гормональные препараты для ускорения инволюции.
Если вам нужна консультация специалиста, запишитесь на прием. В центре работают врачи высшей категории с многолетним стажем.
Связанные услуги:
Гинекологическая консультация
Хотите получить онлайн разъяснение от врача МС “Добробут”?
Скачивайте наше приложение Google Play и App Store
Наши врачи
Смотреть всех врачей 746
Наши сертификаты
Сертифікат № QIZ 804 468 C1
Сертифікат № QIZ 804 469 C1
Сертифікат № QIZ 804 470 C1
Сертифікат № QIZ 804 471 C1
Смотреть все сертификаты
Заказать обратный звонок
Введите Ваш телефон
Другие статьи
Последствия многоводия для матери и ребенка. Риск осложнений при родах
Риск осложнений при родах
Что такое многоводие. Причины многоводия. Симптомы острого и хронического многоводия. Многоводие при беременности на поздних сроках. Последствия патологии для матери и ребенка
Что такое целиакия. Причины, симптомы, диагностика и лечение
Непереносимость глютена: причины, роль наследственности, симптомы. Лабораторные методы диагностики. Рекомендации во время лечения больных целиакией: пищевые ограничения. Лечение гормонами.
Что делать, если ребенок проглотил инородное тело – действия родителей
Как правильно действовать, если ребенок проглотил инородное тело. Почему нужно срочно обращаться к врачам, если маленький ребенок проглотил батарейку. Когда можно помогать малышу, а когда стоит дождаться приезда врача
Причины возникновения, симптомы и лечение блефарита
Почему возникает воспаление век. Симптомы блефарита в зависимости от клинической формы. Как вылечить хронический блефарит. Роль антибактериальной терапии, гигиены и укрепления иммунитета.
Симптомы блефарита в зависимости от клинической формы. Как вылечить хронический блефарит. Роль антибактериальной терапии, гигиены и укрепления иммунитета.
Смотреть все статьи
Заказать обратный звонок
Введите Ваш телефон
Субинволюция плацентарной площадки как причина гистерэктомии у молодой женщины
BMJ Case Rep. 2021; 14(2): e238945.
Опубликовано онлайн 2021 февраля 8. doi: 10.1136/bcr-2020238945
, 1 , 2, 3 , 4 и 5
АВТОР информация Заявление об ограничении ответственности
Субинволюция плацентарных площадок (SPS) является редкой, но тяжелой причиной вторичного послеродового кровотечения (PPH). SPS характеризуется аномальным сохранением крупных, расширенных, поверхностно измененных спиральных артерий при отсутствии оставшихся продуктов зачатия. Это важная причина заболеваемости и смертности молодых женщин. В этом исследовании мы представляем случай вторичного послеродового кровотечения у молодой женщины после неосложненного кесарева сечения, которая была признана клинически нестабильной и, наконец, подверглась экстренной тотальной абдоминальной гистерэктомии. Мы рассмотрели литературу с акцентом на патофизиологию этой ситуации. Лечение пациенток с СФС включает консервативную медикаментозную терапию, гистерэктомию и чрескожную эмболотерапию с сохранением фертильности.
В этом исследовании мы представляем случай вторичного послеродового кровотечения у молодой женщины после неосложненного кесарева сечения, которая была признана клинически нестабильной и, наконец, подверглась экстренной тотальной абдоминальной гистерэктомии. Мы рассмотрели литературу с акцентом на патофизиологию этой ситуации. Лечение пациенток с СФС включает консервативную медикаментозную терапию, гистерэктомию и чрескожную эмболотерапию с сохранением фертильности.
Ключевые слова: беременность, репродуктивная медицина
Послеродовое кровотечение (ПРК) является серьезной проблемой во всем мире и до сих пор является основной причиной материнской смертности. 1 Частота послеродового кровотечения составляет примерно 5–20% всех родов, причем большая часть приходится на развивающиеся страны. 1 2 Обычно его делят на две группы: первичный и вторичный ПРК. Первичное послеродовое кровотечение возникает в течение первых 24 часов после родов, тогда как вторичное послеродовое кровотечение возникает между 24 часами и 6 неделями после родов и не особенно связано со способом родоразрешения (вагинальное или кесарево сечение). К причинам первичных ПРК относят атонию матки, задержку плаценты, врожденные или приобретенные нарушения свертывания и травмы. Наиболее частой причиной первичного послеродового кровотечения во всем мире по-прежнему остается атония матки. Вторичные ПРК составляют только 1% всех родов, и их этиология включает тяжелый эндометрит, задержку продуктов зачатия, гестационную трофобластическую болезнь, псевдоаневризму маточной артерии и субинволюцию плацентарной площадки (СПС).
К причинам первичных ПРК относят атонию матки, задержку плаценты, врожденные или приобретенные нарушения свертывания и травмы. Наиболее частой причиной первичного послеродового кровотечения во всем мире по-прежнему остается атония матки. Вторичные ПРК составляют только 1% всех родов, и их этиология включает тяжелый эндометрит, задержку продуктов зачатия, гестационную трофобластическую болезнь, псевдоаневризму маточной артерии и субинволюцию плацентарной площадки (СПС).
СФС определяется как отсроченное или неадекватное физиологическое закрытие и отторжение поверхностных измененных спиральных артерий в плацентарной области (неудачный процесс нормальной инволюции). 3 Об этом впервые в литературе сообщил в 1910 г. Küster, и только в 1945 г. Rutherford и Hertig описали клинические и патологические признаки «неинволюции плацентарного ложа». 4 5 Трудно оценить точную частоту СПС при всех вторичных послеродовых кровотечениях, поскольку для постановки диагноза необходимо гистопатологическое исследование продуктов аспирации после хирургического удаления матки.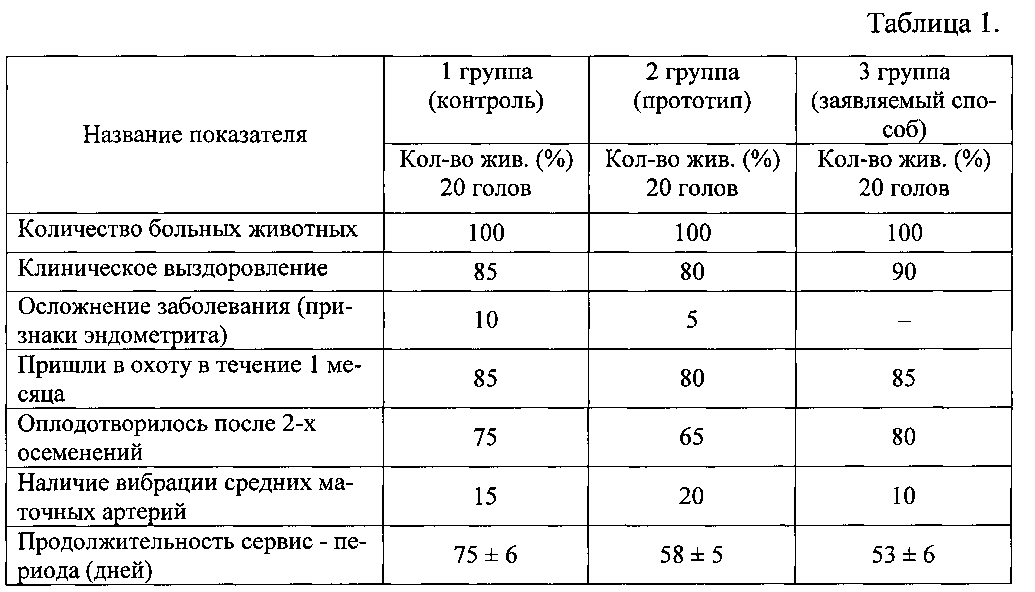 Клиническое лечение СПС требует немедленных действий в короткие сроки из-за тяжести кровотечения. В данном сообщении мы представляем дополнительный случай тяжелого СФС у молодой женщины, перенесшей гистерэктомию, а также обзор литературы.
Клиническое лечение СПС требует немедленных действий в короткие сроки из-за тяжести кровотечения. В данном сообщении мы представляем дополнительный случай тяжелого СФС у молодой женщины, перенесшей гистерэктомию, а также обзор литературы.
34-летняя нерожавшая первобеременная женщина европеоидной расы с нормальной одноплодной беременностью после стимуляции яичников и лечения методом экстракорпорального оплодотворения (ЭКО) из-за плохого овариального резерва поступила на сроке 38+3 недели беременности с признаками родов. Несмотря на хорошие сокращения матки, раскрытие шейки матки через 7 часов составило всего 2 см, и было выполнено кесарево сечение в связи с отсутствием прогрессирования на первом этапе. Послеродовой период протекал гладко, пациентка выписана с рекомендациями на четвертые сутки после операции.
Через три недели ее госпитализировали с сильным вагинальным кровотечением. Трансвагинальное ультразвуковое исследование (УЗИ) выявило возможные организованные тромбы внутри матки. Не было обнаружено эхогенного материала, подозрительного на задержку плаценты в полости эндометрия по данным УЗИ в градациях серого, а цветная допплерография УЗИ была отрицательной для наличия внутреннего сосудистого кровотока. Кроме того, у пациентки не было признаков или симптомов воспаления (эндометрита), лихорадки, озноба, болей в области таза или живота. Общий анализ крови был в норме [гемоглобин (Hb): 12,1 г/дл и тромбоциты: 325 ×10 9 /л, количество лейкоцитов 8,500 × 10 9 /л, СРБ 0,7 мг/л)]. Уровень β-субъединицы гонадотропина ХГЧ (β-ХГЧ) в сыворотке был отрицательным, признаков коагулопатии не было (протромбиновое время, активированное частичное тромбопластиновое время, международное нормализованное отношение (МНО) и уровни фибриногена плазмы были в пределах нормы. Пациент был реанимирован с теплые жидкости и кровь были отправлены на перекрестную совместимость (четыре единицы эритроцитов и четыре единицы свежезамороженной плазмы).Выполнено выскабливание матки, и 150 мл кюретированного материала были отрицательными для задержанных плацентарных продуктов.
Не было обнаружено эхогенного материала, подозрительного на задержку плаценты в полости эндометрия по данным УЗИ в градациях серого, а цветная допплерография УЗИ была отрицательной для наличия внутреннего сосудистого кровотока. Кроме того, у пациентки не было признаков или симптомов воспаления (эндометрита), лихорадки, озноба, болей в области таза или живота. Общий анализ крови был в норме [гемоглобин (Hb): 12,1 г/дл и тромбоциты: 325 ×10 9 /л, количество лейкоцитов 8,500 × 10 9 /л, СРБ 0,7 мг/л)]. Уровень β-субъединицы гонадотропина ХГЧ (β-ХГЧ) в сыворотке был отрицательным, признаков коагулопатии не было (протромбиновое время, активированное частичное тромбопластиновое время, международное нормализованное отношение (МНО) и уровни фибриногена плазмы были в пределах нормы. Пациент был реанимирован с теплые жидкости и кровь были отправлены на перекрестную совместимость (четыре единицы эритроцитов и четыре единицы свежезамороженной плазмы).Выполнено выскабливание матки, и 150 мл кюретированного материала были отрицательными для задержанных плацентарных продуктов. Несмотря на выскабливание эндометрия, ректальное введение мизопростола и внутривенное введение эргометрина малеата (Митротан, ГАП), кровотечение не останавливалось, была произведена внутриматочная тампонада Через 12 часов после выскабливания больная не стабилизировалась, потеряла сознание и продолжала кровоточить с постепенным снижением Hb. давление 100/65 мм рт. ст., а гемоглобин достиг 6 г/дл. повторно измеряли профиль коагуляции (протромбиновое время/активированное частичное тромбопластиновое время увеличились до 12,6 с/41,4 с соответственно, а уровень фибриногена составил 1,7 г/л).
Несмотря на выскабливание эндометрия, ректальное введение мизопростола и внутривенное введение эргометрина малеата (Митротан, ГАП), кровотечение не останавливалось, была произведена внутриматочная тампонада Через 12 часов после выскабливания больная не стабилизировалась, потеряла сознание и продолжала кровоточить с постепенным снижением Hb. давление 100/65 мм рт. ст., а гемоглобин достиг 6 г/дл. повторно измеряли профиль коагуляции (протромбиновое время/активированное частичное тромбопластиновое время увеличились до 12,6 с/41,4 с соответственно, а уровень фибриногена составил 1,7 г/л).
Пациентке было введено четыре единицы эритроцитарной массы и четыре единицы свежезамороженной плазмы, однако повторное УЗИ органов брюшной полости выявило увеличенную матку со скоплением крови вокруг внутриматочного тампона. КТ и МРТ малого таза с контрастом не выявили патологической причины кровотечения. Учитывая, что состояние пациентки считалось клинически нестабильным, была выполнена экстренная тотальная абдоминальная гистерэктомия без дополнительной визуализации, такой как ангиография. При гистопатологическом исследовании матки выявлены крупные тромбы в полости эндометрия и типичные признаки субинволюции сосудов плацентарного ложа. Микроскопические срезы миометрия выявили крупные, расширенные поверхностные кровеносные сосуды миометрия с утолщенными стенками в месте имплантации плаценты, что свидетельствует о СФС (12). Признаков задержки продуктов зачатия или воспаления децидуальной оболочки ни в материале выскабливания, ни в удаленной матке не было. Поставили диагноз СПС.
При гистопатологическом исследовании матки выявлены крупные тромбы в полости эндометрия и типичные признаки субинволюции сосудов плацентарного ложа. Микроскопические срезы миометрия выявили крупные, расширенные поверхностные кровеносные сосуды миометрия с утолщенными стенками в месте имплантации плаценты, что свидетельствует о СФС (12). Признаков задержки продуктов зачатия или воспаления децидуальной оболочки ни в материале выскабливания, ни в удаленной матке не было. Поставили диагноз СПС.
Открыть в отдельном окне
Субинволюция маточно-плацентарных артерий. Расширенные, сгруппированные, миометриальные артерии с частичной облитерацией тромбами (окраска гематоксилин-эозином, увеличение: ×400.
Новорожденный благополучно родился без осложнений и был госпитализирован в отделение для новорожденных на сутки наблюдения с учетом осложнений у матери. сохранена во время тотальной абдоминальной гистерэктомии в связи с сохранением фертильности яичников матери с возможностью дальнейшего суррогатного материнства
ПРК — серьезная акушерская проблема, одна из ведущих причин материнской смертности и заболеваемости. Вторичные ПРК обращаются реже, отчасти из-за того, что большинство пациентов лечатся амбулаторно, без госпитализации. СФС является важной причиной вторичного ПРК, и его следует рассматривать у пациентов с тяжелым ПРК из-за его ассоциации с опасным для жизни кровотечением. СФС диагностируется путем исключения других причин стойких вторичных послеродовых геморрагических выделений из влагалища. К ним относятся эндометрит, задержка продуктов плаценты, гестационная трофобластическая болезнь и коагулопатия. Диагноз СФС может быть подтвержден только гистологически, как это произошло в нашем случае. Исключая все вышеуказанные диагнозы по клиническим данным, УЗИ, лабораторным исследованиям и гистологии продуктов выскабливания, диагноз ПРК оставался неизвестным до окончательного гистопатологического исследования матки. Однако Петрович и др. 6 в своем исследовании отметили, что заподозрить эту ситуацию можно на основе сонографических характеристик патологических сосудов. Заподозрить субинволюцию плацентарной площадки при УЗИ можно в том редком случае, когда вдоль внутренней трети миометрия видны гипоэхогенные извитые сосуды.
Вторичные ПРК обращаются реже, отчасти из-за того, что большинство пациентов лечатся амбулаторно, без госпитализации. СФС является важной причиной вторичного ПРК, и его следует рассматривать у пациентов с тяжелым ПРК из-за его ассоциации с опасным для жизни кровотечением. СФС диагностируется путем исключения других причин стойких вторичных послеродовых геморрагических выделений из влагалища. К ним относятся эндометрит, задержка продуктов плаценты, гестационная трофобластическая болезнь и коагулопатия. Диагноз СФС может быть подтвержден только гистологически, как это произошло в нашем случае. Исключая все вышеуказанные диагнозы по клиническим данным, УЗИ, лабораторным исследованиям и гистологии продуктов выскабливания, диагноз ПРК оставался неизвестным до окончательного гистопатологического исследования матки. Однако Петрович и др. 6 в своем исследовании отметили, что заподозрить эту ситуацию можно на основе сонографических характеристик патологических сосудов. Заподозрить субинволюцию плацентарной площадки при УЗИ можно в том редком случае, когда вдоль внутренней трети миометрия видны гипоэхогенные извитые сосуды. 6 Импульсно-волновая допплерография УЗИ может указывать на увеличение пиковой систолической скорости (PSV; >0,83 м/с; нормальная 0,22 м/с через 3 дня после родов, падение до 0,10 м/с через 6 недель). Области повышенной васкуляризации могут коррелировать с местом имплантации плаценты, зафиксированным до родов. Однако эти находки не всегда являются патогномоничными и могут совпадать с врожденными или приобретенными артериовенозными мальформациями или задержкой продуктов зачатия.
6 Импульсно-волновая допплерография УЗИ может указывать на увеличение пиковой систолической скорости (PSV; >0,83 м/с; нормальная 0,22 м/с через 3 дня после родов, падение до 0,10 м/с через 6 недель). Области повышенной васкуляризации могут коррелировать с местом имплантации плаценты, зафиксированным до родов. Однако эти находки не всегда являются патогномоничными и могут совпадать с врожденными или приобретенными артериовенозными мальформациями или задержкой продуктов зачатия.
Крупные маточно-плацентарные артерии, модифицированные для беременности вневорсинчатыми трофобластами, остаются проходимыми после непосредственного послеродового периода, не подвергаясь нормальному процессу инволюции. Заболеваемость ПРК из-за субинволюции наиболее распространена на второй неделе после родов. 7 Точная частота тяжелого вторичного послеродового кровотечения была оценена Dossou et al. , 8 , которые описали распределение различных причин тяжелых вторичных послеродовых кровотечений после 26 023 родов. Частота тяжелых вторичных ПРК была очень низкой, всего 0,23% (n: 60/26 023). Субинволюция плацентарного ложа отмечена у 13,3% больных, при этом задержка плаценты была наиболее частой причиной кровотечений (30,0%). В отличие от клинических врачей, ветеринары более знакомы с этим состоянием, поскольку СФС является основной причиной выделений из влагалища у собак, возникающих у 10–20% послеродовых сук, начиная с 6 недель после родов. 9
Частота тяжелых вторичных ПРК была очень низкой, всего 0,23% (n: 60/26 023). Субинволюция плацентарного ложа отмечена у 13,3% больных, при этом задержка плаценты была наиболее частой причиной кровотечений (30,0%). В отличие от клинических врачей, ветеринары более знакомы с этим состоянием, поскольку СФС является основной причиной выделений из влагалища у собак, возникающих у 10–20% послеродовых сук, начиная с 6 недель после родов. 9
В патофизиологическом отношении во время беременности произошли нормальные физиологические изменения в спиральных артериях. С ранних сроков беременности (6–9 нед) экстраворсинчатые цитотрофобласты проникают в децидуальную часть спиральных артерий матери, замещая эндотелий, и завершается во втором триместре, когда эндотелиальная выстилка артерии полностью замещается. Этот процесс вызывает ремоделирование сосудов с разрушением мышечно-эластичных тканей медиальной части артерий, которые замещаются фибриноидным материалом. 10 Эти изменения играют важную роль во время беременности, обеспечивая адекватный маточно-плацентарный артериальный кровоток. Хорошо известно, что измененное ремоделирование спиральных артерий вызывает преэклампсию. С этой точки зрения сосуды СФС могут представлять противоположный конец спектра аномальных взаимодействий, обнаруживаемых при преэклампсии. 11
Хорошо известно, что измененное ремоделирование спиральных артерий вызывает преэклампсию. С этой точки зрения сосуды СФС могут представлять противоположный конец спектра аномальных взаимодействий, обнаруживаемых при преэклампсии. 11
В третьем триместре начинается физиологический механизм инволюции измененных маточно-плацентарных сосудов, когда эндоваскулярный цитотрофобласт замещается эндотелиальными клетками материнского происхождения. 7 Маточно-плацентарные артерии подвергаются тромбозу и сморщиванию плацентарной площадки. Сокращение гладкой мускулатуры матки также способствует механическому сморщиванию и инволюции этих сосудов, и матка возвращается в небеременное состояние. 12 При субинволюции места имплантации плаценты нормальное ремоделирование маточно-плацентарных артерий в третьем триместре либо задерживается, либо неадекватно, что приводит к сохранению расширенных сосудов с низким сопротивлением и повышенным кровотоком. 3 При СПС сильно увеличена матка. Гистологически субинволютивные сосуды плацентарного ложа в поверхностном миометрии крупные, проходимые и расширенные, с внутрисосудистым тромбозом (4). Стенки их на микроскопическом срезе деформированы и утолщены за счет отложения гиалина при частичном отсутствии эндотелиальной выстилки. 3 13
Гистологически субинволютивные сосуды плацентарного ложа в поверхностном миометрии крупные, проходимые и расширенные, с внутрисосудистым тромбозом (4). Стенки их на микроскопическом срезе деформированы и утолщены за счет отложения гиалина при частичном отсутствии эндотелиальной выстилки. 3 13
Точный патогенез СПС до сих пор неизвестен. Есть некоторые факторы, которые могут играть роль в этом процессе. Сасагава и др. , 14 был первым, кто предположил, что иммунологические паттерны необходимы для механизма нормальной инволюции маточно-плацентарных артерий, но это исследование не объяснило точную патофизиологию субинволюции этих артерий. Позже Andrew и соавт. 15 обнаружили отсутствие отложения иммуноглобулинов (IgG, IgA, IgM) и белков комплемента (C1q, C3d, C4) в стенках субинволютивных сосудов. Другая теория патофизиологии субинволюции состоит в повышенной экспрессии онкопротеина bcl-2, что связано с ингибированием апоптоза и длительным выживанием клеток в субинволютивных сосудах плацентарного ложа. 16 Онкобелок Bcl-2 в норме не выявляется в маточно-плацентарных артериях в третьем триместре беременности, однако может быть идентифицирован в инволюции и, в большей степени, в субинволюции сосудов плацентарного ложа. Обзор литературы также выявил участие некоторых ядерных факторов, идентифицированных в контроле инвазии трофобласта человека, таких как факторы преобразователя сигнала и активатора транскрипции (STAT), гамма-рецептор, активируемый пролифератором пероксисом (PPAR-γ), гомеобоксные гены или бескрылые и бескрылые гены. Int-1 (WNT)-зависимые факторы транскрипции. 17 Эти факторы могут способствовать патогенезу заболеваний беременных с аномальной плацентацией или нарушением дифференцировки трофобласта. Эпителиальные маркеры, такие как Troma 1 и CAM 5.2, почти всегда выделяют трофобласты, в то время как плацентарная щелочная фосфатаза, человеческий плацентарный лактоген и эпителиальный мембранный антиген не являются патогномоничными. 18
16 Онкобелок Bcl-2 в норме не выявляется в маточно-плацентарных артериях в третьем триместре беременности, однако может быть идентифицирован в инволюции и, в большей степени, в субинволюции сосудов плацентарного ложа. Обзор литературы также выявил участие некоторых ядерных факторов, идентифицированных в контроле инвазии трофобласта человека, таких как факторы преобразователя сигнала и активатора транскрипции (STAT), гамма-рецептор, активируемый пролифератором пероксисом (PPAR-γ), гомеобоксные гены или бескрылые и бескрылые гены. Int-1 (WNT)-зависимые факторы транскрипции. 17 Эти факторы могут способствовать патогенезу заболеваний беременных с аномальной плацентацией или нарушением дифференцировки трофобласта. Эпителиальные маркеры, такие как Troma 1 и CAM 5.2, почти всегда выделяют трофобласты, в то время как плацентарная щелочная фосфатаза, человеческий плацентарный лактоген и эпителиальный мембранный антиген не являются патогномоничными. 18
СФС является важным и клинически неуловимым диагнозом, поскольку этот механизм отвечает за идиопатическую, а не ятрогенную причину послеродового маточного кровотечения. 18 Farley и Kohlmeier 19 описали смерть 19-летней женщины в США из-за СФС. Через восемь дней после родов муж доставил ее в отделение неотложной помощи без пульса и дыхания. Диагноз СПС обычно недооценивается и ставится путем исключения других причин персистирующего вторичного ПРК. Сонографические признаки субинволюции плацентарной площадки посредством визуализации сосудов с низким сопротивлением вдоль внутренней трети миометрия могут помочь в диагностике СПС. 6 Импульсно-волновая допплерография может подтвердить повышенный PSV с помощью волны с низким сопротивлением, которая, учитывая, что сонографические данные с высоким потоком обычно являются результатом истинных артериовенозных сосудистых мальформаций (АВМ), которые могут быть приобретенными (например, ятрогенная травма, приводящая к рубцовая ткань и образование АВМ) или врожденные (например, дефекты развития сосудов, ведущие к ложу аномальных артериовенозных коммуникаций). 20–25 В то время как диагноз СФС подтверждается только гистологическим анализом, высокая степень подозрения на основании клинического анамнеза, такого как аномальное маточное кровотечение или повторная невынашивание беременности, может побудить клинициста запросить визуализацию.
18 Farley и Kohlmeier 19 описали смерть 19-летней женщины в США из-за СФС. Через восемь дней после родов муж доставил ее в отделение неотложной помощи без пульса и дыхания. Диагноз СПС обычно недооценивается и ставится путем исключения других причин персистирующего вторичного ПРК. Сонографические признаки субинволюции плацентарной площадки посредством визуализации сосудов с низким сопротивлением вдоль внутренней трети миометрия могут помочь в диагностике СПС. 6 Импульсно-волновая допплерография может подтвердить повышенный PSV с помощью волны с низким сопротивлением, которая, учитывая, что сонографические данные с высоким потоком обычно являются результатом истинных артериовенозных сосудистых мальформаций (АВМ), которые могут быть приобретенными (например, ятрогенная травма, приводящая к рубцовая ткань и образование АВМ) или врожденные (например, дефекты развития сосудов, ведущие к ложу аномальных артериовенозных коммуникаций). 20–25 В то время как диагноз СФС подтверждается только гистологическим анализом, высокая степень подозрения на основании клинического анамнеза, такого как аномальное маточное кровотечение или повторная невынашивание беременности, может побудить клинициста запросить визуализацию. МРТ с контрастным усилением может подтвердить выраженное расширение сосудов стенки матки, что помогает нам заподозрить СПС до гистерэктомии. 23 24 Ангиография считается золотым стандартом диагностики АВМ и, возможно, СПС. Симптоматика СПС может усилиться при гормональных изменениях, таких как менструация или беременность, что может вызвать дополнительные подозрения. 25
МРТ с контрастным усилением может подтвердить выраженное расширение сосудов стенки матки, что помогает нам заподозрить СПС до гистерэктомии. 23 24 Ангиография считается золотым стандартом диагностики АВМ и, возможно, СПС. Симптоматика СПС может усилиться при гормональных изменениях, таких как менструация или беременность, что может вызвать дополнительные подозрения. 25
Лечение субинволюции плацентарной площадки с кровотечением у пациенток с симптомами остается спорным. Это неотложная ситуация, и необходимо провести полное обследование для исключения любой другой возможной причины вторичного ПРК, а также для немедленной стабилизации состояния пациента до развития диссеминированной внутрисосудистой коагулопатии. В большинстве случаев кюретаж проводят, чтобы исключить задержку продуктов плаценты, даже если УЗИ не выявило видимых аномалий. Допускается консервативный подход с тампонадой матки марлевыми или различными баллонами (бакри) и утеротоническим лечением. Тем не менее, хирургические методы лечения, такие как перевязка маточных сосудов и гистерэктомия, считаются стандартными методами лечения. 26 27 По данным литературы чрескожная эмболизация маточной артерии рассматривается как альтернативная терапия СФС перед гистерэктомией. 4 26–28 Эта процедура обеспечивает сохранение фертильности, но требует специального оборудования и подготовленной бригады медицинских специалистов. Поэтому и в наши дни, к сожалению, не во всех стационарах можно провести эмболизацию артерий.
Тем не менее, хирургические методы лечения, такие как перевязка маточных сосудов и гистерэктомия, считаются стандартными методами лечения. 26 27 По данным литературы чрескожная эмболизация маточной артерии рассматривается как альтернативная терапия СФС перед гистерэктомией. 4 26–28 Эта процедура обеспечивает сохранение фертильности, но требует специального оборудования и подготовленной бригады медицинских специалистов. Поэтому и в наши дни, к сожалению, не во всех стационарах можно провести эмболизацию артерий.
В заключение, SPS является одной из редких, но важных причин вторичного послеродового кровотечения и, как и другие АВМ, может сосуществовать с другими причинами послеродового кровотечения, такими как остаточные продукты зачатия (POC). 29 Это состояние, вероятно, недооценивается гинекологом из-за отсутствия специфических диагностических критериев, как в нашем случае. Только при исключении других форм отсроченного ПРК и после неэффективного выскабливания и консервативной терапии диагноз СФС следует включать в дифференциальный диагноз. МРТ с контрастированием может указывать на очаговые зоны гиперваскуляризации матки. Однако гистологическое подтверждение расширенных, сгруппированных миометриальных артерий, частично закупоренных тромбами, проводится только после экстренной гистерэктомии.
МРТ с контрастированием может указывать на очаговые зоны гиперваскуляризации матки. Однако гистологическое подтверждение расширенных, сгруппированных миометриальных артерий, частично закупоренных тромбами, проводится только после экстренной гистерэктомии.
Пункты обучения
Частота послеродовых кровотечений из-за субинволюции чаще всего возникает на второй неделе после родов. Субинволюция плацентарного ложа отмечена у 13,3% из 26 023 пациенток, при этом задержка плаценты была наиболее частой причиной кровотечений (30,0%).
Точный молекулярный механизм патогенеза субинволюции плацентарного узла до сих пор неизвестен, но теории включают повышенную локальную экспрессию онкопротеина bcl-2, отсутствие отложения иммуноглобулинов и белков комплемента в стенках субинволютивных сосудов, STAT, PPAR- γ, гомеобоксные гены и дерегуляция WNT-зависимого фактора транскрипции.
К сожалению, субинволюция по-прежнему остается гистологическим диагнозом, и нет доступных изображений или других маркеров для выявления предшествующих серьезных осложнений у пациентов.

Авторы: Концепция, анализ, формат, доработка, редактирование, поиск литературы и составление рукописи: ИМ, ДК, ОТ, СК; Поиск литературы, анализ извлечения и составление рукописи: ОТ, СК.
Финансирование: Авторы не объявили о специальном гранте для этого исследования от какого-либо финансирующего агентства в государственном, коммерческом или некоммерческом секторах.
Конкурирующие интересы: Не заявлено.
Согласие пациента на публикацию: Получено.
Происхождение и экспертная оценка: Не введен в эксплуатацию; рецензируется внешними экспертами.
1. Карроли Г., Куэста С., Абалос Э. и др.. Эпидемиология послеродовых кровотечений: систематический обзор. Best Pract Res Clin Obstet Gynaecol 2008; 22:999–1012. 10.1016/j.bpobgyn.2008.08.004 [PubMed] [CrossRef] [Google Scholar]
2. Хан К.С., Войдыла Д., Сэй Л. и др..
Анализ ВОЗ причин материнской смертности: систематический обзор. Ланцет
2006; 367:1066–74. 10.1016/S0140-6736(06)68397-9 [PubMed] [CrossRef] [Google Scholar]
Ланцет
2006; 367:1066–74. 10.1016/S0140-6736(06)68397-9 [PubMed] [CrossRef] [Google Scholar]
3. Akgun H, Gonlusen G, Cartwright J, et al.. Являются ли контрастные вещества на основе гадолиния нефротоксичными? исследование биопсии почки. Arch Pathol Lab Med 2006; 130:1354–7. 10.1043/1543-2165(2006)130[1354:AGCMNA]2.0.CO;2 [PubMed] [CrossRef] [Google Scholar]
4. Кюстер Х. Ueber Spätblutungen im Wochenbett. Neue Gesichtspunkte zur Beurteilung ihrer Aetiologie nach mikroskopischen Untersuchungen. З Гебуртш Гынаек 1910; 67: 430–4. [Академия Google]
5. Резерфорд Р.Н., Хертиг А.Т. Неинволюция плацентарной площадки. Am J Obstet Gynecol 1945; 49: 378–84. 10.1016/0002-9378(45)
-7 [CrossRef] [Google Scholar]
6. Петрович И., Битти М., Джеффри Р.Б. и др.. Субинволюция плацентарной площадки. J УЗИ Мед 2009; 28:1115–9. 10.7863/jum.2009.28.8.1115 [PubMed] [CrossRef] [Google Scholar]
7. Andrew AC, Bulmer JN, Wells M, et al..
Субинволюция маточно-плацентарных артерий в плацентарном ложе человека. гистопатология
1989;15:395–405. 10.1111/j.1365-2559.1989.tb01591.x [PubMed] [CrossRef] [Google Scholar]
гистопатология
1989;15:395–405. 10.1111/j.1365-2559.1989.tb01591.x [PubMed] [CrossRef] [Google Scholar]
8. Dossou M, Debost-Legrand A, Déchelotte P, et al.. Тяжелое вторичное послеродовое кровотечение: историческая когорта. Рождение 2015;42:149–55. 10.1111/birt.12164 [PubMed] [CrossRef] [Google Scholar]
9. Ma K Послеродовые расстройства у собак: Jd B, Dc T, Современная ветеринарная терапия Кирка Xiv. 14-е изд. Сент-Луис, Миссури: Сондерс, 2000: 999–1002. [Google Scholar]
10. Gerretsen G, Huisjes HJ, Hardonk MJ, et al.. Изменения трофобласта в плацентарном ложе в связи с физиологическими изменениями спиральных артерий. Br J Obstet Gynaecol 1983;90:34–39. 10.1111/j.1471-0528.1983.tb06743.x [PubMed] [CrossRef] [Google Scholar]
11. Meekins JW, Pijnenborg R, Hanssens M, et al..
Исследование спиральных артерий плацентарного ложа и инвазии трофобласта при нормальной и тяжелой преэклампсии при беременности. БЖОГ
1994; 101: 669–74. 10.1111/j.1471-0528.1994.tb13182. x [PubMed] [CrossRef] [Google Scholar]
x [PubMed] [CrossRef] [Google Scholar]
12. Anderson WR, Davis J. Инволюция плацентарной площадки. Am J Obstet Gynecol 1968; 102: 23–33. 10.1016/0002-9378(68)-6 [PubMed] [CrossRef] [Google Scholar]
13. Уэллс М., Балмер Дж. Н. Плацентарное ложе человека: гистология, иммуногистохимия и патология. гистопатология 1988; 13: 483–98. 10.1111/j.1365-2559.1988.tb02073.x [PubMed] [CrossRef] [Google Scholar]
14. Sasagawa M, Watanabe S, Ohmomo Y, et al.. Реактивность двух моноклональных антител (Troma 1 и CaM 5.2) на срезах тканей человека: анализ их полезности в качестве гистологического маркера трофобласта при нормальной беременности и трофобластическом заболевании. Int J Гинекол Патол 1986; 5: 345–56. 10.1097/00004347-198612000-00006 [PubMed] [CrossRef] [Google Scholar]
15. Эндрю А., Балмер Дж. Н., Моррисон Л. и др.. Субинволюция маточно-плацентарных артерий: иммуногистохимическое исследование. Int J Гинекол Патол 1993; 12:28–33. 10.1097/00004347-199301000-00004 [PubMed] [CrossRef] [Google Scholar]
16. Khong TY, Abdul Rahman H, Rahman A.
Экспрессия Bcl-2 задерживает послеродовую инволюцию индуцированных беременностью сосудистых изменений в плацентарном ложе человека. Int J Гинекол Патол
1997; 16: 138–42. 10.1097/00004347-199704000-00009 [PubMed] [CrossRef] [Google Scholar]
Khong TY, Abdul Rahman H, Rahman A.
Экспрессия Bcl-2 задерживает послеродовую инволюцию индуцированных беременностью сосудистых изменений в плацентарном ложе человека. Int J Гинекол Патол
1997; 16: 138–42. 10.1097/00004347-199704000-00009 [PubMed] [CrossRef] [Google Scholar]
17. Knöfler M Критические факторы роста и сигнальные пути, контролирующие инвазию трофобласта человека. Int J Dev Biol 2010; 54: 269–80. 10.1387/ijdb.082769mk [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
18. Кавалар Р., Арко Д., Фоктер Довник Н. и др.. Субинволюция сосудов плацентарного ложа: клинический случай и обзор литературы. Вена Клин Вохеншр 2012; 124:725–30. 10.1007/s00508-012-0219-9 [PubMed] [CrossRef] [Google Scholar]
19. Фарли Н.Дж., Кольмейер Р.Е. Смерть вследствие субинволюции маточно-плацентарных артерий. J Судебно-медицинская экспертиза 2011;56:803–5. 10.1111/j.1556-4029.2011.01726.x [PubMed] [CrossRef] [Google Scholar]
20. Hoffman MK, Meilstrup JW, Shackelford DP, et al. .
Артериовенозные мальформации матки: редкая причина вагинальных кровотечений. Акушерство Гинекол Сурв
1997; 52: 736–40. 10.1097/00006254-199712000-00004 [PubMed] [CrossRef] [Google Scholar]
.
Артериовенозные мальформации матки: редкая причина вагинальных кровотечений. Акушерство Гинекол Сурв
1997; 52: 736–40. 10.1097/00006254-199712000-00004 [PubMed] [CrossRef] [Google Scholar]
21. Vogelzang RL, Nemcek AA, Skrtic Z, et al.. Артериовенозные мальформации матки: первичное лечение лечебной эмболизацией. Джей Васк Интерв Радиол 1991;2:517–22. 10.1016/S1051-0443(91)72234-3 [PubMed] [CrossRef] [Google Scholar]
22. Huang MW, Muradali D, Thurston WA, et al.. Артериовенозные мальформации матки: особенности шкалы серого и допплеровского УЗИ с корреляцией МРТ. Радиология 1998; 206: 115–23. 10.1148/radiology.206.1.9423660 [PubMed] [CrossRef] [Google Scholar]
23. Godoy LL, Torres US, D’Ippolito G. Субинволюция плацентарного участка, связанная с очаговыми задержкой продуктов зачатия и приращением плаценты, имитирующим артериовенозную мальформацию матки на КТ и МРТ: урок, который необходимо усвоить. Радиол Бюстгальтеры 2018;51:135–136. 10.1590/0100-3984.2016.0131 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
24. Sellmyer MA, Desser TS, Maturen KE, et al..
Физиологические, гистологические и визуализирующие особенности оставшихся продуктов зачатия. Рентгенография
2013;33:781–96. 10.1148/rg.333125177 [PubMed] [CrossRef] [Google Scholar]
Sellmyer MA, Desser TS, Maturen KE, et al..
Физиологические, гистологические и визуализирующие особенности оставшихся продуктов зачатия. Рентгенография
2013;33:781–96. 10.1148/rg.333125177 [PubMed] [CrossRef] [Google Scholar]
25. Aziz N, Lenzi TA, Jeffrey RB, et al.. Послеродовые маточные артериовенозные свищи. Акушерство Гинеколь 2004; 103:1076–1078. 10.1097/01.AOG.0000123241.44401.01 [PubMed] [CrossRef] [Google Scholar]
26. Maleux G, Timmerman D, Heye S, et al.. Приобретенные мальформации сосудов матки: рентгенологические и клинические результаты транскатетерной эмболотерапии. Евро Радиол 2006; 16: 299–306. 10.1007/s00330-005-2799-5 [PubMed] [CrossRef] [Google Scholar]
27. Cheng Y-Y, Hwang J-I, Hung S-W и др.. Ангиографическая эмболизация для неотложной и профилактической помощи при акушерских кровотечениях: четырехлетний опыт. J Chin Med Assoc 2003;66:727. [PubMed] [Google Scholar]
28. Chauleur C, Fanget C, Tourne G и др..
Серьезное первичное послеродовое кровотечение, артериальная эмболизация и будущая фертильность: ретроспективное исследование 46 случаев. Хум Репрод
2008; 23:1553–9. 10.1093/humrep/den122 [PubMed] [CrossRef] [Google Scholar]
Хум Репрод
2008; 23:1553–9. 10.1093/humrep/den122 [PubMed] [CrossRef] [Google Scholar]
29. Iraha Y, Okada M, Toguchi M, et al.. Мультимодальная визуализация при вторичном послеродовом или послеабортном кровотечении: остаточные продукты зачатия и связанные с ними состояния. Jpn J Радиол 2018;36:12–22. 10.1007/s11604-017-0687-y [PubMed] [CrossRef] [Google Scholar]
Subinvolution — RNpedia
Subinvolution — RNpediaУход за матерями и детьми (примечания)
Предыдущая статья Следующая статья
Описание
- Субинволюция — это замедленное возвращение увеличенной матки к нормальным размерам и функциям.
Этиология
- Субинволюция возникает в результате задержки фрагментов и оболочек плаценты, эндометрита или миомы матки; лечение зависит от причины.
Патофизиология
- Атония матки или фрагменты плаценты препятствуют эффективному сокращению матки.

Результаты оценки
Клинические проявления включают:
- Продолжительные лохиальные выделения
- Нерегулярное или чрезмерное кровотечение
- Матка больше нормальной
- Заболоченная матка (иногда)
Сестринский менеджмент
1. Предотвращение чрезмерной кровопотери, инфекции и других осложнений.
- Массаж матки, облегчение мочеиспускания и отчет о кровопотере.
- Контролируйте кровяное давление и частоту пульса.
- Вводить прописанные лекарства. (см. Таблицу лекарственных средств)
- Будьте готовы к возможным D&C.
2. Помочь пациентке и семье справиться с физическим и эмоциональным стрессом послеродовых осложнений.
Таблица лекарств Лекарства, используемые при послеродовых осложнениях
| Классификации | Используется для | Избранные вмешательства |
| Антикоагулянты Гепарин натрия для инъекций |
|
|
| Варфарин натрия (Кумадин, Варфилон) |
|
|
| Окситоксический метилэргоновин |
|


 Эластично-мягкая консистенция свидетельствует о наличии в родовых путях остатков последа. При осмотре зеркалами определяется отек и багровость шейки, цервикальный канал увеличен (легко проходят 1-2 пальца), в его полости выявляют сгустки крови.
Эластично-мягкая консистенция свидетельствует о наличии в родовых путях остатков последа. При осмотре зеркалами определяется отек и багровость шейки, цервикальный канал увеличен (легко проходят 1-2 пальца), в его полости выявляют сгустки крови. Поэтому для ускорения этого процесса применяют гормональные препараты, влияющие на миометрий и его сосуды – окситоцин, метилэргометрил и другие.
Поэтому для ускорения этого процесса применяют гормональные препараты, влияющие на миометрий и его сосуды – окситоцин, метилэргометрил и другие. Регулярное прикладывание новорожденного к груди также способствует сокращению миометрия.
Регулярное прикладывание новорожденного к груди также способствует сокращению миометрия. Причина – слабость миометрия;
Причина – слабость миометрия;



