Мифы и правда о пробе Манту у детей
- Подробности
- Автор: ЛДЦ Нейрон
- Опубликовано: 08 Ноябрь 2015
Большинство родителей с подозрением относятся к пробе Манту у малыша. Многие называют ее прививкой, однако это ошибка и прививкой такая проба не является. Туберкулиновая проба представляет собой тест, который определяет наличие в детском организме обостренного иммунитета, когда выявляется страшный и довольно безжалостный возбудитель опасного заболевания.
Туберкулин был открыт Робертом Кохом, а начиная с 1908 года благодаря Шарлю Манту его стали использовать везде и всюду с целью диагностики.
Сегодня мы поговорим о том, какие же существуют мифы среди родителей по поводу туберкулиновой пробы, проводимой у детей.
Мифы о пробе Манту
1.
 Проба Манту может увеличиться из-за съеденного за день до процедуры.
Проба Манту может увеличиться из-за съеденного за день до процедуры.Это выдумка. Сладости, цитрусовые, соленые блюда или большое количество газированной воды — все это никоим образом не влияет на размер Манту.
2. После процедуры ни в коем случае нельзя мочить место пробы, поскольку непременно образуется положительная реакция.
Результат пробы, которая вводится под кожные покровы малыша, не может измениться от того, что на него попадет несколько капель воды. Однако следует следить за тем, чтобы на месте введения туберкулиновой пробы у ребенка не происходило физических и химических процессов, к примеру, запрещено мазать кремом, тереть мочалкой, приклеивать пластырь, который не пропускает воздух и так далее. Эти процессы способны изменить результат Манту.
3. Проба Манту может вызвать страшное заболевание под названием лейкоз.
Это мнение высказывают чересчур восприимчивые люди, однако это выдумка, не имеющая доказательств.
4. Если перед пробой дать ребенку одно из аллергических средств, результат Манту будет отрицательным.

Это еще один миф, не имеющий подтверждений.
Страхи по поводу туберкулиновой пробы увеличиваются
В последнее время многие родители ставят под сомнение данную процедуру, поскольку появляется все больше детей с увеличенной пробой, которых ставят на учет в туберкулезный диспансер. Безусловно, мамы и папы недовольны этим.
Противники процедуры вызывают панику у родителей, уверяя, что воздействие туберкулина на развивающийся организм ребенка как следует не изучено и проба только вредит. Также они утверждают, что туберкулиновая проба не дает 100 % правильный результат, так как на него оказывают влияние особенности организма ребенка.
Однако на защиту пробы встали врачи. Они руководствуются существенным доводом: туберкулиновая проба у детей сегодня является основным способом выявления туберкулеза на начальном этапе.
Помимо этого они критически относятся к новому методу ПЦР, который представляет собой экспериментальный метод, дающий возможность достичь внушительного увеличения небольших концентраций некоторых фрагментов ДНК в пробе. Именно этот метод рекомендуют использовать вместо пробы Манту.
Именно этот метод рекомендуют использовать вместо пробы Манту.
Компетентные фтизиатры уверяют, что метод ПЦР не позволяет определить заболевание на ранней стадии.
Исходя из статистики, каждый восемнадцатый человек из ста тысяч погибает от страшного заболевания туберкулез. И заражение главным образом осуществляется воздушно-капельным путем. Каждый из нас пользуется общественным транспортом, посещает магазины, рынки и другие места скопления людей. Вероятность подхватить палочку Коха очень высока, особенно у детей и пожилых людей.
А в случае запущенной стадии туберкулеза человек начинает стремительными темпами «сгорать», поскольку от диагностики на ранней стадии — туберкулиновой пробы — многие отказываются.
При этом важно знать всем родителям, что противопоказания к пробе все же существуют.
Противопоказания к туберкулиновой пробе у детей
Процедура запрещена, если ребенок:
- имеет повышенную восприимчивость к фенолу;
- недавно переболел вирусным или простудным заболеванием;
- имеет скрытое заболевание на начальной стадии;
- страдает от аллергической реакции;
- имеет хроническую патологию, в том числе неинфекционного происхождения.

Перед тем как делать пробу Манту, родители должны отвести ребенка к педиатру, который проведет тщательное обследование.
Помимо этого необходимо прислушиваться к тому, что говорит малыш, на что жалуется, обращать внимание на его внешний вид и общее самочувствие.
Помните, что никто не в праве насильно делать пробу Манту вашему малышу.
Проба ставится только с разрешения родителей ребенка. В противном случае вы должны написать отказ от процедуры. Однако при этом подумайте, если проба так вредна для детей, почему же врачи ставят ее всем своим близким и знакомым и рекомендуют использовать только ее. Если вы не являетесь врачом, не следует доверять всем выдумкам и мнениям о пробе Манту, доверяйте специалистам и своему внутреннему голосу, который не подведет вас, поскольку это касается вашего ребенка.
Берегите себя и своих детей!
лдц «Нейрон»
Добавить комментарий
Памятка по иммунопрофилактике — Детская Городская Поликлиника №133
За прошедшие годы благодаря профилактическим прививкам достигнуты грандиозные успехи в борьбе с инфекционными заболеваниями: ликвидирована натуральная оспа — инфекция от которой погибало население городов и целых стран, резко снизилась по сравнению с допривквочной эрой заболеваемость туберкулезом, достигнуты существенные успехи в борьбе со столбняком, дифтерией, гепатитом В и другими управляемыми инфекциями.
Федеральным законом от 17.09.1998 г. №157-ФЗ «об иммунопрофилактике инфекционных болезней» установлены правовые основы государственной политики в сфере иммунопрофилактики. Государство гарантирует доступность для граждан профилактических прививок, бесплатное их проведение в организациях государственной и муниципальной систем здравоохранения, обеспечение современного уровня производства вакцин, государственную поддержку отечественных производителей вакцин.
1. Вирусный гепатит В. Возбудитель содержится в мельчайших каплях крови, слез, слюны. У 95% инфицированных новорождённых развивается хроническая форма гепатита В, которая может спровоцировать развитие цирротических и опухолевых изменений в печени. Не у всех беременных может быть выявлена инфицированностью вирусом гепатита В при лабораторном исследовании.
Первая прививка против гепатита В проводится в течение 24 часов после рождения, вторая — через 1 месяц, третья прививка через 6 месяцев после первой. Детям, относящимся к группам риска, вакцинация против вирусного гепатита В проводится 4-хкратно: 1 доза — в момент начала вакцинации, 2 доза — через месяц после 1 прививки, 3 доза — через 2 месяца от начала вакцинации, 4 доза — через 12 месяцев от начала вакцинации.
Дети, относящиеся к группам риска — это дети, родившиеся от матерей:
— носителей HBsAg:
— больных вирусным гепатитом В или перенесших вирусный гепатит В в третьем триместре беременности, не имеющих результатов обследования на маркеры гепатита В;
2. Туберкулез развивается при инфицировании микобактериями туберкулеза через дыхательные пути, когда бактерия размножается в легочных альвеолах. Лечение противотуберкулезными препаратами продолжается несколько месяцев, иногда — лет.
Лечение противотуберкулезными препаратами продолжается несколько месяцев, иногда — лет.
Иммунизация против туберкулеза проводится новорожденным детям на 3-7 день жизни. Ревакцинация выполняется при отрицательном результате пробы Манту у детей в возрасте 6-7 лет.
3. Пневмококковая инфекция вызывается бактериями пневмококками, которых известно несколько десятков подтипов. Инфекция может проявляться развитием воспаления легких, гнойным пневмококковым менингитом, сепсисом. Многие подтипы пневмококка имеют устойчивость к широкому спектру антибиотиков, что значительно затрудняет лечение.
Вакцинация детей против пневмококковой инфекции проводится двукратно в 2 месяца, затем в 4,5 месяца с однократной ревакцинацией в 15 месяцев. Вакцинация детей, которым иммунопрофилактика против пневмококковой инфекции не была начата в первые 6 месяцев жизни, проводится двукратно с интервалом между прививками не менее 2 месяцев.
4. Дифтерия. У людей высокая восприимчивость к возбудителю дифтерии.
5. Столбняк. Возбудитель столбняка обитает в почве и может попасть в организм при ранах, уколах, ожогах. Столбняк, вызывая поражение нервной системы, у детей без госпитализации и лечения имеет почти 100% смертность.
Вакцинация против дифтерии и столбняка проводится детям в возрасте 3, 4,5 и 6 месяцев. Ревакцинации выполняются в 18 месяцев, 6-7 лет и 14 лет. Вторая и третья ревакцинации проводятся анатоксинами с уменьшенным содержанием антигенов. Для взрослых старше 18 лет обязательно проводится ревакцинация каждые 10 лет от момента последней ревакцинации.
6. Коклюш — заболевание, проявляющееся мучительным приступообразным (спазматическим) кашлем, который часто заканчивается рвотой. Старшие дети школьного возраста и подростки являются частыми источниками инфекции для детей до 1 года, для которых коклюш опасен осложнениями и может привести к смерти.
Иммунизация против коклюша проводятся комплексными вакцинами, содержащими дифтерийный и столбнячный анатоксины. Вакцинируют детей в 3,4,5 и 6 месяцев. Однократная ревакцинация выполняется в 18 месяцев.
7. Гемофильная инфекция типа b. Возбудитель часто обнаруживается при лабораторном исследовании у больных бактериальными менингитами, пневмониями и при сепсисе. Дети-дошкольники могут быть носителями бактерий, от которых возбудитель передается окружающим.
Вакцинация проводится детям из вышеуказанных групп риска в возрасте 3, 4,5 и 6 месяцев с однократной ревакцинацией в 18 месяцев.
8. Корь характеризуется высокой температурой (вплоть до 40°С), воспалением слизистых оболочек рта и дыхательных путей, сыпью, общей интоксикацией. Корь может вызывать тяжелые осложнения: средний отит, пневмонию, коревой энцефалит, а также подострый склерозирующий панэнцефалит как отдаленное осложнение.
9. Краснуха сопровождается лихорадкой, сыпью (мелкими пятнышками), увеличением лимфатических узлов (особенно затылочных), интоксикацией. При заболевании краснухой беременных происходит тяжелое поражение плода.
При заболевании краснухой беременных происходит тяжелое поражение плода.
10. Эпидемический паротит («свинка») поражает нервную систему, околоушные железы. Зачастую паротит становится одной из причин мужского бесплодия.
Схема иммунизации против кори, паротита и краснухи состоит из однократной вакцинации в 12 месяцев и однократной ревакцинации в 6 лет.
11. Грипп — одно из наиболее тяжело протекающих ОРВИ, характеризуется высокой лихорадкой и выраженной интоксикацией, может приводить к осложнениям со стороны сердечно-сосудистой и дыхательной систем, которые в некоторых случаях могут приводить к смерти.
Иммунизация против гриппа особенно показана детям, начиная с 6 месяцев, беременным женщинам, лицам с хроническими соматическими заболеваниями, отягощенным аллергологическим анамнезом и иммунодефицитными состояниями. Вакцинация проводится ежегодно перед началом эпидемического сезона гриппа.
Уволен директор департамента здравоохранения Приморья, где после пробы Манту заболели дети — Общество
ВЛАДИВОСТОК, 14 октября. /Корр. ИТАР-ТАСС Марина Шатилова/. Губернатор Приморского края Владимир Миклушевский уволил директора краевого департамента здравоохранения Олега Бубнова. Причиной стали результаты работы комиссии, которая изучала обстоятельства массового заболевания детей после пробы Манту в селе Новосысоевка Яковлевского района края.
/Корр. ИТАР-ТАСС Марина Шатилова/. Губернатор Приморского края Владимир Миклушевский уволил директора краевого департамента здравоохранения Олега Бубнова. Причиной стали результаты работы комиссии, которая изучала обстоятельства массового заболевания детей после пробы Манту в селе Новосысоевка Яковлевского района края.
Провал руководства департамента здравоохранения
Комиссия установила, что процедура постановки пробы Манту проводилась с грубыми нарушениями: использовался сухой туберкулин, который мог применяться только в условиях стационара. Также не было письменного разрешения родителей на проведение проб Манту. Дети пострадали от аллергической реакции, которая возникла из-за превышения дозы препарата в 2,5 тысячи раз.
Состояние детей, заболевших после пробы Манту, оценивается как удовлетворительное — Минздрав
Губернатор Миклушевский отметил, что ситуация, сложившаяся в Яковлевском районе, — это провал руководства департамента здравоохранения. «Организационная работа департамента здравоохранения Приморского края должна быть признана неудовлетворительной. Департамент должен был заниматься и вопросами повышения квалификации медицинского персонала в районе, и организационной работой», — подчеркнул глава региона.
«Организационная работа департамента здравоохранения Приморского края должна быть признана неудовлетворительной. Департамент должен был заниматься и вопросами повышения квалификации медицинского персонала в районе, и организационной работой», — подчеркнул глава региона.
Глава Минздрава: «Произошло полное безобразие»
По словам министра здравоохранения России Вероники Сковорцовой, эта вопиющая ситуация будет разобрана на видео-селекторе со всеми регионами страны.
«Я еще раз хочу заверить, что это не имеет отношения ни к иммунизации, ни к вакцинации, дети эти ничем не заразились, и наша задача, чтобы такое единичное безобразие не отразилось на отношении нашего населения, прежде всего молодых мам и пап, на отношении к тому, что детей надо прививать», — подчеркнула Сковорцова.
Врач-педиатр стал главным подозреваемым
Врач и медсестра, проводившие инъекции, отстранены от работы. Также отстранен исполняющий обязанности главного врача по Яковлевскому району. «Он не сумел взять ситуацию на контроль», — пояснила вице-губернатор края Ирина Василькова.
«Он не сумел взять ситуацию на контроль», — пояснила вице-губернатор края Ирина Василькова.
По факту заболевания детей возбуждено уголовное дело по статье «Халатность». Следователи допросили около 10 человек, в том числе, сотрудников Яковлевской больницы, а также представителей компании разработчиков и производителей препаратов «туберкулин». Изъята и изучена документация. Главным подозреваемым по эту делу является врач-педиатр, поскольку, по версии следствия, именно в результате ее небрежного отношения к туберкулинодиагностике была допущена медсестра, не входящая в специальную бригаду и не имеющая специального допуска.
Последствия вакцинации неизвестны
7 октября врач-педиатр и медсестра Яковлевской центральной районной больницы провели туберкулинодиагностику 45 учащимся школы села Новосысоевка 5-9 классов без согласия и уведомления их родителей. При этом были превышены допустимые дозы введения препарата.
На следующий день в Арсеньевскую городскую больницу после проведения вакцинации поступили две ученицы седьмого класса. Они жаловались на головную боль и покраснение в области инъекции. Сразу же был проведен осмотр остальных детей, 28 из них были госпитализированы. 11 октября 11 школьников, у которых была выявлена самая сильная реакция на инъекцию, были отправлены на обследование в Москву. В НИИ фтизиопульмонологии имени Сеченова они пройдут полное обследование и будут находиться под наблюдением врачей в течение трех недель. Остальные заболевшие дети остались под наблюдением местных врачей.
Они жаловались на головную боль и покраснение в области инъекции. Сразу же был проведен осмотр остальных детей, 28 из них были госпитализированы. 11 октября 11 школьников, у которых была выявлена самая сильная реакция на инъекцию, были отправлены на обследование в Москву. В НИИ фтизиопульмонологии имени Сеченова они пройдут полное обследование и будут находиться под наблюдением врачей в течение трех недель. Остальные заболевшие дети остались под наблюдением местных врачей.
Специалисты пока не могут сказать, какие последствия будет иметь случившееся для пострадавших детей. По заверениям производителя, эксперименты по введению таких больших доз туберкулина никогда не проводились, поэтому последствия неизвестны.
Жанна Кривошеева: Заменит ли в Беларуси диаскинтест пробу Манту?
Основным методом профилактического обследования детей на инфицирование туберкулезом на протяжении последних ста лет была туберкулинодиагностика — проба Манту.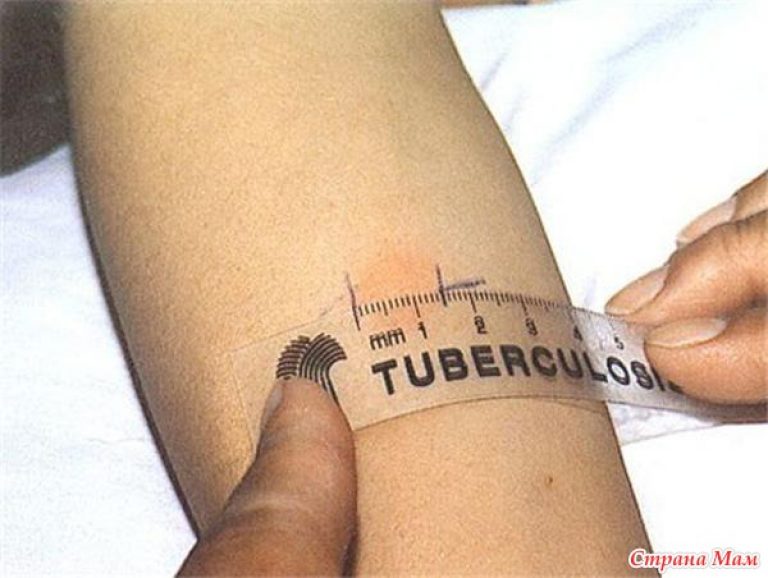 После введения под кожу препарата возникает небольшое специфическое воспаление в виде папулы, или, говоря по-простому, «пуговки». Результат оценивается спустя 72 часа при помощи линейки. В последние годы в ряде стран, в том числе в Беларуси, для диагностики туберкулеза наряду с пробой Манту стали использовать разработку российских ученых — диаскинтест.
После введения под кожу препарата возникает небольшое специфическое воспаление в виде папулы, или, говоря по-простому, «пуговки». Результат оценивается спустя 72 часа при помощи линейки. В последние годы в ряде стран, в том числе в Беларуси, для диагностики туберкулеза наряду с пробой Манту стали использовать разработку российских ученых — диаскинтест.
В Беларуси эта российская инновационная разработка применяется с 2012 года. А не так давно был принят новый приказ Министерства здравоохранения, который скорректировал порядок проведения иммунодиагностики и химиопрофилактики туберкулеза у детей. Каковы новые подходы в этом плане и чем были вызваны изменения, корреспондент БЕЛТА узнала у главного внештатного фтизиопедиатра, доцента кафедры фтизиопульмонологии ГУО «БГМУ» Жанны Кривошеевой.
«До 2012 года у нас в стране для выявления туберкулезной инфекции у детей и подростков до 17 лет применялась массовая туберкулинодиагностика (проба Манту). Ежегодно мы ставили 1,8 млн туберкулиновых проб, каждая обходилась примерно в $1.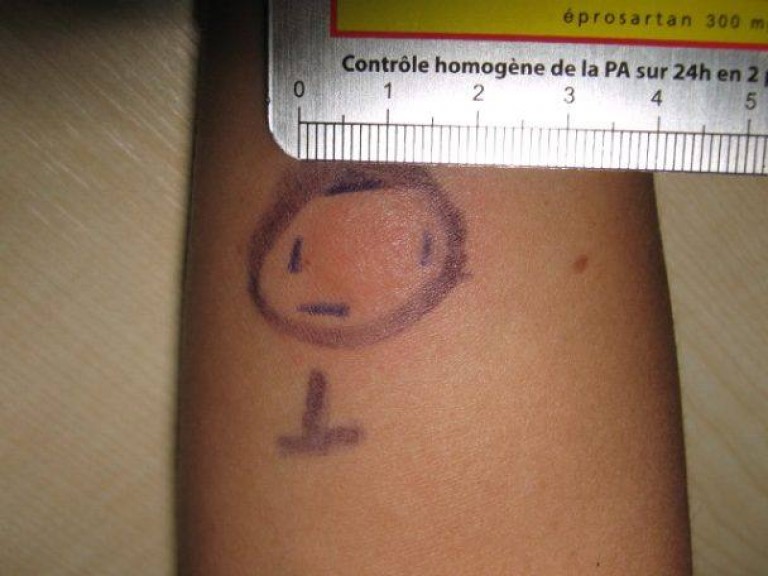 С учетом всех расходных материалов и стоимости туберкулина на это уходило около $2 млн», — рассказывает Жанна Кривошеева.
С учетом всех расходных материалов и стоимости туберкулина на это уходило около $2 млн», — рассказывает Жанна Кривошеева.
При этом из 1,8 млн детей у 20 тыс. ежегодно выявлялась впервые положительная (вираж) или чрезмерная реакция на пробу Манту. Это говорит о том, что ребенок, возможно, болен или инфицирован микобактериями туберкулеза. Детям назначалось дополнительное обследование, консультация фтизиатра и превентивное лечение, чтобы предупредить заболевание туберкулезом у тех, кто недавно инфицировался.
С появлением на белорусском рынке диаскинтеста эту разработку также стали использовать для диагностики туберкулеза. На первых этапах — в качестве дополнительного метода. То есть, если у ребенка возникала положительная реакция на пробу Манту, вторым шагом становилась диагностика с помощью него, и только в случае положительной реакции на этот тест ребенку было показано профилактическое назначение противотуберкулезных лекарственных средств. Благодаря такому шагу значительно (на 60-70%) сократилось количество детей, которым назначалась химиопрофилактика.
Кому Манту, а кому — диаскинтест?
Приказ Минздрава, который вышел в конце 2015 года, четко разграничил и упорядочил применение каждого из тестов. Так, иммунодиагностику туберкулезной инфекции с использованием пробы Манту ежегодно будут проводить детям в возрасте с 1 года до 7 лет из групп высокого риска по развитию туберкулеза. Такие дети составляют более 90% пациентов с этим заболеванием. В первую очередь это касается ВИЧ-инфицированных, детей с иммуносупрессией (то есть ослабленным иммунитетом), признанных находящимися в социально опасном положении, а также проживающих в общежитии, из семей беженцев, мигрантов, из детских интернатных учреждений с круглосуточным пребыванием, детей-инвалидов и др. У детей из очага туберкулезной инфекции такие тесты будут проводиться 2 раза в год. Кроме того, проба Манту предназначена для отбора на иммунизацию вакциной БЦЖ (БЦЖ-М) детей старше 2-месячного возраста, если те по каким-то причинам не прошли вакцинацию против туберкулеза в роддоме.
Детям в возрасте от 8 до 17 лет из групп риска ежегодно будет проводиться диаскинтест (без пробы Манту). Это связано с тем, что в этом возрасте проба Манту, как правило, всегда положительная и малоинформативная. Таким образом планируется исключить большую долю необоснованных дополнительных обследований, в том числе рентгенологических. Также тест будет применяться в некоторых случаях для проведения дополнительной медицинской диагностики по результатам пробы Манту.
По словам Жанны Кривошеевой, диаскинтест считается более специфичным методом. Результат бывает положительным только при наличии активной формы туберкулеза и в случае инфицирования с высоким риском развития заболевания. Проба Манту зачастую дает ложноположительные результаты в тех странах, где существует сплошная и, тем более, многократная БЦЖ-вакцинация против туберкулеза. Сама процедура постановки и оценки результатов обоих кожных тестов ничем не отличаются. Результат реакции оценивается через 72 часа.
Современной альтернативой кожным тестам (Манту, диаскинтест) является квантифероновый тест. Он высокочувствителен и очень специфичен, однако для массового скрининга не подходит, в частности, из-за своей высокой стоимости. Кроме того, для проведения процедуры нужна специализированная лаборатория и специально обученный персонал. Квантифероновый тест в Беларуси применяется в исключительных случаях, когда применение других диагностикумов нежелательно. Например, в случае противопоказаний для постановки пробы Манту или диаскинтеста.
Он высокочувствителен и очень специфичен, однако для массового скрининга не подходит, в частности, из-за своей высокой стоимости. Кроме того, для проведения процедуры нужна специализированная лаборатория и специально обученный персонал. Квантифероновый тест в Беларуси применяется в исключительных случаях, когда применение других диагностикумов нежелательно. Например, в случае противопоказаний для постановки пробы Манту или диаскинтеста.
Противопоказания к применению кожных тестов одинаковы. В первую очередь, это индивидуальная непереносимость. При плановой диагностике эти тесты не применяются в случае острого заболевания, в том числе ОРИ, обострения кожных аллергических заболеваний. Противопоказанием является и карантин в детском коллективе. Однако большинство из этих противопоказаний не учитывается в случае подозрения на туберкулез.
По словам Жанны Кривошеевой, такой проблемы, как отказы родителей от проведения их детям диагностических тестов, в Беларуси нет. Побочные реакции (сыпь, повышение температуры и др. ) возможны лишь в исключительных случаях. В то же время несложные манипуляции позволяют оградить себя и своих близких от болезни, которая лечится достаточно сложно. «Если родители отказываются, а ребенок относится к группе риска, мы имеем право в соответствии с законом о санитарно-эпидемическом благополучии населения направить письменное уведомление о необходимости обследования ребенка на наличие туберкулезной инфекции», — говорит специалист.
) возможны лишь в исключительных случаях. В то же время несложные манипуляции позволяют оградить себя и своих близких от болезни, которая лечится достаточно сложно. «Если родители отказываются, а ребенок относится к группе риска, мы имеем право в соответствии с законом о санитарно-эпидемическом благополучии населения направить письменное уведомление о необходимости обследования ребенка на наличие туберкулезной инфекции», — говорит специалист.
А что с прививками БЦЖ?
Массовой проблемы нет и с отказами от прививки БЦЖ. «Сейчас мы применяем прививку БЦЖ-М, она предназначена для щадящей иммунизации. Если ребенок не вакцинирован, у него вообще нет иммунитета к туберкулезной инфекции. И тогда в раннем возрасте риск заболеть тяжелой формой туберкулеза чрезмерно высок. Прививка препятствует развитию тяжелых генерализованных форм заболевания (менингита, милиарного туберкулеза) у детей первых лет жизни, у которых нет неспецифического (врожденного) иммунитета», — говорит специалист.
Безусловно, некоторые родители могут привести антидовод: в Беларуси низкий уровень распространения туберкулеза среди детей, зачем же проводить вакцинацию? На этот счет Жанна Кривошеева пояснила, что Всемирной организацией здравоохранения разработаны критерии, регламентирующие случаи, когда страна может отказаться от массовой вакцинации против туберкулеза.
«Самый главный критерий — уровень первичного инфицирования детей менее 0,1% в год. Это те дети, которые в течение года впервые встретились с туберкулезной инфекцией. В нашей стране в разных регионах этот показатель составляет от 0,8% до 1,5%. Другой критерий — количество туберкулезных менингитов на 10 млн населения в течение 5 лет. Считается, что если за этот период в стране не было ни одного случая детского менингита, можно отменить массовую вакцинацию. У нас раз в 4-5 лет выявляется один случай туберкулезного менингита у ребенка. Даже судя по этим двум показателям нам пока рано сворачивать профилактические мероприятия», — говорит фтизиопедиатр.
Откажется ли Минздрав от «пуговки» Манту?
Вернемся к диагностическим препаратам. Диаскинтест примерно в два раза дороже туберкулина ($0,98 против $0,43 за одну дозу). В то же время многие специалисты утверждают, что в итоге бюджетные средства будут сэкономлены — благодаря тому, что диаскинтест дает более четкие результаты, повторная диагностика будет требоваться гораздо реже.
Однако некоторые российские ученые считают, что диаскинтест не может быть использован для массового скрининга, поскольку не выявляет туберкулез в период первичной туберкулезной инфекции. В Беларуси в некоторых спорных случаях (если проба Манту положительная, а диаскинтеста — отрицательная) дети приглашаются на повторный анализ через 3 или 6 месяцев.
Так или иначе, полностью отменять пробу Манту для детей школьного возраста или полностью заменять ее диаскинтестом Минздрав Беларуси пока не планирует. Для принятия такого серьезного решения нужен взвешенный подход и оценка результатов массового скрининга на протяжении как минимум 5-10 лет.
Светлана ВАСИЛЕВСКАЯ,
БЕЛТА.-0-
введенная детям доза была превышена в 2,5 тысячи раз
Школьникам из села Новосысоевка вкололи увеличенную дозу препарата для пробы Манту. Об этом агентству «Интерфакс» сообщила Аврора Римская, старший помощник руководителя следственного управления Следственного комитета России по Приморью.
Об этом агентству «Интерфакс» сообщила Аврора Римская, старший помощник руководителя следственного управления Следственного комитета России по Приморью.
«Установлено, что доза препарата, которую получили дети, превышает допустимую в 2,5 тысячи раз», — уточнила она. Этот вывод сделан на основании заключения производителя препарата. Медсестра, проводившая диагностику, не имела необходимого допуска к такой работе и не знала, как разводить препарат, отметили в пресс-службе Следственного управления СК по Приморскому краю. Специалисты не могут сказать, какие последствия будет иметь происшедшее для здоровья детей. Эксперименты по введению таких больших доз туберкулина, по заверениям производителя, не проводились.
Сейчас 11 школьников проходят дополнительное обследование в московском НИИ имени Сеченова. В течение трех недель дети будут находиться под наблюдением специалистов. Остальные 18 пострадавших — в детском противотуберкулезном санатории номер 3 города Арсеньев.
8 октября 30 учеников 5 — 9 классов госпитализировали после проб Манту. Дети жаловались на плохое самочувствие. Проверка показала, что туберкулинодиагностика была проведена с нарушением технологий.
Дети жаловались на плохое самочувствие. Проверка показала, что туберкулинодиагностика была проведена с нарушением технологий.
Губернатор Приморского края Владимир Миклушевский заявил, что работа департамента здравоохранения края должна быть признана неудовлетворительной.
«Сложившаяся ситуация — это провал руководства департамента здравоохранения Приморского края», — сказал глава региона на встрече с вице-губернатором края Ириной Васильковой. Она доложила о результатах расследования.
«Процедура проведения пробы Манту проводилась с грубыми нарушениями. Применяли сухой «туберкулин», который может применяться только в условиях стационара и строго по согласованию с врачом. Также не было письменного разрешения родителей на проведение проб», — перечислила факты Василькова.
Ответственная за проведение и контроль туберкулинодиагностики среди детей Яковлевского района — районный врач-педиатр. Она и является пока главным подозреваемым по делу. По версии следствия, именно в результате ее небрежного отношения, к процедуре был допущен медицинский работник, не входящий в специальную бригаду и не имеющий специального доступа.
границ | Анализ активности туберкулина PPD у естественно инфицированного туберкулезом крупного рогатого скота в качестве меры контроля качества в рамках Ирландской программы ликвидации туберкулеза крупного рогатого скота
Введение
Туберкулез крупного рогатого скота (bTB) является важным инфекционным заболеванием крупного рогатого скота, которое представляет собой проблему «Единое здравоохранение» как риск для общественного здравоохранения из-за его зоонозного потенциала (ВОЗ) (1) и имеет значительные экономические и торговые последствия для Европейского Союза ( ЕС) и Всемирной организации по охране здоровья животных [Международное бюро по эпизоотиям (МЭБ)] (2, 3).Точность и надежность диагностического теста имеют решающее значение для стратегий контроля и ликвидации болезни (2–5). Обнаружение возбудителя Mycobacteria , всех членов туберкулезного комплекса (MTBC), на ранних стадиях заболевания зависит от измерения клеточно-опосредованного иммунного ответа in vivo или in vitro , поскольку циркулирующие антитела остаются не обнаруживается до более поздних этапов прогрессирования заболевания (4, 6). МЭБ (3) и Европейская комиссия (2) признают внутрикожный туберкулиновый тест in vivo (7) основным официальным тестом для диагностики инфицированных ТБ животных.Приложение B торговой директивы ЕС (2) определяет туберкулин как «очищенное белковое производное туберкулина (туберкулин PPD, бычий или птичий) представляет собой препарат, полученный из продуктов роста и лизиса Mycobacterium bovis или Mycobacterium avium , подвергшихся тепловой обработке. (при необходимости), способных выявить замедленную гиперчувствительность у животного, сенсибилизированного к микроорганизмам того же вида». Методология внутрикожной туберкулиновой пробы для диагностики туберкулеза применяется в соответствии с рекомендациями МЭБ во многих странах с использованием различных приложений (3).Однократный внутрикожный туберкулиновый тест, цервикальный (SIT) или хвостовой складки (CFT) и однократный внутрикожный сравнительный туберкулиновый тест (SICTT) широко используются для выявления животных, инфицированных MTBC (7) во многих национальных программах и для международной гарантии свободы от бТБ (3).
МЭБ (3) и Европейская комиссия (2) признают внутрикожный туберкулиновый тест in vivo (7) основным официальным тестом для диагностики инфицированных ТБ животных.Приложение B торговой директивы ЕС (2) определяет туберкулин как «очищенное белковое производное туберкулина (туберкулин PPD, бычий или птичий) представляет собой препарат, полученный из продуктов роста и лизиса Mycobacterium bovis или Mycobacterium avium , подвергшихся тепловой обработке. (при необходимости), способных выявить замедленную гиперчувствительность у животного, сенсибилизированного к микроорганизмам того же вида». Методология внутрикожной туберкулиновой пробы для диагностики туберкулеза применяется в соответствии с рекомендациями МЭБ во многих странах с использованием различных приложений (3).Однократный внутрикожный туберкулиновый тест, цервикальный (SIT) или хвостовой складки (CFT) и однократный внутрикожный сравнительный туберкулиновый тест (SICTT) широко используются для выявления животных, инфицированных MTBC (7) во многих национальных программах и для международной гарантии свободы от бТБ (3).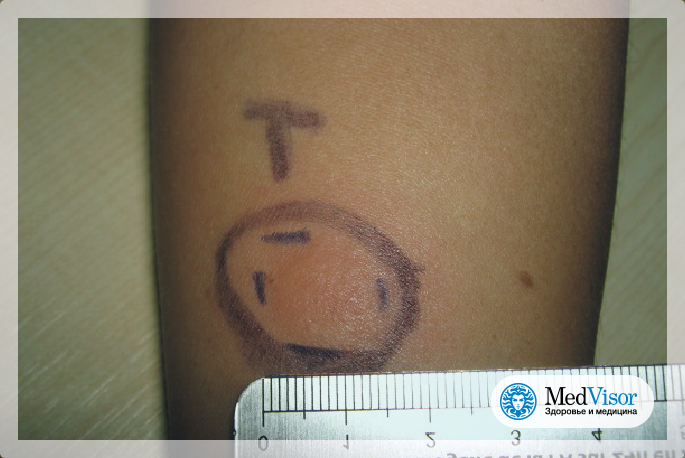 Непрерывная оценка всех элементов, т. е. ресурсов, эффективности и результатов национальной программы контроля/ликвидации болезней, необходима для поддержания эффективности и обеспечения достижения и поддержания максимально возможных стандартов (8, 9).
Непрерывная оценка всех элементов, т. е. ресурсов, эффективности и результатов национальной программы контроля/ликвидации болезней, необходима для поддержания эффективности и обеспечения достижения и поддержания максимально возможных стандартов (8, 9).
Эволюция туберкулинов
Доктор Роберт Кох продемонстрировал, что M. tuberculosis был возбудителем туберкулеза человека (ТБ) в 1882 году. Пытаясь разработать лекарство от туберкулеза, он впервые произвел то, что стало известно как старый туберкулин Коха (КОТ) в 1890 году. из сырой экстракции убитых нагреванием культур M. tuberculosis (10–13). К 1891 г. КОТ использовался для диагностики туберкулеза у крупного рогатого скота, и применялись различные тесты, хотя с ним были связаны проблемы чувствительности (Se) и специфичности (Sp) (4, 12).Первое серьезное улучшение как в производстве туберкулина, так и в последующем тестировании Se и Sp произошло, когда для роста бактерий использовалась синтетическая среда (11). Seibert ввел преципитацию туберкулопротеина в 1934 г., поэтому был введен термин PPD (13). Туберкулин PPD имел меньше примесей и мог быть стандартизирован на основе содержания белка. Однако стандартизация с использованием содержания белка не обязательно коррелирует с биологической активностью, которую необходимо регулярно оценивать по эталонному стандарту (14).
Seibert ввел преципитацию туберкулопротеина в 1934 г., поэтому был введен термин PPD (13). Туберкулин PPD имел меньше примесей и мог быть стандартизирован на основе содержания белка. Однако стандартизация с использованием содержания белка не обязательно коррелирует с биологической активностью, которую необходимо регулярно оценивать по эталонному стандарту (14).
Публикация Good et al. 2018 г. (4) подробно описали, что в 1939 г. Бакстон утверждал, что появление неспецифического ответа может быть преодолено за счет использования синтетической питательной среды и преципитации при производстве туберкулина, и что Бакстон и Гловер приписали точность 87–97% туберкулиновой пробы и рекомендовал использование синтетической среды туберкулина. Первая инструкция по проведению СИКТТ выпущена в 1942 году и подробно описывала проведение СИКТТ для сравнения клеточно-опосредованных иммунных ответов на отдельные внутрикожные инъекции птиц ( М.avium ) и сначала у млекопитающих ( M.tuberculosis ), а затем у крупного рогатого скота ( M. bovis ) Туберкулин PPD у каждого животного для повышения специфичности теста в ответ на сохраняющиеся опасения по поводу возникновения неспецифического ответа у животные, по-видимому, не зараженные ТБ (ложноположительный результат) (4). В 1947 году Фрэнсис подтвердил, что интерпретация теста для SICTT и оптимальное время чтения были «основаны на очень большом количестве испытаний, за которыми последовало посмертных исследований» (4).
bovis ) Туберкулин PPD у каждого животного для повышения специфичности теста в ответ на сохраняющиеся опасения по поводу возникновения неспецифического ответа у животные, по-видимому, не зараженные ТБ (ложноположительный результат) (4). В 1947 году Фрэнсис подтвердил, что интерпретация теста для SICTT и оптимальное время чтения были «основаны на очень большом количестве испытаний, за которыми последовало посмертных исследований» (4).
В 1948 г. Патерсон описал штамм AN5 M. bovis , который рос так же энергично и с такой же производительностью на синтетической среде, как и M. tuberculosis (12). К 1950-м годам бычий туберкулиновый PPD, полученный из M. bovis штамма AN5, все чаще заменял туберкулиновый PPD млекопитающих, полученный из M. tuberculosis , и широко использовался для ликвидации bTB. Основным преимуществом бычьего туберкулина PPD было увеличение Se и Sp при диагностике туберкулеза у крупного рогатого скота по сравнению с туберкулином PPD млекопитающих. Отсюда переход к бычьему PPD в британских и ирландских программах ликвидации туберкулеза в середине 1970-х годов (15). В 1959 г. Патерсон описал туберкулин как наиболее важный диагностический агент в схемах ликвидации БТБ, и он остается таковым и сегодня (4, 16).
Отсюда переход к бычьему PPD в британских и ирландских программах ликвидации туберкулеза в середине 1970-х годов (15). В 1959 г. Патерсон описал туберкулин как наиболее важный диагностический агент в схемах ликвидации БТБ, и он остается таковым и сегодня (4, 16).
Эффективность — это мера активности туберкулинового PPD у животных, сенсибилизированных определенным микроорганизмом, по сравнению с эталонным стандартным туберкулиновым PPD (17). Ричи указал, что для эффективного теста жизненно важно использовать туберкулин с большей эффективностью, чем та, на которую реагирует большинство инфицированных животных (18).Использование сильнодействующего туберкулина крупного рогатого скота повышает чувствительность теста (19), и баланс доказательств, по-видимому, свидетельствует в пользу использования туберкулинового PPD достаточной силы для облегчения выявления максимально возможного числа инфицированных ТБ животных для эффективной ликвидации возбудителя. болезнь (3, 16). Таким образом, рекомендации МЭБ заключаются в том, что в рамках национальных кампаний по ликвидации ВТБ следует использовать дозы бычьего депрессивного протеина до 50 000 МЕ/мл (20). Часто высказываются опасения, что использование сильнодействующего туберкулинового PPD снизит специфичность туберкулиновых тестов и увеличит количество ложноположительных результатов.Однако опыт Ирландии, где тест Sp был математически продемонстрирован в принятой нездоровой популяции как минимум 99,95%, означает, что только доля 1% положительных реакций на SICTT является ложноположительной и где надежность (индекс диагностической способности теста) SICTT определялся как в 1992, так и в 2011 году в районе 97%, что свидетельствует о том, что эти опасения не оправдались (20). Экспериментальные исследования, проведенные в Великобритании с инъекцией туберкулёзному и нетуберкулезному крупному рогатому скоту различных доз PPD, показали, что чем сильнее туберкулин, тем лучше дифференциация специфических реакций (из-за M.bovis ) и неспецифические реакции. (21). В 1993 г. д-р Луис О’Рейли, глава Ирландской центральной ветеринарной исследовательской лаборатории по туберкулезу, в отчете (неопубликованном) об оценке эффективности и ложноположительных результатов в ирландской программе ликвидации ВТБ указал, что когда голландский туберкулин с заявленной эффективностью 40 000 МЕ / мл, которая при анализе на ирландский туберкулез показал, что 40–50 000 МЕ / мл использовалась в Ирландии в период с мая 1979 г.
Часто высказываются опасения, что использование сильнодействующего туберкулинового PPD снизит специфичность туберкулиновых тестов и увеличит количество ложноположительных результатов.Однако опыт Ирландии, где тест Sp был математически продемонстрирован в принятой нездоровой популяции как минимум 99,95%, означает, что только доля 1% положительных реакций на SICTT является ложноположительной и где надежность (индекс диагностической способности теста) SICTT определялся как в 1992, так и в 2011 году в районе 97%, что свидетельствует о том, что эти опасения не оправдались (20). Экспериментальные исследования, проведенные в Великобритании с инъекцией туберкулёзному и нетуберкулезному крупному рогатому скоту различных доз PPD, показали, что чем сильнее туберкулин, тем лучше дифференциация специфических реакций (из-за M.bovis ) и неспецифические реакции. (21). В 1993 г. д-р Луис О’Рейли, глава Ирландской центральной ветеринарной исследовательской лаборатории по туберкулезу, в отчете (неопубликованном) об оценке эффективности и ложноположительных результатов в ирландской программе ликвидации ВТБ указал, что когда голландский туберкулин с заявленной эффективностью 40 000 МЕ / мл, которая при анализе на ирландский туберкулез показал, что 40–50 000 МЕ / мл использовалась в Ирландии в период с мая 1979 г. по апрель 1991 г. проблем со специфичностью теста не возникало.Он также прокомментировал, что «очень маловероятно, что использование более мощного бычьего PPD приведет к большему количеству ложноположительных реакций. На самом деле количество ложноположительных срабатываний должно уменьшиться». Использование сильнодействующего бычьего туберкулина PPD, очевидно, не было проблемой для Ирландии, где, несмотря на дополнительное использование вспомогательных испытаний и более строгую интерпретацию испытаний, количество реакторов, как правило, снижалось с 2000 г. (22–24). Действительно, в самом последнем тендере на поставку туберкулина PPD (от 17 мая 2019 г.) для ирландской программы указано, что активность «Жидкого туберкулина PPD для крупного рогатого скота» «не должна быть <50 000 МЕ/мл» у больных туберкулезом крупного рогатого скота (для обеспечения эффективности как анализировалось и использовалось в программе искоренения за последние 10 лет)» (25).Аналогичным образом, в Великобритании, где используется та же комбинация Tuberculin PPD в SICTT, что и в Ирландии, Goodchild et al.
по апрель 1991 г. проблем со специфичностью теста не возникало.Он также прокомментировал, что «очень маловероятно, что использование более мощного бычьего PPD приведет к большему количеству ложноположительных реакций. На самом деле количество ложноположительных срабатываний должно уменьшиться». Использование сильнодействующего бычьего туберкулина PPD, очевидно, не было проблемой для Ирландии, где, несмотря на дополнительное использование вспомогательных испытаний и более строгую интерпретацию испытаний, количество реакторов, как правило, снижалось с 2000 г. (22–24). Действительно, в самом последнем тендере на поставку туберкулина PPD (от 17 мая 2019 г.) для ирландской программы указано, что активность «Жидкого туберкулина PPD для крупного рогатого скота» «не должна быть <50 000 МЕ/мл» у больных туберкулезом крупного рогатого скота (для обеспечения эффективности как анализировалось и использовалось в программе искоренения за последние 10 лет)» (25).Аналогичным образом, в Великобритании, где используется та же комбинация Tuberculin PPD в SICTT, что и в Ирландии, Goodchild et al. (26) утверждает, что в Великобритании SICTT Sp на уровне животных составляет 99,87% (сверхтяжелая интерпретация), и что 91,1–93,7% реакторов в Великобритании действительно заражены туберкулезом, что демонстрирует, что SICTT, даже с использованием высокоэффективного бычьего PPD, как показано анализом крупного рогатого скота (таблица 1) сохраняет очень высокий Sp с небольшим числом ложноположительных респондентов.
(26) утверждает, что в Великобритании SICTT Sp на уровне животных составляет 99,87% (сверхтяжелая интерпретация), и что 91,1–93,7% реакторов в Великобритании действительно заражены туберкулезом, что демонстрирует, что SICTT, даже с использованием высокоэффективного бычьего PPD, как показано анализом крупного рогатого скота (таблица 1) сохраняет очень высокий Sp с небольшим числом ложноположительных респондентов.
Таблица 1 . Анализы PPD с бычьим туберкулином у крупного рогатого скота, инфицированного естественным путем ТБ: 2010–2017 гг., PPD, используемые в ирландской программе; 2006, 2010 и 2018 годы, INBS и BIS; 2004, 2008, испытания с использованием PPD в туберкулиновых тестах.
Международные стандарты
Чтобы обеспечить единообразие в производстве и использовании Tuberculin PPD во всем мире, ВОЗ установила Международные биологические стандарты эффективности туберкулинов. В 1952 г. ВОЗ установила международный стандарт (IS) для туберкулинового PPD млекопитающих (человека), приготовленного с использованием M. tuberculosis , с установленной активностью 50 000 МЕ на мг (17, 28). Точно так же IS для птичьего туберкулина PPD с назначенной активностью 50 000 I.ед. на мг была установлена ВОЗ в 1954 г. (29). Исследования, проведенные в 1995 г., показали, что качество птичьего туберкулина PPD является удовлетворительным как с точки зрения активности, так и специфичности на массу, и этот же стандарт используется до сих пор (29). Эффективность потенциального туберкулинового PPD затем определяют путем сравнения кожных реакций (после внутрикожной инъекции) с реакциями, вызываемыми соответствующим эталонным стандартным туберкулиновым PPD с известной активностью у животных, сенсибилизированных соответствующим антигеном.Таким образом, активность бычьего туберкулина PPD оценивается с использованием животных, сенсибилизированных к M. bovis , а эффективность птичьего туберкулина PPD оценивается на животных, сенсибилизированных к M. avium . Эффективность выражается в международных единицах (МЕ) на мл; это позволяет сравнивать туберкулины во всем мире.
tuberculosis , с установленной активностью 50 000 МЕ на мг (17, 28). Точно так же IS для птичьего туберкулина PPD с назначенной активностью 50 000 I.ед. на мг была установлена ВОЗ в 1954 г. (29). Исследования, проведенные в 1995 г., показали, что качество птичьего туберкулина PPD является удовлетворительным как с точки зрения активности, так и специфичности на массу, и этот же стандарт используется до сих пор (29). Эффективность потенциального туберкулинового PPD затем определяют путем сравнения кожных реакций (после внутрикожной инъекции) с реакциями, вызываемыми соответствующим эталонным стандартным туберкулиновым PPD с известной активностью у животных, сенсибилизированных соответствующим антигеном.Таким образом, активность бычьего туберкулина PPD оценивается с использованием животных, сенсибилизированных к M. bovis , а эффективность птичьего туберкулина PPD оценивается на животных, сенсибилизированных к M. avium . Эффективность выражается в международных единицах (МЕ) на мл; это позволяет сравнивать туберкулины во всем мире. Международная единица – это мера биологической активности в установленном количестве ИС (17).
Международная единица – это мера биологической активности в установленном количестве ИС (17).
В 1964 году ЕЭС приняла Голландский национальный стандарт крупного рогатого скота, приготовленный из культур М.bovis , штамм AN5, в качестве стандарта EEC для бычьего туберкулина PPD и присвоил ему мощность 50 000 единиц, называемую Community Tuberculin Units (CTU) (30, 31). Рабочая группа EEC показала, что человеческий туберкулин PPD IS не подходит для оценки эффективности бычьего туберкулина PPD из-за различных характеристик реакции на дозу обоих туберкулинов (32).
В 1976 г. ВОЗ начала оценку потенциальных депрессоров туберкулина крупного рогатого скота, чтобы выбрать новый международный стандартный депрессор туберкулина крупного рогатого скота (BIS) (30).В 1986 г. в качестве BIS был принят голландский бычий туберкулин PPD, полученный в 1979 г. из культур M. bovis , штамм AN5. Международные совместные анализы на крупном рогатом скоте и морских свинках в сравнении со старым голландским стандартом туберкулина крупного рогатого скота (1964 г. ) установили, что этот новый BIS имел эффективность 32 500 КТЕ/мл и что КТЕ и МЕ для туберкулина крупного рогатого скота эквивалентны (31).
) установили, что этот новый BIS имел эффективность 32 500 КТЕ/мл и что КТЕ и МЕ для туберкулина крупного рогатого скота эквивалентны (31).
Руководство МЭБ по диагностическим тестам и вакцинам для наземных животных 2018 г. (20) со ссылкой на серию технических отчетов ВОЗ 1968 г. №.384 (33) говорится, что «испытание эффективности следует проводить на животных и в условиях, в которых туберкулины будут использоваться на практике». Он также ссылается на серию технических отчетов ВОЗ № 745 (34) за 1985 г., в которой указывается, что калибровка лабораторных (внутренних) «эталонных препаратов должна проводиться посредством ряда испытаний» в соответствии с соответствующими IS на «видах животных, у которых следует использовать туберкулин» и что «контроль активности последовательных партий может быть затем проведен с помощью биологических анализов на морских свинках с использованием лабораторного эталонного препарата.В отчете Комитета экспертов ВОЗ за 2007 г. по выбору и использованию основных лекарственных средств (35) также содержится требование о том, чтобы все туберкулины соответствовали Серии технических отчетов ВОЗ № 745 (34). Далее в Руководстве МЭБ (20) говорится, что «бычий туберкулин следует анализировать у естественно зараженного туберкулезом крупного рогатого скота. Поскольку это требование трудновыполнимо, рутинная проверка потенции проводится на морских свинках. Однако необходимы периодические испытания на туберкулезном скоте, а стандартные препараты всегда требуют калибровки на крупном рогатом скоте» (20).Кроме того, рутинное использование крупного рогатого скота для целей анализа потенции может быть как непрактичным, так и дорогостоящим из-за отсутствия естественно инфицированного крупного рогатого скота или затрат, связанных с лабораторным заражением, поэтому в качестве альтернативы используются морские свинки. Патерсон рекомендовал использовать морских свинок для контроля при приготовлении/производстве с периодическими контрольными анализами на крупном рогатом скоте, но при изменении типа туберкулина или при подозрении на изменение свойств следует обращаться к анализу на крупном рогатом скоте (12).
Далее в Руководстве МЭБ (20) говорится, что «бычий туберкулин следует анализировать у естественно зараженного туберкулезом крупного рогатого скота. Поскольку это требование трудновыполнимо, рутинная проверка потенции проводится на морских свинках. Однако необходимы периодические испытания на туберкулезном скоте, а стандартные препараты всегда требуют калибровки на крупном рогатом скоте» (20).Кроме того, рутинное использование крупного рогатого скота для целей анализа потенции может быть как непрактичным, так и дорогостоящим из-за отсутствия естественно инфицированного крупного рогатого скота или затрат, связанных с лабораторным заражением, поэтому в качестве альтернативы используются морские свинки. Патерсон рекомендовал использовать морских свинок для контроля при приготовлении/производстве с периодическими контрольными анализами на крупном рогатом скоте, но при изменении типа туберкулина или при подозрении на изменение свойств следует обращаться к анализу на крупном рогатом скоте (12). .
.
Из-за ограниченного предложения BIS ЕС и МЭБ рекомендовали откалибровать национальные и «внутренние» стандартные туберкулиновые PPD по BIS, а затем широко использовать для национальных и рутинных производственных анализов активности. В 1994 году на заводе CVL в Лелистаде был произведен Ирландский национальный стандарт туберкулина для крупного рогатого скота (INBS), и до сих пор имеются значительные запасы. Калибровка по BIS, как у морских свинок, сенсибилизированных живым M. bovis , так и у естественно сенсибилизированного крупного рогатого скота, показала, что INBS имеет эффективность 33 700 МЕ/мл (26).В 2018 году Франкена и соавт. (36) предложили новую модель для калибровки национальных и «внутренних» эталонных стандартов для максимально точного использования 30 естественно инфицированных ТБ голов крупного рогатого скота (целевые виды) и для подтверждения точности и правильности оценки эффективности с использованием 54 морских свинок в 6 отдельных случаях. анализы потенции. Вариабельность оценок эффективности можно уменьшить, повторив анализ на морской свинке 5 или более раз для каждого образца (36).
Вариабельность оценок эффективности можно уменьшить, повторив анализ на морской свинке 5 или более раз для каждого образца (36).
Производство и композиция туберкулинов
Tuberculin PPD был описан как нечетко определенная сложная смесь, содержащая более 100 отдельных компонентов на разных стадиях денатурации (37, 38).В зависимости от того, где будет использоваться Tuberculin PPD или если он предназначен для экспорта на международные рынки, его спецификация должна соответствовать требованиям соответствующих международных стандартов, установленных ВОЗ, МЭБ и законодательными требованиями ЕС (2, 20, 35, 39). Туберкулины должны быть стерильными и не иметь аномальной токсичности. Они также должны быть неантигенными, т. е. не сенсибилизирующими при введении, чтобы не вызывать реакции при последующих введениях у животных, свободных от ТБ. Тесты на стерильность, безопасность и сенсибилизирующий эффект изложены в Руководстве МЭБ по диагностическим тестам и вакцинам для наземных животных 2018 г. (20).
(20).
Потенциал
В процессе производства производители должны определять и контролировать активность партий туберкулина у морских свинок по эталонному стандарту (34, 35). Тем не менее, морские свинки и крупный рогатый скот имеют разные отношения доза-эффект, и, кроме того, часто наблюдается лишь ограниченное согласие между анализами эффективности на морских свинках и крупном рогатом скоте (31, 40, 41) (таблица 1). Точность оценки потенции и соответствие между расчетами, выполненными на морских свинках и крупном рогатом скоте, можно улучшить, но за счет нежелательных затрат на проведение повторных анализов с использованием большего количества крупного рогатого скота и большего количества морских свинок (5, 28, 36).Степень вариабельности биотестирования на морских свинках обсуждалась ранее (38, 42). Признавая эту проблему, Директива 64/432/ЕЕС (2015) (2) требует, чтобы доверительные пределы погрешности ( P = 0,95) составляли не <50% и не более 200% расчетной эффективности. Расчетная активность должна быть не <75% и не более 133% от заявленной активности для птичьего туберкулина и не <66% и не более 150% от заявленной активности для туберкулина крупного рогатого скота и соответствовать Директиве 2001/82/ ЕС (2, 43).Содержание туберкулопротеина в M. bovis Tuberculin PPD регулируется на основе анализа эффективности на морских свинках для достижения целевой эффективности не <20 000 МЕ на мл в каждой партии конечного продукта. МЭБ рекомендует для БД туберкулина следующее: « Крупному рогатому скоту с пониженной аллергической чувствительностью необходима более высокая доза туберкулина крупного рогатого скота, а в национальных кампаниях по ликвидации рекомендуются дозы до 5000 МЕ (т. е. 50 000 МЕ на мл) Таким образом, производители могут искать и производить бычий туберкулин PPD с целевой активностью, превышающей 20 000 МЕ на мл (20).
Расчетная активность должна быть не <75% и не более 133% от заявленной активности для птичьего туберкулина и не <66% и не более 150% от заявленной активности для туберкулина крупного рогатого скота и соответствовать Директиве 2001/82/ ЕС (2, 43).Содержание туберкулопротеина в M. bovis Tuberculin PPD регулируется на основе анализа эффективности на морских свинках для достижения целевой эффективности не <20 000 МЕ на мл в каждой партии конечного продукта. МЭБ рекомендует для БД туберкулина следующее: « Крупному рогатому скоту с пониженной аллергической чувствительностью необходима более высокая доза туберкулина крупного рогатого скота, а в национальных кампаниях по ликвидации рекомендуются дозы до 5000 МЕ (т. е. 50 000 МЕ на мл) Таким образом, производители могут искать и производить бычий туберкулин PPD с целевой активностью, превышающей 20 000 МЕ на мл (20).
Метод сенсибилизации морских свинок к антигенам M. bovis может повлиять на результаты анализа активности.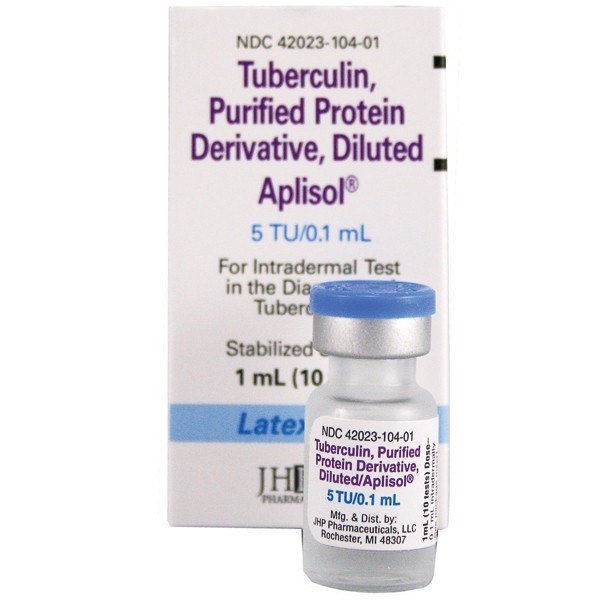 Неоднократно исследования показывали, что наиболее тесная корреляция с анализами крупного рогатого скота достигается при сенсибилизации морских свинок живым M. bovis , т. е. при фактическом заражении этих морских свинок M. bovis (32, 44, 45). Сенсибилизация морских свинок убитыми нагреванием M. bovis или живыми M. bovis БЦЖ дает менее надежные результаты, предположительно потому, что не вырабатывается полный набор антигенов, выделяемых на стадиях размножения микобактерий активной инфекции.Точно так же анализы эффективности, проведенные на крупном рогатом скоте, сенсибилизированном умерщвленным нагреванием M. bovis , ненадежны (46). Крупный рогатый скот, экспериментально инфицированный живым M. bovis , подходит для анализа активности, как и крупный рогатый скот, инфицированный естественным путем. Преимущество использования естественно инфицированного крупного рогатого скота из полевых случаев заражения bTB заключается в том, что это представляет более полный спектр воздействия и стадий инфекции, которые будут иметь место при естественной инфекции, чем использование группы однородно инфицированного крупного рогатого скота.
Неоднократно исследования показывали, что наиболее тесная корреляция с анализами крупного рогатого скота достигается при сенсибилизации морских свинок живым M. bovis , т. е. при фактическом заражении этих морских свинок M. bovis (32, 44, 45). Сенсибилизация морских свинок убитыми нагреванием M. bovis или живыми M. bovis БЦЖ дает менее надежные результаты, предположительно потому, что не вырабатывается полный набор антигенов, выделяемых на стадиях размножения микобактерий активной инфекции.Точно так же анализы эффективности, проведенные на крупном рогатом скоте, сенсибилизированном умерщвленным нагреванием M. bovis , ненадежны (46). Крупный рогатый скот, экспериментально инфицированный живым M. bovis , подходит для анализа активности, как и крупный рогатый скот, инфицированный естественным путем. Преимущество использования естественно инфицированного крупного рогатого скота из полевых случаев заражения bTB заключается в том, что это представляет более полный спектр воздействия и стадий инфекции, которые будут иметь место при естественной инфекции, чем использование группы однородно инфицированного крупного рогатого скота.
Специфичность каждой производственной партии бычьего туберкулина PPD оценивается на морских свинках, сенсибилизированных инактивированным нагреванием M. avium по методу Фишера (46). Реакции кожи, вызванные PPD крупного рогатого скота, сравнивают с реакцией IS на PPD птиц. Специфичность PPD туберкулина птиц оценивается на морских свинках, сенсибилизированных живым M. bovis , с использованием той же методики.
Paterson, Haagsma et al., ВОЗ и МЭБ рекомендовали в качестве эффективной практики периодически проверять результаты анализов активности морских свинок путем оценки активности части производственных партий у естественно или искусственно инфицированного крупного рогатого скота (12, 20, 29). –33).Однако, несмотря на то, что это может быть хорошей практикой и было предусмотрено в первоначальной Директиве 64/432/ЕЕС (1964) (47), а в 1979 г. эксперты подгруппы ЕС Научно-ветеринарной комиссии по туберкулины (32), он был исключен при внесении изменений в Директиву 64/432/ЕЭС в 2002 г. (Регламент Комиссии 2002 г.). Руководство МЭБ по диагностическим тестам и вакцинам для наземных животных (Глава 2.4.6 — Туберкулез крупного рогатого скота) (20) по-прежнему содержит рекомендацию о проведении анализа эффективности у крупного рогатого скота, больного туберкулезом, при этом делается ссылка на серию технических отчетов ВОЗ No.745 (34).
(Регламент Комиссии 2002 г.). Руководство МЭБ по диагностическим тестам и вакцинам для наземных животных (Глава 2.4.6 — Туберкулез крупного рогатого скота) (20) по-прежнему содержит рекомендацию о проведении анализа эффективности у крупного рогатого скота, больного туберкулезом, при этом делается ссылка на серию технических отчетов ВОЗ No.745 (34).
Несмотря на попытки ВОЗ, МЭБ и ЕС стандартизировать производство, оценку качества и эффективности туберкулиновых депрессорных пар, качественные и количественные различия между туберкулиновыми депрессорами разных производителей существуют. Эти различия возникают из-за различных факторов, таких как различия в расположении производственных мощностей, возможные различия в средах для выращивания и штаммах производственного посевного материала. Различия в методах калибровки потенции производителя, включая опыт персонала и внимание к деталям, а также качество используемого эталонного стандарта, могут повлиять на оцениваемую потенцию у морских свинок и, как следствие, на потенцию у крупного рогатого скота.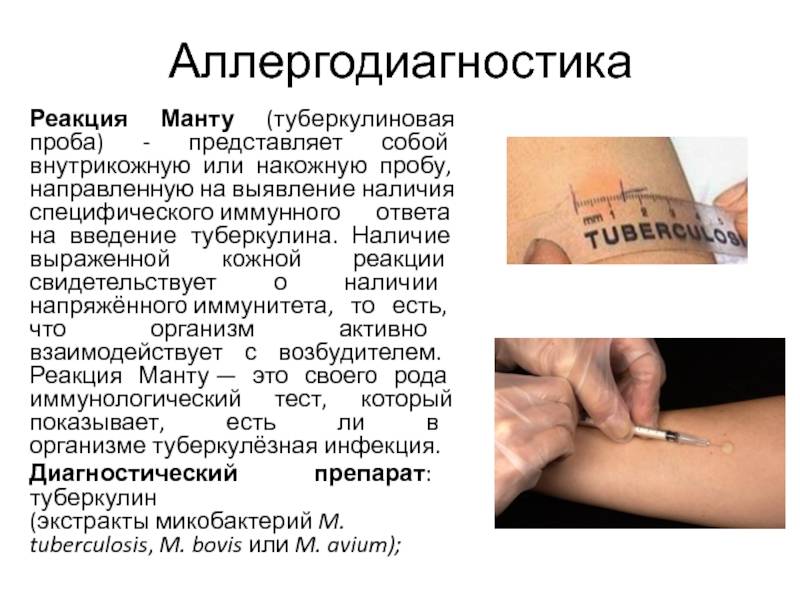 Кроме того, средства сенсибилизации морских свинок и количество морских свинок, использованных производителем для анализа, будут влиять на точность оценки активности и в дальнейшем приводить к межлабораторным различиям в оценках активности. Эти различия приводят к большим различиям как в содержании белка, так и в антигенном профиле, и, таким образом, следует ожидать различий в активности и специфичности между различными продуктами туберкулиновой PPD, а также относительной активности птичьих и бычьих туберкулиновых PPD, используемых для SICTT, и Анализ интерферона-γ (IFN-γ) будет влиять на эффективность теста, Se, Sp и прогностическую ценность (44, 48–52).
Кроме того, средства сенсибилизации морских свинок и количество морских свинок, использованных производителем для анализа, будут влиять на точность оценки активности и в дальнейшем приводить к межлабораторным различиям в оценках активности. Эти различия приводят к большим различиям как в содержании белка, так и в антигенном профиле, и, таким образом, следует ожидать различий в активности и специфичности между различными продуктами туберкулиновой PPD, а также относительной активности птичьих и бычьих туберкулиновых PPD, используемых для SICTT, и Анализ интерферона-γ (IFN-γ) будет влиять на эффективность теста, Se, Sp и прогностическую ценность (44, 48–52).
Ирландская программа ликвидации туберкулеза
В Ирландии bTB вызывается преимущественно инфекцией M. bovis . Департамент сельского хозяйства, продовольствия и морских ресурсов (DAFM) руководит ирландской программой ликвидации ВТБ, которая включает в себя ежегодный скрининг всех стад крупного рогатого скота, оперативное удаление животных с положительным тестом (реакторов) и животных, удаленных по эпидемиологическим причинам ветеринарным инспектором, или животных, удаленных после результаты дополнительных анализов крови, таких как анализ на интерферон-гамма (IFN-γ), послеубойное наблюдение практикующими ветеринарными врачами за всеми тушами крупного рогатого скота при забое для употребления в пищу человеком, ограничения на передвижение и дальнейшее последующее тестирование инфицированных стад (22– 24). Гуд и др. в 2011 г. заявляют, что около 7% крупного рогатого скота дали положительный результат при однократном внутрикожном тесте, но не при SICTT, и что различные патогенные микобактерии, например, Mycobacterium paratuberculosis subsp. avium и непатогенные микобактерии из окружающей среды, такие как M. hiberniae , широко распространены в ирландской среде и вызывают неспецифическую сенсибилизацию к бычьему туберкулину PPD (20, 53). Соответственно, SICTT является основным скрининговым тестом, используемым в программе, и включает в себя ~8.5 миллионов тестов на животных каждый год (7, 22–24). Внутрикожные инъекции 0,1 мл птичьего (25 000 МЕ/мл) и бычьего (30 000 МЕ/мл) туберкулинового PPD, оцененного на морских свинках (поставляется Prionics, Lelystad B.V.), вводят в среднюю треть шеи; Толщина кожи в месте испытания регистрируется во время инъекции и при измерении через 72 часа [±4 часа]. Характер любой реакции и относительное увеличение (измеряемое в миллиметрах) толщины кожной складки в каждом месте инъекции оценивают при тестировании.
Гуд и др. в 2011 г. заявляют, что около 7% крупного рогатого скота дали положительный результат при однократном внутрикожном тесте, но не при SICTT, и что различные патогенные микобактерии, например, Mycobacterium paratuberculosis subsp. avium и непатогенные микобактерии из окружающей среды, такие как M. hiberniae , широко распространены в ирландской среде и вызывают неспецифическую сенсибилизацию к бычьему туберкулину PPD (20, 53). Соответственно, SICTT является основным скрининговым тестом, используемым в программе, и включает в себя ~8.5 миллионов тестов на животных каждый год (7, 22–24). Внутрикожные инъекции 0,1 мл птичьего (25 000 МЕ/мл) и бычьего (30 000 МЕ/мл) туберкулинового PPD, оцененного на морских свинках (поставляется Prionics, Lelystad B.V.), вводят в среднюю треть шеи; Толщина кожи в месте испытания регистрируется во время инъекции и при измерении через 72 часа [±4 часа]. Характер любой реакции и относительное увеличение (измеряемое в миллиметрах) толщины кожной складки в каждом месте инъекции оценивают при тестировании. Любое животное, у которого проявляются клинические признаки в месте инъекции бычьего туберкулина, такие как отек, экссудативный некроз, жар и/или боль, в ответ на инъекцию туберкулина крупного рогатого скота, при считывании теста считается положительным и, следовательно, «реактором» независимо от относительного увеличение в соответствии с Директивой 64/432/ЕЭС (2015 г.) (2). В конце 1970-х годов Ирландия столкнулась с проблемами низкой активности туберкулина, поставляемого для программы. Впоследствии, в 1980 г., Ирландия сменила поставщика Tuberculin PPD и разработала строгие критерии для своих требований, а также в качестве меры контроля качества включила анализ активности на естественно инфицированном крупном рогатом скоте (23, 24).
Любое животное, у которого проявляются клинические признаки в месте инъекции бычьего туберкулина, такие как отек, экссудативный некроз, жар и/или боль, в ответ на инъекцию туберкулина крупного рогатого скота, при считывании теста считается положительным и, следовательно, «реактором» независимо от относительного увеличение в соответствии с Директивой 64/432/ЕЭС (2015 г.) (2). В конце 1970-х годов Ирландия столкнулась с проблемами низкой активности туберкулина, поставляемого для программы. Впоследствии, в 1980 г., Ирландия сменила поставщика Tuberculin PPD и разработала строгие критерии для своих требований, а также в качестве меры контроля качества включила анализ активности на естественно инфицированном крупном рогатом скоте (23, 24).
Требования туберкулиновой PPD для Ирландской программы ликвидации туберкулеза
В соответствии с законодательством Ирландии единственным туберкулином, который может использоваться в ирландской программе ликвидации bTB, является туберкулин, поставляемый DAFM.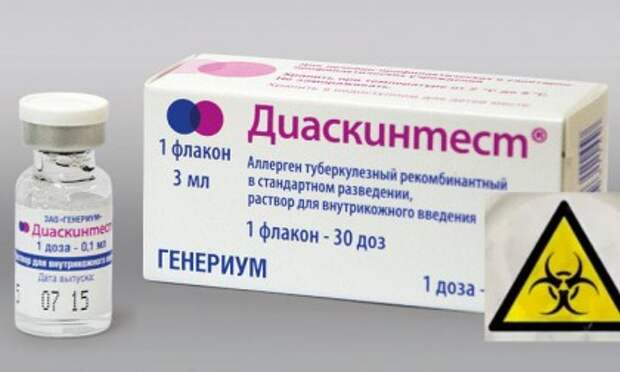 Он должен иметь регистрационное удостоверение (MA) от Регуляторного органа по охране здоровья (HPRA) в Ирландии в соответствии с законодательством ЕС (39, 54). Prionics Lelystad BV (ранее Lelystad Biologicals BV или ID-Lelystad BV) в Лелистаде, Нидерланды, поставила туберкулин PPD для птиц и крупного рогатого скота, используемый в ирландской программе с 1980 года по тендеру.
Он должен иметь регистрационное удостоверение (MA) от Регуляторного органа по охране здоровья (HPRA) в Ирландии в соответствии с законодательством ЕС (39, 54). Prionics Lelystad BV (ранее Lelystad Biologicals BV или ID-Lelystad BV) в Лелистаде, Нидерланды, поставила туберкулин PPD для птиц и крупного рогатого скота, используемый в ирландской программе с 1980 года по тендеру.
Спецификация
Приготовление, эффективность и маркировка Tuberculin PPD должны соответствовать статье 51 Директивы 2001/82/ЕС и директиве 91/412/ЕЕС (54). Хранить следует при температуре 4°C, но, в соответствии с регистрационным удостоверением (MA), он должен оставаться стабильным в течение 14 дней при температуре окружающей среды от +2°C до +37°C.
Эффективность
В соответствии с MA концентрация общего белка в Avian Tuberculin PPD 2500 должна составлять от 0,5 до 0,8 мг/мл, а в Bovine Tuberculin PPD 3000 — в пределах 1.0 и 1,4 мг/мл при этом одновременно:
— Бычий туберкулин PPD, поставляемый в рамках МА, должен иметь эффективность 3000 МЕ/доза для дозы 0,1 мл [66–150%, т. е. между 1980 МЕ и 4500 МЕ] при тестировании на морских свинках, сенсибилизированных живыми M. bovis , штамм AN5, а в последнем тендере на поставку туберкулина PPD (от 17 мая 2019 г.) «не менее 50 000» МЕ/мл «у крупного рогатого скота, больного туберкулезом» и что «активность будет определяться или от имени представителя закупающего органа и до приемки любой партии туберкулина по контракту» (25) и
е. между 1980 МЕ и 4500 МЕ] при тестировании на морских свинках, сенсибилизированных живыми M. bovis , штамм AN5, а в последнем тендере на поставку туберкулина PPD (от 17 мая 2019 г.) «не менее 50 000» МЕ/мл «у крупного рогатого скота, больного туберкулезом» и что «активность будет определяться или от имени представителя закупающего органа и до приемки любой партии туберкулина по контракту» (25) и
— Птичий туберкулин PPD должен иметь эффективность 2500 МЕ/доза для 0.1 мл дозы [75–133%, т. е. между 1875 МЕ и 3325 МЕ] на дозу при анализе на морских свинках, сенсибилизированных нагреванием, инактивированные M. avium и
— пары туберкулиновых PPD для SICTT не должны превышать максимальную разницу в активности 500 МЕ на дозу (с использованием эффективности, оцененной на морских свинках) между обоими (птичьим и бычьим туберкулином) в наборе Tuberculin PPD Kit.
Это заявленное требование к эффективности бычьего PPD превышает минимум 20 000 МЕ/мл, указанный в Директиве 64/432/EEC (2). Анализы проводятся на морских свинках, как указано в Директиве ЕС 64/432/ЕЕС (2), с использованием «эталонного препарата туберкулина (бычьего или птичьего, в зависимости от обстоятельств)» PPD, «откалиброванного в международных единицах» компанией или от ее имени. Прионикс Лелистад Б.В.
Анализы проводятся на морских свинках, как указано в Директиве ЕС 64/432/ЕЕС (2), с использованием «эталонного препарата туберкулина (бычьего или птичьего, в зависимости от обстоятельств)» PPD, «откалиброванного в международных единицах» компанией или от ее имени. Прионикс Лелистад Б.В.
Анализ активности крупного рогатого скота
Эффективность Bovine Tuberculin PPD 3000, поставляемого для использования в Ирландии, оценивается в Лелистаде на морских свинках, сенсибилизированных живыми M. bovis , относительно BIS PPD от имени производителя.Эффективность одной или нескольких поставляемых партий Tuberculin PPD ежегодно проверяется в Ирландии на естественно инфицированном крупном рогатом скоте по шкале INBS, которая была откалибрована в 1994 г. на крупном рогатом скоте и морских свинках (28). Эффективность туберкулиновых PPD, используемых в различных исследованиях туберкулинового тестирования в Ирландии, также оценивалась (19, 27). Туберкулин INBS также периодически анализируется против BIS у естественно инфицированного ирландского крупного рогатого скота в Ирландии и у морских свинок компанией Prionics Lelystad BV в соответствии с Директивой ЕС 64/432 (2). Недавний анализ, включающий INBS против BIS в 2018 году у естественно инфицированного ирландского крупного рогатого скота, показал эффективность 32 265, более ранний анализ в 2006 году показал эффективность 46 079, а анализ BIS против INBS в 2013 году показал эффективность 25 821. (Таблица 1). Результаты этих двух последних анализов вызвали некоторое беспокойство. Впоследствии на конференции M. bovis в Кардиффе в 2014 г. (55) сообщалось о проблемах, когда очевидные визуальные различия и даже невизуальное ухудшение BIS в некоторых ампулах, поставляемых NIBSC, приводили к получению сильно различающихся результатов анализа активности. у морских свинок при введении одинаковых количеств из разных флаконов.Д-р Баккер сообщил, что в испорченных флаконах BIS больше не был полностью растворим в воде и содержал различное количество крупных частиц, которые влияли на анализ активности, и хотя их можно было центрифугировать (3000 × g) и удалить, затем произошла потеря антигена ( 55). Следовательно, NIBSC удалил ампулы с видимым износом со своих складов, а МЭБ создало в 2015 году специальную рабочую группу с задачей найти новый источник бычьего PPD, и в настоящее время ведется работа по разработке нового BIS.
Недавний анализ, включающий INBS против BIS в 2018 году у естественно инфицированного ирландского крупного рогатого скота, показал эффективность 32 265, более ранний анализ в 2006 году показал эффективность 46 079, а анализ BIS против INBS в 2013 году показал эффективность 25 821. (Таблица 1). Результаты этих двух последних анализов вызвали некоторое беспокойство. Впоследствии на конференции M. bovis в Кардиффе в 2014 г. (55) сообщалось о проблемах, когда очевидные визуальные различия и даже невизуальное ухудшение BIS в некоторых ампулах, поставляемых NIBSC, приводили к получению сильно различающихся результатов анализа активности. у морских свинок при введении одинаковых количеств из разных флаконов.Д-р Баккер сообщил, что в испорченных флаконах BIS больше не был полностью растворим в воде и содержал различное количество крупных частиц, которые влияли на анализ активности, и хотя их можно было центрифугировать (3000 × g) и удалить, затем произошла потеря антигена ( 55). Следовательно, NIBSC удалил ампулы с видимым износом со своих складов, а МЭБ создало в 2015 году специальную рабочую группу с задачей найти новый источник бычьего PPD, и в настоящее время ведется работа по разработке нового BIS.
В Ирландии крупный рогатый скот для анализа отбирается в соответствии со Стандартными операционными процедурами для анализа туберкулиновой активности на ТБ крупного рогатого скота в изоляторе на исследовательской ферме DAFM, целью которых является обеспечение благополучия крупного рогатого скота и достоверность проводимых анализов. вне. Анализы крупного рогатого скота подпадают под строгие условия лицензирования отдельных проектов, которые выдаются и проверяются HPRA.
Крупный рогатый скот из зараженных туберкулезом ферм происхождения, давший положительный результат на SICTT, у которого увеличение толщины кожной складки в месте инъекции крупного рогатого скота более чем на 4 мм больше, чем увеличение при птичьей инъекции сайте и являются положительными по IFN-γ BOVIGAM ® (Prionics, Lelystad B.V.) анализ (56), выбраны для анализов в блоке изоляции. Для простоты обращения и содержания обычно выбирают молодых бычков в возрасте от ~ 6 месяцев до 2 лет. Интервал между SICTT на ферме происхождения и анализом эффективности должен составлять не менее 60 дней (57). Животных обычно содержат не более двух анализов или до года и при необходимости заменяют другими положительными полевыми тестами, как указано выше.
Животных обычно содержат не более двух анализов или до года и при необходимости заменяют другими положительными полевыми тестами, как указано выше.
Анализы эффективности на партиях стандартного туберкулинового PPD крупного рогатого скота проводятся по лицензии 2–3 раза в год в зависимости от наличия достаточного количества подходящего полевого реакторного скота.В каждом анализе эффективность трех выбранных тестовых партий оценивается по сравнению с IBNS бычьим туберкулином PPD с анализируемой эффективностью 33 700 МЕ/мл. Каждая ампула лиофилизированного IBNS содержит 1,8 мг PPD в глюкозо-фосфатном буфере, содержащем фенол (28). Готовят разведение до 1 мг/мл добавлением 1,8 мл дистиллированной воды. Изотонический фосфатно-солевой буфер, рН 7,3, используется для приготовления 20%-ных разведений всех туберкулиновых PPD для анализа, представляющих концентрацию белка 0,2 мг/мл (30).Каждый из 3 туберкулиновых PPD для анализа и сравнительный INBS и/или BIS, соответственно, используют в двух разведениях, соответствующих концентрациям белка 1,0 и 0,2 мг/мл.
Таким образом, имеется восемь препаратов туберкулина (4 неразбавленных и 4 разведенных), которые вводят каждому животному в четыре места на каждой стороне шеи, как показано на рис. 1. Расстояние между местами введения составляет ~10–12 см.
Рисунок 1 . Места инъекций с реакциями, показывающими последовательность инъекций/измерений, 1–4 (с каждой стороны шеи), для анализа PPD бычьего туберкулина.
Группа из восьми голов крупного рогатого скота должна поочередно чередовать все 8 инъекций (т. е. эталонный стандарт и 3 испытуемых PPD, каждая в двух разведениях) последовательно через каждое из восьми возможных мест на шее с использованием схемы латинского квадрата. Это необходимо для учета разной чувствительности на разных участках шеи крупного рогатого скота (12, 17). Туберкулиновые PPD распределяются по местам на основе рандомизированного графика, заранее изложенного в рабочих листах анализа. Для рутинных анализов используют три группы по восемь голов крупного рогатого скота, чтобы повысить надежность анализа до приемлемого уровня точности, т. е.э., по тем же причинам, что рекомендованы Frankena et al. для анализа на морских свинках (36). Для каждой группы используется отдельный рабочий лист, каждый с уникальным паттерном распределения туберкулиновых PPD по участкам шейки.
е.э., по тем же причинам, что рекомендованы Frankena et al. для анализа на морских свинках (36). Для каждой группы используется отдельный рабочий лист, каждый с уникальным паттерном распределения туберкулиновых PPD по участкам шейки.
Места инъекций вырезают и измеряют толщину кожной складки в каждом месте инъекции с помощью штангенциркуля с делением 1 мм в 0 ч. С помощью шприцев McLintock внутрикожно вводят по 0,1 мл каждого Tuberculin PPD. Все аспекты каждого теста (введение туберкулина, первоначальное и последующее измерение кожи) на каждом исследуемом животном проводятся одним и тем же ветеринаром.Каждое измерение толщины кожи в месте инъекции проводят и записывают через 0 и 72 часа. В таблице 2 показан пример данных измерения кожи, зарегистрированных для одной из 3 групп из 8 голов крупного рогатого скота в недавнем анализе.
Таблица 2 . Пример данных измерений в месте инъекции для группы из 8 быков в анализе активности бычьего туберкулина PPD.
Измерения, регистрирующие увеличение в различных местах инъекции для каждого анализируемого разведения PPD и эталонного стандарта, анализируются с использованием стандартных статистических методов для анализов с параллельными линиями (58) с использованием процедуры GLM в SAS v9.1 (59). Место инъекции и сторона шеи включаются в окончательную модель, если это значимо ( P <0,05). 95%-й доверительный интервал для относительной активности рассчитывают по методу Фишера (46). Этот анализ оценивает эффективность трех рутинных туберкулиновых PPD по сравнению с IBNS Tuberculin PPD (46). Активность выражается в МЕ/мл, исходя из активности INBS при 1,0 мг/мл 33 700 МЕ/мл, предварительно откалиброванной по BIS (28). В Таблице 3 показаны результаты анализа для анализа, указанного в Таблице 2.
Таблица 3 . Пример относительной активности и рассчитанных международных единиц для 3 испытуемых депрессорных доз туберкулина крупного рогатого скота в таблице 2.
Морские свинки и крупный рогатый скот имеют разные зависимости доза-эффект, и если не использовать несколько групп крупного рогатого скота и морских свинок, то точность оценки эффективности и корреляция эффективности между видами будут плохими (11, 28, 29, 32, 36, 54, 60). ). Несмотря на многочисленные анализы для каждого вида, активность, оцененная на морской свинке (пять анализов, каждый с 9 морскими свинками), отличается от таковой, полученной при анализе крупного рогатого скота (три анализа, каждый с 8 головами крупного рогатого скота), о чем свидетельствуют результаты, представленные в таблице 1.По крайней мере, некоторые различия, вероятно, связаны с тем, что BIS используется в качестве эталонного стандарта для анализа на морских свинках. BIS, как указывалось ранее, ухудшается по сравнению с периодом до 2005 года, когда о нем впервые было опубликовано (36), и с тех пор дает сильно различающиеся результаты анализа активности на морских свинках при введении одинаковых количеств из разных флаконов (55). Тем не менее, последовательные анализы показали (Таблица 1), что партии, которые соответствуют требуемой активности 30 000 [66–150%] МЕ/мл в анализах на морских свинках, также достигли или превзошли эту эффективность при анализе на крупном рогатом скоте и действительно в последние годы часто достигают или превышает мощность, рекомендованную МЭБ для использования в программах ликвидации bTB.Судя по результатам, представленным в таблице 1, представляется вероятным, что результаты анализа на морских свинках занижают эффективность анализируемых PPD на различные количества, что, скорее всего, зависит от степени ухудшения BIS во флаконе, использованном для анализа.
Тем не менее, последовательные анализы показали (Таблица 1), что партии, которые соответствуют требуемой активности 30 000 [66–150%] МЕ/мл в анализах на морских свинках, также достигли или превзошли эту эффективность при анализе на крупном рогатом скоте и действительно в последние годы часто достигают или превышает мощность, рекомендованную МЭБ для использования в программах ликвидации bTB.Судя по результатам, представленным в таблице 1, представляется вероятным, что результаты анализа на морских свинках занижают эффективность анализируемых PPD на различные количества, что, скорее всего, зависит от степени ухудшения BIS во флаконе, использованном для анализа.
Обсуждение
Еще в 1908 г. сетовали на то, что «некоторые туберкулины на рынке бесполезны и бесполезны», и Бакстон также комментировал качество туберкулина в 1934 г. (60–63). В 2011 году Гуд (19) сравнил «влияние разных активностей одного туберкулина бычьего PPD на полевые показатели» SICTT и SIT и обнаружил «существенную разницу в количестве реакций, обнаруженных при использовании туберкулинов высокой и низкой активности. Это исследование также показало, что туберкулин с низкой активностью, хотя и не самый низкий из обнаруженных в продаже, не смог обнаружить животных, которые из-за отрицательной реакции в месте инъекции крупного рогатого скота индивидуально соответствовали бы сертификации МЭБ как не содержащие bTB для экспортных целей, несмотря на то, что впоследствии обнаружены множественные туберкулезные поражения, видимые при рутинном убое (3, 5, 19).
Это исследование также показало, что туберкулин с низкой активностью, хотя и не самый низкий из обнаруженных в продаже, не смог обнаружить животных, которые из-за отрицательной реакции в месте инъекции крупного рогатого скота индивидуально соответствовали бы сертификации МЭБ как не содержащие bTB для экспортных целей, несмотря на то, что впоследствии обнаружены множественные туберкулезные поражения, видимые при рутинном убое (3, 5, 19).
Когда Великобритания (Великобритания) перешла с использования Weybridge Tuberculin PPD на Dutch Tuberculin PPD, было обнаружено, что источник производства туберкулина повлиял как на Se, так и на Sp SICTT (63).Данные международных исследований показывают, что диапазон чувствительности на уровне отдельных животных составляет 68–96,8 % и специфичность 96–98,8 % для CFT (чувствительность 80–91 % и специфичность 75,5–96,8 %), для SIT и для SICTT ( 55,1–93,5% чувствительности и 88,8–100% специфичности) (7, 60, 64). Каудальная складка неоднократно определялась как наименее чувствительное место, доступное для внутрикожного теста, и, следовательно, CFT требует более сильнодействующего туберкулина для достижения приемлемого Se для использования в программах контроля/ликвидации BTB; средняя треть шеи оказалась наиболее чувствительным участком для внутрикожного теста (4). Различия в чувствительности и специфичности теста в значительной степени связаны с распространенностью bTB, различиями в методах тестирования, различиями в дозах туберкулина, туберкулиновыми PPD с различными антигенными профилями, активностью туберкулиновой PPD, относительной эффективностью птичьих и бычьих PPD в сравнительном тесте, интерпретацией результатов. кожные реакции и преобладание неспецифических или перекрестно-реактивных антигенов в окружающей среде (19, 23, 38, 50). Различные результаты различных исследований объясняются множеством факторов, в том числе различиями в дизайне исследований, отбором животных на разных стадиях инфекции, частотой тестирования и, что наиболее важно, тем, как определялся инфекционный статус животных.На специфичность теста будет влиять сенсибилизация к микобактериям окружающей среды или другим организмам, имеющим общие антигены с M. bovis (65). Уровень перекрестной сенсибилизации будет варьироваться от региона к региону. В Ирландии контакт крупного рогатого скота с многочисленными микобактериями окружающей среды может привести к перекрестным реакциям на бычий PPD (53), тем не менее, как указывалось ранее, надежность SICTT, являющегося относительно грубым показателем диагностической способности теста, основанного на Se и Sp теста в среде, в которой он используется, оценивается как находящаяся в районе 97% (20, 66).
Различия в чувствительности и специфичности теста в значительной степени связаны с распространенностью bTB, различиями в методах тестирования, различиями в дозах туберкулина, туберкулиновыми PPD с различными антигенными профилями, активностью туберкулиновой PPD, относительной эффективностью птичьих и бычьих PPD в сравнительном тесте, интерпретацией результатов. кожные реакции и преобладание неспецифических или перекрестно-реактивных антигенов в окружающей среде (19, 23, 38, 50). Различные результаты различных исследований объясняются множеством факторов, в том числе различиями в дизайне исследований, отбором животных на разных стадиях инфекции, частотой тестирования и, что наиболее важно, тем, как определялся инфекционный статус животных.На специфичность теста будет влиять сенсибилизация к микобактериям окружающей среды или другим организмам, имеющим общие антигены с M. bovis (65). Уровень перекрестной сенсибилизации будет варьироваться от региона к региону. В Ирландии контакт крупного рогатого скота с многочисленными микобактериями окружающей среды может привести к перекрестным реакциям на бычий PPD (53), тем не менее, как указывалось ранее, надежность SICTT, являющегося относительно грубым показателем диагностической способности теста, основанного на Se и Sp теста в среде, в которой он используется, оценивается как находящаяся в районе 97% (20, 66).
Немногие исследования, если таковые имеются, обсуждают диапазон чувствительности и сравнивают результатов прижизненных тестов в разных странах или регионах или с течением времени, рассматривая различия в производителе или силе действия туберкулина как критические для тестирования Se и большей части более поздних в литературе, в частности, предполагается, что все туберкулины будут действовать одинаково как в кожном тесте, так и в анализе IFN-γ (48, 67–71). Например, в научном заключении EFSA от 2012 г. говорится, что выбор популяции крупного рогатого скота, история тестирования крупного рогатого скота на туберкулез крупного рогатого скота и распространенность микобактерий в окружающей среде могли повлиять на оценки эффективности в выборках контрольной популяции, используемых в их анализе латентного класса, в частности упоминая низкую чувствительность кожного теста в одном наборе данных (68).Тем не менее, они не упоминают как уместного, что тесты, которые они сравнивали в наборах данных, использовали туберкулин, птичий и бычий PPD от 3 разных производителей и, по крайней мере, с бычьим туберкулином PPD в 2 разных заявленных потенциях, с, в то время, были получены данные, в каждой юрисдикции использовались туберкулиновые PPD разных производителей. Например, в отношении туберкулина, используемого в анализе IFN-γ, Tameni et al. (51) отметили, что значительные колебания результатов анализа IFN-γ были связаны с использованием разных серий PPD и что туберкулины не поддавались простой стандартизации их антигенного содержания.Касаль и др. (69) сравнили эффективность SIT, ID-Vet IFN γ и Bovigam ® , отметив, что «из 113 голов крупного рогатого скота с подтвержденным туберкулезом (группа 2) 32 (28,3%) были классифицированы Bovigam как положительные реакции. ® , но тест SIT отрицательный; и в той же группе «36 голов крупного рогатого скота (31,9%) были положительными в отношении Bovigam ® (0,05 точка отсечения), но отрицательными в анализе IDvet IFN-γ (35% п/п точки отсечения)». Однако сходные результаты были достигнуты между анализами IFN-γ с использованием 0.1 точка отсечения в тесте Bovigam и отношение S/P 16 в тесте IDvet. Эти результаты были сопоставимы с результатами, полученными de la Cruz et al.
Например, в отношении туберкулина, используемого в анализе IFN-γ, Tameni et al. (51) отметили, что значительные колебания результатов анализа IFN-γ были связаны с использованием разных серий PPD и что туберкулины не поддавались простой стандартизации их антигенного содержания.Касаль и др. (69) сравнили эффективность SIT, ID-Vet IFN γ и Bovigam ® , отметив, что «из 113 голов крупного рогатого скота с подтвержденным туберкулезом (группа 2) 32 (28,3%) были классифицированы Bovigam как положительные реакции. ® , но тест SIT отрицательный; и в той же группе «36 голов крупного рогатого скота (31,9%) были положительными в отношении Bovigam ® (0,05 точка отсечения), но отрицательными в анализе IDvet IFN-γ (35% п/п точки отсечения)». Однако сходные результаты были достигнуты между анализами IFN-γ с использованием 0.1 точка отсечения в тесте Bovigam и отношение S/P 16 в тесте IDvet. Эти результаты были сопоставимы с результатами, полученными de la Cruz et al. (70), которые также обнаружили, что анализ IDvet IFN-γ менее чувствителен, чем Bovigam ® , но что Se анализа IDvet IFN-γ может быть улучшен путем корректировки пороговых значений. На листовке с противотуберкулезным набором Bovigam указано, что BOVIGAM Tuberculin PPD, производимый Prionics Lelystad B.V., использует бычий туберкулин PPD с эффективностью 30 000 МЕ/мл и птичий туберкулин PPD с эффективностью 25 000 МЕ/мл (https://assets.thermofisher.com/TFS-Assets/LSG/Flyers/animalhealth_flier_bovigam_tb_CO121138.pdf). В брошюре IDvet указано, что их тест IDvet для определения клеточного ответа на Mycobacterium bovis использует бычий PPD в качестве источника специфического антигена и птичий PPD в качестве источника неспецифических антигенов с соответствующими потенциями бычьего и птичьего туберкулинов, но активность/мл не указано (https://www.id-vet.com/wp-content/uploads/2014/07/brochure_IFNG_BovineTB_doc250.pdf). При обсуждении Se, Sp и эффективности для выявления инфицированных ТБ животных в различных тестах ни одна из групп авторов не рассматривала источник туберкулиновых PPD, птиц и крупного рогатого скота, индивидуальную эффективность или относительную активность этих PPD в тестах.
(70), которые также обнаружили, что анализ IDvet IFN-γ менее чувствителен, чем Bovigam ® , но что Se анализа IDvet IFN-γ может быть улучшен путем корректировки пороговых значений. На листовке с противотуберкулезным набором Bovigam указано, что BOVIGAM Tuberculin PPD, производимый Prionics Lelystad B.V., использует бычий туберкулин PPD с эффективностью 30 000 МЕ/мл и птичий туберкулин PPD с эффективностью 25 000 МЕ/мл (https://assets.thermofisher.com/TFS-Assets/LSG/Flyers/animalhealth_flier_bovigam_tb_CO121138.pdf). В брошюре IDvet указано, что их тест IDvet для определения клеточного ответа на Mycobacterium bovis использует бычий PPD в качестве источника специфического антигена и птичий PPD в качестве источника неспецифических антигенов с соответствующими потенциями бычьего и птичьего туберкулинов, но активность/мл не указано (https://www.id-vet.com/wp-content/uploads/2014/07/brochure_IFNG_BovineTB_doc250.pdf). При обсуждении Se, Sp и эффективности для выявления инфицированных ТБ животных в различных тестах ни одна из групп авторов не рассматривала источник туберкулиновых PPD, птиц и крупного рогатого скота, индивидуальную эффективность или относительную активность этих PPD в тестах. возможные причины различий в наблюдаемых результатах тестовых характеристик.Точно так же Кек и соавт. (71) наблюдали очень низкие показатели положительных результатов ТСН во время двух скрининговых кампаний, в ходе которых было обнаружено, что использование теста Bovigam ® повышает чувствительность выявления ТБ более чем на 30% по сравнению с ТСН с использованием официального бычьего туберкулина PPD и влияние различных используемых PPD не обсуждалось как возможный фактор наблюдаемого различия Se (71).
возможные причины различий в наблюдаемых результатах тестовых характеристик.Точно так же Кек и соавт. (71) наблюдали очень низкие показатели положительных результатов ТСН во время двух скрининговых кампаний, в ходе которых было обнаружено, что использование теста Bovigam ® повышает чувствительность выявления ТБ более чем на 30% по сравнению с ТСН с использованием официального бычьего туберкулина PPD и влияние различных используемых PPD не обсуждалось как возможный фактор наблюдаемого различия Se (71).
В значительной степени из-за плохо определенной природы антигенов в туберкулиновом PPD, а также сложности производства туберкулинового PPD, на сегодняшний день достигнут незначительный прогресс в улучшении туберкулиновых PPD для повышения специфичности и чувствительности теста (37, 52).Успешная ликвидация bTB была достигнута во многих странах за счет строгого применения туберкулиновых тестов и выбраковки реакторного скота. В то время как качество используемого туберкулинового PPD, несомненно, имеет решающее значение для эффективности испытаний в программах контроля и ликвидации ВТБ, а также для поддержки сертификации свободы от болезни на уровне животных и поголовья, сравнение имеющихся в продаже туберкулинов показало эффективность туберкулинов крупного рогатого скота и, в В меньшей степени птичьи туберкулины сильно различались, так что большинство из них не соответствовало бы требуемой минимальной дозе 2000 МЕ, если бы они применялись в качестве стандарта 0. Доза 1 мл (5, 42). Использование туберкулинов с меньшей активностью имеет прямое значение для диагностики ВТБ и для уверенности в последующем выдаче сертификатов на отсутствие болезней в стаде и животных (5, 19). В то время как Европейская фармакопея, ВОЗ, МЭБ и ЕС установили стандарты для туберкулинов (2, 20, 33–35, 39, 43, 54), не существует независимого органа, оценивающего коммерчески доступные препараты или устанавливающего и поддерживающего стандарты туберкулиновых PPD. потенция сродни Международной организации по стандартизации (https://www.iso.org) ISO, которая назначена для независимой оценки и подтверждения стандартов, заявленных производителями. Европейская референс-лаборатория по туберкулезу и/или МЭБ может играть потенциальную роль в проверке активности туберкулина. Разумно было бы ожидать, что в случае несоблюдения стандартов власти должны принять меры для предотвращения использования таких продуктов. Также, несомненно, было бы желательно иметь альтернативную методологию анализа активности PPD, менее зависящую от заражения морских свинок и наличия крупного рогатого скота, инфицированного туберкулезом.
Доза 1 мл (5, 42). Использование туберкулинов с меньшей активностью имеет прямое значение для диагностики ВТБ и для уверенности в последующем выдаче сертификатов на отсутствие болезней в стаде и животных (5, 19). В то время как Европейская фармакопея, ВОЗ, МЭБ и ЕС установили стандарты для туберкулинов (2, 20, 33–35, 39, 43, 54), не существует независимого органа, оценивающего коммерчески доступные препараты или устанавливающего и поддерживающего стандарты туберкулиновых PPD. потенция сродни Международной организации по стандартизации (https://www.iso.org) ISO, которая назначена для независимой оценки и подтверждения стандартов, заявленных производителями. Европейская референс-лаборатория по туберкулезу и/или МЭБ может играть потенциальную роль в проверке активности туберкулина. Разумно было бы ожидать, что в случае несоблюдения стандартов власти должны принять меры для предотвращения использования таких продуктов. Также, несомненно, было бы желательно иметь альтернативную методологию анализа активности PPD, менее зависящую от заражения морских свинок и наличия крупного рогатого скота, инфицированного туберкулезом. Из-за проблем с активностью при поставках туберкулина в прошлом и с учетом вышеупомянутых публикаций, демонстрирующих, что эффективность имеет решающее значение для эффективности теста, Ирландия провела независимую проверку эффективности туберкулинового PPD из бычьего туберкулина, используя естественно зараженный туберкулезом крупный рогатый скот. программа.
Из-за проблем с активностью при поставках туберкулина в прошлом и с учетом вышеупомянутых публикаций, демонстрирующих, что эффективность имеет решающее значение для эффективности теста, Ирландия провела независимую проверку эффективности туберкулинового PPD из бычьего туберкулина, используя естественно зараженный туберкулезом крупный рогатый скот. программа.
Заявление о доступности данных
Все наборы данных, созданные для этого исследования, включены в рукопись/дополнительные файлы.
Заявление об этике
Анализы Tuberculin PPD и использование в них животных были рассмотрены комитетом по этике Департамента сельского хозяйства и морского судоходства/Университетского колледжа Дублина в рамках процесса подачи заявки на получение разрешения на проект Управления по регулированию продуктов медицинского назначения (HPRA).HPRA является компетентным органом в Ирландии, ответственным за выполнение законодательства ЕС (Директива 2010/63/EU) по защите животных, используемых в научных целях. HPRA стремится обеспечить, чтобы уход за животными и их использование в научных целях соответствовали принципам 3R — Замена, Сокращение и Уточнение. Соответственно, проектам и частным лицам требуется разрешение на проведение исследований с использованием животных, включая разрешение учреждения, в котором содержатся животные.Использование животных для анализа активности Tuberculin PPD, лица, которые проводят анализы, и помещения, в которых содержатся животные, разрешены (лицензированы) HPRA и подчиняются строгим условиям лицензирования отдельных проектов, которые включают отчетность и ежегодный аудит.
HPRA стремится обеспечить, чтобы уход за животными и их использование в научных целях соответствовали принципам 3R — Замена, Сокращение и Уточнение. Соответственно, проектам и частным лицам требуется разрешение на проведение исследований с использованием животных, включая разрешение учреждения, в котором содержатся животные.Использование животных для анализа активности Tuberculin PPD, лица, которые проводят анализы, и помещения, в которых содержатся животные, разрешены (лицензированы) HPRA и подчиняются строгим условиям лицензирования отдельных проектов, которые включают отчетность и ежегодный аудит.
Вклад авторов
г. н.э. задумал исследование. AD, DB и MG проанализировали данные. AD и MG провели поиск литературы и написали первоначальную рукопись. Все авторы участвовали в рассмотрении, редактировании, прочтении и утверждении окончательного проекта, а также совместно работали над созданием окончательной версии.
Финансирование
Эта работа полностью финансировалась Министерством сельского хозяйства, продовольствия и морских ресурсов в рамках Программы ликвидации ТБ крупного рогатого скота.
Конфликт интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Благодарности
Авторы хотели бы поблагодарить сотрудников DAFM за поиск инфицированного крупного рогатого скота для туберкулиновых анализов, сотрудников Исследовательского центра DAFM и, в частности, Эймона Костелло (на пенсии) и Колма Брейди из DAFM за их помощь.Также мы высоко ценим помощь персонала Prionics Lelystad BV в технических аспектах производства туберкулина и анализах на морских свинках. Авторы также хотели бы поблагодарить Дэниела М. Коллинза за помощь в подготовке рукописи и рисунка.
Сноски
Ссылки
4. Гуд М., Баккер Д., Дуиньян А., Коллинз Д.М. История туберкулинового тестирования in vivo у крупного рогатого скота: туберкулез, выпуск «Единое здоровье». Front Vet Sci .(2018) 5:59. doi: 10.3389/fvets.2018.00059
doi: 10.3389/fvets.2018.00059
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
5. Баккер Д., Гуд М. Контроль качества очищенных белковых производных туберкулинов: необходим для эффективного контроля и программ искоренения туберкулеза крупного рогатого скота. В: Международный симпозиум по ветеринарной эпидемиологии и экономике. Чиангмай (2018).
Академия Google
7. Монаган М.Л., Доэрти М.Л., Коллинз Дж.Д., Казда Дж.Ф., Куинн П.Дж. Туберкулиновая проба. Вет микробиол. (1994) 40:111–24.
Реферат PubMed | Академия Google
9. Clegg TA, Good M, Doyle M, Duignan A, More SJ, Gormley E. Эффективность гамма-анализа интерферона при использовании в качестве диагностического теста или теста для обеспечения качества в стадах, инфицированных Mycobacterium bovis . Пред. Вет. мед. (2017) 140:116–21. doi: 10.1016/j.prevetmed.2017.03.007
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
11.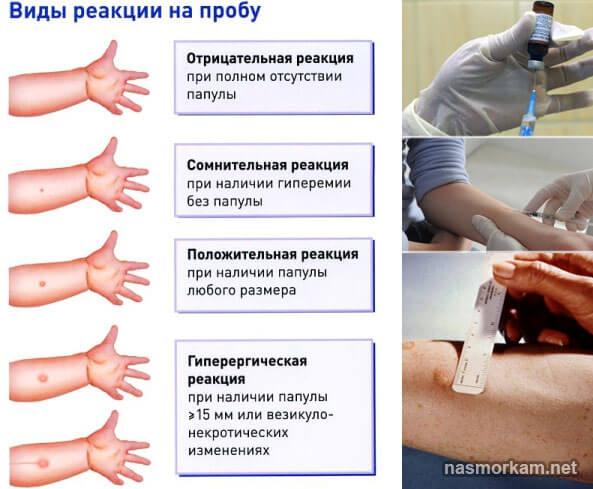 Дорсет М.Сравнение старого туберкулина Коха с новым туберкулином на синтетической среде. J Am Vet Med Assoc . (1934) 84:439–51.
Дорсет М.Сравнение старого туберкулина Коха с новым туберкулином на синтетической среде. J Am Vet Med Assoc . (1934) 84:439–51.
Академия Google
13. Зайберт Ф.Б. Выделение и свойства очищенного белкового производного туберкулина. Am Rev Tuberc Pulm Dis. (1934) 30: 713–20.
Академия Google
14. Хаагсма Дж. Тестирование активности туберкулинов крупного рогатого скота. (На Международном симпозиуме по вакцинам БЦЖ и туберкулинам. Будапешт, Венгрия, 1983 г.). Стенд Dev Biol. (1986) 58:639–94.
Реферат PubMed | Академия Google
15. О’Рейли Л.М., МакКлэнси Б.Н. Сравнение точности человеческого и бычьего туберкулина PPD для тестирования крупного рогатого скота со сравнительным цервикальным тестом. Ir Vet J. (1975) 29:63–70.
Академия Google
16. Патерсон А.Б. Туберкулез. В: Stableforth AW, Galloway IA, редакторы. Болезни, вызываемые бактериями , Vol. 2. Лондон: Бутервортс (1959). п. 671–87.
п. 671–87.
Академия Google
17. Лесли И.В. Корреляция биологической активности человеческих и бычьих туберкулиновых PPD у морских свинок, крупного рогатого скота и человека. J Биол Стенд. (1976) 4:39–42.
Реферат PubMed | Академия Google
18. Ричи Дж. Н. Туберкулез. В: Stableforth AW, Galloway IA, редакторы. Болезни, вызываемые бактериями. Лондон: Бутервортс (1959). п. 713–44.
Академия Google
19. Гуд М., Клегг Т.А., Костелло Э., Оре С.Дж.Сравнительная эффективность однократного внутрикожного туберкулинового теста и однократного внутрикожного сравнительного туберкулинового теста у ирландского крупного рогатого скота с использованием комбинаций туберкулина PPD различной активности. Vet J. (2011) 190:e60–5. doi: 10.1016/j.tvjl.2011.01.005
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
21. Патерсон А.Б., Стюарт П., Лесли И.В. Использование тестов на бойнях крупного рогатого скота для оценки относительной активности туберкулинов и для расчета дискриминационных тестов. J Гигиена. (1958) 56:1–18.
J Гигиена. (1958) 56:1–18.
Реферат PubMed | Академия Google
23. Good M. Ликвидация туберкулеза крупного рогатого скота в Ирландии. Ir Vet J. (2006). 59:154–62.
Академия Google
26. Гудчайлд А.В., Даунс С.Х., Аптон П., Вуд Дж.Л.Н., де ла Руа-Доменек Р. Специфичность сравнительного кожного теста на туберкулез крупного рогатого скота в Великобритании. Ветрек. (2015) 177:258. дои: 10.1136/vr.102961
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
27.Good M, Clegg TA, Murphy F, More SJ. Сравнительная эффективность однократного внутрикожного сравнительного туберкулинового теста у ирландского крупного рогатого скота с использованием комбинаций туберкулина PPD от разных производителей. Вет Микробиол . (2011) 151:77–84. doi: 10.1016/j.vetmic.2011.02.028
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
28. O’Reilly LM, Haagsma J. Калибровка ирландского эталонного препарата для Bovine PPD. Производство и стандартизация туберкулина. В: Материалы Второй Международной конференции по туберкулезу животных в Африке и на Ближнем Востоке .Рабат (1997).
Производство и стандартизация туберкулина. В: Материалы Второй Международной конференции по туберкулезу животных в Африке и на Ближнем Востоке .Рабат (1997).
Академия Google
29. Haagsma J, Eger A. Тестирование качества туберкулинов и его практические последствия для диагностики туберкулеза крупного рогатого скота. В: Материалы Второй Международной конференции по туберкулезу животных в Африке и на Ближнем Востоке . Рабат (1997).
Академия Google
30. Haagsma J, O’Reilly LM, Dobbelaer R, Murphy TM. Сравнение относительной эффективности различных туберкулинов PPD крупного рогатого скота у естественно инфицированного туберкулезом крупного рогатого скота. J Биол Стенд. (1982) 10: 273–84.
Реферат PubMed | Академия Google
31. Хаагсма Дж. Производство и стандартизация туберкулина. В: Материалы Второй Международной конференции по туберкулезу животных в Африке и на Ближнем Востоке . Рабат (1997).
Академия Google
32. Schneider W, Augier J, Cavrini C, Dam A, Dobbelaer R, Gayot G, et al. Заключительный отчет подгруппы Научной ветеринарной комиссии по туберкулинам 2577/VI/79-EN Rev.4 от имени Комиссии Европейских сообществ, Генеральный директорат по сельскому хозяйству VI/B/II2. (1979).
Schneider W, Augier J, Cavrini C, Dam A, Dobbelaer R, Gayot G, et al. Заключительный отчет подгруппы Научной ветеринарной комиссии по туберкулинам 2577/VI/79-EN Rev.4 от имени Комиссии Европейских сообществ, Генеральный директорат по сельскому хозяйству VI/B/II2. (1979).
Академия Google
33. Всемирная организация здравоохранения. Иммунологические препараты — Туберкулин стр. 13 Требования к биологическим веществам — Требования к туберкулинам стр. 21- и Приложение 1. Двадцатый отчет Комитета экспертов ВОЗ по биологической стандартизации. Серия технических отчетов № 384. Женева (1968). п. 23–41. Доступно в Интернете по адресу: http://whqlibdoc.who.int/trs/WHO_TRS_384.pdf?ua=1 (по состоянию на 8 июня 2019 г.).
Академия Google
34. Всемирная организация здравоохранения. Требования к биологическим веществам — Требования к туберкулинам стр. 27 и (Приложение 1). Тридцать шестой доклад Комитета экспертов ВОЗ по биологической стандартизации. Серия технических отчетов № 745. Женева (1987). п. 31–58. Доступно на сайте: http://whqlibdoc.who.int/trs/WHO_TRS_745.pdf?ua=1
Серия технических отчетов № 745. Женева (1987). п. 31–58. Доступно на сайте: http://whqlibdoc.who.int/trs/WHO_TRS_745.pdf?ua=1
Академия Google
36. Франкена К., Джейкобс Л., ван Дейк Т., Гуд М., Дуиньян А., де Йонг М.К.М.Новая модель для калибровки эталонного стандарта очищенного белкового производного туберкулина крупного рогатого скота у целевых видов. Front Vet Sci. (2018) 5:232. doi: 10.3389/fvets.2018.00232
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
38. Даниэль Т.М., Яницкий Б.В. микобактериальные антигены; обзор выделения, химии и иммунологических свойств. Microbiol Rev. (1978) 42:84–113.
Реферат PubMed | Академия Google
40.Дэвидсон И. Методы лабораторного анализа бычьего туберкулина PPD. (Отчет группы экспертов по ветеринарным сывороткам и вакцинам Европейской комиссии по фармакопее). Стенд Dev Biol. (1983) 58:607–16.
Реферат PubMed | Академия Google
41.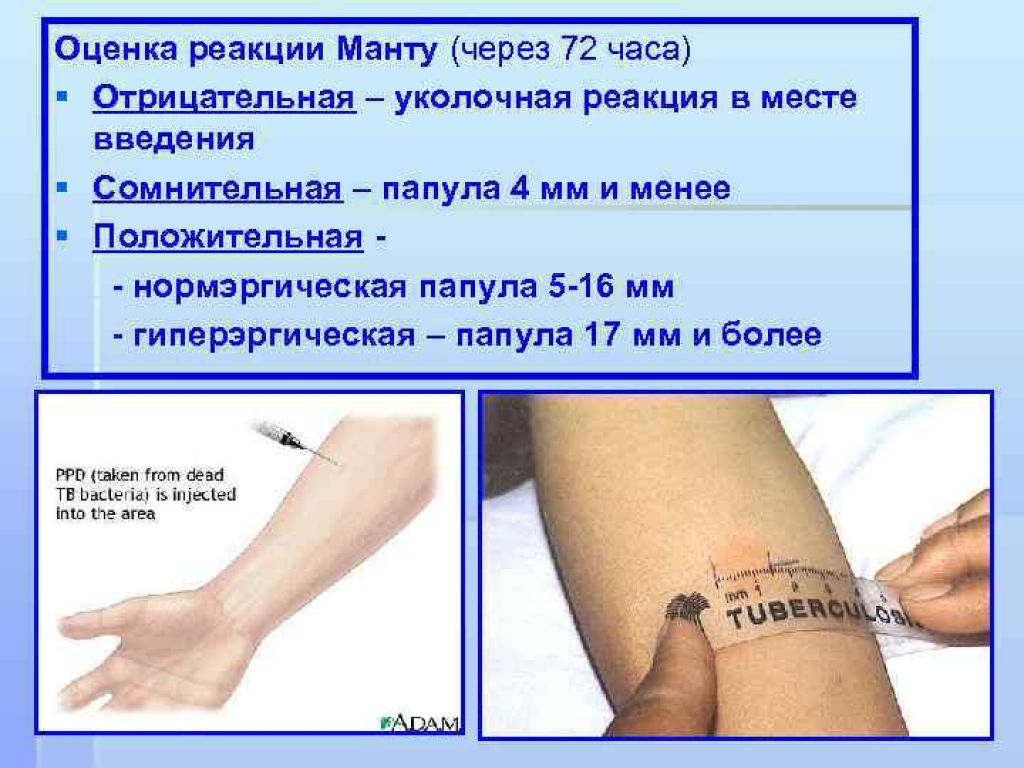 Джозеф К. Die diagnostische Bedeutung der intrakutanen Tuberkulinreaktion (оригинал на немецком языке диагностическое значение внутрикожного туберкулина). Berl tierärztl Wochenschr . (1909) 46:847–51.
Джозеф К. Die diagnostische Bedeutung der intrakutanen Tuberkulinreaktion (оригинал на немецком языке диагностическое значение внутрикожного туберкулина). Berl tierärztl Wochenschr . (1909) 46:847–51.
Академия Google
42.Bakker D, Eger A, McNair J, Riepema K, Willemsen PTJ, Haagsma J, et al. Сравнение имеющихся в продаже PPD: практические соображения по диагностике и борьбе с туберкулезом крупного рогатого скота (постерная презентация). В: Четвертая международная конференция по Mycobacterium bovis . Дублин (2005).
Академия Google
44. Дэвидсон И. Лабораторные методы анализа бычьего туберкулина PPD (отчет группы экспертов по ветеринарным сывороткам и вакцинам Европейской фармакопеи). Стенд Dev Biol. (1986) 58:607–16.
Реферат PubMed | Академия Google
45. Dobbelaer R, O’Reilly LM, Génicot A, Haagsma J. Эффективность туберкулинов PPD крупного рогатого скота у морских свинок и у больных туберкулезом крупного рогатого скота. J Биол Стенд. (1983) 11: 213–20.
J Биол Стенд. (1983) 11: 213–20.
Реферат PubMed | Академия Google
48. Downs SH, Parry JE, Upton PA, Broughan JM, Goodchild AV, Nuñez-Garcia J, et al. Методология и предварительные результаты систематического обзора литературы по прижизненным и посмертным диагностическим тестам на туберкулез крупного рогатого скота. Пред. Вет. мед. (2018) 153:117–26. doi: 10.1016/j.prevetmed.2017.11.004
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
49. Santema W, Overdijk M, Barends J, Krijgsveld J, Rutten V, Koets A. Поиск белков Mycobacterium avium подвида paratuberculosis с диагностическим потенциалом путем сравнительного качественного протеомного анализа микобактериального туберкулина. Вет микробиол. (2009) 138:191–6. doi: 10.1016/j.ветмик.2009.03.021
Полнотекстовая перекрестная ссылка | Академия Google
50. Schiller I, Oesch B, Vordermeier HM, Palmer MV, Harris BN, Orloski KA, et al.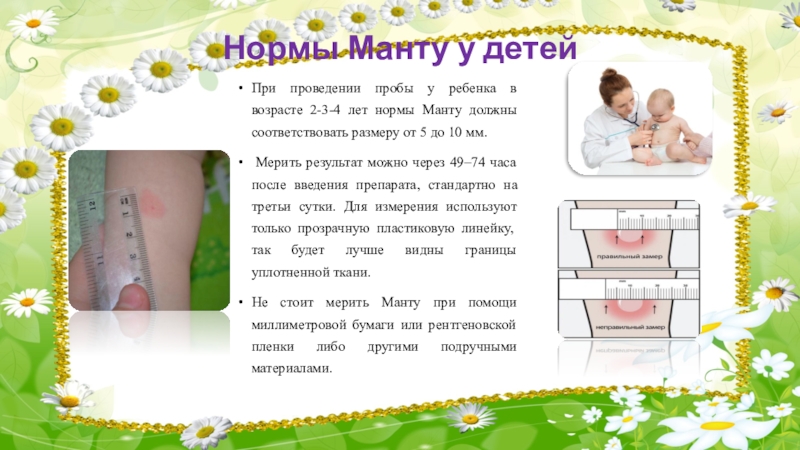 Туберкулез крупного рогатого скота: обзор современных и новых диагностических методов с учетом их актуальности для контроля и искоренения болезни. Transbound Emerg Dis. (2010) 57:205–20. doi: 10.1111/j.1865-1682.2010.01148.x
Туберкулез крупного рогатого скота: обзор современных и новых диагностических методов с учетом их актуальности для контроля и искоренения болезни. Transbound Emerg Dis. (2010) 57:205–20. doi: 10.1111/j.1865-1682.2010.01148.x
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
51. Tameni S, Amadori M, Scaccaglia P, Quondam-Giandomenico R, Tagliabue S, Archetti IL, et al.Контроль качества и in vitro диагностическая эффективность туберкулинов PPD крупного рогатого скота. Биопрепараты. (1998) 26:225–35.
Реферат PubMed | Академия Google
52. Инфантес-Лоренцо Х.А., Морено И., де лос Анхелес Рисальде М., Рой А., Вильяр М., Ромеро Б. и др. Протеомная характеристика очищенных белковых производных крупного рогатого скота и птиц и идентификация специфических антигенов для серодиагностики туберкулеза крупного рогатого скота. Клин Протеомика. (2017) 14:36. дои: 10.1186/с12014-017-9171-з
Полнотекстовая перекрестная ссылка | Академия Google
53. Cooney R, Kazda J, Quinn J, Cook B, Muller K, Monaghan M. Экологические микобактерии в Ирландии как источник неспецифической сенсибилизации к туберкулинам. Ir Vet J. (1997) 50:370–3.
Cooney R, Kazda J, Quinn J, Cook B, Muller K, Monaghan M. Экологические микобактерии в Ирландии как источник неспецифической сенсибилизации к туберкулинам. Ir Vet J. (1997) 50:370–3.
Академия Google
54. Европейская комиссия. EudraLex — Том 4 — Руководство по надлежащей производственной практике (GMP) Том 4 «Правил, регулирующих лекарственные препараты в Европейском союзе», содержит Руководство по интерпретации принципов и рекомендаций по надлежащей производственной практике лекарственных средств для человека и ветеринарии. Внесено в Директивы Комиссии 91/356/ЕЕС с поправками, внесенными Директивой 2003/94/ЕС, и 91/412/ЕЕС соответственно .(2018). Доступно в Интернете по адресу: https://ec.europa.eu/health/documents/eudralex/vol-4_en (по состоянию на 15 октября 2018 г.).
Академия Google
55. Баккер Д. Практические аспекты иммунологических диагностических тестов для борьбы с туберкулезом крупного рогатого скота. В: Материалы VI -й -й Международной конференции M. bovis . Кардифф (2014).
bovis . Кардифф (2014).
Академия Google
56. Гормли Э., Дойл М.Б., Фитцсаймонс Т., Макгилл К., Коллинз Д.Д. Диагностика инфекции Mycobacterium bovis у крупного рогатого скота с использованием анализа гамма-интерферона (Бовигам ® ). Вет Микро. (2006) 112:171–9. doi: 10.1016/j.vetmic.2005.11.029
Полнотекстовая перекрестная ссылка | Академия Google
57. Радунц Б.Л., Lepper AWD. Подавление кожной реакции на бычий туберкулин при повторных испытаниях. Aust Vet J. (1985) 62:191–4.
Реферат PubMed | Академия Google
58. Финни Диджей. Статистические методы в биологических анализах , 3-е изд. Лондон: Чарльз Гриффин и компания с ограниченной ответственностью (1978).
Академия Google
61.Бакстон Дж.Б. Некоторые аспекты роли туберкулина в борьбе с туберкулезом. Секция сравнительной медицины, Послание Президента. Proc R Soc Med. (1934) xxvIII: 257–64.
Академия Google
62. Молер Дж.Р. Туберкулиновый тест крупного рогатого скота на туберкулез . Вашингтон, округ Колумбия: Министерство сельского хозяйства США; Правительственная типография (1909 г.).
Молер Дж.Р. Туберкулиновый тест крупного рогатого скота на туберкулез . Вашингтон, округ Колумбия: Министерство сельского хозяйства США; Правительственная типография (1909 г.).
Академия Google
63. Downs SH, Clifton-Hadley RS, Upton PU, Milne I, Ely E, Gopal R, et al.Источник производства туберкулина и уровень заболеваемости туберкулезом крупного рогатого скота в Великобритании, 2005–2009 гг. Ветрек. (2013) 172:98. дои: 10.1136/vr.100679
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
64. O’Hagan MJH, Ni H, Menzies FD, Pascual-Linaza AD, Georgaki AA, Stegeman JA. Характеристики туберкулиновой кожной пробы и патологоанатомического исследования для диагностики туберкулеза крупного рогатого скота в Северной Ирландии, оцененные с помощью байесовского анализа латентных классов с поправкой на ковариаты. Эпидемиол Инфекция. (2019) 147:e209. дои: 10.1017/S09502688188
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
65. Де ла Руа-Доменек Р., Гудчайлд А.Т., Фордермейер Х.М., Хьюинсон Р.Г., Кристиансен К.Х., Клифтон-Хэдли Р.С. Предубойная диагностика туберкулеза крупного рогатого скота: обзор туберкулиновых проб, гамма-интерферонового анализа и других вспомогательных методов диагностики. Res Vet Sci. (2006) 81:190–210. doi: 10.1016/j.rvsc.2005.11.005
Де ла Руа-Доменек Р., Гудчайлд А.Т., Фордермейер Х.М., Хьюинсон Р.Г., Кристиансен К.Х., Клифтон-Хэдли Р.С. Предубойная диагностика туберкулеза крупного рогатого скота: обзор туберкулиновых проб, гамма-интерферонового анализа и других вспомогательных методов диагностики. Res Vet Sci. (2006) 81:190–210. doi: 10.1016/j.rvsc.2005.11.005
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
66.О’Рейли Л.М. Специфичность и чувствительность туберкулиновых тестов: обзор. В: Труды Международной конференции по туберкулезу в Африке и на Ближнем Востоке . Каир (1992).
Академия Google
67. Nuñez-Garcia J, Downs SH, Parry JE, Abernethy DA, Broughan JM, Cameron AR, et al. Мета-анализ чувствительности и специфичности прижизненных и посмертных диагностических тестов на туберкулез крупного рогатого скота в Великобритании и Ирландии. Предыдущий ветеринарный медицинский . (2018) 153:94–107.doi: 10.1016/j.prevetmed.2017.02.017
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
68. Группа EFSA по здоровью и благополучию животных (AHAW). Научное мнение об использовании гамма-интерферонового теста для диагностики туберкулеза крупного рогатого скота. EFSA J. (2012) 10:2975. doi: 10.2903/j.efsa.2012.2975
Группа EFSA по здоровью и благополучию животных (AHAW). Научное мнение об использовании гамма-интерферонового теста для диагностики туберкулеза крупного рогатого скота. EFSA J. (2012) 10:2975. doi: 10.2903/j.efsa.2012.2975
Полнотекстовая перекрестная ссылка | Академия Google
69. Casal C, Infantes JA, Risalde MA, Díez-Guerrier A, Domínguez M, Moreno I, et al. Тесты на обнаружение антител повышают чувствительность диагностики туберкулеза у крупного рогатого скота. Res Vet Med. (2017) 112: 214–21. doi: 10.1016/j.rvsc.2017.05.012
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
70. де ла Круз М.Л., Бранскум А.Дж., Накар Дж., Пейдж Э., Позо П., Перес А. и соавт. Оценка эффективности теста IDvet IFN-gamma для диагностики туберкулеза крупного рогатого скота в Испании. Front Vet Sci. (2018) 5:229. doi: 10.3389/fvets.2018.00229
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
71. Кек Н., Бошироли М.Л., Смей Ф., Фоглер В., Мойен Дж.Л., Десво С. Успешное применение анализа гамма-интерферона в программе искоренения туберкулеза крупного рогатого скота: опыт французского корриды. Front Vet Sci. (2018) 5:27. doi: 10.3389/fvets.2018.00027
Кек Н., Бошироли М.Л., Смей Ф., Фоглер В., Мойен Дж.Л., Десво С. Успешное применение анализа гамма-интерферона в программе искоренения туберкулеза крупного рогатого скота: опыт французского корриды. Front Vet Sci. (2018) 5:27. doi: 10.3389/fvets.2018.00027
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
Предвидя нехватку антигенов при кожных тестах на ТБ, CDC предлагает перейти на лабораторные тесты IGRA
НЬЮ-ЙОРК. В то время, когда клиницисты уже все чаще переходят на анализы на основе высвобождения гамма-интерферона (IGRA) для тестирования на туберкулез, Центры по контролю за заболеваниями США и Предупреждение недавно предупредили об ожидаемой нехватке ключевых антител для туберкулиновых кожных проб (ТКП), проводимых в клиниках.
Из-за ожидаемой нехватки один поставщик тестов IGRA, Oxford Immunotec Global, ожидает резкого увеличения доходов, а другой, Qiagen, активно увеличил производство тестовых наборов, по словам своего клиента Laboratories Corporation of America.
Центры по контролю и профилактике заболеваний (CDC) недавно объявили об ожидаемой в течение 3-10 месяцев общенациональной нехватке Aplisol, одного из двух очищенных белковых производных туберкулиновых антигенов, одобренных Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США для использования в диагностике туберкулеза на основе TST.CDC сообщил, что производитель аплисола, Par Pharmaceuticals, уведомил его о ожидаемом прекращении поставок аплисола 5 мл, начиная с июня, за которым следует прекращение поставок аплисола 1 мл в ноябре или раньше, если потребность в антигене возрастет. Ожидается перерыв в поставках 50 многодозовых флаконов Аплисола 5 мл и 10 многодозовых флаконов Аплисола 1 мл.
В качестве средства правовой защиты CDC рекомендовал клиницистам уделять приоритетное внимание назначению TST и, возможно, отложить тестирование TST для некоторых пациентов — по согласованию с государственными и местными органами здравоохранения.
Кроме того, было рекомендовано заменить ТКП на анализы крови IGRA или заменить аплисол туберсолом во время кожных проб. Туберсол, производимый Санофи-Пастер, является вторым туберкулиновым антигеном, одобренным Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA).
Туберсол, производимый Санофи-Пастер, является вторым туберкулиновым антигеном, одобренным Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA).
Клиницисты могут использовать ТКП на основе антигенов или анализы крови IGRA для обнаружения Mycobacterium tuberculosis , бактерии, вызывающей туберкулез у людей. Большинство случаев туберкулеза в США диагностируются с помощью комбинации методов, включая результаты одного из этих тестов.
Oxford Immunotec, Qiagen и клиенты их лабораторий выиграют, если клиницисты решат отказаться от кожных тестов. Oxford Immunotec, базирующаяся в Оксфорде, Великобритания, производит тест T-Spot.TB, который был одобрен для продажи более чем в 50 странах. Тест основан на том принципе, что Т-клетки инфицированного пациента реагируют на специфические антигены и секретируют гамма-интерферон.
В апреле Hilden, основанная в Германии компания Qiagen объявила, что ее тест QuantiFeron-TB для обнаружения туберкулезных инфекций превысил 60 миллионов тестов. Разработанный компанией тест QuantiFeron-TB Gold Plus, продаваемый более чем в 75 странах, сочетает в себе гибкий рабочий процесс сбора крови с технологией Т-клеток CD4/CD8.
Разработанный компанией тест QuantiFeron-TB Gold Plus, продаваемый более чем в 75 странах, сочетает в себе гибкий рабочий процесс сбора крови с технологией Т-клеток CD4/CD8.
Неясно, приведет ли текущий дефицит антигенов к увеличению количества тестов IGRA.
Донника Смоллс, представитель CDC, отметила, что замена анализов крови IGRA кожными тестами на туберкулез является лишь одним из трех подходов, которые CDC рекомендует для предотвращения снижения возможностей тестирования на туберкулез.
«Несмотря на наличие IGRA, многие клиники общественного здравоохранения и партнеры по сообществу по-прежнему используют TST для скрининга», — сказала в интервью Джули Хигаси, президент Национальной ассоциации контролеров туберкулеза (NTCA).«Хотя мы находимся на ранней стадии дефицита, его воздействие, вероятно, затронет население, имеющее ограниченный доступ к медицинской помощи и нуждающееся в проверке на доступ к таким услугам, как приют и лечение от наркозависимости и психического здоровья», — сказала она.
По оценкам Oxford Immunotec, около 75 процентов всех тестов на туберкулез по-прежнему основаны на кожных тестах.
Элица Тил, консультант отдела клинической микробиологии в Mayo Clinic Laboratories, сказала в интервью, что некоторые клиницисты могут предпочесть увеличить закупки туберсола, альтернативы аплисолу, потому что его легко внедрить. уже использовал.
Несмотря на это удобство, некоторые клиницисты могут полностью перейти на тестирование IGRA отчасти потому, что этот подход позволяет клиницистам предоставлять пациентам результаты за одно посещение, сказал Тил. Пациент, сдающий кожный тест, должен вернуться в клинику примерно через 48 часов после внутрикожной инъекции.
Лаборатории Mayo Clinic Laboratories, которые используют для тестирования продукт Qiagen QuantiFeron, уже наблюдают, как клиницисты отдают предпочтение IGRA, а не кожным тестам, о чем свидетельствует увеличение объемов тестов IGRA на 10–15 процентов в последние годы, сказал Тил.
Представитель LabCorp Моник Смоллс сообщила 360Dx , что компания из Берлингтона, Северная Каролина, и Qiagen, ее поставщик тестов IGRA, «готовы к потенциальному увеличению спроса в результате рекомендации CDC заменить ТКП анализами крови IGRA. » Она сказала, что Qiagen «активно увеличила производство тестовых наборов», чтобы подготовиться «к потенциальному увеличению объемов».
» Она сказала, что Qiagen «активно увеличила производство тестовых наборов», чтобы подготовиться «к потенциальному увеличению объемов».
Хема Капур, медицинский директор по инфекционным заболеваниям и иммунологии в Quest Diagnostics, сказала в интервью, что, хотя реакция на текущее объявление будет зависеть от того, как на него отреагируют клиницисты, на протяжении многих лет она наблюдала постоянный рост тестирования IGRA, поддерживаемого в соответствии с руководствами, в которых для определенных групп населения рекомендуется проводить тестирование на туберкулез вместо кожного тестирования.
В руководстве 2016 года Американского торакального общества, Американского общества инфекционных заболеваний и Центра по контролю и профилактике заболеваний рекомендуется проводить тест IGRA, а не туберкулиновую кожную пробу, у людей пяти лет и старше, которые соответствуют определенным критериям. Руководство, рекомендованное тестирование IGRA для людей, которые могут быть инфицированы M. tuberculosis ; имеют низкий или промежуточный риск прогрессирования заболевания; либо имеют историю вакцинации БЦЖ, либо вряд ли вернутся, чтобы прочитать их ТКП; или для которых тестирование на латентную туберкулезную инфекцию является оправданным.Однако в руководстве говорилось, что TST является приемлемой альтернативой, «особенно в ситуациях, когда IGRA недоступна, слишком дорога или слишком обременительна».
tuberculosis ; имеют низкий или промежуточный риск прогрессирования заболевания; либо имеют историю вакцинации БЦЖ, либо вряд ли вернутся, чтобы прочитать их ТКП; или для которых тестирование на латентную туберкулезную инфекцию является оправданным.Однако в руководстве говорилось, что TST является приемлемой альтернативой, «особенно в ситуациях, когда IGRA недоступна, слишком дорога или слишком обременительна».
«За более чем 12 лет, что Quest предлагает тест IGRA, мы видели… многие медицинские учреждения и поставщики услуг переходят с TST на IGRA», — сказал Капур, добавив, что есть несколько причин, по которым врачи переходят на тест IGRA. Тесты IGRA, в том числе более высокая точность, возможность проведения скрининга за одно посещение и отсутствие перекрестной реактивности с противотуберкулезной вакциной Bacillus Calmette-Guérin, что оказалось проблемой при кожных тестах.
Компания Quest заявила, что предоставляет услуги по тестированию на туберкулез на основе анализов крови Qiagen и Oxford Immunotec IGRA.
Это не первый случай нехватки очищенных белковых производных туберкулиновых антигенов. В апреле 2013 года Санофи Пастер объявила, что нехватка туберсола по всей стране будет ощущаться как минимум до конца мая того же года. В то же время JHP Pharmaceuticals уведомила FDA о том, что ее продукт доступен в ограниченном количестве.
На своем веб-сайте компания Vasserve, принадлежащая Санофи Пастер, сообщила, что Tubersol «в настоящее время находится под ограничением заказа.
Ни Par Pharmaceuticals, базирующаяся в Вудклифф-Лейк, штат Нью-Джерси, ни Sanofi-Pasteur, базирующаяся в Лионе, не ответили на электронные письма с запросами комментариев для этой статьи. Qiagen также не ответила на электронные письма с запросами комментариев.
Оксфорд Immunotec заявила, что объявление CDC является еще одним свидетельством необходимости для клиницистов перейти на тестирование IGRA.
«Когда мы ранее наблюдали нехватку туберсола, мы испытали небольшой рост объемов испытаний», — Джонатан Френд, вице-президент по коммерческим операциям в США. для Oxford Immunotec, сказал в интервью.«Многие клиенты, которые перешли из-за проблем с цепочкой поставок в то время, продолжали заказывать тестирование T-spot после того, как проблемы с поставками были решены», — сказал он.
для Oxford Immunotec, сказал в интервью.«Многие клиенты, которые перешли из-за проблем с цепочкой поставок в то время, продолжали заказывать тестирование T-spot после того, как проблемы с поставками были решены», — сказал он.
С 2014 года фирма наблюдает «значительный рост» объемов и доходов от своего продукта T-Spot, сказал Френд, добавив: «С недавним приобретением Quest нашей сервисной лаборатории в США, T-spot также стал более доступным. .»
Он отметил, что, поскольку кожные тесты по-прежнему занимают около 75 процентов рынка тестирования на ТБ, у тестирующих компаний IGRA есть много дополнительных возможностей для роста доходов и объемов.
«Мы уверены, что по мере того, как тестирование кожи становится менее доступным из-за цепочки поставок и других проблем, все больше людей будут выбирать анализы крови», — сказал Френд.
Тем не менее, финансовый директор компании Мэтью Маклафлин сказал, что, учитывая потенциальное увеличение объемов тестирования на основе текущего объявления, фирма будет «подождать и посмотреть, что произойдет в течение следующих нескольких месяцев и кварталов».
Клиническая больница Майо в своих стационарных и амбулаторных службах ранее проводила кожные пробы, а иногда также заказывала тесты IGRA в своих лабораториях, но из-за более раннего объявления CDC, в котором были обновлены рекомендации по скринингу, тестированию и лечению туберкулеза для медицинского персонала США. «Теперь он прекратит проводить ежегодные кожные тесты и перейдет на IGRA для всех базовых тестов», — сказал Тил.
Это имеет значение для больничных лабораторий и особенно для преаналитической обработки образцов, которая включает инкубацию цельной крови, центрифугирование и проверку объема. По словам Тила, переход на тестирование IGRA требует увеличения лабораторных площадей и количества людей, проводящих тесты, а также установки дополнительных инкубаторов.
В настоящее время только два тукулина были приняты в качестве стандартные туберкулины ВОЗ, т.е. , PPD-S и PPD RT 23. Международные стандартные туберкулины находятся на хранении в Лаборатории Биологические стандарты, Staten, Институт сыворотки, Копенгаген, Дания(2). В Индии PPD-RT 23 производится в лаборатории Guindy, Ченнаи. Немного такие страны, как США, используют PPD-S (Siebert) из партии 49608. Все туберкулины были стандартизированы по активности в туберкулиновых единицах против PPD-S. А стандартная доза 5 туберкулиновых единиц (5TU) PPD-S определяется как отсроченная кожная активность, содержащаяся в 0.1 г/0,1 мл дозы PPD-S. 1 ТУ ППД-РТ 23 эквивалентен 5 ТЕ ППД-С(3). Это для поддержания единообразие и сопоставимость различных результатов испытаний во всем мире. Любые лекарственные формы фармацевтической компании, содержащие любые другие типа PPD или с любой другой силой, отличной от упомянутой выше лучше всего игнорировать. ППД-РТ 23 с твином 80 в количестве 1 ТУ и 2 ТЕ
стандартизированные туберкулины, доступные в Индии, поставляемые вакциной БЦЖ
Лаборатория, Гинди, Ченнаи. Рекомендуется использовать туберкулин в дозе 1 ТУ.
стандартная проба Манту в Индии и большинство туберкулиновых обследований, проведенных в Индии
были проведены с использованием 1 ТУ ППД-РТ 23 по ранее
рекомендация ВОЗ.За последние 10 лет использование 2TU для опросов
была предложена ВОЗ, но некоторые страны продолжают использовать 1TU для
обследования населения(5). Недавнее исследование, проведенное в Индии, предполагает, что с
неспецифическая чувствительность (чувствительность, обусловленная атипичными микобактериями)
высокий в нашей стране, 1TU лучше в разделении зараженных лиц
с заболеванием от инфицированных субъектов без заболевания (6). Чувствительность к туберкулину относится к замедленному типу
реакция гиперчувствительности в виде уплотнения в месте пробы в
сенсибилизированный хозяин.Гистологически выявляется самая ранняя фаза реакции.
в виде периваскулярной манжетки мононуклеарных клеток, за которой следует более
обширная экссудация мононуклеарных и полиморфноядерных клеток,
позже мигрируют, оставляя только мононуклеарные клетки. Когда эти сенсибилизированные T
клетки вступают в контакт со специфическими антигенами, они секретируют лимфокины
которые, в свою очередь, привлекают больше лимфоцитов в очаг воспаления и
вызывают характерный ответ типа IV (7). Induartion может быть связано
инфекции микобактериями из окружающей среды, чувствительности к БЦЖ или
чувствительность вследствие инфицирования Mycobacterium tuberculosis .То
размер уплотнения также будет варьироваться от региона к региону из-за
разница в распространенности атипичных микобактерий. При использовании туберкулиновой пробы следует помнить что вообще определяет только наличие или отсутствие заражения, т.е. , воздействие М.tuberculosis. Количество уплотнений может свидетельствовать о активное болезненное состояние, но обычно не используется в качестве единственного диагностического критерии туберкулеза.Размеры индурации варьируются от популяции к населения в зависимости от распространенности туберкулеза. Отсечки упомянутые в Учебнике педиатрии Нельсона, основаны на критериях CDC для американского населения, которое имеет очень низкую общую распространенность туберкулезная инфекция, а также болезнь (9). Прогностическая ценность положительный тест в популяции с низкой распространенностью низкий, потому что в отсутствие факторы риска положительный результат, скорее всего, будет ложноположительным один. Следовательно, они определили более низкие пороговые значения для групп населения с высоким риском. и выше для населения в целом.Интерпретация туберкулиновой пробы полностью клиницист должен четко понимать эпидемиологию туберкулёз в обществе и правильные показания для туберкулина тестирование личности. В нашей стране с высокой распространенностью туберкулез, для практических целей величина уплотнения туберкулиновой пробы можно интерпретировать следующим образом: ( i ) Уплотнение менее 5 мм отсутствие контакта с туберкулезными бациллами. Однако иногда травмы из-за игла может вызвать уплотнение до 4 мм; ( ii ) Уплотнение между 5-9 мм это может быть связано с атипичными микобактериями или прививкой БЦЖ.Это может указывать на инфекцию у детей с ослабленным иммунитетом, например, на ВИЧ. инфекция или другая иммуносупрессия; и ( iii ) Углубление 10 мм или более уплотнение 10 мм и более через 48-72 часа с 1TU PPD-RT 23 у ребенка с симптомами туберкулеза следует интерпретировать как туберкулезное заболевание. В ситуациях высокого риска т.е. ., у детей с наличием в анамнезе контакта с больными туберкулезом с положительным мазком, дети проживание со взрослыми, получающими противотуберкулезную терапию, и детьми с истощением, уплотнение 10 мм и более может быть индикатором наличия болезнь.Чем больше уплотнение, тем выше вероятность активное заболевание. Следовательно, стандартная рекомендация 10 мм, как указано в рекомендациях Пересмотренной национальной противотуберкулезной программы (RNTPC) (10) уместно и актуально для нашей страны. Изменения ситуации в обследования населения, где для проведения теста берется отсечение >15 мм более конкретно, например. , недавнее исследование National Tuberculosis Центр, Бангалор, использовал отсечку 17 мм с 1TU PPD-RT 23 для идентификации дети с инфекцией М.туберкулез в популяции опрос (6). В таких обследованиях проба Манту используется как единственный критерий для нахождения вне распространенности туберкулеза без помощи риска факторы для любого другого исследования. В таких случаях пороги разные от региона к региону в зависимости от распространенности атипичных микобактерии и вакцинация БЦЖ (11,12). Следовательно, интерпретация туберкулиновой пробы будет зависят от ситуаций и факторов, упомянутых выше. Однако значение 10 мм и более с 1 ТУ ППД-РТ 23 считается значительным при дети. Анджу Аггарвал, |
|
Arkray Mantoux Test PPD 10 Tu, Химические реагенты, Лабораторные реагенты, Аналитические реагенты, Химические реактивы, Порошковый реагент — ASEnterprises, Джайпур
Arkray Mantoux Test PPD 10 Tu, Химические реактивы, Лабораторные реагенты, Аналитические реактивы Порошок — А.S.Enterprises, Джайпур | ID: 23196248797Спецификация продукта
| Brand | Arkray | Arkray | |
| для Mantoux Test | |||
| Размер | 5 мл | ||
| Материал | Reagent |
Описание продукта
аркрай ППД 10Ту
УПАКОВКА 5 МЛ
МРП 168
Заинтересованы в этом товаре?Уточнить цену у продавца
Связаться с продавцом
Изображение продукта
О компании
Год основания1998
Юридический статус фирмы Физическое лицо — Собственник
Сфера деятельностиПроизводитель
Количество сотрудниковДо 10 человек
Годовой оборотRs.50 лакхов — 1 крор
IndiaMART Участник с октября 2018 г.
GST08JJLPS5216P1Z7
используйте веб-сайт для дальнейшего звонка 9782567842.Уважаемый господин / госпожа,
Мы поставляем и заключаем сделки со всеми биохимическими, лабораторными, патологическими, рентгеновскими, пластиковыми и стеклянными предметами , которые являются расходными материалами в больницах и диагностических лабораториях . Мы сосредоточены на предоставлении высококачественных продуктов и с длительным сроком годности из одного источника с 1998 года.
Спасибо за приглашение, за предложение следующих продуктов вашей уважаемой организации. Мы предлагаем вам нашу лучшую цену и спецификацию для вашего обзора и дальнейших действий в нашу пользу.
Спасибо Вернуться к началу 1 Есть потребность?
Лучшая цена
Есть потребность?
Получите лучшую цену
Кожный туберкулиновый тест в сравнении с анализом высвобождения гамма-интерферона среди пользователей отдела общественного здравоохранения в Северо-Восточной Португалии — FullText — Portugal Journal of Public Health 2020, Vol.38, № 3
Скрининг групп высокого риска развития туберкулеза (ТБ) является приоритетным направлением в целях борьбы с этим заболеванием. Поскольку не существует золотого стандарта диагностики латентной туберкулезной инфекции (ЛТБИ), для этой цели использовались как туберкулиновая кожная проба (ТКП), так и анализ высвобождения гамма-интерферона (IGRA). Цель этого исследования состояла в том, чтобы определить долю ЛТБИ с помощью тестов ТКП и IGRA, а также оценить факторы риска, связанные с расхождением результатов между тестами в нескольких группах риска, рекомендованных для скрининга в Северо-Восточной Португалии.Данные были собраны из базы данных пациентов с подозрением на ЛТИ и рекомендованы для скрининга в отделении общественного здравоохранения (с января 2014 г. по декабрь 2015 г.). Доля ЛТБИ была рассчитана с использованием обоих тестов. В моделях логистической регрессии оценивались факторы риска для положительного теста и для противоречивых результатов между тестами. Были получены скорректированное отношение шансов (ОШ) и соответствующий 95% доверительный интервал (95% ДИ). Из 367 пациентов, включенных в анализ, у 79,8% была положительная ТКП и у 46,0% из них была положительная IGRA.По сравнению с контактировавшими с больными активным туберкулезом, медицинские работники и заключенные демонстрировали более высокие шансы положительного результата ТКП (ОШ 4,38, 95% ДИ 1,59–12,09 и ОШ 4,74, 95% ДИ 1,45–15,49 соответственно), но у людей с ослабленным иммунитетом этот показатель был ниже. ТКП положительный (ОШ 0,14; 95% ДИ 0,06–0,31). Вместо этого медицинские работники (ОШ 0,44, 95% ДИ 0,24–0,80) и люди с ослабленным иммунитетом (ОШ 0,24, 95% ДИ 0,10–0,56) имели более низкие шансы положительного результата IGRA. Было 42,0% согласующихся положительных результатов, 16,1% согласующихся отрицательных результатов и 41.9% противоречивых результатов, при этом медицинские работники демонстрируют более высокие шансы несогласованных результатов (ОШ 3,34, 95% ДИ 1,84–6,05). Доля ЛТБИ, оцененная с помощью ТКП и IGRA, среди людей, которым рекомендовано пройти скрининг в наших условиях, высока, что подчеркивает необходимость профилактических стратегий. Медицинским работникам результаты ТКП следует читать с осторожностью, поскольку более высокая доля противоречивых результатов с положительными результатами ТКП предполагает влияние бустерной реакции в этой группе.
© 2021 Автор(ы).Опубликовано S. Karger AG, Базель от имени Национальной школы общественного здравоохранения NOVA. туберкулез (ТБ) é uma prioridade para o controlo da doença. Не существует золотого стандарта для диагностики латентной инфекции (ITBL), внутрикожного туберкулинового теста (TST) и теста обнаружения интерференционной гаммы (IGRA).O objetivo deste estudo foi determinar proporção de ILTB através do TST e do teste IGRA e avaliar osfatores associados à discordância de resultsados entre testes, учитывал различные группы риска, согласующиеся с пунктом rastreio no Nordeste de Portugal. Os dados foram obtidos da base de dados de utentes de uma unidade local de saúde com suspeita de ILTB e orientados para rastreio (janeiro de 2014 dezembro de 2015). Foi obtida proporção de ILTB usando ambos os testes. Os modelos de regressão logística avaliaram os fatores de risco para um teste positivo e para resultsados discordantes entre os testes.Obtiveram-se как оценочное отношение шансов (OR) e o respetivo intervalo de confiança de 95% (IC95%). Dos 367 pacientes incluídos na análise, 79,8% um TST positivo e 46,0 % delestiveram um IGRA positivo. Сравнение с контактными лицами, вызывающими активный туберкулез, или риском положительной ТКП у основных специалистов и президентов (ОШ = 4,38; 95% ДИ: 1,59–12,09 e ОШ = 4,74, 95% ДИ: 1,45–15,49, повторно) e менорный иммунокомпрометид (ОШ = 0,14; 95% ДИ: 0,06–0,31). Por outro lado, os profissionais de saúde (ИЛИ = 0.44; 95% ДИ: 0,24–0,80) e Иммунокомпрометид (ОШ = 0,24; IC95%: 0,10–0,56) присутствует положительный менорный риск IGRA. У 42,0% согласующихся положительных результатов, 16,1% согласованных отрицательных результатов и 41,9% несогласующихся результатов, com os profissionais de saúde a Presentarem maior risco de resultsados discordantes (ОШ = 3,34; 95% ДИ: 1,84–6,05). A proporção de ILTB estimada pelo TST e IGRA Nestes utentes aconselhados a fazer rastreio revelou-se alta, evidenciando a necessidade de estratégias preventivas.Entre os profissionais de saúde, os resultsados do TST devem ser lidos com cautela, pois a maior proporção de resultsados discordantes com um TST positivo sugere o Impacto do efeito booster neste grupo.
Введение
Туберкулез (ТБ) возникает в результате инфекции Mycobacterium tuberculosis , которая поражает почти четверть населения мира и остается важной причиной плохого состояния здоровья и смертности во всем мире [1]. Более 90% инфицированных остаются бессимптомными и не заразными из-за стойкого иммунного ответа на M.tuberculosis , который сохраняется в организме человека в виде латентной туберкулезной инфекции (ЛТБИ). Люди с ЛТИ подвержены риску развития активной формы туберкулеза и могут стать заразными в течение жизни, что может привести к смерти, если их не лечить [2]. Определенные группы людей имеют высокий риск развития ТБ, в том числе контакты больных ТБ [3-5], ВИЧ-позитивные люди [6], работники здравоохранения (МР) [6, 7], иммигранты из стран с высоким бременем ТБ [3], пациенты с ослабленным иммунитетом [6], заключенные, бездомные и наркоманы [8].
Профилактика лиц с ЛТБИ является стратегией борьбы с активным туберкулезом, однако точных методов выявления таких лиц не существует [1]. Диагностика ЛТБИ основывается на измерении иммунного ответа хозяина на антигены M.tuberculosis , который основан на специфическом иммунном ответе против бациллы, с использованием туберкулинового кожного теста (ТКП) или анализа высвобождения интерферона-гамма (ИФН-γ). (ИГРА) [2, 9-11]. TST измеряет реакцию гиперчувствительности замедленного типа на внутрикожную инъекцию очищенного белкового производного, сырой смеси нескольких микобактериальных антигенов, общих для M.tuberculosis , M. bovis БЦЖ и нетуберкулезных микобактерий (НТМ) [10]. В свою очередь, IGRA представляет собой анализ крови in vitro, выявляющий высвобождение IFN-γ циркулирующими Т-лимфоцитами в ответ на эпитопы из специфических антигенов, ассоциированных с комплексом M.tuberculosis , а именно ESAT-6 и CFP-10 [2, 11]. TST является простым и экономически эффективным тестом, но требует последующего визита для интерпретации результатов [10, 11], в то время как для IGRA требуются образцы крови и лаборатория для быстрой их обработки после сбора [11].
Существует ряд исследований по сравнению эффективности ТКП и IGRA у населения в целом [12] и у конкретных подгрупп населения, таких как дети, люди с ослабленным иммунитетом, лица из стран с высоким уровнем заболеваемости туберкулезом [13], контакты с активным туберкулезом случаи [4, 14, 15], бездомные, беженцы, ВИЧ-позитивные случаи [16] и медработники [14, 17-22]. В исследованиях нет согласованных результатов, и такая вариабельность может быть объяснена различиями в демографических характеристиках [16, 20], бременем туберкулеза в сообществе [4, 13], иммунным статусом [13] или распространенностью вакцинации БЦЖ [16]. , 20].
Хотя уровень заболеваемости ТБ в Португалии снижается, он остается одним из самых высоких показателей ТБ в Европе [23], что требует эффективного выявления и лечения лиц с ЛТБИ. Насколько нам известно, эффективность ТКП и IGRA для диагностики ЛТБИ в португальском населении ограничивалась скринингом HCW [21, 22]. Таким образом, мы стремились определить долю ЛТБИ с помощью ТКП и теста IGRA, а также оценить факторы риска, связанные с несоответствием результатов между тестами в нескольких группах риска, рекомендованных для скрининга в Северо-Восточной Португалии.
Материалы и методы
Это исследование проводилось в отделении общественного здравоохранения на северо-востоке Португалии. Данные были собраны из базы данных пациентов с подозрением на ЛТИ и рекомендованы для скрининга. В наших условиях обязательно заполнение анкеты с просьбой предоставить соответствующую информацию до того, как пациенты пройдут скрининговые тесты на ЛТБИ. В анкете запрашивается следующая информация: возраст, пол, статус прививки БЦЖ, диагноз ВИЧ/SIDA и причина подозрения на ЛТИ.Все 377 пациентов, прошедших скрининг в период с января 2014 г. по декабрь 2015 г., которые прошли как ТКП, так и IGRA, считались подходящими участниками. После исключения 3 (0,8%) пациентов с неопределенной IGRA и 7 (1,9%) пациентов из-за диагноза активного ТБ в настоящий анализ были включены 367 участников.
TST и IGRA
Кровь была собрана для IGRA и проанализирована с помощью набора QuantiFERON Gold In-Tube (Cellestis/Qiagen, Дюссельдорф, Германия). Метод IGRA позволяет количественно определить IFN-γ, высвобождаемый после инкубации крови с коктейлем пептидов, полученных из ESAT-6, CFP-10 и TB7.7 (Rv2654c) антигенов [24]. IGRA считали положительным, если уровень IFN-γ составлял 0,35 МЕ/мл и более [24].
ТКП проводили с помощью внутрикожной инъекции 5 ЕД туберкулина (Институт Пастера, Париж, Франция) на ладонной стороне предплечья. Поперечный диаметр уплотнения определяли через 72 ч [25]. В соответствии с последними рекомендациями ТКП считалась положительной, если диаметр уплотнения составлял 5 мм и более у детей в возрасте до 5 лет, людей с ослабленным иммунитетом и лиц с диагнозом ВИЧ/SIDA [26].
Потенциальные предикторы
Следующие переменные считались потенциальными предикторами положительности ТКП или IGRA и были извлечены из базы данных: пол, возраст, иммунизация БЦЖ, ВИЧ-статус и группа риска по ТБ (контакты с активным ТБ, медработники, заключенные, иммунодепрессия статус и другие обстоятельства).
Статистический анализ
Участники были классифицированы как ЛТИ-положительные или ЛТИ-отрицательные для каждого теста (TST и IGRA) и были разделены на четыре группы: отрицательные для обоих тестов (TST-/IGRA-), положительные для обоих тестов (TST+/IGRA+). ), дискордантный с положительным результатом TST (TST+/IGRA-) и дискордантный с положительным IGRA (TST-/IGRA+).Доля положительных ТКП (≥5 мм у детей в возрасте до 5 лет, людей с ослабленным иммунитетом и лиц с диагнозом ВИЧ/SIDA или ≥10 мм у других людей) или положительных IGRA (≥0,35 МЕ/мл), конкордантно-положительных , конкордантные отрицательные и дискордантные тесты были рассчитаны. Был проведен двумерный анализ для сравнения групп по результатам ТКП и IGRA. Был проведен многомерный логистический регрессионный анализ для оценки связи между положительным результатом ТКП, положительным результатом IGRA или дискордантным результатом в качестве зависимых переменных и возрастом, полом, ВИЧ-статусом, статусом иммунизации БЦЖ и группой риска пациентов в качестве потенциальных предикторов. доли ЛТБИ.Были получены оценки отношения шансов (ОШ) с поправкой на все эти потенциальные предикторы и соответствующий 95% доверительный интервал (95% ДИ). Анализы проводились с использованием статистического программного обеспечения SPSS для Windows (версия SPSS 26.0). Общий уровень значимости был установлен на уровне 0,05.
Результаты
Всего в этот анализ было включено 367 человек; 42,7% ( n = 157) были контактными больными активным туберкулезом, 23,4% ( n = 86) были медработниками, 15,8% ( n = 58) были заключенными, 10.1% ( n = 37) были людьми с иммуносупрессией, а 7,9% ( n = 29) соответствовали другим группам риска. Из всех участников 79,8% ( n = 293) имели положительную ТКП и 46,0% ( n = 169) из них имели положительную IGRA.
В таблице 1 представлена доля положительных результатов ТКП или положительных результатов IGRA. Согласно двумерному анализу, доля положительных ТКП значительно различалась в группах риска по ТБ ( p < 0,001), варьируя от 40.от 5% (люди с ослабленным иммунитетом) до 94,2% (медицинские работники). Доля положительных результатов IGRA значительно различалась между группами при иммунизации БЦЖ ( p = 0,005), варьируя от 32,9% (вакцинированные) до 58,1% (невакцинированные), а также между группами риска по туберкулезу ( p = 0,001). , варьируя от 27,0% (люди с ослабленным иммунитетом) до 60,3% (заключенные). После корректировки всех других переменных пожилые люди с большей вероятностью имели положительный результат ТКП (ОШ 1,03, 95% ДИ 1,01–1,05) или положительный результат IGRA (ОШ 1.02, 95% ДИ 1,00–1,03). По сравнению с людьми, контактировавшими с больными туберкулезом, вероятность положительного результата ТКП была выше среди медработников и заключенных (ОШ 4,38, 95% ДИ 1,59–12,09 и ОШ 4,74, 95% ДИ 1,45–15,49 соответственно), но ниже среди субъектов с ослабленным иммунитетом (ОШ 0,14, 95% ДИ 0,06–0,31). Вероятность положительного результата IGRA была ниже среди вакцинированных БЦЖ людей (ОШ 0,34, 95% ДИ 0,15–0,76) по сравнению с невакцинированными людьми. По сравнению с людьми, контактировавшими с больными ТБ, у медработников и людей с ослабленным иммунитетом шансы положительного результата IGRA были ниже (ОШ 0,44, 95% ДИ 0.24–0,80 и ОШ 0,24, 95% ДИ 0,10–0,56 соответственно).
Таблица 1.
Предикторы положительного IGRA или положительного TST
В таблице 2 показано соотношение несогласующихся и согласующихся результатов по группам в соответствии с потенциальными предикторами. Было 42,0% ( n = 154) ТКП+/ИГРА+, 16,1% ( n = 59) ТКП-/ИГРА-, 4,1% ( n = 15) ТКП-/ИГРА+ и 37,9% ( н = 139) ТСТ+/ИГРА–. Согласно двумерному анализу, некоторые переменные показали значительную связь с противоречивыми результатами, а именно возраст ( p = 0.009), иммунизация БЦЖ ( p = 0,019) и группы риска по туберкулезу ( p < 0,001). Однако после поправки на все остальные переменные только группы риска по ТБ были связаны с противоречивым результатом; по сравнению с лицами, контактировавшими с больными ТБ, у медработников вероятность несогласованного результата была в 3 раза выше (ОШ 3,34, 95% ДИ 1,84–6,05).
Таблица 2.
Риск несоответствия результатов ТКП+/IGRA–
Обсуждение
Это первое исследование, проведенное на северо-востоке Португалии по доле ЛТБИ, для этой цели мы использовали ТКП и IGRA.Согласно нашим результатам, доля ЛТБИ, оцененная IGRA и TST, составила 46 и 80% соответственно. Среди медработников доля положительных IGRA составила 34%, что аналогично данным, представленным в предыдущем исследовании, проведенном в Португалии [21]. Однако, согласно недавнему систематическому обзору, распространенность ЛТИ среди медработников с использованием IGRA в странах с низким уровнем заболеваемости составила всего 16% [27]. Кроме того, доля ЛТБИ, обнаруженная нами среди контактов с ТБ и заключенных, была выше, чем в других европейских странах [4, 14, 28, 29].Наши результаты, вероятно, отражают бремя ТБ в Португалии, стране с одним из самых высоких показателей заболеваемости (20,5 новых случаев и рецидивов ТБ на 100 000 населения) и одним из самых низких показателей успешного лечения ТБ (37,3%) среди европейских стран в 2018 г. [23].
В предыдущих исследованиях сообщалось о связи между положительными результатами ТКП или IGRA и несколькими предикторами ТБ [5, 12, 15, 17-20], но в исследованиях нет согласованных результатов. Мы обнаружили связь между возрастом и положительными результатами обоих тестов, при этом пожилые люди представляют более высокий риск положительного теста в соответствии с некоторыми предыдущими исследованиями [12, 15].Однако в других исследованиях возраст был связан только с результатами IGRA [14, 18] или не существовало никакой связи между возрастом и положительным результатом, как с TST, так и с IGRA [5, 19, 20].
Мы не обнаружили связи между иммунизацией БЦЖ и положительным результатом ТКП. Интересно, что положительный результат IGRA был менее вероятен среди иммунизированных людей, в соответствии с предыдущими исследованиями, предполагающими актуальность скринингового теста IGRA для оценки ЛТБИ [12, 19]. Более высокая специфичность IGRA для выявления инфекции M.tuberculosis [29] и защитный эффект вакцинации БЦЖ на M.tuberculosis [12] может объяснить наши результаты.
Несмотря на отсутствие золотого стандарта для диагностики ЛТИ, мы сравнили IGRA с результатами ТКП для оценки доли ЛТИ среди людей с подозрением на ЛТБИ и рекомендовали пройти скрининг. Наши результаты показали низкую частоту TST-/IGRA- (16,1%), в то время как частота TST+/IGRA+ достигла 42,0%. Предыдущие исследования, в которых участвовали контакты с ТБ и медработники [14, 17, 19], сообщали о более низкой частоте TST+/IGRA+ и более высокой частоте TST–/IGRA–, чем мы обнаружили. В некоторых условиях диагноз ЛТБИ ставится только при положительных результатах обоих тестов [3]; поэтому наши результаты свидетельствуют о высоком риске ЛТИ среди людей, которым рекомендовано пройти скрининг в наших условиях, что требует профилактических стратегий против ТБ.
Обнаруженная нами доля ЛТИ была выше при использовании ТКП, чем при использовании IGRA, что приводит к более высокой доле ТКП+/IGRA– среди противоречивых результатов, и эти результаты согласуются с предыдущими исследованиями [14, 17, 19, 20 ]. Однако наш уровень противоречивых результатов (41,9%) был выше, особенно среди медработников (61%), чем сообщалось в предыдущих исследованиях [14, 17, 19]. Согласно нашим результатам, по сравнению с контактами с ТБ, у медработников была более высокая доля положительных результатов ТКП, но более низкая доля положительных результатов IGRA.Сообщалось, что IGRA обеспечивают более высокую специфичность, чем TST [30]. TST более чувствителен, чем IGRA [2, 11, 30], поскольку положительный TST может быть связан с вакцинацией БЦЖ или воздействием НТМ из окружающей среды [2, 11]. Согласно нашим результатам, вакцинация БЦЖ не объясняет противоречивые результаты после поправки на другие переменные, что указывает на влияние других факторов, а не вакцинации БЦЖ, на объяснение противоречивых результатов. Действительно, только HCW остается предиктором противоречивых результатов, а дискордантными результатами в этой группе являются TST+/IGRA–.Повторная ТКП в качестве стратегии надзора среди медработников может усилить реакцию ТКП среди лиц с предшествующей инфекцией M.tuberculosis или NTM [31, 32], аналогично тому, что наблюдалось среди людей, вакцинированных БЦЖ [32]. Неясно, можно ли объяснить эти результаты воздействием НТМ [2], поскольку инфекции НТМ, по-видимому, ответственны за положительные ТКП среди медработников [31].
В соответствии с рекомендациями ВОЗ для оценки ЛТБИ можно использовать либо ТКП, либо IGRA, поскольку нет убедительных доказательств того, что один тест следует предпочесть другому для прогнозирования прогрессирования заболевания до активной формы ТБ [8].Однако результаты ТКП и IGRA, которые мы наблюдали в группах риска, предполагают необходимость осторожности при чтении ТКП, поскольку на нее, по-видимому, влияют другие факторы, а не недавнее воздействие M. tuberculosis .
Настоящее исследование дает представление о доле ЛТБИ в нескольких группах риска по туберкулезу путем включения всех лиц с подозрением на ЛТИ в конкретном сообществе на северо-востоке Португалии, которым было рекомендовано пройти скрининг. Тем не менее, есть некоторые ограничения. Поскольку мы использовали данные одного отдела общественного здравоохранения, мы должны быть осторожны при обобщении результатов.Кроме того, мы упустили некоторые детали. У нас нет информации о количестве лет работы в сфере здравоохранения, уровне профессионального риска или категории работы, а также времени воздействия M. tuberculosis , которые, как сообщалось, связаны с ЛТИ [4, 17, 33]. .
Заключение
Доля ЛТИ, оцененная с помощью ТКП и IGRA, высока среди людей, которым рекомендовано пройти скрининг на ЛТИ в Северо-Восточной Португалии, что подчеркивает необходимость стратегий борьбы с ТБ. Интерпретация результатов ТКП требует осторожности, особенно среди медработников, из-за более высокой доли ТКП+/IGRA–, что предполагает влияние бустерной реакции на предыдущую М.туберкулез облучение. Необходимы дальнейшие исследования с включением более подробной информации об участниках.
Благодарности
Авторы благодарят Unidade Local de Saúde do Nordeste за предоставление доступа к данным.
Заявление об этике
Авторы заявляют, что соблюдали этические нормы. Протокол исследования был одобрен Комитетом по этике Местного объединения единства Сауде-ду-Нордесте (№ 28/2020).
Заявление о конфликте интересов
Авторы заявляют об отсутствии конфликта интересов.
Источники финансирования
Для этого исследования не было источников финансирования.
Вклад авторов
A.L.F.A. задумал это исследование и участвовал в сборе данных; Б.М.П. собрал данные; С.М.Т. провели статистический анализ данных. А.Дж.Н. руководил всеми аспектами этой работы. Все авторы внесли свой вклад в интерпретацию результатов, написание статьи и корректуру рукописи.
Эта статья находится под лицензией Creative Commons Attribution-NonCommercial 4.0 Международная лицензия (CC BY-NC). Использование и распространение в коммерческих целях требует письменного разрешения. Дозировка препарата: авторы и издатель приложили все усилия, чтобы гарантировать, что выбор препарата и дозировка, указанные в этом тексте, соответствуют текущим рекомендациям и практике на момент публикации. Тем не менее, в связи с продолжающимися исследованиями, изменениями в правительственных постановлениях и постоянным потоком информации, касающейся лекарственной терапии и реакций на лекарства, читателю настоятельно рекомендуется проверять вкладыш в упаковке для каждого лекарства на предмет любых изменений в показаниях и дозировке, а также для дополнительных предупреждений. и меры предосторожности.Это особенно важно, когда рекомендуемый агент является новым и/или редко используемым лекарственным средством. Отказ от ответственности: заявления, мнения и данные, содержащиеся в этой публикации, принадлежат исключительно отдельным авторам и участникам, а не издателям и редакторам. Появление рекламы и/или ссылок на продукты в публикации не является гарантией, одобрением или одобрением рекламируемых продуктов или услуг или их эффективности, качества или безопасности. Издатель и редактор(ы) отказываются от ответственности за любой ущерб, нанесенный людям или имуществу в результате любых идей, методов, инструкций или продуктов, упомянутых в содержании или рекламе.
Манту | Рабочая посадка
Манту не является простой иммунизацией. Он никогда не был лицензирован, и производители не собираются платить за его лицензию. Поэтому применяются особые правила. Агентство по регулированию лекарственных средств и изделий медицинского назначения разъяснило процедуру в электронном письме мне от 27/05/2015 следующим образом:
Мы понимаем, что Манту является нелицензионным лекарственным средством. По закону нелицензированное лекарство должно быть заказано врачом или другим правомочным независимым лицом, назначающим лекарства (например, независимой медсестрой, выписывающей рецепты) для отдельных пациентов под его/ее собственную ответственность.Таким образом, врач несет ответственность за решение о введении нелицензированной вакцины соответствующему лицу. Ему или ей необходимо авторизовать администрацию, и это может быть сделано через конкретное указание пациента, охватывающее несколько пациентов. Однако направления должны быть для названных пациентов. Страницы авторизации с именами, впоследствии добавленными кем-то другим, будет недостаточно.
В связи с подобными запросами мы также сообщили, что врач, назначающий лекарство, должен иметь адекватные знания о состоянии здоровья пациента и быть уверенным в том, что лекарство, которое будет назначено, отвечает индивидуальным потребностям каждого пациента в этом списке.
Те же соображения применимы и к другим независимым врачам, назначающим препараты, таким как медсестры и фармацевты, использующим нелицензионные продукты.
Таким образом, службы OH, предоставляющие Манту, должны подготовить список пациентов, нуждающихся в Манту. Затем это должно быть подписано (или иным образом санкционировано) врачом или правомочным независимым врачом. Вы не можете подписать чистый лист и добавить имена позже.
Вероятно, было бы целесообразно иметь надежную политику для оценки тех, кто нуждается в Манту, чтобы обеспечить адекватную информацию о здоровье пациента и убедиться, что это соответствует потребности.Медсестра может добавить свои имена в список, отформатированный как Указание для конкретного пациента. Затем это может быть подписано OHP. При необходимости список можно отправить по электронной почте в OHP, и ответ по электронной почте может быть авторизацией.
Туберкулин — wikidoc
Главный редактор: C. Майкл Гибсон, MS, MD [1]; Заместитель главного редактора (ов): Киран Сингх, доктор медицины [2]
WikiDoc НЕ ДАЕТ НИКАКИХ ГАРАНТИЙ ДЕЙСТВИТЕЛЬНОСТИ. WikiDoc не является профессиональным поставщиком медицинских услуг и не может заменить лицензированного поставщика медицинских услуг.WikiDoc задуман как образовательный инструмент, а не как средство оказания медицинской помощи. Образовательный контент на страницах WikiDoc, посвященных лекарствам, основан на вкладыше в пакет FDA, материалах Национальной медицинской библиотеки и практических рекомендациях/согласованных заявлениях. WikiDoc не пропагандирует введение каких-либо лекарств или устройств, которые не соответствуют их маркировке. Пожалуйста, прочитайте наш полный отказ от ответственности здесь.
Обзор
Туберкулин — это диагностический агент, одобренный FDA для диагностики туберкулезной инфекции.Общие побочные реакции включают эритему в месте инъекции, обморок, реакцию гиперчувствительности.
Показания и дозировка для взрослых
Показания и дозировка с маркировкой FDA (для взрослых)
Показания
- TUBERSOL, туберкулиновое очищенное производное белка (манту), показано для диагностики туберкулезной инфекции (ТБ) у лиц с повышенным риском развития активного заболевания.
- Центры по контролю и профилактике заболеваний (CDC) опубликовали рекомендации для групп населения, которым может быть полезна туберкулиновая кожная проба (ТКП).Текущие рекомендации доступны по телефону:
- Предыдущая вакцинация БЦЖ не является противопоказанием для туберкулинового тестирования. Результаты кожных проб у лиц, вакцинированных БЦЖ, могут использоваться для подтверждения или исключения диагноза туберкулезной инфекции. Тем не менее, одобренный FDA анализ высвобождения гамма-интерферона предпочтительнее туберкулиновой кожной пробы для лиц в возрасте 5 лет и старше, которые ранее были вакцинированы БЦЖ.
Дозировка
- Пять (5) туберкулиновых единиц (ТЕ) на тестовую дозу 0.1 мл — это стандартная концентрация, используемая для внутрикожной пробы Манту.
Применение и дозировка не по назначению (для взрослых)
Использование, поддерживаемое руководством
- Имеется ограниченная информация относительно Off-Label Guideline-Supported Use туберкулина у взрослых пациентов.
Использование, не соответствующее рекомендациям
- Имеется ограниченная информация о применении туберкулина не по прямому назначению, не поддерживаемому рекомендациями, у взрослых пациентов.
Педиатрические показания и дозировка
Показания и дозировка с маркировкой FDA (для детей)
- Информация об использовании туберкулина с маркировкой FDA у детей ограничена.
Использование и дозировка не по прямому назначению (для детей)
Использование, поддерживаемое руководством
- Имеется ограниченная информация о Off-Label Guideline-Supported Use туберкулина у педиатрических пациентов.
Использование, не соответствующее рекомендациям
- Имеется ограниченная информация о применении туберкулина не по прямому назначению, не поддерживаемому рекомендациями, у педиатрических пациентов.
Противопоказания
- Аллергия на любой компонент TUBERSOL или анафилактическая или другая аллергическая реакция на предыдущий тест туберкулина PPD является противопоказанием к использованию TUBERSOL.
- TUBERSOL не следует вводить:
- человек, у которых была тяжелая реакция (например, некроз, волдыри, анафилактический шоки или изъязвления) до предыдущего TST,
- с подтвержденным активным туберкулезом или наличием в анамнезе лечения туберкулезной инфекции или заболевания,
- Лица с обширными ожогами или экземой.
Предупреждения
Гиперчувствительность
- Аллергические реакции могут возникать после применения туберсола даже у лиц, ранее не имевших повышенной чувствительности к компонентам продукта.Инъекции адреналина (1:1000) и другие соответствующие препараты, используемые для контроля немедленных аллергических реакций, должны быть доступны немедленно.
Обморок
- Обморок (обморок) может возникнуть в связи с введением инъекционных препаратов, включая ТУБЕРСОЛ. Должны быть предусмотрены процедуры, чтобы избежать травм при падении и восстановить церебральную перфузию после обморока.
Побочные реакции
Опыт клинических испытаний
- Индурация в месте инъекции туберсола является ожидаемой реакцией на положительный кожный тест.
- Информация о нежелательных явлениях была собрана на основе исторических клинических исследований и постмаркетингового опыта применения TUBERSOL.
Общие расстройства и состояния в месте введения
Боль в месте инъекции, зуд в месте инъекции и дискомфорт в месте инъекции.
- Эритема в месте инъекции или сыпь в месте инъекции (без уплотнения), возникающие в течение 12 часов после тестирования. Эти реакции не указывают на инфицирование туберкулезом.
- Кровоизлияние в месте инъекции и гематома в месте инъекции в течение трех дней после введения теста.
- Везикулы в месте инъекции, язва в месте инъекции или некроз в месте инъекции у лиц с высокой чувствительностью.
- Рубец на месте инъекции в результате резко положительной реакции.
Нарушения иммунной системы
Заболевания органов дыхания, грудной клетки и средостения
Болезни кожи и подкожной клетчатки
Заболевания нервной системы
- Предобморочное состояние, обмороки (включая обмороки, связанные с тонико-клоническими движениями и другой судорожной активностью), иногда приводящие к временной потере сознания при травме
Пострегистрационный опыт
На этикетке препарата имеется ограниченная информация о Postmarketing Experience туберкулина.
Лекарственные взаимодействия
- Реакция на тест может быть снижена или подавлена у лиц, получающих кортикостероиды или иммунодепрессанты.
- Реакция на TUBERSOL может быть временно подавлена некоторыми живыми вирусными вакцинами (корь, эпидемический паротит, краснуха, оральный полиомиелит, желтая лихорадка и ветряная оспа). Если недавно была введена парентеральная живая аттенуированная вирусная вакцина, туберкулиновое тестирование следует отложить более чем на 1 месяц после вакцинации.
- Когда туберкулиновый скрининг требуется одновременно с коревой вакциной или другой парентеральной живой аттенуированной вирусной вакциной, предпочтительным вариантом является одновременное введение ТУБЕРСОЛА и вакцины в разные места.
Использование в определенных группах населения
Беременность
Категория беременности (FDA): БЕРЕМЕННОСТЬ КАТЕГОРИЯ C
- Исследования репродукции животных с TUBERSOL не проводились.Также неизвестно, может ли ТУБЕРСОЛ нанести вред плоду при введении беременной женщине или повлиять на репродуктивную способность. ТУБЕРСОЛ следует давать беременной женщине только в случае крайней необходимости.
Категория беременности (Австралия):
- Австралийский комитет по оценке лекарственных средств (ADEC) Категория беременных
Австралийский комитет по оценке лекарственных средств (ADEC) не рекомендует применять туберкулин у беременных женщин.
Работа и доставка
Руководство FDA по использованию туберкулина во время родов отсутствует.
Кормящие матери
- Неизвестно, проникает ли ТУБЕРСОЛ в грудное молоко. Поскольку многие препараты выделяются с грудным молоком, следует соблюдать осторожность при назначении Туберсола кормящим женщинам.
Использование в педиатрии
- Возрастных противопоказаний к кожным туберкулиновым пробам у младенцев нет. Поскольку их иммунная система незрела, многие младенцы в возрасте до 6 недель, инфицированные M.туберкулез не реагируют на туберкулиновые пробы.
Использование в пожилом возрасте
- Клинические исследования TUBERSOL не включали достаточное количество субъектов в возрасте 65 лет и старше, чтобы определить, отличаются ли их реакции от более молодых субъектов.
Пол
Руководство FDA по применению туберкулина для определенных полов отсутствует.
Гонка
Нет руководства FDA по использованию туберкулина в отношении определенных расовых групп населения.
Почечная недостаточность
Руководство FDA по применению туберкулина у пациентов с почечной недостаточностью отсутствует.
Печеночная недостаточность
Руководство FDA по применению туберкулина у пациентов с печеночной недостаточностью отсутствует.
Самки с репродуктивным потенциалом и самцы
Руководство FDA по применению туберкулина у женщин с репродуктивным потенциалом и у мужчин отсутствует.
Пациенты с ослабленным иммунитетом
Нет руководства FDA по использованию туберкулина у пациентов с ослабленным иммунитетом.
Администрирование и мониторинг
Администрация
- TUBERSOL показан только для внутрикожных инъекций. Не вводить внутривенно, внутримышечно или подкожно. Если происходит подкожная инъекция, тест не может быть интерпретирован.
- Перед использованием проверьте на наличие посторонних твердых частиц и/или изменение цвета. Если эти условия существуют, не вводить продукт.
- Для каждой инъекции используйте отдельный шприц и иглу.
- Для выполнения пробы Манту рекомендуется следующая процедура:
- Предпочтительным местом проведения пробы является ладонная поверхность предплечья. Избегайте областей на коже, которые покраснели или опухли. Избегайте видимых вен.
- Очистите участок кожи подходящим гермицидом и дайте ему высохнуть перед инъекцией антигена.
- Введите тестовую дозу (0.1 мл) TUBERSOL с помощью шприца на 1 мл, откалиброванного с точностью до десятых долей и оснащенного короткой иглой размером от четверти до половины дюйма, калибра 26 или 27.
- Протрите пробку флакона подходящим бактерицидным средством и дайте ему высохнуть перед введением иглы. Затем аккуратно вставьте иглу через пробку и наберите в шприц 0,1 мл ТУБЕРСОЛА. Избегайте введения избыточного воздуха при удалении каждой дозы, чтобы не создать избыточное давление во флаконе и, возможно, вызвать просачивание в месте прокола.
- Введите острие иглы в самые поверхностные слои кожи срезом иглы, направленным вверх, и введите дозу путем медленной внутрикожной инъекции. Если внутрикожная инъекция выполнена правильно, на кончике иглы поднимется определенный бледный пузырек диаметром около 10 мм (⅜»). Этот пузырек рассосется в течение нескольких минут. Не перевязывайте это место. После инъекции в месте введения может появиться капля крови.Слегка промокните участок, чтобы удалить кровь, но избегайте выдавливания введенной жидкости для туберкулинового теста.
- В случае неправильно выполненной инъекции (т. е. отсутствие пузырька) немедленно повторите тест в другом месте, на расстоянии не менее 2 дюймов от первого места, и обведите второе место инъекции, чтобы указать, что это сайт для чтения.
- Сообщите пациенту о необходимости вернуться для прочтения теста квалифицированным медицинским работником.Самостоятельное чтение может быть неточным и настоятельно не рекомендуется.
Мониторинг
ИНТЕРПРЕТАЦИЯ ТЕСТА
- Кожные пробы должны быть прочитаны обученным медицинским работником через 48–72 часа после введения TUBERSOL. Чувствительность кожных проб определяется только уплотнением; покраснение не следует измерять.
- Измерьте диаметр уплотнения поперек длинной оси предплечья и запишите результат измерения в миллиметрах (включая 0 мм).(8) Кончик шариковой ручки, осторожно сдвинутый под углом 45° к месту инъекции, остановится на краю уплотнения.
- Также запишите наличие и размер (если есть) некроза и отека, хотя они не используются при интерпретации теста.
Положительные реакции
- Туберкулиновая реактивность может указывать на латентную инфекцию, предшествующую инфекцию и/или заболевание M.tuberculosis и не обязательно указывает на наличие активного туберкулезного заболевания.Лица с положительными туберкулиновыми реакциями должны считаться положительными в соответствии с действующими рекомендациями общественного здравоохранения и направляться для дальнейшего медицинского обследования. Повторное тестирование неинфицированных людей не повышает их чувствительность к TUBERSOL.
- Значимость измерений уплотнения в диагностике латентной ТБ-инфекции следует учитывать с точки зрения анамнеза пациента и риска развития активного ТБ, как указано в таблице 1.
- Конверсия TST определяется как увеличение уплотнения на ≥ 10 мм в течение 2-летнего периода, независимо от возраста.
- Следует учитывать возможность того, что чувствительность кожных проб также может быть обусловлена предшествующим контактом с атипичными микобактериями или предшествующей вакцинацией БЦЖ.
Отрицательные реакции
- Лицо, не показавшее положительной реакции на 5 ТЕ при первом тесте, но с подозрением на ТБ, может пройти повторное тестирование с 5 ТЕ.Любой человек, который не показывает положительной реакции на первоначальную инъекцию 5 ТЕ или повторный тест с 5 ТЕ, может считаться туберкулинотрицательным.
Ложноположительные реакции
- Ложноположительные туберкулиновые реакции могут возникать у лиц, инфицированных другими микобактериями, в том числе при вакцинации БЦЖ. положительная реакция ТКП, особенно если человек был или находится в группе повышенного риска заражения туберкулезом.
Ложноотрицательные реакции
- Не у всех инфицированных людей будет отсроченная реакция гиперчувствительности на туберкулиновую пробу.
- У лиц пожилого возраста или тех, кто проходит тестирование впервые, реакции могут развиваться медленно и достигать пика только через 72 часа.
- Поскольку для развития туберкулиновой чувствительности может потребоваться до 8 недель после заражения M.tuberculosis, лица с отрицательным результатом туберкулиновой пробы менее 8 недель после возможного контакта с ТБ должны пройти повторное тестирование через ≥8–10 недель после последнего известного или подозреваемого заражения. воздействие.
Измененный иммунный статус
- Нарушение или ослабление клеточно-опосредованного иммунитета (КМИ) потенциально может вызвать ложноотрицательную туберкулиновую реакцию. Сообщалось, что многие факторы вызывают снижение способности реагировать на туберкулиновый тест при наличии туберкулезной инфекции, включая вирусные инфекции (например, корь, эпидемический паротит, ветряная оспа и ВИЧ), живые вакцины против вируса (например, кори, эпидемического паротита, краснухи, пероральные инфекции). полиомиелит и желтая лихорадка), распространенный туберкулез, другие бактериальные инфекции, лейкемия, саркоидоз, грибковые инфекции, метаболические нарушения, состояния с низким содержанием белка, болезни, поражающие лимфоидные органы, лекарственные препараты (кортикостероиды и многие другие иммунодепрессанты), злокачественные новообразования или стресс.ТКП следует отложить для пациентов с серьезными вирусными инфекциями или вакцинацией против живого вируса в прошлом месяце. Больные простудой могут пройти туберкулиновую пробу.
- Поскольку результаты ТКП у ВИЧ-инфицированных менее надежны по мере снижения количества CD4, скрининг следует проводить как можно раньше после заражения ВИЧ.
IV Совместимость
- На этикетке препарата имеется ограниченная информация о совместимости IV Туберкулина .
Передозировка
- На этикетке препарата имеется ограниченная информация о Хронической передозировке туберкулина.
Фармакология
Механизм действия
- Сенсибилизация после инфицирования микобактериями происходит главным образом в регионарных лимфатических узлах. Малые лимфоциты (Т-лимфоциты) пролиферируют в ответ на антигенный стимул с образованием специфически сенсибилизированных лимфоцитов. Через 3-8 недель эти лимфоциты попадают в кровоток и циркулируют годами.(7) Последующая повторная стимуляция этих сенсибилизированных лимфоцитов тем же или подобным антигеном, например внутрикожная инъекция TUBERSOL, вызывает местную реакцию, опосредованную этими клетками.
- Характерно, что отсроченные реакции гиперчувствительности на туберкулин начинаются через 5–6 часов, достигают максимума через 48–72 часа и стихают в течение нескольких дней. Результирующий иммунный ответ состоит из индурации из-за клеточной инфильтрации и иногда везикуляции и некроза. Клинически реакция гиперчувствительности замедленного типа на туберкулин является проявлением предшествующей инфекции M.tuberculosis или различными нетуберкулезными бактериями.В большинстве случаев сенсибилизация вызывается естественной микобактериальной инфекцией или вакцинацией вакциной БЦЖ.
Структура
- TUBERSOL®, Очищенное туберкулиновое производное белка (манту) (PPD) (1) для внутрикожного туберкулинового тестирования получают из большой маточной партии Connaught Tuberculin (CT68) и представляют собой бесклеточную очищенную белковую фракцию, полученную из человеческого штамма Mycobacterium tuberculosis, выращенных на безбелковой синтетической среде и инактивированных. Использование стандартного препарата, полученного из одной партии (CT68), было принято для того, чтобы исключить различия между партиями одного и того же производителя.
- ТУБЕРСОЛ — прозрачная бесцветная жидкость.
- Перед выпуском каждая последующая партия тестируется на эффективность по сравнению со стандартным туберкулином PPD-S США.
- Независимые исследования, проведенные Службой общественного здравоохранения США на людях, определили количество CT68 в стабилизированном растворе, необходимое для обеспечения биоэквивалентности с туберкулином PPD-S (в фосфатном буфере без полисорбата 80) с использованием 5 единиц США (TU). Туберкулин PPD-S как стандарт.
Фармакодинамика
Информация о Фармакодинамике туберкулина на этикетке препарата ограничена.
Фармакокинетика
Существует ограниченная информация о фармакокинетике туберкулина на этикетке препарата.
Доклиническая токсикология
КАНЦЕРОГЕНЕЗ, МУТАГЕНЕЗ, НАРУШЕНИЕ ПЛОДОЛОЖНОСТИ
- TUBERSOL не оценивался на предмет его канцерогенного или мутагенного потенциала или снижения фертильности.
Клинические исследования
Информация о клинических исследованиях туберкулина на этикетке препарата ограничена.
Способ поставки
- TUBERSOL, очищенное туберкулиновое производное белка (манту), биоэквивалент 5 единиц США (TU) PPD-S на тестовую дозу (0,1 мл), поставляется в:
- 10-тестовый флакон, 1 мл. упаковка из 1 флакона, НДЦ № 54868-2972-1
- Пробка флакона для этого продукта не содержит натурального латексного каучука.
Хранение
- Хранить при температуре от 2° до 8°C (от 35° до 46°F). (21) Не замерзай. Выбросьте продукт, если он подвергся замораживанию.
- Беречь от света. На растворы туберкулина PPD может отрицательно повлиять воздействие света. Продукт следует хранить в темноте, за исключением случаев, когда дозы фактически извлекаются из флакона.
- Флакон TUBERSOL, который был введен и использовался в течение 30 дней, должен быть утилизирован.
- Не использовать после истечения срока годности.
Изображения
Изображения наркотиков
| Название наркотика : Ингредиент : |
| Это изображение таблетки предоставлено PillBox Национальной медицинской библиотеки. |
Панель для упаковки и этикеток
Это изображение предоставлено Национальной медицинской библиотекой. Это изображение предоставлено Национальной медицинской библиотекой.Информация для консультирования пациентов
На этикетке препарата содержится ограниченная информация о Информация для консультирования пациентов о туберкулине.
Меры предосторожности при обращении с алкоголем
- Взаимодействие алкоголя и туберкулина не установлено. Поговорите со своим врачом о последствиях приема алкоголя с этим лекарством.
Торговые марки
Похожие названия лекарств
Цена
Ссылки
Содержание этой этикетки FDA предоставлено Национальной медицинской библиотекой.
.


 Другие туберкулины, доступные на рынке
не стандартизированы. Твин 80 — моющее средство, добавляемое к туберкулину для
предотвращают их адсорбцию на стеклянных или пластиковых поверхностях. В настоящее время все
туберкулины производятся и стандартизируются с помощью Tween 80(4). Следовательно
старая концепция 1TU с твином 80 эквивалентна 5 TU без
Tween 80 применяется только к старому туберкулину (OT), а не к PPD-S или PPD-RT.
23.
Другие туберкулины, доступные на рынке
не стандартизированы. Твин 80 — моющее средство, добавляемое к туберкулину для
предотвращают их адсорбцию на стеклянных или пластиковых поверхностях. В настоящее время все
туберкулины производятся и стандартизируются с помощью Tween 80(4). Следовательно
старая концепция 1TU с твином 80 эквивалентна 5 TU без
Tween 80 применяется только к старому туберкулину (OT), а не к PPD-S или PPD-RT.
23. Поэтому сдвиг
до 2 ТЕ в нашей стране не рекомендуется. Для диагностики мы
следует продолжать использовать 1TU.
Поэтому сдвиг
до 2 ТЕ в нашей стране не рекомендуется. Для диагностики мы
следует продолжать использовать 1TU. Индурация из-за БЦЖ
и атипичных микобактерий меньше, чем обусловленных болезнями, на М.
tuberculosis и обычно составляет менее 10 мм(8).
Индурация из-за БЦЖ
и атипичных микобактерий меньше, чем обусловленных болезнями, на М.
tuberculosis и обычно составляет менее 10 мм(8).