Детская больница округа Муром — Поствакцинальные реакции, побочные реакции вакцин и возможные осложнения
Контрастная версия
ГБУЗ ВО ДБОМ, город Муром, улица Войкова, дом 17, корпус 2. колл-центр: 8(49234)2-90-72
Поствакцинальные реакции, побочные реакции вакцин и возможные осложнения
Природа вакцинальных реакций
- Введение в организм человека как живых, так и инактивированных бактериальных или вирусных вакцин приводит к развитию вакцинального процесса, нередко сопровождающегося стереотипными клиническими проявлениями, протекающими в виде общих (повышение температуры, недомогание, головная боль др.) и местных (гиперемия, болезненность, инфильтрат) реакций.
- Вакцинальные реакции для инактивированных вакцин, как правило, однотипны, а для живых вакцин специфичны. Они характеризуются кратковременным и нередко циклическим течением и обычно не вызывают серьезных расстройств жизнедеятельности организма.
 Однако в тех случаях, когда вакцинальные реакции проявляются в виде выраженного патологического процесса, их называют поствакцинальными осложнениями.
Однако в тех случаях, когда вакцинальные реакции проявляются в виде выраженного патологического процесса, их называют поствакцинальными осложнениями. - Различия между постпрививочными реакциями и поствакцинальными осложнениями весьма условны. Поэтому оба типа реакций объединяют термином «побочные реакции».
- Помимо «истинных» поствакцинальных осложнений, в постпрививочном периоде могут наблюдаться патологические процессы, возникающие в результате провоцирующего действия прививок. Речь идет об обострении хронических болезней и оживлении латентной инфекции у привитых. при этом прививки являются скорее не причиной, а скорее условием, благоприятствующим развитию указанных процессов.
Доказательства поствакцинальных осложнений.
- Появление клинических симптомов после введения вакцины вовсе не означает, что именно вакцина вызвала эти симптомы. Последние могут быть связаны с присоединением какой-либо интеркуррентной инфекции, которая может изменить и утяжелить реакцию организма на прививку, а в ряде случаев способствовать развитию поствакцинальных осложнений.

- В таких случаях для доказательства причинной связи между вакцинацией и патологическим синдромом должно быть проведено тщательное расследование. Так, после введения живых вирусных вакцин наиболее доказанной эта связь является при выделении и идентификации вакцинного штамма от больного. Вместе с тем, после прививки живой полиомиелитной вакциной вакцинный штамм может выделяться из стула вакцинированного в течение нескольких недель, и поэтому появление в этом периоде клинических симптомов энцефалита вовсе не означает, что они обусловлены вирусом полиомиелита. Более надежным доказательством причинной связи в таких случаях может быть выделение вируса из естественно стерильной ткани или жидкости организма, таких как мозг или ликвор.
Сроки возникновения реакций.
- Побочные действия вакцин, как правило, проявляются в пределах 4-х недель после иммунизации. лишь после БЦЖ-прививки остеомиелиты могут проявляться даже через 14 месяцев после вакцинации.
- Реакции на инактивированные вакцины обычно развиваются рано (в течение нескольких часов) и их проявления являются более кратковременными.

- При введении живых вакцин реакции (кроме аллергических немедленного типа) не могут проявляться раньше 4-го дня и более чем через 12-14 дней после введения коревой и 30 дней после введения полиомиелитной и паротитной вакцины. Это связано с тем, что общие реакции после прививок живыми вакцинами развиваются после «инкубационного периода», необходимого для размножения микроорганизма.
Виды побочных реакций
- Различают местные и общие реакции. Местные реакции возникают обычно на месте введения препарата и варьируют от легкого покраснения, лимфаденитов до тяжелого гнойного абсцесса. Общие реакции чаще всего проявляются в виде аллергических, а также незначительного или сильного повышения температуры с вовлечением в процесс различных систем и органов, наиболее тяжелым из которых является поражение центральной нервной системы.
- Часто встречающиеся побочные реакции
- У разных вакцин побочные эффекты могут различаться. Однако существует ряд реакций, которые могут встречаться во многих случаях:
- Аллергические реакции на компоненты вакцины.

- Эффекты болезни в мягкой форме.
- Живые вакцины могут быть опасны для людей с ослабленной иммунной системой (иммунодефицитами).
- Местные реакции в месте инъекции.
- Повышенная температура.
- При применении вакцин существует также другая опасность — с течением времени эффект прививки снижается, и пациент может заболеть. Тем не менее, болезнь будет проходить легче и давать меньше осложнений, чем у непривитых.
Частота поствакцинальных осложнений
- Первое место в структуре поствакцинальных осложнений занимают осложнения после АКДС-вакцинации (до 60% всех осложнений). Можно надеяться, что в перспективе широкое использование бесклеточного коклюшного компонента приведет к значительному снижению этих осложнений.
Наиболее частые причины осложнений
- Неправильная дозировка вакцины
- Неправильно выбрана техника иммунизации
- Нарушение техники стерилизации приборов
- Вакцина приготовлена с использованием неправильного растворителя
- Неправильное разведение вакцины
- Неправильно приготовление вакцины (например, вакцина не была перемешана перед употреблением)
- Загрязнение вакцины
- Неправильное хранение вакцины
- Не были приняты во внимание противопоказания
Вакцинные реакции
| Местные реакции на вакцинацию (в месте введения) | Общие реакции на вакцинацию |
|
|
Нормальные реакции на вакцины
| Вакцина | Нормальные реакции |
| БЦЖ | В месте инъекции появляется папула, затем она эрозируется, после чего на её месте остаётся рубчик. |
| Гепатит В | Болезненность в месте инъекции в течении 1-3-х дней. |
| АКДС | Боль и незначительная отёчность в месте инъекции, подъём температуры тела до субфебрильный — фебрильных цифр в течении 1-3 дней, редко более 3-х дней. |
| ОПВ | Протекает без общей реакции организма. |
| Корь, Краснуха, Эпид.паротит | Болезненность в месте инъекции и редко субфебрилитет. |
Осложнения связанные с вакцинацией
| Клиническая форма осложнений | Вакцины | Сроки |
| Анафилактический шок | Все кроме БЦЖ и ОПВ | Сразу и до 12 часов |
| Тяжёлые генерализованные аллергические реакции (отёк Квинке, с-м Лайелла, с-м Джонсона) | Все кроме БЦЖ и ОПВ | До 5 дней |
| Синдром сывороточной болезни | Все кроме БЦЖ и ОПВ | До 15 дней |
| Энцефалит | АКДС, АДС | До 3 дней |
| Коревая вакцина | С 5 по 15 день | |
|
|
|
|
Резидуальные судорожные состояния, афебрильные судороги, повторившиеся в течении 12 месяцев после прививки |
|
|
|
ОПВ |
|
| Тромбоцитопеническая пурпура | Коревая и краснушная вакцины | С 10 по 25 день |
| Артралгия, артрит | Краснушная вакцина | С 5 по 40 день |
| Генерализованная инфекция вызванная вакцинным штаммом | БЦЖ, БЦЖ-М | После 6 недель |
| Остеит (остит, остеомиелит) вызванный вакциной | БЦЖ, БЦЖ-М | После 6 недель |
| Лимфаденит, келоидный рубец | БЦЖ, БЦЖ-М | После 6 недель |
Противопоказания к вакцинации
- (Плановая вакцинация откладывается до окончания острых проявлений заболевания или обострения хронических заболеваний.
 При нетяжёлых ОРВИ, ОКИ прививки проводят сразу же после нормализации температуры.)
При нетяжёлых ОРВИ, ОКИ прививки проводят сразу же после нормализации температуры.)
- К группам вакцин:
- Ко всем вакцинам – сильная реакция на предыдущую дозу. (Сильной реакцией считается подъём температуры свыше 40,0 градусов, в месте введения вакцины отёк и гиперемия диаметром более 8 см.)
- Живые вакцины – ИДС, (первичный иммунодефицит, иммуносупресия, злокачественные новообразования, беременность)
- К отдельным вакцинам:
- БЦЖ – масса ребёнка < 2000 гр., келоидный рубец после 1-й дозы
- АКДС – прогрессирующее заболевание нервной системы, афебрильные судороги в анамнезе (афебрильные судороги – это судороги при температуре тела менее 38, 5 градусов и которых не было до вакцинации)
- АДС, АДС-М – абсолютных противопоказаний нет
- ЖКВ (коревая) – тяжёлая реакция на аминогликозиды
- ЖПВ (паротитная) – анафилаксия к яичному белку
- Краснушная – анафилаксия к яичному белку
- Гриппозная — анафилаксия к яичному белку
Риск развития осложнений после вакцинацией и риск после соответствующих инфекций
| Вакцина | Поствакцинальные осложнения число случаев/число вакцинированных |
Вероятность осложнений в случае заболевания непривитых |
| Корь-паротит-краснуха | Тромбоцитопения 1/40000 | до 1/300 |
| Асептический (паротитный) менингит (штамм Jeryl Lynn) меньше 1/100000 |
до 1/300 | |
| Корь | Тромбоцитопения 1/40000 | до 1/300 |
| Энцефалопатия 1/100000 | до 1/300 | |
| смертельный исход до 1/500 | ||
| Коклюш-дифтерия-столбняк | Энцефалопатия до 1/300000 | до 1/1200 |
| Коклюш смертельный исход 1/800 | ||
| Дифтерия смертельный исход 1/20 | ||
| Столбняк смертельный исход 1/5 | ||
| Вирус папилломы | Тяжёлая аллергическая реакция 1/500000 | Рак шейки матки до 1/4000 |
| Гепатит В | Тяжёлая аллергическая реакция1/600000 | Риск заражения до 1/700 |
| Туберкулёз | Диссеминированная БЦЖ-инфекция до 1/300000 | Риск заболеть до 1/500 |
| БЦЖ-остеит до 1/100 000 | ||
| Полиомиелит | Вакциноассоциированный вялый паралич до 1/160000 | Паралич до 1/100 |
| Характер осложнений | Частота при коклюше на 100000 случаев | Частота после вакцинации на 100000 вакцинированных |
| Стойкие мозговые нарушения | 600-2000 | 0,2-0,6 |
| Энцефалопатия и энцефалит | 90-4000 | 0,1-3,0 |
| Судороги | 600-8000 | 0,3-90 |
| Смерть | 100-4000 | 0,2 |
- Помните, что своевременно сделанная прививка защитит Вас и Ваших близких от инфекционных заболеваний и их тяжелых осложнений.
 Отказываться от прививок не стоит, так как это высочайшее изобретение человечества, которое позволило сохранить миллионы человеческих жизней.
Отказываться от прививок не стоит, так как это высочайшее изобретение человечества, которое позволило сохранить миллионы человеческих жизней.
- Вы здесь:
- Главная
- Информация для пациентов
- Статьи врачей
- Потница у детей
Поствакцинальные реакции и осложнения: как обезопасить ребенка
- Главная >
- Вакцинация >
- Поствакцинальные реакции и осложнения: как обезопасить ребенка
Нельзя забывать, что прививка является иммунобиологическим препаратом, который вводится в организм с целью формирования стойкой невосприимчивости к определенным, потенциально опасным инфекционным заболеваниям. Именно из-за своих свойств и назначения прививки способны вызывать определенные реакции со стороны организма.
Именно из-за своих свойств и назначения прививки способны вызывать определенные реакции со стороны организма.
Вся совокупность таких реакций делится на две категории:
- Поствакцинальные реакции (ПВР).
- Поствакцинальные осложнения (ПВО).
Поствакцинальные реакции представляют собой различные изменения состояния ребенка, которые развиваются после введения вакцины и проходят самостоятельно в течение небольшого промежутка времени. Они не представляют собой угрозу и не приводят к стойкому нарушению здоровья.
Поствакцинальные осложнения – стойкие изменения в организме человека, которые произошли после введения прививки. В этом случае нарушения являются длительными, значительно выходят за рамки физиологической нормы и влекут за собой разнообразные нарушения здоровья человека. Рассмотрим подробнее возможные осложнения прививок.
К сожалению, ни одна из вакцин не является абсолютно безопасной. Все они обладают определенной степенью реактогенности, которая ограничена нормативной документацией на препараты.
Все они обладают определенной степенью реактогенности, которая ограничена нормативной документацией на препараты.
Побочные явления, которые могут возникать при введении вакцин, весьма разнообразны. Факторы, способствующие возникновению побочных реакций и осложнений, можно разделить на 4 группы:
- игнорирование противопоказаний к применению;
- нарушение процедуры вакцинации;
- индивидуальные особенности состояния организма привитого;
- нарушение условий производства, правил транспортировки и хранения вакцин, плохое качество вакцинного препарата.
Но даже несмотря на возможные осложнения при введении вакцин современная медицина признает значительное преимущество их полезных свойств для снижения возможных последствий болезни по сравнению с возможным естественным заражением.
| Вакцина | Поствакцинальные осложнения | Осложнения в ходе заболевания | Летальность при заболевании |
| Оспа | Вакцинальный менингоэнцефалит – 1/500 000 |
Менингоэнцефалит – 1/500 Осложнения ветряной оспы регистрируются с частотой 5–6%. |
0,001% |
| Корь-паротит-краснуха |
Тромбоцитопения – 1/40 000. Асептический (паротитный) менингит (штамм Jeryl Lynn) – менее чем 1/100 000.
|
Тромбоцитопения – до 1/300. Асептический (паротитный) менингит (штамм Jeryl Lynn) – до 1/300. У 20-30% заболевших паротитом мальчиков-подростков и взрослых мужчин воспаляются яички (орхит), у девушек и женщин в 5% случаев вирус эпидемического паротита поражает яичники (оофорит). Оба этих осложнения могут стать причиной бесплодия. У беременных женщин краснуха приводит к спонтанным абортам (10-40%), мертворождению (20%), гибели новорожденного (10-20%). |
Краснуха 0,01-1%. Паротит — 0,5-1,5%. |
| Корь |
Тромбоцитопения – 1/40 000. Энцефалопатия – 1/100 000. |
Тромбоцитопения – до 1/300. Энцефалопатия – до 1/300. |
Болезнь ответственна за 20% всех детских смертей. Летальность до 1/500. |
| Коклюш-дифтерия- столбняк | Энцефалопатия – до 1/300 000. |
Энцефалопатия – до 1/1200. Дифтерия. Инфекционно-токсический шок, миокардиты, моно- и полиневриты, включая поражения черепных и периферических нервов, полирадикулоневропатию, поражения надпочечников, токсический нефроз – в зависимости от формы в 20-100% случаев. Столбняк. Асфиксия, пневмония, разрывы мышц, переломы костей, компрессионные деформации позвоночника, инфаркт миокарда, остановка сердца, мышечные контрактуры и параличи III, VI и VII пар черепных нервов. Коклюш. Частота осложнений болезни: 1/10 – воспаление легких, 20/1000 – судороги, 4/1000 – поражение головного мозга (энцефалопатия). |
Дифтерия – 20% взрослые, 10% дети. Столбняк – 17 — 25% (при современных методах лечения), 95% – у новорожденных. Коклюш – 0,3% |
| Вирусы папилломавирусной инфекции | Тяжёлая аллергическая реакция – 1/500 000. | Цервикальный рак – до 1/4000. | 52% |
| Гепатит В | Тяжёлая аллергическая реакция – 1/600 000. | Хронические инфекции развиваются у 80-90% детей, инфицированных в течение первого года жизни.
Хронические инфекции развиваются у 30-50% детей, инфицированных в возрасте до шести лет. |
0,5-1% |
| Туберкулёз | Диссеминированная БЦЖ-инфекция – до 1/300 000.
БЦЖ-остеит – до 1/100 000 |
Туберкулезный менингит, легочное кровотечение, туберкулезный плеврит, туберкулезные пневмонии, распространение туберкулезной инфекции на другие органы и системы (милиарный туберкулез) у детей раннего возраста, развитие легочно-сердечной недостаточности. | 38%
(Вторая по значимости причина смертности от инфекционного агента (после ВИЧ- инфекции). Возбудителем туберкулеза инфицированы 2 млрд человек — треть населения нашей планеты. |
| Полиомиелит | Вакциноассоциированный вялый паралич – до 1/ 160 000. | Паралич – до 1/100 | 5 — 10% |
На основе данных: А.Н.Мац (НИИ вакцин и сывороток им. И.И.Мечникова РАМН) — Врачам об антипрививочном
движении и его вымыслах в СМИ
Риск осложнений после вакцинации в сотни и тысячи раз меньше, чем риск осложнений после перенесенных заболеваний. Так, например, если прививки против коклюша-дифтерии-столбняка могут вызвать энцефалопатию (поражение головного мозга) всего лишь в одном случае на 300 тыс. привитых детей, то при естественном течении этой болезни риску подобного осложнения подвергается один ребенок на 1200 заболевших детей. При этом высок риск летальности у непривитых детей при этих болезнях: дифтерия – 1 к 20 заболевшим, столбняк – 2 к 10, коклюш – 1 к 800. Вакцина против полиомиелита вызывает вялый паралич в менее чем одном случае на 160 тысяч привитых детей, в то время как риск летального исхода при заболевании — 5 – 10%.Таким образом, защитные функции прививок многократно уменьшают возможность осложнений, которые можно получить в ходе естественного течения заболевания. Любая прививка в сотни раз безопаснее заболевания, от которого она защищает.
Так, например, если прививки против коклюша-дифтерии-столбняка могут вызвать энцефалопатию (поражение головного мозга) всего лишь в одном случае на 300 тыс. привитых детей, то при естественном течении этой болезни риску подобного осложнения подвергается один ребенок на 1200 заболевших детей. При этом высок риск летальности у непривитых детей при этих болезнях: дифтерия – 1 к 20 заболевшим, столбняк – 2 к 10, коклюш – 1 к 800. Вакцина против полиомиелита вызывает вялый паралич в менее чем одном случае на 160 тысяч привитых детей, в то время как риск летального исхода при заболевании — 5 – 10%.Таким образом, защитные функции прививок многократно уменьшают возможность осложнений, которые можно получить в ходе естественного течения заболевания. Любая прививка в сотни раз безопаснее заболевания, от которого она защищает.
ЧАСТОТА РАЗВИТИЯ НЕСПЕЦЕФИЧЕСКИХ ВАКЦИНАЛЬНЫХ РЕАКЦИЙ
Наиболее часто после вакцинации возникают местные реакции, которые не имеют ничего общего с осложнениями. Местные реакции (боль, припухлость) на месте прививки не требуют специального лечения. Самый большой показатель развития местных реакций – у вакцины БЦЖ – 90-95%. Примерно в 50% случаев возникают местные реакции на вакцину АКДС цельноклеточную, при этом всего лишь около 10% – на бесклеточную. Вакцина против гепатита В, которую самой первой вводят еще в роддоме, вызывает местные реакции менее чем у 5% детей. Она же способна вызвать повышение температуры выше 380 С г (от 1 до 6% случаев). Повышение температуры, раздражительность, недомогание относятся к неспецифическим системным реакциям на вакцины. Лишь цельноклеточная вакцина АКДС вызывает системные неспецифические вакцинальные реакции в 50% случаев. Для других вакцин этот показатель составляет менее 20%, во многих случаях (например, при прививке от гемофильной инфекции) – менее 10%. А возможность возникновения неспецифических системных реакций при приеме оральной вакцины против полиомиелита – менее 1%.
Местные реакции (боль, припухлость) на месте прививки не требуют специального лечения. Самый большой показатель развития местных реакций – у вакцины БЦЖ – 90-95%. Примерно в 50% случаев возникают местные реакции на вакцину АКДС цельноклеточную, при этом всего лишь около 10% – на бесклеточную. Вакцина против гепатита В, которую самой первой вводят еще в роддоме, вызывает местные реакции менее чем у 5% детей. Она же способна вызвать повышение температуры выше 380 С г (от 1 до 6% случаев). Повышение температуры, раздражительность, недомогание относятся к неспецифическим системным реакциям на вакцины. Лишь цельноклеточная вакцина АКДС вызывает системные неспецифические вакцинальные реакции в 50% случаев. Для других вакцин этот показатель составляет менее 20%, во многих случаях (например, при прививке от гемофильной инфекции) – менее 10%. А возможность возникновения неспецифических системных реакций при приеме оральной вакцины против полиомиелита – менее 1%.
ОЖИДАЕМАЯ ЧАСТОТА РАЗВИТИЯ СЕРЬЕЗНЫХ НЯПИ
В настоящее время число нежелательных явлений (НЯ) тяжелой степени выраженности после прививок сведены к минимуму. Так, при прививке БЦЖ регистрируется 0,000019-0,000159% развития диссеминированного туберкулеза. И даже при таких минимальных значениях причина этого осложнения не в самой вакцине, а в небрежности при вакцинации, врожденных иммунодефицитах. При прививке от кори энцефалит развивается не чаще, чем в 1 случае на 1 млн доз. При вакцинации от пневмококковой инфекции вакцинами ПКВ7 и ПКВ13 не было выявлено редких и очень редких явлений тяжелой степени выраженности, хотя в мире уже введено свыше 600 млн доз этих вакцин.
Так, при прививке БЦЖ регистрируется 0,000019-0,000159% развития диссеминированного туберкулеза. И даже при таких минимальных значениях причина этого осложнения не в самой вакцине, а в небрежности при вакцинации, врожденных иммунодефицитах. При прививке от кори энцефалит развивается не чаще, чем в 1 случае на 1 млн доз. При вакцинации от пневмококковой инфекции вакцинами ПКВ7 и ПКВ13 не было выявлено редких и очень редких явлений тяжелой степени выраженности, хотя в мире уже введено свыше 600 млн доз этих вакцин.
В России официальный учет и контроль количества осложнений в результате вакцинации осуществляется только с 1998 года. И надо отметить, что благодаря совершенствованию прививочных процедур и самих вакцин количество осложнений существенно сокращается. По данным Роспотребнадзора, число зарегистрированных поствакцинальных осложнений уменьшилось с 323 случаев в январе-декабре 2013 года до 232 случаев за тот же период 2014 года (по всем прививкам совокупно).
Побочные реакции, вызванные вакциной Bacillus Calmette-Guerin: двадцать тунисских случаев
Indian J Dermatol. 2018 январь-февраль; 63(1): 62–65.
2018 январь-февраль; 63(1): 62–65.
doi: 10.4103/ijd.IJD_327_17
, , , 1 , , 1 , 1 , 1 , , 1 , 1 and
Author information Примечания к статье Информация об авторских правах и лицензии Заявление об ограничении ответственности
Справочная информация:
Вакцина Bacillus Calmette-Guérin (BCG) является широко используемой вакциной. Ведение местных осложнений БЦЖ различается у разных клиницистов, и оптимальный подход остается неясным.
Цели:
Мы стремимся описать эпидемиологические, клинические и терапевтические аспекты побочных эффектов вакцины БЦЖ в Sfax.
Пациенты и методы:
Это было ретроспективное исследование всех случаев побочных реакций на вакцину БЦЖ, зарегистрированных в отделениях дерматологии и педиатрии Университетской больницы Хеди Чакер в Сфаксе за период 10 лет (2005–2015).
Результаты:
В течение периода исследования было зарегистрировано 20 случаев побочных реакций БЦЖ. На самом деле у 80% пациентов отмечались местные побочные реакции. Результат был хорошим у всех наблюдаемых пациентов. Частота диссеминированной БЦЖ-инфекции составила 20%. Биологические тесты иммунитета выявили первичный иммунодефицит в трех случаях, в двух случаях исход был летальным.
На самом деле у 80% пациентов отмечались местные побочные реакции. Результат был хорошим у всех наблюдаемых пациентов. Частота диссеминированной БЦЖ-инфекции составила 20%. Биологические тесты иммунитета выявили первичный иммунодефицит в трех случаях, в двух случаях исход был летальным.
Заключение:
Побочные реакции на вакцину БЦЖ варьируются от легких до тяжелых. Однако лечение доброкачественных местных реакций остается неясным. Диссеминированная БЦЖ-инфекция должна насторожить клиницистов в отношении возможности первичного иммунодефицита.
Ключевые слова: Побочные реакции , бацилла Кальметта-Герена вакцина , туберкулез
Что было известно?
Местные реакции на вакцину БЦЖ включают лимфаденит (в основном с вовлечением ипсилатеральных подмышечных лимфоузлов, реже надключичных, затылочных или шейных), абсцессы, изъязвление и стойкие реакции в месте инъекции. В Тунисе нет серий, посвященных исключительно побочным реакциям на вакцину БЦЖ.
Бацилла Кальметта-Герена (БЦЖ) представляет собой живую аттенуированную Mycobacterium bovis , используемую в качестве вакцины против туберкулеза (ТБ). Тип вакцины, применяемой в нашей стране, — M. bovis (французский [Пастер] штамм 1173-P2). Специфические осложнения вакцины БЦЖ встречаются редко.[1] Они часто характеризуются легкими местными реакциями, включая лимфаденит, абсцессы, изъязвление и реакции в месте инъекции. Их управление до сих пор неясно. Серьезные диссеминированные формы встречаются редко, в основном у детей с ослабленным иммунитетом.[3] Эти осложнения, однако, требуют интенсивной терапии. В этой серии мы стремимся описать эпидемиологические, клинические и терапевтические аспекты побочных эффектов вакцины БЦЖ в Сфаксе (восточный центр Туниса).
Мы провели ретроспективное исследование всех случаев побочных реакций на вакцину БЦЖ, зарегистрированных в наших отделениях дерматологии и педиатрии за 10-летний период (2005–2015 гг.). Критериями включения были клинические данные, согласующиеся с побочными реакциями БЦЖ и/или гистопатологическими особенностями (некротизирующие гранулемы). Мы собрали данные о клинической картине, лабораторных тестах, лечении и исходах.
Мы собрали данные о клинической картине, лабораторных тестах, лечении и исходах.
В нашу серию вошли двадцать детей в возрасте от 7 дней до 7 лет, средний возраст которых составил 12,3 месяца. Мальчики были поражены чаще, чем девочки, с соотношением полов 1,8: 1. Большинство из них были здоровы, за исключением трех детей (синдром Денди-Уокера, цереброваскулярный тромбоз и дефицит главного комплекса гистосовместимости [MHC] класса II). Осложнения прививки БЦЖ возникали в среднем через 9.8 месяцев после вакцинации.
У шестнадцати детей (80%) отмечались местные побочные реакции. У 10 из них был лимфаденит с вовлечением левых подмышечных лимфоузлов []. У двоих был отек левой грудной области []. У одного пациента были затылочные лимфатические узлы, у другого была только местная реакция БЦЖ, и у двух пациентов была аберрантная локализация БЦЖ-индуцированного заболевания с отеком левого бедра []. Более того, у шести пациентов образовалась фистула. Позиция «наблюдай и жди» применялась в девяти случаях. Антибиотики и/или местное лечение использовались в четырех случаях. Эти меры решили проблемы. На самом деле ни одно из поражений не было аспирировано (с помощью иглы и шприца). Оперативное вмешательство проведено в двух случаях нефистулезного поражения. Это помогло поставить диагноз, так как патологоанатомическое исследование выявило некротические гранулемы. Противотуберкулезная терапия проводилась пациенту 16 с дефицитом MHC класса II [].
Антибиотики и/или местное лечение использовались в четырех случаях. Эти меры решили проблемы. На самом деле ни одно из поражений не было аспирировано (с помощью иглы и шприца). Оперативное вмешательство проведено в двух случаях нефистулезного поражения. Это помогло поставить диагноз, так как патологоанатомическое исследование выявило некротические гранулемы. Противотуберкулезная терапия проводилась пациенту 16 с дефицитом MHC класса II [].
Открыто в отдельном окне
Местная побочная реакция: Фистулированный гнойный левый подмышечный лимфаденит
Открыто в отдельном окне
Местная побочная реакция: Отек левой грудной области
Открыто в отдельном окне
Местная побочная реакция: Отек левого бедра в месте инъекции
Таблица 1
Данные пациентов с местными побочными реакциями, вызванными Bacillus Calmette-Guerin
Открыть в отдельном окне
У четырех детей (20%) была диссеминированная БЦЖ-инфекция [] с лимфаденопатиями, костными, гематологическими и/или кожными поражениями []; жар; и нарушение общего состояния. Бактериологические пробы были отрицательными, а вероятностные антибиотики неэффективны. Гистология, выполненная в четырех случаях, подтвердила диагноз побочных эффектов вакцины БЦЖ, обнаружив туберкулоидную гранулему с некрозом в трех случаях. Биологические тесты иммунитета (выполненные в трех случаях) выявили первичный иммунодефицит: хронический септический гранулематоз, тяжелый комбинированный иммунодефицит (ТКИД) или дефект оси интерлейкин-12/интерферон-γ. Лечение состояло из противотуберкулезной терапии. Двое детей умерли от септического шока и поливисцеральной недостаточности. 9Таблица 2 был впервые использован у людей в 1921 году.[2] В странах, эндемичных по туберкулезу, таких как наша, новорожденным рекомендуется как можно раньше после рождения, без ревакцинации.[4] Защищает от легочного и внелегочного туберкулеза. После внутрикожной инъекции в месте инокуляции возникает гранулематозная реакция как ожидаемый иммунологический ответ на Mycobacterium .[1] Системное распространение БЦЖ возможно, но истинные симптомы туберкулезной инфекции встречаются редко.
Бактериологические пробы были отрицательными, а вероятностные антибиотики неэффективны. Гистология, выполненная в четырех случаях, подтвердила диагноз побочных эффектов вакцины БЦЖ, обнаружив туберкулоидную гранулему с некрозом в трех случаях. Биологические тесты иммунитета (выполненные в трех случаях) выявили первичный иммунодефицит: хронический септический гранулематоз, тяжелый комбинированный иммунодефицит (ТКИД) или дефект оси интерлейкин-12/интерферон-γ. Лечение состояло из противотуберкулезной терапии. Двое детей умерли от септического шока и поливисцеральной недостаточности. 9Таблица 2 был впервые использован у людей в 1921 году.[2] В странах, эндемичных по туберкулезу, таких как наша, новорожденным рекомендуется как можно раньше после рождения, без ревакцинации.[4] Защищает от легочного и внелегочного туберкулеза. После внутрикожной инъекции в месте инокуляции возникает гранулематозная реакция как ожидаемый иммунологический ответ на Mycobacterium .[1] Системное распространение БЦЖ возможно, но истинные симптомы туберкулезной инфекции встречаются редко. Побочные реакции на вакцину БЦЖ наблюдаются у 1–10% вакцинированных, но о них, по-видимому, не сообщается [2]. Обычно они наблюдаются в течение первых 6 месяцев после вакцинации, но могут возникнуть и через 12 месяцев.[5] Позднее начало было зарегистрировано у пяти наших пациентов и достигло 7 лет у пациента 2. Некоторые авторы предположили связь между возникновением побочных реакций и типом инъецируемого штамма или типа препарата. [2,6] По сравнению с слабые штаммы, сильные штаммы, обладающие высокой иммуногенностью, чаще вызывают побочные реакции.[7] Другие факторы, такие как доза вакцины, метод введения и лежащий в основе иммунодефицит [8,9].] также может увеличить их частоту. В исследовании, проведенном в Саудовской Аравии, в ходе которого было собрано 145 случаев БЦЖ-лимфаденита, авторы рекомендовали вводить вакцину БЦЖ позже после рождения, так как дети младшего возраста обычно болеют [10]. Однако риск заражения Mycobacterium в эндемичных странах ограничивает отсрочку вакцинации.
Побочные реакции на вакцину БЦЖ наблюдаются у 1–10% вакцинированных, но о них, по-видимому, не сообщается [2]. Обычно они наблюдаются в течение первых 6 месяцев после вакцинации, но могут возникнуть и через 12 месяцев.[5] Позднее начало было зарегистрировано у пяти наших пациентов и достигло 7 лет у пациента 2. Некоторые авторы предположили связь между возникновением побочных реакций и типом инъецируемого штамма или типа препарата. [2,6] По сравнению с слабые штаммы, сильные штаммы, обладающие высокой иммуногенностью, чаще вызывают побочные реакции.[7] Другие факторы, такие как доза вакцины, метод введения и лежащий в основе иммунодефицит [8,9].] также может увеличить их частоту. В исследовании, проведенном в Саудовской Аравии, в ходе которого было собрано 145 случаев БЦЖ-лимфаденита, авторы рекомендовали вводить вакцину БЦЖ позже после рождения, так как дети младшего возраста обычно болеют [10]. Однако риск заражения Mycobacterium в эндемичных странах ограничивает отсрочку вакцинации.
Местные побочные реакции включают лимфаденит (в основном вовлекающий ипсилатеральные подмышечные лимфатические узлы, как в нашей серии, редко надключичные, затылочные или шейные), абсцессы, изъязвление и стойкие реакции в месте инъекции. Диагноз клинический. Поражение бедра у пациентов 4 и 9необычно. Это может быть связано с ошибкой инъекций: введением вакцины БЦЖ в мышцу бедра или использованием одной и той же иглы при инъекции вакцины БЦЖ и витамина К (вводится одновременно). Негнойный лимфаденит можно рассматривать как часть нормального течения вакцинации БЦЖ со спонтанным разрешением в течение нескольких недель или месяцев.[11] Однако лечение гнойного лимфаденита до сих пор остается спорным [12]. Даже если в некоторых случаях консервативного лечения может быть достаточно, эффективность противотуберкулезной терапии остается неопределенной. Пациентам с абсцессом лимфаденита может потребоваться пункционная аспирация. Местное введение изониазида также может сократить время восстановления в этих случаях. [12] Хирургическое иссечение не рекомендуется в качестве подхода первой линии, но может потребоваться после неудачной аспирации [1]. Цитогистопатологический диагноз (после аспирации или хирургического вмешательства) основывается на наличии некротизирующихся или ненекротизирующих гранулем, положительной культуре на кислото- и спиртоустойчивые бациллы и/или положительной полимеразной цепной реакции [13,14] 9.0003
[12] Хирургическое иссечение не рекомендуется в качестве подхода первой линии, но может потребоваться после неудачной аспирации [1]. Цитогистопатологический диагноз (после аспирации или хирургического вмешательства) основывается на наличии некротизирующихся или ненекротизирующих гранулем, положительной культуре на кислото- и спиртоустойчивые бациллы и/или положительной полимеразной цепной реакции [13,14] 9.0003
Системные осложнения вакцины БЦЖ встречаются редко. На самом деле их частота колеблется в разных исследованиях от 1% до 17%.[15] Остеит и остеомиелит обычно имели хороший прогноз и разрешались без последствий.[2] Однако диссеминированные БЦЖ-инфекции являются опасными для жизни осложнениями и часто наблюдаются у детей с первичным иммунодефицитом, особенно с ТКИН. Bernatowska и соавт. предложили диагностические критерии диссеминированной БЦЖ-инфекции у лиц с первичным иммунодефицитом.[15] Руководств по лечению диссеминированной БЦЖ-инфекции не существует. Противотуберкулезная терапия всегда полезна и была назначена всем нашим пациентам. Необходимо всегда учитывать лечение иммунодефицита. Показатели смертности варьируются от 25% до > 70% в разных исследованиях [15,16] (50% в нашей серии).
Необходимо всегда учитывать лечение иммунодефицита. Показатели смертности варьируются от 25% до > 70% в разных исследованиях [15,16] (50% в нашей серии).
Это первая тунисская серия, в которой сообщается исключительно о побочных реакциях, вызванных вакциной БЦЖ. В 2006 г. Hajlaoui и соавт. зарегистрировали 12 случаев БЦЖ-специфических реакций среди 38 тунисских случаев кожного ТБ в течение 12 лет.[17] Используя наше исследование в больнице, мы не можем дать точную оценку общей частоты осложнений, связанных с вакцинацией БЦЖ. Однако в последние годы они, похоже, увеличиваются.
Осложнения вакцины БЦЖ следует подозревать при любой вакцине БЦЖ с кожными поражениями, которые могут иметь системную диссеминацию инфекции или устойчивость к антибиотикам. Поэтому необходимы своевременная диагностика и лечение, особенно при диссеминированных формах, чтобы избежать серьезных последствий. В таких ситуациях клиницисты должны знать о возможности первичного иммунодефицита, особенно ТКИН. Было бы полезно собрать данные о побочных эффектах вакцин, особенно вакцины БЦЖ, в национальных или международных реестрах для лучшего анализа и последующих подходящих действий.
Было бы полезно собрать данные о побочных эффектах вакцин, особенно вакцины БЦЖ, в национальных или международных реестрах для лучшего анализа и последующих подходящих действий.
Финансовая поддержка и спонсорство
Нет.
Конфликт интересов
Конфликт интересов отсутствует.
Что нового?
Мы сообщаем о необычной локализации побочных реакций БЦЖ на бедре. Это может быть связано с ошибкой впрыска. Это первая тунисская серия, в которой сообщается исключительно о побочных реакциях, вызванных вакциной БЦЖ.
1. Antaya RJ, Gardner ES, Bettencourt MS, Daines M, Denise Y, Uthaisangsook S, et al. Кожные осложнения вакцинации БЦЖ у детей раннего возраста с иммунными нарушениями: два случая и обзор литературы. Педиатр Дерматол. 2001; 18: 205–9.. [PubMed] [Google Scholar]
2. Венкатараман А., Юсуфф М., Либешуец С., Ридделл А., Прендергаст А.Дж. Ведение и исход побочных реакций на вакцину Bacille Calmette-Guérin. вакцина. 2015;33:5470–4. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2015;33:5470–4. [Бесплатная статья PMC] [PubMed] [Google Scholar]
3. Conti F, Lugo-Reyes SO, Blancas Galicia L, He J, Aksu G, Borges de Oliveira E, Jr, et al. Микобактериальная болезнь у пациентов с хронической гранулематозной болезнью: ретроспективный анализ 71 случая. J Аллергия Клин Иммунол. 2016; 138: 241–8. е3. [PubMed] [Академия Google]
4. Министерство здравоохранения. Республика Тунис; 2014. Июль, График прививок. [Google Scholar]
5. Тео С.С., Смелдерс Н., Шингадия Д.В. Гнойный лимфаденит, ассоциированный с вакциной БЦЖ. вакцина. 2005; 23: 2676–9. [PubMed] [Google Scholar]
6. Milstien JB, Gibson JJ. Контроль качества вакцины БЦЖ со стороны ВОЗ: обзор факторов, которые могут влиять на эффективность и безопасность вакцины. Всемирный орган здравоохранения Быка. 1990; 68: 93–108. [Бесплатная статья PMC] [PubMed] [Google Scholar]
7. Норузи С., Агамохаммади А., Мамиши С., Розенцвейг С.Д., Резаи Н. Бацилла Кальметта-Герена (БЦЖ) осложнения, связанные с первичными иммунодефицитными заболеваниями. J заразить. 2012; 64: 543–54. [Бесплатная статья PMC] [PubMed] [Google Scholar]
J заразить. 2012; 64: 543–54. [Бесплатная статья PMC] [PubMed] [Google Scholar]
8. Bolger T, O’Connell M, Menon A, Butler K. Осложнения, связанные с вакцинацией Bacille Calmette-Guérin в Ирландии. Арч Дис Чайлд. 2006; 91: 594–7. [Бесплатная статья PMC] [PubMed] [Google Scholar]
9. Риордан А., Коул Т., Брумфилд С. Пятнадцатиминутная консультация: абсцесс и лимфаденит Bacillus Calmette-Guérin. Arch Dis Child Educ Pract Ed. 2014;99:87–9. [PubMed] [Google Scholar]
10. Бухари Э., Альзахрани М., Алсубайе С., Альрабиа А., Алзамил Ф. Бациллярный лимфаденит Кальметта-Герена: 6-летний опыт работы в двух саудовских больницах. Индиан Дж. Патол Микробиол. 2012;55:202–5. [PubMed] [Google Scholar]
11. Cuello-García CA, Pérez-Gaxiola G, Jimenez Gutiérrez C. Лечение БЦЖ-индуцированной болезни у детей. Кокрановская система базы данных, ред. 2013; 1:CD008300. [Бесплатная статья PMC] [PubMed] [Google Scholar]
12. Mahmoudi S, Khaheshi S, Pourakbari B, Ahamohammadi A, Keshavarz Valian S, Bahador A, et al. Побочные реакции на Mycobacterium bovis бацилла Кальметта-Герена вакцинация против туберкулеза у иранских детей. Clin Exp Вакцина Res. 2015;4:195–9. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Побочные реакции на Mycobacterium bovis бацилла Кальметта-Герена вакцинация против туберкулеза у иранских детей. Clin Exp Вакцина Res. 2015;4:195–9. [Бесплатная статья PMC] [PubMed] [Google Scholar]
13. Сатайнараяна С., Матхур А.Д., Верма Й., Прадхан С., Бхандари М.К. Аспирация иглой как диагностический инструмент и метод лечения гнойного лимфаденита после вакцинации Bacillus Calmette Guerin. J Assoc врачей Индии. 2002; 50: 788–91. [PubMed] [Google Scholar]
14. Su WJ, Huang CY, Huang CY, Perng RP. Использование ПЦР для экспресс-диагностики БЦЖ-инфекции у детей. Int J Tuberc Lung Dis. 2001; 5: 380–4. [PubMed] [Академия Google]
15. Bernatowska EA, Wolska-Kusnierz B, Pac M, Kurenko-Deptuch M, Zwolska Z, Casanova JL, et al. Диссеминированная инфекция Bacillus Calmette-Guérin и иммунодефицит. Эмердж Инфекция Дис. 2007; 13: 799–801. [Бесплатная статья PMC] [PubMed] [Google Scholar]
16. Talbot EA, Perkins MD, Silva SF, Frothingham R. Диссеминированная болезнь Bacille Calmette-Guérin после вакцинации: история болезни и обзор. Клин Инфекция Дис. 1997; 24:1139–46. [PubMed] [Google Scholar]
Клин Инфекция Дис. 1997; 24:1139–46. [PubMed] [Google Scholar]
17. Hajlaoui K, Fazaa B, Zermani R, Zeglaoui F, El Fekib N, Ezzine N, et al. Кожный туберкулез. Обзор 38 дел. Тунис Мед. 2006; 84: 537–41. [PubMed] [Академия Google]
Продолжительные эффекты вакцинации БЦЖ как на гетерологичные ответы Th2/Th27, так и на врожденный тренированный иммунитет — полный текст — Journal of Innate Immunity 2014, Vol. 6, No. 2
Недавно мы показали, что вакцинация БЦЖ (Бацилла Кальметта-Герена) у здоровых добровольцев вызывает эпигенетическое перепрограммирование моноцитов, приводящее к увеличению продукции цитокинов в ответ на неродственные патогены в течение 3 месяцев после вакцинации. Это явление получило название «тренированный иммунитет». В настоящем исследовании мы оценили, способна ли БЦЖ вызывать длительные эффекты как на тренированный иммунитет, так и на гетерологичные Т-хелперы 1 (Th2) и Th27 иммунные ответы через 1 год после вакцинации. Продукция TNFα и IL-1β микобактериями или неродственными патогенами была выше через 2 недели и 3 месяца после вакцинации, но эти эффекты были менее выражены через 1 год после вакцинации. Однако моноциты, восстановленные через 1 год после вакцинации, имели повышенную экспрессию рецепторов распознавания образов, таких как CD14, Toll-подобный рецептор 4 (TLR4) и рецептор маннозы, и это коррелировало с увеличением продукции провоспалительных цитокинов после стимуляции лигандом TLR4 липополисахаридом. Гетерологичная продукция Th2 (IFN-γ) и Th27 (IL-17 и IL-22) иммунных ответов на немикобактериальную стимуляцию оставалась сильно повышенной даже через 1 год после вакцинации БЦЖ. Таким образом, БЦЖ вызывает устойчивые изменения в иммунной системе, связанные с неспецифическим ответом на инфекции как на уровне врожденного тренированного иммунитета, так и на уровне гетерологичных Th2/Th27-ответов.
Однако моноциты, восстановленные через 1 год после вакцинации, имели повышенную экспрессию рецепторов распознавания образов, таких как CD14, Toll-подобный рецептор 4 (TLR4) и рецептор маннозы, и это коррелировало с увеличением продукции провоспалительных цитокинов после стимуляции лигандом TLR4 липополисахаридом. Гетерологичная продукция Th2 (IFN-γ) и Th27 (IL-17 и IL-22) иммунных ответов на немикобактериальную стимуляцию оставалась сильно повышенной даже через 1 год после вакцинации БЦЖ. Таким образом, БЦЖ вызывает устойчивые изменения в иммунной системе, связанные с неспецифическим ответом на инфекции как на уровне врожденного тренированного иммунитета, так и на уровне гетерологичных Th2/Th27-ответов.
Введение
Неспецифические благоприятные эффекты БЦЖ (бациллы Кальметта-Герена) описаны на протяжении многих десятилетий. Вскоре после ее появления в 1920-х годах эпидемиологические исследования неожиданно показали, что БЦЖ защищает от младенческой смертности независимо от ее влияния на туберкулез (ТБ) [1,2,3,4,5]. Недавние исследования подтвердили эти выводы и предложили снижение бремени инфекций, отличных от туберкулеза [6,7,8,9,10]. Например, БЦЖ снизила неонатальную смертность детей вдвое в нескольких недавних исследованиях в Западной Африке [8,9].,11,12,13,14], в то время как в исследовании случай-контроль в Бразилии БЦЖ снижала риск смерти от пневмонии на 50% у детей в возрасте до 1 года [7]. В свете этих данных возникает вопрос, какие механизмы опосредуют эти неспецифические иммунные эффекты БЦЖ и как долго они длятся?
Недавние исследования подтвердили эти выводы и предложили снижение бремени инфекций, отличных от туберкулеза [6,7,8,9,10]. Например, БЦЖ снизила неонатальную смертность детей вдвое в нескольких недавних исследованиях в Западной Африке [8,9].,11,12,13,14], в то время как в исследовании случай-контроль в Бразилии БЦЖ снижала риск смерти от пневмонии на 50% у детей в возрасте до 1 года [7]. В свете этих данных возникает вопрос, какие механизмы опосредуют эти неспецифические иммунные эффекты БЦЖ и как долго они длятся?
Два возможных иммунологических механизма были предложены для объяснения неспецифических положительных эффектов вакцинации. Первым таким механизмом является гетерологичный иммунитет, при котором перекрестная защита опосредуется ответами памяти гетерологичных Т-клеток [15]. Однако для развития гетерологичного иммунитета требуется как минимум пара недель, и, таким образом, маловероятно, что он отвечает за очень быстрое воздействие, наблюдаемое на перинатальный иммунитет [14]. Недавно был предложен второй механизм защиты в виде эпигенетического перепрограммирования иммунных клеток, явления, придающего неспецифическую иммунную память врожденным иммунным ответам и получившего название «тренированный иммунитет» [16]. Многие виды организмов, лишенные адаптивного иммунитета, такие как растения [17] или насекомые [18,19], проявляют сильную иммунную память после предыдущего воздействия инфекций или определенных микробных компонентов, а адаптивные особенности врожденного иммунитета также были продемонстрированы у мышей, лишенных функциональных адаптивных иммунных ответов [20,21]. Выдающимися микробными компонентами, способными усиливать эффекторную функцию клеток врожденного иммунитета и защищать от инфекций, являются микобактериальные стимулы, такие как БЦЖ, полный адъювант Фрейнда и мурамилдипептид [22,23,24,25]. Недавно мы показали, что вакцинация БЦЖ у здоровых добровольцев приводила к NOD2-зависимому эпигенетическому репрограммированию моноцитов, что приводило к усилению экспрессии клеточных рецепторов на моноцитах, сопровождаемому повышенной продукцией цитокинов в ответ на неродственные патогены [26].
Недавно был предложен второй механизм защиты в виде эпигенетического перепрограммирования иммунных клеток, явления, придающего неспецифическую иммунную память врожденным иммунным ответам и получившего название «тренированный иммунитет» [16]. Многие виды организмов, лишенные адаптивного иммунитета, такие как растения [17] или насекомые [18,19], проявляют сильную иммунную память после предыдущего воздействия инфекций или определенных микробных компонентов, а адаптивные особенности врожденного иммунитета также были продемонстрированы у мышей, лишенных функциональных адаптивных иммунных ответов [20,21]. Выдающимися микробными компонентами, способными усиливать эффекторную функцию клеток врожденного иммунитета и защищать от инфекций, являются микобактериальные стимулы, такие как БЦЖ, полный адъювант Фрейнда и мурамилдипептид [22,23,24,25]. Недавно мы показали, что вакцинация БЦЖ у здоровых добровольцев приводила к NOD2-зависимому эпигенетическому репрограммированию моноцитов, что приводило к усилению экспрессии клеточных рецепторов на моноцитах, сопровождаемому повышенной продукцией цитокинов в ответ на неродственные патогены [26]. Этот недавно описанный механизм может служить объяснением быстрых неспецифических защитных эффектов, вызываемых вакцинацией БЦЖ. Однако неизвестно, как долго сохраняется сформированный иммунитет и/или гетерологичный иммунитет после вакцинации БЦЖ. Поэтому в настоящем исследовании мы исследовали долгосрочные неспецифические эффекты вакцинации БЦЖ у здоровых добровольцев, оценивая реакцию как врожденных, так и адаптивных иммунных клеток на немикобактериальную стимуляцию в период до 1 года после вакцинации.
Этот недавно описанный механизм может служить объяснением быстрых неспецифических защитных эффектов, вызываемых вакцинацией БЦЖ. Однако неизвестно, как долго сохраняется сформированный иммунитет и/или гетерологичный иммунитет после вакцинации БЦЖ. Поэтому в настоящем исследовании мы исследовали долгосрочные неспецифические эффекты вакцинации БЦЖ у здоровых добровольцев, оценивая реакцию как врожденных, так и адаптивных иммунных клеток на немикобактериальную стимуляцию в период до 1 года после вакцинации.
Материалы и методы
Субъекты
Людей (в возрасте от 20 до 36 лет), которым планировалось сделать прививку БЦЖ в службе общественного здравоохранения в связи с поездками или работой в эндемичных по ТБ странах, было предложено принять участие в этом испытании. Двадцать здоровых людей были включены в период с августа по ноябрь 2010 года. Кровь брали до и через 2 недели, 3 месяца и 1 год после вакцинации БЦЖ. Два участника были потеряны для последующего наблюдения через 3 месяца. Исследование было одобрено Этическим комитетом Арнема-Неймегена.
Исследование было одобрено Этическим комитетом Арнема-Неймегена.
Анализы стимуляции РВМС
Для анализов стимуляции РВМС фракцию мононуклеарных клеток выделяли центрифугированием плотности из крови, разбавленной 1:1 в апирогенном солевом растворе над Ficoll-Paque (Pharmacia Biotech, Uppsala, Sweden). Клетки дважды промывали физиологическим раствором и ресуспендировали в культуральной среде (RPMI, Invitrogen, Карлсбад, Калифорния, США) с добавлением 10 мкг/мл гентамицина, 10 мМ L-глутамина и 10 мМ пирувата. Клетки подсчитывали на счетчике Коултера (Coulter Electronics) и количество доводили до 5 × 10 9 .0010 6 клеток/мл. Всего 5 × 10 5 мононуклеарных клеток в объеме 100 мкл добавляли в круглодонные 96-луночные планшеты (Greiner) с RPMI или обработанными ультразвуком Mycobacterium tuberculosis (MTB) h47Rv (1 мкг/мл). конечная концентрация белка), убитые нагреванием Candida albicans (1 × 10 6 микроорганизмов/мл, штамм UC820), Staphylococcus aureus (1 × 10 6 микроорганизмов/мл, клинический изолят) или Escherichia кишечная палочка липополисахарид (ЛПС; 1 нг/мл; Sigma-Aldrich, Сент-Луис, Миссури, США). Через 24, 48 ч или 7 сут супернатанты хранили при -20°С. Концентрацию цитокинов в супернатантах оценивали с помощью твердофазного иммуноферментного анализа (ELISA).
Через 24, 48 ч или 7 сут супернатанты хранили при -20°С. Концентрацию цитокинов в супернатантах оценивали с помощью твердофазного иммуноферментного анализа (ELISA).
Измерение цитокинов
Циркулирующие IFN-γ, IL-17 и IL-22 измеряли в плазме с помощью наборов Sanquin Pelikine ELISA (IFN-γ) или наборов R&D Quantikine ELISA (IL-17 и IL-22; R&D Systems, Minneapolis , Миннесота, США) соответственно по описанию производителя. Измерения цитокинов TNFα, IL-1β, IFN-γ, IL-17 и IL-22 после стимуляции PBMC проводили в супернатантах с использованием коммерческих наборов ELISA от R&D Systems (TNFα, IL-1β, IL-17 и IL-22). или Sanquin (IFN-γ; Амстердам, Нидерланды). В небольшой части исходных образцов, в которых концентрации цитокинов превышали предел обнаружения, эти выбросы были исключены из анализа.
Анализ FACS
Клетки фенотипически анализировали с помощью десятицветной и пятицветной проточной цитометрии с использованием Coulter Navios и Coulter Cytomics FC 500 соответственно (Beckman Coulter, Fullerton, FL, USA) и оценивали с использованием программного обеспечения Kaluza 1. 1 (Beckman Коултер). Чтобы гарантировать надежные результаты, проточная цитометрия была откалибрована с помощью шариков Flow Set Pro (Beckman Coulter). Клетки промывали в PBS с 1% бычьим сывороточным альбумином перед мечением mAb, конъюгированными с флуорохромом. После инкубации в течение 30 мин при 4°С в темноте клетки дважды отмывали от несвязавшихся антител и анализировали. Для окрашивания клеточной поверхности использовали следующие mAb: CD3-PECy7 (737657), CD4-PB (A82789), CD8-APC-A700 (A66332), CD45-PO (A96416), CD11b-PE (IM25814), CD14-ECD (IM2707U), CD45-PC7 (IM3548; все от Beckman Coulter Corporation), CD284-PE (TLR4 ; 312806) и CD206-PE (321106; оба образуют Biolegend), CD16-FITC (335035) и CD282-APC (TLR2; 558319; оба от BD biosciences) и декстин-1-APC (FAB1859A; R&D Systems).
1 (Beckman Коултер). Чтобы гарантировать надежные результаты, проточная цитометрия была откалибрована с помощью шариков Flow Set Pro (Beckman Coulter). Клетки промывали в PBS с 1% бычьим сывороточным альбумином перед мечением mAb, конъюгированными с флуорохромом. После инкубации в течение 30 мин при 4°С в темноте клетки дважды отмывали от несвязавшихся антител и анализировали. Для окрашивания клеточной поверхности использовали следующие mAb: CD3-PECy7 (737657), CD4-PB (A82789), CD8-APC-A700 (A66332), CD45-PO (A96416), CD11b-PE (IM25814), CD14-ECD (IM2707U), CD45-PC7 (IM3548; все от Beckman Coulter Corporation), CD284-PE (TLR4 ; 312806) и CD206-PE (321106; оба образуют Biolegend), CD16-FITC (335035) и CD282-APC (TLR2; 558319; оба от BD biosciences) и декстин-1-APC (FAB1859A; R&D Systems).
Статистический анализ
Различия анализировали с использованием критерия знакового ранга Уилкоксона или критерия Фридмана для парных выборок. p < 0,05 считали статистически значимым. Если не указано иное, данные представлены как совокупные результаты данных, полученных у всех добровольцев (среднее значение + стандартная ошибка среднего).
Результаты
Влияние вакцинации БЦЖ на гетерологичные ответы Th2 и Th27
FACS-анализ субпопуляций Т-клеток не показал серьезных сдвигов в лимфоцитах CD4 и CD8 (онлайн-приложение, рис. 1; все материалы онлайн-приложения см. www.karger.com/doi/10.1159/000355628). Циркулирующие концентрации цитокинов Т-клеточного происхождения IFN-γ, IL-17 и IL-22 были ниже предела обнаружения во все моменты времени (данные не показаны). Напротив, через 2 недели и 3 месяца после вакцинации БЦЖ продукция IFN-γ, индуцированная MTB была в 7 раз выше, чем продукция до вакцинации, о чем также сообщалось ранее [26]. Интересно, что этот эффект сохранялся не менее 1 года (рис. 1а). Аналогичное увеличение продукции цитокинов через 2 недели и 3 месяца наблюдалось при стимуляции клеток неродственными патогенами ( C. albicans или S. aureus ; рис. 1b, c). Увеличение производства сохранялось до 1 года после вакцинации в случае S. aureus , в то время как оно в значительной степени возвращалось к уровням до вакцинации через 9 лет.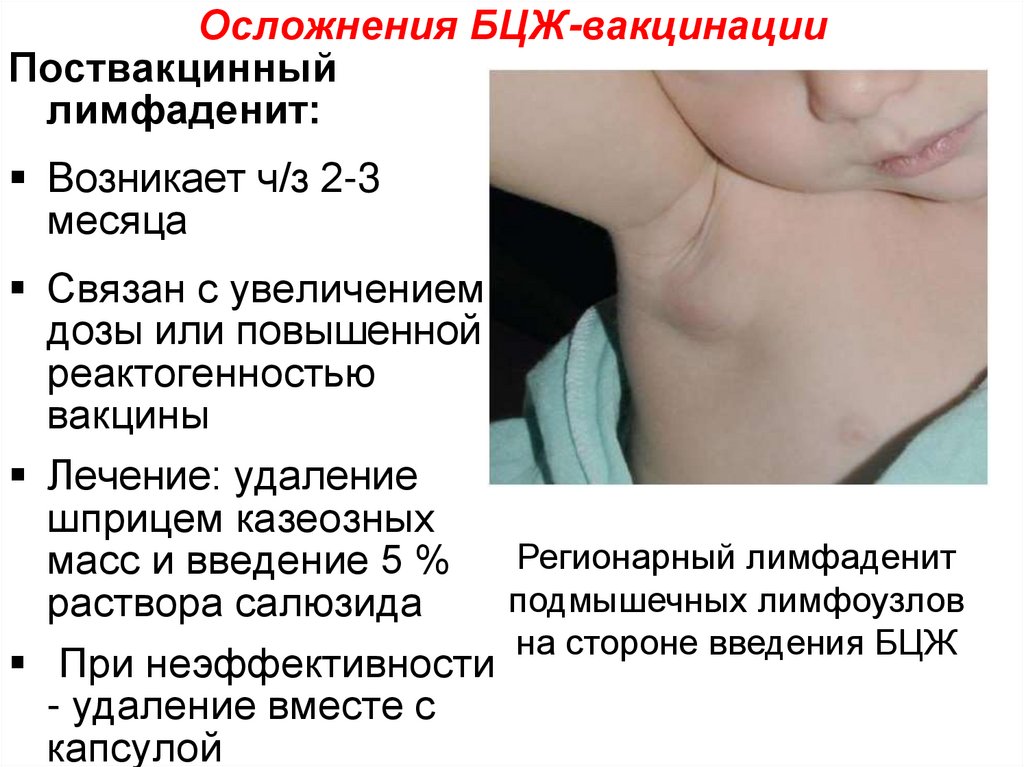 0197 C. albicans стимуляция.
0197 C. albicans стимуляция.
Рис. 1
Вакцинация БЦЖ повышала гетерологичные ответы Th2. РВМС, выделенные от 18 добровольцев до и после (2 недели, 3 месяца и 1 год) вакцинации, стимулировали in vitro обработанными ультразвуком MTB ( a ), убитыми нагреванием дрожжами C. albicans (b ) и . S. aureus ( c ). Продукцию IFN-γ оценивали в супернатантах с помощью ELISA. * р < 0,05; ** р < 0,01.
В дополнение к ее влиянию на ответы Th2, мы стремились исследовать влияние вакцинации БЦЖ на выработку цитокинов, происходящих из Th27, а именно IL-17 и IL-22. MTB -стимулированная продукция IL-17 была значительно выше в клетках, извлеченных после вакцинации БЦЖ (рис. 2а). Более того, этот эффект не зависел от стимулирующего патогена, так как постоянно повышенная продукция IL-17 также наблюдалась при стимуляции C. albicans (рис. 2b) и S. aureus 9.0198 (рис. 2в). Повышение гетерологичного Th27-иммунитета также отражалось в потенцировании продукции IL-22 после вакцинации БЦЖ. Это было очевидно после стимуляции клеток MTB, C. albicans или S. aureus (рис. 2d-f).
Это было очевидно после стимуляции клеток MTB, C. albicans или S. aureus (рис. 2d-f).
Рис. 2
БЦЖ вызывает длительные гетерологичные ответы Th27. РВМС, выделенные от 18 добровольцев до и после (2 недели, 3 месяца и 1 год) вакцинации, стимулировали in vitro обработанным ультразвуком MTB 9.0198 ( a , d ), убитые нагреванием дрожжи C. albicans ( b , e ) и S. aureus ( c
, 8). Продукцию IL-17 ( a-c ) и IL-22 ( d-f ) оценивали с помощью ELISA в супернатантах. * р < 0,05; ** р < 0,01; *** р < 0,005.
Влияние вакцинации БЦЖ на тренированный иммунитет
Ранее мы сообщали, что БЦЖ влияет на выработку провоспалительных цитокинов, продуцируемых моноцитами, прототипом популяции клеток врожденного иммунитета [26]. В то время как продукция TNFα и IL-1β была выше через 2 недели и 3 месяца после вакцинации, она в значительной степени вернулась к норме через 1 год после вакцинации БЦЖ. Этот уменьшающийся эффект на высвобождение TNFα и IL-1β наблюдался при стимуляции клеток MTB , а также с неродственным возбудителем C. albicans (рис. 3а, б) или S. aureus (не показаны). Аналогичные данные были получены по продукции IL-1β (данные не показаны). Однако индуцированная ЛПС продукция TNFα (рис. 3c) и IL-1β (рис. 3d) через 1 год после вакцинации оставалась значительно выше по сравнению с уровнями до вакцинации.
Этот уменьшающийся эффект на высвобождение TNFα и IL-1β наблюдался при стимуляции клеток MTB , а также с неродственным возбудителем C. albicans (рис. 3а, б) или S. aureus (не показаны). Аналогичные данные были получены по продукции IL-1β (данные не показаны). Однако индуцированная ЛПС продукция TNFα (рис. 3c) и IL-1β (рис. 3d) через 1 год после вакцинации оставалась значительно выше по сравнению с уровнями до вакцинации.
Рис. 3
Влияние БЦЖ на цитокины врожденного иммунитета. РВМС, выделенные от 18 добровольцев до и после (2 недели, 3 месяца и 1 год) вакцинации, стимулировали in vitro с помощью ультразвука 9.0197 MTB ( a ), убитые нагреванием дрожжи C. albicans ( b ) и LPS ( c , d ). Продукцию TNFα ( а-с ) и IL-1β ( d ) оценивали с помощью ELISA в супернатантах. * р < 0,05; ** р < 0,01.
Влияние вакцинации БЦЖ на экспрессию рецепторов на моноцитах
Экспрессия нескольких рецепторов распознавания образов и маркеров активации на моноцитах демонстрировала устойчивый рост экспрессии с течением времени.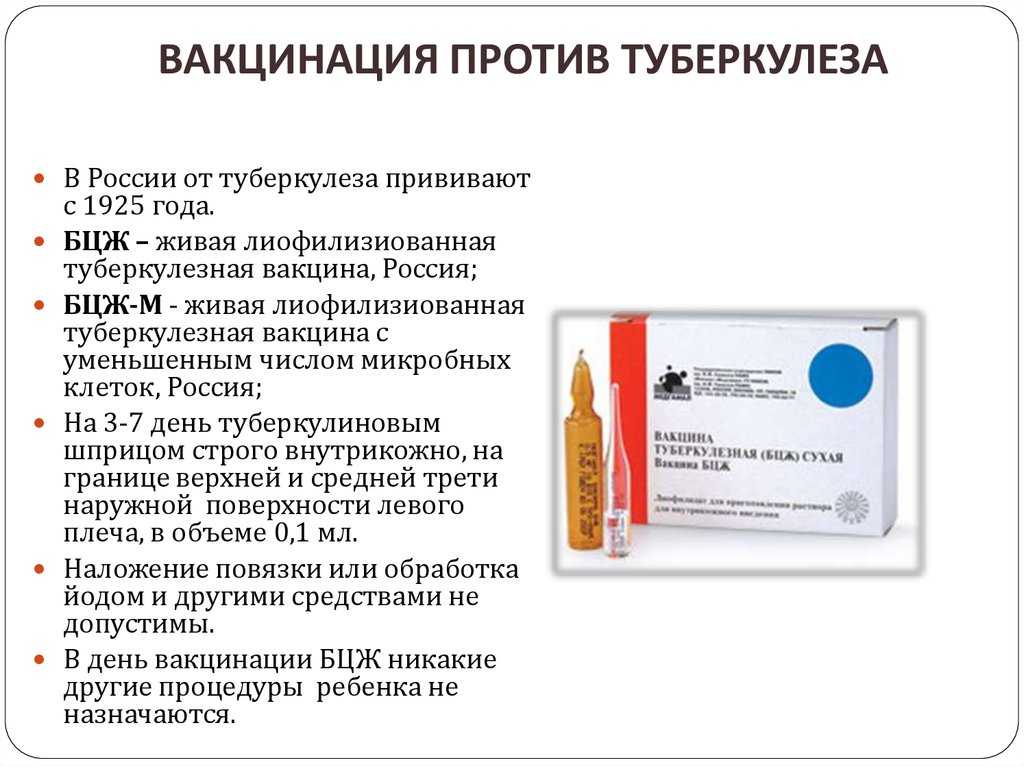 На рис. 4 представлены средние флуоресцентные индексы (MFI) маркеров активности моноцитов (CD14 и CD11b; рис. 4а, б), Toll-подобного рецептора 4 (TLR4) и TLR2 (рис. 4в, г) и С-типа. лектины (рецептор маннозы, MR и dectin-1; рис. 4д, е). Увеличение MFI было специфичным для рецептора, так как не на все TLR или лектины С-типа влияла вакцинация. Маркеры активности CD14 и CD11b демонстрировали стойкие более высокие уровни экспрессии на моноцитах, которые сохранялись не менее 1 года. Также экспрессия TLR4 и MR на моноцитах увеличивалась после вакцинации БЦЖ через 1 год после вакцинации. Никакого влияния на экспрессию TLR2 или dectin-1 не наблюдалось (рис. 4d, f). На дополнительном онлайн-рисунке 2 показана стратегия гейтирования для моноцитов, использованная на рис. 4. Кроме того, на дополнительном онлайн-рисунке 3 представлены репрезентативные гистограммы всех рецепторов, показанных на рис. 4.
На рис. 4 представлены средние флуоресцентные индексы (MFI) маркеров активности моноцитов (CD14 и CD11b; рис. 4а, б), Toll-подобного рецептора 4 (TLR4) и TLR2 (рис. 4в, г) и С-типа. лектины (рецептор маннозы, MR и dectin-1; рис. 4д, е). Увеличение MFI было специфичным для рецептора, так как не на все TLR или лектины С-типа влияла вакцинация. Маркеры активности CD14 и CD11b демонстрировали стойкие более высокие уровни экспрессии на моноцитах, которые сохранялись не менее 1 года. Также экспрессия TLR4 и MR на моноцитах увеличивалась после вакцинации БЦЖ через 1 год после вакцинации. Никакого влияния на экспрессию TLR2 или dectin-1 не наблюдалось (рис. 4d, f). На дополнительном онлайн-рисунке 2 показана стратегия гейтирования для моноцитов, использованная на рис. 4. Кроме того, на дополнительном онлайн-рисунке 3 представлены репрезентативные гистограммы всех рецепторов, показанных на рис. 4.
Рис. 4
БЦЖ изменяет фенотип циркулирующих моноцитов у здоровых добровольцев. Средние уровни поверхностной экспрессии маркеров активации CD14+ ( a ) и CD11b ( b ), TLR4 ( c ) и TLR2 ( d ), рецепторов лектина С-типа MR ( e ) и дектин- 1 ( f ) в популяции моноцитов CD14+, выделенных от 18 добровольцев до и после вакцинации БЦЖ. * р < 0,05; ** р < 0,01; *** р < 0,005.
* р < 0,05; ** р < 0,01; *** р < 0,005.
Обсуждение
БЦЖ благотворно влияет на инфекции, отличные от туберкулеза, однако иммунологические механизмы, ответственные за эти эффекты, остаются неясными. Недавно были предложены два иммунологических механизма, опосредующих эти эффекты: краткосрочные эффекты, скорее всего, опосредованы эпигенетическим перепрограммированием врожденных иммунных клеток, процесс, называемый «тренированным иммунитетом» [26], в то время как долгосрочные эффекты могут быть опосредованы гетерологичный Th2/Th27-иммунитет [15], возможно, в сочетании с остаточными эффектами тренированного иммунитета. В настоящем исследовании мы показываем, что вакцинация БЦЖ вызывает неспецифические потенцирующие эффекты как врожденного тренированного иммунитета, так и гетерологичных Т-хелперных ответов, которые явно присутствуют в течение по крайней мере 1 года после вакцинации.
Долгосрочные эффекты после вакцинации БЦЖ наиболее заметны при гетерологичных ответах Th2 и Th27.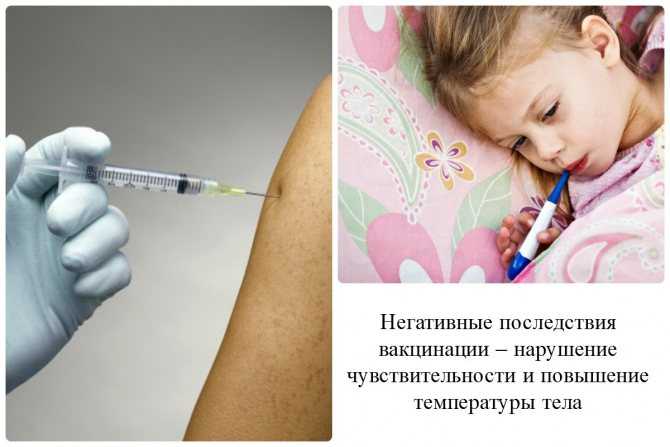 Объяснением этого может быть процесс «перекрестной защиты», описанный 5 десятилетий назад [27] или позже названный «гетерологичным иммунитетом» [15,28]. Классическая форма перекрестной защиты опосредована лимфоцитами, которые высвобождают IFN-γ после стимуляции первым встреченным патогеном и впоследствии активируют макрофаги-наблюдатели, вызывая состояние временного повышенного врожденного иммунитета против вторичной инфекции, который быстро ослабевает после заражения первичным патогеном. устраняется [29]. Вторая форма является долгоживущей и поэтому, возможно, более сопоставима с нашими выводами: Berg et al. [30] описали, что как эффекторные клетки, так и клетки памяти CD8+ способны секретировать IFN-γ в ответ на IL-12 и IL-18 в отсутствие родственного антигена. IL-12 и IL-18 вырабатываются на начальных стадиях вторичной инфекции. Еще одним возможным объяснением может быть совместное использование эпитопа, как описано ранее, хотя это вряд ли сыграет важную роль в объяснении повышенного ответа на C.
Объяснением этого может быть процесс «перекрестной защиты», описанный 5 десятилетий назад [27] или позже названный «гетерологичным иммунитетом» [15,28]. Классическая форма перекрестной защиты опосредована лимфоцитами, которые высвобождают IFN-γ после стимуляции первым встреченным патогеном и впоследствии активируют макрофаги-наблюдатели, вызывая состояние временного повышенного врожденного иммунитета против вторичной инфекции, который быстро ослабевает после заражения первичным патогеном. устраняется [29]. Вторая форма является долгоживущей и поэтому, возможно, более сопоставима с нашими выводами: Berg et al. [30] описали, что как эффекторные клетки, так и клетки памяти CD8+ способны секретировать IFN-γ в ответ на IL-12 и IL-18 в отсутствие родственного антигена. IL-12 и IL-18 вырабатываются на начальных стадиях вторичной инфекции. Еще одним возможным объяснением может быть совместное использование эпитопа, как описано ранее, хотя это вряд ли сыграет важную роль в объяснении повышенного ответа на C.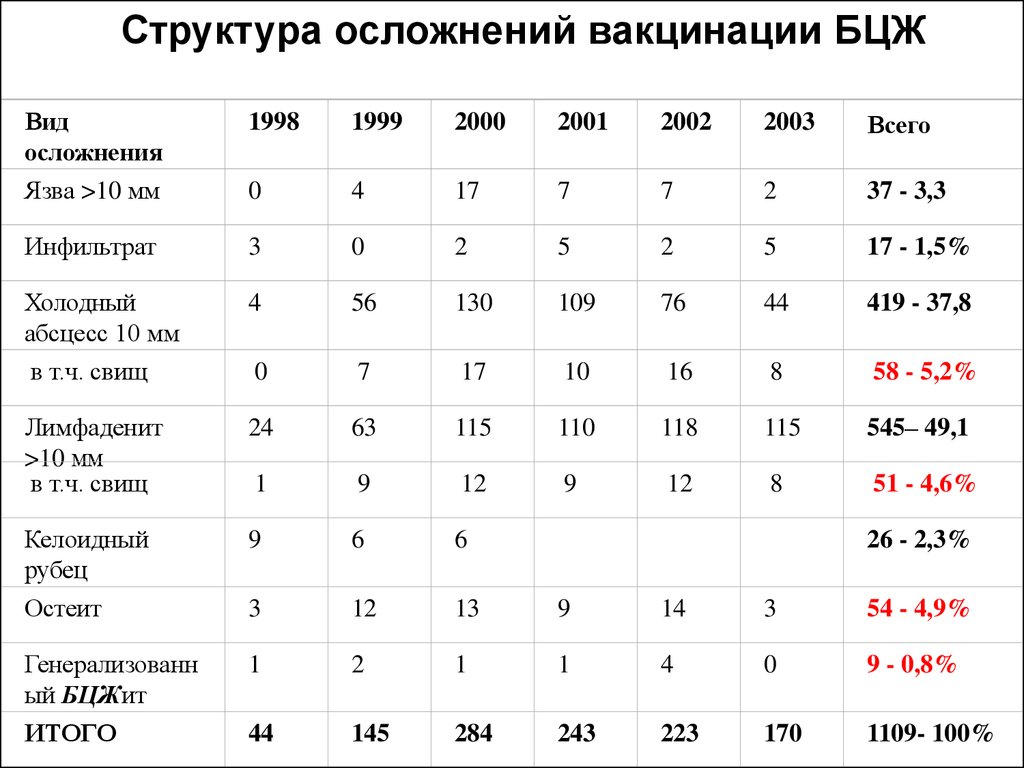 albicans или S. aureus после вакцинации БЦЖ.
albicans или S. aureus после вакцинации БЦЖ.
Можно предположить, что повышенная реактивность клеток Th27 происходит аналогичным образом. Общий принцип индукции Th27-ответов аналогичен принципу Th2-иммунитета, с той разницей, что IL-1β и IL-23 (а не IL-12 и IL-18) являются цитокинами, ответственными за дифференцировку Th27. Повышенная экспрессия рецепторов распознавания образов, которые, как известно, вызывают ответы Th27, такие как MR [31], и провоспалительные цитокины, такие как IL-1β [32], могут, по крайней мере, частично объяснять индукцию гетерологичного иммунитета Th27. Таким образом, увеличение этих типичных врожденных иммунных ответов во время индукции тренированного иммунитета может способствовать гетерологичным ответам Т-хелперов, но эта прямая связь еще предстоит формально продемонстрировать в будущих исследованиях. Кроме того, можно также предположить о потенциальных вредных эффектах гетерологичного иммунитета, индуцированного БЦЖ, при аутоиммунных процессах. Важное различие между вакцинацией БЦЖ и аутоиммунными заболеваниями заключается в том, что в то время как аутоиммунитет индуцирует спонтанную выработку ИЛ-17 с аутоиммунным повреждением тканей, вакцинация БЦЖ лишь индуцирует примированное состояние клеток для более сильного ответа на вторичную микробную стимуляцию. Без стимуляции более высокой продукции этих цитокинов не наблюдалось. В соответствии с этим в одном исследовании даже сообщалось о положительном влиянии вакцинации БЦЖ на сахарный диабет 1 типа [33], а также сообщалось о положительном влиянии на астму и аллергии [34].
Важное различие между вакцинацией БЦЖ и аутоиммунными заболеваниями заключается в том, что в то время как аутоиммунитет индуцирует спонтанную выработку ИЛ-17 с аутоиммунным повреждением тканей, вакцинация БЦЖ лишь индуцирует примированное состояние клеток для более сильного ответа на вторичную микробную стимуляцию. Без стимуляции более высокой продукции этих цитокинов не наблюдалось. В соответствии с этим в одном исследовании даже сообщалось о положительном влиянии вакцинации БЦЖ на сахарный диабет 1 типа [33], а также сообщалось о положительном влиянии на астму и аллергии [34].
Помимо воздействия на гетерологичный иммунитет, вакцинация БЦЖ также оказывает долгосрочное воздействие на врожденный тренированный иммунитет. Это проявляется стойким увеличением продукции провоспалительных цитокинов, опосредованной ЛПС, и экспрессией рецепторов распознавания образов и маркеров активации моноцитов. Можно предположить, что эти два эффекта связаны, так как именно экспрессия рецепторов ЛПС TLR4 и CD14 [35], оставшаяся высокой через 1 год после введения БЦЖ, ответственна за усиленный цитокиновый ответ после стимуляции ЛПС. В отличие от этого, вакцинация БЦЖ не влияла на экспрессию других рецепторов распознавания образов, таких как dectin-1 и TLR2. В то время как изменения в S. aureus и C. albicans -опосредованная продукция цитокинов отчетливо присутствовала через 2 недели и 3 месяца после вакцинации, эти эффекты уменьшались через 1 год. Это говорит о том, что, по крайней мере, для некоторых врожденных иммунных путей эпигенетическое перепрограммирование, ответственное за эффекты тренированного иммунитета [26], относительно короткоживущее и присутствует в течение месяцев, а не лет.
В отличие от этого, вакцинация БЦЖ не влияла на экспрессию других рецепторов распознавания образов, таких как dectin-1 и TLR2. В то время как изменения в S. aureus и C. albicans -опосредованная продукция цитокинов отчетливо присутствовала через 2 недели и 3 месяца после вакцинации, эти эффекты уменьшались через 1 год. Это говорит о том, что, по крайней мере, для некоторых врожденных иммунных путей эпигенетическое перепрограммирование, ответственное за эффекты тренированного иммунитета [26], относительно короткоживущее и присутствует в течение месяцев, а не лет.
В заключение, в настоящем исследовании мы охарактеризовали долгосрочные неспецифические иммунологические эффекты вакцинации БЦЖ. Ранее мы показали, что врожденный иммунитет имеет адаптивные черты, называемые тренированным иммунитетом [16]. Несмотря на то, что на сегодняшний день сообщается о максимальной продолжительности эффектов тренированного иммунитета в 3 месяца [26], в настоящем исследовании мы показали, что неспецифические тренировочные эффекты вакцинации БЦЖ на экспрессию рецепторов и LPS-индуцированные провоспалительные цитокины являются давними и присутствуют. не менее 1 года. Кроме того, через 1 год после вакцинации наблюдалось сильное усиление гетерологичных ответов Th2 и Th27. Эти двойные эффекты вакцинации БЦЖ как на тренированный иммунитет, так и на ответы гетерологичных Т-клеток обеспечивают вероятное объяснение как краткосрочных, так и долгосрочных неспецифических эффектов БЦЖ, которые были известны на протяжении десятилетий и могут иметь важные последствия для разработки вакцин и политики здравоохранения. .
не менее 1 года. Кроме того, через 1 год после вакцинации наблюдалось сильное усиление гетерологичных ответов Th2 и Th27. Эти двойные эффекты вакцинации БЦЖ как на тренированный иммунитет, так и на ответы гетерологичных Т-клеток обеспечивают вероятное объяснение как краткосрочных, так и долгосрочных неспецифических эффектов БЦЖ, которые были известны на протяжении десятилетий и могут иметь важные последствия для разработки вакцин и политики здравоохранения. .
Благодарности
J.Q. и М.Г.Н. были поддержаны грантом Vici от Нидерландской организации научных исследований (для MGN). Р.В.К. был поддержан грантом Види Нидерландской организации научных исследований. R.J.X. был поддержан грантами (AI 062773, DK 043351, DK 83756) Национальных институтов здравоохранения США и Фонда Хелмсли. CVIVA поддерживается Датским национальным исследовательским фондом (DNRF108). CSB финансировался стартовым грантом ERC (через грант ERC-2009-StG -243149).
Авторское право: Все права защищены. Никакая часть данной публикации не может быть переведена на другие языки, воспроизведена или использована в любой форме и любыми средствами, электронными или механическими, включая фотокопирование, запись, микрокопирование или любую систему хранения и поиска информации, без письменного разрешения издателя. .
Никакая часть данной публикации не может быть переведена на другие языки, воспроизведена или использована в любой форме и любыми средствами, электронными или механическими, включая фотокопирование, запись, микрокопирование или любую систему хранения и поиска информации, без письменного разрешения издателя. .
Дозировка препарата: авторы и издатель приложили все усилия, чтобы гарантировать, что выбор препарата и дозировка, указанные в этом тексте, соответствуют текущим рекомендациям и практике на момент публикации. Тем не менее, в связи с продолжающимися исследованиями, изменениями в правительственных постановлениях и постоянным потоком информации, касающейся лекарственной терапии и реакций на лекарства, читателю настоятельно рекомендуется проверять вкладыш в упаковке для каждого лекарства на предмет любых изменений в показаниях и дозировке, а также для дополнительных предупреждений. и меры предосторожности. Это особенно важно, когда рекомендуемый агент является новым и/или редко используемым лекарственным средством.

 Однако в тех случаях, когда вакцинальные реакции проявляются в виде выраженного патологического процесса, их называют поствакцинальными осложнениями.
Однако в тех случаях, когда вакцинальные реакции проявляются в виде выраженного патологического процесса, их называют поствакцинальными осложнениями.

 в диаметре в месте инъекции)
в диаметре в месте инъекции) При нетяжёлых ОРВИ, ОКИ прививки проводят сразу же после нормализации температуры.)
При нетяжёлых ОРВИ, ОКИ прививки проводят сразу же после нормализации температуры.) Отказываться от прививок не стоит, так как это высочайшее изобретение человечества, которое позволило сохранить миллионы человеческих жизней.
Отказываться от прививок не стоит, так как это высочайшее изобретение человечества, которое позволило сохранить миллионы человеческих жизней. 30% осложнений – неврологические, 20% – пневмонии и бронхиты, 45% – местные осложнения, сопровождающиеся образованием рубцов на коже. У 10-20% переболевших вирус ветряной оспы пожизненно остается в нервных ганглиях и в дальнейшем вызывает другое заболевание, которое может проявиться в более старшем возрасте – опоясывающий лишай или герпес.
30% осложнений – неврологические, 20% – пневмонии и бронхиты, 45% – местные осложнения, сопровождающиеся образованием рубцов на коже. У 10-20% переболевших вирус ветряной оспы пожизненно остается в нервных ганглиях и в дальнейшем вызывает другое заболевание, которое может проявиться в более старшем возрасте – опоясывающий лишай или герпес.