Энтеровирусные инфекции
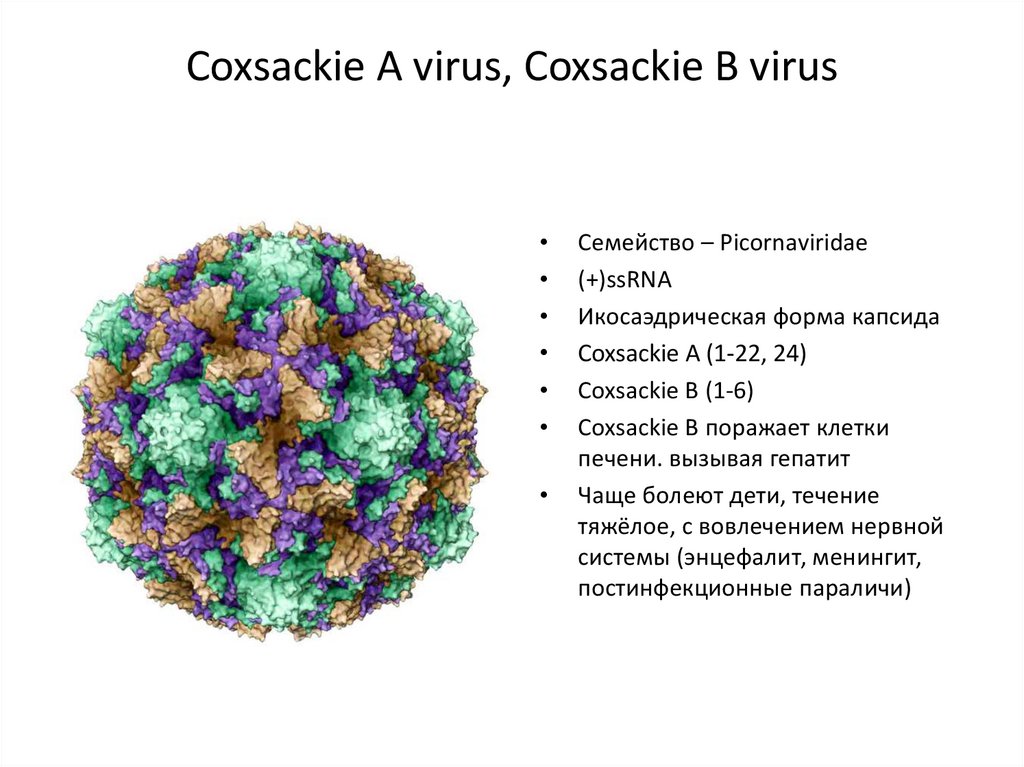
Энтеровирусные инфекции – группа заболеваний, причина которых – вирусы Коксаки и ЕСНО, рода Enterovirus, семейства Picornaviridae. Особенность этих вирусов – размножение в кишечнике, выделение с фекалиями и самое страшное – политропность, то есть способность поражать разные органы, что ведет к появлению самых непредвиденных симптомов.
Особенности энтеровирусной инфекции (ЭИ) как таковой
- Инкубационный период – время от момента заражения до появления первых симптомов болезни – длится при ЭИ 2-7 дней.
- Механизм передачи заболевания – фекально-оральный, пути передачи – пищевой, водный.
- Источники инфекции – вирусоноситель или заболевший человек.
- Наиболее восприимчивы к болезни дети.
Симптомы и формы болезни
Болезнь начинается с лихорадки 39-40˚С, головной боли, общей слабости, снижения аппетита, нарушения сна. Наблюдается покраснение кожи лица и шеи, глаз, сыпь в виде пятен и узелков по всему телу. Слизистая оболочка неба отечная и покрасневшая.
Наблюдается покраснение кожи лица и шеи, глаз, сыпь в виде пятен и узелков по всему телу. Слизистая оболочка неба отечная и покрасневшая.
Существуют различные формы болезни, что по-разному проявляются клинически.
• Серозный менингит
Как правило, имеет отчетливую картину с менингеальными симптомами, что ярко проявляются на высоте лихорадки и исчезают с 3 недели болезни. Лихорадка длится около 2 недель. Боль концентрируется в лобной части головы. Сопровождается сыпью, похожей на корь. Часто появляются катаральные явления: слезотечение, светобоязнь, жидкие выделения с носа. Подтверждается диагноз анализом спинномозговой жидкости.
• Герпетическая ангина
При осмотре горла в глаза бросается зернистость задней стенки глотки. На покрасневших небных дужках с самого начала болезни появляются высыпания в такой последовательности: узелки—пузырьки—язвы с красным ободком, элементы не склонны к слиянию, их количество — от 2 до 15. Пациент отмечает болезненность при глотании, лимфатические узлы на ощупь увеличены и уплотнены. Исход герпетической ангины, как правило, благоприятный.
Исход герпетической ангины, как правило, благоприятный.
• Кишечная форма энтеровирусных инфекций
Протекает в виде гастроэнтерита с температурой тела до 39˚С. Для данной формы характерно наличие диспепсического синдрома: пенистая диарея около 5 раз на сутки с примесью слизи и зелени, со специфическим неприятным запахом, неоднократная рвота, вздутие, урчание, и разлитые боли в животе. Но зияние ануса и спазмы кишечника отсутствуют. Во время пальпации больной отмечает болезненные ощущения ниже пупка вдоль белой линии живота, что свидетельствует о втягивание в процесс корешков нижне-грудного отдела спинного мозга. Продолжительность болезни – до 2 недель.
Важно знать!
Дети труднее переносят кишечную форму болезни: их долго беспокоят боли в животе и расстройства пищеварения (характерна вторая волна симптомов), им угрожает быстрое обезвоживание организма из-за постоянных диарей и легко поражаются верхние дыхательные пути.
• Миокардит, перикардит
Развиваются практически одновременно, поскольку вирусы-возбудители одинаково склонны к обеим тканям сердца – перикарду (околосердечная сумка) и собственно сердечной мышце — миокарду. Заболевание сначала напоминает ОРВИ, а через 1 неделю присоединяются боли в сердце, неприятные ощущения в области грудной клетки, общая слабость, лихорадка. При прослушивании сердца врач отмечает появление глухих тонов и специфического шума, а на ЭКГ наблюдаются нарушения ритма.
Заболевание сначала напоминает ОРВИ, а через 1 неделю присоединяются боли в сердце, неприятные ощущения в области грудной клетки, общая слабость, лихорадка. При прослушивании сердца врач отмечает появление глухих тонов и специфического шума, а на ЭКГ наблюдаются нарушения ритма.
• Конъюнктивит
Проявляется резями в глазах, боязнью яркого света, слезотечением, отечностью век и склер. Выделения из глаз поначалу мутные, с желтоватым оттенком, а со временем становятся гнойными. Через несколько дней «светлого промежутка» возможно поражение спинного мозга и развитие лихорадки.
• Миалгии
Слово происходит от латинских слов «Мио» – мышца, «алгия» – боль. Миалгии – болевые ощущения в скелетных мышцах, интенсивность которых возрастает при движениях, длительность от 30 секунд до 1,5 минуты. Мышцы живота при пальпации напряжены, дыхание щадящее, поверхностное, кожа бледная. Болезнь продолжается около недели.
Диагностика
• Врачу необходимо узнать о возможном контакте пострадавшего с вирусным больным,
• обратить внимание на симптомы заболевания,
• объективная оценка врачом состояния пациента, осмотр узкими специалистами (ЛОР, невролог, кардиолог, окулист).
• Спинномозговая жидкость (ликвор) – 2-3 тыс. лейкоцитов в 1 мм куб., сначала превышает количество палочкоядерных нейтрофилов, а в дальнейшем сохраняется лимфоцитоз (на пользу вирусной инфекции). Ликвор бесцветный, прозрачный, вытекает под давлением.
• Носоглоточные смывы подходят как материал для диагностики на протяжении первых 2-3 недель болезни.
• Кал как материал для анализов подходит при выраженном поносе, а выделение вируса из кишечника длится первые 6-8 недель.
• Перикардиальная жидкость, которая находится между сердечной мышцей и околосердечной сумкой — отличный материал для исследования вовремя миоперикардита. Но к манипуляции редко прибегают из-за ее сложности и негативных последствий.
Совет!
При подозрении на энтеровирусную инфекцию необходимо сразу назначать специфические анализы с использованием биологических выделений, поскольку период максимального выделения вируса из организма — первая неделя заболевания.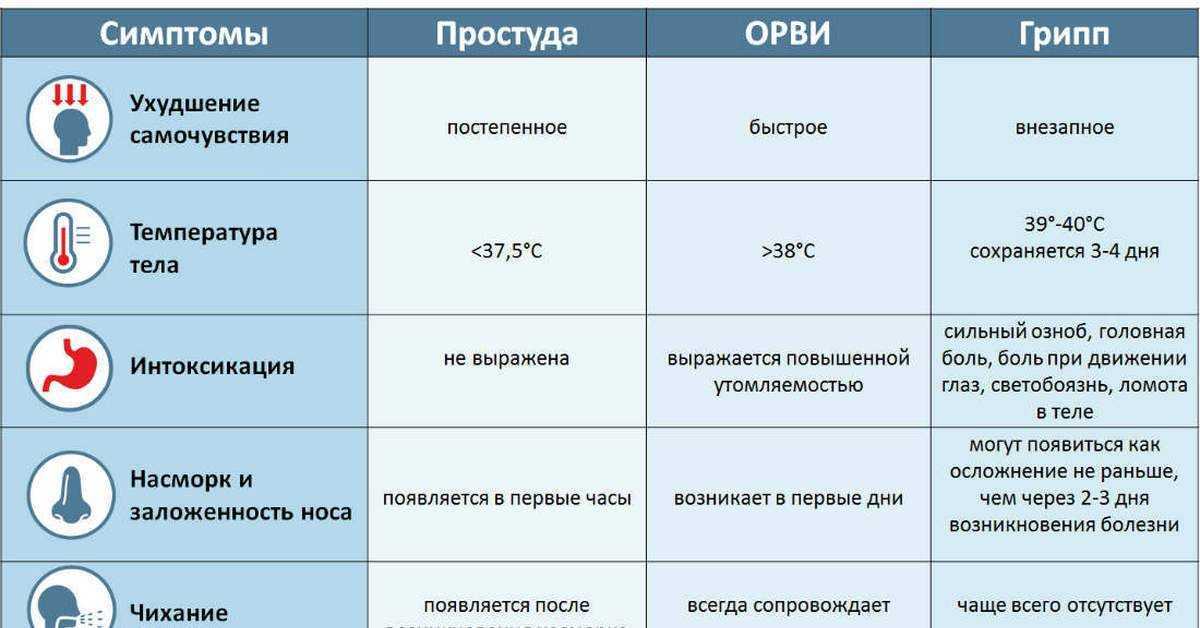
К сожалению, даже серологическое исследование не всегда доказывает присутствие в организме энтеровирусов. Только четырехразовое нарастание антител в парных сыворотках (взятие производится в первые дни и на 2-3 неделю болезни у пациента или выздоравливающего человека) и является достоверным признаком данной инфекции.
Лечение
✔ Постельный режим, диета с исключением экстрактивных веществ и клетчатки.
✔ К сожалению, средств, конкретно нацеленных на энтеровирус, не существует. Применяются противовирусные препараты «Виферон», «Циклоферон».
✔ При затяжном и тяжелом течении патологии возможно присоединение агрессивных бактерий, и тогда используют антибактериальные средства.
Совет!
Антибиотики первого ряда для лечения кишечных инфекций — это нитрофураны, триметоприм. Во время их использования стоит помнить о назначении полезных бактерий и средств, что улучшают состояние микрофлоры кишечника и предупреждают развитие дисбактериоза – «Линекс», «Бифиформ», «Бифилиз», лактулоза.
✔ В основном лечение симптоматическое.
- При отеке мозга используют мочегонные средства, например, фуросемид. Глюкозу в данном случае используют с осторожностью и только при лабораторно подтверждённом низком уровне сахара крови, чтобы не усилить отек мозга.
- Откорректировать водно-солевой баланс, нарушение которого происходит вследствие рвоты, диареи, повышенной потливости, помогают растворы «Регидрон», «Дисоль», «Трисоль», реополиглюкин, натрия хлорид, «Неогемодез».
- Выведение вредных веществ осуществляется при помощи «Смекты», «Атоксила», активированного угля.
Совет!
Особенного подхода к возобновлению жидкости в организме требуют дети.
При І степени обезвоживания суточное количество жидкости составляет 130-150 мл/кг массы тела, при ІІ степени -170-200 мл/кг, при ІІІ степени -200-220 мл/кг. При обезвоживании ІІ и ІІІ степеней растворы вводят внутривенно.
- Состояние больного при конъюнктивите с кровоизлияниями облегчают использованием глазных антисептических капель и нахождением в затемненном помещении.
- Болевой синдром при миалгии купируют обезболивающими препаратами, такими, как анальгин или баралгин. Отвлекающая терапия горчичниками и грелками также эффективна.
- При герпетической ангине стоит отказаться от употребления острой и механически грубой еды, полоскать рот после приема пищи ромашковым или содовым раствором.
- Лечение воспаления сердечных оболочек должно осуществляться в стационаре под присмотром кардиолога.
Профилактика
• Неспецифическая: очистка загрязнения внешней среды, обеззараживание отходов.
• Специфическая предусматривает использование белков для стимуляции иммунитета: людям, которые контактировали с больными, вводится внутримышечно иммуноглобулин, а на протяжении недели капается в нос интерферон.
При появлении симптомов энтеровирусной инфекции немедленно обратитесь к врачу.
Здоровья Вам и Вашим близким!
Статью подготовил врач медицины неотложных состояний Загродская Татьяна Владимировна.
Противовирусная терапия острых респираторных инфекций у детей | #08/12
Проблема лечения и профилактики острых инфекционных болезней органов дыхания, особенно вирусной этиологии, остается актуальной для практического здравоохранения, несмотря на широкий выбор имеющихся в настоящее время на фармацевтическом рынке препаратов.
Достижения медицинской науки и иммунопрофилактики позволили за последние годы раскрыть многие стороны сложной и многоплановой проблемы лечения и профилактики острых респираторных вирусных инфекций (ОРВИ), среди которых особое место по тяжести и последствиям занимает грипп. Эффективным методом профилактики инфекций является вакцинация, приводящая к развитию специфической резистентности [1]. Но на сегодняшний день в отношении огромного числа респираторных возбудителей она ограничена и проводится, как известно, лишь против гриппа, гемофильной и пневмококковой инфекций.
Острые респираторные заболевания являются наиболее распространенной патологией у детей и взрослых и занимают ведущее место в структуре общей заболеваемости населения. При этом проблема острых респираторных инфекций (ОРИ) наиболее актуальна в педиатрической практике, что обусловлено их значительной распространенностью в детской популяции, а также высоким риском развития серьезных осложнений [3]. Хорошо известно, что 90–95% всех ОРИ имеют вирусное происхождение.
Диагностика ОРВИ и гриппа основана на совокупности клинико-эпидемиологических данных. Биологические свойства вирусов, также как и особенности других микроорганизмов, определяют поражение слизистой оболочки респираторного тракта и, следовательно, клинические проявления заболевания. В настоящее время для раннего подтверждения диагноза существует возможность экспресс-диагностики вирусных инфекций дыхательных путей с использованием современных диагностических тест-систем [4].
В настоящее время для раннего подтверждения диагноза существует возможность экспресс-диагностики вирусных инфекций дыхательных путей с использованием современных диагностических тест-систем [4].
Благодаря развитию молекулярно-биологических лабораторных методов исследования, в последние годы произошли значительные изменения в структуре респираторных инфекций. Если в прежние годы при постановке ребенку диагноза ОРВИ предполагались, прежде всего, хорошо изученные и известные возбудители — такие как вирусы гриппа, парагриппа, аденовирусы, респираторно-синцитиальный вирус (РС-вирус), энтеро- и риновирусы, то в последние годы возрос удельный вес герпес-вирусов и атипичных возбудителей, обнаружены ранее неизвестные вирусы, вызывающие инфекции респираторного тракта человека: коронавирусы, метапневмовирус, бокавирус [5–8].
Процессы, вызванные вирусной инфекцией, в значительной степени определяют характер течения инфекционного процесса и его исход. Степень виремии — вирусной нагрузки — прямо коррелирует с проявлениями токсикоза, тяжестью состояния больного, лихорадкой, реакцией иммунной системы. Важной биологической особенностью вирусов является возможность персистирования в организме и развитие хронической или латентной вирусной инфекции [9]. Установлено, что и вирусы гриппа, парагриппа, аденовирусы, РС-вирус могут длительное время персистировать в организме после перенесенной болезни [10]. Персистенция вирусов вызывает дефекты иммунной реактивности и создает благоприятные условия для бактериальной инфекции.
Важной биологической особенностью вирусов является возможность персистирования в организме и развитие хронической или латентной вирусной инфекции [9]. Установлено, что и вирусы гриппа, парагриппа, аденовирусы, РС-вирус могут длительное время персистировать в организме после перенесенной болезни [10]. Персистенция вирусов вызывает дефекты иммунной реактивности и создает благоприятные условия для бактериальной инфекции.
Все это объясняет необходимость решения лечащим врачом вопроса о проведении этиотропной противовирусной терапии ОРВИ и гриппа. Однако противовирусных препаратов, обладающих клинически доказанной эффективностью, существует гораздо меньше, чем антибиотиков [11]. Кроме того, несмотря на то, что современные противовирусные химиопрепараты способны подавлять вирусную репликацию, они обладают токсичностью при действии на клетки организма, а к некоторым — быстро возникает устойчивость [12]. Наряду с узкой специфичностью и формированием устойчивости вирусов к противовирусному действию ряда таких препаратов, токсичность является ограничивающим фактором для их применения в клинической практике, особенно для назначения детям [13].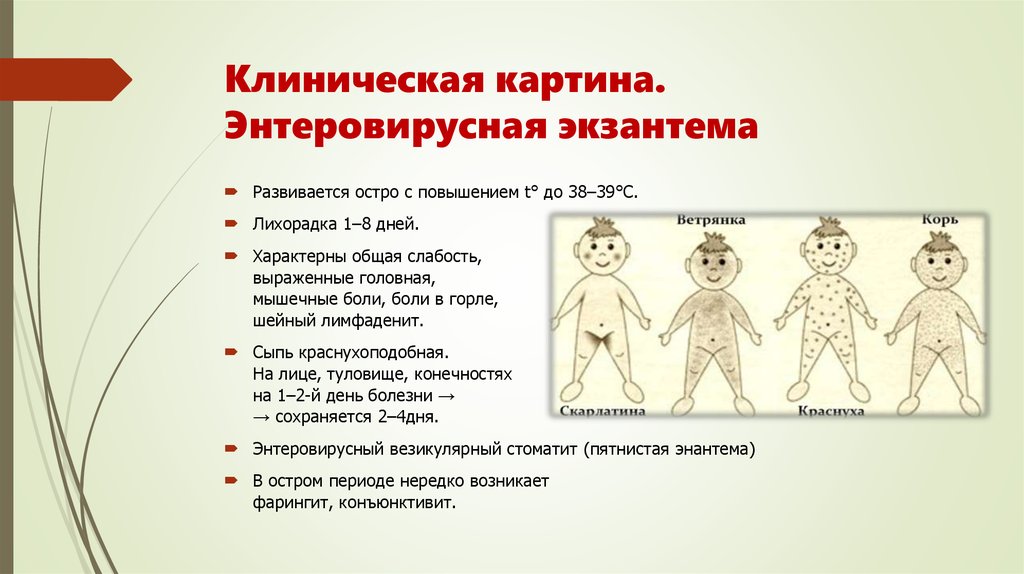
Приоритет при выборе противовирусных препаратов заключается в избирательном подавлении репродукции вирусов без существенного нарушения жизнедеятельности клеток макроорганизма. К таким препаратам относится Изопринозин (инозин пранобекс), обладающий этиопатогенетическим действием при лечении ОРВИ и гриппа. Преимущественным свойством препарата является и его комплексное действие — противовирусное и иммуномодулирующее. Инозин пранобекс в соответствии с международной классификацией лекарственных средств относится к группе противомикробных антивирусных препаратов для системного использования и к группе иммуномодуляторов (код АТС J05AX05). В Российской Федерации Изопринозин зарегистрирован для лечения и профилактики острых и хронических вирусных инфекций и разрешен для применения в педиатрической практике (www.drugreg.ru).
Изопринозин обладает прямым противовирусным действием — подавляет репликацию ДНК и РНК вирусов посредством связывания с рибосомой клетки и изменения ее стереохимического строения, в результате чего в клетке нарушается синтез вирусных белков и снижается интенсивность размножения вируса.
Противовирусная активность Изопринозина доказана и в отношении респираторных вирусов, включая вирусы гриппа А и В, парагриппа, аденовирусы, респираторно-синцитиальный вирус [16]. Ингибирующее влияние препарата на репродукцию вирусов гриппа выявлено как при предварительной обработке культуры клеток (профилактический режим), так и при внесении препарата непосредственно после инфицирования клеток (терапевтический режим). В специальном исследовании, проведенном в НИИ гриппа РАМН (Санкт-Петербург, 2009 г.), было показано, что Изопринозин проявляет отчетливую противогриппозную активность в культуре клеток, зараженных вирусом «свиного» гриппа.
Противовирусный механизм Изопринозина реализуется уже к концу первых суток приема препарата [17, 18]. Инозин пранобекс нарушает на стадии транскрипции синтез вирусной РНК, что впоследствии делает невозможными процессы репликации полноценных РНК и ДНК соответствующих типов вирусов, т. е. нарушается воспроизводство вирусов и снижается вирусемия [19]. При этом Изопринозин не влияет на развитие и функции здоровых клеток (отсутствие токсического эффекта), что очень важно при выборе лекарственного средства в педиатрической практике.
е. нарушается воспроизводство вирусов и снижается вирусемия [19]. При этом Изопринозин не влияет на развитие и функции здоровых клеток (отсутствие токсического эффекта), что очень важно при выборе лекарственного средства в педиатрической практике.
Как известно, сохранение постоянства внутренней среды организма иммунная система осуществляет с помощью факторов врожденного и приобретенного иммунитета путем распознавания и элиминации из организма чужеродных веществ антигенной природы как экзогенного (в основном это возбудители инфекции), так и эндогенного происхождения (клетки, измененные вирусами, ксенобиотиками, злокачественные клетки и т. д.). Противовирусное действие Изопринозина активно обсуждалось в ранних его исследованиях и считалось главным свойством препарата. Было установлено, что инозин пранобекс, проникнув в инфицированные клетки, ингибирует синтез вирусных мРНК, а в нормальных клетках, наоборот, ускоряет экспрессию как общего РНК, так и мРНК, что особенно важно для клеток иммунной системы. С одной стороны, Изопринозин блокирует размножение вирионов, ингибируя вирусную мРНК в инфицированных клетках, а с другой, поддерживает функциональную активность иммунокомпетентных клеток [20]. Таким образом, этиотропная противовирусная эффективность Изопринозина может быть дополнительно связана и с его иммуномодулирующими возможностями. В последующем на основании результатов многочисленных исследований действия препарата было показано, что наряду с антивирусным эффектом инозин пранобекс обладает свойствами иммуномодулятора [21, 22].
С одной стороны, Изопринозин блокирует размножение вирионов, ингибируя вирусную мРНК в инфицированных клетках, а с другой, поддерживает функциональную активность иммунокомпетентных клеток [20]. Таким образом, этиотропная противовирусная эффективность Изопринозина может быть дополнительно связана и с его иммуномодулирующими возможностями. В последующем на основании результатов многочисленных исследований действия препарата было показано, что наряду с антивирусным эффектом инозин пранобекс обладает свойствами иммуномодулятора [21, 22].
Инозин пранобекс, стимулируя дифференцировку Т-лимфоцитов в цитотоксические Т-клетки и Т-хелперы, а также повышая продукцию лимфокинов, стимулирует выработку интерлейкина (IL) 1, IL-2, интерферона-гамма (IFNγ) и функциональную активность NK-клеток (естественные киллеры, англ. Natural killer cells). Изопринозин также потенцирует морфофункциональную состоятельность нейтрофилов и моноцитов, усиливая хемотаксис макрофагов и фагоцитоз, тем самым нормализует клеточный иммунитет. В то же время, стимулируя дифференцировку В-лимфоцитов в плазматические клетки и повышая продукцию антител, нормализует гуморальный иммунитет. При этом происходит повышение концентрации иммуноглобулинов IgG, IgA и IgM, а также поверхностных маркеров комплемента и вируснейтрализирующих антител. Активизируя функцию иммунокомпетентных клеток, Изопринозин еще и опосредованно подавляет синтез вирусной РНК, что сопровождается ингибированием вирусной репродукции.
В то же время, стимулируя дифференцировку В-лимфоцитов в плазматические клетки и повышая продукцию антител, нормализует гуморальный иммунитет. При этом происходит повышение концентрации иммуноглобулинов IgG, IgA и IgM, а также поверхностных маркеров комплемента и вируснейтрализирующих антител. Активизируя функцию иммунокомпетентных клеток, Изопринозин еще и опосредованно подавляет синтез вирусной РНК, что сопровождается ингибированием вирусной репродукции.
По данным зарубежных авторов, после применения Изопринозина для лечения ОРВИ у детей и взрослых клиническое улучшение наблюдалось в 89,6% изученных случаев (у 1573 из 1754 пациентов), при этом иммунологическое улучшение было достоверно установлено в 93,1% изученных случаев (у 1273 из 1376 пациентов). Показано, что Изопринозин потенцирует хемотаксис и фагоцитирующую активность нейтрофилов, моноцитов и макрофагальных клеток (Kozma D. et al., 1989), повышает функциональную активность цитотоксических Т-лимфоцитов, естественных клеток-киллеров и продукцию вируснейтрализующих антител (Wiedermann D. et al., 1987). Действие препарата сопровождается повышением продукции цитокинов иммунокомпетентными клетками (Hersey P. et al., 1994). Важным его эффектом является увеличение секреции эндогенного IFNγ, а также снижение биосинтеза IL4. В экспериментах с помощью инозин пранобекса удавалось преодолевать даже генетически детерминированный блок функций иммунокомпетентных клеток (Fischbach M., Taleb N., 1985). Таким образом, Изопринозин модулирует неспецифический иммунитет, увеличивая резистентность организма к широкому спектру вирусов.
et al., 1987). Действие препарата сопровождается повышением продукции цитокинов иммунокомпетентными клетками (Hersey P. et al., 1994). Важным его эффектом является увеличение секреции эндогенного IFNγ, а также снижение биосинтеза IL4. В экспериментах с помощью инозин пранобекса удавалось преодолевать даже генетически детерминированный блок функций иммунокомпетентных клеток (Fischbach M., Taleb N., 1985). Таким образом, Изопринозин модулирует неспецифический иммунитет, увеличивая резистентность организма к широкому спектру вирусов.
Инозин пранобекс — синтетический аналог инозина, состоит из соли пара-ацетамидобензоевой кислоты и N, N-диметил-амино-2-пропанола и бета-изомера инозина в соотношении 3:1, получен путем соединения инозина с вспомогательной молекулой, которая повышает доступность инозина для лимфоцитов и, таким образом, усиливает его иммуностимулирующие свойства. Инозин является природным пуриновым соединением, присутствующим в пище и входящим в состав некоторых важных веществ: пуриновых коэнзимов, высокоэнергетических фосфатных соединений (АТФ, ГТФ) и циклических пуриновых нуклеотидов. Инозин принимает участие в регуляции многих физиологических процессов в организме. Как и другие нуклеозиды, проявляет свойство стимулировать лейкопоэз, процессы регенерации и репарации, функциональную активность клеток иммунной системы.
Инозин принимает участие в регуляции многих физиологических процессов в организме. Как и другие нуклеозиды, проявляет свойство стимулировать лейкопоэз, процессы регенерации и репарации, функциональную активность клеток иммунной системы.
Известно, что снижение общего иммунитета может быть обусловлено недостаточным поступлением субстратов энергетического обмена в клетку, вследствие чего иммунокомпетентные клетки находятся в состоянии энергетического дефицита и адекватно ответить на инфекцию не могут. Эти состояния зачастую формируют вторичную иммунную недостаточность (ВИН), когда изменений в количественном составе иммунокомпетентных клеток при иммунологических исследованиях не выявляется, а причина частой заболеваемости до конца не ясна. Само по себе частое чередование инфекционных процессов, например у часто болеющих респираторными инфекциями детей, также сопровождается развитием энергодефицитных состояний и снижением функциональной активности иммунокомпетентных клеток вследствие их энергетического голода [23], что в свою очередь способствует как обострению имеющихся хронических воспалительных заболеваний, так и хронизации вирусной инфекции. Необходимо также учитывать, что ВИН приводит к так называемому синдрому послевирусной астении, который может развиваться у больных в течение одного месяца после начала инфекции и отличается разнообразной клинической симптоматикой, ведущими среди которой являются усталость и эмоциональные нарушения. Назначение Изопринозина в подобной ситуации способствует нормализации энергетического обмена в клетках. Проникая в клетки, инозин пранобекс повышает их энергетический уровень, усиливает устойчивость к цитопатогенному действию вирусов и препятствует развитию синдрома поствирусной астении, особенно характерного при гриппе и повторных ОРВИ [24].
Необходимо также учитывать, что ВИН приводит к так называемому синдрому послевирусной астении, который может развиваться у больных в течение одного месяца после начала инфекции и отличается разнообразной клинической симптоматикой, ведущими среди которой являются усталость и эмоциональные нарушения. Назначение Изопринозина в подобной ситуации способствует нормализации энергетического обмена в клетках. Проникая в клетки, инозин пранобекс повышает их энергетический уровень, усиливает устойчивость к цитопатогенному действию вирусов и препятствует развитию синдрома поствирусной астении, особенно характерного при гриппе и повторных ОРВИ [24].
Эффективность и безопасность инозина пранобекса с позиций доказательной медицины подтверждена зарубежными и отечественными исследованиями. Применение Изопринозина при гриппе и ОРВИ сокращает продолжительность и выраженность симптомов заболевания (лихорадочного периода, интоксикации, катаральных симптомов в носоглотке). Показано уменьшение продолжительности болезни и купирование симптомов заболевания через 48–72 часа после назначения препарата детям в возрасте от 1 мес до 12 лет при ОРВИ (ринофарингит, острый ринофарингит), у пролеченных пациентов температура была невысокой и держалась не более 2 дней, общие симптомы исчезали за 1–2 дня [19].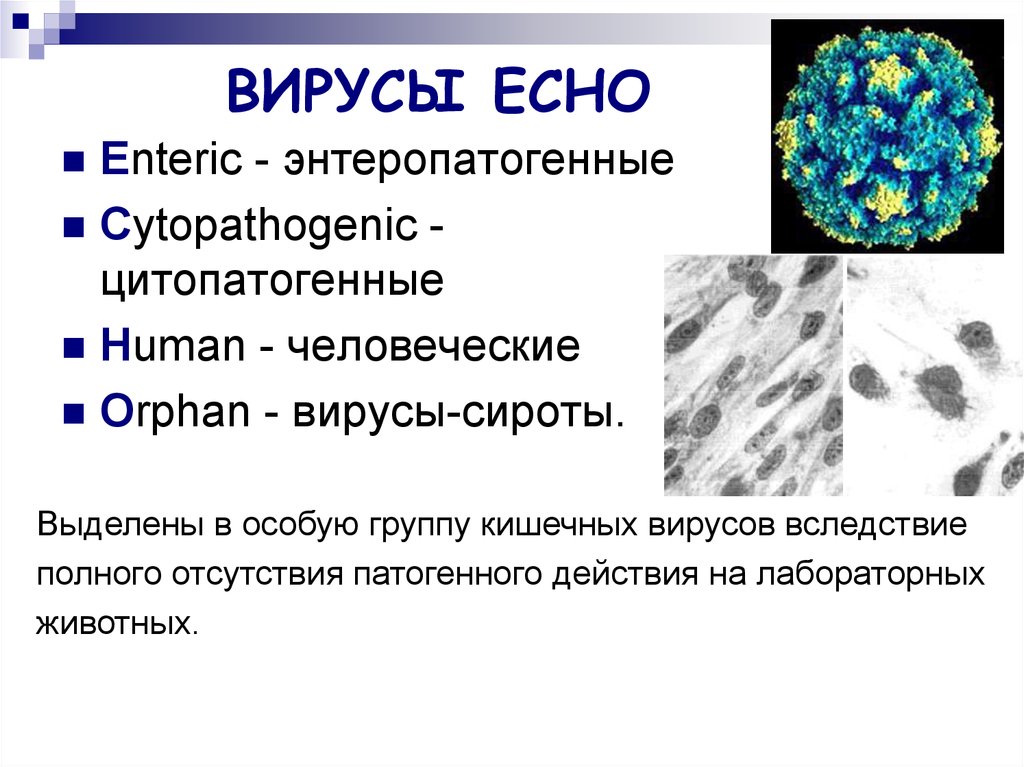 Результаты использования Изопринозина в терапии при бронхиолите (возраст пациентов от 2 до 17 мес), острого бронхита (дети от 1 мес до 8 лет) и бронхопульмонита (пациенты от 15 мес до 3 лет) свидетельствуют о быстром улучшении состояния и наступлении ремиссии через 3–4 дня [25]. Применение Изопринозина для лечения ОРВИ у пациентов с ослабленным иммунитетом позволяет снизить потребность в назначении антибиотиков, не требует дополнительного назначения других лекарственных средств, сокращает сроки госпитализации [26–29].
Результаты использования Изопринозина в терапии при бронхиолите (возраст пациентов от 2 до 17 мес), острого бронхита (дети от 1 мес до 8 лет) и бронхопульмонита (пациенты от 15 мес до 3 лет) свидетельствуют о быстром улучшении состояния и наступлении ремиссии через 3–4 дня [25]. Применение Изопринозина для лечения ОРВИ у пациентов с ослабленным иммунитетом позволяет снизить потребность в назначении антибиотиков, не требует дополнительного назначения других лекарственных средств, сокращает сроки госпитализации [26–29].
Лечебно-профилактическая эффективность Изопринозина продемонстрирована в многоцентровом постмаркетинговом исследовании в рамках программы «Здоровый ребенок», проведенном в 13 городах РФ (2007) с участием более 2,5 тыс. детей в возрасте 12 мес и старше с ОРВИ [16, 30]. Согласно результатам исследования, применение Изопринозина у детей, включая лиц с неблагополучным преморбидным фоном (часто болеющих детей, пациентов с аллергозами, с хроническими инфекциями ЛОР-органов и респираторного тракта), способствовало сокращению продолжительности симптомов заболевания, в том числе температурной реакции, интоксикации и катаральных явлений в носоглотке. Похожие данные представлены Golebiowska-Wawrzyniak M. et al. (2005) по результатам обследования детей с неблагоприятным преморбидным фоном и рецидивирующими респираторными инфекциями [14].
Похожие данные представлены Golebiowska-Wawrzyniak M. et al. (2005) по результатам обследования детей с неблагоприятным преморбидным фоном и рецидивирующими респираторными инфекциями [14].
Метаанализ оценки клинической и иммунологической эффективности инозина пранобекса при респираторных инфекциях у иммунокомпрометированных пациентов по данным опубликованных исследований, в которых 2,5 тыс. пациентам (детям и взрослым) инозин пранобекс использовался с лечебно-профилактической целью, также подтвердил эффективность терапии [31].
Инозин пранобекс является препаратом выбора для лечения детей с герпесвирусными и смешанными респираторными инфекциями, оптимизации программы лечения часто болеющих детей [32]. Анализ различных схем лечения детей с рецидивирующими респираторными заболеваниями смешанной этиологии выявил лучший положительный клинико-серологический результат при лечении Изопринозином — у 77% пациентов (Ацикловиром у 50%, Арбидолом или Циклофероном у 30%) [33].
Инозин пранобекс относится к малотоксичным веществам и в этом отношении имеет преимущества перед другими синтетическими противовирусными препаратами и иммуномодулирующими средствами с противовирусной активностью. Клинические исследования продемонстрировали его хорошую переносимость. По данным зарубежных и отечественных исследований, среди побочных эффектов, связанных с приемом препарата, были отмечены головные боли и головокружение, зуд, тяжесть в области желудка, которые встречались редко и купировались при его отмене. При длительном приеме может наблюдаться повышение уровня мочевой кислоты в крови и моче, которые возвращаются к норме после прекращения лечения. В России применение препарата в форме таблеток разрешено у детей с трех лет. За рубежом он доступен также в форме сиропа и не имеет возрастных ограничений.
Клинические исследования продемонстрировали его хорошую переносимость. По данным зарубежных и отечественных исследований, среди побочных эффектов, связанных с приемом препарата, были отмечены головные боли и головокружение, зуд, тяжесть в области желудка, которые встречались редко и купировались при его отмене. При длительном приеме может наблюдаться повышение уровня мочевой кислоты в крови и моче, которые возвращаются к норме после прекращения лечения. В России применение препарата в форме таблеток разрешено у детей с трех лет. За рубежом он доступен также в форме сиропа и не имеет возрастных ограничений.
При ОРВИ и гриппе Изопринозин назначается из расчета 50 мг/кг в сутки, разделенных на 3–4 приема в течение всего острого периода болезни (от 5 до 10 дней): взрослым 6–8 таблеток в сутки, детям (с трех лет) по 1 таблетке на 10 кг/массы тела в сутки.
Клинико-иммунологическая эффективность Изопринозина изучалась нами при лечении ОРИ у детей с бронхиальной астмой, находящихся на стационарном и амбулаторном лечении в Научном центре здоровья детей РАМН (Москва) [35]. При этом исключалось использование противовирусных препаратов (Ремантадин и др.), применяемых для лечения гриппа или других ОРВИ. Эффективность препарата оценивалась по срокам уменьшения симптомов интоксикации, катаральных явлений, клинических проявлений болезни, данных лабораторного исследования, свидетельствующих об активности патологического процесса, элиминации вирусов со слизистой полости носа, данных иммунного статуса (табл.).
При этом исключалось использование противовирусных препаратов (Ремантадин и др.), применяемых для лечения гриппа или других ОРВИ. Эффективность препарата оценивалась по срокам уменьшения симптомов интоксикации, катаральных явлений, клинических проявлений болезни, данных лабораторного исследования, свидетельствующих об активности патологического процесса, элиминации вирусов со слизистой полости носа, данных иммунного статуса (табл.).
В обеих группах до лечения и сразу после выздоровления в мазках носоглоточных смывов иммунофлюоресцентным методом определялись вирусные антигены. Этиология ОРВИ была установлена у 93,3% из всех наблюдавшихся пациентов, в том числе у половины обследованных детей выявлена смешанная вирусная инфекция. В основном диагностировались грипп (в т. ч. грипп типа А1, А2, В), парагрипп, аденовирусная инфекция (серотипы 1–3, 5–7). Повторное обследование детей после окончания лечения в обеих группах выявило сохранение различных респираторных вирусов, однако в группе пролеченных Изопринозином отмечена тенденция к снижению числа тестируемых у них вирусов и частоты выявления смешанной респираторно-вирусной инфекции. Морфометрический показатель активности (МПА) вирусной инфекции после лечения Изопринозином снизился в среднем в 1,2 раза (рис. 1).
Морфометрический показатель активности (МПА) вирусной инфекции после лечения Изопринозином снизился в среднем в 1,2 раза (рис. 1).
Результаты клинического мониторинга свидетельствовали о более легком течении гриппа и ОРВИ у детей, получивших Изопринозин (рис. 2).
Мониторинг биохимических показателей крови и гемограммы не выявил существенных изменений как у детей, получавших Изопринозин, так и у детей в группе сравнения (p > 0,05). У всех детей, получавших препарат, отмечалось достоверное повышение sCD4+, sCD25, IL12 и IL8 (р < 0,05) и уменьшение sCD30, TNFα (р < 0,05) после приема препарата. Отмечалась тенденция к незначительному понижению IL4 (р > 0,05). Выявлялось достоверно значимое увеличение концентрации IFNγ (р < 0,001), сохранявшееся и в период реконвалесценции ОРВИ. Вероятно, достигаемый применением Изопринозина терапевтический эффект связан с активацией Th2?иммунного ответа, проявляемой повышением продукции IFNγ и IL12, которые вызывают пролиферацию NК-клеток, оказывающих противовирусное действие.
Переносимость Изопринозина была хорошей. Выбывших из исследования пациентов в связи с нежелательными побочными явлениями и индивидуальной непереносимостью препарата не было.
Таким образом, прием Изопринозина ослабляет симптомы острой респираторной вирусной инфекции, сокращает время болезни, предотвращает осложнения и восстанавливает ослабленный иммунитет, он эффективен не только в первые часы развития заболевания, но и в последующий период. Инозин пранобекс является препаратом многоцелевого влияния, кроме прямого противовирусного действия он обладает иммуномодулирующим и энерготропным эффектами. Применение препарата при лечении ОРВИ и гриппа позволяет уменьшить потребность в назначении других лекарственных средств и снизить медикаментозную нагрузку на организм. Изопринозин может применяться как для лечения, так и для профилактики гриппа и ОРВИ у взрослых и детей.
Литература
- Баранов А. А., Таточенко В. К., Намазова-Баранова Л.
 С. Достижения и проблемы иммунопрофилактики // Вестник Российской академии медицинских наук. 2011. № 6. С. 21–26.
С. Достижения и проблемы иммунопрофилактики // Вестник Российской академии медицинских наук. 2011. № 6. С. 21–26. - Костинов М. П., Чучалин А. Г., Чебыкина А. В. Особенности формирования поствакцинального иммунитета к гриппу у пациентов с хронической бронхолегочной патологией // Инфекционные болезни. 2011. № 3. С. 35–40.
- Коровина Н. А., Заплатников А. Л., Леписева И. В. и др. Современные возможности иммунопрофилактики острых респираторных инфекций у часто болеющих детей // Педиатрическая фармакология. 2008. Т. 5. № 1. С. 21–25.
- Носик Н. Н., Стаханова В. М. Лабораторная диагностика вирусных инфекций // Клин. микробиол. антимикроб. химиотер. 2000. № 2 (2). С. 70–78.
- Williams J. V., Harris P. A., Tollefson S. J. et al. Human metapneumovirus and lower respiratory tract disease in other-wise healthy infants and children // N. Engl. J. Med. 2004. Vol. 350 (5). P. 443–450.
- Wenzel R.
 P., Fowler A. A. 3 rd. Clinical practice: Acute bronchitis // N. Engl. J. Med. 2006. Vol. 355 (20). P. 2125–2130.
P., Fowler A. A. 3 rd. Clinical practice: Acute bronchitis // N. Engl. J. Med. 2006. Vol. 355 (20). P. 2125–2130. - Боковой А. Г. Герпетические инфекции как ведущий фактор формирования вторичных иммунодефицитов в детском возрасте // Эпидемиология и инфекционные болезни. 2007. № 6. С. 34–39.
- Булгакова В. А., Зубкова И. В. Хламидийная и микоплазменная инфекции при атопической бронхиальной астме у детей // Инфекционные болезни. 2008. Т. 6. № 3. С. 56–60.
- Жукова О. Б., Рязанцева Н. В., Новицкий В. В. Вирусная персистенция: иммунологические и молекулярно-генетические аспекты // Бюллетень сибирской медицины. 2003. № 4. С. 113–119.
- Замахина Е. В., Фомина В. Л., Кладова О. В. и др. Клинико-патогенетическое значение персистенции респираторных вирусов у часто болеющих ОРЗ детей // Педиатрия. 2009. Т. 87, № 3. С. 42–47.
- Ханова Н. И., Смирнов И. Е., Пятигорская Н. В., Береговых В.
 В. Организация лекарственного обеспечения педиатрического научного учреждения // Российский педиатрический журнал. 2011. № 3. С. 49–54.
В. Организация лекарственного обеспечения педиатрического научного учреждения // Российский педиатрический журнал. 2011. № 3. С. 49–54. - Бурцева Е. И., Шевченко Е. С., Белякова Н. В. и др. Мониторинг чувствительности эпидемических штаммов вирусов гриппа изолированных в России к этиотропным препаратам // Вопросы вирусологии. 2009. Т. 54. № 5. С. 24–87.
- Ершов Ф. И. Антивирусные препараты: справочник (2-е издание). М.: Геотар-медиа, 2006. 312 с.
- Golebiowska-Wawrzyniak M., Markiewicz K., Kozar A. et al. Immunological and clinical study on therapeutic efficiacy of inosine pranobex // Pol. Merkuriusc. Lek. 2005. Vol. 19. P. 379–382.
- Campoli-Richards, Deborah M., Sorkin, Eugene M., Heel, Rennie C. Inosine Pranobex: A Preliminary Review of its Pharmacodynamic and Pharmacokinetic Properties, and Therapeutic Efficacy // Drugs. 1986. Vol. 32 (5). P. 383–424.
- Осидак Л. В., Зарубаев В.
 В., Образцова Е. В. и др. Изопринозин в терапии ОРВИ у часто болеющих детей // Детские инфекции. 2008. № 4. С. 35–41.
В., Образцова Е. В. и др. Изопринозин в терапии ОРВИ у часто болеющих детей // Детские инфекции. 2008. № 4. С. 35–41. - Khakoo R. A., Watson G. W., Waldman R. H., Ganguly R. Effect of inosiplex (Isoprinosine) on induced human influenza A infection //J. Antimicrob. Chemother. 1981. Vol. 7. P. 389–397.
- Robert J., Ghipponi J., Guerrier G. et al. Prevention des infections respiratoires recidivantes de I’enfant par Isoprinosine // Gasette Medicale. 1987. Vol. 94 (45). P. 60–62.
- Cohen A. L., Antonini G. M., Stefano J. C. et al. Clinical study of different viral diseases treated with the syrup dosage form of metisoprinol // La Prensa Medica Argentina. 1973. Vol. 60. P. 267–278.
- Ohnishi H., Kosuzume H., Inaba H. et al. Mechanism of host defense suppression induced by viral infection: mode of action of inosiplex as an antiviral agent // Infect. Immun. 1982. Vol. 38 (1). P. 243–250.
- Земсков В.
 М. Иммуномодулирующие свойства препаратов инозина и их аналогов. Успехи современной биологии, 1989. T. 107. Вып. 1. С. 69–78.
М. Иммуномодулирующие свойства препаратов инозина и их аналогов. Успехи современной биологии, 1989. T. 107. Вып. 1. С. 69–78. - Rhodes J. Discovery of immunopotentiatory drugs: current and future strategies // Clin. Exp. Immunol. 2002. Vol. 130. P. 363–369.
- Измайлова Т. Д., Петричук С. В., Шищенко В. М., Писарева И. В. От здоровой клетки к здоровому организму // Лечащий Врач. 2005. № 4. С. 66–68.
- Иммунокоррекция в пульмонологии/Под ред. А. Г. Чучалина. М.: Медицина, 1989. 256 с.
- Lo Lacono F., Angello D., Malizia R., Balsamo M. Metisoprinol in the treatment of certain diseases of the upper respiratory tract in children // Aggiornamento Pediatrico. 1982. Vol. 33 (1–2). P. 85–90.
- Краснов В., Кулова А., Кулова Е. и др. Реабилитация в закрытых детских учреждениях часто болеющих детей с маркерами активности герпетических инфекций // Врач. 2007. № 12. С. 68–70.
- Абелевич М.
 М., Иванова Е. Л., Лукушкина Е. Ф. Этиопатогенетическая терапия инозином пранобексом у детей с осложненным течением аллергических заболеваний // НМЖ. 2008. № 1. С. 60–64.
М., Иванова Е. Л., Лукушкина Е. Ф. Этиопатогенетическая терапия инозином пранобексом у детей с осложненным течением аллергических заболеваний // НМЖ. 2008. № 1. С. 60–64. - Аралова Е. В. Рациональная комплексная терапия острых респираторных вирусных инфекций у детей: автореферат дисс. кандидата медицинских наук. М., 2010. 26 с.
- Маркова Т. П. Применение иммунотропных препаратов в комплексном лечении и вакцинации детей с иммунодефицитными состояниями: автореферат дисс. доктора медицинских наук. М., 2011. 48 с.
- Эрман Е. С. Оценка клинико-эпидемиологической эффективности новых средств для профилактики гриппа и ОРИ другой этиологии у часто болеющих детей: автореферат дисс. кандидата медицинских наук. СПб, 2009. 21 с.
- Елисеева М. Ю., Царев В. Н., Масихи К. Н. и др. Эффективность вспомогательной иммунотерапии у пациентов с иммунодефицитом и часто болеющих детей: систематический обзор и метаанализ применения инозина пранобекса при ОРВИ // РМЖ.
 2010. Том 18. № 5 (369). С. 313–320.
2010. Том 18. № 5 (369). С. 313–320. - Симованьян Э. Н., Денисенко В. Б., Григорян А. В. Эффективность применения инозина пранобекс у часто болеющих детей с хронической Эпштейна-Барр вирусной инфекцией: результаты рандомизированного исследования // Вопросы современной педиатрии. 2011. Т. 10. № 2. С. 16–21.
- Савенкова М. С., Афанасьева А. А., Минасян В. С., Тюркина С. И. Лечение часто болеющих детей со смешанной инфекцией // Вопросы современной педиатрии. 2011. Т. 10. № 4. С. 83–88.
- Булгакова В. А. Научное обоснование и эффективность иммунопрофилактики и иммунотерапии вирусной и бактериальной инфекции у детей с бронхиальной астмой: автореферат дисс. доктора медицинских наук. М., 2009. 50 с.
- Лозовская Л. С., Ермакова М. К., Менемчиадис Г. И. и др. Хроническая врожденная Коксаки-вирусная инфекция и ее участие в этиологии аллергических болезней, выявляемых у детей // Вопросы вирусологии. 1999. № 6.
 С. 268–272.
С. 268–272.
В. А. Булгакова, доктор медицинских наук
ФГБУ НЦЗД РАМН, Москва
Контактная информация об авторе для переписки: [email protected]
Противовирусное лечение инфекции, вызванной вирусом Коксаки В, в островках поджелудочной железы человека
Сравнительное исследование
. 2007 г., апрель; 74 (1): 65–71.
doi: 10.1016/j.antiviral.2006.12.001. Epub 2006, 29 декабря.
Анна-Карин Берг 1 , Анника Олссон, Олле Корсгрен, Ган Фриск
принадлежность
- 1 Отделение женского и детского здоровья, Уппсальский университет, Академическая больница, ing 95/96 nbv, SE-751 85 Уппсала, Швеция.
 Анна-Карин.Берг@kbh.uu.se
Анна-Карин.Берг@kbh.uu.se
- PMID: 17239967
- DOI: 10.1016/j.антивирус.2006.12.001
Сравнительное исследование
Анна-Карин Берг и др. Противовирусный рез. 2007 Апрель
. 2007 г., апрель; 74 (1): 65–71.
doi: 10.1016/j.antiviral.2006.12.001. Epub 2006, 29 декабря.
Авторы
Анна-Карин Берг 1 , Анника Олссон, Олле Корсгрен, Ган Фриск
принадлежность
- 1 Отделение женского и детского здоровья, Уппсальский университет, Академическая больница, ing 95/96 nbv, SE-751 85 Уппсала, Швеция.
 Анна-Карин.Берг@kbh.uu.se
Анна-Карин.Берг@kbh.uu.se
- PMID: 17239967
- DOI: 10.1016/j.антивирус.2006.12.001
Абстрактный
Считается, что энтеровирусные инфекции островков поджелудочной железы запускают или ускоряют почти полное разрушение бета-клеток, которое представляет собой диабет 1 типа (СД1). В этом исследовании изучалась способность антипикорнавирусного соединения плеконарила блокировать репликацию двух штаммов бета-клеточного тропного вируса Коксаки B4 (CBV-4) в изолированных островках человека. Два штамма, VD2921 и V894557, с продемонстрированной способностью вызывать нелитическую персистенцию или литическую инфекцию, соответственно, в островках, представляет собой два разных потенциальных механизма, лежащих в основе вирус-индуцированного СД1. Репликацию вируса в островках изучали с добавлением плеконарила и без него. Кроме того, каждый день изучали морфологию островков. Чтобы проверить эффекты плеконарила и/или ДМСО на секрецию инсулина бета-клетками, проводили перфузию глюкозы на обработанных и необработанных островках. Титрование вируса показало явное снижение репликации обоих штаммов после обработки плеконарилом. ВД2921 штамм был ингибирован до неопределяемого уровня. Штамм V89 4557, однако, показал первоначальное снижение титров, но затем титры вируса увеличились, несмотря на добавление второй дозы плеконарила. Это неполное ингибирование репликации вируса предполагает существование резистентного подтипа в этом штамме. Лечение плеконарилом снижало секрецию инсулина бета-клетками в ответ на стимуляцию глюкозой в некоторых экспериментах и вызывало небольшие морфологические изменения в островках по сравнению с необработанными контролями. Таким образом, плеконарил снижал репликацию двух бета-клеточных тропных штаммов CBV-4 в островках человека.
Репликацию вируса в островках изучали с добавлением плеконарила и без него. Кроме того, каждый день изучали морфологию островков. Чтобы проверить эффекты плеконарила и/или ДМСО на секрецию инсулина бета-клетками, проводили перфузию глюкозы на обработанных и необработанных островках. Титрование вируса показало явное снижение репликации обоих штаммов после обработки плеконарилом. ВД2921 штамм был ингибирован до неопределяемого уровня. Штамм V89 4557, однако, показал первоначальное снижение титров, но затем титры вируса увеличились, несмотря на добавление второй дозы плеконарила. Это неполное ингибирование репликации вируса предполагает существование резистентного подтипа в этом штамме. Лечение плеконарилом снижало секрецию инсулина бета-клетками в ответ на стимуляцию глюкозой в некоторых экспериментах и вызывало небольшие морфологические изменения в островках по сравнению с необработанными контролями. Таким образом, плеконарил снижал репликацию двух бета-клеточных тропных штаммов CBV-4 в островках человека. Однако генетические различия между этими штаммами повлияли на эффективность лечения плеконарилом. Это подчеркивает важность использования нескольких вирусных штаммов в противовирусных тестах.
Однако генетические различия между этими штаммами повлияли на эффективность лечения плеконарилом. Это подчеркивает важность использования нескольких вирусных штаммов в противовирусных тестах.
Похожие статьи
Противовирусный эффект никотинамида на инфицированных энтеровирусами островках человека in vitro: влияние на репликацию вируса и секрецию хемокинов.
Моэль А., Ског О., Алин Э., Корсгрен О., Фриск Г. Моэль А. и соавт. J Med Virol. 2009 г., июнь; 81 (6): 1082-7. doi: 10.1002/jmv.21476. J Med Virol. 2009. PMID: 19382275
Полная нуклеотидная последовательность штамма вируса Коксаки B-4, способного вызывать персистентную инфекцию в островковых клетках поджелудочной железы человека: влияние на высвобождение инсулина, синтез проинсулина и морфологию клеток.

Инь Х., Берг А.К., Вестман Дж., Хеллерстрем К., Фриск Г. Инь Х. и др. J Med Virol. 2002 декабрь; 68 (4): 544-57. doi: 10.1002/jmv.10236. J Med Virol. 2002. PMID: 12376963
Воздействие на изолированные клетки островков поджелудочной железы человека после заражения штаммами энтеровируса, выделенными при клинических проявлениях сахарного диабета 1 типа.
Эльшебани А., Олссон А., Вестман Дж., Тувемо Т., Корсгрен О., Фриск Г. Эльшебани А. и др. Вирус рез. 2007 март; 124 (1-2): 193-203. doi: 10.1016/j.virusres.2006.11.004. Epub 2006 12 декабря. Вирус Рез. 2007. PMID: 17169456
Роль вируса Коксаки В4 в патогенезе сахарного диабета 1 типа.
Джайдан Х., Хобер Д. Джайдане Х. и др.
 Диабет метаб. 2008 г., декабрь; 34 (6 ч. 1): 537–48. doi: 10.1016/j.diabet.2008.05.008. Epub 2008 31 октября.
Диабет метаб. 2008.
PMID: 18951821
Рассмотрение.
Диабет метаб. 2008 г., декабрь; 34 (6 ч. 1): 537–48. doi: 10.1016/j.diabet.2008.05.008. Epub 2008 31 октября.
Диабет метаб. 2008.
PMID: 18951821
Рассмотрение.Влияние факторов окружающей среды на развитие инсулинозависимого сахарного диабета.
Yoon JW, Kim CJ, Pak CY, McArthur RG. Юн Дж.В. и др. Клин Инвест Мед. 1987 г., сен; 10 (5): 457-69. Клин Инвест Мед. 1987. PMID: 3315367 Рассмотрение.
Посмотреть все похожие статьи
Цитируется
Разработка и синтез нового класса N -сульфонамидов на основе пиридина, обладающих противовирусными, антимикробными и ферментативными свойствами ингибирования.
Аззам Р.А., Эльсайед Р.
 Э., Эльгемейе Г.Х.
Аззам Р.А. и соавт.
АСУ Омега. 29 сентября 2020 г.; 5(40):26182-26194. doi: 10.1021/acsomega.0c03773. Электронная коллекция 2020 13 октября.
АСУ Омега. 2020.
PMID: 33073144
Бесплатная статья ЧВК.
Э., Эльгемейе Г.Х.
Аззам Р.А. и соавт.
АСУ Омега. 29 сентября 2020 г.; 5(40):26182-26194. doi: 10.1021/acsomega.0c03773. Электронная коллекция 2020 13 октября.
АСУ Омега. 2020.
PMID: 33073144
Бесплатная статья ЧВК.Эффективный синтез и исследования новых пиримидинсульфонамидных каркасов на основе бензотиазола в качестве новых противовирусных агентов и ингибиторов Hsp90α.
Аззам Р.А., Осман Р.Р., Эльгемейе Г.Х. Аззам Р.А. и соавт. АСУ Омега. 2020 9 января;5(3):1640-1655. doi: 10.1021/acsomega.9b03706. Электронная коллекция 2020 28 января. АСУ Омега. 2020. PMID: 32010839 Бесплатная статья ЧВК.
Что такое HLA-I! Классические и неклассические HLA класса I и их потенциальная роль в развитии диабета 1 типа.
Wyatt RC, Lanzoni G, Russell MA, Gerling I, Richardson SJ.
 Wyatt RC и соавт.
Curr Diab Rep. 9 декабря 2019 г.; 19 (12): 159. doi: 10.1007/s11892-019-1245-z.
Курр Диаб, представитель 2019 г..
PMID: 31820163
Бесплатная статья ЧВК.
Рассмотрение.
Wyatt RC и соавт.
Curr Diab Rep. 9 декабря 2019 г.; 19 (12): 159. doi: 10.1007/s11892-019-1245-z.
Курр Диаб, представитель 2019 г..
PMID: 31820163
Бесплатная статья ЧВК.
Рассмотрение.Интерферон-альфа: ключевой триггер диабета 1 типа.
Ломбарди А., Цомос Э., Хаммерстад С.С., Томер Ю. Ломбарди А. и др. J Аутоиммун. 2018 ноябрь;94:7-15. doi: 10.1016/j.jaut.2018.08.003. Epub 2018 14 августа. J Аутоиммун. 2018. PMID: 30115527 Бесплатная статья ЧВК. Рассмотрение.
Вирусные инфекции при сахарном диабете 1 типа — почему β-клетки?
Оп де Бек А., Эйзирик Д.Л. Op de Beeck A, et al. Нат Рев Эндокринол. 2016 май; 12(5):263-273. doi: 10.1038/nrendo.2016.30. Epub 2016 29 марта. Нат Рев Эндокринол.
 2016.
PMID: 27020257
Бесплатная статья ЧВК.
Рассмотрение.
2016.
PMID: 27020257
Бесплатная статья ЧВК.
Рассмотрение.
Просмотреть все статьи «Цитируется по»
Типы публикаций
термины MeSH
вещества
Оценка хлорохина в качестве противовирусного средства широкого действия против ящура и ящура.
ПОКАЗЫВАЮТСЯ 1-10 ИЗ 29 ССЫЛОК
СОРТИРОВАТЬ ПОРелевантностьНаиболее влиятельные документыНедавность
Энтеровирус человека 71 и кистевидный ящур
Болезнь кистей, ящура обычно представляет собой доброкачественное фебрильное экзантематозное детское заболевание, вызываемое энтеровирусом человека 71 (HEV-71), но серьезные вспышки с неврологическими и сердечно-легочными осложнениями, по-видимому, более распространены в Азиатско-Тихоокеанском регионе, чем где-либо еще в мире.
Статус исследования и разработки вакцин против энтеровируса 71.
- Z. Reed, M. Cardosa
Медицина
Вакцина
- 2016
Молекулярная эпидемиология энтеровируса 71, вируса Коксаки A16 и A6, связанного с кистевидным ящуром в Испании.
- M. Cabrerizo, D. Tarragó, G. Trallero
Биология, медицина
Клиническая микробиология и инфекции: официальная публикация Европейского общества клинической микробиологии и инфекционных заболеваний
- 2014
0 Последнее увеличение
0 случаев HFMD в Испании и других европейских странах было связано с большей заболеваемостью циркулирующими энтеровирусами вида А, в основном CV-A6 и CV-A16, и появлением новых генетических вариантов этих вирусов.
Вакцина EV71, новый инструмент для борьбы со вспышками кистей, ящура (HFMD)
- Q. Mao, Yi-ping Wang, Lian-lian Bian, Miao Xu, Zhenglun Liang
Медицина
Эксперт обзор вакцин
- 2016
До достижения эффективной защиты от тяжелой формы HFMD после выхода на рынок вакцин EV71 еще далеко, и оцениваются узкие места и перспективы широкого применения вакцины EV71 после ее одобрения.

Циклические модели заболеваний рук, ящура и рта, вызванных энтеровирусом A71, в Малайзии
Циклический характер эпидемий EV-A71 в Малайзии, составляющий 2–3 года, в основном обусловлен падением популяционного иммунитета, сопровождающим накопление восприимчивых детей между эпидемиями , влияя на будущее планирование, сроки и целевые группы населения для программ вакцинации.
Обнаружение и характеристика вирусов, вызывающих заболевания рук, ящура у детей в Сери Кембанган, Малайзия.
HFMD в Сери-Кембангане были вызваны различными типами энтеровирусов, а именно EV71, CVA6 и CVA16, которые тесно связаны со штаммами на Тайване и в Японии.
Энтеровирусная инфекция 71 и неврологические осложнения
Лечение внутривенным иммуноглобулином и милриноном рекомендуется в случаях тяжелых неврологических осложнений от инфекции EV71, таких как энцефалит ствола мозга, который может вызвать нейрогенное легочное кровотечение/отек, приводящий к смерти.


 С. Достижения и проблемы иммунопрофилактики // Вестник Российской академии медицинских наук. 2011. № 6. С. 21–26.
С. Достижения и проблемы иммунопрофилактики // Вестник Российской академии медицинских наук. 2011. № 6. С. 21–26. P., Fowler A. A. 3 rd. Clinical practice: Acute bronchitis // N. Engl. J. Med. 2006. Vol. 355 (20). P. 2125–2130.
P., Fowler A. A. 3 rd. Clinical practice: Acute bronchitis // N. Engl. J. Med. 2006. Vol. 355 (20). P. 2125–2130. В. Организация лекарственного обеспечения педиатрического научного учреждения // Российский педиатрический журнал. 2011. № 3. С. 49–54.
В. Организация лекарственного обеспечения педиатрического научного учреждения // Российский педиатрический журнал. 2011. № 3. С. 49–54.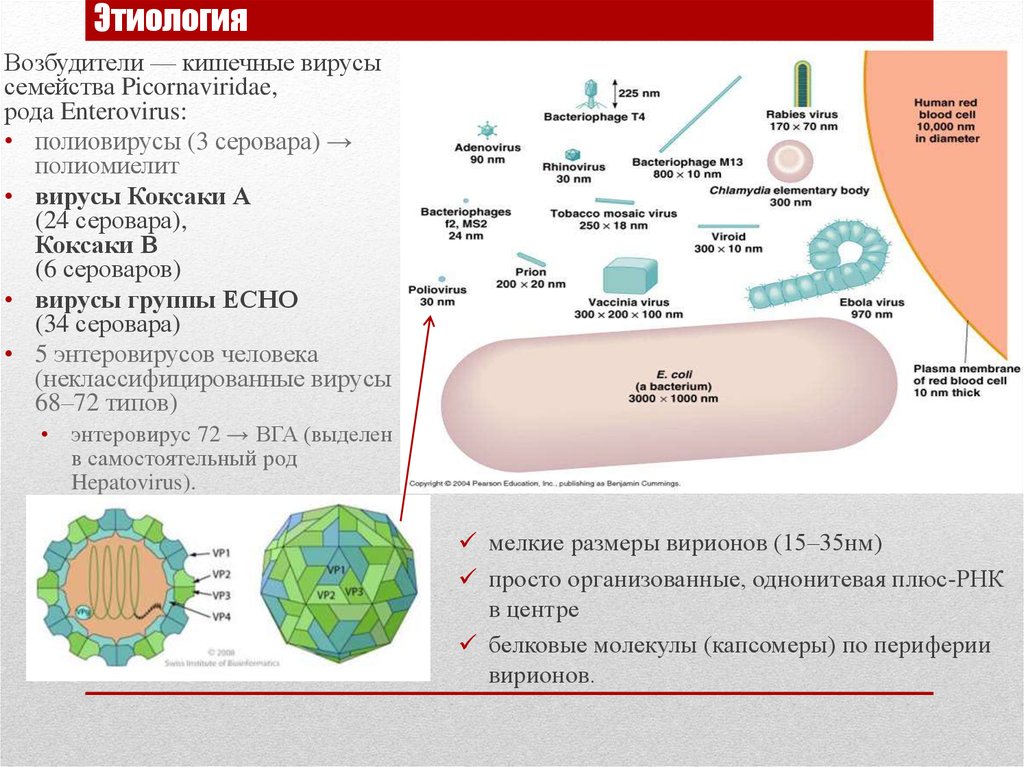 В., Образцова Е. В. и др. Изопринозин в терапии ОРВИ у часто болеющих детей // Детские инфекции. 2008. № 4. С. 35–41.
В., Образцова Е. В. и др. Изопринозин в терапии ОРВИ у часто болеющих детей // Детские инфекции. 2008. № 4. С. 35–41. М. Иммуномодулирующие свойства препаратов инозина и их аналогов. Успехи современной биологии, 1989. T. 107. Вып. 1. С. 69–78.
М. Иммуномодулирующие свойства препаратов инозина и их аналогов. Успехи современной биологии, 1989. T. 107. Вып. 1. С. 69–78. М., Иванова Е. Л., Лукушкина Е. Ф. Этиопатогенетическая терапия инозином пранобексом у детей с осложненным течением аллергических заболеваний // НМЖ. 2008. № 1. С. 60–64.
М., Иванова Е. Л., Лукушкина Е. Ф. Этиопатогенетическая терапия инозином пранобексом у детей с осложненным течением аллергических заболеваний // НМЖ. 2008. № 1. С. 60–64. 2010. Том 18. № 5 (369). С. 313–320.
2010. Том 18. № 5 (369). С. 313–320. С. 268–272.
С. 268–272. Анна-Карин.Берг@kbh.uu.se
Анна-Карин.Берг@kbh.uu.se Анна-Карин.Берг@kbh.uu.se
Анна-Карин.Берг@kbh.uu.se
 Диабет метаб. 2008 г., декабрь; 34 (6 ч. 1): 537–48. doi: 10.1016/j.diabet.2008.05.008. Epub 2008 31 октября.
Диабет метаб. 2008.
PMID: 18951821
Рассмотрение.
Диабет метаб. 2008 г., декабрь; 34 (6 ч. 1): 537–48. doi: 10.1016/j.diabet.2008.05.008. Epub 2008 31 октября.
Диабет метаб. 2008.
PMID: 18951821
Рассмотрение. Э., Эльгемейе Г.Х.
Аззам Р.А. и соавт.
АСУ Омега. 29 сентября 2020 г.; 5(40):26182-26194. doi: 10.1021/acsomega.0c03773. Электронная коллекция 2020 13 октября.
АСУ Омега. 2020.
PMID: 33073144
Бесплатная статья ЧВК.
Э., Эльгемейе Г.Х.
Аззам Р.А. и соавт.
АСУ Омега. 29 сентября 2020 г.; 5(40):26182-26194. doi: 10.1021/acsomega.0c03773. Электронная коллекция 2020 13 октября.
АСУ Омега. 2020.
PMID: 33073144
Бесплатная статья ЧВК. Wyatt RC и соавт.
Curr Diab Rep. 9 декабря 2019 г.; 19 (12): 159. doi: 10.1007/s11892-019-1245-z.
Курр Диаб, представитель 2019 г..
PMID: 31820163
Бесплатная статья ЧВК.
Рассмотрение.
Wyatt RC и соавт.
Curr Diab Rep. 9 декабря 2019 г.; 19 (12): 159. doi: 10.1007/s11892-019-1245-z.
Курр Диаб, представитель 2019 г..
PMID: 31820163
Бесплатная статья ЧВК.
Рассмотрение. 2016.
PMID: 27020257
Бесплатная статья ЧВК.
Рассмотрение.
2016.
PMID: 27020257
Бесплатная статья ЧВК.
Рассмотрение.