Кальпротектин в кале
Кальпротектин – это белок, вырабатывающийся в лейкоцитах, его концентрация в кале прямо пропорционально числу лейкоцитов, попавших в кишечник. Определение количества кальпротектина в кале – исследование, позволяющее диагностировать воспалительные заболевания кишечника.
Синонимы русские
Фекальный кальпротектин, белок нейтрофилов, маркер кишечного воспаления.
Синонимы английские
Calprotectin, CALPRO, Stool Calprotectin, Calprotectin in human faeces.
Метод исследования
Иммуноферментный анализ (ИФА).
Диапазон определения: от 19.5 до > 800 мкг/г.
Единицы измерения
Мкг/г (микрограмм на грамм).
Какой биоматериал можно использовать для исследования?
Кал.
Как правильно подготовиться к исследованию?
Специальной подготовки не требуется.
Общая информация об исследовании
В медицинской практике определение количества кальпротектина в кале пациента в совокупности с клиническими проявлениями применяется для диагностики воспалительных заболеваний кишечника.
Анализ рекомендуется проводить при подозрении на воспалительные заболевания кишечника (выявление у пациента спазмов, нарушения моторики кишечника, нерегулярного стула с примесью слизи, потери массы тела, лихорадки, повышенной потливости, общей слабости, повышенной утомляемости, артралгий, обильных выделений крови с калом, патологии перианальной области (свищи, абсцессы), запоров, болей в правом нижнем квадранте живота, вокруг пупка, тошноты, рвоты), при необходимости дифференциальной диагностики с синдромом раздраженного кишечника, другими причинами болей в животе, желудочно-кишечного кровотечения.
Измерение количества кальпротектина в образце стула пациента – это простой, неинвазивный способ диагностики воспалительных заболеваний кишечника, позволяющий врачу отличить эту группу заболеваний от синдрома раздраженного кишечника, при котором воспаление слизистой оболочки желудочно-кишечного тракта отсутствует.
Кальпротектин – это белок нейтрофилов. По сути, это протеин, связанный с кальцием. Он составляет более 60 % от общего количества белков, содержащихся в цитоплазме нейтрофильных гранулоцитов (каждый нейтрофил содержит 25 пикограммов кальпротектина). Кальпротектин высвобождается из активированных лейкоцитов, что приводит к увеличению концентрации этого протеина в фекалиях воспалительных заболеваниях соответствующих органов.
Он составляет более 60 % от общего количества белков, содержащихся в цитоплазме нейтрофильных гранулоцитов (каждый нейтрофил содержит 25 пикограммов кальпротектина). Кальпротектин высвобождается из активированных лейкоцитов, что приводит к увеличению концентрации этого протеина в фекалиях воспалительных заболеваниях соответствующих органов.
Воспалительные заболевания кишечника (ВЗК) возникают вследствие нарушения иммунного ответа хозяина и кишечной микрофлоры. Основными заболеваниями, относящимися к этой группе, являются язвенный колит и болезнь Крона, при которых может поражаться слизистая оболочка любого отдела желудочно-кишечного тракта. Существует наследственная предрасположенность к возникновению ВЗК, также пациенты, страдающие данной патологией, более склонны к развитию злокачественных новообразований.
Существует ряд исследований для подтверждения диагноза воспалительных заболеваний кишечника, но ни один из этих методов не является специфическим, и результаты должны оцениваться специалистом в совокупности с данными обследования и клинической картины. Основным в лечении пациентов, страдающих ВЗК, является поэтапная симптоматическая терапия, направленная на заживление дефектов слизистой оболочки желудочно-кишечного тракта, предотвращение осложнений заболевания.
Основным в лечении пациентов, страдающих ВЗК, является поэтапная симптоматическая терапия, направленная на заживление дефектов слизистой оболочки желудочно-кишечного тракта, предотвращение осложнений заболевания.
Для чего используется исследование?
- Для обследования пациентов при подозрении на воспалительные заболевания кишечника;
- для дифференциальной диагностики с синдромом раздраженной кишки, другими причинами болей в животе, желудочно-кишечного кровотечения;
- для профилактического обследования здоровых людей.
Когда назначается исследование?
- При выявлении у пациента спазмов, нарушения моторики кишечника, нерегулярного стула с примесью слизи, потери массы тела, лихорадки, повышенной потливости, общей слабости, повышенной утомляемости, артралгий, задержки развития у детей, обильных выделений крови с калом, патологии перианальной области (свищи, абсцессы), запоров, болей в животе (в правом нижнем квадранте живота, вокруг пупка), тошноте, рвоте.

Что означают результаты?
Референсные значения:*
* Референсные значения различаются для некоторых регионов из-за использования различных тест-систем для исследования.
Если уровень кальпротектина в кале пациента находится в пределах референсных значений, значит, у него отсутствуют воспалительные заболевания кишечника.
Умеренное повышение уровня кальпротектина требует дальнейшего наблюдения пациента и выполнения исследования в динамике. Сильное повышение (с учетом клинической картины) свидетельствует о том, что пациент страдает воспалительным заболеванием кишечника, поэтому требуется целенаправленное обследование и специфическая терапия. Также оно может быть следствием следующих патологических состояний: бактериальных и вирусных инфекций ЖКТ (сальмонеллез, кампилобактериоз, аденовирусы, ротавирусы, норовирусы), новообразований кишечника, дивертикулов, муковисцидоза, аллергии к коровьему молоку, целиакии, кишечного кровотечения.
Также рекомендуется
- Анализ кала на скрытую кровь
- Копрограмма
- Раковый эмбриональный антиген (РЭА)
- С-реактивный белок, количественно (высокочувствительный метод)
- Общий анализ крови
- Лейкоцитарная формула
- Скорость оседания эритроцитов (СОЭ)
- Ревматоидный фактор
- Антитела к ядерным антигенам (ANA), скрининг
Кто назначает исследование?
Гастроэнтеролог, педиатр, терапевт, врач общей практики.
Литература
- J. Walkowiak, S. Nousia-Arvanitakis, J. Henker, S. Stern, M. Sinaasappel, J.A. Dodge Indirect pancreatic function tests in children // J. Pediatr Gastroenterol Nutr, 40 (2) (2005), pp. 107–114.
- Aomatsu T, Yoden A, Matsumoto K, et al. Fecal calprotectin is a useful marker for disease activity in pediatric patients with inflammatory bowel disease. Dig Dis Sci. 2011 Aug;56(8):2372-7.

- Damms A, Bischoff SC. Validation and clinical significance of a new calprotectin rapid test for the diagnosis of gastrointestinal diseases. Int J Colorectal Dis. 2008 Oct;23(10):985-92.
- Jellema P, van der Windt DAWM, Schellevis FG, van der Horst HE: Systematic review: accuracy of symptom-based criteria for diagnosis of irritable bowel syndrome in primary care // Alimentary Pharmacology & Therapeutics 2009, 30(7):695-706.
- Gisbert JP, McNicholl AG: Questions and answers on the role of faecal calprotectin as a biological marker in inflammatory bowel disease // Dig Liver Dis 2009, 41(1):56-66.
- Van Rheenen PF, Van de Vijver E, Fidler V: Faecal calprotectin for screening of patients with suspected inflammatory bowel disease: diagnostic meta-analysis // BMJ 2010, 341:c3369.
Копрограмма с идентификацией гельминтов для собак в ветеринарной клинике SQ-lap
Копрограмма— вид лабораторного исследования кала, позволяющий оценить некоторые аспекты работы органов пищеварительной системы.
Что такое кал?
Исследуемый материал представляет собой продукт, получаемый в результате продвижения пищевых масс (и переваривания/всасывания жидкости) по желудочно-кишечному тракту. Кал — содержимое толстого кишечника, выделяющееся при дефекации. У здорового животного кал содержит 75-80% воды и 20-25% плотного остатка. Плотная часть состоит на 1/3 из остатков принятой пищи, на 1/3 — из остатков отделяемого желудочно-кишечного тракта, на 1/3 — из микробов, около 30% которых мертвы.
Для чего необходимо делать копрограмму?
Наряду с другими лабораторными исследованиями у животных, в нашей ветеринарной клинике проводится анализ кала. Данный вид исследования вместе с биохимичеческим анализом крови, необходим для выявления патологий желудочно-кишечного тракта и печени. С его помощью обнаруживаются заболевания воспалительного характера, инвазионные (гельминтозы) болезни, простейшие микроорганизмы, нарушения всасывания в кишечнике, нарушение поступления желчи в двенадцатиперстную кишку, нарушение работы поджелудочной железы.
Как подготовить животное к сдаче анализа?
Анализ кала в большинстве случаев проводят без специальной подготовки, однако рекомендуется за 2-3 дня до исследования избегать приема лекарственных препаратов, меняющих характер кала и вызывающих функциональные нарушения ЖКТ (препараты железа, висмута, слабительные средства). Время от дефекации до исследования должно составлять не более 12 часов (при хранении в холодильнике), а в некоторых случаях — не более 20-30 минут (при диагностике паразитарных заболеваний).
Какие исследования включает в себя копрограмма?
Анализ включает макроскопическое, микроскопическое и простое химическое исследования. Микробиологическое исследование кала производят при подозрении на инфекционное кишечное заболевание.
1. Макроскопическое исследование
• Консистенция и форма кала: кал здорового животного имеет плотную консистенцию и цилиндрическую форму. Простой осмотр каловых масс позволяет обнаружить взрослых гельминтов, членики ленточных гельминтов, определить характер кормления животного, наличие нежелательных компонентов (острые кости, палки, веревки, полиэтилен и т.д.). Консистенция зависит от количества воды, клетчатки, слизи и жира. Плотный, оформленный кал выделяется у здоровых животных. Мазевидная консистенция обусловлена нарушением секреции поджелудочной железы (острый панкреатит, некроз поджелудочной железы, муковисцидоз). Твердым кал становится при снижении скорости продвижения химуса по кишечнику. Жидкие фекалии сопровождают недостаточное переваривание в тонкой кишке при энтерите, ускоренной эвакуации, колите с изъязвлениями. Кашицеобразным кал становится при бродильной диспепсии, колите, хроническом энтероколите. Пенистый характер приобретается в результате бродильного колита, дисбиоза, дисбактериоза. Лентовидную, карандашеобразную форму кал приобретает при наличии геморроидальных узлов, спазме ректального сфинктера, трещине ануса, опухоли прямой кишки.
Простой осмотр каловых масс позволяет обнаружить взрослых гельминтов, членики ленточных гельминтов, определить характер кормления животного, наличие нежелательных компонентов (острые кости, палки, веревки, полиэтилен и т.д.). Консистенция зависит от количества воды, клетчатки, слизи и жира. Плотный, оформленный кал выделяется у здоровых животных. Мазевидная консистенция обусловлена нарушением секреции поджелудочной железы (острый панкреатит, некроз поджелудочной железы, муковисцидоз). Твердым кал становится при снижении скорости продвижения химуса по кишечнику. Жидкие фекалии сопровождают недостаточное переваривание в тонкой кишке при энтерите, ускоренной эвакуации, колите с изъязвлениями. Кашицеобразным кал становится при бродильной диспепсии, колите, хроническом энтероколите. Пенистый характер приобретается в результате бродильного колита, дисбиоза, дисбактериоза. Лентовидную, карандашеобразную форму кал приобретает при наличии геморроидальных узлов, спазме ректального сфинктера, трещине ануса, опухоли прямой кишки.
• Запах обусловлен, в основном, продуктами распада белков. Гнилостный запах появляется при недостаточности желудочного пищеварения, гнилостной диспепсии, язвенном колите. Зловонный (запах прогорклого масла)- при нарушении секреции липазы поджелудочной железой, отсутствии поступления желчи. Кислый запах обусловлен бродильными процессами в толстой кишке, нарушением всасывания жирных кислот в тонкой кишке.
•Цвет — при смешанном режиме питания — коричневый, при мясной диете — бо¬лее темный, при бродильной диспепсии — желтый кал, при гнилостной — темно-коричневый. Цвет кала в норме коричневый, в норме становится желтым при молочной диете, темно-коричневым при мясной. Черный цвет фекалии приобретают при кровотечении в переднем отделе ЖКТ (желудок, двенадцатиперстной и тонкой кишке). Темно-коричневый наблюдается при недостаточности желудочного пищеварения, гнилостной диспепсии, колите с запором, колите с изъязвлениями, повышенной секреторной функции толстой кишки. Светло-коричневым кал становится ускоренной эвакуации из толстой кишки.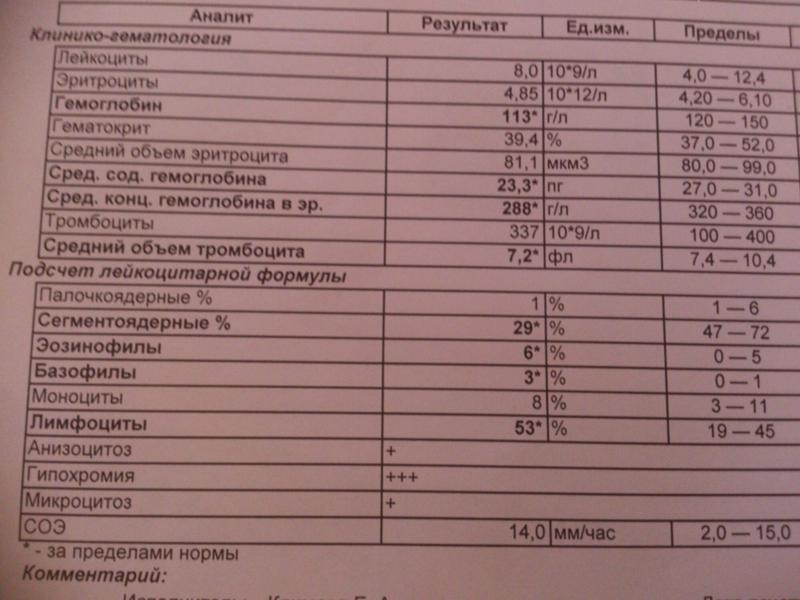 Красноватый цвет обусловлен наличием кровотечения в задних отделах ЖКТ. Желтый цвет наблюдается при недостаточности переваривания в тонкой кишке и бродильной диспепсии. Серый цвет обусловлен недостаточностью поджелудочной железы. Белым кал становится при интрагепатальном застое или полной обтурации общего желчного протока.
Красноватый цвет обусловлен наличием кровотечения в задних отделах ЖКТ. Желтый цвет наблюдается при недостаточности переваривания в тонкой кишке и бродильной диспепсии. Серый цвет обусловлен недостаточностью поджелудочной железы. Белым кал становится при интрагепатальном застое или полной обтурации общего желчного протока.
•Реакция кала – слабощелочная, реже нейтральная или слабокислая (РН 5,5 — 7,0). Выраженная щелочная реакция — при гнилостной диспепсии, вследствие усиле¬ния процессов гниения белков. Кислая реакция обусловлена наличием в кале свободных органических кислот, возникающих вследствие брожения углеводов и расцепления жиров микробами масляно-кислого брожения при бродильной диспепсии. Усиление процессов бактериального разложения белков (гниения) сопровождается образованием аммиака, придающего каловым массам щелочную реакцию, а усиление процессов брожения — выделением СО2, органических кислот и сдвигом рН в кислую сторону.
Недостаточное переваривание белков в тонком кишечнике или недостаточности поджелудочной железы, а также выделение в просвет кишки воспалительного экссудата (колиты) активизируют гнилостную флору кишечника, и реакция кала становится резко щелочной.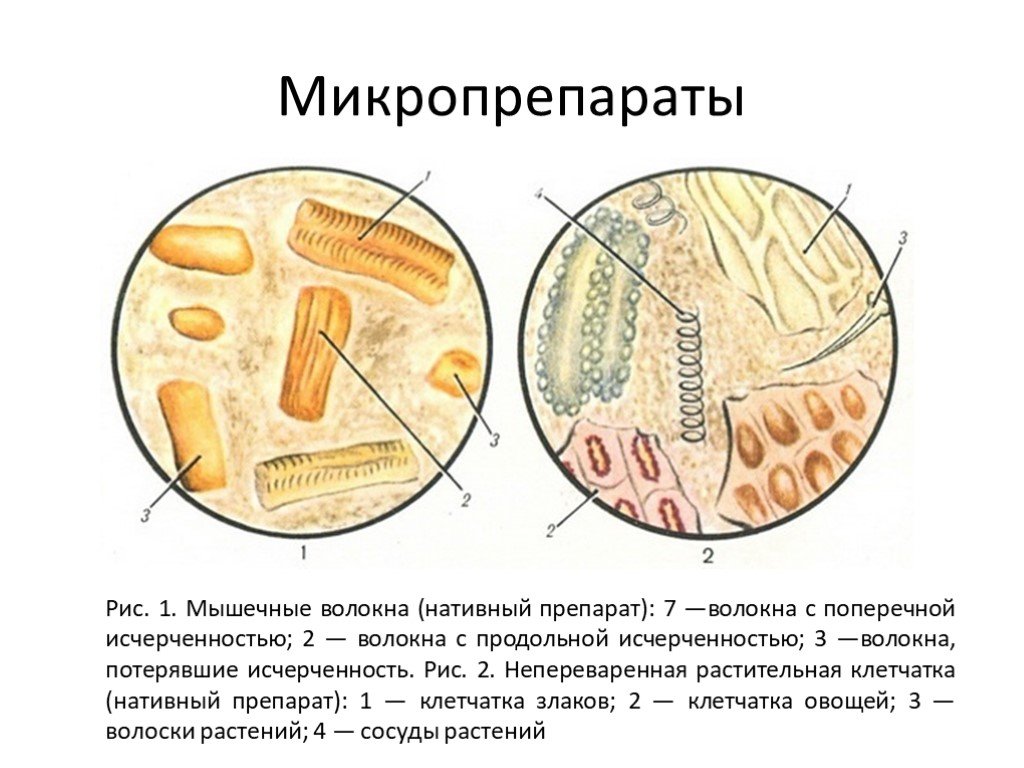
Недостаточное переваривание и усиление перистальтики кишечника при энтеритах способствуют активизации бродильной микрофлоры, и реакция кала становится кислой.
Слизь в кале. У здоровых животных каловые массы всегда покрыты тонким слоем слизи с единичными клетками цилиндрического эпителия. Появление слизи в виде хлопьев со значительным количеством кишечного эпителия, лейкоцитов и эритроцитов свидетельствует о воспалительном про¬цессе в кишечнике.
2. Микроскопическое и бактериоскопическое исследование
•Яйца гельминтов, простейшие или их цист обнаруживают с помощью флотационного метода. Также можно обнаружить артефакты (попадают в кал извне, например блохи, клещи и т.д.). Исследование кала на паразитов позволяет выявить гельминтозы (токсокароз, токсаскароз, различные виды цепней), а также лямблиоз (лямблии — мелкие простейшие, обитающие в толстом кишечнике и вызывающие его воспаление). Данное исследование позволяет эффективно подбирать антигельминтики (препараты от глистов) и составлять схему лечебной дегельминтизации, а также проводить контроль эффективности лечения при гельминтозах и лямблиозе.
Данное исследование позволяет эффективно подбирать антигельминтики (препараты от глистов) и составлять схему лечебной дегельминтизации, а также проводить контроль эффективности лечения при гельминтозах и лямблиозе.
•Мышечные волокна — принято делить на: измененные и не измененные. Характер¬ной особенностью измененых мышечных волокон является отсутствие поперечной исчерченности. В норме выявляются лишь измененные мышеч¬ные волокна в небольшом количестве. Обнаружение в кале не измененных мышечных волокон свидетельствует: о недостаточности функции желудка и поджелудочной железы, о недостаточности переваривания в тонкое кишке и ускоренной эвакуации.
•Растительная клетчатка — различают переваренную и не переваренную клетчатку. Переваренная клетчатка — это та часть клетчатки, которая под влиянием микрофлоры илеоцекального отдела кишечника расщепляется. В норме она, как правило, не обнаруживается. Количество не переваренной клетчатки в кале зависит от количества поступающей в пищеварительный тракт пищи, богатой не перевариваемой клетчаткой. Много перевариваемой клетчатки при бродильной и гнилостной диспепсии.
Много перевариваемой клетчатки при бродильной и гнилостной диспепсии.
•Жир в кале. Поступающие с пищей жиры, как животного, так и растительного происхождения усваиваются почти полностью в условиях нормального пище¬варения. В кале здорового животного жир выявляется в небольшом количестве в виде жирных кислот, их кристаллов и мыл. Появление в кале нейтрального жира или обильного количества жирных кислот, их кристаллов и мыл указы-вают на недостаточную функцию поджелудочной железы, печени, обтурацию желчевыводящих путей или быструю эвакуацию пищевых масс из кишечника, недостаточное переваривание в тонкой кишке. Значительное количество мыл и жирных кислот обнаруживается при бродильной диспепсии.
•Крахмал — в норме крахмал в кале отсутствует. При патологии пище-варения обнаруживается в переваренной клетчатке в виде внутриклеточных или внеклеточных зерен. В значительном количестве крахмал появляется при недостаточности переваривания углеводов вследствие болезни поджелудочной железы: особенно большое диагностическое значение при этом имеет внеклеточный крахмал. Очень много крахмала при бродильной диспепсии.
Очень много крахмала при бродильной диспепсии.
•Соединительная ткань — в кале здоровых животных в условиях полноценного пищеварения соединительной ткани нет. Появление её связано с недостаточностью желудочного пищеварения, т.е. отсутствием в желудочном соке соляной кислоты.
Основные синдромы заболевания ЖКТ и интерпретация копрограммы
|
Синдром |
Признаки |
Лечение |
|
Желудочная недостаточность |
Мышечные волокна, зерна крахмала. |
Абомин, пепсидил |
|
Недостаточность желчеотделения |
Нерасщепленный жир, кристаллы жирных кислот.
|
Фестал, дигестал, желчегонные |
|
Панкреатическая недостаточность |
Обильный стул, большое количество нейтрального жира |
Панкреатин, панзинорм, холензим. |
|
Энтеритный синдром |
Мышечные волокна, крахмал, не переваренная клетчатка, слизь, йодофильная флора. |
Панзинорм, мезим-форте, панкурмен. |
3. Химическое исследование кала
•Реакция на скрытую кровь (р-ция Грегерсена). Определение скрытой крови в кале имеет важное диагностическое значение, особенно при так «скрытых» желудочно-кишечных кровотечениях, когда макроскопически кровь в каловых массах не определяется.
•Реакция на желчные пигменты (билирубин, стеркобилин). Стеркобилин является конечным продуктом восстановления билирубина, выделяющегося в кишечник из общего желчного протока, придает калу животных характерную коричневую окраску. Стеркобилин присутствует в норме (выделяется в зависимости от массы животного 20 – 350 мг/в сутки). Отсутствие или резкое уменьшение количества стеркобилина в кале (ахоличный кал) чаще всего свидетельствует об обтурации общего желчного протока камнем, сдавливании его опухолью или резком снижении функции печени (например при остром вирусном гепатите). Увеличение количества стеркобилина в кале возникает при массивном гемолизе эритроцитов или усиленном желчеотделении. Выявление в кале кошек и собак не измененного билирубина указывает на нарушение процесса восстановления билирубина в кишечнике под действием микробной флоры. Наиболее частыми причинами этого нарушения являются: подавление жизнедеятельности бактерий кишечника под влиянием больших доз антибиотиков (дисбактериоз кишечника), резкое усиление перистальтики кишечника.
•Реакция Трибуле — определение растворимого белка. В ходе пищеварения белки подвергаются расщеплению и всасыванию. Поэтому в кале здоровых людей растворимый белок, как правило, не встречается. Он появляется при воспалительных процессах или изъязвлениях в области тонкого и толстого кишечника.
Непереносимость белков — StatPearls — NCBI Bookshelf
Непрерывное обучение
Непереносимость белков — это расстройство, возникающее в результате неблагоприятного воздействия белков пищи. Это вызвано различными механизмами и обычно связано с симптомами, затрагивающими желудочно-кишечный тракт. В этом мероприятии рассматривается оценка и лечение непереносимости белка и подчеркивается роль межпрофессиональной команды в уходе за пациентами с этим заболеванием.
Цели:
Объясните патофизиологию непереносимости белка.
Опишите соответствующую оценку непереносимости белка.
Ознакомьтесь с общими вариантами ведения пациентов с непереносимостью белка.

Обобщить стратегии межпрофессиональной команды по улучшению координации помощи и коммуникации для улучшения ухода за пациентами с непереносимостью белка и улучшения результатов.
Получите доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Введение
Белковая непереносимость — это расстройство, возникающее в результате неблагоприятного воздействия приема пищевых белков. Он развивается за счет иммунологических, неиммунологических, метаболических, генетических и фармакологических механизмов. Это часто связано с желудочно-кишечными симптомами. При раннем выявлении состояния и вмешательстве расстройство в основном поддается лечению и имеет благоприятный прогноз.
Этиология
Непереносимость белка вызвана неспособностью переваривать или эффективно расщеплять аминокислоты. Когда пищевые белки плохо перевариваются, они могут действовать как антигены, что приводит к аллергии на пищевые белки. Чаще всего причиной пищевой непереносимости в младенчестве являются белки коровьего молока.[1] Синдром энтероколита, вызванный пищевыми белками, также обычно связывают с непереносимостью белков коровьего молока. У пораженных лиц наблюдаются диарея, отеки и гипоальбуминемия. С увеличением возраста и введением различных продуктов непереносимость яичного белка, аллергия на сою и арахис становятся более распространенными.[2]
Чаще всего причиной пищевой непереносимости в младенчестве являются белки коровьего молока.[1] Синдром энтероколита, вызванный пищевыми белками, также обычно связывают с непереносимостью белков коровьего молока. У пораженных лиц наблюдаются диарея, отеки и гипоальбуминемия. С увеличением возраста и введением различных продуктов непереносимость яичного белка, аллергия на сою и арахис становятся более распространенными.[2]
Непереносимость белка наблюдается при следующих состояниях:
Иммунологическая непереносимость пищевого белка: может быть IgE-опосредованной или не-IgE-опосредованной.
IgE mediated conditions include:
Cow’s milk allergy
Oral allergy syndrome
Immediate GI hypersensitivity
Eosinophilic esophagitis
Eosinophilic gastritis
Eosinophilic gastroenteritis
Условия, опосредованные не IGE, включают в себя:
, индуцированный пищевым белком энтероколит
Фудовый белок, индуцированный энтеропатией
ПЕРСОНАЛЬНЫЙ ПЕРСОВЛЕНИЕ АЛЕГИМИЧЕСКИЙ АВТОКОЛИТ
Фенилкетонурия (PKU)
Болезнь мочи кленового сиропа (MSUD)
Tyrosinememe
HomocyshystinuriraRENMERELENTIRELERENTIOLERENITELERELENTIONMIREL INLEAREL INLEAREL INLEAREL INLEARELERENCE
.Дневник питания: важно вести дневник питания, поскольку он помогает клиницистам сопоставить симптомы и выяснить взаимосвязь пищи с симптомы пациента.
Кожный прик-тест: Этот тест позволяет выявить IgE-опосредованную аллергию на пищевой белок. Хотя положительный результат теста может свидетельствовать о наличии антител IgE, он имеет низкую прогностическую ценность, в то время как отрицательный результат теста имеет высокую прогностическую точность.
Патч-тест на атопию: тест используется для выявления отсроченной непереносимости пищевых белков (клеточно-опосредованные реакции).
Анализ сывороточного специфического IgE: Его также проводят для выявления антигенспецифического IgE в сыворотке пациента.
Отказ от диеты: если есть подозрение на непереносимость пищевого белка или аллергию, пациенту следует соблюдать диету, свободную от подозреваемого белка, в течение 2–4 недель.
 Если симптомы улучшаются, в качестве диагностического теста может быть проведен тест на пероральную пищевую провокацию.
Если симптомы улучшаются, в качестве диагностического теста может быть проведен тест на пероральную пищевую провокацию.Оральный тест на пищевую провокацию: это тест золотого стандарта, который проводится под наблюдением врача для диагностики или исключения пищевой аллергии. Диагноз непереносимости пищевого белка может быть поставлен, когда симптомы исчезают после исключения из рациона соответствующего продукта, а затем симптомы возвращаются после введения того же продукта. Реакции и симптомы должны быть воспроизводимы при повторных тестах на исключение диеты и пищевых пробах. Некоторые реакции со стороны желудочно-кишечного тракта могут проявляться с отсроченным началом, вызывая появление симптомов через несколько часов или дней после приема внутрь.
Радиоаллергосорбентный тест (РАСТ): Этот тест выявляет аллерген-специфические антитела Ig-E с помощью радиоиммуноанализа. Он полезен для определения причин аллергии и часто дает положительный результат при гиперчувствительности немедленного желудочно-кишечного тракта.

Дифференциальный подсчет лейкоцитов: Этот тест подтверждает диагноз аллергического эозинофильного гастрита, аллергического эозинофильного гастроэнтерита и других аллергических состояний, когда наблюдается периферическая эозинофилия.
Анализ кала: Анализ кала может выявить скрытую кровь или фекальные лейкоциты и указать на наличие воспаления.
Биопсия: при аллергическом эозинофильном эзофагите, гастрите и гастроэнтерите биопсия показывает эозинофильную инфильтрацию слизистой и подслизистой оболочки. Биопсия тощей кишки при синдроме энтероколита и глютеновой болезни показывает атрофию ворсин и кишечную инфильтрацию лимфоцитами.
Кишечные инфекции: Кишечные инфекции могут также проявляться симптомами, сходными с непереносимостью белков, или предрасполагать к ним. Пациенты с кишечными инфекциями часто имеют признаки инфекции и могут лечиться противомикробными препаратами.
Целиакия: Целиакия является широко многофакторным заболеванием с сильным наследственным компонентом и ассоциацией с HLA (DQ2 и DQ8). Они могут проявляться аутоиммунной реакцией на глютеновый белок в пищевых продуктах. Тестирование на сывороточные антитела IgA к тканевой трансглютаминазе (анти-tTG IgA) может помочь в диагностике целиакии или исключить ее как причину непереносимости белка.

Гастроэзофагеальная рефлюксная болезнь (ГЭРБ): у детей наблюдаются такие симптомы, как нарушения сна, рвота, плохой аппетит, плохой рост, хрипы и стридор. Взрослые испытывают изжогу, рвоту и срыгивание. ГЭРБ можно лечить с помощью фармакотерапии и хирургического вмешательства или без них. Они не имеют отношения к тому или иному пищевому белку.
Воспалительные заболевания кишечника (ВЗК): они включают болезнь Крона и язвенный колит, которые могут проявляться обычными желудочно-кишечными симптомами, такими как диарея, ректальное кровотечение и боль в животе. Однако важно исключить ВЗК, поскольку они являются системными хроническими заболеваниями и требуют обширного лечения.
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
- 1.
Флом Д.Д., Зихерер С.Х. Эпидемиология аллергии на коровье молоко. Питательные вещества. 2019 May 10;11(5) [бесплатная статья PMC: PMC6566637] [PubMed: 31083388]
- 2.
Savage J, Johns CB. Пищевая аллергия: эпидемиология и естественное течение. Иммунол Аллергия Клин Норт Ам. 2015 фев; 35 (1): 45-59. [Бесплатная статья PMC: PMC4254585] [PubMed: 25459576]
- 3.
Ахонди Х., Росс А.Б. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 19 января., 2022. Медицинские проблемы, связанные с глютеном. [PubMed: 30860740]
- 4.
Untersmayr E.
 Влияние желудочного пищеварения на развитие пищевой аллергии. Преподобный отец Аллергол (2009). 2015 ноябрь;55(7):444-447. [Бесплатная статья PMC: PMC5467726] [PubMed: 28616101]
Влияние желудочного пищеварения на развитие пищевой аллергии. Преподобный отец Аллергол (2009). 2015 ноябрь;55(7):444-447. [Бесплатная статья PMC: PMC5467726] [PubMed: 28616101]- 5.
Lomer MC. Обзорная статья: этиология, диагностика, механизмы и клинические проявления пищевой непереносимости. Алимент Фармакол Тер. 2015 фев; 41 (3): 262-75. [В паблике: 25471897]
- 6.
Rona RJ, Keil T, Summers C, Gislason D, Zuidmeer L, Sodergren E, Sigurdardottir ST, Lindner T, Goldhahn K, Dahlstrom J, McBride D, Madsen C. Распространенность продуктов питания аллергия: метаанализ. J Аллергия Клин Иммунол. 2007 г., сен; 120 (3): 638-46. [PubMed: 17628647]
- 7.
Mehr S, Frith K, Campbell DE. Эпидемиология синдрома энтероколита, вызванного пищевыми белками. Курр Опин Аллергия Клин Иммунол. 2014 июнь;14(3):208-16. [Бесплатная статья PMC: PMC4011623] [PubMed: 24686277]
- 8.
Сингх П., Арора А., Стрэнд Т.
 А., Леффлер Д.А., Катасси С., Грин П.Х., Келли С.П., Ахуджа В., Махария Г.К. Глобальная распространенность глютеновой болезни: систематический обзор и метаанализ. Клин Гастроэнтерол Гепатол. 2018 июнь;16(6):823-836.e2. [PubMed: 29551598]
А., Леффлер Д.А., Катасси С., Грин П.Х., Келли С.П., Ахуджа В., Махария Г.К. Глобальная распространенность глютеновой болезни: систематический обзор и метаанализ. Клин Гастроэнтерол Гепатол. 2018 июнь;16(6):823-836.e2. [PubMed: 29551598]- 9.
Ивкович-Юрекович И. [Синдром оральной аллергии]. Acta Med Croatica. 2014 июнь; 68 (3): 283-7. [PubMed: 26016219]
- 10.
Roussel JM, Pandit S. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 14 августа 2021 г. Эозинофильный эзофагит. [В паблике: 29083829]
- 11.
Ingle SB, шарнир Ingle CR. Эозинофильный гастроэнтерит: необычный тип гастроэнтерита. Мир J Гастроэнтерол. 2013 21 августа; 19 (31): 5061-6. [Бесплатная статья PMC: PMC3746377] [PubMed: 23964139]
- 12.
Tarlow MJ, Hadorn B, Arthurton MW, Lloyd JK. Дефицит кишечной энтерокиназы. Недавно обнаруженное нарушение переваривания белков. Арч Дис Чайлд. 1970 окт; 45 (243): 651-5.
 [Бесплатная статья PMC: PMC1647492] [PubMed: 5477679]
[Бесплатная статья PMC: PMC1647492] [PubMed: 5477679]- 13.
Сатьянараяна Рао Т.С., Ерагани В.К. Гипертонический криз и сыр. Индийская психиатрия. 2009 Январь; 51 (1): 65-6. [Бесплатная статья PMC: PMC2738414] [PubMed: 19742203]
- 14.
Tabanelli G. Биогенные амины и качество продуктов питания: новые проблемы и проблемы общественного здравоохранения. Еда. 2020 Jul 01;9(7) [PMC бесплатная статья: PMC7404793] [PubMed: 32630178]
- 15.
Giannetti A, Cipriani F, Indio V, Gallucci M, Caffarelli C, Ricci G. Влияние атопического дерматита об аллергии на коровье молоко у детей. Медицина (Каунас). 201910 августа 55(8) [бесплатная статья PMC: PMC6723735] [PubMed: 31405131]
- 16.
Мураро А., Верфель Т., Хоффманн-Зоммергрубер К., Робертс Г., Бейер К., Биндслев-Дженсен К., Кардона В., Дюбуа А., Дютуа Г., Эйгенманн П., Фернандес Ривас М., Халкен С., Хикштейн Л., Хёст А., Кнол Э., Лак Г., Маркизотто М.
 Дж., Ниггеманн Б., Нвару Б.И., Пападопулос Н.Г., Поульсен Л.К., Сантос А.Ф., Скайпала И. , Шёпфер А., Ван Ри Р., Вентер С., Ворм М., Влиг-Бурстра Б., Панесар С., де Сильва Д., Соарес-Вайзер К., Шейх А., Балмер-Вебер Б.К., Нильссон С., де Йонг Н.В., Акдис К.А., Группа рекомендаций EAACI по пищевой аллергии и анафилаксии. Рекомендации EAACI по пищевой аллергии и анафилаксии: диагностика и лечение пищевой аллергии. Аллергия. 2014 авг; 69(8):1008-25. [PubMed: 24909706]
Дж., Ниггеманн Б., Нвару Б.И., Пападопулос Н.Г., Поульсен Л.К., Сантос А.Ф., Скайпала И. , Шёпфер А., Ван Ри Р., Вентер С., Ворм М., Влиг-Бурстра Б., Панесар С., де Сильва Д., Соарес-Вайзер К., Шейх А., Балмер-Вебер Б.К., Нильссон С., де Йонг Н.В., Акдис К.А., Группа рекомендаций EAACI по пищевой аллергии и анафилаксии. Рекомендации EAACI по пищевой аллергии и анафилаксии: диагностика и лечение пищевой аллергии. Аллергия. 2014 авг; 69(8):1008-25. [PubMed: 24909706]- 17.
Гонсалвес Н. Эозинофильные желудочно-кишечные расстройства. Клин Рев Аллергия Иммунол. 2019 окт;57(2):272-285. [PubMed: 30
- 9]
- 18.
Урасима М., Мезава Х., Окуяма М., Урасима Т., Хирано Д., Гочо Н., Татимото Х. Первичная профилактика сенсибилизации коровьего молока и пищевой аллергии путем отказа от добавок с коровьим молоком при рождении: рандомизированное клиническое исследование. JAMA Педиатр. 01 декабря 2019 г.; 173(12):1137-1145. [Бесплатная статья PMC: PMC6806425] [PubMed: 31633778]
- 19.

Nowak-Wegrzyn A, Czerkies L, Reyes K, Collins B, Heine RG. Подтверждена гипоаллергенность новой интенсивно гидролизованной детской смеси на основе молочной сыворотки, содержащей два олигосахарида грудного молока. Питательные вещества. 2019 Jun 26;11(7) [PMC бесплатная статья: PMC6682865] [PubMed: 31248026]
Объясните патофизиологию непереносимости белка.
Опишите соответствующую оценку непереносимости белка.
Ознакомьтесь с общими вариантами ведения пациентов с непереносимостью белка.

Обобщить стратегии межпрофессиональной команды по улучшению координации помощи и коммуникации для улучшения ухода за пациентами с непереносимостью белка и улучшения результатов.
Cow’s milk allergy
Oral allergy syndrome
Immediate GI hypersensitivity
Eosinophilic esophagitis
Eosinophilic gastritis
Eosinophilic gastroenteritis
, индуцированный пищевым белком энтероколит
Фудовый белок, индуцированный энтеропатией
ПЕРСОНАЛЬНЫЙ ПЕРСОВЛЕНИЕ АЛЕГИМИЧЕСКИЙ АВТОКОЛИТ
Фенилкетонурия (PKU)
Болезнь мочи кленового сиропа (MSUD)
Tyrosinememe
HomocyshystinuriraRENMERELENTIRELERENTIOLERENITELERELENTIONMIREL INLEAREL INLEAREL INLEAREL INLEARELERENCE
.Дневник питания: важно вести дневник питания, поскольку он помогает клиницистам сопоставить симптомы и выяснить взаимосвязь пищи с симптомы пациента.
Кожный прик-тест: Этот тест позволяет выявить IgE-опосредованную аллергию на пищевой белок. Хотя положительный результат теста может свидетельствовать о наличии антител IgE, он имеет низкую прогностическую ценность, в то время как отрицательный результат теста имеет высокую прогностическую точность.
Патч-тест на атопию: тест используется для выявления отсроченной непереносимости пищевых белков (клеточно-опосредованные реакции).
Анализ сывороточного специфического IgE: Его также проводят для выявления антигенспецифического IgE в сыворотке пациента.
Отказ от диеты: если есть подозрение на непереносимость пищевого белка или аллергию, пациенту следует соблюдать диету, свободную от подозреваемого белка, в течение 2–4 недель.
 Если симптомы улучшаются, в качестве диагностического теста может быть проведен тест на пероральную пищевую провокацию.
Если симптомы улучшаются, в качестве диагностического теста может быть проведен тест на пероральную пищевую провокацию.Оральный тест на пищевую провокацию: это тест золотого стандарта, который проводится под наблюдением врача для диагностики или исключения пищевой аллергии. Диагноз непереносимости пищевого белка может быть поставлен, когда симптомы исчезают после исключения из рациона соответствующего продукта, а затем симптомы возвращаются после введения того же продукта. Реакции и симптомы должны быть воспроизводимы при повторных тестах на исключение диеты и пищевых пробах. Некоторые реакции со стороны желудочно-кишечного тракта могут проявляться с отсроченным началом, вызывая появление симптомов через несколько часов или дней после приема внутрь.
Радиоаллергосорбентный тест (РАСТ): Этот тест выявляет аллерген-специфические антитела Ig-E с помощью радиоиммуноанализа. Он полезен для определения причин аллергии и часто дает положительный результат при гиперчувствительности немедленного желудочно-кишечного тракта.

Дифференциальный подсчет лейкоцитов: Этот тест подтверждает диагноз аллергического эозинофильного гастрита, аллергического эозинофильного гастроэнтерита и других аллергических состояний, когда наблюдается периферическая эозинофилия.
Анализ кала: Анализ кала может выявить скрытую кровь или фекальные лейкоциты и указать на наличие воспаления.
Биопсия: при аллергическом эозинофильном эзофагите, гастрите и гастроэнтерите биопсия показывает эозинофильную инфильтрацию слизистой и подслизистой оболочки. Биопсия тощей кишки при синдроме энтероколита и глютеновой болезни показывает атрофию ворсин и кишечную инфильтрацию лимфоцитами.
Кишечные инфекции: Кишечные инфекции могут также проявляться симптомами, сходными с непереносимостью белков, или предрасполагать к ним. Пациенты с кишечными инфекциями часто имеют признаки инфекции и могут лечиться противомикробными препаратами.
Целиакия: Целиакия является широко многофакторным заболеванием с сильным наследственным компонентом и ассоциацией с HLA (DQ2 и DQ8). Они могут проявляться аутоиммунной реакцией на глютеновый белок в пищевых продуктах. Тестирование на сывороточные антитела IgA к тканевой трансглютаминазе (анти-tTG IgA) может помочь в диагностике целиакии или исключить ее как причину непереносимости белка.

Гастроэзофагеальная рефлюксная болезнь (ГЭРБ): у детей наблюдаются такие симптомы, как нарушения сна, рвота, плохой аппетит, плохой рост, хрипы и стридор. Взрослые испытывают изжогу, рвоту и срыгивание. ГЭРБ можно лечить с помощью фармакотерапии и хирургического вмешательства или без них. Они не имеют отношения к тому или иному пищевому белку.
Воспалительные заболевания кишечника (ВЗК): они включают болезнь Крона и язвенный колит, которые могут проявляться обычными желудочно-кишечными симптомами, такими как диарея, ректальное кровотечение и боль в животе. Однако важно исключить ВЗК, поскольку они являются системными хроническими заболеваниями и требуют обширного лечения.
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
- 1.
Флом Д.Д., Зихерер С.Х. Эпидемиология аллергии на коровье молоко. Питательные вещества. 2019 May 10;11(5) [бесплатная статья PMC: PMC6566637] [PubMed: 31083388]
- 2.
Savage J, Johns CB. Пищевая аллергия: эпидемиология и естественное течение. Иммунол Аллергия Клин Норт Ам. 2015 фев; 35 (1): 45-59. [Бесплатная статья PMC: PMC4254585] [PubMed: 25459576]
- 3.
Ахонди Х., Росс А.Б. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 19 января., 2022. Медицинские проблемы, связанные с глютеном. [PubMed: 30860740]
- 4.
Untersmayr E.
 Влияние желудочного пищеварения на развитие пищевой аллергии. Преподобный отец Аллергол (2009). 2015 ноябрь;55(7):444-447. [Бесплатная статья PMC: PMC5467726] [PubMed: 28616101]
Влияние желудочного пищеварения на развитие пищевой аллергии. Преподобный отец Аллергол (2009). 2015 ноябрь;55(7):444-447. [Бесплатная статья PMC: PMC5467726] [PubMed: 28616101]- 5.
Lomer MC. Обзорная статья: этиология, диагностика, механизмы и клинические проявления пищевой непереносимости. Алимент Фармакол Тер. 2015 фев; 41 (3): 262-75. [В паблике: 25471897]
- 6.
Rona RJ, Keil T, Summers C, Gislason D, Zuidmeer L, Sodergren E, Sigurdardottir ST, Lindner T, Goldhahn K, Dahlstrom J, McBride D, Madsen C. Распространенность продуктов питания аллергия: метаанализ. J Аллергия Клин Иммунол. 2007 г., сен; 120 (3): 638-46. [PubMed: 17628647]
- 7.
Mehr S, Frith K, Campbell DE. Эпидемиология синдрома энтероколита, вызванного пищевыми белками. Курр Опин Аллергия Клин Иммунол. 2014 июнь;14(3):208-16. [Бесплатная статья PMC: PMC4011623] [PubMed: 24686277]
- 8.
Сингх П., Арора А., Стрэнд Т.
 А., Леффлер Д.А., Катасси С., Грин П.Х., Келли С.П., Ахуджа В., Махария Г.К. Глобальная распространенность глютеновой болезни: систематический обзор и метаанализ. Клин Гастроэнтерол Гепатол. 2018 июнь;16(6):823-836.e2. [PubMed: 29551598]
А., Леффлер Д.А., Катасси С., Грин П.Х., Келли С.П., Ахуджа В., Махария Г.К. Глобальная распространенность глютеновой болезни: систематический обзор и метаанализ. Клин Гастроэнтерол Гепатол. 2018 июнь;16(6):823-836.e2. [PubMed: 29551598]- 9.
Ивкович-Юрекович И. [Синдром оральной аллергии]. Acta Med Croatica. 2014 июнь; 68 (3): 283-7. [PubMed: 26016219]
- 10.
Roussel JM, Pandit S. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 14 августа 2021 г. Эозинофильный эзофагит. [В паблике: 29083829]
- 11.
Ingle SB, шарнир Ingle CR. Эозинофильный гастроэнтерит: необычный тип гастроэнтерита. Мир J Гастроэнтерол. 2013 21 августа; 19 (31): 5061-6. [Бесплатная статья PMC: PMC3746377] [PubMed: 23964139]
- 12.
Tarlow MJ, Hadorn B, Arthurton MW, Lloyd JK. Дефицит кишечной энтерокиназы. Недавно обнаруженное нарушение переваривания белков. Арч Дис Чайлд. 1970 окт; 45 (243): 651-5.
 [Бесплатная статья PMC: PMC1647492] [PubMed: 5477679]
[Бесплатная статья PMC: PMC1647492] [PubMed: 5477679]- 13.
Сатьянараяна Рао Т.С., Ерагани В.К. Гипертонический криз и сыр. Индийская психиатрия. 2009 Январь; 51 (1): 65-6. [Бесплатная статья PMC: PMC2738414] [PubMed: 19742203]
- 14.
Tabanelli G. Биогенные амины и качество продуктов питания: новые проблемы и проблемы общественного здравоохранения. Еда. 2020 Jul 01;9(7) [PMC бесплатная статья: PMC7404793] [PubMed: 32630178]
- 15.
Giannetti A, Cipriani F, Indio V, Gallucci M, Caffarelli C, Ricci G. Влияние атопического дерматита об аллергии на коровье молоко у детей. Медицина (Каунас). 201910 августа 55(8) [бесплатная статья PMC: PMC6723735] [PubMed: 31405131]
- 16.
Мураро А., Верфель Т., Хоффманн-Зоммергрубер К., Робертс Г., Бейер К., Биндслев-Дженсен К., Кардона В., Дюбуа А., Дютуа Г., Эйгенманн П., Фернандес Ривас М., Халкен С., Хикштейн Л., Хёст А., Кнол Э., Лак Г., Маркизотто М.

9644. Реакционно-индуцированный Аутоколит
Реакционно-индуцированный Аутоколит
9.
4.-Индуцированный Аутоколит. белки обнаруживаются при целиакии, чувствительности к глютену, не связанной с целиакией, аллергии на пшеницу, глютеновой атаксии и герпетиформном дерматите.
Дефицит фермента: дефицит энтерокиназы (энтеропептидазы)
Метаболические расстройства:
Фармакологические: Хроническое применение препаратов для подавления выработки желудочного сока[4]
Токсические реакции на биогенные амины:
Не определено: Синдром раздраженного кишечника
Эпидемиология
Пищевая непереносимость встречается у 15-20% населения.[5] Аллергия на коровье молоко (CMA), реакция на белки в коровьем молоке, является наиболее распространенной пищевой аллергией в раннем возрасте с предполагаемым диапазоном распространенности от 0,5% до 3% в возрасте 1 года. [1][2][6]. ] Однако, судя по естественному течению CMA, его разрешение является распространенным явлением, и ожидается, что его распространенность будет ниже у взрослых.
[1][2][6]. ] Однако, судя по естественному течению CMA, его разрешение является распространенным явлением, и ожидается, что его распространенность будет ниже у взрослых.
В австралийском исследовании у одного из 10 000 младенцев в возрасте до 2 лет был обнаружен синдром энтероколита, вызванного пищевыми белками (FPIES). Обнаружено, что FPIES встречается преимущественно у младенцев и связан с обычными пищевыми триггерами (белки в коровьем молоке, соя, рис, овес и яйца), но эпидемиологические данные все еще отсутствуют [7].
Целиакия считается серьезной проблемой общественного здравоохранения, и о ней сообщают во всем мире. Он наиболее распространен в Западной Европе и Соединенных Штатах, но у большинства больных он не диагностируется. Метаанализ, проведенный в 2018 году, показал, что распространенность целиакии составляет 1,4% на основе серологических тестов и 0,7% на основе биопсии.[8]
Хотя предрасположенность к половому признаку неизвестна, FPIES и эозинофильный гастроэнтерит имеют незначительное преобладание у мужчин, в то время как женщины несколько чаще страдают глютеновой болезнью.
Патофизиология
Макромолекулы пищевого белка состоят из последовательностей аминокислот, связанных пептидными связями. Эти связи должны быть гидролизованы и подвергнуты ферментативному воздействию до того, как будут абсорбированы свободные аминокислоты. Процесс переваривания белков начинается в желудке пепсинами с помощью соляной (HCl) кислоты. Затем этот частично переваренный белок достигает двенадцатиперстной кишки, где высокий рН останавливает пептическую активность, а ферменты поджелудочной железы (трипсин, химотрипсин, карбоксипептидазы) берут на себя процесс пищеварения. Небольшие цепочки аминокислот, образующиеся в просвете, теперь подвергаются мембранному перевариванию на щеточной кайме энтероцитов. Мембранные экзопептидазы гидролизуют цепи аминокислот с образованием отдельных аминокислот, которые всасываются в энтероциты и попадают в кровоток для использования в организме.
Непереносимость белка может возникать из-за любых отклонений в процессах пищеварения или метаболизма. Когда пищевые белки не полностью денатурируются желудочной кислотой, это приводит к сенсибилизации белка в кишечнике, что приводит к пищевой аллергии. Гипоацидные состояния, наблюдаемые у пациентов, длительно лечившихся от диспепсических расстройств, часто приводят к развитию аллергии на пищевые белки.[4]
Когда пищевые белки не полностью денатурируются желудочной кислотой, это приводит к сенсибилизации белка в кишечнике, что приводит к пищевой аллергии. Гипоацидные состояния, наблюдаемые у пациентов, длительно лечившихся от диспепсических расстройств, часто приводят к развитию аллергии на пищевые белки.[4]
Анамнез и физикальное исследование
Клинические проявления непереносимости пищевого белка затрагивают различные системы органов и варьируют в зависимости от различных заболеваний. Тем не менее, у пациентов в основном проявляются желудочно-кишечные проявления. При неиммунологической непереносимости пищевого белка количество потребляемой пищи, как правило, более непосредственно связано с тяжестью симптомов. Чрезмерное газообразование в кишечнике, вздутие живота, боль в животе и диарея являются распространенными симптомами. Принимая во внимание, что при иммунологической аллергии на пищевой белок даже следовые количества сенсибилизированного пищевого белка могут вызвать взрывную реакцию и могут поразить кожу и кровеносные сосуды. IgE-опосредованные реакции возникают в течение от нескольких минут до часа после приема пищевого белка, и симптомы варьируют от кожной сыпи, крапивницы, ангионевротического отека, свистящего дыхания до анафилаксии, тогда как не-IgE-опосредованные реакции могут развиваться в течение от нескольких часов до нескольких дней.
IgE-опосредованные реакции возникают в течение от нескольких минут до часа после приема пищевого белка, и симптомы варьируют от кожной сыпи, крапивницы, ангионевротического отека, свистящего дыхания до анафилаксии, тогда как не-IgE-опосредованные реакции могут развиваться в течение от нескольких часов до нескольких дней.
Типичным проявлением у младенцев может быть диарея у младенцев в возрасте до 6 месяцев и со временем рвота после кормления молочной смесью в течение нескольких недель. Синдром пищевого проктоколита является распространенным состоянием, при котором у здоровых младенцев возникает диарея, но вес не снижается. Принимая во внимание, что в случае FPIES младенец может обезвоживаться и терять вес.
Вот некоторые из симптомов и физических признаков, наблюдаемых при различных нарушениях непереносимости белка:
Синдром оральной аллергии: Реакция в основном возникает из-за перекрестной реактивности между пыльцой и пищей растительного происхождения (фруктами и овощами), а симптомы локализуются на слизистой оболочке полости рта.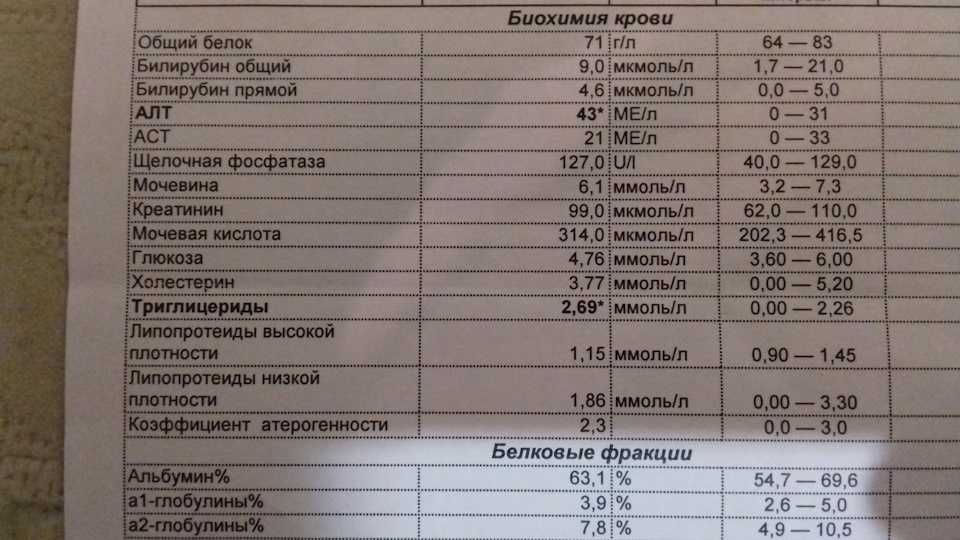 [9] Симптомы включают зуд и жжение в области губ, языка, неба и горла. Возможны ангионевротический отек и рвота.
[9] Симптомы включают зуд и жжение в области губ, языка, неба и горла. Возможны ангионевротический отек и рвота.
Немедленная гиперчувствительность ЖКТ: у пациентов появляются тошнота, боль в животе и рвота в течение 1–2 часов после приема сенсибилизированного пищевого белка, часто с последующей диареей. Пораженные люди имеют периодические боли в животе, плохой аппетит и плохую прибавку в весе.
Эозинофильный эзофагит (ЭоЭ): у пациентов возникают затруднения при глотании, застревание твердой пищи, боли в животе, регургитация или рвота и снижение аппетита. У детей младшего возраста могут возникнуть трудности с кормлением и плохая прибавка в весе. Симптомы часто совпадают, и их часто путают с гастроэзофагеальной рефлюксной болезнью (ГЭРБ). Однако у пациентов с ЭоЭ часто обнаруживают в анамнезе и другие аутоиммунные и аллергические состояния.[10]
Эозинофильный гастрит: они обычно проявляются признаками гастрита, такими как боль в животе, постпрандиальная рвота, раннее насыщение, анорексия и задержка развития. Заболевание очень чувствительно к диетическим ограничениям у детей. Примерно 50% этих пациентов также имеют признаки атопии.
Заболевание очень чувствительно к диетическим ограничениям у детей. Примерно 50% этих пациентов также имеют признаки атопии.
Эозинофильный гастроэнтерит: это редкое заболевание с хроническим рецидивирующим течением, характеризующееся инфильтрацией эозинофилов в слизистую оболочку желудочно-кишечного тракта. Презентация может быть разной. У детей могут наблюдаться задержка развития, задержка роста, задержка полового созревания или аменорея. Часто у взрослых возникают боли в животе, дисфагия или диарея. У них также могут быть признаки энтеропатии с потерей белка, желудочно-кишечного кровотечения или мальабсорбции.[11]
Синдром энтероколита, вызванного пищевыми белками (FPIES): у пациентов может наблюдаться рвота через один-три часа после кормления. У них также может быть вздутие живота, кровавый понос, анемия и потеря веса, и обычно они провоцируются смесями на основе коровьего молока или соевого белка. При физическом осмотре могут быть очевидны признаки обезвоживания. Отсутствуют респираторные симптомы или классические IgE-опосредованные аллергические кожные реакции.
Энтеропатия, вызванная пищевым белком: Пациенты с энтеропатией, вызванной пищевым белком, имеют стеаторею и задержку развития в первые несколько месяцев жизни.
Аллергический проктоколит, вызванный пищевым белком: обычно наблюдается у здоровых младенцев, находящихся на грудном вскармливании. У них появляются симптомы стула с прожилками крови в первые несколько месяцев жизни.
Целиакия: у пациентов с целиакией обычно наблюдаются диарея, дурно пахнущий стул, стеаторея, урчание в носу, метеоризм и потеря веса. Больные жалуются на слабость и быструю утомляемость, обычно связанные с неправильным питанием. Могут быть очевидны признаки анемии. Может отмечаться герпетиформный дерматит, зудящая папуловезикулярная сыпь на разгибательных поверхностях конечностей, туловище и ягодицах.
Дефицит энтерокиназы: У младенцев с дефицитом этого фермента с рождения развивается диарея, и они плохо развиваются. При хронической мальабсорбции белка склонны к развитию гипопротеинемических отеков. Пероральное введение экстракта поджелудочной железы приводит к быстрому контролю симптомов и способствует ускорению роста.[12]
Пероральное введение экстракта поджелудочной железы приводит к быстрому контролю симптомов и способствует ускорению роста.[12]
Врожденные нарушения обмена веществ: Эти нарушения приводят к накоплению метаболитов перед дефектным ферментом (аминокислоты и/или аммиак), вызывая интоксикацию. Симптомы варьируются в зависимости от пораженных ферментов.
Токсические реакции на биогенные амины: Проглатывание некоторых биогенных аминов способствует развитию токсических реакций. Пациенты могут жаловаться на головную боль, сердцебиение, рвоту, диарею и аллергию. Установлено, что употребление выдержанного сыра, содержащего тирамин, в сочетании с применением ингибиторов моноаминоксидазы (ИМАО) вызывает головные боли и гипертонический криз.[13] Гистамин более токсичен и может вызывать такие эффекты, как гипотензия, раздражение кожи, головная боль, сердцебиение, приступы астмы и т. д. Эта симптоматика известна как «отравление скомброидной рыбой», которое наблюдается после употребления рыбы из Scombridae и Scomberesocidae семейств (тунец, скумбрия, пеламида, луфарь и т. д.), содержащие высокие уровни гистамина.[14]
д.), содержащие высокие уровни гистамина.[14]
Дерматологические проявления:
Белковая непереносимость часто связана с дерматологическими атопическими состояниями. Исследование, проведенное в Италии, показало, что 71% детей с сопутствующей аллергией на коровье молоко имеют сопутствующий атопический дерматит.[15] Другие дерматологические симптомы включают крапивницу, сыпь и ангионевротический отек.
Оценка
Не существует какого-либо конкретного теста для диагностики непереносимости пищевого белка. Состояние оценивается в первую очередь на основе подробного анамнеза и физического осмотра. Клиницисты должны распознавать и дифференцировать иммунологическую непереносимость пищевого белка от неиммунологической, чтобы предотвратить симптомы и управлять ими. При IgE-опосредованной пищевой аллергии обычно очевидны положительные кожные прик-тесты на пищевые белки наряду с обнаружением специфических пищевых IgE-антител. Однако в большинстве случаев непереносимость пищевых белков не опосредована IgE.
При подозрении на непереносимость пищевого белка в диагностике помогают следующие меры и тесты:
Лечение/управление
Единственным окончательным методом лечения непереносимости пищевого белка является строгое исключение пищевого белка из рациона. Пациентов следует консультировать по вопросам контроля за составом пищевых продуктов и соблюдения элиминационной диеты. Пациенты, находящиеся на долгосрочной элиминационной диете, также должны иметь доступ к соответствующим диетическим консультациям, в идеале диетологом или диетологом, и к регулярному мониторингу роста, особенно у детей.
Матерям, находящимся на грудном вскармливании, следует рекомендовать избегать коровьего молока и молочных продуктов. В качестве средства выбора для лечения аллергии на коровье молоко, особенно у младенцев и детей младшего возраста, не находящихся на грудном вскармливании, следует рекомендовать интенсивно гидролизованную смесь с подтвержденной гипоаллергенностью. Для пациентов с более тяжелыми симптомами также могут быть рекомендованы формулы аминокислот.[16]
Стероиды являются основным средством лечения IgE-опосредованной иммунологической непереносимости пищевых белков, включая эозинофильные желудочно-кишечные расстройства.[17]
Новорожденных с острым FPIES с легкими симптомами (без вялости, бледности или апатии) можно лечить дома с помощью пероральной регидратации. Но при тяжелых симптомах их необходимо лечить в медицинском учреждении с помощью внутривенных вливаний. Внутримышечный адреналин и антигистаминные препараты не играют никакой роли в лечении реакций FPIES.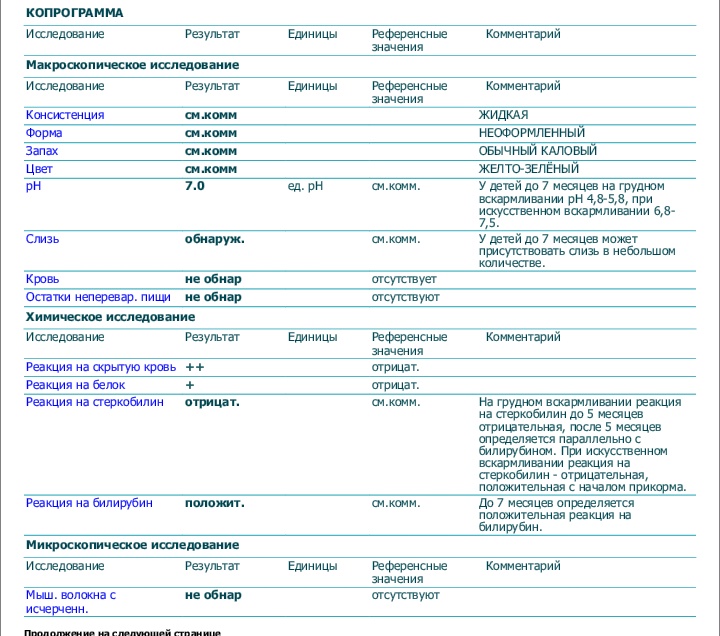
При подозрении на острые аллергические реакции или анафилаксию следует немедленно отказаться от вероятного продукта питания и оказать неотложную медицинскую помощь. Им могут выписать рецепт на автоинъекционное устройство с адреналином и проинструктировать, как им правильно пользоваться.
Дифференциальный диагноз
Некоторые распространенные дифференциальные диагнозы при непереносимости пищевого белка обсуждаются ниже:
Прогноз
Прогноз при многих случаях непереносимости белков благоприятный при соблюдении строгой диеты. Многие исследования показали, что прогноз при непереносимости белка коровьего молока благоприятен: у большинства пациентов аллергия перерастает в детстве и раннем подростковом возрасте. [2] Однако у некоторых детей с IgE-опосредованной непереносимостью белков развиваются аллергический риноконъюнктивит и астма.
[2] Однако у некоторых детей с IgE-опосредованной непереносимостью белков развиваются аллергический риноконъюнктивит и астма.
Осложнения
Белок является важным питательным веществом для здоровья и развития нашего организма. Общие осложнения непереносимости белка, приводящие к дефициту белка, включают потерю мышечной массы, задержку роста, задержку развития и ослабление иммунной системы. У пострадавших людей могут быть такие симптомы, как отеки ног, лица и других частей тела, сухие и ломкие волосы, усталость и частые инфекции.
У взрослых аллергические реакции на белки коровьего молока часто осложняются непереносимостью лактозы, которая усиливается с возрастом. IgE-опосредованные аллергические состояния могут вызывать анафилактические реакции и ангионевротический отек, которые без лечения могут быть опасными для жизни. Диарея и рвота, связанные с FPIES и эозинофильным гастроэнтеритом, могут привести к осложнениям, включая тяжелое обезвоживание и гиповолемический шок.
Сдерживание и просвещение пациентов
У здоровых младенцев рекомендуется обеспечить исключительно грудное вскармливание до 6 месяцев грудного возраста и постепенное введение твердой пищи после 6 месяцев, чтобы предотвратить пищевую аллергию или непереносимость. Младенцы с аллергией на коровье молоко должны избегать молочных смесей и должны находиться на грудном вскармливании. Кормящим матерям желательно исключить из рациона молочные продукты. Если пострадавший младенец не находится на грудном вскармливании, может быть назначена интенсивно гидролизованная смесь. Медицинские работники должны информировать пациентов о важности отмены диеты при подозрении на непереносимость белка или аллергию. Пациентам следует обратить внимание на подозреваемый ингредиент в пищевых продуктах. Пациенты, находящиеся на элиминационной диете, также должны получать соответствующие рекомендации от диетолога или нутрициолога. Пациентам с острыми реакциями гиперчувствительности на пищевые белки в анамнезе следует назначать шприц-ручки с адреналином.
Улучшение результатов работы команды здравоохранения
Белковая непереносимость — это расстройство, которое требует подхода межпрофессиональной команды как для диагностики, так и для лечения. От сбора анамнеза, проведения исследований до постановки правильного диагноза от медицинских работников требуются хорошие коммуникативные и диагностические навыки. Соблюдение со стороны пациента не менее важно в лечении этого состояния. Поскольку отказ от диеты остается основным методом лечения непереносимости белка, необходимо уделять большое внимание регулярным консультациям с диетологом или нутрициологом. Управление индивидуально для каждого пациента. У пациентов, у которых развиваются острые реакции (например, реакции гиперчувствительности при состояниях, опосредованных IgE, тяжелое обезвоживание или шок при FPIES), медсестры и фельдшеры играют жизненно важную роль в межпрофессиональной группе, поскольку они будут контролировать жизненные показатели пациента, вводить жидкости и лекарства, и помочь с образованием пациента и его семьи.
Аллергологи также играют важную роль в диагностике непереносимости белка, поскольку расстройство часто связано с сенсибилизацией к пищевым белкам. Часто родители или опекуны педиатрических пациентов или сами взрослые пациенты с хронической или тяжелой непереносимостью белка испытывают значительное бремя, тревогу, беспокойство и стресс, о которых следует заботиться с помощью консультантов, психологов или психиатров, когда это необходимо.
Прогноз при непереносимости белка благоприятный. Надлежащая идентификация возбудителя и его избегание помогает контролировать расстройство. Недавние данные свидетельствуют о том, что сенсибилизацию к коровьему молоку, ведущую к непереносимости и аллергии, можно в первую очередь предотвратить, избегая добавления смесей на основе коровьего молока в течение как минимум первых 3 дней жизни.[18] [Уровень 1] Исследование, проведенное в 2019 годутакже успешно продемонстрировала гипоаллергенность новой смеси на основе сыворотки с широким гидролизом, которая содержит два олигосахарида грудного молока. [19] [Уровень 1] Различные текущие исследования добавили новые аспекты в профилактику и лечение непереносимости пищевого белка.
[19] [Уровень 1] Различные текущие исследования добавили новые аспекты в профилактику и лечение непереносимости пищевого белка.
Контрольные вопросы
Каталожные номера
Непереносимость белков — StatPearls — NCBI Bookshelf
Непрерывное обучение
Непереносимость белков является неблагоприятным результатом непереносимости белков влияние приема пищевых белков. Это вызвано различными механизмами и обычно связано с симптомами, затрагивающими желудочно-кишечный тракт. В этом мероприятии рассматривается оценка и лечение непереносимости белка и подчеркивается роль межпрофессиональной команды в уходе за пациентами с этим заболеванием.
Цели:
Получите доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Введение
Белковая непереносимость — это расстройство, возникающее в результате неблагоприятного воздействия приема пищевых белков. Он развивается за счет иммунологических, неиммунологических, метаболических, генетических и фармакологических механизмов. Это часто связано с желудочно-кишечными симптомами. При раннем выявлении состояния и вмешательстве расстройство в основном поддается лечению и имеет благоприятный прогноз.
Этиология
Непереносимость белка вызвана неспособностью переваривать или эффективно расщеплять аминокислоты. Когда пищевые белки плохо перевариваются, они могут действовать как антигены, что приводит к аллергии на пищевые белки. Чаще всего причиной пищевой непереносимости в младенчестве являются белки коровьего молока.[1] Синдром энтероколита, вызванный пищевыми белками, также обычно связывают с непереносимостью белков коровьего молока. У пораженных лиц наблюдаются диарея, отеки и гипоальбуминемия. С увеличением возраста и введением различных продуктов непереносимость яичного белка, аллергия на сою и арахис становятся более распространенными.[2]
Чаще всего причиной пищевой непереносимости в младенчестве являются белки коровьего молока.[1] Синдром энтероколита, вызванный пищевыми белками, также обычно связывают с непереносимостью белков коровьего молока. У пораженных лиц наблюдаются диарея, отеки и гипоальбуминемия. С увеличением возраста и введением различных продуктов непереносимость яичного белка, аллергия на сою и арахис становятся более распространенными.[2]
Непереносимость белка наблюдается при следующих состояниях:
Иммунологическая непереносимость пищевого белка: может быть IgE-опосредованной или не-IgE-опосредованной.
IgE mediated conditions include:
Условия, опосредованные не IGE, включают в себя:
9644. Реакционно-индуцированный Аутоколит
Реакционно-индуцированный Аутоколит
9.
4.-Индуцированный Аутоколит. белки обнаруживаются при целиакии, чувствительности к глютену, не связанной с целиакией, аллергии на пшеницу, глютеновой атаксии и герпетиформном дерматите.
Дефицит фермента: дефицит энтерокиназы (энтеропептидазы)
Метаболические расстройства:
Фармакологические: Хроническое применение препаратов для подавления выработки желудочного сока[4]
Токсические реакции на биогенные амины:
Не определено: Синдром раздраженного кишечника
Эпидемиология
Пищевая непереносимость встречается у 15-20% населения.[5] Аллергия на коровье молоко (CMA), реакция на белки в коровьем молоке, является наиболее распространенной пищевой аллергией в раннем возрасте с предполагаемым диапазоном распространенности от 0,5% до 3% в возрасте 1 года. [1][2][6]. ] Однако, судя по естественному течению CMA, его разрешение является распространенным явлением, и ожидается, что его распространенность будет ниже у взрослых.
[1][2][6]. ] Однако, судя по естественному течению CMA, его разрешение является распространенным явлением, и ожидается, что его распространенность будет ниже у взрослых.
В австралийском исследовании у одного из 10 000 младенцев в возрасте до 2 лет был обнаружен синдром энтероколита, вызванного пищевыми белками (FPIES). Обнаружено, что FPIES встречается преимущественно у младенцев и связан с обычными пищевыми триггерами (белки в коровьем молоке, соя, рис, овес и яйца), но эпидемиологические данные все еще отсутствуют [7].
Целиакия считается серьезной проблемой общественного здравоохранения, и о ней сообщают во всем мире. Он наиболее распространен в Западной Европе и Соединенных Штатах, но у большинства больных он не диагностируется. Метаанализ, проведенный в 2018 году, показал, что распространенность целиакии составляет 1,4% на основе серологических тестов и 0,7% на основе биопсии.[8]
Хотя предрасположенность к половому признаку неизвестна, FPIES и эозинофильный гастроэнтерит имеют незначительное преобладание у мужчин, в то время как женщины несколько чаще страдают глютеновой болезнью.
Патофизиология
Макромолекулы пищевого белка состоят из последовательностей аминокислот, связанных пептидными связями. Эти связи должны быть гидролизованы и подвергнуты ферментативному воздействию до того, как будут абсорбированы свободные аминокислоты. Процесс переваривания белков начинается в желудке пепсинами с помощью соляной (HCl) кислоты. Затем этот частично переваренный белок достигает двенадцатиперстной кишки, где высокий рН останавливает пептическую активность, а ферменты поджелудочной железы (трипсин, химотрипсин, карбоксипептидазы) берут на себя процесс пищеварения. Небольшие цепочки аминокислот, образующиеся в просвете, теперь подвергаются мембранному перевариванию на щеточной кайме энтероцитов. Мембранные экзопептидазы гидролизуют цепи аминокислот с образованием отдельных аминокислот, которые всасываются в энтероциты и попадают в кровоток для использования в организме.
Непереносимость белка может возникать из-за любых отклонений в процессах пищеварения или метаболизма. Когда пищевые белки не полностью денатурируются желудочной кислотой, это приводит к сенсибилизации белка в кишечнике, что приводит к пищевой аллергии. Гипоацидные состояния, наблюдаемые у пациентов, длительно лечившихся от диспепсических расстройств, часто приводят к развитию аллергии на пищевые белки.[4]
Когда пищевые белки не полностью денатурируются желудочной кислотой, это приводит к сенсибилизации белка в кишечнике, что приводит к пищевой аллергии. Гипоацидные состояния, наблюдаемые у пациентов, длительно лечившихся от диспепсических расстройств, часто приводят к развитию аллергии на пищевые белки.[4]
Анамнез и физикальное исследование
Клинические проявления непереносимости пищевого белка затрагивают различные системы органов и варьируют в зависимости от различных заболеваний. Тем не менее, у пациентов в основном проявляются желудочно-кишечные проявления. При неиммунологической непереносимости пищевого белка количество потребляемой пищи, как правило, более непосредственно связано с тяжестью симптомов. Чрезмерное газообразование в кишечнике, вздутие живота, боль в животе и диарея являются распространенными симптомами. Принимая во внимание, что при иммунологической аллергии на пищевой белок даже следовые количества сенсибилизированного пищевого белка могут вызвать взрывную реакцию и могут поразить кожу и кровеносные сосуды. IgE-опосредованные реакции возникают в течение от нескольких минут до часа после приема пищевого белка, и симптомы варьируют от кожной сыпи, крапивницы, ангионевротического отека, свистящего дыхания до анафилаксии, тогда как не-IgE-опосредованные реакции могут развиваться в течение от нескольких часов до нескольких дней.
IgE-опосредованные реакции возникают в течение от нескольких минут до часа после приема пищевого белка, и симптомы варьируют от кожной сыпи, крапивницы, ангионевротического отека, свистящего дыхания до анафилаксии, тогда как не-IgE-опосредованные реакции могут развиваться в течение от нескольких часов до нескольких дней.
Типичным проявлением у младенцев может быть диарея у младенцев в возрасте до 6 месяцев и со временем рвота после кормления молочной смесью в течение нескольких недель. Синдром пищевого проктоколита является распространенным состоянием, при котором у здоровых младенцев возникает диарея, но вес не снижается. Принимая во внимание, что в случае FPIES младенец может обезвоживаться и терять вес.
Вот некоторые из симптомов и физических признаков, наблюдаемых при различных нарушениях непереносимости белка:
Синдром оральной аллергии: Реакция в основном возникает из-за перекрестной реактивности между пыльцой и пищей растительного происхождения (фруктами и овощами), а симптомы локализуются на слизистой оболочке полости рта. [9] Симптомы включают зуд и жжение в области губ, языка, неба и горла. Возможны ангионевротический отек и рвота.
[9] Симптомы включают зуд и жжение в области губ, языка, неба и горла. Возможны ангионевротический отек и рвота.
Немедленная гиперчувствительность ЖКТ: у пациентов появляются тошнота, боль в животе и рвота в течение 1–2 часов после приема сенсибилизированного пищевого белка, часто с последующей диареей. Пораженные люди имеют периодические боли в животе, плохой аппетит и плохую прибавку в весе.
Эозинофильный эзофагит (ЭоЭ): у пациентов возникают затруднения при глотании, застревание твердой пищи, боли в животе, регургитация или рвота и снижение аппетита. У детей младшего возраста могут возникнуть трудности с кормлением и плохая прибавка в весе. Симптомы часто совпадают, и их часто путают с гастроэзофагеальной рефлюксной болезнью (ГЭРБ). Однако у пациентов с ЭоЭ часто обнаруживают в анамнезе и другие аутоиммунные и аллергические состояния.[10]
Эозинофильный гастрит: они обычно проявляются признаками гастрита, такими как боль в животе, постпрандиальная рвота, раннее насыщение, анорексия и задержка развития. Заболевание очень чувствительно к диетическим ограничениям у детей. Примерно 50% этих пациентов также имеют признаки атопии.
Заболевание очень чувствительно к диетическим ограничениям у детей. Примерно 50% этих пациентов также имеют признаки атопии.
Эозинофильный гастроэнтерит: это редкое заболевание с хроническим рецидивирующим течением, характеризующееся инфильтрацией эозинофилов в слизистую оболочку желудочно-кишечного тракта. Презентация может быть разной. У детей могут наблюдаться задержка развития, задержка роста, задержка полового созревания или аменорея. Часто у взрослых возникают боли в животе, дисфагия или диарея. У них также могут быть признаки энтеропатии с потерей белка, желудочно-кишечного кровотечения или мальабсорбции.[11]
Синдром энтероколита, вызванного пищевыми белками (FPIES): у пациентов может наблюдаться рвота через один-три часа после кормления. У них также может быть вздутие живота, кровавый понос, анемия и потеря веса, и обычно они провоцируются смесями на основе коровьего молока или соевого белка. При физическом осмотре могут быть очевидны признаки обезвоживания. Отсутствуют респираторные симптомы или классические IgE-опосредованные аллергические кожные реакции.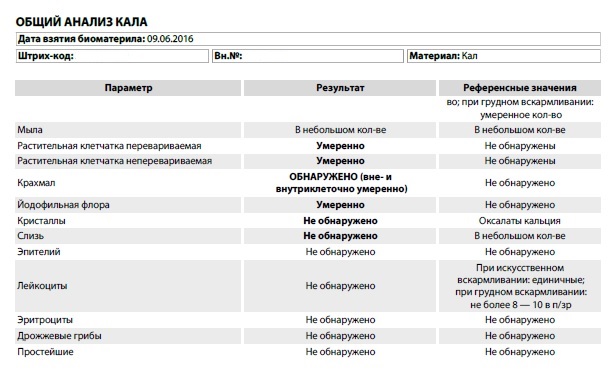
Энтеропатия, вызванная пищевым белком: Пациенты с энтеропатией, вызванной пищевым белком, имеют стеаторею и задержку развития в первые несколько месяцев жизни.
Аллергический проктоколит, вызванный пищевым белком: обычно наблюдается у здоровых младенцев, находящихся на грудном вскармливании. У них появляются симптомы стула с прожилками крови в первые несколько месяцев жизни.
Целиакия: у пациентов с целиакией обычно наблюдаются диарея, дурно пахнущий стул, стеаторея, урчание в носу, метеоризм и потеря веса. Больные жалуются на слабость и быструю утомляемость, обычно связанные с неправильным питанием. Могут быть очевидны признаки анемии. Может отмечаться герпетиформный дерматит, зудящая папуловезикулярная сыпь на разгибательных поверхностях конечностей, туловище и ягодицах.
Дефицит энтерокиназы: У младенцев с дефицитом этого фермента с рождения развивается диарея, и они плохо развиваются. При хронической мальабсорбции белка склонны к развитию гипопротеинемических отеков.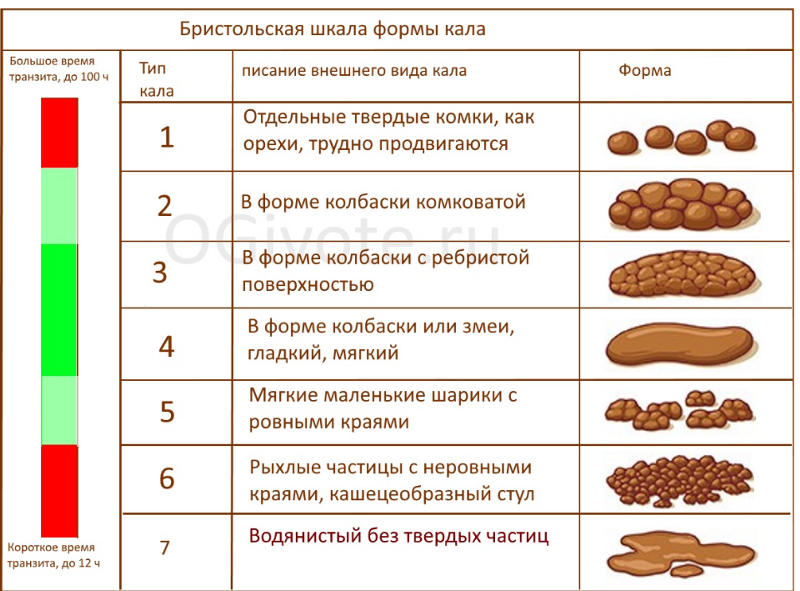 Пероральное введение экстракта поджелудочной железы приводит к быстрому контролю симптомов и способствует ускорению роста.[12]
Пероральное введение экстракта поджелудочной железы приводит к быстрому контролю симптомов и способствует ускорению роста.[12]
Врожденные нарушения обмена веществ: Эти нарушения приводят к накоплению метаболитов перед дефектным ферментом (аминокислоты и/или аммиак), вызывая интоксикацию. Симптомы варьируются в зависимости от пораженных ферментов.
Токсические реакции на биогенные амины: Проглатывание некоторых биогенных аминов способствует развитию токсических реакций. Пациенты могут жаловаться на головную боль, сердцебиение, рвоту, диарею и аллергию. Установлено, что употребление выдержанного сыра, содержащего тирамин, в сочетании с применением ингибиторов моноаминоксидазы (ИМАО) вызывает головные боли и гипертонический криз.[13] Гистамин более токсичен и может вызывать такие эффекты, как гипотензия, раздражение кожи, головная боль, сердцебиение, приступы астмы и т. д. Эта симптоматика известна как «отравление скомброидной рыбой», которое наблюдается после употребления рыбы из Scombridae и Scomberesocidae семейств (тунец, скумбрия, пеламида, луфарь и т. д.), содержащие высокие уровни гистамина.[14]
д.), содержащие высокие уровни гистамина.[14]
Дерматологические проявления:
Белковая непереносимость часто связана с дерматологическими атопическими состояниями. Исследование, проведенное в Италии, показало, что 71% детей с сопутствующей аллергией на коровье молоко имеют сопутствующий атопический дерматит.[15] Другие дерматологические симптомы включают крапивницу, сыпь и ангионевротический отек.
Оценка
Не существует какого-либо конкретного теста для диагностики непереносимости пищевого белка. Состояние оценивается в первую очередь на основе подробного анамнеза и физического осмотра. Клиницисты должны распознавать и дифференцировать иммунологическую непереносимость пищевого белка от неиммунологической, чтобы предотвратить симптомы и управлять ими. При IgE-опосредованной пищевой аллергии обычно очевидны положительные кожные прик-тесты на пищевые белки наряду с обнаружением специфических пищевых IgE-антител. Однако в большинстве случаев непереносимость пищевых белков не опосредована IgE.
При подозрении на непереносимость пищевого белка в диагностике помогают следующие меры и тесты:
Лечение/управление
Единственным окончательным методом лечения непереносимости пищевого белка является строгое исключение пищевого белка из рациона. Пациентов следует консультировать по вопросам контроля за составом пищевых продуктов и соблюдения элиминационной диеты. Пациенты, находящиеся на долгосрочной элиминационной диете, также должны иметь доступ к соответствующим диетическим консультациям, в идеале диетологом или диетологом, и к регулярному мониторингу роста, особенно у детей.
Матерям, находящимся на грудном вскармливании, следует рекомендовать избегать коровьего молока и молочных продуктов. В качестве средства выбора для лечения аллергии на коровье молоко, особенно у младенцев и детей младшего возраста, не находящихся на грудном вскармливании, следует рекомендовать интенсивно гидролизованную смесь с подтвержденной гипоаллергенностью. Для пациентов с более тяжелыми симптомами также могут быть рекомендованы формулы аминокислот.[16]
Стероиды являются основным средством лечения IgE-опосредованной иммунологической непереносимости пищевых белков, включая эозинофильные желудочно-кишечные расстройства.[17]
Новорожденных с острым FPIES с легкими симптомами (без вялости, бледности или апатии) можно лечить дома с помощью пероральной регидратации. Но при тяжелых симптомах их необходимо лечить в медицинском учреждении с помощью внутривенных вливаний. Внутримышечный адреналин и антигистаминные препараты не играют никакой роли в лечении реакций FPIES.
При подозрении на острые аллергические реакции или анафилаксию следует немедленно отказаться от вероятного продукта питания и оказать неотложную медицинскую помощь. Им могут выписать рецепт на автоинъекционное устройство с адреналином и проинструктировать, как им правильно пользоваться.
Дифференциальный диагноз
Некоторые распространенные дифференциальные диагнозы при непереносимости пищевого белка обсуждаются ниже:
Прогноз
Прогноз при многих случаях непереносимости белков благоприятный при соблюдении строгой диеты. Многие исследования показали, что прогноз при непереносимости белка коровьего молока благоприятен: у большинства пациентов аллергия перерастает в детстве и раннем подростковом возрасте. [2] Однако у некоторых детей с IgE-опосредованной непереносимостью белков развиваются аллергический риноконъюнктивит и астма.
[2] Однако у некоторых детей с IgE-опосредованной непереносимостью белков развиваются аллергический риноконъюнктивит и астма.
Осложнения
Белок является важным питательным веществом для здоровья и развития нашего организма. Общие осложнения непереносимости белка, приводящие к дефициту белка, включают потерю мышечной массы, задержку роста, задержку развития и ослабление иммунной системы. У пострадавших людей могут быть такие симптомы, как отеки ног, лица и других частей тела, сухие и ломкие волосы, усталость и частые инфекции.
У взрослых аллергические реакции на белки коровьего молока часто осложняются непереносимостью лактозы, которая усиливается с возрастом. IgE-опосредованные аллергические состояния могут вызывать анафилактические реакции и ангионевротический отек, которые без лечения могут быть опасными для жизни. Диарея и рвота, связанные с FPIES и эозинофильным гастроэнтеритом, могут привести к осложнениям, включая тяжелое обезвоживание и гиповолемический шок.
Сдерживание и просвещение пациентов
У здоровых младенцев рекомендуется обеспечить исключительно грудное вскармливание до 6 месяцев грудного возраста и постепенное введение твердой пищи после 6 месяцев, чтобы предотвратить пищевую аллергию или непереносимость. Младенцы с аллергией на коровье молоко должны избегать молочных смесей и должны находиться на грудном вскармливании. Кормящим матерям желательно исключить из рациона молочные продукты. Если пострадавший младенец не находится на грудном вскармливании, может быть назначена интенсивно гидролизованная смесь. Медицинские работники должны информировать пациентов о важности отмены диеты при подозрении на непереносимость белка или аллергию. Пациентам следует обратить внимание на подозреваемый ингредиент в пищевых продуктах. Пациенты, находящиеся на элиминационной диете, также должны получать соответствующие рекомендации от диетолога или нутрициолога. Пациентам с острыми реакциями гиперчувствительности на пищевые белки в анамнезе следует назначать шприц-ручки с адреналином.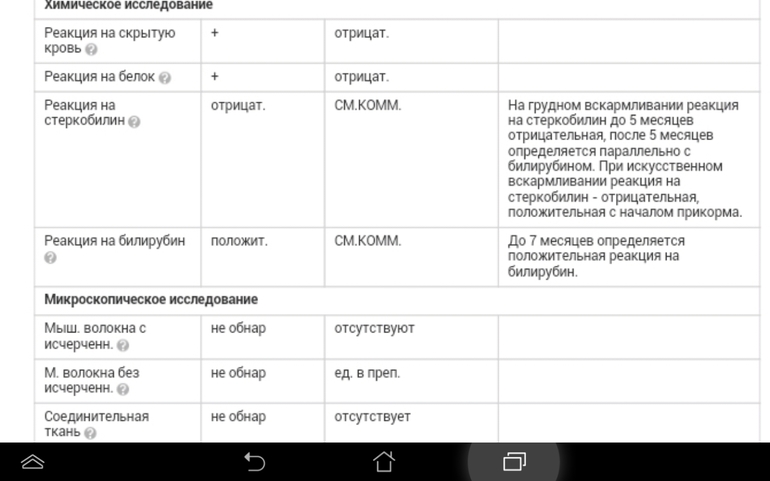
Улучшение результатов работы команды здравоохранения
Белковая непереносимость — это расстройство, которое требует подхода межпрофессиональной команды как для диагностики, так и для лечения. От сбора анамнеза, проведения исследований до постановки правильного диагноза от медицинских работников требуются хорошие коммуникативные и диагностические навыки. Соблюдение со стороны пациента не менее важно в лечении этого состояния. Поскольку отказ от диеты остается основным методом лечения непереносимости белка, необходимо уделять большое внимание регулярным консультациям с диетологом или нутрициологом. Управление индивидуально для каждого пациента. У пациентов, у которых развиваются острые реакции (например, реакции гиперчувствительности при состояниях, опосредованных IgE, тяжелое обезвоживание или шок при FPIES), медсестры и фельдшеры играют жизненно важную роль в межпрофессиональной группе, поскольку они будут контролировать жизненные показатели пациента, вводить жидкости и лекарства, и помочь с образованием пациента и его семьи.
Аллергологи также играют важную роль в диагностике непереносимости белка, поскольку расстройство часто связано с сенсибилизацией к пищевым белкам. Часто родители или опекуны педиатрических пациентов или сами взрослые пациенты с хронической или тяжелой непереносимостью белка испытывают значительное бремя, тревогу, беспокойство и стресс, о которых следует заботиться с помощью консультантов, психологов или психиатров, когда это необходимо.
Прогноз при непереносимости белка благоприятный. Надлежащая идентификация возбудителя и его избегание помогает контролировать расстройство. Недавние данные свидетельствуют о том, что сенсибилизацию к коровьему молоку, ведущую к непереносимости и аллергии, можно в первую очередь предотвратить, избегая добавления смесей на основе коровьего молока в течение как минимум первых 3 дней жизни.[18] [Уровень 1] Исследование, проведенное в 2019 годутакже успешно продемонстрировала гипоаллергенность новой смеси на основе сыворотки с широким гидролизом, которая содержит два олигосахарида грудного молока. [19] [Уровень 1] Различные текущие исследования добавили новые аспекты в профилактику и лечение непереносимости пищевого белка.
[19] [Уровень 1] Различные текущие исследования добавили новые аспекты в профилактику и лечение непереносимости пищевого белка.



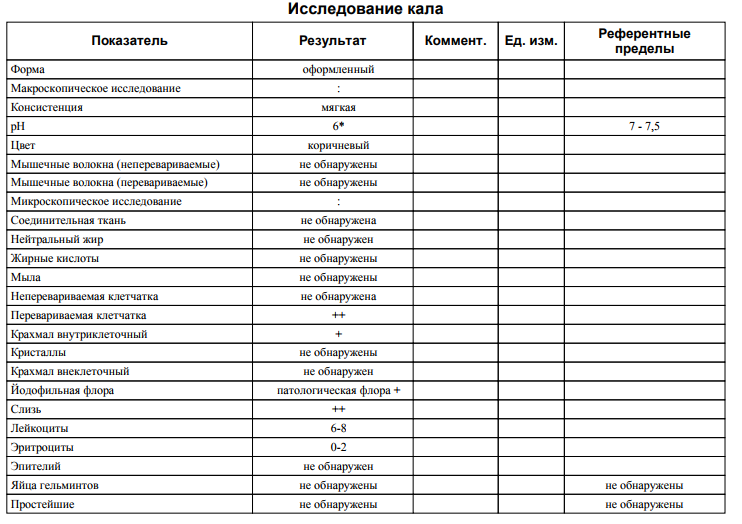
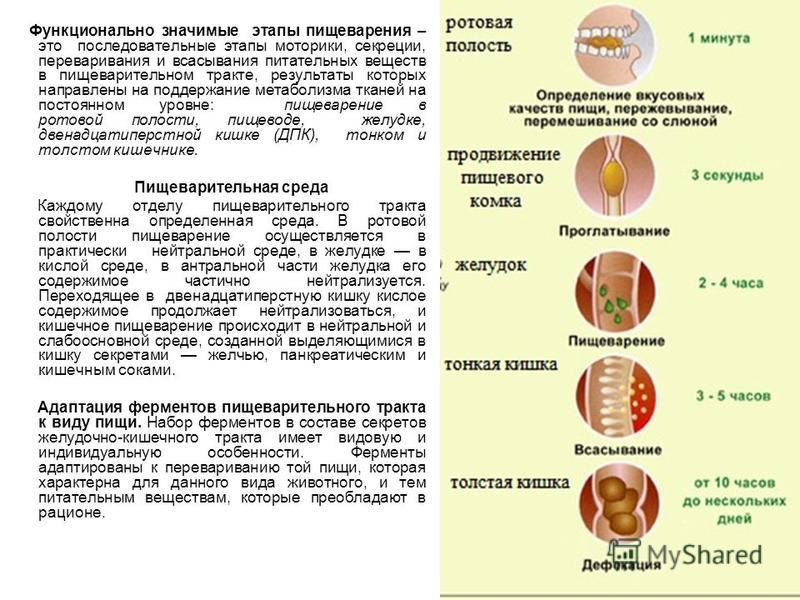
 Если симптомы улучшаются, в качестве диагностического теста может быть проведен тест на пероральную пищевую провокацию.
Если симптомы улучшаются, в качестве диагностического теста может быть проведен тест на пероральную пищевую провокацию.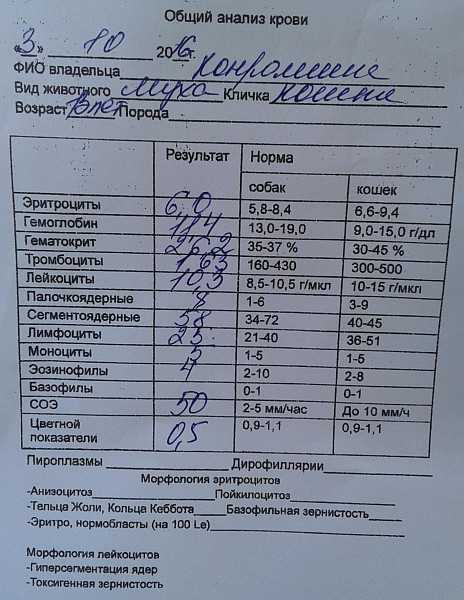

 Влияние желудочного пищеварения на развитие пищевой аллергии. Преподобный отец Аллергол (2009). 2015 ноябрь;55(7):444-447. [Бесплатная статья PMC: PMC5467726] [PubMed: 28616101]
Влияние желудочного пищеварения на развитие пищевой аллергии. Преподобный отец Аллергол (2009). 2015 ноябрь;55(7):444-447. [Бесплатная статья PMC: PMC5467726] [PubMed: 28616101] А., Леффлер Д.А., Катасси С., Грин П.Х., Келли С.П., Ахуджа В., Махария Г.К. Глобальная распространенность глютеновой болезни: систематический обзор и метаанализ. Клин Гастроэнтерол Гепатол. 2018 июнь;16(6):823-836.e2. [PubMed: 29551598]
А., Леффлер Д.А., Катасси С., Грин П.Х., Келли С.П., Ахуджа В., Махария Г.К. Глобальная распространенность глютеновой болезни: систематический обзор и метаанализ. Клин Гастроэнтерол Гепатол. 2018 июнь;16(6):823-836.e2. [PubMed: 29551598]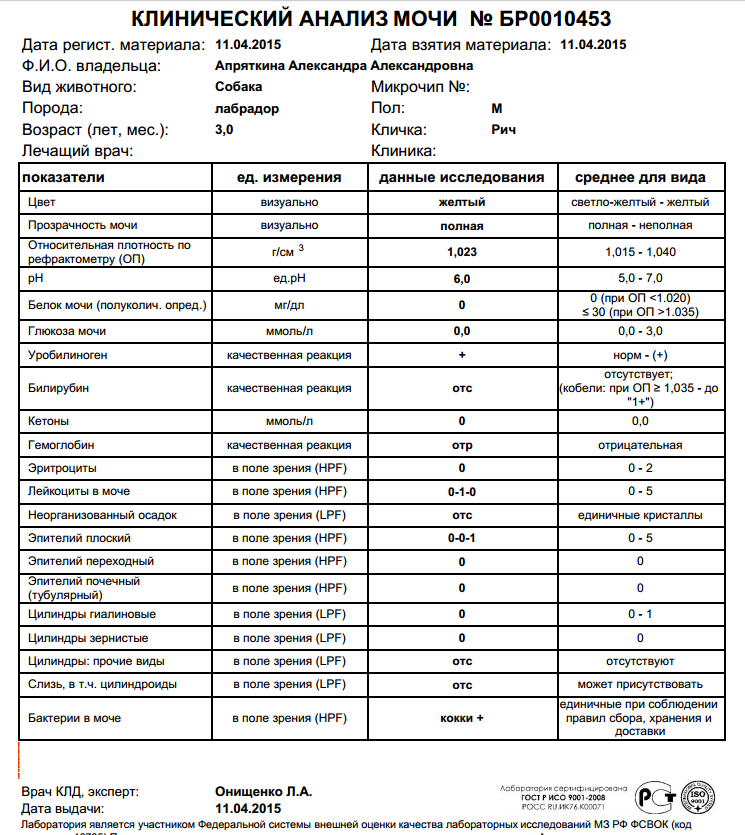 [Бесплатная статья PMC: PMC1647492] [PubMed: 5477679]
[Бесплатная статья PMC: PMC1647492] [PubMed: 5477679] Дж., Ниггеманн Б., Нвару Б.И., Пападопулос Н.Г., Поульсен Л.К., Сантос А.Ф., Скайпала И. , Шёпфер А., Ван Ри Р., Вентер С., Ворм М., Влиг-Бурстра Б., Панесар С., де Сильва Д., Соарес-Вайзер К., Шейх А., Балмер-Вебер Б.К., Нильссон С., де Йонг Н.В., Акдис К.А., Группа рекомендаций EAACI по пищевой аллергии и анафилаксии. Рекомендации EAACI по пищевой аллергии и анафилаксии: диагностика и лечение пищевой аллергии. Аллергия. 2014 авг; 69(8):1008-25. [PubMed: 24909706]
Дж., Ниггеманн Б., Нвару Б.И., Пападопулос Н.Г., Поульсен Л.К., Сантос А.Ф., Скайпала И. , Шёпфер А., Ван Ри Р., Вентер С., Ворм М., Влиг-Бурстра Б., Панесар С., де Сильва Д., Соарес-Вайзер К., Шейх А., Балмер-Вебер Б.К., Нильссон С., де Йонг Н.В., Акдис К.А., Группа рекомендаций EAACI по пищевой аллергии и анафилаксии. Рекомендации EAACI по пищевой аллергии и анафилаксии: диагностика и лечение пищевой аллергии. Аллергия. 2014 авг; 69(8):1008-25. [PubMed: 24909706]

 Если симптомы улучшаются, в качестве диагностического теста может быть проведен тест на пероральную пищевую провокацию.
Если симптомы улучшаются, в качестве диагностического теста может быть проведен тест на пероральную пищевую провокацию.

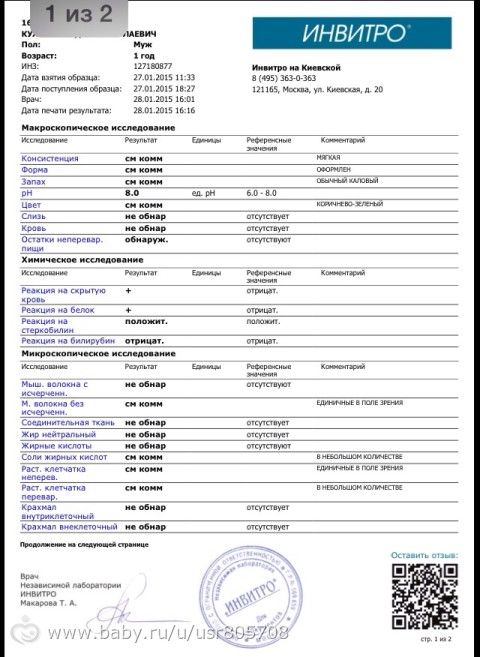 Влияние желудочного пищеварения на развитие пищевой аллергии. Преподобный отец Аллергол (2009). 2015 ноябрь;55(7):444-447. [Бесплатная статья PMC: PMC5467726] [PubMed: 28616101]
Влияние желудочного пищеварения на развитие пищевой аллергии. Преподобный отец Аллергол (2009). 2015 ноябрь;55(7):444-447. [Бесплатная статья PMC: PMC5467726] [PubMed: 28616101] А., Леффлер Д.А., Катасси С., Грин П.Х., Келли С.П., Ахуджа В., Махария Г.К. Глобальная распространенность глютеновой болезни: систематический обзор и метаанализ. Клин Гастроэнтерол Гепатол. 2018 июнь;16(6):823-836.e2. [PubMed: 29551598]
А., Леффлер Д.А., Катасси С., Грин П.Х., Келли С.П., Ахуджа В., Махария Г.К. Глобальная распространенность глютеновой болезни: систематический обзор и метаанализ. Клин Гастроэнтерол Гепатол. 2018 июнь;16(6):823-836.e2. [PubMed: 29551598] [Бесплатная статья PMC: PMC1647492] [PubMed: 5477679]
[Бесплатная статья PMC: PMC1647492] [PubMed: 5477679]