Что такое pН воды и почему важно его знать
Что такое pН воды и почему важно его знать
Уровень активности ионов водорода в воде является одним из важнейших факторов, влияющих на оценку качества жидкости. Именно от данного критерия зависит уровень кислотно-щелочного баланса и направленность биохимических реакций, которые будут происходить в организме после употребления этой жидкости. В данной статье мы подробнее остановимся на вопросе, что такое pН воды, каким образом его определяют, а также же как повысить или понизить pН воды.
Из этой статьи вы узнаете:
-
Что такое pН воды
-
Какова норма pН воды
-
Чем грозит низкий уровень pH воды
-
Как измерить pН воды
Что такое pН воды
Показатель pH является единицей активности иона водорода, которая равна обратному логарифму активности водородных ионов. Так, например, вода, pH которой составляет 7, обладает 10–7 моль на один литр ионов водорода. Следовательно, жидкость с pH равном 6 – 10–6 моль на один литр. Шкала показателей pH при этом варьирует в диапазоне от 0 до 14. Если pH воды менее 7, то она является кислой, а если более 7 – тогда щелочной. Норма pH для поверхностных водных систем составляет 6,5–8,5, для подземных – 6–8,5.
Показатель pH воды равняется 7 при 25 °С, но при взаимодействии с диоксидом углерода в атмосфере данное значение будет составлять 5,2. Уровень pH тесно связан с атмосферным газом и температурой, поэтому воду следует проверить в самые короткие сроки. pH воды не сможет дать полной характеристики и повода для ограничения подачи воды.
Когда в воде растворяются различные химические вещества, то данный баланс подлежит изменению, что, в свою очередь, провоцирует изменение показателя pH. Если в воду добавить кислоту, концентрация ионов водорода возрастает, и концентрация гидроксид-ионов, в свою очередь, понижается. Если в жидкость добавить щелочь, тогда концентрация гидроксид-ионов возрастает, а содержание ионов водорода понижается.
Статьи, рекомендуемые к прочтению:
Уровень pН воды показывает уровень кислотности или щелочности среды, а кислотность и щелочность характеризуется количественным содержанием в воде элементов, нейтрализующих щелочь и кислоту. Так, например, температура отражает уровень нагрева вещества, но не количественный показатель тепла. Если мы коснемся воды рукой, то мы определим, теплая она или холодная, но мы не сможем сказать, какое количество тепла в ней содержится (другими словами, сколько потребуется времени для того, чтобы вода остыла).
Показатель pH – один из основных качественных характеристик воды. Он отражает кислотно-щелочной баланс и определяет, каким образом будут происходить те или иные биологические и химические процессы. Величиной pH воды определяется скорость протекания той или иной химической реакции, уровень коррозионной агрессивности жидкости, степень токсичности загрязняющего вещества и многие другие факторы. Более того, кислотно-щелочной баланс среды организма определяет наше состояние здоровья, настроение и самочувствие.
Различают следующие группы воды, в зависимости от показателя pH:
|
Тип воды |
Величина рН |
|
Сильнокислые воды |
<3 |
|
Кислые воды |
3–5 |
|
Слабокислые воды |
5–6,5 |
|
Нейтральные воды |
6,5–7,5 |
|
Слабощелочные воды |
7,5–8,5 |
|
Щелочные воды |
8,5–9,5 |
|
|
>9,5 |
Контролировать уровень pН воды необходимо на каждом этапе очистки жидкости, поскольку смещение баланса может негативно отразиться на вкусовых качествах, запахе и оттенке воды, а также снизить эффективность ее очистки.
Каков нормальный pН воды
Из-за стремительного темпа современной жизни, неправильного питания, нарушения пищевого и питьевого режимов уровень pН в организме человека падает. Так, кислотно-щелочной баланс смещается в сторону повышенной кислотности (pН до значения 7 подразумевает кислую среду, и до 14 – щелочную, соответственно, чем ниже данный уровень, тем выше кислотность), что может привести к серьезным заболеваниям. Решать эту проблему можно с помощью ежедневного употребления минеральной воды с оптимальным уровнем активности ионов водорода. Именно поэтому важно знать, какая величина pН является нормой для воды, которую вы регулярно употребляете в пищу.
Итак, какой должен быть pН воды? Профессионалы утверждают, что эта величина должна ориентировочно соответствовать нормальному показателю pН крови человека (7,5). Именно поэтому для питьевой воды норму pН рассчитывают от 7 до 7,5. Благодаря чистой питьевой воде с нормальным показателем активности ионов водорода улучшаются обменные процессы в организме, увеличивается общая продолжительность жизни и оптимизируется обмен кислорода. И наоборот, из-за сладких, газированных и содержащих красители напитков уменьшается pН человеческой крови, что можно сразу заметить по неприятной сухости во рту.
Поэтому лучше всего отдавать предпочтение воде с «правильным» показателем pН. Вы всегда сможете найти эту информацию на этикетке любой бутылки. Никакой фильтр с наполнителями и абсорбентами не сможет заменить настоящую природную воду с оптимальным уровнем pН. Некоторые пытаются понизить кислотность воды pН и придать жидкости полезные свойства, добавляя лимонный или огуречный сок, тем не менее это далеко не всегда оказывает должный эффект. Еще один известный способ изменения pН воды – это электролиз, который позволяет получить в двух емкостях щелочную и кислую воду. Щелочная вода с высоким pН считается «живой», ее используют для лечения, а кислая – «мертвой», которую чаще всего используют для умывания.
Тем не менее такие способы не подойдут для ежедневного использования. В этой ситуации остается только одно рациональное решение – отдать предпочтение слабоминеральной природной воде с необходимым для здоровья уровнем кислотности.
Измерение pН воды
Не стоит забывать о том, что человеческий организм на целых 70 % состоит из воды! Продукты обмена веществ в клетках представляют собой кислоты, в то время как основная масса внутренних жидкостей организма, за исключением желудочной кислоты, слабощелочные. Особое значение при этом имеют показатели крови. Организм человека нормально функционирует, если его кровь слабощелочная, и величина ее pН составляет от 7,35 до 7,45.
В том случае, когда в кровь и межклеточную жидкость попадает большое количество кислот, происходит нарушение кислотно-щелочного баланса. Даже небольшое отклонение уровня pН от данных показателей (от 7,35 до 7,45) может привести к серьезному нарушению здоровья. Если продолжается процесс повышения кислотности крови и дальнейшее понижение значения pН до 6,95, то наступает кома и возникает настоящий риск для жизни человека! Именно по этой причине необходимо отслеживать величину pН питьевой воды, которая является одной из важнейших показателей ее качества!
- Лакмусовая бумага.
Уровень pН воды вы сможете определить самостоятельно, в домашних условиях. В качестве прибора для измерения pН воды вы можете использовать лакмусовую (индикаторную) бумагу, которая меняет свой оттенок при кратковременном погружении в изучаемую среду. Так, при погружении в кислотную среду лакмусовая полоска приобретает красный оттенок, а в щелочную – синий. Далее следует сравнить получившийся цвет с цветной шкалой, в которой для каждого оттенка соответствует конкретный уровень pН, чтобы определить данный показатель у исследуемой жидкости. Данный метод определения pН является самым простым и дешевым.
Для наиболее точного определения уровня pН используют pН-метр для воды. Данный прибор для определения pН воды более дорогостоящий, чем лакмусовая бумага, тем не менее он определяет уровень pН жидкости в точности до сотых!
РН-метры для воды бывают бытовыми (портативными) и лабораторными. Чаще всего используют первый вариант, мы остановимся на них подробнее. Они различаются:
-
Степенью защиты от воды.
-
Наличием (или отсутствием) автоматической калибровки.
-
Точностью результатов.
Последний параметр определяется количеством калибруемых точек (1 или 2). Точками называют буферные растворы, с помощью которых и производят калибровку РН-метра. Рекомендуем приобрести прибор с автоматической калибровкой.
- Самодельные тест-полоски.
Существуют специальные тест-полоски, определяющие уровень pН-среды. Такие полоски очень удобны в использовании. Их упаковка оснащена шкалой, с помощью которой определяют концентрацию водородных ионов. Но такие тест-полоски не так часто появляются в продаже, при этом они довольно дорогостоящие.
При всех своих преимуществах pН-метры для воды также отличаются сравнительно высокой ценой.
Вы можете воспользоваться самодельными тест-полосками, чтобы определить pН воды.
Существуют различные вещества, которые меняют свой цвет в зависимости от содержания водородных ионов в жидкости. Например, чай вместо коричневого оттенка приобретает желтый, если в него добавить ломтик лимона.
Таким же образом меняют свой цвет, в зависимости от содержания водородных ионов, вишневый, смородинный соки и т. д. В природе существует огромное количество таких органических индикаторов. И на основе таких индикаторов создают самодельные тест-полоски, которые позволяют определить pН воды.
Мы воспользуемся веществом, входящим в состав красной цветной капусты. Данный овощ содержит пигмент anthocyanin, относящийся к категории флавоноидов. Именно он отвечает за оттенок сока капусты и меняет его, в зависимости от уровня кислотности.
Антоцианы в кислой среде приобретают красный оттенок, а в щелочной – синий, в фиолетовый они окрашиваются, находясь в нейтральной среде. Аналогичными свойствами обладает и пигмент свеклы.
Для проведения эксперимента вам потребуется половина качана красной цветной капусты среднего размера, который следует мелко нарезать. Затем нарезанную капусту необходимо положить в емкость и залить литром воды. Затем вскипятите воду и оставьте данное зелье вариться в течение 20–30 минут.
За это время часть жидкости испарится, и вы получите отвар насыщенного фиолетового оттенка. Затем остудите зелье и приготовьте основу для теста.
Идеальным вариантом в этом случае послужит белая принтерная бумага, которая не будет вносить погрешности в цвет жидкости. Также ее преимущество заключается в том, что она хорошо впитывает отвар индикатора. Бумага должна быть нарезана полосками ориентировочно 1×5 см.
Перед тем как вы будете определять уровень pН воды, необходимо пропитать тест-полоски индикаторным раствором. Для этого процедите остывший отвар сквозь марлю и опустите в него бумагу. Следите за тем, чтобы тест-полоски пропитались равномерно. Пропитывать бумагу следует в течение 10 минут. В результате бумага должна приобрести бледно-сиреневый оттенок.
Далее просушите тест-полоски, разложив их на чистой бумаге или развесив на бельевой веревке.
Когда бумага, пропитанная отваром, высохнет, вы можете приступать к определению уровня pН воды. Затем сложите тест-полоски в коробку или полиэтиленовый пакетик, чтобы уберечь их от влаги.
Использовать данный метод определения уровня pН очень легко. Возьмите пипетку и капните одну-две капли испытуемого раствора на тест-полоску. Подождите одну-две минуты, чтобы индикатор вступил в реакцию с бумагой. В зависимости от показателя pН воды бумага приобретет определенный оттенок, который следует сравнить с цветной шкалой, имеющей следующий вид:
Для калибровки цветной шкалы используются вещества, которые в первоначальном виде имеют постоянный pH среды. Ниже расположена подробная таблица этих элементов:|
Некоторые значения pН |
|
|
Вещество |
pH |
|
Лимонный сок (5 % р-р лимонной кислоты) |
2,0±0,3 |
|
Пищевой уксус |
2,4 |
|
Кока-кола |
3,0±0,3 |
|
Яблочный сок |
3,0 |
|
Пиво |
4,5 |
|
Кофе |
5,0 |
|
Шампунь |
5,5 |
|
Чай |
5,5 |
|
Слюна |
6,35–6,85 |
|
Молоко |
6,6–6,9 |
|
Чистая вода |
7,0 |
|
Морская вода |
8,0 |
|
Мыло (жировое) для рук |
9,0–10,0 |
|
Нашатырный спирт |
11,5 |
|
Отбеливатель (хлорная известь) |
12,5 |
|
Концентрированные растворы щелочей |
>13 |
Данная таблица вам поможет в том случае, если вы захотите провести эксперимент, используя какой-либо другой индикатор (например, свекольный отвар, сок черной смородины или шелковицы).
Если полученный результат не внушает вам доверия, или вы по каким-то причинам не смогли решить проблему несбалансированного pН воды, тогда обратитесь к профессионалам.
На российском рынке присутствует немало компаний, которые занимаются разработкой систем водоочистки. Самостоятельно, без помощи профессионала, выбрать тот или иной вид фильтра для очистки воды довольно сложно. И уж тем более не стоит пытаться смонтировать систему водоочистки самостоятельно, даже если вы прочитали несколько статей в Интернете и вам кажется, что вы во всем разобрались.
Наша компания Biokit предлагает широкий выбор систем обратного осмоса, фильтры для воды и другое оборудование, способное вернуть воде из-под крана ее естественные характеристики.
Специалисты нашей компании готовы помочь вам:
-
подключить систему фильтрации самостоятельно;
-
разобраться с процессом выбора фильтров для воды;
-
подобрать сменные материалы;
-
устранить неполадки или решить проблемы с привлечением специалистов-монтажников;
-
найти ответы на интересующие вопросы в телефонном режиме.
Доверьте очистку воды системам от Biokit – пусть ваша семья будет здоровой!
biokit.ru
Кислотно-щелочное равновесие. Здоровый показатель pH
Кислотно-щелочное равновесие.
Показатель pH и его влияние на качество питьевой воды.
Что такое pH?
pH («potentia hydrogeni» — сила водорода, или «pondus hydrogenii» — вес водорода) — это единица измерения активности ионов водорода в любом веществе, количественно выражающая его кислотность.
Данный термин появился в начале ХХ века в Дании. Показатель pH ввел датский химик Сорен Петр Лауриц Соренсен (1868-1939), хотя утверждения о некой «силе воды» встречаются и у его предшественников.
Активность водорода определяется как отрицательный десятичный логарифм концентрации водородных ионов, выраженной в молях на литр:
pH = -log[H+]
Для простоты и удобства при вычислениях был введен показатель pH. рН определяется количественным соотношением в воде ионов Н+ и ОН-, образующихся при диссоциации воды. Принято измерять уровень pH по 14-цифровой шкале.
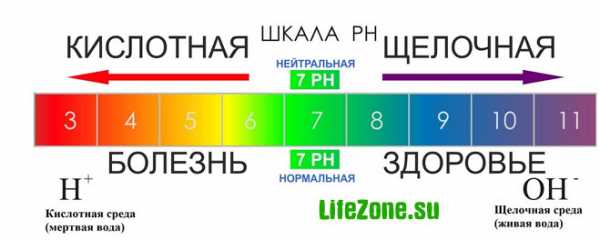
Если в воде пониженное содержание свободных ионов водорода [H+] (рН больше 7) по сравнению с ионами гидроксида [ОН-], то вода будет иметь щелочную реакцию, а при повышенном содержании ионов Н+ (рН меньше 7) — кислую реакцию. В идеально чистой дистиллированной воде эти ионы будут уравновешивать друг друга.
кислая среда: [H+] > [OH-]
нейтральная среда: [H+] = [OH-]
щелочная среда: [OH-] > [H+]
Когда концентрации обоих видов ионов в растворе одинаковы, говорят, что раствор имеет нейтральную реакцию. В нейтральной воде показатель рН равен 7.
При растворении в воде различных химических веществ этот баланс изменяется, что приводит к изменению значения рН. При добавлении к воде кислоты концентрация ионов водорода увеличивается, а концентрация гидроксид-ионов соответственно уменьшается, при добавлении щелочи — наоборот, повышается содержание гидроксид-ионов, а концентрация ионов водорода падает.
рН показатель отражает степень кислотности или щелочности среды, в то время как «кислотность» и «щелочность» характеризуют количественное содержание в воде веществ, способных нейтрализовывать соответственно щелочи и кислоты. В качестве аналогии можно привести пример с температурой, которая характеризует степень нагрева вещества, но не количество тепла. Опустив руку в воду, мы можем сказать какая вода — прохладная или теплая, но при этом не сможем определить сколько в ней тепла (т.е. условно говоря, как долго эта вода будет остывать).
pH считается одним из важнейших показателей качества питьевой воды. Он показывает кислотно-щелочное равновесие и влияет на то, как будут протекать химические и биологические процессы. В зависимости от величины pH может изменяться скорость протекания химических реакций, степень коррозионной агрессивности воды, токсичность загрязняющих веществ и т.д. От кислотно-щелочного равновесия среды нашего организма напрямую зависит наше самочувствие, настроение и здоровье.
Современный человек живет в загрязненной окружающей среде. Многие приобретают и употребляют пищу, изготовленную из полуфабрикатов. Кроме этого практически каждый человек ежедневно подвергается стрессовому воздействию. Все это оказывает влияние на кислотно-щелочное равновесие среды организма, смещая его в сторону кислот. Чай, кофе, пиво, газированные напитки снижают показатель pH в организме.
Считается, что кислая среда является одной из основных причин разрушения клеток и повреждения тканей, развития заболеваний и процессов старения, росту болезнетворных организмов. В кислой среде до клеток не доходит строительный материал, разрушается мембрана.
Кислая среда провоцирует множество заболеваний, среди которых сердечно-сосудистые заболевания, артрит, остеопороз, онкологические заболевания и др, а так же способствует развитию бактерий, вирусов, грибков, гельминтов и прочих паразитов. Паразиты предпочитают кислую среду обитания, и именно в кислотной среде они проявляют себя наиболее патогенно. Кислую среду в организме создают психические и физические перегрузки, мясо, пища, прошедшая глубокую термическую и иную технологическую обработку, снижающую содержание в ней полезных веществ. Эти же источники закисления наполняют организм свободными радикалами, которые перегружают иммунную систему. Один из признаков закисления организма — некомфортная сухость во рту.
Внешне о состоянии кислотно-щелочного равновесия крови человека можно судить по цвету его конъюнктивы в уголках глаз. При оптимальном кислотно-щелочном балансе цвет конъюнктивы ярко-розовый, если же у человека повышается щелочность крови, конъюнктива приобретает темно-розовый окрас, а при повышении кислотности окрас конъюнктивы становится бледно-розовым. При чем цвет конъюнктивы изменяется уже через 80 секунд после употребления веществ, влияющих на кислотно-щелочное равновесие.
Организм регулирует рН внутренних жидкостей, поддерживая значения на определенном уровне. Кислотно-щелочной баланс организма — это определенное соотношение кислот и щелочей, способствующее его нормальному функционированию. Кислотно-щелочной баланс зависит от сохранения относительно постоянных пропорций между межклеточными и внутриклеточными водами в тканях организма. Если кислотно-щелочное равновесие жидкостей в организме не будет поддерживаться постоянно, нормальное функционирование и сохранение жизни окажутся невозможными. Поэтому важно контролировать то, что вы потребляете.
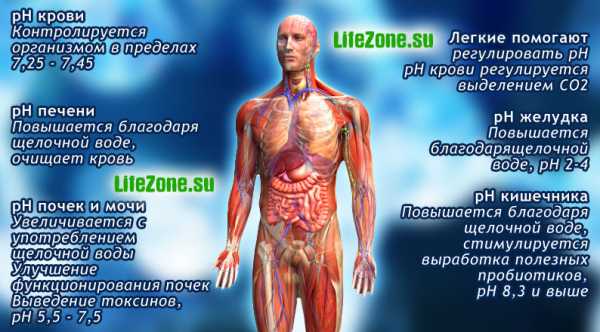
Кислотно-щелочной баланс – это наш индикатор здоровья. Чем мы «кислее», тем скорее стареем и больше болеем. Для нормальной работы всех внутренних органов уровень рН в организме должен быть щелочным, в интервале от 7 до 9.
pH внутри нашего тела не всегда одинаков — некоторые его части более щелочные, а некоторые кислотные. Организм регулирует и поддерживает гомеостаз уровня pH лишь в отдельных случаях, например pH крови. На уровень pH почек и других органов, кислотно-щелочное равновесие которых не регулируются организмом, влияют пища и напитки, которые мы употребляем.
pH крови
Уровень pH крови поддерживается организмом в диапазоне 7.35-7.45. Нормальным показателем pH крови человека считается 7,4-7,45. Даже незначительное отклонение этого показателя влияет на способность крови переносить кислород. Если pH крови повышается до 7,5, она переносит на 75% кислорода больше. При снижении показателя pH крови до 7,3 человеку уже сложно подняться с постели. При 7,29 он может впасть в кому, если показатель pH крови снизится ниже 7,1 — человек умирает.
Уровень pH крови должен поддерживаться в здоровом диапазоне, поэтому организм использует органы и ткани для поддержания его постоянства. Вследствие этого, уровень pH крови не меняется из-за употребления щелочной или кислотной воды, но ткани и органы тела, используемые для регулировки pH крови, меняют свой pH.
pH почек
На параметр pH почек оказывает влияние вода, пища, метаболические процессы в организме. Кислотная еда (например мясные продукты, молочные продукты и др.) и напитки (сладкие газированные напитки, алкогольные напитки, кофе и пр.) приводят к низкому уровню pH в почках, потому что организм выводит излишнюю кислотность через мочу. Чем ниже уровень pH мочи, тем тяжелее приходится работать почкам. Поэтому кислотная нагрузка, приходящаяся от такой еды и напитков на почки, называется потенциальной кислотно-почечной нагрузкой.
Употребление щелочной воды приносит почкам пользу — происходит повышение уровня pH мочи, снижается кислотная нагрузка на организм. Увеличение pH мочи повышает pH организма в целом и избавляет почки от кислотных токсинов.
pH желудка
В пустом желудке содержится не больше чайной ложки желудочной кислоты, выработанной в последний прием пищи. Желудок производит кислоту по мере необходимости при употреблении пищи. Желудок не выделяет кислоту, когда человек пьет воду.
Очень полезно — пить воду на пустой желудок. Показатель pH увеличивается при этом до уровня 5-6. Увеличенный pH будет иметь мягкий антацидный эффект и приведет к увеличению количества полезных пробиотиков (благотворных бактерий). Увеличение pH желудка повышает pH организма, что ведет к здоровому пищеварению и освобождает от симптомов расстройства желудка.
pH подкожного жира
Жировые ткани организма имеют кислотный pH, поскольку в них откладываются излишние кислоты. Организму приходится хранить кислоту в жировых тканях, когда она не может быть выведена или нейтрализована иными способами. Поэтому смещение pH организма в кислую сторону — это один из факторов лишнего веса.
Позитивное влияние щелочной воды на массу тела состоит в том, что щелочная вода помогает выводить из тканей излишнюю кислоту, поскольку помогает почкам работать более рационально. Это помогает контролировать вес, поскольку многократно снижается количество кислоты, которое тело должно «хранить». Щелочная вода также улучшает результаты здоровой диеты и упражнений, помогая организму справиться с излишней кислотностью, выделяемой жировыми тканями в процессе потери веса.
Кости
У костей щелочной pH, так как они в основном состоят из кальция. Их pH постоянен, но если кровь нуждается в регулировке pH, кальций забирается из костей.
Польза, приносимая щелочной водой костям, состоит в их защите, путем снижения количества кислоты, с которым организму приходится бороться. Исследования показали, что употребление щелочной воды снижает рассасывание костей — остеопороз.
pH печени
У печени слабощелочной pH, на уровень которого влияет и пища, и напитки. Сахар и алкоголь должны быть расщеплены в печени, а это приводит к излишкам кислоты.
Польза, приносимая щелочной водой печени, состоит в наличии в такой воде антиоксидантов; установлено, что щелочная вода усиливает работу двух антиоксидантов, находящихся в печени, способствующих более эффективному очищению крови.
pH организма и щелочная вода
Щелочная вода позволяет частям тела, сохраняющим pH крови, работать с большей производительностью. Повышение уровня pH в частях тела, отвечающих за поддержание pH крови, поможет этим органам оставаться здоровыми и работать оперативно.
Между приемами пищи Вы можете помочь Вашему организму нормализовать показатель pH, употребляя щелочную воду. Даже небольшое увеличение pH может оказать огромное влияние на состояние здоровья.
По данным исследований японских ученых, показатель pH питьевой воды, находящийся в диапазоне 7-8, повышает продолжительность жизни населения на 20-30%.
В зависимости от уровня рН воды можно условно разделить на несколько групп:
• сильнокислые воды < 3
• кислые воды 3 — 5
• слабокислые воды 5 — 6.5
• нейтральные воды 6.5 — 7.5
• слабощелочные воды 7.5 — 8.5
• щелочные воды 8.5 — 9.5
• сильнощелочные воды > 9.5
Обычно уровень рН питьевой водопроводной воды находится в пределах, при которых он непосредственно не влияет на потребительские качества воды. В речных водах pH обычно находится в пределах 6.5-8.5, в атмосферных осадках 4.6-6.1, в болотах 5.5-6.0, в морских водах 7.9-8.3.
ВОЗ не предлагает какой-либо рекомендуемой по медицинским показателям величины для рН. Известно, что при низком рН вода обладает высокой коррозионной активностью, а при высоких уровнях (рН>11) вода приобретает характерную мылкость, неприятный запах, способна вызывать раздражение глаз и кожи. Именно поэтому для питьевой и хозяйственно-бытовой воды оптимальным считается уровень рН в диапазоне от 6 до 9.
| |||||||||||||||||||||||||||||||||||||||||||||||

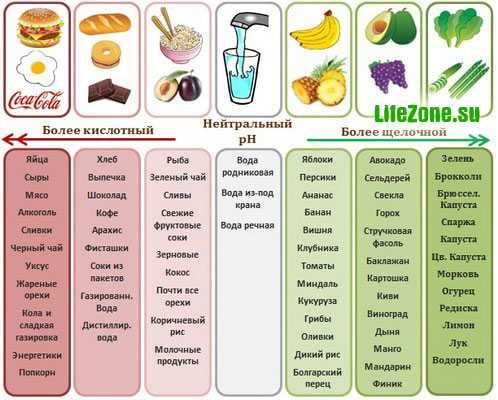


Интересно знать: Немецкий биохимик ОТТО ВАРБУРГ, удостоенный в 1931 Нобелевской премии по физиологии и медицине доказал, что недостаток кислорода (кислая среда pH<7.0) в тканях приводит к изменению нормальных клеток в злокачественные.
Ученый обнаружил, что раковые клетки теряют способность к развитию в среде, насыщенной свободным кислородом с показателем pH=7,5 и выше! Это означает, что когда жидкости в организме становятся кислыми, стимулируется развитие рака.
Его последователи в 60-х годах прошлого столетия доказали, что любая патогенная флора теряет способность размножаться при pH=7,5 и выше, и наша иммунная система легко справляется с любыми агрессорами!
Для сохранения и поддержания здоровья нам необходима правильная щелочная вода (рН=7.5 и выше). Это позволит лучше сохранять кислотно-щелочное равновесие жидкостей организма, так как основные жизненные среды имеют слабощелочную реакцию.
Уже при нейтральной биологической среде организм может обладать удивительной способностью к самоисцелению.
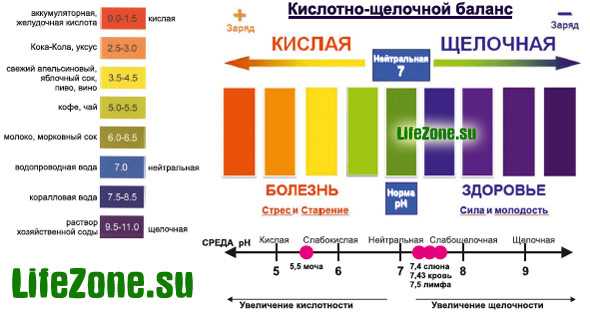
Не знаете где можно взять правильную воду? Я подскажу!
Обратите внимание:
Нажатие на кнопку «Узнать» не ведет к каким-либо финансовым тратам и обязательствам.
Вы лишь получите информацию о доступности правильной воды в Вашем регионе,
а так же получите уникальную возможность бесплатно стать членом клуба здоровых людей
и получить скидку 20% на все предложения + накопительный бонус.

Вступи в международный клуб здоровья Coral Club, получи БЕСПЛАТНО дисконтную карту, возможность участия в акциях, накопительный бонус и другие привилегии!
lifezone.su
1.7. Водородный показатель среды растворов – pH.
Водородный показатель – рН – это мера активности (в случае разбавленных растворов отражает концентрацию) ионов водорода в растворе, количественно выражающая его кислотность, вычисляется как отрицательный (взятый с обратным знаком) десятичный логарифм активности водородных ионов, выраженной в молях на литр.
pН = – lg[H+]
Это понятие было введено в 1909 году датским химиком Сёренсеном. Показатель называется pH, по первым буквам латинских слов potentia hydrogeni – сила водорода, или pondus hydrogenii – вес водорода.
Несколько меньшее распространение получила обратная pH величина – показатель основности раствора, pOH, равная отрицательному десятичному логарифму концентрации в растворе ионов OH:
рОН = – lg[OH–]
В чистой воде при 25°C концентрации ионов водорода ([H+]) и гидроксид-ионов ([OH—]) одинаковы и составляют 10-7моль/л, это напрямую следует из константы автопротолиза воды Кw, которую иначе называют ионным произведением воды:
Кw = [H+] · [OH–] =10–14 [моль2/л2] (при 25°C)
рН + рОН = 14
Когда концентрации обоих видов ионов в растворе одинаковы, говорят, что раствор имеет нейтральную реакцию. При добавлении к воде кислоты концентрация ионов водорода увеличивается, а концентрация гидроксид-ионов соответственно уменьшается, при добавлении основания – наоборот, повышается содержание гидроксид-ионов, а концентрация ионов водорода падает. Когда [H+] > [OH–] говорят, что раствор является кислым, а при [OH–] > [H+] – щелочным.
Определение рН
Для определения значения pH растворов широко используют несколько способов.
1) Водородный показатель можно приблизительно оценивать с помощью индикаторов, точно измерять pH-метром или определять аналитически путём, проведением кислотно-основного титрования.
Для грубой оценки концентрации водородных ионов широко используются кислотно-основные индикаторы – органические вещества-красители, цвет которых зависит от pH среды. К наиболее известным индикаторам принадлежат лакмус, фенолфталеин, метиловый оранжевый (метилоранж) и другие. Индикаторы способны существовать в двух по-разному окрашенных формах – либо в кислотной, либо в основной. Изменение цвета каждого индикатора происходит в своём интервале кислотности, обычно составляющем 1-2 единицы (см. Таблица 1, занятие 2).
Для расширения рабочего интервала измерения pH используют так называемый универсальный индикатор, представляющий собой смесь из нескольких индикаторов. Универсальный индикатор последовательно меняет цвет с красного через жёлтый, зелёный, синий до фиолетового при переходе из кислой области в щелочную. Определения pH индикаторным методом затруднено для мутных или окрашенных растворов.
2) Аналитический объёмный метод – кислотно-основное титрование – также даёт точные результаты определения общей кислотности растворов. Раствор известной концентрации (титрант) по каплям добавляется к исследуемому раствору. При их смешивании протекает химическая реакции. Точка эквивалентности – момент, когда титранта точно хватает, чтобы полностью завершить реакцию, – фиксируется с помощью индикатора. Далее, зная концентрацию и объём добавленного раствора титранта, вычисляется общая кислотность раствора.
Кислотность среды имеет важное значение для множества химических процессов, и возможность протекания или результат той или иной реакции часто зависит от pH среды. Для поддержания определённого значения pH в реакционной системе при проведении лабораторных исследований или на производстве применяют буферные растворы, которые позволяют сохранять практически постоянное значение pH при разбавлении или при добавлении в раствор небольших количеств кислоты или щёлочи.
Водородный показатель pH широко используется для характеристики кислотно-основных свойств различных биологических сред (Табл. 2).
Кислотность реакционной среды особое значение имеет для биохимических реакций, протекающих в живых системах. Концентрация в растворе ионов водорода часто оказывает влияние на физико-химические свойства и биологическую активность белков и нуклеиновых кислот, поэтому для нормального функционирования организма поддержание кислотно-основного гомеостаза является задачей исключительной важности. Динамическое поддержание оптимального pH биологических жидкостей достигается благодаря действию буферных систем.
3) Использование специального прибора – pH-метра – позволяет измерять pH в более широком диапазоне и более точно (до 0,01 единицы pH), чем с помощью индикаторов, отличается удобством и высокой точностью, позволяет измерять pH непрозрачных и цветных растворов и потому широко используется.
С помощью рН-метра измеряют концентрацию ионов водорода (pH) в растворах, питьевой воде, пищевой продукции и сырье, объектах окружающей среды и производственных систем непрерывного контроля технологических процессов, в т. ч. в агрессивных средах.
рН-метр незаменим для аппаратного мониторинга pH растворов разделения урана и плутония, когда требования к корректности показаний аппаратуры без её калибровки чрезвычайно высоки.
Прибор может использоваться в лабораториях стационарных и передвижных, в том числе полевых, а также клинико-диагностических, судебно-медицинских, научно-исследовательских, производственных, в том числе мясо-молочной и хлебопекарной промышленности.
Последнее время pH-метры также широко используются в аквариумных хозяйствах, контроля качества воды в бытовых условиях, земледелия (особенно в гидропонике), а также – для контроля диагностики состояния здоровья.
Таблица 2. Значения рН для некоторых биологических систем и других растворов
Система (раствор) | рН |
Двенадцатиперстная кишка | 7,0 – 7,8 |
Желудочный сок | 1,6 – 1,8 |
Кровь человека | 7,35 – 7,45 |
Ликвор | 7,5 |
Моча | 4,8 – 7,5 |
Мышечная ткань | 6,7 – 6,8 |
Панкреатический сок | 8,3 |
Пот | 4,0 – 8,0 |
Почки | 6,6 – 6,9 |
Протоплазма клеток | 6,4 – 7,0 |
Связки | 7,2 |
Слёзы | 7,4 |
Слюна | 6,35 – 6,85 |
Тонкая кишка | 6,2 – 7,3 |
Молоко | 6,6 – 6,9 |
Морская вода | 8,0 |
Белок куриного яйца | 8,0 |
Апельсиновый сок | 2,6 – 4,4 |
Томатный сок | 4,3 |
Кофе | 5,0 |
Чай | 5,5 |
studfiles.net
Водородный показатель (pH-фактор)
Водородный показатель (pH-фактор) — это мера активности ионов водорода в растворе, количественно выражающая его кислотность. Когда pH не на оптимальном уровне, растения начинают терять способность поглощать некоторые из необходимых для здорового роста элементы. Для всех растений есть специфический уровень pH который позволяет достичь максимальных результатов при выращивании. Большинство растений предпочитают слабокислую среду роста (между 5.5-6.5).
Водородный показатель в формулах
В очень разбавленных растворах водородный показатель эквивалентен концентрации ионов водорода. Равен по модулю и противоположен по знаку десятичному логарифму активности водородных ионов, выраженной в молях на один литр:
pH = -lg[H+]
При стандартних условиях значение pH лежит в приделах от 0 до 14. В чистой воде, при нейтральном pH, концентрация H+ равна концентрации OH— и составляет 1·10-7 моль на литр. Максимально возможное значение pH определяется как сумма pH и pOH и равна 14.
Вопреки распространённому мнению, pH может изменяться не только в интервале от 0 до 14, а может и выходить за эти пределы. Например, при концентрации ионов водорода [H+] = 10−15 моль/л, pH = 15, при концентрации ионов гидроксида [OH—] 10 моль/л pOH = −1.
Важно понимать! Шкала pH логарифмическая, что означает, что каждая единица изменения равняется десятикратному изменению концентрации ионов водорода. Другими словами, раствор с pH 6 в десять раз более кислый, чем раствор с pH 7, и раствор с pH 5 будет в десять раз более кислый, чем раствор с pH 6 и в сто раз более кислый, чем раствор с pH 7. Это означает, что когда вы регулируете pH вашего питательного раствора, и вам необходимо изменить pH на два пункта (например с 7.5 до 5.5) вы должны использовать в десять раз больше корректора pH, чем если бы изменяли pH только на один пункт (с 7.5 до 6.5).
Методы определения значения pH
Для определения значения pH растворов широко используют несколько методик. Водородный показатель можно приблизительно оценивать с помощью индикаторов, точно измерять pH-метром или определять аналитически путём, проведением кислотно-основного титрования.
Кислотно-основные индикаторы
Для грубой оценки концентрации водородных ионов широко используются кислотно-основные индикаторы — органические вещества-красители, цвет которых зависит от pH среды. К наиболее известным индикаторам принадлежат лакмус, фенолфталеин, метиловый оранжевый (метилоранж) и другие. Индикаторы способны существовать в двух по-разному окрашенных формах — либо в кислотной, либо в основной. Изменение цвета каждого индикатора происходит в своём интервале кислотности, обычно составляющем 1-2 единицы.
Универсальный индикатор
 Для расширения рабочего интервала измерения pH используют так называемый универсальный индикатор, представляющий собой смесь из нескольких индикаторов. Универсальный индикатор последовательно меняет цвет с красного через жёлтый, зелёный, синий до фиолетового при переходе из кислотной области в основную.
Для расширения рабочего интервала измерения pH используют так называемый универсальный индикатор, представляющий собой смесь из нескольких индикаторов. Универсальный индикатор последовательно меняет цвет с красного через жёлтый, зелёный, синий до фиолетового при переходе из кислотной области в основную.
Растворами таких смесей — «универсальных индикаторов» обычно пропитывают полоски «индикаторной бумаги», с помощью которых можно быстро (с точностью до единиц рН, или даже десятых долей рН) определить кислотность исследуемых водных растворов. Для более точного определения полученный при нанесении капли раствора цвет индикаторной бумаги немедленно сравнивают с эталонной цветовой шкалой, вид которой представлен на изображениях.
Определения pH индикаторным методом затруднено для мутных или окрашенных растворов.
Учитывая тот факт, что оптимальные значения pH для питательных растворов в гидропонике имеют весьма узкий интервал (обычно от 5.5 до 6.5) использую и другие комбинации индикаторов. Так, например, наш жидкий pH тест имеет рабочий диапазон и шкалу от 4.0 до 8.0, что делает такой тест более точным в сравнении с универсальной индикаторной бумагой.

pH-метр
 Использование специального прибора — pH-метра — позволяет измерять pH в более широком диапазоне и более точно (до 0,01 единицы pH), чем с помощью универсальных индикаторов. Способ отличается удобством и высокой точностью, особенно после калибровки индикаторного электрода в избранном диапазоне рН. Позволяет измерять pH непрозрачных и цветных растворов и потому широко используется.
Использование специального прибора — pH-метра — позволяет измерять pH в более широком диапазоне и более точно (до 0,01 единицы pH), чем с помощью универсальных индикаторов. Способ отличается удобством и высокой точностью, особенно после калибровки индикаторного электрода в избранном диапазоне рН. Позволяет измерять pH непрозрачных и цветных растворов и потому широко используется.

Для более подробного изучения темы рекомендуем посетить соответствующий раздел форума: «pH-метры».
Аналитический объёмный метод
Аналитический объёмный метод — кислотно-основное титрование — также даёт точные результаты определения кислотности растворов. Раствор известной концентрации (титрант) по каплям добавляется к исследуемому раствору. При их смешивании протекает химическая реакция. Точка эквивалентности — момент, когда титранта точно хватает, чтобы полностью завершить реакцию, — фиксируется с помощью индикатора. Далее, зная концентрацию и объём добавленного раствора титранта, вычисляется кислотность раствора.
Влияние температуры на значения pH
Значение pH может меняться в широком диапазоне при изменение температуры. Так, 0,001 молярный раствор NaOH при 20°C имеет pH=11,73, а при 30°C pH=10,83. Влияние температуры на значения pH объясняется различной диссоциацией ионов водорода (H+) и не является ошибкой эксперимента. Температурный эффект невозможно компенсировать за счет электроники pH-метра.
Регулирование pH питательного раствора
Подкисление питательного раствора
Питательный раствор обычно приходится подкислять. Поглощение ионов растениями вызывает постепенное подщелачивание раствора. Любой раствор, имеющий pH 7 или выше, чаще всего приходится доводить до оптимального pH. Для подкисления питательного раствора можно использовать различные кислоты. Чаще всего применяют серную или фосфорную кислоты. Более верным решением для гидропонных растворов являются буферные добавки, такие как pH minus Bloom и pH minus Grow. Данные средства не только доводят значения pH до оптимального, но и стабилизируют значения на длительный период.
При регулировании pH как кислотами, так и щелочами нужно надевать резиновые перчатки, чтобы не вызвать ожогов кожи. Опытный химик умело обращается с концентрированной серной кислотой, он по каплям добавляет кислоту к воде. Но начинающим гидропонистам, пожалуй, лучше обратиться к опытному химику и попросить его приготовить 25%-ный раствор серной кислоты. Во время добавления кислоты раствор перемешивают и определяют его pH. Узнав примерное количество серной кислоты, в дальнейшем ее можно добавлять из мерного цилиндра.
Серную кислоту нужно прибавлять небольшими порциями, чтобы не слишком сильно подкислить раствор, который тогда придется опять подщелачивать. У неопытного работника подкисление и подщелачивание могут продолжаться до бесконечности. Помимо напрасной траты времени и реактивов, такое регулирование выводит из равновесия питательный раствор вследствие накопления ненужных растениям ионов.
Подщелачивание питательного раствора
Слишком кислые растворы подщелачивают едким натрием (гидроксид натрия). Как следует из его названия — это едкое вещество, поэтому нужно пользоваться резиновыми перчатками. Рекомендуется приобретать едкий натрий в виде пилюль. В магазинах бытовой химии едкий натрий можно приобрести как средство для очистки труб, например «Крот». Растворяют одну пилюлю в 0,5 л воды и постепенно приливают щелочной раствор к питательному раствору при постоянном помешивании, часто проверяя его pH. Никакими математическими расчетами не удается вычислить, сколько кислоты или щелочи нужно добавить в том или ином случае.
Если в одном поддоне хотят выращивать несколько культур, нужно подбирать их так, чтобы совпадал не только их оптимальный pH, но и потребности в других факторах роста. Например, желтым нарциссам и хризантемам нужен pH 6,8, но различный режим влажности, поэтому их невозможно выращивать на одном и том же поддоне. Если давать нарциссам столько же влаги, сколько хризантемам, луковицы нарциссов загниют. В опытах ревень достигал максимального развития при pH 6,5, но мог расти даже при pH 3,5. Овес, предпочитающий pH около 6, дает хорошие урожаи и при pH 4, если сильно увеличить дозу азота в питательном растворе. Картофель растет при довольно широком интервале pH, но лучше всего он развивается при pH 5,5. Ниже этого pH также получают высокие урожаи клубней, но они приобретают кислый вкус. Чтобы получать максимальные урожаи высокого качества, нужно точно регулировать pH питательных растворов.
floragrowing.com
определение и свойства. Ph-тест — OneKu
Содержание статьи:Кислоты и щелочи — два крайних положения одной шкалы: их свойства (совершенно противоположные) обусловливает одна и та же величина — концентрация ионов водорода (H+). Однако само по себе это число очень неудобное: даже в кислых средах, где концентрация ионов водорода выше, это число составляет сотые, тысячные доли единицы. Поэтому для удобства пользуются десятичным логарифмом этого значения, умноженным на минус один. Принято говорить, что это pH (potentia Hydrogen), или же водородный показатель.
Возникновение понятия
Вам будет интересно:Какие свойства воздуха использует костер? Или все-таки люди, его разжигая?
Вообще тот факт, что кислая среда и щелочная среда определяются концентрацией ионов водорода H+ и что чем выше их концентрация, тем раствор более кислый (и наоборот, чем ниже концентрация H+, тем более щелочная среда и выше концентрация противоположных ионов OH-), был известен науке достаточно давно. Однако лишь в 1909 году датский химик Серенсен впервые опубликовал исследования, в которых пользовался понятием водородного показателя — PH, впоследствии замененным на pH.
Расчет кислотности

При расчете водородного показателя исходят из того, что молекулы воды в растворе, хоть и в очень малых количествах, все же диссоциируют на ионы. Эта реакция называется автопротолизом воды:
h3O —> H+ + OH-
Реакция обратима, поэтому для нее определена константа равновесия (показывающая, какие в среднем устанавливаются концентрации каждого компонента). Здесь дано значение константы для стандартных условий — температуры 22 °С.
Внизу в квадратных скобках — молярные концентрации указанных компонентов. Молярная концентрация воды в воде — приблизительно 55 моль/литр, то есть величина второго порядка. Следовательно, произведение концентраций ионов H+ и OH- — около 10-14. Эта величина называется ионным произведением воды.
В чистой воде концентрации ионов водорода и гидроксид-ионов равны 10-7. Соответственно, водородный показатель воды будет приблизительно 7. Это значение pH принимают за нейтральную среду.

Далее нужно отвлечься от воды и рассмотреть раствор какой-нибудь кислоты или щелочи. Возьмем, например, уксусную кислоту. Ионное произведение воды останется прежним, однако баланс между ионами H+ и OH- сместится в сторону первых: ионы водорода придут от частично продиссоциировавшей уксусной кислоты, а «лишние» гидроксид-ионы уйдут в недиссоциировавшие молекулы воды. Таким образом, концентрация ионов водорода будет выше, и pH будет меньше (не надо забывать, что логарифм берется со знаком «минус»). Соответственно, кислая среда и щелочная среда связаны с pH. И связаны следующим образом. Чем меньше значение водородного показателя, тем более кислая среда.
Свойства кислой среды
Кислая среда — это растворы с pH меньше 7. Следует оговориться, что, хотя значение ионного произведения воды на первый взгляд ограничивает значения водородного показателя в пределах от 1 до 14, на самом деле растворы с pH меньше единицы (и даже меньше нуля) и больше 14 существуют. Например, в концентрированных растворах сильных кислот (серной, соляной) pH может достигать -2.
Вам будет интересно:Термин таймшит. Таймшит — это…
От того, имеем ли мы кислую среду или среду щелочную, может зависеть растворимость некоторых веществ. Например, возьмем гидроксиды металлов. Растворимость определяется величиной произведения растворимости, которое по структуре есть то же, что и ионное произведение воды: перемноженные концентрации. В случае с гидроксидом в произведение растворимости входит концентрация иона металла и концентрация гидроксид-ионов. В случае избытка ионов водорода (в кислой среде) они будут активнее «вырывать» гидроксид-ионы из осадка, тем самым смещая равновесие в сторону растворенной формы, повышая растворимость осадка.
Также стоит упомянуть, что весь пищеварительный тракт человека имеет кислую среду: pH желудочного сока колеблется от 1 до 2. Отклонение от этих значений в меньшую или большую сторону может являться признаком различных заболеваний.
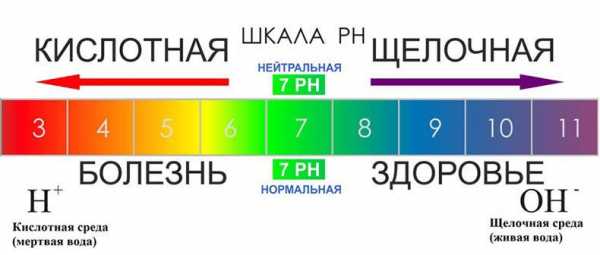
Свойства щелочной среды
В щелочной среде водородный показатель принимает значения, превышающие 7. Для удобства в средах с высокой концентрацией гидроксид-ионов вместо водородного показателя кислотности pH пользуются показателем основности pOH. Нетрудно догадаться, что он обозначает величину, равную -lg[OH-] (отрицательный десятичный логарифм концентрации гидроксид-ионов). Непосредственно из ионного произведения воды следует равенство pH + pOH =14. Поэтому pOH = 14 — pH. Таким образом, у всех утверждений, верных для показателя кислотности pH, верны обратные утверждения для показателя основности pOH. Если pH щелочной среды большой по определению, то ее pOH, очевидно, маленький, и чем сильнее раствор щелочи, тем меньше показатель pOH.
В этом предложении только что появился логический парадокс, вносящий путаницу во многие рассуждения о кислотности: маленький показатель кислотности обозначает высокую кислотность среды, и наоборот: большие значения pH соответствуют низкой кислотности. Этот парадокс появляется потому, что логарифм берется со знаком минус, и шкала кислотности как бы инвертируется.
Практическое определение кислотности
Для определения кислотности среды применяются так называемые индикаторы. Обычно это достаточно сложно устроенные органические молекулы, которые меняют свой цвет в зависимости от pH среды. Индикатор меняет свой цвет в очень узком интервале pH: это используется в кислотно-основном титровании, чтобы добиться точных результатов: титрование прекращают, как только индикатор меняет цвет.
Наиболее известные индикаторы — метиловый оранжевый (интервал перехода в области с маленьким pH), фенолфталеин (интервал перехода в области с большим pH), лакмус, тимоловый голубой и другие. В кислых средах и щелочных средах применяются разные индикаторы в зависимости от того, в какой области лежит их интервал перехода.
Существуют также универсальные индикаторы — они меняют свой цвет постепенно с красного на глубоко фиолетовый при переходе из сильно кислотных сред в сильно щелочные. На самом деле универсальные индикаторы представляют собой смесь из обычных.
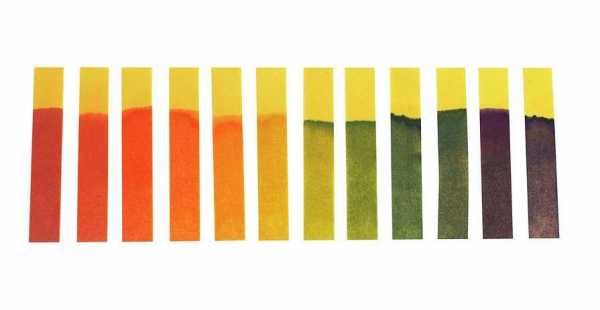
Для более точного определения кислотности используют прибор — pH-метр (потенциометр, метод, соответственно, называется потенциометрия). Его принцип работы основан на измерении ЭДС в цепи, элементом которой является раствор с измеряемым pH. Потенциал электрода, погруженного в раствор, чувствителен к концентрации ионов водорода в растворе — отсюда изменение ЭДС, на основании которого рассчитывается реальный pH.

Кислотность различных сред в быту
Показатель кислотности имеет большое значение в повседневной жизни. Например, слабые кислоты — уксусная, яблочная — используются в качестве консервантов. Щелочные растворы являются моющими средствами, в том числе и мыло. Самое простое мыло представляет собой натриевые соли жирных кислот. В воде они диссоциируют: остаток жирной кислоты — очень длинный — с одной стороны имеет отрицательный заряд, а с другой своей стороны — длинную неполярную цепочку атомов углерода. Тот конец молекулы, на котором заряд участвует в гидратации, собирает вокруг себя молекулы воды. Второй конец присоединяется к другим неполярным вещам, например, молекулам жира. В результате образуются мицеллы — шарики, у которых наружу торчат «хвосты» с отрицательным зарядом, а внутри спрятаны «хвосты» и частички жира и грязи. Поверхность отмывается от жира и грязи за счет того, что моющее средство связывает весь жир и грязь в такие мицеллы.
Кислотность и здоровье
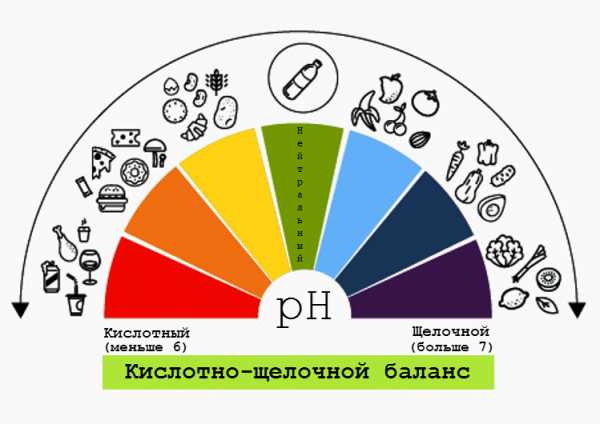
Уже было упомянуто, что pH имеет большое значение для человеческого организма. Кроме пищеварительного тракта, показатель кислотности важно контролировать и в других частях организма: кровь, слюна, кожа — для многих биологических процессов имеют большое значение кислая среда и щелочная среда. Их определение позволяет оценить состояние организма.
Сейчас набирают популярность pH-тесты — так называемые экспресс-тесты для проверки кислотности. Они представляют собой обычные полоски универсальной индикаторной бумаги.
Источник
1ku.ru
Водородный показатель pH. Таблицы показателей pH.
Что такое pH . Водородный показатель. Кислые и основные (щелочные) свойства растворов / сред.
pH = -log [H+], или еще строже говоря pH = -log [H3O+] (химики утверждают, что именно в таком виде положительный ион водорода живет в водном растворе). pH показывает кислотно / щелочной балласнс раствора, а не кислотность или щелочность (основность) отдельно.
pH измеряется в степенях числа 10. Концентрация ионов водорода в растворесс pH 1.0 в 10 раз выше, чем концентрация ионов водорода в растворе с pH 2.0. Чем выше концентрация ионов водорода, тем ниже pH
- при pH > 7 раствор щелочной (основной)
- при pH < 7 раствор кислый, или кислотный
В чистой нейтральной воде концентрация ионов водорода и гидроксильных ионов = гидроксид-ионов = OH— обе равны 10-7 моль/л.
| pH | Концентрация ионов моль/л | Тип раствора / какие ионы |
| 0 | 1.0 | Кислотный раствор (кислый) / |
| 1 | 0.1 | |
| 2 | 0.01 | |
| 3 | 0.001 | |
| 4 | 0.0001 | |
| 5 | 0.00001 | |
| 6 | 0.000001 | |
| 7 | 0.0000001 | Нейтральный раствор |
| 8 | 0.000001 | Основной (щелочной) раствор / гидроксильные ионы OH— |
| 9 | 0.00001 | |
| 10 | 0.0001 | |
| 11 | 0.001 | |
| 12 | 0.01 | |
| 13 | 0.1 | |
| 14 | 1.0 |
В целом химическая теория — сложнее, но pH отличный практический показатель «кислотности» ,» щелочности» и «нейтральности».
Изменение окраски кислотно-основных индикаторов в зависимости от pH раствора. Лакмус, фенолфтолеин, метилоранж.
Название | Окраска индикатора в среде | ||
Кислая [H+]* > [OH-] | Нейтральная[H+] = [OH-] | Щелочная [OH-] > [H+] | |
Лакмус | красный | фиолетовый | синий |
Фенолфталеин | бесцветный | бесцветный | малиновый |
Метилоранж | розовый | оранжевый | желтый |
* [ x ] — концентрация ионов ‘x’
Таблица pH бытовых веществ, материалов и продуктов.
| Вещество | pH |
|---|---|
| Электролит в свинцовых аккумуляторах | <1.0 |
| Желудочный сок | 1,0—2,0 |
| Лимонный сок | 2,5±0,5 |
| Лимонад Кола | 2,5 |
| Уксус | 2,9 |
| Яблочный сок | 3,5±1,0 |
| Пиво | 4,5 |
| Кофе | 5,0 |
| Модный шампунь | 5,5 |
| Чай | 5,5 |
| Кислотный дождь | < 5,6 |
| Кожа здорового человека | ~6,5 |
| Слюна | 6,35—6,85 |
| Молоко | 6,6-6,9 |
| Чистая вода | 7,0 |
| Кровь | 7,36—7,44 |
| Морская вода | 8,0 |
| Мыло (жировое) для рук | 9,0—10,0 |
| Нашатырный спирт | 11,5 |
| Отбеливатель (хлорка) | 12,5 |
| Раствор соды | 13,5 |
Водородный показатель (pH) некоторых распространенных продуктов питания.
Продукт | Приблизительный | Продукт | Приблизительный |
| Абрикосовый нектар | 3.8 | Малина | 3.2 — 3.6 |
| Абрикосы | 3.3 — 4.8 | Мамалыга | 6.8 — 8.0 |
| Авокадо | 6.3 — 6.6 | Манго | 5.8 — 6.0 |
| Алое Вера | 6.1 | Маслины | 6.0 — 7.0 |
| Апельсины | 3.0 — 4.0 | Масло | 6.1 — 6.4 |
| Арахисовое масло | 6.3 | Меласса (черная патока) | 4.9 — 5.4 |
| Арбуз | 5.2 — 5.6 | Молоко | 6.4 — 6.8 |
| Артишоки | 5.5 — 6.0 | Морковь | 5.9 — 6.3 |
| Бананы | 4.5 — 5.2 | Морское ушко | 6.1 — 6.5 |
| Батат (сладкий картофель) | 5.3 — 5.6 | Мука пшеничная | 5.5 — 6.5 |
| Батат (сладкий картофель), вареный. | 5.5 — 6.8 | Мякоть томата | 4.3 — 4.5 |
| Белый хлеб | 5.0 — 6.2 | Нектарины | 3.9 — 4.2 |
| Бобы | 5.6 — 6.5 | Овощной сок | 3.9 — 4.3 |
| Брокколи | 5.3 | Окунь, морской, жаренный | 6.6 — 6.8 |
| Вино | 2.8 — 3.8 | Оливки | 3.6 — 3.6 |
| Виноград | 3.5 — 4.5 | Пахта | 4.4 — 4.8 |
| Вишня | 3.2 — 4.5 | Персики | 3.4 — 4.1 |
| Газированные напитки | 2.0 — 4.0 | Печень трески | 6.2 |
| Горох | 5.8 — 6.4 | Пиво | 4.0 — 5.0 |
| Горчица | 3.5 — 6.0 | Питьевая вода | 6.5 — 8.0 |
| Грейпфрут | 3.0 — 3.7 | Помидоры | 4.3 — 4.9 |
| Груши | 3.6 — 4.0 | Ревень | 3.1 — 3.2 |
| Дыня | 6.0 — 6.7 | Сардины | 5.7 — 6.6 |
| Ежевика | 3.9 — 4.5 | Свежие яйца | 7.6 — 8.0 |
| Изюм | 2.8 — 3.0 | Свекла | 4.9 — 6.6 |
| Кактус | 4.7 | Сельдерей | 5.7 — 6.0 |
| Кальмары | 5.8 | Сельдь | 6.1 |
| Каперсы | 6.0 | Сидр | 2.9 — 3.3 |
| Капуста | 5.2 — 5.4 | Соевое молоко | 7.0 |
| Каракатица | 6.3 | Соевый соус | 4.4 — 5.4 |
| Карп | 6.0 | Соус Карри | 6.0 |
| Картофель | 5.6 — 6.0 | Соус Чили | 2.8 — 3.7 |
| Кетчуп | 3.9 | Спаржа | 6.0 — 6.7 |
| Кислая капуста | 3.4 — 3.6 | Сыр | 4.8 — 6.4 |
| Кленовый сироп | 4.6 — 5.5 | Томатный сок | 4.1 — 4.6 |
| Клубника, земляника | 3.0 — 3.9 | Тунец | 5.9 -6.1 |
| Клубничный (земляничный) джем | 3.0 — 3.4 | Турнепс (репа) | 5.2 — 5.6 |
| Клюквенный сок | 2.3 — 2.5 | Тыква | 4.8 — 5.2 |
| Кокос | 5.5 — 7.8 | Уксус | 2.4 — 3.4 |
| Кокосовое молоко | 6.1 — 7.0 | Уксус яблочный | 3.1 |
| Крабовое мясо | 6.5 — 7.0 | Устрицы | 5.7 — 6.2 |
| Красный перец | 4.6 — 5.2 | Финики | 6.5 — 8.5 |
| Креветки | 6.8 — 7.0 | Фруктовое желе | 2.8 — 3.4 |
| Крекеры | 6.5 — 8.5 | Фруктовый джем | 3.5 — 4.0 |
| Крыжовник | 2.8 — 3.1 | Фруктовый коктейль | 3.6 — 4.0 |
| Кукуруза | 5.9 — 7.3 | Херес | 3.4 |
| Курага( сушеные абрикосы) | 3.4 — 3.8 | Хрен | 5.4 |
| Лайм | 1.8 — 2.0 | Чай | 7.2 |
| Лаймовый сок | 2.0 — 2.4 | Черника | 3.1 — 3.4 |
| Лимоны | 2.2 — 2.4 | Шпинат | 5.5 — 6.8 |
| Лимонный сок | 2.0 — 2.6 | Яблоки | 3.3 — 3.9 |
| Лосось | 6.1 — 6.3 | ||
| Лук-порей | 5.5 — 6.2 |
Таблица. Значения pH оснований, щелочей (растворы)
Значения pH для некоторых распространенных оснований и щелочей приведены в таблице ниже.
Основания, щелочи | Нормальность раствора | pH |
| Аммиак /Ammonia | н. | 11.5 |
| Аммиак /Ammonia | 0.1 н. | 11.1 |
| Аммиак /Ammonia | 0.01 н. | 10.6 |
| Ацетат натрия / Sodium acetate | 0.1 н. | 8.9 |
| Барбитал — натрий / Barbital sodium | 0.1 н. | 9.4 |
| Бензойнокислый натрий /Sodium benzoate | 0.1 н. | 8.0 |
| Бикарбонат калия / Potassium bicarbonate | 0.1 н. | 8.2 |
| Бикарбонат натрия /Sodium bicarbonate | 0.1 н. | 8.4 |
| Гидроокись железа /Ferrous hydroxide | насыщенный | 9.5 |
| Гидроокись калия / Potassium hydroxide | н. | 14.0 |
| Гидроокись калия / Potassium hydroxide | 0.1 н. | 13.0 |
| Гидроокись калия / Potassium hydroxide | 0.01 н. | 12.0 |
| Гидроокись кальция /Calcium hydroxide | насыщенный | 12.4 |
| Гидроокись натрия / Sodium hydroxide | н. | 14.0 |
| Гидроокись натрия / Sodium hydroxide | 0.1 н. | 13.0 |
| Гидроокись натрия / Sodium hydroxide | 0.01 н. | 12.0 |
| Карбонат кальция / Calcium carbonate | насыщенный | 9.4 |
| Метасиликат натрия / Sodium metasilicate | 0.1 н. | 12.6 |
| Оксид магнияия / Magnesia | насыщенный | 10.5 |
| Пироборнокислый натрий (Бура)/ Borax | 0.01 н. | 9.2 |
| Сесвикарбонат натрия / Sodium sesquicarbonate | 0.1 н. | 10.1 |
| Тринатрийфосфат / Trisodium phosphate | 0.1 н. | 12.0 |
| Углекислый калий / Potassium carbonate | 0.1 н. | 11.5 |
| Углекислый натрий / Sodium carbonate | 0.1 н. | 11.6 |
| Уксуснокислый калий / Potassium acetate | 0.1 н. | 9.7 |
| Цианид калия / Potassium cyanide | 0.1 н. | 11.0 |
Таблица значений PH кислот. (Растворов).
В таблице представлены серная, уксусная и другие распространенные кислоты.
pH- это мера активности ионов водорода в растворах, и, таким образом, их кислотности или щелочности. Таким образом, в таблице ниже указана кислотность некоторых обычных кислот.
Кислота | Нормальность раствора | pH |
| Азотная / Nitric | 0.1н. | 1.0 |
| Алюминиевые квасцы / Alum | 0.1 н. | 3.2 |
| Бензойная / Benzoic | 0.1 н. | 3.0 |
| Борная / Boric | 0.1 н. | 5.2 |
| Винная / Tartaric | 0.1 н. | 2.2 |
| Желудочный сок / Stomach Acid | 1 | |
| Лимонная / Citric | 0.1н. | 2.2 |
| Лимонный сок / Lemon Juice | 2 | |
| Молочная / Lactic | 0.1 н. | 2.4 |
| Муравьиная / Formic | 0.1 н. | 2.3 |
| Мышьяковистая / Arsenious | насыщенный | 5.0 |
| Оксиянтарная (яблочная) / Malic | 0.1 н. | 2.2 |
| Ортофосфорная / Orthophosphoric | 0.1 н. | 1.5 |
| Салициловая / Salicylic | насыщенный | 2.4 |
| Серная / Sulfuric | н. | 0.3 |
| Серная / Sulfuric | 0.1 н. | 1.2 |
| Серная / Sulfuric | 0.01 н. | 2.1 |
| Сернистая / Sulfurous | 0.1 н. | 1.5 |
| Сероводородная / Hydrogen sulfide | 0.1 н. | 4.1 |
| Трихлороуксусная / Trichloracetic | 0.1 н. | 1.2 |
| Угольная (Углеродная) / Carbonic | насыщенный | 3.8 |
| Уксус столовый (3-15%) / Vinegar | 3 | |
| Уксусная / Acetic | 2.4 | |
| Уксусная / Acetic | 0.1 н. | 2.9 |
| Уксусная / Acetic | 0.01 н. | 3.4 |
| Хлористоводородная / Hydrochloric | н. | 0.1 |
| Хлористоводородная / Hydrochloric | 0.1 н. | 1.1 |
| Хлористоводородная / Hydrochloric | 0.01 н. | 2.0 |
| Цианистоводородная (синильная) / Hydrocyanic | 0.1 н. | 5.1 |
| Щавелевая / Oxalic | 0.1 н. | 1.3 |
| Янтарная / Succinic | 0.1н. | 2.7 |
Возможно, вам это будет интересно:
meandr.org
Кислотно-щелочной баланс организма (рН-баланс), или Кислотно-щелочное равновесие (КЩР)

Можете ли вы себе представить, что развитие многих болезней зависит от одной причи-ны? Многие специалисты диетологи и фитотерапевты эту скрытую опасность теперь обозначают двумя словами: кислота и щелочь.
Высокая кислотность разрушает наиважнейшие системы в организме и он становится беззащитен перед болезнями. Сбалансированная pH-среда обеспечивает нормальное протекание метаболических процессов в организме, помогая ему бороться с заболеваниями. Здоровый организм имеет запас щелочных веществ, которые он использует в случае необходимости.
Что такое pH?
Соотношение кислоты и щелочи в каком-либо растворе называется кислотно-щелочным равновесием (КЩР), хотя физиологи считают, что более правильно называть это соот-ношение кислотно-щелочным состоянием. КЩР характеризуется специальным показа-телем pH (power Hidrogen – «сила водорода”), который показывает число водородных атомов в данном растворе. При pH равном 7,0 говорят о нейтральной среде. Чем ниже уровень pH – тем среда более кислая (от 6,9 до 0). Щелочная среда имеет высокий уро-вень pH (от 7,1 до 14,0).
Тело человека на 80% состоит из воды, поэтому вода – это одна из наиболее важных его составляющих. Тело человека имеет определенное кислотно-щелочное соотношение, характеризуемое pH (водородным) показателем. Значение показателя pH зависит от соотношения между положительно заряженными ионами (формирующими кислую среду) и отрицательно заряженными ионами (формирующими щелочную среду). Организм че-ловека постоянно стремится уравновесить это соотношение, поддерживая строго опре-деленный уровень pH. При нарушенном балансе могут возникать множество серьезных заболеваний.
рН, или показатель кислотно-щелочного равновесия.
Это мера относительной концентрации водородных (Н+) и гидроксильных (ОН—) ионов в жидкой системе и выражается в масштабе от 0 (полное насыщение ионами водорода Н+) до 14 (полное насыщение гидроксильными ионами ОН—), дистиллированная вода считается нейтральной с рН 7,0.
Повышение концентрации положительных ионов водорода (Н+) в любой из жидких сред организма вызывает смещение значений рН в сторону нуля и носит название кислотного сдвига.
Повышение концентрации гидроксильных ионов OН вызывает смещение значений рН в сторону значения 14 и носит название щелочного сдвига.
Проверьте свой кислотно-щелочной баланс с помощью
pH тест-полосокС помощью pH тест-полосок можно легко, быстро и точно определить уровень pH, не выходя из дома. Если уровень pH мочи колеблется в пределах 6,0-6,4 утром и 6,4-7,0 вечером, то ваш организм функционирует нормально. Если в слюне отметка уровня pH остается между 6,4-6,8 в течение всего дня – это также свидетельствует о здоровье ва-шего организма. Наиболее оптимальный уровень pH слюны и мочи слегка кислый, в пределах 6,4-6,5.
 Лучшее время для определения уровня pH – за 1 час до еды или спустя 2
часа после еды. Регулярно проверяйте уровень вашего pH.
Лучшее время для определения уровня pH – за 1 час до еды или спустя 2
часа после еды. Регулярно проверяйте уровень вашего pH.Изменение показателей рН-баланса могут привести к печальным последствиям:
А) Повышенная кислотность в организме (самый распространенный случай).
Из-за неправильного питания и употребления в пищу кислых продуктов, а также недос-татка воды происходит закисление организма. Большинство нынешних продуктов пита-ния кислые (батоны, булочки, газированные напитки, сахар и его заменители и т.д.). При закисленности организма ухудшается перенос кислорода к органам и тканям, организм плохо усваивает минералы, а некоторые минералы, такие как Ca, Na, K, Mg выводятся из организма. От недостатка минералов страдают жизненно важные органы, повышается риск сердечно сосудистых заболеваний, снижается иммунитет, появляется хрупкость костей и многое другое. Если в организме находится большое количество кислоты и на-рушены механизмы ее вывода (с мочой и калом, с дыханием, с потом и т.д.), организм подвергается сильнейшей интоксикации. Единственный выход – это ощелачивание ор-ганизма.
Состояние повышенной кислотности называется — Ацидоз. Не выявленный вовремя аци-доз может вредить организму незаметно, но постоянно в течение нескольких месяцев и даже лет. Злоупотребление алкоголем часто приводит к ацидозу. Ацидоз может возни-кать, как осложнение диабета.
При Ацидозе могут появиться следующие проблемы:
Заболевания сердечно-сосудистой системы, включая стойкий спазм сосудов и уменьшение концентрации кислорода в крови. Прибавление в весе и диабет.
Заболевания почек и мочевого пузыря, образование камней.
Снижение иммунитета. Общая слабость.
Увеличение вредного воздействия свободных радикалов, которые могут способ-ствовать онкогенезу. Хрупкость костей вплоть, до перелома шейки бедра, а также других нарушениях опорно-двигательного аппарата, как например, образование остеофитов (шпор). Появление суставных болей и болевых ощущений в мышцах, связанных с нако-плением молочной кислоты.
В течение 7 лет, проводилось исследование в Калифорнийском Университете (штат Сан-Франциско), где были обследованы 9 тыс. женщин. Результаты показали, что при постоянном повышенном уровне кислотности кости становятся ломкими. Специалисты, проводившие этот эксперимент, уверены, что большинство проблем женщин среднего возраста связано с излишним употреблением мясной и недостатком употребления овощной пищи. Поэтому организму ничего не остается, как забирать кальций из соб-ственных костей, и с его помощью регулировать уровень рН.
Б) Повышенное содержание щёлочи в организме.
При повышенном содержании щелочи в организме, а это состояние называется Алкалоз, также как при ацидозе, нарушается усвоение минералов. Пища усваивается гораздо медленнее, что позволяет токсинам проникать из желудочно-кишечного тракта в кровь. Повышенное содержание щелочи в организме опасно и трудно поддается корректиров-ке, но случается это довольно редко. Как правило, алкалоз является результатом упот-ребления лекарств, содержащих щелочь.
Повышенное содержание щелочи может спровоцировать:
• Проблемы с кожей и печенью.
• Сильный и неприятный запах изо рта и тела.
• Активизацию жизнедеятельности паразитов.
• Разнообразные аллергические проявления, в том числе связанные с пищей и загрязнением окружающей среды.
• Обострение хронических заболеваний.
• Запоры и другие проблемы с кишечником.
Значение рН мочи
Результаты рН тестов мочи показывают, насколько хорошо организм усваивает минералы, такие как кальций, натрий, калий и магний. Эти минералы называ-ют «кислотными демпферами», так как они регулируют уровень кислотности в организме. Если кислотность слишком высокая, организм не продуцирует кислоту. Он должен ней-трализовать кислоту. Для этого организм начинает заимствовать минералы из различ-ных органов, костей, мышц и проч. для того, чтобы нейтрализовать излишки кислоты, которая начинает накапливаться в тканях. Таким образом, происходит регулирование уровня кислотности.
Значение рН слюны
Рационально также знать уровень рН слюны. Результаты тестиро-вания показывают активность ферментов пищеварительного тракта, особенно печени и желудка. Этот показатель дает представление о работе как всего организма в целом так и отдельных его систем. Некоторые люди могут иметь повышенную кислотность, как мо-чи, так и слюны — в таком случае мы имеем дело с «двойной кислотностью».
Значение рН крови рН крови одна из самых жестких физиологических констант орга-низма. В норме этот показатель может меняться в пределах 7,3б — 7,42. Сдвиг этого по-казателя хотя бы на 0,1 может привести к тяжелой патологии. Заметьте, в экстренных случаях врачи первым делом делают укол слабо-щелочного раствора (физраствор) в кровь.
При сдвиге рН крови на 0,2 развивается коматозное состояние, на 0,3 — человек погибает.
Поддерживайте правильный рН баланс для сохранения крепкого здоровья
Организм способен правильно усваивать и накапливать минералы и питательные веще-ства только при надлежащем уровне кислотно-щелочного равновесия. В ваших силах помочь своему организму получать, а не терять полезные вещества. Например, железо может усваиваться организмом при рН 6,0-7,0, а йод — при рН 6,3-6,6. Наш организм ис-пользует соляную кислоту для расщепления пищи. В процессе жизнедеятельности орга-низма требуются как кислые, так и щелочные продукты распада, причем первых образу-ется в 20 раз больше, нежели вторых. Поэтому защитные системы организма, обеспечи-вающие неизменность его КЩР, «настроены» прежде всего на нейтрализацию и выведе-ние прежде всего кислых продуктов распада.
Основными механизмами поддержания этого равновесия являются: буферные системы крови (карбонатная, фосфатная, белковая, гемоглобиновая), респираторная (легочная) система регуляции, почечная (выделительная система).
В Ваших интересах поддерживать правильный рН-баланс.
Даже «самая правильная» программа питания, либо программа лечения каких либо болезней не будет эффективно работать, если ваш рН-баланс организма нарушен.
Как организм управляет уровнем кислотности:
• Выделяет кислоты — через желудочно-кишечный тракт, почки, легкие, кожу;
• Нейтрализует кислоты — с помощью минералов: кальций, магний, калий, натрий;
• Накапливает кислоты — в тканях, прежде всего в мышцах.
Отто Варбург потратил 24 года своей жизни на то, чтобы доказать тот факт, что в среде, насыщенной кислородом, при pH 7,43 и выше (слабощелочная среда), ра-ковые клетки не размножаются. В 1932 году он получил за это Нобелевскую пре-мию по химии. А его ученики позже доказали, что в этой среде не развиваются па-разиты, вирусы, бактерии и грибки.
Что делать, если pH-баланс в норме?
Ответ простой – способствовать сохранению этого баланса в здоровой зоне.
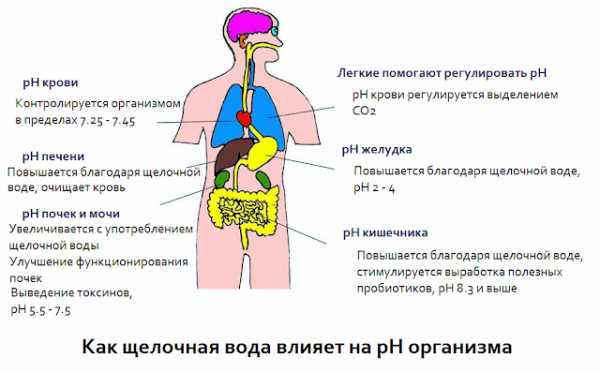
1. Вода.
Необходимо пить достаточное количество чистой воды, а конкретно — 30 мл на кило-грамм веса в день.
2. Еда.
Если кислотно щелочное равновесие уже нарушено, то стоит задуматься о своем
питании, и уменьшить потребление кислой еды (батоны, булочки, чипсы, сладости,
газированные напитки и т.д.).


3. Ферменты.
Без ферментов организм не способен регулировать уровень pH. Они оздоравливают и улучшают пищеварение, усвояемость минералов (особенно кальция). Чтобы пополнить свой рацион дополнительными ферментами рекомендуем цветочную пыльцу.

4. Коррекция минерального обмена.
Кальций – самый важный минерал для регулирования pH-баланса.
Кроме указанного выше кальция, организму необходимы другие минералы, в том числе фосфор, цинк, бор, калий, магний. Они все реже встречаются в нашем рационе из-за того, что проводится очищение пищевого сырья, пища подвергается чрезмерной кули-нарной обработке, овощи и фрукты, выращенные на истощенной почве, изначально не содержат полный набор минеральных веществ. vashe-zdorovie.ru
Кислотно-щелочной баланс нашего организма
Огулов А.Т. Кислотно-щелочное равновесие и сода
www.vedamost.info
