Полимилекс
ПОЛИМИЛЕКС
вакцина для профилактики полиомиелита инактивированная
(Производство прививочного состава Полимилекс осуществляет как российский производитель OOO “Нанолек”, так и расположенная на территории Нидерландов компания Билтховен Биолоджикалз)
Полиомиелит — Это острое вирусное заболевание, поражающее центральную нервную систему, в первую очередь спинной мозг. Часто после перенесенного заболевания развиваются стойкие параличи с явлениями атрофии, деформации, приводящие к инвалидности.
Болеют преимущественно дети до 10 лет (60-80% — приходится на детей до 4 лет).
Полиомиелит неизлечим, его можно только предотвратить!!!
Поэтому единственной мерой эффективной и длительной защиты от полиомиелита является вакцинация.
Первые 2 вакцинации против полиомиелита проводят вакциной ИПВ в сроки, установленные национальным календарем профилактических прививок, — детям до года, а также детям более старшего возраста, не получившим прививки против полиомиелита ранее.
Сохраняющийся для России РИСК ЗАНОСА дикого возбудителя полиомиелита из граничащих государств (Афганистан, Пакистан) обусловливают необходимость сочетанного применения живой и инактивированной полиовакцин в рамках рутинной иммунизации.
Оральная вакцина вызывает не только гуморальный иммунитет, но и тканевый, чего невозможно достичь с помощью инактивированного препарата.
Возможные побочные эффекты:
Прививка препаратом Полимилекс переносится хорошо. Однако в некоторых случаях возможно появление неприятных симптомов: вялости, ощущения слабости или усталости, а также повышения температуры до 37 С. Перечисленные признаки являются естественной реакцией организма на вторжение инфекционного агента. Такие симптомы обычно проходят в течение первых 2-3 суток и не считаются серьезными осложнениями. При повышении температуры ребенку необходимо дать жаропонижающий препарат в возрастной дозе (Ибуклин, Нурофен), при появлении местной реакции – использовать противоэкссудативную (противоотечную) мазь (Троксевазин, Траумель).
Учитывая возможность развития аллергических реакций немедленного типа у особо чувствительных детей, за привитыми необходимо обеспечить медицинское наблюдение в течение 30 минут.
В России зарегистрированы следующие вакцины от полиомиелита:
— БиВак полио (Вакцина полиомиелитная пероральная, двухвалентная, живая аттенуированная 1, 3 типов) – препарат капается в рот.
http://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=b4c16c3b-2f61-4ad9-8f8d-83b726ff8fbe&t=
— Полимилекс – (вакцина против полиомиелита, содержащая три типа (1, 2, 3) инактивированного полиовируса) -предназначена для внутримышечного или подкожного введения.
http://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=b8626f1c-ca5f-48cf-9b03-809121e07b70&t=
Также, имеются комбинированные вакцины, защищающие от нескольких инфекций, включая полиомиелит:
— Пентаксим фирмы Санофи Пастер С. А., Франция (вакцина для профилактики дифтерии, коклюша, полиомиелита, столбняка и гемофильной инфекции).
А., Франция (вакцина для профилактики дифтерии, коклюша, полиомиелита, столбняка и гемофильной инфекции).
http://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=f169b74f-1612-4c41-886f-23afd7180254&t=
— Инфанрикс-гекса фирмы ГлаксоСмитКляйн, Бельгия. (вакцина против коклюша, дифтерии и полиомиелита, столбняка, вирусного гепатита В и гемофильной инфекции).
http://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=526fd45a-0b08-4d0f-8a43-72c72b4f35f3&t=
Более подробную информацию по вакцинам вы сможете получить по представленным ссылкам.
Поделиться:
МАНИПУЛЯЦИЯ: В состав вакцин входят вирусы, вызывающие рак
Проверка фейков в рамках партнерства с Facebook
Сетью распространяют изображения с подписями о том, что официальные органы США вроде признали, что в вакцинах могут содержаться вирусы, вызывающие рак, и что вакцины — это «рак в шприце»:
Обычно вакцина от конкретного вируса включает в себя именно этот вирус. Например, вакцина от кори содержит вирус кори. А вирусы, вызывающие рак, добавляют только в те вакцины, которыми человека иммунизируют от этих канцерогенных вирусов.
Например, вакцина от кори содержит вирус кори. А вирусы, вызывающие рак, добавляют только в те вакцины, которыми человека иммунизируют от этих канцерогенных вирусов.
Онкологические заболевания могут быть вызваны вирусом Эпштейна-Барр, вирусом папилломы человека (ВПЧ), вирусами гепатитов В и С, герпесвирусом человека 8-го типа и лимфотропным вирусом человека типа 1. Сейчас существуют вакцины только от ВПЧ и вируса гепатита B. В состав вакцины от ВПЧ входят только белки вируса папилломы человека типов 6, 11, 16 и 18. Вакцины против гепатита В содержат один из белков из оболочки вируса гепатита В (поверхностный антиген HepB или HBsAg).
В состав любых других вакцин вирусы, которые вызывают рак, не входят.
В 1960-х годах в США обнаружили, что одна из вакцин от полиомиелита была загрязнена вирусом SV40, который потенциально способствует росту опухолей. Однако исследования относительно риска заболевания раком в результате вакцинации против полиомиелита не находят достаточно доказательств, что эта вакцина могла вызвать рак.
К тому же в вакцины добавляют живые ослабленные или мертвые вирусы (или вообще только их частицы), поэтому они не могут спровоцировать заболевание. Вакцина помогает организму развить иммунитет, имитируя болезнь. Она заставляет иммунную систему вырабатывать антитела и Т-лимфоциты к возбудителю, но человек не болеет.
Вакцины, содержащие вирусы, вызывающие рак, не являются канцерогенами — они не вызывают онкологию. Организм наоборот развивает определенный уровень защиты от этих заболеваний. Поэтому утверждать, что вакцина — это «рак в шприце», неправильно.
Все о вакцинации. Виды вакцин
СОДЕРЖАНИЕ
Что такое вакцинопрофилактика? Это система мероприятий, осуществляемых в целях предупреждения, ограничения распространения и ликвидации инфекционных болезней путем проведения профилактических прививок. Вакцины защищают людей от очень тяжелых инфекционных болезней.
Вакцины защищают людей от очень тяжелых инфекционных болезней.
Еще несколько десятилетий назад врачам приходилось неустанно бороться с такими инфекциями, как натуральная оспа, полиомиелит, дифтерия, коклюш, корь, эпидемический паротит, краснуха. Многих больных спасти не удавалось, многие оставались инвалидами.
Все радикально изменилось с появлением вакцин. Мир полностью избавлен от натуральной оспы, во многих странах ликвидирован полиомиелит, резко сократилось число и тяжесть течения дифтерии, коклюша, кори, краснухи, эпидемического паротита. С помощью прививок врачи научились бороться с такой инфекцией, как гепатит В, который чрезвычайно опасен возможностью формирования хронического поражения печени (цирроз, рак).
Человеку свойственно быстро забывать неприятные для него вещи: вот и вспышки инфекционных заболеваний, уносившие тысячи, а иногда и миллионы, человеческих жизней, забылись. По мнению некоторых, эпидемии инфекций – это пройденный этап в человеческой истории.
К сожалению – нет!
При снижении порога вакцинации возможна новая вспышка инфекций.
Например:
1973-1974 года – натуральная оспа в Стокгольме;
1990-1999 года – дифтерия в СССР;
Вспышка кори в г. Екатеринбурге в 2016-17 годах у непривитых от кори лиц.
Благодаря вакцинопрофилактике появилась возможность защиты от 40 инфекционных заболеваний. Часть из этих прививок ставят всему населению, часть – по эпидемическим показаниям. Это зависит от опасности распространения инфекции на данной территории.
Обязательными на всей территории России являются прививки против туберкулеза (БЦЖ), коклюша, дифтерии, столбняка, кори, эпидемического паротита, краснухи, пневмококковой и гемофильной (ХИБ) инфекций. На территории Свердловской области в календарь прививок включены прививки против клещевого энцефалита (вся территория области является опасной по возможности инфицирования клещевым энцефалитом), ветряной оспы (велика заболеваемость этой инфекцией), гепатита А.
Дети, организм которых ослаблен в силу разных причин врожденного или приобретенного характера, особенно подвержены инфекции, болеют тяжело, часто с осложнениями и возможным неблагоприятным исходом. Такие дети нуждаются в защите от инфекционных болезней в первую очередь.
КАЛЕНДАРЬ ПРИВИВОК
|
Возраст |
Наименование прививки |
|
Новорожденные в первые 24 часа жизни |
Первая вакцинация против гепатита В |
|
Новорожденные (при выписке из родильного дома) |
Вакцинация против туберкулеза |
|
1 месяц |
Вторая вакцинация против гепатита В |
|
2 месяца |
Первая вакцинация против пневмококковой инфекции Первая вакцинация против ротавирусной инфекции |
|
3 месяца |
Первая вакцинация против дифтерии, коклюша, столбняка Первая вакцинация против полиомиелита Первая вакцинация против гемофильной инфекции Вторая вакцинация против ротавирусной инфекции |
|
4,5 месяца |
Вторая вакцинация против дифтерии, коклюша, столбняка Вторая вакцинация против полиомиелита Вторая вакцинация против гемофильной инфекции Вакцинация против пневмококковой инфекции Третья вакцинация против ротавирусной инфекции |
|
6 месяцев |
Третья вакцинация против гепатита В Третья вакцинация против дифтерии, коклюша, столбняка Третья вакцинация против полиомиелита Третья вакцинация против гемофильной инфекции |
|
9 месяцев |
Первая вакцинация против менингококковой инфекции |
|
11 месяцев |
Вторая вакцинация против менингококковой инфекции |
|
12 месяцев |
Четвертая вакцинация против гепатита В Вакцинация против кори, краснухи, эпидемического паротита Вакцинация против ветряной оспы |
|
15 месяцев |
Ревакцинация против пневмококковой инфекции Первая вакцинация против клещевого энцефалита |
|
18 месяцев |
Первая ревакцинация против дифтерии, коклюша, столбняка Первая ревакцинация против полиомиелита Ревакцинация против гемофильной инфекции |
|
20 месяцев |
Вторая ревакцинация против полиомиелита Первая вакцинация против гепатита |
|
21 месяц |
Вторая вакцинация против клещевого энцефалита |
|
26 месяцев |
Вторая вакцинация против гепатита А |
|
2 года 6 месяцев |
Первая ревакцинация против клещевого энцефалита |
|
6 лет |
Ревакцинация против кори, краснухи, эпидемического паротита Вторая вакцинация против ветряной оспы |
|
6-7 лет |
Вторая ревакцинация против дифтерии, столбняка Ревакцинация против туберкулеза |
|
13 лет (обоего пола) |
Вакцинация против папилломавирусной инфекции |
|
14 лет |
Третья ревакцинация против дифтерии, столбняка Третья ревакцинация против полиомиелита |
АКДС
– это вакцина, защищающая от трех тяжелых инфекций – от коклюша, дифтерии и столбняка.

Коклюш вызывается коклюшной палочкой. Заболевание характеризуется приступами спазматического кашля, поражением дыхательной, сердечно-сосудистой и нервной систем. Происходит скапливание густой стекловидной мокроты в бронхах, которую тяжело откашлять и взрослому человеку. Ребенок «заходится» в кашле. Опасен коклюш и своими осложнениями, которые развиваются у 30% — 50% и выше заболевших: воспалением легких (пневмонией), а у маленьких детей – поражением головного мозга (энцефалопатией) с возможными повторными судорогами. При заболевании коклюшем непривитых детей в возрасте до года умереть может каждый пятый ребенок.
Дифтерия – инфекция, которую вызывает дифтерийная палочка. Клинические проявления заболевания обусловлены действием дифтерийного токсина (продукта жизнедеятельности дифтерийной палочки). Могут поражаться миндалины, зев, гортань, нос, кожа, слизистые оболочки. У непривитых заболевание характеризуется тяжелым течением с последующим развитием осложнений со стороны сердечнососудистой и нервной системы.

От дифтерии среди непривитых умирают 10 – 20% заболевших. Антибиотики при лечении дифтерии неэффективны, лечение проводят специфической противодифтерийной сывороткой, введение которой само может вызвать тяжелые аллергические состояния.
Столбняк – инфекция, которую вызывает столбнячная палочка. Это заболевание с явлениями выраженной интоксикации нервной системы, проявляющейся в виде тонических и клонических мышечных судорог. Смерть наступает от паралича дыхательной мускулатуры. От столбняка умирают от 67 до 91% заболевших.
В состав вакцины входят: коклюшная убитая вакцина, дифтерийный и столбнячный анатоксины (иммунитет к дифтерии и столбняку вырабатывается против токсинов, обуславливающих заболевание).
Вакцинация проводится с трехмесячного возраста трехкратно с интервалом в 1,5 месяца, затем в 1 год 6 месяцев проводится первая ревакцинация. Вакцины АКДС и инфанрикс взаимозаменяемые. АКДС вводится глубоко внутримышечно в передненаружную область бедра.
Зачем нужна ревакцинация?
С годами иммунитет к заболеванию может несколько снизиться. Для поддержания иммунитета на уровне, способном защитить организм от инфекции, проводятся ревакцинации.
Для поддержания иммунитета на уровне, способном защитить организм от инфекции, проводятся ревакцинации.
Введение любой вакцины вызывает ответную реакцию организма. Это начинает работать иммунная система в ответ на введение антигенов возбудителя. Иногда эти реакции имеют клинические проявления. Это обычные, нормальные вакцинальные реакции (процессы), под которыми понимают изменения в организме, развивающиеся с определенным постоянством после введения той или иной вакцины. Вакцинальные реакции бывают местными и общими.
Местная нормальная реакция – уплотнение тканей, краснота, не превышающая 8 см в диаметре, иногда легкая болезненность в месте введения вакцины; развивается сразу после введения препарата, проходит в течение 1-4 дней, встречается у 5 – 15 % привитых детей.
Общая нормальная реакция проявляется повышением температуры до 37,50 – 38,60С, иногда появляются нарушения сна, аппетита, недомогание.
К крайне редким тяжелым поствакцинальным реакциям относят: температуру более 400С, местную реакцию 8 см. в диаметре и более.
в диаметре и более.
Крайне редко встречаются осложнения: аллергические реакции местные и общие, осложнения со стороны нервной системы (судороги, продолжительный пронзительный крик, энцефалопатия). Эти состояния при тщательном расследовании часто оказываются заболеваниями, начало которых по времени совпадает с вакцинальным процессом.
ИНФАНРИКС
– это вакцина, защищающая от трех тяжелых инфекций – от коклюша, дифтерии и столбняка.
Коклюш вызывается коклюшной палочкой. Заболевание характеризуется приступами спазматического кашля, поражением дыхательной, сердечно-сосудистой и нервной систем. Происходит скапливание густой стекловидной мокроты в бронхах, которую тяжело откашлять и взрослому человеку. Ребенок «заходится» в кашле. Опасен коклюш и своими осложнениями, которые развиваются у 30% — 50% и выше заболевших: воспалением легких (пневмонией), а у маленьких детей – поражением головного мозга (энцефалопатией) с возможными повторными судорогами. При заболевании коклюшем непривитых детей в возрасте до года умереть может каждый пятый ребенок.
Дифтерия – инфекция, которую вызывает дифтерийная палочка. Клинические проявления заболевания обусловлены действием дифтерийного токсина (продукта жизнедеятельности дифтерийной палочки). Могут поражаться миндалины, зев, гортань, нос, кожа, слизистые оболочки. У непривитых заболевание характеризуется тяжелым течением с последующим развитием осложнений со стороны сердечнососудистой и нервной системы. От дифтерии среди непривитых умирают 10 – 20% заболевших. Антибиотики при лечении дифтерии неэффективны, лечение проводят специфической противодифтерийной сывороткой, введение которой само может вызвать тяжелые аллергические состояния.
Столбняк – инфекция, которую вызывает столбнячная палочка. Это заболевание с явлениями выраженной интоксикации нервной системы, проявляющейся в виде тонических и клонических мышечных судорог. Смерть наступает от паралича дыхательной мускулатуры. От столбняка умирают от 67 до 91% заболевших.
В состав вакцины входят: коклюшная бесклеточная вакцина, дифтерийный и столбнячный анатоксины (иммунитет к дифтерии и столбняку вырабатывается против токсинов, обуславливающих заболевание). За счет того, что коклюшная вакцина, входящая в состав вакцины «инфанрикс» не имеет поверхностной оболочки, тяжелые реакции и осложнения встречаются после ее введения много реже, чем после АКДС.
За счет того, что коклюшная вакцина, входящая в состав вакцины «инфанрикс» не имеет поверхностной оболочки, тяжелые реакции и осложнения встречаются после ее введения много реже, чем после АКДС.
Вакцинация проводится с трехмесячного возраста трехкратно с интервалом в 1,5 месяца, затем в 1 год 6 месяцев проводится первая ревакцинация. Вакцины АКДС и инфанрикс взаимозаменяемые. Учитывая сложную эпид. обстановку по коклюшу на территории Свердловской области, МЗ Свердловской области рекомендована 2 ревакцинация против коклюша вакциной «инфанрикс» в возрасте 6 лет. Инфанрикс вводится глубоко внутримышечно в передненаружную область бедра.
Зачем нужна ревакцинация? С годами иммунитет к заболеванию может несколько снизиться. Для поддержания иммунитета на уровне, способном защитить организм от инфекции, проводятся ревакцинации.
Введение любой вакцины вызывает ответную реакцию организма. Это начинает работать иммунная система в ответ на введение антигенов возбудителя. Иногда эти реакции имеют клинические проявления. Это обычные, нормальные вакцинальные реакции (процессы), под которыми понимают изменения в организме, развивающиеся с определенным постоянством после введения той или иной вакцины. Вакцинальные реакции бывают местными и общими.
Это обычные, нормальные вакцинальные реакции (процессы), под которыми понимают изменения в организме, развивающиеся с определенным постоянством после введения той или иной вакцины. Вакцинальные реакции бывают местными и общими.
Местная нормальная реакция – уплотнение тканей, краснота, не превышающая 8 см в диаметре, иногда легкая болезненность в месте введения вакцины; развивается сразу после введения препарата, проходит в течение 1-4 дней, встречается у 5 – 15 % привитых детей.
Общая нормальная реакция проявляется повышением температуры до 37,50 – 38,60С, иногда появляются нарушения сна, аппетита, недомогание.
К крайне редким тяжелым поствакцинальным реакциям относят: температуру более 400С, местную реакцию 8 см. в диаметре и более.
Крайне редко встречаются осложнения: аллергические реакции местные и общие, осложнения со стороны нервной системы (судороги, продолжительный пронзительный крик, энцефалопатия). Эти состояния при тщательном расследовании часто оказываются заболеваниями, начало которых по времени совпадает с вакцинальным процессом
АДС
– это вакцина, защищающая от двух тяжелых инфекций – от дифтерии и столбняка.

Дифтерия – инфекция, которую вызывает дифтерийная палочка. Клинические проявления заболевания обусловлены действием дифтерийного токсина (продукта жизнедеятельности дифтерийной палочки). Могут поражаться миндалины, зев, гортань, нос, кожа, слизистые оболочки. У непривитых заболевание характеризуется тяжелым течением с последующим развитием осложнений со стороны сердечнососудистой и нервной системы. От дифтерии среди непривитых умирают 10 – 20% заболевших. Антибиотики при лечении дифтерии неэффективны, лечение проводят специфической противодифтерийной сывороткой, введение которой само может вызвать тяжелые аллергические состояния.
Столбняк – инфекция, которую вызывает столбнячная палочка. Это заболевание с явлениями выраженной интоксикации нервной системы, проявляющейся в виде тонических и клонических мышечных судорог. Смерть наступает от паралича дыхательной мускулатуры. От столбняка умирают от 67 до 91% заболевших.
В состав вакцины входят: дифтерийный и столбнячный анатоксины, (иммунитет к дифтерии и столбняку вырабатывается против токсинов, обуславливающих заболевание).
Так как в состав вакцины не входит коклюшная вакцина, АДС применяется для вакцинации против дифтерии и столбняка у детей младше 6 лет при наличии противопоказаний к введению вакцины АКДС и Инфанрикс. Вакцина в этом случае вводится двукратно с интервалом 1,5 месяца. АДС вводится глубоко внутримышечно в передненаружную область бедра.
Введение любой вакцины вызывает ответную реакцию организма. Это начинает работать иммунная система в ответ на введение антигенов возбудителя. Иногда эти реакции имеют клинические проявления. Это обычные, нормальные вакцинальные реакции (процессы), под которыми понимают изменения в организме, развивающиеся с определенным постоянством после введения той или иной вакцины. Вакцинальные реакции бывают местными и общими.
Местная нормальная реакция – уплотнение тканей, краснота, не превышающая 8 см в диаметре, иногда легкая болезненность в месте введения вакцины; развивается сразу после введения препарата, проходит в течение 1-4 дней, встречается у 5 – 15 % привитых детей.
Общая нормальная реакция проявляется повышением температуры до 37,50 – 38,60С, иногда появляются нарушения сна, аппетита, недомогание.
К крайне редким тяжелым поствакцинальным реакциям относят: температуру более 400С, местную реакцию 8 см. в диаметре и более.
Крайне редко (много реже, чем при АКДС) встречаются осложнения: аллергические реакции местные и общие, осложнения со стороны нервной системы (судороги, продолжительный пронзительный крик, энцефалопатия). Эти состояния при тщательном расследовании часто оказываются заболеваниями, начало которых по времени совпадает с вакцинальным процессом.
АДС-М
– это вакцина, защищающая от двух тяжелых инфекций – от дифтерии и столбняка.
Дифтерия – инфекция, которую вызывает дифтерийная палочка. Клинические проявления заболевания обусловлены действием дифтерийного токсина (продукта жизнедеятельности дифтерийной палочки). Могут поражаться миндалины, зев, гортань, нос, кожа, слизистые оболочки. У непривитых заболевание характеризуется тяжелым течением с последующим развитием осложнений со стороны сердечнососудистой и нервной системы. От дифтерии среди непривитых умирают 10 – 20% заболевших. Антибиотики при лечении дифтерии неэффективны, лечение проводят специфической противодифтерийной сывороткой, введение которой само может вызвать тяжелые аллергические состояния.
От дифтерии среди непривитых умирают 10 – 20% заболевших. Антибиотики при лечении дифтерии неэффективны, лечение проводят специфической противодифтерийной сывороткой, введение которой само может вызвать тяжелые аллергические состояния.
Столбняк – инфекция, которую вызывает столбнячная палочка. Это заболевание с явлениями выраженной интоксикации нервной системы, проявляющейся в виде тонических и клонических мышечных судорог. Смерть наступает от паралича дыхательной мускулатуры. От столбняка умирают от 67 до 91% заболевших.
В состав вакцины входят: дифтерийный и столбнячный анатоксины, (иммунитет к дифтерии и столбняку вырабатывается против токсинов, обуславливающих заболевание).
Так как содержание дифтерийного и столбнячного анатоксинов в вакцине АДС-М уменьшено по сравнению с вакцинами АКДС, инфанрикс, АДС, вакцина АДС-М не годится для вакцинации детей до 6 лет и применяется только для вакцинации и ревакцинации детей старше 6 лет и взрослых. Хотя в крайне редких случаях, когда все названные вакцины противопоказаны, вакцина АДС-М применяется и для вакцинации против дифтерии и столбняка детям до 6 лет, которая проводятся двукратно с интервалом в 1,5 месяца.
Ревакцинации вакциной АДС-М проводятся в 7 лет, 14 лет и далее 1 раз в 10 лет пожизненно. АДС-М детям раннего и дошкольного возраста вводится внутримышечно в передненаружную область бедра, старшим детям и взрослым ее можно вводить глубоко подкожно.
Зачем нужна ревакцинация? С годами иммунитет к заболеванию может несколько снизиться. Для поддержания иммунитета на уровне, способном защитить организм от инфекции, проводятся ревакцинации.
Введение любой вакцины вызывает ответную реакцию организма. Это начинает работать иммунная система в ответ на введение антигенов возбудителя. Иногда эти реакции имеют клинические проявления. Это обычные, нормальные вакцинальные реакции (процессы), под которыми понимают изменения в организме, развивающиеся с определенным постоянством после введения той или иной вакцины. Вакцинальные реакции бывают местными и общими.
Местная нормальная реакция – уплотнение тканей, краснота, не превышающая 8 см в диаметре, иногда легкая болезненность в месте введения вакцины; развивается сразу после введения препарата, проходит в течение 1-4 дней, встречается у 5 – 15 % привитых детей.
Общая нормальная реакция проявляется повышением температуры до 37,50 – 38,60С, иногда появляются нарушения сна, аппетита, недомогание.
К крайне редким тяжелым поствакцинальным реакциям относят: температуру более 400С, местную реакцию 8 см. в диаметре и более.
Крайне редко(много реже, чем при АКДС) встречаются осложнения: аллергические реакции местные и общие, осложнения со стороны нервной системы (судороги, продолжительный пронзительный крик, энцефалопатия). Эти состояния при тщательном расследовании часто оказываются заболеваниями, начало которых по времени совпадает с вакцинальным процессом.
ПОЛИОМИЕЛИТНЫЕ ВАКЦИНЫ
Полиомиелит — это острая вирусная инфекция. Вызывается вирусами полиомиелита трех типов. Поражается в основном спиной мозг, но иногда и головной. Возникают параличи (ребенок не может ходить) или парезы конечностей (хромота). Заболевание ведет к инвалидизации (пораженная конечность плохо растет, слабеет, мышцы атрофируются).
Схема вакцинации: трехкратно с интервалом в 1,5 месяца на первом году жизни, ревакцинации в 1 год 6 месяцев, 1 год 8 месяцев и в 14 лет.
Зачем нужна ревакцинация? С годами иммунитет к заболеванию может несколько снизиться. Для поддержания иммунитета на уровне, способном защитить организм от инфекции, проводятся ревакцинации.
Введение любой вакцины вызывает ответную реакцию организма. Это начинает работать иммунная система в ответ на введение антигенов возбудителя. Иногда эти реакции имеют клинические проявления. Это обычные, нормальные вакцинальные реакции (процессы), под которыми понимают изменения в организме, развивающиеся с определенным постоянством после введения той или иной вакцины. Вакцинальные реакции бывают местными и общими.
Крайне редко после введения инактивированной (неживой) вакцины против полиомиелита может быть местная реакция. Местная нормальная реакция – уплотнение тканей, краснота, не превышающая 8 см в диаметре, иногда легкая болезненность в месте введения вакцины; развивается сразу после введения препарата, проходит в течение 1-4 дней, встречается у 5 – 15 % привитых детей. Могут быть аллергические реакции при наличии аллергии к стрептомицину.
Введение живой полиомиелитной вакцины реакции обычно не вызывает. Очень редко, с частотой 1 на 1 000 000 доз, у детей с иммунодефицитным состоянием возможно развитие вакциноассоциированного паралитического полиомиелита.
Для профилактики этого осложнения все дети получают комбинированную схему вакцинации – первые 2 прививки проводятся инактивированной полиомиелитной вакциной, а третья вакцинация и все ревакцинации – живой. При этом инактивированная полиомиелитная вакцина создает хороший общий иммунитет к полиомиелиту, на его фоне живая полиомиелитная вакцина создает местный иммунитет, надежно защищающий от вируса полиомиелита. При такой схеме вакцинации вакциноассоциированный паралитический полиомиелит не возникает.
Вакцины для профилактики полиомиелита:
- Живая полиомиелитная вакцина – БиВак полио. Вакцину закапывают в рот.
- Имовакс – инактивированная полиомиелитная вакцина
- Полиорикс — инактивированная полиомиелитная вакцина.
- Полимилекс — инактивированная полиомиелитная вакцина
Инактивированные полиомиелитные вакцины вводятся внутримышечно в передненаружную область бедра.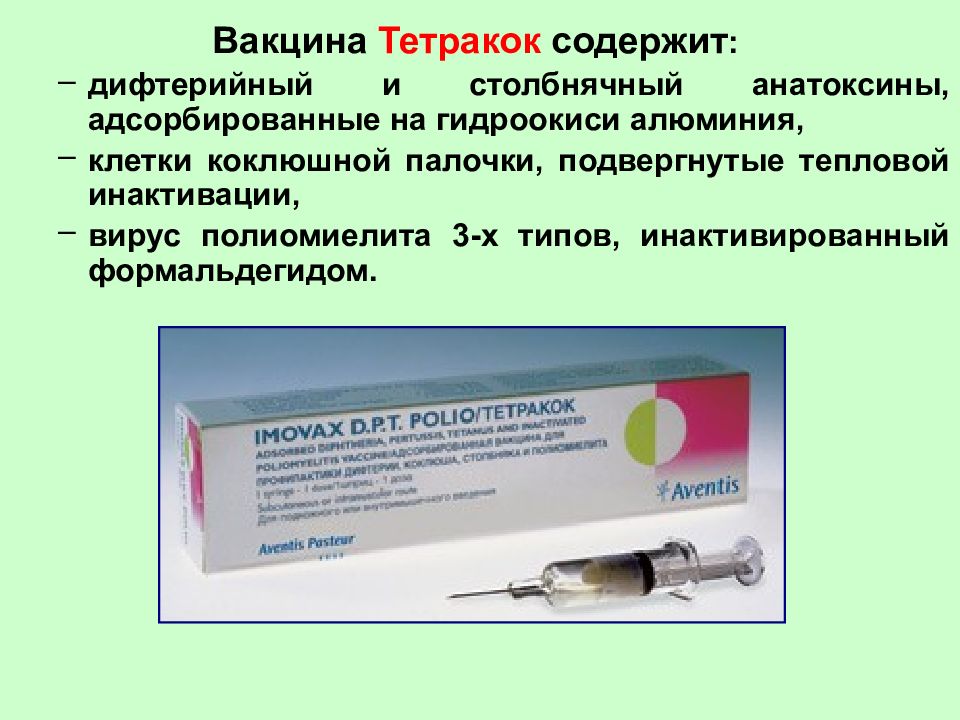 Живая полиомиелитная вакцина – в виде капель на корень языка ребенка.
Живая полиомиелитная вакцина – в виде капель на корень языка ребенка.
ВАКЦИНА ПРОТИВ КОРИ
Корь — острое, чрезвычайно заразное вирусное заболевание, встречающееся только у людей. При контакте с вирусом вероятность развития болезни близка к 100%. Заболевание характеризуется высокой температурой тела, общим тяжелым состоянием, кашлем, насморком, отечностью век, светобоязнью, гнойными выделения из глаз и сыпью. Корь опасна тяжелыми осложнениями: тяжелыми пневмониями с поражением плевры и образованием абсцессов в легких, язвенно-некротическими поражениями слизистых оболочек полости рта и кишечника, вплоть до распада мягких тканей, гнойным отитом, судорогами, редко – воспалением головного мозга (энцефалит), после которого наступает инвалидизация ребенка. По всему миру от кори ежегодно погибает до миллиона детей. Корью может заразиться и взрослый. Причем заболевание у него протекает тяжелее, чем у детей.
Для вакцинации против кори используется отечественная живая коревая вакцина
Вакцинация против кори проводится детям в возрасте 1 год, ревакцинация – в 6 лет. Если ребенок не был привит своевременно, то вакцинация осуществляется в любом возрасте, ревакцинация — через 6 месяцев от вакцинации. Вакцина вводится подкожно под лопатку или в наружную область плеча.
Если ребенок не был привит своевременно, то вакцинация осуществляется в любом возрасте, ревакцинация — через 6 месяцев от вакцинации. Вакцина вводится подкожно под лопатку или в наружную область плеча.
Зачем нужна ревакцинация? С годами иммунитет к заболеванию может несколько снизиться. Для поддержания иммунитета на уровне, способном защитить организм от инфекции, проводятся ревакцинации.
Введение любой вакцины вызывает ответную реакцию организма. Это начинает работать иммунная система в ответ на введение антигенов возбудителя. Иногда эти реакции имеют клинические проявления. Это обычные, нормальные вакцинальные реакции (процессы), под которыми понимают изменения в организме, развивающиеся с определенным постоянством после введения той или иной вакцины. Вакцинальные реакции бывают местными и общими.
Местная нормальная реакция – уплотнение тканей, краснота, не превышающая 8 см в диаметре, иногда легкая болезненность в месте введения вакцины; развивается сразу после введения препарата, проходит в течение 1-4 дней, встречается у 5 – 15 % привитых детей.
Общая нормальная реакция проявляется повышением температуры до 37,50 – 38,60С, иногда появляются нарушения сна, аппетита, недомогание.
К крайне редким тяжелым поствакцинальным реакциям относят: температуру более 400С, местную реакцию 8 см. в диаметре и более.
Вакцина против кори малореактогенна, но живой вирус у некоторых людей (редко) вызывает специфические реакции. У небольшого числа привитых, начиная с 4-5 дня после прививки может подняться температура, с 8-го по 12-й день даже до высоких цифр (выше 39,00С), появиться насморк, кашель, единичные элементы сыпи. Это является допустимой (обычной) реакцией организма на введение живой коревой вакцины, и на 13-14-й день состояние ребенка нормализуется. Реакции на вторую дозу возникают еще реже.
Крайне редко встречаются осложнения: аллергические реакции местные и общие, осложнения со стороны нервной системы (судороги, продолжительный пронзительный крик, энцефалопатия). Эти состояния при тщательном расследовании часто оказываются заболеваниями, начало которых по времени совпадает с вакцинальным процессом.
ВАКЦИНА ПРОТИВ ЭПИДЕМИЧЕСКОГО ПАРОТИТА («свинки»)
Эпидемический паротит – острая вирусная инфекция, при которой в основном поражаются слюнные железы. Они распухают, ребенку больно жевать и глотать. Кроме слюнных желез вирус эпидемического паротита может вызвать поражение поджелудочной железы (панкреатит), а также головного мозга (менингит, менингоэнцефалит). У 20-30% заболевших мальчиков-подростков воспаляются яички (орхит), что может послужить причиной бесплодия. У 5% заболевших девочек могут быть воспалены яичники (оофорит).
Для вакцинации против эпидемического паротита используется отечественная живая паротитная вакцина
Вакцинация против эпидемического паротита проводится детям в возрасте 1 год, ревакцинация – в 6 лет. Если ребенок не был привит своевременно, то вакцинация осуществляется в любом возрасте, ревакцинация — через 6 месяцев от вакцинации. Вакцина вводится подкожно под лопатку или в наружную область плеча.
Зачем нужна ревакцинация? С годами иммунитет к заболеванию может несколько снизиться. Для поддержания иммунитета на уровне, способном защитить организм от инфекции, проводятся ревакцинации.
Для поддержания иммунитета на уровне, способном защитить организм от инфекции, проводятся ревакцинации.
Введение любой вакцины вызывает ответную реакцию организма. Это начинает работать иммунная система в ответ на введение антигенов возбудителя. Иногда эти реакции имеют клинические проявления. Это обычные, нормальные вакцинальные реакции (процессы), под которыми понимают изменения в организме, развивающиеся с определенным постоянством после введения той или иной вакцины. Вакцинальные реакции бывают местными и общими.
Местная нормальная реакция – уплотнение тканей, краснота, не превышающая 8 см в диаметре, иногда легкая болезненность в месте введения вакцины; развивается сразу после введения препарата, проходит в течение 1-4 дней, встречается у 5 – 15 % привитых детей.
Общая нормальная реакция проявляется повышением температуры до 37,50 – 38,60С, иногда появляются нарушения сна, аппетита, недомогание.
К крайне редким тяжелым поствакцинальным реакциям относят: температуру более 400С, местную реакцию 8 см. в диаметре и более.
в диаметре и более.
Вакцина против эпидемического паротита малореактогенна, но живой вирус у некоторых людей (редко) вызывает специфические реакции. У небольшого числа привитых возможно повышение температуры с 5 по 13-14-й день и очень редко – на один-два дня припухание слюнных желез. Это является допустимой (обычной) реакцией организма на введение живой паротитной вакцины, и на 13-14-й день состояние ребенка нормализуется.
Крайне редко встречаются осложнения: аллергические реакции местные и общие, осложнения со стороны нервной системы (судороги, продолжительный пронзительный крик, энцефалопатия). Эти состояния при тщательном расследовании часто оказываются заболеваниями, начало которых по времени совпадает с вакцинальным процессом.
ВАКЦИНА ПРОТИВ КРАСНУХИ
Краснуха – острая вирусная инфекция, характеризующаяся невысоким подъемом температуры, увеличением лимфатических узлов, особенно на затылке, и мелкопятнистой сыпи. Обычно краснуха у детей протекает легко, но в редких случаях может поражаться головной мозг с развитием энцефалита.

Заболевание опасно для беременных женщин. Если беременная заболевает краснухой, особенно в первые три месяца беременности, то нередко беременность заканчивается выкидышем, рождением мертвого ребенка или ребенка с синдромом врожденной краснухи (врожденный порок сердца, слепота, глухота, в последствии – умственная отсталость), при заражении на поздних сроках беременности у ребенка может возникнуть энцефалит.
Для вакцинации против краснухи используется живая краснушная вакцина
Вакцинация против краснухи проводится детям в возрасте 1 год, ревакцинация – в 6 лет. Если ребенок не был привит своевременно, то вакцинация осуществляется в любом возрасте. Вакцина вводится подкожно под лопатку или в наружную область плеча.
Зачем нужна ревакцинация? С годами иммунитет к заболеванию может несколько снизиться. Для поддержания иммунитета на уровне, способном защитить организм от инфекции, проводятся ревакцинации.
Введение любой вакцины вызывает ответную реакцию организма. Это начинает работать иммунная система в ответ на введение антигенов возбудителя. Иногда эти реакции имеют клинические проявления. Это обычные, нормальные вакцинальные реакции (процессы), под которыми понимают изменения в организме, развивающиеся с определенным постоянством после введения той или иной вакцины. Вакцинальные реакции бывают местными и общими.
Это начинает работать иммунная система в ответ на введение антигенов возбудителя. Иногда эти реакции имеют клинические проявления. Это обычные, нормальные вакцинальные реакции (процессы), под которыми понимают изменения в организме, развивающиеся с определенным постоянством после введения той или иной вакцины. Вакцинальные реакции бывают местными и общими.
Местная нормальная реакция – уплотнение тканей, краснота, не превышающая 8 см в диаметре, иногда легкая болезненность в месте введения вакцины; развивается сразу после введения препарата, проходит в течение 1-4 дней, встречается у 5 – 15 % привитых детей.
Общая нормальная реакция проявляется повышением температуры до 37,50 – 38,60С, иногда появляются нарушения сна, аппетита, недомогание.
К крайне редким тяжелым поствакцинальным реакциям относят: температуру более 400С, местную реакцию 8 см. в диаметре и более.
Вакцина против краснухи малореактогенна, но живой вирус у некоторых людей (редко) вызывает специфические реакции. У небольшого числа привитых возможно повышение температуры с 5 по 13-14-й день, появление сыпи, кашля, насморка, а у взрослых – болей в суставах. Это является допустимой (обычной) реакцией организма на введение живой краснушной вакцины, и на 13-14-й день состояние ребенка нормализуется.
У небольшого числа привитых возможно повышение температуры с 5 по 13-14-й день, появление сыпи, кашля, насморка, а у взрослых – болей в суставах. Это является допустимой (обычной) реакцией организма на введение живой краснушной вакцины, и на 13-14-й день состояние ребенка нормализуется.
Крайне редко встречаются осложнения: аллергические реакции местные и общие, осложнения со стороны нервной системы (судороги, продолжительный пронзительный крик, энцефалопатия). Эти состояния при тщательном расследовании часто оказываются заболеваниями, начало которых по времени совпадает с вакцинальным процессом.
ПРИОРИКС
Это вакцина, защищающая сразу от трех вирусных инфекций – кори, эпидемического паротита, краснухи.
Корь — острое, чрезвычайно заразное вирусное заболевание, встречающееся только у людей. При контакте с вирусом вероятность развития болезни близка к 100%. Заболевание характеризуется высокой температурой тела, общим тяжелым состоянием, кашлем, насморком, отечностью век, светобоязнью, гнойными выделения из глаз и сыпью.
 Корь опасна тяжелыми осложнениями: тяжелыми пневмониями с поражением плевры и образованием абсцессов в легких, язвенно-некротическими поражениями слизистых оболочек полости рта и кишечника, вплоть до распада мягких тканей, гнойным отитом, судорогами, редко – воспалением головного мозга (энцефалит), после которого наступает инвалидизация ребенка. По всему миру от кори ежегодно погибает до миллиона детей. Корью может заразиться и взрослый. Причем заболевание у него протекает тяжелее, чем у детей.
Корь опасна тяжелыми осложнениями: тяжелыми пневмониями с поражением плевры и образованием абсцессов в легких, язвенно-некротическими поражениями слизистых оболочек полости рта и кишечника, вплоть до распада мягких тканей, гнойным отитом, судорогами, редко – воспалением головного мозга (энцефалит), после которого наступает инвалидизация ребенка. По всему миру от кори ежегодно погибает до миллиона детей. Корью может заразиться и взрослый. Причем заболевание у него протекает тяжелее, чем у детей.Эпидемический паротит – острая вирусная инфекция, при которой в основном поражаются слюнные железы. Они распухают, ребенку больно жевать и глотать. Кроме слюнных желез вирус эпидемического паротита может вызвать поражение поджелудочной железы (панкреатит), а также головного мозга (менингит, менингоэнцефалит). У 20-30% заболевших мальчиков-подростков воспаляются яички (орхит), что может послужить причиной бесплодия. У 5% заболевших девочек могут быть воспалены яичники (оофорит).
Краснуха – острая вирусная инфекция, характеризующаяся невысоким подъемом температуры, увеличением лимфатических узлов, особенно на затылке, и мелкопятнистой сыпи.
 Обычно краснуха у детей протекает легко, но в редких случаях может поражаться головной мозг с развитием энцефалита.
Обычно краснуха у детей протекает легко, но в редких случаях может поражаться головной мозг с развитием энцефалита.В состав вакцины «приорикс», производства ГлаксоСмитКляйн, Бельгия, входят живые вакцины против кори, эпидемического паротита и краснухи.
Вакцинация проводится детям в возрасте 1 год, ревакцинация – в 6 лет. Вакцина альтернативная, т.е. приобретается за счет средств родителей и по желанию родителей. Вакцина вводится подкожно под лопатку или в наружную область плеча.
Введение любой вакцины вызывает ответную реакцию организма. Это начинает работать иммунная система в ответ на введение антигенов возбудителя. Иногда эти реакции имеют клинические проявления. Это обычные, нормальные вакцинальные реакции (процессы), под которыми понимают изменения в организме, развивающиеся с определенным постоянством после введения той или иной вакцины. Вакцинальные реакции бывают местными и общими.
Местная нормальная реакция – уплотнение тканей, краснота, не превышающая 8 см в диаметре, иногда легкая болезненность в месте введения вакцины; развивается сразу после введения препарата, проходит в течение 1-4 дней, встречается у 5 – 15 % привитых детей.
Общая нормальная реакция проявляется повышением температуры до 37,50 – 38,60С, иногда появляются нарушения сна, аппетита, недомогание.
К крайне редким тяжелым поствакцинальным реакциям относят: температуру более 400С, местную реакцию 8 см. в диаметре и более.
Вакцина малореактогенна, но живой вирус у некоторых людей (редко) вызывает специфические реакции. У небольшого числа привитых возможно повышение температуры с 5 по 13-14-й день, появление сыпи, кашля, насморк, очень редко – на один-два дня припухание слюнных желез. Это является допустимой (обычной) реакцией организма на введение живой вакцины, и на 13-14-й день состояние ребенка нормализуется.
Крайне редко встречаются осложнения: аллергические реакции местные и общие, осложнения со стороны нервной системы (судороги, продолжительный пронзительный крик, энцефалопатия). Эти состояния при тщательном расследовании часто оказываются заболеваниями, начало которых по времени совпадает с вакцинальным процессом.
ВАКЦИНЫ ПРОТИВ ТУБЕРКУЛЕЗА
Туберкулез – бактериальная инфекция, вызываемая микобактериями туберкулеза человека или животного.
 Поражаются легкие, кости, кожа, мочеполовая система, нервная система, глаза, лимфатические узлы. Туберкулез не поражает только волосы и ногти! Наиболее тяжелой формой заболевания является туберкулезный менингит (воспаление мозговых оболочек).
Поражаются легкие, кости, кожа, мочеполовая система, нервная система, глаза, лимфатические узлы. Туберкулез не поражает только волосы и ногти! Наиболее тяжелой формой заболевания является туберкулезный менингит (воспаление мозговых оболочек).В наши дни в мире ежегодно заболевают туберкулезом более 9 млн. человек и 3-4 млн. умирают от него.
В России заболеваемость туберкулезом ( в том числе детей) за последние годы выросла более, чем в 2 раза и продолжает расти.
Для туберкулеза характерно постепенное, часто незаметное начало заболевания. Клинические проявления туберкулезной инфекции могут быть разные. Но всегда это сопровождается явлениями интоксикации. И всегда требует лечения.
Для вакцинации против туберкулеза существует две вакцины: БЦЖ и БЦЖ-М
Вводят вакцины внутрикожно в наружную верхнюю треть руки. Кожу после введения вакцины не обрабатывают, повязку не накладывают. В месте введения вакцины в течение 3-6 месяцев последовательно развиваются пятно, гнойничковый элемент, корочка и рубчик. Наличие рубчика свидетельствует о правильном проведении прививки. Подъема температуры, ухудшения общего состояния не бывает.
Наличие рубчика свидетельствует о правильном проведении прививки. Подъема температуры, ухудшения общего состояния не бывает.
Вакцинацию против туберкулеза проводят новорожденным в роддоме на 3-7 сутки жизни вакциной БЦЖ, или при наличии при наличии временных противопоказаний – после их отмены дома вакциной БЦЖ-М. До 2-х месячного возраста прививки против туберкулеза проводятся без предварительной реакции Манту, после 2-х месяцев жизни – при отрицательном результате р. Манту. Ревакцинацию вакциной БЦЖ (повторное введение) проводят при отрицательном результате туберкулиновой пробы в 7 лет и в 14 лет.
Возможные осложнения после введения вакцины БЦЖ и БЦЖ-М: лимфаденит, инфильтрат, холодный абсцесс, язва, келоидный рубец, остеит, генерализованный БЦЖ-ит. Осложнения встречаются не часто, но при появлении у ребенка каких-либо симптомов, жалоб необходимо обратиться к врачу.
ВАКЦИНЫ ПРОТИВ ГЕПАТИТА В
Гепатит В – вирусная инфекция, широко распространенная во всем мире, вызывающая поражение печени, вплоть до цирроза (гибели клеток печени с образованием рубцовой ткани) или рака печени.
 Вирус содержится в крови и любых жидкостях организма зараженного человека (слюна, сперма, вагин6альный секрет). Путей заражения гепатитом В много: при инъекциях, половым путем, при тесном контакте с больным в быту через парезы, раны, при использовании общих инструментов (ножниц, бритв, игл для татуировки), мочалок, расчесок, зубных щеток и т.п. Новорожденный ребенок может заразиться от больной (инфицированной ) матери. По данным Всемирной организации здравоохранения (ВОЗ), ежегодно от гепатита В в мире погибает около 1 000 000 человек.
Вирус содержится в крови и любых жидкостях организма зараженного человека (слюна, сперма, вагин6альный секрет). Путей заражения гепатитом В много: при инъекциях, половым путем, при тесном контакте с больным в быту через парезы, раны, при использовании общих инструментов (ножниц, бритв, игл для татуировки), мочалок, расчесок, зубных щеток и т.п. Новорожденный ребенок может заразиться от больной (инфицированной ) матери. По данным Всемирной организации здравоохранения (ВОЗ), ежегодно от гепатита В в мире погибает около 1 000 000 человек.Вакцины против гепатита В не содержат вирус, созданы генно-инженерным путем, содержат белок пищевых дрожжей.
Первую прививку против гепатита В проводят в роддоме в первый день жизни ребенка, через 1 месяц – вторую вакцинацию, в 6 месяцев – третью. Детям, родившимся от матерей-носителей вируса гепатита В или больных гепатитом В, вакцинацию проводят 4-х кратно: в первый день жизни, в 1 месяц, в 2 месяца, в 12 месяцев. Все вакцины против гепатита В вводят внутримышечно: детям до 2 лет – в бедро, старше – в дельтовидную мышцу (высоко в руку).
На месте введения вакцины могут появиться уплотнение и краснота, которые проходят через несколько дней. Небольшое повышение температуры бывает редко и быстро проход.
Теоретически возможна аллергическая сыпь на вакцину при наличии аллергической реакции на пекарские дрожжи, но т.к. аллергическая реакция на пекарские дрожжи встречается крайне редко, аллергическая сыпь на вакцину тоже почти не регистрируется в мире.
БУБОКОКК
Это вакцина против коклюша, дифтерии, столбняка, гепатита В.
Коклюш вызывается коклюшной палочкой. Заболевание характеризуется приступами спазматического кашля, поражением дыхательной, сердечно-сосудистой и нервной систем. Происходит скапливание густой стекловидной мокроты в бронхах, которую тяжело откашлять и взрослому человеку. Ребенок «заходится» в кашле. Опасен коклюш и своими осложнениями, которые развиваются у 30% — 50% и выше заболевших: воспалением легких (пневмонией), а у маленьких детей – поражением головного мозга (энцефалопатией) с возможными повторными судорогами. При заболевании коклюшем непривитых детей в возрасте до года умереть может каждый пятый ребенок.
При заболевании коклюшем непривитых детей в возрасте до года умереть может каждый пятый ребенок.
Дифтерия – инфекция, которую вызывает дифтерийная палочка. Клинические проявления заболевания обусловлены действием дифтерийного токсина (продукта жизнедеятельности дифтерийной палочки). Могут поражаться миндалины, зев, гортань, нос, кожа, слизистые оболочки. У непривитых заболевание характеризуется тяжелым течением с последующим развитием осложнений со стороны сердечнососудистой и нервной системы. От дифтерии среди непривитых умирают 10 – 20% заболевших. Антибиотики при лечении дифтерии неэффективны, лечение проводят специфической противодифтерийной сывороткой, введение которой само может вызвать тяжелые аллергические состояния.
Столбняк – инфекция, которую вызывает столбнячная палочка. Это заболевание с явлениями выраженной интоксикации нервной системы, проявляющейся в виде тонических и клонических мышечных судорог. Смерть наступает от паралича дыхательной мускулатуры. От столбняка умирают от 67 до 91% заболевших.
Гепатит В – вирусная инфекция, широко распространенная во всем мире, вызывающая поражение печени, вплоть до цирроза (гибели клеток печени с образованием рубцовой ткани) или рака печени. Вирус содержится в крови и любых жидкостях организма зараженного человека (слюна, сперма, вагин6альный секрет). Путей заражения гепатитом В много: при инъекциях, половым путем, при тесном контакте с больным в быту через парезы, раны, при использовании общих инструментов (ножниц, бритв, игл для татуировки), мочалок, расчесок, зубных щеток и т.п. Новорожденный ребенок может заразиться от больной (инфицированной) матери. По данным Всемирной организации здравоохранения (ВОЗ), ежегодно от гепатита В в мире погибает около 1 000 000 человек.
В состав вакцины входят: коклюшная убитая вакцина, дифтерийный и столбнячный анатоксины (иммунитет к дифтерии и столбняку вырабатывается против токсинов, обуславливающих заболевание), а также рекомбинантная вакцина против гепатита В.
Вакцина применяется в том случае, если ребенку необходимо сделать АКДС и вакцинацию против гепатита В, вводится глубоко внутримышечно в передненаружную область бедра.
Введение любой вакцины вызывает ответную реакцию организма. Это начинает работать иммунная система в ответ на введение антигенов возбудителя. Иногда эти реакции имеют клинические проявления. Это обычные, нормальные вакцинальные реакции (процессы), под которыми понимают изменения в организме, развивающиеся с определенным постоянством после введения той или иной вакцины. Вакцинальные реакции бывают местными и общими.
Местная нормальная реакция – уплотнение тканей, краснота, не превышающая 8 см в диаметре, иногда легкая болезненность в месте введения вакцины; развивается сразу после введения препарата, проходит в течение 1-4 дней, встречается у 5 – 15 % привитых детей.
Общая нормальная реакция проявляется повышением температуры до 37,50 – 38,60С, иногда появляются нарушения сна, аппетита, недомогание.
К крайне редким тяжелым поствакцинальным реакциям относят: температуру более 400С, местную реакцию 8 см. в диаметре и более.
Крайне редко встречаются осложнения: аллергические реакции местные и общие, осложнения со стороны нервной системы (судороги, продолжительный пронзительный крик, энцефалопатия). Эти состояния при тщательном расследовании часто оказываются заболеваниями, начало которых по времени совпадает с вакцинальным процессом.
Эти состояния при тщательном расследовании часто оказываются заболеваниями, начало которых по времени совпадает с вакцинальным процессом.
МОНОВАКЦИНЫ ПРОТИВ ГЕМОФИЛЬНОЙ ТИПА b ИНФЕКЦИИ (ХИБ-ИНФЕКЦИИ)
Гемофильная типа b (Хиб) инфекция является причиной 40% всех гнойных менингитов у маленьких детей, умирает 5 – 25% всех заболевших, 40% переболевших инвалидизируется в результате поражения нервной системы, зрения, слуха (развивается глухота). Инфекция вызывает также воспаление легких, суставов, полости рта, является причиной повторных гнойных отитов, респираторных заболеваний. Болеют в основном дети от 2 месяцев до 5 лет и дети с нарушением иммунитета в любом возрасте.
Схема вакцинации против гемофильной типа b (Хиб) инфекции:
— дети, начинающие получать прививки против Хиб-инфекции с 3 до 6 месяцев прививаются трехкратно с интервалов в 1,5 месяца с ревакцинацией в 1 год 6 месяцев;
— дети, начинающие получать прививки против Хиб-инфекции с 6 до 12 месяцев прививаются двукратно с интервалов в 1,5 месяца с ревакцинацией в 1 год 6 месяцев;
— дети старше года прививаются однократно
Для вакцинации против гемофильной типа b (Хиб) инфекции используются две вакцины: Хиберикс (ГласкоСитКляйн, Бельгия) и Акт-хиб (Санофи Пастер, Франция). Вакцины против гемофильной типа b (Хиб) инфекции вводятся внутримышечно или подкожно.
Вакцины против гемофильной типа b (Хиб) инфекции вводятся внутримышечно или подкожно.
Введение любой вакцины вызывает ответную реакцию организма. Это начинает работать иммунная система в ответ на введение антигенов возбудителя. Иногда эти реакции имеют клинические проявления. Это обычные, нормальные вакцинальные реакции (процессы), под которыми понимают изменения в организме, развивающиеся с определенным постоянством после введения той или иной вакцины. Вакцинальные реакции бывают местными и общими.
Местная нормальная реакция – уплотнение тканей, краснота, не превышающая 8 см в диаметре, иногда легкая болезненность в месте введения вакцины; развивается сразу после введения препарата, проходит в течение 1-4 дней, встречается у менее 10 % привитых детей.
Общая нормальная реакция проявляется повышением температуры до 37,50 – 38,60С (до 1% привитых детей).
К крайне редким тяжелым поствакцинальным реакциям относят: температуру более 400С, местную реакцию 8 см. в диаметре и более.
Вакцины не имеют специальных противопоказаний, кроме гиперчувствительности к ее компонентам и сильной реакцией на предыдущую дозу. ВИЧ-инфекция не является противопоказанием.
ПЕНТАКСИМ
Это вакцина против коклюша (бесклеточная), дифтерии, столбняка, полиомиелита (инактивированная) и гемофильной инфекции типа b.
Коклюш вызывается коклюшной палочкой. Заболевание характеризуется приступами спазматического кашля, поражением дыхательной, сердечно-сосудистой и нервной систем. Происходит скапливание густой стекловидной мокроты в бронхах, которую тяжело откашлять и взрослому человеку. Ребенок «заходится» в кашле. Опасен коклюш и своими осложнениями, которые развиваются у 30% — 50% и выше заболевших: воспалением легких (пневмонией), а у маленьких детей – поражением головного мозга (энцефалопатией) с возможными повторными судорогами. При заболевании коклюшем непривитых детей в возрасте до года умереть может каждый пятый ребенок.
Дифтерия – инфекция, которую вызывает дифтерийная палочка. Клинические проявления заболевания обусловлены действием дифтерийного токсина (продукта жизнедеятельности дифтерийной палочки). Могут поражаться миндалины, зев, гортань, нос, кожа, слизистые оболочки. У непривитых заболевание характеризуется тяжелым течением с последующим развитием осложнений со стороны сердечнососудистой и нервной системы. От дифтерии среди непривитых умирают 10 – 20% заболевших. Антибиотики при лечении дифтерии неэффективны, лечение проводят специфической противодифтерийной сывороткой, введение которой само может вызвать тяжелые аллергические состояния.
Клинические проявления заболевания обусловлены действием дифтерийного токсина (продукта жизнедеятельности дифтерийной палочки). Могут поражаться миндалины, зев, гортань, нос, кожа, слизистые оболочки. У непривитых заболевание характеризуется тяжелым течением с последующим развитием осложнений со стороны сердечнососудистой и нервной системы. От дифтерии среди непривитых умирают 10 – 20% заболевших. Антибиотики при лечении дифтерии неэффективны, лечение проводят специфической противодифтерийной сывороткой, введение которой само может вызвать тяжелые аллергические состояния.
Столбняк – инфекция, которую вызывает столбнячная палочка. Это заболевание с явлениями выраженной интоксикации нервной системы, проявляющейся в виде тонических и клонических мышечных судорог. Смерть наступает от паралича дыхательной мускулатуры. От столбняка умирают от 67 до 91% заболевших.
Полиомиелит — это острая вирусная инфекция. Вызывается вирусами полиомиелита трех типов. Поражается в основном спиной мозг, но иногда и головной. Возникают параличи (ребенок не может ходить) или парезы конечностей (хромота). Заболевание ведет к инвалидизации (пораженная конечность плохо растет, слабеет, мышцы атрофируются).
Возникают параличи (ребенок не может ходить) или парезы конечностей (хромота). Заболевание ведет к инвалидизации (пораженная конечность плохо растет, слабеет, мышцы атрофируются).
Гемофильная типа b (Хиб) инфекция является причиной 40% всех гнойных менингитов у маленьких детей, умирает 5 – 25% всех заболевших, 40% переболевших инвалидизируется в результате поражения нервной системы, зрения, слуха (развивается глухота). Инфекция вызывает также воспаление легких, суставов, полости рта, является причиной повторных гнойных отитов, респираторных заболеваний. Болеют в основном дети от 2 месяцев до 5 лет и дети с нарушением иммунитета в любом возрасте.
Вакцина вводится глубоко внутримышечно в передненаружную область бедра.
Введение любой вакцины вызывает ответную реакцию организма. Это начинает работать иммунная система в ответ на введение антигенов возбудителя. Иногда эти реакции имеют клинические проявления. Это обычные, нормальные вакцинальные реакции (процессы), под которыми понимают изменения в организме, развивающиеся с определенным постоянством после введения той или иной вакцины. Вакцинальные реакции бывают местными и общими.
Вакцинальные реакции бывают местными и общими.
Местная нормальная реакция – уплотнение тканей, краснота, не превышающая 8 см в диаметре, иногда легкая болезненность в месте введения вакцины; развивается сразу после введения препарата, проходит в течение 1-4 дней, встречается у 5 – 15 % привитых детей.
Общая нормальная реакция проявляется повышением температуры до 37,50 – 38,60С, иногда появляются нарушения сна, аппетита, недомогание.
К крайне редким тяжелым поствакцинальным реакциям относят: температуру более 400С, местную реакцию 8 см. в диаметре и более.
Крайне редко встречаются осложнения: аллергические реакции местные и общие, осложнения со стороны нервной системы (судороги, продолжительный пронзительный крик, энцефалопатия). Эти состояния при тщательном расследовании часто оказываются заболеваниями, начало которых по времени совпадает с вакцинальным процессом.
ВАКЦИНЫ ПРОТИВ ГЕПАТИТА А
Гепатит А – острое вирусное заболевание, поражающее печень.
 Проявляется заболевание слабостью, снижением аппетита, рвотой, желтой окраской кожи, обесцвеченным стулом, темной окраской мочи. Бывает затяжное и осложненное течение гепатита А. Наиболее тяжело болеют люди с хроническими заболеваниями печени, у них возможен смертельный исход.
Проявляется заболевание слабостью, снижением аппетита, рвотой, желтой окраской кожи, обесцвеченным стулом, темной окраской мочи. Бывает затяжное и осложненное течение гепатита А. Наиболее тяжело болеют люди с хроническими заболеваниями печени, у них возможен смертельный исход.Для профилактики гепатита А применяются убитые отечественные (ГЕП-А-ин-ВАК, с 3-х лет) и зарубежные (Хаврикс, с 1 года, и Аваксим, с2 лет) вакцины.
Схема вакцинации две прививки с интервалом 6 – 18 месяцев. Вакцина вводится внутримышечно (предпочтительно) или подкожно.
Введение любой вакцины вызывает ответную реакцию организма. Это начинает работать иммунная система в ответ на введение антигенов возбудителя. Иногда эти реакции имеют клинические проявления. Это обычные, нормальные вакцинальные реакции (процессы), под которыми понимают изменения в организме, развивающиеся с определенным постоянством после введения той или иной вакцины. Вакцинальные реакции бывают местными и общими.
Местная нормальная реакция – уплотнение тканей, краснота, не превышающая 8 см в диаметре, иногда легкая болезненность в месте введения вакцины; развивается сразу после введения препарата, проходит в течение 1-4 дней, встречается у 5 – 15 % привитых детей.
Общая нормальная реакция проявляется повышением температуры до 37,50 – 38,60С, иногда появляются нарушения сна, аппетита, недомогание.
К крайне редким тяжелым поствакцинальным реакциям относят: температуру более 400С, местную реакцию 8 см. в диаметре и более.
Крайне редко встречаются осложнения: аллергические реакции местные и общие. Эти состояния при тщательном расследовании часто оказываются заболеваниями, начало которых по времени совпадает с вакцинальным процессом.
ВЕТРЯНАЯ ОСПА
Ветряная оспа -это острое инфекционное заболевание, передающееся воздушно-капельным путем. Инфекция крайне заразна. Она характеризуется лихорадкой, умеренно выраженной интоксикацией и распространенной везикулезной сыпью. Кроме часто встречающейся легкой формы ветряная оспа может протекать в виде среднетяжелой и тяжелой форм, когда резко выражены симптомы интоксикации, может быть поражение головного мозга. А также бывают геморрагическая форма (могут быть кровоизлияния в кожу, слизистые, носовые кровотечения, кровавая рвота), гангренозная форма (некрозы и глубокие язвы на месте пузырьков). Осложнения при ветряной оспе встречаются редко. К ним относятся пневмонии, круп, энцефалиты, менингоэнцефалиты, миелиты, невриты. Возможно присоединение бактериальной инфекции.
Осложнения при ветряной оспе встречаются редко. К ним относятся пневмонии, круп, энцефалиты, менингоэнцефалиты, миелиты, невриты. Возможно присоединение бактериальной инфекции.
Для вакцинации против ветряной оспы используются следующие живые вакцины:
- Варилрикс (ГласкоСмитКляйн, Бельгия)
- Окавакс ( Институт Бикен, Япония)
Схема вакцинации: вакцинация в год и ревакцинация в 6 лет, при вакцинации против ветряной оспы детей старше 6 лет – прививки проводятся двукратно с интервалом в 6 небель. Вакцины против ветряной оспы вводятся подкожно.
У детей, перенесших ветряную оспу, вакцина уменьшает частоту опоясывающего лишая.
Введение любой вакцины вызывает ответную реакцию организма. Это начинает работать иммунная система в ответ на введение антигенов возбудителя. Иногда эти реакции имеют клинические проявления. Это обычные, нормальные вакцинальные реакции (процессы), под которыми понимают изменения в организме, развивающиеся с определенным постоянством после введения той или иной вакцины. Вакцинальные реакции бывают местными и общими.
Вакцинальные реакции бывают местными и общими.
Местная нормальная реакция – уплотнение тканей, краснота, не превышающая 8 см в диаметре, иногда легкая болезненность в месте введения вакцины; развивается сразу после введения препарата, проходит в течение 1-4 дней, встречается у 5 – 15 % привитых детей.
Общая нормальная реакция проявляется повышением температуры до 37,50 – 38,60С, иногда появляются нарушения сна, аппетита, недомогание.
К крайне редким тяжелым поствакцинальным реакциям относят: температуру более 400С, местную реакцию 8 см. в диаметре и более.
Вакцина малореактогенна, но живой вирус у некоторых людей (редко) вызывает специфические реакции. У небольшого числа привитых возможно повышение температуры с 5 по 13-14-й день, появление сыпи. Это является допустимой (обычной) реакцией организма на введение живой вакцины, и на 13-14-й день состояние ребенка нормализуется.
В исключительно редких случаях (частота 1:1 000 000) в период от нескольких дней до трех недель после вакцинации может развиться идеопатическая тромбоцитопеническая пурпура.
ВАКЦИНЫ ПРОТИВ ПНЕВМОКОККОВОЙ ИНФЕКЦИИ
Пневмококковая инфекция – вызывается бактериями и характеризуется тяжелыми заболеваниями ушей (отит), легких, других органов, заражением крови (сепсис), поражением мозговых оболочек (менингит). Пик заболеваемости наблюдается на 1 – 2 году жизни и у пожилых людей. Иммунизация рекомендуется детям первых лет жизни, пожилым людям, пожилым людям, пациентам в учреждениях постоянного пребывания, больным при отсутствии селезенки, онкологических заболеваниях, сахарным диабетом, хронической почечной патологией, ВИЧ. Вакцина показана часто болеющим, детям с увеличением аденоидов, с бронхолегочной патологией, инфицированным туберкулезом.
Для вакцинации против пневмококковой инфекции используется три вакцины: превенар и синфлорикс, разрешенные к применению с 2-х месячного возраста, и пневмо-23, разрешенная к применению с 2-х летнего возраста.
Схема вакцинации:
Вакцинация проводится двукратно (в 2 мес. и 4,5 мес.) с ревакцинацией в 1 год 3 месяца.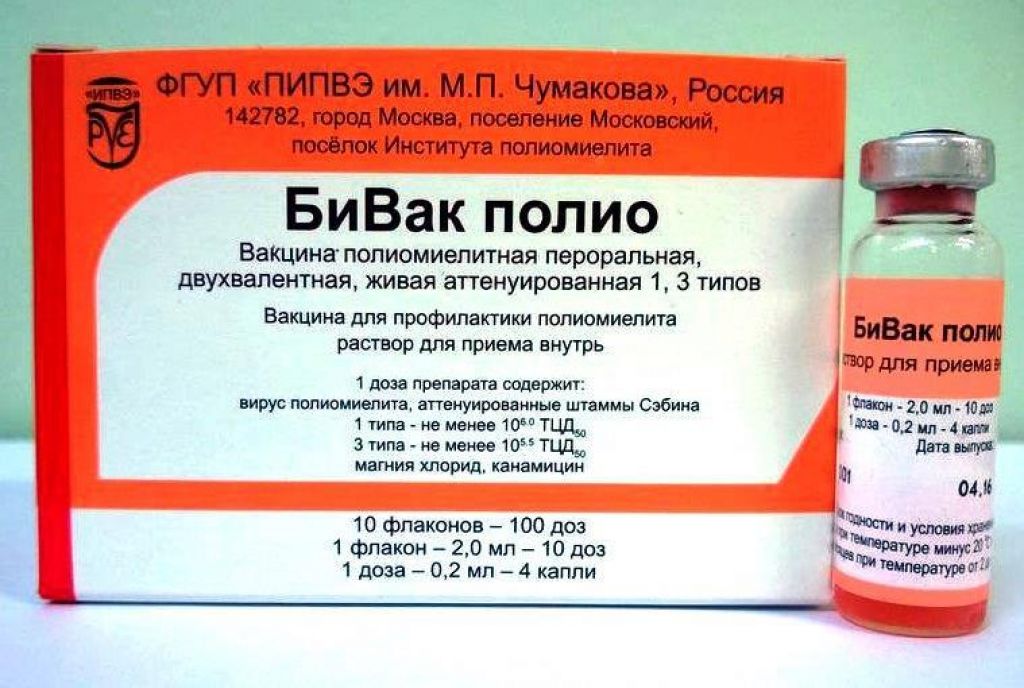 Если ребенок прививается на втором году жизни – двукратно без ревакцинации. У лиц старше 2 лет – однократно.
Если ребенок прививается на втором году жизни – двукратно без ревакцинации. У лиц старше 2 лет – однократно.
Вакцины против пневмококковой инфекции вводятся внутримышечно, детям первых лет жизни в передненаружную поверхность бедра.
Введение любой вакцины вызывает ответную реакцию организма. Это начинает работать иммунная система в ответ на введение антигенов возбудителя. Иногда эти реакции имеют клинические проявления. Это обычные, нормальные вакцинальные реакции (процессы), под которыми понимают изменения в организме, развивающиеся с определенным постоянством после введения той или иной вакцины. Вакцинальные реакции бывают местными и общими.
Местная нормальная реакция – уплотнение тканей, краснота, не превышающая 8 см в диаметре, иногда легкая болезненность в месте введения вакцины; развивается сразу после введения препарата, проходит в течение 1-4 дней, встречается у 5% привитых детей.
Общая нормальная реакция проявляется повышением температуры до 37,50 – 38,60С, иногда появляются нарушения сна, аппетита, недомогание.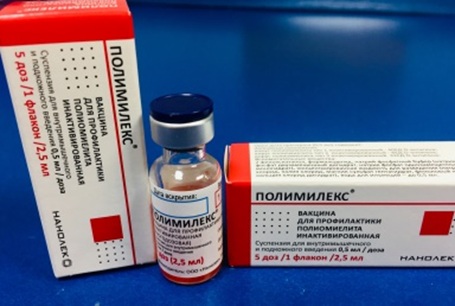
К крайне редким тяжелым поствакцинальным реакциям относят: температуру более 400С, местную реакцию 8 см. в диаметре и более.
К редко встречающимся осложнениям при использовании вакцины «превенар» относятся отек Квинке, бронхоспазм, судороги, дерматит, зуд, крапивница.
ВАКЦИНЫ ПРОТИВ КЛЕЩЕВОГО ЭНЦЕФАЛИТА
Клещевой энцефалит – природно-очаговое (характерно только для определенных территорий) вирусное заболевание с преимущественным поражением центральной нервной системы. Переносчиками и резервуарами клещевого энцефалита являются иксодовые клещи. Заражение возможно при употреблении в пищу сырого коровьего или козьего молока. Вирус сохраняется в клещах в течение всей их жизни и передается от поколения к поколению, что делает клещей природным очагом инфекции. Заражение клещевым энцефалитом может произойти и без посещения леса – клещ может быть принесен домой с ветками, цветами, на шерсти домашних животных, на одежде людей. При заболевании вирус поражает головной и спиной мозг, характерны упорные головные боли, судороги, параличи. Заболевание никогда не проходит бесследно, у переболевших на всю жизнь остаются осложнения различной степени тяжести.
Заболевание никогда не проходит бесследно, у переболевших на всю жизнь остаются осложнения различной степени тяжести.
Наша область является эндемичной по этому заболеванию, т.е. опасность инфицирования клещевым энцефалитом на территории Свердловской области (в т.ч. и в нашем городе) довольно велика.
Для вакцинации детского населения применяются следующие вакцины:
- «ФСМЕ-ИММУН Инжект» Австрия, разрешенная к применению с годовалого возраста;
- «ЭНЦЕПУР» Германия, разрешенная к применению с годовалого возраста;
- Вакцина против клещевого энцефалита культуральная очишенная концентрированная инактивированная сухая (г. Москва), разрешенная к применению с 4-х летнего возраста;
- КлещЭвак (г. Москва), разрешенная к применению с годовалого возраста.
- «ЭнцеВир Нео детский» (Россия)
Схема вакцинации: вакцинация двукратно с интервалом для отечественной вакцины 1-6 месяцев, для импортной 1-2 месяца; первая ревакцинация для всех вакцин через год после вакцинации, отдаленные ревакцинации 1 раз в 3 года. Вакцины вводятся внутримышечно, а отечественная для старших возрастов может быть введена подкожно в подлопаточную область.
Вакцины вводятся внутримышечно, а отечественная для старших возрастов может быть введена подкожно в подлопаточную область.
Введение любой вакцины вызывает ответную реакцию организма. Это начинает работать иммунная система в ответ на введение антигенов возбудителя. Иногда эти реакции имеют клинические проявления. Это обычные, нормальные вакцинальные реакции (процессы), под которыми понимают изменения в организме, развивающиеся с определенным постоянством после введения той или иной вакцины. Вакцинальные реакции бывают местными и общими.
Местная нормальная реакция – уплотнение тканей, краснота, не превышающая 8 см в диаметре, иногда легкая болезненность в месте введения вакцины; развивается сразу после введения препарата, проходит в течение 1-4 дней, встречается у 5% привитых детей.
Общая нормальная реакция проявляется повышением температуры до 37,50 – 38,60С, иногда появляются нарушения сна, аппетита, недомогание.
После первой дозы иногда наблюдается кратковременное повышение температуры, головная боль, боли в конечностях, тошнота и рвота. На следующие дозы эти симптомы наблюдаются еще реже.
На следующие дозы эти симптомы наблюдаются еще реже.
К крайне редким тяжелым поствакцинальным реакциям относят: температуру более 400С, местную реакцию 8 см. в диаметре и более.
Крайне редки аллергические реакции.
ВАКЦИНЫ ПРОТИВ ГРИППА
Грипп – это острое инфекционное вирусное заболевание, передающееся воздушно-капельным путем, поражающее верхние дыхательные пути.
По своей социальной значимости он находится на первом месте среди всех болезней человека. Заболеваемость гриппом и ОРВИ превышает суммарную заболеваемость всеми остальными инфекциями: даже вне эпидемии грипп и ОРВИ составляют до 40% всех заболеваний взрослых и более 60% заболеваний среди детей. Ежегодно по всему земному шару фиксируется ни одна сотня тысяч смертей. Каждые 2-3 года возникают эпидемии. Во время эпидемии каждый пятый россиянин болеет гриппом.
Случаются и пандемии, когда заболевает большинство населения по всему земному шару. Такое массовое инфицирование населения происходит при возникновении нового типа вируса, имеющего незнакомые для иммунной системы человека антигены, т. е. когда у всего населения земного шара нет иммунитета к данному вирусу. Пандемии опасны из-за своего масштаба, из-за тяжести заболевания у многих. Так пандемия 1918-1919 гг. унесла 20 миллионов жизней.
е. когда у всего населения земного шара нет иммунитета к данному вирусу. Пандемии опасны из-за своего масштаба, из-за тяжести заболевания у многих. Так пандемия 1918-1919 гг. унесла 20 миллионов жизней.
Иммунитет после перенесенного гриппа кратковременный, типоспецифический (т.е. только к тому типу вируса, который вызвал заболевание). Повторные заболевания, вызванные этим же типом вируса возможны через 2-5 лет.
Наиболее частым осложнением гриппа является вторичная бактериальная пневмония. Именно от нее погибает большинство детей младшего возраста, пожилых людей и больных, страдающих хроническими заболеваниями. Пневмония развивается спустя 4-14 дней после исчезновения симптомов гриппа.
Кроме пневмонии встречаются и другие респираторные осложнения: круп (ларинготрахеит), средний отит, синусит, ринит. Грипп также может спровоцировать обострение хронических заболеваний легких (астма, бронхит), декомпенсацию сердечно-сосудистых заболеваний (миокардит, перикардит), почечной недостаточности или эндокринных расстройств (сахарный диабет).
Для профилактики гриппа используются живые, инактивированные, субъединичные и сплит-вакцины.
В Свердловской области преимущественно для вакцинации против гриппа используются субъединичные и сплит-вакцины.:
- Гриппол и Гриппол-плюс. Применяется с 6-ти месячного возраста.
- Совигрипп. Применяется с 6-ти месячного возраста.
- Ультрикс. Применяется с 6 лет.
- Флюарикс (Бельгия) Применяется с 12-ти месяцев.
- Инфлювак (Нидерланды) Применяется с 6-ти месяцев.
- Агриппал (Италия) Применяется с 6-ти месяцев.
- Бегривак (Германия) Применяется с 6-ти месяцев.
- Ваксигрип (Франция) Применяется с 12-ти месяцев.
Инактивированные вакцины вводят внутримышечно или глубоко подкожно в верхнюю треть наружной поверхности плеча.
Говоря обо всех этих вакцинах, хотелось бы отметить, что в состав данных вакцин не входит вирус ни в живом, ни в убитом виде. Все перечисленные вакцины содержат только поверхностные антигены вируса, на которые и вырабатывается иммунитет. Заболевание они вызывать не могут. Наличие же симптомов вирусной инфекции после прививки у некоторых людей связано с тем, что прививки против гриппа делаются в период роста респираторной инфекции. Это просто ОРВИ, которая была бы и без прививки. Это случайное совпадение. От гриппа же прививки эти защищают очень надежно, даже если иммунитет после прививки формируется на фоне ОРВИ. При этом не утяжеляется течение респираторной инфекции. Прививки против гриппа лучше делать до начала эпидемического сезона гриппа.
Заболевание они вызывать не могут. Наличие же симптомов вирусной инфекции после прививки у некоторых людей связано с тем, что прививки против гриппа делаются в период роста респираторной инфекции. Это просто ОРВИ, которая была бы и без прививки. Это случайное совпадение. От гриппа же прививки эти защищают очень надежно, даже если иммунитет после прививки формируется на фоне ОРВИ. При этом не утяжеляется течение респираторной инфекции. Прививки против гриппа лучше делать до начала эпидемического сезона гриппа.
Прививочные реакции и осложнения. Живые вакцины в течение 3 суток после вакцинации у 2% привитых могут вызывать повышение температуры до 37,50С, легкое недомогание, головную боль, катаральные явления. При подкожном введении убитых вакцин допускается кратковременное повышение температуры выше 37,50С или инфильтратов до 50 мм не более, чем у 3% привитых. При впрыскивании вакцины в нос также возможно кратковременное повышение температуры. Субъединичные и сплит-вакцины дают слабые кратковременные реакции.
Возможны аллергические реакции при наличии анафилактической реакции на куриный белок. В этом случае прививки против гриппа противопоказаны.
ВАКЦИНЫ ПРОТИВ ПАПИЛЛОМАВИРУСНОЙ ИНФЕКЦИИ
В настоящее время известно более 120 типов вируса паппиломы человека, некоторые из них вызывают бородавки на коже, но более 30 типов инфицируют половой тракт. Инфицирование женщин вирусом паппиломы человека является важнейшим фактором канцерогенеза шейки матки. Этот вирус был выявлен в 99,7% биоптатов у женщин с раком шейки матки. Рак шейки матки занимает второе место среди злокачественных опухолей репродуктивных органов у женщин и уступает только раку молочной железы.
По региональному календарю прививки против папилломавирусной инфекции рекомендованы девушкам с 13 летнего возраста.
Для иммунопрофилактики используется две вакцины:
- Гардасил (Мерк Шарп и Доум) – 1 доза (0,5 мл) содержит белок L1 типов 6 и 18 (по 20 мкг), 11 и 16 (по 40 мкг), сорбент –маморфный алюминия гидроксифофатсульфат.
 Схема введения: 0-2-6 мес.
Схема введения: 0-2-6 мес. - Церварикс (ГласкоСмитКляйн) — 1 доза (0,5 мл) содержит белок L1 типов 6 и 18 (по 20 мкг), 50 мкг 3-О-дезацил 1-4-монофосфорил липид А, алюминия 0,5 мг, 0,624 мг дигидрофосфат-динидрата. Схема введения: 0-1-6 мес.
Вакцины вводятся внутримышечно.
Введение любой вакцины вызывает ответную реакцию организма. Это начинает работать иммунная система в ответ на введение антигенов возбудителя. Иногда эти реакции имеют клинические проявления. Это обычные, нормальные вакцинальные реакции (процессы), под которыми понимают изменения в организме, развивающиеся с определенным постоянством после введения той или иной вакцины.
Из всех реакций на вакцину чаще регистрируется боль в месте инъекции и головная боль, кратковременное повышение температуры, тошнота, рвота, боли в мышцах и суставах. Крайне редко могут быть сыпи, зуд, воспаление органов малого таза.
ВАКЦИНЫ ПРОТИВ РОТОВИРУСНОЙ ИНФЕКЦИИ
Ротовирусная инфекция – основная причина острого гастроэнтерита, к возрасту 5 лет ею переболевают практически все дети.
 Эпидемии наблюдаются в зимне-весенний период. В мире ротовирус уносит более 600000 детских жизней в год.
Эпидемии наблюдаются в зимне-весенний период. В мире ротовирус уносит более 600000 детских жизней в год.Инкубационный период составляет до пяти суток, при этом острый период начинается с третьего-седьмого дня. Для восстановления после перенесённой болезни ребёнку требуется до пяти суток.
Для данного заболевания характерно острое начало. Основными его признаками являются рвота, резкое повышение температуры тела, часто возникает понос. Стул при данном патологическом состоянии довольно характерный. В первый день он жидкий, желтый, затем приобретает глинообразную окраску. Обычно среди заболевших отмечается появление насморка, покраснение горла и болезненные ощущения при глотании. Для острого периода характерно отсутствие аппетита, а также состояние упадка сил. Ротовирусная инфекция у детей имеет следующее течение: утром отмечается вялость, капризность, тошнота, возможна рвота (иногда со слизью). Аппетит значительно снижен, после принятия пищи рвота характеризуется присутствием кусочков непереваренной еды, также она возникает при употреблении жидкости в объёме свыше пятидесяти миллилитров. В течение дня повышается температура тела, причём к вечеру она может достигать тридцати девяти градусов. Длительность состояния с повышенной температурой может составлять пять дней.
В течение дня повышается температура тела, причём к вечеру она может достигать тридцати девяти градусов. Длительность состояния с повышенной температурой может составлять пять дней.
Самолечение грозит развитием осложнений и более тяжёлым течением заболевания. К таким осложнениям относят присоединение к вирусу бактериальной инфекции, отмирание клеток головного мозга (при значительном повышении температуры). В тяжёлых случаях может отмечаться летальный исход.
В Российской Федерации зарегистрировано две вакцины против ротовирусной инфекции:
- Роторикс (Англия)
- РотаТек (Швецария)
Реактогенность обеих вакцин низкая. Вакцины живые в виде капель в рот. Крайне редко в поствакцинальный период может быть повышение температуры, разжижение стула, иногда – рвота.
Первую прививку против ротовирусной инфекции необходимо поставить в возрасте с 6 до 12 недель, все три – до 32 недель. Вакцинация проводится трехкратно с интервалом между прививками в 1 месяц.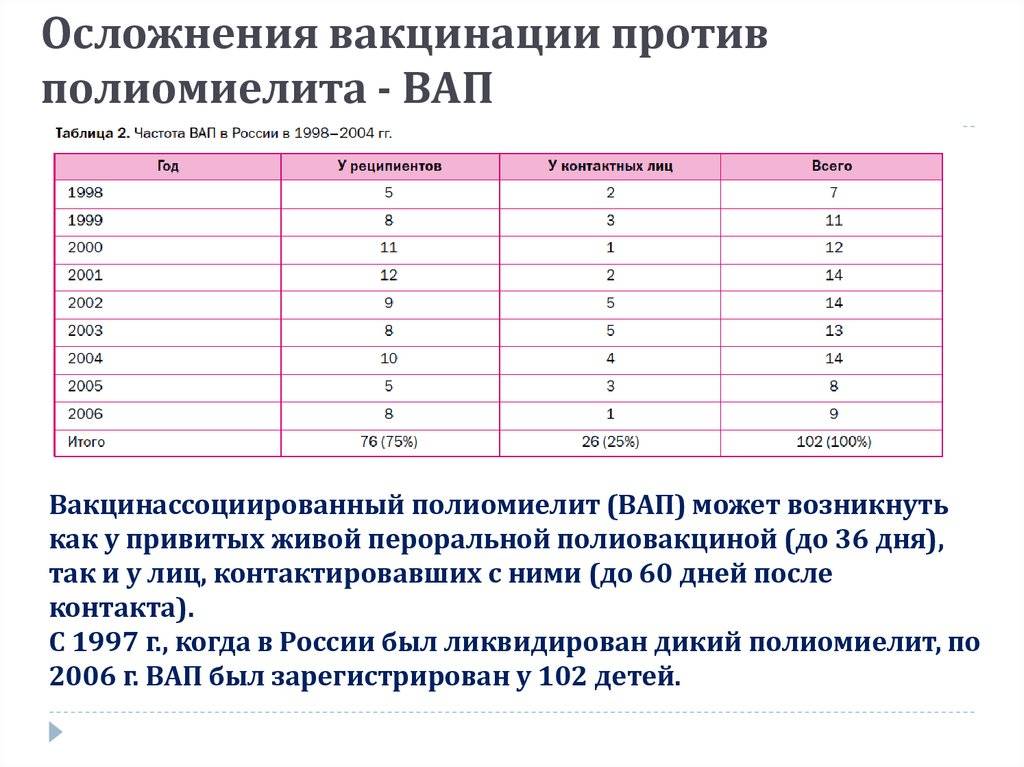
Полиомиелит — сделать прививку в Москве в ЦКБ РАН
Полиомиелит – это высоко заразное заболевание, вызываемое полиовирусом (poliovirus hominis). Особую опасность инфекция представляет для детей первых пяти лет жизни.
Вирус поражает нервную систему и может вызвать паралич или даже смерть всего за несколько часов. Возбудитель распространяется фекально-оральным путем от больного человека или здорового носителя через общие предметы обихода (игрушки, посуда, полотенце) и загрязненные руки; может содержаться в воде, молоке, пищевых продуктах.
В редких случаях, ребенок, непривитый против полиомиелита, может заразиться от сверстников, вакцинированных оральной живой полиомиелитной вакциной (ОПВ), так как после иммунизации ОПВ вирус может выделяться вакцинированным человеком с калом до 60 дней. Длительный инкубационный период и неспецифические симптомы в начале болезни не сразу могут позволить установить диагноз полиомиелита. Эффективных средств лечения этого заболевания не разработано.
Эффективных средств лечения этого заболевания не разработано.
Полиовирус представляет опасность для человека в любом возрасте с развитием стойкого необратимого паралича конечностей и их дальнейшей деформации (чаще всего нижних конечностей).
В одном из 200 случаев инфицирования развивается необратимый паралич, а 5-10% из числа таких парализованных людей умирают из-за наступающего паралича дыхательных мышц.
Полиомиелит опасен и другими осложнениями, такими как воспаление легких (пневмония), сердечной мышцы (миокардит), кровотечением и язвой желудочно-кишечного тракта.
По данным ВОЗ, в настоящее время эндемичными по полиомиелиту являются 2 страны — Афганистан и Пакистан, — но в связи с миграцией населения ежегодно отмечаются единичные «завозные» случаи из Индии, Африки, Юго-Восточной и Средней Азии.
Вакцинация против полиомиелита входит в Национальный календарь профилактических прививок РФ и начинает проводиться с первых месяцев жизни.
Первые две прививки против полиомиелита проводятся инактивированной вакциной в форме инъекции.
Для защиты от вируса возможно использование моновакцин (Полимилекс, Имовакс Полио, Полиорикс), либо в составе комбинированных вакцин (Пентаксим, Инфанрикс гекса), включающих антигены против коклюша, дифтерии и столбняка, вирусного гепатита В, гемофильной инфекции типа b.
Дальнейшая иммунизация ребенка проводится живой ослабленной вакциной перорально (в виде капель в рот) — БиВак Полио, что способствует обеспечению долговременной защиты против полиомиелита.
Важно помнить!!! Риск заболеть полиомиелитом для детей значительно выше, чем риск побочных последствий от применения оральной полиовакцины.
Вакцинопрофилактика
Забор крови (из вены)
- понедельник, среда, четверг – 8.00-9.40,
- пятница – 8.00-9.00
В это время другие манипуляции не проводятся!
- 12.
 30-16.00 – уборка, кварцевание, проветривание, работа с документами.
30-16.00 – уборка, кварцевание, проветривание, работа с документами.
|
Понедельник |
10.00 – 12.30 |
16.00 – 19.30 |
|---|---|---|
|
Вторник |
08.00 – 12.30 |
16.00 – 19.30 |
|
Среда |
10.00 – 12.30 |
16.00 – 19.30 |
|
Четверг |
10.00 – 12.30 |
16.00 – 19.30 |
|
Пятница |
08.00 – 12.30 |
16. |
Вакцинопрофилактика для детей – наиболее удобный и распространенный способ защиты организма от инфекционных заболеваний. В настоящее время прививки успешно защищают людей от серьезных инфекционных заболеваний, способных вызвать тяжелые осложнения, сделать человека инвалидом или стать причиной смерти. При введении в организм ребенка, вакцины обеспечивают выработку специфической защиты (антител и специальных клеток). Когда организм встречается с настоящим возбудителем инфекции, то выработанная защита препятствует развитию болезни или смягчает тяжесть ее течения.
Если мама сама была защищена от всех инфекций, то через плаценту она передаст своему малышу специфические антитела. Они обеспечат защиту ребенка от опасных инфекций в первые месяцы жизни. Но с трех-пяти месяцев начинают разрушаться антитела, защищающие от дифтерии, столбняка и т. д. К 12 месяцам разрушаются антитела, защищающие против кори. Поэтому именно с этого возраста необходимо начать создавать защиту с помощью введения вакцин. Чтобы к тому времени, когда антитела, которые получены от мамы разрушатся, у малыша была уже собственная защита.
Чтобы к тому времени, когда антитела, которые получены от мамы разрушатся, у малыша была уже собственная защита.
В каждой стране формируется свой Национальный календарь профилактических прививок: он включает перечень инфекционных заболеваний, против которых целесообразно сформировать защиту, возраст, в котором целесообразно сделать ту или иную прививку. В календарь прививок входят не все возможные инфекционные заболевания, против которых существуют эффективные вакцины, а только те инфекции, которые могут иметь массовое (активное) распространение на территории страны, которые могут протекать тяжело, давая осложнения и даже смертельные исходы.
В Национальном календаре прививок обозначены минимальные интервалы между прививками. Эти интервалы нельзя сокращать, но в случае необходимости можно увеличивать.
В календаре прививок используется два термина: «вакцинация» и «ревакцинация». Что это такое?
«Вакцинация» — это первичное (или несколько первичных) введений вакцины (анатоксина), которое обеспечивает формирование базового иммунитета против той или иной инфекции. Например, для того, чтобы сформировать базовый иммунитет против дифтерии необходимо трехкратное введение противодифтерийного анатоксина.
Например, для того, чтобы сформировать базовый иммунитет против дифтерии необходимо трехкратное введение противодифтерийного анатоксина.
«Ревакцинация» — повторное (или повторные) введения вакцины (анатоксина), которые способствуют поддержанию (продлению) сформированного ранее базового иммунитета.
В поликлинике имеются в наличии вакцины:- Эупента — (АКДС+ВГВ+ХИБ(V-1-2-3) комбинированная вакцина для профилактики дифтерии, столбняка, коклюша ( цельно-клеточный компонент), вирусного гепатита В и гемафильной инфекции. Страна производитель-Корея.
- Хаврикс — вакцина для профилактики вирусного гепатита «А» у детей в возрасте с 1 года. Страна производитель-Бельгия.
- АКДС – вакцина коклюшно-дифтерийно-столбнячная адсорбированная. Страна производитель-Россия.
- Приорикс – комбинированная живая вакцина для профилактики кори, эпидемического паротита и краснухи. Страна производитель-Бельгия.

- Имовакс Полио – инактивированная вакцина для профилактики полиомиелита. Страна производитель-Франция.
- АДС-м (в возрасте 6 и 16 лет) — адсорбированная комбинированная вакцина с уменьшенным содержанием антигена против дифтерии и столбняка. Страна производитель-Россия.
- Гриппол плюс – инактивированная вакцина для профилактики гриппа начиная с 6-мес. жизни. Страна производитель – Россия.
- По показаниям (ВКК): Синфлорикс, Гексаксим, Акт-хиб
Вакцина ЭУПЕНТА (LG Chem, Korea) предназначена для профилактики пяти инфекций: коклюша (цельноклеточный компонент), дифтерии, столбняка, вирусного гепатита В и гемофильной инфекции.
Плановая вакцинация 1-3 против коклюша, дифтерии и столбняка будет осуществляться с использованием вакцины ЭУПЕНТА. Вакцинация 2-3, начатая вакцинами АКДС или Тетраксим может, быть продолжена или завершена вакциной ЭУПЕНТА (основание письмо МЗ РБ от 04.01.2018 №6-18/58)
Вакцина прошла все необходимые испытания на безопасность и эффективность и рекомендована ВОЗ к широкому применению.
Вакцина ЭУПЕНТА (АКДС+ВГВ+ХИБ) является удобным вакцинным препаратом, позволяющим сократить количество инъекций для достижения иммунитета сразу к пяти инфекционным болезням. Вакцину получат все дети первого года жизни 3-кратно.
Согласно письму МЗ РБ от 26.01.2018 № 7-18/1212 вакцинация против коклюша, дифтерии, столбняка, гемофильной инфекции, вирусного гепатита В и полиомиелита по следующим схемам:
1. Детям, получившим вакцинацию-1 и вакцинацию-2 против вирусного гепатита В с использованием моновакцин и не получившим вакцинацию против коклюша, дифтерии, столбняка и полиомиелита проводить:
1.1. вакцинацию-1 против коклюша, дифтерии и столбняка с использованием вакцины ЭУПЕНТА (при этом ребенок получит вакцинацию-3 против вирусного гепатита В и вакцинацию-1 против гемофильной инфекции) и вакцинацию-1 против полиомиелита с использованием инактивированной полиомиелитной вакцины;
1.2. вакцинацию-2 против коклюша, дифтерии и столбняка с использованием вакцины ЭУПЕНТА (при этом ребенок получит вакцинацию-4 против вирусного гепатита В и вакцинацию-2 против гемофильной инфекции) и вакцинацию-2 против полиомиелита с использованием инактивированной полиомиелитной вакцины;
1. 3. вакцинацию-3 против коклюша, дифтерии и столбняка с использованием вакцины АКДС и вакцинацию-3 против полиомиелита с использованием инактивированной полиомиелитной вакцины;
3. вакцинацию-3 против коклюша, дифтерии и столбняка с использованием вакцины АКДС и вакцинацию-3 против полиомиелита с использованием инактивированной полиомиелитной вакцины;
2. Детям, получившим вакцинацию-1, вакцинацию-2 и вакцинацию-3 против вирусного гепатита В с использованием моновакцин и не получившим вакцинацию против коклюша, дифтерии, столбняка и полиомиелита проводить:
2.1. вакцинацию-1 против коклюша, дифтерии и столбняка с использованием вакцины ЭУПЕНТА (при этом ребенок получит вакцинацию-4 противовирусного гепатита В и вакцинацию-1 против гемофильной инфекции) и вакцинацию-1 против полиомиелита с использованием инактивированной полиомиелитной вакцины;
2.2. вакцинацию-2 против коклюша, дифтерии и столбняка с использованием вакцины АКДС и вакцинацию-2 против полиомиелита с использованием инактивированной полиомиелитной вакцины;
2.3. вакцинацию-3 против коклюша, дифтерии и столбняка с использованием инактивированной полиомиелитной вакцины.
С целью формирования полноценной защиты против гемофильной инфекции вакцинацию 1 и (или) 2, начатую вакциной ЭУПЕНТА целесообразно завершить с использованием монокомпонентной вакцины против гемофильной инфекции (при наличии иммунобиологического лекарственного средства против данного инфекционного заболевания).
Вышеуказанная тактика вакцинации рассмотрена на заседании экспертного совета по иммунизации Министерства здравоохранения Республики Беларусь 24.01.2018 г. и одобрена его членами.
Согласно письму МЗ РБ от 20.02.2018 № 7-10/2405 «О вакцинации против вирусного гепатита В» вакцинация против вирусного гепатита В может проводится по следующим схемам:
1. в 3-дозовом графике первая доза вакцины против гепатита В (моновакцины) вводится при рождении, а вторая и третья дозы (моновакцины или комбинированной вакцины) – одновременно с введением первой и третьей дозы АКДС-содержащий вакцины.
2. в 4-дозовом графике первая доза вакцины против гепатита В (моновакцины) вводится при рождении, далее вводится три дозы (моновакцины или комбинированной вакцины), одновременно с введением трех доз АКДС-содержащий вакцины. При этом дополнительная доза вводимой вакцины против гепатита В является безопасной. Интервал между дозами должен быть минимун четыре недели.
Внимание! Имеющиеся моновакцины или комбинированные вакцины, содержащие компонент против гепатитаВ, могут быть взаимозаменяемыми в рамках программ иммунизации».
Директор Центра имени Чумакова советует ревакцинироваться через 6-9 месяцев после первой прививки
В России официально зарегистрированы четыре вакцины от COVID-19. Для ревакцинации можно использовать любую из них, считает генеральный директор Федерального научного центра исследований и разработки иммунобиологических препаратов им. М.П. Чумакова РАН Айдар Ишмухаметов. В интервью «Парламентской газете» глава центра, создавшего третью отечественную вакцину, «КовиВак», рассказал об особенностях препарата и оценил его эффективность при защите от «индийского» штамма коронавируса, которым сегодня болеет большинство заразившихся россиян.
— Айдар Айратович, чем «КовиВак» отличается от «Спутника» и «ЭпиВакКороны»?
— Вакцина произведена по классической технологии, которую наш институт использовал при создании препарата от полиомиелита и жёлтой лихорадки. Технология эта небыстрая, поэтому процесс создания вакцины занял почти год. Если вкратце, то такой способ предполагает сначала выделение вируса и выращивание его в определённых средах. Затем мы этот вирус размножаем и чистим, чтобы он был инактивированным, но в нём осталось действующее вещество-антиген. После чего убитый вирус включается в состав профилактического средства, именуемого вакциной. Вот в чём основное отличие цельновирионной вакцины от современных препаратов, где используют либо фрагменты, либо информационную часть (РНК) вируса.
Затем мы этот вирус размножаем и чистим, чтобы он был инактивированным, но в нём осталось действующее вещество-антиген. После чего убитый вирус включается в состав профилактического средства, именуемого вакциной. Вот в чём основное отличие цельновирионной вакцины от современных препаратов, где используют либо фрагменты, либо информационную часть (РНК) вируса.
— А среди зарубежных вакцин есть произведённые по классической технологии?
— По такому же пути, как и мы, пошли китайские разработчики. В Индии сейчас работают над живой вакциной «Ковивак». С моей точки зрения, у живой вакцины большое будущее. Для примера, разработанная нашим институтом вакцина от полиомиелита уже 60 лет спасает людей от этой болезни. Ничего лучше пока придумать не могут.
— Когда центр Чумакова начал работу над вакциной, был распространён «уханьский» штамм. Как защитит «Ковивак» от «индийского» штамма?
— Здесь надо учитывать, что COVID-19 — вирус новый и имеет определённый запас изменчивости. При распространении в разных странах он видоизменяется, отсюда и различные ветки вируса. Но мы исходим из того, что это не кардинальные изменения, они касаются доли процентов в отношении самого размера вируса. Ведь коронавирус достаточно сложный, с большим антигенным составом.
При распространении в разных странах он видоизменяется, отсюда и различные ветки вируса. Но мы исходим из того, что это не кардинальные изменения, они касаются доли процентов в отношении самого размера вируса. Ведь коронавирус достаточно сложный, с большим антигенным составом.
Мы рассчитываем, что при вакцинации цельным вирусом мы захватываем наибольшее количество антигенов, поэтому изменчивость коронавируса не будет играть решающей роли.
Но пока не проведены все испытания, это умозрительные заключения. Нам предстоит большая работа по созданию модели взаимодействия нашей вакцины с новым вирусом. По её итогам мы будем знать, насколько антитела, которые создаются, нейтрализуют индийский штамм. Думаю, что течение 2-3 недель у меня будет предварительный ответ на эти вопросы.
— Кому сейчас показана вакцина «КовиВак»? Планируете ли вы разработку универсальной вакцины, рассчитанной на широкий круг людей?
— Она изначально рассчитана на всех. Я абсолютно уверен в том, что вакцина в том варианте, в котором она есть сейчас, годится и для детей. Но нужно провести испытания. Таков регламент.
Я абсолютно уверен в том, что вакцина в том варианте, в котором она есть сейчас, годится и для детей. Но нужно провести испытания. Таков регламент.
Сейчас мы на старте третьей фазы испытаний, разрешение получено две недели назад. Этот этап предполагает испытания на людях с сопутствующими патологиями: хроническими заболеваниям лёгких, аутоиммунными заболеваниями, онкологией. Разумеется, все испытания будут проходить с профильными специалистами. Потом подведём итоги.
Пока, по итогам двух первых фаз испытаний, могу сказать, что наша вакцина не имеет побочных эффектов: нам не удалось зафиксировать ни одного такого случая. Вакцина получилась довольно лёгкая, поэтому она подходит для ревакцинации после других препаратов.
— То есть через полгода после «Спутника» и «ЭпиВакКороны» человек может сделать прививку «КовиВаком»?
— Совершенно верно. И мировой опыт это доказывает. Сегодня не описано противопоказаний к тому, чтобы вакцинироваться одной вакциной, а через полгода поставить другую. Многие профилактические препараты, к примеру, от полиомиелита, клещевого энцефалита, предполагают обязательную ревакцинацию. Повторюсь, побочных эффектов от «КовиВака» пока найти не удалось. Следовательно, дополнительное введение препарата через полгода точно пагубного эффекта иметь не будет
Многие профилактические препараты, к примеру, от полиомиелита, клещевого энцефалита, предполагают обязательную ревакцинацию. Повторюсь, побочных эффектов от «КовиВака» пока найти не удалось. Следовательно, дополнительное введение препарата через полгода точно пагубного эффекта иметь не будет
С коронавирусом мы многое проходим заново. Ожидания разработчиков вакцин, что мы получим защиту на длительный период — год, два или даже пожизненную, не оправдались. По-видимому, в период эпидемий ревакцинироваться потребуется где-то через полгода — девять месяцев после прививки. Может быть, со временем, когда будет достигнут иммунитет и будут фиксироваться отдельные заболевания, мы перейдём к одной вакцинации в год.
— Как оценивают созданную центром Чумакова вакцину в ВОЗ?
— Мы подали документы, к нам приезжали представители Всемирной организации здравоохранения. Они нас хорошо знают по проекту создания вакцины от жёлтой лихорадки ещё в доковидные времена. Поясню, регистрацию ведь проходит не только сам препарат. Регистрируют площадку, условия выпуска и, конечно, кадры. Мы, напомню, единственный в стране научно-производственный комплекс Минобрнауки, нас поддерживает РАН. То есть лаборатория, где разрабатывают вакцину, и завод в одном лице. Научный потенциал, который был наработан за 60 лет, — это и есть основа экспертизы для ВОЗ. Полагаем, что процесс регистрации «КовиВак» пройдёт легче, чем вакцина от жёлтой лихорадки.
Регистрируют площадку, условия выпуска и, конечно, кадры. Мы, напомню, единственный в стране научно-производственный комплекс Минобрнауки, нас поддерживает РАН. То есть лаборатория, где разрабатывают вакцину, и завод в одном лице. Научный потенциал, который был наработан за 60 лет, — это и есть основа экспертизы для ВОЗ. Полагаем, что процесс регистрации «КовиВак» пройдёт легче, чем вакцина от жёлтой лихорадки.
Но сейчас главная проблема не в том, зарегистрирует ВОЗ наш препарат или нет, а в том, что в нашей стране должен быть достигнут популяционный иммунитет. Пока он недостаточный.
— Какие инициативы вы ждёте от восьмого созыва Госдумы, чтобы ваш институт имел возможность как можно скорее разрабатывать и запускать в оборот новые вакцины на благо всей страны?
— Как руководителя научно-производственного комплекса меня больше всего беспокоит закон о госзакупках. Уверен, существующая система закупок нуждается в изменениях. Вопросы, связанные с приобретением за счёт госсредств современного оборудования, подопытных животных, сегодня не вполне отредактированы. Это мнение разделяют многие мои коллеги.
Вопросы, связанные с приобретением за счёт госсредств современного оборудования, подопытных животных, сегодня не вполне отредактированы. Это мнение разделяют многие мои коллеги.
«Я узнала состав вакцин, и у меня был шок!» Почему пермские родители отказываются прививать детей, и к чему это может привести
Интернет-журнал «Звезда» разыскал пермских родителей, которые сознательно отказались прививать своих детей. И поговорил с медиками о том, к чему может привести отказ от вакцинации.
«Врачи не вызывают доверия»
У Анны Докшуковой — неоконченное высшее образование. Она училась в педагогическом институте на психолога-логопеда, сейчас большую часть своего времени посвящает воспитанию младшей дочери. Ко вторым родам Анна тщательно готовилась. Два года назад она рожала в бассейне, девочка появилась на свет здоровой.
Иллюстрация: Вероника Быстрых«Во время беременности я слушала много лекций на тему прививок, пополняла информацию. И очень рада, что не сделала дочери ни одной прививки, — заявляет Анна.
— За эти два года мы ничем не болели. С врачами я не консультировалась. Медики, с которыми мне приходилось общаться, доверия не вызывают. С ними мне общаться не о чем».
Родители черпают информацию о вакцинации из интернета и социальных сетей. На запрос «Стоит ли делать прививки ребёнку?» поисковик выдает более полутора миллионов ответов. Среди них есть сайты, которые пропагандируют отказ от прививок. На «Движении жизни» (создатели говорят, что его цель — «чтобы превратилась наша Земля во фруктовый сад, чтобы пробудились Люди ото сна крепкого, вышли из системы искусственно созданной, осознали бытие и сделали всё сущее Счастливым») самые популярные статьи «25 причин сказать прививкам — нет!» и «Как отказаться от прививок на законных основаниях».
В социальных сетях созданы десятки антипрививочных сообществ. Самые большие российские группы — «Правда о прививках», на которую подписано 94 тыс. пользователей, «Прививки: „за“ и „против“» (40 тыс. ) и «Мамы и папы против прививок». (6 тыс.). В пермском сегменте такие группы тоже представлены. В «Пермский край против прививок» 478 пользователей, а в «Прививкам — нет! Пермь» — 442.
) и «Мамы и папы против прививок». (6 тыс.). В пермском сегменте такие группы тоже представлены. В «Пермский край против прививок» 478 пользователей, а в «Прививкам — нет! Пермь» — 442.
Вакцина «обучает» иммунную систему
Смысл вакцинации заключается в том, что в организм человека вводят ослабленные, убитые возбудители различных инфекций или искусственно синтезированные белки, которые идентичны белкам возбудителя. Когда вакцина попадает в организм, иммунная система изучает её, запоминает и начинает вырабатывать специальные вещества для её уничтожения. Поэтому у человека вырабатывается специфический иммунитет. Вакцина как бы «обучает» иммунную систему, подготавливая её к борьбе с «полноценной» инфекцией.
Иными словами, попадая в организм, вакцины вызывают такую же перестройку иммунной системы, которая происходит в результате настоящего заражения. Но человек при этом не заболевает. После такой подготовки попадание инфекционных агентов в организм вызывает быстрое и мощное противодействие иммунной системы, и болезнь не развивается.
С помощью вакцинации можно предотвратить более 30 опасных заболеваний. Многие прививки можно делать одновременно. При этом существует ряд препаратов, которые изначально представляют собой смесь нескольких вакцин — АКДС, например, направлена против коклюша, дифтерии и столбняка.
Некоторые вакцины создают иммунитет с первого раза, другие приходится вводить повторно. Это называется ревакцинация, она направлена на поддержание иммунитета, выработанного предыдущими прививками. Обычно она проводится через несколько лет после первой вакцинации.
Врачи говорят, что у вакцинации есть противопоказания. Не следует делать прививки, если у человека были аллергические реакции на предыдущие введения вакцины, аллергия к отдельным компонентам, высокая температура, тяжёлая гипертония и ревматические болезни.
Медики и эпидемиологи разработали национальные календари прививок. В них прописывают, от каких инфекций и в каком возрасте человек должен пройти очередную вакцинацию. Календари есть в любой стране мира.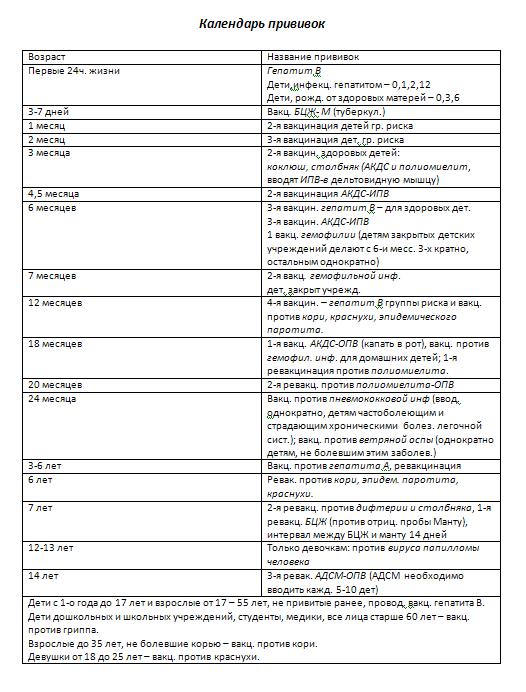 В США он предполагает защиту от 17 инфекций, в европейских странах — от 14-15, а в России — от 12. В ближайшие годы его хотят расширить на 2-3 позиции.
В США он предполагает защиту от 17 инфекций, в европейских странах — от 14-15, а в России — от 12. В ближайшие годы его хотят расширить на 2-3 позиции.
Календари прививок составляются на основе двух факторов — актуальности инфекции для той ли иной страны и возможности бюджета обеспечить граждан вакциной. Современные иммунобиологические препараты довольно дорогостоящие.
В России Национальный календарь прививок — это официальный документ, утверждённый приказом Минздрава. Виды и сроки вакцинаций в нём определены программой обязательного медицинского страхования, то есть бесплатны для застрахованных.
«В составе формальдегид, им консервируют трупы»
Антонина Комкова окончила Пермский политех, сейчас работает главным бухгалтером в ТСЖ. У Антонины двое детей. Она их не прививает, потому что «слишком много факторов, которые влияют на конечный результат: хранение вакцины, навык медсестры и реакция организма ребёнка». Однажды она пришла в поликлинику и попросила показать состав вакцины.
— Там был фенол, который добавляют в средство для опрыскивания овощей; формальдегид, которым консервируют трупы; оксид ртути; оксид алюминия; средство для стерилизации (я забыла, как оно называется) и многое другое. Я пришла в ужас! — вспоминает она.
Маму четверых детей Юлию Будько тоже пугает состав вакцин с «вредными веществами»:
— В них входят соединения ртути, алюминия, фенол и другие ядовитые консерванты, которые могут вызывать тяжёлые повреждения мозга, сильные аллергии и другие последствия вплоть до летального исхода. Есть официально признанные последствия, которые могут появиться после вакцинации. Я не хочу подвергать риску своих детей ради сомнительного эффекта от вакцин.
Иллюстрация: Вероника БыстрыхЕкатерина Шишкина находится в декретном отпуске. Своего семимесячного ребёнка прививать она отказывается:
— Состав прививок негативно влияет на организм человека вплоть до летального исхода. При этом медицинские работники не рассказывают о вреде и возможности осложнений после вакцинации и ответственность за это не несут.
Мама двух дошколят Надежда Попова считает, что в составе бесплатных вакцин есть «тяжёлые металлы», а в платных — «обезьяньи почки или ткани абортированных младенцев»:
— У медиков нет исследований, подтверждающих безопасность данных материалов. А уж религиозный аспект я здесь даже не рассматриваю.
У госслужащей Ирины Соболевой двое детей — старшему 12, младшему четыре.
— Когда я начала изучать, из чего состоят вакцины, какой у них срок годности, для чего это нужно и какие последствия могут быть, у меня был шок! Я зареклась, что больше никаких вакцин — хватит травить детей химией! У моего старшего ребёнка с детства была аллергия, чуть до астмы не дошло. Он часто очень болел, иммунитет был ослаблен. Но я не подозревала, что это может быть от вакцин.
«Причина отказов — это страх»
По официальным данным Роспотребнадзора, количество отказов от прививок в России не превышает 5 % от общего числа прививающихся. Неофициальные источники говорят о других цифрах. В одном из интервью ведущий эксперт по вакцинопрофилактике, профессор Владимир Таточенко сказал, что охват прививками составляет около 65-70 %. В опроснике, в котором приняли участие более 22 тыс. человек, проведённом осенью прошлого года в одном из сообществ «ВКонтакте», только 54 % респондентов высказались «за» вакцинацию. Точной цифры «отказников» никто не знает.
В одном из интервью ведущий эксперт по вакцинопрофилактике, профессор Владимир Таточенко сказал, что охват прививками составляет около 65-70 %. В опроснике, в котором приняли участие более 22 тыс. человек, проведённом осенью прошлого года в одном из сообществ «ВКонтакте», только 54 % респондентов высказались «за» вакцинацию. Точной цифры «отказников» никто не знает.
— Причины отказов — боязнь осложнений и мировоззрение родителей, — говорит заведующая отделением Пермской краевой клинической детской больницы, врач-иммунолог Екатерина Троицкая. — Некоторые считают, что «всё должно быть естественным», а «причина заболеваний, в том числе и инфекционных, — нарушения в организме из-за плохой экологии и медицинских вмешательств».
С ней соглашается аллерголог-иммунолог Закамского центра иммунопрофилактики Людмила Евдокименко.
— Самая распространённая причина — это страх, — рассуждает она. — Сейчас нет вспышек тяжёлых инфекционных заболеваний, которые удалось победить с помощью прививок. Дети не умирают от дифтерии или туберкулёзного менингита и не становятся инвалидами после полиомиелита. В тоже время риск возникновения поствакцинального осложнения, хоть и минимальный, но есть. Страх перед инфекциями ушёл, страх перед прививками стал перевешивать. Складывается ложное впечатление мнимого благополучия: зачем делать прививку и рисковать, если рядом никто не болеет?
Дети не умирают от дифтерии или туберкулёзного менингита и не становятся инвалидами после полиомиелита. В тоже время риск возникновения поствакцинального осложнения, хоть и минимальный, но есть. Страх перед инфекциями ушёл, страх перед прививками стал перевешивать. Складывается ложное впечатление мнимого благополучия: зачем делать прививку и рисковать, если рядом никто не болеет?
Людмила Евдокименко говорит, что риск заполучить тяжёлое осложнение после вакцинации в тысячи раз меньше,чем получить серьёзные осложнения после самого заболевания.
Иллюстрация: Вероника Быстрых«Есть очень хорошее выражение, что прививки стали жертвами свой эффективности, — продолжает она. — И как это не прискорбно, но чтобы общество развернулось в сторону вакцинации… видимо, нужна эпидемия. Понадобилось ухудшение с ситуацией по кори, а ведь эта инфекция практически была побеждена, чтобы в СМИ заговорили о пользе прививок и их необходимости, а не насаждали в умы людей идеи о „всемирном фармацевтическом заговоре“ и о том, что „прививки — это зло“, как это было ещё три-пять лет назад на фоне относительного благополучия».
Медики утверждают, что вакцинация безопасна, а опасения родителей — не обоснованы. Никаких доказательств, что прививки вызывают психические или онкологические заболевания, нет. В состав вакцин, действительно, входят стабилизаторы, консерванты и антисептики. Вакцины могут содержать различные химические соединения, но их концентрация ничтожно мала. Чтобы они стали ядом, их содержание должно быть увеличено в тысячи раз.
«Фенол становится токсичным для организма в дозах, которые в тысячи раз выше дозы, содержащейся в туберкулине, — рассказывает Людмила Евдокименко. — Кстати, фенол входит в состав не только вакцин, но многих других лекарственных препаратов: антисептиков, анальгетиков, антиагрегантов и косметических средств. А ещё он образуется в тканях организма и присутствует в различных продуктах питания: сырах, рыбе, какао, орехах, чае, растительном масле и других».
Тоже самое касается ртути, которая встречается в продуктах питания, питьевой воде и организме любого человека — даже новорождённого. А в разовой дозе вакцины АКДС количество этого вещества значительно меньше, чем в воздухе, который мы вдыхаем в течение суток. Оно не опасно для здоровья человека, но эффективно предотвращает возможность загрязнения вакцины микробами.
А в разовой дозе вакцины АКДС количество этого вещества значительно меньше, чем в воздухе, который мы вдыхаем в течение суток. Оно не опасно для здоровья человека, но эффективно предотвращает возможность загрязнения вакцины микробами.
«После прививки мы попали в реанимацию»
Состав вакцин — не единственный аргумент в отказе от прививок. Многих родителей пугают последствия. Старшая дочь Антонины Комковой ходит в садик. Перед этим ей поставили тест Манту для проверки на заболевание туберкулёзом.
— После этого у дочки заболели глаза, полтора года мы лечили конъюнктивит. Все врачи и работники минздрава утверждают, что это не от Манту — тест только спровоцировал болезнь. Я решила отказаться и от Манту — мало ли что ещё он спровоцирует. Буду обследовать другими способами, без вмешательства в организм и иммунную систему, — говорит она.
Подобные истории «Звезде» охотно рассказали многие мамы.
— После очередной прививки АКДС моему ребёнку стало плохо, мы попали в реанимацию с судорогами и высокой температурой. Я пережила такой страх потерять ребёнка, что занялась вплотную этим вопросом.
Я пережила такой страх потерять ребёнка, что занялась вплотную этим вопросом.
— У ребёнка после прививки БЦЖ случился паралич левой части тела. Во всем обвинили мать, якобы это она не подготовила ослабленного ребёнка к прививке.
Медики говорят, что реакции на прививки (повышение температуры, боль в месте укола и т. п.) не представляют угрозы для организма и встречаются с частотой в несколько процентов в зависимости от вида вакцины.
«Осложнения при вакцинации развиваются реже, чем при применении других лекарственных препаратов, и намного реже, чем при инфекционных заболеваниях, — успокаивает Екатерина Троицкая. — Причиной реакций и осложнений на вакцинацию могут быть особенности организма ребёнка. При всех нарушениях здоровья ребёнка необходимо проконсультироваться с врачом, в неотложных ситуациях — вызвать скорую помощь».
Врачи призывает не путать осложнения с реакциями на прививки — это совершенно нормальный ответ иммунной системы на введение вакцины в организм.
— Как правило, реакции не требуют медицинского вмешательства, проходят самостоятельно в течение 2-3 дней и не наносят никакого вреда ребёнку, — говорит Людмила Евдокименко. — Я в таких случаях говорю родителям: «Лучше день-два температура, чем, предположим, кашель на полгода, который ничем не снять, когда ребёнок изматывает и себя, и родителей».
Но медик соглашается, что осложнения от прививок тоже бывают.
— Они могут приводить к серьёзным, стойким нарушениям здоровья. К счастью, они встречаются чрезвычайно редко. В каждом случае происходит очень тщательный разбор с привлечением специалистов, производителей, поставщиков вакцины, чтобы выяснить, что привело к его возникновению.
Самые частые причины — это индивидуальная реакция организма или недооценка состояния здоровья ребёнка и несоблюдение правил, особенно при введении живых вакцин.
Иллюстрация: Вероника Быстрых«В нашей стране, увы, имеет место быть такая тенденция, что любое неблагоприятное событие, возникшее в поствакцинальном периоде, будет списано именно на прививку.
Но нужно чётко понимать, что „после“ не означает „из-за“. И при тщательном обследовании, как правило, оказывается, что ухудшение в состоянии здоровья пациента вызвано отнюдь не вакцинацией, а совершенно иными причинами», — поясняет Людмила.
«Союзников в среде врачей нет»
Родители говорят, что некоторые медики молчаливо одобряют отказы от прививок. Подруга Антонины Комковой работает медсестрой, она всегда её убеждала в пользе вакцинации.
— Когда я ей рассказала, почему не ставлю, она своим детям тоже перестала ставить прививки. Многие врачи, когда узнают мое мнение, кивают и не убеждают в обратном. Моя мама очень переживает, что в свое время она не могла отказаться от нашей вакцинации. Друзья в моем окружении и родные мои тоже не ставят.
У Анастасии Мудровой двое детей — сыну шесть, а дочери девять. Она вспоминает, как однажды попала на лекцию к пермскому педиатру, которая давно вышла на пенсию:
— Она-то и поведала по секрету, что непривитые дети здоровее, не болеют и вообще крепче, умнее и сильнее.
Надежда Попова рассказывает, что когда пять лет назад родился её первенец, по медицинским причинам ему нельзя было ставить прививки два месяца:
«За это время я услышала, что некоторые врачи не ставят прививки своим детям, а в карте отмечают, что поставили. И мне стало интересно, почему так. Я записалась на консультацию к врачу-иммунологу и спросила, почему в странах Европы и Америки прививка БЦЖ признана неэффективной, а у нас её ставят. Врач мне ответил, что у нас, к сожалению, пока ничего другого не придумали. Ещё я спрашивала, правда ли, что прививка не даёт полной защиты от заболевания, а иммунитет не является пожизненным. В ответ я услышала, что это так, но заболевание может протекать менее остро, чем у непривитого ребёнка».
Людмила Евдокименко опровергает утверждение, что сами врачи не ставят своим детям прививки. Она говорит, что не знает ни одного иммунолога в Перми, который отказался от вакцинации. Как правило, они прививают своих близких ещё и вакцинами, которые не входят в Национальный календарь.
— Мои дети привиты дополнительно от клещевого энцефалита, гепатита А, менингококковой инфекции, — рассказывает она. — Потому что я слишком хорошо понимаю, чем грозят эти инфекции детям, эффективного лечения от которых практически не существует. Отговорить от прививок может только тот, кто совершенно не понимает основ иммунологии и механизм действия вакцин. Сейчас в профессиональном сообществе очень остро стоит вопрос о повышении знаний медиков всех специальностей в области вакцинопрофилактики и введении меры ответственности за призыв к отказу от вакцинации. Один из популярных иммунологов в нашей стране Андрей Продеус заявил, что если врач только заикнулся о вреде прививок, он должен положить диплом на стол и уйти из профессии. И в этом я с ним солидарна, потому современный врач, разбирающийся в основах иммунологии, не может выступать против прививок.
«Все медики коррумпированы»
Многие мамы обвиняют медиков в коррумпированности. Юлия Будько уверена, что у врачей план по вакцинации, за выполнение которого им дают премии:
— Поэтому большинство [медиков] говорят, что нужно ставить прививки, причём не рассказывают ни о составе вакцин, ни о последствиях. Редкие врачи неофициально говорят, что прививки нужно ставить хотя бы после трёх лет, когда иммунитет уже установился, а лучше вообще не ставить.
Также некоторые родители говорят о запугивании со стороны врачей, мол, идёт какая то эпидемия — например, сейчас пугают корью. Другие сетуют, что нет статистики, которая бы указывала на количество заболевших привитых детей.
Иллюстрация: Вероника БыстрыхВрач-иммунолог Людмила Евдокименко говорит, что разговоры о коррумпированности медиков — это очередной миф.
— Никаких денежных выплат за проведение вакцинации доктора дополнительно не получают. Это входит в круг их профессиональных обязанностей.
«Родители приходят с отказом, а в итоге прививают ребёнка»
Российское законодательство не предусматривает санкций для родителей, которые отказываются от вакцинации детей. Отсутствие прививок может привести лишь к запрету на выезд в страны, пребывание в которых требует профилактических прививок. Кроме того, непривитому ребёнку могут временно отказать в приёме в детские сады, школы и санатории, если там есть эпидемия или её угроза.
«Я считаю, что дети без прививок не должны посещать организованные коллективы, — говорит Людмила Евдокименко. — Мы почему-то всегда помним только о своих правах и забываем об обязанностях. Но раз уж ты живёшь в обществе и пользуешься определёнными его благами, будь добр нести ответственность. Ведь другие дети так же имеют право на безопасную среду обучения. И вам бы, наверное, так же не хотелось, чтобы у соседа по парте вашего ребёнка вдруг оказалась открытая форма туберкулёза? Не следует забывать и о детях, которые в силу состояния здоровья или возраста не могут быть вакцинированы. Прививаясь, мы защищаем не только себя, но и создаём своеобразный „щит“ для таких детей».
Врач считает, что в России нет качественной пропаганды и развенчания мифов о прививках. Необходимо создать государственную программу по ограничению деятельности антипрививочников и адекватной разъяснительной работы населения о необходимости прививок и их целесообразности.
Сама Людмила читает лекции для пациентов и медработников, а ещё ведет группу «Вакцинопрофилактика» во «ВКонтакте», которую создала пару лет назад вместе с коллегой.
«Мы просто не знали, как ещё бороться с недостаточностью знаний и информации в области вакцинопрофилактики. Предполагалось, что участниками группы будут педиатры, семейные врачи, иммунологи и другие узкие специалисты. Потом стали давать ссылку своим пациентам. Порой это удобней — на досуге мама прочитает информацию и осмыслит её. Потом мы поняли, что тема вакцинации интересна родителям и докторам из других регионов. Группа стала расти. Но цель её была и остаётся одна — повышения информированности населения о достижениях вакцинопрофилактики, её значении и современных тенденциях в этой области».
Людмила Евдокимова всегда радуется, если родителей удаётся убедить в необходимости прививок и малыш оказывается защищённым.
— Бывает, родители приходят с отказом, а в итоге прививают ребёнка — просто им до этого никто доступно и понятно не объяснил смысл вакцинации, её риски и риски, связанные с отказом от прививок, а начитавшись антипрививочных сайтов, они пребывают в растерянности — чему верить и как не навредить малышу, — говорит она. — С ними нужно и необходимо разговаривать и находить нужные доводы и слова, хотя в эмоциональном плане это очень тяжело.
***
Ранее мы разбирались, почему после прививки отечественной вакцины против клещевого энцефалита заболели 186 пермских школьников.
Читайте также о том, как пермского пятиклассника не пускали в школу из-за не поставленной пробы Манту. Его мама обратилась к губернатору по поводу методов диагностики туберкулёза
| 14 | 1904 14 | 1904 14 | 1960 | 1960 | Гвинея Свинья | алюминиевый фосфат | IPV | Два инъекциями SQ, приведенные 14 дней, апартаменты либо адъюмантного IPV (14 Гвинея свиней) или неадъювантная ИПВ (12 морских свинок ), повторенная как с более низкой дозой, так и с более высокой дозой ИПВ. | Значительно более высокие значения GMT антител, нейтрализующих полиомиелит, для серотипов 1 и 2 в группе адъювантов при использовании низких доз ИПВ (5, 32 и 10.8 против 2, 14,2 и 3,2 для серотипов 1, 2 и 3 соответственно в группах с адъювантом и без адъюванта). Незначительная тенденция к более высоким GMT для всех серотипов в группе с адъювантом при использовании высоких доз ИПВ (50,8, 101,6 и 40,3 против 18, 45,2 и 35,9 для серотипов 1, 2 и 3 соответственно в группах с адъювантом и без адъюванта). | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 16 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 16 | 1 | RHESUS Оксид алюминия | оксид алюминия | Mahoneent (тип 1 Mahoney) IPV | восемь групп из шести обезьян каждый дан либо адъювандный или неаджулатный IPV, либо IM или SQ, либо по схеме с 2 дозами (в дни 0 и 42), либо по схеме с 3 дозами (в дни 0, 28 и 60) группы после введения всех доз вакцины (33.5 против 4,5). Обезьян заражали тремя внутримышечными инъекциями активного полиовируса серотипа 1 + стероиды. После контрольного заражения у 2/16 (12,5%) из обезьян, вакцинированных адъювантной ИПВ, по сравнению с 15/19 (78,9%) обезьян, вакцинированных неадъювантной ИПВ, по сравнению с 9/10 обезьян (90%) из невакцинированной контрольной группы, развился паралич. полиомиелит. При гистологическом исследовании 3/16 (18,7%) группы адъювантной терапии по сравнению с 18/19 (94,7%) группы без адъювации имели поражение центральной нервной системы. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 17 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 17 | 1967 | RHESUS Оксид алюминия | Оксид алюминия | Моновалентное Типы 1 или 2 или Трехвалентный IPV | Шестные группы с от 5 до 12 животных были даны инъекции либо 2 или 3 доз (40 дней между дозами 1 и 2, по крайней мере 60 дней между дозами 2 и 3) либо адъювантной, либо неадъювантной ИПВ. | Значительно более высокие GMT полиомиелитных нейтрализующих антител для серотипа(ов) вакцины после введения всех доз вакцины в группах с адъювантом (примерно в 2–8 раз выше GMT в группах с адъювантом).Обезьян заражали тремя внутримышечными инъекциями активного полиовируса + стероиды. После заражения полиовирусом типа 1 паралитический полиомиелит развился у 11,1–20% по сравнению с 77,7– 88,8% обезьян из группы, получавшей адъювантное и неадъювантное лечение. После заражения полиовирусом типа 2 у 25% против 75% обезьян из группы с адъювантом и без адъюванта развился паралитический полиомиелит. После заражения полиовирусом типа 3 у 0% против 16,6% обезьян из группы с адъювантом и без адъюванта развился паралитический полиомиелит. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 19 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 19 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| человека | Комбинированный алюминий Гидроксид и Алюминиевый фосфат | EIPV | Две группы из 100 младенцев Каждый, дан Pediarix® (DTAP, HBV и IPV— , содержащий алюминиевый адъювант ) по сравнению с отдельными компонентами, все внутримышечно в 3 дозах по через 2, 4 и 6 месяцев. | Значительно более высокие значения GMT полиомиелитных нейтрализующих антител для серотипов 1 и 3 в группе с адъювантом (415, , 514 и 1729 по сравнению с 213, 329 и 432 для серотипов 1, 2 и 3 соответственно в группах с адъювантом и без адъюванта).Сходные показатели сероконверсии во всех группах (100%, 98,8% и 100% против 100%, 100% и 100% для серотипов 1, 2 и 3 соответственно в группах с адъювантом и без адъюванта). | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 20 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 20 | 2011 | человека | Алюминиевый гидроксид | EIPV | Две группы по 264 младенцам Каждая, дана PENTAXIM® (DTAP, HIB и IPV— , содержащий алюминиевый адъювант) VS Автономные компоненты, все в/м в 3 дозах в возрасте 3, 4 и 5 месяцев. | Значительно более высокие значения GMT полиомиелитных нейтрализующих антител для всех серотипов в группе с адъювантом (299,2, , 160,1 и 525,5 по сравнению с 130,1, 78,8 и 222,6 для серотипов 1, 2 и 3 соответственно в группах с адъювантом и без адъюванта). Сходные показатели сероконверсии во всех группах (100%, 100% и 99,6% против 100%, 99,6% и 99,6% для серотипов 1, 2 и 3 соответственно в группах с адъювантом и без адъюванта). | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 21 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 21 | 2009 | 2009 | человека | алюминиевый фосфат | EIPV | Две группы 485 младенцев Каждый дан PENTACEL® (DTAP, HIB и IPV— , содержащий алюминиевый адъювант) VS Автономные компоненты, все IM по 3 доз в возрасте 2, 4 и 6 месяцев. | Аналогичные GMT нейтрализующих полиомиелит антител (398,13, 1032 и 969,82 против 463,49, 913,35 и 902,12 для серотипов 1, 2 и 3 соответственно в группах с адъювантом и без адъюванта). Одинаковая частота сероконверсии во всех группах (99,4%, 100% и 100% против 100%, 100% и 100% для серотипов 1, 2 и 3 соответственно в группах с адъювантом и без адъюванта) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 28 |
| RHESUS | RHESUS Monkey | IFA с 166 М. Butyricum | Живой вирус (тип 2 Лансинг штамм) | Три группы из 6 обезьян каждый дан либо IM неадъюправленный полиовирус или полиовирус с парафиновое масло с или без М.butyricum , в 3 приема с интервалом 5 900–15 недель и 11 недель. | Средние титры нейтрализующих антител составляли 1,9, 3,1 и 3,3 через месяц после первой инъекции, 3,1, 3,9 и 4,2 через две недели после второй инъекции и 3,4, 4,3 и 3,7 через неделю после третьей инъекции в без адъюванта, масло и масло + M. butyricum группы соответственно. Следует отметить, что 4 из 6 обезьян в группе масло + M. butyricum умерли от смертельного аллергического энцефалита, двое до первого забора крови. | |||||
| 29 | 1951 | RHESUS Monkey | RHESUS IFA | Live Virus (штамм Lansing тип 2 ) | пять групп из 6 обезьян Каждый, одна доза IM , 4 разведения с адъювантом VS неаджувант . | Выраженный адъювантный эффект с адъювантными вакцинами, продуцирующими титры антител 1:3200, 1:120, 1:5 и 0 в 10, 100, 1000 и 10000-кратном разведении вируса по сравнению с 1:16 в неадъювантной 10 кратно разведенный вирус . | ||||
| 30 | ||||||||||
| 30 | 1 | RHESUS Monkey | IFA | IPV | IPv | Девять групп по 12 обезьян Каждый, Принимая вакцина против IM в 1 или 2 дозах (28 дней) под адъювантыми или неаджуванской вакциной разведенной 1/10 или 1/4 плюс контрольная группа, получившая 3 доз неразбавленной вакцины без адъюванта. | Заметно более высокие GMT полиомиелитных нейтрализующих антител и коэффициенты сероконверсии для всех трех серотипов для адъювантной вакцины .СГТ примерно в 20 раз выше в группах с адъювантом с той же дозой вакцины, и аналогичной между двумя 1/10 дозами ИПВ с адъювантом по сравнению с тремя полными дозами ИПВ без адъюванта (315, 440 и 104 против 330, 294 и 157 для серотипов 1 (Mahoney ), 2 и 3 соответственно). Показатели сероконверсии 100%, 100% и 100% по сравнению с 50%, 100% и 10% для двух 1/10 доз ИПВ с адъювантом и без адъюванта для серотипов 1, 2 и 3 соответственно. Показатели сероконверсии 100%, 100% и 100% по сравнению с 42%, 92% и 17% для адъювантной и неадъювантной двух доз 1/4 ИПВ для серотипов 1, 2 и 3 соответственно. Показатели сероконверсии для 3 доз неразбавленной неадъювантной вакцины 100% для всех 3 серотипов. | |||
| 31 | ||||||||||
| 31 | 1963 | человека | ||||||||
| человека | IPA | IPV | Три группы | Три группы, получающие IM DOSES One месяц друг от друга: 31 Младенцы Удаются 3 дозы Неадъювантное IPv, 34 Данные 2 дозы Adsuvanted 1/10 доза IPV, 31 младенец получал DPT-Salk (состав ИПВ отличается от других 2 групп). Все групп получили бустерную дозу в возрасте 9 месяцев. | Меньшие нейтрализующие полиомиелит СГТ после бустерной дозы в группе с 2 адъювантными дозами 1/10 ИПВ по сравнению с группой с 3 полными дозами ИПВ без адъюванта: 50, 50 и 120 по сравнению с 220, 110 и 320 в серотипах 1, 2 и 3 соответственно . Более низкая частота сероконверсии после ревакцинации в группе с 2 адъювантными дозами 1/10 ИПВ по сравнению с группой из 3 полных доз ИПВ без адъювантов: 100%, 96% и 100% по сравнению с 90%, 80% и 87% для серотипов 1, 2, и 3 соответственно. Более низкая частота сероконверсии до бустерной дозы в группе 2 адъювантных доз 1/10 ИПВ по сравнению с группой 3 полных доз ИПВ без адъюванта: 83%, 55% и 84% по сравнению с 52%, 42% и 48% для серотипов 1, 2, и 3 соответственно.3 дозы вакцины Salk-DPT имели показатели сероконверсии, сравнимые с группой, получавшей 2 дозы 1/10 ИПВ с адъювантом, но более низкие GMT после ревакцинации (25, 25 и 50 для группы Salk-DPT для серотипов 1, 2, и 3 соответственно). | |||||
| 33 | ||||||||||
| 33 | 2011 | RAT | Эмульсия на основе | MF59, Стабильная эмульсия масла или алюминий | IPV | Несколько групп из 4-10 крыс Каждый , получающий 1-2 дозы (1 месяц друг от друга ) различных разведений ИПВ с или без одного из трех адъювантов. | Более высокие титры полиомиелитных нейтрализующих антител с адъювантными вакцинами по сравнению с неадъювантной вакциной после одной дозы, которые достигают значения только для серотипа 2 с адъювантами на масляной основе. Более высокий уровень нейтрализующих антител против полиомиелита с вакцинами с адъювантом по сравнению с вакциной без адъюванта после двух доз, которые достигли значения для стабильной масляной эмульсии для серотипа 1 (3-кратное снижение дозы) и всех адъювантов для серотипов 2 и 3 (адъювант, подобный MF59, индуцировал 15-кратное увеличение дозы). более высокие титры для серотипа 2, и оба адъюванта на масляной основе индуцировали в 30 раз более высокие титры для серотипа 3 по сравнению с неадъювантной вакциной). | |||
| 37 | 2011 | 2011 | CAT & Mouse | Chitosan (наночастицы и раствор глутамата) | IPv и Инактивированные Monolenent Sabin штаммов | Несколько групп 4-6 мышей, получают 2-3 доз в дни 0, 21, +/- 31 из неразбавленной или разведенной вакцины с адъювантом или без адъюванта. Несколько групп из 5 крыс , получающих одну внутримышечную дозу неразбавленной или разведенной вакцины с адъювантом или без него. | Титры нейтрализующих антител по меньшей мере в 16 раз выше после 2 инактивированных доз Сэбина с адъювантом по сравнению с контролем без адъюванта для всех 3 серотипов у мышей. Для инактивированного типа 1 по Сэбину 2 дозы вакцины с адъювантом, разведенной в 4- раз, давали титры, эквивалентные 2 дозам неразбавленной вакцины без адъюванта. После введения 2 доз мышам ИПВ с адъювантом давала в 5-16 раз более высокие титры, чем ИПВ без адъюванта, при этом наночастицы давали самые высокие титры. В экспериментах на крысах наночастицы хитозана повышали иммуногенность ИПВ примерно в 100 раз (для всех 3 серотипов ИПВ с адъювантом, разведенная в 100 раз, давала титры антител, аналогичные титрам неразбавленной ИПВ без адъюванта). | |||
| 43 | 2006 | Мышь | Мышь | Витамин D (DHVD3) в фракционированный триглицерид кокосового масла | моновалентный IPV (все серотипов) | Многоуснежные группы по 8-18 мышам Каждая, внутрибрюшинных инъекций 2 или 3 дозы, 2-недельные интервалы, ИПВ с адъювантом или без него. | Значительное увеличение в группе с адъювантом по сравнению с группой без адъюванта наблюдалось для слюны IgA серотипов 1 и 3 (процент мышей с обнаруживаемым IgA в слюне составлял 43%, 92% и 33% против 7%, 76%, и 16% для серотипов 1, 2 и 3 соответственно в группах с адъювантом и без адъюванта), сывороточный IgG серотипа 2 и полиомиелитные нейтрализующие антитела в сыворотке для всех 3 серотипов (>400%, >500% и >800% выше для серотипы 1, 2 и 3 соответственно в группе с адъювантом). | |||
| 47 | 2009 | Мышь | Мышь | Мышь | Алюминиевый или CPG Олигодеоксидротидотиды | Инактивированные Моновалентное Штамс Sabin | Несколько групп из 8 мышей вводят IM с 1 или 2 дозами (28 дней) из разбавленных или неразбавленная вакцина с адъювантом с CpG-ODN, алюминием, обоими или ни тем, ни другим. | Для серотипа 2: титры нейтрализующих антител 120, 91, 223 и 33,5 для вакцины с адъювантом CpG- ODN, алюминием, обоими или ни тем, ни другим; экономия дозы в 4 раза при использовании одного адъюванта и >16 раз при использовании обоих адъювантов вместе взятых.Для серотипа 1: экономия дозы в 4 раза при сочетании обоих адъювантов. Для серотипа 3: экономия дозы более чем в 16 раз при сочетании обоих адъювантов. Для каждого адъюванта нейтрализуют титров только последовательно выше для серотипа 2. | ||
| 51 | 1 | 51 | 19015 | Cynomolgus | Cynomolgus Monkey | STEARYL TYROSINE | IPV | Четыре группы из 4 обезьян каждый, 3 IM инъекций на 0 , 28 и 168 дней, с IPV, разбавленным 1:1 или 1:4 с адъювантом или без него. | Отношение титров антител к эталонной сыворотке заметно выше в группах с адъювантом (шесть дней после 3-й дозы: 33,81, 49,16 и 125,31 против 7,36, 34,76 и 35,99 для серотипов 1, 2 и 3 соответственно в разведенном 1:1 с адъювантом по сравнению с группами без адъюванта; 7,89, 21,4 и 58,46 по сравнению с 0,26, 0,03 и 0,46 для серотипов 1, 2 и 3 соответственно в группах с разведением 1:4 с адъювантом и без адъюванта). | |
| 53 | 1991 | мышь | мышь | Липосомы | (с пептид либо на поверхность — , связанные или захваченные или захваченные) | Poliovirus серотип 1 или 3 VP2 пептиды | шесть групп из 5 мышей каждый вводят IM- 2 дозы с интервалом в 1 месяц — с серотипами 1 и 3 VP2 либо в свободном виде, либо в липосомах , связанных с поверхностью, либо в липосомах. | Реакция антител (измеренная с помощью ELISA, показанная спектрофотометрически при 492 нм) составляла примерно 0,8; связанная, захваченная и свободная вакцина соответственно. Реакции антител составляли примерно 1,0, 0,1 и 0 через месяц после первой дозы и 0,25, 0,1 и 0 через 10 дней после второй дозы пептида серотипа 1 в поверхностно-связанной, инкапсулированной и свободной вакцине соответственно. |
История вакцинации против полиомиелита
World J Virol. 2012 12 августа; 1(4): 108–114.
Anda Baicus, Национальный институт исследований и разработок в области микробиологии и иммунологии Cantacuzino, Университет медицины и фармации им. Кэрол Давила, 050096 Бухарест, Румыния
Вклад авторов: Baicus A внес исключительный вклад в написание этой статьи.Адрес для переписки: Анда Байкус, доктор медицинских наук, преподаватель микробиологии, руководитель Национальной полиомиелитной лаборатории, Национальный институт исследований и разработок в области микробиологии и иммунологии Кантакузино, Университет медицины и фармации им. Кэрол Давила, 050096 Бухарест, Румыния.or.onizucatnac@suciaba
Телефон: +40-740-213102 Факс: +40-215-287305
Поступила в редакцию 11 октября 2011 г.; Пересмотрено 12 июня 2012 г.; Принято 13 июля 2012 г.
Copyright © 2012 Baishideng. Все права защищены. Эта статья цитировалась в других статьях PMC.Abstract
Полиомиелит — острое паралитическое заболевание, вызываемое тремя серотипами полиовируса (ПВ). Менее 1% инфекций PV приводят к острому вялому параличу. Заболевание контролировали с помощью инактивированной формалином полиомиелитной вакцины Солка (ИПВ) и пероральной полиомиелитной вакцины Сэбина (ОПВ).Глобальная ликвидация полиомиелита была предложена Всемирной организацией здравоохранения в 1988 г. ее государствам-членам. В стратегическом плане определены мероприятия, необходимые для ликвидации полиомиелита, сертификации для регионов, фазы прекращения использования ОПВ и фазы после применения ОПВ. ОПВ является предпочтительной вакциной для программы ликвидации полиомиелита, поскольку она индуцирует как системный, так и слизистый иммунный ответ. Основными рисками вакцинации ОПВ являются появление случаев вакциноассоциированного паралитического полиомиелита (ВАПП) и появление штаммов полиовирусов вакцинного происхождения.Дополнительная иммунизация моновалентными штаммами ОПВ типа 1 или типа 3 или новой бивалентной оральной полиовакциной бОПВ (содержащей PV типа 1 и типа 3) была введена в тех регионах, где вирус было трудно контролировать. Большинство стран изменили график вакцинации, используя ИПВ вместо ОПВ, поскольку она не представляет риска заболевания, связанного с вакциной. До 2008 г. полиомиелит контролировали в Румынии, восточноевропейской стране, преимущественно с помощью ОПВ. Альтернативный график вакцинации (ИПВ/ОПВ) был введен с сентября 2008 г., а с 2009 г. вакцинация проводилась только ИПВ.Риск ВАПП исчезнет во всем мире с прекращением использования ОПВ. Иммунизацию от полиомиелита необходимо проводить не менее 5–10 лет с использованием ИПВ.
Ключевые слова: Полиомиелит, инактивированная формалином полиомиелитная вакцина, оральная полиомиелитная вакцина
ВВЕДЕНИЕ
Полиовирус (PV), энтеровирус, принадлежащий к семейству Picornaviridae, является этиологическим агентом полиомиелита, острого паралитического заболевания. Это заболевание возникает в результате поражения нижних двигательных нейронов и характеризуется асимметричной персистирующей слабостью (вялый паралич).О передаче этого вируса в древности предположили после исследований египетских мумий, показавших укорочение нижней конечности у ребенка. В 1789 г. во втором издании «Трактата о болезнях детей» Майкл Андервуд описал болезнь как «слабость нижних конечностей у детей»[1]. Никаких упоминаний о вспышках этого заболевания он не зафиксировал.
Badham [2] описал острый паралич, напоминающий полиомиелит, у четырех детей в 1835 году.В 1840 г. Гейне [3] опубликовал монографию, в которой полиомиелит был признан и определен как детский спинальный паралич. Duchenne в 1855 г., а затем Charcot и др. [4] в 1870 г. локализовали атрофию в передних рогах серого вещества спинного мозга. Это открытие дало начало патологическому термину «полиомиелит» от греческого polios «серый» и myelos «спинной мозг». В 1875 г. Эрб ввел термин «острый передний полиомиелит». Медин впервые сообщил об эпидемической форме этого заболевания в 1890 г., после эпидемии 44 случаев в Стокгольме летом 1887 г.Он выделил системную фазу заболевания, которая часто не приводила к неврологическому парезу, и разработал ее классификацию. Викман ввел в 1907 году эпоним «болезнь Гейне-Медина» в честь вклада Медина. Патнэм и др. [5] зафиксировали самые ранние описания эпидемического полиомиелита с использованием основных эпидемиологических методов в 1893 г., Каверли [6] в 1894 г. в США и Викман в 1905 г. в Швеции. В эпидемиологических исследованиях, проведенных между 1910 и 1912 годами во время эпидемий в Соединенных Штатах, Фрост обнаружил широкое распространение полиомиелита, но низкую заболеваемость клиническим заболеванием у тех, кто восприимчив к инфекции.Во время эпидемии на северо-востоке США в 1916 г. роль бессимптомных лиц в распространении инфекции была зафиксирована Службой общественного здравоохранения. Эта эпидемия вызвала всеобщую панику; Сообщается, что более 27 000 человек были парализованы, 6000 человек погибли.
Вспышки полиомиелита постепенно становились все более серьезными, более частыми и широко распространенными в Европе и Соединенных Штатах в начале 20-го века. Эпидемиология PV постепенно стала понятной.Модель распространения полиомиелита была нерегулярной, и многие пациенты не имели прямого контакта с известным источником. В 1905 году Викман впервые признал полиомиелит инфекционным заболеванием. Ландштейнер и Поппер продемонстрировали в 1909 г., что этиологическим агентом полиомиелита является фильтрующийся вирус. Они передали болезнь обезьяне Cynocephalus путем внутрибрюшинной инъекции нервной ткани человека со смертельным исходом. В 1910 году Flexner предположил, что PV является строго нейротропным. Он считал, что PV попадает в организм человека через дыхание [7], но позже эта гипотеза была опровергнута.Howe и Bodian рассматривали возможность орального алиментарного пути заражения полиомиелитом в 1930-х годах[8]. В конце 1930-х годов Армстронг произвел экспериментальный полиомиелит у мышей. Это было преимуществом для изучения PV и для разработки теста нейтрализации для измерения антител. Предположение о том, что существует более одного типа PV, было выдвинуто Бернетом и Макнамарой в 1931 году и подтверждено Полом и Траском путем наблюдения в экспериментах на обезьянах. Три различных типа были идентифицированы штаммом-прототипом: Brunhilde (тип I), Lansing (тип II) и Leon (тип III) [9].Концепция полиомиелита как кишечной инфекции возникла в 1932 году, когда Пол и Траск обнаружили вирус в фекалиях и в течение нескольких недель извлекали вирус из пациентов и здоровых контактов. В 1936 г. Sabin и Olitsky сообщили, что PV можно успешно выращивать in vitro во фрагментах нервной ткани эмбриона человека, культивируемых в стеклянных сосудах. При анализе сточных вод в Нью-Йорке в периоды распространения паралитического полиомиелита было установлено, что на каждый паралитический случай приходится 100 случаев субклинической инфекции[10].В 1950-х годах было установлено, что ВВ можно выделить от мух, собранных во время эпидемий. Исследованиями в лаборатории с мухами, вылупившимися из личинок, не было зарегистрировано никаких признаков размножения вируса[11]. В 1949 году Эндерс, Веллер и Роббинс успешно культивировали штамм Lansing в культуре ненейронной ткани, что привело к возможности безопасного производства вируса в достаточном количестве, что открыло путь для производства вирусных вакцин. Серологические исследования сывороточных антител против PV в слаборазвитых странах показали, что после контакта и заражения даже бессимптомные люди были иммунизированы на всю жизнь.В развитых странах дети, живущие в густонаселенных районах, заражаются в более раннем возрасте, чем дети из более высоких социально-экономических слоев. К 1952 г. серологическими исследованиями было установлено, что антитела к ПВ присутствуют у больного вскоре после начала заболевания и увеличиваются в период выздоровления. В 1952 г. полевые испытания, проведенные Хэммоном, показали, что пассивная иммунизация введением γ-глобулина обеспечивает защиту от болезни всего на 2–5 недель. Летняя передача инфекции была связана с повышенным содержанием PV в сточных водах.Лабораторными исследованиями были подтверждены две фазы заболевания: желудочно-кишечная инфекция с последующей виремией и инвазия в ЦНС.
РАЗРАБОТКА ВАКЦИН PV
В 1935 году Броди испытал инактивированную вакцину с 10% формалиновой суспензией PV, взятой из спинного мозга инфицированных обезьян; он попробовал это сначала на 20 обезьянах, затем на 3000 калифорнийских детей. Результаты были плохими, и дополнительные исследования на людях никогда не проводились. В том же году Коллмер попробовал живой аттенуированный вирус, состоящий из 4% суспензии PV из спинного мозга инфицированных обезьян, обработанных рицинолеатом натрия.Он использовал его на обезьянах, а затем на нескольких тысячах детей. Острый паралич возник примерно у 1/1000 вакцин вскоре после введения, а некоторые случаи закончились летальным исходом.
Открытие того, что различные антигенные штаммы PV могут быть сгруппированы в три различных вирусных типа, и размножение PV in vitro привело к разработке вакцин против полиомиелита: инактивированной формалином вакцины (IPV) Джонаса Солка. (1953) и живые аттенуированные вакцины (ОПВ) Альберта Сабина (1956)[12].
ИПВ
Первая инактивированная вакцина против полиомиелита (ИПВ) была произведена Солком с использованием вируса, выращенного на клетках почки обезьяны и инактивированного формалином. В 1954 году инактивированная вакцина была протестирована в плацебо-контролируемом испытании, в котором приняли участие 1,6 миллиона детей в Канаде, Финляндии и США[13]. В апреле 1955 года вакцина Солка была принята во всех Соединенных Штатах. Заболеваемость паралитическим полиомиелитом в США снизилась с 13,9 случаев на 100 000 населения в 1954 году до 0.8 случаев на 100 000 населения в 1961 г.[14]. Некоторыми недостатками вакцины Солка в то время были снижение титров циркулирующих антител в течение нескольких лет после вакцинации, дальнейшая циркуляция дикой PV и ее последствия во вспышках, а также большое количество обезьян (около 1500), необходимое для вакцинации. быть принесены в жертву для производства каждого 1 миллиона инактивированных доз. В вакцине использовались штаммы вируса Mahoney (тип 1), MEF-I (тип 2) и Saukett (тип 3). Вскоре после лицензирования вакцины Солка за неудачей инактивации вакцинного вируса в Cutter Laboratories, Беркли, последовало 260 случаев полиомиелита с PV типа 1 и 10 летальных исходов.Предполагалось, что вирус был устойчив к инактивации формальдегидом, потому что он содержал больше чужеродных белков, чем оптимально, или что вирус мог слипаться. В производственный процесс был введен второй этап фильтрации для удаления агрегатов, которые могли образоваться во время обработки, и были улучшены тесты на безопасность. Использование высоковирулентного штамма Mahoney в производстве вакцин вызывает споры, а после инцидента с Каттером — еще больше. В Швеции предпочтение отдавалось штамму Brunenders для типа 1.В 1980 г. в производство ИПВ были внедрены концентрирование и очистка антигенов полиомиелита и повышена иммуногенность вакцины. Первоначальная ИПВ содержала 20, 2 и 4 единицы D-антигена PV типов 1, 2 и 3. Ван Везель представил технологию производства ИПВ с повышенной активностью. Он решил сконцентрировать и очистить вирус перед обработкой формалином. С момента введения этой процедуры сбоев в процессе инактивации зафиксировано не было. Благодаря внедрению новой методики культивирования с использованием клеток на гранулах микроносителей в суспензиях, культивируемых в больших резервуарах из нержавеющей стали, была получена более мощная ИПВ, содержащая 40, 8 и 32 единицы D-антигена типов 1, 2 и 3 [15,16].Испытания с этой усиленной ИПВ (eIPV) показали более 90% серопозитивности против всех 3 типов PV после одной дозы и 100% серопозитивности после двух доз [17]. ИПВ с повышенной эффективностью была лицензирована в США в 1987 г., с хорошим ответом на типы 1 и 3 при интервале между дозами в 4 или 8 недель и после 8 недель на тип 2. Рекомендуемый график вакцинации в разных странах содержит 4 дозы ИПВ в первичной серии были введены в возрасте 2, 4, 6 и 15-18 месяцев [18] и бустерная доза в возрасте 4-6 лет.Для оптимальной ревакцинации необходим минимальный интервал не менее 6 месяцев между дозами 4 и 5. Вакцины ИПВ ингибируют фарингеальную инфекцию PV и снижают кишечную экскрецию.
OPV
Разработка аттенуированной вакцины против PV начинается с пассирования штаммов PV у крыс и мышей с последующим пассированием в клеточной культуре. Снижение вирулентности штаммов ВВ было зафиксировано в 1946 г. Тейлером, пассировавшим штамм Лансинга на крысах и мышах более 50 раз, и Эндерсом, Веллером и Робинсом, пассировавшим тот же штамм в культуре клеток.
Штаммы-кандидаты аттенуированного PV, подходящие для иммунизации людей, были независимо разработаны в США компаниями Koprowski (Институт Wistar, Филадельфия), Cox (Lederle Laboratories) и Sabin (Научно-исследовательский фонд детской больницы).
В 1950 году Копровски начал эксперименты с адаптированным к грызунам PV типа 2, которым скармливали небольшой группе в Калифорнии. Он, Кокс и их коллеги накормили миллионы людей по всему миру тремя типами вирусов[19]. Выделение ПВ со свойствами штамма Кокса из ткани мозга умершего отца привитого ребенка сопровождалось изъятием этого штамма [20].
В 1960 г. Сабин описал в статье, опубликованной в журналах JAMA , Live , перорально введенную полиовирусную вакцину [21], результаты, полученные с помощью его недавно разработанной трехвалентной пероральной вакцины у 26 033 детей из города с населением 100 человек. 000 человек в Южной Америке. Поскольку штаммы, разработанные Сэбином, обеспечивали хорошие уровни антител и были менее нейротропными для обезьян, они были отобраны и лицензированы в США в период с 1961 по 1963 год для широкого применения.Первая общенациональная кампания по вакцинации против полиомиелита была проведена на Кубе в 1962 г.[22]. Во время встречи Сабина и Чумакова в 1956 году Сабин предоставил результаты своих экспериментов и свои штаммы вакцины против полиомиелита Чумакову, который начал производить ее для использования в своей стране. Несколько миллионов детей из Эстонии и Литвы (в то время входивших в состав Советского Союза) получили эту вакцину к 1959 году, и это была история успеха, которая способствовала рекомендации по лицензированию трех моновалентных штаммов, разработанных Сэбином [23].
ОПВ Сэбина состоит из трех живых аттенуированных штаммов полиовируса Сэбина, полученных в результате последовательных пассажей in vitro и in vivo пассажей диких штаммов. Вирулентные штаммы P1/Mahoney/41, P2/P712/56 и P3/Leon/37 послужили источником аттенуированных штаммов Сэбина: P1/Lsc,2ab, P2/P712,Ch,2ab и P3/Leon,12a 1 б.
Вначале трехвалентная ОПВ содержала три типа PV в равных пропорциях, но были зарегистрированы более низкие уровни сероконверсии к типам 1 и 3.При использовании сбалансированного состава трехвалентной ОПВ, который содержал 10 6 , 10 5 и 10 5,5 TCID50 (50% инфицирующей дозы тканевой культуры) типов Сэбина 1, 2 и 3, нейтрализующие антитела против всех трех типов PV были выявлены практически у всех лиц. Увеличение количества вируса типа 3 в трехвалентной вакцине улучшило иммуногенность[24], и Глобальная консультативная группа Расширенной программы иммунизации рекомендовала состав трехвалентной ОПВ, который содержал TCID50 типов Сэбина 1, 2 и 3 на дозу [25].Вакцину ОПВ было легче вводить, и она обладала стадным эффектом, индуцируя долговременный защитный системный, гуморальный и клеточный иммунитет, а также местную резистентность слизистых оболочек к инфекции PV. В 1972 году Сабин передал свои вакцинные штаммы PV Всемирной организации здравоохранения (ВОЗ), тем самым увеличив доступность этой вакцины для развивающихся стран. С 1977 по 1995 год процент всех детей в мире, получивших необходимые три дозы ОПВ в первые годы жизни, увеличился с 5% до 80%.
Основными рисками вакцинации ОПВ являются появление случаев вакциноассоциированного паралитического полиомиелита (ВАПП) и появление штаммов полиовирусов вакцинного происхождения (ВРПВ), причем штаммы ОПВ имеют более чем 1% нуклеотидных расхождений с исходными вакцинными штаммами в Кодирующая область генома VP1. Появление случаев ВАПП связано с реверсией к нейровирулентности вакцинных штаммов. Во время репликации в кишечнике штаммы OPV могут подвергаться генетической изменчивости путем точечных мутаций со средней частотой 10 -4 за счет РНК-полимеразы или за счет естественной рекомбинации.Заболеваемость ВАПП у иммунокомпетентных детей, получивших первую дозу ОПВ, оценивалась как один случай на 750 000 доз и один случай на 6,9 млн последующих доз [26]. Тип 3 был наиболее распространенным изолятом, связанным с параличом у реципиентов вакцины, а тип 2 был связан с параличом в основном среди контактов заболевших. Штаммы ПВВП могут быть циркулирующими (цПВВП, которые могут распространяться в популяциях с низким уровнем охвата вакцинацией), могут возникать после репликации у лиц с иммунодефицитом, контактировавших с ОПВ (иПВВП), или могут быть сомнительными ПВВП (аПВВП, когда они выделяются из иммунокомпетентных лиц или источник в окружающей среде не был идентифицирован).Одна доза ОПВ вызывает иммунитет против всех трех серотипов PV примерно у 50% реципиентов; три дозы вызывают иммунитет более чем у 95% реципиентов.
СМЕШАННАЯ ИПВ И ОПВ
Для устранения риска ВАПП среди реципиентов ОПВ в мире применялась последовательная схема вакцинации ИПВ/ОПВ. Однако преиммунизация младенцев двумя дозами ИПВ в возрасте 2 и 4 мес с последующим введением двух доз ОПВ в 18 мес и в возрасте от 4 до 6 лет не устраняла риск ВАПП среди контактировавших с вакцинами.
ВАКЦИНАЦИЯ ПОЛИОМИЕЛИТА В РУМЫНИИ
В Румынии, восточноевропейской стране, между 1927 и 1960 гг. полиомиелит развивался спорадически и эпидемически. Заболеваемость паралитическим полиомиелитом в Румынии снизилась с 10 случаев на 100 000 в 1949 г. до 0,1 случая на 100 000 к середине 1980-х годов за счет использования инактивированной PV вакцины в 1957 г. и пероральной PV вакцины в 1961 г. Вакцинация против полиомиелита началась в 1957 г., когда была произведена вакцина Лепина. Пастеровским институтом в Париже, но не охватывала все младенческое население (или даже весь контингент детей, рожденных в этом году) и сопровождалась в 1959 г. ИПВ, произведенной в СССР, которой были вакцинированы все младенцы (две дозы за раз). интервал 2 месяца).Успех применения ОПВ, определивший ликвидацию эпидемий полиомиелита во многих странах, привел к решению использовать этот новый тип вакцины против полиомиелита в Румынии. Во-первых, вакцина была закуплена в СССР, и все население Румынии в возрасте до 30 лет получило эту вакцину в период между 1961 и 1962 годами. Институт Кантакузино в Бухаресте начал производство ОПВ в 1962 году, сначала используя посевной вирус вакцины, полученный из Исследовательского центра полиомиелита. института в Москве и позднее (с 1967 г.) вакцинный посевной вирус получали непосредственно от Сабина.Между 1961 и 1963 годами младенцы получали первую дозу ИПВ, а затем ОПВ. Начиная с 1964 года трехвалентная пероральная вакцина, стабилизированная хлоридом магния, разработанная Институтом Кантакузино, использовалась для широкомасштабной иммунизации в Румынии. Введение пероральной вакцины против полиомиелита проводилось в рамках ежегодных национальных кампаний с 1961 по 1978 год. Через несколько лет после широкого применения ОПВ заболеваемость паралитическим полиомиелитом резко снизилась, но стали появляться случаи ВАПП. В 1974 году ВОЗ утвердила Институт Кантакузино в качестве предприятия по производству ОПВ.С 1970 года Румыния на протяжении более 15 лет вместе с 11 другими государствами участвовала в совместном исследовании ВОЗ риска случаев ВАПП, и риск был самым высоким в этой стране. Органы здравоохранения Румынии решили в 1978 г. прекратить использование существующих запасов вакцины (приготовленной из посевных вирусов ВОЗ, полученных в 1974 г.) и использовать новый посевной материал вируса ВОЗ-В (Behring). Этот посевной вирус должен был быть доступен летом 1978 г., но из-за проблем с подготовкой и особенно контролем посевного материала вирусы ВОЗ-В распространялись ВОЗ только с конца 1979 г.Из-за этой проблемы в период с июля 1978 г. по март 1980 г. вакцинация проводилась только моновалентной ОПВ типа 1 с однократной дозой, вводимой детям в возрасте 6 недель. За этот период в Румынии не было зарегистрировано ни одного случая паралитического полиомиелита. Вакцинация была возобновлена существующими запасами вакцины в апреле-июне. Следствием этого двухлетнего перерыва стали эпидемии, произошедшие в 1980-1982 гг., вызванные диким PV типа 1 (161 случай) и типа 2 (15 случаев). Эпидемия прекратилась в третьем квартале 1982 года.Распространение диких PV было остановлено кампанией иммунизации трехвалентной ОПВ (ТОПВ). Эпидемия полиомиелита в Румынии в 1980-1982 гг. позволила сделать важный вывод: перерыва в вакцинации ТОПВ на 2 года было достаточно для создания контингента детей с высокой восприимчивостью к заражению ВВ, что позволило осуществить реимплантацию диких ВВ и их активные перемещения с последующим в связи с возникновением эпидемии полиомиелита. В 1983 г. кампании по вакцинации были проведены весной и осенью.График вакцинации был разработан таким образом, чтобы каждый ребенок в первые 10 лет жизни получил 4 дозы ВОПВ; первая доза между 2 и 7 месяцами, вторая доза между 4 и 9 месяцами, третья доза между 10-15 месяцами и ревакцинация в 9 лет жизни. Охват вакцинацией тремя дозами ТОПВ в возрасте 2 лет составил более 90%. С 1983 г. по май 1990 г. случаев паралитического полиомиелита, вызванного дикими PV, не зарегистрировано. Последняя вспышка PV дикого типа 1 произошла в период с ноября 1990 г. по апрель 1992 г.Вспышка охватила непривитых или недостаточно привитых детей из цыганской общины. Четыре из 13 диких случаев PV были инфицированы ВИЧ [27]. Все случаи паралитического полиомиелита, имевшие место в Румынии в 1984-1992 гг., имели место у детей младше 5 лет, что показало, что иммунитет к трем серотипам PV был почти 100% у детей старше 5 лет и взрослых.
Пероральная вакцина против PV, применявшаяся в Румынии до сентября 1990 г., была произведена Институтом Кантакузино.Из-за высокой заболеваемости вакциноассоциированным паралитическим полиомиелитом, зарегистрированным в 1970-1984 гг., начиная с ноября 1990 г., пероральная вакцина, одобренная ВОЗ, была импортирована и заменила вакцину, произведенную в Румынии[28]. Однако исследование случай-контроль показало, что причиной повышенного риска вакциноассоциированного паралитического полиомиелита в Румынии был не производитель вакцины PV, а введение множественных внутримышечных инъекций антибиотиков в течение 30 дней после получения ОПВ, что увеличивало риск паралича. в 2-10 раз[29].Снижение риска ВАПП было достигнуто за счет сокращения парентерального лечения реципиентов ОПВ и изменения схемы введения оральной полиовакцины с 2 кампаний по два раунда на круглогодичную вакцинацию с апреля 1995 г. С 1992 г. В 1994 г. проект Министерства здравоохранения, поддержанный Фондом Марселя Мерье, продемонстрировал осуществимость, безопасность и высокую иммуногенность последовательного применения высокоактивной ИПВ с последующей ОПВ в 1 из 41 округа Румынии[30].До 2008 г. полиомиелит контролировали в Румынии преимущественно с помощью ОПВ, вводившейся в возрасте 2, 4, 6 и 12 месяцев, и ревакцинации в возрасте 9 лет; альтернативный график вакцинации (ИПВ/ОПВ) был введен с сентября 2008 г., а в начале 2009 г. было принято решение о вакцинации только ИПВ[31]. Сообщаемый охват вакцинацией 4 дозами ТОПВ в первые 14 месяцев жизни с 1980 г. составляет более 90%. Риск ВАПП снизился с менее чем 2 случаев ВАПП в год в 1995-2006 гг. до 0 случаев ВАПП с 2007 г. 32].В 2002 г., через 1 месяц после Сертификации европейского региона как свободного от полиомиелита, штамм PV 1 типа, рекомбинантный Sabin1/Sabin2/Sabin1, был выделен из случая ВАПП, не вакцинированного против полиомиелита, и от 8 здоровых контактов, считающихся подверженными риску[33]. . В 2008 г. мы изучали циркуляцию и биоразнообразие энтеровирусов в группе детей из числа меньшинств с низким охватом вакцинацией против полиомиелита из того же района, где в 2002 г. был выделен штамм ПВВП. Были обнаружены доказательства внутричеловеческой циркуляции штаммов Сэбина [34], но штамм ПВВП не был выделен.Надзор за группами риска из районов риска и поддержание полного охвата населения вакцинацией являются важными задачами в рамках глобальной ликвидации полиомиелита.
ЗАКЛЮЧЕНИЕ
С разработкой и использованием вакцин полная ликвидация полиомиелита стала целью. В 1988 г. ВОЗ предложила своим государствам-членам ликвидировать полиомиелит во всем мире. Стратегический план Глобальной инициативы по ликвидации полиомиелита (ГИЛП) определил мероприятия, необходимые для ликвидации полиомиелита, сертификации для регионов, фазы прекращения использования ОПВ и фазы после применения ОПВ.Первоначально этот план был основан на поддержании высокого охвата вакцинацией (> 80%) детей, применении дополнительных доз вакцины во время национальных дней вакцинации (НВД), подчищающей вакцинации и внедрении эффективных систем эпиднадзора за инфекцией PV и мероприятиях по сдерживанию . Наличие восприимчивых подгрупп с пробелами в иммунизации способствует внедрению диких штаммов PV в вакцинированное население. Штаммы OPV стали основным инструментом программы ликвидации PV дикого типа, поскольку они индуцируют как системный, так и слизистый иммунный ответ.Большинство стран изменили график вакцинации против полиомиелита, используя ИПВ вместо ОПВ. Преимущество использования ИПВ заключается в том, что оно не представляет риска заболевания, связанного с вакциной. Недостатками глобального внедрения ИПВ являются ее стоимость, внутримышечное введение, ее неспособность обеспечить оптимальный кишечный иммунитет и биоизоляция, необходимая для ее производства. В 2011 г., через 23 года после принятия ВОЗ решения о глобальной ликвидации полиомиелита, дикий PV (тип 1 и 3) по-прежнему эндемичен только в четырех странах: Афганистане, Индии, Нигерии и Пакистане.Штамм дикого PV типа 2 был ликвидирован во всем мире с 1999 г., в то время как циркулирующий штамм PV вакцинного происхождения (цПВВП) 2 типа сохраняется в северной Нигерии с 2006 г. [35]. Необходимо разработать план прекращения плановой иммунизации ОПВ против PV типа 2[36]. В тех регионах, где вирус было трудно контролировать, проводилась дополнительная иммунизация моновалентными штаммами ОПВ типа 1[37] или типа 3[38] или новой бивалентной оральной полиовакциной бОПВ (содержащей PV типа 1 и типа 3). введено[39].В 2008 г. план ГИЛП был обновлен с целью преодоления барьеров, препятствующих прекращению передачи дикой PV. Целями на 2010-2012 гг. являются: прекращение дикой передачи PV в Азии и Африке; усиление эпиднадзора за PV и реагирования на вспышки; и укрепление систем иммунизации. В 2010 г. вспышка случаев дикого PV типа 1, генетически связанного с диким PV, циркулировавшим в 2009 г. в Индии, была зарегистрирована в Таджикистане, входящем в Европейский регион ВОЗ, сертифицированный как свободный от полиомиелита в 2002 г.[40]. Этот эпизод продемонстрировал, что если регион свободен от полиомиелита, риск завоза дикой полиомиелита из эндемичных регионов сохраняется до тех пор, пока полиомиелит не будет искоренен во всем мире.Поскольку большинство штаммов ПВВП, вызывающих вспышки полиомиелита во всем мире, являются рекомбинантными штаммами ОПВ и неполиомиелитными штаммами энтеровируса человека вида C[41], необходимо усилить эпиднадзор за коциркуляцией и эволюцией полиомиелитных и неполиомиелитных энтеровирусов. Риск ВАПП исчезнет с прекращением использования ОПВ. Некоторые исследовательские программы инициированы ВОЗ для получения доступной ИПВ путем снижения необходимой дозы антигена путем внутрикожного введения [42, 43], с использованием адъювантов [44] и путем введения штаммов Сэбина в качестве посевного материала [45, 46].В первые 5–10 лет после глобального прекращения применения ОПВ необходимо обеспечить поддержание иммунитета к полиомиелиту за счет использования ИПВ[47].
Сноски
Рецензент: Ян М. Маккей, доктор философии, лаборатория Qpid, Центр исследования вирусов сэра Альберта Сакзевски, Королевская детская больница, Херстон-роуд, Херстон Q4029, Австралия
S-редактор Zhang SS L-редактор Roemmele A E-редактор Zheng XM
Литература
1. Андервуд М. Слабость нижних конечностей. В: Трактат о болезнях детей.Лондон: Дж. Мэтьюз; 1789. стр. 53–57. [Google Академия]2. Бэдхэм Дж. Паралич в детстве: четыре замечательных случая внезапно вызванного паралича конечностей без каких-либо явных церебральных или спинномозговых поражений. Лондон Мед Газ. 1835; 17: 215–218. [Google Академия]3. Heine J. Beobachtungen uber lahmungustande der untern extremitaten und deren behandlung. Штутгарт: Ф. Х. Колер; 1840. [Google Scholar]4. Шарко Дж. М., Жоффруа А. Одно наблюдение за инфантильным параличом, сопровождающим изменение передних рогов де ла серого вещества де ла моэль.CR Soc Biol (Париж) 1870; 1: 312–315. [Google Академия]5. Патнэм Дж.Дж., Тейлор Э.В. Острый полиомиелит необычайно распространен в этом сезоне. Boston Med Surg J. 1893; 129: 509–510. [Google Академия]6. Каверли КС. Предварительный отчет об эпидемии паралитического заболевания, произошедшей в Вермонте летом 1894 года. Yale Med J. 1894; 1: 1–5. [Google Академия]7. Флекснер С., Льюис П.А. Экспериментальный полиомиелит у обезьян: активная иммунизация и пассивная сывороточная защита. ДЖАМА. 1910; 54: 1780–1782. [Google Академия]9. Пол младший.История полиомиелита. Нью-Хейвен, Коннектикут: Издательство Йельского университета; 1971. [Google Scholar] 10. Мельник Дж.Л. Вирус полиомиелита в городских сточных водах в эпидемическое и неэпидемическое время. Am J Hyg. 1947; 45: 240–253. [PubMed] [Google Scholar] 11. Мельник Дж.Л. Моя роль в открытии и классификации энтеровирусов. Анну Рев Микробиол. 1996; 50:1–24. [PubMed] [Google Scholar] 12. Сабин А.Б., Боулджер Л.Р. История штаммов оральной живой вакцины аттенуированного полиовируса Сэбина. J Биол Стенд. 1973; 1: 115–118. [Google Академия] 13.Монто АС. Полевые испытания инактивированной полиомиелитной вакцины Фрэнсисом: предыстория и уроки на сегодняшний день. Epidemiol Rev. 1999; 21:7–23. [PubMed] [Google Scholar] 14. Стребель П.М., Саттер Р.В., Кочи С.Л., Беллик Р.Дж., Бринк Э.В., Кью О.М., Палланш М.А., Оренштейн В.А., Хинман А.Р. Эпидемиология полиомиелита в США через десять лет после последнего зарегистрированного случая заболевания, связанного с местным диким вирусом. Клин Инфекция Дис. 1992; 14: 568–579. [PubMed] [Google Scholar] 15. ван Везель А.Л., ван Стинис Г., ван дер Марел П., Остерхаус А.Д.Инактивированная полиомиелитная вакцина: современные методы производства и новые разработки. Преподобный Заражает Дис. 1984; 6 Приложение 2: S335–S340. [PubMed] [Google Scholar] 16. Montagnon BJ, Fanget B, Vincent-Falquet JC. Промышленное производство инактивированной вакцины против полиомиелита, приготовленной культурой клеток Vero на микроносителе. Преподобный Заражает Дис. 1984; 6 Приложение 2: S341–S344. [PubMed] [Google Scholar] 17. Бернье РХ. Усовершенствованная инактивированная вакцина против полиомиелита: обновление. Педиатр Infect Dis. 1986; 5: 289–292. [PubMed] [Google Scholar] 18.фон Магнус Х., Петерсен И. Вакцинация инактивированной вакциной против полиомиелита и оральной вакциной против полиомиелита в Дании. Преподобный Заражает Дис. 1984; 6 Приложение 2: S471–S474. [PubMed] [Google Scholar] 19. Центры по контролю и профилактике заболеваний (CDC) Прогресс на пути к глобальной ликвидации полиомиелита, 1988-1993 гг. MMWR Morb Mortal Wkly Rep. 1994; 43: 499–503. [PubMed] [Google Scholar] 20. Кук Дж. С., Уолсинг Д. Х., Ламех Дж., Олсон К. А., Корреа П. Е., Сади В., Блюменталь Э. М., Розенбаум Дж. С. Характеристика гена RDC1, который кодирует собачий гомолог предложенного рецептора VIP человека.Экспрессия не коррелирует с увеличением сайтов связывания VIP. ФЭБС лат. 1992; 300:149–152. [PubMed] [Google Scholar] 21. Сабин А.Б., Рамос-Альварес М., Альварес-Амескита Дж., Пелон В., Майклс Р.Х., Спигленд И., Кох М.А., Барнс Дж.М., Рим Дж.С. Знаменательная статья от 6 августа 1960 г.: Живая вакцина против полиомиелита, вводимая перорально. Влияние быстрой массовой иммунизации на население в условиях массивной кишечной инфекции другими вирусами. Альберт Б. Сабин, Мануэль Рамос-Альварес, Хосе Альварес-Амескита, Уильям Пелон, Ричард Х.Майклс, Илья Спигленд, Мейнрад А. Кох, Джоан М. Барнс и Джонг С. Рим. ДЖАМА. 1984; 251:2988–2993. [PubMed] [Google Scholar] 22. Хинман АР. Важная перспектива: массовая вакцинация против полиомиелита. ДЖАМА. 1984; 251:2994–2996. [PubMed] [Google Scholar] 23. Агол В.И., Дроздов С.Г. Российский вклад в ОПВ. Биопрепараты. 1993; 21: 321–325. [PubMed] [Google Scholar] 24. Патриарка П.А., Лендер Ф., Палмейра Г., Оливейра М.Дж., Лима Филью Дж., Дантес М.С., Кордейро М.Т., Риси Д.Б., Оренштейн В.А. Рандомизированное исследование альтернативных составов пероральной полиовакцины в Бразилии.Ланцет. 1988; 1: 429–433. [PubMed] [Google Scholar] 25. Расширенная программа иммунизации. Глобальная консультативная группа — Часть II. Wkly Epidemiol Rec. 1991;66:9–12. [PubMed] [Google Scholar] 26. Prevots DR, Sutter RW, Strebel PM, Weibel RE, Cochi SL. Полнота отчетности по паралитическому полиомиелиту, США, 1980–1991 гг. Значение для оценки риска вакциноассоциированного заболевания. Arch Pediatr Adolesc Med. 1994; 148: 479–485. [PubMed] [Google Scholar] 27. Стребель П.М., Обер-Комбиску А., Ион-Неделку Н., Бибери-Морояну С., Комбеску М., Саттер Р.В., Кью О.М., Палланш М.А., Патриарка П.А., Кочи С.Л.Паралитический полиомиелит в Румынии, 1984-1992 гг. Доказательства высокого риска вакциноассоциированного заболевания и повторного занесения инфекции дикого вируса. Am J Эпидемиол. 1994; 140:1111–1124. [PubMed] [Google Scholar] 29. Стребель П.М., Ион-Неделку Н., Боуман А.Л., Саттер Р.В., Кочи С.Л. Внутримышечные инъекции в течение 30 дней после иммунизации пероральной полиовирусной вакциной — фактор риска вакциноассоциированного паралитического полиомиелита. N Engl J Med. 1995; 332: 500–506. [PubMed] [Google Scholar] 30. Ион-Недельку Н., Стребель П.М., Тома Ф., Бибери-Морояну С., Комбеску М., Персу А., Обер-Комбиску А., Плоткин С.А., Саттер Р.В.Последовательное и комбинированное применение инактивированной и оральной вакцин против полиомиелита: округ Долж, Румыния, 1992-1994 гг. J заразить Dis. 1997; 175 Приложение 1:S241–S246. [PubMed] [Google Scholar] 32. Байкуш А., Персу А., Комбеску М., Обер-Комбеску А. Поддержание активного лабораторного эпиднадзора за случаями острого вялого паралича (ОВП) в Румынии в рамках стратегического плана глобальной инициативы по ликвидации полиомиелита. Роум Арч Микробиол Иммунол. 2007; 66: 44–50. [PubMed] [Google Scholar] 33.Комбеску М., Гийо С., Персу А., Байкус А., Питигой Д., Баланант Дж., Оприсан Г., Крайник Р., Дельпейру Ф., Обер-Комбиску А. Циркуляция штамма полиовируса рекомбинантного вакцинного происхождения типа 1 на ограниченной территории в Румынии. Арх Вирол. 2007; 152: 727–738. [PubMed] [Google Scholar] 34. Байкус А., Персу А., Дину С., Жоффре М.Л., Дельпейру Ф., Оприсан Г. Частота и биоразнообразие полиовирусных и неполиомиелитных энтеровирусных штаммов, выделенных у здоровых детей, проживающих на ограниченной территории в Румынии. Арх Вирол.2011; 156:701–706. [PubMed] [Google Scholar] 35. Аду Ф., Ибер Дж., Букбук Д., Гумеде Н., Ян С.Дж., Джорба Дж., Кампаньоли Р., Суле В.Ф., Ян С.Ф., Бернс С. и др. Выделение рекомбинантного полиовируса вакцинного происхождения типа 2 (ПВВП) у нигерийского ребенка. Вирус рез. 2007; 127:17–25. [PubMed] [Google Scholar] 37. Grassly NC, Wenger J, Durrani S, Bahl S, Deshpande JM, Sutter RW, Heymann DL, Aylward RB. Защитная эффективность моновалентной оральной вакцины против полиомиелита 1 типа: исследование случай-контроль. Ланцет. 2007; 369:1356–1362.[PubMed] [Google Scholar] 38. Центры по контролю и профилактике заболеваний (CDC) Прогресс в направлении прекращения передачи дикого полиовируса — по всему миру, 2008 г. MMWR Morb Mortal Wkly Rep. 2009; 58:308–312. [PubMed] [Google Scholar]40. Страновой офис Всемирной организации здравоохранения в Таджикистане; Европейское региональное бюро ВОЗ; Европейский центр профилактики и контроля заболеваний. Вспышка полиомиелита в Таджикистане в 2010 г.: риск завоза и влияние на эпиднадзор за полиомиелитом в Европе. Евронаблюдение. 2010;15:pii=19558.[PubMed] [Google Scholar]41. Центры по контролю и профилактике заболеваний (CDC) Обновленная информация о полиовирусах вакцинного происхождения. MMWR Morb Mortal Wkly Rep. 2006; 55: 1093–1097. [PubMed] [Google Scholar]42. Мохаммед А.Дж., АлАвайди С., Бавикар С., Куруп П.Дж., Эламир Э., Шабан М.М., Шариф С.М., ван дер Авоорт Х.Г., Палланш М.А., Маланкар П. и др. Дробные дозы инактивированной вакцины против полиомиелита в Омане. N Engl J Med. 2010;362:2351–2359. [PubMed] [Google Scholar]43. Резик С., Техеда А., Лаго П.М., Диас М., Карменатес А., Сармьенто Л., Алемани Н., Галиндо Б., Бертон А., Фриде М. и др.Рандомизированное контролируемое клиническое исследование дробных доз инактивированной полиовирусной вакцины, вводимой внутрикожно с помощью безыгольного устройства на Кубе. J заразить Dis. 2010; 201:1344–1352. [PubMed] [Google Scholar]44. Болдуин С.Л., Фокс С.Б., Палланш М.А., Колер Р.Н., Рид С.Г., Фриде М. Повышение эффективности инактивированной трехвалентной вакцины против полиомиелита с помощью эмульсий масло-в-воде. вакцина. 2011; 29: 644–649. [PubMed] [Google Scholar]45. Kreeftenberg H, van der Velden T, Kersten G, van der Heuvel N, de Bruijn M. Перенос технологии Sabin-IPV на новые рынки развивающихся стран.Биопрепараты. 2006; 34: 155–158. [PubMed] [Google Scholar]46. Simizu B, Abe S, Yamamoto H, Tano Y, Ota Y, Miyazawa M, Horie H, Satoh K, Wakabayashi K. Разработка инактивированной полиовирусной вакцины, полученной из штаммов Sabin. Биопрепараты. 2006; 34: 151–154. [PubMed] [Google Scholar]47. Эйлуорд Б., Ямада Т. Финал полиомиелита. N Engl J Med. 2011;364:2273–2275. [PubMed] [Google Scholar]Вакцина против полиомиелита, инактивированная (путь инъекции) Описание и торговые названия
Описание и торговые марки
Информация о лекарствах предоставлена: IBM Micromedex
Торговая марка США
- Ипол
Описание
Вакцина против полиомиелита является активным иммунизирующим средством, используемым для профилактики полиомиелита (полиомиелита).Он работает, заставляя ваше тело вырабатывать собственную защиту (антитела) против вируса, вызывающего полиомиелит.
Существует два типа вакцины против полиомиелита, которые вводятся путем инъекций: инактивированная вакцина против полиомиелита (IPV) и инактивированная вакцина против полиомиелита повышенной эффективности (eIPV). В США и Канаде типом вакцины, которая вводится путем инъекции, является eIPV. Тип вакцины, которую вводят перорально, называется живой пероральной вакциной против полиомиелита (ОПВ).
Полиомиелит — очень серьезная инфекция, вызывающая паралич мышц, в том числе мышц, позволяющих ходить и дышать.Инфекция полиомиелита может сделать человека неспособным дышать без помощи «железного легкого», неспособным ходить без скоб для ног или прикованным к инвалидному креслу. Лекарства от полиомиелита нет.
Иммунизация против полиомиелита рекомендуется всем младенцам в возрасте от 6 до 12 недель, всем детям, всем подросткам в возрасте до 18 лет и некоторым взрослым, которые подвергаются большему риску заражения полиовирусами, чем население в целом, в том числе:
- Лица, путешествующие в районы или страны, где полиомиелит не контролируется, независимо от того, были ли они вакцинированы против полиомиелита в прошлом.
- Лица, проживающие в районах, где полиомиелит все еще встречается.
- Взрослые, которые не были вакцинированы или которым не была сделана полная серия вакцинаций против полиомиелита и которые живут в домохозяйствах с детьми, которым необходимо сделать оральную вакцину против полиомиелита (ОПВ).
- Работники детских садов и групповых домов для детей, таких как детские дома.
- Сотрудники медицинских учреждений, таких как больницы и кабинеты врачей.
- Работники лаборатории, работающие с образцами, которые могут содержать вирусы полиомиелита.
Иммунизация против полиомиелита не рекомендуется для младенцев в возрасте до 6 недель, поскольку антитела, полученные ими от матерей до рождения, могут снизить эффективность вакцины. Младенцы, которые были иммунизированы против полиомиелита в возрасте до 6 недель, должны получить полную серию прививок против полиомиелита.
Эта вакцина должна вводиться только вашим врачом или другим медицинским работником или под его наблюдением.
Этот продукт доступен в следующих лекарственных формах:
Получите самую свежую медицинскую информацию от экспертов Mayo Clinic.
Зарегистрируйтесь бесплатно и будьте в курсе последних научных достижений, советов по здоровью и актуальных тем, связанных со здоровьем, таких как COVID-19, а также экспертных знаний по управлению здоровьем.
Узнайте больше об использовании данных Mayo Clinic.Чтобы предоставить вам наиболее актуальную и полезную информацию, а также понять, какие информация полезна, мы можем объединить вашу электронную почту и информацию об использовании веб-сайта с другая информация о вас, которой мы располагаем. Если вы пациент клиники Майо, это может включать защищенную информацию о здоровье.Если мы объединим эту информацию с вашей защищенной медицинской информации, мы будем рассматривать всю эту информацию как информацию и будет использовать или раскрывать эту информацию только так, как указано в нашем уведомлении о практики конфиденциальности. Вы можете отказаться от получения сообщений по электронной почте в любое время, нажав на ссылка для отписки в письме.
Подписаться!
Спасибо за подписку
Наш электронный информационный бюллетень Housecall будет держать вас в курсе последней медицинской информации.
Извините, что-то пошло не так с вашей подпиской
Повторите попытку через пару минут
Повторить попытку
Последнее обновление частей этого документа: февр.01, 2021
Copyright © 2022 IBM Watson Health. Все права защищены. Информация предназначена только для использования Конечным пользователем и не может быть продана, перераспределена или иным образом использована в коммерческих целях.
.
NIBSC — Новые вакцины против полиомиелита
С 1950-х годов существуют две безопасные и эффективные вакцины против полиомиелита:
- инактивированная (убитая) вакцина против полиомиелита, известная как ИПВ или Солк, которая производится из диких штаммов и вводится путем инъекции
- живая аттенуированная (ослабленная) пероральная полиомиелитная вакцина – ОПВ или Сэбина – для перорального введения
ОПВ использовалась в рамках Глобальной инициативы по ликвидации полиомиелита для снижения случаев полиомиелита более чем на 99% и ограничения циркуляции полиовируса в нескольких странах.
Но это живая вирусная вакцина, которая со временем может эволюционировать в более вирулентные штаммы. Из-за этого многие страны, в том числе Великобритания, перешли на ИПВ. ИПВ обеспечивает превосходный иммунитет против полиомиелита, но менее эффективна, чем ОПВ, для предотвращения инфекции и передачи инфекции, поэтому для успешной ликвидации болезни необходимы обе вакцины.
Геномная структура штаммов для клеточных вакцин Vero
Полиовирус имеет геном одноцепочечной РНК, транслируемый как полипротеин — четыре капсидных белка, которые определяют серотип и антигенную структуру и происходят от гена P1.
Семена вакцины кодируют P1 из трех штаммов, используемых в настоящее время в ИПВ, а также из трех штаммов Сэбина. Неструктурные белки происходят от Sabin 3 и были модифицированы в гене 2A таким образом, чтобы адаптировать их к росту клеток Vero. Некодирующие области, которые контролируют инфекционность и генетическую стабильность штаммов, происходят из конструкции под названием S19.
Чтобы завершить и поддерживать глобальную ликвидацию полиомиелита, предстоит решить еще несколько проблем, в том числе:
- биоизоляция диких полиовирусов, например тех, которые используются при производстве ИПВ, для предотвращения их утечки из учреждений во внешний мир
- профилактика и контроль вспышек, вызванных штаммами ОПВ, которые превратились в по существу дикие вирусы – сейчас и в будущем
Новые вакцины
Благодаря многолетнему опыту NIBSC в области вакцин против полиомиелита и в рамках нашего вклада в общественное здравоохранение во всем мире мы участвуем в трех проектах по разработке новых вакцин для искоренения болезни.
Во-первых, мы разработали новые штаммы полиовируса для производства ИПВ без риска его случайного проникновения в человеческую популяцию из учреждения. Это означает, что его можно производить в местах с более низким иммунитетом людей и неидеальными санитарными условиями, как во многих странах с низкими издержками. Эти штаммы теперь лицензированы для крупного производителя вакцин.
Второй подход включает в себя разработку капсидных белков полиовируса, позволяющую производить вирусоподобные частицы (ВПЧ), которые антигенно эквивалентны живым вирусам и достаточно стабильны, чтобы можно было производить вакцину с использованием рекомбинантной экспрессии – без использования какого-либо живого вируса – который идеально подходит для мира после искоренения.
В-третьих, мы разрабатываем новые живые аттенуированные штаммы, которые являются генетически стабильными и которые с меньшей вероятностью вернут свойства дикого типа. Они были бы полезны для борьбы со вспышками после прекращения вакцинации штаммами Сэбина.
Штаммы
Разработанные нами посевные штаммы ИПВ могут размножаться в клеточной культуре, что позволяет производить вакцину, но они фактически неинфекционны для человека и в результате сильно ослаблены. Штаммы генетически стабильны, поэтому они не должны снова стать инфекционными во время производства.Благодаря своей конструкции штаммы вызывают такой же защитный иммунитет, как и нынешняя ИПВ.
Штаммы S19-IPV
Термостабильные полиовирусные вирусоподобные частицы (ВПЧ)
ВПЧ, не содержащие вирусной РНК – пустые капсиды – образуются естественным путем во время полиовирусных инфекций. Внешняя поверхность ВПЧ неотличима от поверхности вирусной частицы, но несколько внутренних аминокислотных цепей неупорядочены. В результате ВПЧ являются иммуногенными, но конформационно нестабильными при физиологических температурах.
Мы идентифицировали замены аминокислот, которые стабилизируют VLP без изменения антигенности, и эти VLP, по-видимому, не менее термостабильны, чем современная инактивированная вакцина Солка против полиомиелита. Мы разрабатываем производство стабильных VLP с использованием рекомбинантных систем экспрессии млекопитающих, дрожжей, бактерий, бакуловирусов и растений в сотрудничестве с несколькими британскими лабораториями:
Генетически стабильные штаммы ОПВ
5’-некодирующая область генома полиовируса сильно структурирована.РНК-домен V — критический как для инфекционности кишечника, так и для аттенуации — является частью более крупной структуры, которая контролирует инициацию трансляции, а уровень аттенуации определяется ее термодинамической стабильностью.
Мы модифицировали домен V, чтобы сделать его генетически стабильным, удалив все пары оснований U-G. Любая одиночная мутация в стеблях, состоящих из пар оснований, ослабит эту структуру и создаст более аттенуированный вирус.
Мы также переместили важный цис--действующий элемент репликации (cre) из области P2 ближе к 5′-концу, чтобы снизить риск потери этой части генома в результате рекомбинации.Таким образом, для замены домена V требуются два события рекомбинации — одно событие также удалит cre, и полученный геном будет неинфекционным.
В сотрудничестве с Andino Lab Калифорнийского университета в Сан-Франциско мы также модифицируем полимеразу, внося мутации, которые повышают ее точность и снижают ее способность катализировать гомологичную рекомбинацию.
Солк и Сэбин: иммунизация против полиомиелита
Первое десятилетие ХХ века ознаменовалось волной исследований полиомиелита.Однако лечение и профилактика были малоэффективны, и эпидемии продолжались, что приводило к большим потерям в виде остаточной инвалидности.
Вакцины
В 1935 году Морис Броди попытался модифицировать вирус, подвергнув его воздействию формальдегида. Эту инактивированную формалином «вакцину» сначала опробовали на 20 обезьянах, а затем на 3000 детях. Результаты были плохими, и вакцина Броди больше никогда не использовалась. 1 Джон Коллмер использовал живой аттенуированный вирус, который также оказался неэффективным и стал причиной многих случаев полиомиелита, некоторые из которых были смертельными.
Попытки разработать вакцину против полиомиелита продолжаются. В 1955 г. Солк 2 разработал инактивированную полиовирусную вакцину; таким образом началась повсеместная иммунизация. За этим последовала живая аттенуированная пероральная вакцина, разработанная Сэбином в 1960 году. 3 Эффект был впечатляющим. Из 28 000 зарегистрированных случаев полиомиелита в 1955 г. в 1956 г., через год после иммунизации, было зарегистрировано только 15 000 случаев.
Лаборатория Солка в Питтсбурге была создана в 1948 году для типирования полиовирусов.Солк был новичком в исследованиях полиомиелита. В его работе над вирусом гриппа военного времени использовался «убитый вирус». Для полиомиелита он использовал тот же подход, применяя недавно разработанные методы культивирования тканей. К 1954 году он оказался эффективным против всех трех штаммов полиовируса. Солк сообщил о результатах в январе 1953 года. Возможно, из-за самой страшной в истории эпидемии полиомиелита в 1952 году комитет Национального фонда поддержал работу Солка. В испытаниях 1954 г. более миллиона детей были случайным образом разделены на вакцинированные и невакцинированные группы.Вакцинация снизила заболеваемость до менее чем 50%; когда привитый ребенок заражался полиомиелитом, он обычно не был паралитическим.
Йонас Солк (1914–1995)
Родившийся в семье русско-еврейских родителей, Солк учился в медицинской школе Нью-Йоркского университета. Он провел год, исследуя недавно открытый вирус гриппа. Его техника увенчалась успехом и легла в основу его более поздней работы по полиомиелиту:
. «Принцип, который я пытался установить, заключался в том, что на самом деле не было необходимости подвергаться риску заражения, который имел бы место, если бы кто-то пытался разработать аттенуированную или ослабленную полиовирусную вакцину.И поэтому мне казалось, что это более безопасный и верный путь. Если бы мы могли инактивировать вирус, мы могли бы очень быстро перейти к вакцине».
В 1947 году он был назначен в Питтсбургский университет для работы с Национальным фондом детского паралича. К 1955 году испытания его вакцины против полиомиелита показали ее эффективность. Когда 12 апреля 1955 года стало известно об открытии, Солка провозгласили чудотворцем. Он еще больше расположил к себе публику, отказавшись запатентовать вакцину или получить прибыль от своего открытия.В 1963 году он основал Институт биологических исследований Солка. Он продолжал проводить исследования и публиковать книги, некоторые в сотрудничестве со своими сыновьями, которые также являются учеными-медиками. Книги Солка включают Человек, разворачивающийся (1972), Выживание мудрейших (1973), Население мира и человеческие ценности: новая реальность (1981) и Анатомия реальности (1983). В 1954 году он был удостоен Нобелевской премии за первую эффективную вакцину против полиомиелита. Последние годы своей жизни он провел в поисках вакцины против СПИДа.Великий пионер Солк умер 23 июня 1995 года в возрасте 80 лет.
Альберт Сабин (1906–1993)
Сэбин показал, что полиовирус сначала вторгся в пищеварительный тракт, а затем в нервную систему. Он также был среди тех, кто идентифицировал три типа полиовируса. Он разработал живую, но аттенуированную пероральную вакцину, которая показала себя лучше в применении, но также обеспечивала более длительный иммунитет, чем вакцина Солка. После столкновения между соперничающими лагерями и их лидерами к 1962 году вакцина Солка была заменена вакциной Сэбина. 4 Эффективность доказана в полевых испытаниях (1958 и 1959 гг.).
Альберт Брюс Сабин 5 родился 26 августа 1906 года в Белостоке, Польша, тогда часть России. Он и его семья эмигрировали в США в 1921 году, спасаясь от расовых преследований. Он окончил Нью-Йоркский университет в 1928 году. Год в Институте профилактической медицины Листера в Лондоне способствовал его обучению. В 1935 году он присоединился к персоналу Рокфеллеровского университета, а в 1939 году перебрался в Детскую больницу Цинциннати, чтобы проводить исследования вирусов.Он был консультантом армии во время Второй мировой войны, выделил вирус лихорадки москитов и помог разработать вакцину против лихорадки денге. Его исследования включали токсоплазмоз и вирусный энцефалит. После войны Сабин вернулся в Цинциннати, чтобы разработать вакцину против полиомиелита в 1954 году.
В 1970 году он стал президентом Научного института Вейцмана в Израиле, но позже ушел в отставку из-за болезни сердца. Он получил множество наград: избрание в Национальную академию наук в 1951 году; Мемориальная премия Брюса Американского колледжа врачей, 1961 г .; премия Фельтнелли Римской академии деи Линчеи, 1964 г .; Премия Ласкера за клинические исследования в 1965 году; и Национальная медаль науки США в 1971 году.
Значение работы Солка и Сабина неизмеримо. Сабин умер 3 марта 1993 года.
Каталожные номера
- ↵
Пол Младший . История полиомиелита. Нью-Хейвен: издательство Йельского университета, 1971: 256.
- ↵
Солк JE . Исследования на людях по активной иммунизации против полиомиелита. 1. Предварительный отчет. J Amer Med Assoc1953;151:1081–98.
- ↵
Сабин А.Б. . Характеристики и генетические возможности экспериментально полученных и встречающихся в природе вариантов вируса полиомиелита. Ann NY Acad Sci1955;61:924–38.
- ↵
Сабин А.Б. . Характеристики и генетические возможности экспериментально полученных и встречающихся в природе вариантов вируса полиомиелита. Ann NY Acad Sci1955;61:924–38.
- ↵
Некролог доктора Сабина .Нью-Йорк Таймс, 4 марта 1993 г.
Пероральная вакцина против полиомиелита – обзор
Роль ИПВ в ликвидации полиомиелита
Роль ИПВ в содействии ликвидации и ее верификации вызывает много споров, начиная от нулевой роли 304, 321 9051 ИПВ за ОПВ. 322
Непрерывная циркуляция диких полиовирусов ликвидирована в нескольких регионах ВОЗ, но в некоторых из них, например, в России 323 , в последнее время имели место изолированные завозы полиовирусов, которые могут продолжаться.
Основным оружием в усилиях по искоренению была ОПВ, применявшаяся в рамках национальных кампаний, хотя та же цель была достигнута во многих европейских странах с использованием ИПВ. Кампании ОПВ также оказывают заметное влияние на заболеваемость полиомиелитом в традиционно эндемичных районах, таких как Индийский субконтинент и Африка. 311 Однако уверенность в возможности искоренения пошатнулась. 312 Во-первых, потому что в 2003 г. ложные журналистские слухи о заражении ОПВ ВИЧ и эстрогенами привели к прекращению вакцинации в Нигерии, что впоследствии привело к циркуляции полиовируса и его распространению в 18 странах; 313 во-вторых, потому что было обнаружено явление эпидемий, вызванных ПВВП, которое можно отнести к обширным мутациям и рекомбинациям после циркуляции; 314 и в-третьих, потому что расходы на программу стали вызывать усталость доноров.Хотя успешная ликвидация дикого полиомиелита в Индии была достигнута при беспрецедентно низком уровне заболеваемости полиомиелитом в конце 2011 года, 306 некоторые индийские ученые особенно громко призывали к более широкому использованию ИПВ. 315–317 По мнению ВОЗ, в качестве основного средства ликвидации полиомиелита в развивающихся странах следует использовать только ОПВ. 303, 304 Однако Джон, 305 , работающий в Южной Индии, показал, что ИПВ может быть очень эффективной в профилактике полиомиелита без проблем, связанных с ОПВ (ВАПП и необходимость повторного введения для получения однородной сероконверсии).Тем не менее, Индии, возможно, удалось ликвидировать полиомиелит, используя только ОПВ. По состоянию на май 2012 г. в Индии в течение 2011 г. был зарегистрирован только один случай острого вялого паралича, вызванного диким полиовирусом, случай в Западной Бенгалии, начавшийся в январе. 306 ВОЗ признает, что в мире может быть до 500 случаев ВАПП в год, 318 , что ПВВП стал реальной угрозой для ликвидации, 319 и что моновалентные и бивалентные ОПВ необходимы для повышения эффективности. 320
Предлагались различные стратегии для «эндшпиля». Заявленная стратегия ВОЗ заключается в прекращении использования ОПВ после подтверждения ликвидации. 313 Консультативные группы ВОЗ сейчас обсуждают, какой должна быть роль ИПВ после ликвидации. Вполне вероятно, что как минимум ИПВ будет использоваться во всех странах, производящих ИПВ, и также вероятно, что ИПВ будет доступна для других стран, которые захотят ее использовать. Что более спорно, так это то, будет ли ИПВ рекомендована для всех стран или же отдельным странам будет предоставлено право самим делать свой выбор.Риск для стран, не использующих ИПВ, заключается в возможности позднего распознавания возвращения полиовирусов. Поскольку очень многие инфекции являются субклиническими, к тому времени, когда случаи будут выявлены, их может быть очень трудно сдержать, особенно если исходный популяционный иммунитет составляет 0% среди когорт, родившихся после прекращения применения ОПВ. Эта стратегия включает простое наблюдение за циркуляцией полиовируса и случаями вызванного полиовирусом паралича в отсутствие вакцинации, а затем повторное введение моновалентной ОПВ для сдерживания любых выявленных вспышек. 324, 325 Кроме того, сообщения о лицах с ослабленным иммунитетом, выделяющих полиовирус в течение длительного периода времени 328 , вызывают подозрение на повторное заражение вирусом.
Второй стратегией было бы продолжение вакцинации ОПВ при попытках обнаружить циркулирующий дикий полиовирус, но сегодня трудность будет заключаться в обнаружении дикого вируса в море выделяемых аттенуированных вирусов, некоторые из которых мутировали в сторону вирулентности, а некоторые рекомбинантны с другими полиовирусами. 326, 327 ВАПП будет продолжаться, поэтому паралич, вызванный полиовирусами, не будет полностью искоренен. Еще большую озабоченность вызвало осознание того, что ревертанты штаммов Сэбина стали эпидемиями в Египте, Гаити, Доминиканской Республике, Мадагаскаре, Китае и на Филиппинах, хотя, за исключением недавней Нигерии, большинство этих вспышек были довольно небольшими по сравнению с количество вызванных ими случаев. 314, 320, 329, 330 С другой стороны, вспышка цПВВП в Нигерии указывает на потенциал этих вирусов для восстановления полной нейровирулентности и характеристик трансмиссивности диких вирусов.
Можно предложить третью стратегию, состоящую в постепенном переходе от ОПВ к комбинированным педиатрическим вакцинам, содержащим ИПВ (например, АКДС/Hib/гепатит В/ИПВ), по мере исчезновения дикого полиовируса во все большем числе стран. Вакцинация ИПВ облегчила бы поиск полиовирусов в окружающей среде, поскольку вакцинные штаммы ОПВ не мешали скринингу, и при этом сохранялась бы защита от полиомиелита. Такая стратегия может быть еще более ценной, поскольку было подсчитано, что даже после 5-летнего периода без случаев полиомиелита все еще остается 0.Вероятность тихой передачи от 1% до 1,0%. 331
Также активно рассматривается возможность одновременного использования ОПВ/ИПВ в кампаниях массовой вакцинации в районах высокого риска, чтобы максимизировать индукцию иммунитета при каждом контакте с ребенком. Вопрос заключается в том, может ли охват инъекционной вакциной, используемой в режиме кампании, быть достаточно высоким для повышения иммунитета населения, или же снижение охвата перевешивает любые преимущества повышения иммунитета при одновременном использовании обеих вакцин.Следует упомянуть потенциальную роль ИПВ в процессе перехода от тОПВ к бОПВ, поскольку ДПВ2, по-видимому, был ликвидирован. Преимущество ИПВ будет заключаться в обеспечении постоянного иммунитета к типу 2 для предотвращения повторного появления диких вирусов типа 2 или цПВВП, а также в повышении иммунитета против типов 1 и 3, что может ускорить ликвидацию этих двух типов.
Результаты программы внедрения ИПВ в провинции Джокьякарта на Филиппинах, осуществляемой с 2007 г., иллюстрируют влияние стратегии перехода с ОПВ на ИПВ.С момента принятия отдельной вакцины ИПВ (со схемой 3+1) в сентябре 2007 г. в популяции численностью 3 571 865 человек с годовой когортой рождений 52 723, уровень охвата вакцинацией не снизился в течение 4 лет последующего наблюдения (осталось > 95%). Отбор проб окружающей среды (входные сточные воды) подтвердил отсутствие циркуляции ДПВ и очень быстрое снижение количества изолированных полиовирусов только в 5 образцах с вирусами Сэбина и без ПВВП (с оговоркой, что 24 месяца из 55-месячного периода наблюдения были пропущены).Наконец, исследование серопревалентности и сероконверсии от дозы 3 к дозе 4, проведенное на 188 младенцах, выявило 100% серопротекцию после дозы 3 и увеличение GMT от дозы 3 к дозе 4.
страны уже используют или скоро перейдут на ИПВ, главным образом для того, чтобы избежать спорадических или эпидемических ВАПП, связанных с использованием ОПВ. Некоторые из наиболее богатых развивающихся стран также воспользуются ИПВ. Ввиду возможного использования полиовируса в качестве биологического оружия многие страны будут продолжать использовать ИПВ, даже если будет достигнута ликвидация циркуляции дикого вируса. 332 Развивающимся странам может также не понравиться риск возобновления полиомиелита, если иммунизация ОПВ будет прекращена из-за неопределенности в отношении постоянной циркуляции диких или ревертантных вакцинных вирусов среди здоровых людей и лиц с ослабленным иммунитетом. 333, 334
Основными аргументами против перехода с ОПВ на ИПВ во многих развивающихся странах с низким уровнем дохода являются стоимость, происхождение вакцины и снижение кишечного иммунитета. 335 В некоторой степени первые два пункта связаны между собой, поскольку большие объемы производства снижают затраты на производство и контроль качества и позволяют лучше планировать, но отдают все карты в руки ограниченному числу игроков.До сих пор у компаний не было стимула производить больше ИПВ. Тем не менее, более убедительным ответом на стоимость является то, что ИПВ следует использовать не как отдельную вакцину с сопутствующими расходами на отдельное введение, а вместо этого как часть комбинированной вакцины. 336 Комбинации, содержащие ИПВ на основе дифтерийно-столбнячно-коклюшной бесклеточной вакцины, легко доступны, но ключевым отсутствующим продуктом является действительно доступная пятивалентная или шестивалентная комбинация, вероятно, изготовленная на основе цельноклеточной коклюшной АКДС (при условии, что фармацевтические технические проблемы, связанные с эффект консервантов в многодозовых презентациях решен).Если бы был спрос (вспомните часто высказываемое желание включить новые вакцины в календарь РПИ), стоимость ИПВ была бы ничтожной в составе таких доступных комбинаций на основе АКДС. Но в этом контексте ключевым фактором для будущей эффективности ИПВ будет уровень охвата, достигнутый посредством плановой иммунизации. Вопрос о значении защиты населения, вызванной ИПВ, в контексте показателей охвата вакцинацией от 50% до 80% все еще требует уточнения. Если бы единственным способом увеличить этот охват вакцинацией было бы проведение Национальных дней иммунизации ОПВ, то было бы труднее доказать дополнительную ценность использования ИПВ.
В ближайшем будущем возможно ежегодное производство от 200 до 300 миллионов доз ИПВ. Чтобы уменьшить потребность в большем количестве, использование ИПВ в развивающихся странах может быть нацелено на страны или регионы стран, граничащие с районами, где полиовирус предположительно ликвидирован; таким образом, появление вируса можно было распознать по выделению из экскрементов, а не по вспышкам паралича.
Хотя вакцинация ОПВ должна быть продолжена в странах, где полиовирусы дикого типа все еще циркулируют, или в странах с высоким риском реинтродукции полиовирусов дикого типа, других странах с высоким охватом вакцинацией и отсутствием циркуляции полиовирусов дикого типа или при умеренном риске повторного введения следует рассмотреть возможность перехода на последовательные схемы ИПВ/ОПВ или только на ИПВ.Более того, страны, которые прекращают использование ОПВ после предполагаемой ликвидации дикого полиовируса, должны рассмотреть вопрос о включении ИПВ в свои графики вакцинации, чтобы защитить свое население от повторного появления полиовирусов.
Полный список литературы доступен на сайте http://www.expertconsult.com
|

 Схема введения: 0-2-6 мес.
Схема введения: 0-2-6 мес. 30-16.00 – уборка, кварцевание, проветривание, работа с документами.
30-16.00 – уборка, кварцевание, проветривание, работа с документами. 00 – 19.30
00 – 19.30
 — За эти два года мы ничем не болели. С врачами я не консультировалась. Медики, с которыми мне приходилось общаться, доверия не вызывают. С ними мне общаться не о чем».
— За эти два года мы ничем не болели. С врачами я не консультировалась. Медики, с которыми мне приходилось общаться, доверия не вызывают. С ними мне общаться не о чем».
 Но нужно чётко понимать, что „после“ не означает „из-за“. И при тщательном обследовании, как правило, оказывается, что ухудшение в состоянии здоровья пациента вызвано отнюдь не вакцинацией, а совершенно иными причинами», — поясняет Людмила.
Но нужно чётко понимать, что „после“ не означает „из-за“. И при тщательном обследовании, как правило, оказывается, что ухудшение в состоянии здоровья пациента вызвано отнюдь не вакцинацией, а совершенно иными причинами», — поясняет Людмила.