Степень зрелости плаценты по неделям (таблица). Нормы и отклонения зрелости плаценты
Плацента – важный орган беременной женщины, который формируется и существует на протяжении всего времени роста плода. После появления новорождённого на свет детское место отторгается. Этот уникальный временный орган связывает мать и ребёнка во время беременности. Именно благодаря плаценте малыш получает необходимые питательные вещества.
Детское место, как и любой живой организм, формируется, созревает и стареет. Каждый из этих физиологических процессов должен происходить в своё время. В таком случае беременность будет протекать успешно, а ребёнок будет здоров. Если будущая мама хочет узнать, какой, к примеру, должна быть степень зрелости плаценты в 33 недели беременности, ей следует воспользоваться специальной таблицей с нормативными показателями. Такая схема будет приведена в статье ниже. Благодаря ей можно узнать, правильно ли развивается детское место.
Когда формируется плацента?
Слово placenta в переводе с латыни означает «лепёшка». Этот орган назвали так благодаря его дисковидной приплюснутой форме.
Этот орган назвали так благодаря его дисковидной приплюснутой форме.
Примерно на десятый день после зачатия клетки, предназначением которых является обеспечение связи между мамой и плодом, начинают активно делиться. Вследствие этого происходит выработка специальных ферментов. Их задачей является создание в полости матки благоприятных условий для последующей возможности насыщения ребёнка питательными веществами из организма мамы. После этого формируется постоянный кровообмен между беременной и малышом. Рост плаценты становится настолько активным, что размеры этого органа на начальных стадиях даже превышают величину эмбриона.
Далее происходит постоянное увеличение массы и рост ворсинчатого древа детского места. Продолжается разветвление кровеносных сосудов вследствие разделения каждого их отростка на несколько новых. Такой временный орган заканчивает процесс роста уже почти перед самыми родами. Правильность развития детского места характеризуется таким показателем, как степень зрелости плаценты по неделям. Таблица с соответствующим описанием характеристик будет представлена ниже.
Таблица с соответствующим описанием характеристик будет представлена ниже.
Для чего нужна плацента?
Основной задачей плаценты является обеспечение жизнедеятельности плода в течение всего периода беременности. Детское место выполняет следующие важные функции:
- обеспечивает иммунологическую защиту плода, пропуская необходимые антитела беременной женщины к малышу, но при этом удерживает определённые клетки иммунной системы матери, которые могли бы запустить механизм отторжения эмбриона, приняв его за чужеродный объект;
- выводит токсины;
- защищает малыша от негативного влияния окружающей среды, вредного воздействия бактерий и вирусов;
- выполняет функции железы внутренней секреции, синтезируя определённые гормоны, которые необходимы для удачного протекания беременности;
- снабжает плод кислородом и выводит образующийся углекислый газ;
- доставляет ребёнку питательные вещества и помогает избавиться от продуктов жизнедеятельности.
Состояние плаценты оказывает крайне важное влияние на состояние малыша и на процесс протекания беременности в целом.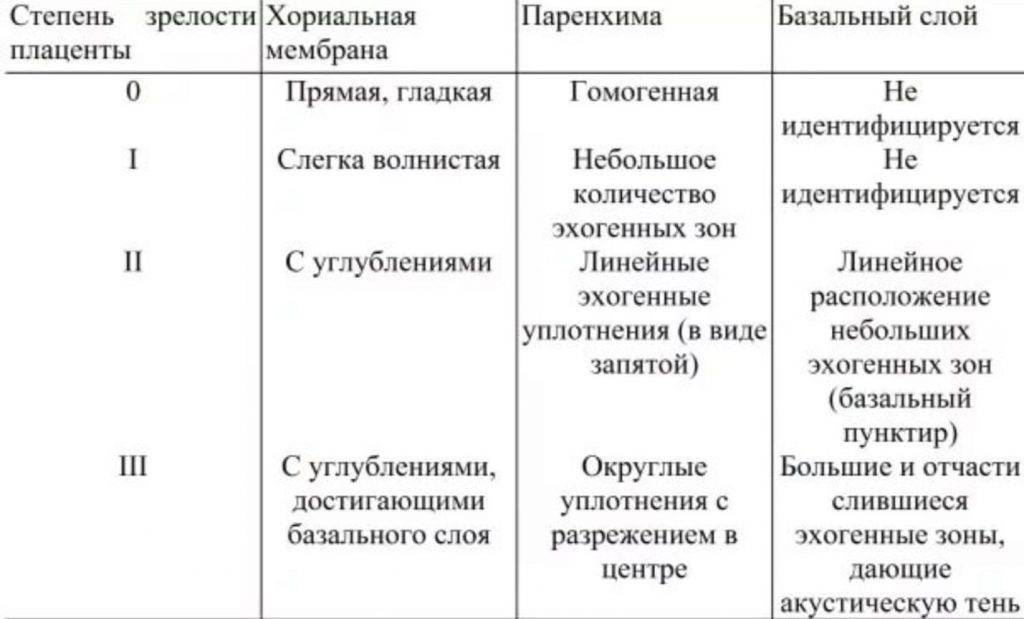 Для поддержания здоровья этого органа нужно беречь его от вредных воздействий различного характера. К примеру, рекомендуется избегать скоплений большого количества людей, ведь даже банальные ОРВИ или ОРЗ могут быть опасными. Будущей матери не следует курить. Если у женщины имеются половые инфекции, от них нужно избавляться.
Для поддержания здоровья этого органа нужно беречь его от вредных воздействий различного характера. К примеру, рекомендуется избегать скоплений большого количества людей, ведь даже банальные ОРВИ или ОРЗ могут быть опасными. Будущей матери не следует курить. Если у женщины имеются половые инфекции, от них нужно избавляться.
Нормативная толщина плаценты
С самого начала беременности плацента активно растёт и развивается. К 16-18 неделе этот орган становится полностью функциональным. Толщина детского места незначительно увеличивается изо дня в день. Своего максимума этот показатель достигает к 34 неделе. Если беременность протекает благополучно, то ещё через пару недель рост и увеличение толщины плаценты останавливаются, а иногда даже идут на спад.
Этот показатель, характеризующий состояние детского места, может быть определён исключительно путём ультразвуковой диагностики. Измерять следует участок с наибольшей толщиной.
Если толщина детского места на конкретном сроке беременности не соответствует нормативным показателям, значит, функционирование этого органа нарушено. При этом может страдать и ребёнок.
При этом может страдать и ребёнок.
Ещё одним показателем, с помощью которого можно оценить состояние детского места, является степень зрелости плаценты по неделям. Таблица с нормативными значениями поможет грамотно оценить ситуацию. А сейчас рассмотрим случаи, когда толщина детского места отличается от стандартной.
Если толщина плаценты больше нормы
Причиной чрезмерного утолщения плаценты у беременной женщины может быть анемия, гестоз, резус-конфликт, сахарный диабет. Также негативное влияние на состояние детского места оказывают инфекционные заболевания. Причём опасность существует даже в том случае, когда будущая мама является просто переносчиком бактерий. Если беременная курит, употребляет алкоголь или наркотические вещества, то толщина её плаценты также может быть увеличена.
Темпы старения детского места с такой патологией ускорены, а значит, этот орган справляется со своими функциями недостаточно эффективно. Если плацента утолщена, она отекает, структура её стенок становится другой, происходит нарушение гормонального фона. Результатом таких изменений является недостаточное обеспечение ребёнка кислородом и питательными веществами. Это может стать причиной задержки внутриутробного развития малыша, гипоксии, преждевременных родов или даже гибели плода.
Результатом таких изменений является недостаточное обеспечение ребёнка кислородом и питательными веществами. Это может стать причиной задержки внутриутробного развития малыша, гипоксии, преждевременных родов или даже гибели плода.
Основываясь на результатах ультразвуковой диагностики, допплерографии или кардиотокографии, доктор назначает беременной женщине с утолщённым детским местом препараты, которые стимулируют маточно-плацентарный обмен и поддерживают нормальное развитие малыша. Если состояние плода не внушает опасений, врач может ограничиться более пристальным наблюдением за будущей мамой.
Тонкая плацента может свидетельствовать о гипоплазии детского места. Так называется состояние, когда этот орган недостаточно развит и не способен эффективно справляться со своими функциями.
Чрезмерное уменьшение толщины плаценты может быть как особенностью конституции беременной (чаще всего так происходит у женщин некрупного телосложения), так и являться следствием ряда других причин. К примеру, такая патология может возникнуть после того, как будущая мама перенесла инфекционное заболевание. Также могут сказаться гипертония, гемолитическая болезнь или атеросклероз.
К примеру, такая патология может возникнуть после того, как будущая мама перенесла инфекционное заболевание. Также могут сказаться гипертония, гемолитическая болезнь или атеросклероз.
Если недостаточная толщина плаценты является следствием какого-либо заболевания будущей мамы, на увеличение этого показателя можно повлиять путём излечения соответствующей болезни. В остальных случаях доктор применяет медикаментозную терапию, направленную на минимизацию возможных негативных последствий развития ребёнка.
Настало время рассмотреть такой важный показатель, как зрелость плаценты.
Что такое зрелость плаценты?
Созревание плаценты – естественный процесс, сопутствующий росту этого органа. Развитие детского места происходит таким образом, чтобы оно могло полноценно и своевременно обеспечивать потребности плода.
Степень зрелости детского места – это важнейший показатель. С его помощью можно оценить состояние плацентарного комплекса. Также эта характеристика помогает вовремя выявить патологические изменения в структуре детского места, которые могут оказать негативное влияние на плод.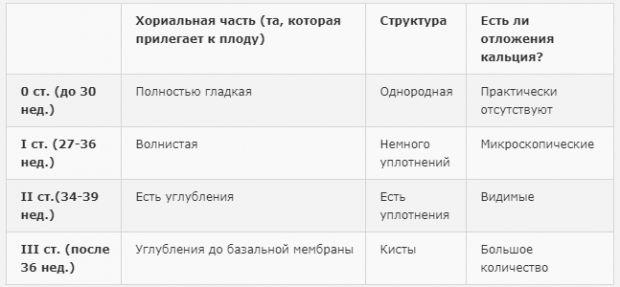
Если беременность протекает нормально, то за её период плацента проходит 4 степени зрелости. Подробное описание каждой из них следует ниже.
Степень зрелости плаценты по неделям (таблица)
Различают 4 степени зрелости детского места. Каждая из них соответствует определённому периоду развития этого органа.
Ниже приведена сводная схема, описывающая каждую степень зрелости плаценты по неделям. Таблица содержит характеристики структуры детского места и хориальной ткани на различных сроках беременности.
Степень зрелости плаценты | Нормативный срок беременности | Структура плаценты | Характеристика прилегающей к плоду хориальной ткани | Наличие кальциевых отложений |
Нулевая | По 30 неделю | Однородная | Гладкая и ровная | Практически отсутствуют |
Первая | С 27 по 36 неделю | Имеется небольшое количество уплотнений | Присутствуют отдельные эхогенные включения. | Имеются в малом количестве |
Вторая | С 34 по 39 неделю | В большом количестве имеются ярко выраженные уплотнения | Имеются мелкие эхогенные включения в большом количестве. Хориальная пластина приобретает ещё большую волнистость | Присутствуют хорошо различимые участки |
Третья | После 36 недели | Возможно присутствие кист | Волнистость хориальной пластины ярко выражена. Плацента имеет дольчатую структуру | Имеются в большом количестве |
Из таблицы видно, что нулевая степень зрелости плаценты в 30 недель – показатель, который находится в пределах нормы. Если врач после обследования будущей мамы именно так оценил взросление детского места, значит, беременность протекает хорошо.
Подробное описание каждой из степеней зрелости плаценты
Следующий этап созревания плаценты в норме длится с 27 по 36 неделю беременности. В этот период размеры детского места останавливают свой рост, а вот его толщина постепенно увеличивается. Первая степень зрелости плаценты в 34 недели – это хороший показатель. Хотя на таком сроке после посещения доктора существует возможность узнать, что взросление детского места достигло второго уровня. И это тоже будет нормой.
С 34 недели наступает самый спокойный и стабильный этап взросления детского места. Вторая степень зрелости плаценты в 39 недель – это граничный показатель. После этого срока развитие временного органа должно перейти на третий уровень. Если такой переход произойдёт раньше указанного срока, не следует волноваться. Чаще всего причин для тревоги в этом случае не существует.
Далее наступает третья степень зрелости плаценты. В 36 недель и позже детское место входит в заключительную фазу своего развития. В течение такого периода происходит биологическое старение временного органа. Оно сопровождается сокращением обменной площади плаценты и появлением большого количества участков кальциевых отложений.
Оно сопровождается сокращением обменной площади плаценты и появлением большого количества участков кальциевых отложений.
Если детское место опережает норму своего развития или, наоборот, отстаёт от неё, возможно развитие патологий. Такие ситуации рассмотрены ниже.
Несвоевременное развитие плаценты
Одной из проблем, связанных с детским местом, может стать его преждевременное созревание. О такой патологии можно вести речь, если 2 степень зрелости плаценты на 32 неделе беременности уже наступила. В этом случае за состоянием плода необходимо тщательно следить. Ведь такая ситуация свидетельствует о плацентарной недостаточности. Подробнее этот распространённый случай будет рассмотрен ниже.
Ещё одна проблема, которая встречается несколько реже предыдущей, – это позднее созревание детского места. Чаще всего такая патология характерна в том случае, когда существуют врождённые пороки развития плода. Дополнительными факторами риска является заболевание будущей мамы сахарным диабетом, резус-конфликт или наличие у беременной таких вредных привычек, как курение или употребление алкоголя. Если имеет место задержка созревания плаценты, то увеличивается степень риска рождения мёртвого ребёнка.
Если имеет место задержка созревания плаценты, то увеличивается степень риска рождения мёртвого ребёнка.
Преждевременное созревание плаценты
Преждевременным считается такое развитие, когда настаёт вторая степень зрелости плаценты в 32 недели беременности и раньше.
Причины возникновения такой патологии следующие:
- гестоз;
- нарушенный гормональный фон;
- заболевания сердечно-сосудистой системы или сахарный диабет у беременной;
- присутствие возбудителей инфекционных болезней;
- гипертония у будущей мамы;
- многоплодная беременность;
- избыточное содержание кальция в организме женщины;
- предлежание либо отслойка плаценты;
- резус-конфликт;
- употребление беременной алкоголя, никотина, наркотических веществ.
Также преждевременным считается взросление, когда третья степень зрелости плаценты настаёт раньше 36 недели беременности. Однако само по себе раннее старение детского места не является непосредственной угрозой здоровью или жизни плода. Опасна такая патология в случае, когда врач после обследования беременной выявил нарушения, которые могут привести к негативным последствиям. Это может быть гипоксия плода, его внутриутробная задержка развития, риск преждевременных родов.
Опасна такая патология в случае, когда врач после обследования беременной выявил нарушения, которые могут привести к негативным последствиям. Это может быть гипоксия плода, его внутриутробная задержка развития, риск преждевременных родов.
Докторам следует удостовериться в наличии патологии, используя другие методы диагностики. Если опасения подтвердились, то беременной назначается соответствующее лечение, в отдельных случаях даже стационарное.
Заключение
Самым важным показателем состояния плаценты является степень её зрелости. Эта характеристика даёт возможность оценить как физиологические, так и патологические изменения временного органа. Используя приведённую в статье специальную таблицу, будущая мама может узнать для конкретного срока беременности соответствующую степень зрелости плаценты. 31 неделя, к примеру, должна характеризоваться первым уровнем развития детского места.
Если результаты диагностики лишь немного отличаются от нормативных показателей, не нужно волноваться.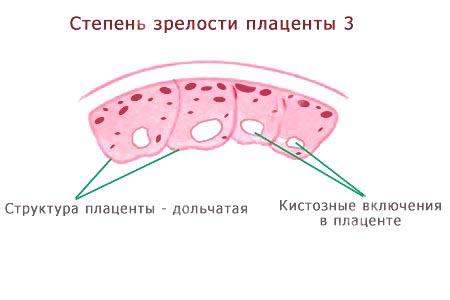 Доверьтесь своему доктору. Он проведёт дополнительные исследования, оценит состояние плода и при необходимости назначит соответствующее лечение.
Доверьтесь своему доктору. Он проведёт дополнительные исследования, оценит состояние плода и при необходимости назначит соответствующее лечение.
0, 1, 2, 3 по неделям беременности. Калькулятор
Степень зрелости плаценты – 0
Степень зрелости плаценты 0 (нулевая степень) в норме наблюдается до 30 недель беременности.
Хориальная мембрана при 0 степени представляет собой гладкую, прямую эхогенную линию, без выемок. Паренхима гомогенная (однородная), пониженной эхоплотности. Базальный слой не идентифицируется.
Нулевая степень зрелости плаценты
Степень зрелости плаценты – 1
Степень зрелости плаценты 1 (первая степень) в норме наблюдается с 27 по 34 неделю беременности. В основном первая степень отмечается на сроке с тридцатой по тридцать вторую неделю беременности.
Для 1 степени зрелости характерна слегка волнистая хориальная пластина. В ткани появляются случайно распределенные отдельные эхогенные включения различной формы. Базальный слой не идентифицируется.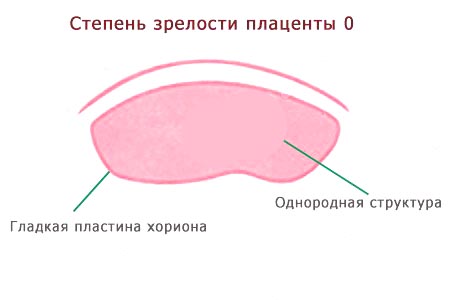
Первая степень зрелости плаценты
Степень зрелости плаценты – 2
Степень зрелости плаценты 2 (вторая степень) в норме наблюдается c 34 по 39 неделю беременности.
При 2 степени зрелости волнистость хориальной пластины увеличивается. На хориальной пластине появляются углубления, переходящие в перпендикулярные линейные уплотнения, но не доходящие до базального слоя. Видны множественные мелкие эхопозитивные включения в виде линий и точек, так называемая конфигурация «точка-тире-точка».
Вторая степень зрелости плаценты
Степень зрелости плаценты – 3
Третья степень зрелости плаценты наблюдается после 37 недели гестации и характерна для доношенной беременности. Наступление 3 стадии до 37 недель беременности обычно расценивают как преждевременное созревание – один из показателей фетоплацентарной недостаточности, что требует постоянного тщательного наблюдения за состоянием плода.
Для 3 степени зрелости характерным является выраженная извилистость хориальной мембраны, наличие углублений в хориальной пластине, переходящих в перпендикулярные линейные уплотнения, которые доходят до базального слоя. Плацента приобретает дольчатую структуру. Видная значительная кальцификация базальной пластинки (определяются округлые участки повышенной эхоплотности).
Плацента приобретает дольчатую структуру. Видная значительная кальцификация базальной пластинки (определяются округлые участки повышенной эхоплотности).
Третья степень зрелости плаценты
Несоответствие сроку беременности (преждевременное или раннее созревание плаценты)
В конце беременности наступает так называемое физиологическое старение плаценты, сопровождающееся уменьшением площади ее обменной поверхности, появлением участков отложения солей.
Если плацента изменяет структуру раньше положенного срока (например, появление 1 степени зрелости ранее 27 недели беременности, 2 степени до 32 недели, а 3 степени зрелости до 36 недели), то это свидетельствует о преждевременном ее созревании и говорят о преждевременном старении – один из показателей плацентарной недостаточности, что требует постоянного тщательного наблюдения за состоянием плода.
Причины преждевременного созревания плаценты различные: нарушением кровотока, внутриутробные инфекции, гестоз, кровянистые выделения в первом триместре беременности, гормональные нарушения (например, сахарный диабет мамы), угрозой прерывания беременности, беременность двойней и другие.
Поэтому, при определении 1, 2, 3 степени зрелости плаценты раннее установленных сроков, врач ультразвуковой диагностики в заключение исследования выносит диагноз «преждевременное созревание плаценты».
При выявлении преждевременного созревания плаценты лечащим врачом назначается комплексное лечение при помощи лекарственных препаратов по улучшению функции плаценты и профилактики гипоксии плода. Также рекомендуется допплерометрия (наблюдения за состоянием кровообращения в системе мать—плацента—плод), КТГ плода (кардиомониторное исследование) – в 33-34 недели и повторное УЗИ через 1 месяц. Назначаются препараты, улучшающие кровообращение в плаценте (например, курантил), витамины, отдых и полноценное питание.
Позднее созревание плаценты встречается реже и характерно чаще всего для врожденных пороков развития плода. Однако факторами риска могут являться наличие сахарного диабета у будущей мамы, резус-конфликт, курение во время беременности. При задержке созревания плаценты повышается риск рождения мертвого ребенка.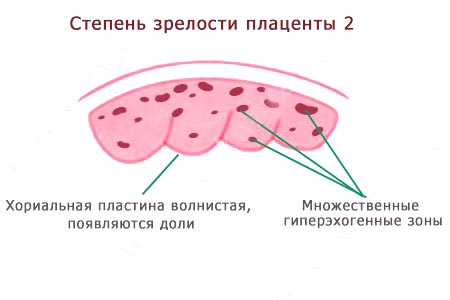
Определение степени зрелости плаценты играет важную роль в тактике ведения беременности. Однако, степень зрелости – фактор субъективный, устанавливается только при ультразвуковом исследовании и так как оценка данного показателя определяется «на глаз», то степень зрелости может отличаться у каждого врача-диагноста.
Критерии оценки зрелости плаценты очень субъективны и могут отличаться у каждого врача УЗ-диагностики.
Если имеет место незначительное несоответствие степени зрелости плаценты сроку беременности, то в этом нет ничего страшного. Скорее всего, раннее её созревание является особенностью беременной женщины. Если же старение плаценты началось гораздо раньше положенного срока, то это служит одним из важных диагностических признаков фетоплацентарной недостаточности.
При преждевременном старении проявляется уменьшение или увеличение толщины плаценты. Так «тонкая» плацента (менее 20 мм в 3 триместре беременности) характерна для позднего токсикоза, угрозы прерывания беременности, гипотрофии плода, в то время как при гемолитической болезни и сахарном диабете о плацентарной недостаточности свидетельствует «толстая» плацента (50 мм и более). Истончение или утолщение плаценты указывает на необходимость проведения лечебных мероприятий и требует повторного ультразвукового исследования.
Истончение или утолщение плаценты указывает на необходимость проведения лечебных мероприятий и требует повторного ультразвукового исследования.
Позднее созревание плаценты (длительная незрелость) наблюдается редко, чаще у беременных с сахарным диабетом, резус-конфликтом, а также при врожденных пороках развития плода. Задержка созревания плаценты приводит к тому, что она неправильно выполняет свои функции. Часто позднее созревание ведет к мертворождениям и умственной отсталости у плода.
таблица норм при беременности, что означает – созрела раньше срока, 0 степень
На протяжении второго и третьего триместра врачи при помощи ультразвуковой диагностики обязательно определяют степень зрелости плаценты. Далеко не каждая будущая мама представляет себе, о чем идет речь, а это очень важный показатель во время вынашивания малыша. В этой статье мы расскажем, что собой представляет степень зрелости «детского места» и какой она должна быть в норме на разных сроках.
Далеко не каждая будущая мама представляет себе, о чем идет речь, а это очень важный показатель во время вынашивания малыша. В этой статье мы расскажем, что собой представляет степень зрелости «детского места» и какой она должна быть в норме на разных сроках.
Что это такое?
Плацента — орган временный, ее задачи и функции ограничены сроком беременности, а после рождения малыша в «детском месте» нет никакой необходимости. Зато в период вынашивания малыша без плаценты никак не обойтись — она защищает ребенка, обеспечивает ему доступ кислорода, витаминов, воды, минеральных веществ, выводит в мамин организм продукты жизнедеятельности малыша, углекислый газ, вырабатывает множество гормонов, которые необходимы для вынашивания малыша и подготовки молочных желез женщины к грудному вскармливанию. 
К 12-14 неделе беременности молодая плацента начинает функционировать, но пока еще не имеет определенных очерченных форм. Окончательную форму плацента приобретает к 18-20 неделе беременности. Рост «детского места» продолжается до середины второго триместра, после этого плацента уже не растет.
К родам временный орган жизнеобеспечения растущего в утробе ребенка постепенно утрачивает свои функции, «стареет», вырабатывая ресурс.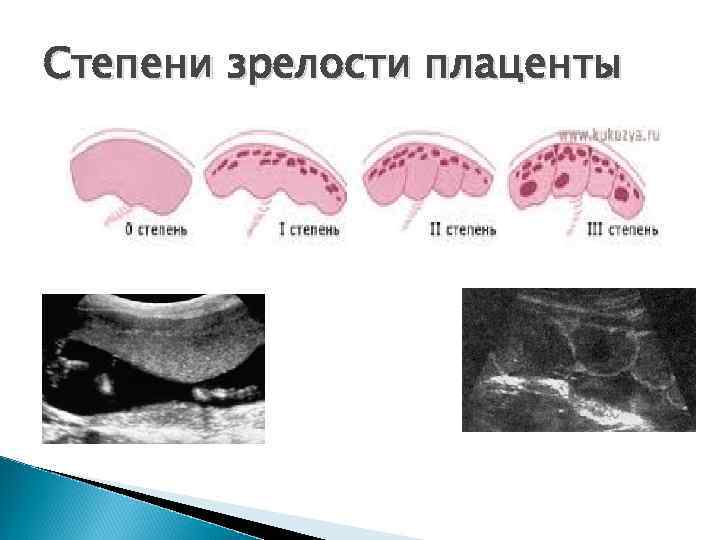 Процесс старения отслеживается врачами на УЗИ и оценивается в степенях зрелости. Если плацента по каким-то причинам начнет стареть раньше срока, малыш недополучит кислород и питание, его развитие может замедлиться, а гипоксия, связанная с нехваткой кислорода, может стать причиной необратимых процессов в его нервной системе, головном мозге, опорно-двигательном аппарате, а также стать причиной внутриутробной гибели малыша.
Процесс старения отслеживается врачами на УЗИ и оценивается в степенях зрелости. Если плацента по каким-то причинам начнет стареть раньше срока, малыш недополучит кислород и питание, его развитие может замедлиться, а гипоксия, связанная с нехваткой кислорода, может стать причиной необратимых процессов в его нервной системе, головном мозге, опорно-двигательном аппарате, а также стать причиной внутриутробной гибели малыша.
Молодая плацента постоянно наращивает толщину, разрастается новыми кровеносными сосудами. Во второй половине беременности рост прекращается, плацента некоторое время сохраняет свою толщину, а потом становится не губчатой, как вначале, а более плотной из-за отложения кальция. Функциональность «детского места» угасает также постепенно.
Степени зрелости
Существует четыре степени зрелости «детского места».
Первая степень зрелости означает, что в плаценте уже начались изменения — она перестала расти и наращивать толщину. На УЗИ такая плацента определяется как ровная, с незначительной волнообразной мембраной и единичными эхогенными включениями.
Вторая степень говорит о выраженных дегенеративных процессах.
Третья степень зрелости — это совершенно зрелая плацента. На УЗИ заметно ее визуальное разделение на доли, мембрана покрыта глубокими углублениями, структура меняется — отложения солей становятся более обширными, эхогенные области на мониторе УЗИ сливаются между собой в более обширные участки.
Кроме того, существуют промежуточные стадии. Например, женщине могут по результатам УЗИ поставить 0-1 степень зрелости плаценты или 1-2 степень. Это означает, что при визуальном исследовании доктор обнаружил признаки перехода одной базовой степени в другую, но окончательно этот переход еще не завершился.
Нормы
В норме до 30 недели беременности у женщины должна определяться нулевая степень зрелости «детского места». После 27 недели может определяться и 0-1 переходная степень, и ее будут считать условно нормальной, если нет других осложнений беременности, например, предлежания или краевого положения плаценты. До начала третьего триместра плацента при здоровой и нормальной беременности считается незрелой.
С 30 по 34 неделю обычно наблюдается первая степень зрелости «детского места». Если в этот период на УЗИ обнаруживается 1-2 степень, это расценивается, как однозначная патология — преждевременное старение. Динамика старения плаценты по неделям далее протекает более интенсивно. С 35 по 38 неделю у женщин в норме диагностируется вторая степень зрелости, а после 38 недели — переходная 2-3 степень.
Незадолго до родов на УЗИ может быть определена третья степень и это не должно быть основанием для переживаний — все процессы, если они своевременны, компенсируются в организме человека, а потому и зрелая плацента вполне справляется со своими обязанностями, если у женщины, к примеру, 39-40 неделя беременности.
Чтобы представить себе процесс старения плаценты при нормальной, не осложненной беременности более наглядно, посмотрите, как это выглядит в таблице.
Причины преждевременного старения
Если плацента стареет в установленные в акушерстве сроки, то старение называется физиологическим, то есть вполне естественным. Если же «детское место» созрело раньше срока, речь идет о преждевременном старении плаценты, и это очень тревожная патология, требующая обязательной медицинской помощи.
Если же «детское место» созрело раньше срока, речь идет о преждевременном старении плаценты, и это очень тревожная патология, требующая обязательной медицинской помощи.
Причины преждевременного созревания «детского места» могут быть различными. Чаще всего такое происходит у беременных, которые не смогли или не захотели хотя бы на время вынашивания плода расстаться с вредными привычками — курением и пристрастием к алкоголю. Также в группу риска по преждевременному созреванию плаценты попадают женщины, которым довелось перенести во время беременности инфекционные заболевания, в том числе ОРВИ и грипп.
Довольно часто плацента раньше срока стареет у женщин с отрицательным резус-фактором, вынашивающих своих резус-положительных малышей на фоне развившегося резус-конфликта, на что указывает титр антител в крови беременной.
В зоне риска и будущие мамы, которые подвергаются воздействию вредных веществ (бытовой химии, токсинов, красок и лаков, растворителей) или радиоактивному излучению. Врачи склонны считать, что стадии созревания плаценты протекают быстрее нормативных сроков у женщин, проживающих в крупных городах, где экологическая обстановка оставляет желать лучшего.
Фактор преждевременного старения нередко зависит от наследственности — дочь рискует повторить сценарий беременности своей матери. Причиной старения могут быть также некоторые аномалии строения самой плаценты, которые сформировались еще во время закладки этого временного органа.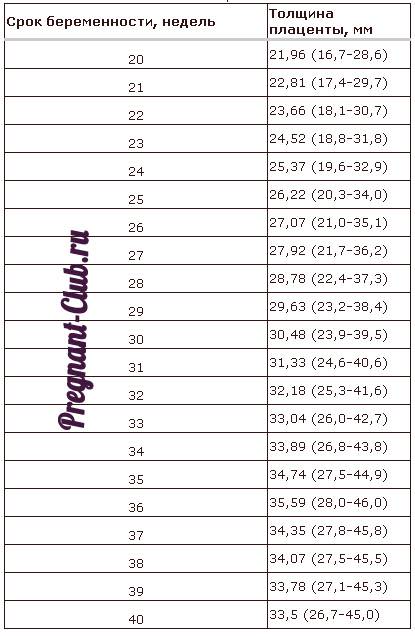
Также наиболее часто причинами преждевременного старения «детского места» считаются:
- гестоз, поздний токсикоз у будущей мамы;
- гипертония, перепады артериального давления;
- наличие фактов отслойки на разных сроках беременности, предлежание плаценты;
- многоплодная беременность;
- гормональные нарушения в организме будущей матери.
Причины патологической незрелости
Другое отклонение от нормы — патологическая незрелость плаценты. Она встречается значительно реже, но является не менее опасной ситуацией. Если у женщины 35 неделя беременности, а плацента остается незрелой и на УЗИ определяется 0 или 0-1 ее степень, то у врача есть все основания полагать, что такое «детское место» тоже не справляется с функциями, возложенными на него природой.
Незрелая плацента не может обеспечить растущему ребенку необходимое количество кислорода и питательных веществ, что приводит к рождению малыша с малым весом и задержкой развития, а также к гипоксии плода.
По мере роста малыша плацента и пуповина «перекачивают» все большее количество крови как от малыша с продуктами обмена веществ, так и к нему — обогащенной кислородом и витаминами. Незрелая плацента не может обеспечить бесперебойного кровотока в таком режиме. В ней задерживаются продукты жизнедеятельности крохи, а также углекислый газ, что негативно отражается на состоянии ребенка и на здоровье самой плаценты.
Прогнозы менее благоприятны, чем при преждевременном старении плаценты, поскольку не всегда медицина может повлиять на процессы созревания этого временного органа. Не исключается мертворождение, а также рождение детей с тяжелыми умственными отклонениями, парезами и параличами, нарушениями работы ЦНС из-за хронической гипоксии по время беременности.
Причины, которые могут привести к медленному созреванию и развитию плаценты, также довольно многообразны. Чаще всего такое нарушение встречается у женщин, которые еще до беременности страдали сахарным диабетом, а также у будущих мам, которым гестационный диабет диагностировали уже во время вынашивания малыша. Курящие и выпивающие беременные — вторые в списке вероятных пациенток с диагнозом «патологическая незрелость плаценты».
Никотин и алкоголь, особенно при систематическом употреблении, замедляют естественные процессы и подавляют выработку необходимых половых гормонов.
Незрелое «детское место» нередко диагностируется у женщин, которые вынашивают ребенка на фоне обострения хронических заболеваний печени, почек, сердца и сосудов. Нарушения гемостаза (свертываемости крови) также являются фактором риска.
Нарушения гемостаза (свертываемости крови) также являются фактором риска.
При обнаружении несозревания плаценты женщине обязательно рекомендуют пройти дополнительную диагностику, направленную на установление рисков рождения ребенка с хромосомными и генетическими патологиями, а также тяжелыми пороками развития внутренних органов. Именно такое «заторможенное» поведение плаценты свойственно беременностям больными и смертельно больными малышами.
Лечение
В первую очередь женщине следует успокоиться и взять себя в руки — нервные потрясения и длительный стресс создают не менее опасные предпосылки для патологий плаценты, чем контакт беременной с химикатами или вирусные недуги. При преждевременном старении «детского места» врач обычно принимает решение в пользу госпитализации будущей мамы в гинекологический стационар. Если срок беременности не превысил 36 недель, то ей будут проводить сохраняющую терапию и наблюдать за состоянием малыша.
Если срок беременности не превысил 36 недель, то ей будут проводить сохраняющую терапию и наблюдать за состоянием малыша.
Для лечения используются препараты, улучшающие маточно-плацентарный кровоток, а также спазмолитики, чтобы матка реже приходила в тонус. Также капельно вводятся витаминные препараты для малыша.
Женщине рекомендуют прием кислородных коктейлей. За состоянием плаценты внимательно наблюдают, повторяя УЗИ раз в несколько дней с обязательной оценкой скорости и интенсивности кровотока в маточно-плацентарных сосудах.
Если срок беременности на момент обнаружения преждевременного старения «детского места» превышает 36 недель, врач может предложить досрочное родоразрешение. Это будет зависеть от конкретной ситуации и степени зрелости. Иногда также принимается решение о госпитализации и ежедневном контроле за состоянием ребенка.
Будущей маме каждый день делают КТГ, чтобы убедиться, что у малыша не начались признаки кислородного голодания. При появлении таких признаков сохраняющая терапия отменяется и проводятся досрочные роды или кесарево сечение.
При появлении таких признаков сохраняющая терапия отменяется и проводятся досрочные роды или кесарево сечение.
При выявлении позднего созревания плаценты, если степень ее зрелости не дотягивает до нормы, женщине также рекомендуется стационарный режим. Лечение назначают после установления отсутствия пороков развития плода. Если генетические анализы или амниоцентез подтверждают, что малыш здоров, а на экспертном УЗИ не обнаруживается признаков аномалий строения его органов, то лечение проводят такое же, как при преждевременном старении — витамины, препараты для улучшения кровотока в матке и плаценте, а также легкие седативные препараты для успокоения.
Если ребенок оказывается больным, женщине предлагают прервать беременность. При отказе малыша сохраняют стандартной терапией.
Если причиной незрелости становятся гормональные нарушения, женщине может быть рекомендовано гормональное лечение, которое должно ускорить рост плацентарной ткани и расширение кровеносных сосудов в ней.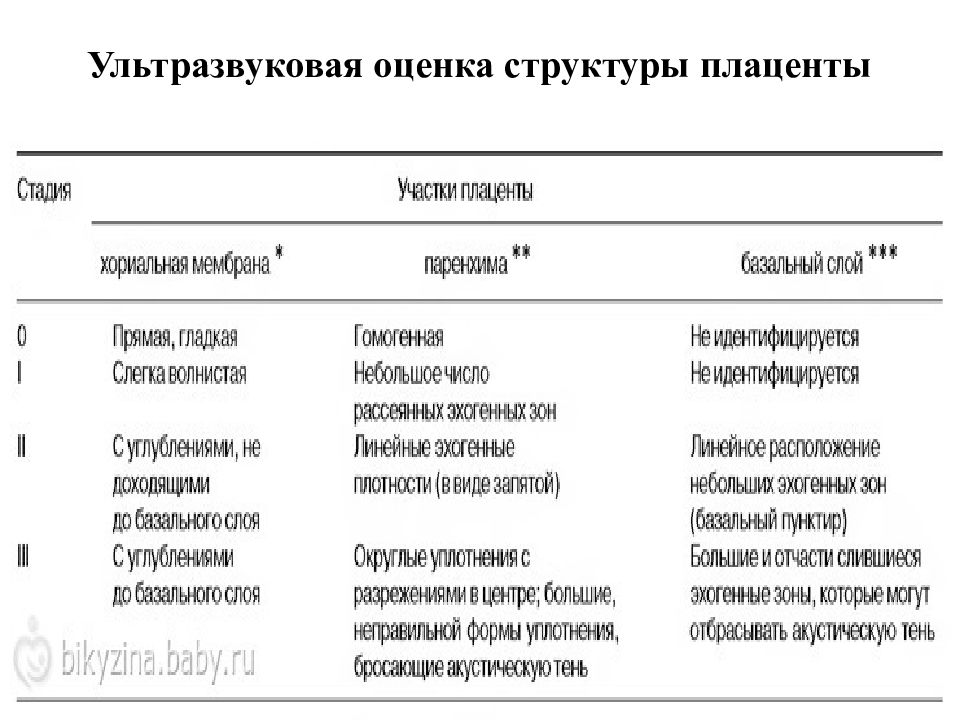
Конкретный препарат и дозировку определяет лечащий врач, желательно проходить такое лечение под контролем специалистов в условиях стационара.
Состояние малыша также контролируется посредством УЗИ, УЗДГ и КТГ (после 28-30 недели). При обнаружении признаков, указывающих на выраженный дискомфорт и страдания малыша в утробе, также принимается решение о досрочном родоразрешении для спасения детской жизни. Обычно проводят кесарево сечение и впоследствии выхаживают недоношенного ребенка с привлечением опытных неонатологов в условиях хорошо оснащенной реанимации.
Что считать отклонением?
Отклонением следует считать существенное отличие состояния плаценты беременной от нормативных значений. Если у женщины 30 неделя беременности, а УЗИ показало 0-1 степень зрелости «детского места», это условная норма. А если степень уже первая или первая-вторая, то женщине как можно скорее нужно отправиться в стационар, чтобы начать лечение.
Если у женщины 30 неделя беременности, а УЗИ показало 0-1 степень зрелости «детского места», это условная норма. А если степень уже первая или первая-вторая, то женщине как можно скорее нужно отправиться в стационар, чтобы начать лечение.
Самые строгие требования предъявляются к нормам на переходе 1-2 и 2-3 степеней. При 1-2 степени ребенок обычно еще не может жить самостоятельно или может родиться глубоко недоношенным. Спасая такого малыша из материнской утробы, где ему не хватает питания и кислорода, врачи рискуют, ведь кроха может не выжить из-за собственной незрелости и неготовности к жизни в этом мире.
Любое отклонение должен оценивать врач, а не сама беременная. Только доктор скажет, в какой ситуации и при каких сопутствующих диагнозах степень зрелости будет нормой или окажется патологией. Решение также принимается с учетом индивидуальных особенностей протекания гестационного срока.
Профилактика
Не всегда женщина может повлиять на процессы, протекающие в плаценте, но снизить риски ее преждевременного старения или патологической незрелости она может вполне. Для этого нужно отказаться от вредных привычек, не пить таблетки и сиропы без ведома врача, а также правильно и сбалансировано питаться и больше дышать свежим воздухом. Вредные химические вещества следует убрать подальше.
Для этого нужно отказаться от вредных привычек, не пить таблетки и сиропы без ведома врача, а также правильно и сбалансировано питаться и больше дышать свежим воздухом. Вредные химические вещества следует убрать подальше.
О степени зрелости плаценты по неделям смотрите в следующем видео.
Степени зрелости плаценты – на бэби.ру!
В утробе матери происходит активный рост и развитие плода. Поддерживает жизнедеятельность будущего малыша плацента — эмбриональный орган, формирующийся из зародышевых оболочек. Эти оболочки прилегают к стенке матки, формируют ворсинки, врастающие в слизистую. Так устанавливается прочная связь между плодом и материнским организмом, что необходимо для осуществления газообменной, трофической и выделительной, гормональной, защитной функций. Таким образом, формируется гемоплацентарный барьер. Эмбрион с плацентой связываются пуповиной.
Эти оболочки прилегают к стенке матки, формируют ворсинки, врастающие в слизистую. Так устанавливается прочная связь между плодом и материнским организмом, что необходимо для осуществления газообменной, трофической и выделительной, гормональной, защитной функций. Таким образом, формируется гемоплацентарный барьер. Эмбрион с плацентой связываются пуповиной.
Степень зрелости плаценты
Плацента — уникальный орган. Она формируется только в период беременности, принадлежит и организму матери, и организму плода. Является временным формированием, развивающимся поэтапно, а покидает организм через половые пути с рождением ребенка, точнее, в течение 10-50 минут после рождения (в зависимости от тактики ведения родов).
Зрелость плаценты
В ходе внутриутробного развития плацента претерпевает структурные изменения. Формулировка “старение плаценты” не вполне корректна, желательно говорить “созревание”.
Степень зрелости плаценты — это ультразвуковой параметр.
Проводится УЗ-исследование. Определяется локализация, оценивается площадь поверхности, масса и величина. Помимо плацентометрии оценивается и степень зрелости структуры. Эхографически принято выделять четыре степени. О созревании говорит визуализация включений повышенной акустической плотности. Если она акустически однородна, отсутствует дольчатость, субэпителиальная мембрана не утолщена, то говорят о 0 степени зрелости.
По мере прогрессии беременности степень зрелости возрастает, и перед родами может иметь и 0, и 3 степень.
Как созревает плацента?
В конце шестой недели беременности происходит вскрытие просвета спиральных артерий как следствие врастания цитотрофобласта в стенку сосудов отпадающей оболочки. Эти события и обусловливают возникновение маточно-плацентарного кровообращения.
К 13 неделе беременности заканчивается плацентация. На этот период в морфофукнциональном плане плацента не является зрелой — сформированы только основные элементы.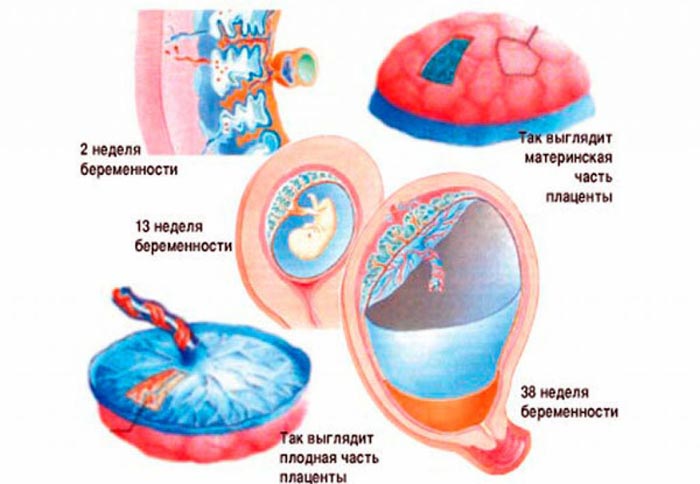 Структурная единица сформированной плаценты — котиледон. В зрелом последе таких чашеобразных образований насчитывают до 50.
Структурная единица сформированной плаценты — котиледон. В зрелом последе таких чашеобразных образований насчитывают до 50.
Функциональной зрелости достигает на 16 неделе — теперь она полноценно осуществляет газообменную, трофическую и выделительную, гормональную, протективную функции.
На втором триместре происходит фетализация плаценты. Развитие плода в этот период не догоняет рост плаценты. С 22 недели, напротив, рост плода опережает рост плаценты, и к 36 неделе детское место в норме успевает достигнуть полной зрелости.
К концу пренатального периода происходит т.н. старение плаценты, что свидетельствует о протекании гормонозависимых процессов в организме будущего малыша, которые индуцируют приобретение морфологической и функциональной зрелости его легочной ткани.
Зрелость плаценты по неделям
Плацента должна проходить этапы развития, соответствующие потребностям растущего плода, в противном случае она не смогла бы эффективно справляться с возлагаемыми на нее задачами.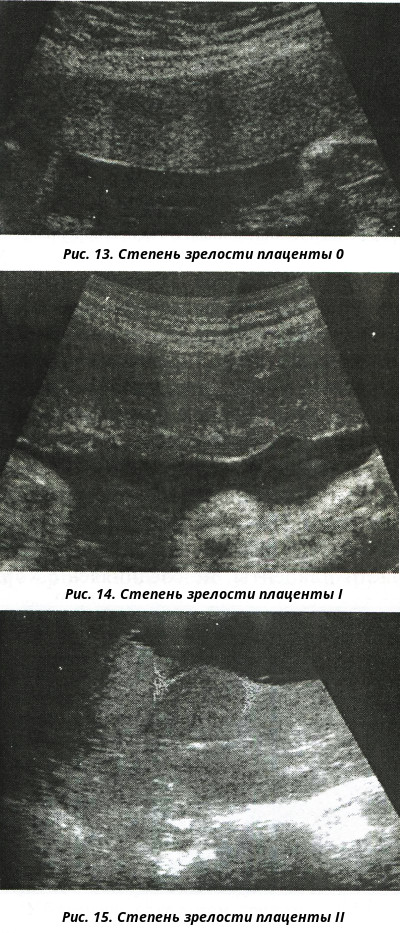 Как было отмечено выше, по мере созревания обнаруживаются соответствующие преобразования — размерные, структурные и т.д. Поговорим об этом детальнее.
Как было отмечено выше, по мере созревания обнаруживаются соответствующие преобразования — размерные, структурные и т.д. Поговорим об этом детальнее.
- Нулевая степень зрелости. Также ее называют этапом формирования, который длится со второй по тридцатую неделю. Ткань увеличивается в объеме, массе. Акустически однородна, отсутствует дольчатость, включений нет.
- Первая степень зрелости. Этап роста до 34 нед. Обнаруживаются эхогенные включения. Ткани уплотняются, хориальная пластина становится волнистой.
- Вторая степень зрелости. Период зрелости, до 39 нед. Усиливается извилистость хориальной пластины, акустическая плотность повышена, обнаруживаются множественные включения.
- Третья степень зрелости. С 37 нед. Площадь и объем уменьшаются. Хориальная пластина приобретает извилистость.
Читайте также:
Преждевременное созревание плаценты
Преждевременное созревание плаценты никаким образом не проявляет себя, но могут беспокоить заболевания, спровоцировавшие ПСП. То есть превалирует симптоматика основного заболевания. Возможно изменение двигательной активности плода — как учащение шевелений, так и их полное отсутствие.
То есть превалирует симптоматика основного заболевания. Возможно изменение двигательной активности плода — как учащение шевелений, так и их полное отсутствие.
Выявляют в ходе планового УЗ-исследования, как правило.
Провоцирующие факторы:
- Хронические заболевания репродуктивных органов, инфекционные заболевания (специфические генитальные, общие инфекционные).
- Экстрагенитальные патологии. Соматические, в частности, эндокринные нарушения.
- Изосерологическая несовместимость.
- Гестозы.
Преждевременное созревание плаценты всегда связано с усилением функционирования системы мать-плод, что провоцируется перечисленными выше факторами. Пусковыми так или иначе становятся неблагоприятные условия. Как бы банально ни прозвучало, это недостаточная или избыточная масса тела женщины, несбалансированное питание, употребление спиртного, табакокурение, причем не только во время вынашивания.
Если говорить о патогенезе, преждевременное созревание — компенсаторная реакция в ответ на фетоплацентарную недостаточность. Детское место растет и формируется более интенсивно в связи неблагоприятными факторами (нарушение трофической функции, например). В итоге уменьшаются функциональные возможности плаценты.
Вне зависимости от того, на каком сроке была выявлена фетоплацентарная недостаточность, акушер-гинеколог в тандеме с соответствующим профильным специалистом проводит активное лечение основной патологии. Также подключаются лекарственные средства, улучшающие кровоснабжение плода.
Позднее созревание
Позднее созревание плаценты может быть связано с наличием у матери заболеваний, особенно хронических. В ряде случаев имеют место генетические заболевания, что в итоге отразится в разного рода пороках развития. Впрочем, раннее созревание — явление более частое.
Таблица зрелости плаценты
Для наглядности представлена таблица, иллюстрирующая нормы степени зрелости плаценты по неделям:
| Степень зрелости плаценты | Недели беременности | ||||||||||||
| 0 | 28 | 29 | 30 | ||||||||||
| 0-I | 29 | 30 | |||||||||||
| I | 30 | 31 | 32 | ||||||||||
| I-II | 32 | 33 | 34 | ||||||||||
| II | 34 | 35 | 36 | 37 | 38 | 39 | 40 | ||||||
| II-III | 35 | 36 | 37 | 38 | 39 | 40 | |||||||
| III | 38 | 39 | 40 | ||||||||||
Читайте также:
Фото: Depositphotos
Степень зрелости плаценты в зависимости от срока беременности
Фото: UGCМногие женщины осведомлены о том, что во время беременности кроху в утробе защищает плацента. Однако детально о ее функциях знают не многие. Недоумение вызывает и термин «степень зрелости плаценты». Попробуем детально рассмотреть вопросы и ответить на них обывательским языком.
Однако детально о ее функциях знают не многие. Недоумение вызывает и термин «степень зрелости плаценты». Попробуем детально рассмотреть вопросы и ответить на них обывательским языком.
Внимание! Материал носит лишь ознакомительный характер. Не следует прибегать к описанным в нем методам лечения без предварительной консультации с врачом.
Что такое плацента
Прежде чем приступать к обсуждению вопроса зрелости, узнаем, что такое плацента. Возможно, вам о чем-то скажет название «послед». Также можете встретить термин «детское место».
Практика показывает, что, несмотря на обилие источников информации, не все женщины осведомлены о плаценте и ее функциях. Я лично не раз наблюдала, как удивляются будущие мамочки, узнав о том, что такое на самом деле послед.
Плацента — это орган, который находится непосредственно в матке. Это связующее звено между организмами матери и ребенка. Плацента есть не только у людей, но и также у некоторых животных.
Внешне плацента похожа на большую лепешку, пронизанную кровеносными сосудами. От нее отходит небольшой хвостик — пуповина. Циркуляция крови между матерью и ребенком проходит исключительно через этот отросток. Благодаря барьеру кровь малыша и матери никогда не соединяется.
Детское место формируется из ворсинок, которые потом превращаются в клетки и оболочки. Со стороны ребенка плацента гладкая, а со стороны женщины — бугристая. Изначально толщина органа составляет всего около 10 мм, а затем в процессе беременности он утолщается до 33 мм.
Фото: Цузмер А.М., Петришина О.Л. Биология. Человек и его здоровье. 9 класс. — 19-е изд., перераб. — М.: Просвещение, 1990. — 239 с.: UGCПлацента, фото которой выглядит не очень эстетично, выполняет сразу несколько функций. Среди них:
- Газообменная. Кислород, который получает мама, через орган доставляется к малышу. Обратно выходит углекислый газ.
- Трофическая. С помощью детского места ребенок получает воду, питательные вещества, витамины.

- Выделительная. Мочевина и другие продукты жизнедеятельности распадаются вследствие работы плаценты.
- Гормональная. Детское место также вырабатывает важные гормоны, необходимые для матери и ребенка.
- Защитная. Плацента выполняет роль иммунной системы. Однако этот орган не может защитить организм малыша от никотина, спирта, лекарств.
Женщины, которые уже рожали, знают, что плацента выходит из организма после малыша. Иногда процедура доставляет не слишком приятные ощущения.
Меня часто спрашивают: зачем врачи обязательно детально рассматривают плаценту? Доктора анализируют структуру, цвет последа. Это позволяет узнать, не страдал ли ребенок в матке, не было ли у него гипоксии и других отклонений в развитии. Также врачи проверяют, не остались ли кусочки последа в матке.
Фото: Матяш Н.Ю. Биология. 8 класс. — К.: Наука, 2016. — 288 с.: UGCТаким образом, понятно, что один из самых важных органов, которые формируются во время беременности, — это плацента. Строение органа позволяет ему выполнять все необходимые функции. Отклонение в деятельности, размере или структуре детского места могут привести к серьезным последствиям.
Строение органа позволяет ему выполнять все необходимые функции. Отклонение в деятельности, размере или структуре детского места могут привести к серьезным последствиям.
Степень зрелости плаценты: что это такое
Плацента формируется, меняется и растет вместе с крохой. Однако она защищает малыша далеко не сразу и не возникает при зачатии. Когда образуется плацента? Это происходит приблизительно на двенадцатой неделе беременности.
Созревание плаценты происходит в несколько этапов. Всего их четыре. Обозначаются степени цифрами, однако отсчет начинается не с единицы, а с ноля. Чем выше цифра, тем больше зрелость плаценты. Толщина плаценты по неделям также увеличивается в прогрессии. Определить степень зрелости плаценты по неделям можно с помощью ультразвукового исследования.
Рассмотрим каждую стадию подробнее, основываясь на статье моей коллеги Татьяны Смирновой:
Нулевая
Период зрелости плаценты с 12 по 30 неделю оценивается цифрой ноль.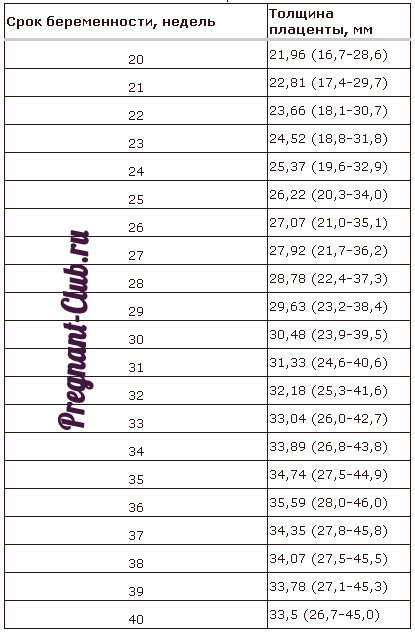 В степени зрелости эта цифра означает, что структура органа однородная, гладкая. В этот период еще пока тонкая плацента выполняет все свои функции.
В степени зрелости эта цифра означает, что структура органа однородная, гладкая. В этот период еще пока тонкая плацента выполняет все свои функции.
Первая
С тридцатой недели развитие плаценты переходит в первую стадию. Структура последа начинает немного видоизменяться. На плаценте можно увидеть небольшие образования кальция, она приобретает волнистые очертания. Первая степень длится примерно до 34-й недели развития плода.
Читайте также: Желтые выделения при беременности: есть ли повод для волнения
Вторая
На УЗИ можно увидеть, что структура плаценты стала еще более волнистой и плотной. На последе проявляются углубления, становятся заметнее кальциевые отложения и извилистые мембраны. Степень зрелости плаценты 2 может длиться до 37–39-й недели вынашивания малыша.
Фото: Зенкина В.Г., Сахоненко В.А., Зенкин И.С. Патоморфологические особенности плаценты на разных этапах гестации / Современные проблемы науки и образования. – 2019. – №6. : UGC
: UGCТретья
Приблизительно с 38-й недели начинается старение плаценты. Это естественный процесс. Период 3 степень зрелости плаценты продолжается до самых родов. В этот момент можно наблюдать крупную волнистость структуры последа, множество отложений, углублений. Толщина плаценты достигает максимума.
Такие сроки и структура плаценты по степеням считается нормой. В этом случае никакой опасности для женщины и малыша нет. Однако если плацента стареет раньше, чем положено, это несет серьезную угрозу здоровью крохи.
Чем опасно преждевременное старение плаценты
В моей практике бывало немало случаев, когда во время ультразвукового исследования врачи диагностировали у будущей мамы преждевременное старение плаценты. Обычно эта формулировка очень пугает женщину.
Действительно, ничего хорошего в таком диагнозе нет. Однако современная медицина умеет бороться и с такими случаями. Поэтому, если столкнулись с тем, что планета постарела раньше, не паникуйте.
Поэтому, если столкнулись с тем, что планета постарела раньше, не паникуйте.
Чем опасно преждевременное старение плаценты? Вы уже знаете, какие функции выполняет детское место. Поэтому при преждевременном старении плацента уже не может должным образом защищать ребенка, вырабатывает меньше гормонов.
Также в организм крохи поступает мало витаминов и питательных веществ. Однако главная опасность, которую несет в себе преждевременное старение, — это гипоксия плода. Если малышу не будет хватать воздуха, его развитие может быть нарушено.
Фото: Зенкина В.Г., Сахоненко В.А., Зенкин И.С. Патоморфологические особенности плаценты на разных этапах гестации /Современные проблемы науки и образования. – 2019. – №6.: UGCВажно вовремя заметить старение плаценты и начать действовать. В противном случае в самых тяжелых случаях малыш может даже погибнуть. Поэтому не пускайте ситуацию на самотек.
Почему наблюдается раннее старение плаценты? Исследуя данную тему, ученые Э. Айламазян, Е. Лапина и И.Кветной говорят о том, что наиболее важный аспект — это образ жизни будущей мамы. Если у женщины:
Лапина и И.Кветной говорят о том, что наиболее важный аспект — это образ жизни будущей мамы. Если у женщины:
- недостаток или избыток веса;
- много стрессовых ситуаций в жизни;
- мало активности;
- недостаток прогулок на свежем воздухе;
- есть вредные привычки, — то факторы риска старения последа повышаются.
Провоцируют развитие отклонений предыдущие аборты, вирусные инфекции, различные заболевания, диабет и поздний токсикоз беременных.
Не волнуйтесь, если отклонения от нормы составляют период около двух недель. Например, вторая степень зрелости на сроке в 32 недели считается не такой страшной. Обязательно стоит пройти доплерометрию, чтобы убедиться в нормальном функционировании кровеносной системы матери и малыша.
Фото: Савельева Г.М., Кулаков В.И. Акушерство. — М.: Медицина, 2000: UGCНаучный опыт моих коллег показывает, что наиболее опасным становится раннее старение плаценты третьей степени. В таком случае будущей маме стоит обязательно наблюдаться в стационаре. Часто последняя стадия развития плаценты на 36-й неделе беременности и позже вынуждает врачей идти на кесарево сечение.
Часто последняя стадия развития плаценты на 36-й неделе беременности и позже вынуждает врачей идти на кесарево сечение.
Я настоятельно рекомендую будущим мамам не пропускать процедуры обязательного ультразвукового исследования. Это никоим образом не вредит будущему малышу. Напротив, с помощью УЗИ можно выявить ряд проблем, в том числе и преждевременное старение плаценты.
Вы узнали, когда формируется плацента, какие важные функции выполняет орган и чем опасно его раннее старение. Внимательно следите за своим состоянием и регулярно посещайте врача. Будьте здоровы!
Читайте также: Беременность: ранние признаки, этапы, правила и запреты
Внимание! Материал носит лишь ознакомительный характер. Не следует прибегать к описанным в нем методам без предварительной консультации с врачом.
Автор: кандидат медицинских наук Анна Ивановна Тихомирова
Рецензент: кандидат медицинских наук, профессор Иван Георгиевич Максаков
Оригинал статьи: https://www. nur.kz/health/motherhood/1841581-stepen-zrelosti-placenty-v-zavisimosti-ot-sroka-beremennosti/
nur.kz/health/motherhood/1841581-stepen-zrelosti-placenty-v-zavisimosti-ot-sroka-beremennosti/
Степень зрелости плаценты по неделям в таблице
Плацента – это уникальный орган, связывающий плод и мать во время беременности. Именно через нее к малышу поступают все нужные вещества, поэтому от состояния плаценты зависит благополучный исход беременности. Одним из показателей работы плацентарного комплекса является степень его зрелости.
Что такое плацента?
В переводе с латинского placenta – пирог, лепешка. Такое название этот орган получил благодаря своей дисковидной приплюснутой форме. Он формируется только во время беременности, а после рождения малыша выводится вместе с плодовыми оболочками.
Функции плаценты:
- Дыхательная (поступление к малышу кислорода, выведение углекислого газа)
- Питательная (транспорт питательных веществ от матери к плоду)
- Выводящая (все продукты жизнедеятельности плода выводятся именно через плаценту)
- Барьерная (защита ребенка от вредных веществ в крови матери)
- Гормональная (плацента вырабатывает множество гормонов, позволяющих беременности развиваться)
Как развивается плацента?
Образование полноценного «детского места» начинается далеко не с первых дней беременности.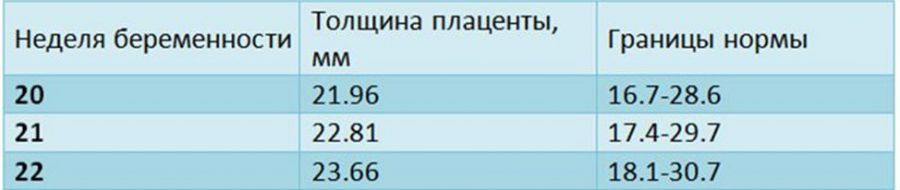 На сроке 4 недели все плодное яйцо окружено особой ворсинчатой тканью – хорионом. К 9-10 неделе формируется ранняя плацента – оставшиеся хориальные ворсинки, проникшие в верхний слой матки и соединившиеся с ее кровеносными сосудами. К концу беременности малыша и маму связывает полукилограммовый орган диаметром 15-20 см.
На сроке 4 недели все плодное яйцо окружено особой ворсинчатой тканью – хорионом. К 9-10 неделе формируется ранняя плацента – оставшиеся хориальные ворсинки, проникшие в верхний слой матки и соединившиеся с ее кровеносными сосудами. К концу беременности малыша и маму связывает полукилограммовый орган диаметром 15-20 см.
Вплоть до 32 недели беременности проницаемость плацентарной мембраны увеличивается. Растущий ребенок требует все больше кислорода и питательных веществ. Для поддержания его здоровья количество сосудов плаценты растет, а сама плацентарная мембрана становится тоньше. После этого срока плацента перестает развиваться, начинается ее старение.
Что такое старение плаценты?
После 33 недели в плацентарной ткани начинаются процессы «старения». Это абсолютная норма, предусмотренная природой. По одной из гипотез начало родов связано именно с максимальной зрелостью плаценты. Она к концу срока перестает выполнять свои функции, организм плода выбрасывает в кровь матери гормоны стресса, что запускает схватки.
Что значат степени зрелости плаценты?
Все изменения в зависимости от срока беременности определяют с помощью ультразвукового исследования (см. расчет срока беременности). Есть ряд специальных параметров, по которым врач выставляет ту или иную степень созревания плаценты.
- 0 степень – до 30 недели беременности
- I степень – на 27 – 36 неделе
- II степень – на 34 – 39 неделе
- III степень — после 36 недели беременности
Для определения стареющей плаценты специалист УЗИ оценивает ее толщину, наличие кист и отложения кальция. Несмотря на высокую информативность ультразвуковых методов, при определении зрелости имеет место избыточная диагностика.
До недавнего времени считалось, что преждевременно постаревшая плацента приводит к выкидышам, антенатальной гибели и рождению маловесных детей. После проведенных исследований эти предположения не подтвердились. Женщины с III степенью зрелости плаценты до 35 недель просто входят в группу повышенного внимания.
Таблица степеней зрелости плаценты по неделям
| Хориальная часть (прилегающая к плоду) | Структура плаценты | Наличие кальциевых отложений | |
| 0 степень (до 30 недели) | Абсолютно гладкая | Однородная | Практически нет |
| I степень (27-36 недель) | Волнистая | Небольшое количество уплотнений | Микроскопические |
| II степень (34-39 недель) | Есть углубления | Уплотнения | Видимые |
| III степень (после 36 недели) | Углубления достигают базальной мембраны | Кисты плаценты | Очень много |
Факторы, способствующие раннему старению плаценты
- Гипертония беременных
Чаще всего гестационная гипертония (повышенное давление при беременности) связано именно с функцией плаценты. По разным причинам послед формирует неполноценные сосуды, что влияет на состояние плода и матери. Беременная женщина может страдать от отеков, повышенного давления и даже преэклампсии. Малыш, находясь в утробе, не может получить достаточно кислорода через неполноценные артерии. Поэтому плацента работает на полную мощность, старея раньше срока.
Беременная женщина может страдать от отеков, повышенного давления и даже преэклампсии. Малыш, находясь в утробе, не может получить достаточно кислорода через неполноценные артерии. Поэтому плацента работает на полную мощность, старея раньше срока.
- Инфекции во время беременности
Любая инфекция во время беременности, включая банальную ОРВИ, заставляет плацентарную ткань активно работать. Она фильтрует материнскую кровь от вирусов, пропускает к ребенку защитные антитела и повышенные объемы кислорода, чтобы быстрее справиться с болезнью. Это вызывает ускоренное созревание и старение последа.
- Избыточное употребление кальция
Одним из главных признаков физиологических изменений «детского места» являются отложенния кальция. К концу беременности таких кальцинатов в плаценте становится все больше и больше. Если в организм будущей мамы поступает избыточное количество кальция (при бесконтрольном приеме больших доз витаминов, например), то плацентарная ткань постепенно замещается им, созревая раньше времени.
Прогноз при преждевременном старении плаценты
Всем беременным женщинам нужно запомнить важный факт: само по себе ранее созревание плаценты не грозит осложнениями для мамы и ребенка. Лишь при сочетании «старой» плаценты с другими признаками страдания плода можно говорить об угрозе здоровью. К этим признакам относятся:
- Нарушения маточно-плацентарного и плодово-плацентарного кровотока
- Выраженная внутриутробная задержка развития
- Выраженная гипертония беременных
- Признаки резус-конфликта у плода
- Сахарный диабет матери (декомпенсированный)
Все вышеперечисленные состояния опасны сами по себе, даже без признаков перезревшей плаценты. Поэтому требуют особого внимания, специального лечения, а иногда и срочного родоразрешения.
Чем опасна несозревшая плацента?
Плаценту, не достигшую к концу беременности II-III степени зрелости считают несозревшей. Такое состояние встречается редко, и чаще вызвано диагностическими ошибками.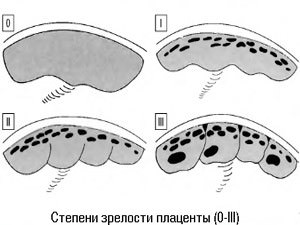 Например, при резус-конфликте матери и плода плацента может «отекать». Ее повышенная отечная гладкость на УЗИ выглядит как 0 степень зрелости. Поэтому сама по себе несозревшая плацента неопасна, но ее признаки зачастую маскируют серьезные осложнения беременности.
Например, при резус-конфликте матери и плода плацента может «отекать». Ее повышенная отечная гладкость на УЗИ выглядит как 0 степень зрелости. Поэтому сама по себе несозревшая плацента неопасна, но ее признаки зачастую маскируют серьезные осложнения беременности.
Дополнительные методы исследования
УЗИ с допплером
Оценить состояние плода по данным о степени зрелости плаценты невозможно. Поэтому главным критерием нормальной беременности являются нормальные показатели допплерографии. Этот метод, основанный на отражении ультразвуковых волн от разных биологических сред, позволяет оценить кровоток через плаценту. При нормально протекающей беременности после 20 недели происходит снижение сопротивления крови в сосудах, соединяющих матку, плаценту и плод. Это стабильное сопротивление обеспечивает поступление к ребенку кислорода и питательных веществ. Даже если плацентарная ткань на УЗИ выглядит старее, чем должна быть, хороший результат допплерографии отметает все опасения. И наоборот, плацента нормальной зрелости может не справляться со своей задачей, что тотчас же скажется на состоянии плода.
И наоборот, плацента нормальной зрелости может не справляться со своей задачей, что тотчас же скажется на состоянии плода.
Кардиотокография
КТГ – метод, позволяющий оценить состояние малыша в реальном времени, здесь и сейчас. Специальные датчики улавливают сердцебиение плода, подсчитывают его шевеления, регистрируют сокращения матки. Все это помогает определить минимальные нарушения в работе плаценты.
Если на УЗИ была определена преждевременно постаревшая плацента, то единственным способом узнать состояние ребенка будет допплерография и КТГ.
Как затормозить созревание плаценты?
Обычно после заключения врача УЗИ о преждевременном созревании плаценты, будущие мамы начинают беспокоиться и искать способы «омолодить» ее. Это бессмысленное и бесперспективное занятие. Всем беременным женщинам нужно знать следующие факты:
- Само по себе раннее созревание плаценты не несет угрозы маме и малышу.
- При определении зрелости последа очень часто возникают диагностические ошибки.

- Постаревшая плацента – повод провести допплерографию и КТГ, но не повод волноваться
- При нормальных показателях кровотока в плаценте и сердцебиения плода можно забыть о степени зрелости «детского места»
- При выраженной гипоксии малыша (по КТГ и допплеру) требуется либо наблюдение, либо лечение причины, либо экстренное родоразрешение
- Лекарств, замедляющих старение плаценты, не существует. Актовегин, курантил, пентоксифиллин, поливитамины и другие препараты не имеют никакой доказательной базы
Профилактика раннего старения плаценты
- Планирование беременности
- Отказ от курения, употребления спиртных напитков
- Умеренная физическая нагрузка, прогулки на свежем воздухе
- Своевременное проведение скринингов, допплерографии и КТГ
- Прием фолиевой кислоты
- Прием препаратов железа при анемии
- Избегание скоплений людей (с целью профилактики ОРВИ).
степень зрелости плаценты 0, 1, 2, 3 – что это значит, таблица по неделям
Содержание статьи:Детское место (плацента) является временным органом, который появляется у беременных женщин, а после рождения ребенка отторгается. Именно этот уникальный орган обеспечивает обмен веществ между матерью и ребенком. Как и все органы плацента проходит несколько физиологических периодов — формирование, созревание и старение. От своевременности этих этапов зависит общее состояние будущей матери и ее ребенка в утробе. Данная статья расскажет о том, какой должна быть плацента в норме на разных сроках вынашивания ребенка.
Именно этот уникальный орган обеспечивает обмен веществ между матерью и ребенком. Как и все органы плацента проходит несколько физиологических периодов — формирование, созревание и старение. От своевременности этих этапов зависит общее состояние будущей матери и ее ребенка в утробе. Данная статья расскажет о том, какой должна быть плацента в норме на разных сроках вынашивания ребенка.
Что означают степени зрелости плаценты?
Физиологический процесс, который сопутствует постепенному развитию детского места, называется созреванием плаценты. На протяжении всей беременности этот орган должен полностью удовлетворять нужды плода в питательных веществах и выводе токсинов из его развивающегося организма. Чтобы контролировать этот процесс медики ввели такое понятие как степень зрелости плаценты. Этот показатель помогает определить наличие патологий детского места, которые могут оказать негативное влияние на малыша. При нормальном протекании беременности различают четыре степени зрелости плаценты.
Нулевая степень зрелости плаценты
В норме нулевая степень зрелости детского места сохраняется до 30 недели беременности. На этом этапе орган имеет однородную структуру, прямую и гладкую мембрану, а женщина не испытывает проблем со здоровьем.
Первая степень зрелости плаценты
Этот этап наблюдается у беременных женщин на сроке 30-34 недель. Именно в этот период плацента перестает расти и начинает утолщать свои ткани. Хориальная мембрана плаценты становится слегка волнистой, а на УЗИ можно увидеть эхогенные вкрапления в ее структуре. Если на этом сроке УЗИ покажет вторую степень зрелости детского места, то беременной необходимо пролечиться. В таких случаях лечащий акушер-гинеколог назначает препараты, которые стимулируют кровообращение, а также витаминные комплексы. Важно чтобы будущая мамочка соблюдала правила здорового питания, это положительно влияет на состояние плаценты.
Вторая степень зрелости плаценты
На сроке 35-37 недель полноценная плацента должна находиться во второй степени зрелости. Этому этапу характерно истончение плаценты в некоторых местах, а также появление соляных отложений на ее поверхности. Углубления в мембране начинают увеличиваться, но еще не достигают базального слоя. При второй степени зрелости количество эхогенных включений в плаценте значительно увеличивается. Несмотря на такие изменения детское место продолжает выполнять свою работу и питать ребенка необходимыми веществами из материнского организма.
Этому этапу характерно истончение плаценты в некоторых местах, а также появление соляных отложений на ее поверхности. Углубления в мембране начинают увеличиваться, но еще не достигают базального слоя. При второй степени зрелости количество эхогенных включений в плаценте значительно увеличивается. Несмотря на такие изменения детское место продолжает выполнять свою работу и питать ребенка необходимыми веществами из материнского организма.
Третья степень зрелости плаценты
В норме данная степень зрелости наступает на 37 неделе беременности и продолжается непосредственно до самих родов. Детское место на этом этапе приобретает дольчатую структуру, эхегенные вкрапления увеличиваются и могут сливаться между своей, углубления проникают к базальному слою. Стоит отметить, что при физиологическом старении обменная площадь поверхности плаценты уменьшается.
Таблица степени зрелости плаценты по неделям (норма)
Увидеть наглядно степени зрелости по неделям можно в таблице. Там же указаны дополнительные характеристики плаценты в разных степенях зрелости.
Там же указаны дополнительные характеристики плаценты в разных степенях зрелости.
Преждевременное старение плаценты
Каждая степень созревания детского места сопровождается характерными признаками постепенного старения. Если они начинают проявляться в тот период, когда не должны проявиться, то это свидетельствует о том, что плацента преждевременно стареет. Например, в некоторых случаях к тридцатой неделе плацента приобретает первую степень зрелости. Это может быть вызвано негативным внешним воздействием, например, вирусное заболевание или вредные привычки у будущей мамы.
Определить степень созревания можно с помощью УЗИ. В случаях, когда на 32 недели плацента имеет вторую степень зрелости, то доктора берут ситуацию под усиленный контроль. Будущей маме назначают допплерографическое исследование, чтобы проконтролировать маточно-плацентарное кровообращение. Чаще всего такую беременную госпитализируют в стационар, где она проходит курс лечения, который направлен на снижение маточного тонуса. Чтобы предотвратить кислородное голодание ребенка в утробе врач рекомендует женщине в положении длительные пешие прогулки на свежем воздухе.
Чтобы предотвратить кислородное голодание ребенка в утробе врач рекомендует женщине в положении длительные пешие прогулки на свежем воздухе.
Наглядно увидеть ультразвуковую картину созревания плаценты можно в видео:
Плацента выполняет важную функцию в организме беременной женщины. Благодаря этому органу ребенок получает кислород и питательные вещества. Также детское место предотвращает интоксикацию плода, так как выводит все продукты жизнедеятельности малыша. При преждевременном старении плаценты женщине требуется соответствующее лечение, а если возникает угроза жизни плода, то врачи прибегают к вызову родовой деятельности.
Развитие плода: по месяцам беременности
Когда наступает беременность?
Фактически начало беременности — это первый день вашей последней менструации. Это называется сроком беременности или менструальным возрастом. Это примерно за две недели до фактического зачатия. Хотя это может показаться странным, дата первого дня последней менструации будет важной датой при определении срока родов. Ваш лечащий врач спросит вас об этом свидании и будет использовать его, чтобы выяснить, как долго вы находитесь в беременности.
Это называется сроком беременности или менструальным возрастом. Это примерно за две недели до фактического зачатия. Хотя это может показаться странным, дата первого дня последней менструации будет важной датой при определении срока родов. Ваш лечащий врач спросит вас об этом свидании и будет использовать его, чтобы выяснить, как долго вы находитесь в беременности.
Как происходит зачатие?
Каждый месяц ваше тело проходит репродуктивный цикл, который может закончиться одним из двух способов. У вас либо будет менструальный цикл, либо вы забеременеете. Этот цикл постоянно происходит в течение вашего репродуктивного возраста — от полового созревания в подростковом возрасте до менопаузы примерно в 50 лет.
В цикле, который заканчивается беременностью, есть несколько этапов. Сначала группа яйцеклеток (называемых ооцитами) готовится покинуть яичник для овуляции (выхода яйцеклетки).Яйца развиваются в небольших заполненных жидкостью кистах, называемых фолликулами. Думайте об этих фолликулах как о маленьких контейнерах для каждой незрелой яйцеклетки. Из этой группы яиц одно созреет и продолжит цикл. Затем этот фолликул подавляет все остальные фолликулы в группе. Остальные фолликулы перестают расти.
Из этой группы яиц одно созреет и продолжит цикл. Затем этот фолликул подавляет все остальные фолликулы в группе. Остальные фолликулы перестают расти.
Созревший фолликул открывается и высвобождает яйцеклетку из яичника. Это овуляция. Овуляция обычно происходит примерно за две недели до начала следующего менструального цикла.Обычно это середина вашего цикла.
После овуляции открытый (разорванный) фолликул развивается в структуру, называемую желтым телом. Это выделяет (высвобождает) гормоны прогестерон и эстроген. Прогестерон помогает подготовить эндометрий (слизистую оболочку матки). Эта подкладка — место, где оплодотворенная яйцеклетка оседает и развивается. Если вы не забеременеете во время цикла, эта подкладка — это то, что сбрасывается во время менструации.
В среднем оплодотворение происходит примерно через две недели после последней менструации.Когда сперма проникает в яйцеклетку, в белковой оболочке яйца происходят изменения, препятствующие проникновению других сперматозоидов.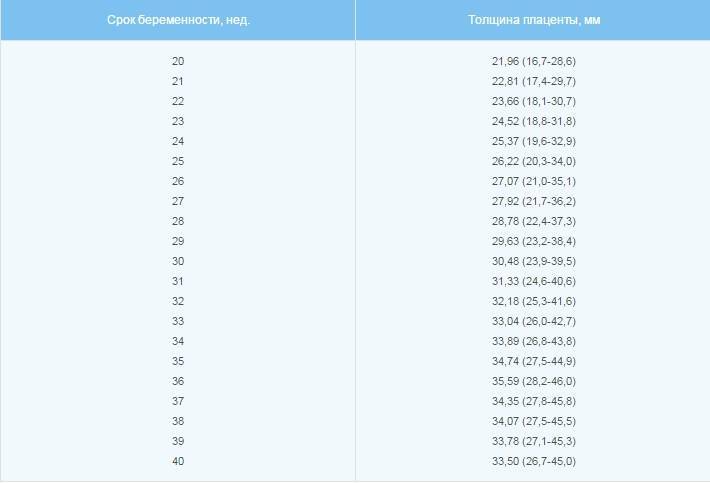
В момент оплодотворения генетический состав вашего ребенка, включая его пол, завершен. Пол вашего ребенка зависит от того, какой сперматозоид оплодотворяет яйцеклетку в момент зачатия. Как правило, у женщин генетическая комбинация XX, а у мужчин — XY. Женщины предоставляют каждой яйцеклетке X. Каждый сперматозоид может быть X или Y. Если оплодотворенная яйцеклетка и сперма представляют собой комбинацию X и Y, это мальчик.Если икс два, то это девочка.
Что происходит сразу после зачатия?
В течение 24 часов после оплодотворения яйцеклетка начинает быстро делиться на множество клеток. Он остается в маточной трубе примерно три дня после зачатия. Затем оплодотворенная яйцеклетка (теперь называемая бластоцитом) продолжает делиться, медленно проходя через маточную трубу в матку. Оказавшись там, его следующая задача — прикрепиться к эндометрию. Это называется имплантацией.
Однако перед имплантацией бластоцит вырывается из своего защитного покрытия.Когда бластоцит контактирует с эндометрием, эти два гормона обмениваются, чтобы помочь бластоциту прикрепиться. Некоторые женщины замечают кровянистые выделения (небольшое кровотечение) в течение одного или двух дней после имплантации. Это нормально, и вам не о чем беспокоиться. В этот момент эндометрий становится толще, а шейка матки (отверстие между маткой и родовыми путями) закрывается слизистой пробкой.
Некоторые женщины замечают кровянистые выделения (небольшое кровотечение) в течение одного или двух дней после имплантации. Это нормально, и вам не о чем беспокоиться. В этот момент эндометрий становится толще, а шейка матки (отверстие между маткой и родовыми путями) закрывается слизистой пробкой.
В течение трех недель клетки бластоцитов в конечном итоге образуют маленький шарик или эмбрион.К этому времени уже сформировались первые нервные клетки.
Ваш развивающийся плод уже претерпел несколько изменений в имени в первые несколько недель беременности. Обычно его называют эмбрионом от зачатия до восьмой недели развития. После восьмой недели он называется плодом до тех пор, пока не появится на свет.
Как рано я могу узнать, что беременна?
С момента зачатия в вашей крови будет присутствовать гормон хорионический гонадотропин человека (ХГЧ). Этот гормон создается клетками, образующими плаценту (источник пищи для растущего плода).Это также гормон, обнаруженный в тесте на беременность. Несмотря на то, что этот гормон присутствует с самого начала, ему нужно время, чтобы сформироваться в вашем теле. Обычно требуется от трех до четырех недель с первого дня последней менструации, чтобы уровень ХГЧ увеличился до уровня, достаточного для определения с помощью тестов на беременность.
Несмотря на то, что этот гормон присутствует с самого начала, ему нужно время, чтобы сформироваться в вашем теле. Обычно требуется от трех до четырех недель с первого дня последней менструации, чтобы уровень ХГЧ увеличился до уровня, достаточного для определения с помощью тестов на беременность.
Когда мне следует обратиться к поставщику медицинских услуг по поводу новой беременности?
Большинство поставщиков медицинских услуг заставят вас подождать, пока вы не придете на прием, пока у вас не будет положительного результата домашнего теста на беременность.Эти тесты будут очень точными, если по вашему телу будет циркулировать достаточное количество ХГЧ. Это может быть через несколько недель после зачатия. После положительного результата теста на беременность лучше всего позвонить своему лечащему врачу, чтобы записаться на прием.
Когда вы позвоните, ваш лечащий врач может спросить вас, принимаете ли вы витамины для беременных. Эти добавки содержат фолиевую кислоту.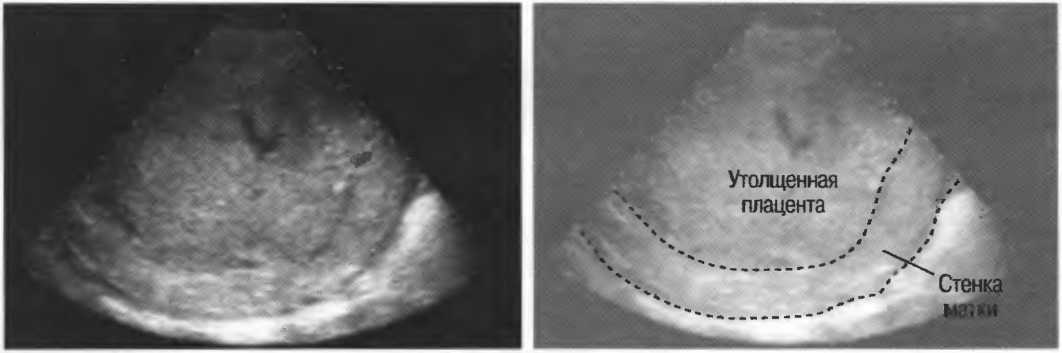 Важно, чтобы вы получали не менее 400 мкг фолиевой кислоты каждый день во время беременности, чтобы нервная трубка плода (в начале мозга и позвоночника) развивалась правильно.Многие медицинские работники рекомендуют вам принимать пренатальные витамины с фолиевой кислотой, даже если вы не беременны. Если вы не принимали витамины для беременных до беременности, ваш врач может попросить вас начать как можно раньше.
Важно, чтобы вы получали не менее 400 мкг фолиевой кислоты каждый день во время беременности, чтобы нервная трубка плода (в начале мозга и позвоночника) развивалась правильно.Многие медицинские работники рекомендуют вам принимать пренатальные витамины с фолиевой кислотой, даже если вы не беременны. Если вы не принимали витамины для беременных до беременности, ваш врач может попросить вас начать как можно раньше.
Каковы сроки развития плода?
Плод может сильно измениться на протяжении типичной беременности. Это время разделено на три этапа, называемых триместрами. Каждый триместр — это набор примерно из трех месяцев. Ваш лечащий врач, вероятно, расскажет вам о развитии плода в неделях.Итак, если у вас три месяца беременности, вам около 12 недель.
Вы увидите отчетливые изменения в организме плода и в себе в течение каждого триместра.
Традиционно мы думаем о беременности как о девятимесячном процессе. Однако так бывает не всегда. Срок доношенной беременности составляет 40 недель или 280 дней. В зависимости от того, на каком месяце вы беременны (некоторые короче, а некоторые длиннее) и на какой неделе вы родите, вы можете быть беременными в течение девяти или десяти месяцев. Это совершенно нормально и здорово.
В зависимости от того, на каком месяце вы беременны (некоторые короче, а некоторые длиннее) и на какой неделе вы родите, вы можете быть беременными в течение девяти или десяти месяцев. Это совершенно нормально и здорово.
Когда вы приближаетесь к концу беременности, вы можете услышать несколько названий категорий, касающихся начала родов. Эти ярлыки разделяют последние несколько недель беременности. Их также используют для выявления определенных осложнений у новорожденных. Младенцы, родившиеся в раннем сроке или ранее, могут иметь более высокий риск проблем с дыханием, слухом или обучением, чем дети, родившиеся на несколько недель позже в течение полного срока. Когда вы смотрите на эти ярлыки, важно знать, как они написаны.Сначала вы можете увидеть неделю (38), а затем вы увидите два числа, разделенных косой чертой (6/7). Это означает, сколько дней вы в настоящее время находитесь на гестационной неделе. Итак, если вы видите 38 6/7, это означает, что вы находитесь на 6-м дне вашей 38-й недели.
Последние несколько недель беременности делятся на следующие группы:
- Ранний семестр : от 37 0/7 недель до 38 6/7 недель.
- Полный семестр : от 39 0/7 недель до 40 6/7 недель.
- Поздний семестр : от 41 0/7 недель до 41 6/7 недель.
- Срок службы : 42 0/7 недель и далее.
Поговорите со своим врачом по любым вопросам, которые могут у вас возникнуть относительно гестационного возраста и срока родов.
Этапы роста по месяцам при беременности
Первый триместр
Первый триместр длится от зачатия до 12 недель. Обычно это первые три месяца беременности. В течение этого триместра оплодотворенная яйцеклетка превратится из небольшой группы клеток в плод, который начинает приобретать черты ребенка.
1 месяц (недели с 1 по 4)
По мере роста оплодотворенного яйца вокруг него образуется водонепроницаемая оболочка, постепенно заполняющаяся жидкостью. Это называется амниотическим мешком, и он помогает смягчить растущий эмбрион.
Это называется амниотическим мешком, и он помогает смягчить растущий эмбрион.
За это время также развивается плацента. Плацента — это круглый плоский орган, который передает питательные вещества от матери к плоду и отходы от плода. Считайте плаценту источником пищи для плода на протяжении всей беременности.
В эти первые несколько недель примитивное лицо примет форму с большими темными кругами вместо глаз. Развиваются рот, нижняя челюсть и горло. Клетки крови обретают форму, и начинается кровообращение. К концу четвертой недели крошечная «сердечная» трубка будет биться 65 раз в минуту.
К концу первого месяца плод вырастает примерно на 1/4 дюйма в длину — меньше рисового зерна.
Месяц 2 (недели с 5 по 8)
Черты лица продолжают развиваться.Каждое ухо начинается с небольшой складки кожи сбоку от головы. Формируются крошечные бутоны, которые со временем превращаются в ручки и ножки. Также формируются пальцы рук и ног и глаза.
Нервная трубка (головной, спинной и другие нервные ткани центральной нервной системы) в настоящее время хорошо сформирована. Начинают развиваться пищеварительный тракт и органы чувств. Кость начинает заменять хрящ.
В этом месте голова большая по сравнению с остальным телом. Примерно на 6 неделе обычно можно определить сердцебиение.
После 8-й недели медицинские работники называют его плодом, а не эмбрионом.
К концу второго месяца плод достигает около 1 дюйма в длину и весит около 1/30 унции.
Месяц 3 (недели с 9 по 12)
Руки, кисти, пальцы, стопы и пальцы ног полностью сформированы. На этом этапе плод начинает немного исследовать, делая такие вещи, как открывание и закрывание кулаков и рта. Начинают развиваться ногти на руках и ногах и формируются наружные уши.Под деснами формируются зачатки зубов. Половые органы тоже развиваются, но пол все еще сложно определить на УЗИ.
К концу третьего месяца плод полностью сформирован. Все органы и конечности (конечности) присутствуют и будут продолжать развиваться, чтобы стать функциональными. Кровеносная и мочевыделительная системы также работают, печень производит желчь.
Все органы и конечности (конечности) присутствуют и будут продолжать развиваться, чтобы стать функциональными. Кровеносная и мочевыделительная системы также работают, печень производит желчь.
В конце третьего месяца плод достигает 4 дюймов в длину и весит около 1 унции.
Поскольку произошло наиболее серьезное развитие, вероятность выкидыша значительно снижается через три месяца.
Второй триместр
Этот средний период беременности часто считается лучшей частью опыта. К этому времени утреннее недомогание, вероятно, исчезнет, а неприятные ощущения от ранней беременности исчезнут. В этом месяце у плода начнут развиваться черты лица. Вы также можете почувствовать движение, когда плод переворачивается и поворачивается в матке.В течение этого триместра многие люди узнают, будет ли их ребенок при рождении обозначен как мальчик или девочка. Обычно это делается во время анатомического сканирования (ультразвукового исследования, которое проверяет физическое развитие) около 20 недель.
4 месяц (с 13 по 16 недели)
Сердцебиение плода теперь можно слышать с помощью прибора, называемого допплером. Пальцы рук и ног четко очерчены. Формируются веки, брови, ресницы, ногти и волосы. Зубы и кости уплотняются. Плод может даже сосать большой палец, зевать, потягиваться и гримасничать.
Нервная система начинает работать. Репродуктивные органы и гениталии теперь полностью развиты, и ваш врач может увидеть на УЗИ, будет ли плод при рождении определен как мужской или женский.
К концу четвертого месяца плод достигает 6 дюймов в длину и весит около 4 унций.
Месяц 5 (недели с 17 по 20)
На этой стадии вы можете почувствовать, как плод двигается. Плод развивает мышцы и тренирует их.Это первое движение называется ускорением и может ощущаться как трепетание.
На голове начинают расти волосы. Плечи, спина и виски покрыты мягкими тонкими волосами, называемыми лануго. Эти волосы защищают плод и обычно выпадают в конце первой недели жизни вашего ребенка.
Кожа покрыта белесым налетом, называемым vernix caseosa. Считается, что это «сырное» вещество защищает кожу плода от длительного воздействия околоплодных вод. Этот налет сбрасывается незадолго до рождения.
К концу пятого месяца плод достигает 10 дюймов в длину и весит от 1/2 до 1 фунта.
6 месяц (с 21 по 24 недели)
Если бы вы могли заглянуть внутрь матки прямо сейчас, вы бы увидели, что кожа плода красноватого цвета, морщинистая, а сквозь полупрозрачную кожу видны вены. Видны отпечатки пальцев рук и ног. На этом этапе веки начинают раздвигаться, а глаза открываются.
Плод реагирует на звуки движением или учащением пульса.Вы можете заметить подергивание, если плод икнет.
При преждевременном рождении ваш ребенок может выжить после 23-й недели при интенсивной терапии.
К концу шестого месяца плод достигает 12 дюймов в длину и весит около 2 фунтов.
7 месяц (с 25 по 28 недели)
Плод продолжает созревать и накапливать жировые отложения.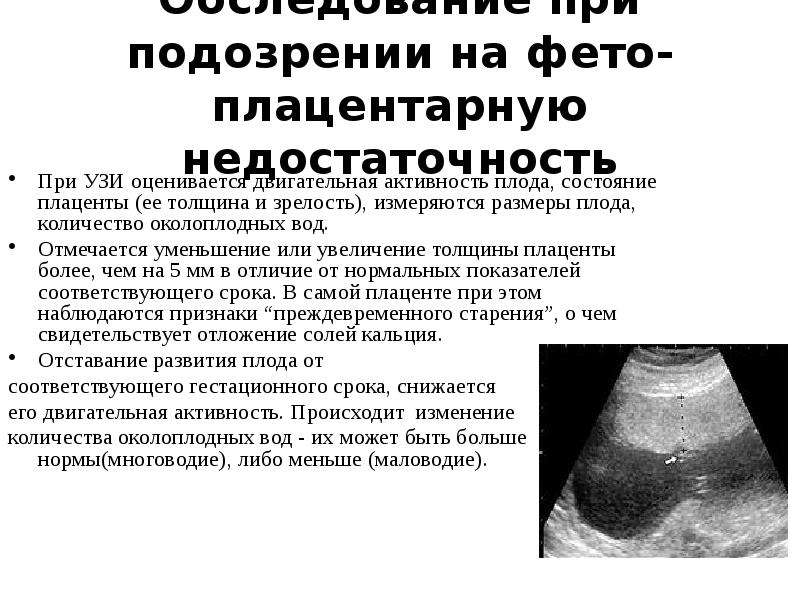 К этому моменту слух полностью развит. Плод часто меняет положение и реагирует на раздражители, включая звук, боль и свет.Амниотическая жидкость начинает уменьшаться.
К этому моменту слух полностью развит. Плод часто меняет положение и реагирует на раздражители, включая звук, боль и свет.Амниотическая жидкость начинает уменьшаться.
В случае преждевременного рождения ваш ребенок, скорее всего, выживет после седьмого месяца.
В конце седьмого месяца плод достигает 14 дюймов в длину и весит от 2 до 4 фунтов.
Третий триместр
Это последняя часть вашей беременности. У вас может возникнуть соблазн начать обратный отсчет до срока родов и надеяться, что он наступит раньше, но каждая неделя этого заключительного этапа развития помогает плоду подготовиться к рождению.В течение третьего триместра плод быстро набирает вес, добавляя жировые отложения, которые помогут после рождения.
Помните, хотя популярная культура упоминает только девять месяцев беременности, на самом деле вы можете быть беременны в течение 10 месяцев. Типичная доношенная беременность составляет 40 недель, что может привести к десятому месяцу беременности. Также возможно, что вы можете просрочить срок на неделю или две (41 или 42 недели). Ваш лечащий врач будет внимательно следить за вами по мере приближения срока родов. Если у вас истечет срок родов и у вас не начнутся самопроизвольные роды, ваш поставщик может побудить вас.Это означает, что лекарства будут использоваться для того, чтобы у вас начались схватки и роды. Обязательно поговорите со своим врачом о своем плане родов в этом триместре.
Также возможно, что вы можете просрочить срок на неделю или две (41 или 42 недели). Ваш лечащий врач будет внимательно следить за вами по мере приближения срока родов. Если у вас истечет срок родов и у вас не начнутся самопроизвольные роды, ваш поставщик может побудить вас.Это означает, что лекарства будут использоваться для того, чтобы у вас начались схватки и роды. Обязательно поговорите со своим врачом о своем плане родов в этом триместре.
8 месяц (недели с 29 по 32)
Плод продолжает созревать и накапливать жировые отложения. Вы можете заметить больше ударов ногами. Мозг в это время быстро развивается, и плод может видеть и слышать. Большинство внутренних систем хорошо развиты, но легкие еще могут быть незрелыми.
Плод около 18 дюймов в длину и весит до 5 фунтов.
9 месяц (с 33 по 36 недели)
На этой стадии плод продолжает расти и созревать. К этому моменту легкие почти полностью развиты.
У плода координированные рефлексы, он может моргать, закрывать глаза, поворачивать голову, крепко сжимать руки и реагировать на звуки, свет и прикосновения.
Плод составляет от 17 до 19 дюймов в длину и весит от 5 ½ фунтов до 6 ½ фунтов.
10 месяц (с 37 по 40 недели)
В этот последний месяц у вас могут начаться роды в любое время.Вы можете заметить, что движения меньше, потому что места мало. На этом этапе положение плода могло измениться, чтобы подготовиться к рождению. В идеале это должна быть голова в матке. Вы можете чувствовать себя очень некомфортно в этот последний отрезок времени, когда плод опускается в ваш таз и готовится к рождению.
Теперь ваш ребенок готов познакомиться с миром. Они от 18 до 20 дюймов в длину и весят около 7 фунтов.
Старение или кальциноз плаценты
Что означает «стареющая плацента» или «кальцификация плаценты»?
Кальцификация плаценты — это медицинский термин, обозначающий некоторые изменения, происходящие с плацентой по мере прогрессирования беременности. Многие исследователи считают кальцификацию плаценты нормальным процессом старения, а не изменением, связанным с болезнью или недомоганием.
Плацента обычно описывается как имеющая четыре степени: от 0 (наиболее незрелая) до III (наиболее зрелая).
Все плаценты начинаются с нулевой степени на ранних сроках беременности. Изменения можно увидеть начиная с 12 недель. По мере развития беременности плацента созревает и кальцифицируется.
Он подразделяется на следующие классы на разных стадиях беременности, примерно в следующие сроки:
Как измеряется кальцификация или возраст плаценты?
Существует некоторая неуверенность в том, можно ли точно измерить изменения в плаценте, поскольку объективная оценка плаценты может быть затруднена.Многое зависит от интерпретации ультразвуковых изображений врачом УЗИ. Также могут возникнуть некоторые различия, поскольку это зависит от того, как врач интерпретирует результат.Как стареющая или кальцинированная плацента повлияет на мои роды?
Трудно сказать, как стареющая плацента влияет на роды. Эксперты, похоже, расходятся во мнениях о значении кальцинированной плаценты при родах из-за отсутствия убедительных доказательств.
Некоторые изменения плаценты на поздних сроках беременности считаются нормальным явлением во время беременности и не вызывают беспокойства.Однако в случаях, когда изменения происходят раньше, чем ожидалось, существуют некоторые разногласия относительно их значимости.
Некоторые риски, которые, как известно, связаны с кальцификацией плаценты на каждом этапе беременности, перечислены ниже.
Изменения между 28 и 36 неделями
Одно исследование показывает, что женщины с высоким риском беременности, у которых кальцинированная плацента развивается между 28 и 34 неделями, нуждаются в более тщательном наблюдении. Некоторые примеры беременностей с высоким риском включают беременность, осложненную предлежанием плаценты, диабетом, высоким кровяным давлением или тяжелой анемией.
Изменения с 36 недель
Одно исследование показало, что наличие плаценты III степени на 36 неделе связано с повышенным риском связанных с беременностью высоких артериальное давление и наличие ребенка с низкой массой тела при рождении.

Следовательно, ультразвуковое сканирование, показывающее кальцификацию плаценты на 36 неделе, может помочь в выявлении беременностей с высоким риском.
Изменения с 37 до 42 недель
Кальцифицированная плацента III степени, начиная с 37 недель и старше, встречается примерно в 20-40% нормальных беременностей. Однако считается, что это не имеет большого клинического значения.
Эффекты кальцинированной плаценты, вероятно, необходимо оценивать в индивидуальном порядке, в зависимости от:
- насколько рано видны изменения
- насколько они серьезны
- , будь то беременность с высоким риском или нет
- мнение вашего врача
Вредно ли для моего ребенка, если моя плацента кальцинируется или стареет слишком рано?
Преждевременный кальциноз плаценты может быть вредным для ребенка в утробе матери, но это также зависит от степени и стадии беременности. Некоторые исследования показывают, что кальцификация плаценты до 32 недель беременности может привести к рождению детей с низкой массой тела, младенцев с низкой оценкой по шкале Апгар и даже к мертворождению.
Некоторые исследования показали, что наличие плаценты II степени в возрасте от 30 до 34 недель может предсказать, что ребенок родится с низкой массой тела. Но это только среди женщин, курящих во время беременности.
Что я могу сделать, чтобы предотвратить преждевременную кальцификацию или старение плаценты?
Точные причины старения плаценты до сих пор не очень ясны, поэтому трудно сказать, что могло бы предотвратить это.Однако некоторые исследования показывают, что кальцификация плаценты более вероятна у:- более молодых женщин
- при первой беременности
- курящих женщин во время беременности
Ваш врач будет следить за вашим здоровьем на протяжении всей беременности. Так что убедитесь, что вы не пропустите ни один дородовый осмотр и прием на УЗИ.
यह लेख हिंदी में पढ़ें!
Подробнее на:
Список литературы
Абрамович Я.С., Шейнер Э.2007. Внутриутробная визуализация плаценты: важность при заболеваниях беременности. Плацента. 21 (Дополнение A): S14 – S22.
Плацента. 21 (Дополнение A): S14 – S22.Bricker L, Neilson JP, Dowswell T. Обычное ультразвуковое исследование на поздних сроках беременности (после 24 недель беременности). Кокрановская база данных систематических обзоров 2008 г., выпуск 4. Ст. №: CD001451. DOI: 10.1002 / 14651858.CD001451.pub3.
Чен К. Х., Чен Л. Р., Ли Ю. Х. 2012. Роль преждевременной кальцификации плаценты при беременности с высоким риском как предиктор плохого маточно-плацентарного кровотока и неблагоприятного исхода беременности.Ультразвук Med Biol. 38 (6): 1011-8. Онлайн первый 3 апр.
Граннум PA, Berkowitz RL, Hobbins JC. 1979. Ультразвуковые изменения созревающей плаценты и их связь с легочной зрелостью плода. Американский журнал акушерства и гинекологии. 133: 915–22.
Hill LM. Брекл Р. Рагоззино MW. Вольфграм КР. О’Брайен ПК. Плацентация 3 степени: частота и исходы новорожденных. Акушерство и гинекология. 61 (6): 728-32, июнь 1983 г., Аннотация. Полный текст доступен для стипендиатов, членов и стажеров.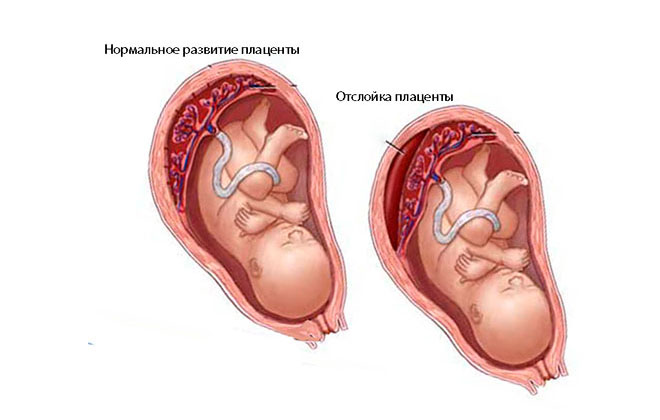
Хиллз Д. Ирвин, Джорджия. Так С. 1984. Распределение плацентарной степени у беременных с высоким риском. AJR. Американский журнал рентгенологии. 143 (5): 1011-3.
Каззи Г.М., Гросс Т.Л. и др. 1984. Взаимосвязь степени плаценты, зрелости легких плода и неонатального исхода при нормальной и осложненной беременности. Am J Obstet Gynecol.; 148 (1): 54-8
McKenna D, Tharmaratnam S, Mahsud S, 2005. Ультразвуковые доказательства кальцификации плаценты на 36 неделе беременности: исходы для матери и плода.Acta Obstet Gynecol Scand. 84 (1): 7-10.
Miller JM Jr, Brown HL, Kissling GA, Gabert HA. Взаимосвязь степени плаценты с размером и ростом плода в срок. Am J Perinatol 1988; 5: 19–21.
Моран М., Райан Дж., Хиггинс М. и др. 2011. Плохая договоренность между операторами о классификации плаценты. J Obstet Gynaecol. 31 (1): 24-8.
Гордый Дж., Грант А.М. 1987. Оценка плаценты в третьем триместре с помощью УЗИ как тест благополучия плода. BMJ 294: 1641–4.
Smith R, Maiti K, Aitken RJ.2013. Необъяснимые дородовые мертворождения: следствие старения плаценты? Плацента. 34 (4): 310-3. На сайте впервые 26 февраля
Шимановски К., Хмай-Вежховска К., Флорек Э. и др. 2007. Обнаруживает ли кальциноз плаценты только курение матери? Przegl Lek. 2007; 64 (10): 879-81.
Walker MG, Hindmarsh PC, Geary M и др. 2010. Сонографическое созревание плаценты через 30–34 недели не связано с маркерами плацентарной недостаточности во втором триместре при беременностях с низким риском.J Obstet Gynaecol. 32 (12): 1134.– 39.
Yin TT, Loughna P, Ong SS и др. 2009. Отсутствует корреляция между оценкой плаценты при УЗИ на 31-34 неделе беременности и суррогатной оценкой функции органа в срок, полученной стереологическим анализом. Плацента. 30 (8): 726-30. Онлайн первые 12 июн
Толщина плаценты и ее корреляция с гестационным возрастом и параметрами роста плода — поперечное ультразвуковое исследование
J Clin Diagn Res. 2012 Dec; 6 (10): 1732–1735.
2012 Dec; 6 (10): 1732–1735.
T Karthikeyan
1 Доцент кафедры анатомии Медицинского колледжа Шри Баладжи, Университет Бхарата, Ченнаи, Тамилнад, Индия
Рамеш Кумар Субраманиам
2 Профессор Университета Рамакатомира и ХОД, , Ченнаи, Индия
WMS Johnson
3 Профессор кафедры анатомии, Медицинский колледж Шри Баладжи, Университет Бхарата, Ченнаи, Тамилнаду, Индия
К. Прабху
4 Доцент кафедры анатомии Шри Баладжи Медицинский колледж, Университет Бхарата, Ченнаи, Тамилнад, Индия
1 Доцент, кафедра анатомии, Медицинский колледж Шри Баладжи, Университет Бхарата, Ченнаи, Тамилнаду, Индия
2 Профессор и HOD, кафедра анатомии, Шри Университет Рамачандры, Ченнаи, Индия
3 Профессор кафедры анатомии, Sree Balaji Medical Co llege, Университет Бхарата, Ченнаи, Тамилнад, Индия
4 Доцент кафедры анатомии, Медицинский колледж Шри Баладжи, Университет Бхарата, Ченнаи, Тамилнаду, Индия
НАЗВАНИЕ, АДРЕС, ЭЛЕКТРОННАЯ ПОЧТА ИДЕНТИФИКАЦИЯ АВТОРА: Д-Р . Т. Картикеян, доцент кафедры анатомии, 5А, колония ВВ, 2-я улица, Бриндхаваннагар, Адамбаккам, Ченнаи-600088, Тамилнаду, Индия. Телефон:
Т. Картикеян, доцент кафедры анатомии, 5А, колония ВВ, 2-я улица, Бриндхаваннагар, Адамбаккам, Ченнаи-600088, Тамилнаду, Индия. Телефон:50848 Эл. Почта: moc.liamg@xineohpihtrakt
Поступила в редакцию 7 июля 2012 г .; Изменения запрошены 11 ноября 2012 г .; Принята к печати 24 ноября 2012 г.
Copyright © 2012 Журнал клинических и диагностических исследований Эта статья цитируется в других статьях в PMC.Abstract
Предпосылки
Гестационный возраст (GA) часто завышается или занижается, поскольку стандартная оценка гестации основана на последнем менструальном периоде (LMP) и ультразвуковом исследовании (USG).Многие люди не знают о своем LMP и нерегулярных менструациях, и УЗИ обязательно будет иметь предвзятость, что создает трудности при оценке GA.
Цель
Это исследование было направлено на оценку PT (толщины плаценты) и изучение взаимосвязи между PT и параметрами роста плода при нормальных одноплодных беременностях.
Материалы и методы
Двести одиннадцать беременных женщин были набраны для перекрестного проспективного исследования. Беременность длилась от 11 до 40 недель и не была осложнена ни материнскими, ни внутриутробными заболеваниями.Бипариетальный диаметр (BPD), окружность живота (AC), окружность головы (HC), длина бедра (FL) и PT были измерены с помощью УЗИ с использованием датчика 3,5 МГц.
Беременность длилась от 11 до 40 недель и не была осложнена ни материнскими, ни внутриутробными заболеваниями.Бипариетальный диаметр (BPD), окружность живота (AC), окружность головы (HC), длина бедра (FL) и PT были измерены с помощью УЗИ с использованием датчика 3,5 МГц.
Результаты
Максимальное среднее значение PT в 1-м, 2-м, 3-м и комбинированном триместрах было 16,5 мм, 23,78 мм, 35,81 мм и 28,49 мм соответственно. Корреляция между PT и другими параметрами плода была исследована с помощью корреляционного анализа Пирсона. Значения были выражены как среднее + стандартное отклонение.Статистические тесты были двусторонними, со значением p <0,01, что указывало на статистическую значимость. Между PT и GA была сильная положительная корреляция, при этом значения коэффициента корреляции для 1, 2 и 3 триместров были r = 0,609, r = 0,812 и r = 0,814 соответственно. Также наблюдалась значимая положительная корреляция между PT и BPD, AC, FL, ABC, HC и FW. Математические отношения между PT и GA, BPD, AC, FL, ABC, HC, FW были получены с помощью регрессионного анализа. Полученное уравнение регрессии: (x — 22,92) = (0,3604) (w-27,86446) + (1,0256) (y-1,1678) + (0,0015) (z-216,2841) + (0,1047) (t-43,1555) + ( 0,027) (u.192.79000) + (0,0042) (v-60.3725), где x = GA в неделях, w = PT в мм, y = FW в кг, z = HC в мм, t = FL в мм, u = AC в мм и v = BPD в мм.
Полученное уравнение регрессии: (x — 22,92) = (0,3604) (w-27,86446) + (1,0256) (y-1,1678) + (0,0015) (z-216,2841) + (0,1047) (t-43,1555) + ( 0,027) (u.192.79000) + (0,0042) (v-60.3725), где x = GA в неделях, w = PT в мм, y = FW в кг, z = HC в мм, t = FL в мм, u = AC в мм и v = BPD в мм.
Заключение
Мы пришли к выводу, что PT можно использовать в качестве предиктора GA. Субнормальный PT для соответствующего GA следует оценивать для любого болезненного состояния. Таким образом, измерение PT должно проводиться регулярно во время акушерского УЗИ.
Ключевые слова: Гестационный возраст, Толщина плаценты, УЗИ, Последняя менструация
Введение
Наилучший уход в дородовой период и успешные роды всегда основаны на точном знании гестационного возраста (GA). Гестационный возраст имеет первостепенное значение при интерпретации биохимических тестов, таких как скрининг на расширенные биомаркеры материнской сыворотки (хорионический гонадротропин человека, белок Альфа Фето и уровни эстрогена и прогестерона) для оценки риска различных аномалий плода, при оценке рост плода, отличая нормальное развитие плода от патологического.
Это позволяет акушеру назначить меры, которые улучшат исход для плода [1]. При обнаружении аномалии используемый метод вмешательства зависит от срока беременности. Фактически, все важные клинические решения, включая кесарево сечение, плановое стимулирование родов и т. Д., Зависят от знания гестационного возраста. Срок беременности составляет примерно 280 дней, который исчисляется с первого дня последней менструации, поэтому срок беременности начинается еще до оплодотворения.Определение срока беременности — частая клиническая проблема. Ультрасонография (УЗИ) обычно используется для оценки гестационного возраста путем измерения таких размеров плода, как бипариетальный диаметр (BPD), окружность живота (AC), окружность головы (HC) и длина бедра (FL). Ультрасонограф имеет тенденцию к предвзятости наблюдателя, так как это зависит от технических навыков наблюдателя. Кроме того, параметры плода, различные методы измерения и позиционные проблемы могут снизить точность оценки гестационного возраста [2]. Вольфсон и др. Показали, что бипариетальный диаметр не является надежным у плодов, у которых был преждевременный разрыв плодных оболочек [3]. Указанные выше параметры при оценке гестационного возраста имеют некоторые недостатки. Итак, необходим еще один параметр для дополнения оценки гестационного возраста с минимальной ошибкой. Nyberg и Finberg сообщили, что толщина плаценты соответствует сроку беременности [4].
Вольфсон и др. Показали, что бипариетальный диаметр не является надежным у плодов, у которых был преждевременный разрыв плодных оболочек [3]. Указанные выше параметры при оценке гестационного возраста имеют некоторые недостатки. Итак, необходим еще один параметр для дополнения оценки гестационного возраста с минимальной ошибкой. Nyberg и Finberg сообщили, что толщина плаценты соответствует сроку беременности [4].
Материалы и методы
Настоящее исследование представляет собой проспективное перекрестное исследование, в котором участвовали 211 дородовых женщин, которые были направлены на УЗИ после исключения материнских заболеваний.Используемый ультразвуковой аппарат был Volusen E8 ex BT 08 с использованием преобразователя с выпуклой решеткой 3,5 МГц. Каждый плод измерялся только один раз за все время исследования.
Критерии включения были следующие
Одноплодная беременность, 11-40 недель
Последняя известная менструация.

Регулярные менструации в анамнезе.
Критерии исключения были следующими
Материнские болезни
Гестационный диабет.
Гипертония (системная гипертензия и гипертензия, вызванная беременностью)
Анемия
Аномалии плода.
Предлежание Palcenta, аномалии плаценты и плохая визуализация плаценты
Многоплодная беременность.
Последняя менструация неизвестна или нерегулярные менструации.
Трансабдоминальный сканер (датчик 3,5 МГц) использовался для определения аномалий плода, если таковые были.Срок беременности определялся путем измерения бипариетального диаметра, окружности живота, длины крестца коронки, окружности головы и длины бедренной кости. Толщину плаценты измеряли на уровне прикрепления пуповины; максимальная толщина отмечена в поперечном сечении. Каждую плаценту измеряли с точностью до 1 мм при максимальной толщине, которая была перпендикулярна стенке матки. Миометрий матки и ретроплацентарные вены были исключены. Пациенты находились в положении лежа на спине с полным мочевым пузырем, пока они проходили ультразвуковое исследование.
Миометрий матки и ретроплацентарные вены были исключены. Пациенты находились в положении лежа на спине с полным мочевым пузырем, пока они проходили ультразвуковое исследование.
Статистический анализ был выполнен с использованием SPSS 17 и Excel 2007.
Разрешение этического комитета было получено в Медицинском колледже и больнице Шри Баладжи, Университет Бхарат, Ченнаи, Индия. Информированное согласие было получено от субъектов перед началом исследования.
Результаты
Из [&] ясно, что толщина плаценты увеличивается с гестационным возрастом и что толщина плаценты является переменной, зависящей от гестационного возраста.В первом триместре (12-13 недель), 2-м триместре (14-26 недель) и 3-м триместре (27-40 недель) при размерах выборки 32, 89 и 90 соответственно, толщина плаценты увеличивалась с возрастом гестации.
[Таблица / Рис-1]:
Средние значения толщины плаценты в 1-м триместре-12 и 13 недель (32 субъекта) 2-й триместр 14-26 недель (89 субъектов)
| Возраст беременности в неделях | Образец Испытуемые (n) | Среднее со стандартным отклонением | ||||
|---|---|---|---|---|---|---|
| 12 | 18 | 15. 16 ± 0,5 16 ± 0,5 | ||||
| 13 | 14 | 17,84 ± 0,79 | ||||
| 14 | 6 | 18 ± 0,46 | ||||
| 15 | 5 | ± 0,74± 0,74 | 21,95 ± 1,60 | |||
| 17 | 2 | 21,65 ± 6,98 | ||||
| 18 | 2 | 23,6 ± 8,89 | ||||
| 19 | 2 | 2 | 2 | 11 | 22. 4 ± 1,15 4 ± 1,15 | |
| 21 | 24 | 23,7 ± 0,88 | ||||
| 22 | 15 | 25,64 ± 1,15 | ||||
| 23 | 8 | ± 1,6724,57 | 26,62 ± 2,99 | |||
| 25 | 3 | 27,73 ± 0,62 | ||||
| 26 | 3 | 31,73 ± 0,57 |
[Таблица / Фиг.
 толщина в 3 триместре 27-40 недель (90 субъектов) и в общей сложности (211)
толщина в 3 триместре 27-40 недель (90 субъектов) и в общей сложности (211)| Возраст беременности в неделях | Субъекты выборки (n) | Среднее со стандартным отклонением | |||||
|---|---|---|---|---|---|---|---|
| 27 | 2 | 30.3 ± 3,81 | |||||
| 28 | 3 | 33,61 ± 0,24 | |||||
| 29 | 3 | 30,03 ± 0,62 | |||||
| 30 | 3 | 336,06 | 3 | 36,06 | 35,12 ± 0,31 | ||
| 32 | 8 | 34,13 ± 0,81 | |||||
| 33 | 18 | 34,75 ± 0,51 | |||||
| 34 | ± 0,51|||||||
| 34 | 14 35,5478 | ||||||
| 35 | 15 | 34,99 ± 0,65 | |||||
| 36 | 4 | 37,6 ± 2,04 | |||||
| 37 | 3 | 39,33 ± 6,13 903 40,06 ± 4,58 | |||||
| 39 | 6 | 39,64 ± 1,29 | |||||
| 40 | 3 | 40,2 ± 1,38 | |||||
| Весь триместр | 211 | 211 | 49 ± 1.
Толщина плаценты увеличивается более чем на 2 мм в неделю в первом триместре. С 15 по 20 неделю толщина плаценты увеличилась более чем на 4 мм, а с 20 по 25 неделю — более чем на 5 мм. С 19 по 20 неделю толщина плаценты уменьшилась на 0,85 мм. Между 22 -й и 23-й -й неделей толщина плаценты уменьшилась на 0,97 мм. Толщина плаценты увеличивается более чем на 2 мм за неделю в первом триместре.Между 28-й и 29-й неделями толщина плаценты уменьшилась на 3,5 мм, но затем толщина плаценты увеличивается с возрастом гестации без значительного снижения. Максимальная толщина плаценты составила 42,2 мм на 38 неделе, минимальная — 13,9 мм на 12 неделе. Средняя толщина плаценты составила 28,4924 мм ± (1,03) для всех триместров.
Чтобы доказать, что существует корреляция между толщиной плаценты и сроком беременности, был рассчитан коэффициент корреляции, который оказался равным r = 0.609, r = 0,812 и r = 0,814 для 1-го, 2-го и 3-го триместров соответственно, а значение «p» было <0,001, тем самым устанавливая положительную корреляцию между двумя переменными, как показано в []. Есть некоторые исследования корреляции между PT и 1-3 параметрами плода. Некоторые авторы провели исследование корреляции между PT, BPD и AC. В этом исследовании мы провели множественный корреляционный анализ между GA (USG), BPD, FL, AC, HC, FW и PT с использованием преобразования Z Фишера с 5% доверительным интервалом в матричной форме.Вероятно, это могло быть первое исследование, в котором проводился такой множественный корреляционный анализ. Из [] можно сделать вывод, что корреляция между сроком беременности и толщиной плаценты составила r = 0,968, что было значимым при 5% доверительном интервале. Это показывает очень высокую положительную корреляцию между GA и толщиной плаценты. Из [] можно сделать вывод, что «все корреляции моментов продукта» между любыми двумя переменными являются статистически значимыми (односторонний t-критерий — все значения P были меньше 0.001, что свидетельствует о высокой положительной корреляции).
Есть некоторые исследования корреляции между PT и 1-3 параметрами плода. Некоторые авторы провели исследование корреляции между PT, BPD и AC. В этом исследовании мы провели множественный корреляционный анализ между GA (USG), BPD, FL, AC, HC, FW и PT с использованием преобразования Z Фишера с 5% доверительным интервалом в матричной форме.Вероятно, это могло быть первое исследование, в котором проводился такой множественный корреляционный анализ. Из [] можно сделать вывод, что корреляция между сроком беременности и толщиной плаценты составила r = 0,968, что было значимым при 5% доверительном интервале. Это показывает очень высокую положительную корреляцию между GA и толщиной плаценты. Из [] можно сделать вывод, что «все корреляции моментов продукта» между любыми двумя переменными являются статистически значимыми (односторонний t-критерий — все значения P были меньше 0.001, что свидетельствует о высокой положительной корреляции).
[Таблица / Рис-3]:
Результаты t-теста для трех триместров для коэффициента корреляции
| Триместр | Размер выборки | Корреляция между толщиной плаценты и гестационным возрастом | Значение P (односторонний тест) |
|---|---|---|---|
| Первый триместр | 32 | 0,609 | 0,000 <0,001 |
| Второй триместр | 89 | 0. 812 812 | 0,000 <0,001 |
| Третий триместр | 90 | 0,814 | 0,000 <0,001 |
[Таблица / Рис-4]:
Матрица корреляции, показывающая PT, значения коэффициента корреляции между FW, HC, FL, AC и BPD
| w (PT) | y (FW) | z (HC) | t (FL) | u (AC) | v (BPD ) | x (GA) | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| w (PT) | 1 | 0. 902 902 | 0,926 | 0,935 | 0,946 | 0,914 | 0,968 | ||||||
| y (FW) | 0,902 | 1 | 0,889 | 0, 7 0,96 (HC) | 0,926 | 0,889 | 1 | 0,955 | 0,954 | 0,948 | 0,954 | ||
| т (FL) | 0,935 | 0,913 | 0. 955 955 | 1 | 0,967 | 0,967 | 0,972 | ||||||
| u (AC) | 0,946 | 0,916 | 0,954 | 0,967 | 1 | 40,945 | 0,914 | 0,900 | 0,948 | 0,967 | 0,955 | 1 | 0,972 |
| x (GA) | 0,968 | 0,931 | 4 0,954 0,954972 | 0,949 | 0,972 | 1 |
Показывает распределение значений корреляции между PT и GA у 211 субъектов.
Поскольку между указанными выше переменными была высокая положительная корреляция, мы вывели уравнение регрессии для прогнозирования ГА на основе других параметров плода с минимальной ошибкой.
Уравнение регрессии
(x-22.92) = (0.3604) (w-27.86446) + (1.0256) (y-1, 1678) + (0.0015) (z-216.2841) + (0.1047) (t-43.1555) ( 0.027) (u-192,7900) + (0,0042) (v = 60,3725).
Обсуждение
Плацента — материнско-плодный орган, который формируется немного позже плода; он питает и защищает плод, а после родов он умирает. Поскольку он тесно связан с плодом и матерью, он действует как зеркало, отражая статусы как матери, так и плода. Kulman и Warsoff заявили, что PT <25 мм во время родов был связан с задержкой внутриматочного роста (IUGR) [5].Толщина плаценты при доношении> 40 мм связана с гестационным диабетом, внутриматочными инфекциями и водянкой плода [6]. Ла Торре полагает, что ни на одном этапе беременности толщина плаценты косвенно не превышает 40 мм, что указывает на пороговое значение для верхнего предела [7]. Среди беременных с ЦМВ-инфекцией толщина плаценты была увеличена примерно у 93,3% испытуемых [8]. Tsonge et al. В своем исследовании обнаружили, что средняя толщина плаценты между 18-21 неделей у здоровых беременных женщин и при беременности с болезнью Hbbarts составляла 24.6 + 5,2 мм и 34,5 + 6,7 мм соответственно. В этом исследовании, которое проводилось при нормальных одноплодных беременностях, средняя толщина плаценты на соответствующих неделях беременности составляла 23,23 мм [9]. Частота перинатальной смертности и аномалий плода была выше у пациентов с толстой плацентой [10]. Хабиб и др. В своем исследовании заявили, что PT составлял 22 мм на 36 неделе у плодов с массой <2500 г и что PT составлял 34,8 мм на 36 неделе у плодов с массой> 2500 граммов. Они пришли к выводу, что ПВ была предиктором рождения детей с низкой массой тела [11].В нашем исследовании средняя толщина плаценты на 36 неделе составила 37,6 мм. Толщина плаценты была увеличена у пациентов с α-талассемией типа 1, чем у их нормальных сверстников [12].
Среди беременных с ЦМВ-инфекцией толщина плаценты была увеличена примерно у 93,3% испытуемых [8]. Tsonge et al. В своем исследовании обнаружили, что средняя толщина плаценты между 18-21 неделей у здоровых беременных женщин и при беременности с болезнью Hbbarts составляла 24.6 + 5,2 мм и 34,5 + 6,7 мм соответственно. В этом исследовании, которое проводилось при нормальных одноплодных беременностях, средняя толщина плаценты на соответствующих неделях беременности составляла 23,23 мм [9]. Частота перинатальной смертности и аномалий плода была выше у пациентов с толстой плацентой [10]. Хабиб и др. В своем исследовании заявили, что PT составлял 22 мм на 36 неделе у плодов с массой <2500 г и что PT составлял 34,8 мм на 36 неделе у плодов с массой> 2500 граммов. Они пришли к выводу, что ПВ была предиктором рождения детей с низкой массой тела [11].В нашем исследовании средняя толщина плаценты на 36 неделе составила 37,6 мм. Толщина плаценты была увеличена у пациентов с α-талассемией типа 1, чем у их нормальных сверстников [12]. Из приведенного выше обсуждения очевидно, что снижение PT связано с IUGR. Таким образом, субнормальный ПВ может быть самым ранним индикатором ЗВУР, который можно вылечить, если он будет диагностирован как можно раньше. Увеличение плаценты (плацентомегалия) подозревают, если PT> 40 мм в срок и если это связано с гестационным сахарным диабетом, внутриматочными инфекциями, водянкой плода, анемией и α-талассемией [1].Таким образом, повышенный PT для этого GA должен вызвать подозрения о возможных болезненных состояниях. PT — это зависимая переменная GA. В этом исследовании из [Table / Fig-1 & 2] очевидно, что PT находится в линейной зависимости от GA. Это исследование соответствовало ряду других исследований в этом отношении [12-15]. Таким образом, при оценке GA можно рискнуть заменить любые аномальные параметры плода, такие как ПРЛ при гидроцефалии на ПВ при УЗИ. Поскольку все вышеупомянутые исследования были перекрестными исследованиями, неразумно заявлять, что PT может использоваться в качестве надежного предиктора гестационного возраста.
Из приведенного выше обсуждения очевидно, что снижение PT связано с IUGR. Таким образом, субнормальный ПВ может быть самым ранним индикатором ЗВУР, который можно вылечить, если он будет диагностирован как можно раньше. Увеличение плаценты (плацентомегалия) подозревают, если PT> 40 мм в срок и если это связано с гестационным сахарным диабетом, внутриматочными инфекциями, водянкой плода, анемией и α-талассемией [1].Таким образом, повышенный PT для этого GA должен вызвать подозрения о возможных болезненных состояниях. PT — это зависимая переменная GA. В этом исследовании из [Table / Fig-1 & 2] очевидно, что PT находится в линейной зависимости от GA. Это исследование соответствовало ряду других исследований в этом отношении [12-15]. Таким образом, при оценке GA можно рискнуть заменить любые аномальные параметры плода, такие как ПРЛ при гидроцефалии на ПВ при УЗИ. Поскольку все вышеупомянутые исследования были перекрестными исследованиями, неразумно заявлять, что PT может использоваться в качестве надежного предиктора гестационного возраста. Но есть возможность войти в этот сегмент и выйти с его уточнением после проведения многоцентровых продольных исследований с несколькими большими выборками.
Но есть возможность войти в этот сегмент и выйти с его уточнением после проведения многоцентровых продольных исследований с несколькими большими выборками.
Ограничения
Это было перекрестное исследование, и мы измеряли толщину плаценты только один раз у каждого субъекта в течение исследования. Размер выборки был небольшим, и присутствовал только один наблюдатель. Поскольку измерение USG было выполнено, была вероятность смещения наблюдателя (вариабельность внутри наблюдателя), инструментальной смещения и т. Д.
Выводы
Из нашего исследования можно сделать вывод, что PT может использоваться в качестве предиктора ГА у женщин, у которых LMP ненадежен или неизвестен. Можно рискнуть заменить любые аномальные параметры плода, такие как ПРЛ при гидроцефалии на ПВ при УЗИ при оценке общего состояния. При патологическом PT для соответствующего GA необходимо устранить болезненные состояния, которые вызывают повышенное или пониженное PT. Уравнение регрессии можно использовать для расчета GA по другим параметрам плода с минимальной ошибкой.
Выражение признательности
Мы с благодарностью выражаем признательность участникам исследования и руководству больницы Excellent Care Hospital, Велачерри, Ченнаи, Индия, за их сотрудничество и технический персонал для сбора данных.
Источники
[1] Каллен П.У., редактор. Ультрасонография в акушерстве и гинекологии. 5-е изд. Филадельфия: Elsevier, подразделение Reed Elsevier India Limited; 2002. С. 225–65. Глава 7 — УЗИ-оценка биометрии плода и аномального роста.[Google Scholar] [2] Малхотра Н., Кумар П. Ультразвук в акушерстве и гинекологии. 3-е изд. Мумбаи: Джейпи Бразерс Медикал Паблишерс Частное Лтд; 1999. Глава 11, Измерение параметров плода; Глава 27, УЗИ и прием в родах. Глава 55, Подводные камни в USG; pp92-98,198-200,386-88. [Google Scholar] [3] Вольфсон Р.Н., Задор И.Е., Хаворсен П., Эндрюс Б., Сокол Р.Дж. Бипариетальный диаметр при преждевременном разрыве плодных оболочек: ошибки в оценке гестационного возраста. Дж. Клин Ультразвук.1983; 11: 371–74. [PubMed] [Google Scholar] [4] Ниберг Д.А., Финберг Х.Дж. Плацента, плацентарные оболочки и пуповина. Журнал по ультразвуковой диагностике аномалий плода. 1990; 21 (4): 623–75. [Google Scholar] [5] Kunlmann RS, Warsof S. Ультразвук плаценты. Clin Afr. Jou Obstet. Гинеколь. 1996; 39: 34. [Google Scholar] [6] Бенришке К., Кауфманн П. Анатомия и патология пуповины и крупных сосудов плода. 2 округлено. Нью-Йорк: Спрингер-Верлаг; 1998. Глава 29 патология плаценты человека 319–77.[Google Scholar] [7] Ла Торре Р., Джованни Нигро, Мануэла Маццокко М., Бест Стюарт П. Ультразвуковые изменения созревающей плаценты. Am J Obstet and Gynecol. 1979; 42: 915. [Google Scholar] [8] Tongsong T, Wanapirak C, Sirichotiyakue S. Толщина плаценты в середине беременности как предиктор болезни HbBarts. Журнал по пренатальной диагностике. 1999; 19: 1027. [PubMed] [Google Scholar] [9] Эльчалал У., Эзра Й., Леви Й. и др. Сонографически толстая плацента: маркер повышенного перинатального риска — проспективное поперечное исследование.
[PubMed] [Google Scholar] [4] Ниберг Д.А., Финберг Х.Дж. Плацента, плацентарные оболочки и пуповина. Журнал по ультразвуковой диагностике аномалий плода. 1990; 21 (4): 623–75. [Google Scholar] [5] Kunlmann RS, Warsof S. Ультразвук плаценты. Clin Afr. Jou Obstet. Гинеколь. 1996; 39: 34. [Google Scholar] [6] Бенришке К., Кауфманн П. Анатомия и патология пуповины и крупных сосудов плода. 2 округлено. Нью-Йорк: Спрингер-Верлаг; 1998. Глава 29 патология плаценты человека 319–77.[Google Scholar] [7] Ла Торре Р., Джованни Нигро, Мануэла Маццокко М., Бест Стюарт П. Ультразвуковые изменения созревающей плаценты. Am J Obstet and Gynecol. 1979; 42: 915. [Google Scholar] [8] Tongsong T, Wanapirak C, Sirichotiyakue S. Толщина плаценты в середине беременности как предиктор болезни HbBarts. Журнал по пренатальной диагностике. 1999; 19: 1027. [PubMed] [Google Scholar] [9] Эльчалал У., Эзра Й., Леви Й. и др. Сонографически толстая плацента: маркер повышенного перинатального риска — проспективное поперечное исследование.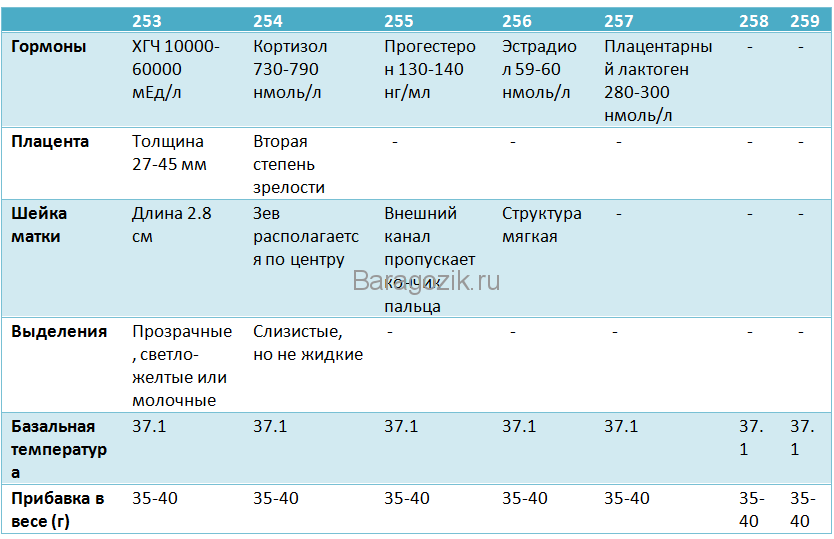 Журнал клинического ультразвука. 2000; 21: 268–72. [PubMed] [Google Scholar] [10] Хабиб Ф.А. Прогнозирование новорожденных с низкой массой тела при ультразвуковом измерении диаметра и толщины плаценты. Анналы медицины юга Саудовской Аравии. 2002; 22 ((5-6)): 312–14. [PubMed] [Google Scholar] [11] Цанг-Мин Кой, доктор медицины, Ли-Хуэй Цзэн, Пи-Мей Сю, Сяо-Линь Хва, Цзы-Яо, Чуанг Соу-Мин. Ультрасонографическое сканирование толщины плаценты и пренатальная диагностика гомозиготной альфа-талассемии -1 во 2 триместре.Японский журнал по акушерству и гинекологии. 2005. 17 (4): 112–33. [Google Scholar] [12] Охагву С.К., Абу П.О., Эзекеке Ю.О., Угва А.К. Взаимосвязь между толщиной плаценты и параметрами роста у нормальных нигерийских плодов. Африканский журнал биотехнологии. 2009. 8 (2): 133–38. Январь [Google Scholar] [13] Охагву С.К., Ошиотсе Абу П., Эффионг Удох Б. Толщина плаценты: сонографический индикатор гестационного возраста при нормальных одноплодных беременностях у нигерийских женщин.
Журнал клинического ультразвука. 2000; 21: 268–72. [PubMed] [Google Scholar] [10] Хабиб Ф.А. Прогнозирование новорожденных с низкой массой тела при ультразвуковом измерении диаметра и толщины плаценты. Анналы медицины юга Саудовской Аравии. 2002; 22 ((5-6)): 312–14. [PubMed] [Google Scholar] [11] Цанг-Мин Кой, доктор медицины, Ли-Хуэй Цзэн, Пи-Мей Сю, Сяо-Линь Хва, Цзы-Яо, Чуанг Соу-Мин. Ультрасонографическое сканирование толщины плаценты и пренатальная диагностика гомозиготной альфа-талассемии -1 во 2 триместре.Японский журнал по акушерству и гинекологии. 2005. 17 (4): 112–33. [Google Scholar] [12] Охагву С.К., Абу П.О., Эзекеке Ю.О., Угва А.К. Взаимосвязь между толщиной плаценты и параметрами роста у нормальных нигерийских плодов. Африканский журнал биотехнологии. 2009. 8 (2): 133–38. Январь [Google Scholar] [13] Охагву С.К., Ошиотсе Абу П., Эффионг Удох Б. Толщина плаценты: сонографический индикатор гестационного возраста при нормальных одноплодных беременностях у нигерийских женщин. Интернет-журнал медицинских новостей. 2009. 4 (2): 9–14.Июль. [Google Scholar] [14] Анупама Джайн, Ганеш Кумар, Агарвал У., Хараквал С. Толщина плаценты — сонографический индикатор гестационного возраста. Джоу из Обста и Гин Индии. 2001. 51 (3): 48–49. [Google Scholar] [15] Mital P, Hooja N, Mehndiratta K. Толщина плаценты — сонографический параметр для оценки гестационного возраста плода. Индийский журнал радиологии и визуализации. 2002; 12: 553–54. [Google Scholar]
Интернет-журнал медицинских новостей. 2009. 4 (2): 9–14.Июль. [Google Scholar] [14] Анупама Джайн, Ганеш Кумар, Агарвал У., Хараквал С. Толщина плаценты — сонографический индикатор гестационного возраста. Джоу из Обста и Гин Индии. 2001. 51 (3): 48–49. [Google Scholar] [15] Mital P, Hooja N, Mehndiratta K. Толщина плаценты — сонографический параметр для оценки гестационного возраста плода. Индийский журнал радиологии и визуализации. 2002; 12: 553–54. [Google Scholar]Зрелость плода — обзор
Преждевременные роды
Понимание механизмов, связывающих скорость созревания плода со сроками рождения, обеспечивает фундаментальную область для биологических исследований, которые так же важны для выживания млекопитающих, как и последовательность производящих событий дифференцированный многоклеточный организм из одноклеточного эмбриона.Помимо этого присущего научному интересу, выяснение детерминант начала человеческих родов будет способствовать развитию вмешательств, возможно, при наиболее сложном и трудно поддающемся лечению синдроме женского и детского здоровья — преждевременных родах. 512 Преждевременные роды человека, определяемые как роды на сроке менее 37 полных недель беременности, приводят к 75% перинатальной смертности и большей части длительной перинатальной заболеваемости. 513 Хотя определение преждевременных родов на сроке менее 37 недель, данное Всемирной организацией здравоохранения, является несколько произвольным, ясно, что рождение на каждом сроке беременности раньше срока, в том числе на 37-й и 38-й неделях гестации, связано с повышенной перинатальной заболеваемостью и неонатальная смертность. 514,515 Приблизительно 75% преждевременных родов происходят между 34 и 36 неделями беременности, которые называются «поздними преждевременными» родами. Частота родов растет экспоненциально по мере приближения срока, так что примерно 5% преждевременных родов или менее 1% от общего числа родов происходят на сроке менее 28 недель полной беременности, когда смертность и заболеваемость плода являются самыми высокими. 208 Однако не следует недооценивать влияние поздних преждевременных родов, поскольку среди младенцев, рожденных в этом гестационном возрасте, было обнаружено трех-шестикратное увеличение неонатальной смертности.
512 Преждевременные роды человека, определяемые как роды на сроке менее 37 полных недель беременности, приводят к 75% перинатальной смертности и большей части длительной перинатальной заболеваемости. 513 Хотя определение преждевременных родов на сроке менее 37 недель, данное Всемирной организацией здравоохранения, является несколько произвольным, ясно, что рождение на каждом сроке беременности раньше срока, в том числе на 37-й и 38-й неделях гестации, связано с повышенной перинатальной заболеваемостью и неонатальная смертность. 514,515 Приблизительно 75% преждевременных родов происходят между 34 и 36 неделями беременности, которые называются «поздними преждевременными» родами. Частота родов растет экспоненциально по мере приближения срока, так что примерно 5% преждевременных родов или менее 1% от общего числа родов происходят на сроке менее 28 недель полной беременности, когда смертность и заболеваемость плода являются самыми высокими. 208 Однако не следует недооценивать влияние поздних преждевременных родов, поскольку среди младенцев, рожденных в этом гестационном возрасте, было обнаружено трех-шестикратное увеличение неонатальной смертности.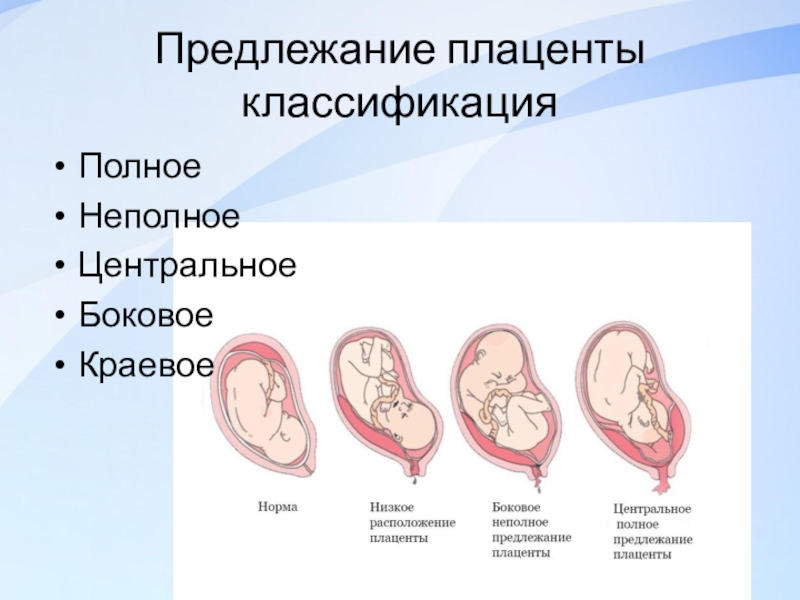 516
516
Существует несколько недавних всеобъемлющих обзорных статей, посвященных эпидемиологии преждевременных родов у людей. 208,512,517,518 Концептуальная основа для анализа этиологии преждевременных родов сначала начинается с разделения модели родов на «спонтанные» или «по медицинским показаниям». Роды по медицинским показаниям составляют примерно 30% преждевременных родов. Подавляющее большинство родов, показанных с медицинской точки зрения, происходят в окне позднего преждевременного гестационного возраста и инициируются из-за появления аномалий матери или плода, которые в конечном итоге могут поставить под угрозу здоровые исходы беременности, включая смерть матери или плода.Частым предшественником родов по медицинским показаниям является преэклампсия. 519,520 Диагноз преэклампсии включает повышение артериального давления у матери (систолическое> 140 мм рт.ст. или диастолическое> 90 мм рт.ст.) с протеинурией (> 300 мг белка за 24 ч сбора мочи). Существует спектр тяжести преэклампсии с дополнительными проявлениями, включая церебральные или зрительные нарушения у матери, отек легких, нарушения функции печени и тромбоцитопению, а также задержку роста плода.Важно отметить, что это заболевание, которое проявляется структурными сосудистыми изменениями в материнской почке и других органах с нарушением перфузии тканей из-за вазоспазма, разрешается с доставкой плаценты. 521–523 Полное обсуждение патофизиологии и этиологии преэклампсии выходит за рамки данной главы, но его можно найти в нескольких превосходных обзорах. 519,524 Остальная часть обсуждения преждевременных родов будет сосредоточена на причинах самопроизвольных преждевременных родов, которые могут возникнуть либо из-за нарушения регуляции типичных механизмов контроля за родами, либо из-за различных патологических путей.
Существует спектр тяжести преэклампсии с дополнительными проявлениями, включая церебральные или зрительные нарушения у матери, отек легких, нарушения функции печени и тромбоцитопению, а также задержку роста плода.Важно отметить, что это заболевание, которое проявляется структурными сосудистыми изменениями в материнской почке и других органах с нарушением перфузии тканей из-за вазоспазма, разрешается с доставкой плаценты. 521–523 Полное обсуждение патофизиологии и этиологии преэклампсии выходит за рамки данной главы, но его можно найти в нескольких превосходных обзорах. 519,524 Остальная часть обсуждения преждевременных родов будет сосредоточена на причинах самопроизвольных преждевременных родов, которые могут возникнуть либо из-за нарушения регуляции типичных механизмов контроля за родами, либо из-за различных патологических путей.
Среди 70% преждевременных родов, которые считаются самопроизвольными, примерно две трети связаны с самопроизвольными преждевременными родами, а одна треть — в результате PPROM. 208 По данным 2011 года, в США 11,7% родов являются преждевременными. 525 Этот показатель на 15% выше, чем показатель преждевременных родов в 1990 году, хотя он отражает последовательное снижение по сравнению с пиком в 2006 году на 12,8%. 526 Этиология снижения преждевременных родов в Соединенных Штатах в значительной степени связана с изменениями в акушерской практике в отношении индукции родов или кесарева сечения у лиц, родившихся на поздних сроках. 208 517 525 527 528 Роды на сроке менее 34 недель после завершения беременности, напротив, за последние 20 лет существенно не изменились по частоте. Более чем в половине случаев прямые причинные пути самопроизвольных преждевременных родов при любой конкретной беременности неизвестны. 208 518 Многоплодная беременность, возникающая естественным путем или в результате вспомогательных репродуктивных технологий, осложняет 2–3% беременностей, но приводит к 15% всех преждевременных родов.
208 По данным 2011 года, в США 11,7% родов являются преждевременными. 525 Этот показатель на 15% выше, чем показатель преждевременных родов в 1990 году, хотя он отражает последовательное снижение по сравнению с пиком в 2006 году на 12,8%. 526 Этиология снижения преждевременных родов в Соединенных Штатах в значительной степени связана с изменениями в акушерской практике в отношении индукции родов или кесарева сечения у лиц, родившихся на поздних сроках. 208 517 525 527 528 Роды на сроке менее 34 недель после завершения беременности, напротив, за последние 20 лет существенно не изменились по частоте. Более чем в половине случаев прямые причинные пути самопроизвольных преждевременных родов при любой конкретной беременности неизвестны. 208 518 Многоплодная беременность, возникающая естественным путем или в результате вспомогательных репродуктивных технологий, осложняет 2–3% беременностей, но приводит к 15% всех преждевременных родов. В то время как традиционный механизм ранних родов при многоплодной или многоплодной беременности объясняется чрезмерным растяжением матки, недавние данные об измерении деформации стенки матки ставят эту модель под сомнение. 529
В то время как традиционный механизм ранних родов при многоплодной или многоплодной беременности объясняется чрезмерным растяжением матки, недавние данные об измерении деформации стенки матки ставят эту модель под сомнение. 529
При одноплодной беременности несколько демографических характеристик матери были связаны с повышенным риском преждевременных родов. К ним относятся низкий индекс массы тела матери (ИМТ), крайние значения материнского возраста, афроамериканская раса, низкий социально-экономический статус, курение, отсутствие дородового ухода, короткий интервал между беременностями и предыдущие преждевременные роды. 208,530–532 Как эти характеристики нарушают нормальное время родов, остается неясным. Помимо этих материнских демографических факторов, убедительные доказательства указывают на причинную связь генетики, инфекции и стресса с риском преждевременных родов. 518,533–539
Генетика и риск преждевременных родов : Несколько линий доказательств сходятся, чтобы указать на важность генетических факторов у матери или плода как влияющих на продолжительность беременности и риск преждевременных родов. Особенно информативными были исследования, изучающие семейные модели для определения времени рождения. Крупномасштабные эпидемиологические анализы европейского населения демонстрируют значительно повышенный риск преждевременных родов у сестер женщин, переживших преждевременные роды, но незначительный или нулевой рост риска для женщин, которые являются сестрами отцов, родивших недоношенных детей. 540,541 Анализ времени рождения детей, рожденных от монозиготных близнецов, в сравнении с дизиготными близнецами или братьями и сестрами, не являющимися близнецами, подтверждает важную роль материнской генетики в определении гестационного возраста при рождении с оценками наследуемости от 14% до 40%. 542–545 Роль отцовских генов не была так тщательно изучена, но исследования предполагают гораздо меньшую роль, основанную на смешанной беременности. 546 или отсутствие роли на основе анализа детей близнецов. 543 В последнее время большое внимание уделяется роли генов плода в родах.
Особенно информативными были исследования, изучающие семейные модели для определения времени рождения. Крупномасштабные эпидемиологические анализы европейского населения демонстрируют значительно повышенный риск преждевременных родов у сестер женщин, переживших преждевременные роды, но незначительный или нулевой рост риска для женщин, которые являются сестрами отцов, родивших недоношенных детей. 540,541 Анализ времени рождения детей, рожденных от монозиготных близнецов, в сравнении с дизиготными близнецами или братьями и сестрами, не являющимися близнецами, подтверждает важную роль материнской генетики в определении гестационного возраста при рождении с оценками наследуемости от 14% до 40%. 542–545 Роль отцовских генов не была так тщательно изучена, но исследования предполагают гораздо меньшую роль, основанную на смешанной беременности. 546 или отсутствие роли на основе анализа детей близнецов. 543 В последнее время большое внимание уделяется роли генов плода в родах. Элегантные исследования на основе семейного и двойного моделирования продемонстрировали важную роль генетики плода, внося примерно 11% вариабельности в сроки рождения, 545 547 , что подтверждается анализом сегрегации в семейных родословных. 548
Элегантные исследования на основе семейного и двойного моделирования продемонстрировали важную роль генетики плода, внося примерно 11% вариабельности в сроки рождения, 545 547 , что подтверждается анализом сегрегации в семейных родословных. 548
Вооружившись этими данными о генетических факторах, влияющих на время рождения человека, поиск геномных вариаций человека, которые способствуют риску преждевременных родов, привлек значительное внимание.Первоначальный опрос о роли полиморфизмов генов использовал подходы генов-кандидатов, исследуя пути, которые участвовали в родах, такие как воспаление и иммунитет, ремоделирование соединительной ткани, гемостаз и контроль сократимости и покоя миометрия. В то время как отдельные исследования обнаружили небольшие или умеренные ассоциации с вариантами цитокинов, их рецепторов, ММП, факторов свертывания и адренергических рецепторов, например, они в целом не были воспроизведены или обобщены.Недавно было опубликовано несколько прекрасных резюме исследований генов-кандидатов при преждевременных родах. 537 549 550 Беспристрастные, полногеномные исследования ассоциаций и секвенирование всего экзома в настоящее время продолжаются, но на сегодняшний день не сообщается о новых общих или редких генетических вариантах, дающих новое представление о путях родов.
537 549 550 Беспристрастные, полногеномные исследования ассоциаций и секвенирование всего экзома в настоящее время продолжаются, но на сегодняшний день не сообщается о новых общих или редких генетических вариантах, дающих новое представление о путях родов.
Инфекция и риск преждевременных родов : Клинические, гистологические и микробиологические данные свидетельствуют о том, что инфекция может быть причиной 25–40% преждевременных родов. 208 462 539 Бактериальная колонизация плаценты или околоплодных вод, в частности Ureaplasma urealyticum , по данным посева или полимеразной цепной реакции, обнаруживается у 79% беременностей при рождении на 23 неделе гестации и снижается до 11% при беременности с роды на 31–34 неделе беременности. 551 Интересно, что у женщин, у которых обнаружена колонизация в околоплодных водах Ureaplasma в середине беременности, только 30% продолжают рожать преждевременно. 552,553 Гистологические свидетельства воспалительных реакций как матери, так и плода одинаково увеличиваются по частоте в случаях, которые иначе считались идиопатическими спонтанными преждевременными родами, поскольку гестационный возраст при рождении уменьшается. 554 В совокупности эти данные свидетельствуют о том, что инфекция может наиболее заметно способствовать преждевременным родам на очень ранних сроках беременности. К сожалению, у беременных с вагинальной колонизацией Ureaplasma или Mycoplasma , получающих профилактическое лечение антибиотиками, не наблюдается снижения частоты преждевременных родов. 555
554 В совокупности эти данные свидетельствуют о том, что инфекция может наиболее заметно способствовать преждевременным родам на очень ранних сроках беременности. К сожалению, у беременных с вагинальной колонизацией Ureaplasma или Mycoplasma , получающих профилактическое лечение антибиотиками, не наблюдается снижения частоты преждевременных родов. 555
Более поздние концепции, касающиеся роли бактериальных патогенов как факторов риска преждевременных родов, рассматривают, а не первичный микроорганизм, сдвиг в микробном сообществе как движущую силу неблагоприятных исходов беременности. 556–559 Одним из таких примеров является бактериальный вагиноз. Аналогично результатам попыток искоренить Ureaplasma , лечение бактериального вагиноза, 560 или других хронических инфекций низкой степени, таких как трихомониаз 561 и пародонтоз, 562 не снизил риск преждевременных родов. Текущие попытки более полно охарактеризовать все микробное сообщество — включая бактерии, грибы и вирусы — определение метагенома беременности могут выявить новые, ранее загадочные патогены, которые не были бы уничтожены предыдущими вмешательствами антибиотиков.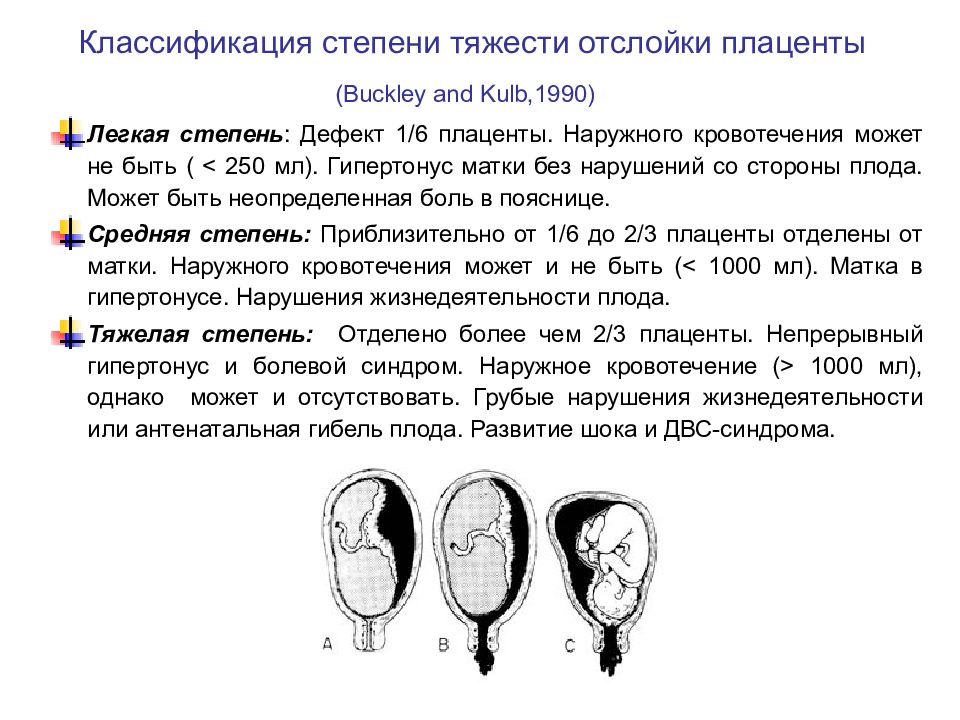
Стресс и риск преждевременных родов : Многие демографические факторы матери, повышающие риск преждевременных родов, прямо или косвенно связаны с частотой и серьезностью физиологического или психосоциального стресса, который испытывают матери. 208 518 536 563 564 Примеры этих демографических факторов включают жизнь в бедности, низкий ИМТ матери, статус незамужнего и статус расового меньшинства. Как первоначально описал Селье, отклонение организма от его гомеостатической уставки (т.е. стресс) инициирует высококонсервативный эндокринный и симпатический нервный ответ, способствующий адаптации и возвращению к гомеостазу. 565,566 Основной эндокринный ответ сосредоточен на синтезе и секреции глюкокортикоидов, кортизола у людей и кортикостерона у грызунов из надпочечников. Глюкокортикоиды оказывают множество эффектов на метаболизм, иммунную функцию и познавательные способности, которые резко ускоряют адаптацию, но ставят под угрозу благополучие, если присутствуют хронически. 567,568 Глюкокортикоиды независимо друг от друга играют решающую роль в созревании плода и сроках родов у многих видов.Считается, что у людей повышение уровня глюкокортикоидов на поздних сроках типичной доношенной беременности способствует созреванию легких и других органов плода при подготовке к родам и ускоряет родовой процесс, индуцируя синтез PG мембранами плода. 186–188,569,570 Предполагается, что преждевременное, хронически повышенное содержание глюкокортикоидов, связанное со стрессом во время беременности, индуцирует ПГ до родов и вызывает реакции сосудов, шейки матки и миометрия, которые способствуют преждевременным родам. В соответствии с этим представлением, при неосложненных беременностях высокий психосоциальный стресс был связан со значительным увеличением биомаркеров воспаления, таких как С-реактивный белок и укорочение шейки матки на поздних сроках беременности. 571 Кроме того, женщины с более высокими индексами тревожности по опроснику Спилбергера продемонстрировали повышенный средний индекс сопротивления маточной артерии, 572 — параметр, связанный с более высокой частотой преждевременных родов.
567,568 Глюкокортикоиды независимо друг от друга играют решающую роль в созревании плода и сроках родов у многих видов.Считается, что у людей повышение уровня глюкокортикоидов на поздних сроках типичной доношенной беременности способствует созреванию легких и других органов плода при подготовке к родам и ускоряет родовой процесс, индуцируя синтез PG мембранами плода. 186–188,569,570 Предполагается, что преждевременное, хронически повышенное содержание глюкокортикоидов, связанное со стрессом во время беременности, индуцирует ПГ до родов и вызывает реакции сосудов, шейки матки и миометрия, которые способствуют преждевременным родам. В соответствии с этим представлением, при неосложненных беременностях высокий психосоциальный стресс был связан со значительным увеличением биомаркеров воспаления, таких как С-реактивный белок и укорочение шейки матки на поздних сроках беременности. 571 Кроме того, женщины с более высокими индексами тревожности по опроснику Спилбергера продемонстрировали повышенный средний индекс сопротивления маточной артерии, 572 — параметр, связанный с более высокой частотой преждевременных родов. 573
573
Границы | Развитие плаценты человека и сердца плода: синергетическое или независимое?
Введение
Плацента и сердце плода — два из первых органов, которые дифференцируются, и поэтому предполагается, что их развитие взаимосвязано.Общие гены и питательные микроэлементы, такие как фолиевая кислота, регулируют важные этапы формирования обоих органов, поэтому сердечные и плацентарные аномалии часто сосуществуют (Linask, 2013). Однако появляется все больше свидетельств того, что первичные дефекты развития плаценты могут влиять на развитие сердца плода и его функцию после родов.
Концептуально влияние плаценты может быть двояким. Во-первых, эффективность плаценты как источника кислорода и питательных веществ, а также как селективного барьера для ксенобиотиков может иметь глубокое влияние на морфогенез и функциональную способность многих систем органов через программирование развития (Burton et al., 2016). Во-вторых, несмотря на отсутствие экспериментальных данных, весьма вероятно, что гемодинамика пупочно-плацентарного кровообращения влияет на развитие сердца плода (Linask et al. , 2014). Плацента — самый большой из органов плода, и в срок получает ~ 40% сердечного выброса плода. Сопротивление, обеспечиваемое артериальной и капиллярной сетью в ворсинчатых деревьях плаценты, будет варьироваться в зависимости от стадии развития и наличия патологии плаценты. Поскольку экспрессия сердечных генов очень чувствительна к биомеханическим сигналам, эта устойчивость может влиять на дифференцировку кардиомиоцитов и морфогенез сердца (Hove et al., 2003; Ковальский и др., 2014).
, 2014). Плацента — самый большой из органов плода, и в срок получает ~ 40% сердечного выброса плода. Сопротивление, обеспечиваемое артериальной и капиллярной сетью в ворсинчатых деревьях плаценты, будет варьироваться в зависимости от стадии развития и наличия патологии плаценты. Поскольку экспрессия сердечных генов очень чувствительна к биомеханическим сигналам, эта устойчивость может влиять на дифференцировку кардиомиоцитов и морфогенез сердца (Hove et al., 2003; Ковальский и др., 2014).
В этом обзоре мы сосредотачиваемся на потенциальных биомеханических сигналах, предлагаемых внеэмбриональной циркуляцией, которые могут синергизировать развитие плаценты и сердца человека. Мы концентрируемся на анатомическом и физиологическом развитии желточного и хориоаллантоического плацентарного кровообращения и рассматриваем, как гемодинамика плацентарного кровообращения плода, оцененная in vivo с помощью ультразвукового допплера, дает дополнительную информацию о потенциальном влиянии патологий плаценты на пупочную гемодинамику. .
.
Развитие фетально-плацентарного кровообращения
Экстракорпоральное кровообращение к внеэмбриональным мембранам включает два кровообращения: во вторичный желточный мешок, желточное кровообращение, и в окончательную плаценту, хорионическое или пупочное кровообращение. Из них желточное кровообращение развивается первым, и его максимальная функция совпадает с морфогенезом сердца (Jones and Jauniaux, 1995; Gittenberger-de Groot et al., 2013).
Капиллярная сеть может быть идентифицирована в мезенхимальном слое желточного мешка человека с гестационного возраста ~ 5 недель (Pereda and Niimi, 2008), а венозный отток осуществляется через область развивающейся печени в венозный синус (Рисунок 1). Размер этих капилляров остается ниже разрешения стандартной ультразвуковой визуализации в течение биологической жизни вторичного желточного мешка, и только более крупные сосуды желточного протока были изучены in utero с помощью цветного допплеровского изображения ближе к концу первого — триместр, когда он больше не функционирует (Mäkikallio et al. , 2004). Желточный мешок демонстрирует дегенеративные изменения с 10 недель беременности, что позволяет предположить, что его инволюция при нормальной беременности является спонтанным событием, а не результатом механического сжатия расширяющейся амниотической полостью (Jauniaux et al., 1991d). При ранней гибели плода желточный мешок увеличивается в размерах и становится менее плотным из-за отека непосредственно перед или сразу после остановки сердца плода. Эти различия в размере и внешнем виде желточного мешка являются следствием аномального развития или смерти плода, а не основной причиной неудач беременности на ранних сроках (Jauniaux et al., 1991г).
, 2004). Желточный мешок демонстрирует дегенеративные изменения с 10 недель беременности, что позволяет предположить, что его инволюция при нормальной беременности является спонтанным событием, а не результатом механического сжатия расширяющейся амниотической полостью (Jauniaux et al., 1991d). При ранней гибели плода желточный мешок увеличивается в размерах и становится менее плотным из-за отека непосредственно перед или сразу после остановки сердца плода. Эти различия в размере и внешнем виде желточного мешка являются следствием аномального развития или смерти плода, а не основной причиной неудач беременности на ранних сроках (Jauniaux et al., 1991г).
Рисунок 1 . Внезапные тиражи. Желточный мешок — это первая из внеэмбриональных оболочек, которая подвергается васкуляризации и, вероятно, играет ключевую роль в транспортировке от матери к плоду в период органогенеза до того, как хорионическое кровообращение полностью установится примерно через 12 недель. Изменения резистентности, обеспечиваемые каждой циркуляцией, могут влиять на экспрессию генов и дифференцировку кардиомиоцитов плода. Из Burton et al. (2016) с разрешения.
Из Burton et al. (2016) с разрешения.
Биологические функции желточного мешка человека изучаются редко (Gulbis et al., 1998), и поэтому плохо изучены. Недавние данные по RNA-Seq указывают на сохранение транскриптов у разных видов, что это может быть важно для транспортировки питательных веществ к раннему плоду на ранних сроках беременности (Cindrova-Davies et al., 2017). В частности, транскрипты, кодирующие белки, участвующие в обработке и метаболизме холестерина, являются одними из самых распространенных. Холестерин необходим для образования мембран клеток и органелл и, следовательно, для репликации клеток, но он также является важным кофактором для сигнальных молекул, таких как sonic hedgehog, которые играют критическую роль во время морфогенеза (Lewis et al., 2001). Помимо транспорта макро- и микроэлементов, желточный мешок также экспрессирует многие переносчики АТФ-связывающих кассет (ABC), которые могут играть важную роль в защите развивающегося эмбриона в критический период органогенеза за счет оттока токсинов окружающей среды и ксенобиотиков.
Элементы хорионического кровообращения впервые можно наблюдать в мезенхиме ворсин плаценты на 5-й неделе беременности. Гемангиобластные кластеры дифференцируются и дают начало обширной сети капилляров, лежащих преимущественно непосредственно под базальной мембраной трофобласта (Demir et al., 1989; Чарнок-Джонс и Бертон, 2000; Аплин и др., 2015). Число капиллярных профилей на профиль ворсинок и процент стромального ядра ворсинок, занятого капиллярами, неуклонно увеличиваются с 6 по 15 недель беременности (Jauniaux et al., 1991a). Ранние капилляры обладают относительно низким покрытием перицитов, это указывает на то, что они пластичны и способны к ремоделированию (Zhang et al., 2002).
Обширное ремоделирование происходит к концу первого триместра, когда формируется дефинитивная плацента.Первоначально ворсинки развиваются на протяжении всего гестационного мешка, но примерно с 8 недель беременности ворсинки над поверхностным полюсом начинают регрессировать, образуя гладкие мембраны или хориональный слой. Регрессия связана с прогрессирующим началом артериального кровообращения матери к плаценте, сначала на периферии, а затем в остальной части плаценты. Этот процесс опосредуется миграцией вневорсинчатых трофобластических клеток (EVT) в плацентарное ложе и модулируется локально высокими уровнями окислительного стресса внутри ворсинок (Jauniaux et al., 2003а). В соответствии с этой теорией соединительные комплексы между эндотелиальными клетками, формирующими капилляры внутри регрессирующих ворсинок, теряют свою целостность, и ворсинки становятся бессосудистыми, гипоцеллюлярными призраками (Burton et al., 2010).
Регрессия связана с прогрессирующим началом артериального кровообращения матери к плаценте, сначала на периферии, а затем в остальной части плаценты. Этот процесс опосредуется миграцией вневорсинчатых трофобластических клеток (EVT) в плацентарное ложе и модулируется локально высокими уровнями окислительного стресса внутри ворсинок (Jauniaux et al., 2003а). В соответствии с этой теорией соединительные комплексы между эндотелиальными клетками, формирующими капилляры внутри регрессирующих ворсинок, теряют свою целостность, и ворсинки становятся бессосудистыми, гипоцеллюлярными призраками (Burton et al., 2010).
События на этой стадии развития играют ключевую роль в определении окончательного размера и формы плаценты (Burton et al., 2010; Salafia et al., 2012), и поэтому могут повлиять на развитие сердца плода. Чрезмерная или асимметричная регрессия ворсинок может привести к большему количеству эллипсовидных плацент или эксцентрическому прикреплению пуповины, причем последнее менее эффективно, как оценивается по соотношению веса плода / плаценты (Ямпольский и др.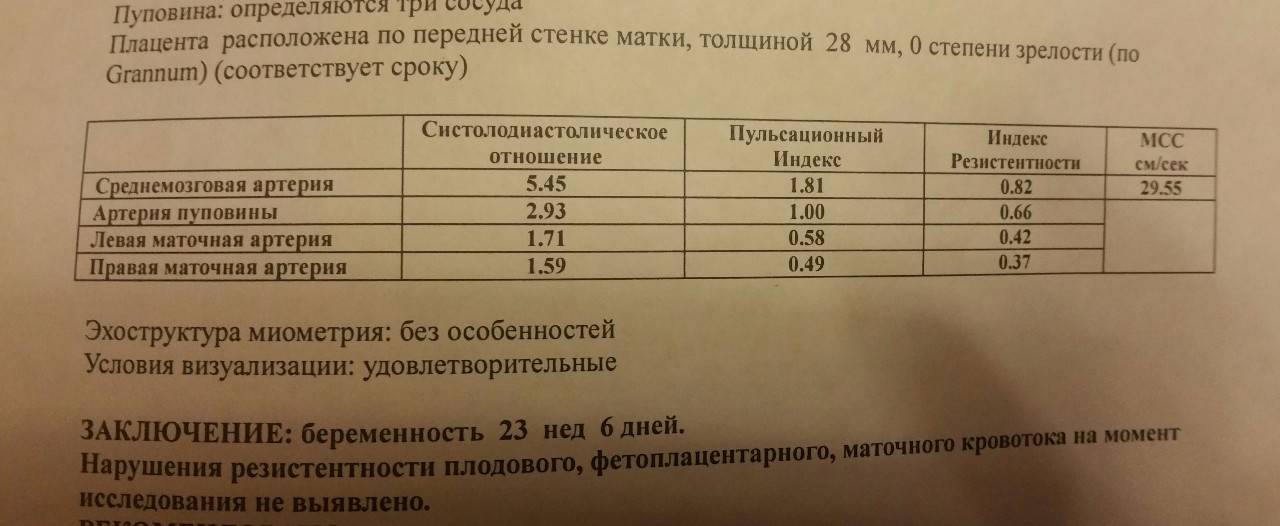 , 2009). Снижение эффективности может ограничивать поступление питательных веществ к плоду, но, кроме того, схема ветвления хорионических артерий, когда они расходятся по хорионической пластинке, будет различаться в зависимости от положения введения пуповины. Предсказать влияние этих различий на сопротивление сети сложно. Когда прикрепление пуповины является центральным, паттерн ветвления артерий преимущественно дихотомический, тогда как при эксцентричном прикреплении пуповины преобладает моноподиальный паттерн ветвления (Gordon et al., 2007). Моделирование показывает, что потери энергии минимальны в точках моноподиального ветвления, и, следовательно, этот образец может быть предпочтительным для обеспечения равномерного распределения кровотока, когда необходимо пройти относительно большие расстояния через хорионическую пластинку (Gordon et al., 2007). Однако в большинстве плацент паттерн ветвления представляет собой смесь двух типов, что затрудняет прогнозирование сосудистого сопротивления, обеспечиваемого хорионическими артериями.
, 2009). Снижение эффективности может ограничивать поступление питательных веществ к плоду, но, кроме того, схема ветвления хорионических артерий, когда они расходятся по хорионической пластинке, будет различаться в зависимости от положения введения пуповины. Предсказать влияние этих различий на сопротивление сети сложно. Когда прикрепление пуповины является центральным, паттерн ветвления артерий преимущественно дихотомический, тогда как при эксцентричном прикреплении пуповины преобладает моноподиальный паттерн ветвления (Gordon et al., 2007). Моделирование показывает, что потери энергии минимальны в точках моноподиального ветвления, и, следовательно, этот образец может быть предпочтительным для обеспечения равномерного распределения кровотока, когда необходимо пройти относительно большие расстояния через хорионическую пластинку (Gordon et al., 2007). Однако в большинстве плацент паттерн ветвления представляет собой смесь двух типов, что затрудняет прогнозирование сосудистого сопротивления, обеспечиваемого хорионическими артериями.
Развитие периферических компонентов ворсинчатых деревьев, промежуточных и терминальных ворсинок, экспоненциально увеличивается примерно с 20 недель беременности (Jackson et al., 1992). Капиллярная сеть плода развивается соразмерно и в срок включает ~ 550 км капилляров и содержит ~ 35 мл фетальной крови (Burton and Jauniaux, 1995). Ворсинки расположены в 30–40 долек плода, каждая из которых снабжается материнской кровью по спиральной артерии и представляет собой независимую единицу обмена матери и плода.
Внутри терминальных ворсинок существуют многочисленные связи между отдельными капиллярами (Jirkovská et al., 2008; Plitman Mayo et al., 2016a).Эти соединения создают ряд, казалось бы, параллельных контуров, и возможно, что поток движется в разных направлениях в разное время в соответствии с местными перепадами давления. Моделирование предполагает, что направление потока через сеть мало влияет на эффективность диффузионного обмена (Plitman Mayo et al., 2016b). Локализованные расширения капилляров плода, называемые синусоидами, возникают по всей их длине, особенно в местах резких изгибов.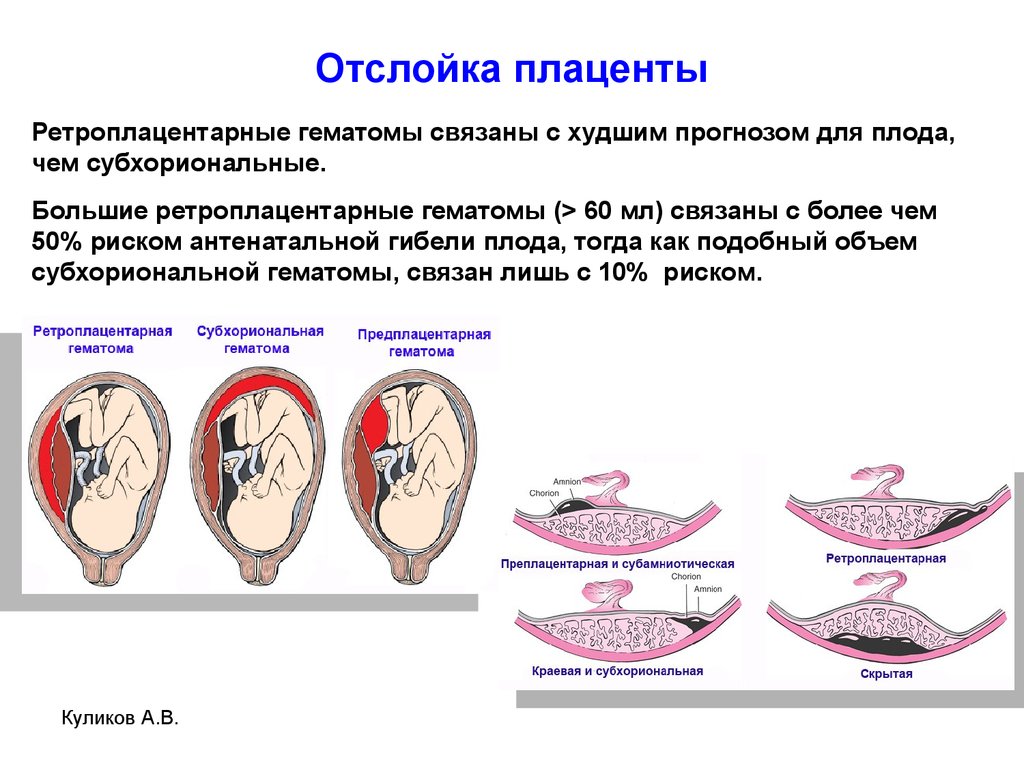 Было высказано предположение, что синусоиды служат для снижения сопротивления внутри капиллярной петли и тем самым обеспечивают равномерную перфузию внутри ворсинки или ряда ворсинок (Kaufmann et al., 1988). Однако они могут иметь и другие функции, поскольку синусоиды приводят внешнюю стенку своего капилляра в тесный контакт с внутренней поверхностью трофобластного эпителия, покрывающего ворсинки, который локально истончается. В результате ворсинчатая мембрана, разделяющая кровообращение матери и плода, чрезвычайно ослаблена, и эти участки, называемые васкулосинцитиальными мембранами, являются наиболее важными местами для диффузионного обмена (Plitman Mayo et al., 2016b). Локальное увеличение площади поперечного сечения капилляров также приводит к замедлению скорости потока, облегчая обмен.
Было высказано предположение, что синусоиды служат для снижения сопротивления внутри капиллярной петли и тем самым обеспечивают равномерную перфузию внутри ворсинки или ряда ворсинок (Kaufmann et al., 1988). Однако они могут иметь и другие функции, поскольку синусоиды приводят внешнюю стенку своего капилляра в тесный контакт с внутренней поверхностью трофобластного эпителия, покрывающего ворсинки, который локально истончается. В результате ворсинчатая мембрана, разделяющая кровообращение матери и плода, чрезвычайно ослаблена, и эти участки, называемые васкулосинцитиальными мембранами, являются наиболее важными местами для диффузионного обмена (Plitman Mayo et al., 2016b). Локальное увеличение площади поперечного сечения капилляров также приводит к замедлению скорости потока, облегчая обмен.
Начало хорионического кровообращения
Эмбриональное сердце начинается как примитивная трубка, и первые сокращения наблюдаются примерно через 22 дня (начало 5-й недели после последней менструации).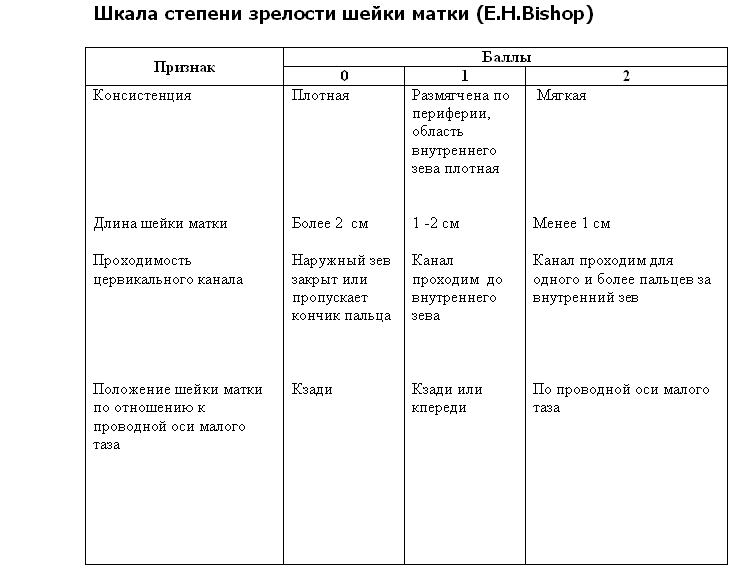 Сердце начинает биться до развития проводящей системы и до того, как сформируется компетентный клапанный механизм (Collins, 2016). Примитивные двусторонние аорты, каждая из которых состоит из вентральной и дорсальной частей, сливаются в течение 4-й эмбриональной недели (6 недель LMP), образуя единую дефинитивную нисходящую аорту.Пупочные артерии соединяются с примитивной дорсальной аортой (рис. 1). Сердечный выброс и частота сердечных сокращений увеличиваются пропорционально развивающемуся эмбриональному телу. К 10 неделям частота сердечных сокращений плода достигает своего пика на уровне около 170 ударов в минуту (ударов в минуту), а затем снижается до 120–160 ударов в минуту до конца беременности (van Heeswijk et al., 1990). Аномально медленная (Doubilet and Benson, 2005) и высокая (Doubilet et al., 2000) частота сердечных сокращений на втором месяце беременности связана с высоким риском гибели эмбриона.Предполагается, что последующая гипоперфузия вторичного желточного мешка, вызывающая прогрессирующую потерю структуры и некроз или отек, может объяснить, почему при беременности, обреченной на выкидыш, изменения диаметра мешка могут предшествовать остановке сердца эмбриона на несколько дней.
Сердце начинает биться до развития проводящей системы и до того, как сформируется компетентный клапанный механизм (Collins, 2016). Примитивные двусторонние аорты, каждая из которых состоит из вентральной и дорсальной частей, сливаются в течение 4-й эмбриональной недели (6 недель LMP), образуя единую дефинитивную нисходящую аорту.Пупочные артерии соединяются с примитивной дорсальной аортой (рис. 1). Сердечный выброс и частота сердечных сокращений увеличиваются пропорционально развивающемуся эмбриональному телу. К 10 неделям частота сердечных сокращений плода достигает своего пика на уровне около 170 ударов в минуту (ударов в минуту), а затем снижается до 120–160 ударов в минуту до конца беременности (van Heeswijk et al., 1990). Аномально медленная (Doubilet and Benson, 2005) и высокая (Doubilet et al., 2000) частота сердечных сокращений на втором месяце беременности связана с высоким риском гибели эмбриона.Предполагается, что последующая гипоперфузия вторичного желточного мешка, вызывающая прогрессирующую потерю структуры и некроз или отек, может объяснить, почему при беременности, обреченной на выкидыш, изменения диаметра мешка могут предшествовать остановке сердца эмбриона на несколько дней. (Датта и Раут, 2017).
(Датта и Раут, 2017).
Хотя внутри первых ворсинок видна обширная капиллярная сеть, имеется мало свидетельств эффективного хорионического кровообращения в течение первого триместра. Капилляры остаются небольшого калибра и заполнены крупными ядросодержащими эритроцитами плода, выходящими из вторичного желточного мешка, которые плотно упакованы вместе (рис. 2).Наличие ядер делает эритроциты менее деформируемыми, чем их зрелые формы, и, таким образом, кровь имеет высокую вязкость (Jauniaux et al., 1991c). Примитивные эритроциты характеризуются присутствием эмбриональных глобинов с высоким кислородным сродством (Manning et al., 2017). Когда дефинитивный эритропоэз начинается в печени плода примерно на 8 неделе беременности (Baron et al., 2013), количество ядерных эритроцитов падает (Jauniaux et al., 1991b) и происходит переключение на глобины плода / взрослого.Точно так же серийные реконструкции эмбрионов на этой стадии развития показывают, что связь между нисходящей аортой и пупочным кровообращением чрезвычайно узкая (Corner, 1929). Первоначально интерпретированное Корнером как свидетельство того, что два кровообращения дифференцируются независимо in situ , сужение должно ограничивать кровоток к плаценте, возможно, защищая формирующееся сердце от высокого сопротивления плацентарного кровообращения в этом процессе. Эти ограничения на установление обеих плацентарных циркуляций в течение первых 2 месяцев беременности подтверждают концепцию о том, что развивающийся эмбрион и его плацента защищены от чрезмерного воздействия кислорода в течение чувствительного периода органогенеза (Jauniaux et al., 2003b). Комбинация анатомических и физиологических барьеров обеспечивает эмбрион всем необходимым для его развития (Jauniaux et al., 2003c).
Первоначально интерпретированное Корнером как свидетельство того, что два кровообращения дифференцируются независимо in situ , сужение должно ограничивать кровоток к плаценте, возможно, защищая формирующееся сердце от высокого сопротивления плацентарного кровообращения в этом процессе. Эти ограничения на установление обеих плацентарных циркуляций в течение первых 2 месяцев беременности подтверждают концепцию о том, что развивающийся эмбрион и его плацента защищены от чрезмерного воздействия кислорода в течение чувствительного периода органогенеза (Jauniaux et al., 2003b). Комбинация анатомических и физиологических барьеров обеспечивает эмбрион всем необходимым для его развития (Jauniaux et al., 2003c).
Рисунок 2 . Развитие сосудистой сети плаценты. (A) Плацентарные ворсинки гестационного возраста 6 недель до начала циркуляции хориона, что свидетельствует о наличии ядерных эритроцитов в развивающихся капиллярах плода (указано стрелкой). (B) Ворсинки на сроке гестации 14 недель, показывающие присутствие неядерных эритроцитов в более крупных сосудах внутри стромального ядра, что свидетельствует о начале хорионического кровообращения. (C) Ворсинки гестационного возраста 27 недель. К настоящему времени прорабатываются более мелкие периферические ворсинки. (D) Ворсинки гестационного возраста 40 недель с хорошо васкуляризованными терминальными ворсинками. Масштаб для всех изображений = 50 мкм. Пятно; гематоксилин и эозин для всех.
(B) Ворсинки на сроке гестации 14 недель, показывающие присутствие неядерных эритроцитов в более крупных сосудах внутри стромального ядра, что свидетельствует о начале хорионического кровообращения. (C) Ворсинки гестационного возраста 27 недель. К настоящему времени прорабатываются более мелкие периферические ворсинки. (D) Ворсинки гестационного возраста 40 недель с хорошо васкуляризованными терминальными ворсинками. Масштаб для всех изображений = 50 мкм. Пятно; гематоксилин и эозин для всех.
Хорионическое кровообращение прогрессивно развивается на 3-м месяце беременности и совпадает с установлением артериального притока в межворсинчатое пространство плаценты (Jauniaux et al., 2000).Как координируется начало этих двух кровообращений, неизвестно, но сигналы могут заключаться в изменении перепада давления на ворсинчатой мембране после расширения межворсинчатого пространства, связанного с этим увеличения оксигенации или изменений в выработке местных цитокинов или гормонов вторичным трофобластом. к увеличению напряжения сдвига на поверхности ворсинок.
к увеличению напряжения сдвига на поверхности ворсинок.
Установление материнского артериального кровообращения к плаценте
Вопреки многим стандартным описаниям в учебниках по эмбриологии, артериальное кровообращение матери к плаценте человека не устанавливается полностью при нормальной беременности до конца первого триместра (Jauniaux et al., 2000). В течение первых недель беременности спиральные артерии матери, которые в конечном итоге будут снабжать плаценту, претерпевают обширное ремоделирование, которое включает потерю эластина и гладких мышц их стенок и расширение терминальных сегментов, которые открываются в межворсинчатое пространство (Harris, 2010). Это ремоделирование обеспечивает постоянный высокий объем материнского кровотока через плаценту после начала кровообращения в конце первого триместра, но с низкой скоростью и давлением, что позволяет избежать механического повреждения ворсинок и обеспечивает адекватное время прохождения крови для матери. -плодный обмен (Burton et al. , 2009).
, 2009).
Ремоделирование достигается за счет действия клеток вневорсинчатого трофобласта (EVT), которые мигрируют из плаценты в нижележащую децидуальную оболочку, как через строму, так и вниз по просветам спиральных артерий в качестве интерстициального и эндоваскулярного трофобласта соответственно. Величина эндоваскулярной миграции такова, что устья артерий эффективно закупорены в течение большей части первого триместра (Hustin and Schaaps, 1987; Burton et al., 1999), и только сеть межклеточных пространств соединяет просвет артерии с ней. межворсинчатое пространство (рисунок 3).Плазма может проходить через эти пространства с медленной скоростью, но эритроциты в значительной степени исключены. Следовательно, плацента заполнена прозрачной жидкостью на протяжении большей части первого триместра (Hustin et al., 1988), а концентрация кислорода относительно низкая (Jauniaux et al., 1999, 2000), хотя нет никаких доказательств того, что плацентарный ткани гипоксичны (Cindrova-Davies et al. , 2015). Гистотрофное питание желез эндометрия способствует поддержанию концепции в настоящее время (Burton et al., 2002) и обеспечивает богатый запас глюкозы для поддержания гликолиза (Burton et al., 2017).
, 2015). Гистотрофное питание желез эндометрия способствует поддержанию концепции в настоящее время (Burton et al., 2002) и обеспечивает богатый запас глюкозы для поддержания гликолиза (Burton et al., 2017).
Рисунок 3 . Цветное допплеровское картирование маточно-плацентарного кровообращения на 7 неделе 2 дня беременности, показывающее отсутствие кровообращения в плаценте (P). ECC, экзоколеомная полость; F, плод.
К концу первого триместра сеть межклеточных пространств постепенно сливается и расширяется, образуя каналы через эндоваскулярные «пробки», позволяя материнской артериальной крови свободно течь в межворсинчатое пространство (Burton et al., 1999; Roberts et al., 2017). Это развитие было задокументировано с помощью ультразвукового исследования, но лучше всего подтверждается трехкратным увеличением концентрации кислорода в плаценте между 10 и 12 неделями беременности, измеренным с помощью внутриартериального зонда (Jauniaux et al., 2000). Это повышение оксигенации и / или увеличение напряжения сдвига на поверхности ворсинок, вызванное кровотоком матери, который на этой стадии все еще пульсирует (Collins et al. , 2012), может стимулировать высвобождение местных вазодилататоров, таких как оксид азота (NO) из синцитиотрофобласта.Такие агенты, в свою очередь, могут действовать на близко расположенные капилляры плода, тем самым открывая хорионическое кровообращение. Это привлекательная гипотеза, но ее еще предстоит проверить; синцитиотрофобласт содержит синтазу оксида азота (NOS) (Myatt et al., 1993), но пока нет доступных данных, указывающих на чувствительность этого фермента к напряжению сдвига.
, 2012), может стимулировать высвобождение местных вазодилататоров, таких как оксид азота (NO) из синцитиотрофобласта.Такие агенты, в свою очередь, могут действовать на близко расположенные капилляры плода, тем самым открывая хорионическое кровообращение. Это привлекательная гипотеза, но ее еще предстоит проверить; синцитиотрофобласт содержит синтазу оксида азота (NOS) (Myatt et al., 1993), но пока нет доступных данных, указывающих на чувствительность этого фермента к напряжению сдвига.
Нарушения ремоделирования спиральной артерии связаны с рядом осложнений беременности, включая выкидыш, преэклампсию, задержку роста плода (FGR) и преждевременные роды (Brosens et al., 2011). Как будет обсуждаться позже, возможно, что дефекты сердечного миогенеза возникают вторично по отношению к плохой плацентации из-за неправильной перфузии плаценты и генерации чрезмерного внутриплацентарного оксидативного стресса.
Оценка хорионического кровообращения
in vivo Появление ультразвуковой допплеровской визуализации позволило отслеживать характеристики хорионического кровообращения на ранних сроках беременности путем мониторинга форм волн в пупочных артериях и их основных внутриплацентарных ветвях (Jauniaux et al. , 1991c, 1992). Ранние исследования показали взаимосвязь с продвижением беременности между изменениями формы волны скорости потока на допплеровском изображении и морфологическим развитием ворсинчатых деревьев и содержащихся в них капиллярных сетей (Loquet et al., 1988; Jauniaux et al., 1991b; Huisman et al. ., 1992; Mercé et al., 1996). Все эти исследования показали серьезные изменения в сопротивлении кровотоку в пуповинно-плацентарной системе кровообращения в период перехода между первым и вторым триместрами.До 10 недели беременности конечный диастолический кровоток в пуповине отсутствует, что свидетельствует о высоком сопротивлении (рис. 4). Конечный диастолический кровоток постепенно появляется в пуповине между 12 и 14 неделями беременности (рис. 5), что указывает на снижение сопротивления и обеспечение непрерывной перфузии ворсин дефинитивной плаценты в течение всего сердечного цикла (Jauniaux et al., 1991b ). Механизм снижения сопротивления сосудов через фетоплацентарный кровоток во втором триместре неизвестен.
, 1991c, 1992). Ранние исследования показали взаимосвязь с продвижением беременности между изменениями формы волны скорости потока на допплеровском изображении и морфологическим развитием ворсинчатых деревьев и содержащихся в них капиллярных сетей (Loquet et al., 1988; Jauniaux et al., 1991b; Huisman et al. ., 1992; Mercé et al., 1996). Все эти исследования показали серьезные изменения в сопротивлении кровотоку в пуповинно-плацентарной системе кровообращения в период перехода между первым и вторым триместрами.До 10 недели беременности конечный диастолический кровоток в пуповине отсутствует, что свидетельствует о высоком сопротивлении (рис. 4). Конечный диастолический кровоток постепенно появляется в пуповине между 12 и 14 неделями беременности (рис. 5), что указывает на снижение сопротивления и обеспечение непрерывной перфузии ворсин дефинитивной плаценты в течение всего сердечного цикла (Jauniaux et al., 1991b ). Механизм снижения сопротивления сосудов через фетоплацентарный кровоток во втором триместре неизвестен. Между 9 и 15 неделями концентрации NO в ворсинчатой ткани и циклического гуанозинмонофосфата (цГМФ) положительно коррелируют с импедансом пупочной артерии, что позволяет предположить, что эти молекулы модулируют снижение сопротивления в пупочно-плацентарной циркуляции, которое происходит в первом триместре беременности (Lees и др., 1998). Прохождение фетальной крови через анатомически высокий контур сопротивления может, возможно, привести к стимуляции эндотелиальной активности NOS, таким образом поддерживая расширение сосудов в пупочно-плацентарной циркуляции до тех пор, пока не произойдет дальнейшее развитие ворсинчатого дерева.С другой стороны, это может быть связано с заменой ядерных эритроцитов их более легко деформируемыми безъядерными аналогами (Jauniaux et al., 1991b).
Между 9 и 15 неделями концентрации NO в ворсинчатой ткани и циклического гуанозинмонофосфата (цГМФ) положительно коррелируют с импедансом пупочной артерии, что позволяет предположить, что эти молекулы модулируют снижение сопротивления в пупочно-плацентарной циркуляции, которое происходит в первом триместре беременности (Lees и др., 1998). Прохождение фетальной крови через анатомически высокий контур сопротивления может, возможно, привести к стимуляции эндотелиальной активности NOS, таким образом поддерживая расширение сосудов в пупочно-плацентарной циркуляции до тех пор, пока не произойдет дальнейшее развитие ворсинчатого дерева.С другой стороны, это может быть связано с заменой ядерных эритроцитов их более легко деформируемыми безъядерными аналогами (Jauniaux et al., 1991b).
Рисунок 4 . Кривые скорости кровотока в пупочной артерии через 10 недель и 6 дней показывают отсутствие конечного диастолического кровотока во всех сердечных циклах.
Рисунок 5 . Кривые скорости потока в пупочной артерии через 13 недель и 1 день показывают частичный конечный диастолический кровоток. В некоторых сердечных циклах кровоток наблюдается на протяжении почти всей диастолической фазы, что указывает на снижение сосудистого сопротивления в пупочно-плацентарном сосудистом русле.
Кривые скорости потока в пупочной артерии через 13 недель и 1 день показывают частичный конечный диастолический кровоток. В некоторых сердечных циклах кровоток наблюдается на протяжении почти всей диастолической фазы, что указывает на снижение сосудистого сопротивления в пупочно-плацентарном сосудистом русле.
Пиковая систолическая скорость увеличивается более чем в три раза между 7 и 10 неделями, а индекс сопротивления пуповины резко снижается примерно через 10 недель (Mäkikallio et al., 2005). Поскольку диаметр пути оттока увеличивается за тот же период, авторы пришли к выводу, что должно быть значительное увеличение пупочно-плацентарного объема кровотока в конце первого триместра. Это увеличение временно совпадает с завершением сердечного органогенеза (Gittenberger-de Groot et al., 2013), и с началом двухфазного диастолического наполнения предсердий, что свидетельствует об более активном пупочно-плацентарном кровообращении и повышенном венозном возврате к сердцу (Mäkikallio et al. , 2005). Поскольку сосудистая сеть плаценты показывает только постепенные изменения длины и диаметра сосудов в течение этого периода (Jauniaux et al., 1991a), эти гемодинамические изменения должны предположительно отражать открытие либо соединения между аортой и пупочными артериями, либо существующих капилляров внутри ворсинок и уменьшение количества ядерных эритроцитов и, следовательно, общей вязкости крови.
, 2005). Поскольку сосудистая сеть плаценты показывает только постепенные изменения длины и диаметра сосудов в течение этого периода (Jauniaux et al., 1991a), эти гемодинамические изменения должны предположительно отражать открытие либо соединения между аортой и пупочными артериями, либо существующих капилляров внутри ворсинок и уменьшение количества ядерных эритроцитов и, следовательно, общей вязкости крови.
Во время нормальной беременности постепенное снижение сопротивления кровотоку в пупочной артерии продолжается во втором и третьем триместрах, отражая увеличение сосудистой сети плаценты и / или развитие периферических ворсинок и создание более параллельных цепей. При беременности, осложненной тяжелым течением FGR, сопротивление может снова увеличиваться во второй половине беременности, что приводит к отсутствию или даже обратному конечному диастолическому кровотоку. У них есть следующие патологические корреляты.
Патология плаценты и развитие сердца плода
Эпидемиологические данные связывают индивидуальный риск сердечных заболеваний с различными характеристиками плаценты, включая ее вес, площадь поверхности и толщину (Barker et al. , 2010, 2012; Eriksson et al., 2011). Хотя можно было ожидать, что изменение развития плаценты влияет на развитие сердца плода, как это происходит со многими другими органами, экспериментальных доказательств прямой связи мало. Сообщалось, что манипуляции с рецептором пероксисомного пролифератора-активатора (PPAR) или митоген-активируемым протеином (MAP) киназными путями в плаценте сами по себе вызывают сердечные дефекты у мышей (Barak et al., 1999; Адамс и др., 2000). Механизмы остаются неизвестными, и необходимы дальнейшие исследования, чтобы полностью оценить степень того, что было названо осью сердце-плацента (Linask, 2013).
, 2010, 2012; Eriksson et al., 2011). Хотя можно было ожидать, что изменение развития плаценты влияет на развитие сердца плода, как это происходит со многими другими органами, экспериментальных доказательств прямой связи мало. Сообщалось, что манипуляции с рецептором пероксисомного пролифератора-активатора (PPAR) или митоген-активируемым протеином (MAP) киназными путями в плаценте сами по себе вызывают сердечные дефекты у мышей (Barak et al., 1999; Адамс и др., 2000). Механизмы остаются неизвестными, и необходимы дальнейшие исследования, чтобы полностью оценить степень того, что было названо осью сердце-плацента (Linask, 2013).
Связь между пороками сердца и аномалиями плаценты была обнаружена после патологического исследования плаценты после родов. Таким образом, синдром гипоплазии левых отделов сердца был связан с уменьшением веса плаценты, незрелостью ворсинок с уменьшением васкуляризации и васкулосинцитиальных мембран, а также с увеличением отложения фибрина (Jones et al., 2015). Неизвестно, опосредованы ли эффекты снижением эффективности транспорта, изменением эндокринной функции — было повышение уровня лептина в плаценте или гемодинамические изменения в пуповине. О тенденции к уменьшению объема плаценты также сообщалось в проспективном исследовании сложных врожденных пороков сердца с использованием МРТ, а отсутствие статистической значимости может быть связано с относительно небольшим размером выборки (Andescavage et al., 2015). Сильная связь с FGR была недавно обнаружена у женщин, вынашивающих плод с врожденным пороком сердца и имеющих более высокий риск (отношение шансов 3.32; 95% ДИ от 2,39 до 4,56) для веса при рождении ниже 3-го центиля (Ruiz et al., 2016). Эксцентрическое введение пуповины также было связано с более высоким риском врожденного порока сердца (отношение шансов 2,33–3,76) (Albalawi et al., 2017). Основными дефектами были конотрункальные и лево-правые пороки сердца, и снова была связь с FGR. Наконец, тромботическая васкулопатия плода была связана с шестикратным увеличением врожденных пороков сердца (Saleemuddin et al.
Неизвестно, опосредованы ли эффекты снижением эффективности транспорта, изменением эндокринной функции — было повышение уровня лептина в плаценте или гемодинамические изменения в пуповине. О тенденции к уменьшению объема плаценты также сообщалось в проспективном исследовании сложных врожденных пороков сердца с использованием МРТ, а отсутствие статистической значимости может быть связано с относительно небольшим размером выборки (Andescavage et al., 2015). Сильная связь с FGR была недавно обнаружена у женщин, вынашивающих плод с врожденным пороком сердца и имеющих более высокий риск (отношение шансов 3.32; 95% ДИ от 2,39 до 4,56) для веса при рождении ниже 3-го центиля (Ruiz et al., 2016). Эксцентрическое введение пуповины также было связано с более высоким риском врожденного порока сердца (отношение шансов 2,33–3,76) (Albalawi et al., 2017). Основными дефектами были конотрункальные и лево-правые пороки сердца, и снова была связь с FGR. Наконец, тромботическая васкулопатия плода была связана с шестикратным увеличением врожденных пороков сердца (Saleemuddin et al. , 2010).
, 2010).
Отделить эффекты функции плаценты от эффектов аберрантной пупочной гемодинамики в ситуации человека сложно. Экспериментальные манипуляции на животных моделях показали, что гемодинамика внутри желточного или пупочного кровотока может иметь большое влияние на дифференциацию кардиомиоцитов и развитие сердца (Kowalski et al., 2014; Midgett et al., 2017). Общая тема многих патологических исследований — это ЛГР. Как описано ранее, эти беременности часто связаны с отсутствием или изменением конечного диастолического артериального кровотока в пуповине, что свидетельствует о повышенном сопротивлении сосудов плаценты (Arbeille, 1997; Soregaroli et al., 2002). Морфологические исследования, направленные на поиск коррелятов после родов, были сосредоточены на артериях внутри ворсинок ствола, которые, как полагают, являются основными сосудами сопротивления в плацентарной циркуляции. Хотя не происходит уменьшения количества сосудов внутри ворсинок (Jackson et al., 1995), что позволяет предположить, что васкулогенез и ангиогенез изначально были нормальными, были постоянные сообщения о медиальной гипертрофии и уменьшении просвета просвета (Fok et al. , 1990; Salafia et al., 1997; Mitra et al., 2000).
, 1990; Salafia et al., 1997; Mitra et al., 2000).
Мы недавно продемонстрировали, что эти изменения можно имитировать in vitro , подвергая артериальные эксплантаты, взятые из доношенной плаценты, окислительному стрессу (Lu et al., 2017). Индукция стресса вызывает подавление активности фермента цистатионин-γ-лиазы, который генерирует сероводород, являющийся трансмиттером газа. Сероводород поддерживает клетки гладких мышц сосудов в дифференцированном состоянии, а блокирование его производства заставляет клетки принимать патологический пролиферативный фенотип.Как обсуждалось ранее, беременности, осложненные FGR, обычно связаны с плохой плацентацией и недостаточным ремоделированием материнских спиральных артерий (Brosens et al., 2011). Аберрантное ремоделирование является мощным индуктором оксидативного стресса плаценты либо из-за повышенного напряжения сдвига на поверхности ворсинок, либо из-за неправильной перфузии и повреждения типа ишемии-реперфузии (Burton and Jauniaux, 2011). Поэтому мы предполагаем, что изменение сопротивления сосудов плаценты и формы волны пупочной артерии является вторичным по отношению к усилению оксидативного стресса плаценты на более поздних сроках беременности, хотя патофизиологические семена появляются в первом триместре.Влияние на сердце плода в настоящее время неизвестно, но можно предположить, что повышенное сопротивление пупочно-плацентарного кровообращения вызывает определенную степень гиперплазии.
Поэтому мы предполагаем, что изменение сопротивления сосудов плаценты и формы волны пупочной артерии является вторичным по отношению к усилению оксидативного стресса плаценты на более поздних сроках беременности, хотя патофизиологические семена появляются в первом триместре.Влияние на сердце плода в настоящее время неизвестно, но можно предположить, что повышенное сопротивление пупочно-плацентарного кровообращения вызывает определенную степень гиперплазии.
Выводы
Развитие сердца и плаценты, вероятно, тесно взаимосвязано через несколько механизмов. Во-первых, неправильная плацентация приводит к задержке роста плода, а нарушение снабжения питательными веществами или неблагоприятная эндокринная среда плода могут оказывать неспецифическое влияние на рост и дифференциацию многих систем органов (Burton et al., 2016). Недавнее исследование на приматах, отличных от человека, показало, что ограничение роста имитирует ускоренное старение сердца (Kuo et al., 2017), но подробное рассмотрение этих эффектов выходит за рамки настоящего обзора. Во-вторых, сердечные и плацентарные аномалии могут сосуществовать из-за полиморфизма в генетических путях развития, общих для обоих органов, в частности, регулируемых с помощью передачи сигналов Wnt / ß-катенина, или из-за отсутствия ключевых микронутриентов, таких как фолиевая кислота (Linask, 2013). Во время эволюции генные сети, лежащие в основе развития других органов, были задействованы плацентой (Cross et al., 2003), и поэтому основные процессы, такие как клеточная адгезия и ангиогенез, разделяются с сердцем. Следовательно, нарушение интегрина альфа 4 или его лигандной молекулы адгезии сосудистых клеток (VCAM-1) связано как с основными плацентарными, так и с сердечными аномалиями. В плаценте происходит нарушение слияния аллантоиса с хорионом, тогда как в сердце наблюдается аберрантное развитие эпикарда и коронарных сосудов (Kwee et al., 1995; Yang et al., 1995). Аналогичная ситуация возникает с Hand-1 (McFadden et al., 2005), при этом эмбрионы мышей с нокаутом умирают на E8.5 из-за плацентарной недостаточности.
Во-вторых, сердечные и плацентарные аномалии могут сосуществовать из-за полиморфизма в генетических путях развития, общих для обоих органов, в частности, регулируемых с помощью передачи сигналов Wnt / ß-катенина, или из-за отсутствия ключевых микронутриентов, таких как фолиевая кислота (Linask, 2013). Во время эволюции генные сети, лежащие в основе развития других органов, были задействованы плацентой (Cross et al., 2003), и поэтому основные процессы, такие как клеточная адгезия и ангиогенез, разделяются с сердцем. Следовательно, нарушение интегрина альфа 4 или его лигандной молекулы адгезии сосудистых клеток (VCAM-1) связано как с основными плацентарными, так и с сердечными аномалиями. В плаценте происходит нарушение слияния аллантоиса с хорионом, тогда как в сердце наблюдается аберрантное развитие эпикарда и коронарных сосудов (Kwee et al., 1995; Yang et al., 1995). Аналогичная ситуация возникает с Hand-1 (McFadden et al., 2005), при этом эмбрионы мышей с нокаутом умирают на E8.5 из-за плацентарной недостаточности. В-третьих, серьезные аномалии, такие как транспозиции, могут возникнуть, если плацента не может функционировать как селективный барьер для ксенобиотиков и других тератогенов. Наконец, основное внимание здесь уделяется тому, что отклоняющаяся от нормы гемодинамика пупочно-плацентарного кровообращения может влиять на развитие сердца. Поскольку это кровообращение устанавливается только к концу периода органогенеза сердца, более вероятно, что проблемы с плацентой влияют на биомеханическую дифференцировку сердца на более поздних сроках беременности, когда плацента получает ~ 40% сердечного выброса плода.Изменения сопротивления пупочных сосудов из-за тромботической васкулопатии или медиальной гиперплазии в артериях стволовых ворсинок могут влиять на дифференцировку кардиомиоцитов, что приводит к гипо- или гиперпластическим синдромам. Для проверки этой гипотезы требуются дополнительные исследования, но если она окажется верной, то вмешательство, например донорство сероводорода, может оказаться полезным (Lu et al.
В-третьих, серьезные аномалии, такие как транспозиции, могут возникнуть, если плацента не может функционировать как селективный барьер для ксенобиотиков и других тератогенов. Наконец, основное внимание здесь уделяется тому, что отклоняющаяся от нормы гемодинамика пупочно-плацентарного кровообращения может влиять на развитие сердца. Поскольку это кровообращение устанавливается только к концу периода органогенеза сердца, более вероятно, что проблемы с плацентой влияют на биомеханическую дифференцировку сердца на более поздних сроках беременности, когда плацента получает ~ 40% сердечного выброса плода.Изменения сопротивления пупочных сосудов из-за тромботической васкулопатии или медиальной гиперплазии в артериях стволовых ворсинок могут влиять на дифференцировку кардиомиоцитов, что приводит к гипо- или гиперпластическим синдромам. Для проверки этой гипотезы требуются дополнительные исследования, но если она окажется верной, то вмешательство, например донорство сероводорода, может оказаться полезным (Lu et al. , 2017).
, 2017).
Авторские взносы
Все перечисленные авторы внесли существенный, прямой и интеллектуальный вклад в работу и одобрили ее к публикации.
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Благодарности
Авторы выражают признательность за вклад, внесенный в идеи, представленные здесь, их многочисленными коллегами на протяжении многих лет, а также за щедрость финансирующих агентств, поддержавших их исследования.
Список литературы
Адамс, Р.Х., Поррас, А., Алонсо, Г., Джонс, М., Винтерстен, К., Панелли, С. и др. (2000). Существенная роль киназы p38alpha MAP в плацентарном, но не эмбриональном сердечно-сосудистом развитии. Мол. Cell 6, 109–116. DOI: 10.1016 / S1097-2765 (05) 00014-6
CrossRef Полный текст | Google Scholar
Альбалави А. , Бранкузи Ф., Аскин Ф., Эхсанипур Р., Ван Дж., Бурд И. и др. (2017). Плацентарные особенности плодов с врожденным пороком сердца. J. Ultrasound Med. 36, 965–972. DOI: 10.7863 / ультра.16.04023
, Бранкузи Ф., Аскин Ф., Эхсанипур Р., Ван Дж., Бурд И. и др. (2017). Плацентарные особенности плодов с врожденным пороком сердца. J. Ultrasound Med. 36, 965–972. DOI: 10.7863 / ультра.16.04023
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Andescavage, N., Yarish, A., Donofrio, M., Bulas, D., Evangelou, I., Vezina, G., et al. (2015). Трехмерная объемная МРТ-оценка плаценты у плодов со сложным врожденным пороком сердца. Плацента 36, 1024–1030. DOI: 10.1016 / j.placenta.2015.06.013
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Аплин, Дж. Д., Уиттакер, Х., Яна Лим, Ю. Т., Свитлик, С., Чарнок, Дж., И Джонс, К. Дж. (2015). Гемангиобластные очаги в плаценте первого триместра человека: распределение и гестационный профиль. Плацента 36, 1069–1077. DOI: 10.1016 / j.placenta.2015.08.005
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Барак Ю., Нельсон М. К., Онг, Э. С., Джонс, Ю. З., Руис-Лозано, П., Чиен, К. Р. и др. (1999). Гамма PPAR необходима для развития плацентарной, сердечной и жировой ткани. Мол. Cell 4, 585–595. DOI: 10.1016 / S1097-2765 (00) 80209-9
З., Руис-Лозано, П., Чиен, К. Р. и др. (1999). Гамма PPAR необходима для развития плацентарной, сердечной и жировой ткани. Мол. Cell 4, 585–595. DOI: 10.1016 / S1097-2765 (00) 80209-9
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Баркер Д. Дж., Ларсен Г., Осмонд К., Торнбург К. Л., Каянти Э. и Эрикссон Дж. Г. (2012). Плацентарные истоки внезапной сердечной смерти. Внутр. J. Epidemiol. 41, 1394–1399. DOI: 10.1093 / ije / dys116
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Баркер, Д. Дж., Торнбург, К. Л., Осмонд, К., Каянти, Э., и Эрикссон, Дж. Г. (2010). Площадь поверхности плаценты и гипертония у потомства в более зрелом возрасте. Внутр. J. Dev. Биол. 54, 525–530. DOI: 10.1387 / ijdb.082760db
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Brosens, I., Pijnenborg, R., Vercruysse, L., and Romero, R. (2011). «Великие акушерские синдромы» связаны с нарушениями глубокой плацентации. Am. J. Obstet. Гинеколь. 204, 193–201. DOI: 10.1016 / j.аджог.2010.08.009
Am. J. Obstet. Гинеколь. 204, 193–201. DOI: 10.1016 / j.аджог.2010.08.009
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бертон, Г. Дж., И Жонье, Э. (1995). Сонографические, стереологические и велосиметрические оценки допплеровского потока для оценки зрелости плаценты. Br. J. Obstet. Gynaecol. 102, 818–825. DOI: 10.1111 / j.1471-0528.1995.tb10849.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бертон, Г. Дж., Жоно, Э., и Чарнок-Джонс, Д. С. (2010). Влияние внутриутробной среды на развитие плаценты человека. Внутр. J. Dev. Биол. 54, 303–312. DOI: 10.1387 / ijdb.082764gb
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бертон, Дж. Дж., Жоно, Э., Мюррей, А. Дж. (2017). Кислородное и плацентарное развитие; параллели и различия с биологией опухоли. Плацента 56, 14–18. DOI: 10.1016 / j.placenta.2017.01.130
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бертон, Г. Дж., Жоно, Э., и Уотсон, А. Л. (1999).Материнские артериальные связи с межворсинчатым пространством плаценты в течение первого триместра беременности человека; Возвращение к коллекции Бойда. Am. J. Obstet. Гинеколь. 181, 718–724. DOI: 10.1016 / S0002-9378 (99) 70518-1
Дж., Жоно, Э., и Уотсон, А. Л. (1999).Материнские артериальные связи с межворсинчатым пространством плаценты в течение первого триместра беременности человека; Возвращение к коллекции Бойда. Am. J. Obstet. Гинеколь. 181, 718–724. DOI: 10.1016 / S0002-9378 (99) 70518-1
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бертон, Дж. Дж., Уотсон, А. Л., Хэмпсток, Дж., Скеппер, Дж. Н., и Жоно, Э. (2002). Маточные железы обеспечивают гистиотрофное питание плода человека в первом триместре беременности. J. Clin. Эндокринол. Метаб. 87, 2954–2959. DOI: 10.1210 / jcem.87.6.8563
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бертон, Дж. Дж., Вудс, А. В., Жоно, Э., и Королевство, Дж. К. (2009). Реологические и физиологические последствия преобразования материнских спиральных артерий в маточно-плацентарный кровоток во время беременности человека. Плацента 30, 473–482. DOI: 10.1016 / j.placenta.2009.02.009
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Циндрова-Дэвис, Т. , Jauniaux, E., Elliot, M. G., Gong, S., Burton, G.J., и Charnock-Jones, D. S. (2017). RNA-seq показывает сохранение функции желточных мешков человека, мыши и курицы. Proc. Natl. Акад. Sci. США 114, E4753 – E4761. DOI: 10.1073 / pnas.1702560114
, Jauniaux, E., Elliot, M. G., Gong, S., Burton, G.J., и Charnock-Jones, D. S. (2017). RNA-seq показывает сохранение функции желточных мешков человека, мыши и курицы. Proc. Natl. Акад. Sci. США 114, E4753 – E4761. DOI: 10.1073 / pnas.1702560114
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Циндрова-Дэвис, Т., ван Патот, М. Т., Гарднер, Л., Жонье, Э., Бертон, Г. Дж., И Чарнок-Джонс, Д. С. (2015). Энергетический статус и передача сигналов HIF в ворсинках хориона не показывают доказательств гипоксического стресса во время раннего развития плаценты у человека. Мол. Гм. Репрод. 21, 296–308. DOI: 10,1093 / мольхр / gau105
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Коллинз П. (2016). «Раннее эмбриональное кровообращение», в Grays Anatomy , ed S. Standring (Филадельфия, Пенсильвания: Elsevier), 200–204.
Коллинз, С. Л., Биркс, Дж. С., Стивенсон, Г. Н., Папагеоргиу, А. Т., Ноубл, Дж. А., и Импи, Л. (2012). Измерение струй спиральной артерии: общие принципы и различия, наблюдаемые при беременности с малым размером для гестационного возраста. Акушер УЗИ. Гинеколь. 40, 171–178. DOI: 10.1002 / uog.10149
(2012). Измерение струй спиральной артерии: общие принципы и различия, наблюдаемые при беременности с малым размером для гестационного возраста. Акушер УЗИ. Гинеколь. 40, 171–178. DOI: 10.1002 / uog.10149
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Корнер, Г. У. (1929). Хорошо сохранившийся человеческий эмбрион из 10 сомитов. Contrib. Эмбриол. 20, 81–102.
Google Scholar
Кросс, Дж. К., Бачик, Д., Добрич, Н., Хембергер, М., Хьюз, М., Симмонс, Д. Г. и др. (2003). Гены, развитие и эволюция плаценты. Плацента 24, 123–130. DOI: 10.1053 / plac.2002.0887
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Датта М. Р. и Раут А. (2017). Эффективность параметров УЗИ в первом триместре для прогнозирования самопроизвольного аборта на ранних сроках. Внутр. J. Gynaecol. Акушерство. 138, 325–330. DOI: 10.1002 / ijgo.12231
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Демир Р. , Кауфманн П., Кастеллуччи М., Эрбенги Т. и Котовски А. (1989). Васкулогенез и ангиогенез плода в ворсинах плаценты человека. Acta Anat. 136, 190–203. DOI: 10.1159 / 000146886
, Кауфманн П., Кастеллуччи М., Эрбенги Т. и Котовски А. (1989). Васкулогенез и ангиогенез плода в ворсинах плаценты человека. Acta Anat. 136, 190–203. DOI: 10.1159 / 000146886
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Doubilet, P. M., Benson, C. B., and Chow, J. S. (2000). Исход беременностей с учащенным сердцебиением эмбриона в начале первого триместра. Am. Ж. Рентгенол . 175, 67–69. DOI: 10.2214 / ajr.175.1.1750067
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Doubilet, P. M., and Benson, C. B. (2005). Исход беременностей в первом триместре с низкой частотой сердечных сокращений эмбриона на 6-7 неделях беременности и нормальной частотой сердечных сокращений к 8 неделям при УЗИ. Радиология 236, 643–646. DOI: 10.1148 / radiol.2362040880
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Эрикссон, Дж. Г., Каянти, Э., Торнбург, К. Л., Осмонд, К., и Баркер, Д. Дж. (2011). Размер тела матери и размер плаценты предсказывают ишемическую болезнь сердца у мужчин. Eur. Heart J. 32, 2297–2303. DOI: 10.1093 / eurheartj / ehr147
Размер тела матери и размер плаценты предсказывают ишемическую болезнь сердца у мужчин. Eur. Heart J. 32, 2297–2303. DOI: 10.1093 / eurheartj / ehr147
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Фок Р.Ю., Павлова З., Бениршке К., Пол Р. Х. и Платт Л. Д. (1990). Корреляция артериальных поражений с допплеровской велосиметрией пупочной артерии в плаценте при недоношенных беременностях. Акушерство. Гинеколь. 75, 578–583.
PubMed Аннотация | Google Scholar
Gittenberger-de Groot, A.C., Bartelings, M.M., Poelmann, R.E., Haak, M.C., and Jongbloed, M.R. (2013). Эмбриология сердца и ее влияние на понимание болезней сердца плода и новорожденного. Семин. Fetal Neonatal Med. 18, 237–244. DOI: 10.1016 / j.siny.2013.04.008
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гордон, З., Эйтан, О., Яффа, А. Дж., И Элад, Д. (2007). Кровоток плода в моделях ветвления сосудистой сети хорионической артерии. Ann. Акад. Sci. 1101, 250–265. DOI: 10.1196 / анналы.1389.037
Ann. Акад. Sci. 1101, 250–265. DOI: 10.1196 / анналы.1389.037
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Gulbis, B., Jauniaux, E., Cotton, F., and Stordeur, P. (1998). Белковые и ферментные структуры в жидких полостях гестационного мешка в первом триместре: отношение к абсорбционной роли вторичного желточного мешка. Мол. Гм. Репрод. 4, 857–862. DOI: 10,1093 / моль · ч / 4,9,857
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Харрис, Л. К. (2010). Обзор: взаимодействие трофобластов и сосудов на ранних сроках беременности: как реконструировать сосуд. Плацента 31 (Дополнение), S93 – S98. DOI: 10.1016 / j.placenta.2009.12.012
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хоув, Дж. Р., Кёстер, Р. В., Фороухар, А. С., Асеведо-Болтон, Г., Фрейзер, С.Э., и Гариб М. (2003). Силы внутрисердечной жидкости являются важным эпигенетическим фактором эмбрионального кардиогенеза. Природа 421, 172–177. DOI: 10.1038 / nature01282
Природа 421, 172–177. DOI: 10.1038 / nature01282
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хьюисман, Т. У., Стюарт, П. А., и Владимирофф, Дж. У. (1992). Допплерография нормального раннего кровообращения плода. Акушер УЗИ. Гинеколь. 2, 300–305. DOI: 10.1046 / j.1469-0705.1992.02040300.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хастин, Дж.и Шаапс Дж. П. (1987). Эхографо-анатомические исследования границы матернотрофобласта в первом триместре беременности. Am. J. Obstet. Гинеколь. 157, 162–168. DOI: 10.1016 / S0002-9378 (87) 80371-X
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хастин, Дж., Шаапс, Дж. П., и Ламботт, Р. (1988). Анатомические исследования маточно-плацентарной васкуляризации в I триместре беременности. Трофоб. Res. 3, 49–60.
Google Scholar
Джексон, М.Р., Мэйхью, Т. М., и Бойд, П. А. (1992). Количественное описание развития и созревания ворсинок от 10 недель беременности до срока. Плацента 13, 357–370. DOI: 10.1016 / 0143-4004 (92)-7
Плацента 13, 357–370. DOI: 10.1016 / 0143-4004 (92)-7
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Джексон, М. Р., Уолш, А. Дж., Морроу, Р. Дж., Маллен, Дж. Б., Лай, С. Дж. И Ричи, Дж. У. (1995). Уменьшение образования ворсинок плаценты при беременностях с малым для гестационного возраста беременностью: взаимосвязь с допплеровскими кривыми пупочной артерии. Am. J. Obstet. Гинеколь. 172, 518–525. DOI: 10.1016 / 0002-9378 (95)-9
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Jauniaux, E., Burton, G.J., Moscosco, G.J. и Hustin, J. (1991a). Развитие ранней плаценты: морфометрическое исследование. Плацента 12, 269–276.
PubMed Аннотация | Google Scholar
Jauniaux, E., Hempstock, J., Greenwold, N., and Burton, G.J. (2003a). Трофобластный оксидативный стресс в связи с временными и региональными различиями материнского плацентарного кровотока при нормальных и аномальных ранних беременностях. Am. J. Pathol. 162, 115–125. DOI: 10.1016 / S0002-9440 (10) 63803-5
Am. J. Pathol. 162, 115–125. DOI: 10.1016 / S0002-9440 (10) 63803-5
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Jauniaux, E., Gulbis, B., and Burton, G.J. (2003b). Гестационный мешок человека в первом триместре беременности ограничивает, а не способствует передаче кислорода плоду — обзор. Плацента 24 (Дополнение A), S86 – S93.
PubMed Аннотация | Google Scholar
Jauniaux, E., Gulbis, B., and Burton, G.J. (2003c). Физиологические последствия материнско-плодного градиента кислорода на ранних сроках беременности человека. Репродукция. Биомед. Интернет 7, 250–253.
PubMed Аннотация | Google Scholar
Jauniaux, E., Jurkovic, D., and Campbell, S. (1991b). in vivo исследования анатомии и физиологии раннего плацентарного кровообращения человека. УЗИ. Акушер. Гинеколь. 1, 435–445.
PubMed Аннотация | Google Scholar
Jauniaux, E., Jurkovic, D., Campbell, S., and Hustin, J. (1992). Допплеровские ультразвуковые особенности развивающегося плацентарного кровообращения: корреляция с анатомическими данными. Am. J. Obstet. Гинеколь. 166, 585–587. DOI: 10.1016 / 0002-9378 (92)
(1992). Допплеровские ультразвуковые особенности развивающегося плацентарного кровообращения: корреляция с анатомическими данными. Am. J. Obstet. Гинеколь. 166, 585–587. DOI: 10.1016 / 0002-9378 (92)
-4
CrossRef Полный текст | Google Scholar
Jauniaux, E., Jurkovic, D., Campbell, S., Kurjak, A., and Hustin, J. (1991c). Исследование плацентарного кровообращения с помощью цветного допплера. Am. J. Obstet. Гинеколь. 164, 486–488.
Google Scholar
Jauniaux, E., Jurkovic, D., Henriet, Y., Rodesch, F., and Hustin, J. (1991d). Развитие вторичного желточного мешка человека: соотношение сонографических и анатомических особенностей. Хум. Репрод. 6, 1160–1166.
Google Scholar
Jauniaux, E., Watson, A. L., Hempstock, J., Bao, Y.-P., Skepper, J. N., and Burton, G.J. (2000). Начало артериального кровотока у матери и оксидативный стресс плаценты; возможный фактор несостоятельности беременности у человека на ранних сроках. Am. J. Pathol. 157, 2111–2122. DOI: 10.1016 / S0002-9440 (10) 64849-3
Am. J. Pathol. 157, 2111–2122. DOI: 10.1016 / S0002-9440 (10) 64849-3
CrossRef Полный текст | Google Scholar
Jauniaux, E., Watson, A. L., Ozturk, O., Quick, D.и Бертон Г. (1999). In-vivo Измерение внутриматочных газов и кислотно-щелочных значений на ранних сроках беременности человека. Хум. Репрод. 14, 2901–2904. DOI: 10.1093 / humrep / 14.11.2901
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Йирковска, М., Яначек, Й., Калаб, Й., и Кубинова, Л. (2008). Трехмерное расположение капиллярного ложа и его связь с микрореологией терминальных ворсинок нормальной доношенной плаценты. Плацента 29, 892–897.DOI: 10.1016 / j.placenta.2008.07.004
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Джонс, К. Дж., И Жонье, Э. (1995). Ультраструктура материнско-эмбрионального интерфейса в первом триместре беременности. Микрон 26, 145–173. DOI: 10.1016 / 0968-4328 (95) 00002-L
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Джонс, Х. Н., Ольбрих, С. К., Смит, К. Л., Кнота, Дж. Ф., Хабли, М., Рамос-Гонсалес, О., и др. (2015).Синдром гипоплазии левых отделов сердца связан со структурными и сосудистыми аномалиями плаценты и нарушением регуляции лептина. Плацента 36, 1078–1086. DOI: 10.1016 / j.placenta.2015.08.003
Н., Ольбрих, С. К., Смит, К. Л., Кнота, Дж. Ф., Хабли, М., Рамос-Гонсалес, О., и др. (2015).Синдром гипоплазии левых отделов сердца связан со структурными и сосудистыми аномалиями плаценты и нарушением регуляции лептина. Плацента 36, 1078–1086. DOI: 10.1016 / j.placenta.2015.08.003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Кауфманн П., Лакхардт М. и Лейзер Р. (1988). Трехмерное изображение сосудистой системы плода в плаценте человека. Трофоб. Res. 3, 113–137. DOI: 10.1007 / 978-1-4615-8109-3_9
CrossRef Полный текст | Google Scholar
Ковальский, В.Дж., Пеккан, К., Тинни, Дж. П., и Келлер, Б. Б. (2014). Изучение биомеханики сердечно-сосудистой системы и причин врожденных пороков сердца. Фронт. Physiol. 5: 408. DOI: 10.3389 / fphys.2014.00408
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Куо, А. Х., Ли, К., Ли, Дж., Хубер, Х. Ф., Натаниэльс, П. В., и Кларк, Г. Д. (2017). Ремоделирование сердца в модели бабуина с ограничением внутриутробного развития имитирует ускоренное старение. Дж.Physiol. 595, 1093–1110. DOI: 10.1113 / JP272908
Дж.Physiol. 595, 1093–1110. DOI: 10.1113 / JP272908
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Кви, Л., Болдуин, Х. С., Шен, Х. М., Стюарт, К. Л., Бак, К., Бак, К. А. и др. (1995). Нарушение развития эмбриональной и внеэмбриональной систем кровообращения у мышей с дефицитом молекулы адгезии сосудистых клеток (VCAM-1). Разработка 121, 489–503.
PubMed Аннотация | Google Scholar
Lees, C., Jauniaux, E., Jurkovic, D.и Кэмпбелл С. (1998). Продукция оксида азота плацентой и сопротивление сосудов пупочной артерии на ранних сроках беременности. Акушерство. Гинеколь. 91 (5 Pt 1), 761–765.
PubMed Аннотация | Google Scholar
Льюис, П. М., Данн, М. П., МакМэхон, Дж. А., Логан, М., Мартин, Дж. Ф., Сен-Жак, Б. и др. (2001). Модификация холестерина sonic hedgehog необходима для активности передачи сигналов на большие расстояния и эффективной модуляции передачи сигналов с помощью Ptc1. Cell 105, 599–612. DOI: 10.1016 / S0092-8674 (01) 00369-5
DOI: 10.1016 / S0092-8674 (01) 00369-5
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Линаск, К. К. (2013). Ось сердце-плацента в первый месяц беременности: индукция и профилактика сердечно-сосудистых врожденных дефектов. J. Беременность 2013: 320413. DOI: 10.1155 / 2013/320413
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Линаск, К. К., Хан, М., и Браво-Валенсуэла, Н. Дж. (2014). Изменения желточной и маточно-плацентарной гемодинамики: последствия для развития сердечно-сосудистой системы. Фронт. Physiol. 5: 390. DOI: 10.3389 / fphys.2014.00390
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Локет П., Бротон Пипкин Ф., Саймондс Э. М. и Рубин П. С. (1988). Кривые скорости кровотока и сосудистое образование плаценты. Ланцет 2, 1252–1253.
PubMed Аннотация
Лу, Л., Кингдом, Дж., Бертон, Дж. Дж., И Циндрова-Дэвис, Т. (2017). Ремоделирование артерий стволовых ворсинок плаценты, связанное со сниженным синтезом сероводорода, способствует задержке роста плода человека. Am. J. Pathol. 187, 908–920. DOI: 10.1016 / j.ajpath.2016.12.002
Am. J. Pathol. 187, 908–920. DOI: 10.1016 / j.ajpath.2016.12.002
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Мякикаллио К., Йуппила П. и Текай А. (2004). Гемодинамика матки, плаценты и желточного мешка в первом триместре при преэклампсии и преждевременных родах. Хум. Репрод. 19, 729–733. DOI: 10.1093 / humrep / deh206
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Мэннинг, Л. Р., Попович, А. М., Падован, Дж.К., Чайт Б. Т. и Мэннинг Дж. М. (2017). Гель-фильтрация разбавленных эмбриональных гемоглобинов человека выявляет основу для их повышенного связывания с кислородом. Анал. Биохим. 519, 38–41. DOI: 10.1016 / j.ab.2016.12.008
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Макфадден, Д. Г., Барбоза, А. К., Ричардсон, Дж. А., Шнайдер, М. Д., Шривастава, Д., и Олсон, Е. Н. (2005). Факторы транскрипции Hand1 и Hand2 регулируют расширение желудочков сердца эмбриона в зависимости от дозы гена. Развитие 132, 189–201. DOI: 10.1242 / dev.01562
Развитие 132, 189–201. DOI: 10.1242 / dev.01562
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Мерсе, Л. Т., Барко, М. Дж., И Бау, С. (1996). Цветная допплеровская сонографическая оценка плацентарного кровообращения в первом триместре нормальной беременности. J. Ultrasound Med. 15, 135–142. DOI: 10.7863 / jum.1996.15.2.135
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Миджетт М., Торнбург К. и Ругоньи С.(2017). Паттерны кровотока лежат в основе пороков развития сердца. Am. J. Physiol. Heart Circ. Physiol. 312, H632 – H642. DOI: 10.1152 / ajpheart.00641.2016
PubMed Аннотация | CrossRef Полный текст
Митра, С. К., Сешан, С. В., и Риачи, Л. Е. (2000). Морфометрия плацентарных сосудов при задержке роста и повышенном сопротивлении допплеровскому кровотоку пупочной артерии. J. Matern. Fetal Med. 9, 282–286. DOI: 10.1002 / 1520-6661 (200009/10) 9: 5 <282 :: AID-MFM5> 3.0.CO; 2-J
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Мятт, Л., Брокман, Д. Э., Эйс, А. Л., и Поллок, Дж. С. (1993). Иммуногистохимическая локализация синтазы оксида азота в плаценте человека. Плацента 14, 487–495. DOI: 10.1016 / S0143-4004 (05) 80202-4
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Переда, Дж., И Ниими, Г. (2008). Эмбриональный эритропоэз в желточном мешке человека: два разных отсека для двух разных процессов. Microsc. Res. Tech. 71, 856–862. DOI: 10.1002 / jemt.20627
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Плитман Мэйо, Р., Чарнок-Джонс, Д. С., Бертон, Г. Дж., И Ойен, М. Л. (2016a). Трехмерное моделирование терминальных ворсинок плаценты человека. Плацента 43, 54–60. DOI: 10.1016 / j.placenta.2016.05.001
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Плитман Мэйо, Р., Олстхорн, Дж., Чарнок-Джонс, Д.С., Бертон, Дж. Дж., И Ойен, М. Л. (2016b). Компьютерное моделирование взаимосвязи структура-функция в терминальных ворсинах плаценты человека. J. Biomech. 49, 3780–3787. DOI: 10.1016 / j.jbiomech.2016.10.001
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Робертс, В. Х. Дж., Морган, Т. К., Беднарек, П., Морита, М., Бертон, Г. Дж., Ло, Дж. О. и др. (2017). В начале первого триместра маточно-плацентарный кровоток и прогрессирующая дезинтеграция спиральных артериальных пробок: новые выводы из ультразвукового исследования с контрастным усилением и тканевой гистопатологии. Хум. Репрод. 32, 2382–2393. DOI: 10.1093 / humrep / dex301
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Руис А., Феррер К., Санчес О., Рибера И., Аревало С., Аломар О. и др. (2016). Плацентарные осложнения у женщин, вынашивающих плод с врожденным пороком сердца. J. Matern. Fetal Neonatal Med. 29, 3271–3275. DOI: 10.3109 / 14767058.2015.1121480
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Салафия, К.М., Пецзулло, Дж. К., Миниор, В. К., и Дивон, М. Ю. (1997). Плацентарная патология отсутствия и обратного конечного диастолического кровотока у плодов с задержкой роста. Акушерство. Гинеколь. 90, 830–836. DOI: 10.1016 / S0029-7844 (97) 00473-0
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Салафия, К. М., Ямпольский, М., Шлахтер, А., Мандель, Д. Х., и Шварц, Н. (2012). Разнообразие формы плаценты: когда оно возникает? Плацента 33, 164–170. DOI: 10.1016 / j.плацента.2011.12.002
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Салимуддин, А., Тантбиройн, П., Сиройс, К., Крам, К. П., Бойд, Т. К., Творогер, С., и др. (2010). Акушерские и перинатальные осложнения плаценты при тромботической васкулопатии плода. Pediatr. Dev. Патол. 13, 459–464. DOI: 10.2350 / 10-01-0774-OA.1
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Сорегароли, М., Бонера, Р., Данти, Л., Динольфо, Д., Taddei, F., Valcamonico, A., et al. (2002). Прогностическая роль допплеровской велосиметрии пупочной артерии у плодов с задержкой роста. J. Matern. Fetal Neonatal Med. 11, 199–203. DOI: 10.1080 / jmf.11.3.199.203
PubMed Аннотация | CrossRef Полный текст | Google Scholar
van Heeswijk, M., Nijhuis, J. G., and Hollanders, H.M. (1990). Частота сердечных сокращений плода на ранних сроках беременности. Early Hum. Dev. 22, 151–156.
PubMed Аннотация | Google Scholar
Ямпольский, М., Салафия, К. М., Шлахтер, О., Хаас, Д., Ойкер, Б., и Торп, Дж. (2009). Центральное расположение пуповины в плаценте человека влияет на эффективность плаценты. Плацента 30, 1058–1064. DOI: 10.1016 / j.placenta.2009.10.001
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Янг Дж. Т., Рейберн Х. и Хайнс Р. О. (1995). События клеточной адгезии, опосредованные интегринами альфа-4, важны для развития плаценты и сердца. Развитие 121, 549–560.
PubMed Аннотация | Google Scholar
Чжан, Э. К., Бертон, Г. Дж., Смит, С. К., и Чарнок-Джонс, Д. С. (2002). Адаптация плацентарных сосудов во время беременности и на большой высоте: изменение диаметра и покрытия периваскулярных клеток. Плацента 23, 751–762. DOI: 10.1053 / plac.2002.0856
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Амниотическая жидкость: физиология и оценка
Производство амниотической жидкости
В первой половине беременности околоплодные воды извлекаются из отделов плода и, возможно, матери.Вода и растворенные вещества свободно проходят через кожу плода, а также могут диффундировать через амнион и хорион. 1 Таким образом, околоплодные воды на ранних сроках беременности представляют собой диализат, идентичный плазме плода и матери, но с более низкой концентрацией белка. Ранее предполагалось, что активная секреция жидкости из амниотического эпителия играет роль в раннем образовании околоплодных вод, но это не было продемонстрировано.
Ко второму триместру кожа плода ороговевает, делая ее непроницаемой для дальнейшего распространения.В это время плод пополняет объем и состав околоплодных вод почти исключительно через мочеиспускание. Моча была обнаружена в плодном пузыре уже через 11 недель трансабдоминально 2 и через 9 недель трансвагинально. 3 Поскольку моча плода является гипотонической (80–140 мОсм / л), она приводит к прогрессивно гипотонической жидкости (250–260 мОсм / л в ближайшем будущем), которая содержит возрастающие концентрации мочевины, мочевой кислоты и креатинина по мере созревания почек плода. . К срокам плод производит в среднем от 500 до 700 мл / день с небольшим снижением почасовой выработки мочи у плода после 40 недель беременности. 4 , 5 , 6
Удаление околоплодных вод
Удаление околоплодных вод с помощью как минимум трех механизмов. Первичный источник выведения — глотание плода, которое наблюдается уже на 16 неделе. 7 Исследования с использованием радиоактивных эритроцитов и радиоактивных коллоидов показали, что в среднем плод глотает от 200 до 450 мл / день в срок, удаляя 50% околоплодных вод, образующихся при мочеиспускании плода.Эта жидкость всасывается через желудочно-кишечный тракт плода и либо рециркулируется через почки, либо передается в материнский отсек через плаценту.
Вторым, более спорным способом удаления околоплодных вод может быть респираторный тракт. Дыхательная активность плода наблюдается уже на 11 неделе беременности. 8 При доношенных сроках инспираторный поток у плода составляет примерно 200 мл / кг / день, до 600-800 мл / день. 9 Поскольку амниотическая жидкость более гипотонична, чем плазма плода, предполагается, что воздействие амниотической жидкости на ложе альвеолярных капилляров плода приводит к чистому перемещению воды из амниотической полости в плод.Хотя радиоизотопы были обнаружены в легких плода после интраамниотической инстилляции, это количество было небольшим и непостоянным, 2 заставило исследователей усомниться в фактическом вкладе дыхания плода в удаление околоплодных вод. Фактически, поверхностно-активные фосфолипиды, происходящие из альвеол плода, обнаруживаются в амниотической полости, что позволяет предположить, что легкие плода действительно могут вносить чистый вклад в объем амниотической жидкости.
Амниотическая жидкость также потенциально может быть удалена непрерывным потоком (т.е.т.е. через гидростатические и онкотические силы). Обмен жидкости может происходить в хорионической пластинке, где воздействие относительно гипотонической околоплодной жидкости на поверхность плаценты плода может привести к чистой реабсорбции воды плодом (до 80 мл / день). Транспорт через амнион может происходить через межклеточные каналы между амниотическими эпителиальными клетками и может регулироваться уровнем пролактина в амниотической жидкости. 10 Hebertson и его коллеги представили предположительные доказательства регулирующей роли амниотического эпителия в транспортировке жидкости.Наблюдали ультраструктурные изменения амниона беременных, осложненных нарушением объема околоплодных вод. 11 Отражают ли эти изменения причинную роль в этих расстройствах или, скорее, реакцию на длительный дисбаланс жидкости, еще предстоит определить.
Последний, возможно, недооцененный путь регуляции объема может происходить внутри самой плаценты. Большая площадь поверхности межворсинчатого интерфейса плода может увеличивать небольшие осмолярные градиенты между матерью и плодом, приводя к большим объемам чистого переноса воды. 12 Обмен воды на этом уровне может повлиять на внутрисосудистый объем плода и потенциально повлиять на почечный кровоток и продукцию мочи.
В дополнение к объемному потоку жидкости, который происходит по путям, которые являются как фазовыми (мочеиспускание и глотание), так и нефазовыми (опосредованными гидростатическими и онкотическими градиентами), существует также двунаправленный поток воды между амниотическим и материнским отделами. 12 , 13 Этот процесс происходит за счет диффузии, но без чистого изменения объема жидкости.В срок вода может покидать амниотическую полость со скоростью 400–500 мл / час за счет диффузии плюс объемный поток. 14
Заболеваемость и происхождение
Многоводие, или гидрамнион, определяется как чрезмерный объем околоплодных вод по сравнению с гестационным возрастом. Многоводие бывает острым или хроническим. Острое многоводие обычно протекает во втором триместре, быстро накапливая жидкость в течение нескольких дней. 18 Хроническое многоводие имеет более постепенное начало и течение, часто проявляясь в третьем триместре.Заболеваемость варьируется в зависимости от клинического или сонографического диагноза. В целом многоводие осложняет примерно 0,3–1,6% всех беременностей. 18 , 19 , 20 , 21 , 22 Хроническое многоводие встречается чаще, превышая частоту острого многоводия в соотношении 50: 1. 18
Факторы риска многоводия в широком смысле можно разделить на материнское, фетальное, плацентарное и идиопатическое происхождение (таблица 1).
Таблица1. Факторы риска для многоводием
Материнские условия | Isoimmunization | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Сахарный диабет | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
плацентарные условия | Chorioangioma | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
желобоватых плацента | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Заболевания плода | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Многоплодная беременность | Синдром трансфузии от близнецов к близнецам | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Энцефалопластический анастомоз 89 поджелудочная железа, заворот средней кишки, диафрагмальная грыжа, омфалоцеле, гастрошизис | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Поражения ЦНС | Анэнцефалия, гидроцефалия, энцефалоцеле, расщелина позвоночника, микроцефалия 5 | 9 0456Пороки развития скелета | Множественный артрогрипоз, несовершенный остеогенез, танатофорная дисплазия | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Опухоли плода | Кистозная тератоиденоматоза | Кистозная терато-аденоматоза тератоиденоматоза шейки матки | Тяжелые врожденные пороки сердца, аритмии плода | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Генетические нарушения | Синдром Дауна, трисомия 13 и 18, синдром Пена-Шокейра, множественные врожденные аномалии, дистрофическая миотония | 4684 эндокринные нарушенияВазопрессиновая недостаточность | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Гематологические нарушения | Гомозиготная α-талассемия, фето-материнское кровоизлияние | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Разное | Неиммунная водянка плода, ретроперитонеальный фиброз плода | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Автор | Население | Самый большой карман c riteria | % | Чувствительность (%) | Специфичность (%) | Положительный прогнозируемый 9229 9229 прогнозируемый 9018 2 2 прогнозируемый 9018 2 2 значение (%) | ||||||||||||||||||||
Crowley (1980) 46 | > 42 недель | Субъективно | 35 | фетрессан 100 | 68 | 12 | 100 | |||||||||||||||||||
Укомплектование персоналом (1981) 51 | Предполагаемый IUGR | <1 см | 000 | 000 | 97 | 90 | 95 | |||||||||||||||||||
Philipson (1983) 40 | Невыбранный | 5000 468 | 68 | 68 | 68 16 | 97 | 40 | 91 | ||||||||||||||||||
Днище (1986) 33 | 32 | 83 | 23 | 89 | ||||||||||||||||||||||
Хилл (1983) 39 | Невыбранный | <1 см | 0 | 4680 | 46800 100 | — | 98 | |||||||||||||||||||
Субъективно | 1 | 68 | SGA | 99 | ||||||||||||||||||||||
Хэддик (1984) 52 | Ретроспективная беременность SGA | <1 см | 4 974 975468468 | 477 | 4GA —— | — | ||||||||||||||||||||
Mercer (1984) 53 | Ретроспективный невыбранный | <1 см | 3 | Apgar 5 <7 | — | — | 0 | — | ||||||||||||||||||
Чемберлен (1984) 54 | Относится к биофизическому профилю | Вертикальный | 68 4 | 0 68 | 9GA | 98 | 25 | 95 | ||||||||||||||||||
| 74 | 45 | > 41 недели | <1 см | 3 | Апгар 5 <7 | 25 | 98 | 29 | 97 | 9174 9177 | 3 | 97 | 17 | 83 | ||||||||||||
Bastide (1986) 55 | биофизический профиль 9174 9174 8 0.7 | SGA | — | — | 37 | — | ||||||||||||||||||||
Паттерсон (1987) 9684 9307 56000 | Паттерсон 9684 9307 56000 В среднем<3,2 см | 15 | SGA | 40 | 91 | 50 | 86 | |||||||||||||||||||
«Объем» <60 | 46 | Несовершеннолетний | 90 | 64 | 36 5 | 36 5 | (1987) 57 Беременность «высокого риска» | Сумма 4 верт. Квадранты | 8 | Кесарево сечение при «дистрессе плода» | 30 | 93 | 11 | ) 44 | 41 неделя | Среднее значение 3 по вертикали <3.8 см | 54 | Родоразрешение по неутешительному графику ЧСС плода | 79 | 55 | 41 | 87 | Беременность «группы риска» | Вертикальная <2 см | 3 | SGA | — | — | 68 68 68 68 68 |
Субъективная ультразвуковая оценка объема околоплодных вод
Кроули использовал субъективные критерии для оценки объема околоплодных вод при беременности после 42 недель, выявляя наличие или отсутствие анэхогенного пространства между конечностями плода и стенкой матки, а также между конечностями и плодом. багажник. 46 Филипсон и его коллеги использовали субъективные критерии нехватки околоплодных вод, скученности частей плода и «плохого межжелудочкового промежутка между плодами и жидкостью». 40 При проецировании этих критериев на теоретическую исследуемую популяцию для прогнозирования малолетних детей с гестационным возрастом (SGA) чувствительность составила 15,5%, а положительная прогностическая ценность — 39,6%. Позже и коллеги сравнили пятиуровневую субъективную оценку (олигогидрамнион, уменьшение, норма, увеличение, гидрамнион) с объективным измерением максимального вертикального диаметра кармана, последнее измерено с датчиком, удерживаемым под прямым углом к сагиттальной плоскости живота матери. . 33 При использовании младенцев с SGA в качестве аномальной конечной точки чувствительность и прогностическая ценность положительных результатов были одинаковыми для двух методов (32% против 31% и 83% против 82%, соответственно). Точно так же Голдштейн и Фили также продемонстрировали хорошую корреляцию между субъективной и объективной оценками объема околоплодных вод. 59
Полуколичественная ультразвуковая оценка объема околоплодных вод
В 1981 году концепция «правила 1 см» была введена в отобранной популяции пациентов с высоким риском. 33 В исследование были включены пациенты с подозрением на задержку роста плода (FGR) на основании измерений высоты дна матки. Объем произвольно классифицировался как уменьшенный, если самый большой карман для жидкости составлял менее 1 см в самом широком измерении. Было обнаружено, что у 24% из этих субъектов уменьшился объем околоплодных вод, и у 90% из них были рождены дети с диагнозом SGA. И наоборот, у 84% младенцев с SGA наблюдалось уменьшение жидкости. Однако последующие исследования были менее оптимистичными, показывая меньшую распространенность и более низкую чувствительность олигогидрамниона как предиктора ЗВУР. 33 , 39 , 40 , 52
Правило 1 см было пересмотрено в 1984 году. 54 Объем амниотической жидкости был зарегистрирован у всех пациентов, направленных на биофизический профиль измеряя вертикальный и поперечный размер самого большого кармана околоплодных вод с датчиком, ориентированным перпендикулярно контуру матки. Вертикальные диаметры менее 1 см классифицировались как уменьшенные, 1-2 см как крайние и от более 2 см до менее 8 см как нормальные.Было обнаружено, что 0,9% уменьшились и 2% имели околоплодные воды на краю. В результате повышения чувствительности при обнаружении ЛГР за счет включения маргинальной категории (5,5% для уменьшенных, 13,2% для уменьшенных плюс маргинальных групп) было высказано предположение, что правило 1 см может быть слишком строгим. Впоследствии компонент околоплодных вод биофизического профиля был изменен на 2 см в двух перпендикулярных плоскостях.
Помимо правила 2 см, оценивались и другие объективные методы определения объема околоплодных вод.Паттерсон и его коллеги измерили вертикальное и два горизонтальных размера самого большого жидкостного кармана и вычислили среднее значение трех измерений. 56 Были включены только карманы без пуповины и конечностей. Используя кривую рабочих характеристик приемника, статистический инструмент, который используется для максимизации чувствительности и специфичности, была установлена граница 3,2 см. Используя это значение, 15% исследуемой популяции, «подверженной риску недостаточности питания плода», были отклонены от нормы.Отсечка 3,2 см была 40% чувствительностью и 91% специфичностью, с 50% положительной прогностической ценностью и 86% отрицательной прогностической ценностью для обнаружения младенцев с SGA. Наблюдаемые различия в среднем объеме жидкости, скорее всего, связаны с истинными различиями между пациентами, а не с ошибкой измерения; измерение среднего размера самого большого кармана околоплодных вод имело вариабельность между пациентами, которая была в четыре раза выше, чем вариабельность внутри наблюдателя. Напротив, использование максимального вертикального диаметра имело вариабельность внутри наблюдателя, которая была выше, чем вариабельность между пациентами.Авторы пришли к выводу, что средний объем околоплодных вод был более воспроизводимым, чем наибольший вертикальный диаметр, и был бы лучшим скрининговым тестом для выявления истощенных плодов.
В 1987 году Фелан и его коллеги представили четырехквадрантную технику оценки объема околоплодных вод. 32 При использовании 353 gravidas на сроке 36–42 недель, которые были направлены по поводу наружной головной версии или беременности после родов от 36 до 42 недель, был измерен и суммирован наибольший вертикальный диаметр в каждом квадранте.При всех измерениях датчик держали в сагиттальной плоскости перпендикулярно полу. Это число в сантиметрах было названо индексом околоплодных вод (AFI). Между 36 и 40 неделями средний AFI составил 12,4 ± 4,6 см. В то время как два стандартных отклонения ниже и выше среднего привели бы к статистическим пороговым значениям 3,7 и 22,1 см соответственно, авторы использовали пороговые значения 5 см для произвольного определения уменьшения количества околоплодных вод и 20 см для избыточного количества жидкости. Дальнейшее исследование, проведенное этими авторами, продемонстрировало значительное увеличение количества жидкости, окрашенной меконием, после кесарева сечения и низкие показатели по шкале Апгар у пациентов с AFI менее 5 см. 57
Мур и Кейл впоследствии оценили индекс околоплодных вод при 791 нормальной беременности на сроке от 16 до 42 недель. 60 Поскольку наблюдались значительные различия между преждевременными, доношенными и послеродовыми беременностями, что согласуется с физиологическими изменениями жидкости, происходящими на протяжении всей беременности, данные были стратифицированы по неделям беременности. Было рассчитано среднее значение AFI на каждой неделе беременности, а также доверительные интервалы 90–95% (таблица 4).Это исследование продемонстрировало важность установления специфичных для беременностей норм для AFI, а не единственного порогового значения. Интересно, что значение AFI 2,5-го процентиля на каждом сроке беременности было больше порога в 5 см, установленного Феланом. 32 Следовательно, использование порога 2,5-го процентиля приведет к более частой диагностике маловодия.
Таблица 4. Значения индекса околоплодных вод при нормальной беременности (в мм)
Процентильные значения индекса околоплодных вод | ||||||||||||||||||||||||||
неделя | 2000 9.5-я | 5-я | 50-я | 95-я | 97,5-я | 9109 | 73 | 79 | 121 | 185 | 201 | 32 | ||||||||||||||
000 | 9177 9174 9177 | 9177 127 | 194 | 211 | 26 | |||||||||||||||||||||
18 | 80 | 87 | 468487 | 17 | ||||||||||||||||||||||
19 9 0468 | 83 | 90 | 137 | 207 | 225 | 14 | ||||||||||||||||||||
000 | 000 | 141 | 212 | 230 | 25 | |||||||||||||||||||||
21 | 88 | 95 | 4000595 | 400095 | 49177 | 14 | ||||||||||||||||||||
22 | 89 | 97 | 145 | 216 | 686 | 90 | 98 | 146 90 468 | 218 | 237 | 14 | |||||||||||||||
24 | 90 | 98 | 98 | 0009 23 | ||||||||||||||||||||||
25 | 89 | 97 | 147 | 221 | 240 | 121774240 0 | 97 | 147 | 223 | 242 | 11 | |||||||||||||||
27 | 468427 | 9177 226 | 245 | 17 90 468 | ||||||||||||||||||||||
28 | 86 | 94 | 146 | 228 | 249 | 000 249 | 000 840004 | 68 | 92 | 145 | 231 | 254 | 12 | |||||||||||||
30 | 684 | 258 | 17 | |||||||||||||||||||||||
31 | 79 | 88 | 144 | 46840003 | ||||||||||||||||||||||
32 | 77 | 86 | 144 | 242 | 269 | 25 | ||||||||||||||||||||
33 | 74 | 474 | 4274 | 30 | ||||||||||||||||||||||
34 | 72 | 81 | 142 | 684 | 35 | 70 | 79 | 140 | 249 | 279 | 27 | 27 | 27 | 9456000 9456000138 | 249 | 279 | 39 | |||||||||
37 | 66 | 75 | 135 | 244 | 4684244 | 4244 | 465 | 73 | 132 | 239 | 269 | 27 | ||||||||||||||
127 | 226 | 255 | 12 | ||||||||
40 | 63 | 71774 | 71774 | 964 | |||||||
41 | 63 | 70 | 116 | 194 | 216 | 162 | |||||
000 | 04 | 9177 | 175 | 192 | 30 |
(Moore TR, Cayle JE: Индекс околоплодных вод при нормальной беременности человека.Am J Obstet Gynecol 162: 1168, 1990)
Сравнение результатов ультразвуковой оценки объема околоплодных вод
На сегодняшний день ни один метод оценки объема околоплодных вод не оказался наиболее ценным с клинической точки зрения. Сложность в сравнении методов оценки жидкости возникает из-за различий в исследуемой популяции, выбранной аномальной конечной точки и разнообразия ультразвуковых критериев. Правило 2 см традиционно использовалось наиболее широко, преимущественно как компонент биофизического профиля.Однако в последнее время индекс амниотической жидкости все чаще появляется в литературе и в клинической практике. AFI, измеряя все четыре квадранта, по-видимому, более точно оценивает серийные изменения объема жидкости с течением времени по сравнению с одним вертикальным карманом, который может подвергаться большему изменению из-за расположения плода. Кроме того, используя нормы, специфичные для беременности, AFI может более точно отражать отклонения в объеме жидкости по сравнению с правилом 2 см. Тем не менее, AFI не оценивался так широко для выявления плода с риском ЗВУР, компрессии пуповины и аномальных перинатальных исходов.Для сравнения: использование субъективных критериев, которые могут в меньшей степени зависеть от положения плода при серийном тестировании, больше полагается на гештальт объема жидкости, чем на какое-либо одно значение измерения. В результате опыт экзаменатора может быть более важным при определении того, подходят ли околоплодные воды для гестационного возраста, поскольку тот же субъективно нормальный объем околоплодных вод на 42 неделе может быть уменьшен на 34 недели. Кроме того, субъективные критерии могут варьироваться от человека к человеку, что затрудняет взаимодействие между наблюдателями и статистические сравнения.В учреждении автора объем околоплодных вод изначально оценивается субъективно. Если это нормально, то AFI или самый большой вертикальный карман не измеряются. Однако, если жидкость субъективно кажется уменьшенной, рассчитывается AFI.
Вариабельность определений олигогидрамниона на основе ультразвукового исследования была подчеркнута в клиническом комментарии Маганна и его коллег, который содержал призыв к будущим исследованиям, которые коррелируют оценку объема околоплодных вод с клинически значимыми перинатальными исходами. 61 Фишер и его коллеги оценили женщин в послеродовой период и сравнили различные ультразвуковые критерии маловодия с композитным перинатальным исходом. 62 Самый большой карман в каждом квадранте был измерен в двух перпендикулярных плоскостях. Оцениваемые показатели включали наибольший вертикальный карман, наибольший поперечный карман, AFI, наибольшее изделие кармана (вертикальное x поперечное), сумму всех измерений кармана и сумму произведений кармана. Они обнаружили, что самый большой вертикальный карман, AFI и сумма всех карманов значительно различались между группами нормальных и аномальных перинатальных исходов.Используя кривые рабочих характеристик приемника для определения оптимальных пороговых значений, вертикальный карман 2,7 был идеальным для определения аномального перинатального исхода. На основе кривой ROC невозможно установить оптимальное значение отсечки AFI.
Чаухан и его коллеги провели проспективное рандомизированное клиническое исследование, сравнив AFI с самым большим вертикальным карманом. 63 Они случайным образом назначили 1080 гравидов высокого риска, за которыми следовали еженедельные нестрессовые тесты и либо AFI, либо самый большой вертикальный карман.Они определили олигогидрамнион либо как AFI размером 5 см или меньше, либо как отсутствие кармана для жидкости размером не менее 2 x 1 см. У женщин, которым следовали AFI, было значительно больше шансов получить диагноз олигогидрамниона, чем у женщин в группе с наибольшим вертикальным карманом (17% против 10%, p = 0,002). Однако не было никакой разницы между двумя методами оценки жидкости в отношении кесарева сечения для неутешительной оценки сердечного ритма плода, оценки по шкале Апгар, pH пупочной артерии <7.1, либо поступление в отделение интенсивной терапии новорожденных. Авторы пришли к выводу, что использование AFI увеличивает количество вмешательств по поводу маловодия без улучшения перинатального исхода. Они также отметили, что оба метода оценки околоплодных вод являются плохими диагностическими тестами для прогнозирования неблагоприятного перинатального исхода.
Несоответствия в ультразвуковой оценке объема околоплодных вод
Трудности возникают при сравнении различных критериев олигогидрамниона. Одна переменная, которая не часто рассматривается в исследованиях, — это включение или исключение карманов с жидкостью, которые содержат петли пуповины.При олигогидрамнионе пуповина составляет повышенную долю карманов с жидкостью. В некоторых исследованиях исключались любые карманы, в которых был шнур, в то время как в других измерялись размеры жидкости, окружающей шнур.
Часто упускаемый из виду, но критически важный вопрос — это расположение преобразователя. В некоторых отчетах датчик держали под прямым углом к контуру матки, 54 , 58 , тогда как в других плоскость ультразвука была перпендикулярна полу или сагиттальной плоскости живота. 32 , 33 Многие исследования не показали, как датчик был ориентирован. Ориентация имеет решающее значение при оценке вертикального диаметра. Если датчик держать перпендикулярно контуру матки, вид сбоку матки может ошибочно создать вертикальный карман на экране УЗИ. Для единообразия рекомендуется ориентировать датчик продольно и перпендикулярно плоскости пола (плоскости, в которой находится наслоенная жидкость), тем самым минимизируя различия, если объект смещается в поперечном направлении.
Клиническая значимость олигогидрамниона
Литература предполагает, что маловодие действительно увеличивает риск у плода без серьезных аномалий. Однако клиническое значение олигогидрамниона различается между исследованиями в зависимости от используемых критериев и оцениваемых конечных точек. В целом, уменьшение количества околоплодных вод связано с более высокой частотой новорожденных с SGA (менее 10-го перцентиля для гестационного возраста), синдромом переношенности, переменным и поздним замедлением родов, кесаревым сечением для неутешительного отслеживания сердечного ритма плода, более низким pH пупочной артерии, более низким Оценка по шкале Апгар и более высокая перинатальная смертность.Маловодие во втором триместре особенно связано с неблагоприятными перинатальными исходами в результате как гипоплазии легких, так и летальных врожденных аномалий. 64
Относительная степень, в которой повышенная заболеваемость является результатом либо основного состояния, вызывающего маловодие, либо прямого воздействия пониженной жидкости (, т.е. ., Компрессия пуповины), не была определена. Однако есть предположение, что часть риска компрессии пуповины может быть обратимой, о чем свидетельствуют исследования, в которых жидкость удалялась по сравнению с теми, в которых жидкость была заменена (амниоинфузия) для определения клинического эффекта.Габбе и его коллеги отметили, что удаление околоплодных вод из амниотической полости эмбриональных обезьян приводило к различным замедлениям, вторичным по отношению к сдавлению пуповины. 65 Эта картина разрешилась после амниоинфузии. Подтверждение этого открытия на людях было продемонстрировано Миядзаки и соавторами, которые наблюдали значительное уменьшение вариабельных децелераций во время родов у 51% пациентов, получавших амниоинфузию через катетер внутриматочного давления. 66 Nageotte и его коллеги наблюдали значительно более низкую частоту вариабельных замедлений и более высокие значения pH пуповины у пациентов с PROM и прошедших профилактическую амниоинфузию. 67
Легочная гипоплазия, определяемая по низкой массе влажных легких, низкому содержанию ДНК в легких и низкому количеству лучевых альвеол, может возникнуть после PROM и маловодия при очень преждевременных сроках беременности (<24 недель). 68 Это может быть результатом ограничения расширения легких из-за длительного внешнего сжатия, подавления дыхательных движений плода и отсутствия циркуляции жидкости в конечных альвеолах, что может потребовать факторов роста, содержащихся в околоплодных водах, которые имеют решающее значение для развития альвеол. 69 В одном исследовании PROM, в котором наблюдалась гипоплазия легких, большинство случаев было менее 26 недель на момент разрыва мембраны, что позволяет предположить, что развивающиеся терминальные воздушные мешочки более восприимчивы к повреждающему действию олигогидрамниона. 70 Кроме того, продолжительное маловодие увеличивает риск развития последовательности Поттера, которая, помимо гипоплазии легких, включает деформации скелета и лица плода из-за длительного внешнего сжатия. 69
Дородовое ведение спонтанного олигогидрамниона
Прямое лечение дородового олигогидрамниона при отсутствии разрыва мембраны или обструкции мочевыводящих путей плода не известно.Олигогидрамнион при отсутствии серьезных врожденных аномалий может быть маркером предшествующей адаптации плода к хронической маточно-плацентарной недостаточности или частичной окклюзии пуповины, а также фактором, предрасполагающим к сдавлению пуповины. Поэтому, как правило, рекомендуется, в зависимости от гестационного возраста, за этими пациентами либо внимательно следить с помощью серийных антенатальных тестов (нестрессовый тест, биофизический профиль), включая оценку наличия переменных замедлений, либо родить. Однако при наличии олигогидрамниона в настоящее время нет единого мнения о критическом интервале между диагностикой и доставкой.При наличии выраженного олигогидрамниона в срок родоразрешение следует начинать в течение 24–48 часов после постановки диагноза или раньше при наличии сопутствующих результатов, таких как спонтанные переменные замедления. Требуются дальнейшие исследования для определения преимуществ такого подхода как для краткосрочной, так и для долгосрочной заболеваемости.
Олигогидрамнион, возникший в результате врожденной непроходимости мочевыводящих путей (, например, , клапаны задней уретры), можно лечить, особенно при преждевременной беременности, с помощью ультразвуковых процедур, которые направляют мочу из мочевого пузыря в амниотическую полость. 71 У плода с сохраненной функцией почек на основе серийного анализа электролитов в моче, полученных при везикоцентезе, пузырно-амниотическое шунтирование может быть полезной временной мерой для декомпрессии мочевого пузыря, облегчения маловодия и предотвращения гипоплазии легких. 72 , 73 Ведение во время родов
Олигогидрамнион увеличивает риск компрессии пуповины во время родов; следовательно, за плодом следует внимательно следить на предмет различных замедлений.Стойкие, умеренные или тяжелые вариабельные замедления могут быть улучшены с помощью амниоинфузии во время родов.
Во время родов доказательства кальцификации плаценты долгое время были связаны с дистресс-синдромом плода в родах (1 ). С введением ультразвука в акушерстве различия в фактуре плаценты и их значение заинтриговали поколения специалистов по ультразвуковой диагностике.Винсберг был одним из первых, кто связал определяемые ультразвуком изменения плаценты со зрелостью плода (2), а Grannum et al. были первыми, кто разработал систему оценки созревания плаценты (3). Используя эту систему оценок, Grannum et al. коррелировала легочная зрелость плода при рождении с ранее обнаруженной плацентой III степени при ультразвуковом сканировании. Дальнейшее исследование показало, что на 42 неделе беременности у 54% пациентов будет плацента III степени (классификация Grannum), а на 40 неделе беременности примерно у 16% пациентов будет ультразвуковое подтверждение плаценты III степени 4-6). .Ранние исследования были сосредоточены на взаимосвязи зрелой плаценты при ультразвуковом сканировании с созреванием легких плода при рождении. Brown et al. показали, что плацента III степени (по классификации Grannum) раньше срока связана с курением матери (7). Кроме того, в неотобранной акушерской популяции было показано, что плацента III степени на сроке беременности 35 недель или менее связана с последующим развитием преэклампсии (8), а выявленные таким образом беременности имеют повышенный риск неонатальной заболеваемости и смертности (9, 10). ).
Мы разработали проспективное исследование, чтобы изучить частоту возникновения плаценты III степени (по классификации Grannum) на сроке беременности 36 недель в акушерской популяции с низким риском. Затем мы изучили взаимосвязь между плацентой III степени на 36 неделе беременности и характеристиками матери, которые могут считаться важными при беременности. Мы также изучили взаимосвязь между плацентой III степени на 36 неделе беременности и исходом беременности.
Материалы и методы
Исследование одобрило местный комитет по этике.Критериями включения в исследование были одноплодная беременность и известный гестационный возраст, подтвержденный ультразвуком на сроке гестации <20 недель. Критерии исключения: многоплодная беременность; известная материнская медицинская проблема; акушерское осложнение перенесенной беременности; акушерские осложнения при беременности до 36 недель; и известные аномалии плода. Зрелость плаценты определяли по классификации Grannum (3). Для целей исследования мы объединили исходные оценки 0 и I по Grannum в единую категорию, называемую степенью I.Плацента нулевой степени имеет легко очерченную, относительно прямую хорионическую пластинку и однородную текстуру на всем протяжении. Плацента I степени характеризуется волнообразной хорионической пластиной и рассеянными эхогенными участками внутри. Плацента II степени распознается по наличию небольших эхогенных участков вдоль базального слоя плаценты и разделению эхогенных плотностей, напоминающих запятую плаценты, которые берут начало в хорионической пластинке. Плацента III степени характеризуется эхогенными углублениями, простирающимися от хорионической пластинки до базального слоя, разделяющими плаценту на отдельные компоненты, напоминающие семядоли.Кроме того, вблизи хорионической пластинки иногда наблюдаются неоднородные плотности, отбрасывающие акустические тени. Все сканирования выполнялись с использованием криволинейного зонда 3,5 МГц сканера ATL Ultramark 4. В исследуемую группу вошли пациенты с плацентой III степени на сроке беременности 36 недель. Контрольную группу составили пациенты без плаценты III степени. Случаи и контроль сравнивались по возрасту матери, паритету, курению и употреблению алкоголя матерью, гипертонии, вызванной беременностью, дистрессу плода во время родов, способу родоразрешения, Apgars, потребности в реанимации при родах, массе тела при рождении и поступлении в отделение интенсивной терапии новорожденных.Статистический анализ проводился с использованием SPSS (11) и Epi-Info (12). Показатели результатов сравнивались между группами с использованием критерия χ 2 с поправкой Йейтса, а также рассчитывались относительные риски с 95% доверительным интервалом (CL).
Результаты
В этой акушерской популяции с низким риском на 36 неделе беременности у 3,8% (68) была плацента III степени (классификация Grannum). Плацента II степени была выявлена у 18,5% (333) пациентов и 77.7% (1401) продемонстрировали плаценту нулевой или первой степени.
Плацента III степени чаще была обнаружена у нерожавших пациенток, 55,9% (38/68) против 41,6% (721/1734). p = 0,03 (Таблица I). Пациенты в исследуемой группе чаще были младше 25 лет: 55,9% (38/68) по сравнению с 26,8% (465/1734), p <0,01. В основной группе курили 52,9% (36/68) пациентов по сравнению с 33,6% (583/1734) в контрольной группе, p <0,01.
Таблица I.Характеристики матери и плода| Плацента III степени ( п = 68) | Контроль ( n = 1734) | Коэффициент риска 95% CL | п | |
|---|---|---|---|---|
| нерожавшие | 38 | 721 | 1.34 (1,08, 1,67) | 0,03 |
| Возраст <25 лет | 34 | 465 | 1,86 (1,45, 2,39) | <0,01 |
| Употребление табака | 36 | 583 | 1.57 (1,25, 1,99) | <0,01 |
| Употребление алкоголя | 10 | 217 | 1,18 (0,65, 2,11) | 0,73 |
| Мужской плод | 40 | 903 | 1.12 (0,91, 1,37) | 0,37 |
У пяти пациенток (7,4%) с плацентой III степени впоследствии развилась протеинурическая гипертензия, вызванная беременностью. Это для сравнения с 27 пациентами (1,56%) в контрольной группе, p <0,01. Интересно, что ни у одного из этих пациентов не было протеинурии или гипертонии на момент 36-недельного сканирования (Таблица II).
Таблица II. Исходы беременности| Плацента III степени ( п = 68) | Контроль ( n = 1734) | Коэффициент риска 95% CL | п | |
|---|---|---|---|---|
| Протеинурический PIH | 5 | 27 | 4.7 (1,87, 11,83) | <0,01 |
| Индукция (компромисс плода) | 11 | 60 | 4,65 (2,57, 8,44) | <0,01 |
| Самопроизвольные роды | 34 | 1017 | 0.85 (0,67, 1,08) | 0,18 |
| Аномальный CTG | 13 | 215 | 1,54 (0,93, 2,55) | 0,15 |
| Мекониевый щелок | 7 | 167 | 1.07 (0,52, 2,19) | 0,98 |
| Нормальные вагинальные роды | 42 | 1148 | 0,93 (0,77, 1,12) | 0,49 |
| Реанимация новорожденных | 51 | 1277 | 1.01 (0,88, 1,16) | 0,19 |
| Масса при рождении <10-го центиля | 12 | 97 | 3,13 (1,81, 5,41) | <0,01 |
| Вес при рождении> 90-го центиля | 7 | 192 | 0.92 (0,45, 1,88) | 0,98 |
| Поступление в отделение интенсивной терапии | 1 | 32 | 0,79 (0,11, 5,70) | 0,64 * |
- CL, доверительный интервал; PIH — гипертензия, вызванная беременностью; КТГ, кардиотокография; NICU, отделение интенсивной терапии новорожденных.
В этой группе низкого риска из 1802 пациенток в общей сложности у 71 пациентки были индуцированы роды из-за подозрения на компромисс плода на более позднем этапе беременности. Плацента III степени на 36 неделе беременности помогла выявить эти осложненные беременности: 16,2% (11/68) против 3,5% (60/1734), относительный риск 4,65 (2,57, 8,44), p <0,01.
У пациентов с плацентой III степени, 17.6% (12) родили детей с массой тела при рождении ниже 10-го центиля (13). Это сопоставимо с 5,6% (97) в контрольной группе, p <0,01. Относительный риск рождения ребенка с массой тела при рождении ниже 10-го центиля составил 3,13 (1,81, 5,41) среди детей с плацентой III степени.
Плацента III степени не ассоциировалась с плохим перинатальным исходом. Дистресс плода во время родов (аномальный кардиотокограф и ликвор, окрашенный меконием) не был связан с плацентой III степени и не был связан с повышенной потребностью в реанимации новорожденных, относительный риск 1.01 (0,88, 1,16), p = 0,19.
Обсуждение
Ведение антенатальных пациентов «низкого риска» мало изменилось за последние 30 лет. Мы все еще оцениваем самочувствие плода путем пальпации живота матери. При этом мы пытаемся выявить плод с задержкой роста или беременность, осложненную маловодием или многоводием. Мы делаем это, зная, что клиническая оценка веса плода и объема околоплодных вод имеет чувствительность менее 50% в руках большинства практикующих врачей (14).Рандомизированное контролируемое исследование Tucker et al. (15) спросили: «Должны ли акушеры осматривать женщин с нормальной беременностью?» Они пришли к выводу, что регулярные посещения специалиста для женщин, изначально относящихся к группе низкого риска осложнений беременности, практически не приносят клинической или потребительской пользы. Однако единственным перинатальным исходом, рассмотренным в этом исследовании, была перинатальная смертность. Их вывод был основан на том, что эти потери были разделены более или менее поровну между специалистом и неспециалистом. Другая интерпретация этих цифр заключается в том, что существующая практика не позволяет идентифицировать плод с высоким риском в популяции с низким риском.
При пальпации живота матери функция плаценты грубо «оценивается» путем оценки объема околоплодных вод. Кальцификация плаценты, связанная с плохим перинатальным исходом (9), не может быть определена. В нашей популяции плацента III степени ассоциировалась с беременностями, которые, как мы знаем, с большей вероятностью будут осложнены: молодая, нерожавшая пациентка, которая курит.
В нашем исследовании у матери с плацентой III степени на 36 неделе беременности была почти в пять раз выше вероятность развития преэклампсии на более поздних сроках беременности.Более того, ни у одного из этих пациентов на момент сканирования не было гипертонии или протеинурии. Плацента III степени при сканировании помогает выявить пациентов, у которых впоследствии разовьется преэклампсия.
Аудиторское исследование Euronatal предполагает, что мертворождение можно снизить за счет улучшения выявления задержки роста и лечения детей с задержкой роста (16). В нашей серии исследований матери с плацентой III степени на 36 неделе беременности имели в три раза больше шансов родить ребенка с массой тела при рождении ниже 10-го центиля.Ограничение внутриутробного развития при отсутствии серийных сканирований роста является ретроспективным клиническим диагнозом после родов. Некоторые маленькие дети по своему телосложению будут маленькими и совершенно здоровыми. Однако общепринято считать, что 30% детей, рожденных с массой тела ниже 10-го центиля, не смогут достичь своего потенциала внутриутробного развития и будут страдать от задержки внутриутробного развития (17).
Классификация плаценты в третьем триместре оценивалась в рандомизированном контролируемом исследовании (10).Предполагается, что плацента III степени связана с низкой массой тела при рождении, проблемами во время родов, плохим состоянием при рождении и перинатальной смертью. Кроме того, это исследование показало, что если врач, ответственный за уход за пациентами, знал о классификации плаценты, дальнейшая оценка внутриутробной среды и вмешательства снижали риск перинатальной смерти в группе, в которой классификация была известна.
Мы предполагаем, что плацента III степени на 36 неделе беременности в популяции с низким риском действует как инструмент скрининга для выявления плода с высоким риском.Ультразвуковое сканирование может быть выполнено за считанные минуты акушерами со скромной подготовкой и навыками. После определения высокого риска исход беременности можно оптимизировать с помощью инструментов (ультразвуковая допплерография и т. Д.), Предназначенных для ранее выявленных беременностей с высоким риском, таких как предыдущие мертворождения и ограничение внутриутробного развития при предыдущей беременности.
Как акушеры, мы являемся экспертами по ведению наших матерей в дородовой период. Мы должны спросить себя: «Так ли хорошо мы оцениваем наших детей в утробе матери ?» Четвертый ежегодный отчет конфиденциального исследования мертворождений и смертей в младенчестве показал, что наибольшая область для снижения перинатальной смертности связана с необъяснимыми мертворождениями в дородовом периоде (18).В этом может помочь ультразвуковое исследование кальцификации плаценты на сроке беременности 36 недель.
Список литературы
- 1 Фокс Х. Кальцификация плаценты. J Obstet Gynaecol Br Commonw 1964; 17: 759.
- 2 Винсберг Ф.Эхографические изменения при старении плаценты. J Clin Ультразвук 1973; 1:52.
- 3 Граннум ПАТ, Берковиц Р.Л., Hobbins JC. Ультразвуковые изменения в созревающей плаценте и их связь с легочной зрелостью плода. Am J Obstet Gynecol 1979; 133: 915–22.
- 4 Фернандо М, Граннум П, Пинто К, Bracken M, Кадар Н, Hobbins JC.Ультразвуковая оценка беременности в позднем периоде. Акушер-гинекол 1985; 3: 319–22.
- 5 Петруча Р.А., Голд Ш., Platt LD. УЗИ плаценты в режиме реального времени для оценки зрелости легких плода. Am J Obstet Gynecol 1982; 142: 463.
- 6 Хилл Л.М., Брекл Р, Рагоззино М.В., Вольфграм КР, О’Брайен ПК.Плацентация 3 степени: частота и исходы новорожденных. Акушер-гинекол 1983; 61: 728–32.
- 7 Коричневый HL, Миллер Дж. М., Khawli O, Гарберт Х.А. Преждевременная кальцификация плаценты у курильщиц сигарет. Акушер-гинекол 1988; 71: 914–17.
- 8 Кэрролл Б.Ультразвуковые особенности преэклампсии. J Clin Ультразвук 1980; 8: 483.
- 9 Читланж СМ, Хазари К.Т., Джоши СП, Шах РК, Mehta AC. Ультразвуковое исследование преждевременной плаценты III степени и перинатального исхода. Int J Gynaecol Obstet 1990; 31: 325–8.
- 10 Гордый J, Грант А.М.Оценка плаценты в третьем триместре с помощью УЗИ как тест благополучия плода. Br Med J 1987; 294: 1641–4.
- 11 Справочное руководство по синтаксису SPSS 10.0. Чикаго: SPSS Inc., 1999.
- 12 Дин АГ, Дин Дж. А., Куломбье D, Брендель К.А., Смит, округ Колумбия, Burton AH et al. Epi-Info, версия 6: программа для обработки текстов, баз данных и статистики для общественного здравоохранения на IBM-совместимых микрокомпьютерах. Атланта, Джорджия, США: Центры по контролю и профилактике заболеваний, 1995.
- 13 СП Фримен, Коул TJ, Чинн С, Джонс PRM, Белый ЭМ, Прис М.А. Базовые кривые роста и веса в поперечном сечении для Великобритании, 1990 г. Arch Dis Детский 1986; 73: 17–24.
- 14 Хепберн М, Розенберг К. Аудит выявления и ведения маленьких для гестационного возраста детей. Br J Obstet Gynaecol 1996; 93: 212–16.
- 15 Такер Дж. С., Корпус MH, Хауи П.В., Рид МЕНЯ, Барбур RS, Du Florey V. et al. Должны ли акушеры встречаться с женщинами с нормальной беременностью? Многоцентровое рандомизированное контролируемое испытание рутинной дородовой помощи врачей общей практики и акушерок в сравнении с коллективной помощью под руководством акушеров. Br Med J 1997; 312: 554–9.
- 16 Ричардус JH, Граафманс WC, Ван дер Пал-де Брюин К.М., Амелинк-Вербург депутат, Верлове-Ванхорик ИП, Machenbach JP. Европейские согласованные действия по изучению достоверности перинатальной смертности в качестве индикатора результата для качества дородовой и перинатальной помощи. J Perinat Med 1985; 25: 313–24.
- 17 Chiswick ML. Задержка внутриутробного развития. Br Med J 1985; 291: 845–8.
- 18 Конфиденциальное расследование мертворождений и смертей в младенчестве. Четвертый годовой отчет с 1 января по 31 декабря 1995 г., посвященный смертельным случаям во время родов, 1994–2005 гг.Лондон: Консорциум по охране здоровья матери и ребенка, 1997 г.

 Хориальная пластина приобретает волнистость
Хориальная пластина приобретает волнистость Проводится УЗ-исследование. Определяется локализация, оценивается площадь поверхности, масса и величина. Помимо плацентометрии оценивается и степень зрелости структуры. Эхографически принято выделять четыре степени. О созревании говорит визуализация включений повышенной акустической плотности. Если она акустически однородна, отсутствует дольчатость, субэпителиальная мембрана не утолщена, то говорят о 0 степени зрелости.
Проводится УЗ-исследование. Определяется локализация, оценивается площадь поверхности, масса и величина. Помимо плацентометрии оценивается и степень зрелости структуры. Эхографически принято выделять четыре степени. О созревании говорит визуализация включений повышенной акустической плотности. Если она акустически однородна, отсутствует дольчатость, субэпителиальная мембрана не утолщена, то говорят о 0 степени зрелости.

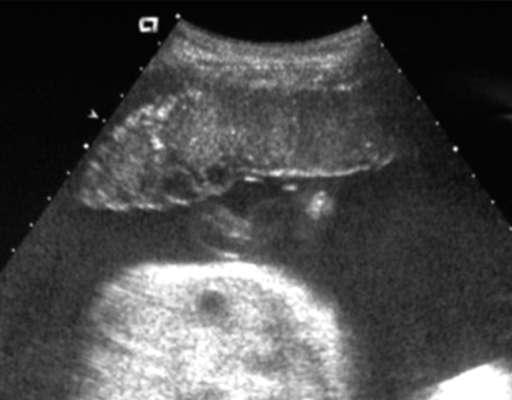
 03
03