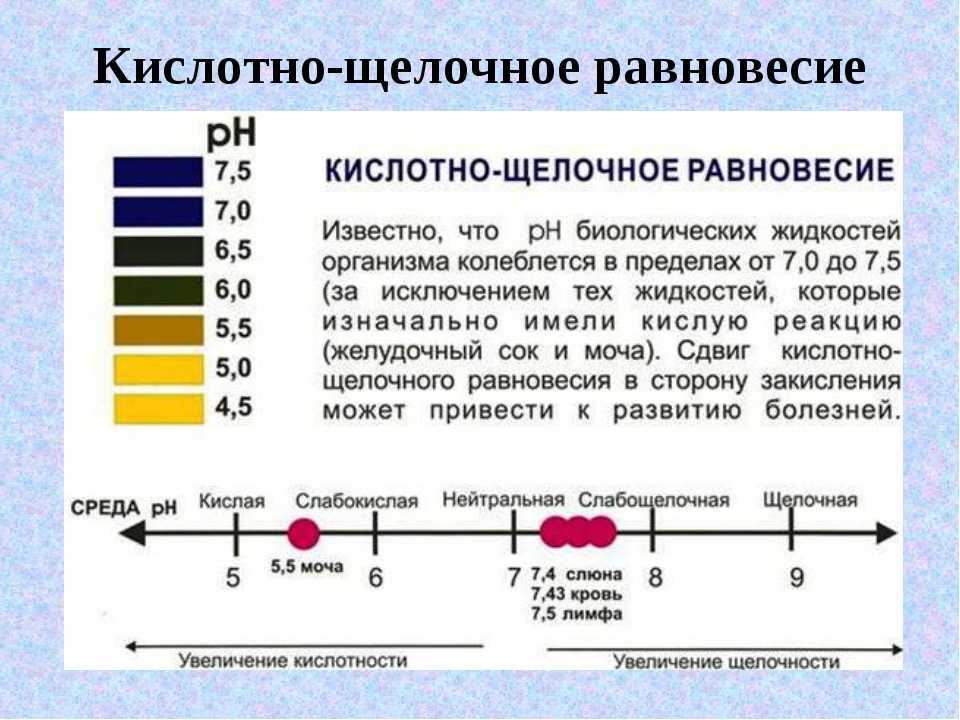
Что такое ph в анализе мочи и для чего определяют реакцию
Кислотность мочи – это показатель, который отражает концентрацию ионов водорода в урине. В лаборатории тест выполняется pH-метром или методом индикации. По показателю рН определяют нарушение кислотно-щелочного баланса. Тест проводится при подозрении на мочекаменную болезнь, уретрит, гломерулонефрит и другие урологические болезни. По кислотности урины определяют сдвиги в кислотно-щелочном балансе организма, которые влияют на метаболизм в почках.
Что значит pH мочи
Кислотность – лабораторный показатель, по которому определяют концентрацию гидроксильных и водородных ионов в жидкости. В зависимости от его значений в общем анализе мочи, выявляют:
- метаболические сбои;
- патологии дыхательной системы;
- нарушение кислотно-щелочного баланса;
- некорректность работы мочевыделительной, эндокринной систем.
Определение pH мочи нужно при подозрении на урологические болезни. По ее кислотности определяют состав конкрементов у больных с камнями в почках. Если в моче преобладают компоненты со щелочными свойствами, pH больше 7. При высокой концентрации кислотных веществ этот показатель меньше 7.
По ее кислотности определяют состав конкрементов у больных с камнями в почках. Если в моче преобладают компоненты со щелочными свойствами, pH больше 7. При высокой концентрации кислотных веществ этот показатель меньше 7.
Изменение кислотности урины – следствие нарушения обмена веществ, системных болезней, некорректности работы многих органов:
- почек;
- легких;
- печени;
- паращитовидной железы.
В медицинской практике показатель кислотности определяют в рамках общего анализа мочи (ОАМ). В зависимости от причины обращения человека в поликлинику, лабораторные данные предоставляют специалисту разную информацию. По степени нарушения рН-баланса мочи врач определяет:
- характер течения болезни;
- стратегию терапии;
- эффективность лечения диуретиками;
- необходимость применения физиотерапии;
- особенности диетического питания.
В клиниках для определения кислотности биоматериала применяются электронные ионометры или индикаторная бумага.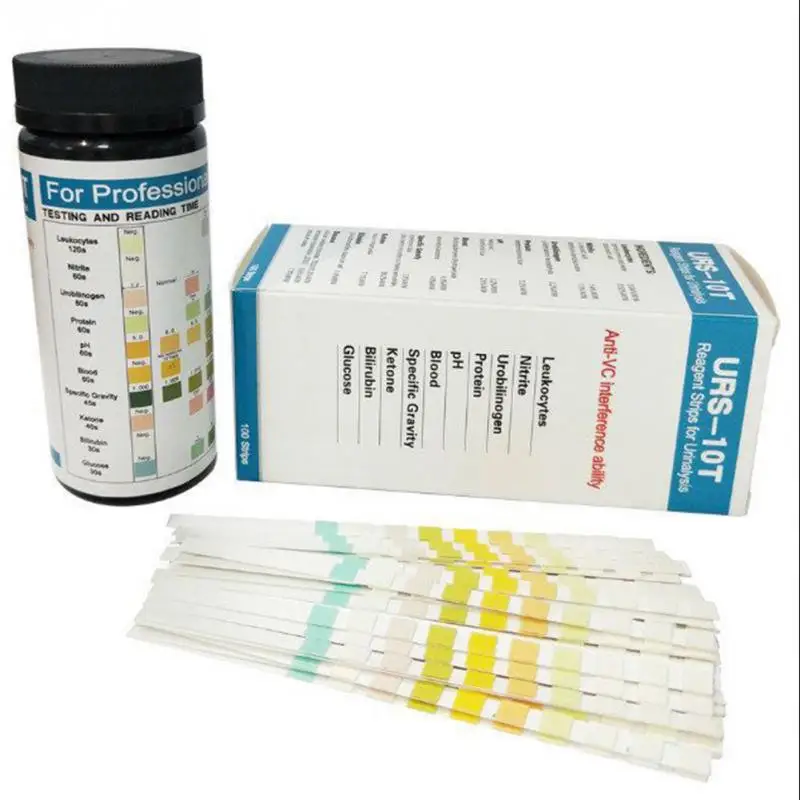
От чего зависит кислотность урины
Показатель pH в моче колеблется на протяжении суток. Он зависит от многих факторов:
- водного режима;
- особенностей питания;
- корректности работы ЖКТ.
Наиболее низкий показатель кислотности приходится на ночное время и раннее утро – 4.9-5.2 единицы. После завтрака он резко поднимается до 7-8 единиц. Если значения pH мочи отклоняются на 0.5-1 единицу, такое состояние считается физиологическим.
На кислотность влияют:
- скорость обменных процессов;
- воспаление органов мочеполовой системы;
- корректность работы канальцевой системы почек;
- кислотность желудочного сока;
- болезни, приводящие к защелачиванию и закислению крови.
При соблюдении молочно-овощной диеты щелочность мочи увеличивается. Если в меню преобладают хлебобулочные изделия и мясо, увеличивается ее кислотность. Нарушение кислотно-щелочного баланса наблюдается у больных с диареей.
Как правильно подготовиться и собрать материал на анализ
Для ОАМ используют утреннюю мочу, которую собирают сразу после пробуждения. В большинстве лабораторий pH определяют методом индикаторов. Результаты исследования зависят от правильности подготовки к сбору материала. Чтобы избежать ложноположительных и ложноотрицательных результатов, вносят изменения в рацион и водный режим.
В большинстве лабораторий pH определяют методом индикаторов. Результаты исследования зависят от правильности подготовки к сбору материала. Чтобы избежать ложноположительных и ложноотрицательных результатов, вносят изменения в рацион и водный режим.
За 2 дня до сдачи анализа надо соблюдать диету. Из рациона исключают продукты, которые меняют цвет мочи и влияют на ее кислотность:
- зелень;
- спиртное;
- свекла;
- красные ягоды;
- рыбные консервы;
- жирная пища;
- копчености;
- морепродукты;
- морковь.
Предъявляются требования к образу жизни больного. За 2 суток до забора мочи следует:
Правила сбора биоматериала:
- перед сбором урины обмывают гениталии с нейтральным мылом;
- первые 30 мл мочи спускают в унитаз;
- собирают в контейнер 60 мл средней порции;
- емкость с мочой закрывают плотной крышкой и ставят в холодильник.
Биоматериал доставляют в лабораторию в течение 1.
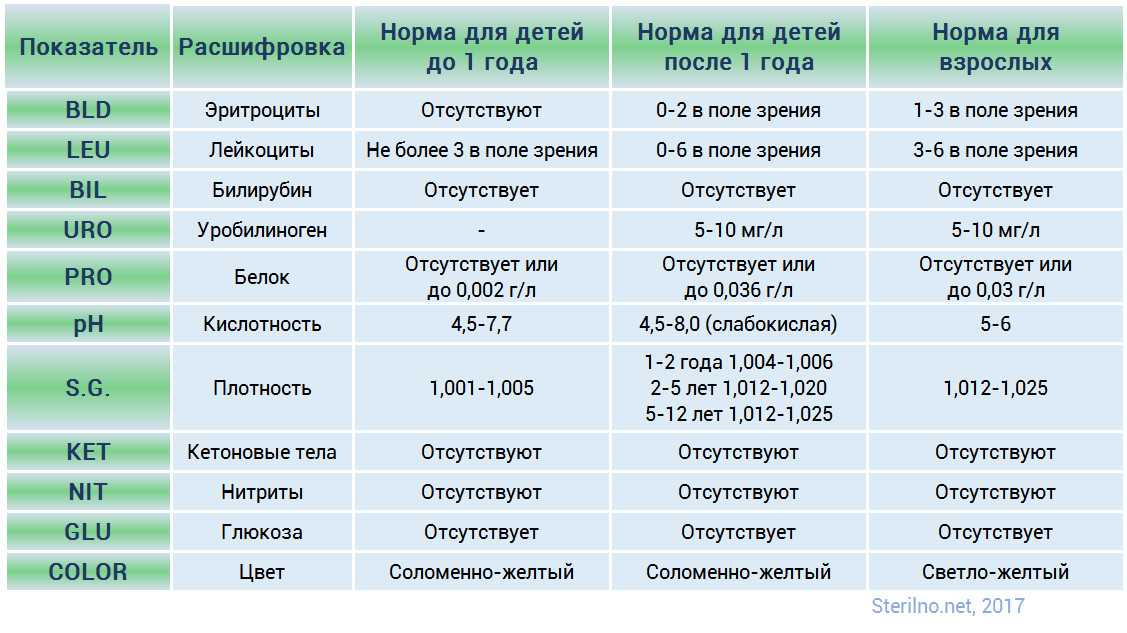
Норма кислотности
Расшифровка результатов ОАМ осуществляется с учетом пола, возраста и времени сбора биоматериала. pH мочи в норме находится в диапазоне от 5 до 7. Если показатель не превышает 6 единиц, реакция слабокислая, а если больше 7 – щелочная. В зависимости от рациона и водного режима, нормальная кислотность может снижаться до 4.5 или подниматься до 8 единиц.
У детей
Уровень pH мочи у грудничка, рожденного в срок, составляет 5.4-5.9. У недоношенных детей он находится в пределах 4.8-5.3. Спустя несколько суток водородный показатель колеблется в широком диапазоне. Это связано с нестабильностью работы органов пищеварительной, эндокринной и мочевыделительной систем.
Кислотность урины зависит от особенностей питания ребенка:
- при грудном вскармливании – 6.9-7.7;
- при вскармливании молочными смесями – 5.

Со временем кислотно-щелочной баланс стабилизируется, и pH достигает нормальных значений.
У женщин
У здорового человека кислотность урины не превышает 7. У 90% женщин этот показатель находится в пределах 6.0-6.5. Колебания в кислую и щелочную сторону не всегда связаны с болезнями. Во время вынашивания плода, при менструации в организме происходят изменения, которые сильно влияют на метаболизм.
Нормальная кислотность у женщин:
- при беременности – 4.5-8;
- во время лактации – 6.4-7.7.
Врачи не рекомендуют сдавать мочу на анализ во время менструаций. При смешении с кровью ее кислотность сильно меняется. С возрастом у большинства женщин pH смещается в кислую сторону. Недостаток эстрогена ведет к вымыванию из костей минералов, которые нейтрализуют в организме кислоты.
У мужчин
Кислотность мочи у мужчины и женщины отличаются незначительно. Но у мужчин процентное содержание мышечной ткани выше, в их рационе преобладают белки. В результате pH мочи смещается преимущественно в кислую сторону:
В результате pH мочи смещается преимущественно в кислую сторону:
| Параметры, влияющие на кислотность биоматериала | Нормальный pH |
| сбор биоматериала в утренние часы | 6.0-6.5 |
| слаборазвитая мускулатура | 6.3-6.6 |
| развитая мускулатура | 6.7-7.1 |
На скорость метаболизма и кислотно-щелочной баланс влияет прием анаболиков. Поэтому у мужчин, занимающихся спортом, кислотность биоматериала колеблется в диапазоне от 6 до 8.
Как определить pH в домашних условиях
Не обязательно проводить анализ pH мочи в поликлинике. Существуют домашние способы определения водородного показателя. Они используются людьми с хроническими болезнями (уратурией, уролитиазом, сахарным диабетом), которые должны постоянно контролировать кислотность мочи.
Чтобы измерить pH мочи, используют такие способы:
- Тест-полоска. Специальные индикаторы продаются в аптеках. Они имеют вид продолговатых бумажных полос желтого цвета.

- Метод Магаршака. В аптеках продаются специальные контейнеры с реагентами. При помещении в него собранной жидкости происходит химическая реакция. По цвету выпавшего осадка вычисляют кислотность мочи. Если оттенок ярко-фиолетовый, pH понижен, а если зеленоватый – повышен.
- Индикаторная бумага. Для анализа используют бумажные полосы красного и синего цвета. Их помещают в контейнер с мочой. Если оттенок индикаторов не меняется, кислотность находится в пределах нормы. Окрашивание синей полосы в красный цвет указывает на закисление, а красной полосы в синий цвет – на защелачивание жидкости.
При необходимости постоянного контроля кислотного баланса урины рекомендуется использовать pH-метры (иономеры). Внутрь прибора помещают образец биоматериала, после чего на экран выводится значение кислотности. Этот метод наиболее точно определяет pH.
Внутрь прибора помещают образец биоматериала, после чего на экран выводится значение кислотности. Этот метод наиболее точно определяет pH.
Современные pH-метры подходят для измерения кислотности не только жидкостей, но и пищевых продуктов. Это помогает людям с камнями в почках корректировать диету, добавлять в меню новые блюда.
Причины кислой реакции мочи
Кислая моча (ацидурия) – это когда pH ниже 5. Кислая среда создает благоприятные условия для размножения болезнетворных бактерий. К причинам закисления урины относятся:
- злоупотребление кислыми фруктами и напитками;
- избыточные физические нагрузки;
- цистит;
- нефротический синдром;
- диарея;
- подагра;
- туберкулез почек;
- повышенная выработка альдостерона;
- протеиновая диета;
- длительное голодание;
- острое инфицирование крови;
- пиелонефрит;
- дефицит калия;
- сахарный диабет;
- почечный ацидоз;
- красная волчанка;
- болезнь Вильсона.

Кислотность жидкости повышается при лечении гормональными препаратами, инфузионном вливании раствора хлористого натрия. Если проявляются симптомы отравления – головные боли, тошнота, рвотные позывы, – это указывает на ацидоз. Кислотность среды увеличивается на фоне недостаточной вентиляции легких.
Причины ощелачивания
Щелочная реакция мочи в 80% случаев сопутствует урологическим болезням. Но иногда pH повышается после неукротимой рвоты или диареи. Щелочь в моче обнаруживается при длительном лечении минеральными водами.
Если pH мочи повышен у ребенка, это указывает на аллергические реакции или злоупотребление жирной пищей.
Основные причины ощелачивания урины:
- недостаточность почек;
- гломерулонефрит;
- повышенная кислотность желудочного сока;
- гиперактивность паращитовидной железы;
- примеси крови в моче;
- переизбыток калия в организме;
- молочно-растительная диета;
- недостаток альдостерона;
- опухолевое поражение мочевых путей.

Как нормализовать кислотно-щелочное соотношение
Чтобы уменьшить или повысить водородный показатель урины, определяют причину нарушения метаболизма. Если ощелачивание или закисление спровоцировала инфекция мочевыводящих путей, используют лекарства нескольких групп:
- антибиотики – Аугментин, Амосин, Цеклор, Кефлекс;
- сорбенты – Смекта, Мультисорб, Сорбекс, Энтеросгель;
- уросептики – Нолицин, Канефрон, Фурагин, Уролесан;
- литолитики (препараты для растворения камней) – Солутан, Уролит-У, Магурлит, Блемарен.
Для снижения кислотности применяются народные средства – содовая вода, морковный и томатный сок, настой из шпината. Для восстановления метаболизма пациенты должны придерживаться диетотерапии. При закислении мочи соблюдают молочно-растительную, а при защелачивании – белковую диету.
pH-метрия – один из способов определения нарушений метаболизма, воспалений и других проблем. Кислотность мочи увеличивается и понижается при сбое в работе мочеполовой системы. По результатам исследования определяют эффективность лечения диуретиками, риск камнеобразования в почках. Чтобы избежать колебаний pH мочи, нужно сбалансированно питаться, вовремя лечить инфекции, вести здоровый образ жизни.
По результатам исследования определяют эффективность лечения диуретиками, риск камнеобразования в почках. Чтобы избежать колебаний pH мочи, нужно сбалансированно питаться, вовремя лечить инфекции, вести здоровый образ жизни.
Влияние рН мочи на процессы камнеобразования при уролитиазе. рН мочи что это ?
8 мая 2022
Кислотность (pH) мочи является одним из ключевых показателей, позволяющих оценить активность процессов литогенеза при мочекаменной болезни (МКБ).
Нормальные показатели pH мочи могут варьировать в достаточно широких пределах. Это связано с тем, что pH мочи не является жесткой физиологической константой организма, как, например, pH крови. Показатель pH мочи можно отнести к так называемым мягких или пластических физиологических констант, которые могут отклоняться от стабильного уровня в относительно широких пределах без существенных изменений для функционирования организма.
Согласно современным представлениям о патогенезе МКБ, изменения pH мочи играют важную роль в процессах камнеобразования. Исследовано и описано показатели pH мочи, специфические для образования того или иного типа мочевых камней. Определены значения pH мочи, которые являются фактором риска литогенеза и, наоборот, при которых процессы камнеобразования не протекают или протекают не так интенсивно.
Исследовано и описано показатели pH мочи, специфические для образования того или иного типа мочевых камней. Определены значения pH мочи, которые являются фактором риска литогенеза и, наоборот, при которых процессы камнеобразования не протекают или протекают не так интенсивно.
Хорошо известно, что кристаллизация кальция фосфата, мочевой кислоты, струвита, цистина напрямую зависит от показателей pH мочи. Известно, что риск образования мочекислых конкрементов возрастает при pH мочи 6,5. Струвитного камни образуются при pH мочи> 7,0.
При этом изменения pH мочи могут быть связаны не только с МКБ, но и с другими патологическими процессами. В том числе такими, протекающими в мочевыводящих путях (уротелиальний рак, метаболические нарушения).
Известны хронические неинфекционные заболевания, для которых характерны изменения pH мочи. Одним из самых распространенных хронических заболеваний, при котором наблюдается закисление мочи, ожирение и метаболический синдром. Доказано, что значение показателя рН мочи обратно пропорционально индекса массы тела (ИМТ) у пациентов с МКБ. Высокий ИМТ увеличивает риск развития МКБ. Известно, что у пациентов, страдающих ожирением и имеют ИМТ> 33,1 кг / м2, выше риск развития мочекислых и струвитного конкрементов.
Высокий ИМТ увеличивает риск развития МКБ. Известно, что у пациентов, страдающих ожирением и имеют ИМТ> 33,1 кг / м2, выше риск развития мочекислых и струвитного конкрементов.
Некоторые авторы считают, что у пациентов, страдающих метаболическим синдромом и ожирением, инсулинорезистентность может выступать в качестве патогенетической основы нарушенного кислотно-щелочного равновесия, приводит в конечном счете к ацидификации мочи. Проведенные исследования показали, что инсулинорезистентность способна приводить к нарушению экскреции иона аммония (Nh5 +) что, в свою очередь, приводит к снижению pH мочи у данной группы пациентов.
Известно, что к изменениям pH мочи также могут приводить такие состояния как почечный канальцевый ацидоз (НКА), хроническая уреазопродукуюча инфекция мочевых путей.
Кроме патологических процессов, протекающих в мочевых путях, метаболического синдрома, НКА к изменению показателей pH мочи могут приводить особенности питания человека.
Обычно, частое употребление богатой животным белком пищи, злоупотребление алкоголем приводит к подкисление мочи. Высокие показатели pH мочи наблюдаются при соблюдении вегетарианской диеты, использовании щелочных добавок.
Высокие показатели pH мочи наблюдаются при соблюдении вегетарианской диеты, использовании щелочных добавок.
Таким образом, pH мочи, с одной стороны, является одним из значимых маркеров, сигнализирующих о наличии патологических изменений как в организме в целом, так и в мочевыделительной системе в частности. С другой стороны, pH мочи остается одним из ключевых параметров, регулирующих состояние мочевыделительной системы, определяющие тип метаболических литогенных нарушений при МКБ.
Учитывая все вышесказанное, целью данной работы стало изучение влияния pH мочи на образование мочевых камней различного химического состава и на уровень экскреции с мочой основных веществ, образующих камни.
Материалы и методы
Работа выполнена на базе НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина — филиал ФГБУ «НМИЦ радиологии» Минздрава России.
В исследовании были изучены данные 708 пациентов (303 мужчины и 405 женщин) с диагнозом МКБ, проходивших как амбулаторное, так и стационарное лечение на базе института. Исследование проводилось ретроспективно.
Исследование проводилось ретроспективно.
Всем пациентам выполнялся биохимический анализ крови (кальций, натрий, магний, фосфор, хлор, мочевая кислота, мочевина, креатинин), биохимический анализ суточной мочи (определение pH утренней мочи, кальций, натрий, магний, фосфор, хлор, мочевая кислота, мочевина, креатинин), определение химического состава мочевого камня.
Биохимическое исследование крови и мочи выполнялось на анализаторе ADVIA 1200 (Bayer-Siemens) по стандартным методикам с помощью диагностических наборов реагентов фирмы Siemens (Германия).
Определение химического состава мочевого камня выполнялось методом инфракрасной спектроскопии с использованием спектрометра Nicolet iS10 (Thermo Scientific, США). В процессе работы применялась стандартная библиотека спектров мочевых камней, предоставленная производителем. Распределение смешанных мочевых камней по группам происходило следующим образом: при наличии в составе исследуемого конкремента более 50% минерального компонента идентичного заявленного в группе данные о пациенте заносились в соответствующую группу. Такой подход к классификации типов мочевых конкрементов является наиболее распространенным.
Такой подход к классификации типов мочевых конкрементов является наиболее распространенным.
Поиск статистической зависимости между частотой заболеваемости типов мочевых камней и величиной pH мочи выполнялся с помощью критерия χ2-Хи-квадрата Пирсона с введенной формулы в Microsoft Excel.
РЕЗУЛЬТАТЫ
В зависимости от показателей pH мочи все больные были разделены на несколько групп (табл. 1):
- В первой группе (ph2) показатели pH мочи составили 4,8-5,0. К этой группе включены данные 111 пациентов;
- Вторая группа (ph3): интервал значений pH мочи составил 5,1-5,3 включены данные 71 пациента;
- Третья группа (ph4): интервал значений pH мочи составил 5,4-5,5 включены данные 162 пациентов;
- Четвертая группа (ph5): интервал значений pH мочи 5,6-5,9, включены данные 74 пациентов;
- Пятая группа (pH5): интервал значений pH мочи 6,0-6,1, включены данные 129 пациентов;
- Шестая группа (pH6): интервал значений pH мочи 6,2-6,5, включены данные 61 пациента;
- Седьмая группа (pH7): интервал значений pH мочи 6,6-7,0, включены данные 57 пациентов;
- Восьмая группа (pH8): интервал значений pH мочи 7,1-9,0, включены данные 38 пациентов
Таблица 1. Распределение типов мочевых камней пациентов по группам в зависимости от показателей pH мочи (в% от общего числа камней в группе)
Распределение типов мочевых камней пациентов по группам в зависимости от показателей pH мочи (в% от общего числа камней в группе)
Table 1. Urinary stones types distribution by groups depending on the urine pH (% of the total number of stones in the group)
| Параметры Indicator | рН1 | рН2 | рН3 | рН4 | рН5 | рН6 | рН7 | рН8 |
|---|---|---|---|---|---|---|---|---|
| Интервал значений рН / рН level | 4,8 — 5,0 | 5,1 — 5,3 | 5,4 — 5,5 | 5,6 — 5,9 | 6,0 — 6,1 | 6,2 — 6,5 | 6,6 — 7,0 | 7,1 — 9,0 |
| Камни всех типов / All type stones | 111 | 71 | 162 | 74 | 129 | 61 | 57 | 38 |
| СаОХ камни (n) # / СаОХ stones (n) # | 43 | 26 | 73 | 38 | 35 | 23 | 17 | 4 |
| СаОх %* | 38,7 | 36,6 | 45,1 | 51,4 | 27,1 | 37,7 | 29,8 | 10,5 |
| Ur камни (n) # / Ur stones (n) # | 47 | 24 | 27 | 10 | 18 | 2 | 7 | 1 |
| Ur %* | 42,3 | 33,8 | 16,7 | 13,5 | 14,0 | 3,3 | 12,3 | 2,6 |
| Dh камни (n) # / Dh stones (n) # | 16 | 15 | 42 | 17 | 61 | 31 | 22 | 18 |
| Dh%* | 14,4 | 21,1 | 25,9 | 23,0 | 47,3 | 50,8 | 38,6 | 47,4 |
| OxDh камни (n) # / OxDh stones (n) # | 21 | 16 | 46 | 29 | 44 | 10 | 13 | 4 |
| OxDh %* | 18,9 | 22,5 | 28,4 | 39,2 | 34,1 | 32,8 | 22,8 | 10,5 |
| Str камни (n) # / Str stones (n) # | 1 | 2 | 8 | 5 | 12 | 3 | 11 | 14 |
| Str %* | 0,9 | 2,8 | 4,9 | 6,8 | 9,3 | 4,9 | 19,3 | 36,8 |
| AmUr камни (n) # / AmUr stones (n) # | 1 | 1 | 2 | 0 | 0 | 2 | 0 | 1 |
| AmUr %* | 0,9 | 1,4 | 1,2 | 0 | 0 | 3,3 | 0 | 2,6 |
| Другие # / Others # | 3 | 3 | 10 | 5 | 3 | 0 | 0 | 0 |
| Другие %* / Others % | 2,7 | 4,2 | 6,2 | 6,8 | 2,3 | 0 | 0 | 0 |
Примечание: Преобладающий компонент мочевых камней: СаОх — кальция оксалат, Ur — мочевая кислота, Dh — Далли (карбонатапатит), OxDh — кальция оксалат / карбонатапатит, Str — струвит, AmUr — аммония урат. # — абсолютное число камней каждого типа в группах рН1-рН8; * — процентное распределение камней каждого типа в группах рН1-рН8; Note: The predominant component of urinary stones: СаОх — calcium oxalate, Ur — uric acid, Dh — dallite (carbonatapatite), OxDh — calcium oxalate / carbonatapatite, Str — struvite, AmUr — ammonium urate. # — absolute number of stones of each type in groups рН1-рН8; * — percentage distribution of stones of each type in groups рН1-рН8
# — абсолютное число камней каждого типа в группах рН1-рН8; * — процентное распределение камней каждого типа в группах рН1-рН8; Note: The predominant component of urinary stones: СаОх — calcium oxalate, Ur — uric acid, Dh — dallite (carbonatapatite), OxDh — calcium oxalate / carbonatapatite, Str — struvite, AmUr — ammonium urate. # — absolute number of stones of each type in groups рН1-рН8; * — percentage distribution of stones of each type in groups рН1-рН8
Рис. 1. Частота образования основных типов мочевых камней (в% от общего количества) в зависимости от рН мочи
Fig. 1. Frequency of occurrence of the main types of urinary stones (in% of the total amount) depending on urine pH
Анализ полученных данных показал, что частота образования мочевых камней, состоящих из мочевой кислоты, снижается по мере роста показателей pH мочи с 42,3% (ph2) до 2,6% (pH8) (р = 0,0000004) (рис. 1, табл.1).
Результаты проведенного исследования во многом совпадают с данными, представленными в других подобных работах. Считается, что низкие показатели pH мочи является одним из основных факторов риска развития мочекислого уролитиаза. Известно, что при смещении показателей pH мочи в кислую сторону снижается и растворимость мочевой кислоты в моче.
Считается, что низкие показатели pH мочи является одним из основных факторов риска развития мочекислого уролитиаза. Известно, что при смещении показателей pH мочи в кислую сторону снижается и растворимость мочевой кислоты в моче.
Так, при pH мочи равном 5,35 для получения перенасыщенного раствора необходимо добиться концентрации мочевой кислоты в моче 200 мг / л. При pH мочи равном 6,5 для получения перенасыщенной мочи необходимо уже 1200 мг / л мочевой кислоты. Таким образом, pH мочи является одним из основных факторов, стимулирующих мочекислый литогенез.
Кроме низких показателей pH мочи (<5,6) существенным фактором риска развития мочекислого уролитиаза является высокий уровень экскреции мочевой кислоты с мочой. Анализ полученных данных показал, что уровень экскреции мочевой кислоты в интервалах ph2 — ph5 рос с 3,256 ммоль / сут до 3,814 ммоль / сут, в интервалах ph5 — pH8 снижался с 3,814 ммоль / сут до 2,826 ммоль / сут (табл.2, рис. 2). Максимальный уровень экскреции мочевой кислоты с мочой был зафиксирован в диапазоне pH мочи равном 5,6-5,9 (ph5) и составил 3,814 ммоль / сут (табл. 2, рис.2).
2, рис.2).
Рис.2. Средние значения показателей экскреции (ммоль / сут) магния, фосфатов, кальция и мочевой кислоты в ранжированных интервалах значений рН мочи
Fig.2. Average values of magnesium, phosphates, calcium and uric acid excretion depending of urine pH level
Таблица 2. Распределение средних значений показателей экскреции основных литогенных веществ в зависимости от показателей pH мочи
Table 2. The main lithogenic substances excretion level depending on the urine pH
| Параметры Indicator | рН1 | рН2 | рН3 | рН4 | рН5 | рН6 | рН7 | рН8 |
|---|---|---|---|---|---|---|---|---|
| Интервал значений рН / рН level | 4,8 — 5,0 | 5,1 — 5,3 | 5,4 — 5,5 | 5,6 — 5,9 | 6,0 — 6,1 | 6,2 — 6,5 | 6,6 — 7,0 | 7,1 — 9,0 |
| Камни всех типов (всего n=708) / All type stones (total n=708) | 111 | 71 | 162 | 74 | 129 | 61 | 57 | 38 |
Экскреция кальция в интервалах сер. значення / Calcium excretion значення / Calcium excretion |
4,365 | 4,554 | 5,1185 | 6,184 | 4,897 | 4,992 | 4,06 | 3,01 |
| Стандартная ошибка среднего (SE) / Standard error of the mean (SE) | 0,237 | 0,329 | 0,197 | 0,316 | 0,216 | 0,375 | 0,347 | 0,317 |
| Экскреция мочевой кислоты в интервалах сер.значення / Uric acid excretion | 3,256 | 3,268 | 3,314 | 3,814 | 3,310 | 2,802 | 3,020 | 2,826 |
| Стандартная ошибка среднего (SE) / Standard error of the mean (SE) | 0,126 | 0,145 | 0,103 | 0,155 | 0,109 | 0,142 | 0,169 | 0,175 |
Экскреция фосфатов в интервалах сер. значення / Phosphate excretion значення / Phosphate excretion |
27,703 | 25,787 | 26,349 | 29,149 | 24,911 | 23,931 | 24,658 | 19,203 |
| Стандартная ошибка среднего (SE) / Standard error of the mean (SE) | 1,129 | 1,346 | 0,823 | 1,357 | 0,909 | 1,441 | 1,420 | 1,546 |
| Экскреция магния в интервалах сер.значення / Magnesium excretion | 3,832 | 3,908 | 3,693 | 4,316 | 3,762 | 3,553 | 3,393 | 2,896 |
| Стандартная ошибка среднего (SE) / Standard error of the mean (SE) | 0,217 | 0,273 | 0,149 | 0,231 | 0,199 | 0,254 | 0,254 | 0,392 |
Таким образом, контроль за показателями pH мочи, поддержание pH мочи на уровне> 5,9 является одним из основных методов профилактики рецидива мочекислого уролитиаза.
Частота встречаемости кальций-оксалатных конкрементов росла в интервалах pH 5,1 (ph3) — 5,9 (ph5) и 6,1 (pH5) — 6,5 (pH6) (табл.1, рис.1). При этом в интервалах pH 5,6 (ph5) — 6,1 (pH5) и 6,5 (pH6) — 9,0 (pH8) было зафиксировано резкое снижение частоты рождения кальций-оксалатных мочевых камней (табл.1, рис. 1).
Существует мнение, что как местный, так и системный ацидоз способен стимулировать кальций-оксалатный литогенез. Ацидоз подавляет экспрессию и активность кальциевого канала TRPV5, который локализован в конце дистального канальцев. В то же время, ацидоз увеличивает экспрессию кальцийсвязывающего белка кальбиндина 28к. Таким образом, местный и системный ацидоз способен стимулировать выведение с мочой кальция и фосфора и тем самым увеличивать риск образования кальцийоксалатних мочевых камней.
Полученные в этом исследовании данные частично подтверждают результаты предыдущих работ: анализ показал, что наибольшие показатели кальциурии наблюдались при pH мочи 5,4 (ph4) — 6,1 (pH5) (табл. 2, рис.2). Максимальный уровень экскреции кальция с мочой был зафиксирован при pH мочи 5,6-5,9 (ph5).
2, рис.2). Максимальный уровень экскреции кальция с мочой был зафиксирован при pH мочи 5,6-5,9 (ph5).
Таким образом, ацидоз стимулирует увеличение уровня экскреции кальция с мочой. Однако в то же время, следует отметить, что высокий уровень кальциурии (6,184 ммоль / сут) был зафиксирован при умеренном смещении pH мочи в кислую сторону (5,4-6,1), в то время как при резко кислой моче (pH мочи <5,0), показатели экскреции кальция находились на низких значениях — 4,365 ммоль / сут, так же, как и при pH мочи 6,6-7,0 (pH7) (4,06 ммоль / сут).
Соответственно, фактором риска формирования оксалатных конкрементов являются показатели pH мочи уровне 5,6-5,9. Именно при данных показателях pH мочи отмечается высокий уровень кальциурии и наибольшая частота рождения кальций-оксалатных мочевых камней.
Данное исследование также показало, что распространенность карбонатапатитних мочевых камней увеличивается при росте показателей pH мочи. Данная тенденция прослеживается особенно четко в интервалах pH мочи 5,6 (ph5) — 6,5 (pH6): распространенность камней из фосфата кальция увеличилась с 23,0% до 50,8% (табл. 1, рис.1) (р = 0,00003). Максимальная частота рождения карбонатапатитних конкрементов была зафиксирована при показателях pH мочи 6,2-6,5 и составила 50,8%.
1, рис.1) (р = 0,00003). Максимальная частота рождения карбонатапатитних конкрементов была зафиксирована при показателях pH мочи 6,2-6,5 и составила 50,8%.
Увеличение распространенности карбонатапатитних камней при увеличении значений pH мочи можно объяснить. Проведенные ранее работы показали, что растворимость кальция фосфата существенно зависит от pH мочи: при pH мочи <6,2 растворимость солей фосфата кальция существенно улучшается, что, соответственно, снижает вероятность литогенеза.
По данным, полученным в данной работе, высокий уровень фосфатурии (29,149 ммоль / сут), так же, как и высокие показатели кальциурии, наблюдались при показателях pH мочи 5,6-5,9 (ph5).
Несмотря на то, что максимальный уровень экскреции как кальция, так и фосфора с мочой был зафиксирован при pH мочи 5,6-5,9, максимальная частота образования карбонатапатитних камней зафиксирована на цифрах pH мочи равных 6,0-6,5. Вероятно, при уролитиазе с камнями из фосфата кальция уровень концентрации веществ, образующих камни в моче является второстепенным. Уровень pH мочи оказывает большее влияние на литогенез, так как влияет на растворимость солей фосфата кальция. Соответственно, при проведении профилактических мероприятий по предотвращению повторного камнеобразования необходимо контролировать pH мочи на уровне <5,9.
Уровень pH мочи оказывает большее влияние на литогенез, так как влияет на растворимость солей фосфата кальция. Соответственно, при проведении профилактических мероприятий по предотвращению повторного камнеобразования необходимо контролировать pH мочи на уровне <5,9.
Исследование показало, что резкий рост встречи струвитного конкрементов наблюдается в интервалах pH мочи 6,6 (pH7) — 9,0 (pH8) (табл.1, рис.1) (р = 0,00004). Полученные данные можно сравнить с общепринятыми представлениями о литогенез струвитного камней.
ВЫВОДЫ
Показатель pH мочи является одним из основных факторов, влияющих на литогенез при МКБ. Полученные данные позволили сделать вывод, что при метафилактици оксалатного уролитиаза необходимо поддерживать pH мочи на цифрах> 5,9, фосфатного (карбонатапатитного) уролитиаза 5,9, при струвитного камнях <6,6.
Поделиться
Поделиться
Поделиться
Поделится
Поделится
Новый комментарий
Войти с помощью
Отправить
рН мочи — что он говорит нам, как измерять и что означает — PURI
рН мочи может многое сказать нам о нашем здоровье. В этой статье мы рассмотрим, как измерить pH мочи и как вы можете использовать его для управления своим здоровьем.
В этой статье мы рассмотрим, как измерить pH мочи и как вы можете использовать его для управления своим здоровьем.
Одной из основных функций почек является регулирование кислотности. pH мочи является одним из способов измерения кислотно-щелочного баланса нашего организма.
«Важной функцией почек является регулирование кислотности. По мере метаболизма клеток они постоянно производят кислоты. Продукты, которые мы едим, могут увеличить кислотность в нашем организме».
Мундт, Лилиан; Шанахан, Кристи. Учебник Граффа по анализу мочи и биологических жидкостей (стр. 12). LWW. Киндл издание. Твитнуть
Что такое рН?
pH является мерой кислотности или щелочности жидкости. Технически это мера количества ионов водорода в растворе. Это относительная мера, и шкала pH используется для измерения того, насколько кислым или щелочным является раствор.
Шкала начинается с 0 и идет до 14. От 0 до 6 — кислая, 7 — нейтральная и от 8 до 14 — щелочная.
От 0 до 6 — кислая, 7 — нейтральная и от 8 до 14 — щелочная.
Некоторые примеры того, что это означает в реальной жизни:
- автомобильный аккумулятор имеет рН 0 и очень опасен при прикосновении или проглатывании
- вода имеет рН 7, она нейтральна и не причинит нам вреда
- отбеливатели и очистители канализации имеют pH 14 и, опять же, очень опасны для человека
pH мочи
pH мочи может дать нам полезную информацию о нашем здоровье.
В организме есть два органа, которые уравновешивают кислоту в нашем организме. И легкие, и почки играют роль в поддержании рН крови.
На рН мочи влияет роль почек в поддержании кислотно-щелочного баланса в организме. Почки работают, чтобы поддерживать pH крови на уровне около 7,4. Это означает, что по мере прохождения крови через почки рН мочи изменяется в зависимости от того, что требуется для поддержания рН крови.
Моча человека может варьироваться от 4,6 до 8,0. Средний рН мочи составляет около 6. Это означает, что наша моча слабокислая.
Средний рН мочи составляет около 6. Это означает, что наша моча слабокислая.
Мы рассмотрим причины кислотности.
pH крови
Хотя в этой статье мы обсуждаем pH мочи, важно отметить, что в клинических условиях pH крови обычно проверяется и используется.
Поддержание кислотно-щелочного баланса
Организму необходимо поддерживать кислотно-щелочной баланс для правильного функционирования нашего организма.
Когда уровень кислоты в нашей крови слишком высок, это называется ацидозом. Когда кровь слишком щелочная, это называется алкалозом. Оба условия могут вызвать серьезные проблемы.
Причины ацидоза и алкалоза
Некоторые из причин метаболического ацидоза включают:
- Лактоацидоз от шока, инфекции, гипоксии.
- Почечная недостаточность
- Кетоны, вызванные сахарным диабетом или алкоголем
- Лекарства или токсины.
- Почечный канальцевый ацидоз
- Диарея
- Болезнь Аддисона.

Causes of metabolic alkalosis include:
- Vomiting
- diuretics
- Excessive alkali drugs, such as for acid dyspepsia
- Burns
Treatment for acidosis or alkalosis is the treatment of the underlying причины.
Как измерить рН мочи?
Измерить рН мочи очень просто. Мы написали полную статью, доступ к которой вы можете получить здесь.
Низкий рН мочи: новый признак метаболического синдрома
Кислотно-основные и электролитные расстройства
У вас есть доступ Ограниченный доступ
Khashayar SakhaeeCJASN, сентябрь 2007 г., 2 (5) 883-888; DOI.
Abstract
Предпосылки и цели. Метаболический синдром связан с изменениями функции почек. Чрезмерно кислая моча была описана как почечное проявление метаболического синдрома у пациентов с мочекаменной болезнью. В этом исследовании изучалась связь между метаболическим синдромом и рН мочи у лиц без истории нефролитиаза.
В этом исследовании изучалась связь между метаболическим синдромом и рН мочи у лиц без истории нефролитиаза.
Дизайн, обстановка, участники и измерения. В этом перекрестном амбулаторном исследовании приняли участие в общей сложности 148 взрослых, у которых не было камней в почках. Были получены данные о росте, весе, АД, крови натощак и 24-часовом биохимическом анализе мочи. рН мочи измеряли рН-электродом. Оценивались следующие признаки метаболического синдрома: АД; индекс массы тела; концентрации триглицеридов, глюкозы и холестерина ЛПВП в сыворотке. Степень резистентности к инсулину оценивали с помощью оценки модели гомеостаза резистентности к инсулину.
Результаты. У участников с метаболическим синдромом рН мочи в течение 24 часов был значительно ниже по сравнению с участниками без метаболического синдрома. Средний 24-часовой рН мочи, скорректированный с учетом возраста, пола, клиренса креатинина и 24-часового содержания сульфата мочи, снизился с 6,15, 6,10, 5,99, 5,85 до 5,69 с увеличением числа нарушений метаболического синдрома. Связь наблюдалась между 24-часовым рН мочи и каждым метаболическим признаком. После поправки на возраст, пол, клиренс креатинина, сульфат мочи и индекс массы тела была отмечена значимая обратная связь между рН мочи за 24 часа и степенью резистентности к инсулину.
Связь наблюдалась между 24-часовым рН мочи и каждым метаболическим признаком. После поправки на возраст, пол, клиренс креатинина, сульфат мочи и индекс массы тела была отмечена значимая обратная связь между рН мочи за 24 часа и степенью резистентности к инсулину.
Выводы. Чрезмерно кислая моча является признаком метаболического синдрома и связана со степенью резистентности к инсулину.
Метаболический синдром (МС) характеризуется совокупностью метаболических признаков, включая дислипидемию, гипергликемию, гипертонию, ожирение и резистентность к инсулину (1,2). Этот набор признаков тесно связан с диабетом 2 типа, атеросклеротическими сердечно-сосудистыми заболеваниями и повышенной сердечно-сосудистой смертностью и смертностью от всех причин (3,4). Изменения почечных гомеостатических механизмов также связаны с РС и его особенностями (5–7). Задержка натрия и мочевой кислоты связана с резистентностью к инсулину (7–9), тогда как гипергемодинамическое состояние почек приписывают ожирению (10). Более того, недавно была описана связь между РС и хронической болезнью почек (ХБП); пациенты с нарастающими признаками РС имели большую частоту и распространенность ХБП (11,12).
Более того, недавно была описана связь между РС и хронической болезнью почек (ХБП); пациенты с нарастающими признаками РС имели большую частоту и распространенность ХБП (11,12).
Другим новым почечным проявлением рассеянного склероза может быть чрезмерно кислая моча. Эта находка была впервые описана у пациентов с мочекислыми камнями в почках, большинство из которых страдали рассеянным склерозом (13). Кроме того, недавно у пациентов с сахарным диабетом 2 типа, не страдающих камнеобразованием, была обнаружена чрезмерно кислая моча (14). Это перекрестное исследование расширяет эти результаты и изучает взаимосвязь между кислотностью мочи и многочисленными признаками рассеянного склероза у широкого круга лиц, не страдающих камнеобразованием.
Материалы и методы
Участники исследования
Мы использовали местные объявления для набора добровольцев, которые хотели участвовать в исследовании. Критериями включения были возраст старше 21 года и способность дать информированное согласие. Мы хотели оценить людей с широким диапазоном массы тела; поэтому масса тела и/или индекс массы тела (ИМТ) не использовались в качестве критериев включения/исключения. Из исследования были исключены лица с состояниями, которые, как известно, изменяют pH мочи, такими как ХБП (определяемая по клиренсу креатинина <70 мл/мин [<1,17 мл/с]), почечный тубулярный ацидоз, хронические диарейные заболевания, почечнокаменная болезнь ( в анамнезе), первичный гиперпаратиреоз или инфекции мочевыводящих путей. Участники были проинструктированы держать любые лекарства, которые, как известно, влияют на рН мочи ( например ., щелочная терапия, диуретики) в течение 1 недели до исследования. К участию допускались лица с диабетом 2 типа, если они не принимали инсулин или тиазолидиндионы. Исследование было одобрено экспертным советом Юго-западного медицинского центра Техасского университета (Даллас, Техас).
Мы хотели оценить людей с широким диапазоном массы тела; поэтому масса тела и/или индекс массы тела (ИМТ) не использовались в качестве критериев включения/исключения. Из исследования были исключены лица с состояниями, которые, как известно, изменяют pH мочи, такими как ХБП (определяемая по клиренсу креатинина <70 мл/мин [<1,17 мл/с]), почечный тубулярный ацидоз, хронические диарейные заболевания, почечнокаменная болезнь ( в анамнезе), первичный гиперпаратиреоз или инфекции мочевыводящих путей. Участники были проинструктированы держать любые лекарства, которые, как известно, влияют на рН мочи ( например ., щелочная терапия, диуретики) в течение 1 недели до исследования. К участию допускались лица с диабетом 2 типа, если они не принимали инсулин или тиазолидиндионы. Исследование было одобрено экспертным советом Юго-западного медицинского центра Техасского университета (Даллас, Техас).
Сбор данных и измерения
Все участники собрали 24-часовой образец мочи под минеральным маслом, и во время сбора контейнер с мочой хранился в холодильнике или хранился в ящике со льдом. В конце сбора мочи у участников брали кровь натощак и измеряли рост, вес и АД. Американская кардиологическая ассоциация/Национальный институт сердца, легких и крови обновили определение метаболического синдрома в 2005 г. (15) до наличия трех или более из следующих признаков: ( 1 ) Повышенный уровень глюкозы в крови натощак (≥100 мг/дл, ≥6 ммоль/л) или медикаментозное лечение повышенного уровня глюкозы; ( 2 ) повышенное АД, определяемое как систолическое АД (САД) > 135 мм рт. ст., диастолическое АД > 85 мм рт. ст., или медикаментозное лечение гипертонии; ( 3 ) повышенный уровень триглицеридов в сыворотке крови натощак, определяемый как >150 мг/дл (>1,70 ммоль/л), или медикаментозное лечение гипертриглицеридемии; ( 4 ) низкий уровень холестерина ЛПВП в сыворотке крови натощак <50 мг/дл (<1,30 ммоль/л) у женщин и <40 мг/дл (<1,04 ммоль/л) у мужчин или медикаментозное лечение низкого уровня ЛПВП; и ( 5 ) абдоминальное ожирение, определяемое как окружность талии >88 см у женщин и >102 см у мужчин.
В конце сбора мочи у участников брали кровь натощак и измеряли рост, вес и АД. Американская кардиологическая ассоциация/Национальный институт сердца, легких и крови обновили определение метаболического синдрома в 2005 г. (15) до наличия трех или более из следующих признаков: ( 1 ) Повышенный уровень глюкозы в крови натощак (≥100 мг/дл, ≥6 ммоль/л) или медикаментозное лечение повышенного уровня глюкозы; ( 2 ) повышенное АД, определяемое как систолическое АД (САД) > 135 мм рт. ст., диастолическое АД > 85 мм рт. ст., или медикаментозное лечение гипертонии; ( 3 ) повышенный уровень триглицеридов в сыворотке крови натощак, определяемый как >150 мг/дл (>1,70 ммоль/л), или медикаментозное лечение гипертриглицеридемии; ( 4 ) низкий уровень холестерина ЛПВП в сыворотке крови натощак <50 мг/дл (<1,30 ммоль/л) у женщин и <40 мг/дл (<1,04 ммоль/л) у мужчин или медикаментозное лечение низкого уровня ЛПВП; и ( 5 ) абдоминальное ожирение, определяемое как окружность талии >88 см у женщин и >102 см у мужчин. Поскольку окружность талии не была доступна для многих людей, ИМТ ≥30 кг/м 2 использовался в качестве индекса ожирения. ИМТ считается удовлетворительной заменой окружности талии, поскольку эти два параметра тесно связаны (16). ИМТ использовался вместо окружности талии в модифицированных критериях определения МС в нескольких предыдущих исследованиях (17,18). Инсулинорезистентность рассчитывали по измерениям уровня глюкозы и инсулина натощак с использованием модели оценки гомеостаза инсулинорезистентности (HOMA-IR) (19).,20).
Поскольку окружность талии не была доступна для многих людей, ИМТ ≥30 кг/м 2 использовался в качестве индекса ожирения. ИМТ считается удовлетворительной заменой окружности талии, поскольку эти два параметра тесно связаны (16). ИМТ использовался вместо окружности талии в модифицированных критериях определения МС в нескольких предыдущих исследованиях (17,18). Инсулинорезистентность рассчитывали по измерениям уровня глюкозы и инсулина натощак с использованием модели оценки гомеостаза инсулинорезистентности (HOMA-IR) (19).,20).
Аналитические процедуры
Электролиты сыворотки, глюкоза, триглицериды, общий холестерин и холестерин ЛПВП, креатинин и концентрации мочевой кислоты измерялись с использованием автоматизированной системы (Beckman CX9ALX, Fullerton, CA). рН мочи измеряли рН-электродом. Креатинин мочи определяли методом пикриновой кислоты, клиренс эндогенного креатинина рассчитывали по значениям креатинина в сыворотке и моче. Сульфат мочи оценивали с помощью ионной хроматографии. Бикарбонат мочи (HCO 3 − ) рассчитывали по pH мочи и Pco 2 . Аммоний в моче (NH 4 + ) определяли методом глутаматдегидрогеназы, а титруемую кислотность мочи измеряли непосредственно с помощью автоматизированной системы титрования по конечной точке с бюреткой (Radiometer, Копенгаген, Дания). Цитрат мочи оценивали ферментативно с использованием реагентов Boehringer-Mannheim Biochemicals (Индианаполис, Индиана), а миллиэквиваленты цитрата рассчитывали по pH мочи и pKa цитрата 2- /цитрат 3- из 5.6. Чистая экскреция кислоты с мочой (NAE) рассчитывалась как моча (NH 4 + + титруемая кислотность) — (цитрат + HCO 3 — ), все в миллиэквивалентах. Доля чистой кислоты, экскретируемой в виде аммония, описывается отношением NH 4 + к NAE (NH 4 + /NAE). Инсулин в сыворотке оценивали с помощью ELISA (Mercodia, Metuchen, NJ).
Бикарбонат мочи (HCO 3 − ) рассчитывали по pH мочи и Pco 2 . Аммоний в моче (NH 4 + ) определяли методом глутаматдегидрогеназы, а титруемую кислотность мочи измеряли непосредственно с помощью автоматизированной системы титрования по конечной точке с бюреткой (Radiometer, Копенгаген, Дания). Цитрат мочи оценивали ферментативно с использованием реагентов Boehringer-Mannheim Biochemicals (Индианаполис, Индиана), а миллиэквиваленты цитрата рассчитывали по pH мочи и pKa цитрата 2- /цитрат 3- из 5.6. Чистая экскреция кислоты с мочой (NAE) рассчитывалась как моча (NH 4 + + титруемая кислотность) — (цитрат + HCO 3 — ), все в миллиэквивалентах. Доля чистой кислоты, экскретируемой в виде аммония, описывается отношением NH 4 + к NAE (NH 4 + /NAE). Инсулин в сыворотке оценивали с помощью ELISA (Mercodia, Metuchen, NJ).
Статистический анализ
Категориальные сравнения были выполнены с использованием χ 2 тест. Триглицериды сыворотки и HOMA-IR перед статистическим анализом подвергали логарифмическому преобразованию. Для нормально распределенных непрерывных переменных сравнения участников с МС и без него проводились с помощью двухвыборочного теста t . Для мочи NH 4 + /NAE использовали критерий суммы рангов Уилкоксона. Тесты линейного тренда проводились с помощью однофакторного дисперсионного анализа с полиномиальными контрастами. Тренд NH 4 + /NAE в моче анализировали с помощью теста Jonckheere-Terpstra. Анализ ковариационных моделей использовался для изучения взаимосвязи между рН мочи и количеством аномалий МС, а также для оценки каждого признака МС с поправкой на возможные смешанные эффекты ковариатов. ИМТ, возраст, пол, сульфат мочи и клиренс креатинина были включены как коварианты. Статистический анализ проводился с использованием SAS 9. .1.3 (Институт SAS, Кэри, Северная Каролина).
.1.3 (Институт SAS, Кэри, Северная Каролина).
Результаты
Демографические характеристики
Всего в исследовании приняли участие 148 человек. Демографические характеристики всей когорты показаны в таблице 1. Средний возраст (± SD) составлял 44 ± 14 лет, а средний ИМТ был 28,4 ± 6,7 кг/м 2 . Среднее количество признаков РС составило 1,76 ± 1,51, и 29,7% когорты соответствовали определению РС.
Таблица 1.
Характеристики участников исследования a
рН мочи и МС
Демографические и метаболические характеристики участников с (МС+) и без (МС-) МС показаны в таблице 2. Не было существенной разницы в расовом распределении между МС+ и РС − участники. Участники MS+ были значительно старше и имели значительно более высокие ИМТ, САД и диастолическое АД, а также уровень глюкозы и триглицеридов в сыворотке. У участников с МС был значительно более низкий 24-часовой рН мочи по сравнению с участниками без МС (5,71 ± 0,47 ± 9). 0003 против 6,11 ± 0,42; P < 0,001). Эта значительная разница в pH мочи между участниками MS + и MS- была отмечена у обоих полов. 24-часовой уровень калия в моче не отличался между двумя группами. У участников MS+ были значительно выше NH 4 + и NAE, хотя NH 4 + /NAE был значительно ниже, чем у участников MS-.
0003 против 6,11 ± 0,42; P < 0,001). Эта значительная разница в pH мочи между участниками MS + и MS- была отмечена у обоих полов. 24-часовой уровень калия в моче не отличался между двумя группами. У участников MS+ были значительно выше NH 4 + и NAE, хотя NH 4 + /NAE был значительно ниже, чем у участников MS-.
Таблица 2.
Биохимические особенности у участников с МС и без него a
рН мочи и особенности МС
Участники были дополнительно классифицированы в соответствии с количеством метаболических нарушений (таблица 3). Средние значения рН мочи по ряду признаков МС представлены в табл. 3. Средние значения рН мочи за 24 часа уменьшались с увеличением числа признаков МС (с 6,19, 6,14, 5,96, 5,83 до 5,60; P < 0,0001 для тенденция). Возраст, клиренс креатинина и 24-часовой уровень содержания сульфата мочи (заменитель пищевой кислоты) также значимо коррелировали с рН мочи в однофакторном анализе (9). 0003 P < 0,05). Эти переменные были включены в многофакторную модель для изучения взаимосвязи между рН мочи и МС. Средний 24-часовой рН мочи с поправкой на возраст, пол, клиренс креатинина и сульфат мочи снизился с 6,15, 6,10, 5,99, 5,85 до 5,69 с увеличением количества метаболических нарушений ( P < 0,005 для тренда; рисунок 1).
0003 P < 0,05). Эти переменные были включены в многофакторную модель для изучения взаимосвязи между рН мочи и МС. Средний 24-часовой рН мочи с поправкой на возраст, пол, клиренс креатинина и сульфат мочи снизился с 6,15, 6,10, 5,99, 5,85 до 5,69 с увеличением количества метаболических нарушений ( P < 0,005 для тренда; рисунок 1).
Рисунок 1.
Среднее значение рН мочи за 24 часа, скорректированное с учетом возраста, пола, клиренса креатинина и содержания сульфата мочи за 24 часа в зависимости от ряда признаков метаболического синдрома (МС). Столбцы обозначают среднее значение ± стандартная ошибка среднего. P < 0,005 для линейного тренда. Проверка линейной тенденции была проведена путем анализа ковариационной модели, сравнивающей рН мочи с количеством аномалий МС с поправкой на возраст, пол, клиренс креатинина и 24-часовой сульфат мочи.
Таблица 3.
Распределение биохимических признаков по количеству признаков МС
Суточный рН мочи достоверно коррелировал с холестерином ЛПВП в сыворотке крови и обратно пропорционально и значимо ассоциировался с ИМТ, САД, глюкозой сыворотки и триглицериды сыворотки (таблица 4).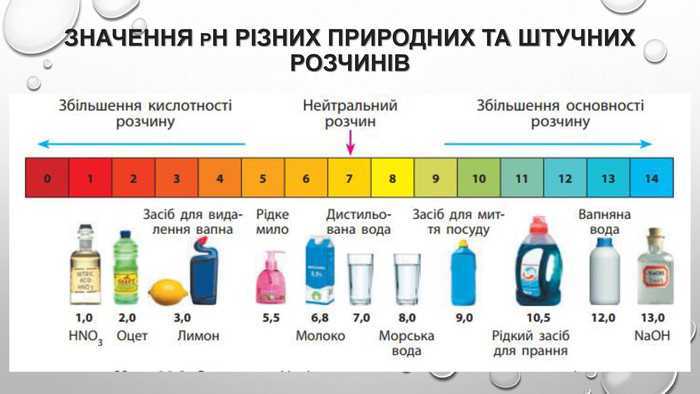 После поправки на возраст, пол, клиренс креатинина и сульфат мочи 24-часовой рН мочи по-прежнему был значительно связан с ИМТ, САД, уровнем глюкозы в сыворотке и холестерином ЛПВП в сыворотке, хотя величина связи уменьшилась (таблица 4).
После поправки на возраст, пол, клиренс креатинина и сульфат мочи 24-часовой рН мочи по-прежнему был значительно связан с ИМТ, САД, уровнем глюкозы в сыворотке и холестерином ЛПВП в сыворотке, хотя величина связи уменьшилась (таблица 4).
Таблица 4.
Взаимосвязь между pH мочи и индивидуальными характеристиками МС a
pH мочи и резистентность к инсулину HOMA-IR (
P <0,0001; таблица 4). После поправки на возраст, пол, ИМТ, клиренс креатинина и сульфат мочи обратная связь между 24-часовым рН мочи и HOMA-IR оставалась статистически значимой (таблица 4).Обсуждение
Рассеянный склероз связан с различными физиологическими и метаболическими изменениями. В этом перекрестном исследовании оценивалась взаимосвязь между МС и рН мочи. В разнообразной амбулаторной популяции у пациентов с РС была обнаружена более кислая моча, чем у лиц без РС. Кроме того, мы обнаружили сильную, достоверную обратную зависимость между рН мочи за 24 часа и количеством признаков МС. Эта корреляция не зависела от факторов, которые, как известно, влияют на рН мочи, включая возраст, пол, клиренс креатинина и сульфат мочи.
Эта корреляция не зависела от факторов, которые, как известно, влияют на рН мочи, включая возраст, пол, клиренс креатинина и сульфат мочи.
Наше исследование впервые продемонстрировало обратную зависимость между рН мочи за 24 часа и количеством признаков МС. В предыдущих отчетах была показана обратная корреляция между массой тела и pH мочи у людей с образованием камней в почках (21) и без образования камней (14). Аналогичным образом, в недавнем отчете была обнаружена обратная зависимость между ИМТ и рН мочи среди людей с камнями и без камней (22). Наше исследование подтверждает эти выводы, потому что более высокий ИМТ, суррогат абдоминального ожирения, был связан с более кислой мочой. Однако 24-часовой рН мочи также коррелировал с каждым из других компонентов МС после поправки на ИМТ, что позволяет предположить, что взаимосвязь определяется не только массой тела. Связь рН мочи с САД, уровнем глюкозы в сыворотке, триглицеридами и холестерином ЛПВП ранее не сообщалась.
Основным вредным последствием чрезмерно кислой мочи является образование камней в почках, содержащих мочевую кислоту.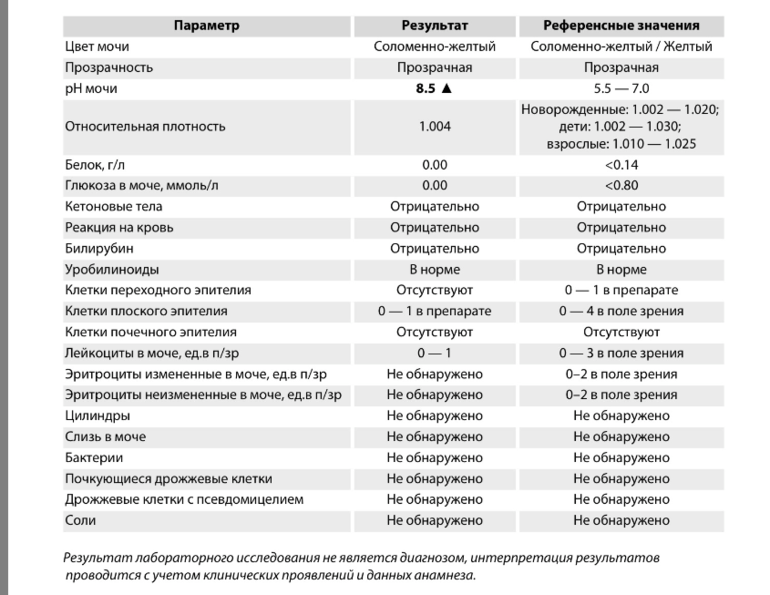 Мочевая кислота плохо растворима и имеет pKa 5,51 при 37°C (23). Когда рН мочи превышает это значение, увеличивается доля мочевой кислоты в форме ее основания, уратов, которые относительно растворимы. Таким образом, рН мочи является основной детерминантой осаждения мочевой кислоты, и, по сути, чрезмерно кислая моча является основным патогенным признаком уратокислых камней (24). Наши данные свидетельствуют о том, что наличие увеличивающегося числа признаков рассеянного склероза увеличивает склонность к образованию камней из мочевой кислоты. Это мнение подтверждается поперечными исследованиями, которые показывают значительно большую распространенность мочекислого нефролитиаза среди лиц с ожирением и камнеобразованием, а также у пациентов с нефролитиазом и диабетом 2 типа (25–28). Инсулинорезистентность является общим признаком ожирения (29), диабет 2 типа (30) и рассеянный склероз (2), и считается, что он вызывает чрезмерно кислую мочу у пациентов с этими состояниями (14,21). Эта концепция подтверждается нашим обнаружением значительной связи между 24-часовым pH мочи и HOMA-IR, мерой резистентности к инсулину.
Мочевая кислота плохо растворима и имеет pKa 5,51 при 37°C (23). Когда рН мочи превышает это значение, увеличивается доля мочевой кислоты в форме ее основания, уратов, которые относительно растворимы. Таким образом, рН мочи является основной детерминантой осаждения мочевой кислоты, и, по сути, чрезмерно кислая моча является основным патогенным признаком уратокислых камней (24). Наши данные свидетельствуют о том, что наличие увеличивающегося числа признаков рассеянного склероза увеличивает склонность к образованию камней из мочевой кислоты. Это мнение подтверждается поперечными исследованиями, которые показывают значительно большую распространенность мочекислого нефролитиаза среди лиц с ожирением и камнеобразованием, а также у пациентов с нефролитиазом и диабетом 2 типа (25–28). Инсулинорезистентность является общим признаком ожирения (29), диабет 2 типа (30) и рассеянный склероз (2), и считается, что он вызывает чрезмерно кислую мочу у пациентов с этими состояниями (14,21). Эта концепция подтверждается нашим обнаружением значительной связи между 24-часовым pH мочи и HOMA-IR, мерой резистентности к инсулину.
Точный патофизиологический механизм, лежащий в основе чрезмерной кислотности мочи при резистентности к инсулину, до конца не выяснен. Низкий рН мочи может быть результатом повышенной экскреции кислоты, нарушения буферной функции мочи или того и другого. Более высокий NAE может возникать из-за более низкого потребления пищевой щелочи, большего потребления пищевой кислоты или более высокого производства эндогенной кислоты. В нашем исследовании уровень калия в моче, косвенный показатель потребления щелочи с пищей, не различался у участников с РС и без него, что позволяет предположить, что различия в потреблении щелочи вряд ли объясняют различия в рН мочи. Кроме того, более низкий рН мочи при МС сохранялся после поправки на сульфат мочи, что свидетельствует о том, что только диетические факторы не могут объяснить более кислую мочу. С другой стороны, у этих пациентов может быть повышенная эндогенная продукция кислоты, хотя мы специально не исследовали эту возможность. Низкий рН мочи также может быть результатом нарушения буферизации мочи.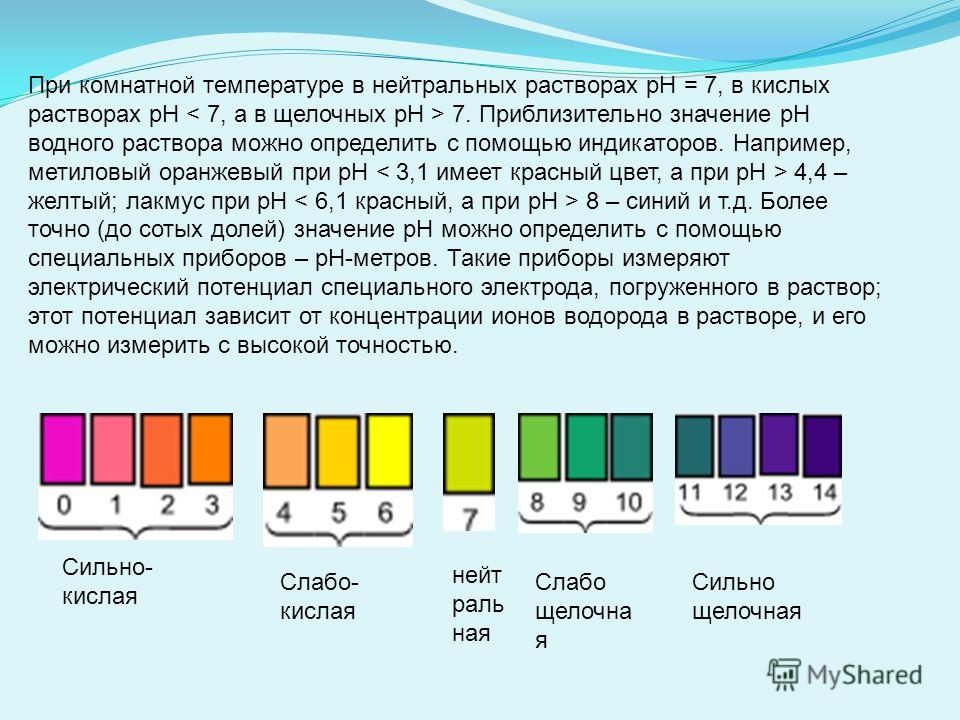 Аммоний является важным мочевым буфером (31). Производство и экскреция аммония почками регулируются кислотно-щелочной средой окружающей среды. Инсулин влияет на эти два процесса (32,33), и механизмы кислотно-щелочного гомеостаза могут быть изменены в состоянии резистентности к инсулину (13). В соответствии с этой возможностью, участники с рассеянным склерозом в нашей когорте демонстрировали более низкую экскрецию аммония на NAE (NH 4 + /NAE).
Аммоний является важным мочевым буфером (31). Производство и экскреция аммония почками регулируются кислотно-щелочной средой окружающей среды. Инсулин влияет на эти два процесса (32,33), и механизмы кислотно-щелочного гомеостаза могут быть изменены в состоянии резистентности к инсулину (13). В соответствии с этой возможностью, участники с рассеянным склерозом в нашей когорте демонстрировали более низкую экскрецию аммония на NAE (NH 4 + /NAE).
Одним из ограничений этого исследования является оценка лиц, находящихся на выборочной амбулаторной диете, поскольку диетические факторы могут влиять на рН мочи. Хотя наблюдалась тенденция к увеличению сульфата мочи с увеличением количества компонентов МС, связь между рН мочи и характеристиками МС сохранялась после учета содержания сульфата в моче.
Выводы
Это исследование является первым, демонстрирующим взаимосвязь между МС и низким рН мочи, которая не зависит от возраста и функции почек. Кроме того, было отмечено прогрессивное снижение рН мочи с увеличением числа признаков МС. Более кислая моча делает пациентов с рассеянным склерозом более предрасположенными к мочекислому нефролитиазу. Необходимы дальнейшие исследования для выяснения механизма (механизмов), ответственного за более низкий рН мочи у людей с рассеянным склерозом.
Более кислая моча делает пациентов с рассеянным склерозом более предрасположенными к мочекислому нефролитиазу. Необходимы дальнейшие исследования для выяснения механизма (механизмов), ответственного за более низкий рН мочи у людей с рассеянным склерозом.
Раскрытие информации
Нет.
Благодарности
Авторы получили поддержку Национального института здоровья (R01-48482, P01-DK20543, M01-RR00633 и K23-RR21710) и Национального почечного фонда.
Сноски
Опубликовано в Интернете до печати. Дата публикации доступна на сайте www.cjasn.org.
См. соответствующую редакционную статью «Метаболический синдром: возникающая угроза функции почек» на страницах 869–871.
- Принята 6 февраля 2007 г.
- Принята 29 мая 2007 г. Ланцет365 :1415– 1428,2005
- ↵
Группа экспертов по выявлению, оценке и лечению высокого уровня холестерина в крови у взрослых: Резюме третьего отчета Национальной образовательной программы по холестерину (NCEP) Группа экспертов по выявлению, оценке и лечению высокого уровня холестерина в крови у взрослых (панель лечения взрослых III).
 ДЖАМА285
:2486–
2497,2001
ДЖАМА285
:2486–
2497,2001 - ↵
Hu G, Qiao Q, Tuomilehto J, Balkau B, Borch-Johnsen K, Pyorala K: Распространенность метаболического синдрома и его связь со смертностью от всех причин и сердечно-сосудистой смертностью у недиабетических европейских мужчин и женщины. Арх стажер Med164 :1066– 1076,2004
- ↵
Лоренцо С., Околоисе М., Уильямс К., Стерн М.П., Хаффнер С.М.: Метаболический синдром как предиктор диабета 2 типа: исследование сердца в Сан-Антонио. Лечение диабета26 :3153– 3159,2003
- ↵
Locatelli F, Pozzoni P, Del Vecchio L: Почечные проявления при метаболическом синдроме. J Am Soc Nephrol17 [Приложение] :S81– S85,2006
Чжан Р., Ляо Дж., Морс С., Донелон С., Рейсин Э. Заболевание почек и метаболический синдром. Am J Med Sci330 :319– 325,2005
- ↵
Reaven GM: Почка: невольный сообщник синдрома X. Am J почек Dis30 :928– 931,1997
Facchini FS, DoNascimento C, Reaven GM, Yip JW, Ni XP, Humphreys MH: Артериальное давление, потребление натрия, резистентность к инсулину и экскреция нитратов с мочой.
 Гипертония33
:1008–
1012,1999
Гипертония33
:1008–
1012,1999 - ↵
Facchini F, Chen YD, Hollenbeck CB, Reaven GM: Связь между резистентностью к инсулин-опосредованному поглощению глюкозы, клиренсом мочевой кислоты с мочой и концентрацией мочевой кислоты в плазме. ДЖАМА266 :3008– 3011,1991
- ↵
Chagnac A, Weinstein T, Korzets A, Ramadan E, Hirsch J, Gafter U: Гломерулярная гемодинамика при тяжелом ожирении. Am J Physiol Renal Physiol278 :F817– F822,2000
- ↵
Chen J, Muntner P, Hamm LL, Jones DW, Batuman V, Fonseca V, Whelton PK, He J: Метаболический синдром и хроническая болезнь почек у взрослых в США. Энн Интерн Мед140 : 167– 174,2004
- ↵
Kurella M, Lo JC, Chertow GM: Метаболический синдром и риск хронического заболевания почек у взрослых без диабета. Дж Ам Сок Нефрол16 :2134– 2140,2005
- ↵
Abate N, Chandalia M, Cabo-Chan AV, Moe OW, Sakhaee K: Метаболический синдром и мочекислый нефролитиаз: новые особенности почечного проявления резистентности к инсулину.
 Почки Int65
:386–
392,2004
Почки Int65
:386–
392,2004 - ↵
Cameron MA, Maalouf NM, Adams-Huet B, Moe OW, Sakhaee K: Состав мочи при диабете 2 типа: предрасположенность к мочекислому нефролитиазу. Дж Ам Сок Нефрол17 :1422– 1428,2006
- ↵
Гранди С.М., Климан Д.И., Дэниелс С.Р., Донато К.А., Эккель Р.Х., Франклин Б.А., Гордон Д.Дж., Краусс Р.М., Сэвидж П.Дж., Смит С.К., Спертус Д.А., Коста Ф.; Американская кардиологическая ассоциация, Национальный институт сердца, легких и крови: Диагностика и лечение метаболического синдрома: Научное заявление Американской кардиологической ассоциации/Национального института сердца, легких и крови. Тираж112 :2735– 2752,2005 [опубликованная опечатка появляется в Тираж 112: e297, e298, 2005]
- ↵
Ford ES, Mokdad AH, Giles WH: Тенденции изменения окружности талии среди взрослого населения США. Обес Res11 :1223– 1231,2003
- ↵
Sundstrom J, Riserus U, Byberg L, Zethelius B, Lithell H, Lind L: Клиническое значение метаболического синдрома для долгосрочного прогнозирования общей и сердечно-сосудистой смертности: проспективное популяционное когортное исследование .
 БМЖ332
:878–
882,2006
БМЖ332
:878–
882,2006 - ↵
Малик С., Вонг Н.Д., Франклин С.С., Камат Т.В., L’Italien GJ, Pio JR, Williams GR: Влияние метаболического синдрома на смертность от ишемической болезни сердца, сердечно-сосудистых заболеваний и всех причин у взрослых в США. Тираж110 :1245– 1250,2004
- ↵
Леви Дж. К., Мэтьюз Д. Р., Херманс М. П.: Для оценки правильной модели гомеостаза (HOMA) используется компьютерная программа. Лечение диабета21 :2191– 2192,1998
- ↵
Wallace TM, Levy JC, Matthews DR: Использование и злоупотребление моделированием HOMA. Лечение диабета27 :1487– 1495,2004
- ↵
Maalouf NM, Sakhaee K, Parks JH, Coe FL, Adams-Huet B, Pak CY: Ассоциация pH мочи с массой тела при нефролитиазе. Почки Int65 :1422– 1425,2004
- ↵
Taylor EN, Curhan GC: Размер тела и состав мочи за 24 часа. Am J почек Dis48 :905– 915,2006
- ↵
Финлейсон Б.
 , Смит Л.Х.: Стабильность первого диссоциирующего протона мочевой кислоты.
J Chem Engl Data19
:94–
97,1974
, Смит Л.Х.: Стабильность первого диссоциирующего протона мочевой кислоты.
J Chem Engl Data19
:94–
97,1974 - ↵
Pak CY, Sakhaee K, Peterson RD, Poindexter JR, Frawley WH: Биохимический профиль идиопатического мочекислого нефролитиаза. Почки Int60 :757– 761,2001
- ↵
Ekeruo WO, Tan YH, Young MD, Dahm P, Maloney ME, Mathias BJ, Albala DM, Preminger GM: Метаболические факторы риска и влияние медикаментозной терапии на лечение нефролитиаза у пациентов с ожирением пациенты. Дж Урол172 :159– 163,2004
Daudon M, Lacour B, Jungers P: Влияние размера тела на состав мочевых камней у мужчин и женщин. Урол Рес34 :193– 199,2006
Pak CY, Sakhaee K, Moe O, Preminger GM, Poindexter JR, Peterson RD, Pietrow P, Ekeruo W: Биохимический профиль камнеобразующих пациентов с сахарным диабетом. Урология61 :523– 527,2003
- ↵
Daudon M, Traxer O, Conort P, Lacour B, Jungers P: Диабет 2 типа повышает риск образования камней из мочевой кислоты.





 ДЖАМА285
:2486–
2497,2001
ДЖАМА285
:2486–
2497,2001  Гипертония33
:1008–
1012,1999
Гипертония33
:1008–
1012,1999 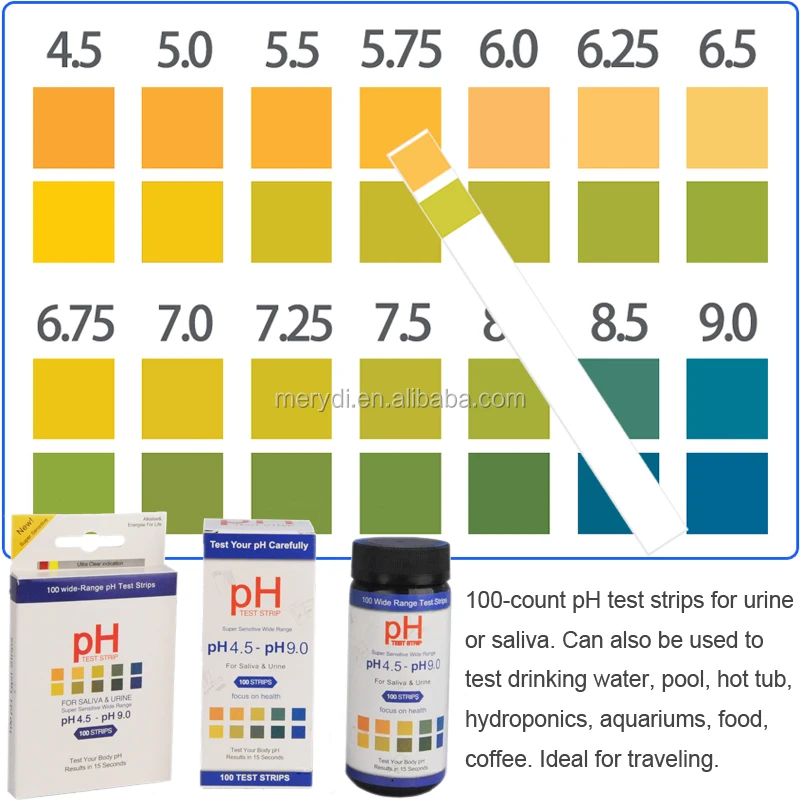 Почки Int65
:386–
392,2004
Почки Int65
:386–
392,2004  БМЖ332
:878–
882,2006
БМЖ332
:878–
882,2006  , Смит Л.Х.: Стабильность первого диссоциирующего протона мочевой кислоты.
J Chem Engl Data19
:94–
97,1974
, Смит Л.Х.: Стабильность первого диссоциирующего протона мочевой кислоты.
J Chem Engl Data19
:94–
97,1974