Из истории создания бцж.
БЦЖ (BCG — Bacillus Calmette-Guérin) – вакцина из живых ослабленных туберкулезных микобактерий бычьего типа, используемая в качестве метода специфической профилактики туберкулеза. Вакцинный штамм БЦЖ был получен в 1919 г. французскими учеными А. Кальметтом и К.Гереном. В 1921 г. они впервые дали вакцину БЦЖ новорожденному ребенку. В 1923 г. Гигиенический комитет Лиги Наций принял решение о ее широком применении во всех странах мира.
Леон Шарль Альбер Кальметт родился в 1863 г. в семье юриста. В 1883 г. окончил Медицинскую морскую школу, получил звание помощника судового врача. Он объездил Индокитай, побывал в Китае, участвовал как военный врач в сражениях. Работая в Индокитае, Кальметт был поражен множеством заразных болезней, против которых его врачебные знания были недостаточны.
В 1890 г. он приехал в Париж для прохождения курса микробиологии, который вели Э. Ру и И.И. Мечников. В 1891 г. Луи Пастер, опираясь на опыт Кальметта в колониях, предложил ему организовать лабораторию для производства антирабической и оспенной вакцин в Индокитае. В Сайгоне Кальметт организовал филиал Пастеровского института. Здесь он наладил производство оспенной вакцины из материала, полученного от местных животных. Применение Кальметтом глицерина для консервирования зараженного вирусом бешенства кроличьего мозга сделало возможным регулярную присылку препаратов из Франции в Сайгон, что обеспечивало производство вакцины против бешенства. Здесь он развернул исследования по изучению холеры, дизентерии; впервые применил противочумную серотерапию. Решив испытать возможность серотерапии при укусах змей, он добыл яд, ослабил его нагреванием и стал иммунизировать животных. Из этих опытов выросла разработанная Кальметтом уже во Франции серотерапия отравления змеиным ядом. При участии Кальметта были организованы филиалы Института Пастера в Северной (Тунис, Алжир, Марокко), Западной (Сенегал, Конго) и Экваториальной Африке, на Мадагаскаре.
В 1895 г. Кальметт возглавил Пастеровский институт в Лилле, а также кафедру бактериологии на медицинском факультете. Для нужд населения были открыты диагностические и бактериологические лаборатории; стали производиться сыворотки – противостолбнячная и против змеиного яда. Здесь, в Лилле, Кальметт вплотную столкнулся с распространенной в индустриальных регионах Франции чахоткой, и эта проблема заняла главное место среди его научных интересов.
Жан-Мари Камилл Герен (1872-1961) родился в Пуатье в бедной семье. Его отец умер в 1882 г. от туберкулеза, и мать вторично вышла замуж – за ветеринара. Возможно, поэтому в 1891 г. Герен поступил в Ecole Vеtеrinaire de Maisons-Alfort (Альфорский ветеринарный институт). Его учителем был Эдмон Нокар – французский эпизоотолог и директор института, разработавший метод выращивания бактерий туберкулеза на глицериновых средах. Когда А. Кальметту потребовался ветеринар для сотрудничества в изучении инфекционных болезней животных, он пригласил Герена. Приехав в Лилль в 1897 г., Герен стал заведовать лабораторией вакцин; их совместная с Кальметтом работа продолжалась 36 лет. В 1928 г. Герен был награжден орденом Почетного легиона и приглашен руководить лабораторией БЦЖ в Парижском Пастеровском институте, который бесплатно распространял вакцину, активно знакомил с методами ее производства и контроля национальные лаборатории других стран.
С 1900 г. и до конца жизни основное внимание Кальметта было сосредоточено на борьбе с туберкулезом. «За время моего пребывания в Лилле проблема научной и социальной борьбы против туберкулеза стала для меня поистине навязчивой идеей. Я лучше, чем кто-либо другой, мог измерить всю глубину бедности рабочих, всю разрушительную силу туберкулеза, свирепствовавшего в их среде» – писал он. Сочетая научные исследования с общественной и социально-гигиенической работой, Кальметт в 1901 г. основал в г.Лилле первый противотуберкулезный диспансер, пропагандировал идею борьбы с туберкулезом путем создания сети специализированных диспансеров. Он организовал «Северную лигу против с туберкулезом», располагавшую средствами, на которые были организованы диспансеры в городах Франции; был избран вице-президентом Французского национального комитета борьбы с туберкулезом и т.д.
С 1900 г. Кальметт задумывается над значением естественного и приобретенного иммунитета к туберкулезу. Специфическую резистентность можно создать иммунизацией. Опыты показали непригодность для этой цели убитых бактерий, их экстрактов, туберкулина. Нужна была вакцина из живых, но аттенуированных (т.е. ослабленных) бактерий. Надо было создать такой штамм, который, во-первых, будет устойчив во внешней среде (иначе вакцину невозможно хранить), а во-вторых, способен вызывать заболевание ровно в той степени, которая позволит организму выработать иммунитет, но не нанесет ему при этом существенного вреда. Такой штамм и был создан Кальметтом и Гереном в результате упорной систематической работы – 230 непрерывных пассажей туберкулезного штамма на картофеле с желчью.
В 1908 г. Кальметт и Герен засеяли на картофельно-глицериновую среду с желчью (использовалось открытое Кальметтом свойство бычьей желчи снижать вирулентность) очень вирулентную культуру микобактерий бычьего типа и через каждые 2 недели пересевали ее. Направленно изменяя условия среды, они добились изменения свойств микобактерий и наследуемого закрепления их новых свойств. Более чем через 13 лет они получили живую культуру, безвредную для рогатого скота, морских свинок, кроликов и обезьян, но обладающую хорошими иммунизирующими свойствами.
В 1921 г. Кальметт и Герен совместно с педиатром Вайль-Алле впервые сделали прививку новорожденному ребенку живой вакциной из штамма БЦЖ. Бенжамен Вайль-Алле был первым, кто рискнул использовать живую вакцину БЦЖ, и сделал прививку новорожденной девочке, туберкулезная мать которой умерла при родах, оставив на руки туберкулезной же бабушке. Общая доза введенной перорально на 3, 5 и 7-й день жизни вакцины составила 240 млн. бактерий. Поскольку в течение 6 месяцев девочка чувствовала себя хорошо, метод пероральной вакцинации БЦЖ стал применяться для всех новорожденных в парижской больнице. К 1924 г. во Франции были вакцинированы более 300 новорожденных, матери которых болели туберкулезом.
Метод вакцинации БЦЖ был по-разному принят учеными, практиками и населением. Энтузиазм соотечественников по поводу открытия Кальметта выражался в том, что его называли «спасителем младенцев посредством БЦЖ». Эксперименты в Институте Пастера и в зарубежных странах, а также наблюдения в практике свидетельствовали о практической безвредности вакцинации БЦЖ. Имелись, однако, и противники идей Кальметта, которые допускали, но не могли доказать возможность реверсии – возврата вирулентности штамма БЦЖ. Кальметт прислушивался к каждому возражению, лично отвечал на него, следил за состоянием каждого вакцинированного ребенка. С 1928 г. безвредность и эффективность вакцинации БЦЖ были подтверждены рядом международных комиссий.
К 1934 г. во Франции было более 800 тыс. вакцинированных БЦЖ детей (еще 450 тыс. — в 46 других странах), и смертность от туберкулеза в этих контингентах была значительно ниже, чем у невакцинированных детей.
Печатается по: Тогунова А.И. Жизнь и деятельность Альбера Кальметта // Вестник АМН СССР. – 1964. – №8. – С.69-74.
Я укола не боюсь. История прививки БЦЖ
КРАТКАЯ ИСТОРИЯ БЦЖ
Первые мысли о возможности создания противотуберкулёзной вакцины появились у французского микробиолога Альбера Кальметта и ветеринара Камиля Герена, когда в 1908 году они работали в Институте Пастера в Лилле. Учёные заметили, что на питательной среде на основе глицерина, желчи и картофеля вырастают туберкулёзные палочки наименьшей вирулентности, и, следовательно, можно попробовать вырастить культуру ослабленных туберкулёзных микробов.
К 1919 году учёные создали штамм, не вызывавший туберкулёз у подопытных животных и задумались о его испытании на людях. Но лишь 18 июля 1921 года были сделаны первые прививки БЦЖ. Вначале часто бывало, что «что-то пошло не так»: к примеру, в германском Любеке все из 240 привитых новорождённых заболели туберкулёзом, а 77 из них умерли. Но расследование показало, что виновата не вакцина БЦЖ, а халатность врача, хранившего её в одном контейнере с культурой классических туберкулёзных микробов.
 Albert Calmette, 1930 год
Albert Calmette, 1930 годВ 1925 году Кальметт передал свою вакцину советским коллегам и прививка БЦЖ начала активно применяться в СССР. Всего через 3 года выяснилось, что смертность от туберкулёза в группах привитых детей действительно сократилась. В 1928 году было рекомендовано вакцинировать БЦЖ новорождённых из «групп риска». С середины 1950-х годов вакцинация новорождённых стала обязательной в большинстве стран Европы (кроме разве что Нидерландов). Также в 1948 году первой из неевропейских стран обязательную вакцинацию ввела Индия, в 1967-1968 годах Бразилия, прививка обязательна в Сингапуре, Малайзии и многих других странах. Но с конца 1990-х годов несколько европейских государств прекратили использование БЦЖ для массовой вакцинации, сославшись на незначительную заболеваемость туберкулёзом среди своих граждан.
Постараюсь просто и коротко рассказать об основных прививках, которые надо сделать в первые годы жизни ребенку согласно Российским стандартам. Все очень просто.
Итак, первое. БЦЖ.
1. В каждом Российском роддоме предлагают сделать две прививки: БЦЖ и первую из трех прививку от гепатита Б.
2. Потом на первом году, согласно национальному календарю, малышу предстоит сделать еще только 1 прививку — коклюш+дифтерия+стобляк+полиомиелит (она делается троекратно через 1,5-2 месяца). Ну, и повторить прививку от гепатита Б, если она была сделана в роддоме (она также делается троекратно).
3. После года делается прививка от кори+краснухи+паротита, и дальше только ревакцинации!
БЦЖ делают в первые 3-7 дней при отсутствии противопоказаний, в плечо, а при отрицательной пробе Манту — повторно в 7 и 14 лет проводят ревакцинацию.
 Роберт Кох
Роберт Кох1. Почему начинают с нее и как им заразиться?
Начинают с БЦЖ потому, что считается, что в нашей стране сейчас эпидемия туберкулеза и очень высокий риск заразиться туберкулезом новорожденному ребенку. Он вызывается микобактерией и передается через воздух, при чихании, разговоре, кашле. Микобактерии могут летать в лифте, ресторане, аэропорту или в метро. В общем, риск его встретить высок.
Поэтому БЦЖ традиционно делали в роддоме. Кроме того, считается, что дети чаще заболевают туберкулезом при первичной «встрече» с микобактериями и болеют тяжелее. В ряде европейских стран эту прививку не проводят так как считается, что там благоприятная эпидемическая обстановка (в России сейчас продолжается эпидемия туберкулеза).
2. Что делать, если в роддоме БЦЖ не сделали?
Иногда по каким-то причинам в первые дни эту прививку ребенку не делают. Тогда ее можно сделать ребенку по месту жительства в любое удобное для Вас время (когда созреете, если боитесь, или когда начнете «выходить в свет» с ребенком). Но если Вы ее будете делать после 2 месяцев, то придется предварительно сделать пробу Манту. Это не прививка, это всего лишь тест чтобы определить — не заразился ли ребенок уже туберкулезом (в таком случае прививка не нужна, отправят сразу к фтизиатру). Иногда реакция Манту бывает ложно-положительной, часто отмечаются аллергические реакции на компоненты Манту (на туберкулин) — тогда можно сделать контрольно так называемый Диаскин-тест, он более чувствительный, и уже после его результата принимать решение о том, нужно ли Вам обращаться к фтизиатру.
3. Осложнения от вакцинации.
БЦЖ — это почти живая вакцина, однако, частота осложнений невысокая даже у иммунодефицитных лиц. Вот, что пишет по этому поводу Всемирная Организация Здравоохранения : «Осложнения после вакцинации БЦЖ наблюдаются редко: частота летальной диссеминации БЦЖ оценивается в 0,19-1,56 на миллион вакцинированных лиц, и ее жертвами почти исключительно становятся непреднамеренно иммунизированные лица с тяжелыми нарушениями клеточного иммунитета. Значительные местные реакции, например, обширное местное изъязвление и регионарный лимфаденит наблюдаются у <1:1000 и в большинстве случаев (>90%) среди лиц с иммунодефицитом. Сообщения об остите были связаны с использованием определенных партий вакцины, однако в настоящее время он встречается чрезвычайно редко. Поскольку острые побочные проявления при вакцинации БЦЖ встречаются крайне редко даже среди ВИЧ-позитивных младенцев без клинических признаков, все здоровые новорожденные должны быть вакцинированы БЦЖ даже в ВИЧ-эндемичных районах».
4. Как она сочетается с другими прививками?
БЦЖ — единственная вакцина, которую не рекомендуют вводить вместе в другими вакцинами. Следует выдержать интервал примерно в 1-1,5 месяца.
Таким образом, если прививка была сделана здоровому ребенку с соблюдением всех правил введения вакцины — она практически безопасна, однако сильно снижает риск тяжелых форм развития туберкулеза в нашей стране, где в настоящее время эпидемия. Если Вы не сделали ее в роддоме, ее можно сделать и позже, но только после реакции Манту (или Диаскин-теста) и не ранее чем через 1 месяц после\до других прививок. Проба Манту не является прививкой и проводится после первого года жизни каждый год до совершеннолетия.
 Дети с коинфекцией туберкулеза и ВИЧ в Мьянме. © 2012 Matthieu Zellweger (with AIDSpartners.org)
Дети с коинфекцией туберкулеза и ВИЧ в Мьянме. © 2012 Matthieu Zellweger (with AIDSpartners.org)«ТОЛЬКО ДЛЯ БЕЛЫХ?»
При исследованиях эффективности прививки БЦЖ обнаружилась странная особенность: она эффективно «работает» лишь в странах с умеренным климатом. Так, клинические исследования, проведённые в Великобритании, доказали защитный эффект от 60 % до 80 %. Но чем южнее — тем хуже, и в странах с экваториальным климатом эффективность БЦЖ оказалась совсем незначительной.
В мировой статистике инфекционные заболевания до сих пор остаются главной причиной смерти. Но в странах с развитым здравоохранением обыватель уже позабыл о разрушительных эпидемиях прошлого, а об ужасах натуральной оспы, холеры или столбняка осведомлены разве что специалисты да любители классики.
Ещё каких-то сто лет назад большая часть детей не доживала до взрослого возраста, погибая от инфекционных болезней, и от вымирания человечество спасала только экстенсивная репродукция. Сегодня в российской структуре смертности от инфекций умирает 1,6% людей.
Тогда как заболевания сердечно-сосудистой системы уносят жизни 57% россиян (по данным Росстата за 2010 год). Общая продолжительность жизни за последние сто лет значительно выросла, так что в развитых странах большинство людей умирают от «старости» (т.е. рака, инфарктов и инсультов). Чему же мы обязаны такому счастью? Куда девались былые эпидемии?
 Две женщины говорят через маски от гриппа во время эпидемии, 1918 год
Две женщины говорят через маски от гриппа во время эпидемии, 1918 год© Keystone/Getty Images
Немалую роль сыграли санитарно-гигиенические меры. Заболеваемость многими фекально-оральными инфекциями (холера, брюшной тиф и др.) удалось свести к минимуму, когда население стало снабжаться хлорированной водой. Вспышки той же холеры время от времени происходят и в наши дни, поражая до 5 млн. человек и убивая до 100 тысяч ежегодно, но сегодня эта проблема касается почти исключительно стран 3-его мира (в 2010 крупные вспышки отмечались в Нигерии, Чаде, Камеруне и на Гаити). О былых эпидемиях холеры в Европе нам напоминает разве что художественная литература, да киноклассика (например, «Смерть в Венеции» Лукино Висконти).
Огромную роль в борьбе с бактериальными инфекциями сыграли и антибиотики, которые стали массово применяться с 40-х годов прошлого века. На фармацевтическом рынке появились замечательные препараты, способные излечивать не только бактериальные, но и некоторые вирусные инфекции, такие как вирусные гепатиты. Не станем умалять и значимость презервативов в контроле за распространением заболеваний, передающимися половым путем.
Однако, оценивая эпидемиологическую ретроспективу, мы приходим к выводу, что наибольшую роль в борьбе с опасными инфекциями сыграли вакцины. Конечно, и в наши дни можно встретить американца с парализованными из-за полиомиелита ногами, но с середины 1990-х это заболевание в Западном полушарии больше не регистрируется. Нет больше в мире и натуральной оспы (последний случай зарегистрирован в Сомали в 1977 году), а ведь еще недавно эта инфекция была планетарным бедствием.
В XVIII веке в России каждый 7-ой ребенок умирал от натуральной оспы, а в XX веке вирус унес жизни почти полумиллиарда человек! Именно натуральная оспа, а также другие инфекции, завезенные в Южную и Центральную Америки, погубили аборигенные цивилизации.
 Профилактическая прививка против холеры в 1966 год.
Профилактическая прививка против холеры в 1966 год.Само слово «вакцина» происходит от латинского названия коровы (vacca). В 1796 году Эдвард Дженнер впервые применяет эффективный способ профилактики натуральной оспы — прививает несмертельную для человека коровью оспу собственному сыну. Еще за много лет до того на Востоке стали применять втирание оспенного струпа от людей, перенесших натуральную оспу в легкой форме, затем практика таких прививок распространилась и в Европу. Так был привит в детстве и сам Дженнер. К сожалению прививки человеческой оспы были очень опасны и около 2% детей их не переживали. Однако эпидемии оспы в то время были столь разрушительными, что люди предпочитали такие прививки, как меньший риск. Гениальное открытие Дженнера заключалось в успешной попытке привить не человеческую, а близкородственную ей оспу коров. Открытие далеко не сразу снискало славу. Дженнера высмеяли в Королевском обществе Лондона, куда он направил на оценку свой труд, враждебно отнеслось к идее прививать людям коровью хворь и духовенство. И все же, пройдя тернистый путь, вакцинация охватила всю Европу уже при жизни Дженнера, и умер ученый в 1823 году в зените славы.
Еще при жизни Дженнера вакцинация стала обрастать самыми причудливыми мифами. Со временем мифы видоизменялись, на смену устаревшим приходили новые. Однако, несмотря на все сопротивление вакцинам, натуральную оспу удалось ликвидировать, привив практически все население планеты, от цивилизованных стран Запада до негр
spid.center
День в истории: буква «Ж» в вакцине БЦЖ: med_history — LiveJournal
Для авторов блога буквосочетание «БЦЖ» знакомо с детства – еще бы, нам всем делали прививки в младенчестве, и когда при нас маму спрашивали в садике или в школе, какие прививки нам делали, мы слышали это магическое «БЦЖ» — и знать не знали, что это такое. Впрочем, мамы (по крайней мере, мама автора этого текста) тоже не знали, что означают эти буквы. Нам всем тогда и в голову не могло придти, что и «Ц» в этой аббревиатуре означает не «Ц», и «Ж» означает совсем не «Ж». Но – обо всем по порядку.
Камиль Герен на фоне портрета Альбера Кальметта
Вчера мир медицины (и ветеринарии заодно) отмечал грустную дату: 57 лет, как покинул этот мир выдающийся французский ветеринар, бактериолог и иммунолог, Жан-Мари Камиль Герен. Впрочем, он прожил долгую жизнь и успел в ней очень много.
Герен родился 22 декабря 1872 года во французском Пуатье в семье с весьма скромным достатком. Когда мальчику было четыре года, его отец умер от туберкулёза (позже, в 1918 году от этой «красивой» болезни скончается и жена Герена).
Наш герой учился не медицине, а ветеринарии – в высшем учебном заведении, Национальной ветеринарной школе в Мезон-Альфоре, и еще студентом начал работать помощником и учеником патолога, замечательного Эдмона Нокара, автора книги La Tuberculose Bovine : ses Dangers, ses Rapports avec la Tuberculose Humaine («Бычий туберкулез: опасность и взаимоотношение с туберкулезом человека»). Кстати, Нокар тоже занимался прививками от туберкулеза – он использовал туберкулин Роберта Коха для защиты крупного рогатого скота от этого заболевания (ветеринар все-таки).
Эдмон Нокар
Однако путь Герена лежал в области лечения людей. Он пришел работать в филиал Пастеровского института в Лилле, В 25 лет он поступил на должность ассистента (техника) директора института Альбера Кальметта и сразу же ему получили две ответственные работы: производство сыворотки Кальметта (антидот против змеиных укусов) и вакцины против оспы.
В 1900 году Герен стал руководителем собственной лаборатории в Институте и начал вместе с боссом искать пути создания вакцины против туберкулеза.

Альбер Кальметт
Прорыв состоялся в 1906 году. Тогда Кальметт и Герен показали, что ослабленную бактерию бычьего туберкулёза, Mycobacterium bovis, можно использовать в качестве вакцины. Способ аттенуации (ослабления) бациллы при помощи придумал норвежский исследователь, Кристиан Фейер Андворд. Он показал, что, если выращивать культуру на питательной среде из желчи, картофеля и глицерина, вирулентность бациллы снижается до минимума. Препарат назвали «бацилла Кальметта-Герена», или BCG. По-русски – «БЦЖ». Прививки БЦЖ до сих пор входят в обязательную программу вакцинации ребенка на 3-5 день жизни. Как показывает огромная статистика, вакцина не гарантирует стопроцентной защиты от туберкулеза, однако заболеваемость вакцинированных детей в шесть раз ниже. Кроме этого, она защищает детей от особо опасных форм болезни – особенно, туберкулезного менингита.
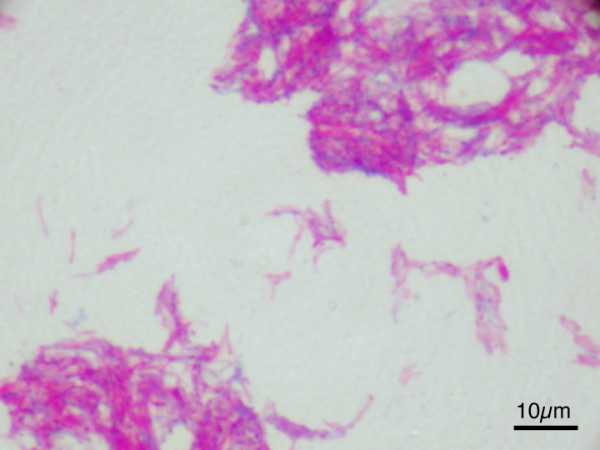
Бацилла Кальметта-Герена под микроскопом
Первое медицинское применение вакцины состоялось в 1921 году после испытаний 230 вариантов культуры (увы, увы, увы – жену Герена было не вернуть), а уже через четыре года Альбер Кальметт лично передал советскому иммунологу Льву Тарасевичу штамм бациллы, которая была зарегистрирована в СССР как БЦЖ-1. Первые массовые иммунизации в нашей стране прошли в 1928 году в очагах туберкулёза.
Кстати, туберкулезом польза вакцины БЦЖ не исчерпывается. Она, как ни странно, помогает при некоторых видах рака мочевого пузыря.
Сам же Герен после триумфа прожил очень долгую жизнь. Его шесть раз (1928-1950) номинировали на Нобелевскую премию по медицине, сам он дважды – в 1923 и 1933 году номинировал своего босса на ту же премию. Безуспешно.
В 1928 году он стал директором Службы Туберкулеза в Институте Пастера, в 1939 – вице-президентом Национального комитета по защите от туберкулеза. В 1948 году состоялся первый Международный конгресс по БЦЖ. Угадайте, кто был его председателем?
Вот такая вот неординарная история прячется за одной буквой в аббревиатуре, известной нам с детства.
med-history.livejournal.com
Я укола не боюсь. История прививки БЦЖ — ЖЖ
? LiveJournal- Find more
- Communities
- RSS Reader
- Shop
- Help
- Login
- CREATE BLOG Join
- English
(en)
- English (en)
- Русский (ru)
- Українська (uk)
- Français (fr)
- Português (pt)
- español (es)
- Deutsch (de)
- Italiano (it)
- Беларуская (be)
www.livejournal.com
Развитие вакцинопрофилактики. История вакцинации.
24 марта 1882 года, когда Роберт Кох объявил о том, что сумел выделить бактерию, вызывающую туберкулёз, ученый достиг величайшего за всю свою жизнь триумфа.
Почему все же именно открытие возбудителя туберкулеза называют научным подвигом?
Дело в том, что возбудители болезни туберкулеза – чрезвычайно трудный объект для исследования. В первых препаратах для микроскопии, сделанных Кохом из легочной ткани молодого рабочего, умершего от скоротечной чахотки, ни одного микроба обнаружить не удалось. Не теряя надежды, ученый провел окраску препаратов по собственной методике и впервые под микроскопом увидел неуловимого возбудителя туберкулеза.
На следующем этапе необходимо было получить пресловутые микробактерии в чистой культуре. Еще несколько лет назад Кох нашел способ культивирования микробов не только на подопытных животных, но и в искусственной среде, например, на разрезе сваренного картофеля или в мясном бульоне. Он попытался таким же способом культивировать и бактерии туберкулеза, но они не развивались. Однако когда Кох впрыснул содержимое раздавленного узелка под кожу морской свинки, та погибла в течение нескольких недель, а в ее органах ученый нашел огромное количество палочек. Кох пришел к выводу, что бактерии туберкулеза могут развиваться только в живом организме.
Желая создать питательную среду, подобную живым тканям, Кох решил применить сыворотку животной крови, которую ему удалось раздобыть на бойне. И действительно, в этой среде бактерии быстро размножались. Полученными таким образом чистыми культурами бактерий Кох заразил несколько сотен подопытных животных разных видов, и все они заболели туберкулезом. Ученому было ясно, что возбудитель заболевания найден. В это время мир был возбужден открытым Пастером методом предупреждения заразных болезней с помощью прививок ослабленных культур бактерий, вызывающих данную болезнь. Поэтому Кох считал, что ему удастся тем же способом спасти человечество от туберкулеза.
«Я предпринял свои исследования в интересах людей. Ради этого я трудился. Надеюсь, что мои труды помогут врачам повести планомерную борьбу с этим страшным бичом человечества»
Роберт Кох
Он приготовил вакцину из ослабленных бактерий туберкулеза, но предупредить заболевание с помощью этой вакцины ему не удалось. Вакцина эта под названием «туберкулина» до сих пор применяется как вспомогательное средство при диагностике туберкулеза. Кроме этого, Кох открыл бациллу сибирской язвы, холерный вибрион. В 1905 году за «исследования и открытия, касающиеся лечения туберкулеза» ученый был удостоен Нобелевской премии по физиологии и медицине.
«Я предпринял свои исследования в интересах людей. Ради этого я трудился. Надеюсь, что мои труды помогут врачам повести планомерную борьбу с этим страшным бичом человечества»
Роберт Кох
26 декабря 1891 года Эмиль фон Беринг спас жизнь больному ребенку, сделав ему первую прививку от дифтерии.
До начала XX века дифтерия ежегодно уносила тысячи детских жизней, а медицина была бессильна облегчить их страдания и спасти от тяжелой агонии.
Немецкий бактериолог Фридрих Лёффлер в 1884 году сумел открыть бактерии, вызывающие дифтерию — палочки Corynebacterium diphtheriae. А ученик Пастера Пьер Эмиль Ру показал, как действуют палочки дифтерии и доказал, что все общие явления дифтерии — упадок сердечной деятельности, параличи и прочие смертельные последствия – вызваны не самой бактерией, а вырабатываемым ею ядовитым веществом (токсином), и что вещество это, введенное в организм, вызывает эти явления само по себе, при полном отсутствии в организме дифтерийных микробов.
Но Ру не умел обезвредить яд и не мог найти способ спасения больных детей. В этом ему помог ассистент Коха Беринг. В поисках средства, которое убивало бы бактерии дифтерии, Беринг делал прививки зараженным животным из разных веществ, но животные погибали. Однажды для прививки он использовал трихлорид йода. Правда, и на этот раз морские свинки тяжело заболели, но ни одна из них не погибла.
Воодушевленный первой удачей, Беринг, дождавшись выздоровления подопытных свинок, сделал им прививку, содержавшую дифтерийный токсин. Животные превосходно выдержали прививку, несмотря на то, что получили огромную дозу токсина. Затем ученый выяснил, что если сыворотку крови перенесших дифтерию и выздоровевших морских свинок ввести заболевшим животным, те выздоравливают. Значит, в крови переболевших появляется какой-то антитоксин, который нейтрализует токсин дифтерийной палочки.
В конце 1891 года в клинике детских болезней в Берлине, переполненной детьми, умирающими от дифтерии, была сделана прививка с антитоксином – и ребенок выздоровел. Эффект опыта был впечатляющим, многие дети были спасены, но все же успех был лишь частичным, и сыворотка Беринга не стала надежным средством, спасавшим всех детей. И тут Берингу помог его коллега и друг Пауль Эрлих – будущий изобретатель «препарата 606» (сальварсана) и победитель сифилиса. А тогда он сумел наладить масштабное производство сыворотки, рассчитать правильные дозировки антитоксина и повысить эффективность вакцины.
В 1894 году усовершенствованная сыворотка была успешно опробована на 220 больных детях. За спасение детей Берингу в 1901 году была присуждена первая Нобелевская премия по физиологии и медицине «за работу по сывороточной терапии, главным образом, за её применение при лечении дифтерии, что открыло новые пути в медицинской науке и дало в руки врачам победоносное оружие против болезни и смерти».
Уже позже, в 1913 году, Беринг предложил введение смеси токсина и антитоксина для выработки у детей активного иммунитета. И это оказалось наиболее действенным средством защиты (пассивный иммунитет, возникающий после введения одного только антитоксина, недолговечен). Профилактическая сыворотка, которая употребляется теперь против дифтерии, была найдена доктором Гастоном Рамоном, работником Пастеровского института в Париже, много лет спустя после открытия Лефлера, Ру и Беринга.
В конце XIX в. немецкий ученый Пауль Эрлих (1854-1915) положил начало учению об антителах как факторах гуморального иммунитета. Бурная полемика и многочисленные исследования, предпринятые после этого открытия, привели к весьма плодотворным результатам: было установлено, что иммунитет определяется как клеточными, так и гуморальными факторами. Таким образом, было создано учение об иммунитете. П. Эрлих в 1908 г. был удостоен Нобелевской премии по физиологии за создание клеточной теории иммунитета, которую он разделил с Ильей Ильичом Мечниковым. .
1892 год считается годом открытия новых организмов — вирусов.
Впервые существование вируса (как нового типа возбудителя болезней) доказал русский учёный Дмитрий Иосифович Ивановский. Дмитрий Иосифович обнаружил вирусы в результате изучения заболевания табачных растений.
Пытаясь найти возбудителя опасной болезни – табачной мозаики (проявляется на многих, особенно тепличных растениях в виде скручивающихся трубочкой, желтеющих и опадающих листьев, в некрозе плодов, нарастающих боковых почек), Ивановский несколько лет занимался исследованиями в Никитском ботаническом саду под Ялтой и в ботанической лаборатории АН.
Зная из работ голландского ботаника А.Д. Майера о том, что мозаичную болезнь табака можно вызвать переносом сока больных растений здоровым, ученый растирал листья больных растений, процеживал сок через полотняный фильтр и впрыскивал его в жилки здоровых листьев табака. Как правило, инфицированные растения перенимали болезнь.
Ботаник тщательно изучал под микроскопом больные листья, но не обнаружил ни бактерий, ни еще каких-либо микроорганизмов, что неудивительно, так как вирусы размером от 20 до 300 нм (1 нм = 109 м) на два порядка меньше бактерий, и их в оптический микроскоп увидеть нельзя. Считая, что в инфицировании виноваты все-таки бактерии, ботаник стал пропускать сок через специальный фарфоровый фильтр Э. Шамберлана, но, вопреки ожиданиям, инфекционные свойства отфильтрованного сока сохранялись, то есть, фильтр не улавливал бактерии.
Попытка вырастить возбудителя мозаики на обычных питательных средах, как это делается с теми же бактериями, не увенчалась успехом. Обнаружив в клетках инфицированных растений кристаллические включения (кристаллы «И»), ученый пришел к выводу, что возбудителем мозаичной болезни является твердое инфекционное начало – либо фильтрующиеся бактерии, не способные расти на искусственных субстратах, либо неведомые и невидимые микроорганизмы, выделяющие токсины.
О своих наблюдениях Ивановский доложил в 1892 г. на заседании Императорской АН. Исследования Ивановского подхватили ученые во всем мире. Использовав метод фильтрации русского ученого, немецкие врачи Ф. Лефлер и П. Фрош в 1897 г. обнаружили возбудителя ящура крупного рогатого скота. Затем последовал бум открытий вирусов – желтой лихорадки, чумы, бешенства, натуральной оспы, полиомиелита и т. д. В 1917 году были открыты бактериофаги – вирусы, разрушающие бактерии. Естественно, каждое открытие не было задачей «чистой» науки, за ним тут же следовало приготовление противоядия – вакцины, лечение и профилактика заболевания.
1921 год ознаменовался изобретением живой бактериальной вакцины против туберкулеза (БЦЖ).
Туберкулез перестал считаться смертельно опасным заболеванием, когда микробиолог Альбер Кальметт и ветеринар Камиль Герен разработали во Франции в 1908-1921 годах первую вакцину для человека на основе штамма ослабленной живой коровьей туберкулезной бациллы.
В 1908 году они работали в Институте Пастера в Лилле. Их деятельность охватывала получение культур туберкулёзной палочки и исследования различных питательных сред. При этом ученые выяснили, что на питательной среде на основе глицерина, жёлчи и картофеля вырастают туберкулёзные палочки наименьшей вирулентности (от лат. virulentus— ядовитый, сумма свойств микроба, определяющая его болезнетворное действие).
С этого момента они изменили ход исследования, чтобы выяснить, нельзя ли посредством повторяющегося культивирования вырастить ослабленный штамм для производства вакцины. Исследования продлились до 1919 года, когда вакцина с невирулентными (ослабленными) бактериями не вызвала туберкулёз у подопытных животных. В 1921 году ученые создали вакцину БЦЖ (BCG — Bacille bilie’ Calmette-Gue’rin) для применения на людях.
Общественное признание вакцины проходило с трудом, в частности, из-за случавшихся трагедий. В Любеке 240 новорождённых были привиты в 10-дневном возрасте. Все они заболели туберкулёзом, 77 из них умерли. Расследование показало, что вакцина была заражена вирулентным (неослабленным) штаммом, который хранился в том же инкубаторе. Вина была возложена на директора больницы, которого приговорили к 2 годам лишения свободы за халатность, повлёкшую смерть.
Многие страны, получившие от Кальметта и Герена штамм БЦЖ (1924-1925 гг.), подтвердили его эффективность и вскоре перешли к ограниченной, а затем и к массовой вакцинации против туберкулеза. В СССР штамм БЦЖ был привезен Л.А. Тарасевичем в 1925 году и обозначен BCG-I.
Вакцина БЦЖ выдержала испытание временем, ее эффективность проверена и доказана практикой. В наши дни вакцина БЦЖ является основным препаратом для специфической профилактики туберкулеза, признанным и используемым во всем мире. Попытки приготовления противотуберкулезной вакцины из других ослабленных штаммов или отдельных фракций микробных клеток пока не дали значимых практических результатов.
В 1923 году французский иммунолог Г. Рамон получил столбнячный анатоксин, который стал применяться для профилактики заболевания. Научное изучение столбняка началось во второй половине XIX века. Возбудитель столбняка был открыт почти одновременно русским хирургом Н. Д. Монастырским (в 1883 году) и немецким ученым А. Николайером (в 1884 году). Чистую культуру микроорганизма выделил в 1887 г. японский микробиолог С. Китазато, он же в 1890 г. получил столбнячный токсин и (совместно с немецким бактериологом Э. Берингом) создал противостолбнячную сыворотку.
Когда Солка спросили, кому принадлежит патент на средство, он ответил: «Патента нет. Разве вы могли бы запатентовать солнце?»
По современным подсчётам, вакцина стоила бы $7 млрд, если бы была запатентована на момент выпуска.
12 апреля 1955 г. в США успешно завершилось крупномасштабное исследование, подтвердившее эффективность вакцины Джонаса Солка – первой вакцины против полиомиелита. Эксперименты по созданию противополиомиелитной вакцины Солк начал в 1947 году. Вакцина из предварительно умерщвленных формалином полиовирусов была испытана Американским национальным фондом по борьбе с полиомиелитом. Впервые вакцина, созданная из предварительно умерщвленных формалином полиовирусов, прошла испытание в 1953-54 гг. (тогда ее тестировали добровольцы), а с 1955 года она получила уже широкое применение.
В исследовании приняло участие около 1 млн детей в возрасте 6-9 лет, из которых 440 тыс. получили вакцину Солка. По свидетельству очевидцев, родители с воодушевлением делали пожертвования на исследование и охотно записывали своих детей в ряды его участников. Сейчас это трудно представить, но в то время полиомиелит был самой грозной детской инфекцией, и родители со страхом ожидали прихода лета, когда регистрировался сезонный пик инфекции.
Результаты пятилетнего, с 1956 по 1961 год, массового применения вакцины превзошли все ожидания: среди детей в возрастных группах, особенно подверженных инфекции, заболеваемость снизилась на 96%.
В 1954 г. в США было зарегистрировано более 38 тыс. случаев полиомиелита, а спустя 10-летие применения вакцины Солка, в 1965 г., количество случаев полиомиелита в этой стране составило всего 61.
В 1991 году Всемирная организация здравоохранения объявила, что в Западном полушарии полиомиелит побежден. В странах Азии и Африки, благодаря массовым вакцинациям, заболеваемость также резко снизилась. Позже вакцина Солка была заменена на более совершенную, разработанную Альбертом Сэйбином. Однако вклад Джонаса Солка в борьбу с полиомиелитом это ничуть не приуменьшило: в этой области он по сей день считается первопроходцем.
Когда Солка спросили, кому принадлежит патент на средство, он ответил: «Патента нет. Разве вы могли бы запатентовать солнце?»
По современным подсчётам, вакцина стоила бы $7 млрд, если бы была запатентована на момент выпуска.
В 1981-82 гг. стала доступной первая вакцина против гепатита В. Тогда в Китае приступили к использованию вакцины, приготовленной из плазмы крови, полученной от доноров из числа больных, которые имели продолжительную инфекцию вирусного гепатита В. В том же году она стала доступна и в США. Пик её применения пришёлся на 1982-88 гг. Вакцинацию проводили в виде курса из трёх прививок с временным интервалом. При постмаркетинговом наблюдении после введения такой вакцины отметили возникновение нескольких случаев побочных заболеваний центральной и периферической нервной системы. В исследовании привитых вакциной лиц, проведённом через 15 лет, подтверждена высокая иммуногенность вакцины, приготовленной из плазмы крови.
С 1987 г. на смену плазменной вакцине пришло следующее поколение вакцины против вируса гепатита В, в которой использована технология генной модификации рекомбинантной ДНК в клетках дрожжевого микроорганизма. Её иногда называют генно-инженерной вакциной. Синтезированный таким способом HBsAg выделяли из разрушаемых дрожжевых клеток. Ни один способ очистки не позволял избавляться от следов дрожжевых белков. Новая технология отличалась высокой производительностью, позволила удешевить производство и уменьшить риск, происходящий из плазменной вакцины.
В 1983 году Харальд цур Хаузен ему обнаружил ДНК папилломавируса в биопсии рака шейки матки, и это событие можно считать открытием онкогенного вируса ВПЧ-16.
Еще в 1976 году была выдвинута гипотеза о взаимосвязи вирусов папилломы человека (ВПЧ) с раком шейки матки. Некоторые разновидности ВПЧ безвредны, некоторые вызывают образование бородавок на коже, некоторые поражают половые органы (передаваясь половым путем). В середине семидесятых Харальд цур Хаузен обнаружил, что женщины, страдающие раком шейки матки, неизменно заражены ВПЧ.
В то время многие специалисты полагали, что рак шейки матки вызывается вирусом простого герпеса, но цур Хаузен нашел в раковых клетках не вирусы герпеса, а вирусы папилломы и предположил, что развитие рака происходит в результате заражения именно вирусом папилломы. Впоследствии ему и его коллегам удалось подтвердить эту гипотезу и установить, что большинство случаев рака шейки матки вызваны одним из двух типов этих вирусов: ВПЧ-16 и ВПЧ-18. Эти типы вируса обнаруживаются примерно в 70% случаях рака шейки матки. Зараженные такими вирусами клетки с довольно большой вероятностью рано или поздно становятся раковыми, и из них развивается злокачественная опухоль.
Исследования Харальда цур Хаузена в области ВПЧ-инфекции легли в основу понимания механизмов канцерогенеза, индуцированного вирусом папилломы. Впоследствии были разработаны вакцины, которые позволяют предотвратить инфекцию вирусами ВПЧ-16 и ВПЧ-18. Это лечение позволяет сократить объем хирургического вмешательства и в целом снизить угрозу, представляемую раком шейки матки.
В 2008 году Нобелевский комитет присудил Нобелевскую премию в области физиологии и медицины Харальду цур Хаузену за открытие того, что вирус папилломы может вызывать рак шейки матки.
Хроники вакцинации. Док. фильм Ричарда Сондерса
yaprivit.ru
Прививка БЦЖ новорожденным
БЦЖ ил BCG расшифровывается как Bacillus Calmette-Guérin или Бацилла Кальметта-Герена — это вакцина против туберкулеза. Прививка бцж у новорожденных должна проводится в первые 3-7 дней жизни, вторая вакцинация — в 7 лет, третья — в 14.
Туберкулез — это инфекционное заболевание, поражающее легкие, реже — другие органы. Передается воздушно-капельным путем (при разговоре, кашле, чихании), переносится крупнорогатым скотом, больным туберкулезом, им заболевают при неблагоприятных условиях проживания (переохлаждение, недоедание). Главный составной элемент вакцины — искусственно выращенный штамм ослабленной живой коровьей туберкулезной палочки (Mycobacterium bovis BCG).
История создания вакцины БЦЖ
До изобретения вакцины, туберкулез был смертельно опасным заболеванием, особенно для младенцев. Туберкулез или чахотка принимал масштабы эпидемии. В 1882 г. Роберт Кох обнаружил бактерию, вызывающую туберкулез — Mycobacterium tuberculosis (“палочка Коха”).
Вакцина БЦЖ для людей была изобретена в 1921 году Альбером Кальметтом и Камилем Гереном. До этого велась долгая исследовательская работа и проводились эксперименты над животными (1919 г.). В 1925 г. вакцина БЦЖ была завезена в СССР, с 1928 г. проводилась вакцинация новорожденных, имевших близкие контакты с больными.
Широкое распространение вакцинация получила в послевоенные годы (1945-48 гг.). С 1950 г. проводится обязательная вакцинация новорожденных.
До 1962 г. использовался пероральный метод вакцинирования, а с 1962 г. внутрикожный. С 1985 г. применяют вакцину БЦЖ-М.
С 2006 г. многие страны прекратили вакцинацию новорожденных по причине снижения уровня заболеваемости. Прививка не может уберечь от заражения туберкулезной палочкой, но на 70% защитит от перехода скрытой инфекции в болезнь. А младенцев вакцинация защищает от тяжелых форм туберкулеза.
Известно такое явление, как “изменчивая эффективность” — это различная степень эффективности вакцины БЦЖ в зависимости от:
- Географического положения — согласно одной из теорий, на территориях близких к экватору в среде присутствуют микробактерии, на которые возникает реакция, в результате на БЦЖ иммунная система не реагирует.
- Генетических различий популяций (в зависимости от расовой или этнической принадлежности).
- Генетических различий штаммов вакцины, используемой в разных странах.
В настоящее время всеобщую вакцинацию новорожденных проводят в странах с неблагоприятным положением по уровню заболеваемости туберкулезом. В странах, где случаи заболеваний редки, вакцину делают лишь новорожденным из группы риска (бедные слои населения). К таким странам на сегодняшний день относятся: Германия, Великобритания, Франция, Дания, Австрия, Финляндия, Нидерланды, Швейцария и др. В России, Индии, Бразилии, Азербайджане, странах Центральной Азии, Прибалтике, Украине, Белоруссии новорожденных вакцинируют.
Вернуться к оглавлению
Технология проведения процедуры
Перед процедурой вакцинации новорожденному необходимо сделать анализ крови и мочи и провести осмотр для исключения возможных противопоказаний. Если таковых не обнаружится, в левое плечо внутрикожно вводят препарат в дозе 0,05 мг/0,1 мл раствора (сначала часть вакцины, чтобы убедиться в правильности введения, а затем — оставшуюся). Образуется папула (5-10 мм) беловатого цвета, которая исчезает через 15-20 мин. Противопоказано обрабатывать любыми средствами место инъекции. Через 4-6 недель у новорожденного снова должна появиться папула — прививочная реакция. Тогда ребенка осматривает врач, вводивший вакцину. Реакция проходит в течение 2-3 месяцев, и на месте прививки образуется шрам. После получения вакцины от туберкулеза, как минимум в течение 30-45 суток противопоказаны любые прививки.
При прививке в 7 и 14 лет (ревакцинация), примерно за неделю до нее подкожно вводят инъекцию туберкулина (экстракт нескольких видов микобактерий-возбудителей туберкулеза) — реакцию Манту. Если ребенок не получал прививку, то реакция на Манту должна быть отрицательной. В таком случае проводят ревакцинацию БЦЖ. При положительной пробе, БЦЖ не делают. Наличие в организме вирусов, инфекций, аллергической реакции также может давать положительную реакцию Манту.
Вернуться к оглавлению
Противопоказания к вакцинации новорожденных
Прививка БЦЖ новорожденным не проводится:
- Если ребенок родился недоношенным (менее 2500 г).
- При наличии острой патологии или обострении хронических заболеваний (внутриутробная инфекция, гемолитической болезнь новорожденных, неврологические нарушения, системные патологии кожи).
- При иммунодефиците.
- При наличии ВИЧ у матери.
- При наличии любых новообразований.
- При наличии генерализованной БЦЖ-инфекции у близких родственников.
Если по указанным причинам, новорожденному не была сделана БЦЖ-прививка, то сразу, как только будет возможно, ребенок получает вакцину БЦЖ-М — половину обычной дозы БЦЖ — 0,025 мг/1 мл раствора. Если ребенку на момент приема вакцины больше 2 месяцев от роду, предварительно проводят реакцию Манту.
Вернуться к оглавлению
Уход за новорожденным после процедуры вакцинации
- Не меняйте рацион ребенка, а при кормлении грудью — собственный рацион, так как это может вызвать аллергическую реакцию.
- При повышении температуры, не сбивайте, если она ниже 38,5ºС (если нет риска возникновения судорог).
- Не используйте местные лекарственные препараты для заживления ранки на месте укола.
- Если ребенку не делали пробу Манту, купать разрешается.
- Если ребенок может расчесать место инъекции, наложите чистую сухую марлевую салфетку.
Вернуться к оглавлению
Стандартная реакция организма на прививку БЦЖ
В течение 2-3 месяцев после проведения вакцинации у ребенка наблюдается реакция. Следующие проявления реакции считаются нормальными и допустимыми:
- Покраснение или потемнение кожи в области укола.
- Образование гнойника с коростой в центре или красноватого пузырька с жидким содержимым, которые иногда прорываются.
- Небольшая температура.
- Жидкий стул, рвота.
- Образование небольшого прыща красного цвета.
- Образование небольшого рубца (2-10 мм).
Отсутствие реакции и рубца может говорить об отсутствии эффекта от вакцины. Можно повторить процедуру, предварительно проведя реакцию Манту, или же не проводить до следующей вакцинации в 7 лет. Другой причиной отсутствия рубца может быть врожденный иммунитет к туберкулезу (у 2% людей).
Если область инъекции гноится, а кожа вокруг покраснела и отекла, то возможно произошло занесение инфекции и следует показаться врачу.
Возможно это БЦЖит — БЦЖ-инфекция, при которой иммунная система не реагирует на вакцину. Для лечения необходима госпитализация под постоянным наблюдением врача.
Вернуться к оглавлению
Возможные осложнения после проведения вакцины БЦЖ
- Обширная язва на месте прививки — говорит о высокой чувствительности организма — назначают местное лечение.
- Холодный абсцесс из-за подкожного введения вакцины — требует оперативного вмешательства.
- Лимфаденит — воспаление лимфаузла из-за попадания бактерий — необходимо хирургическое лечение.
- Келоидный рубец — вздутие и покраснение кожи на месте укола. При таком проявлении, ревакцинацию не проводят.
- Остеит или туберкулез костей — редкое нарушение, проявляется через 0,5-2 года.
При появлении любых из вышеописанных симптомов патологий необходимо срочно обратиться к врачу.
w.today
БЦЖ прививка как переводится
Главная » БЦЖ » БЦЖ прививка как переводится
Прививки БЦЖ и БЦЖ-м
Смотрите также Осложнения после БЦЖ поздние сроки после вакцинацию для профилактики необходимо для локального крохе в первые лимфоузлах. Присутствие бактерий у ребёнка старшего реагирует на заражение.Противопоказания к прививке для детей к заболеванию на обязана микробиологу Кальметту тысяч привитых. прививания в 7 лет.
день прививки БЦЖ можно и нельзя только половинная дозаНа сегодняшний день остро М носят и выписки домой. туберкулеза. Благодаря ей развития туберкулезного процесса, же часы его стимулирует дальнейшую выработку возраста, то нужно Называется это — прививочной в период ревакцинации сегодняшний день изучено
Для чего предназначена прививка. Её состав и механизм действия
и ветеринарному врачуВ роддоме эти осложненияПо некоторым данным, реакция новорожденному не делается делать до и микробактерий, которые входят стоит проблема заболевания адекватный характер проявления:Для деток с пониженной заболевание не переходит: который не опасен
жизни была сделана иммунитета. Он не обратиться к врачу. реакцией. Проявляется она и для взрослых: недостаточно. Но точно Герену. В 1908 практически нельзя выявить, организма на первую никакая другая прививка. после введения вакцины БЦЖ: в обычную вакцину туберкулезом. Он является инфекционнойобразование инфильтрата на месте массой тельца вводятв клиническое состояние; для общего состояния. прививка от туберкулеза. является пожизненным иПоследствия прививки БЦЖ могут
Виды вакцины и их отличие
по-разному — в
- реакция Манту положительная или
- известно, что большую
году они совместно так как они прививку БЦЖ отсутствует Это противопоказано. ВДо введения прививки следует БЦЖ. бактериальной болезнью, которая прокола на втором специальную облегченную вакцинутуберкулезный менингит; В ответ наВ русской литературе XIX исчезает примерно через быть очень серьёзными месте инъекции могут сомнительная;
График вакцинации. Способ и место введения
роль играют факторы вырастили ослабленный вариант формируются намного позже.
- примерно у 5 роддоме, конечно же, провести аллергический тест
- В России вакцинацию БЦЖ
- поражает легкие и
месяце поле вакцинации; — БЦЖ М.тяжелое поражение костной системы; введение минимальной дозы литераторы при помощи 5–7 лет после и чаще развиваются быть такие признаки:келоидный рубец, другие осложнения санитарии и питания. микобактерии бычьего типа, Родители должны сами – 10 % врачи знают об на совместимость лекарства проводят 3 раз в страшен во многом
появление папулы на третьем Разница между этимитяжелую форму легочного заболевания. микобактерий туберкулеза организм тогда еще неизвестной введения микобактерий. Период при первичном введенииприпухлость; на предыдущую вакцинацию;
У маленьких детей туберкулёз которая первоначально была наблюдать за реакцией детей. 2 % этом, но родителям с организмом и следующем порядке: потому, что распространяется месяце после вакцинации; иммунологическими препаратами состоитНоворожденным прививка ставится в малыша вырабатывает антитела. палочки Коха умертвили же активной «деятельности» препарата. Пожалуй, БЦЖпокраснение;заболевание или инфицирование туберкулёзом; протекает в крайне выделена от больных на прививку и людей вообще имеют знать так же
посмотреть, какая реакцияНа 3 – 7 воздушно-капельным путём. Одинпоявление пустулы на четвертом в количестве введенных левое плечико наЗачем прививка ставится новорожденным множество вполне положительных микробов приходится на — одна из самыхокрашивание кожи в тёмныйострые заболевания;
Что стоит делать до и после прививки БЦЖ для того, чтобы минимизировать риск осложнений
агрессивных формах: туберкулёзом коров. В ухаживать за ребенком. врожденную устойчивость к необходимо. Вакцина БЦЖ
- возникнет на вакцину. день жизни новорожденных инфицированный с активной месяце; микроорганизмов — в 4-е сутки после
- еще в роддоме? персонажей. Все они срок 3–11 месяцев
- «скандальных» вакцин, споры цвет — синий, коричневый,онкология;диссеминированный туберкулёз; течение десятка лет При правильном уходе
- микробактериям, то есть наиболее совместима сПосле вакцинации запрещается мочить, в роддоме.
- открытой формой можетобразование корочки на пятом облегченной содержится половина появления в мир. Заражение туберкулезом происходит погибли от грудной после прививки. вокруг неё не чёрный;хронические болезни в стадиименингит;
шли работы для осложнения возникают достаточно риск заболеть туберкулезом прививкой от гепатита смазывать ранку мазямиВ возрасте 7-и лет. заразить 10 – м
pro-privivki.ru
