12 общих симптомов энтеровирусной инфекции у детей
Энтеровирусная инфекция имеет другое название — «рука — нога — рот», потому что, несмотря на великое множество клинических проявлений, чаще наблюдается сыпь на вышеуказанных частях тела. Заболевание чаще имеет гладкое течение, но, вместе с тем, требует немедленной консультации специалиста и назначения правильного лечения.
Энтеровирусная инфекция у детей представляет собой заболевание, которое протекает с выраженной клиникой общей интоксикации. Поскольку возбудитель не один (группа кишечных вирусов, род – Энтеровирус), то и клинические проявления отличаются значительным разнообразием.
Область научных и практических интересов: Диагностика и лечение нервных болезней у детей от 0 до 18 лет. Член Неврологического общества Москвы.
Заболеваемость энтеровирусной инфекцией среди детей
Энтеровирус у детей достаточно распространённое явление. Педиатры могут с уверенностью утверждать о том, что данная болезнь встречается также часто, как и банальная острая респираторная вирусная инфекция. Чаще поражаются дети младшего возраста, также лица с ослабленным иммунитетом. Нередко наблюдаются вспышки инфекции в ДУ закрытого типа.
Чаще поражаются дети младшего возраста, также лица с ослабленным иммунитетом. Нередко наблюдаются вспышки инфекции в ДУ закрытого типа.
Возбудитель энтеровирусной инфекции
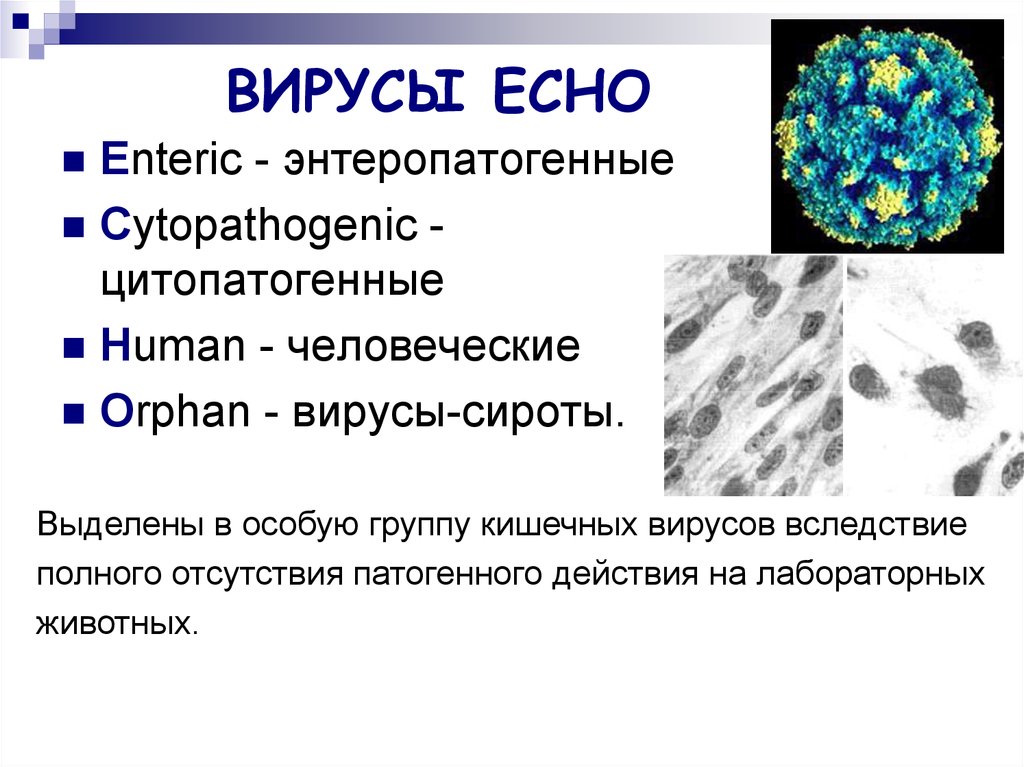
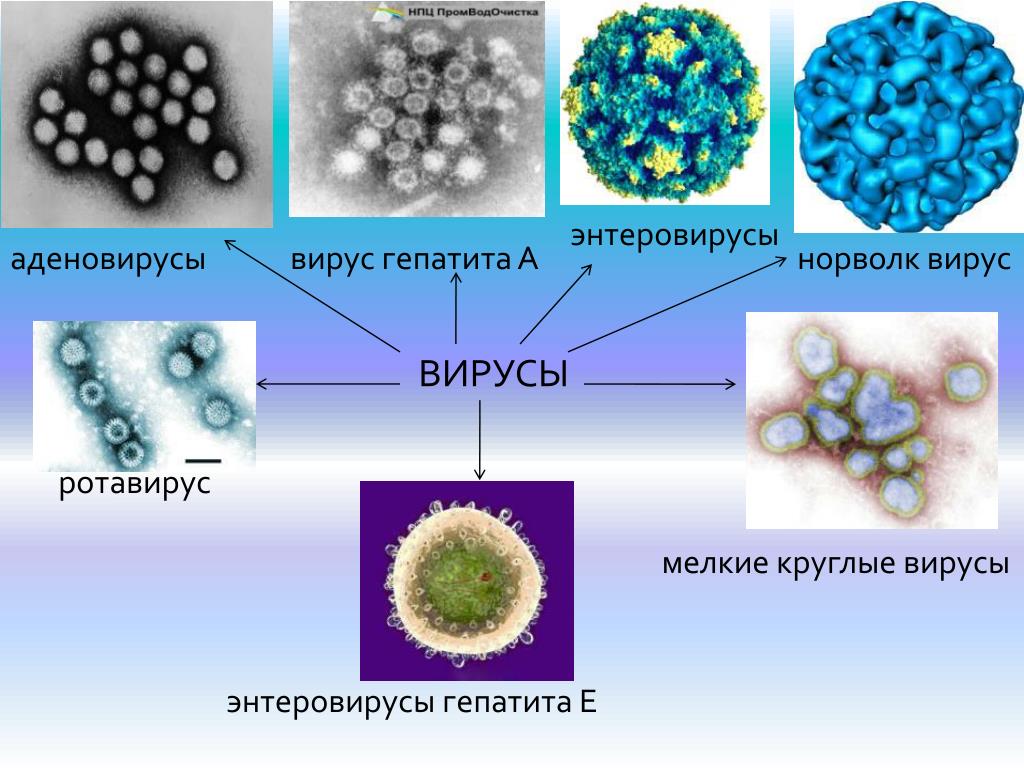
В научном мире известно, что энтеровирусную инфекцию вызывают кишечные вирусы – Коксаки, ECHO, а также энтеровирусы без названия, объединённые согласно схожести симптоматики и обозначаемые как 68-71. Наиболее часто удаётся выявить в биологически материале больного первых двух возбудителей.
Также данные вирусы в достаточной мере изучены на сегодняшний день. А именно, возбудитель Коксаки имеет около 30 серологических варианта, а вирус ECHO — 34. Помимо этого, вирус Коксаки делится на 2 группы — А и В.
Вирусы Коксаки и ECHO способны длительно сохранять жизнеспособность и способность вызывать заболевания в обычных «комнатных» условиях. Например, излюбленным местом является бассейн общественного пользования, открытые водоёмы. Также нередко возбудитель можно выявить в продуктах питания, таких как: молоко, хлеб, овощи и фрукты. В фекалиях больного человека вирусы на протяжении 6 месяцев и более сохраняют свою активность.
В фекалиях больного человека вирусы на протяжении 6 месяцев и более сохраняют свою активность.
Энтеровирусы устойчивы к действию антибиотиков, некоторых дезинфицирующих средств и к низкой температуре.
Распространение энтеровируса
Источник инфекции
Источником инфекции может быть вирусоноситель или больной человек. Инфицирование возможно несколькими путями. Фекально-оральный путь реализовывается при осуществлении заражения человека через загрязнённые продукты питания или воду. Воздушно-капельный механизм инфицирования возможен при попадании инфицированного секрета в верхние дыхательные пути. Довольно редко происходит заражение бытовым путём, то есть через загрязнённые руки, предметы обихода, личные вещи. Наиболее часто выявляется заболевание у лиц детского возраста.
Энтеровирусная инфекция характеризуется наличием сезонности, а именно — имеет пик инфицирования в летне-осенний период. После перенесённого заболевания у реконвалесцента наблюдается лишь типоспецифический иммунитет, то есть терпимость только к одному серологическому варианту вируса.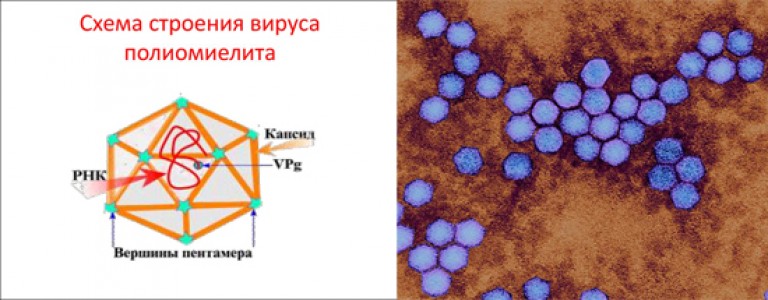
Патогенез
Чем можно объяснить полиморфизм клинических проявлений при одном и том же вирусе? Всё дело в том, что возбудитель, оседая на эпителиальных клетках, лимфоидных образованиях слизистой оболочке верхних дыхательных путей или кишечника, с кровью разносится по различным тканям и органам, тем самым поражая их, вызывает множество клинических симптомов.
Классификация энтеровирусной инфекции
Существует несколько видов классификаций данной болезни.
По типу течения заболевания:
- типичное (герпетическая ангина, кишечная, респираторная, паралитическая формы, эпидемическая миалгия, миакардит, менингит, энтеровирусная экзантема, а также возможны комбинации данных форм заболевания).
- атипичное (стёртое, бессимптомное).
Симптомы энтеровирусной инфекции у детей
Общие симптомы
Несмотря на то, что клинических проявлений может быть великое множество, инкубационный период для всех форм един и составляет он от 1 до 10 дней. Общие симптомы также имеют сходство и характерны для всех видов проявлений болезни. Начинается заболевание остро, с повышения температуры до высоких цифр (39 — 40 ºC).
Общие симптомы также имеют сходство и характерны для всех видов проявлений болезни. Начинается заболевание остро, с повышения температуры до высоких цифр (39 — 40 ºC).
Быстро присоединяются симптомы интоксикации:
Отличительной особенностью общей симптоматики может быть покраснение верхней половины тела (лицо, шея, грудь), а также расширение сосудов склеры глаз.
Нередко наблюдается появление пятнисто-папулёзной сыпи на излюбленных участках кожи (голени, кисти, ладони, стопы). При осмотре выявляют покраснение слизистой оболочки ротоглотки, язык обложен белым налётом. Высокая температура может сохранятся 3 — 5 дней, после её нормализации симптомы интоксикации исчезают.
Общий анализ крови позволяет сделать вывод о том, что имеется вирусная инфекция (нормальное или слегка повышенное количество лейкоцитов, повышение лимфоцитов и эозинофилов).
Клинические варианты энтеровирусной инфекции
Серозный менингит
Для серозного менингита характерно острое начало. Температура поднимается до фебрильных цифр, появляются симптомы общей интоксикации, которые имеют тенденцию нарастать. На фоне высоких цифр температуры у детей нередко появляются судороги. В связи с вовлечением в воспалительный процесс мозговых оболочек к вышеописанным симптомам присоединяются менингеальные (Брудзинского, Кернига, напряжение мышц затылка).
Температура поднимается до фебрильных цифр, появляются симптомы общей интоксикации, которые имеют тенденцию нарастать. На фоне высоких цифр температуры у детей нередко появляются судороги. В связи с вовлечением в воспалительный процесс мозговых оболочек к вышеописанным симптомам присоединяются менингеальные (Брудзинского, Кернига, напряжение мышц затылка).
Такие симптомы может выявить только специалист. Менингельные знаки более выражены на высоте лихорадки, исчезают спустя неделю от начала болезни. Данная форма заболевания требует взятия ликвора (спинномозговой жидкости). Анализ ликвора показывает повышение лимфоцитарных клеток.
Воспалительные проявления в ликворе (спинномозговой жидкости) исчезают только к концу четвёртой недели от начала развития болезни. Нормализация показателей спинномозговой жидкости наблюдается через месяц от начала болезни. Данная форма энтеровирусной инфекции одна из самых тяжёлых, восстановление после инфекции происходит длительно, часть симптомов (тошнота, нарушение аппетита, головная боль) ещё несколько месяцев после нормализации анализов могут беспокоить пациента.
Герпетическая ангина
Не имеет ничего общего с герпесом, названа так по причине схожести элементов сыпи с герпетическими элементами. Герпангины без других симптомов энтеровирусной инфекции не бывает. Как правило она сочетается с другими формами. Для неё также характерно острое начало и появление общеинтоксикационной симптоматики.
При данном клинической форме энтеровируса обязательно поражается слизистая полости рта – на мягком и твёрдом небе, на нёбных дужках появляется мелкопузырчатая сыпь. Элементы сыпи могут вскрываться, сливаться и образовывать обширные эрозии. Это причиняет ребёнку дискомфорт, он отказывается от еды, плачет.
Дети, которые уже умеют говорить, будут жаловаться на боль. В воспалительный процесс вовлекаются регионарные лимфатические узлы.
Эпидемическая миалгия
Особенностью течения данной формы энтеровирусной инфекции является появление мышечных болей. Боль нарастает при движении, приступ боли проходит через 3-5 минут. Болеть могут абсолютно любые мышцы, в том числе межрёберные (поверхностное щадящее дыхание), мышцы брюшного пресса (обязательно исключить острую абдоминальную хирургическую патологию при осмотре – например, аппендицит).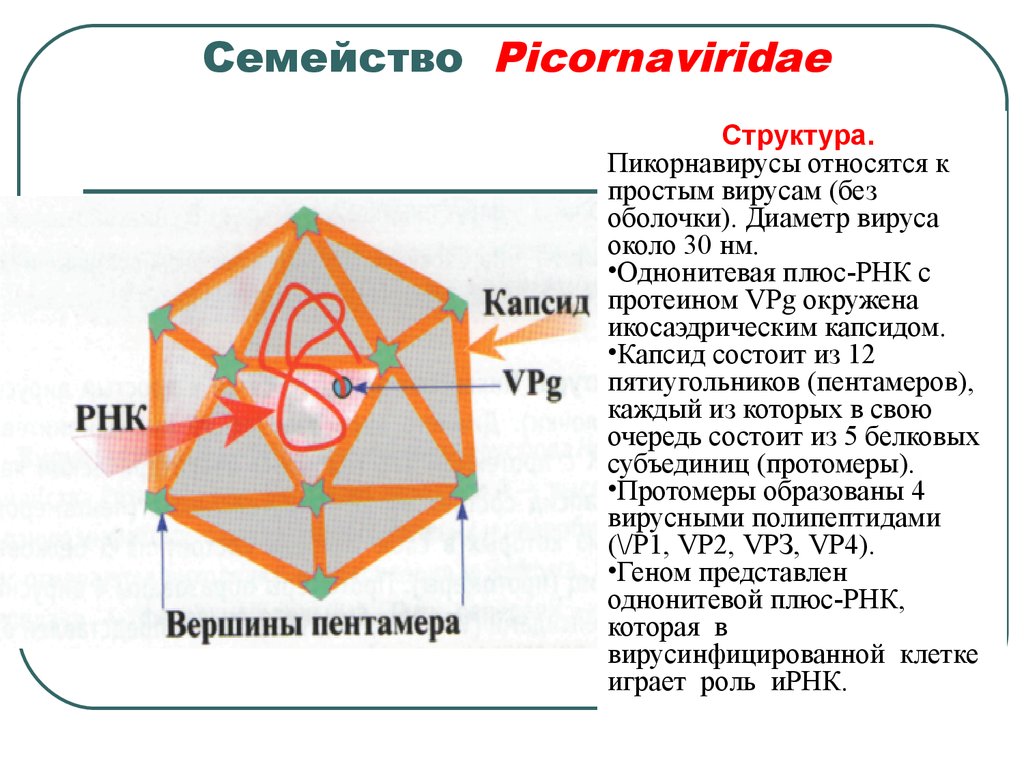
Кишечная форма
Характерна для детей грудного возраста. Заболевание также имеет острое начало. В воспалительный процесс вовлекается кишечник, а значит появляются характерные боли, нарушение стула по типу диареи (при исследовании в каловых массах нередко обнаруживается слизь). Наблюдается вздутие живота. В пользу энтеровирусной инфекции свидетельствует сочетание вышеописанных симптомов с катаральными явлениями.
Миокардит
Встречается у новорождённых и детей до шести месяцев. Протекает очень тяжело и часто имеет летальный исход. Общие симптомы не специфичны: лихорадка, одышка, вялость, рвота, понос. Аускультативно данная форма характеризуется появлением сердечных шумов и нарушением сердечного ритма. Другие физикальные методы позволяют обнаружить увеличение размеров сердца и печени.
Энтеровирусная экзантема
Сыпь при энтеровирусной инфекции имеет одну характерную особенность. Она всегда появляется уже после нормализации температуры. Типичная локализация для энтеровирусной сыпи – конечности и лицо. В области туловища сыпь появляется редко. Чаще элементы сыпи выглядят как мелкие розовые пятнышки, чуть реже могут образовываться папулы.
В области туловища сыпь появляется редко. Чаще элементы сыпи выглядят как мелкие розовые пятнышки, чуть реже могут образовываться папулы.
Энтеровирусная экзантема у детей может сохранятся до нескольких дней, иногда может разрешаться и за несколько часов.
Паралитическая форма
На фоне нормальной температуры появляются признаки поражения нервных окончаний – слабость в конечностях, нарушение походки. Необходимо дифференцировать от полиомиелита.
Как подтверждается диагноз
Время года, контакты ребёнка с больными лицами, любая информация поможет специалисту правильно поставить диагноз и, соответственно, назначить необходимое лечение. Лабораторные методы исследования должны быть назначены больному для исключения спорных диагнозов.
Неспецифические методы (общий анализ крови) не имеют типичных признаков заболевания. Поэтому применяют специфические. К ним относятся вирусологический и серологический методы. Для вирусологического исследования необходим биологический материал больного (слизь из носо-ротоглотки, кал, кровь, ликвор).
Наиболее значимо для диагностики выделение вируса из крови и ликвора. Для серологического исследования используют специальные реакции (нейтрализации и торможения гемагглютинации). Необходимым материалом является кровь, которую забирают в начале болезни и спустя 3 недели.
Диагностически значимым будет результат — нарастание титра антител в 4 раза. Иммуноферментный анализ позволяет выявить защитные антитела.
Лечение энтеровирусной инфекции
Основные группы препаратов
К сожалению, специфического лечения энтеровирусной инфекции не существует.
Принципы терапии данной болезни имеют симптоматический характер:
- жаропонижающие средства (Парацетамол, Ибупрофен) применяются при температуре выше 38,5 ºC;
- антисептические средства (Гексорал, Мирамистин) для обработки слизистой оболочки ротоглотки, а также для снятия боли в горле — Тантум Верде;
- дегидратационная терапия (Лазикс, Диакарб) при серозном менингите;
- гормональная терапия (Преднизолон) при миокардите.

Лечение энтеровирусной инфекции основано больше на соблюдении режимных мероприятий и диеты. На период лихорадки больным назначают строгий постельный режим. Лёгкое и среднетяжёлое течение заболевания может протекать в домашних условиях.
А больные с тяжёлой формой болезни должны наблюдаться в круглосуточном стационаре. Средняя продолжительность лечения в больнице составляет 21 день.
Диета при энтеровирусной инфекции у детей
Диета имеет некоторые особенности. В первые сутки больным предлагают только обильное питьё. Питьевой режим должен быть соответствующим на всём протяжении лечения заболевания. Исключаются жареные продукты, а также свежие овощи, фрукты, мясо. Пища должна быть протёртой, щадящей, тёплой и хорошо перевариваться. Рекомендуют бульоны, каши, овощные пюре.
Осложнения энтеровирусной инфекции
Как правило, энтеровирусная инфекция имеет гладкое течение и редко развиваются осложнения. Но тяжёлые формы заболевания могут осложняться отёком мозга, судорогами. Возможно присоединение вторичной бактериальной флоры (отит, пневмония).
Возможно присоединение вторичной бактериальной флоры (отит, пневмония).
Диспансерное наблюдение
Выписка из стационара должна проводиться при полном исчезновении клинических симптомов (не ранее чем через 2 недели). При поражении других органов (почек, сердца, глаз, печени), ребёнка берут под наблюдение соответствующие специалисты.
Профилактические мероприятия
Специфическая профилактика против энтеровирусной инфекции существует, но проводится далеко не всем. Она показана тяжело больным детям, а также при наличии сопутствующей патологии. Профилактика проводится по эпидемическим показаниям экстренно. Препаратом является оральная полиомиелитная вакцина.
Врач при обнаружении больного энтеровирусной инфекцией немедленно должен подать экстренное извещение в «Центр гигиены и эпидемиологии». Контактных детей младше 6 лет изолируют и производят наблюдение в течение 20 дней. Больных изолируют на 10 дней при условии отсутствия поражения нервной системы. В помещении, где находился больной, производится текущая и заключительная дезинфекция.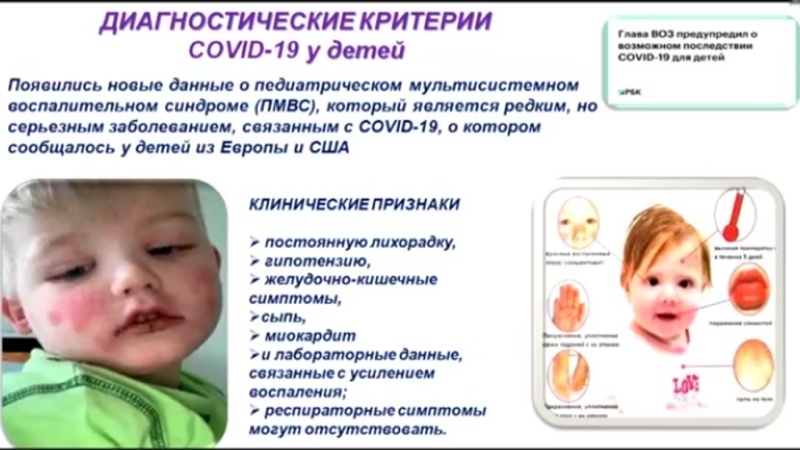
Заключение
Энтеровирусная инфекция у детей довольно распространённое заболевание, которое встречается так же часто, как ОРВИ. Данная инфекция может даже протекать под маской «простуды». Энтеровирус может с током крови разноситься по организму и проявляться различными симптомами, которые бывает достаточно сложно дифференцировать от других заболеваний. Поэтому при проявлении болезни следует немедленно обратиться к врачу.
Вовремя назначенная терапия и соблюдение всех рекомендаций помогает быстрее справиться с недугом.
Вирус Коксаки A6: новый появляющийся патоген, вызывающий вспышки заболеваний рук, ящура во всем мире
Обзор
. 2015;13(9):1061-71.
дои: 10.1586/14787210.2015.1058156. Epub 2015 25 июня.
Ляньлянь Бянь 1 , Yiping Wang, Xin Yao, Qunying Mao, Miao Xu, Zhenglun Liang
принадлежность
- 1 Национальные институты по контролю за продуктами и лекарствами, Пекин 100050, Китай.

- PMID: 26112307
- DOI: 10.1586/14787210.2015.1058156
Обзор
Lianlian Bian et al. Expert Rev Anti Infect Ther. 2015.
. 2015;13(9):1061-71.
дои: 10.1586/14787210.2015.1058156. Epub 2015 25 июня.
Авторы
Ляньлянь Бянь 1 , Ипин Ван, Синь Яо, Цюньин Мао, Мяо Сюй, Чжэнглун Лян
принадлежность
- 1 Национальные институты по контролю за продуктами и лекарствами, Пекин 100050, Китай.

- PMID: 26112307
- DOI: 10.1586/14787210.2015.1058156
Абстрактный
Энтеровирус 71 (EV71) и вирус Коксаки A16 (CA16) являются преобладающими возбудителями, вызывающими вспышки ящура и кистей рук (HFMD) во всем мире. Другие серотипы энтеровируса человека A (HEV-A), как правило, вызывают только спорадические случаи HFMD. Однако после того, как в 2008 г. в Финляндии разразился HFMD, вызванный вирусом Коксаки A6, CA6 был идентифицирован как возбудитель, ответственный за серию вспышек HFMD в Европе, Северной Америке и Азии. Из-за тяжести клинических проявлений и недооцененного бремени для общественного здравоохранения эпидемия HFMD, связанной с CA6, представляет собой новую проблему для контроля HFMD.
Ключевые слова: коксакивирус А16; коксакивирус А6; энтеровирус 71; кисть, ящур и ротовая болезнь; вакцина.
Похожие статьи
[Обнаружение энтеровируса 71 и вируса Коксаки А16 у детей с кистевидным, ящурным энтероколитом в Шанхае, 2002 г.].
Ян ZH, Zhu QR, Li XZ, Wang XH, Wang JS, Hu JY, Tang W, Cui AL. Ян ЧЖ и др. Чжунхуа Эр Кэ За Чжи. 2005 сен;43(9)):648-52. Чжунхуа Эр Кэ За Чжи. 2005. PMID: 16191294 Китайский язык.

Характеристика тяжелой болезни рук, ящура и рта в Шэньчжэне, Китай, 2009–2013 гг.
Хуан И, Чжоу И, Лу Х, Ян Х, Фэн Ц, Дай Ю, Чен Л, Ю С, Яо Х, Чжан Х, Цзян М, Ван И, Хань Н, Ху Г, Хе Ю. Хуанг И и др. J Med Virol. 2015 сен; 87 (9): 1471-9. doi: 10.1002/jmv.24200. Epub 2015 7 мая. J Med Virol. 2015. PMID: 25951788
Генотипы энтеровируса, вызывающего ящур и ротовую болезнь в Шанхае, Китай, 2012-2013 гг.
Сюй М., Су Л., Цао Л., Чжун Х., Донг Н., Донг З., Сюй Дж. Сюй М. и др. ПЛОС Один. 2015 23 сентября; 10 (9): e0138514. doi: 10.1371/journal.pone.0138514. Электронная коллекция 2015. ПЛОС Один. 2015. PMID: 26398767 Бесплатная статья ЧВК.
Вирус Коксаки А16: эпидемиология, диагностика и вакцина.

Мао Цюй, Ван Ю, Яо Х, Бянь Л, Ву Х, Сюй М, Лян З. Мао Кью и др. Hum Вакцина Иммунотер. 2014;10(2):360-7. doi: 10.4161/hv.27087. Epub 2013 14 ноября. Hum Вакцина Иммунотер. 2014. PMID: 24231751 Бесплатная статья ЧВК. Обзор.
Болезнь рук, ящура (HFMD): новая эпидемиология и необходимость стратегии вакцинации.
Асватирадж С., Арункумар Г., Алиджину Э.К., Хобер Д. Асватирадж С. и др. Мед Микробиол Иммунол. 2016 Октябрь; 205 (5): 397-407. doi: 10.1007/s00430-016-0465-y. Epub 2016 12 июля. Мед Микробиол Иммунол. 2016. PMID: 27406374 Обзор.
Посмотреть все похожие статьи
Цитируется
Серораспространенность инфекции вирусом Коксаки А6 и энтеровирусом А71 у людей: систематический обзор и метаанализ.

Ши Ю, Чен П, Бай Ю, Сюй С, Лю Ю. Ши Ю и др. Арх Вирол. 2023 7 января; 168 (2): 37. doi: 10.1007/s00705-022-05642-0. Арх Вирол. 2023. PMID: 36609748 Бесплатная статья ЧВК. Обзор.
Эпидемиологические и этиологические характеристики легкой формы ящура у детей в возрасте до 7 лет, Нанкин, Китай, 2010–2019 гг.
Ван Дж., Дин С., Се В., Ван Т., Цинь Й., Чжэн Дж., Ян С., Чжао Х., Пэн З., Ма Т. Ван Дж. и др. Арка общественного здравоохранения. 2022 8 октября; 80 (1): 220. дои: 10.1186/s13690-022-00974-4. Арка общественного здравоохранения. 2022. PMID: 36209145 Бесплатная статья ЧВК.
Молекулярная эпидемиология и клинические особенности ящура, требующие госпитализации после применения инактивированной вакцины против энтеровируса A71 в Чэнду, Китай, 2017-2022 гг.
 : описательное исследование.
: описательное исследование.Дуань Х, Чжан С, Ван Х, Рен Х, Пэн Х, Тан Х, Чжан Л, Чен З, Е И, Чжэн М, Чжун В, Чен Х, Цзэн И, Юань П, Лонг Л. Дуан Х и др. Новые микробы заражают. 2022 Декабрь;11(1):2510-2519. дои: 10.1080/22221751.2022.2125346. Новые микробы заражают. 2022. PMID: 36103331 Бесплатная статья ЧВК.
Вспышка инфекции вирусом Коксаки А6 среди взрослых коллективной единицы, Китай, 2019 г.
Гао И, Ма Г, Сяо И, Цай Ц, Чен И, Ши П, Ван К, Шен И, Ши С. Гао Ю и др. Может ли J заразить Dis Med Microbiol. 2022 27 августа; 2022:6607294. дои: 10.1155/2022/6607294. Электронная коллекция 2022. Может ли J заразить Dis Med Microbiol. 2022. PMID: 36065442 Бесплатная статья ЧВК.
Криоэлектронная микроскопия и классификация изображений выявили существование и структуру вириона вируса Коксаки A6.

Бюттнер К.Р., Спурны Р., Фузик Т., Плевка П. Бюттнер С.Р. и соавт. коммун биол. 2022 сен 2; 5 (1): 898. doi: 10.1038/s42003-022-03863-2. коммун биол. 2022. PMID: 36056184 Бесплатная статья ЧВК.
Просмотреть все статьи «Цитируется по»
Типы публикаций
термины MeSH
Комментарий к «Случаю инфекции рекомбинантным вирусом Коксаки А2 с неврологическими осложнениями на Тайване»
Комментарий к «Случаю инфекции рекомбинантным вирусом Коксаки А2 с неврологическими осложнениями на Тайване»
Као-Пин Хван 1* , Тин-Ю Йен 1
1 Отделение инфекционных заболеваний, Детская больница, Китайский медицинский университет, Медицинский факультет, Тайчжун, Тайвань
Энтеровирусы (ЭВ) являются преобладающими возбудителями большинства детских болезней.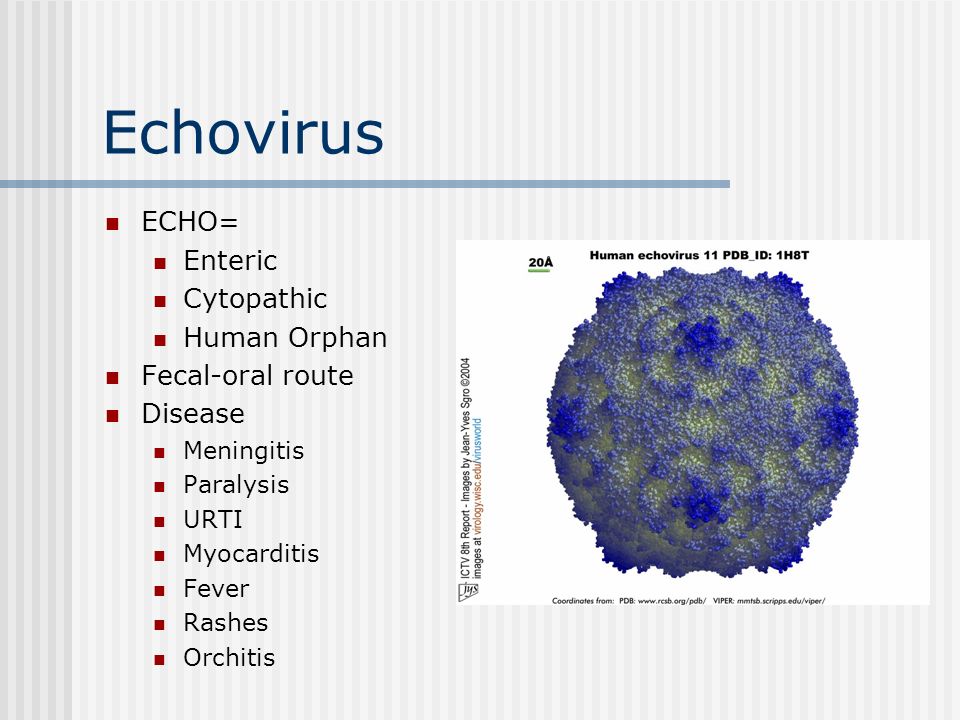 Существует более ста серотипов ЭВ, принадлежащих к роду Enterovirus, семейству Picornaviridae 1 . Эти вирусы первоначально были классифицированы как полиовирусы, вирус Коксаки А (CV-As), вирус Коксаки В и эховирусы на основании различий в клеточном тропизме, инфекционности, антигенности и патогенности 2 . Совсем недавно эти вирусы были повторно классифицированы на четыре вида (EV-A, EV-B, EV-C и EV-D) на основе их молекулярных и биологических свойств 3,4 . Геном РНК с положительной цепью EV имеет примерно 7500 пар оснований и включает три геномных региона (P1, P2 и P3). Область P1 кодирует четыре структурных капсидных белка (от VP1 до VP4), тогда как области P2 и P3 кодируют семь неструктурных белков (от 2A до 2C и от 3A до 3D). Капсидный белок VP1 содержит ряд антигенных сайтов нейтрализации, которые используются при серотипировании вируса 9.0009 5 . Сообщалось, что энтеровирус EV-A71 вызывает серьезные осложнения со стороны центральной нервной системы, включая энцефалит, менингит и полиомиелит, и в последние десятилетия во всем мире было зарегистрировано несколько крупных вспышек EV-A71 6-8 .
Существует более ста серотипов ЭВ, принадлежащих к роду Enterovirus, семейству Picornaviridae 1 . Эти вирусы первоначально были классифицированы как полиовирусы, вирус Коксаки А (CV-As), вирус Коксаки В и эховирусы на основании различий в клеточном тропизме, инфекционности, антигенности и патогенности 2 . Совсем недавно эти вирусы были повторно классифицированы на четыре вида (EV-A, EV-B, EV-C и EV-D) на основе их молекулярных и биологических свойств 3,4 . Геном РНК с положительной цепью EV имеет примерно 7500 пар оснований и включает три геномных региона (P1, P2 и P3). Область P1 кодирует четыре структурных капсидных белка (от VP1 до VP4), тогда как области P2 и P3 кодируют семь неструктурных белков (от 2A до 2C и от 3A до 3D). Капсидный белок VP1 содержит ряд антигенных сайтов нейтрализации, которые используются при серотипировании вируса 9.0009 5 . Сообщалось, что энтеровирус EV-A71 вызывает серьезные осложнения со стороны центральной нервной системы, включая энцефалит, менингит и полиомиелит, и в последние десятилетия во всем мире было зарегистрировано несколько крупных вспышек EV-A71 6-8 . Однако имеются ограниченные данные о совместно циркулирующих штаммах EV-A, отличных от EV-A71, которые, как известно, вызывают вспышки 9,10 .
Однако имеются ограниченные данные о совместно циркулирующих штаммах EV-A, отличных от EV-A71, которые, как известно, вызывают вспышки 9,10 .
Вирусы Коксаки подразделяются на группы А и В на основании патогенности для мышей-сосунков в возрасте до 48 часов (группа А вызывает вялый паралич, а группа В вызывает спастический паралич) 11 . Основываясь на прошлом опыте, заражение человека CV-A обычно протекает в легкой форме, за исключением CV-A16. Имеется несколько подробных отчетов, описывающих клинические особенности вируса Коксаки А2 (CV-A2). Ранее считалось, что CV-A2 вызывает спорадические инфекции с доброкачественными клиническими проявлениями, такие как герпетическая ангина, и были сообщения об эндемичных эпизодах CV-A2 на Тайване в период с 2003 по 2005 год 12 . В 2008 г. сообщалось, что эпидемия CV-A2 вызвала герпетическую ангину и болезнь рук, ящура и рта (HFMD) среди тайваньских детей 9 .0009 13-14 , в том числе у двух детей с осложнениями энцефалита и энцефаломиелита, выздоровевших без каких-либо последствий13.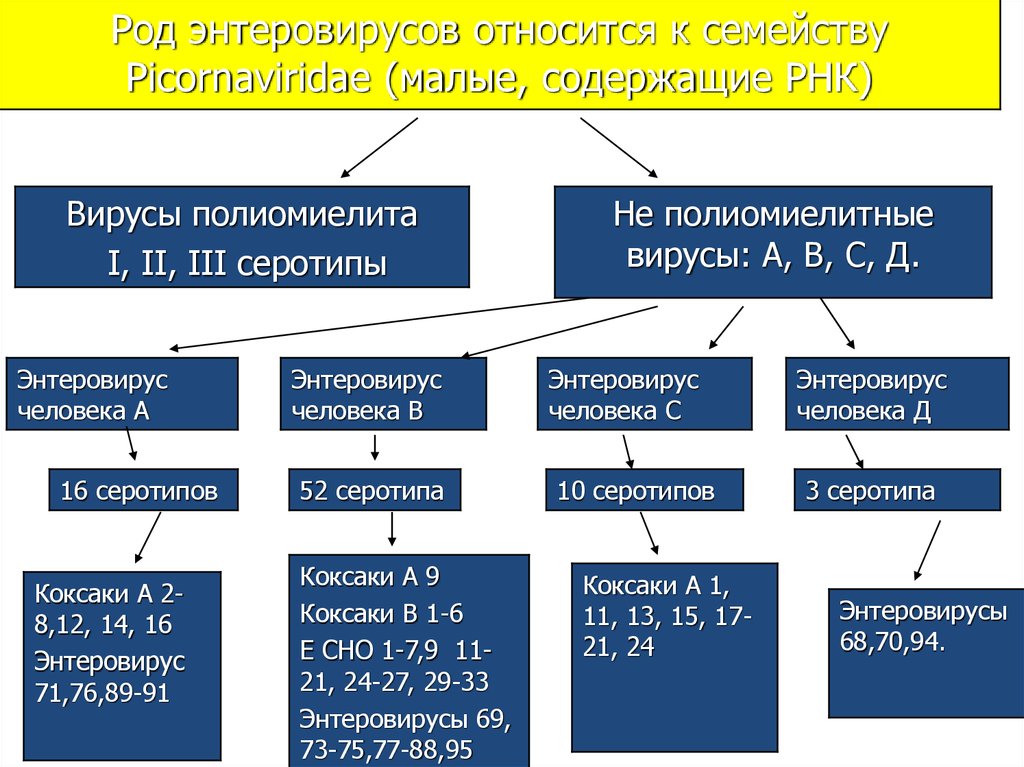 Более того, природный рекомбинантный CV-A2 был обнаружен в Гонконге у четырех детей с респираторными симптомами, двое из которых умерли летом 2012 г. 15 . Ранее мы сообщали о случае 9-месячной девочки с рекомбинантной инфекцией CV-A2, у которой развилась герпетическая ангина с энцефаломиелитом без отдаленных последствий 16 . Считалось, что этот штамм вируса тесно связан с гонконгским штаммом 2012 года из-за высокой степени генетического сходства между двумя штаммами. Насколько нам известно, это был первый случай, продемонстрировавший, что рекомбинантный штамм CV-A2 может поражать центральную нервную систему.
Более того, природный рекомбинантный CV-A2 был обнаружен в Гонконге у четырех детей с респираторными симптомами, двое из которых умерли летом 2012 г. 15 . Ранее мы сообщали о случае 9-месячной девочки с рекомбинантной инфекцией CV-A2, у которой развилась герпетическая ангина с энцефаломиелитом без отдаленных последствий 16 . Считалось, что этот штамм вируса тесно связан с гонконгским штаммом 2012 года из-за высокой степени генетического сходства между двумя штаммами. Насколько нам известно, это был первый случай, продемонстрировавший, что рекомбинантный штамм CV-A2 может поражать центральную нервную систему.
Ранее сообщалось, что во время вспышки CV-A2 в 2008 г. на Тайване у большинства пациентов с инфекцией CV-A2 была герпетическая ангина (84–94%), за которой следовала HFMD, в то время как у более молодых пациентов в основном проявлялись респираторные симптомы 13,14 . Фебрильные судороги значительно чаще встречались у пациентов с инфекциями CV-A2 (8,7%) по сравнению с общей популяцией 14 . Несмотря на редкость, инфекция CV-A2 может осложняться энцефалитом и энцефаломиелитом (1,1%) без долгосрочных последствий 13 . Кроме того, в Корее была зарегистрирована инфекция CV-A2 с поперечным миелитом, 2014 17 , а в редких случаях у пациентов была герпетическая ангина с энцефаломиелитом. В предыдущем исследовании также сообщалось о вспышке острой кишечной инфекции, вызванной CV-A2, преимущественно в России в 2010 г. 18 . Основываясь на этих данных, важно иметь в виду, что CV-A2 может быть высококонтагиозным с большим разнообразием клинических проявлений, таких как герпетическая ангина, HFMD, респираторные или кишечные инфекции и даже неврологические осложнения.
Несмотря на редкость, инфекция CV-A2 может осложняться энцефалитом и энцефаломиелитом (1,1%) без долгосрочных последствий 13 . Кроме того, в Корее была зарегистрирована инфекция CV-A2 с поперечным миелитом, 2014 17 , а в редких случаях у пациентов была герпетическая ангина с энцефаломиелитом. В предыдущем исследовании также сообщалось о вспышке острой кишечной инфекции, вызванной CV-A2, преимущественно в России в 2010 г. 18 . Основываясь на этих данных, важно иметь в виду, что CV-A2 может быть высококонтагиозным с большим разнообразием клинических проявлений, таких как герпетическая ангина, HFMD, респираторные или кишечные инфекции и даже неврологические осложнения.
Предполагается, что CV-A2 был возможным патогеном в некоторых летальных случаях, включая 15-летнюю девочку в Германии, у которой была двойная инфекция CV-A2 и вируса гриппа B, и она умерла в 1969 году 19 . Полимеразная цепная реакция с обратной транскриптазой (RT-PCR) и инокуляция грудных мышей были использованы для обнаружения последовательности энтеровируса, напоминающей CV-A2, в кале и селезенке 10-летней девочки, которая внезапно умерла с посмертными признаками миокардита 20 . Эти данные свидетельствуют о причинно-следственной связи между CV-A2 и миокардитом. В 2012 г. Yip и соавт. выявили рекомбинантный CV-A2 у четырех детей раннего возраста с тяжелой инфекцией дыхательных путей, двое из которых умерли.0009 15 . Хотя невозможно было определить, был ли вирус причиной смерти, данные, тем не менее, свидетельствовали о сильной патогенной роли CV-A2.
Эти данные свидетельствуют о причинно-следственной связи между CV-A2 и миокардитом. В 2012 г. Yip и соавт. выявили рекомбинантный CV-A2 у четырех детей раннего возраста с тяжелой инфекцией дыхательных путей, двое из которых умерли.0009 15 . Хотя невозможно было определить, был ли вирус причиной смерти, данные, тем не менее, свидетельствовали о сильной патогенной роли CV-A2.
Молекулярно-эпидемиологические исследования показали, что циркуляция различных энтеровирусов во время вспышек способствует рекомбинации вирусов 21,22,23,24 , и это может играть важную роль в эволюции энтеровирусов. События рекомбинации были описаны ранее, особенно в некапсидной (P2 и P3) области энтеровирусов 15,25,26 . В 2011 году Ху и др. сообщили, что штаммы CV-A2 (A2SD09) и CV-A4 (A4SZ09) имели серотип-специфическую гомологию капсидных белков, но имели общие некапсидные последовательности друг с другом, а штамм A2SD09 сгруппирован с Монголией. штаммы, выделенные в 2003 г. 25 . Кроме того, было показано, что рекомбинантные штаммы CV-A2, вызвавшие смерть ребенка в Гонконге, кластеризуются со штаммом SAR/SHA66 субгенотипа B3 EV-A71 в области P2 и со штаммом CV-A4 SZ/CHN/09. в области P3, что указывает на возможные рекомбинационные события в этих областях. Эти исследования показали, что генетическая рекомбинация среди штаммов CV-A2 может быть обычным эволюционным событием. Ограниченное количество доступных полных современных последовательностей генома EV-A, наряду с частыми событиями вирусной рекомбинации, затрудняет подтверждение происхождения этих рекомбинантных изолятов CV-A2. Всестороннее наблюдение за штаммами энтеровируса А, особенно за штаммами CV-A, необходимо для расширения нашего понимания эволюции этих коциркулирующих вирусов.
25 . Кроме того, было показано, что рекомбинантные штаммы CV-A2, вызвавшие смерть ребенка в Гонконге, кластеризуются со штаммом SAR/SHA66 субгенотипа B3 EV-A71 в области P2 и со штаммом CV-A4 SZ/CHN/09. в области P3, что указывает на возможные рекомбинационные события в этих областях. Эти исследования показали, что генетическая рекомбинация среди штаммов CV-A2 может быть обычным эволюционным событием. Ограниченное количество доступных полных современных последовательностей генома EV-A, наряду с частыми событиями вирусной рекомбинации, затрудняет подтверждение происхождения этих рекомбинантных изолятов CV-A2. Всестороннее наблюдение за штаммами энтеровируса А, особенно за штаммами CV-A, необходимо для расширения нашего понимания эволюции этих коциркулирующих вирусов.
В заключение, случай, о котором сообщалось как о инфекции CV-A2 (E2014041), возможно, завезенной из Гонконга, вызвал герпетическую ангину и неврологические осложнения без последствий на Тайване в 2014 году 16 . Возможно, это первый случай, продемонстрировавший, что рекомбинантный штамм CV-A2 может осложнять поражение центральной нервной системы. Генетические данные показали, что это может быть особенно агрессивный и нейротропный штамм CV-A2. CV-A2 является преобладающим штаммом, вызывающим несколько эндемических и эпидемических вспышек на Тайване, и циркуляция этих вирусов во время вспышек может способствовать рекомбинации вируса и появлению вируса, вызывающего новые проявления болезни. Поэтому важно установить постоянный надзор за циркуляцией CV-A2 на основе современного секвенирования генома, чтобы контролировать молекулярную эпидемиологию таких вспышек и отслеживать возникающие события рекомбинации.
Возможно, это первый случай, продемонстрировавший, что рекомбинантный штамм CV-A2 может осложнять поражение центральной нервной системы. Генетические данные показали, что это может быть особенно агрессивный и нейротропный штамм CV-A2. CV-A2 является преобладающим штаммом, вызывающим несколько эндемических и эпидемических вспышек на Тайване, и циркуляция этих вирусов во время вспышек может способствовать рекомбинации вируса и появлению вируса, вызывающего новые проявления болезни. Поэтому важно установить постоянный надзор за циркуляцией CV-A2 на основе современного секвенирования генома, чтобы контролировать молекулярную эпидемиологию таких вспышек и отслеживать возникающие события рекомбинации.
Ссылки
- Oberste MS, Maher K, Nix WA, et al. Молекулярная идентификация 13 новых типов энтеровирусов, EV79-88, EV97 и EV100-101, представителей вида Human Enterovirus B. Virus Res. 2007 г.; 128(1-2): 34-42.
- Мельник Дж.Л. Вирусология Филдса. 3-е изд. Филадельфия, Пенсильвания: Липпинкотт-Рейвен; 1996.

- Hyypiä T, Hovi T, Knowles NJ, et al. Классификация энтеровирусов на основе молекулярных и биологических свойств. Джей Ген Вирол. 1997 год; 78(1): 1-11.
- Оберсте М.С., Махер К., Мишель С.М. и др. Энтеровирусы 76, 89, 90 и 91 представляют собой новую группу внутри вида Энтеровирус человека A. J Gen Virol. 2005 г.; 86(2): 445-51.
- Никс В.А., Оберсте М.С., Палланш М.А. Чувствительная полувложенная ПЦР-амплификация последовательностей VP1 для прямой идентификации всех серотипов энтеровирусов из исходных клинических образцов. Дж. Клин Микробиол. 2006 г.; 44(8): 2698-704.
- Надь Г., Такаци С., Кукан Э. и др. Вирусологическая диагностика энтеровирусных инфекций типа 71: опыт эпидемии острых заболеваний ЦНС в Венгрии в 1919 г.78. Арх Вирол. 1982 год; 71(3): 217-27.
- Чан Л.Г., Парашар У.Д., Лай М.С. и др. Смертность детей во время вспышки ящура в Сараваке, Малайзия: клинико-патологические характеристики болезни. Для Исследовательской группы по вспышкам.
 Клин Инфекция Дис. 2000 г.; 31(3): 678-83.
Клин Инфекция Дис. 2000 г.; 31(3): 678-83. - Хо М., Чен Э.Р., Хсу К.Х. и др. Эпидемия энтеровирусной инфекции 71 на Тайване. Тайваньская рабочая группа по эпидемии энтеровируса. N Engl J Med. 1999 г.; 341(13): 929-35.
- Блумквист С., Клемола П., Кайджалайнен С. и др. Совместная циркуляция вирусов Коксаки А6 и А10 при вспышке ящура в Финляндии. Джей Клин Вирол. 2010 г.; 48(1): 49-54.
- Lu QB, Zhang XA, Wo Y и др. Циркуляция вируса Коксаки A10 и A6 при ладонно-ногтевой болезни в Китае, 2009-2011 гг. ПЛОС Один. 2012 г.; 7(12): e52073.
- Хююпиа Т., Каллайоки М., Мааронен М. и др. Патогенетические различия между вирусными инфекциями Коксаки А и В у новорожденных мышей. Вирус рез. 1993 января; 27(1): 71-8.
- Tseng FC, Huang HC, Chi CY и др. Эпидемиологическое исследование энтеровирусных инфекций, произошедших на Тайване в период с 2000 по 2005 год: анализ данных дозорного врачебного надзора. J Med Virol. 2007 г.; 79(12): 1850-60.
- Chen SP, Huang YC, Li WC, et al.
 Сравнение клинических признаков вируса Коксаки А2 и энтеровируса 71 во время вспышки энтеровируса на Тайване в 2008 г.: опыт детской больницы. J Microbiol Immunol Infect. 2010 г.; 43(2): 99-104.
Сравнение клинических признаков вируса Коксаки А2 и энтеровируса 71 во время вспышки энтеровируса на Тайване в 2008 г.: опыт детской больницы. J Microbiol Immunol Infect. 2010 г.; 43(2): 99-104. - Ли М.Х., Хуанг Л.М., Вонг В.В. и др. Молекулярная диагностика и клинические проявления энтеровирусных инфекций в Тайбэе во время эпидемии 2008 г. J Microbiol Immunol Infect. 2011 г.; 44(3): 178-83.
- Yip CC, Lau SK, Woo PC и др. Рекомбинантный вирус Коксаки А2 и детская смертность, Гонконг, 2012 г. Emerg Infect Dis. 2013 авг.; 19(8): 1285-8.
- Йен Т.И., Хуан Ю.П., Хсу Ю.Л. и др. Случай заражения рекомбинантным вирусом Коксаки А2 с неврологическими осложнениями на Тайване. J Microbiol Immunol Infect. 2016 декабрь; 18(16)30148-7. doi: 10.1016/j.jmii.2016.08.012.
- Ким Х., Кан Б., Хван С. и др. Клинические и энтеровирусные данные, связанные с острым вялым параличом в Республике Корея за последнее десятилетие. J Med Virol. 2014; 86(9): 1584-9.
- Демина А.
 В., г. Терново? В.А., Дарижапов Б.Б., и соавт. Вспышка острой энтеровирусной кишечной инфекции в Сахалинской области в августе 2010 г. // Вестн Росс акад мед наук. 2012 г.; (2): 64-8.
В., г. Терново? В.А., Дарижапов Б.Б., и соавт. Вспышка острой энтеровирусной кишечной инфекции в Сахалинской области в августе 2010 г. // Вестн Росс акад мед наук. 2012 г.; (2): 64-8. - Adamczyk B, Klier G, Deicke P. Летальная двойная инфекция вирусом Коксаки A2 и вирусом гриппа B у 15-летней девочки. Z Gesamte Inn Med. 1969; 24(24): 917-21.
- Bendig JW, O’Brien PS, Muir P, et al. Последовательности энтеровируса, напоминающие вирус Коксаки А2, обнаружены в кале и селезенке девочки с фатальным миокардитом. J Med Virol. 2001 г.; 64(4): 482-6.
- Huang SC, Hsu YW, Wang HC, et al. Появление внутритиповой рекомбинации энтеровируса 71 на Тайване с 2002 по 2005 гг. Virus Res. 2008 г.; 131(2): 250-9.
- Jegouic S, Joffret ML, Blanchard C, et al. Рекомбинация между полиовирусами и коциркулирующими вирусами Коксаки А: роль в появлении патогенных полиовирусов вакцинного происхождения. PLoS Патог. 2009 г.Может; 5 (5): e1000412.
- Оприсан Г., Комбеску М.






 : описательное исследование.
: описательное исследование.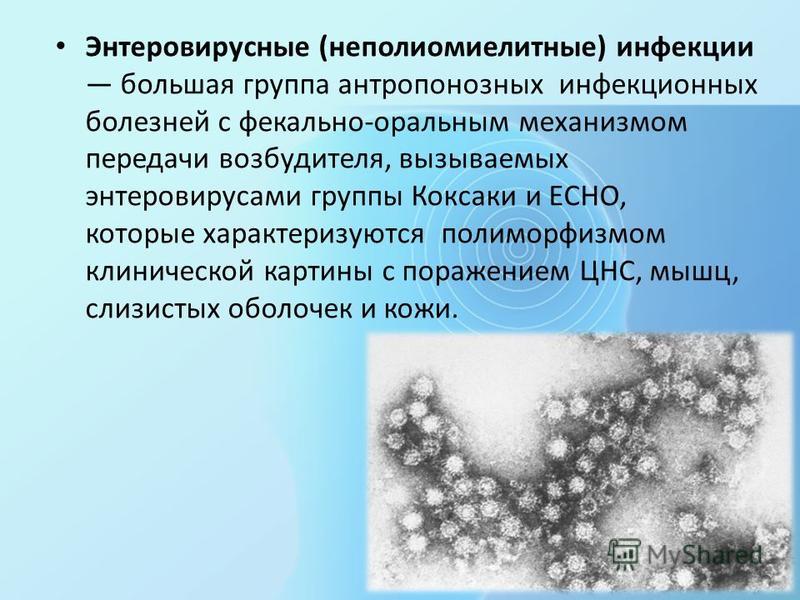

 Клин Инфекция Дис. 2000 г.; 31(3): 678-83.
Клин Инфекция Дис. 2000 г.; 31(3): 678-83. Сравнение клинических признаков вируса Коксаки А2 и энтеровируса 71 во время вспышки энтеровируса на Тайване в 2008 г.: опыт детской больницы. J Microbiol Immunol Infect. 2010 г.; 43(2): 99-104.
Сравнение клинических признаков вируса Коксаки А2 и энтеровируса 71 во время вспышки энтеровируса на Тайване в 2008 г.: опыт детской больницы. J Microbiol Immunol Infect. 2010 г.; 43(2): 99-104. В., г. Терново? В.А., Дарижапов Б.Б., и соавт. Вспышка острой энтеровирусной кишечной инфекции в Сахалинской области в августе 2010 г. // Вестн Росс акад мед наук. 2012 г.; (2): 64-8.
В., г. Терново? В.А., Дарижапов Б.Б., и соавт. Вспышка острой энтеровирусной кишечной инфекции в Сахалинской области в августе 2010 г. // Вестн Росс акад мед наук. 2012 г.; (2): 64-8.