Вакцина против туберкулёза — БЦЖ, когда и сколько раз делают прививку
Автор: врач, научный директор АО «Видаль Рус», Жучкова Т. В., t.zhutchkova@vidal.ru
БЦЖ – это вакцина против туберкулёза, приготовленная из штамма ослабленной живой туберкулёзной палочки, Mycobacterium bovis BCG. Вакцина была разработана французскими учеными Calmette и Guerin в 1919 году. С середины 1950-х годов в большинстве европейских стран вакцинация новорождённых стала обязательной.
Туберкулез является одной из наиболее опасных инфекций. Его распространеноть в разных стрнах знaчительно отличается. К сожаленю, в условиях России, ребенок не застрахован от встречи с этой инфекцией на улице, в поликлинике и даже дома. Именно поэтому вакцинацию против туберкулеза проводят уже в родильном доме на 3-7 сутки жизни. Доказано что чем раньше иммунная система организма познакомится с возбудителем туберкулеза, тем эффективнее будет ее ответ в случае контакта с инфекционным агентом.
В ряде случаев проведение вакцинации в родильном доме может быть противопоказано. Перед тем, как давать согласие на выполнение прививки следует обязательно проконсультироваться с неонатологом. Дети, не привитые в родильном отделении при отсутствии противопоказаний првиваются в детских поликлиниках в течение первых 2-х месяцев жизни. Детям старше 2-х месячного возраста, перед вакцинацией необходимо провести пробу Манту. Вакцина БЦЖ-М содержит меньшее количество бактерий и испольуется для щадящей первичной иммунизации при наличии противопоказаний к введению БЦЖ.
Иммунитет, приобретенный после прививки БЦЖ, сохраняется в среднем 5 лет. Для поддержания приобретенного иммунитета повторные вакцинации (ревакцинации) проводятся в 7 и 14 лет. Следует помнить, что ревакцинация БЦЖ проводится через 4 недели после других профилактических прививок, а после проведенной вакцинации БЦЖ другие профилактические прививки проводятся не ранее, чем через 2 месяцa.
Противопоказанием к ревакцинации БЦЖ служит: инфицированность микобактерией туберкулеза, перенесенный туберкулез, положительная или сомнительная реакция Манту, осложненные реакции на предыдущее введение вакцины БЦЖ или БЦЖ-М, заболевания крови, злокачественные новообразования, иммунодефицитные состояния, беременность.
Временные противопоказания включают: aллергические болезни в стадии обострения, острые заболевания и хронические болезни в стадии обострения (вакцинацию проводят через 1 месяц после выздоровления, ремиссии).
Осложнения после БЦЖ и других вакцин
Недавно был такой случай: привели ребенка, у которого все группы лимфоузлов были воспалены. Началось все с подмышечных узлов, родители обратили внимание — сделали УЗИ, на снимке был небольшой узел. До 1 см мы ничего не трогаем, просто наблюдаем. Постепенно ребенок стал слабым, началось увеличение лимфоузлов — надключишных и подключишных. Обратились в поликлинику — к хирургу, онкологу, сделали биопсию, когда ему уже было около года. Там, естественно, уже клетки Пирогова-Лангханса (признак инфекционно-воспалительного процесса — прим. V), и тогда, наконец, обратились к нам. Но здесь уже было упущено время, потому что у поствакцинальных осложнений тоже есть стадии. Первая стадия, инфильтрация, — скопление гноя. Но когда место уже уплотняется, то в какой-то момент может смягчиться и затем прорваться. Поэтому важно не упустить этот момент, когда увеличивается лимфоузел. Так вот, когда ребенок поступил к нам, к сожалению, мы пропустили этап, когда все можно было исправить консервативным лечением — уже требовалась операция. К счастью, в нашем научном центре есть хороший внелегочный специалист, который аккуратно удалил этот лимфатический узел, затем назначили химиопрофилактическое лечение.
Началось все с подмышечных узлов, родители обратили внимание — сделали УЗИ, на снимке был небольшой узел. До 1 см мы ничего не трогаем, просто наблюдаем. Постепенно ребенок стал слабым, началось увеличение лимфоузлов — надключишных и подключишных. Обратились в поликлинику — к хирургу, онкологу, сделали биопсию, когда ему уже было около года. Там, естественно, уже клетки Пирогова-Лангханса (признак инфекционно-воспалительного процесса — прим. V), и тогда, наконец, обратились к нам. Но здесь уже было упущено время, потому что у поствакцинальных осложнений тоже есть стадии. Первая стадия, инфильтрация, — скопление гноя. Но когда место уже уплотняется, то в какой-то момент может смягчиться и затем прорваться. Поэтому важно не упустить этот момент, когда увеличивается лимфоузел. Так вот, когда ребенок поступил к нам, к сожалению, мы пропустили этап, когда все можно было исправить консервативным лечением — уже требовалась операция. К счастью, в нашем научном центре есть хороший внелегочный специалист, который аккуратно удалил этот лимфатический узел, затем назначили химиопрофилактическое лечение.
В Казахстане в 2021 году используется БЦЖ-вакцина индийского производителя Serum Institute of India Pvt.Ltd. Инструкция к вакцине опубликована на сайте Национального центра экспертизы лекарственных средств и медицинских изделий.
Вакцина прошла преквалификацию ВОЗ и соответствует требованиям Всемирной организации здравоохранения. К такому подходу в выборе производителей вакцин пришли в Казахстане, к сожалению, не сразу. В 2003-2004 годах казахстанских малышей прививали сербской вакциной БЦЖ. Из 214 000 привитых детей у 1067 развился поствакцинальный лимфаденит. Это достаточно высокий показатель осложнений даже для БЦЖ-вакцины. Из-за количества осложнений вакцина была отозвана и на несколько месяцев казахстанские дети остались без возможности получить какую-либо защиту от туберкулёза. Представители Минздрава до сих пор не очень охотно комментируют эту тему. В ответ на наши вопросы о сербской вакцине; детях, получивших осложнения, и о том, какая работа над ошибками была проделана, мы получили такой ответ:
К такому подходу в выборе производителей вакцин пришли в Казахстане, к сожалению, не сразу. В 2003-2004 годах казахстанских малышей прививали сербской вакциной БЦЖ. Из 214 000 привитых детей у 1067 развился поствакцинальный лимфаденит. Это достаточно высокий показатель осложнений даже для БЦЖ-вакцины. Из-за количества осложнений вакцина была отозвана и на несколько месяцев казахстанские дети остались без возможности получить какую-либо защиту от туберкулёза. Представители Минздрава до сих пор не очень охотно комментируют эту тему. В ответ на наши вопросы о сербской вакцине; детях, получивших осложнения, и о том, какая работа над ошибками была проделана, мы получили такой ответ:
«Дети, привитые вакциной сербского производства, наблюдались в течение 1 года, проходили оздоровление в условиях детских санаториев, получали необходимое лечение. В настоящее время в стране проводится закуп вакцины, зарегистрированной и сертифицированной ВОЗ».
По официальным данным 2020 года, процент неблагоприятных последствий после иммунизации (НППИ) у новорожденных детей не превышал 0,027%. Но еще годом ранее, в 2019, он достигал 0,037%. В это время, как и в предыдущие годы, в Казахстане использовалась вакцина Japan BCG Laboratory. В 2019 году производитель отзывал эту вакцину, и в течение месяца в Казахстане была приостановлена вакцинация против туберкулёза. Об этом мы писали в нашем материале «Covid-19 и плановая вакцинация».
Но еще годом ранее, в 2019, он достигал 0,037%. В это время, как и в предыдущие годы, в Казахстане использовалась вакцина Japan BCG Laboratory. В 2019 году производитель отзывал эту вакцину, и в течение месяца в Казахстане была приостановлена вакцинация против туберкулёза. Об этом мы писали в нашем материале «Covid-19 и плановая вакцинация».
Также в течение нескольких последних лет в практике педиатров, работающих с новорожденными, довольно часто встречались осложнения после БЦЖ. Об этом нам рассказала Марина Фаридовна Тараруева — педиатр и детский невропатолог с 30-летним опытом.
Вакцинация от туберкулеза детям в Москве
Не менее трети людей, проживающих на планете, являются носителями микобактерии туберкулеза, однако болезнь развивается только у 5-10% инфицированных. Снизить заболеваемость помогает только вакцинация от туберкулеза детям, поскольку меры по раннему выявлению инфекции не дают должного эффекта для ребенка. При снижении иммунитета, неправильном питании, неудовлетворительной санитарной обстановке спящая бактерия может начать активно размножаться и провоцировать туберкулез, поэтому это заболевание считается социальным.
От заболевания туберкулезом не застрахован никто – прививки рекомендуется делать каждому ребенку независимо от того, в какой социальной обстановке он проживает. БЦЖ не предохраняет от заражения микобактерией, поскольку в современных условиях это невозможно, однако эта вакцина дает два важных результата:
- ослабляет тяжесть течения болезни;
- исключает вероятность менингита и диссеминированных форм туберкулеза, которые практически всегда заканчиваются летальным исходом.
БЦЖ (калька с латинских букв BCG — bacillus Calmette–Guerin) – вакцина против туберкулеза, приготовленная из штамма коровьей туберкулезной палочки, которая утратила вирулентность для человека. В мире приготавливается огромное количество типов вакцин БЦЖ, но в 90% случаев они содержат один из трех штаммов – «Пастеровский», «Глаксо» и Токийский. Их эффективность совершенно одинакова.
Когда и как делают вакцинацию?
В России вакцина БЦЖ применяется ко всем младенцам поголовно из-за неблагоприятной ситуации по туберкулезу (в развитых странах она делается только детям из группы риска). Она производится на 3-7 сутки уже в роддоме. 2/3 детей до 7 лет уже успевают инфицироваться бактерией туберкулеза, БЦЖ помогает не допустить развития тяжелых смертельных форм болезни. Ревакцинация проводится в 7 лет, после чего повторные вакцинации больше не требуются.
Она производится на 3-7 сутки уже в роддоме. 2/3 детей до 7 лет уже успевают инфицироваться бактерией туберкулеза, БЦЖ помогает не допустить развития тяжелых смертельных форм болезни. Ревакцинация проводится в 7 лет, после чего повторные вакцинации больше не требуются.
Для новорожденных примеряется БЦЖ или БЦЖ-м, более щадящий вариант, в котором лишь половина состава составляет микроорганизмы. Он применяется для слабых и недоношенных детей. Препарат вводится внутрикожно в плечо, между верхней и средней третью. Реакция формируется спустя 4-6 недель. На месте введения прививки образуется гнойничок, который покрывается коростой и заживает. После отпадении коросты на всю жизнь остается рубчик, который свидетельствует о поставленной прививке.
Совместно с БЦЖ запрещено вводить какие-либо прививки, это правило касается и периода 4-6 недель после нее. По этой причине младенцу сначала ставят прививку от гепатита В, которая дает реакции сразу (проходят через 3-5 суток). После БЦЖ у ребенка наступает период покоя до 3 месяцев.
Реакция на вакцину и противопоказания
Прививка не должна вызывать болезненных ощущений в первые дни после нее – реакции развиваются через некоторое время после введения. Чаще всего замечаются следующие нормальные и свидетельствующие о правильности усвоения прививки реакции:
- Покраснение – нормальная прививочная реакция, должно находиться в месте инъекции и не распространяться дальше.
- Нагноение и нарывы – нормальная прививочная реакция, прививка должна принять форму гнойничка с корочкой, красноты на данный момент быть не должно (в этом случае следует обратиться к врачу). Если ранка нагнаивается несколько раз, ставится диагноз БЦЖит.
- Место укола опухло – это происходит сразу после введения вакцины и продолжается максимум 2-3 дня. После этого место введения иглы должно стать обычным, не отличимым от других тканей рядом. Нагноение начинается только через 1,5 месяца.
- Зуд – эта реакция является нормальной, однако чесать место прививки не следует.

- Температура – редко появляется сразу после вакцинации, иногда может появиться при образовании гнойничка.
К противопоказаниям для применения вакцины относятся небольшая масса новорожденного, обострение хронических заболеваний, иммунодефицит, наличие ВИЧ у матери, положительная проба Манту, наличие лимфаденита или келоидного рубца после предыдущей вакцины и некоторые другие характеристики.
Прививка от туберкулеза | Областное бюджетное учреждение здравоохранения «Курская городская клиническая больница № 4»
Прививка от туберкулеза
Туберкулез еще 100 лет назад косил без разбора как миллионеров, так и бедняков. Но если вы думаете, что эта напасть осталась в далеком прошлом, то глубоко ошибаетесь. Туберкулез не только медицинская, но и социальная проблема.
С 1989 года в России отмечается ежегодный подъем заболеваемости туберкулезом, причем в первую очередь болезнь поражает детей. Защититься от нее можно одним-единственным способом – с помощью прививки. Более того – Всемирная организация здравоохранения включила Россию в число стран, где рекомендована обязательная вакцинация против туберкулеза.
Более того – Всемирная организация здравоохранения включила Россию в число стран, где рекомендована обязательная вакцинация против туберкулеза.
Туберкулез – хроническое инфекционное заболевание, возбудителем которого является микобактерия туберкулеза, или палочка Коха. Чаще всего инфекция поражает легкие, но не исключено и поражение глаз, костей, кожи, мочеполовой системы, кишечника и т.д. Передается инфекция воздушно-капельным путем, причем заразиться можно где угодно и для этого совсем не обязательно находиться в тесном контакте с заболевшим человеком.
Микобактерии очень устойчивы к влаге, теплу, свету, в уличной пыли они сохраняют жизнеспособность в течение 10 дней, на книжных страницах – целых 3 месяца, в воде – до 150 дней. При активной форме туберкулеза они быстро размножаются в легких больного и разрушают пораженный орган, отравляют организм человека продуктами своей жизнедеятельности – токсинами. Если болезнь не лечить, есть два варианта развития событий: летальный исход через 1-2 года или хронический туберкулез. Самые тяжелые формы туберкулеза возникают у новорожденных детей. Вместе с легкими поражается головной мозг, что приводит к развитию туберкулезного менингита – воспаления оболочек головного мозга.
Самые тяжелые формы туберкулеза возникают у новорожденных детей. Вместе с легкими поражается головной мозг, что приводит к развитию туберкулезного менингита – воспаления оболочек головного мозга.
Лечить туберкулез сложно, так как микобактерии мутируют и появляются формы, устойчивые даже к очень сильным антибиотикам.
Защита от туберкулеза
Надежным средством профилактики болезни является вакцинация. Вакцина против туберкулеза была создана в 1923 году французскими учеными – Кальметтом и Гереном. Отсюда и ее название — Bacillum CalmetteGuerin, BCG; в русской транскрипции — БЦЖ. Она способна предотвратить до 80% случаев тяжелой инфекции и надежно защищает от первичных форм туберкулеза, особенно от тяжелых – таких, как менингит, поражение костей, диагностировать которые и лечить труднее всего. Отказ от прививки чреват высоким риском заражения туберкулезом. Чтобы его избежать, придется раз и навсегда исключить любые контакты ребенка с больными туберкулезом, что практически невозможно сделать, живя в большом городе.
Первую прививку делают прямо в роддоме – она проходит на 3-7 сутки после рождения малыша. С 1 января 2008 года в соответствии с Приложением к приказу Минздравсоцразвития (так тогда называлось Министерство здравоохранения) от 30 октября 2007 года №673 новорожденным делают прививку от туберкулеза вакциной БЦЖ-М. Если в окружении малыша есть больные, вакцинация проводится вакциной БЦЖ.
Эти вакцины содержат живые ослабленные бычьи микобактерии. Вводятся они внутрикожно. В месте укола развивается местный туберкулезный процесс, совершенно неопасный для здоровья крохи.
Через 1,5-2 месяца после введения вакцины в месте прокола возникает небольшое уплотнение, напоминающее комариный укус. Оно может быть красноватым, синеватым, фиолетовым или даже почти черным. Это нормальная реакция организма на прививку БЦЖ, поэтому пугаться ее не нужно. Затем в центре уплотнения (внутри которого находится инфильтрат) формируется маленький прыщик с жидким содержимым. Главное – не трогать этот гнойник. Если из него течет сукровица или гной – следует промокать его ватным диском. Не давайте ребенку расчесывать это место и сдирать образовывающуюся там корочку. Старайтесь не мочить его и не трите мочалкой во время купания. Ранка должна зажить сама. Процесс заживления может длиться несколько месяцев, и в итоге на месте инъекции формируется небольшой, но заметный рубчик диаметром от 0,2 до 1 см. Появление рубца на плече – это следствие перенесенного туберкулезного процесса. Если рубец отсутствует, значит, основная цель вакцинации не достигнута – иммунитет к туберкулезу не сформировался.
Если из него течет сукровица или гной – следует промокать его ватным диском. Не давайте ребенку расчесывать это место и сдирать образовывающуюся там корочку. Старайтесь не мочить его и не трите мочалкой во время купания. Ранка должна зажить сама. Процесс заживления может длиться несколько месяцев, и в итоге на месте инъекции формируется небольшой, но заметный рубчик диаметром от 0,2 до 1 см. Появление рубца на плече – это следствие перенесенного туберкулезного процесса. Если рубец отсутствует, значит, основная цель вакцинации не достигнута – иммунитет к туберкулезу не сформировался.
В результате успешно прошедшей вакцинации организм вырабатывает защитные антитела против палочки Коха. Полноценный противотуберкулезный иммунитет формируется в течение года.
Другие прививки после введения вакцины БЦЖ можно делать только через месяц. Исключение – прививка против гепатита В, которую новорожденному делают за 3-4 дня до БЦЖ.
Противопоказания
Вакцинацию против туберкулеза не делают детям, в семьях которых есть случаи врожденного или приобретенного иммунодефицита, если у братьев или сестер отмечались осложнения после аналогичной прививки, и детям с тяжелыми наследственными заболеваниями или поражениями центральной нервной системы, например, при детском церебральном параличе или синдроме Дауна.
Прививка откладывается до выздоровления при любых ОРЗ и ОРВИ, инфекционных заболеваниях, при гемолитической болезни новорожденных (она развивается из-за несовместимости крови матери и малыша по резус-фактору или группе крови) и при глубокой степени недоношенности.
Осложнения после прививки БЦЖ
Вакцина БЦЖ – хоть и ослабленная, но все-таки живая. Потому возможные осложнения делятся на 2 большие группы: связанные с распространением инфекции и местные. Первые вызывают «неправильное» развитие туберкулезного процесса. Это обычно бывает в тех случаях, когда доктор не увидел существующих противопоказаний к прививке или его о них не проинформировали.
В одном случае из 200 тысяч привитых фиксируется такое осложнение как остеит, или туберкулез костей.
Вторые возникают, когда нарушается техника введения вакцины. В таких случаях месте инъекции может образоваться уплотнение более 1 мм в диаметре, инфильтрат образуется под кожей (должен на коже) и прощупывается под ней как «шарик». Это говорит о том, что вакцину ввели слишком глубоко. Нужно как можно быстрее обратиться к фтизиатру, чтобы содержимое «шарика» не прорвалось внутрь и не попало в кровь. После прививки могут увеличиться также подмышечные лимфоузлы, но при этом они остаются безболезненными. Мама чаще всего замечает это осложнение при купании малыша. В таком случае опять-таки нужна консультация фтизиатра.
Это говорит о том, что вакцину ввели слишком глубоко. Нужно как можно быстрее обратиться к фтизиатру, чтобы содержимое «шарика» не прорвалось внутрь и не попало в кровь. После прививки могут увеличиться также подмышечные лимфоузлы, но при этом они остаются безболезненными. Мама чаще всего замечает это осложнение при купании малыша. В таком случае опять-таки нужна консультация фтизиатра.
Ревакцинация
Иммунитет, приобретенный после прививки БЦЖ, сохраняется в среднем 5 лет. Чтобы поддержать его на должном уровне, рекомендуется пройти ревакцинацию в возрасте 7 и 14 лет. Но проводится она только туберкулиноотрицательным детям, организм которых даже несмотря на вакцинацию БЦЖ, не знаком с палочками Коха или успел уже о них забыть.
Выявить таких детей помогает проба Манту, которую проводят ежегодно. Ее принцип – введение в организм человека малых доз туберкулина – аллергена, полученного от палочки Коха, и наблюдении за реакцией. Если организм с инфекцией встречался, реакция будет бурной, проба – положительной. Через 72 часа после инъекции измеряют диаметр образовавшейся «пуговки» (папулы). В зависимости от его размера и делаются соответствующие выводы. Но надо учитывать, что возможны ложноположительные и ложноотрицательные результаты. Более совершенной пробой является диаскинтест.
Через 72 часа после инъекции измеряют диаметр образовавшейся «пуговки» (папулы). В зависимости от его размера и делаются соответствующие выводы. Но надо учитывать, что возможны ложноположительные и ложноотрицательные результаты. Более совершенной пробой является диаскинтест.
Первая проба Манту предстоит ребенку в 1 год, далее – ежегодно. При отрицательной пробе вакцинацию проводят не позднее, чем через 2 недели после проведения пробы. С рождения до 2 месяцев прививку против туберкулеза делают без предварительной пробы Манту.
Важно помнить, что проба Манту не прививка. Если ребенок по каким-то показаниям освобожден от профилактических прививок, это не значит, что ему нельзя делать пробу Манту. Если же у вас есть опасения по этому поводу, доктор может рекомендовать диаскинтест.
Вакцина туберкулезная (БЦЖ) (Vaccinum tuberculosis (BCG))
Вакцину
БЦЖ применяют внутрикожно в дозе 0,05 мг в объеме 0,1 мл растворителя
(натрия хлорид растворитель для приготовления лекарственных форм для инъекций
0,9%).
Первичную вакцинацию осуществляют здоровым новорожденным детям на 3–7 день жизни (как правило, в день выписки из родильного дома).
Дети, не привитые в период новорожденности, вследствие заболеваний, получают после выздоровления вакцину БЦЖ‑М. Детям в возрасте 2 месяца и старше предварительно проводят пробу Манту 2 ТЕ очищенного туберкулина в стандартном разведении и вакцинируют только туберкулинотрицательных.
Ревакцинации подлежат дети в возрасте 7 лет, имеющие отрицательную реакцию на пробу Манту с 2 ТЕ ППД‑Л. Реакция Манту считается отрицательной при полном отсутствии инфильтрата, гиперемии или при наличии уколочной реакции (1 мм). Инфицированные микобактериями туберкулеза дети, имеющие отрицательную реакцию на пробу Манту, ревакцинации не подлежат. Интервал между постановкой пробы Манту и ревакцинацией должен быть не менее 3 дней и не более 2 недель.
Прививки должен
проводить специально обученный медицинский персонал родильных домов
(отделений), отделений выхаживания недоношенных, детских поликлиник или
фельдшерско-акушерских пунктов. Вакцинацию новорожденных проводят в утренние
часы в специально отведенной комнате после осмотра детей педиатром. В
поликлиниках отбор детей на вакцинацию предварительно проводит врач (фельдшер)
с обязательной термометрией в день прививки, учетом медицинских
противопоказаний и данных анамнеза. При необходимости проводят консультацию с
врачами-специалистами, исследование крови и мочи. При проведении ревакцинации в
школах должны соблюдаться все вышеперечисленные требования. Во избежание
контаминации живыми микобактериями БЦЖ недопустимо совмещение в один день прививки
против туберкулеза с другими парентеральными манипуляциями.
Вакцинацию новорожденных проводят в утренние
часы в специально отведенной комнате после осмотра детей педиатром. В
поликлиниках отбор детей на вакцинацию предварительно проводит врач (фельдшер)
с обязательной термометрией в день прививки, учетом медицинских
противопоказаний и данных анамнеза. При необходимости проводят консультацию с
врачами-специалистами, исследование крови и мочи. При проведении ревакцинации в
школах должны соблюдаться все вышеперечисленные требования. Во избежание
контаминации живыми микобактериями БЦЖ недопустимо совмещение в один день прививки
против туберкулеза с другими парентеральными манипуляциями.
Факт выполнения вакцинации (ревакцинации) регистрируют в установленных учетных формах с указанием даты прививки, названия вакцины, предприятия-производителя, номера серии и срока годности препарата.
Вакцину
растворяют непосредственно перед применением стерильным растворителем,
приложенным к вакцине. Растворитель должен быть прозрачным, бесцветным и не
иметь посторонних включений.
Растворитель должен быть прозрачным, бесцветным и не
иметь посторонних включений.
Шейку и головку ампулы обтирают спиртом. Вакцина запаяна под вакуумом, поэтому сначала надпиливают и осторожно, с помощью пинцета, отламывают место запайки. Затем надпиливают и отламывают шейку ампулы, завернув надпиленный конец в стерильную марлевую салфетку.
Для получения
дозы 0,05 мг БЦЖ в 0,1 мл растворителя в ампулу, содержащую
10 доз вакцины, переносят стерильным шприцем 1 мл натрия хлорида
растворителя для приготовления лекарственных форм для инъекций 0,9%. Вакцина
должна раствориться в течение 1 мин. Допускается наличие хлопьев, которые
должны разбиваться при 3–4‑кратном аккуратном взбалтывании и
перемешивании содержимого путем забора обратно в шприц. Растворенная вакцина
имеет вид грубодисперсной суспензии белого с сероватым или желтоватым оттенком
цвета, без посторонних включений. При наличии в разведенном препарате крупных
хлопьев, которые не разбиваются при 4‑кратном перемешивании шприцем, или
осадка вакцину не используют, ампулу уничтожают.
Разведенную вакцину необходимо предохранять от действия солнечного и дневного света (например, цилиндром из черной бумаги) и использовать сразу после разведения. Разведенная вакцина пригодна к применению не более 1 часа при хранении в асептических условиях при температуре от 2 до 8 °C. Обязательно ведение протокола с указанием времени разведения и уничтожения ампулы с вакциной.
Для одной прививки туберкулиновым шприцем набирают 0,2 мл (2 дозы) разведенной вакцины, затем выпускают через иглу в стерильный ватный тампон около 0,1 мл вакцины для того, чтобы вытеснить воздух и подвести поршень шприца под нужную градуировку — 0,1 мл. Перед каждым набором вакцину следует аккуратно перемешать 2–3 раза с помощью шприца. Прививку проводят сразу после набора в шприц прививочной дозы. Одним шприцем вакцина может быть введена только одному ребенку.
Вакцину БЦЖ
вводят строго внутрикожно на границе верхней и средней трети наружной
поверхности левого плеча после предварительной обработки кожи 70% этиловым
спиртом. Иглу вводят срезом вверх в поверхностный слой натянутой кожи.
Сначала вводят незначительное количество вакцины, чтобы убедиться, что игла
вошла точно внутрикожно, а затем всю дозу препарата (всего 0,1 мл). При
правильной технике введения должна образоваться папула беловатого цвета
диаметром 7–9 мм, исчезающая
обычно через 15–20 мин.
Иглу вводят срезом вверх в поверхностный слой натянутой кожи.
Сначала вводят незначительное количество вакцины, чтобы убедиться, что игла
вошла точно внутрикожно, а затем всю дозу препарата (всего 0,1 мл). При
правильной технике введения должна образоваться папула беловатого цвета
диаметром 7–9 мм, исчезающая
обычно через 15–20 мин.
Прививки детям — ставить или не ставить?
Вопрос, ставить ли ребенку прививки, беспокоит многих родителей. Эта тема связана со множеством страхов, мифов и сомнений. Мы задали самые волнующие вопросы педиатру «ЕвроМед клиники» Елене Сергеевне Кочетковой.
— Елена Сергеевна, может ли быть два мнения по вопросу того, ставить ли прививки ребенку?
— Однозначно нет! Вакцинация – это единственный способ уберечь ребенка от множества опасных (и порой смертельно опасных) инфекций. Многие родители боятся осложнений после прививок, но уверяю вас, риск осложнений от перенесенных инфекций в разы выше. Если говорить про осложнения после прививок, то для начала надо различать нежелательные побочные эффекты и действительно реальные осложнения. Побочные эффекты обычно легко переносятся ребенком и быстро проходят. Что касается серьезных осложнений после прививок, то могу сказать, что за свою более чем 30-летнюю практику я всего два раза сталкивалась с действительно непредсказуемыми и серьезными осложнениями у детей. Да и то нельзя сказать, что они были совсем уж криминальными.
Если говорить про осложнения после прививок, то для начала надо различать нежелательные побочные эффекты и действительно реальные осложнения. Побочные эффекты обычно легко переносятся ребенком и быстро проходят. Что касается серьезных осложнений после прививок, то могу сказать, что за свою более чем 30-летнюю практику я всего два раза сталкивалась с действительно непредсказуемыми и серьезными осложнениями у детей. Да и то нельзя сказать, что они были совсем уж криминальными.
Обычно же осложнений можно избежать, подготовить ребенка к вакцинации с учетом его анамнеза, имеющихся у него заболеваний, аллергий.
— В каких случаях прививку не ставят по медицинским показаниям?
— Большинство наших медотводов – чисто российская перестраховка, уступка тревожным родителям. Заграницей основанием к временному отказу от прививки будет считаться, например, высокая температура, а у нас даже насморк, который был три дня назад для многих является поводом отложить прививку. В большинстве случаев прививка не влияет на выздоровление, так же, как выздоровление не влияет на прививку. Но у нас принято всё, что происходит с ребенком в течение длительного времени после введения вакцины, списывать на прививку. Мы забываем золотое правило: «после» не значит «вследствие».
В большинстве случаев прививка не влияет на выздоровление, так же, как выздоровление не влияет на прививку. Но у нас принято всё, что происходит с ребенком в течение длительного времени после введения вакцины, списывать на прививку. Мы забываем золотое правило: «после» не значит «вследствие».
Разумеется, есть случаи, когда вакцинацию лучше отложить. Это острое состояние при аллергии (в период ремиссии вакцинация аллергикам не просто можно, а нужно делать), высокая температура, ОРВИ, некоторые неврологические заболевания. Отдельный случай, когда вакцинацию рекомендуется отложить – наличие у ребенка до года доброкачественной нейтропении. Это состояние связано с адаптацией ребенка к нашим городским условиям, современным нагрузкам; проявляется тем, что в анализе крови наблюдается недостаточное количество нейтрофилов. Причем это количество не укладывается ни в норму, ни в состояние при болезни, а находится в среднем значении. В такой ситуации лучше не нагружать организм дополнительно, его иммунные силы сейчас и так ослаблены, и все силы направлены на то, чтобы адаптироваться к окружающей среде.
— Можно ли ставить прививки детям, склонным к аллергии, часто болеющим?
— В первую очередь! Конечно, в остром состоянии прививки не ставят. Но в состоянии ремиссии прививаться обязательно. Сами посудите, если ребенок часто болеющий, ослабленный, заразится какой-то серьезной инфекцией, то как он будет болеть? С высокой долей вероятности – очень тяжело, скорее всего, с осложнениями. Что касается аллергиков, то с ними дополнительно возникнет проблема – как их лечить, как он среагирует на заболевание, на лекарственные препараты. Опять же велик риск того, что заболевание будет протекать в тяжелой форме.
Поэтому аллергикам, часто болеющим детям, пациентам с пороком сердца вакцинация нужна обязательно.
— Есть мнение, что вакцинация может спровоцировать развитие аллергии у ребенка. Это так?
— Прямой связи здесь, конечно, нет. Но если у ребенка есть предрасположенность к аллергии, введение вакцины может послужить толчком к развитию заболевания. В данной ситуации сложно предположить, что опаснее, потому что сама инфекция или лекарственные препараты так же могут спровоцировать развитие аллергии.
В данной ситуации сложно предположить, что опаснее, потому что сама инфекция или лекарственные препараты так же могут спровоцировать развитие аллергии.
— Многие родители задаются вопросом, стоит ли ставить прививки от гепатита В и туберкулеза сразу в роддоме – ведь новорожденный малыш еще так слаб. Может быть, разумнее дать ему время адаптироваться, а эти прививки поставить позже – допустим, в 3-6 месяцев?
— Ребенок сразу после рождения (да и еще находясь в утробе матери!) сталкивается с сотней микроорганизмов, и успешно их обрабатывает. Так что дополнительные пара антигенов, которые ему введут во время вакцинации не играют уже особой роди на фоне этого.
Иммунный ответ на БЦЖ (прививку от туберкулеза) развивается в течение 2-3 месяцев. Учитывая, что туберкулез встречается абсолютно во всех социальных слоях, в том числе среди весьма благополучных и обеспеченных людей, то когда же прививать ребенка, чтобы обеспечить ему надежную защиту?
Гепатит В – это такая болезнь, у которой в детском возрасте нет понятия «выздоровление». Если взрослый человек заболеет гепатитом В, то он имеет шанс взять его под контроль – при помощи соответствующего образа жизни и лекарственных препаратов. У детей же это невозможно. Они растут и поэтому гепатит у них может только активно прогрессировать.
Если взрослый человек заболеет гепатитом В, то он имеет шанс взять его под контроль – при помощи соответствующего образа жизни и лекарственных препаратов. У детей же это невозможно. Они растут и поэтому гепатит у них может только активно прогрессировать.
В детском возрасте основной путь заражения гепатитом В – во время медицинских процедур. И никто не может знать, когда ребенку понадобиться медицинская помощь: неотложная операция, переливание крови после травмы, ДТП. Девочкам сейчас очень рано прокалывают уши – и это тоже риск заражения гепатитом.
Прививку от гепатита В неслучайно ставят в первые сутки после рождения – именно потому, что никто не застрахован от срочного медицинского вмешательства.
— Какие еще прививки, помимо тех, которые перечислены в календаре вакцинации, можно порекомендовать поставить ребенку?
— Прививку против ротавирусной инфекции. Ротавирус очень опасен в первые годы жизни ребенка. Более 90% детей с ротавирусной инфекцией госпитализируется в инфекционную больницу. Вообще, по статистике, более половины госпитализаций детей с острыми кишечными заболеваниями связаны с ротавирусной инфекцией. Болезнь сопровождается высокой температурой, сильной рвотой и диареей (поносом), что приводит к обезвоживанию, а для маленьких детей это может быть весьма опасно. Кроме того, дети могут болеть этой инфекцией неоднократно, так как у нее масса разновидностей. Вакцина защищает от ротавируса и значительно облегчает течение заболевания при смежных вирусах (норовирус, астровирус и др.).
Более 90% детей с ротавирусной инфекцией госпитализируется в инфекционную больницу. Вообще, по статистике, более половины госпитализаций детей с острыми кишечными заболеваниями связаны с ротавирусной инфекцией. Болезнь сопровождается высокой температурой, сильной рвотой и диареей (поносом), что приводит к обезвоживанию, а для маленьких детей это может быть весьма опасно. Кроме того, дети могут болеть этой инфекцией неоднократно, так как у нее масса разновидностей. Вакцина защищает от ротавируса и значительно облегчает течение заболевания при смежных вирусах (норовирус, астровирус и др.).
Курс вакцинации включает в себя три прививки с интервалом в 4-10 недель, вакцина вводится перорально (то есть капли в рот). Первая прививка ставится в возрасте от 6 до 12 недель (не позже!), последняя прививка должна быть поставлена не позже 8 месяцев. После полного курса вакцинации у ребенка вырабатывается иммунитет к ротавирусной инфекции, который сохраняется до 5 лет. Ревакцинация не требуется.
Прививку против ветряной оспы. Эта прививка не входит в российский календарь прививок, в отличие от многих зарубежных стран, но я рекомендую ее делать. Ставить прививку от ветряной оспы можно, начиная с года ребенка.
Многие родители задаются вопросом: зачем она нужна, ведь если ребенок переболеет в детстве ветрянкой, то у него и так появится иммунитет на всю жизнь? Все так просто. В детском возрасте ветряная оспа действительно обычно переносится достаточно легко, особенно в случае, если мама ребенка имеет иммунитет к этой инфекции, и, соответственно, у маленького ребенка еще сохраняются материнские антитела. В более взрослом возрасте ветрянка, чаще всего, протекает достаточно тяжело и с большим количеством осложнений.
Многолетний опыт работы позволяет сделать следующие наблюдения: сейчас ветрянка достаточно сильно мутирует. Еще 15 лет назад большинство врачей относились к ветрянке достаточно спокойно, рассуждая так же: переболел с достаточно предсказуемыми последствиями, и иммунитет сформирован.Сейчас же вирус становится более агрессивным, каждый год фиксируются летальные исходы и серьезные осложнения! Высыпания появляются не только на коже, но и на слизистых, на внутренних органах: поверхности кишечника, бронхов, и это может привести к развитию тяжелых осложнений.
Кроме того, важно учитывать, что ветрянка вызывается генерализованной герпетической инфекцией. И герпес после этого из организма не уходит. Зачастую после 40 лет вирус просыпается и проявляется в виде неврологической реакции: опоясывающем лишае в межреберных промежутках. Это обычно связано со стрессами, со снижением иммунитета.
Таким образом, актуальность вакцинации против ветряной оспы уже не вызывает сомнений.
Вакцинация против ВПЧ. Вирус папилломы человека (ВПЧ) является основной причиной развития рака шейки матки. Соответственно, своевременная вакцинация девочек от ВПЧ является надежной защитой от развития рака. Иммунопрофилактика против ВПЧ рекомендована девушкам и молодым женщинам, которые еще не инфицированы ВПЧ. Желательно провести вакцинацию до начала половой жизни, обычно ее рекомендуют девочкам-подросткам в 12 лет. Стандартный курс вакцинации состоит из 3 доз и проводится по схеме (0-2-6 мес.): вторая доза – через 2 месяца после первой; третья доза – через 6 месяцев после первой.
Желательно провести вакцинацию до начала половой жизни, обычно ее рекомендуют девочкам-подросткам в 12 лет. Стандартный курс вакцинации состоит из 3 доз и проводится по схеме (0-2-6 мес.): вторая доза – через 2 месяца после первой; третья доза – через 6 месяцев после первой.
Эту вакцину можно рекомендовать поставить всем девочкам. Но если есть семейный анамнез (онкология у кого-то из близких родственников, особенно – рак шейки матки, вульвы, влагалища), тогда эта прививка особенно нужна!
Мальчиков тоже рекомендуем прививать. Во-первых, с целью защитить их будущих любимых женщин, так как мальчики могут являться переносчиками ВПЧ. Во-вторых, ВПЧ может являться одним из факторов развития онкологии половой системы и у мужчин, хотя это и проявляется значительно реже.
Таким образом, повторим еще раз: только вакцинация является надежной защитой от множества тяжелых инфекций. Давайте не будем ставить эксперименты на своих детях, проверяя их устойчивость к инфекциям и играя в русскую рулетку: легко они переболеют или получат тяжелейшие осложнения от заболевания, от которого мы легко могли их защитить всего лишь поставив прививку.
Справка
- Вакцинация
- – это самое эффективное средство защиты вашего ребенка от инфекционных заболеваний. При помощи прививок успешно борются с вирусами кори, краснухи, паротита (свинки), ветряной оспы, полиомиелита, гепатита В, ротавирусной инфекции и с бактериями, вызывающими туберкулез, дифтерию, коклюш, столбняк, гемофильную инфекцию.
Суть вакцинации заключается в том, что ребенку прививается ослабленный или убитый болезнетворный агент (или искусственно синтезированный, аналогичный настоящему) с целью стимулировать выработку организмом антител к нему.
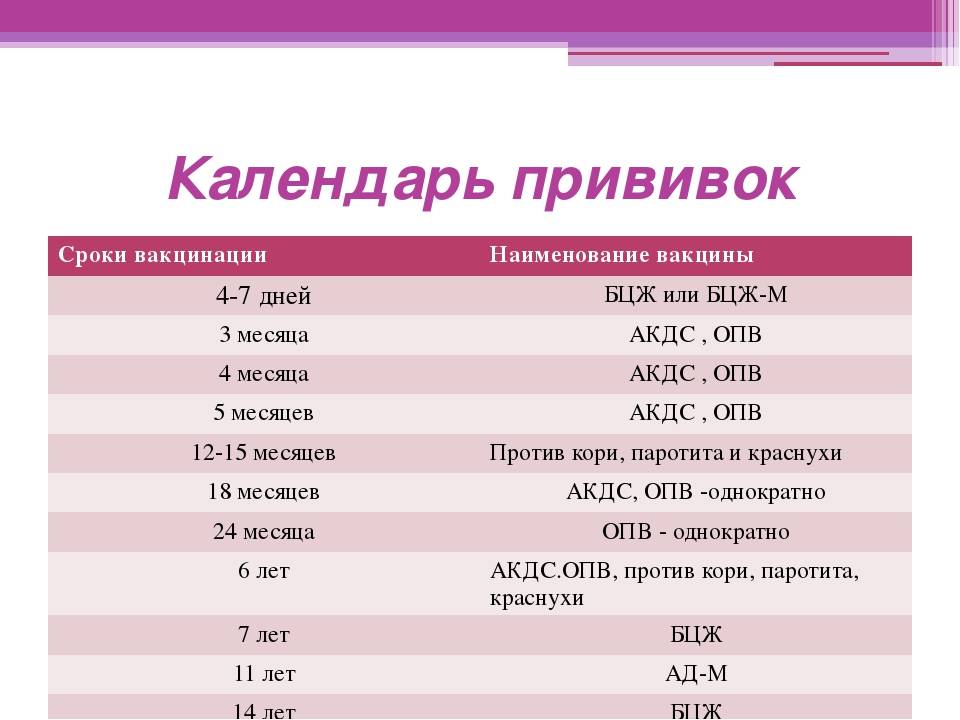
- Календарь прививок
- – это перечень вакцин и схема их введения, утвержденная Министерством здравоохранения РФ. В календаре прививок регламентируются плановые прививки и прививки, которые делают по эпидемиологическим показаниям.
Плановые прививки ставятся от массовых инфекций, которые протекают тяжело, имеют высокую вероятность неблагоприятных последствий или летального исхода.
Их проводят, начиная с рождения ребенка, по специальному графику. Кроме утвержденных в календаре прививок вы можете отдельно поставить по желанию прививки от некоторых тяжелых инфекций: ветряной оспы, вируса папилломы человека, ротавирусной инфекции и др.
Прививки по эпидемическим показаниям ставятся в случае возникновения вспышек некоторых инфекций; людям, живущим или посещающим эпидемиологически неблагополучные районы; работникам определенных специальностей (медицинские работники, учителя и др.). Например, всем жителям Новосибирской области рекомендуется ставить прививку от клещевого энцефалита – опасной инфекции, которой можно заразиться при укусе клеща.
| Категории и возраст граждан, подлежащих профилактическим прививкам | Наименование прививки | Примечания |
|---|---|---|
| Новорожденные в первые 24 часа жизни | Первая вакцинация против вирусного гепатита В | |
| Новорожденные на 3-7 день жизни | Вакцинация против туберкулеза | |
| Дети в 1 месяц | Вторая вакцинация против вирусного гепатита В | |
| Дети в 2 месяца | Третья вакцинация против вирусного гепатита В |
По показаниям, только если ребенок находится в группе риска.
|
| Первая вакцинация от пневмококковой инфекции (дает защиту от пневмоний, бронхитов, отитов и ОРВИ средней степени) | ||
| Дети в 3 месяца | Первая вакцинация против дифтерии, коклюша, столбняка | |
| Первая вакцинация против гемофильной инфекции (гнойные отиты, менингиты) | Курс вакцинации против гемофильной инфекции для детей в возрасте от 3 до 6 месяцев состоит из 3 инъекций по 0,5 мл с интервалом 1-1,5 месяца. | |
| Первая вакцинация против полиомиелита | ||
| Дети в 4, 5 месяцев | Вторая вакцинация против дифтерии, коклюша, столбняка | Проводится детям, получившим первую вакцинацию в 3 месяца |
| Вторая вакцинация против гемофильной инфекции | Проводится детям, получившим первую вакцинацию в 3 месяца | |
| Вторая вакцинация против полиомиелита | Проводится детям, получившим первую вакцинацию в 3 месяца | |
| Дети в 6 месяцев | Третья вакцинация против дифтерии, коклюша, столбняка | Проводится детям, получившим первую и вторую вакцинацию в 3 и 4,5 месяца соответственно |
| Третья вакцинация против вирусного гепатита В | Проводится детям, не относящимся к группам риска, получившим первую и вторую вакцинацию в 0 и 1 месяц соответственно | |
| Третья вакцинация против гемофильной инфекции | Проводится детям, получившим первую и вторую вакцинацию в 3 и 4,5 месяца соответственно | |
| Третья вакцинация против полиомиелита | ||
| Дети в 12 месяцев | Вакцинация против кори, краснухи, эпидемического паротита | |
| Четвертая вакцинация против вирусного гепатита В | Проводится детям из групп риска | |
| Дети в 18 месяцев | Первая ревакцинация против дифтерии, коклюша, столбняка | |
| Первая ревакцинация против полиомиелита | ||
| Ревакцинация против гемофильной инфекции |
Ревакцинации проводят однократно детям, привитым на первом году жизни.
|
|
| Дети в 20 месяцев | Вторая ревакцинация против полиомиелита | |
| Дети в 6 лет | Ревакцинация против кори, краснухи, эпидемического паротита | Проводится детям, получившим вакцинацию против кори, краснухи, эпидемического паротита |
| Дети в 6-7 лет | Вторая ревакцинация против дифтерии, столбняка | |
| Дети в 7 лет | Ревакцинация против туберкулеза | |
| Третья ревакцинация против дифтерии, столбняка | ||
| Третья ревакцинация против полиомиелита | ||
| Ревакцинация против туберкулеза | ||
| Взрослые от 18 лет | Ревакцинация против дифтерии, столбняка | Проводится в соответствии с инструкциями по применению анатоксинов с уменьшенным содержанием антигенов взрослым от 18 лет каждые 10 лет с момента последней ревакцинации |
Противопоказания
· Анатоксин дифтерийно-столбнячный, · Анатоксин дифтерийный, · Анатоксин столбнячный | -Гиперчувствительность к какому-либо компоненту, — острые инфекционные заболевания (не ранее 2–4 недель после выздоровления), -обострение хронических заболеваний, -беременность. | Редко: в первые двое суток могут развиваться кратковременные общие (повышение температуры, недомогание) и местные (болезненность, гиперемия, инфильтрат, отечность) реакции. Крайне редко: аллергические реакции немедленного типа. |
· Вакцина для профилактики вирусного гепатита B, дифтерии и столбняка · Вакцина для профилактики вирусного гепатита B, дифтерии, коклюша и столбняка | -Гиперчувствительность к какому-либо компоненту вакцины, -острые инфекционные заболевания (не ранее 2–4 недель после выздоровления), — обострение хронических заболеваний, — прогрессирующие заболевания нервной системы, — фебрильные судороги в анамнезе. | Редко: в первые двое суток могут развиваться кратковременные общие (повышение температуры, недомогание) и местные (болезненность, гиперемия, инфильтрат, отечность) реакции. Крайне редко: аллергические реакции немедленного типа. |
Вакцина для профилактики вирусного гепатита В | -Гиперчувствительность к какому-либо компоненту вакцины, -острые инфекционные заболевания (не ранее 2–4 недель после выздоровления), -обострение хронических заболеваний. | Редко: в первые двое суток могут развиваться кратковременные общие (повышение температуры, недомогание) и местные (болезненность, гиперемия, инфильтрат, отечность) реакции; усталость, боль в суставах, боль в мышцах, головная боль, головокружение, тошнота, рвота, боль в области живота. Крайне редко: аллергические реакции немедленного типа. |
Вакцина для профилактики гриппа инактивированная | -Гиперчувствительность к какому-либо компоненту вакцины, -сильные поствакцинальные реакции или осложнения на предыдущее введение вакцины, -беременность и возраст до 18 лет (при применении вакцины с консервантом), — возраст до 12 лет (при применении вакцины без консерванта), -острые инфекционные заболевания (не ранее 2–4 недель после выздоровления), — обострение хронических заболеваний, — период грудного вскармливания. | Редко: в первые двое суток могут развиваться кратковременные общие (повышение температуры, недомогание) и местные (болезненность, гиперемия, инфильтрат, отечность) реакции; усталость, головная боль, боль в области живота, першение и боль в горле, легкий насморк, уплотнение, отек и гиперемия кожи в месте введения. Крайне редко: аллергические реакции немедленного типа. |
Вакцина для профилактики гриппа инактивированная с иммуностимулятором | -Гиперчувствительность к какому-либо компоненту вакцины, -сильные поствакцинальные реакции или осложнения на предыдущее введение вакцины, -острые инфекционные заболевания (не ранее 2–4 недель после выздоровления), — обострение хронических заболеваний. | Редко: в первые двое суток – кратковременные общие (повышение температуры, недомогание) и местные (болезненность, гиперемия, инфильтрат, отечность) реакции. Крайне редко: аллергические реакции немедленного типа. |
Вакцина для профилактики полиомиелита | -Гиперчувствительность к какому-либо компоненту вакцины, -сильные поствакцинальные реакции или осложнения на предыдущее введение вакцины, — острые инфекционные заболевания (не ранее 2–4 недель после выздоровления), -обострение хронических заболеваний, — беременность, — неврологические расстройства, сопровождавшие предыдущую вакцинацию, — иммунодефицитное состояние (первичное), -злокачественные новообразования, — иммуносупрессия (не ранее, чем через 3 месяца после окончания курса). | Редко: не ранее 4 дня и не позднее чем через 30 дней после введения вакцины — кратковременные общие (повышение температуры, недомогание) и местные (болезненность, гиперемия, инфильтрат, отечность) реакции; головная боль, рвота. Крайне редко: аллергические реакции немедленного типа. Единичные случаи: возникновение вакциноассоциированного паралитического полиомиелита (ВАПП). |
Вакцина для профилактики дифтерии, коклюша и столбняка | — Гиперчувствительность к какому-либо компоненту, — острые инфекционные заболевания (не ранее 2–4 недель после выздоровления), -обострение хронических заболеваний, -прогрессирующие заболевания нервной системы, -афебрильные судороги в анамнезе, -сильные поствакцинальные реакции или осложнения на предыдущее введение вакцины. | Редко: боль, отек, покраснения в месте инъекции, головная боль, тошнота, диарея, анорексия, миалгия, боль в мышцах или мышечная слабость, отеки в области суставов, общее недомогание, озноб, лихорадка, рвота, кожная сыпь, судороги. Крайне редко: аллергические реакции, крапивница. |
Вакцина для профилактики гемофильной инфекции | -Гиперчувствительность к какому-либо компоненту, — острые инфекционные заболевания (не ранее 2–4 недель после выздоровления), -обострение хронических заболеваний, -сильные поствакцинальные реакции или осложнения на предыдущее введение вакцины. | Редко: незначительная спонтанно исчезающая гиперемия, слабая отечность, болезненность в месте инъекции, субфебрильная температурная реакция, снижение аппетита, беспокойство, необычный плач, лихорадка, тошнота, диарея. |
Вакцина для профилактики кори и паротита | — Гиперчувствительность к какому-либо компоненту, -острые инфекционные заболевания (не ранее 2–4 недель после выздоровления), — обострение хронических заболеваний, — сильные поствакцинальные реакции или осложнения на предыдущее введение вакцины, — беременность, — иммунодефицитное состояние (первичное), — злокачественные новообразования. | Редко: температурные реакции, легкая гиперемия зева, ринит, покашливание, конъюнктивит, слабовыраженный отек, кореподобная сыпь. |
Вакцина для профилактики кори | -Гиперчувствительность к какому-либо компоненту, -острые инфекционные заболевания (не ранее 2–4 недель после выздоровления), — обострение хронических заболеваний, -сильные поствакцинальные реакции или осложнения на предыдущее введение вакцины, -беременность, — иммунодефицитное состояние (первичное), — злокачественные новообразования. | Редко: болезненность в месте инъекции, температурные реакции, легкая гиперемия зева, ринит, покашливание, конъюнктивит, слабовыраженный отек, легкое недомогание, кореподобная сыпь, судорожные реакции, аллергические реакции. |
Вакцина для профилактики краснухи | — Гиперчувствительность к какому-либо компоненту, — острые инфекционные заболевания (не ранее 2–4 недель после выздоровления), -обострение хронических заболеваний, — сильные поствакцинальные реакции или осложнения на предыдущее введение вакцины, — беременность и период грудного вскармливания, — иммунодефицитное состояние (первичное), — злокачественные новообразования. | Редко: необильная кожная сыпь, лимфаденопатия, кратковременная гиперемия, отек и уплотнение, сопровождающееся болезненностью, кашель, насморк, боль в горле, недомогание, головная боль, тошнота, субфебрильные температурные реакции. Очень редко: аллергические реакции, артралгия, артрит, миалгия, парестезия. |
Вакцина для профилактики паротита | — Гиперчувствительность к какому-либо компоненту, -острые инфекционные заболевания (не ранее 2–4 недель после выздоровления), — обострение хронических заболеваний, — сильные поствакцинальные реакции или осложнения на предыдущее введение вакцины, — беременность и период грудного вскармливания, иммунодефицитное состояние (первичное), злокачественные новообразования. | Редко: кратковременное незначительное повышение температуры, легкая гиперемия зева, ринит, отеки в месте инъекции, беспокойство, вялость, нарушение сна. Очень редко: аллергические реакции, доброкачественно протекающий серозный менингит, болезненный кратковременный отек яичек. |
Вакцина для профилактики пневмококковых инфекций | — Гиперчувствительность к какому-либо компоненту, — острые инфекционные заболевания (не ранее 2–4 недель после выздоровления), -обострение хронических заболеваний, — сильные поствакцинальные реакции или осложнения на предыдущее введение вакцины. | Редко: гипертермия, раздражительность, покраснение кожи, болезненные ощущения, уплотнения или отек в месте инъекции, рвота, сонливость, ухудшение сна, ухудшение аппетита, головная боль, генерализованные новые или обострение имеющихся болей в суставах и мышечных болей, озноб, утомляемость, диарея, сыпь, плаксивость, судороги, реакции гиперчувствительности (крапивница, дерматит, зуд, одышка, бронхоспазм), тошнота, случаи гипотонического коллапса, приливы крови к лицу, лимфаденопатия в области места инъекции. |
Вакцина для профилактики туберкулеза | Вакцинация: — Недоношенность, масса тела при рождении менее 2500 г, внутриутробная гипотрофия III–IV степени, — острые инфекционные заболевания (не ранее 2–4 недель после выздоровления), — обострение хронических заболеваний, -иммунодефицитное состояние (первичное), — злокачественные новообразования, -генерализованная инфекция БЦЖ, выявленная у других детей в семье, -необследованность на ВИЧ-инфекцию матери ребенка во время беременности и родов, -отсутствие проведения трехэтапной химиопрофилактики передачи ВИЧ от матери ребенку во время беременности ВИЧ-инфицированной матери – вакцинация не проводится до установления ВИЧ-статуса ребенка в возрасте 18 месяцев. Ревакцинация: Гиперчувствительность к какому-либо компоненту, острые инфекционные заболевания (не ранее 2–4 недель после выздоровления), обострение хронических заболеваний, сильные поствакцинальные реакции или осложнения на предыдущее введение вакцины, иммунодефицитное состояние (первичное), злокачественные новообразования, заболевание туберкулезом, заболевание туберкулёз в анамнезе и инфицирование микобактериями, положительная и сомнительная реакция на пробу Манту с 2 ТЕ ППД-Л, ВИЧ-инфекция, выявление нуклеиновых кислот молекулярными методами. | Очень часто: специфическая реакция в виде инфильтрата, папулы, пустулы, язвы размером 5 – 10 мм в диаметре, поверхностный рубец до 10 мм в диаметре в месте инъекции. Редко: лимфадениты – регионарные, чаще подмышечные, иногда над- или подключичные, язвы, холодные абсцессы, подкожные инфильтраты, келоидный рубец. Крайне редко: персистирующая и диссеминированная БЦЖ-инфекция без летального исхода (волчанка, оститы и др.), пост-БЦЖ синдром аллергического характера, который возникает вскоре после прививки (узловатая эритема, кольцевидная гранулема, сыпи и др.), в отдельных случаях – генерализованное поражение БЦЖ при врожденном иммунодефиците. |
Вакцинация БЦЖ в трех разных возрастных группах: ответ и эффективность
Общие сведения
Поскольку одна треть населения мира уже инфицирована микобактериями туберкулеза (ТБ), эффективный контроль над ТБ, одной из основных угроз здоровью в мире, достигается наилучшим образом сочетанием химиотерапии и вакцинации. Вакцинация против Bacillus Calmette-Guerin (БЦЖ) обязательна в 64 странах и рекомендована в других [1]. Недавно Всемирная организация здравоохранения расширила программы иммунизации и рекомендовала вакцинацию БЦЖ через 3 месяца [2], в то время как во многих областях вакцинация проводится при рождении [3], при поступлении в школу и в подростковом возрасте [4].В течение нескольких лет политика Греции заключалась в том, чтобы регулярно рекомендовать вакцинацию БЦЖ в школах детям в возрасте от 11 до 13 лет, но, скорректированный с учетом текущего индекса туберкулезной инфекции, составляющего 3,4%, этот график недавно был одобрен, предлагая вакцину при поступлении в школу ( в возрасте от 5 до 7 лет) до тех пор, пока риск заражения не снизится повсюду в Греции. Обоснование продолжения вакцинации по всей стране, даже несмотря на то, что в настоящее время туберкулез редко встречается в некоторых областях, связано с мобильностью населения: многие молодые люди учатся, идут в армию или ищут работу в регионах, где туберкулез более распространен [5] .
Вакцинация против Bacillus Calmette-Guerin (БЦЖ) обязательна в 64 странах и рекомендована в других [1]. Недавно Всемирная организация здравоохранения расширила программы иммунизации и рекомендовала вакцинацию БЦЖ через 3 месяца [2], в то время как во многих областях вакцинация проводится при рождении [3], при поступлении в школу и в подростковом возрасте [4].В течение нескольких лет политика Греции заключалась в том, чтобы регулярно рекомендовать вакцинацию БЦЖ в школах детям в возрасте от 11 до 13 лет, но, скорректированный с учетом текущего индекса туберкулезной инфекции, составляющего 3,4%, этот график недавно был одобрен, предлагая вакцину при поступлении в школу ( в возрасте от 5 до 7 лет) до тех пор, пока риск заражения не снизится повсюду в Греции. Обоснование продолжения вакцинации по всей стране, даже несмотря на то, что в настоящее время туберкулез редко встречается в некоторых областях, связано с мобильностью населения: многие молодые люди учатся, идут в армию или ищут работу в регионах, где туберкулез более распространен [5] .
Однако эффективность вакцинации БЦЖ вызывает серьезные сомнения [6]. Исследования детей старшего возраста и взрослых показали защиту 77% в Великобритании [7]), только 14% на юге США [8] и ни одного в Мадрасе [9]. Более того, в ретроспективном исследовании 22 детей с туберкулезом позвоночника в развивающейся стране у всех в анамнезе были шрамы от вакцинации БЦЖ [11]. Кроме того, в нескольких отчетах, рекомендующих продолжить политику вакцинации БЦЖ, обычно предлагаемую в школах, в настоящее время высказывается обеспокоенность по поводу влияния качества вакцины, ее транспортировки и техники ее применения на получаемую защиту [10].Слабость в программах борьбы с туберкулезом и широкое распространение ВИЧ могут также сыграть роль в недавнем возрождении туберкулеза во всем мире [11]. Однако методологическая и статистическая переоценка показала, что различные биологические и экологические условия в отдельных исследованиях и, в основном, погрешности или недостаточная статистическая мощность могли способствовать противоречивым данным [12]. Недавно полученные через 15 лет результаты показали, что даже среди групп населения с высоким уровнем инфицирования и высокой неспецифической чувствительностью, где БЦЖ не обеспечивает никакой защиты от взрослых форм бациллярного туберкулеза легких, БЦЖ обеспечивает определенный уровень общей защиты (до 50%) в дети [13].
Недавно полученные через 15 лет результаты показали, что даже среди групп населения с высоким уровнем инфицирования и высокой неспецифической чувствительностью, где БЦЖ не обеспечивает никакой защиты от взрослых форм бациллярного туберкулеза легких, БЦЖ обеспечивает определенный уровень общей защиты (до 50%) в дети [13].
Чувствительность к туберкулину, индуцированная БЦЖ, является количественной характеристикой и используется для сравнения эффективности вакцины. Было также высказано предположение, что защита, которую некоторые вакцины БЦЖ могут обеспечивать против развития туберкулеза в детстве, может косвенно отражаться в последующем развитии иммунного ответа на БЦЖ [14,15]. Предварительные исследования, однако, ограничивались изучением эффективности только лиофилизированных вакцин и не распространялись на изучение иммунологических свойств лиофилизированных вакцин БЦЖ, используемых в настоящее время в Европе.Более того, эти ограниченные исследования были должным образом ориентированы на оценку защитного эффекта БЦЖ у новорожденных азиатов или новорожденных с высоким риском, поэтому в них было включено слишком мало деталей, чтобы можно было оценить основные клинические проявления приобретенного иммунитета и сделать неоспоримые выводы о значимости и значимости. его производные последствия среди населения в целом.
его производные последствия среди населения в целом.
В рамках проспективной оценки эффективности лиофилизированной вакцины БЦЖ, используемой в текущих схемах БЦЖ в Греции, у нас была возможность оценить ее иммунологический ответ, чтобы изучить взаимосвязь между поствакцинальной чувствительностью к туберкулину и образованием рубцов, а также проанализировать свои эпидемиологические данные у детей, получавших БЦЖ, в трех разных возрастных группах.В течение следующего десятилетия мы сравнительно зарегистрировали 10-летние зарегистрированные случаи туберкулеза у вакцинированных и невакцинированных подростков в возрасте до 24 лет на нашей территории и в соседнем районе, не охваченном аналогичной профилактической программой, и сравнили их с 10- год количество кумулятивных случаев заболевания среди взрослого населения двух районов.
Методы
Участники
Внутрикожная вакцинация БЦЖ регулярно проводится школьникам, проживающим в районе, охваченном нашим медицинским центром, с 1988 года и продолжается до сих пор. В исследование были включены дети, участвовавшие в профилактической программе с 10.01.1988 по 10.01.1993. Чтобы ограничить побеги, схема BCG ежегодно применялась на трех разных уровнях школы, что соответствовало возрасту примерно 6, 12 и 15 лет соответственно. Документально подтверждено, что все дети, находящиеся под наблюдением в каждой из когорт, получили свою первую вакцинацию БЦЖ, когда они были в соответствующих возрастных группах и ранее не были вакцинированы (в Греции нет программы неонатальной вакцинации БЦЖ, а также все дети должны были иметь отрицательный результат тестирования на туберкулин. перед включением в исследование).Дети, которым была сделана вакцинация БЦЖ при рождении или в любое другое время из-за известного контакта с больным туберкулезом, были исключены из исследования. Аналогичным образом, уведомленные субъекты, получавшие химиопрофилактику, независимо от того, были ли они положительными или отрицательными на туберкулин, также были исключены из анализа. Из общего числа 1124 вакцинированных школьников, включенных в окончательный анализ (группа А), 394 получили свою первую вакцинацию в возрасте 6 лет и, соответственно, были отнесены к группе 6-летнего возраста, 483 — к группе первой вакцинации 12-летнего возраста и 247 — к группе детей первого года жизни.
В исследование были включены дети, участвовавшие в профилактической программе с 10.01.1988 по 10.01.1993. Чтобы ограничить побеги, схема BCG ежегодно применялась на трех разных уровнях школы, что соответствовало возрасту примерно 6, 12 и 15 лет соответственно. Документально подтверждено, что все дети, находящиеся под наблюдением в каждой из когорт, получили свою первую вакцинацию БЦЖ, когда они были в соответствующих возрастных группах и ранее не были вакцинированы (в Греции нет программы неонатальной вакцинации БЦЖ, а также все дети должны были иметь отрицательный результат тестирования на туберкулин. перед включением в исследование).Дети, которым была сделана вакцинация БЦЖ при рождении или в любое другое время из-за известного контакта с больным туберкулезом, были исключены из исследования. Аналогичным образом, уведомленные субъекты, получавшие химиопрофилактику, независимо от того, были ли они положительными или отрицательными на туберкулин, также были исключены из анализа. Из общего числа 1124 вакцинированных школьников, включенных в окончательный анализ (группа А), 394 получили свою первую вакцинацию в возрасте 6 лет и, соответственно, были отнесены к группе 6-летнего возраста, 483 — к группе первой вакцинации 12-летнего возраста и 247 — к группе детей первого года жизни. 15-летняя первая группа вакцинации.
15-летняя первая группа вакцинации.
Методология
Вакцина была сделана врачом и группой медицинских работников, имеющих опыт вакцинации. Лиофилизированную вакцину (0,1 мл, Pasteur inst.) Вводили внутрикожно над местом прикрепления левой дельтовидной мышцы для образования волдыря диаметром около 7 мм, используя отдельный шприц и иглу 27-G для каждого человека [ 10]. Восстановленная вакцина, используемая в нашем центре, содержит около 0,15 мг сырого веса организмов Галметта-Герена на мл, что подразумевает концентрацию колониеобразующих единиц жизнеспособных организмов 6 × 10 6 / мл.Во всех случаях использование 10 UI PPD проводилось за три дня до вакцинации вместе с тщательным клиническим обследованием. Туберкулиновое тестирование было повторено через три месяца после вакцинации, когда дети снова были осмотрены. Результат был определен через три дня, и уплотнение на уровне 6 мм или более при считывании поперек предплечья было расценено как положительный результат [14]; уплотнение 4–5,9 мм как слабый положительный результат и уплотнение менее 4 мм как PPD-отрицательный результат. Образование рубца классифицировали как настоящий (> 2 мм), крошечный (≤ 2 мм) или невидимый [10].Никаких других иммунологических исследований не проводилось для корреляции иммунитета к БЦЖ с оценкой других реакций на вакцинацию in vitro, поскольку в такой масштабной программе было бы невозможно сделать многие вещи у многих людей за короткое время, особенно в школьной среде. . Поскольку исследование не повлияло на уход за пациентами, наблюдательный совет учреждения отказался от необходимости информированного согласия родителей.
Образование рубца классифицировали как настоящий (> 2 мм), крошечный (≤ 2 мм) или невидимый [10].Никаких других иммунологических исследований не проводилось для корреляции иммунитета к БЦЖ с оценкой других реакций на вакцинацию in vitro, поскольку в такой масштабной программе было бы невозможно сделать многие вещи у многих людей за короткое время, особенно в школьной среде. . Поскольку исследование не повлияло на уход за пациентами, наблюдательный совет учреждения отказался от необходимости информированного согласия родителей.
Субкогорты
Те, кто дал отрицательный результат, прошли повторное тестирование в течение одного месяца. Пациентам с подтвержденным туберкулиновым отрицательным ответом (Манту <4 мм) предлагалась ревакцинация, и, если было получено согласие, вакцина вводилась отдельно от места рубца, полученного при предыдущей вакцинации БЦЖ (группа R), как было рекомендовано ранее [10].
Контроли
Дети в школах, не участвующих в программе профилактики БЦЖ (школы в соседних районах, не охваченных нашим медицинским центром), использовались в качестве контрольных для периода последующего наблюдения (невакцинированные подростки). Всего за тот же период времени было зарегистрировано 1340 детей контрольной группы сравнительного возраста. Согласно последним данным (2001 г.), полученным Национальным статистическим центром (вакцинировано 375024 и невакцинированных 348236), на этих двух территориях было одинаковое население.
Всего за тот же период времени было зарегистрировано 1340 детей контрольной группы сравнительного возраста. Согласно последним данным (2001 г.), полученным Национальным статистическим центром (вакцинировано 375024 и невакцинированных 348236), на этих двух территориях было одинаковое население.
Последующее наблюдение
Туберкулиновое тестирование было повторено через десять лет после вакцинации у небольшой части детей, все еще посещающих школу, и если ранее было получено информированное согласие родителей. Кроме того, в течение прошедшего десятилетия мы сравнительно зарегистрировали 10-летние зарегистрированные случаи туберкулеза у вакцинированных и невакцинированных подростков в возрасте от 14 до 24 лет на двух территориях. Данные были взяты из записей Центра здоровья и Национального статистического центра инфекционных заболеваний, а затем были проанализированы и сопоставлены с 10-летним числом кумулятивных случаев, наблюдаемых среди взрослого населения (старше 25 лет) в тех же районах (вакцинация).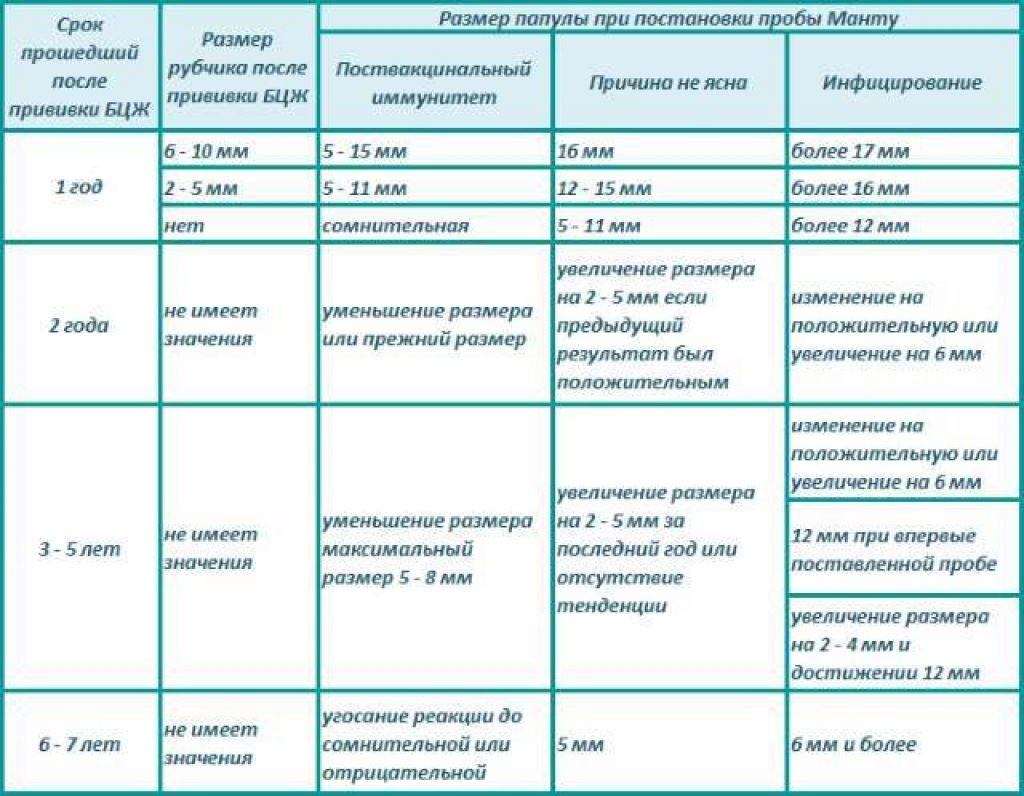 территория, обслуживаемая нашим медицинским центром, и невакцинированная соседняя территория, не охваченная нашим медицинским центром).Эпидемиологические данные о заболеваемости туберкулезом в возрастной группе от 6 до 14 лет отсутствовали.
территория, обслуживаемая нашим медицинским центром, и невакцинированная соседняя территория, не охваченная нашим медицинским центром).Эпидемиологические данные о заболеваемости туберкулезом в возрастной группе от 6 до 14 лет отсутствовали.
Статистический анализ
Методы оценки значимости данных включали двухвыборочную нулевую гипотезу для двустороннего теста, U-критерий Манна-Уитни и критерий x 2 с поправкой Йейтса с использованием стандартного статистического пакета.
Результаты
Переносимость
У всех испытуемых туберкулиновое тестирование перед вакцинацией дало отрицательный результат, и на основании анамнеза или клинического обследования противопоказаний для проведения вакцинации БЦЖ не было.Процедура переносилась хорошо, без остеопатии и лишь с очень небольшим количеством реакций, таких как три случая преходящей лимфаденопатии и один локальный подкожный абсцесс.
Возрастные группы
Подробная информация о туберкулиновом тесте и образовании рубцов в каждой возрастной группе показана на рисунках и. Не было статистически значимой разницы между тремя возрастными группами (6, 12 и 15 лет соответственно) в отношении диаметра туберкулинового уплотнения или образования рубца.Средний (SD) диаметр туберкулиновой реакции составил 11,13 (4,20) мм. Распределение диаметров уплотнения Манту выглядело как нормальная кривая с 95% доверительным интервалом, установленным на 2,73 мм и 19,53 мм (биномиальное распределение). Обширный поиск не выявил признаков активного туберкулеза у школьников с туберкулиновым уплотнением больше или равным 20 мм. Хотя 1034 (92,2%) испытуемых дали положительную реакцию на туберкулин после вакцинации, 45 (4%) дали слабое положительное уплотнение, а 43 (3.8%) дали отрицательный результат по PPD. Настоящее рубцевание образовалось у 96% вакцинированных школьников, а крошечный рубец (≤ 2 мм) — у 3,5%.
Не было статистически значимой разницы между тремя возрастными группами (6, 12 и 15 лет соответственно) в отношении диаметра туберкулинового уплотнения или образования рубца.Средний (SD) диаметр туберкулиновой реакции составил 11,13 (4,20) мм. Распределение диаметров уплотнения Манту выглядело как нормальная кривая с 95% доверительным интервалом, установленным на 2,73 мм и 19,53 мм (биномиальное распределение). Обширный поиск не выявил признаков активного туберкулеза у школьников с туберкулиновым уплотнением больше или равным 20 мм. Хотя 1034 (92,2%) испытуемых дали положительную реакцию на туберкулин после вакцинации, 45 (4%) дали слабое положительное уплотнение, а 43 (3.8%) дали отрицательный результат по PPD. Настоящее рубцевание образовалось у 96% вакцинированных школьников, а крошечный рубец (≤ 2 мм) — у 3,5%.
Поствакцинальное туберкулиновое тестирование в трех группах школьного возраста
Образование рубца БЦЖ в трех группах школьного возраста
Отвердение туберкулина и образование рубца
Обнаружена значимая корреляция (r 2 = 0,87, p <0,0001) между уплотнением туберкулина и образованием рубца (рисунок). Из таблицы видно, что ни у одного из детей без образования рубцов PPD-положительная реакция не развивалась.Вместо этого у 99,4% детей с положительной туберкулиновой кожной пробой наблюдалось образование рубцов по сравнению с 39,5% детей с отрицательной реактивностью на туберкулин (p <0,001). Соответственно, вероятность того, что у школьника не появится видимый рубец, была значительно выше среди детей с отрицательным результатом Манту, чем среди детей, у которых был либо положительный результат Манту (p <0,001), либо слабоположительный туберкулиновый тест (p <0,001). Реальный расчетный процент вероятности отсутствия образования рубца у детей с отрицательным результатом Манту был заключен между 95% -ными пределами от 14% до 38%, наиболее возможное значение - оценочное значение в 23% (биномиальное распределение).
Из таблицы видно, что ни у одного из детей без образования рубцов PPD-положительная реакция не развивалась.Вместо этого у 99,4% детей с положительной туберкулиновой кожной пробой наблюдалось образование рубцов по сравнению с 39,5% детей с отрицательной реактивностью на туберкулин (p <0,001). Соответственно, вероятность того, что у школьника не появится видимый рубец, была значительно выше среди детей с отрицательным результатом Манту, чем среди детей, у которых был либо положительный результат Манту (p <0,001), либо слабоположительный туберкулиновый тест (p <0,001). Реальный расчетный процент вероятности отсутствия образования рубца у детей с отрицательным результатом Манту был заключен между 95% -ными пределами от 14% до 38%, наиболее возможное значение - оценочное значение в 23% (биномиальное распределение).
Корреляция между уплотнением туберкулина и образованием рубца
Таблица 1
Количество (%) рубцовых образований БЦЖ в трех группах различных поствакцинальных туберкулиновых реакций у школьников
| Манту | Дети | Оценка образования рубца [n (%)] | ||
| Индурация (мм) | n | Настоящий рубец (> 2 мм) | Крошечный рубец (≤ 2 мм) | Без рубца (?) |
| Отрицательно (0–3,9) | 43 | 17 (39. 5) * 5) * | 20 (46,5) **, *** | 6 (14) ***, *** |
| Слабый положительный (4–5,9) | 45 | 32 ( 71,1) | 13 (28,9) **, *** | 0 (0) ***, *** |
| Положительный (> 6) | 1036 | 1030 (99,4) * | 6 (0,6) ***, *** | 0 (0) ***, *** |
| Всего | 1124 | 1079 (96,0) | 39 (3 . 5) 5) | 6 (0,5) |
Туберкулин-отрицательные субъекты с большей вероятностью имели крошечный рубец, чем субъекты с положительным (p <0,001) или слабоположительным (p <0,025) тестом Манту, соответственно. Процент крошечных рубцов у детей с туберкулиновыми уплотнениями размером 4–5,9 мм выше, чем у детей с диаметром уплотнения следующего диапазона (6–9 мм) (p <0,001). Реальный расчетный процент наличия крошечного рубца у детей с туберкулиновой реакцией менее 6 мм был включен в пределы 95% от 42% до 54% (среднее 47%, биномиальное распределение)]
Отрицательные реакторы
Из 43 туберкулин-отрицательных реакторов было рассмотрено 32 случая.Отсутствие реактивности было подтверждено, и всем 32 вакцинация БЦЖ была повторена. Удивительно, но после ревакцинации уровни реактивности к 10 МЕ PPD (90,6%) были аналогичны показателям реактивности, зарегистрированным в когорте группы А первичной вакцинации (92,2%, NS), что соответствует образованию 100% рубцов. Наблюдалось не только внешне сходное распределение уплотнений туберкулина (p <0,42), но также аналогичное среднее значение между группами (группа R 12,76 (5,40) мм против 11,13 (4,20) мм для группы A, p = 0,1).
Наблюдалось не только внешне сходное распределение уплотнений туберкулина (p <0,42), но также аналогичное среднее значение между группами (группа R 12,76 (5,40) мм против 11,13 (4,20) мм для группы A, p = 0,1).
Дальнейшие действия
A.Туберкулиновое уплотнение
Десять лет спустя когорты стали непостоянными, и многие дети исчезли (учеба, армия, новые семьи) или — при обнаружении — большинству из них было отказано в повторной пробе Манту. Среди 183 16-летних школьников (бывшая группа 6-летних), посещенных медицинскими посетителями в школах в 2005 г., 110 отказались от участия в последующем исследовании. Таким образом, примерно через 10 лет (2005 г.) нам удалось повторить Манту только у 73 детей 6-летней группы периода 1993–5 гг.Не было статистически значимой разницы между двухлетними периодами в отношении диаметра туберкулиновых уплотнений (средний (SD) диаметр туберкулиновой реакции 8,4 (5) мм в 2005 г. по сравнению с 8,1 (6) мм в 1995 г.). Средняя парная разница теста парных выборок была недостоверной: 0,25 (6) мм (95% доверительный интервал разницы: нижняя: -1,9, верхняя: 2,4 мм). Хотя корреляция парной выборки (рисунок) была значимой (r 2 ,45, p = 0,009), а новые индивидуальные значения были почти идентичны старым у 66% детей (± 2 мм), большая часть 10 -годовые значения были непредсказуемо связаны (снижение на 12%, увеличение на 22%) с исходными (рисунок).
Хотя корреляция парной выборки (рисунок) была значимой (r 2 ,45, p = 0,009), а новые индивидуальные значения были почти идентичны старым у 66% детей (± 2 мм), большая часть 10 -годовые значения были непредсказуемо связаны (снижение на 12%, увеличение на 22%) с исходными (рисунок).
Парная выборочная корреляция (квадратичная регрессия) уплотнений туберкулина между двумя периодами времени (начальный период исследования и 10-летнее наблюдение)
Последующее наблюдение недавних индивидуальных уплотнений (2005 г.) коррелировало с исходными значениями Манту (10-летние интервал времени)
B. Случаи туберкулеза
Данные, имеющиеся в Национальном статистическом центре инфекционных заболеваний и в записях Центра здоровья, показали, что случаи туберкулеза, зарегистрированные среди вакцинированных подростков — от 14 до 24 лет — за последние десятилетие на нашей территории были ниже по сравнению с невакцинированными подростками (17 vs.71 случай за десятилетие). Эти цифры привели бы к неправильной оценке заболеваемости туберкулезом в подростковом возрасте 1,3% по сравнению с 6,3% для вакцинированных школьников и контрольной группы, p <0,0001, если бы они были ограничены только изучаемой популяцией. Однако зарегистрированные случаи туберкулеза были распространены на население десятилетия, включая как минимум в три раза больше детей в каждой группе, получавших одинаковое лечение, что делает невозможным статистический анализ. Число зарегистрированных случаев туберкулеза среди взрослого населения (> 25 лет) на двух территориях, зарегистрированных в течение того же периода, было несколько ниже для вакцинированной территории по сравнению с невакцинированной территорией (77 против101 случай). Таким образом, относительный процент заболеваемости туберкулезом в возрастной группе 14–24 лет по отношению к взрослому населению, получившему ответы, который мог предоставить нам единственные сопоставимые цифры, был значительно ниже среди иммунизированных детей (17/77 * 100) по сравнению с детьми, не получившими ответа.
Эти цифры привели бы к неправильной оценке заболеваемости туберкулезом в подростковом возрасте 1,3% по сравнению с 6,3% для вакцинированных школьников и контрольной группы, p <0,0001, если бы они были ограничены только изучаемой популяцией. Однако зарегистрированные случаи туберкулеза были распространены на население десятилетия, включая как минимум в три раза больше детей в каждой группе, получавших одинаковое лечение, что делает невозможным статистический анализ. Число зарегистрированных случаев туберкулеза среди взрослого населения (> 25 лет) на двух территориях, зарегистрированных в течение того же периода, было несколько ниже для вакцинированной территории по сравнению с невакцинированной территорией (77 против101 случай). Таким образом, относительный процент заболеваемости туберкулезом в возрастной группе 14–24 лет по отношению к взрослому населению, получившему ответы, который мог предоставить нам единственные сопоставимые цифры, был значительно ниже среди иммунизированных детей (17/77 * 100) по сравнению с детьми, не получившими ответа. -иммунизированное население (71/101 * 100) той же возрастной группы (22% против 70% всех возрастов, x 2 = 14,7, p <0,0001).
-иммунизированное население (71/101 * 100) той же возрастной группы (22% против 70% всех возрастов, x 2 = 14,7, p <0,0001).
Обсуждение
Из-за противоречивых результатов крупных контролируемых испытаний вакцинация БЦЖ против туберкулеза остается спорной, несмотря на ее более чем 50-летнее использование.Широкий диапазон значений защитной эффективности БЦЖ, о которых сообщают испытания, расширился от 75%, отражая существенную защиту вакцины [3], до отрицательных значений, указывающих на более высокий уровень заболеваемости туберкулезом среди вакцинированных, чем в контрольной группе [16].
Хотя обычно считалось, что туберкулиновый статус после вакцинации не влияет на степень защиты, обеспечиваемую БЦЖ, дети, которые не стали чувствительны к туберкулину, либо впоследствии умерли от диссеминированного ТБ [17], либо заболели туберкулезным менингитом [18].Кроме того, относительный рост туберкулеза среди преимущественно неиммунизированных когорт, родившихся в европейской стране после 1975 г. , по сравнению с когортами, в основном иммунизированными БЦЖ, родившимися там в период 1969–1974 гг., К концу 1984 г. оценивался в 6 человек (доверительный интервал 95%). интервал от 2,3 до 16,1) [19]. Впоследствии, когда был достигнут высокий уровень поствакцинального иммунного ответа, оцененная защитная эффективность вакцины составила 64% с 95% доверительным интервалом 43% и 77% и предотвращенной фракцией 0.50 [15].
, по сравнению с когортами, в основном иммунизированными БЦЖ, родившимися там в период 1969–1974 гг., К концу 1984 г. оценивался в 6 человек (доверительный интервал 95%). интервал от 2,3 до 16,1) [19]. Впоследствии, когда был достигнут высокий уровень поствакцинального иммунного ответа, оцененная защитная эффективность вакцины составила 64% с 95% доверительным интервалом 43% и 77% и предотвращенной фракцией 0.50 [15].
Противоречивые результаты двух центров в Соединенном Королевстве показали, что только 45–46% вакцинированных детей были положительными по Манту при тестировании в возрасте от 3 месяцев до 2 лет [20]; У 25% не было видимых рубцов [21]. Другое исследование, проведенное в третьем центре, однако, показало, что 353 (98%) из 361 новорожденного азиатского происхождения, получавшего БЦЖ, были туберкулин-положительными при тестировании через три месяца [14]. Показатели конверсии туберкулина 93% или 88% были также установлены после вакцинации БЦЖ у 15 доношенных и 8 недоношенных детей соответственно [22]. Кроме того, более недавнее исследование, проведенное среди 193 вакцинированных из Азии, выявило положительный поствакцинальный тест на туберкулин у 184 из них (95%) [15]; Эти результаты согласуются с результатами настоящего исследования, подтверждающими преобладание иммунного ответа на БЦЖ на 94% в выборке из 1124 вакцинированных греческих школьников. Если ослабленный иммунитет был причиной снижения чувствительности к туберкулину после вакцинации, то можно было бы ожидать, что довольно постоянная доля азиатских или греческих детей не будет реагировать на туберкулин после вакцинации.В другом исследовании было обнаружено, что значительно более высокий процент младенцев, получавших японскую БЦЖ, были преобразователями туберкулина (74,7%) по сравнению с теми, кто получал британскую БЦЖ (51,4%). В наших исследуемых группах не было разницы между первично или повторно вакцинированными детьми (92% против 90%), и это также отразилось на частоте образования невидимых рубцов. Однако в отрицательных реакторах вакцинация БЦЖ могла вызвать защитные (тип Листера), а не антагонистические (туберкулиновый или тип Коха) реакции, которые, как предполагалось, были наиболее защитными [23].
Кроме того, более недавнее исследование, проведенное среди 193 вакцинированных из Азии, выявило положительный поствакцинальный тест на туберкулин у 184 из них (95%) [15]; Эти результаты согласуются с результатами настоящего исследования, подтверждающими преобладание иммунного ответа на БЦЖ на 94% в выборке из 1124 вакцинированных греческих школьников. Если ослабленный иммунитет был причиной снижения чувствительности к туберкулину после вакцинации, то можно было бы ожидать, что довольно постоянная доля азиатских или греческих детей не будет реагировать на туберкулин после вакцинации.В другом исследовании было обнаружено, что значительно более высокий процент младенцев, получавших японскую БЦЖ, были преобразователями туберкулина (74,7%) по сравнению с теми, кто получал британскую БЦЖ (51,4%). В наших исследуемых группах не было разницы между первично или повторно вакцинированными детьми (92% против 90%), и это также отразилось на частоте образования невидимых рубцов. Однако в отрицательных реакторах вакцинация БЦЖ могла вызвать защитные (тип Листера), а не антагонистические (туберкулиновый или тип Коха) реакции, которые, как предполагалось, были наиболее защитными [23]. Подобно результатам других исследований, проведенных на младенцах [24], мы также не наблюдали каких-либо значительных различий в средней туберкулиновой реакции, положительности туберкулина и среднем размере рубца в зависимости от возрастной группы на момент введения.
Подобно результатам других исследований, проведенных на младенцах [24], мы также не наблюдали каких-либо значительных различий в средней туберкулиновой реакции, положительности туберкулина и среднем размере рубца в зависимости от возрастной группы на момент введения.
Результаты нашего исследования подтверждают высокую положительную корреляцию между образованием рубцов и поствакцинальной чувствительностью к туберкулину у школьников разного возраста. Это открытие очень похоже на результаты, предложенные в отчетах из Индии и США, которые показали, что размер рубца после БЦЖ был связан со значительным повышением сенсибилизации к туберкулину [25,26].Аналогичным образом, в недавнем исследовании распространенность положительных результатов кожной пробы также была неизменно выше среди людей по сравнению с теми, у кого не было рубца от БЦЖ [27]. Наши данные подтверждают эту тенденцию, поскольку у детей, у которых не образовался рубец БЦЖ, не было доказательств положительного поствакцинального иммунного ответа на туберкулиновую кожную пробу. Однако важно отметить, что отрицательная реактивность кожной пробы все еще может быть связана с образованием реального (46,5%) или крошечного рубца (39,5%) (37 или 43 пациента, всего 86%).Следует также отметить, что в отличие от большинства предыдущих исследований, в этом исследовании используется лиофилизированная вакцина, демонстрирующая основные характеристики недавно применявшейся вакцины БЦЖ в западной стране на пороге нового тысячелетия.
Однако важно отметить, что отрицательная реактивность кожной пробы все еще может быть связана с образованием реального (46,5%) или крошечного рубца (39,5%) (37 или 43 пациента, всего 86%).Следует также отметить, что в отличие от большинства предыдущих исследований, в этом исследовании используется лиофилизированная вакцина, демонстрирующая основные характеристики недавно применявшейся вакцины БЦЖ в западной стране на пороге нового тысячелетия.
Предполагается, что 1079 субъектов со шрамом проявили первоначальный ответ на вакцинацию, о чем свидетельствует сильный положительный иммунный ответ у 1030 из них (99,4%). Возможно, некоторые отрицательные или слабые ответы были вызваны физиологическими последствиями, такими как общий статус питания, распространенность и особенно вирулентность атипичных микобактерий [23], инфекция M.Kansasii , что составляет примерно 80% потенциальной защиты, предлагаемой BCG [28]. Более того, в популяции с низким уровнем чувствительности к PPD (медиана кожных реакций 3 мм) у 36% субъектов была более выраженная реакция на атипичный антиген, такой как PPD-B [29]. Однако маловероятно, что все отрицательные результаты были вызваны этим, поскольку большинство детей с отрицательной реакцией Манту превратились в положительных реакторов после того, как они впоследствии прошли повторную вакцинацию БЦЖ. Этот вывод, который был дополнительно усилен наблюдаемым, сходным с ожидаемым, согласно нашим результатам, распределением уплотнений туберкулина, согласуется с недавними сообщениями, предполагающими, что ревакцинация привела к значительному увеличению положительной реакции на туберкулин 10 и другие протестированные реагенты. [30].
Однако маловероятно, что все отрицательные результаты были вызваны этим, поскольку большинство детей с отрицательной реакцией Манту превратились в положительных реакторов после того, как они впоследствии прошли повторную вакцинацию БЦЖ. Этот вывод, который был дополнительно усилен наблюдаемым, сходным с ожидаемым, согласно нашим результатам, распределением уплотнений туберкулина, согласуется с недавними сообщениями, предполагающими, что ревакцинация привела к значительному увеличению положительной реакции на туберкулин 10 и другие протестированные реагенты. [30].
Соответственно, кажется маловероятным, что нарушение реакции на туберкулин у некоторых из недавно вакцинированных субъектов было вызвано дефектом первоначального распознавания антигена или неспособностью сохранить эту информацию или даже неспособностью сенсибилизированных лимфоцитов реагировать, потому что человек недоедал или имел серьезную инфекцию [23]. Вместо этого есть косвенные доказательства того, что даже при рождении БЦЖ обеспечивает конверсию туберкулина у большого числа новорожденных [31], независимо от расы [32], этнического происхождения [33] или недоношенности [24]. Поскольку в настоящем исследовании возраст не был значимым фактором, влияющим на иммунный ответ на БЦЖ, возрастная массовая вакцинация должна быть идеально скорректирована в соответствии с возрастом, незадолго до того, как уровень инфицирования будет повышаться [6].
Поскольку в настоящем исследовании возраст не был значимым фактором, влияющим на иммунный ответ на БЦЖ, возрастная массовая вакцинация должна быть идеально скорректирована в соответствии с возрастом, незадолго до того, как уровень инфицирования будет повышаться [6].
Хотя средний (SD) диаметр туберкулиновых реакторов после вакцинации в нашем исследовании был неожиданно высоким (11,13 (4,20) мм), он был значительно ниже среднего значения 17,9 мм, рассчитанного для естественно инфицированных субъектов [33,34], и составлял существенно не отличается от средней реакции после вакцинации 9.4 (2,7) мм, о которых сообщают другие авторы [15]. Удивительно, но гораздо более широкий диапазон распределения уплотнений туберкулина был включен в 95% доверительный интервал для образца (2,73–19,53 мм). Фактически, у 71,1% пациентов со слабоположительным результатом Манту (4–5,9 мм) наблюдается рубец размером> 2 мм, который, как предполагалось ранее, адекватно отражает положительный иммунный ответ на вакцинацию БЦЖ [35]. У остальных (28,9%) был обнаружен крошечный рубец от БЦЖ, предположительно подчеркивающий более плавную и широкую зону перехода между положительной и отрицательной реакциями на ППД.Изучая две разные партии нового туберкулина, Stanford JL и Tala-Heikkila обнаружили, что средний размер рубца БЦЖ составлял 8,1 (стандартное отклонение 4,8) мм, и была тенденция, связывающая меньшие рубцы БЦЖ с меньшими ответами на туберкулин, которые не достигли статистических показателей. значимость [36]. Хотя такое объяснение правого конца кривой, по-видимому, не согласуется с предположением о том, что реакции диаметром более 10 мм, вероятно, представляют инфекцию [30], аналогичная широкая переходная зона для переменных положительных реакций также решительно поддерживается в Наше исследование продемонстрировало предыдущий отрицательный результат теста PPD, сразу за которым последовала вакцинация БЦЖ, которая незадолго до инверсии туберкулина.Таким образом, сильная туберкулиновая реакция, достигнутая у значительной части детей вскоре после БЦЖ, может просто представлять собой сильный клеточно-опосредованный иммунный ответ среди индивидуализированных проявлений недавно приобретенного иммунитета.
У остальных (28,9%) был обнаружен крошечный рубец от БЦЖ, предположительно подчеркивающий более плавную и широкую зону перехода между положительной и отрицательной реакциями на ППД.Изучая две разные партии нового туберкулина, Stanford JL и Tala-Heikkila обнаружили, что средний размер рубца БЦЖ составлял 8,1 (стандартное отклонение 4,8) мм, и была тенденция, связывающая меньшие рубцы БЦЖ с меньшими ответами на туберкулин, которые не достигли статистических показателей. значимость [36]. Хотя такое объяснение правого конца кривой, по-видимому, не согласуется с предположением о том, что реакции диаметром более 10 мм, вероятно, представляют инфекцию [30], аналогичная широкая переходная зона для переменных положительных реакций также решительно поддерживается в Наше исследование продемонстрировало предыдущий отрицательный результат теста PPD, сразу за которым последовала вакцинация БЦЖ, которая незадолго до инверсии туберкулина.Таким образом, сильная туберкулиновая реакция, достигнутая у значительной части детей вскоре после БЦЖ, может просто представлять собой сильный клеточно-опосредованный иммунный ответ среди индивидуализированных проявлений недавно приобретенного иммунитета. Кроме того, вакцинация БЦЖ при рождении и у детей школьного возраста вызывает реактивность на туберкулин, которая сохраняется в течение 20–25 лет, поэтому диаметр уплотнения> 15 мм не исключает вакцинацию [37]. Аналогичным образом, в нашем исследовании среди школьников через 10 лет после первичной вакцинации не было выявлено значительного снижения иммунитета к БЦЖ.Мы также показали, что, хотя иммунный ответ на БЦЖ сохранялся так долго, индивидуальные ответы широко варьировались (увеличивались или уменьшались) у 1/3 детей, что не могло быть экстраполировано. В недавнем исследовании предшествующая вакцинация БЦЖ оказала сильное влияние на результаты кожных проб диаметром <или = 18 мм у лиц моложе 40 лет по сравнению с влиянием факторов, прогнозирующих инфекцию M. tuberculosis [38]. Для вакцинированных субъектов с предыдущим отрицательным туберкулиновым тестом также необходимо исключить бустерный эффект.Таким образом, согласно нашим и другим результатам [39], диаметр уплотнения> 15 мм не исключает вакцинного происхождения [38].
Кроме того, вакцинация БЦЖ при рождении и у детей школьного возраста вызывает реактивность на туберкулин, которая сохраняется в течение 20–25 лет, поэтому диаметр уплотнения> 15 мм не исключает вакцинацию [37]. Аналогичным образом, в нашем исследовании среди школьников через 10 лет после первичной вакцинации не было выявлено значительного снижения иммунитета к БЦЖ.Мы также показали, что, хотя иммунный ответ на БЦЖ сохранялся так долго, индивидуальные ответы широко варьировались (увеличивались или уменьшались) у 1/3 детей, что не могло быть экстраполировано. В недавнем исследовании предшествующая вакцинация БЦЖ оказала сильное влияние на результаты кожных проб диаметром <или = 18 мм у лиц моложе 40 лет по сравнению с влиянием факторов, прогнозирующих инфекцию M. tuberculosis [38]. Для вакцинированных субъектов с предыдущим отрицательным туберкулиновым тестом также необходимо исключить бустерный эффект.Таким образом, согласно нашим и другим результатам [39], диаметр уплотнения> 15 мм не исключает вакцинного происхождения [38]. Кроме того, в некоторых случаях такая реакция может также указывать на то, что сенсибилизация к видам микобактерий могла произойти в очень молодом возрасте. Хотя такая сенсибилизация не может быть обнаружена с помощью туберкулиновой пробы, она может влиять на реакцию на вакцинацию БЦЖ [40]. Заметная разница в скорости туберкулин-реакции между городами Индии убедительно подтверждает такое влияние воздействия микобактерий в окружающей среде [27].Хотя было обнаружено, что в популяции с высоким уровнем чувствительности к PPD (средняя кожная реакция 12 мм), только 7% испытуемых дали больший ответ на атипичный антиген, чем на PPD [31], определение оптимальный диапазон реакций на вакцинацию БЦЖ в данной популяции является более спорным вопросом, который не может быть полностью решен без дополнительной информации о взаимодействии между качеством вакцины, прошедшим временем, распространенностью и вирулентностью атипичных микобактерий, бустерным эффектом , иммунологическая память и механизмы ее реакции на другие реагенты [40].
Кроме того, в некоторых случаях такая реакция может также указывать на то, что сенсибилизация к видам микобактерий могла произойти в очень молодом возрасте. Хотя такая сенсибилизация не может быть обнаружена с помощью туберкулиновой пробы, она может влиять на реакцию на вакцинацию БЦЖ [40]. Заметная разница в скорости туберкулин-реакции между городами Индии убедительно подтверждает такое влияние воздействия микобактерий в окружающей среде [27].Хотя было обнаружено, что в популяции с высоким уровнем чувствительности к PPD (средняя кожная реакция 12 мм), только 7% испытуемых дали больший ответ на атипичный антиген, чем на PPD [31], определение оптимальный диапазон реакций на вакцинацию БЦЖ в данной популяции является более спорным вопросом, который не может быть полностью решен без дополнительной информации о взаимодействии между качеством вакцины, прошедшим временем, распространенностью и вирулентностью атипичных микобактерий, бустерным эффектом , иммунологическая память и механизмы ее реакции на другие реагенты [40]. Поэтому в поздний поствакцинальный период невозможно отличить туберкулиновую реакцию, вызванную вирулентной супраинфекцией, от реакции, вызванной стойкой поствакцинальной чувствительностью, даже в случае сильной положительной реакции на 10 МЕ туберкулина PPD.
Поэтому в поздний поствакцинальный период невозможно отличить туберкулиновую реакцию, вызванную вирулентной супраинфекцией, от реакции, вызванной стойкой поствакцинальной чувствительностью, даже в случае сильной положительной реакции на 10 МЕ туберкулина PPD.
Повторная вакцинация БЦЖ, недостаточность питания и БЦЖ со шрамами представляют трудности при постановке диагноза ТБ, но не влияют на реактивность PPD и подчеркивают необходимость тщательной клинической оценки [41].Хотя высокая чувствительность к туберкулину у здоровых школьников может частично поддерживаться контактом с микобактериями окружающей среды, приписывание «положительной» реакции Манту на прошлую вакцинацию БЦЖ может способствовать ложному чувству безопасности у лиц, недавно переживших инфекционный туберкулез. Наши результаты подтверждают общее предположение о том, что основным недостатком БЦЖ является то, что она затрудняет интерпретацию туберкулиновой кожной пробы [42]. Эти результаты, однако, также предполагают, что уведомление о диаметре уплотнения туберкулина после вакцинации примерно через 3 месяца после вакцинации БЦЖ вполне может служить критерием самоконтроля в случае клинического диагноза ТБ [43], поскольку после вакцинации кожные реакции обычно со временем уменьшаются. Дополнительные факторы, такие как возраст контакта и статус мокроты первичного случая, являются важными детерминантами степени повышенной чувствительности к туберкулину [44]. Однако на пороге нового тысячелетия новые анализы крови (QuantiFERON-TB, CSL Limited), которые измеряют продукцию гамма-интерферона, когда белки, специфичные для M. tuberculosis, такие как ESAT-6, инкубируются с образцами венозной крови, являются многообещающими. для распознавания инфекции Mycobacterium tuberculosis, поскольку на них не влияет прошлое воздействие БЦЖ [45].
Дополнительные факторы, такие как возраст контакта и статус мокроты первичного случая, являются важными детерминантами степени повышенной чувствительности к туберкулину [44]. Однако на пороге нового тысячелетия новые анализы крови (QuantiFERON-TB, CSL Limited), которые измеряют продукцию гамма-интерферона, когда белки, специфичные для M. tuberculosis, такие как ESAT-6, инкубируются с образцами венозной крови, являются многообещающими. для распознавания инфекции Mycobacterium tuberculosis, поскольку на них не влияет прошлое воздействие БЦЖ [45].
Хотя вакцинация не предотвращает развитие инфекции у лиц, подвергшихся воздействию туберкулезных микобактерий, ее действие ограничивает размножение и распространение микобактерий туберкулеза, а также развитие поражений после инфицирования. Прямой эффект вакцинации БЦЖ определяется как профилактика туберкулеза у вакцинированных лиц, а косвенный — как снижение заболеваемости туберкулезом среди населения в целом [30]. Однако результаты эпидемиологических исследовательских лабораторий показали значительные различия в текущей политике вакцинации БЦЖ в разных районах, в то время как население очень мобильно [37]. Чтобы доля непривитых молодых людей увеличивалась, в то время как в Греции ежегодно регистрируется более 3420 новых случаев туберкулеза с положительной мокротой — сейчас их гораздо больше среди жертв СПИДа — увеличивает риск заболевания, которое может не быть диагностировано до тех пор, пока не будут диагностированы другие. инфицированы [46].
Чтобы доля непривитых молодых людей увеличивалась, в то время как в Греции ежегодно регистрируется более 3420 новых случаев туберкулеза с положительной мокротой — сейчас их гораздо больше среди жертв СПИДа — увеличивает риск заболевания, которое может не быть диагностировано до тех пор, пока не будут диагностированы другие. инфицированы [46].
Поскольку имеются доказательства в неонатальном периоде, но не в детстве, опровергающие мнение о том, что сенсибилизация важна для защиты [47], предположение о том, что положительный результат кожной пробы после вакцинации является индикатором индуцированного БЦЖ иммунитета против Mycobacterium tuberculosis, может не был правильным.Однако мы думали, что, поскольку высокий уровень конверсии кожной пробы PPD после вакцинации БЦЖ у школьников и ее стойкая реактивность в течение 10 лет могут повысить степень защиты, предлагаемую БЦЖ, следует сделать вывод, что конкретная лиофилизированная вакцина БЦЖ, используемая для Программы БЦЖ в греческих школах могут обеспечить удовлетворительную защиту от туберкулеза в период полового созревания. Наши результаты подкреплены результатами недавнего исследования, которое показало, что вакцинация БЦЖ при рождении и для детей школьного возраста вызывает реактивность на туберкулин, которая сохраняется в течение 20–25 лет [48].Зарегистрированное снижение заболеваемости туберкулезом среди подростков в вакцинированном районе подчеркивает необходимость поддерживать и, по возможности, активизировать профилактические меры и меры по выявлению случаев во всех группах особого риска [49], но также может указывать на то, что продолжение массового предложения В идеале вакцинация БЦЖ должна проводиться повсюду, включая регионы с низкой распространенностью ТБ [5]. Аналогичным образом, учитывая текущую заболеваемость туберкулезом в Финляндии и вероятность увеличения инфекций лимфатических узлов и повышения чувствительности к микобактериям окружающей среды, рекомендуется продолжить вакцинацию БЦЖ при рождении [37].
Наши результаты подкреплены результатами недавнего исследования, которое показало, что вакцинация БЦЖ при рождении и для детей школьного возраста вызывает реактивность на туберкулин, которая сохраняется в течение 20–25 лет [48].Зарегистрированное снижение заболеваемости туберкулезом среди подростков в вакцинированном районе подчеркивает необходимость поддерживать и, по возможности, активизировать профилактические меры и меры по выявлению случаев во всех группах особого риска [49], но также может указывать на то, что продолжение массового предложения В идеале вакцинация БЦЖ должна проводиться повсюду, включая регионы с низкой распространенностью ТБ [5]. Аналогичным образом, учитывая текущую заболеваемость туберкулезом в Финляндии и вероятность увеличения инфекций лимфатических узлов и повышения чувствительности к микобактериям окружающей среды, рекомендуется продолжить вакцинацию БЦЖ при рождении [37].
Одним из основных ограничений этого исследования является то, что размер выборки для сравнения встречаемости заболеваний между исследуемой и контрольной группами был слишком мал и, следовательно, статистически недостаточен для такого анализа. Кроме того, было бы практически невозможно отслеживать и регистрировать возникновение заболеваний в когортах, поскольку не существовало компьютеризированной системы, импортирующей данные из больниц или страховых агентств в медицинский центр, и пациенты не часто сами раскрывают такую медицинскую конфиденциальность.Соответственно, поскольку мы охватили все школы трех разных возрастных категорий на нашей территории, и на контрольной территории не было программы БЦЖ, мы сделали логическое предположение, что вакцинация была широко распространена на нашей территории и отсутствовала на другой. Однако серьезное ограничение этой гипотезы является предпосылкой второго предположения о том, что за период исследования не должно было произойти никакой значительной миграции и никаких существенных различий в распространенности латентной инфекции ТБ или доле взрослых случаев с положительным мазком мокроты.По всем этим причинам профилактическая часть этого исследования не так сильна и, соответственно, не была основной конечной точкой исследования.
Кроме того, было бы практически невозможно отслеживать и регистрировать возникновение заболеваний в когортах, поскольку не существовало компьютеризированной системы, импортирующей данные из больниц или страховых агентств в медицинский центр, и пациенты не часто сами раскрывают такую медицинскую конфиденциальность.Соответственно, поскольку мы охватили все школы трех разных возрастных категорий на нашей территории, и на контрольной территории не было программы БЦЖ, мы сделали логическое предположение, что вакцинация была широко распространена на нашей территории и отсутствовала на другой. Однако серьезное ограничение этой гипотезы является предпосылкой второго предположения о том, что за период исследования не должно было произойти никакой значительной миграции и никаких существенных различий в распространенности латентной инфекции ТБ или доле взрослых случаев с положительным мазком мокроты.По всем этим причинам профилактическая часть этого исследования не так сильна и, соответственно, не была основной конечной точкой исследования. Еще одним ограничением исследования является то, что нам не удалось продолжить наблюдение за всеми когортами, повторно протестировав их через несколько лет, чтобы оценить возрастные различия, которые могли быть существенными с точки зрения убывающей реакции. Дети 12-15-летних когорт закончили школу, когорты стали непоследовательными, и даже при наличии личных данных (адреса, телефоны) было крайне сложно вернуть людей в поликлинику.Однако реакция пациентов, прошедших повторное тестирование, может дать реалистичное представление о том, какая реакция могла быть обнаружена и в других возрастных группах.
Еще одним ограничением исследования является то, что нам не удалось продолжить наблюдение за всеми когортами, повторно протестировав их через несколько лет, чтобы оценить возрастные различия, которые могли быть существенными с точки зрения убывающей реакции. Дети 12-15-летних когорт закончили школу, когорты стали непоследовательными, и даже при наличии личных данных (адреса, телефоны) было крайне сложно вернуть людей в поликлинику.Однако реакция пациентов, прошедших повторное тестирование, может дать реалистичное представление о том, какая реакция могла быть обнаружена и в других возрастных группах.
Продолжение программ БЦЖ может легко стать мостом к наступающей эре противотуберкулезных вакцин нового поколения. Уже было показано, что вакцинация антигеном ESAT-6 от микобактерий туберкулеза, который является доминирующей мишенью для клеточного иммунитета на ранней стадии туберкулеза, доставляется в комбинации монофосфориллипида А и диметилдиоктадециламмония бромида, которые являются эффективными адъювантами. для индукции клеточного и гуморального иммунного ответа, вызывал сильный ESAT-6-специфический Т-клеточный ответ и защитный иммунитет, сравнимый с таковым, достигнутым с помощью Mycobacterium bovis BCG [50].Поскольку одна треть населения мира уже инфицирована Mycobacterium tuberculosis и поскольку приобретенный иммунный ответ опосредуется различными наборами Т-клеток, могут потребоваться вакцины двух типов: одна для искоренения уже установленной инфекции, а другая — для быстрой борьбы с ней. вторжение микробов [51]. Между тем, особое внимание следует уделять важности качества, транспортировке и сохранности вакцины, а также методам применения [10], которые могут быть причиной широко расходящихся результатов проспективных испытаний вакцины БЦЖ в нескольких странах, которые привели к к текущим сомнениям в эффективности вакцинации БЦЖ в профилактике туберкулеза.
для индукции клеточного и гуморального иммунного ответа, вызывал сильный ESAT-6-специфический Т-клеточный ответ и защитный иммунитет, сравнимый с таковым, достигнутым с помощью Mycobacterium bovis BCG [50].Поскольку одна треть населения мира уже инфицирована Mycobacterium tuberculosis и поскольку приобретенный иммунный ответ опосредуется различными наборами Т-клеток, могут потребоваться вакцины двух типов: одна для искоренения уже установленной инфекции, а другая — для быстрой борьбы с ней. вторжение микробов [51]. Между тем, особое внимание следует уделять важности качества, транспортировке и сохранности вакцины, а также методам применения [10], которые могут быть причиной широко расходящихся результатов проспективных испытаний вакцины БЦЖ в нескольких странах, которые привели к к текущим сомнениям в эффективности вакцинации БЦЖ в профилактике туберкулеза.
Обзор иммунотерапии БЦЖ, Механизм действия БЦЖ, Противопоказания к БЦЖ
Автор
Кара Н. Бабаян, доктор медицины, FACS Доцент, директор урологической онкологии, отделение урологии, Медицинский факультет Университета Южного Иллинойса
Бабаян, доктор медицины, FACS Доцент, директор урологической онкологии, отделение урологии, Медицинский факультет Университета Южного Иллинойса
Кара Н. Бабаян, доктор медицины, FACS является членом следующих медицинских обществ: Американский колледж хирургов , Американское общество клинической онкологии, Американская урологическая ассоциация, Европейская ассоциация урологов, Северо-центральная секция Американской урологической ассоциации (AUA), Общество урологической онкологии, Общество женщин в урологии
Раскрытие информации: участие в клинических испытаниях для: Janssen .
Соавтор (ы)
Паркер Дж. Адамс, BS , доктор медицинских наук, кандидат медицинских наук, Университет медицины и биологических наук Канзас-Сити, Колледж остеопатической медицины
Паркер Дж. Адамс, бакалавр наук, является членом следующих медицинских обществ: Американская урологическая ассоциация
Раскрытие: нечего раскрывать.
Кортни МакКлюр, DO Врач-резидент, Отделение урологии, Ascension Healthcare
Раскрытие информации: Ничего не говорится.
Брэндон Томпкинс, BS , кандидат наук, Канзас-Ситиский университет медицины и биологических наук, Колледж остеопатической медицины
Раскрытие: Ничего не разглашать.
Меган МакМюррей, DO Врач-резидент, отделение урологии, Медицинский факультет Университета Южного Иллинойса
Меган МакМюррей, DO является членом следующих медицинских обществ: Американской ассоциации клинических урологов, Американской ассоциации урологов, Ассоциации женщин-хирургов, Общество женщин-урологов
Раскрытие информации: нечего раскрывать.
Специальная редакционная коллегия
Франсиско Талавера, фармацевт, доктор философии Адъюнкт-профессор, Фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие информации: Получил зарплату от Medscape за работу. для: Medscape.
для: Medscape.
Главный редактор
Брэдли Филдс Шварц, DO, FACS Профессор урологии, директор Центра лапароскопии и эндоурологии, Департамент хирургии, Медицинская школа Университета Южного Иллинойса
Брэдли Филдс Шварц, DO, FACS является членом следующих медицинских обществ: Американский колледж хирургов, Американская урологическая ассоциация, Ассоциация военных врачей-остеопатов и хирургов, Эндурологическое общество, Общество лапароэндоскопических хирургов, Общество университетских урологов
Раскрытие информации: Служить (d) в качестве директора, офицера, партнера, сотрудника, советника, консультанта или попечитель: Совет директоров Общества эндоурологов; Избранный президент Северо-Центральная секция Американской ассоциации урологов
Служить (d) в качестве докладчика или члена бюро докладчиков для: Cook Medical.
Дополнительные участники
Гэри Дэвид Стейнберг, доктор медицинских наук, FACS Профессор и директор программы по борьбе с раком мочевого пузыря Голдштейна, Нью-Йоркский университет Langone Health
Гэри Дэвид Стейнберг, доктор медицины, FACS является членом следующих медицинских обществ: Американской ассоциации исследований рака, Американского колледжа хирургов , Американское общество клинической онкологии, Американская урологическая ассоциация, Международное общество урологов, Общество лапароэндоскопических хирургов, Общество урологической онкологии
Раскрытие информации: Natera, FKD, Ferring, EnGene Bio, SesenBio, BioCanCell, Nucleix, Ipsen, Combat Medical, Astellas , Fergene, Dendreon, Abbvie, Seattle Genetics. для: Heat Biologics; CG Онкология; PhotoCure; Мерк; Roche / Genentech; Цикломед; Taris Biomedical; MDxHealth; Fidia Farmaceuticals; Уроген; Ферринг; Адуро; Boston Scientific; Бристоль Майерс Сквибб, Астра Зенека; Pfizer; Янссен; Epivax Therapeutics; Натера, ФКД ,.
для: Heat Biologics; CG Онкология; PhotoCure; Мерк; Roche / Genentech; Цикломед; Taris Biomedical; MDxHealth; Fidia Farmaceuticals; Уроген; Ферринг; Адуро; Boston Scientific; Бристоль Майерс Сквибб, Астра Зенека; Pfizer; Янссен; Epivax Therapeutics; Натера, ФКД ,.
Куш Сачдева, доктор медицины Southern Oncology and Hematology Associates, Inspira Health Network
Раскрытие информации: раскрывать нечего.
Брендан Курти, доктор медицины Директор, исследования в области мочеполовой онкологии, Центр исследования рака им. Роберта В. Франца, Исследовательский институт Эрла Чайлса, Онкологический центр Провиденс
Брендан Курти, доктор медицины, является членом следующих медицинских обществ: Американского колледжа врачей, Американского Общество клинической онкологии, Медицинская ассоциация Орегона, Общество иммунотерапии рака
Раскрытие информации: выступать (d) в качестве докладчика или члена бюро докладчиков для: Prometheus Pharmaceuticals, BMS
Получил исследовательский грант от: Prometheus Pharmaceuticals, Viralytics, MedImmune, BMS, Galectin Therapeutics.
Баги Р.П. Яна, доктор медицины, магистр делового администрирования, MHA, FACP Профессор онкологической медицины, Онкологический центр Андерсона; Профессор медицины Медицинского отделения Техасского университета в Галвестоне
Баги Р.П. Яна, доктор медицины, магистр делового администрирования, MHA, FACP является членом следующих медицинских обществ: Американского онкологического общества, Американской медицинской ассоциации, Американского общества клинической онкологии, SWOG
Раскрытие информации: нечего раскрывать.
Санджай Дж. Патель, доктор медицины Сотрудник по урологической онкологии, отделение хирургии, отделение урологии, Медицинский центр Чикагского университета
Санджай Дж. Патель, доктор медицины, является членом следующих медицинских обществ: Общество урологической онкологии
Раскрытие информации: Нечего раскрывать.
Благодарности
webmd.com»> Марк Х. Кац, доктор медицинских наук, научный сотрудник по урологической онкологии и малоинвазивной хирургии, Медицинский центр Чикагского университета
Марк Х. Кац, доктор медицинских наук, является членом следующих медицинских обществ: Alpha Omega Alpha, Американской урологической ассоциации, эндоурологического общества и Общества урологической онкологии
Раскрытие: Ничего не раскрывать.
Дэн Теодореску, доктор медицины, доктор философии Пол А. Банн, профессор исследований рака, профессор хирургии и фармакологии, директор Центра комплексного лечения рака Университета Колорадо
Дэн Теодореску, доктор медицины, доктор философии является членом следующих медицинских обществ: Американского онкологического общества, Американского колледжа хирургов, Американской ассоциации урологов, Медицинского общества Вирджинии, Общества фундаментальных урологических исследований и Общества урологической онкологии
.
Раскрытие информации: Доля участия в ключевой Genomics Соучредитель — 50% владения акциями; Членство в Правлении опционов на акции KromaTiD, Inc.
Обзор вакцины БЦЖ от туберкулеза (ТБ)
Вакцина БЦЖ защищает от туберкулеза, также известного как туберкулез.
ТБ — серьезная инфекция, поражающая легкие, а иногда и другие части тела, такие как мозг (менингит), кости, суставы и почки.
Узнайте больше о туберкулезе (ТБ)
Кому и когда следует делать вакцину БЦЖ
Вакцина БЦЖ (расшифровывается как вакцина Bacillus Calmette-Guérin) не является частью плановой вакцинации NHS.
Его выдают в NHS только в том случае, если предполагается, что ребенок или взрослый имеют повышенный риск контакта с туберкулезом.
Вакцину БЦЖ следует вводить только один раз в жизни.
БЦЖ для младенцев
Вакцинация БЦЖ рекомендуется детям до 1 года, которые:
- родились в районах Великобритании с высокими показателями ТБ
- имеют одного из родителей или бабушек или дедушек, родившихся в стране высокий уровень туберкулеза
- живут или находятся в тесном контакте с кем-то с инфекционным туберкулезом
Если вашему ребенку рекомендована вакцина БЦЖ, она обычно будет предложена в возрасте около 28 дней.
Это может быть предложено в больнице, местном медицинском центре или, иногда, в приемном отделении терапевта.
БЦЖ для детей в возрасте 16 лет и младше
Вакцинация БЦЖ также может быть рекомендована для детей старшего возраста с повышенным риском развития ТБ, например:
- детей, чьи родители или бабушка или дедушка родились в стране, где есть высокий уровень заболеваемости туберкулезом
- ребенка, недавно прибывшего из стран с высоким уровнем заболеваемости туберкулезом, включая страны Африки, Индийского субконтинента, некоторых частей Юго-Восточной Азии, некоторых частей Южной и Центральной Америки и некоторых частей Ближнего Востока
- ребенка которые будут жить с местным населением в течение 3 месяцев или дольше в странах с высоким уровнем заболеваемости туберкулезом
- детей, которые живут или находятся в тесном контакте с кем-то с инфекционным туберкулезом
БЦЖ для взрослых
Вакцинация БЦЖ проводится редко. любому человеку старше 16 лет, потому что нет достаточных доказательств того, что он хорошо работает у взрослых.
любому человеку старше 16 лет, потому что нет достаточных доказательств того, что он хорошо работает у взрослых.
Но его дают взрослым в возрасте от 16 до 35 лет, которые подвержены риску заболевания туберкулезом в результате своей работы, например, некоторым медицинским работникам, ветеринарам и работникам скотобойни.
Если вам предлагается вакцинация БЦЖ как взрослому, она обычно будет организована через местный отдел гигиены труда.
Узнайте больше о том, кому следует делать вакцину БЦЖ
Как проводится вакцинация БЦЖ
Вакцинация БЦЖ делается в виде инъекции в левое плечо.
После вакцинации обычно остается небольшой шрам.
Насколько эффективна вакцина БЦЖ
Вакцина БЦЖ изготовлена из ослабленного штамма бактерий ТБ. Поскольку бактерии в вакцине слабы, они запускают иммунную систему для защиты от инфекции, но не вызывают туберкулез.
Поскольку бактерии в вакцине слабы, они запускают иммунную систему для защиты от инфекции, но не вызывают туберкулез.
Обеспечивает постоянную защиту от самых тяжелых форм туберкулеза, таких как туберкулезный менингит у детей.
Он менее эффективен для профилактики туберкулеза, поражающего легкие у взрослых, поэтому оказывает ограниченное влияние на распространение туберкулеза.
Прочтите информационный буклет для пациента по вакцине БЦЖ AJV (PDF, 272kb)
Прочтите ответы на общие вопросы о вакцине БЦЖ против туберкулеза
Побочные эффекты вакцины БЦЖ
Как и все вакцины, вакцина БЦЖ может вызывать побочные эффекты, но они нечасты и обычно легкие.
Некоторые общие побочные эффекты могут включать:
- болезненность или выделения из места инъекции
- высокая температура (лихорадка)
- головная боль
- опухшие железы под подмышкой в руке, в которую была сделана инъекция
Более серьезные осложнения, такие как абсцессы, воспаление костей и широко распространенный туберкулез, возникают редко.
У большинства детей появляется язва в месте инъекции. После заживления рана может оставить небольшой шрам. Это нормально, волноваться не о чем.
Серьезные побочные эффекты вакцины БЦЖ, такие как тяжелая аллергическая реакция (анафилаксия), очень редки.
Схема желтой карточки позволяет сообщать о предполагаемых побочных эффектах вакцины. Он находится в ведении службы контроля безопасности лекарственных средств, Агентства по регулированию лекарственных средств и товаров медицинского назначения (MHRA).
Узнайте больше о побочных эффектах вакцинации БЦЖ
Сравнение ранней и поздней вакцинации БЦЖ младенцев, контактировавших с ВИЧ-1 в Уганде: протокол рандомизированного контролируемого исследования | Испытания
Эльгеро Э., Симондон К.Б., Вогелад Дж., Марра А., Симондон Ф. Неспецифические эффекты вакцинации на выживаемость детей? Перспективное исследование в Сенегале. Trop Med Int Health. 2005. 10 (10): 956–60.
Trop Med Int Health. 2005. 10 (10): 956–60.
PubMed Статья Google Scholar
Кришнан А., Шривастава Р., Двиведи П., Нг Н., Бьясс П., Пандав К.С. Неспецифический дифференцированный по полу эффект вакцинации АКДС может частично объяснить повышенную смертность девочек в Баллабгархе, Индия.Trop Med Int Health. 2013. 18 (11): 1329–37.
Аби П., Бенн С.С., Нильсен Дж., Равн Х. Неспецифические эффекты БЦЖ и АКДС, дифференцированные по полу, в Себу, Филиппины. Int J Epidemiol. 2009. 38 (1): 320–3. ответ автора 323-324.
PubMed Статья Google Scholar
Шенн Ф. Неспецифические эффекты вакцин и расширенная программа иммунизации. J Infect Dis. 2011. 204 (2): 182–4.
PubMed Статья Google Scholar
Шенн Ф. Неспецифические эффекты вакцин. Arch Dis Child. 2010. 95 (9): 662–7.
PubMed Статья Google Scholar
Hirve S, Bavdekar A, Juvekar S, Benn CS, Nielsen J, Aaby P. Неспецифические и дифференцированные по полу эффекты вакцинации на выживаемость детей в сельских районах западной Индии. Вакцина. 2012. 30 (50): 7300–8.
PubMed Статья Google Scholar
Рот А., Гарли М.Л., Дженсен Х., Нильсен Дж., Оби П. Вакцинация против бактерий Кальметта-Герена и младенческая смертность. Экспертные ревакцины. 2006; 5 (2): 277–93.
PubMed Статья Google Scholar
Shann F. Комментарий: вакцинация БЦЖ снижает неонатальную смертность наполовину. Pediatr Infect Dis J. 2012; 31 (3): 308–9.
PubMed Статья Google Scholar
Aaby P, Roth A, Ravn H, Napirna BM, Rodrigues A, Lisse IM, Stensballe L, Diness BR, Lausch KR, Lund N, et al. Рандомизированное испытание вакцинации БЦЖ при рождении детям с низкой массой тела при рождении: положительные неспецифические эффекты в неонатальном периоде? J Infect Dis. 2011. 204 (2): 245–52.
Рандомизированное испытание вакцинации БЦЖ при рождении детям с низкой массой тела при рождении: положительные неспецифические эффекты в неонатальном периоде? J Infect Dis. 2011. 204 (2): 245–52.
CAS PubMed Статья Google Scholar
Биринг-Соренсен С., Оби П., Напирна Б.М., Рот А., Равн Х., Родригес А., Уиттл Х., Бенн С.С.. Небольшое рандомизированное исследование среди детей с низкой массой тела при рождении, получивших вакцинацию против бациллы Кальметта-Герена при первом обращении в медицинский центр.Pediatr Infect Dis J. 2012; 31 (3): 306–8.
PubMed Статья Google Scholar
Roth AE, Stensballe LG, Garly ML, Aaby P. Благоприятные нецелевые эффекты БЦЖ — этические последствия для предстоящего внедрения новых противотуберкулезных вакцин. Туберкулез (Edinb). 2006. 86 (6): 397–403.
CAS Статья Google Scholar
Stensballe LG, Nante E, Jensen IP, Kofoed PE, Poulsen A, Jensen H, Newport M, Marchant A, Aaby P.Острые инфекции нижних дыхательных путей и респираторно-синцитиальный вирус у младенцев в Гвинее-Бисау: положительный эффект вакцинации БЦЖ для девочек, исследование методом случай-контроль. Вакцина. 2005. 23 (10): 1251–7.
CAS PubMed Статья Google Scholar
Джейсон Дж., Арчибальд Л.К., Нваньянву О.К., Казембе П.Н., Чатт Дж. А., Нортон Е., Добби Х., Джарвис В. Р.. Клиническое и иммунное влияние Mycobacterium bovis вакцинация БЦЖ рубцы.Заражение иммунной. 2002. 70 (11): 6188–95.
CAS PubMed PubMed Central Статья Google Scholar
Нанкабирва В., Тамвин Дж. К., Мугаба П.М., Тиллескар Т., Зоммерфельт Н., Группа P-ES. Выживание детей и вакцинация БЦЖ: проспективное когортное исследование на уровне общины в Уганде. BMC Public Health. 2015; 15: 175.
PubMed PubMed Central Статья Google Scholar
Rousseau MC, Parent ME, St-Pierre Y. Потенциальные последствия для здоровья от неспецифической стимуляции иммунной функции в раннем возрасте: пример вакцинации БЦЖ. Pediatr Allergy Immunol. 2008. 19 (5): 438–48.
PubMed Статья Google Scholar
Aaby P, Shaheen SO, Heyes CB, Goudiaby A, Hall AJ, Shiell AW, Jensen H, Marchant A. Ранняя вакцинация БЦЖ и снижение атопии в Гвинее-Бисау. Clin Exp Allergy. 2000. 30 (5): 644–50.
CAS PubMed Статья Google Scholar
Ota MO, van der Sande MA, Walraven GE, Jeffries D, Nyan OA, Marchant A, McAdam KP. Отсутствие связи между гиперчувствительностью замедленного типа к туберкулину и атопией у детей в Гамбии. Clin Exp Allergy. 2003. 33 (6): 731–6.
CAS PubMed Статья Google Scholar
Choi IS, Koh YI.Терапевтические эффекты вакцинации БЦЖ у взрослых пациентов с астмой: рандомизированное контролируемое исследование. Ann Allergy Asthma Immunol. 2002. 88 (6): 584–91.
PubMed Статья Google Scholar
Эллиотт А.М., Накииинги Дж., Куигли М.А., Френч Н., Гилкс К.Ф., Уитворт Д.А. Обратная связь между иммунизацией БЦЖ и заражением кишечными нематодами среди ВИЧ-1-позитивных людей в Уганде. Ланцет. 1999. 354 (9183): 1000–1.
CAS PubMed Статья Google Scholar
Barreto ML, Rodrigues LC, Silva RC, Assis AM, Reis MG, Santos CA, Blanton RE. Снижение заболеваемости, распространенности и интенсивности инфекции у детей с шрамом от вакцинации Bacillus Calmette-Guerin. J Infect Dis. 2000. 182 (6): 1800–3.
CAS PubMed Статья Google Scholar
Рэндалл А.Е., Перес М.А., Флойд С., Блэк Г.Ф., Крампин А.С., Нгвира Б., Пистони В.Н., Мулава Д., Сичали Л., Мваунгулу Л. и др. Характер заражения гельминтами и связь с вакцинацией БЦЖ в округе Каронга на севере Малави.Trans R Soc Trop Med Hyg. 2002. 96 (1): 29–33.
CAS PubMed Статья Google Scholar
Всемирная организация здравоохранения. Глобальный доклад о туберкулезе, 2013 г. Женева: Всемирная организация здравоохранения; 2013.
Google Scholar
Рабочая группа SAGE по неспецифическим эффектам вакцин (март 2013 г. — июнь 2013 г.). http://www.who.int/immunization/sage/sage_wg_non_specific_effects_vaccines_march3013/en/.По состоянию на 15 декабря 2015 г.
Fine PE, Williams TN, Aaby P, Kallander K, Moulton LH, Flanagan KL, Smith PG, Benn CS, Working Group on Non-specific Effects of Vaccines. Эпидемиологические исследования «неспецифических эффектов» вакцин: I – сбор данных в обсервационных исследованиях. Trop Med Int Health. 2009. 14 (9): 969–76.
PubMed Статья Google Scholar
Фаррингтон С.П., Ферт М.Дж., Моултон Л.Х., Равн Х., Андерсен П.К., Эванс С., Рабочая группа по неспецифическим эффектам вакцин.Эпидемиологические исследования неспецифических эффектов вакцин: II – методологические вопросы планирования и анализа когортных исследований. Trop Med Int Health. 2009. 14 (9): 977–85.
CAS PubMed Статья Google Scholar
Кристенсен И., Оби П., Дженсен Х. Рутинные вакцинации и выживаемость детей: последующее исследование в Гвинее-Бисау, Западная Африка. BMJ. 2000. 321 (7274): 1435–8.
CAS PubMed PubMed Central Статья Google Scholar
Vaugelade J, Pinchinat S, Guiella G, Elguero E, Simondon F. Неспецифические эффекты вакцинации на выживаемость детей: проспективное когортное исследование в Буркина-Фасо. BMJ. 2004; 329 (7478): 1309.
CAS PubMed PubMed Central Статья Google Scholar
Кандасами Р., Войси М., Маккуэйд Ф., де Ни К., Райан Р., Орр О., Улиг Ю., Санде С., О’Коннор Д., Поллард А.Дж. Неспецифические иммунологические эффекты выбранных плановых детских иммунизаций: систематический обзор.BMJ. 2016; 355: i5225.
PubMed PubMed Central Статья Google Scholar
Хиггинс Дж. П., Соарес-Вайзер К., Лопес-Лопес Дж. А., Какуру А., Чаплин К., Кристенсен Х., Мартин Н. К., Стерн Дж. А., Рейнгольд А. Л.. Связь вакцины, содержащей БЦЖ, АКДС и кори, с детской смертностью: систематический обзор. BMJ. 2016; 355: i5170.
PubMed PubMed Central Статья Google Scholar
Уилсон CB. Применение современной иммунологии для выяснения гетерологичных эффектов детских вакцин и лучшего информирования о методах иммунизации матери и ребенка. Фронт Иммунол. 2015; 6: 64.
PubMed PubMed Central Статья Google Scholar
Netea MG, Quintin J, van der Meer JW. Тренированный иммунитет: память о врожденной защите хозяина. Клеточный микроб-хозяин. 2011; 9 (5): 355–61.
CAS PubMed Статья Google Scholar
Саид С., Квинтин Дж., Керстенс Х. Х., Рао Н. А., Агаджанирефа А., Матарез Ф., Ченг С. К., Рэттер Дж., Берентсен К., ван дер Энт М. А. и др. Эпигенетическое программирование дифференцировки моноцитов и макрофагов и тренированный врожденный иммунитет. Наука. 2014; 345 (6204): 1251086.
PubMed PubMed Central Статья Google Scholar
Kleinnijenhuis J, Quintin J, Preijers F, Joosten LA, Ifrim DC, Saeed S, Jacobs C., van Loenhout J, de Jong D, Stunnenberg HG, et al.Бацилла Кальметта-Герена индуцирует NOD2-зависимую неспецифическую защиту от повторного заражения посредством эпигенетического репрограммирования моноцитов. Proc Natl Acad Sci U S. A. 2012; 109 (43): 17537–42.
CAS PubMed PubMed Central Статья Google Scholar
Селин Л.К., Варга С.М., Вонг IC, Валлийский РМ. Защитный гетерологичный противовирусный иммунитет и усиленный иммунопатогенез, опосредованный популяциями Т-клеток памяти. J Exp Med. 1998. 188 (9): 1705–15.
CAS PubMed PubMed Central Статья Google Scholar
Маццола Т.Н., да Силва М.Т., Абрамчук Б.М., Морено Ю.М., Лима СК, Зорзето Т.К., Пассето А.С., Вилела М.М. Нарушение клеточного иммунного ответа Bacillus Calmette-Guerin у неинфицированных младенцев, контактировавших с ВИЧ. СПИД. 2011. 25 (17): 2079–87.
PubMed Статья Google Scholar
Hesseling AC, Cotton MF, Fordham von Reyn C, Graham SM, Gie RP, Hussey GD.Заявление о консенсусе по пересмотренным рекомендациям Всемирной организации здравоохранения по вакцинации БЦЖ у ВИЧ-инфицированных младенцев. Int J Tuberc Lung Dis. 2008. 12 (12): 1376–9.
CAS PubMed Google Scholar
Hesseling AC, Caldwell J, Cotton MF, Eley BS, Jaspan HB, Jennings K, Marais BJ, Nuttall J, Rabie H, Roux P и др. Вакцинация БЦЖ младенцев, контактировавших с ВИЧ в Южной Африке, — риски и преимущества. С. Афр Мед Ж. 2009; 99 (2): 88–91.
CAS PubMed PubMed Central Google Scholar
Miles DJ, Gadama L, Gumbi A, Nyalo F, Makanani B, Heyderman RS. Инфекция вируса иммунодефицита человека (ВИЧ) во время беременности индуцирует дифференцировку Т-лимфоцитов CD4 и модулирует ответы на вакцину Бациллы Кальметта-Герена (БЦЖ) у младенцев, не инфицированных ВИЧ. Иммунология. 2010. 129 (3): 446–54.
CAS PubMed PubMed Central Статья Google Scholar
Ota MO, O’Donovan D, Marchant A, Yamuah L, Harding E, Jaffar S, McAdam KP, Corrah T., Whittle H. ВИЧ-отрицательные младенцы, рожденные от ВИЧ-1, но не ВИЧ-2-положительные матери, не развиваются шрам Bacillus Calmette-Guerin. СПИД. 1999. 13 (8): 996–8.
CAS PubMed Статья Google Scholar
Мселлати П., Дабис Ф., Лепаж П., Хитимана Д.Г., Ван Гетем К., Ван де Перре П. Вакцинация БЦЖ и детская ВИЧ-инфекция — Руанда, 1988–1990.MMWR. 1991. 40 (48): 833–6.
Google Scholar
Garly ML, Martins CL, Bale C, Balde MA, Hedegaard KL, Gustafson P, Lisse IM, Whittle HC, Aaby P. Шрам от БЦЖ и положительная реакция на туберкулин, связанные со снижением детской смертности в Западной Африке. А неспецифический положительный эффект БЦЖ? Вакцина. 2003. 21 (21-22): 2782–90.
PubMed Статья Google Scholar
Клеричи М., Сареселла М., Коломбо Ф., Фоссати С., Сала Н., Брикалли Д., Вилла М.Л., Ферранте П., Далли Л., Вигано А. Нарушения созревания Т-лимфоцитов у неинфицированных новорожденных и детей с вертикальным контактом с ВИЧ. Кровь. 2000. 96 (12): 3866–71.
CAS PubMed Google Scholar
Nielsen SD, Jeppesen DL, Kolte L, Clark DR, Sorensen TU, Dreves AM, Ersboll AK, Ryder LP, Valerius NH, Nielsen JO. Нарушение функции клеток-предшественников у ВИЧ-отрицательных младенцев от ВИЧ-положительных матерей приводит к снижению выработки тимуса и снижению числа CD4.Кровь. 2001. 98 (2): 398–404.
CAS PubMed Статья Google Scholar
Эмбри Дж., Буэйо Дж., Нагелькерке Н., Ньенга С., Ньянге П., Ндинья-Ахола Дж., Памба Х, Пламмер Ф. Субпопуляции лимфоцитов у детей, инфицированных и неинфицированных вирусом иммунодефицита человека типа 1, в Найроби. Pediatr Infect Dis J. 2001; 20 (4): 397–403.
CAS PubMed Статья Google Scholar
Chougnet C, Kovacs A, Baker R, Mueller BU, Luban NL, Liewehr DJ, Steinberg SM, Thomas EK, Shearer GM. Влияние материнской среды, инфицированной вирусом иммунодефицита человека, на развитие продукции детского интерлейкина-12. J Infect Dis. 2000. 181 (5): 1590–7.
CAS PubMed Статья Google Scholar
Кун Л., Коутсудис А., Мудли Д., Мнгкунданисо Н., Трабаттони Д., Ширер Г. М., Клеричи М., Кувадия Х. М.. Продукция интерферона-гамма и интерлейкина-10 среди ВИЧ-1-инфицированных и неинфицированных младенцев ВИЧ-1-инфицированных матерей.Pediatr Res. 2001. 50 (3): 412–6.
CAS PubMed Статья Google Scholar
Леви Дж. А., Сюэ Ф, Блэкборн Диджей, Вара Д., Вайнтруб ПС. Нецитотоксическая противовирусная активность клеток CD8 у детей, инфицированных и неинфицированных вирусом иммунодефицита человека. J Infect Dis. 1998. 177 (2): 470–2.
CAS PubMed Статья Google Scholar
Кагина Б.М., Абель Б., Боумейкер М., Скриба Т.Дж., Гелдерблоэм С., Смит Э., Эразмус М., Нене Н., Вальцл Г., Блэк Г. и др.Отсрочка вакцинации БЦЖ с рождения до возраста 10 недель может привести к усилению Т-клеточного ответа CD4 в памяти. Вакцина. 2009. 27 (40): 5488–95.
CAS PubMed PubMed Central Статья Google Scholar
Блэкни А.К., Чакут, Коннектикут, Хесселинг А.С., Кидзеру Э.Б., Джонс С.Э., Пассмор Дж.А., Содора Д.Л., Грей CM, Джаспан HB. Отсроченная вакцинация БЦЖ приводит к минимальным изменениям Т-клеточной иммуногенности бесклеточных иммунизаций против коклюша и столбняка у новорожденных, контактировавших с ВИЧ.Вакцина. 2015; 33 (38): 4782–9.
CAS PubMed PubMed Central Статья Google Scholar
ЮНЭЙДС. Глобальный отчет: отчет ЮНЭЙДС о глобальной эпидемии СПИДа 2010. 2010.
Обновленная информация об эпидемии СПИДа, региональное резюме: Африка к югу от Сахары. http://data.unaids.org/pub/Report/2008/JC1526_epibriefs_subsaharanafrica_en.pdf. По состоянию на 20 января 2014 г.
Mofenson LM. Достижения в профилактике вертикальной передачи вируса иммунодефицита человека.Semin Pediatr Infect Dis. 2003. 14 (4): 295–308.
PubMed Статья Google Scholar
Аганги А., Торн С., Ньюэлл М.Л. Повышение вероятности дальнейших живорождений у ВИЧ-инфицированных женщин в последние годы. BJOG. 2005. 112 (7): 881–8.
PubMed Статья Google Scholar
Филто С. Неинфицированный африканский ребенок, контактировавший с ВИЧ. Trop Med Int Health.2009. 14 (3): 276–87.
PubMed Статья Google Scholar
Афран Л., Гарсия Найт М., Ндуати Е., Урбан БК, Хейдерман Р.С., Роуленд-Джонс С.Л. Неинфицированные дети, контактирующие с ВИЧ: растущее население с уязвимой иммунной системой? Clin Exp Immunol. 2014; 176 (1): 11–22.
CAS PubMed PubMed Central Статья Google Scholar
Slogrove A, Reikie B, Naidoo S, De Beer C, Ho K, Cotton M, Bettinger J, Speert D, Esser M, Kollmann T.Неинфицированные младенцы, контактировавшие с ВИЧ, подвергаются повышенному риску тяжелых инфекций в первый год жизни. J Trop Pediatr. 2012. 58 (6): 505–8.
Slogrove AL, Cotton MF, Esser MM. Тяжелые инфекции у неинфицированных младенцев, контактировавших с ВИЧ: клинические доказательства иммунодефицита. J Trop Pediatr. 2010. 56 (2): 75–81.
CAS PubMed Статья Google Scholar
Taron-Brocard C, Le Chenadec J, Faye A, Dollfus C, Goetghebuer T., Gajdos V, Labaune JM, Perilhou A, Mandelbrot L, Blanche S и др.Повышенный риск серьезных бактериальных инфекций из-за подавления материнского иммунитета у неинфицированных младенцев, контактировавших с ВИЧ, в одной из европейских стран. Clin Infect Dis. 2014; 59 (9): 1332–45.
CAS PubMed Статья Google Scholar
Heresi GP, Caceres E, Atkins JT, Reuben J, Doyle M. Pneumocystis carinii пневмония у младенцев, которые подверглись воздействию вируса иммунодефицита человека, но не были инфицированы: исключение из определения случая эпиднадзора за СПИДом.Clin Infect Dis. 1997. 25 (3): 739–40.
CAS PubMed Статья Google Scholar
Адхикари М., Каучали С., Мудли А. Клинический профиль и картина заболеваемости младенцев, рожденных ВИЧ-инфицированными матерями в Дурбане, Южная Африка. Indian Pediatr. 2006. 43 (9): 804–8.
PubMed Google Scholar
фон Моллендорф С., фон Готтберг А., Темпиа С., Мейринг С., де Гувейя Л., Куан В., Ленгана С., Авенант Т., дю Плесси Н., Элей Б. и др.Повышенный риск и смертность от инвазивной пневмококковой инфекции у контактировавших с ВИЧ, но неинфицированных младенцев в возрасте <1 года в Южной Африке, 2009-2013 гг. Clin Infect Dis. 2015; 60 (9): 1346–56.
Артикул Google Scholar
Изаднегадар Р., Фокс М.П., Джина П., Кази С.А., Теа Д.М. Пересмотр пневмонии и контактного статуса у младенцев, рожденных от ВИЧ-инфицированных матерей. Pediatr Infect Dis J. 2014; 33 (1): 70–2.
PubMed Статья Google Scholar
Manicklal S, van Niekerk AM, Kroon SM, Hutto C, Novak Z, Pati SK, Chowdhury N, Hsiao NY, Boppana SB. Распространенность при рождении врожденного цитомегаловируса среди младенцев от ВИЧ-инфицированных женщин, получающих пренатальную антиретровирусную профилактику в Южной Африке. Clin Infect Dis. 2014. 58 (10): 1467–72.
CAS PubMed Статья Google Scholar
Пайфер Л.Л., Хьюз В.Т., Стагно С., Вудс Д. Инфекция Pneumocystis carinii : данные о высокой распространенности у здоровых детей и детей с ослабленным иммунитетом.Педиатрия. 1978; 61 (1): 35–41.
CAS PubMed Google Scholar
Кун Л., Касонде П., Синкала М., Канкаса К., Семрау К., Скотт Н., Цай В.Й., Вермунд С.Х., Альдрованди Г.М., Теа Д.М. Влияет ли тяжесть ВИЧ-инфекции у ВИЧ-инфицированных матерей на смертность и заболеваемость среди их неинфицированных младенцев? Clin Infect Dis. 2005. 41 (11): 1654–61.
PubMed PubMed Central Статья Google Scholar
Kleinnijenhuis J, Quintin J, Preijers F, Joosten LA, Jacobs C, Xavier RJ, van der Meer JW, van Crevel R, Netea MG. БЦЖ-индуцированный обученный иммунитет в NK-клетках: роль в неспецифической защите от инфекции. Clin Immunol. 2014; 155 (2): 213–9.
CAS PubMed PubMed Central Статья Google Scholar
Тиллескар Т., Джексон Д., Меда Н., Энгебретсен И.М., Чопра М., Диалло А.Х., Доэрти Т., Экстром ЕС, Фаднес Л.Т., Гога А. и др.Эксклюзивная пропаганда грудного вскармливания со стороны равных консультантов в Африке к югу от Сахары (PROMISE-EBF): кластерное рандомизированное исследование. Ланцет. 2011. 378 (9789): 420–7.
PubMed Статья Google Scholar
Всемирная организация здравоохранения. Стандарты роста детей ВОЗ: длина тела / рост к возрасту, масса тела к возрасту, масса тела к длине тела, масса тела к росту и индекс массы тела к возрасту: методы и разработка. Женева: Всемирная организация здравоохранения; 2006. с. 312.
Google Scholar
Всемирная организация здравоохранения. Надлежащая клиническая лабораторная практика (GCLP). Женева: Всемирная организация здравоохранения; 2009.
Каммингс П. Методы оценки скорректированных соотношений рисков. Стата Дж. 2009; 9 (2): 175–96.
Артикул Google Scholar
Шпигельман Д., Герцмарк Э. Простые расчеты SAS для соотношений риска или распространенности и различий.Am J Epidemiol. 2005. 162 (3): 199–200.
PubMed Статья Google Scholar
Zou G. Модифицированный подход регрессии Пуассона к проспективным исследованиям с бинарными данными. Am J Epidemiol. 2004. 159 (7): 702–6.
PubMed Статья Google Scholar
Исследовательская группа ДАМОКЛА. Предлагаемый устав комитетов по мониторингу данных клинических испытаний: помогать им хорошо выполнять свою работу.Ланцет. 2005; 365 (9460): 711–22.
Артикул Google Scholar
Grant AM, Altman DG, Babiker AB, Campbell MK, Clemens FJ, Darbyshire JH, Elbourne DR, McLeer SK, Parmar MK, Pocock SJ, et al. Проблемы мониторинга данных и промежуточного анализа исследований. Оценка медицинских технологий. 2005. 9 (7): 1–238. iii-iv.
CAS PubMed Статья Google Scholar
Siegfried N, van der Merwe L, Brocklehurst P, Sint TT.Антиретровирусные препараты для снижения риска передачи ВИЧ-инфекции от матери ребенку. Кокрановская база данных Syst Rev.2011; 7: CD003510.
Google Scholar
Rieder HL. Возможность заражения и риск заражения: топливо для пандемии туберкулеза. Инфекционное заболевание. 1995; 23 (1): 1–3.
CAS PubMed Статья Google Scholar
Kesho Bora Study G, de Vincenzi I.Тройной антиретровирусный препарат по сравнению с зидовудином и профилактикой однократной дозы невирапина во время беременности и грудного вскармливания для предотвращения передачи ВИЧ-1 от матери ребенку (исследование Кешо Бора): рандомизированное контролируемое исследование. Lancet Infect Dis. 2011; 11 (3): 171–80.
Артикул Google Scholar
Bernatowska EA, Wolska-Kusnierz B, Pac M, Kurenko-Deptuch M, Zwolska Z, Casanova JL, Piatosa B, van Dongen J, Roszkowski K, Mikoluc B, et al.Распространенная бацилла Кальметта-Герена, инфекция и иммунодефицит. Emerg Infect Dis. 2007. 13 (5): 799–801.
PubMed PubMed Central Статья Google Scholar
Правила и процедуры. https://helseforskning.etikkom.no/ikbViewer/page/reglerogrutiner/loverogregler?p_dim=34770&_ikbLanguageCode=us. По состоянию на 23 июня 2014 г.
Вакцинация БЦЖ — обзор
Биомаркеры, предсказывающие защиту
Вакцинация БЦЖ вызывает образование рубцов и реакцию клеток Th2 у младенцев. 10 Измерение интерферона-γ (IFNγ) — сигнатурного цитокина Th2, секретируемого в ответ на саму БЦЖ или на препараты перекрестно-реактивного микобактериального антигена, такие как Mycobacterium tuberculosis, очищенное производное белка (PPD) — может использоваться для надежного считывания иммуногенности. у подростков и младенцев Великобритании. 11,12 Однако, хотя мыши, которые не могут продуцировать IFNγ или отвечать на него, более восприимчивы к инфекции M. tuberculosis и не могут контролировать рост микобактерий, 13 прямое измерение IFNγ не является показателем защиты в модели мышей. 14,15 Фактически, количественное определение секреции IFNγ в ответ на пептиды из антигенов M. tuberculosis является основой двух коммерческих тестов для выявления инфекции M. tuberculosis или заболевания ТБ : QuantiFERON-TB Gold In Tube ( или более новый QuantiFERON-TB Plus) и T.SPOT-TB. Таким образом, обычно предполагается, что, хотя добавление IFNγ к мышиным макрофагам увеличивает их способность контролировать рост микобактерий, IFNγ необходим, но сам по себе недостаточен для защиты.
Можно было надеяться, что полифункциональные Т-клетки, которые продуцируют IFNγ, TNFα и IL-2, могут быть лучшим коррелятом защиты. 16 В дополнение к потенциально синергетическим эффектам продуцирования IL-2 и TNFα, а также IFNγ, исследование Darrah et al. 17, показали, что такие полифункциональные Т-клетки продуцируют больше IFNγ на клетку, чем те Т-клетки, которые продуцируют только IFNγ. Специфические для микобактерий полифункциональные Т-клетки индуцируются, когда иммунологически неопытным младенцам в Соединенном Королевстве дают БЦЖ в возрасте примерно от 3 до 4 месяцев, измеряя ответы, индуцированные в ответ на PPD через 4 или 12 месяцев после вакцинации. 18,19 Невакцинированные младенцы того же возраста, ценная контрольная группа, которая недоступна, за исключением стран, где некоторые, но не все дети получают вакцинацию БЦЖ, демонстрируют мало, если вообще какие-либо из этих микобактериальных антиген-специфичных полифункциональных Т-клеток. Однако эти исследования в условиях низкой заболеваемости туберкулезом не могут иметь в качестве конечной точки развитие болезни или защиту от нее. Таким образом, в последние годы в Южной Африке была проведена серия исследований, в которой чрезвычайно высока заболеваемость туберкулезом, что делает ее идеальным местом для испытаний вакцин. 20 В крупном исследовании, проведенном в Вустере недалеко от Кейптауна, которое обеспечило основу для новых исследований первичной бустерной вакцинации, было набрано достаточное количество младенцев (в общей сложности 5726), чтобы выявить заболевание ТБ в качестве конечной точки, что обеспечило иммунный ответ у тех, кто прогрессировал до туберкулеза в течение 2 лет для сравнения с контролем в домохозяйстве или сообществе. В этом знаменательном исследовании использовались строгие диагностические критерии с исследованиями, которые включали промывание желудка для подтверждения туберкулеза у детей, что обычно является диагностической проблемой. 21 Однако не было различий в частотах полифункциональных Т-клеток, в данном случае измеренных в цельной крови, в ответ на стимуляцию самой БЦЖ через 10 недель после вакцинации с последующим развитием туберкулеза, 22 и не было различий. в частотах Т-клеток, продуцирующих только IFNγ, или Т-клеток, продуцирующих IFNγ только с TNFα, или IFNγ с одним только IL-2. Однако стоит отметить, что частота всех изученных типов клеток сильно варьировала во всех трех группах.Заметная гетерогенность цитокиновых ответов наблюдалась также у вакцинированных БЦЖ младенцев из Гамбии с секрецией IFNγ, IL-5 и IL-13, индуцированной стимуляцией разведенной цельной крови PPD, BCG Ag85, фильтрата краткосрочной культуры M. tuberculosis. , или убило M. tuberculosis по данным ELISA. 23 В недавнем обзоре рассматривались доказательства того, что полифункциональные Т-клетки, специфичные для микобактерий, связаны с защитой от ТБ. 16 Специфичные для микобактерий полифункциональные Т-клетки могут быть индуцированы вакцинами-кандидатами различных типов, включая живые микобактериальные вакцины, вакцины с доставкой вирусного вектора и рекомбинантные белковые вакцины в адъюванте.Однако, хотя есть некоторые исследования, которые показывают связь полифункциональных Т-клеток, индуцированных вакцинацией, с эффективностью вакцины на мышиной модели, есть и другие исследования на мышах, а также исследование Kagina et al. у южноафриканских младенцев 22 , которые не обнаруживают такой ассоциации. 16
В последующем исследовании той же когорты южноафриканских младенцев использовался системный подход к биологии. 24 Никаких специфических, клеточных или цитокиновых сигнатур риска ТБ не было обнаружено в супернатантах от культур цельной крови, стимулированных БЦЖ, измеренных в анализе множественных шариков, а также не было различий в экспрессии маркеров цитотоксических Т-клеток, пролиферации Т-клеток, или частоты обнаруженных миелоидных или лимфоидных клеток.Возможно, более удивительно, что не было сигнатуры экспрессии генов, которая позволяла бы различать младенцев, которые впоследствии прогрессировали до заболевания, по сравнению с контрольной группой домохозяйств, сравнивая сигнатуры мононуклеарных клеток периферической крови (PBMC), стимулированных БЦЖ в течение 12 часов у младенцев в возрасте 10 недель. , вычтя экспрессию гена в нестимулированных культурах. Этот анализ действительно показал, что и случаи, и контроли можно разделить на две подгруппы или кластеры на основе их экспрессии гена, стимулированной БЦЖ, за вычетом экспрессии генов в нестимулированных культурах, хотя последующий анализ показал, что нестимулированные культуры PBMC также делились на те же кластеры. .Гены, характерные для миелоидных клеток и наборов противовоспалительных генов, были обнаружены связанными с одним кластером, а гены, связанные с Т-клетками, были активированы во втором кластере. Дальнейший анализ показал, что младенцы с самым высоким или самым низким соотношением моноцитов к Т-клеткам подвергались большему риску развития ТБ. Такая степень сложности и неоднородности может помочь объяснить, почему в таких исследованиях было трудно определить корреляты защиты и почему, например, более раннее исследование Kagina et al. 22 показали такую неоднородность частот полифункциональных Т-клеток.
Единственное другое опубликованное исследование, которое имело достаточный размер для того, чтобы иметь возможность прогрессировать до ТБ у новорожденных, вакцинированных БЦЖ, в качестве исхода использовало детей из исследования эффективности фазы 2b MVA85A. 25 Вакцина MVA85A, вводимая в качестве бустерной вакцины в возрасте от 4 до 6 месяцев, не смогла вызвать значительную защитную эффективность по сравнению с группой плацебо, которая получала Candin, хотя вакцина MVA85A была способна индуцировать IFNγ-секретирующие клетки к пептидам Ag85A. 26 При сравнении ответов 53 младенцев, у которых развился ТБ, с ответами в 205 подобранных контрольных группах, все из которых получали только БЦЖ, активированные Т-клетки, экспрессирующие HLA-DR, были выше у младенцев, которые прогрессировали до заболевания, а также у детей, прогрессирующих ТБ от другого ребенка. подростковая когорта. 25 В группе младенцев, у которых впоследствии развилось заболевание, скорость прогрессирования была выше у тех, у кого было наибольшее количество HLA-DR-экспрессирующих (активированных) Т-клеток, тогда как скорость прогрессирования была медленнее у тех, у кого было самое высокое количество стимулированных БЦЖ клеток, образующих пятно IFNγ, обнаруженных в анализе ELISPOT.
Необходимы дальнейшие исследования, чтобы выяснить, почему клетки, продуцирующие IFNγ, были связаны с защитой в исследовании Fletcher et al. 25 , но не в том, что было у Кагиной и др. 22 Хотя оба исследования проводились на младенцах из Южной Африки, вакцинированных БЦЖ, наблюдались различия в методологии и возрасте, в котором они изучались. В исследовании Fletcher et al., 25 младенцы были старше при кровотечении, от 4 до 6 месяцев, а не 10 недель, как в исследовании Kagina et al. 22 Исследование Флетчера имело больший размер выборки и использовало три контроля, соответствующих каждому младенцу. 25 Таким образом, в настоящее время, хотя ясно, что для защиты необходимы Т-клетки, продуцирующие IFNγ, необходимо подтверждение того, обеспечивают ли они коррелят защиты.
Вакцинация БЦЖ для защиты медицинских работников от COVID-19 — полный текст
| Госпиталь Святого Винсента, Сидней | |
| Сидней, Новый Южный Уэльс, Австралия, 2010 г. | |
| Больница принца Уэльского | |
| Сидней, Новый Южный Уэльс, Австралия, 2031 | |
| Детская больница Сиднея, Рандвик | |
| Сидней, Новый Южный Уэльс, Австралия, 2145 | |
| Детская больница в Вестмиде | |
| Сидней, Новый Южный Уэльс, Австралия, 2145 | |
| Больница Вестмид | |
| Сидней, Новый Южный Уэльс, Австралия, 2145 | |
| Королевская больница Аделаиды | |
| Аделаида, Южная Австралия, Австралия, 5000 | |
| Больница для женщин и детей | |
| Северная Аделаида, Южная Австралия, Австралия, 5006 | |
| Королевская детская больница | |
| Мельбурн, Виктория, Австралия, 3052 | |
| Epworth Richmond | |
| Мельбурн, Виктория, Австралия, 3121 | |
| Monash Health- Медицинский центр Монаш | |
| Мельбурн, Виктория, Австралия, 3168 | |
| Госпиталь Фионы Стэнли | |
| Мердок, Западная Австралия, Австралия, 6150 | |
| Perth Children’s Hospital | |
| Перт, Западная Австралия, Австралия, 6009 | |
| Госпиталь сэра Чарльза Гэрднера | |
| Перт, Западная Австралия, Австралия, 6009 | |
| Fundação de Medicina Tropical Dr Heitor Vieira Dourado (FMT-HVD) | |
| Манаус, Амазонас, Бразилия, 69040-000 | |
| Госпиталь Санта-Каса | |
| Campo Grande, Mato Grosso Do Sul, Brazil, 79002-230 | |
| CASSEMS Hospital | |
| Campo Grande, Mato Grosso Do Sul, Brazil, 79002-251 | |
| Federal University of Mato Grosso do Sul | |
| Campo Grande, Mato Grosso Do Sul, Brazil, 79070-900 | |
| Hospital Regional de Mato Grosso do Sul | |
| Campo Grande, Mato Grosso Do Sul, Brazil, 79084-180 | |
| Centro de Estudos da Saúde do Trabalhador e Ecologia Humana | |
| Рио-де-Жанейро, RJ, Бразилия, 22780-195 | |
| Centro de Referência Prof Hélio Fraga | |
| Рио-де-Жанейро, RJ, Бразилия, 22780-195 | |
| Noord West Ziekenhuis | |
| Алкмар, Нидерланды, 1815 JD | |
| Госпиталь Рейнстейт | |
| Арнем, Нидерланды, 6815 AD | |
| Больница Амфия | |
| Бреда, Нидерланды, 4818 CK | |
| Больница Святого Антония | |
| Nieuwegein, Нидерланды, 3435 CM | |
| Radboud UMC | |
| Неймеген, Нидерланды, 6525 GA | |
| Университетская больница в Утрехте (UMCU) | |
| Утрехт, Нидерланды, 3584 CX | |
| Университетская больница German Trias I Pujol | |
| Бадалона, Барселона, Испания, 08916 | |
| Университетская больница Мутуа Террасса | |
| Terrassa, Барселона, Испания, 08221 | |
| Университетская больница Крусес | |
| Баракальдо, Бискайя, Испания, 48903 | |
| Университетская больница Маркиза де Вальдесилья | |
| Сантандер, Испания, 39008 | |
| Университетская клиника Вирхен Макарена | |
| Севилья, Испания, 41009 | |
| Teign Estuary Medical Group | |
| Teignmouth, Девон, Великобритания, TQ14 8AB | |
| Ide Lane Surgery | |
| Альфингтон, Эксетер, Великобритания, EX2 8UP | |
| St Leonard’s Practice | |
| St Leonards, Эксетер, Великобритания, EX1 1SB | |
| Travel Clinic | |
| Exeter, United Kingdom, EX1 1PR | |
| Royal Devon and Exeter NHS Foundation Trust | |
| Эксетер, Великобритания, EX2 5DW | |
Внутрипузырная терапия рака мочевого пузыря
При внутрипузырной терапии врач вводит жидкое лекарство прямо в мочевой пузырь, а не вводит его внутрь или в кровь.Препарат вводится через мягкий катетер, который вводится в мочевой пузырь через уретру. Препарат остается в мочевом пузыре до 2 часов. Таким образом, лекарство может повлиять на клетки, выстилающие внутреннюю часть мочевого пузыря, не оказывая значительного воздействия на другие части вашего тела.
Когда применяется внутрипузырная терапия?
после ТУРБ
Внутрипузырная терапия обычно используется после трансуретральной резекции опухоли мочевого пузыря (ТУР мочевого пузыря). Часто это делается в течение 24 часов после процедуры ТУР.Некоторые специалисты говорят, что это нужно делать в течение 6 часов. Цель состоит в том, чтобы убить любые раковые клетки, которые могут остаться в мочевом пузыре.
Для лечения неинвазивного рака мочевого пузыря.
Эти виды рака встречаются только в слизистой оболочке мочевого пузыря. Их можно назвать неинвазивными (стадия 0) или малоинвазивный (стадия I) рак мочевого пузыря. Они не распространились в более глубокие слои мышц стенки мочевого пузыря или других частей тела. На ранних стадиях используется внутрипузырная химиотерапия. рак, потому что лекарства, принимаемые таким образом, в основном влияют на клетки, выстилающие внутреннюю часть мочевого пузыря.Они практически не влияют на другие клетки. Это означает, что любые раковые клетки за пределами оболочки мочевого пузыря, включая те, которые глубоко вросли в стенку мочевого пузыря, не лечатся внутрипузырной терапией. Лекарства, вводимые в мочевой пузырь, также не могут попасть в раковые клетки почек, мочеточников и уретры или те, которые распространились на другие части тела.
Одна доза внутрипузырной химиотерапии может быть единственным методом лечения неинвазивного рака.
Неинвазивный (низкосортный) рак мочевого пузыря низкого риска растет медленно.Их можно лечить 1 дозой внутрипузырной химиотерапии после ТУРМТ. Его используют, чтобы предотвратить возвращение рака.
Внутрипузырная химиотерапия или иммунотерапия может использоваться при промежуточном неинвазивном раке мочевого пузыря. Некоторые исследования показывают, что иммунотерапия работает лучше всего. Это делается один раз в неделю в течение 6 недель и при необходимости может повторяться еще 6 недель. Это называется индукционной терапией. После 4-6-недельного перерыва поддерживающее лечение проводится не менее 1 года.
Неинвазивный рак мочевого пузыря с высоким риском может быть быстрорастущим (высокозлокачественным), большим или может иметь место более одной опухоли. Им проводится индукционная внутрипузырная иммунотерапия. Если есть хороший ответ на индукционную терапию, за ней следует 3 года поддерживающей внутрипузырной иммунотерапии.
Графики поддерживающего лечения внутрипузырной иммунотерапией различаются. Например, лечение может проводиться от 3 до 6 недель каждый месяц, каждые 3 месяца или два раза в год. Это можно сделать от 1 до 3 лет.Ваш врач обсудит с вами лучший план, основанный на деталях вашего рака мочевого пузыря и его реакции на лечение.
Для лечения инвазивного рака мочевого пузыря более высоких стадий
Одна доза внутрипузырной химиотерапии выполняется в течение 24 часов после ТУР. Но другие виды лечения обычно являются следующими шагами при раке мочевого пузыря стадий II — IV (от 2 до 4), поскольку они распространились за пределы выстилающего слоя стенки мочевого пузыря.
Иногда индукционная и поддерживающая внутрипузырная иммунотерапия используется после лучевой и системной (в крови) химиотерапии при раке II стадии, если операция не может быть проведена.Редко используется на стадии III. Когда это так, его используют вместе с другими видами лечения в случаях, когда операция невозможна. Рак мочевого пузыря стадии IV редко поддается лечению внутрипузырной терапией.
Виды внутрипузырной терапии
Существует 2 вида внутрипузырной терапии:
- Иммунотерапия
- Химиотерапия
Внутрипузырная иммунотерапия
Иммунотерапия заставляет собственную иммунную систему организма атаковать раковые клетки.
Bacillus Calmette-Guerin или BCG — это наиболее распространенная внутрипузырная иммунотерапия для лечения рака мочевого пузыря на ранней стадии. Его используют, чтобы предотвратить рост рака и его повторное появление.
БЦЖ — это микроб, связанный с микробом, вызывающим туберкулез (ТБ), но обычно он не вызывает серьезных заболеваний. БЦЖ вводится прямо в мочевой пузырь через катетер. Он достигает раковых клеток и «включает» иммунную систему.Клетки иммунной системы притягиваются к мочевому пузырю и атакуют раковые клетки мочевого пузыря. Чтобы БЦЖ работала, она должна контактировать с раковыми клетками. Вот почему он используется для внутрипузырной терапии.
Лечение БЦЖ может вызвать широкий спектр симптомов. Часто наблюдаются гриппоподобные симптомы, такие как лихорадка, боль, озноб и усталость. Это может длиться от 2 до 3 дней после лечения. Это также часто вызывает чувство жжения в мочевом пузыре, частые позывы к мочеиспусканию и даже кровь в моче.В редких случаях БЦЖ может распространяться в кровь и по организму, что приводит к серьезной инфекции. Это может произойти даже спустя годы после лечения. Одним из признаков этого может быть высокая температура, при которой не помогает Тайленол или подобные ему лекарства. Если это произойдет, немедленно позвоните своему врачу. Возможно, вы захотите спросить о других серьезных побочных эффектах, на которые следует обратить внимание и по поводу которых следует обратиться к врачу.
Внутрипузырная химиотерапия
Для этого лечения химиотерапевтические (химиотерапевтические) препараты вводятся прямо в мочевой пузырь через катетер.Эти препараты убивают активно растущие раковые клетки. Многие из этих препаратов также можно вводить системно (обычно в вену) для лечения более поздних стадий рака мочевого пузыря. Внутрипузырная химиотерапия чаще всего используется, когда внутрипузырная иммунотерапия не работает. Редко используется дольше 1 года.
Химиотерапевтический раствор можно нагреть перед тем, как ввести его в мочевой пузырь. Некоторые эксперты считают, что это улучшает действие препарата и помогает ему попасть в раковые клетки.Когда химиотерапия нагревается, это можно назвать гипертермической внутрипузырной терапией.
Митомицин — препарат, наиболее часто используемый для внутрипузырной химиотерапии. Доставка митомицина в мочевой пузырь вместе с нагреванием внутренней части мочевого пузыря, лечение, называемое электродвижущей терапией митомицином , может работать даже лучше, чем введение митомицина внутрипузырно обычным способом.
Гемцитабин может вызывать меньше побочных эффектов, чем митомицин, и с меньшей вероятностью всасывается в кровь.
Валрубицин можно использовать, если БЦЖ перестает работать. Но не все специалисты согласны с таким лечением.
Основными побочными эффектами внутрипузырной химиотерапии являются раздражение и чувство жжения в мочевом пузыре и кровь в моче.
Основным преимуществом введения химиотерапии прямо в мочевой пузырь вместо инъекции в кровоток является то, что лекарства обычно не достигают других частей тела и не воздействуют на них.



 Сейчас же вирус становится более агрессивным, каждый год фиксируются летальные исходы и серьезные осложнения! Высыпания появляются не только на коже, но и на слизистых, на внутренних органах: поверхности кишечника, бронхов, и это может привести к развитию тяжелых осложнений.
Сейчас же вирус становится более агрессивным, каждый год фиксируются летальные исходы и серьезные осложнения! Высыпания появляются не только на коже, но и на слизистых, на внутренних органах: поверхности кишечника, бронхов, и это может привести к развитию тяжелых осложнений.

 Их проводят, начиная с рождения ребенка, по специальному графику. Кроме утвержденных в календаре прививок вы можете отдельно поставить по желанию прививки от некоторых тяжелых инфекций: ветряной оспы, вируса папилломы человека, ротавирусной инфекции и др.
Их проводят, начиная с рождения ребенка, по специальному графику. Кроме утвержденных в календаре прививок вы можете отдельно поставить по желанию прививки от некоторых тяжелых инфекций: ветряной оспы, вируса папилломы человека, ротавирусной инфекции и др.