Как распознать дефицит железа?
Железо – важнейший элемент для нашего организма, он входит в состав гемоглобина, который является составляющей эритроцитов — красных кровяных телец.
Благодаря гемоглобину клетки нашего организма получают кислород. Железодефицитная анемия – патология, приводящая к снижению в крови уровня гемоглобина и эритроцитов, и, как следствие, – к гипоксии тканей и органов. Чем опасно это состояние и как восстановить уровень железа?
Почему не хватает железа?
Дефицит железа может развиться как у взрослого человека, так и у ребенка, причин для этого множество. Оставлять это заболевание без внимания нельзя, ведь на фоне недостатка кислорода страдают все органы нашего тела, но особенно опасно это состояние для головного мозга.
Железо не вырабатывается в организме самостоятельно, поэтому для поддержания необходимой нормы важна совокупность ряда факторов, таких как питание, усвояемость пищи и наличие каких-либо заболеваний.
К наиболее частым причинам железодефицитной анемии относятся:
1. Недостаточное поступление железа из пищи. Нерегулярное и несбалансированное питание – одна из основных причин дефицита железа. Вегетарианцы, а также люди, подвергающие себя строгим диетам, входят в группу риска. Также железодефицитная анемия может развиться на фоне снижения уровня усвоения железа при заболеваниях ЖКТ, а также в пожилом возрасте.
2. Хронические кровопотери, связанные с заболеваниями: частые носовые кровотечения, обильные менструации, желудочно-кишечные кровотечения, гельминтоз, хронические инфекции и другие патологии. Также к дефициту железа может привести острая кровопотеря в результате травмы или неконтролируемого донорства.
3. Индивидуальное повышение суточной нормы железа. Потребность организма в железе может увеличиться в момент активного роста у детей и подростков, у девочек в период становления цикла менструации, у беременных и кормящих женщин, при сильных физических нагрузках и др.
Симптомы и диагностика железодефицитной анемии
В современном ритме жизни симптомы недостатка железа можно спутать с проявлениями многих других заболеваний, поэтому для постановки диагноза и назначения лечения необходимо посетить врача и сдать анализы.
Симптомы дефицита железа:
- усталость, сонливость, низкая работоспособность;
- частые головокружения, головная боль;
- бледность кожи, онемение конечностей, зябкость;
- недостаток воздуха, шум в ушах, потемнение в глазах;
- тахикардия, одышка, боли в груди;
- смена вкусовых предпочтений;
- выпадение волос, ломкость и изменение структуры ногтей.
В целях диагностики железодефицитной анемии врач назначит ряд анализов крови, в которые обычно входят:
- Клинический и биохимический анализы крови.
- Концентрация железа в сыворотке крови.
- Содержание ферритина и трансферрина в сыворотке крови.

Дополнительно могут быть назначены обследования для выявления причины возникновения анемии:
- Гастроскопия – эндоскопическое исследование органов ЖКТ.
- Колоноскопия – эндоскопическое исследование толстого кишечника.
- УЗИ органов брюшной полости.
- Обследование гинеколога.
- ЭКГ.
Профилактика и лечение дефицита железа
Лечение железодефицитной анемии назначается исключительно врачом на основании результатов обследований и анализов. Если уровень гемоглобина у взрослого и ребенка от 6 лет составляет менее 90 г/л, то это указывает на наличие дефицита, менее 70 г/л считается тяжелой степенью заболевания. До 6 лет показатель гемоглобина в крови у детей должен быть не ниже 110 г/л.
В первую очередь рекомендуется сбалансированная диета, а также лечение заболеваний, которые стали причиной возникновения анемии. Для корректировки уровня гемоглобина врач может назначить прием лекарственных препаратов двухвалентного и трехвалентного железа.
В целях профилактики важно обеспечить организм необходимой суточной нормой железа: 1-2 мг – для взрослого, 0,5-1,2 мг – для ребенка. При выборе продуктов стоит учитывать, насколько хорошо усваивается организмом железо в их составе. Наилучшим вариантом считается железо животного происхождения: мясо, печень, птица, рыба, яйца. Дополнительно, но не как основной источник железа, можно добавлять в диету растительные продукты: зелень, орехи, бобовые, изюм и др.
Также в качестве дополнительного источника железа можно добавить к рациону биологически активные добавки с содержанием этого элемента, например: «Солгар Легкодоступное железо Джентл Айрон», «Железо хелат Анти Эйдж Эвалар».
У препаратов имеются противопоказания. БАД не является лекарственным средством.
Показатели клинического анализа крови — Лаборатория KDL
Гемоглобин (Hb)– один из главных показателей общего анализа крови.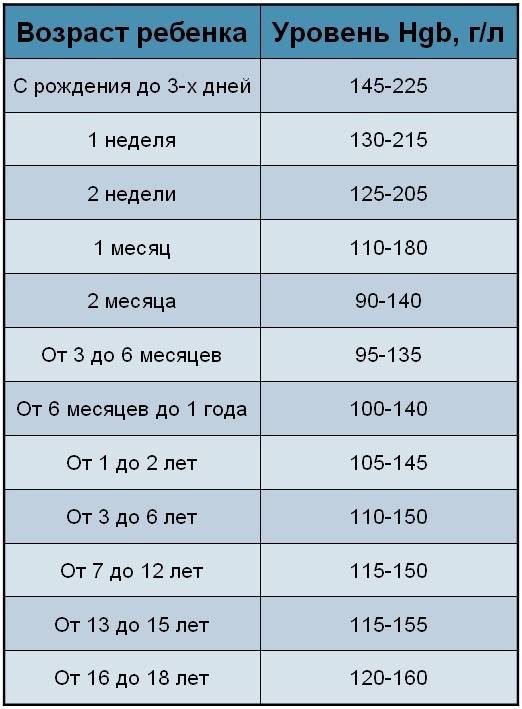 Снижение концентрации гемоглобина довольно частое явление, которое можно встретить в любом возрасте. Именно гемоглобин придает крови такой красный цвет. А необходим он нам для доставки кислорода из легких в наши органы – мозг, сердце, мышцы и другие. Поэтому, если у вас есть одышка уже при незначительной физической нагрузке, постоянная слабость, апатия — стоит обратить внимание именно на этот на показатель. В последнее время врачи рекомендуют думать о возможной анемии уже при гемоглобине ниже 120 г/л у женщин, а у мужчин ниже 130 г/л.
Снижение концентрации гемоглобина довольно частое явление, которое можно встретить в любом возрасте. Именно гемоглобин придает крови такой красный цвет. А необходим он нам для доставки кислорода из легких в наши органы – мозг, сердце, мышцы и другие. Поэтому, если у вас есть одышка уже при незначительной физической нагрузке, постоянная слабость, апатия — стоит обратить внимание именно на этот на показатель. В последнее время врачи рекомендуют думать о возможной анемии уже при гемоглобине ниже 120 г/л у женщин, а у мужчин ниже 130 г/л.
Эритроциты (RBC) – показатель числа эритроцитов, измеряется в количестве клеток на литр крови. Это самый многочисленный тип клеток. Главная задача эритроцитов — нести в себе гемоглобин. Если снижается количество эритроцитов, например, из-за дефицита витамина В12 или фолиевой кислоты (а именно эти витамины нужны для синтеза этих клеток), то гемоглобина в крови также будет не хватать, даже при хорошем запасе железа (ферритина).
Гематокрит (HCT) — объем всех клеток крови, % объемного содержания клеток в крови. При повышении гематокрита за черту 50% риск тромбоза из-за сгущения крови возрастает. В гематологических анализаторах это расчетный показатель т.е. прямым образом на него влияют количество эритроцитов и их средний объем.
Средний объем эритроцитов
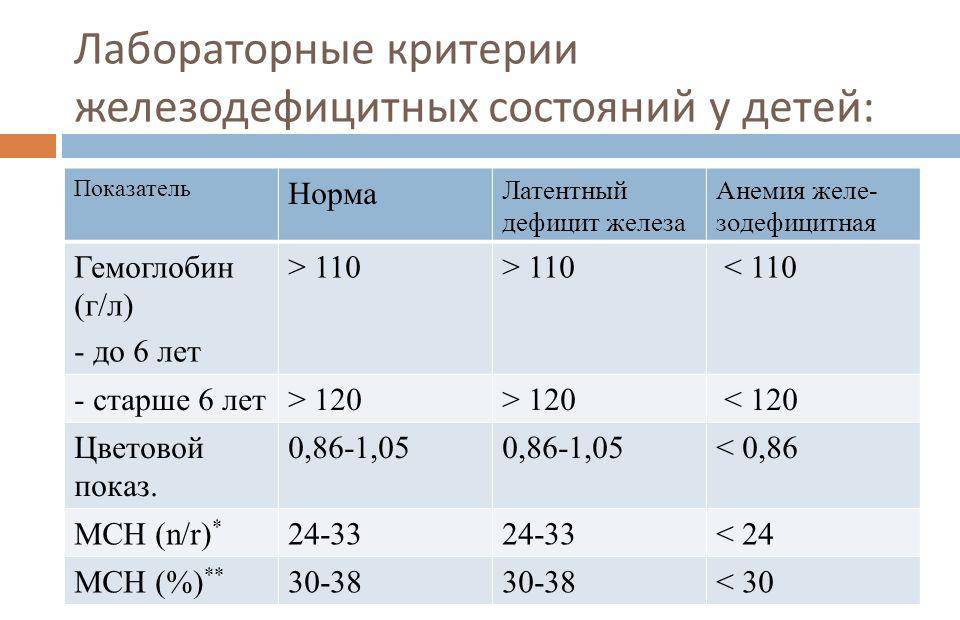
Среднее содержание гемоглобина в эритроците (MCH) –довольно стабильная величина, которая не зависит от возраста. Этот индекс пришел на смену устаревшему цветовому показателю (ЦП). Снижение MCH также говорит о нехватке железа. Повышение может быть признаком гиперхромной анемии.
Средняя концентрация гемоглобина в эритроците (MCHC). Повышение MCHC при сниженном MCV может предполагать наследственный микросфероцитоз – заболевание при котором наблюдается повышенное разрушение эритроцитов и может быть желтушность.
Ширина распределения эритроцитов по объему (RDW) — показатель анизоцитоза (разного размера эритроцитов). До появления гематологических анализаторов гетерогенность размера эритроцитов исторически определялась качественным исследованием мазков периферической крови.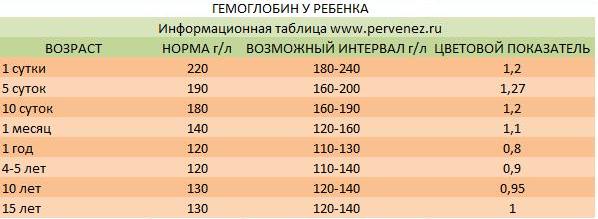 RDW указывает насколько сильно эритроциты различаются по размеру. Увеличивается при дефиците железа, фолиевой кислоты или витамина В12.
RDW указывает насколько сильно эритроциты различаются по размеру. Увеличивается при дефиците железа, фолиевой кислоты или витамина В12.
Тромбоциты (PLT) — самые маленькие клетки крови, но не менее важные чем эритроциты и лейкоциты. Необходимы они нам для свертывания крови. При их снижении в анализе ниже 30 самопроизвольно появляются на коже синяки, так проявляется повышенная кровоточивость. При повышении количества тромбоцитов в первую очередь надо исключать железодефицитную анемию и воспалительную реакцию (сделать анализ на С-реактивный белок).
MPV – средний объем тромбоцитов. Значение MPV повышается в период активного производства тромбоцитов. А уменьшение объема тромбоцитов говорит о возможных проблемах с костным мозгом. На показатель MPV стоит обращать внимание только при снижении количества тромбоцитов и отсутствии агрегации.

PDW — ширина распределения тромбоцитов по объему. PDW также как и MPV используется для диагностики причины снижения тромбоцитов.
Лейкоциты – самый главный показатель нашей иммунной системы. Снижение числа лейкоцитов может быть связано с вирусными инфекциями, токсическим воздействием на организм, приемом некоторых лекарств. Увеличение количества лейкоцитов может говорить об воспалительной реакции, острой инфекции, лейкозе. В этом случае особое внимание нужно обратить на лейкоцитарную формулу, то есть сделать клинический анализ крови с лейкоформулой.
Поделиться статьей:
Остались вопросы?показатели для детей и взрослых
Сохранить здоровье ребенка – это главная задача родителей. Однако если во внутриутробном периоде состояние плода напрямую зависит от здоровья материнского организма, то после рождения малыш обосабливается и с каждым днём становится все более самостоятельным.
Однако если во внутриутробном периоде состояние плода напрямую зависит от здоровья материнского организма, то после рождения малыш обосабливается и с каждым днём становится все более самостоятельным.
Таким образом, поддерживать здоровье ребенка на должном уровне становится сложнее, именно поэтому современная медицина рекомендует постоянно сдавать общий анализ крови детям от пяти месяцев до пяти лет, чтобы не упустить начало развития болезни.
Норма гемоглобина у взрослого человека значительно отличается от уровня гемоглобина у ребенка, это имеет связь с определенными этапами развития сердечно-сосудистой системы. Ведь с каждым годом кровеносная система ребенка развивается по своим законам. У детей в возрасте от нуля до одного года происходят активные процессы кроветворения, именно поэтому содержание гемоглобина в крови достаточно большое даже для взрослого человека и составляет 140 – 225 грамм на литр.
Норма гемоглобина в крови у детей от года до 2 лет несколько ниже – 110 – 140 грамм на литр. Далее эти границы могут слегка варьироваться до тех пор, пока ребенок не достигнет 12 лет. В подростковом возрасте в связи с интенсивными процессами роста уровень гемоглобина опять повышается и может достигать 150 грамм на литр, а с 15 до 17 лет — даже 166 грамм на литр.
Далее эти границы могут слегка варьироваться до тех пор, пока ребенок не достигнет 12 лет. В подростковом возрасте в связи с интенсивными процессами роста уровень гемоглобина опять повышается и может достигать 150 грамм на литр, а с 15 до 17 лет — даже 166 грамм на литр.
Гипогемоглобинемия – это снижение уровня гемоглобина в крови относительно возрастной нормы. Она является главным симптомом анемии (малокровия). При полноценном питании норма гемоглобина в крови у детей может незначительно отклоняться, но в случае недоедания анализ крови будет весьма неутешительным. При таком развитии событий ребенку необходимо срочно восполнить недостаток железа в организме путем введения в рацион красного мяса, красной рыбы, икры, гранатового сока. В качестве вспомогательной терапии могут употребляться препараты железа и фолиевая кислота. Иначе при отсутствии лечения гипогемоглобинемии ребенок может отстать от сверстников в развитии, причем как в физическом так и в психологическом.
Главное, помните, что норма гемоглобина в крови у детей зависит от возраста и пола ребенка.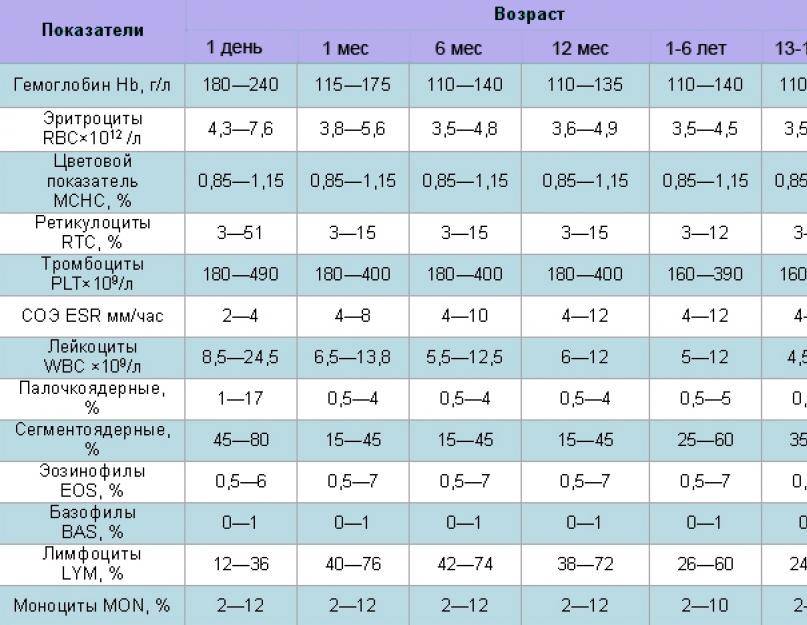 Сдав общий анализ крови (забор периферической крови осуществляется проколом кожи безымянного пальца, а у совсем маленьких кровь берется из сосудов пятки), обратитесь к педиатру или к врачу–гематологу. Специалисты точно определят возрастные нормы и проверят результаты анализов. В случае обнаружения проблем они определят верную стратегию лечения. Предотвратить развитие патологии поможет ежедневное наблюдение за общим состоянием ребенка, мониторинг показателей периферической крови и, конечно, четкие соблюдения рекомендаций врача.
Сдав общий анализ крови (забор периферической крови осуществляется проколом кожи безымянного пальца, а у совсем маленьких кровь берется из сосудов пятки), обратитесь к педиатру или к врачу–гематологу. Специалисты точно определят возрастные нормы и проверят результаты анализов. В случае обнаружения проблем они определят верную стратегию лечения. Предотвратить развитие патологии поможет ежедневное наблюдение за общим состоянием ребенка, мониторинг показателей периферической крови и, конечно, четкие соблюдения рекомендаций врача.
Каждому родителю просто необходимо знать, какая норма гемоглобина в крови у детей. Это значительно упростит процесс обнаружения болезней у ребенка. А вовремя замеченное заболевание вылечить гораздо проще и легче, чем его запущенную форму. Следите за показателями анализов, и ваш ребенок вырастет здоровым и сильным.
Норма гемоглобина у детей. Причины высокого и низкого уровней гемоглобина
Уровень гемоглобина у детей — один из важнейших показателей здоровья.
Что такое гемоглобин?
Гемоглобин, железосодержащий белок, — это строительный материал для красных кровяных телец (эритроцитов), он необходим для переноса кислорода от легких ко всем клеткам организма. Низкий гемоглобин приводит к кислородному голоданию и, как следствие, снижению иммунитета и задержке развития у детей. Повышенный гемоглобин у ребенка тоже опасен — это состояние чревато закупоркой сосудов. Для поддержания гемоглобина в норме организм нуждается в достаточном поступлении железа.
В чем отличие «детского» гемоглобина от «взрослого»?
Гемоглобин начинает вырабатываться у ребенка еще в утробе на самых ранних стадиях формирования плода. Этот гемоглобин принципиально отличается от гемоглобина в крови взрослого человека и называется фетальным гемоглобином. Незадолго до рождения фетальный гемоглобин начинает заменяться «взрослой» формой этого белка — гликолизированным гемоглобином.
В первые годы жизни норма гемоглобина в крови у ребенка значительно изменяется в зависимости от возраста. Этот показатель нужно тщательно контролировать, чтобы вовремя заметить критические отклонения от нормы.
Именно гемоглобин, содержащий железо, придает крови красный цвет. Но далеко не у всех существ на Земле кровь красная. Например, кровь осьминогов, омаров и крабов имеет сине-зеленый оттенок, поскольку в ней функцию гемоглобина выполняет другой белок — гемоцианин, который содержит медь, а не железо.
Как узнать уровень гемоглобина?
Уровень гемоглобина выявить достаточно просто — нужно только сдать кровь на общий анализ. Этот анализ включает в себя определение концентрации гемоглобина, которая измеряется в граммах на литр. Чтобы получить точную информацию, кровь нужно сдавать до кормления, желательно — утром. В течение полутора-двух часов после кормления гемоглобин понижается.
Существуют и косвенные признаки, указывающие на низкий гемоглобин у детей, в частности,
- бледная кожа
- и шелушения.
Содержание гемоглобина в капиллярной крови на 10–20% выше, чем в венозной. Это нужно учитывать при интерпретации результатов анализов.
Какова норма гемоглобина в крови у ребенка?
Уровень гемоглобина у новорожденных в первые дни жизни очень высокий — 180–240 г/л. Это объясняется тем, что у малыша имеется запас железа, накопленный еще во время пребывания в утробе. У недоношенных малышей гемоглобин часто ниже нормы — 160–220 г/л. У таких деток высок риск анемии — критического понижения гемоглобина в крови.
К концу первой недели уровень гемоглобина у детей понижается до 160–200 г/л. В последующие недели и месяцы гемоглобин плавно повышается — к месячному возрасту его норма составляет уже 120–160 г/л, а к году — 110–130 г/л.
В 5 лет нормой считается 110–140 г/л, в 10 — 120–140 г/л[5].
В период полового созревания, примерно к 15 годам, уровень гемоглобина у детей достигает «взрослых» показателей — 125–165 г/л.
Причины и признаки повышения уровня гемоглобина
К повышению уровня гемоглобина у малыша могут привести разные причины. Самыми распространенными являются:
- обезвоживание — как в результате недостаточного поступления жидкости и перегрева, так и в результате диареи;
- врожденные сердечные заболевания, в том числе легочно-сердечная недостаточность;
- онкологические заболевания;
- нарушения синтеза гормона эритропоэтина;
- непроходимость кишечника;
- болезни крови.
Иногда немного повышенный уровень гемоглобина может считаться вариантом нормы. У людей, живущих в условиях высокогорья, гемоглобин немного повышен — это реакция на разреженный воздух. Также гемоглобин может быть немного выше нормы у детей, которые очень активно занимаются спортом.
Дети с повышенным гемоглобином обычно вялые и раздражительные, они страдают от сонливости и быстрой утомляемости, кожа иногда принимает красноватый оттенок.
Чем опасен пониженный гемоглобин у ребенка?
Пониженный гемоглобин у детей встречается чаще, чем повышенный. По данным ВОЗ, нехватка гемоглобина — анемия — встречается у 47,4% детей дошкольного возраста и у 25,4% школьников.
Низкий гемоглобин у ребенка — существенный фактор риска. Он может привести к отставанию в развитии, развитию заболеваний сердца и почек (они наравне с мозгом первыми страдают от кислородного голодания), нарушению функционирования иммунной системы, заболеваниям кожи и отекам. Без лечения анемия может закончиться кардиомиопатией и сердечной недостаточностью, а эти патологии смертельно опасны. При критическом снижении уровня гемоглобина возможна даже гипоксическая кома.
Признаки низкого гемоглобина у детей многочисленны, но неспецифичны, иными словами, они сопровождают не только анемию, но и множество других заболеваний. В любом случае родителей должны насторожить такие симптомы, как слабость, вялость, плаксивость и сонливость малыша, понижение аппетита, бледность кожи. Дети постарше могут жаловаться на головокружения и головную боль. При низком гемоглобине заметно страдают когнитивные функции — память, способность к концентрации внимания, обучаемость. Множество случаев плохой успеваемости объясняется вовсе не ленью, а нехваткой железа и низким гемоглобином.
В любом случае родителей должны насторожить такие симптомы, как слабость, вялость, плаксивость и сонливость малыша, понижение аппетита, бледность кожи. Дети постарше могут жаловаться на головокружения и головную боль. При низком гемоглобине заметно страдают когнитивные функции — память, способность к концентрации внимания, обучаемость. Множество случаев плохой успеваемости объясняется вовсе не ленью, а нехваткой железа и низким гемоглобином.
Сдавать анализ на гемоглобин нужно регулярно, как минимум раз в три месяца. Определить развитие анемии по косвенным признаком непросто, очень часто ее симптомы игнорируются или списываются на другие причины.
Делать анализ крови на гемоглобин необходимо после любых инфекционных болезней, резких изменений рациона (например, после назначения диеты при выявлении аллергии или болезней ЖКТ) и любых неожиданных переменах в поведении малыша. Если ваш ребенок из активного и жизнерадостного малыша внезапно превратился в соню и плаксу, нужно незамедлительно взять направление на анализ.
Низкий гемоглобин нередко отражается и на физическом развитии — такие детки медленно растут и отстают от здоровых сверстников по весу и росту.
Иногда анализы показывают, что гемоглобин у ребенка понижен, и это вызывает обоснованное беспокойство родителей. Чем может быть вызван пониженный гемоглобин у ребенка?
Причины пониженного гемоглобина у детей
- Инфекционные болезни и паразитарные поражения.
- Нехватка железа в питании мамы во время беременности и кормления или его недостаток в рационе самого ребенка. Нередко низкий гемоглобин наблюдается у детей женщин, придерживающихся веганской диеты. Растительная пища тоже содержит железо, но оно усваивается хуже, чем то, что присутствует в продуктах животного происхождения.
- Дефицит витаминов, необходимых для того, чтобы железо всасывалось в кровь — к ним относятся фолиевая кислота и витамин С. Важную роль в усвоении железа играет также и медь.
- Заболевания пищеварительной системы, при которых нарушается всасывание железа.

- Кровопотери после травм и операций, а также после регулярных кровотечений, например назальных.
- Нехватка физической активности и свежего воздуха.
- Врожденные патологии, в частности талассемия.
Профилактика отклонений от нормы
Самая важная мера предотвращения развития осложнений, связанных с изменением уровня гемоглобина, — это регулярные анализы и осмотры у педиатра. Иногда пониженный или повышенный гемоглобин у ребенка говорит о наличии серьезных заболеваний, требующих немедленного лечения. Но многое зависит и от родителей, поскольку отклонения от нормы часто встречаются у здоровых детей из-за погрешностей в питании и режиме.
Профилактика повышенного гемоглобина
- Во время беременности и кормления грудью мамам не стоит принимать витаминные комплексы с железом без консультации с врачом. Во многих случаях дополнительные источники железа необходимы, но крайне важно не превышать рекомендованную дозировку.

- Не покупайте детские витаминные комплексы без консультации с врачом. Если ребенок получает достаточное количество железа и витаминов с пищей, добавочная порция витаминов и минералов может принести больше вреда, чем пользы.
- Пересмотрите рацион ребенка — он должен содержать мясо, овощи и фрукты, богатые железом.
Профилактика пониженного гемоглобина
- Старайтесь кормить ребенка грудью хотя бы в первые 6–9 месяцев. Грудное молоко содержит особый белок, который называется лактоферин, — он способствует всасыванию железа.
- Обеспечьте ребенку свежий воздух и — если говорить о малышах постарше — физическую активность. Прогулки должны занимать не менее 2–4 часов в день. Позволяйте ребенку бегать, играйте с ним в подвижные игры, следите, чтобы он не слишком увлекался компьютерными играми, планшетом и прочими достижениями цивилизации, которые способствуют снижению активности.
- Помните о том, что ребенок должен спать в хорошо проветриваемом помещении.

- Обеспечьте сбалансированный рацион с минимумом сладостей и полуфабрикатов.
В него должны входить
- нежирное мясо и печень,
- бобовые,
- яйца (особенно желтки),
- творог,
- яблоки,
- груши,
- огурцы и свекла,
а также ягоды —
- черная смородина
- и крыжовник.
Эти продукты — чемпионы по содержанию железа. Чтобы улучшить его усвояемость, нужно позаботиться и о достаточном поступлении фолиевой кислоты. Она содержится в листовых овощах —
- салате,
- шпинате,
а также в
- брокколи,
- цитрусовых,
- чечевице,
- орехах
- и семечках.
Необходим для всасывания железа витамин С —
- капуста
- и лесные ягоды,
а также медь
- в креветках,
- горохе,
- говяжьей и свиной печени,
- гречке,
- кунжуте,
- абрикосах.

Можно использовать для повышения содержания железа в крови и поливитамины, БАДы, обогащенные этим элементом, известный всем гематоген, например. Но прежде чем начинать прием таких средств, нужно поговорить с врачом и определить нужную дозировку.
Чем раньше вы заметите изменения в уровне гемоглобина у ребенка, тем проще будет привести этот показатель к норме и избежать нежелательных последствий.
Отказ от ответственности: этот контент, включая советы, предоставляет только общую информацию. Это никоим образом не заменяет квалифицированное медицинское заключение. Для получения дополнительной информации всегда консультируйтесь со специалистом или вашим лечащим врачом.
Добавьте «Правду.Ру» в свои источники в Яндекс.Новости или News.Google, либо Яндекс.Дзен
Быстрые новости в Telegram-канале Правды.Ру. Не забудьте подписаться, чтоб быть в курсе событий.
Низкий уровень гемоглобина у ребенка. Родителям о важном
Анемия при сердечно-сосудистых заболеваниях
С.П. Сидорук, Е.Б. Петрова, Н.П. Митьковская
Госпиталь, Аль-Ахса, Саудовская Аравия, УО «Белорусский государственный медицинский университет»
Анемия часто встречается у пациентов с патологией сердечно-сосудистой системы: может наблюдаться у трети пациентов с застойной сердечной недостаточностью и у 10-20% пациентов с ишемической болезнью сердца (ИБС). Причины анемии при болезнях сердца многофакторны и могут включать хроническое воспаление, абсолютный или функциональный дефицит железа, недостаточную выработку и активность эритропоэтина, гемоделюцию, нарушения функции почек. Гемодинамические и негемодинамические изменения вследствие анемии при наличии сопутствующих хронических болезней сердца вносят вклад в увеличение частоты сердечно-сосудистых осложнений. Анемия является независимым фактором риска неблагоприятного исхода при сердечно-сосудистых заболеваниях и, вероятно, является как медиатором, так и маркером неблагоприятного прогноза. Лечение анемии у пациентов с сердечно-сосудистыми заболеваниями может включать эритропоэтины, переливание крови и прием препаратов железа.
Лечение анемии у пациентов с сердечно-сосудистыми заболеваниями может включать эритропоэтины, переливание крови и прием препаратов железа.
ключевые слова: анемия, сердечно-сосудистые заболевания, ишемическая болезнь сердца, артериальная гипертензия, дефицит железа, карбоскимальтоза
для цитирования: Сидорук С.П., Петрова Е.Б., Митьковская Н.П. Анемия при сердечно-сосудистых заболеваниях. Неотложная кардиология и кардиооваскулярные риски, 2017, Т. 1, №1, С. 38-45.
Введение
Сердечно-сосудистые заболевания являются основной причиной смерти во всем мире. Многие пациенты с сердечно-сосудистой патологией страдают анемией в результате острых или хронических сопутствующих состояний. Согласно критериям Всемирной организации здравоохранения термин «анемия» раскрывается как состояние, при котором наблюдается согласно гендерной принадлежности снижение концентрации гемоглобина в крови: у женщин — менее 120 г/л и менее 130 г/л у мужчин.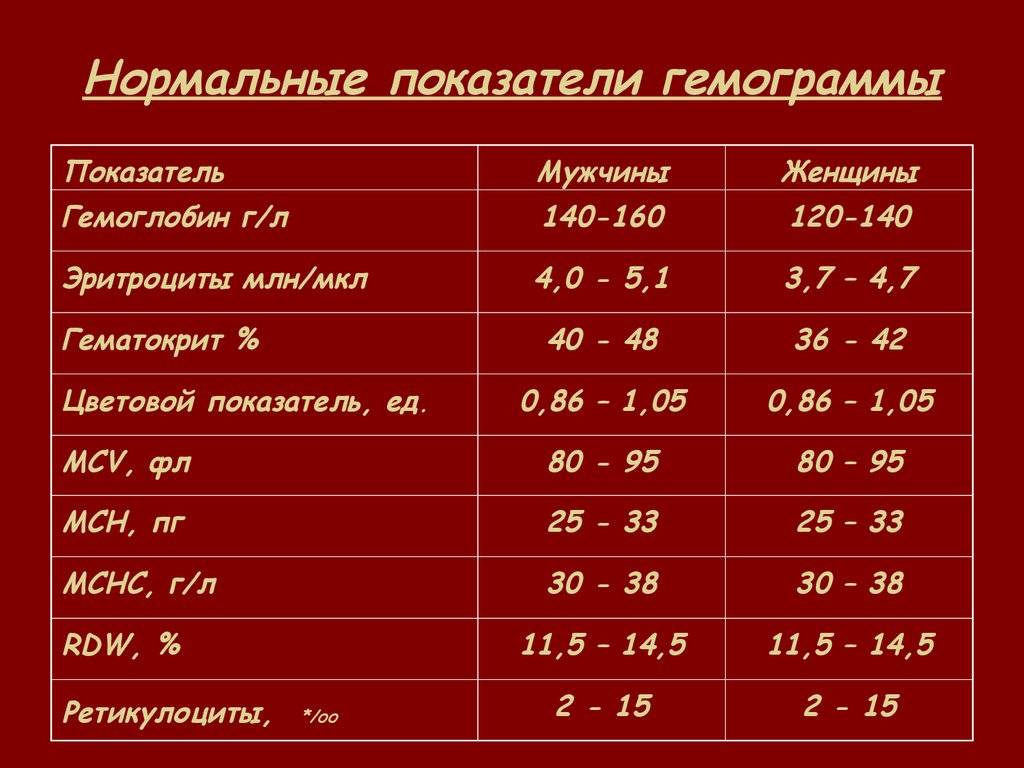 Анемия является важной проблемой практического здравоохранения, так как влияет на качество жизни, смертность и является частой причиной обращения к врачу.
Анемия является важной проблемой практического здравоохранения, так как влияет на качество жизни, смертность и является частой причиной обращения к врачу.
Во всем мире анемией страдают 1,62 миллиарда людей, что составляет 24,8% от общего населения планеты. Наиболее часто анемии подвержены дети дошкольного возраста (47%), а реже всего – мужчины (12,7%). В половине случаев причиной анемии является дефицит железа [1]. Недостаток железа не только нарушает образование эритроцитов, но и ухудшает клеточные функции, связанные с мышечным метаболизмом, влияет на функцию митохондрий, нейротрансмиттеров, синтез ДНК и иммунную систему [2]. Частота анемии увеличивается с возрастом, что делает ее частым спутником сердечно-сосудистых катастроф. Анализ литературных источников продемонстрировал, что анемия является независимым предиктором кардиоваскулярных заболеваний и неблагоприятных исходов [3].
Влияние анемии на сердечно-сосудистую систему
Для оценки патологического влияния снижения концентрации уровня гемоглобина в крови на кардиоваскулярные риски необходимо рассмотреть физиологическую реакцию организма на анемию. Основными факторами, ответственными за газообмен, выступают: интенсивность кровотока и его распределение, потребление кислорода клетками, оксигенация крови. Гипоксия при анемии компенсируется каскадом гемодинамических и гемодинамически не ассоциированных механизмов, таких как активация продукции эритропоэтина, повышение тканевой утилизации кислорода. Реализация основных гемодинамических факторов достигается путем повышения контрактильной способности миокарда, уменьшения постнагрузки, увеличения преднагрузки, реализацией положительного ино- и хронотропных эффектов. Повышение продукции оксида азота, индуцированная гипоксией вазодилатация и снижение вязкости крови являются причиной уменьшения сосудистого сопротивления и приводят к снижению постнагрузки. Хроническая анемия стимулирует ангиогенез и образование новых мелких сосудов. Развитие коллатералей и микроциркуляторного русла способствует снижению постнаргузки. Повышение венозного возврата (преднагрузки) и кровенаполнения левого желудочка способствуют увеличению конечного диастолического объема и фракции выброса левого желудочка.
Основными факторами, ответственными за газообмен, выступают: интенсивность кровотока и его распределение, потребление кислорода клетками, оксигенация крови. Гипоксия при анемии компенсируется каскадом гемодинамических и гемодинамически не ассоциированных механизмов, таких как активация продукции эритропоэтина, повышение тканевой утилизации кислорода. Реализация основных гемодинамических факторов достигается путем повышения контрактильной способности миокарда, уменьшения постнагрузки, увеличения преднагрузки, реализацией положительного ино- и хронотропных эффектов. Повышение продукции оксида азота, индуцированная гипоксией вазодилатация и снижение вязкости крови являются причиной уменьшения сосудистого сопротивления и приводят к снижению постнагрузки. Хроническая анемия стимулирует ангиогенез и образование новых мелких сосудов. Развитие коллатералей и микроциркуляторного русла способствует снижению постнаргузки. Повышение венозного возврата (преднагрузки) и кровенаполнения левого желудочка способствуют увеличению конечного диастолического объема и фракции выброса левого желудочка. При кратковременной анемии эти изменения обратимы, при хронизации процесса — приводят к ремоделированию с формированием эссентрической гипертрофии миокарда левого желудочка, как и при других формах объёмных перегрузок.
При кратковременной анемии эти изменения обратимы, при хронизации процесса — приводят к ремоделированию с формированием эссентрической гипертрофии миокарда левого желудочка, как и при других формах объёмных перегрузок.
Увеличение сердечного выброса в свою очередь способствует развитию артериального ремоделирования центральных сосудов эластического типа, таких как аорта и общие сонные артерии, за счёт увеличения просвета и компенсаторного утолщения комплекса интима-медии. Как следствие — повышение систолического давления и инерции, большая масса крови попадает в дилатированную артериальную систему. Активация симпатической нервной системы усиливает контрактильность левого желудочка и увеличивает частоту сердечных сокращений. В присутствии хронических заболеваний сердца эти дополнительные эффекты, опосредованные анемией, способствуют увеличению частоты сердечно-сосудистых осложнений [4].
Анемия при артериальной гипертензии
Нормохромная анемия – нередкая находка у пациентов, страдающих артериальной гипертензией (АГ), и чаще встречается при неконтролируемой гипертензии..gif) Низкий уровень гемоглобина ассоциируется с плохим контролем артериального давления и является индикатором повышенного сердечно-сосудистого риска [5]. Согласно литературным данным, пациенты, страдающие АГ с сопутствующей анемией, имеют более высокие значения среднесуточного, ночного и недостаточное снижение ночного систолического артериального давления по сравнению с теми, у которых наблюдался нормальный уровень гемоглобина. У пациентов с анемией также прослеживается тенденция к увеличению среднесуточных значений диастолического артериального давления [6]. У пациентов с изолированной систолической гипертензией и гипертрофией левого желудочка с сопутствующим снижением уровня гемоглобина наблюдается увеличение сердечно-сосудистой смертности и частоты развитий острых нарушений мозгового кровообращения [7].
Низкий уровень гемоглобина ассоциируется с плохим контролем артериального давления и является индикатором повышенного сердечно-сосудистого риска [5]. Согласно литературным данным, пациенты, страдающие АГ с сопутствующей анемией, имеют более высокие значения среднесуточного, ночного и недостаточное снижение ночного систолического артериального давления по сравнению с теми, у которых наблюдался нормальный уровень гемоглобина. У пациентов с анемией также прослеживается тенденция к увеличению среднесуточных значений диастолического артериального давления [6]. У пациентов с изолированной систолической гипертензией и гипертрофией левого желудочка с сопутствующим снижением уровня гемоглобина наблюдается увеличение сердечно-сосудистой смертности и частоты развитий острых нарушений мозгового кровообращения [7].
Изменение электрокардиограммы при анемии
Электрокардиографические реполяризационные изменения (депрессия сегмента ST, инверсия зубца Т, удлинение интервала QT) часто встречаются у пациентов с анемией как в покое, так и при нагрузке [8].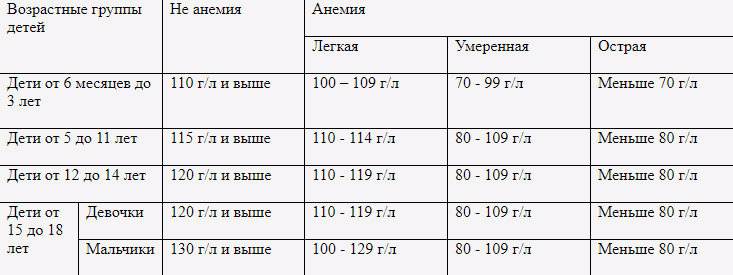 Было обнаружено, что уровень гемоглобина сильно коррелирует с изменениями на электрокардиограмме [9].
Было обнаружено, что уровень гемоглобина сильно коррелирует с изменениями на электрокардиограмме [9].
Удлинение интервала QT является предиктором желудочковой аритмии и внезапной смерти. Гипоксия и нарушение доставки кислорода у пациентов с анемией может быть причиной нарушения реполяризации миокарда. Согласно проведенным исследованиям, анемия, макроцитоз и анизоцитоз коррелируют с удлинением интервала QT у пациентов с артериальной гипертензией и могут учитываться в оценке риска внезапной смерти [10]. Низкий уровень железа в остальном у практически здоровых детей отрицательно коррелирует с интервалами QT и QTс и может указывать на дополнительный риск развития аритмии [11].
Mehta и соавт. продемонстрировал значимую и воспроизводимую депрессию сегмента ST у пациентов с железно-дефицитной анемией во время нагрузочных тестов. Эти электрофизиологические изменения исчезали после лечения препаратами железа ещё до нормализации уровня гемоглобина, что может объясняться эффектом железа на тканевом уровне [12].
Анемия при ишемической болезни сердца
Ишемия миокарда определяется степенью выраженности несоответствия потребности кардиомиоцитов в кислороде и возможностями его доставки. Определяющими факторами, влияющими на заинтересованность миокарда в кислороде, являются: частота сердечных сокращений, контрактильность миокарда и напряжение стенки сердца. Факторами, определяющими доставку кислорода к сердцу, являются содержание кислорода в крови и интенсивность коронарного кровотока. Увеличение доставки кислорода к миокарду в ответ на увеличение потребления происходит путем уменьшения сопротивления коронарного русла. Экстракция кислорода кардиомиоцитами даже в покое составляет около 90% [13]. У пациентов без коронарной патологии даже значительное снижение содержания кислорода в коронарном кровотоке может компенсироваться за счёт периферической вазодилатации. При коронарном стенозе этот механизм имеет ограниченные возможности. Согласно данным литературы, у животных с анемией при остром инфаркте миокарда увеличивалась зона инфарцирования, снижалась насосная функция сердца и выживаемость. Переливание крови животным с анемией до уровня гемоглобина 100 г/л уменьшало зону инфаркта и улучшало контрактильную возможность миокарда. Вместе с тем, переливание крови до уровня гемоглобина 120 г/л было связано с увеличением зоны инфаркта [14].
Переливание крови животным с анемией до уровня гемоглобина 100 г/л уменьшало зону инфаркта и улучшало контрактильную возможность миокарда. Вместе с тем, переливание крови до уровня гемоглобина 120 г/л было связано с увеличением зоны инфаркта [14].
Sabatine et al. обнаружил U-образную зависимость клинических событий при остром коронарном синдроме к 30-му дню: у пациентов с инфарктом миокарда с подъемом сегмента ST наблюдалось увеличение смертности при уровне гемоглобина ниже 140 г/л и выше 170 г/л, в то время как у пациентов с инфарктом миокарда без подъема сегмента ST смертность, размер инфаркта и ишемии увеличивались при уровне гемоглобина менее 110 г/л и более 160 г/л [15].
Анемия является весомым фактором риска при ишемической болезни сердца (ИБС). Пациенты с ишемической болезнью сердца и сопутствующей анемией имеют более выраженную степень коронарной патологии. Согласно ряду публикаций, у пациентов с ИБС и анемией уровень гемоглобина, сывороточного железа и общая железосвязывающая способность крови отрицательно коррелируют с тяжестью коронарной патологии [16].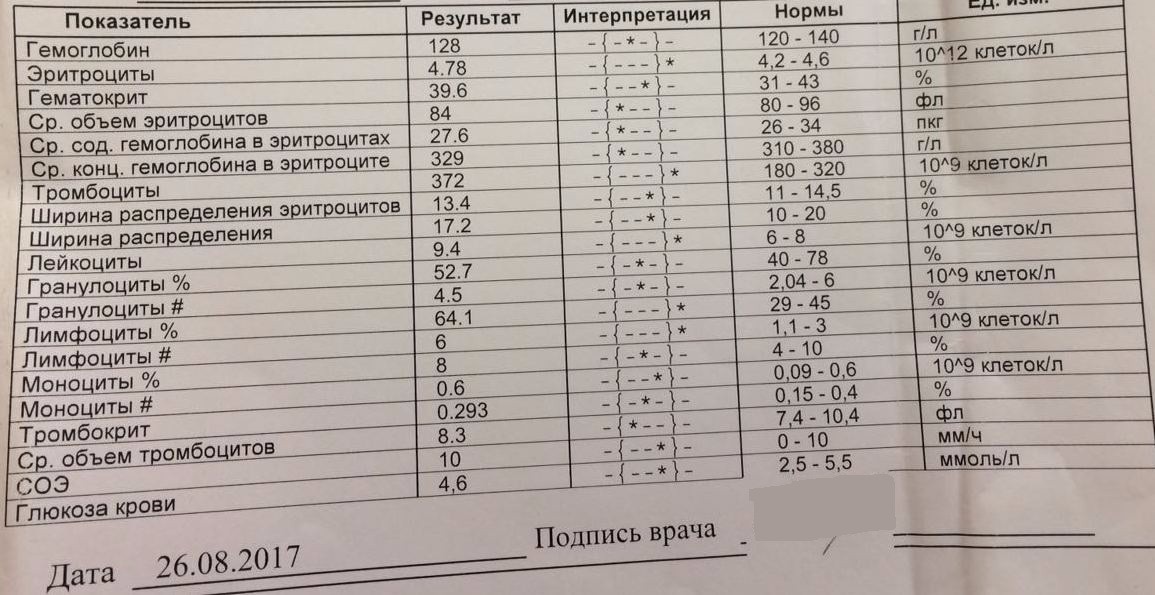 У пациентов с ишемической болезнью сердца и сопутствующей анемией наблюдается увеличение смертности по сравнению с категорией лиц с изолированной ИБС, а анемия выступает независимым предиктором возникновения острого ишемического повреждения миокарда [17].
У пациентов с ишемической болезнью сердца и сопутствующей анемией наблюдается увеличение смертности по сравнению с категорией лиц с изолированной ИБС, а анемия выступает независимым предиктором возникновения острого ишемического повреждения миокарда [17].
Исследование Ferreira и соавт. выявило, что уровень гемоглобина менее 108 г/л являлся одним из наиболее сильных независимых предикторов смертности к концу первого года при остром коронарном синдроме. Он предложил включить уровень гемоглобина в оценку риска пациентов, госпитализированных с острым коронарным синдромом, так как это является доступным параметром и систематически оценивается при госпитализации [18].
В исследовании Cadilac анемия часто встречалась у пациентов, направленных на первичную ангиопластику по поводу острого инфаркта миокарда. Была продемонстрирована сильная корреляционная связь между снижением уровня гемоглобина и развитием неблагоприятных исходов, увеличением смертности. Сделан вывод, что анемия выступала независимым предиктором госпитальной и общей смертности к концу первого года постинфарктного периода [19]. Тяжелая анемия может приводить к дисбалансу между доставкой и потреблением кислорода в миокарде даже при отсутствии гемодинамически значимого коронарного стенозирования. Bailey с соавт. описал пример развития острого коронарного синдрома с подъемом сегмента ST у пациента с тяжелой анемией в отсутствии ангиографически значимого коронарного стеноза, тромбоза или спазма [20].
Тяжелая анемия может приводить к дисбалансу между доставкой и потреблением кислорода в миокарде даже при отсутствии гемодинамически значимого коронарного стенозирования. Bailey с соавт. описал пример развития острого коронарного синдрома с подъемом сегмента ST у пациента с тяжелой анемией в отсутствии ангиографически значимого коронарного стеноза, тромбоза или спазма [20].
Таким образом, причины неблагоприятных исходов у пациентов с анемией и коронарной патологией многочисленны. Уменьшение кислородной емкости крови, а также активация симпатической нервной системы могут повышать потребность миокарда в кислороде и усугублять ишемию.
Анемия при сердечной недостаточности
Анемия – частое сопутствующее патологическое состояние при сердечной недостаточности (СН). У пациентов с сердечной недостаточностью и сопутствующей анемией прослеживается следующая тенденция: у них более выражены симптомы левожелудочковой недостаточности, выше частота госпитализаций по поводу декомпенсации хронической сердечной недостаточности (ХСН), среди них чаще встречаются женщины, пациенты представлены старшей возрастной группой, у них чаще диагностируется сахарный диабет, сопутствующая почечная недостаточность и артериальная гипертензия [21]. Анемия – мощный предиктор повторных госпитализаций и низкой выживаемости при хронической сердечной недостаточности [22]. Частота встречаемости анемии возрастает при увеличении степени тяжести сердечной недостаточности и может достигать 79.1% у пациентов с IV функциональным классом СН по классификации Нью-Йоркской Ассоциации Сердца [23].
Анемия – мощный предиктор повторных госпитализаций и низкой выживаемости при хронической сердечной недостаточности [22]. Частота встречаемости анемии возрастает при увеличении степени тяжести сердечной недостаточности и может достигать 79.1% у пациентов с IV функциональным классом СН по классификации Нью-Йоркской Ассоциации Сердца [23].
Этиология анемии при сердечной недостаточности является многофакторной, и множество механизмов ответственно за это состояние. Увеличение системного воспаления, нейрогуморальная активация, нарушение питания, дисфункция почек, снижение ответа костного мозга на запрос и эффект приема ряда лекарственных средств вносят вклад в ее развитие. Увеличение циркулирующих провоспалительных цитокинов при СН вызывает нарушение мобилизации железа, недостаточную продукцию эритропоэтина в ответ на активацию ренин-ангиотензин-альдостероновой системы и снижение почечного кровотока, снижение функции костного мозга. Использование ингибиторов ангиотензин-превращающего фермента может дополнительно уменьшать секрецию эритропоэтина. Нарушение питания вследствие отсутствия аппетита, желудочно-кишечная мальабсорбция, прием аспирина могут усугублять железодефицитную анемию. Гемоделюция также вносит дополнительный вклад в становление анемии [24].
Нарушение питания вследствие отсутствия аппетита, желудочно-кишечная мальабсорбция, прием аспирина могут усугублять железодефицитную анемию. Гемоделюция также вносит дополнительный вклад в становление анемии [24].
Дефицит железа
Дефицит железа (ДЖ) – наиболее частая причина анемии у пациентов с сердечной недостаточностью [25,26]. Дефицит железа может наблюдаться и при нормальном уровне гемоглобина, а железодефицитное состояние без анемии выявляется у 46% пациентов со стабильной сердечной недостаточностью [27]. ДЖ может быть представлен в абсолютной и функциональной формах. При абсолютном дефиците железа наступает истощение его запасов в организме, а железодефицитная анемия может рассматриваться как конечная стадия этого истощения. Функциональный дефицит железа связан с неадекватным его высвобождением из депо в ответ на потребности костного мозга и встречается при многих острых и хронических воспалительных состояниях. Дефицит железа ассоциируется с прогрессированием симптомов сердечной недостаточности, снижением качества жизни, увеличением смертности и госпитализаций [28-30].
Активация симпатической и ренин-ангиотензин-альдостероновой систем, хроническое воспаление, абсолютный и функциональный дефицит железа, нарушение образования и активности эритропоэтина, гемоделюция, почечная дисфункция ухудшают прогноз у пациентов с сердечной недостаточностью. Вероятно, анемия является как медиатором, так и маркером неблагоприятного прогноза у пациентов с сердечной недостаточностью.
Лечение анемии у пациентов с заболеваниями сердца
Лечение анемии при сердечной недостаточности и ишемической болезни сердца может включать прием эритропоэтинов, при наличии железодефицитных состояний с анемией или без нее — терапию препаратами железа, при тяжелом течении — переливание эритроцитарной массы.
Шестнадцать рандомизированных контролируемых исследований оценивало эффект эритропоэтинов у пациентов с сердечной недостаточностью. Большинство этих исследований включало пациентов с систолической сердечной недостаточностью. Полученные данные с умеренной степенью доказательности продемонстрировали отсутствие улучшения качества жизни и переносимости физических нагрузок при лечении эритропоэтинами. В то же время данные с высокой степенью доказательности продемонстрировали отсутствие снижения смертности при лечении эритропоэтинами. Среди серьезных побочных эффектов, связанных с их применением, выделили развитие сосудистых тромбозов [31].
В то же время данные с высокой степенью доказательности продемонстрировали отсутствие снижения смертности при лечении эритропоэтинами. Среди серьезных побочных эффектов, связанных с их применением, выделили развитие сосудистых тромбозов [31].
Несмотря на то, что анемия часто встречается у пациентов с хронической сердечной недостаточностью и ишемической болезнью сердца, лечение эритропоэтинами не уменьшало смертность, риск кардиоваскулярных событий или частоту госпитализаций [31]. Американский Колледж Врачей не рекомендует использование эритропоэтинов у пациентов с сердечной недостаточностью или коронарной болезнью сердца при незначительной или умеренной степени тяжести анемии [31].
Переливание крови было предложено для коррекции тяжелой анемии у пациентов с коронарной болезнью сердца, но результаты ее эффективности противоречивы. Большинство данных получено при использовании либеральных или рестриктивных протоколов гемотрансфузий. Либеральный подход к переливанию крови был определен как гемотрансфузия при уровне гемоглобина менее 90 г/л. Рестриктивная трансфунзионная стратегия — трансфузия с уровнем гемоглобина менее 70 г/л. Метаанализ 10 исследований, включавший 203,665 пациентов с острым коронарным синдромом выявил, что либеральная гемотрансфузия ассоциировалась с увеличением общей смертности по сравнению с рестриктивной гемотрансфузией или ведением пациентов без нее [32]. Но стоит отметить, что гемотрансфузия ассоциировалась со значимым увеличением риска смерти к 30-му дню только при показателе гематокрита более 25% [32].
Рестриктивная трансфунзионная стратегия — трансфузия с уровнем гемоглобина менее 70 г/л. Метаанализ 10 исследований, включавший 203,665 пациентов с острым коронарным синдромом выявил, что либеральная гемотрансфузия ассоциировалась с увеличением общей смертности по сравнению с рестриктивной гемотрансфузией или ведением пациентов без нее [32]. Но стоит отметить, что гемотрансфузия ассоциировалась со значимым увеличением риска смерти к 30-му дню только при показателе гематокрита более 25% [32].
На сегодняшний день нет единого мнения в отношении либеральной и рестриктивной гемотрансфузионной тактики у пациентов с ИБС. Ряд исследований с низкой степенью доказательности показывают, что ограничительная трансфузия не оказывает эффект на смертность у пациентов с коронарной патологией сердца по сравнению с либеральной трансфузией. Ряд исследований, основанных на клиническом наблюдении пациентов, выдвинули утверждение: гемотрансфузия не имеет практической пользы и может нанести вред пациентам с сердечно-сосудистой патологией при уровне гемоглобина более 100г/л [31]. Пилотное исследование, включавшее 110 пациентов с острым коронарным синдромом или стабильной стенокардией, которые подвергались коронарным вмешательствам, продемонстрировало, что гемоглобин менее 100г/л коррелировал с тенденцией к увеличению больших коронарных событий, включая смерть от сердечно-сосудистых причин у пациентов с либеральной по сравнению с рестриктивной стратегией гемотрансфузий [33].
Пилотное исследование, включавшее 110 пациентов с острым коронарным синдромом или стабильной стенокардией, которые подвергались коронарным вмешательствам, продемонстрировало, что гемоглобин менее 100г/л коррелировал с тенденцией к увеличению больших коронарных событий, включая смерть от сердечно-сосудистых причин у пациентов с либеральной по сравнению с рестриктивной стратегией гемотрансфузий [33].
Из-за противоречивых результатов исследований и недостатка полноценных рандомизированных контролируемых исследований рестриктивная гемотрансфузия может иметь место в условиях острого коронарного синдрома и у госпитализированных пациентов с коронарной болезнью сердца [31, 34].
Положительные эффекты лечения внутривенными препаратами железа при дефиците железа с анемией или без у пациентов с сердечной недостаточностью
Железо является жизненно необходимым элементом для организации целого ряда жизненно важных функций в организме. Оно служит переносчиком кислорода к клеткам, является частью важных ферментных систем в различных тканях. Железосодержащие ферменты выполняют функцию по переносу электронов внутри клетки, а их функция в окислительном метаболизме – перенос энергии внутри митохондрии. Другой ключевой функцией железосодержащих ферментов (например, цитохром Р450) является синтез стероидных гормонов и желчных кислот; обезвреживание токсинов в печени; контроль эффекта нейротрансмиттеров, таких как допамин, и серотониновых систем головного мозга [35].
Железосодержащие ферменты выполняют функцию по переносу электронов внутри клетки, а их функция в окислительном метаболизме – перенос энергии внутри митохондрии. Другой ключевой функцией железосодержащих ферментов (например, цитохром Р450) является синтез стероидных гормонов и желчных кислот; обезвреживание токсинов в печени; контроль эффекта нейротрансмиттеров, таких как допамин, и серотониновых систем головного мозга [35].
Несколько исследований были адресованы лечению пациентов с заболеваниями сердца внутривенными препаратами железа. Данные Fair-HF исследования, которое включало пациентов с анемией и без продемонстрировали: только 27,6% пациентов, получавших препарат карбоксимальтозы железа внутривенно, имели кардиоваскулярные события по сравнению с 50,2% пациентов, получавших плацебо (р=0.01). Внутривенное назначение карбоксимальтозы железа увеличивало переносимость и продолжительность физических нагрузок у пациентов со стабильной сердечной недостаточностью и хроническим заболеванием почек (ХБП), не выше 3 стадии ХБП. У большинства пациентов, включенных в исследование, уровень ферритина был менее 100 мг/л [36]. Это исследование показало, что назначение 200 мг препарата карбоксимальтозы железа внутривенно увеличивало дистанцию теста 6-минутной ходьбы (317 м против 277 м) по сравнению с внутривенным назначением физиологического раствора [36]. Данное исследование с умеренной степенью доказанности продемонстрировало, что внутривенный препарат железа улучшал качество жизни у пациентов с анемией или дефицитом железа со стабильным течением ХСН и хроническим заболеванием почек не выше 3 стадии. Fair-HF исследование показало, что лечение внутривенным препаратом железа улучшало функциональный класс сердечной недостаточности и показатели качества жизни независимо от того, присутствовали в пациента лабораторные признаки анемии или нет [36]. Это исследование также продемонстрировало отсутствие статистически значимой разницы в частоте существенных побочных эффектов между пациентами, принимавшими внутривенно карбосимальтозу железа, и контрольной группой [36].
У большинства пациентов, включенных в исследование, уровень ферритина был менее 100 мг/л [36]. Это исследование показало, что назначение 200 мг препарата карбоксимальтозы железа внутривенно увеличивало дистанцию теста 6-минутной ходьбы (317 м против 277 м) по сравнению с внутривенным назначением физиологического раствора [36]. Данное исследование с умеренной степенью доказанности продемонстрировало, что внутривенный препарат железа улучшал качество жизни у пациентов с анемией или дефицитом железа со стабильным течением ХСН и хроническим заболеванием почек не выше 3 стадии. Fair-HF исследование показало, что лечение внутривенным препаратом железа улучшало функциональный класс сердечной недостаточности и показатели качества жизни независимо от того, присутствовали в пациента лабораторные признаки анемии или нет [36]. Это исследование также продемонстрировало отсутствие статистически значимой разницы в частоте существенных побочных эффектов между пациентами, принимавшими внутривенно карбосимальтозу железа, и контрольной группой [36].
Целью CONFIRM-HF исследования было изучение долгосрочного эффекта от лечения препаратом карбоксимальтозой железа у пациентов с симптоматической сердечной недостаточностью и дефицитом железа. В исследование было включено 304 пациента со стабильной сердечной недостаточностью класса II или III согласно Нью-Йоркской Ассоциации Сердца (NYHA), с фракцией выброса левого желудочка ≤45%, повышенным уровнем натрийуритических пептидов (мозговой натрийуретический пептид >100 пг/мл и/или N-терминальный фрагмент натрийуритического пептида > 400 пг/мл), наличием дефицита железа (уровень сыворочного феритина < 100нг/мл, или от 100 до 300 нг/мл, если сатурация трансферрина < 20%) и гемоглобином до 15 г/дл.
В результате исследования было выявлено, что лечение стабильных симптоматических пациентов с сердечной недостаточностью и дефицитом железа внутривенным препаратом карбоксимальтозой железа приводит к устойчивому улучшению их функционального состояния согласно тесту 6-минутной ходьбы; улучшению качества жизни; значительному уменьшению риска госпитализаций вследствие прогрессирования сердечной недостаточности. Наблюдения за пациентами осуществлялось в течение одного года. Вышеперечисленные положительные эффекты были отмечены во всех подгруппах, включая пациентов с анемией или без нее [37].
Наблюдения за пациентами осуществлялось в течение одного года. Вышеперечисленные положительные эффекты были отмечены во всех подгруппах, включая пациентов с анемией или без нее [37].
Результаты CONFIRM-HF исследования по сравнению с Fair-HF имели более объективные первичную и конечную точки, показали более продолжительный положительный эффект от лечения карбоксимальтозой железа с хорошим профилем безопасности и продемонстрировали значительное снижение риска госпитализации вследствие ухудшения сердечной недостаточности [37].
Метаанализ всех рандомезированных контролируемых исследований, изучавших эффект лечения внутривенными препаратами железа у пациентов с систолической сердечной недостаточностью и дефицитом железа, показал, что ее применение у данной категории пациентов уменьшает риск комбинированных конечных точек: общей смертности и сердечно-сосудистых госпитализаций, сердечно-сосудистой смертности и госпитализации по поводу ухудшения сердечной недостаточности, и риск госпитализаций по причине декомпенсации ХСН. Не было выявлено значимого эффекта на общую и на смертность от сердечно-сосудистых причин. Вместе с тем, внутривенная терапия препаратами железа приводила к улучшению переносимости физических нагрузок, уменьшению симптомов сердечной недостаточности и улучшению качества жизни пациентов [38].
Не было выявлено значимого эффекта на общую и на смертность от сердечно-сосудистых причин. Вместе с тем, внутривенная терапия препаратами железа приводила к улучшению переносимости физических нагрузок, уменьшению симптомов сердечной недостаточности и улучшению качества жизни пациентов [38].
Внутривенное назначение препарата карбоксимальтозы железа должно рассматриваться в качестве лечения у симптомных пациентов с систолической сердечной недостаточностью и дефицитом железа для уменьшения клинических проявлений, повышения толерантности к физическим нагрузкам и улучшения качества жизни [39].
Заключение
Лечение анемии у пациентов с заболеваниями сердца может существенно отличаться от лечения анемии в общей популяции. Однако понимание доказательной базы и использование клинического суждения крайне необходимы для лечения данной категории лиц. Анемия коррелирует с ухудшением прогнозов у пациентов с кардиоваскулярной патологией и становится новой терапевтической мишенью для данной категории пациентов.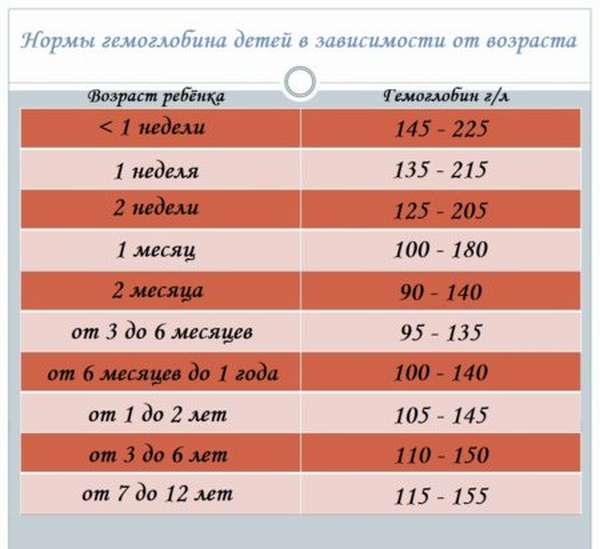 Вопрос, является ли анемия причиной или маркером неблагоприятных исходов и отражает лишь тяжесть сердечно — сосудистого заболевания, остается актуальным по сей день.
Вопрос, является ли анемия причиной или маркером неблагоприятных исходов и отражает лишь тяжесть сердечно — сосудистого заболевания, остается актуальным по сей день.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов, способного повлиять на результаты исследования или их трактовку.
Introduction. Cardiovascular disease is a significant health problem around the world and accounts for the majority of deaths annually. Many of such patients have anemia due to acute blood loss (surgery or trauma) or chronic conditions such as renal failure or cancer.
According to the World Health Organization criteria anemia is defined in cases when hemoglobin is less than 120 g/l in females and less than 30 g/l in males. It is a major health problem that increases the mortality rate, affects physical status, and demands referral to health-care professionals. Globally, anemia affects 1.62 billion people, which corresponds to 24. 8% of the total population. The highest prevalence is in preschool-age children (47.4%), and the lowest prevalence is in men (12.7%). Half of the cases are due to iron deficiency [1] which affects not only red blood cell production but also cellular functions related to muscle metabolism, mitochondrial function, neurotransmitters, DNA synthesis, and the immune system [2].
8% of the total population. The highest prevalence is in preschool-age children (47.4%), and the lowest prevalence is in men (12.7%). Half of the cases are due to iron deficiency [1] which affects not only red blood cell production but also cellular functions related to muscle metabolism, mitochondrial function, neurotransmitters, DNA synthesis, and the immune system [2].
Prevalence of anemia increases with the advanced age making it a common associated comorbidity in patients with cardiovascular diseases. It has been established that anemia is an independent risk factor for cardiovascular diseases (CVD) outcomes [3].
Effects of anemia on the cardiovascular system. Understanding the physiologic response to anemia is important in order to take into account the implications of this state in regards to cardiac diseases. Three main factors are responsible for oxygen delivery to organs: blood flow and its distribution; the oxygen-carrying capacity of the blood, i. e. hemoglobin concentration; and oxygen extraction. Hypoxia in anemia is compensated through several non-hemodynamic (increased erythropoietin production to stimulate erythropoiesis, increased oxygen extraction) and hemodynamic mechanisms. The main hemodynamic factors are decreased afterload, increased preload, and positive inotropic and chronotropic effects. Enhanced nitric oxide activity, hypoxia-induced vasodilatation and lower blood viscosity are responsible for reduced vascular resistance and lead to the decreased afterload. Chronic anemia stimulates angiogenesis and recruitment of new microvessels. Enhanced venous return (preload) and left ventricular (LV) filling lead to the increased LV end-diastolic volume and cardiac output. Increased cardiac output is responsible for arterial remodeling of the central elastic arteries such as the aorta and common carotid artery through arterial enlargement and compensatory arterial intima-media thickening, leading to the elevated systolic pressure and high inertia due to higher blood mass in the dilated arterial system.
e. hemoglobin concentration; and oxygen extraction. Hypoxia in anemia is compensated through several non-hemodynamic (increased erythropoietin production to stimulate erythropoiesis, increased oxygen extraction) and hemodynamic mechanisms. The main hemodynamic factors are decreased afterload, increased preload, and positive inotropic and chronotropic effects. Enhanced nitric oxide activity, hypoxia-induced vasodilatation and lower blood viscosity are responsible for reduced vascular resistance and lead to the decreased afterload. Chronic anemia stimulates angiogenesis and recruitment of new microvessels. Enhanced venous return (preload) and left ventricular (LV) filling lead to the increased LV end-diastolic volume and cardiac output. Increased cardiac output is responsible for arterial remodeling of the central elastic arteries such as the aorta and common carotid artery through arterial enlargement and compensatory arterial intima-media thickening, leading to the elevated systolic pressure and high inertia due to higher blood mass in the dilated arterial system. Activation of sympathetic activity enhances LV contractility, and the heart rate. Short-lasting anemia is reversible but in chronic anemia hemodynamic changes lead to cardiac enlargement and development of eccentric LV hypertrophy (LVH). It also occurs in other forms of the volume overload. In case of heart diseases chronic anemia contributes to a high incidence of cardiovascular complications [4].
Activation of sympathetic activity enhances LV contractility, and the heart rate. Short-lasting anemia is reversible but in chronic anemia hemodynamic changes lead to cardiac enlargement and development of eccentric LV hypertrophy (LVH). It also occurs in other forms of the volume overload. In case of heart diseases chronic anemia contributes to a high incidence of cardiovascular complications [4].
Anemia in arterial hypertension
Normocytic anemia is common in hypertensive patients but more prevalent in uncontrolled hypertension. Lower hemoglobin is associated with poor blood pressure control, indicating a higher cardiovascular risk in uncontrolled hypertension [5]. It was noted that hypertensive patients with anemia had higher nocturnal systolic and mean blood pressure and a lower dipping status compared to the patients with normal hemoglobin levels. There was a trend for increased diastolic blood pressure [6].
In patients with isolated systolic hypertension and left ventricular hypertrophy lower hemoglobin was associated with the increased cardiovascular death or stroke [7].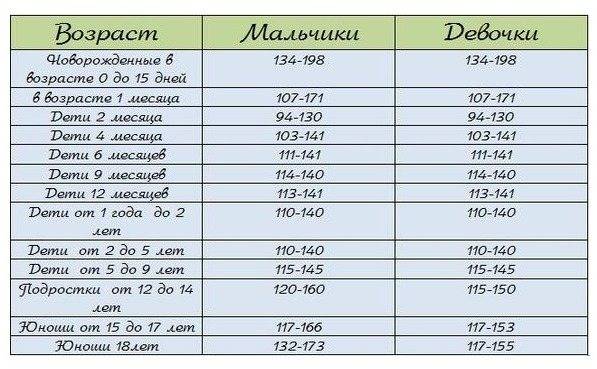
Electrocardiographic changes in anemia.
Electrocardiographic (ECG) repolarization abnormalities (ST segment depression, T wave inversion, prolonged QT) are highly prevalent in anemic patients at rest and during the tests with physical loading [8]. It has been shown that the hemoglobin level is strongly correlated with ECG changes [9].
A long ECG QT interval duration is a predictor of ventricular arrhythmia and sudden cardiac death. Hypoxia and impaired oxygen supply in anemic patients may affect repolarization of the myocardium. It has been found that anemia, macrocytosis and anisocytosis are associated with prolonged QT intervals in hypertensive patients and may contribute to the risk of sudden cardiac death [10]. Low iron stores in otherwise healthy children negatively correlated with QT and QTc intervals and may indicate some risk in developing arrhythmias [11].
Mehta et al. showed significant reproducible ST depression in anemic patients with iron deficiency during the tests with physical loading. These electrophysiological changes were corrected after iron therapy, even before the rise of hemoglobin occurred, which may be explained by the effect of iron on the tissue level [12].
These electrophysiological changes were corrected after iron therapy, even before the rise of hemoglobin occurred, which may be explained by the effect of iron on the tissue level [12].
Anemia in Ischemic Heard Disease
Myocardial ischemia is defined as oxygen delivery that is insufficient to meet oxygen requirements. The determinants of myocardial oxygen demand are wall tension, heart rate and contractility. The determinants of myocardial oxygen delivery are arterial oxygen content and coronary arterial blood flow. The increase of oxygen delivery in response to the enhancement of oxygen demand occurs through the changes in coronary vascular resistance, as the extraction ratio of myocardium at rest is nearly 90% [13]. Patients without coronary artery disease, therefore, have a tremendous ability to compensate the decrease in coronary arterial oxygen content through distal vasodilatation but in the presence of coronary stenosis this compensatory mechanism has a limited ability.
It was proved that anemic animals have the increased infarct size, decreased cardiac function and the survival rate in case of acute myocardial infarction (MI). Transfusion of fresh blood to anemic animals up to 100 g/L Hb reduced the infarct size and improved the cardiac function. However, blood transfusion up to 120 g/L Hb was associated with larger infarcts [14].
Sabatine et al. found out a U-shaped relationship with clinical events by the 30th day: in patients with ST-elevation MI; the mortality rate was higher in those with the hemoglobin levels below 140g/L or above 170g/L, while in patients with non-ST elevation acute coronary syndrome (ACS), death, infarction and ischemia increased in case when hemoglobin levels were below 110g/L or above 160/L [15].
Anemia is a risk factor for ischemic heart disease. Patients with ischemic heard disease (IHD) and anemia have a more advanced degree of ischemic heart disease compared to patients with isolated IHD. In anemic patients with IHD the level of hemoglobin, serum iron and total iron-binding capacity negatively correlated with the severity of IHD [16]. The mortality rate in anemic patients with IHD was higher than in patients with isolated IHD [16]. Anemia was an independent predictor of acute coronary syndrome based on the hemoglobin level, while both anemia and a high hematocrit level were predictors of myocardial infarction based on hematocrit [17].
The mortality rate in anemic patients with IHD was higher than in patients with isolated IHD [16]. Anemia was an independent predictor of acute coronary syndrome based on the hemoglobin level, while both anemia and a high hematocrit level were predictors of myocardial infarction based on hematocrit [17].
The investigations made by Ferreira et al. revealed that hemoglobin<108g/L was one of the strongest independent predictors of one-year mortality in population with acute coronary syndrome (ACS). He suggested including the hemoglobin level in risk stratification scores of patients admitted for ACS, given that it is an easy parameter to measure and is systematically assessed at admission [18].
In the Cadilac trial anemia was common in patients with AMI who underwent primary PCI and was strongly associated with the adverse outcomes and increased mortality [19]. Anemia was an independent predictor of in-hospital mortality by the end of the first year [19].
Severe anemia can lead to disbalance between oxygen delivery and demand in the myocardium even in patients without coronary stenosis. Bailey D et al. reported a case of the ST segment elevation myocardial infarction (STEMI) secondary to severe anemia which occurred in the absence of angiographically significant coronary artery stenosis, thrombosis or coronary artery spasm [20].
Bailey D et al. reported a case of the ST segment elevation myocardial infarction (STEMI) secondary to severe anemia which occurred in the absence of angiographically significant coronary artery stenosis, thrombosis or coronary artery spasm [20].
Thus, there are a number of reasons for the worse outcomes in anemic patients with the obstructive coronary artery disease. Diminished oxygen-carrying capacity, activation of the sympathetic nervous system can increase myocardial oxygen demand and worsen ischemia.
Anemia in Heart Failure
Anemia is a very common comorbidity in chronic heart failure. Anemic patients are elderly women with more advanced symptoms and signs of heart failure, greater functional impairment and a higher hospitalization rate; they have a history of diabetes mellitus, renal insufficiency, and hypertension [21]. Anemia is a powerful predictor of rehospitalization rates and survival in case of chronic heart failure [22]. The prevalence of anemia increases with the severity of heart failure (HF) and can reach 79. 1% in those with Class IV according to the classification of the New York Heart Association [23].
1% in those with Class IV according to the classification of the New York Heart Association [23].
Etiology of anemia in HF may be multifactorial and a number of potential mechanisms may be responsible for such a condition in heart failure. Neurohormonal and inflammatory activation, renal dysfunction, bone marrow hyporesponsiveness, malnutrition, drug effects contribute to its development. Increased circulating proinflammatory cytokines enable defective iron mobilization, inappropriate erythropoietin production, depressed bone marrow function. Activation of the renin-angiotensin-aldosteron system, decreased renal perfusion caused by the low blood pressure and stroke volume stimulate the release of erythropoietin but the response is blunted due to effect of the circulatory cytokines. Poor nutrition due to anorexia, gastrointestinal malabsorbtion and aspirin use may precipitate iron deficiency anemia. Hemodilution can contribute to anemia. The use of the angiotensin-converting enzyme (ACE) inhibitor therapy may reduce secretion of erythropoietin [24].
Iron deficiency (ID) is the most frequent cause of anemia in patients with HF [25, 26] and can be revealed in ∼46% of non-anemic patients with stable systolic HF [27].
Iron deficiency may exist in absolute or functional forms. Absolute iron deficiency occurs when total body iron stores become exhausted and ID anemia can be considered as the final phase of iron stores depletion; functional iron deficiency refers to inadequate iron release in response to the demands of the bone marrow. Functional iron deficiency can be seen in many acute and chronic inflammatory states. ID is associated with the worsening of symptoms in patients with heart failure, impaired life quality, the increased mortality and hospitalization level [28, 29, 30].
Activation of sympathetic and renin-angiotensin-aldosteron systems, chronic inflammation, absolute and functional iron deficiency, impaired production and activity of erythropoietin, hemodilution, renal dysfunction impair prognosis in heart failure patients. Probably, anemia acts as a mediator and a marker of a poor prognosis in HF patients.
Probably, anemia acts as a mediator and a marker of a poor prognosis in HF patients.
Treatment of anemia in patients with heart diseases. Anemia treatment strategies in heart failure and CHD patients include erythropoiesis-stimulating agents (ESAs), red blood cell transfusions and iron replacement in iron deficient patients with or without anemia.
Sixteen randomized, controlled trials assessed the impact of ESAs in patients with heart disease. Most of these studies included patients with CHF and the reduced systolic function. Overall, moderate-quality evidence showed no benefit from ESAs in regard to improving exercise tolerance and duration or quality of life, and high-quality evidence showed no mortality benefit [31]. Serious harmful effects associated with the treatment include mortality and vascular thrombosis [31]. So, the damage outweighs the benefits in treatment of patients with mild to moderate anemia using ESAs. Although anemia is common in patients with CHF and CHD, treatment with ESAs did not decrease mortality, cardiovascular events or hospitalization rates [31]. The American College of Physicians does not recommend using erythropoiesis-stimulating agents to patients with mild to moderate anemia and congestive heart failure or coronary heart disease [31].
The American College of Physicians does not recommend using erythropoiesis-stimulating agents to patients with mild to moderate anemia and congestive heart failure or coronary heart disease [31].
Blood transfusion has been suggested to correct severe anemia in patients with coronary artery disease, but data in regard to its effectiveness are contradictory. In the majority of studies investigating different transfusion protocols, a liberal blood transfusion strategy was defined as any red blood cell transfusion at a hemoglobin level up to 90 g/L, while a restrictive blood transfusion strategy was defined as any transfusion at a hemoglobin level up to 70 g/L. A meta-analysis of 10 studies totaling 203 665 patients with acute coronary syndrome (both STEMI and NSTEMI-ACS) reported that blood transfusion or a liberal transfusion strategy was associated with the increased all-cause mortality, compared with no blood transfusion or a restrictive transfusion strategy [32]. However, a transfusion or liberal transfusion strategy was associated with a significantly higher mortality risk by the 30th day only in case when a nadir hematocrit is more than 25% [32].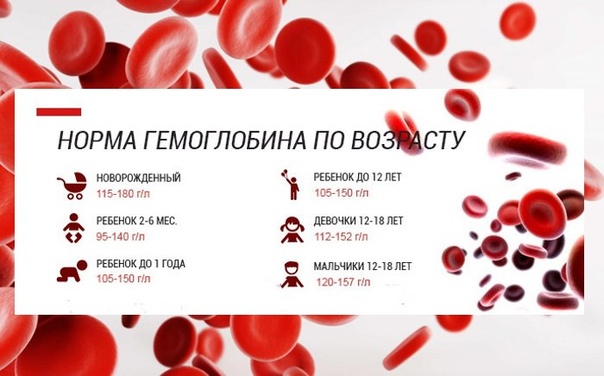
However, low-quality evidence data demonstrate that blood transfusion using restrictive compared with liberal transfusion protocols had no effect on mortality in patients with CHD. Observational studies suggested that transfusion is not beneficial and may be harmful for patients with heart disease and hemoglobin levels of more than 100 g/L (31). A pilot trial of 110 patients with acute coronary syndrome or stable angina undergoing cardiac catheterization and hemoglobin <100 g/L revealed a trend of fewer major cardiac events and deaths in patients with the liberal transfusion strategy as compared with a more restrictive strategy [33].
Due to inconsistent results of the studies and the lack of adequately powered RCTs restrictive red blood cell transfusion strategy may be considered in the settings of ACS and for hospitalized patients with coronary heart disease [31, 34]
Benefits of using intravenous iron injections in treatment of iron deficiency with or without anemia in HF patients.
Iron has several vital functions in the body. It serves as a carrier of oxygen to the tissues, a transport medium for electrons within cells, and an integrated part of important enzyme systems in various tissues. Several iron-containing enzymes act as electron carriers within the cell and their role in the oxidative metabolism is to transfer energy within the cell and mitochondria. Other key functions for the iron-containing enzymes (e.g. cytochrome P450) include synthesis of steroid hormones and bile acids; detoxification of foreign substances in the liver; and signal controlling in some neurotransmitters, such as the dopamine and serotonin systems in the brain [5].
Few studies addressed to intravenous iron therapy for patients with heart disease. Data from Fair-HF study, which included patients with and without anemia demonstrated, that 27.6% of patients treated with intravenous iron carboxymaltose had cardiovascular events compared with 50.2% of patients receiving placebo (p=0. 01). Moderate-quality evidence showed that intravenous iron administration increased exercise tolerance and duration in patients with stable CHF including patients with Stage 3 chronic kidney disease. FAIR-HF trial (Ferinject Assessment in Patients with Iron Deficiency and Chronic Heart Failure) included anemic and nonanemic patients, with the majority of them having ferritin levels less than 100 µg/L [36]. This trial showed that 200 mg of intravenous ferric carboxymaltose (FCM) increased a 6-minute walk distance (313 m vs. 277 m) compared with intravenous saline [36]. Moderate-quality evidence showed that intravenous iron improved quality of life in patients with anemia or iron deficiency, stable CHF, and chronic kidney disease excluding the patients with the 4th and 5th stages. The FAIR-HF study showed that intravenous iron treatment improved Patient Global Assessment scores compared with control patients and the improved NYHA functional class, regardless of the anemia status (hemoglobin level ≤120 g/L) [36].
01). Moderate-quality evidence showed that intravenous iron administration increased exercise tolerance and duration in patients with stable CHF including patients with Stage 3 chronic kidney disease. FAIR-HF trial (Ferinject Assessment in Patients with Iron Deficiency and Chronic Heart Failure) included anemic and nonanemic patients, with the majority of them having ferritin levels less than 100 µg/L [36]. This trial showed that 200 mg of intravenous ferric carboxymaltose (FCM) increased a 6-minute walk distance (313 m vs. 277 m) compared with intravenous saline [36]. Moderate-quality evidence showed that intravenous iron improved quality of life in patients with anemia or iron deficiency, stable CHF, and chronic kidney disease excluding the patients with the 4th and 5th stages. The FAIR-HF study showed that intravenous iron treatment improved Patient Global Assessment scores compared with control patients and the improved NYHA functional class, regardless of the anemia status (hemoglobin level ≤120 g/L) [36].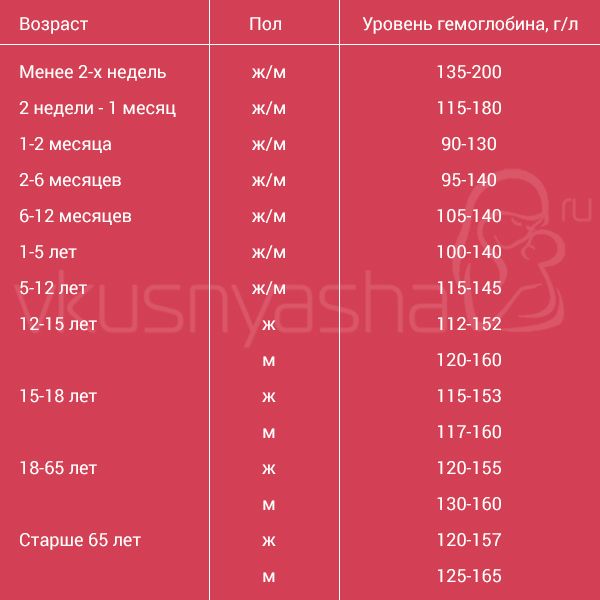 This trial also showed improved life quality. [36]. There was no statistically significant difference in serious harmful effects between the intravenous iron treatment and the control groups [36].
This trial also showed improved life quality. [36]. There was no statistically significant difference in serious harmful effects between the intravenous iron treatment and the control groups [36].
The CONFIRM-HF trial was aimed at studying effects of long-term intravenous iron therapy in ferric carboxymaltose inpatients with symptomatic heart failure and iron deficiency. Totally 304 patients with stable ambulatory HF (class II or III according to New York Heart Association (NYHA) classification) and left ventricular ejection fraction (LVEF) ≤45%, elevated natriuretic peptides (brain natriuretic peptide >100 pg/mL and/or N-terminal-pro-brain natriuretic peptide>400 pg/mL), presence of ID (defined as serum ferritin level <100 ng/mL, or between 100 and 300 ng/mL if transferrin saturation was <20%) and hemoglobin (Hb) up to15 g/L were enrolled in the study. This study showed that treatment of stable, symptomatic, ‘iron-deficient HF patients with intravenous iron (FCM) results in sustainable improvement of functional capacity as measured over a 1-year period using the 6-MWT walking test, improvement in quality of life, significantly reduced risk of hospital admission due to worsening of HF during a1-year follow-up period. These favorable results were consistent across all pre-specified subgroups including patients with and without anemia [37].
These favorable results were consistent across all pre-specified subgroups including patients with and without anemia [37].
The results of CONFIRM-HF compared with FAIR-HF had a more objective primary end-point, documented longer-term sustainability of beneficial effects of treatment with FCM and the acceptable safety profile (i.e. 12 months compared with 6 months or less in previous studies) and provided data on significant risk reduction of the hospitalization due to HF worsening [37].
A meta-analysis of all randomized controlled trials that investigated the effects of intravenous iron therapy in iron-deficient patients with systolic HF (also analyzed separately in anemic and non-anemic subjects) showed that intravenous iron therapy in patients with systolic HF and ID reduced the risk of the combined endpoint of all-cause death or cardiovascular hospitalization, the risk of the combined endpoint of cardiovascular death or hospitalization due to advanced HF. However there was no effect on either all-cause or cardiovascular mortality, parenteral iron therapy resulted in the improved exercise capacity (as reflected by a longer 6MWT distance) and life quality, and also in alleviation of HF symptoms (reduction in the NYHA class) [38].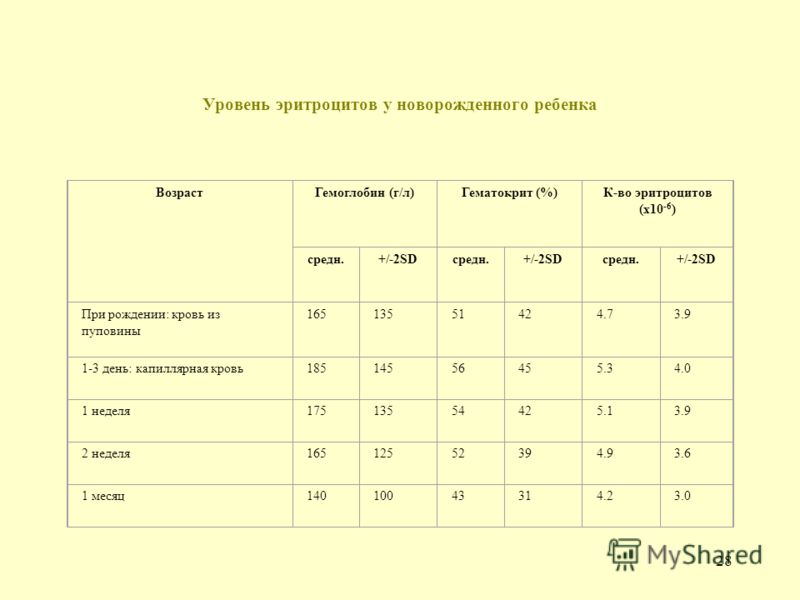
Intravenous FCM should be considered in symptomatic patients with systolic heart failure and iron deficiency (serum ferritin level <100 ng/mL, or between 100 and 300 ng/mL if transferrin saturation <20%) in order to alleviate HF symptoms, and improve exercise capacity and life quality [39].
Conclusion. Management of patients with heart disease and anemia might appropriately differ from that of the general population. Hence, clinical judgment and understanding the evidence base are critical when managing these patients. Anemia is associated with worse outcomes in patients with cardiovascular diseases. However, it is uncertain if anemia is the cause or the marker of poor outcomes and thus it only reflects advanced cardiovascular disease.
1. de Benoist B. et al., eds. Worldwide prevalence of anaemia 1993-2005. WHO Global Database on Anaemia Geneva, World Health Organization, 2008.
2. von DrygalskiA., Adamson J. W. Ironing out fatigue. Blood,2011, vol. 118, pp. 3191-3192.
118, pp. 3191-3192.
3. Sarnak M. J., Tighiouart H., Manjunath G., MacLeod B., Griffith J., Salem D., Levey A. S. Anemia as a Risk Factor for Cardiovascular Disease in the Atherosclerosis Risk in Communities (ARIC) Study. J Am Coll Cardiology, 2002, vol. 40, no. 1, pp. 27-33.
4. Metivier F., Marchais S. J., Guerin A. P., Pannier B., London G. M. Pathophysiology of anaemia: focus on the heart and blood vessels, Nephrol Dial Transplant, 2000, vol. 15, no. 3, pp. 14-18.
5. Paul B., Wilfred N. C., Woodman R., Depasquale C. Prevalence and correlates of anaemia in essential hypertension. Clin Exp Pharmacol Physio, 2008, vol. 35, no. 12, pp. 1461-1464
6. Marketou M., Patrianakos A., Parthenakis F. Systemic blood pressure profile in hypertensive patients with low hemoglobin concentrations. Int J Cardiol, 2010, vol. 142, no. 1, pp. 95-96.
7. Marianne L. Smebye Emil K. Iversen A. H. Effect of Hemoglobin Levels on Cardiovascular Outcomes in Patients With Isolated Systolic Hypertension and Left Ventricular Hypertrophy (from the LIFE Study). Am J Cardiol, 2007, Sep 1, vol. 100, no. 5, pp. 747-912.
Am J Cardiol, 2007, Sep 1, vol. 100, no. 5, pp. 747-912.
8. Stanojevic M., Stankov S. Electrocardiographic changes in patients with chronic anemia. Srp Arh Celok Lek, 1998, Nov-Dec. 126, no. 11-12, pp. 461-466.
9. Gv S., Pk S., Herur A., Chinagudi S., Patil S. S., Ankad R. B., Badami S. V. Correlation Between Haemoglobin Level and Electrocardiographic (ECG) Findings in Anaemia: A Cross-Sectional Study. J Clin Diagn Res, 2014, vol. 8, no.:4, doi: 10.7860/ JCDR/2014/8966.4202.
10. Mozos I., Serban C., Mihaescu R. Anemia and the QT interval in hypertensive patients. Int J Coiiabor Res Int Med Public Health, 2012, vol. 4, no 12, pp. 2084-2091.
11. Karadeniz C., Ozdemir R., Demirol M., Katipoglu N., Yozgat Y., Mege T., Onal N. Low Iron Stores in Otherwise Healthy Children Affect Electrocardiographic Markers of Important Cardiac events. Pediatr Cardiol, 2017, vol. 38, no. 5, pp. 909-914.
12. Mehta B. C., Panjwani D. D., Jhala D. A. Electrophysiologic abnormalities of heart in iron deficiency anemia.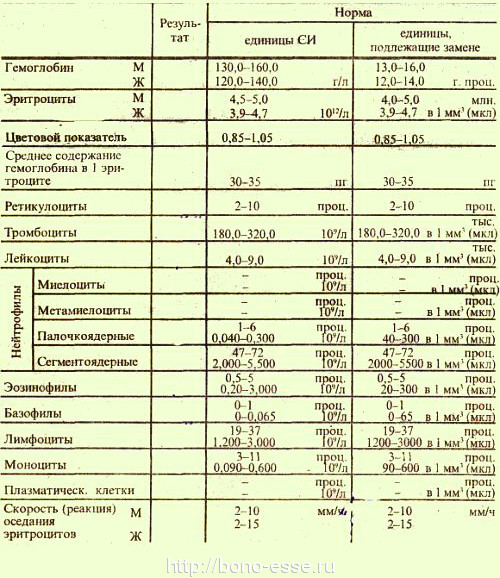 Effect of iron therapy. Acta Haematol, 1983, vol. 70, no. 3, pp. 189-193.
Effect of iron therapy. Acta Haematol, 1983, vol. 70, no. 3, pp. 189-193.
13. Hoffman J. I. Determinants and prediction of transmural myocardial perfusion. Circulation, 1978, vol. 58, pp. 381-339.
14. Hu H., Xenocostas A., Chin-Yee I., Lu X., Feng Q., Effects of anemia and blood transfusion in acute myocardial infarction in rats. Transfusion, 2010, vol. 50, no. 1. pp. 243-251.
15. Sabatine M. S., Morrow D. A., Giugliano R. P., Burton P. B., Murphy S. A., McCabe C.H., Gibson C. M., Braunwald E. Association of hemoglobin levels with clinical outcomes in acute coronary syndromes. Circulation, 2005, vol. 111, pp. 2042-2049.
16. Zeidman A., Fradin Z., Blecher A., Oster H. S., Avrahami Y., Mittelman M., Anemia as a risk factor for ischemic heart disease. Circulation. 2004, vol. 6, no. 1, pp. 16-18.
17. Mahmoodi M. R., Kimiagar S. M., Abadi A. R. Is anemia an independent predictor of occurrence of acute coronary syndrome? Results from the modares heart study. Am Heart Hosp J, 2007, vol. 5, no. 2, pp. 73-79.
5, no. 2, pp. 73-79.
18. Ferreira M., Antonio N., Gongalves F., Hemoglobina: um mero valor analitico ou um poderoso preditor de risco em doentes com sindromes coronarias agudas? Revista Portuguesa de Cardiologia, 2012, vol. 31, pp. 121-130.
19. Nikolsky E., Aymong E. D., Halkin A., Grines C. L., Cox D. A., Garcia E., Mehran R., Tcheng J. E., Griffin J. J., Guagliumi G., Stuckey T., Turco M., Cohen D. A., Negoita M., Lansky A. J., Stone G. W. Impact of anemia in patients with acute myocardial infarction undergoing primary percutaneous coronary intervention: Analysis from the controlled abciximab and device investigation to lower late angioplasty complications (cadillac) trial. J Am Coll Cardiol, 2004, Aug 4, vol. 44, no. 3, pp. 547-553.
20. Bailey D., Aude Y. W., Gordon P., Burtt D. ST-segment elevation myocardial infarction, severe anemia and nonobstructive coronary disease: case report and brief comment. Conn Med, 2003, vol. 67, no. 1, pp. 3-5.
21. Ezekowitz J. A., McAlister F.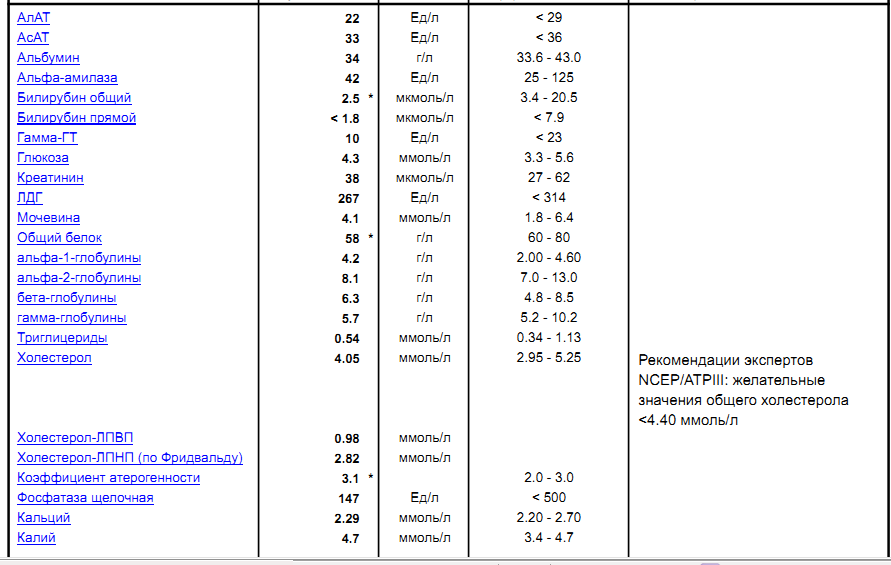 A., Armstrong P. W. Anemia is common in heart failure and is associated with poor outcomes: Insights from a cohort of 12,065 patients with new- onset heart failure. Circulation, 2003, vol. 107, pp. 223-225.
A., Armstrong P. W. Anemia is common in heart failure and is associated with poor outcomes: Insights from a cohort of 12,065 patients with new- onset heart failure. Circulation, 2003, vol. 107, pp. 223-225.
22. Mozaffarian D., Nye R., Levy W. C. Amemia predicts mortality in severe heart failure: The Prospective Randomized Amlodipine Survival Evaluation (PRAISE). J Am Coll Cardiol, 2003, vol. 41, pp. 1933-1939.
23. Silverberg D. S., Wexler D., Blum M., Keren G., Sheps D., Leibovitch E., Brosh D., Laniado S., Schwartz D., Yachnin T., Shapira I., Gavish D., Baruch R., Koifman B., Kaplan C., Steinbruch S., Iaina A. The use of subcutaneous erythropoietin and intravenous iron for the treatment of the anemia of severe, resistant congestive heart failure improves cardiac and renal function and functional cardiac class, and markedly reduces hospitalizations. J Am Coll Cardiol, 2000, vol. 35, no. 7, pp. 1737-1744.
24. Tang Y. D., Katz S. D. Anemia in chronic heart failure: Prevalence, etiology, clinical correlates and treatment options. Circulation, 2006, vol. 113, pp. 2454-2461.
Circulation, 2006, vol. 113, pp. 2454-2461.
25. Nanas J. N., Matsouka C., Karageorgopoulos D., Leonti A., Tsolakis E., Drakos S. G., Tsagalou E. P., Maroulidis G. D., Alexopoulos G. P., Kanakakis J. E., Anastasiou-Nana M. I. Etiology of anemia in patients with advanced heart failure. J Am Coll Cardiol, 2006, vol. 48, pp. 2485-2489.
26. Jankowska E. A., von Haehling S., Anker S. D., Macdougall I. C., Ponikowski P. Iron deficiency and heart failure: diagnostic dilemmas and therapeutic perspectives. Eur Heart J, 2013, vol. 34, pp. 816-829.
27. Klip I. T., Comin-Colet J., Voors A. A., Ponikowski P., Enjuanes C., Banasiak W., Lok D. J., Rosentryt P., Torrens A., Polonski L., van Veldhuisen D. J., van der Meer P., Jankowska E. A. Iron deficiency in chronic heart failure: an international pooled analysis. Am Heart J, 2013, vol. 165, pp. 575-582.e3.
28. Jankowska E. A., Rozentryt P., Witkowska A., Nowak J., Hartmann O., Ponikowska B., Borodulin-Nadzieja L., Banasiak W., Polonski L. , Filippatos G., McMurray J.J., Anker S. D., Ponikowski P. Iron deficiency: an ominous sign in patients with systolic chronic heart failure. Eur Heart J, 2010, vol. 31, pp. 1872-1880.
, Filippatos G., McMurray J.J., Anker S. D., Ponikowski P. Iron deficiency: an ominous sign in patients with systolic chronic heart failure. Eur Heart J, 2010, vol. 31, pp. 1872-1880.
29. Jankowska E. A., Rozentryt P., Witkowska A., Nowak J., Hartmann O., Ponikowska B., Borodulin-Nadzieja L., von Haehling S., Doehner W., Banasiak W., Polonski L., Filippatos G., Anker S. D., Ponikowski P. Iron deficiency predicts impaired exercise capacity in patients with systolic chronic heart failure. J Card Fail, 2011, vol. 17, pp. 899-906.
30. Enjuanes C., Klip I. T., Bruguera J., Cladellas M., Ponikowski P., Banasiak W., van Veldhuisen D. J., van der Meer P., Jankowska E. A., Comin-Colet J. Iron deficiency and health-related quality of life in chronic heart failure: results from a multicenter European study. Int J Cardiol, 2014, vol. 174, pp. 268-275. doi: 10.1016/j.ijcard.2014.03.169.
31. Qaseem A., Humphrey L. L., Fitterman N., Starkey M., Shekelle P. Clinical Guidelines Committee of the American College of Physicians. Treatment of Anemia in Patients With Heart Disease: A Clinical Practice Guideline From the American College of Physicians. Ann Intern Med, 2013, vol. 159, no. 11, pp. 770-779.
Treatment of Anemia in Patients With Heart Disease: A Clinical Practice Guideline From the American College of Physicians. Ann Intern Med, 2013, vol. 159, no. 11, pp. 770-779.
32. Chatterjee S., Wetterslev J., Sharma A., Lichstein E., Mukherjee D. Association of blood transfusion with increased mortality in myocardial infarction: a meta-analysis and diversity-adjusted study sequential analysis. JAMA Intern Med, 2013, vol. 173, pp. 132-139.
33. Carson J. L., Brooks M. M., Abbott J. D., Chaitman B., Kelsey S. F., Triulzi D. J., Srinivas V., Menegus M. A., Marroquin O. C., Rao S. V., Noveck H., Passano E., Hardison R. M., Smitherman T., Vagaonescu T., Wimmer N. J., Williams D. O. Liberal versus restrictive transfusion thresholds for patients with symptomatic coronary artery disease. Am Heart, 2013, vol. 165, no. 6, pp. 964-971.
34. Roffi M., Patron C. ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation. Eur Heart J, 2016, vol.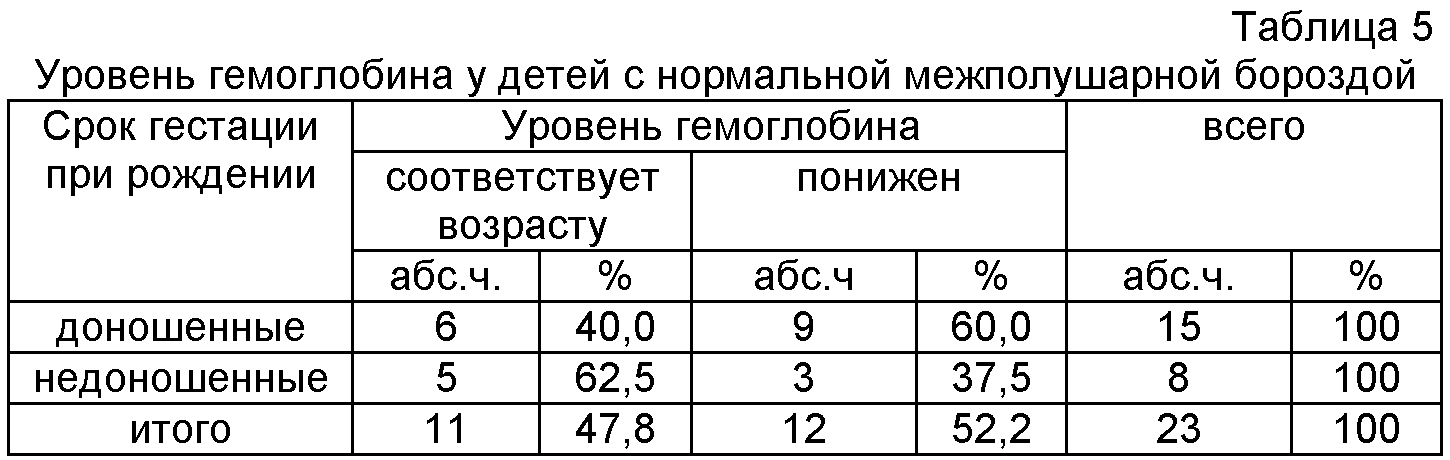 37, pp. 267-315. doi:10.1093/eurheartj/ehv320.
37, pp. 267-315. doi:10.1093/eurheartj/ehv320.
35. Gupta C. P. Role of Iron (Fe) in Body. J Appl Chem (IOSR-JAC), 2014, vol. 7, no. 11, pp. 38-46.
36. Anker S. D., Comin C. J., Filippatos G., Willenheimer R., Dickstein K., Drexler H., Luscher T. F., Bart B., Banasiak W., Niegowska J., Kirwan B. A., Mori C., von Eisenhart R. B., Pocock S. J., Poole-Wilson P.A., Ponikowski P. Ferric carboxymaltose in patients with heart failure and iron deficiency. N Engl J Med, 2009, vol. 361, no. 25, pp. 2436-2448.
37. Ponikowski P., van Veldhuisen D. J., Comin-Colet J., Ertl G., Komajda M., Mareev V., McDonagh T., Parkhomenko A., Tavazzi L., Levesque V., Mori C., Roubert B., Filippatos G., Ruschitzka F., Anker S. D. Beneficial effects of long-term intravenous iron therapy with ferric carboxymaltose in patients with symptomatic heart failure and iron deficiency. Eur Heart J, 2015, vol. 36, no. 11, pp. 657-658.
38. Jankowska E. A., Tkaczyszyn M., Suchocki T., Drozd M., von Haehling S., Doehner W. , Banasiak W., Filippatos G., Anker S. D., Ponikowski P. Effects of intravenous iron therapy in iron-deficient patients with systolic heart failure: a meta-analysis of randomized controlled trials. Eur J Hearts Faii, 2016, vol. 18, no. 7, pp. 786-795. doi:10.1002/ejhf.473
, Banasiak W., Filippatos G., Anker S. D., Ponikowski P. Effects of intravenous iron therapy in iron-deficient patients with systolic heart failure: a meta-analysis of randomized controlled trials. Eur J Hearts Faii, 2016, vol. 18, no. 7, pp. 786-795. doi:10.1002/ejhf.473
39. Ponikowski P., Voors A. A., Anker S. D., Bueno H., Cleland J. G., Coats A. J., Falk V., Gonzalez-Juanatey J.R., Harjola V. P., Jankowska E. A., Jessup M., Linde C., Nihoyannopoulos P., Parissis J. T., Pieske B., Riley J. P., Rosano G. M., Ruilope L. M., Ruschitzka F., Rutten F. H., van der Meer P. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. RevEsp Cardiol (Engl Ed). 2016, vol. 69, no. 12, p. 1167. doi: 10.1016/j.rec.2016.11.005.
|
Эритроциты (RBC) |
Эритроциты выполняют важную функцию питания тканей организма кислородом, а также удаления из тканей углекислого газа, который затем выделяется через легкие. |
|
Гемоглобин (HGB, Hb) |
Гемоглобин – это особый белок, который содержится в эритроцитах и отвечает за перенос кислорода к органам. Снижение уровня гемоглобина (анемия) приводит к кислородному голоданию организма. Повышение уровня гемоглобина, как правило, говорит о высоком количестве эритроцитов, либо об обезвоживании организма. |
|
Гематокрит (HCT) |
Гематокрит — это показатель, который отражает, какой объем крови занимают эритроциты. Гематокрит, как правило, выражается в процентах: например, гематокрит (НСТ) 39% означает, что 39% объема крови представлено красными кровяными тельцами. |
|
Тромбоциты (PLT) |
Тромбоциты – это небольшие пластинки крови, которые участвуют в образовании тромба и препятствуют потере крови при повреждениях сосудов. Повышение уровня тромбоцитов в крови встречается при некоторых заболеваниях крови, а также после операций, после удаления селезенки. Снижение уровня тромбоцитов встречается при некоторых врожденных заболеваниях крови, апластической анемии (нарушение работы костного мозга, который вырабатывает кровяные клетки), идиопатической тромбоцитопенической пурпуре (разрушение тромбоцитов из-за повышенной активности иммунной системы), циррозе печени и др. |
|
Лейкоциты (WBC) |
Лейкоциты (белые кровяные тельца) защищают организм от инфекций (бактерий, вирусов, паразитов). |
|
Лимфоциты (LYM) |
Лимфоцит – это вид лейкоцита, который отвечает за выработку иммунитета и борьбу с микробами и вирусами. Увеличение числа лимфоцитов (лимфоцитоз) встречается при некоторых инфекционных заболеваниях (краснуха,грипп, токсоплазмоз, инфекционный мононуклеоз, вирусный гепатит и др.), а также при заболеваниях крови (хронический лимфолейкоз и др). Уменьшение числа лимфоцитов (лимфопения) встречается при тяжелых хронических заболеваниях, СПИДе, почечной недостаточности, приеме некоторых лекарств, подавляющих иммунитет (кортикостероиды и др.). |
|
Моноциты (MON) |
Моноциты – это лейкоциты, которые, попав в сосуды, вскоре выходят из них в окружающие ткани, где превращаются в макрофаги (макрофаги – это клетки, которые поглощают и переваривают бактерий и погибшие клетки организма). |
|
Скорость оседания эритроцитов, СОЭ |
Скорость оседания эритроцитов – это показатель, который косвенно отражает содержание белков в плазме крови. Повышенная СОЭ указывает на возможное воспаление в организме из-за увеличенного содержания воспалительных белков в крови. Кроме того, повышение СОЭ встречается при анемиях, злокачественных опухолях и др. Уменьшение СОЭ встречается нечасто и говорит о повышенном содержании эритроцитов в крови (эритроцитоз), либо о других заболеваниях крови. |
Чем опасен низкий и высокий гемоглобин для здоровья и какими продуктами его регулировать
О нем слышали даже те, кому еще рано задумываться о здоровье. За ним следят, его повышают, потому что знают: без него организму никак. Для чего же нужен гемоглобин, чем опасно его снижение, как быстро повысить его уровень в крови и что будет, если он окажется выше нормы? Мы собрали все самое важное об этом незаменимом белке в одну статью.
За ним следят, его повышают, потому что знают: без него организму никак. Для чего же нужен гемоглобин, чем опасно его снижение, как быстро повысить его уровень в крови и что будет, если он окажется выше нормы? Мы собрали все самое важное об этом незаменимом белке в одну статью.
Для чего нужен гемоглобин в крови и при чем тут железо
Гемоглобин – это особый сложный белок, который формируется в эритроцитах, когда туда попадают атомы железа. Именно гемоглобин окрашивает кровь в красный цвет. На него возложена важнейшая миссия: он переносит кислород из легких к органам и тканям. И наоборот: транспортирует углекислый газ обратно в легкие, чтобы вывести из организма. Этот важнейший белок участвует также в синтезе ДНК, поддержании кислотно-щелочного баланса, в организации правильного обмена веществ.
Вот почему низкий гемоглобин так опасен: он снижает эффективность работы всех внутренних органов и систем, жизнеспособность и эмоциональное состояние человека. И поэтому его нужно обязательно повышать до нормы.
И поэтому его нужно обязательно повышать до нормы.
Норма гемоглобина у мужчин, женщин и детей
Уровень гемоглобина в крови человека зависит от пола, возраста и различных физиологических особенностей организма. У мужчин гемоглобин в норме при значениях 135–160 г/л. Для женщин допускаются 120–140 г/л. У беременных уровень гемоглобина заметно снижается – до 110 г/л.
Нормы гемоглобина для детей существенно меняются в зависимости от возраста. Максимальный уровень белка у новорожденных в первый месяц жизни – от 140 до 200 г/л. Затем он довольно быстро снижается. В первые полгода нормой считается показатель от 90,5 до 140 г/л. У детей до 18 лет гемоглобин должен быть в пределах 110–150 г/л, а затем сравняться с нормами взрослых.
Как расшифровать единицы измерения гемоглобина в крови? Гемоглобин измеряется в граммах на литр (г/л) или граммах на децилитр, то есть 10 литров (г/дл). Чтобы перевести г/дл в г/л, достаточно умножить первый показатель на 10.
На уровень гемоглобина в крови влияют и врожденные особенности организма, и образ жизни человека: уровень физической активности, окружающая среда, тип питания, наличие вредных привычек.
Почему гемоглобин падает
Гемоглобин не может понизиться и тем более резко упасть без причин. Ими могут быть серьезные болезни или ситуации, вызвавшие потерю крови: операции, травмы, ранения, внутренние и внешние кровотечения. У женщин кратковременное снижение белка возможно на фоне менструации, которая длится 5 дней и более. Самые распространенные причины – недостаток железа, фолиевой кислоты и витамина В12. Однако низкий гемоглобин может быть и следствием серьезных патологий.
Причины низкого гемоглобина:
- сбой в работе эндокринной системы;
- заболевания ЖКТ, патологии кишечника;
- болезни почек;
- проблемы с кровеносной системой;
- пневмония, туберкулез, гепатит и другие серьезные болезни;
- гастрит и новообразования в органах пищеварения;
- онкологические заболевания;
- изнуряющие продолжительные диеты, неправильное питание;
- авитаминоз и недостаток витаминов и минералов;
- сильный стресс или затянувшаяся депрессия;
- многоплодная беременность.

Как видите, причины низкого гемоглобина могут быть крайне серьезными и опасными для здоровья, а потому контроль за этим показателем нужно вести регулярно, а при необходимости – быстро повышать.
Как узнать без анализов, низкий ли у вас гемоглобин: симптомы дефицита
Снижение гемоглобина многие привыкли игнорировать. Зачастую даже от врачей можно услышать фразу: «Я всю жизнь живу с низким гемоглобином, и ничего». Тем не менее это не значит, что не нужно искать причину снижения гемоглобина и устранять ее.
Низкий уровень гемоглобина в крови дает вполне конкретные симптомы, так что заметить их может даже непрофессионал. Вот несколько наиболее распространенных признаков его снижения.
Признаки низкого гемоглобина:
- постоянное ощущение усталости, сонливость, быстрая утомляемость;
- одышка при физических нагрузках и обычном подъеме по лестнице;
- регулярные головные боли;
- низкое артериальное давление;
- сухие и ломкие ногти;
- сухость и активное выпадание волос;
- нарушение работы ЖКТ;
- бледная сухая кожа, возможно шелушение;
- шум в ушах и головокружения;
- снижение аппетита или извращенные вкусовые пристрастия: желание есть мел, сырое тесто или мясо, ощущать запах краски или бензина;
- боль в мышцах, мерзнущие руки и ноги;
- регулярные нарушения менструального цикла у женщин;
- снижение потенции у мужчин;
- частые простуды и вирусные заболевания.

Эти симптомы, особенно если их несколько и наблюдаются они длительное время, говорят о том, что гемоглобин в крови снижен уже достаточно сильно. В тяжелых случаях человек может даже терять сознание. Это значит, что искать решение и принимать меры нужно быстро.
Когда нужно сдавать кровь на гемоглобин
Причиной обратиться к терапевту или гематологу и сдать анализ крови на уровень гемоглобина может стать обнаружение перечисленных выше симптомов – одного или нескольких, серьезное ухудшение состояния здоровья после болезни, значительная потеря крови из-за травмы или в ходе перенесенной операции, соблюдение строгой диеты, выявленное заболевание крови у близких родственников, беременность.
Небольшое понижение может быть незаметным для человека. Чтобы изменение уровня гемоглобина не стало сюрпризом, ситуацию лучше держать под контролем: сдавать кровь на анализ 1–2 раза в год, а при необходимости консультироваться у врача-гематолога.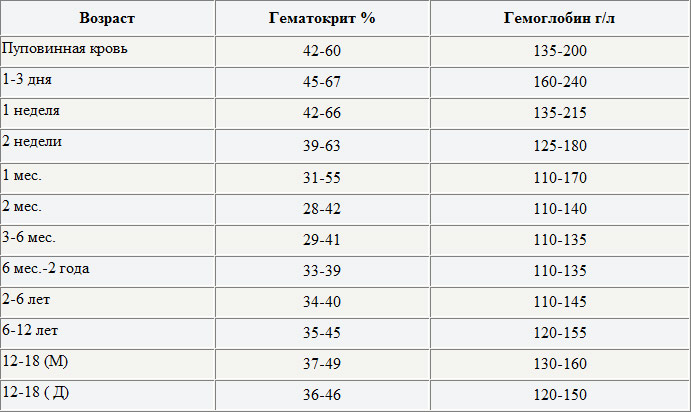
Что такое анемия и как ее диагностировать
Анемией (или малокровием) называют снижение гемоглобина и уменьшение количества эритроцитов в крови. Это состояние приводит к тому, что органы и ткани не получают нужного количества кислорода, ухудшаются обменные процессы и общее самочувствие человека. Первыми симптомами могут быть быстрая утомляемость, одышка, снижение аппетита, сухость кожи, ломкость волос и ногтей и другие признаки, которые не всегда сразу связывают в единую картину.
Вот почему самостоятельно диагностировать анемию крайне сложно, а делать это, опираясь лишь на лабораторные результаты анализов, нельзя. Для постановки диагноза врачи не только смотрят на уровень гемоглобина и железа, но и проверяют уровень холестерина, глюкозы, креатинина, мочевой кислоты и электролитов, оценивают общее состояние пациента и его внутренних органов, проводят комплексную диагностику.
Степени тяжести анемии:
- Легкая анемия: уровень гемоглобина в крови меньше нормы, но больше 100 г/л.
 Симптомы неявные, поэтому человек крайне редко обращается к специалистам на этой стадии заболевания.
Симптомы неявные, поэтому человек крайне редко обращается к специалистам на этой стадии заболевания. - Средняя анемия: уровень гемоглобина в крови – от 66 до 100 г/л. Появляются частые головокружения, тошнота, сонливость, становятся заметны сухость и трещинки на коже.
- Тяжелая анемия: уровень гемоглобина в крови – менее 66 г/л. Критическое состояние, помутнение и потеря сознания, холодные руки, обмороки. Требуется экстренная госпитализация, поскольку есть серьезная угроза жизни.
Однако проконсультироваться как минимум с терапевтом стоит уже при снижении показателя меньше 120 г/л у женщин и ниже 135 г/л у мужчин, не дожидаясь ухудшения состояния.
Чем опасна анемия для человека
Эту болезнь одновременно можно считать и опасной, и относительно безобидной. С одной стороны, в легкой форме анемия встречается достаточно часто и без проблем поддается лечению. С другой – долговременная нехватка железа и пониженный уровень гемоглобина дают серьезную нагрузку на организм.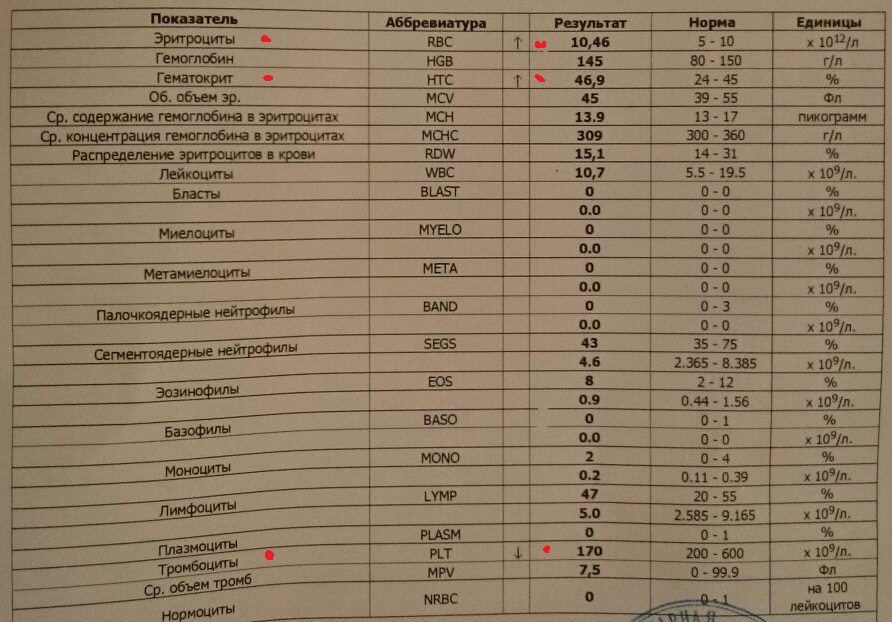 Тяжелая анемия может повлечь за собой серьезные последствия:
Тяжелая анемия может повлечь за собой серьезные последствия:
- сбои в работе почек, печени и других внутренних органов;
- заболевания сердечно-сосудистой системы;
- когнитивные нарушения;
- повышение риска падений и, как следствие, травм и переломов;
- кислородное голодание (гипоксия), риск инфаркта миокарда и инсульта;
- обострение хронических болезней;
- ухудшение работы репродуктивной системы;
- анемическая кома или смерть.
Однако паниковать не стоит. Патологии и осложнения, как правило, развиваются, если гемоглобин сильно понижен в течение нескольких лет. Регулярный контроль и проверка анализов 1–2 раза в год станут достаточной профилактикой и помогут быстро выявить проблему и начать лечение.
Беременным женщинам и маленьким детям важно следить за уровнем гемоглобина в крови и не допускать его снижения. Иначе есть риск осложнения беременности, преждевременных родов и нарушения развития плода – сбой в работе мозга, нервной и дыхательной систем.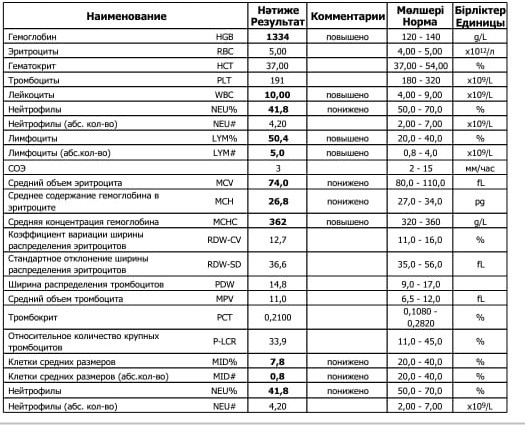 У детей младшего возраста недостаток гемоглобина может спровоцировать задержку интеллектуального развития.
У детей младшего возраста недостаток гемоглобина может спровоцировать задержку интеллектуального развития.
При каком гемоглобине человек умирает
Критически низким уровнем гемоглобина считается 65 г/л. При таких показателях человека нужно экстренно госпитализировать и принимать все возможные меры для его спасения.
Как повысить гемоглобин
Быстро повысить уровень гемоглобина достаточно сложно. Этот процесс занимает обычно около месяца. Не стоит полагать, что самостоятельно назначенные витамины или усиленное питание мясом сотворят чудеса.
Самое главное в процессе нормализации гемоглобина – не закидывать в организм железо, а искать причины недомогания. Важно своевременно и правильно диагностировать заболевание, которое вызывает снижение гемоглобина, и работать в первую очередь с ним. При сильных кровопотерях или болезнях крови пациенту делают переливание крови или отдельных ее компонентов. Это помогает восполнить ее объем.
И уже в комплексе с профессиональным лечением прием железосодержащих препаратов и корректировка рациона питания дадут хороший эффект, помогут избежать осложнений и улучшить состояние пациента.
Важно: прежде чем начинать лечение, необходимо пройти медицинское обследование, сделать анализ крови и получить консультации всех профильных врачей, в зависимости от диагноза. Самолечение недопустимо. Все процедуры и назначения должны быть согласованы с врачом и регулярно им контролироваться.
А в качестве профилактики недостатка железа и снижения гемоглобина рекомендуется скорректировать свой рацион питания, включить в него железосодержащие продукты. Ориентировочные нормы потребления железа в сутки – 10–12 мг для мужчин и 20–30 мг для женщин. Более точные цифры зависят от состояния человека.
В каких продуктах много железа для поднятия гемоглобина
-
Сушеные грибы. Продукт, способный заметно повысить уровень железа в организме.
 Всего 50 г сушеных грибов в сутки помогут восполнить норму содержания железа в крови. Есть их каждый день могут не все, но периодически включать в свой рацион грибы очень полезно.
Всего 50 г сушеных грибов в сутки помогут восполнить норму содержания железа в крови. Есть их каждый день могут не все, но периодически включать в свой рацион грибы очень полезно.
-
Красное мясо. Темный цвет продукта как раз указывает на большое содержание железа. Например, в паровой котлете из говядины весом 100 г содержится примерно 2,7 мг железа – почти 15% суточной нормы. Для сравнения: в такой же котлете из мяса индейки количество железа – около 0,7 мг.
-
Семечки тыквы. Отличный источник железа: 200 г продукта спокойно покрывают суточную норму. Но увлекаться семечками тыквы не стоит: они очень калорийны и могут вызвать сбои в работе ЖКТ. А вот небольшая горстка семечек в салате или горячем блюде будет очень полезна.
-
Субпродукты. По содержанию железа и других полезных микроэлементов субпродукты легко обойдут мясо. В 100 г приготовленной говяжьей печени содержится 36% суточной нормы железа.

-
Гречка и геркулес. Еще пара важных продуктов, способных повысить уровень железа. Порция гречки или геркулеса весом 100 г обеспечит организм полезным элементом примерно на 25%.
-
Бобовые. Важнейшая часть рациона для вегетарианцев и веганов: бобовые не только богаты железом, но еще и очень сытные. Чашка вареной чечевицы, к примеру, покроет примерно 35% суточной нормы железа, а стакан вареной фасоли – 20%.
-
Темный шоколад. Пожалуй, любимый продукт у тех, кто стремится поднять уровень гемоглобина. Главное – выбирать шоколад с содержанием какао не менее 70% и съедать не менее ¼ плитки (25 г) в сутки. Это поможет скомпенсировать около 17% суточной нормы железа и подарит хорошее настроение за счет «гормона счастья».
При недостатке железа и низком гемоглобине также рекомендуются следующие продукты: яйца (особенно желток), киноа, миндаль, грецкие орехи, яблоки с кожурой, гранат, виноград, малина, шиповник, свекла, свежевыжатые фруктовые и овощные соки, морепродукты – икра, рыба, устрицы. Важно, чтобы рацион питания был сбалансирован, продукты содержали разнообразные полезные вещества и витамины.
Важно, чтобы рацион питания был сбалансирован, продукты содержали разнообразные полезные вещества и витамины.
Как сделать так, чтобы железо лучше усваивалось
Чтобы повысить гемоглобин, недостаточно просто включить в рацион железосодержащие продукты. Важно, чтобы полезные вещества максимально усваивались и шли на пользу. Для этого стоит знать, какие продукты можно и нельзя сочетать друг с другом.
Железо лучше всего усваивается в присутствии витаминов С и А. Вот почему морепродукты с лимоном не только вкусные, но и невероятно полезные. Несколько капель лимона можно добавить в салаты и другие блюда. Богаты витамином С почти все свежие овощи и фрукты, например болгарский перец. Витамин А содержится в рыбе, масле, овощах и фруктах оранжевого цвета.
При этом важно обеспечить поступление в организм фолиевой кислоты, которая принимает участие в синтезе эритроцитов. Поэтому нужно регулярно есть говядину, зеленый салат, авокадо, бобовые, рис, арахис и другие продукты с высоким содержанием фолиевой кислоты.
А вот кальций и казеин (молочный белок) снижают всасываемость железа, поэтому вместе с овощными и мясными блюдами не стоит употреблять молочные и кисломолочные продукты, сыры. Негативно влияет на усвояемость железа пшеница и другие злаки. Так что мясо лучше есть без хлеба, а на гарнир использовать не макароны, а овощи. Среди продуктов, которые могут спровоцировать дефицит гемоглобина: чай, кофе и хурма (содержат танины), хлеб, соя, консервы, газировка, плавленые виды сыра. Поэтому злоупотреблять ими не стоит.
Может ли быть слишком много железа в организме
Может. Переизбыток железа для организма так же вреден, как и его недостаток. Он вызывает фиброз органов и тканей. Чаще всего страдают поджелудочная железа, печень и сердце. Однако добиться переизбытка железа только питанием невозможно. За патологией часто стоят генетическая предрасположенность и неправильное или бесконтрольное применение железосодержащих препаратов.
Как называется повышение гемоглобина
Увеличение количества эритроцитов и повышение гемоглобина называется эритроцитозом. Его характерные симптомы: носовое кровотечение, головные боли и головокружение, быстрая утомляемость. Эритроцитоз, в свою очередь, может являться признаком различных заболеваний, определить которые сумеет только врач.
Его характерные симптомы: носовое кровотечение, головные боли и головокружение, быстрая утомляемость. Эритроцитоз, в свою очередь, может являться признаком различных заболеваний, определить которые сумеет только врач.
Что означает, если гемоглобин повышен
Высокий уровень гемоглобина может быть вызван обезвоживанием, курением, раком легких, болезнями сердца и другими патологиями. Повышенный гемоглобин иногда свидетельствует о наличии редкого заболевания – полицитемии. В таком случае организм вырабатывает слишком много эритроцитов, что может привести к образованию тромбов, сердечным приступам и инсультам. Это очень серьезная болезнь, которую важно своевременно выявить и контролировать на протяжение всей жизни.
Как поддерживать нормальный уровень гемоглобина
Для здорового человека без врожденных патологий важно следить за режимом дня, пить достаточное количество воды, сбалансированно питаться, включать в рацион продукты, богатые железом и витаминами, вести активный образ жизни и периодически сдавать общий и биохимический анализы крови.
Эти советы могут показаться вам очевидными и даже банальными, однако они помогут предотвратить снижение гемоглобина, развитие анемии и других заболеваний, улучшить ваше самочувствие и качество жизни.
В этом материале обобщены лучшие исследования доказательной медицины разных лет. Тем не менее он является ознакомительным, не предназначен для назначения лечения и не может быть использован в качестве прямого руководства к действию.
Анемия у детей: что нужно знать
Анемия — распространенное заболевание у детей, от которого страдают около 20% детей в США. Анемия возникает, когда у ребенка недостаточно эритроцитов или гемоглобина (тип белка, который позволяет клетки крови, чтобы переносить кислород к клеткам по всему телу).
Большинство видов анемии поддаются лечению. Симптомы исчезнут через некоторое время, поэтому ребенку следует расслабиться во время выздоровления.
Распространенные причины анемии у детей
У вашего ребенка может быть анемия, если его организм:
Не производит достаточно красных кровяных телец. Это может случиться, если в их обычном рационе не хватает железа или других питательных веществ.
Это может случиться, если в их обычном рационе не хватает железа или других питательных веществ.
Разрушает слишком много красных кровяных телец. Когда ребенок унаследовал заболевание красных кровяных телец, такое как серповидно-клеточная анемия (когда белок, называемый гемоглобином, внутри красных кровяных телец, образует цепочки, которые слипаются вместе и заставляют эритроцит принимать форму полумесяца или буквы C — называется серповидноклеткой) или заболевание, это может произойти.
Теряет эритроциты из-за кровотечения. Это может проявляться в виде длительной кровопотери низкой степени тяжести, иногда с калом. Это также может произойти при значительной кровопотере, например при обильном менструальном кровотечении.
Типы анемии у детей
Существует несколько различных типов анемии:
- Железодефицитная анемия. Когда в крови недостаточно железа.
- Мегалобластная анемия.
 Это происходит, когда красные кровяные тельца становятся слишком большими из-за недостатка фолиевой кислоты или витамина B-12.
Это происходит, когда красные кровяные тельца становятся слишком большими из-за недостатка фолиевой кислоты или витамина B-12. - Гемолитическая анемия. Когда красные кровяные тельца разрушаются, как правило, в результате серьезной инфекции или приема некоторых лекарств.
- Серповидно-клеточная анемия. Унаследованный тип анемии, при котором у ребенка появляются эритроциты неправильной формы.
- Анемия Кули (талассемия). Другая наследственная форма анемии с аномальными эритроцитами.
- Апластическая анемия. Когда костный мозг ребенка не может производить клетки крови.
Какие дети подвержены риску анемии?
Некоторые факторы риска анемии у детей включают:
- Преждевременные роды или низкий вес при рождении
- Жизнь в бедности или неспособность позволить себе продукты, богатые железом
- Употребление коровьего молока в раннем возрасте (у малышей может развиться железодефицитная анемия, если они пьют слишком много коровьего молока)
- Диета с низким содержанием железа, витаминов и минералов
- Операция или несчастный случай с кровопотерей
- Инфекции
- Заболевание почек или печени
- Семейный анамнез наследственной анемии, чаще всего серповидноклеточной анемии
Симптомы анемии у детей
К наиболее частым симптомам анемии у детей относятся:
- Учащение пульса
- Проблемы с задержкой дыхания или одышка
- Отсутствие энергии, легкая усталость
- Головокружение при стоянии
- Головная боль
- Раздражительность
- Боль, опухший язык
- Пожелтение глаз, кожи и рта 90 027 Увеличенная селезенка или увеличенная печень
- Задержка роста и развития
- Плохое заживление ран и тканей
Анемия часто является симптомом другого заболевания.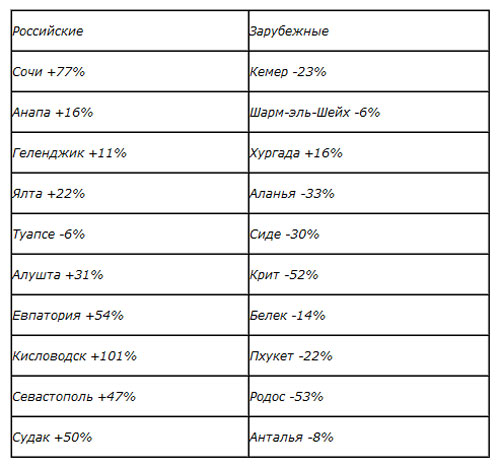 Если вы подозреваете, что у вашего ребенка анемия, немедленно запишитесь на прием к врачу.
Если вы подозреваете, что у вашего ребенка анемия, немедленно запишитесь на прием к врачу.
Диагностика анемии у детей
Ваш врач может помочь диагностировать анемию, выполнив скрининг и несколько анализов крови. Они будут часто:
- Задавать вопросы о симптомах вашего ребенка
- Спрашивать о диете вашего ребенка
- Спросите, есть ли у кого-либо из членов семьи анемия
- Пройдите медицинский осмотр вашего ребенка
Ваш врач может также провести анализы крови и осмотреть на эритроциты под телескопом, чтобы проверить их форму и размер, проверить количество гемоглобина и железа в крови, а также проверить возможные анемии.
Для завершения этих тестов ваш врач вставит иглу в кожу вашего ребенка, чтобы удалить кровь. В зависимости от результатов анализа крови ваш врач может также провести анализы костного мозга вашего ребенка.
Костный мозг — это губчатая часть кости, в которой образуются клетки крови. Врач вводит иглу в кость и берет небольшой образец для исследования в лаборатории.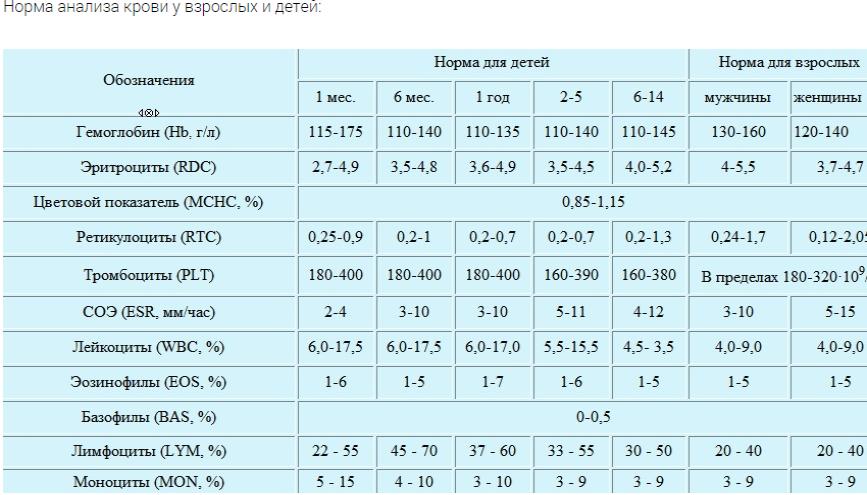
После того, как ваш врач лучше поймет, что вызывает у вашего ребенка анемию, он может помочь составить план лечения.
Лечение анемии у детей
Лечение будет зависеть от симптомов, возраста, состояния здоровья и тяжести анемии вашего ребенка.
Некоторые виды анемии не требуют лечения. Однако при других типах анемии могут потребоваться лекарства, переливание крови, хирургическое вмешательство или пересадка стволовых клеток. В некоторых случаях лечащий врач вашего ребенка может направить вас к гематологу. Это специалист по лечению заболеваний крови.
Наиболее распространенные варианты лечения анемии у детей включают:
- Витаминные и минеральные капли или таблетки
- Добавки железа
- Изменение рациона вашего ребенка
- Прекращение приема лекарства, вызывающего анемию
- Лекарство
- Операция по удалению селезенка
- Переливание крови
- Трансплантация стволовых клеток
Профилактика анемии у детей
Если анемия вашего ребенка связана с дефицитом железа или недостаточностью питания, вы можете помочь предотвратить ее, убедившись, что ваш ребенок придерживается сбалансированной диеты .
Не давайте ребенку коровье молоко. Подождите, пока вашему ребенку исполнится 12 месяцев, прежде чем давать ему коровье молоко. Употребление коровьего молока до того, как ваш ребенок будет готов, может снизить количество железа, всасываемого в его кишечнике, и может вызвать потерю крови с калом.
Если вы кормите грудью, ваш ребенок будет получать достаточное количество железа до 4-месячного возраста. В возрасте 4 месяцев младенцам, находящимся на грудном вскармливании, следует давать добавки железа до тех пор, пока они не начнут есть достаточно продуктов, богатых железом.
Если вы кормите детское питание, используйте детское питание, обогащенное железом.
Накормите ребенка диетой, богатой железом . Молоко вызывает у детей чувство сытости и содержит мало железа, что может снизить вероятность того, что они будут есть другие продукты, богатые железом. Хорошие источники железа — это бобы, яичные желтки, патока, картофель, помидоры, изюм и красное мясо.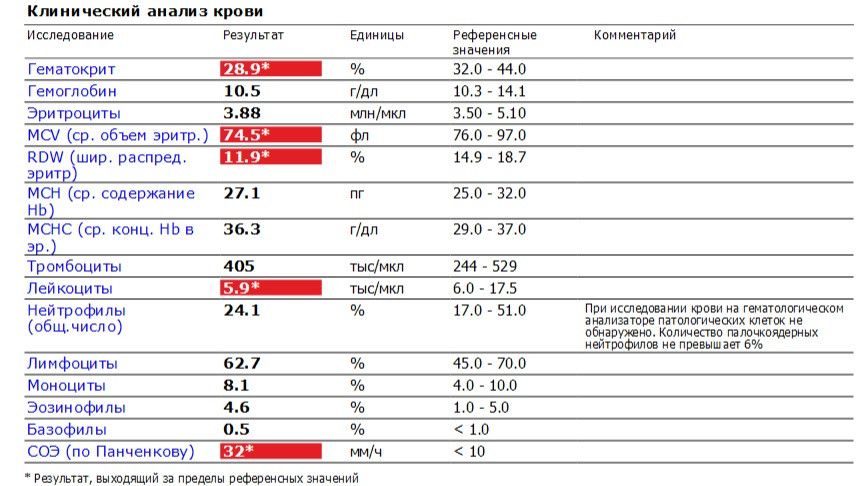
Если у вашего ребенка наследственное заболевание эритроцитов, детский гематолог поможет вам справиться с его симптомами и окажет ребенку поддерживающую терапию.
Анемия у детей и подростков: часто задаваемые вопросы для родителей
Анемия — это состояние, при котором количество красных кровяных телец в организме снижается ниже нормы для возраста вашего ребенка. Из-за этого ваш ребенок может казаться бледным, чувствовать себя капризным, усталым или слабым. Хотя эти симптомы могут вас беспокоить, наиболее частые причины анемии, такие как дефицит железа, обычно легко поддаются лечению, особенно если они обнаруживаются на ранней стадии. Кроме того, родители должны знать, что нужно делать для предотвращения этого состояния.
Поскольку быстрый рост является потенциальной причиной этого состояния, первый год жизни и подростковый возраст — это две возрастные группы, в которых младенцы и дети особенно предрасположены к анемии.
Что такое анемия?
Анемия означает, что в организме недостаточно эритроцитов.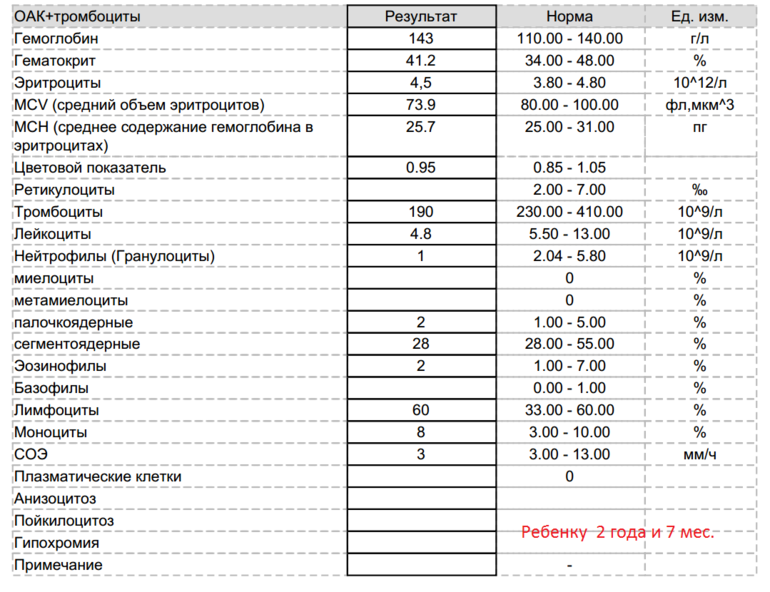 Красные кровяные тельца заполнены гемоглобином, особым пигментированным белком, который позволяет переносить кислород другим клеткам тела. Клеткам в мышцах и органах вашего ребенка для выживания необходим кислород, а уменьшение количества красных кровяных телец может вызвать нагрузку на организм.
Красные кровяные тельца заполнены гемоглобином, особым пигментированным белком, который позволяет переносить кислород другим клеткам тела. Клеткам в мышцах и органах вашего ребенка для выживания необходим кислород, а уменьшение количества красных кровяных телец может вызвать нагрузку на организм.
Ваш ребенок может заболеть анемией, если его или ее тело:
Не производит достаточно красных кровяных телец. Это может произойти, если в ее рационе недостаточно железа или других питательных веществ (например, железодефицитная анемия).
Разрушает слишком много красных кровяных телец. Этот тип анемии обычно возникает, когда ребенок страдает основным заболеванием или унаследовал заболевание эритроцитов (например, серповидноклеточная анемия).
Теряет эритроциты из-за кровотечения. Это может быть очевидная кровопотеря, такая как обильное менструальное кровотечение, или длительная медленная кровопотеря, возможно, со стулом.

Каковы общие признаки и симптомы анемии?
- Бледная или землистая (желтая) кожа
- Бледные щеки и губы
- Подкладка век и ногтевого ложа может выглядеть менее розовой, чем обычно
- Раздражительность
- Легкая слабость
- Легкая утомляемость, частый сон
- У детей с деструкцией эритроцитов может появиться желтуха (пожелтение кожи или глаз) и моча цвета темного чая или колы
У детей с тяжелой анемией могут быть дополнительные признаки и симптомы:
- Одышка
- Учащенное сердцебиение
- Отек рук и ног
- Головные боли
- Головокружение и обмороки
- Синдром беспокойных ног
Когда дети едят непродовольственные товары:
Дети с анемией, вызванной очень низким уровнем железа, содержащегося в их крови, могут также есть странные непищевые продукты, такие как лед, грязь, глина, бумагу, картон и т. д. крахмал.Такое поведение называется « pica » (произносится как пирог). Пика часто возникает у детей с низким содержанием железа и может вызвать запор. У этих детей пика обычно прекращается после лечения анемии препаратами железа.
д. крахмал.Такое поведение называется « pica » (произносится как пирог). Пика часто возникает у детей с низким содержанием железа и может вызвать запор. У этих детей пика обычно прекращается после лечения анемии препаратами железа.
Если у вашего ребенка проявляются какие-либо из этих признаков или симптомов, обратитесь к педиатру.
Даже низкий уровень анемии может повлиять на энергию, концентрацию внимания и способность вашего ребенка учиться. Хроническая железодефицитная анемия может привести к долгосрочным необратимым нарушениям развития.В большинстве случаев анемию можно диагностировать с помощью простого анализа крови.
Как я могу предотвратить развитие анемии у моего ребенка?
Железодефицитную анемию и другие алиментарные анемии можно предотвратить, обеспечив ребенку сбалансированную диету. Поговорите со своим врачом о любых конкретных диетических ограничениях в вашей семье, когда ваш ребенок может потребоваться пищевая добавка для предотвращения анемии.
Вот способы предотвращения пищевой анемии:
|
Как я могу справиться с анемией, если у моего ребенка наследственное нарушение эритроцитов?
Ваш педиатр, скорее всего, направит вас к
детский гематолог, который предоставит вам поддерживающую помощь и проинформирует о конкретном состоянии вашего ребенка.
Помните:
Если у вашего ребенка появляются какие-либо признаки или симптомы анемии, обязательно сообщите об этом своему педиатру.Также узнайте, не болел ли кто-нибудь в вашей семье анемией или проблемами с легким кровотечением. При правильном лечении анемия вашего ребенка должна быстро исчезнуть.
Дополнительная информация:
Информация, содержащаяся на этом веб-сайте, не должна использоваться вместо медицинской помощи и рекомендаций вашего педиатра. Ваш педиатр может порекомендовать различные варианты лечения в зависимости от индивидуальных фактов и обстоятельств.
Недостаток железа у детей: советы по профилактике для родителей
Дефицит железа у детей: советы по профилактике для родителей
Дефицит железа у детей может повлиять на развитие и привести к анемии. Узнайте, сколько железа нужно вашему ребенку, лучшие источники железа и многое другое.
Персонал клиники Мэйо Железо — это питательное вещество, необходимое для роста и развития вашего ребенка, но некоторым детям его не хватает. Узнайте, что вызывает дефицит железа у детей, как распознать его и как предотвратить.
Узнайте, что вызывает дефицит железа у детей, как распознать его и как предотвратить.
Почему железо важно для детей?
Железо помогает перемещать кислород из легких к остальным частям тела и помогает мышцам накапливать и использовать кислород. Если в рационе вашего ребенка не хватает железа, у него может развиться состояние, называемое дефицитом железа.
Дефицит железа у детей — распространенная проблема. Это может произойти на многих уровнях, от легкого дефицита до железодефицитной анемии — состояния, при котором в крови не хватает здоровых эритроцитов.Нелеченный дефицит железа может повлиять на рост и развитие ребенка.
Сколько железа нужно детям?
Младенцы рождаются с железом, запасенным в их телах, но для быстрого роста и развития ребенка требуется постоянное дополнительное количество железа. Вот справочник по потребностям в железе в разном возрасте:
Кто подвержен риску дефицита железа?
Младенцы и дети с самым высоким риском дефицита железа включают:
- Недоношенные дети или дети с низкой массой тела при рождении
- Младенцы, употребляющие коровье или козье молоко в возрасте до 1 года
- Младенцы на грудном вскармливании, которым после 6 месяцев не дают прикорма, содержащего железо
- Младенцы, которые пьют смесь, не обогащенную железом
- Дети в возрасте от 1 до 5 лет, выпивающие более 24 унций (710 миллилитров) коровьего, козьего или соевого молока в день
- Дети с определенными заболеваниями, такими как хронические инфекции или ограниченное питание
- Дети, подвергшиеся воздействию свинца
- Дети, которые не едят достаточно продуктов, богатых железом
- Дети с избыточным весом или ожирением
Девочки-подростки также подвергаются более высокому риску дефицита железа, поскольку их организм теряет железо во время менструации.
Каковы признаки и симптомы дефицита железа у детей?
Слишком мало железа может ухудшить способность вашего ребенка нормально функционировать. Однако большинство признаков и симптомов дефицита железа у детей не проявляются до тех пор, пока не разовьется железодефицитная анемия. Если у вашего ребенка есть факторы риска дефицита железа, поговорите с его врачом.
Признаки и симптомы железодефицитной анемии могут включать:
- Бледная кожа
- Усталость
- Холодные руки и ноги
- Замедленный рост и развитие
- Плохой аппетит
- Аномально учащенное дыхание
- Поведенческие проблемы
- Частые инфекции
- Необычная тяга к непитательным веществам, таким как лед, грязь, краска или крахмал
Как можно предотвратить дефицит железа у детей?
Если вы кормите ребенка смесью, обогащенной железом, он, вероятно, получает рекомендованное количество железа.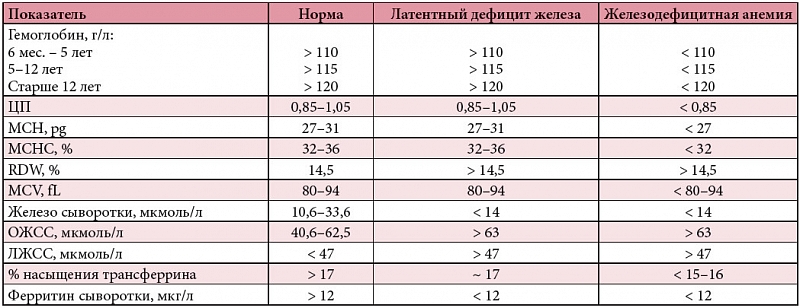 Если вы кормите ребенка грудью, поговорите с врачом о добавках железа. Добавкой железа могут быть капли железа, вводимые в определенной дозе, или железо, входящее в состав витаминных добавок.
Если вы кормите ребенка грудью, поговорите с врачом о добавках железа. Добавкой железа могут быть капли железа, вводимые в определенной дозе, или железо, входящее в состав витаминных добавок.
Вот несколько общих рекомендаций:
- Доношенные дети. Начните давать ребенку железо в возрасте 4 месяцев. Продолжайте давать ребенку добавку, пока он или она не будет есть две или более порции в день продуктов, богатых железом, таких как обогащенные железом хлопья или мясное пюре.Если вы кормите ребенка грудью и даете ребенку смесь, обогащенную железом, и большая часть грудного ребенка кормит ее смесью, прекратите давать ребенку эту добавку.
- Недоношенные. Начните давать ребенку железо в возрасте 2 недель. Продолжайте давать ребенку добавку до 1 года. Если вы кормите ребенка грудью и даете ребенку обогащенную смесь, а большая часть грудного вскармливания является смесью, прекратите давать ребенку добавку.
Другие меры, которые вы можете предпринять для предотвращения дефицита железа, включают:
- Подавайте продукты, богатые железом.
 Когда вы начинаете давать ребенку твердую пищу — обычно в возрасте от 4 до 6 месяцев — давайте продукты с добавлением железа, такие как обогащенные железом детские каши, мясное пюре и протертые бобы. Для детей старшего возраста хорошими источниками железа являются красное мясо, курица, рыба, бобы и шпинат.
Когда вы начинаете давать ребенку твердую пищу — обычно в возрасте от 4 до 6 месяцев — давайте продукты с добавлением железа, такие как обогащенные железом детские каши, мясное пюре и протертые бобы. Для детей старшего возраста хорошими источниками железа являются красное мясо, курица, рыба, бобы и шпинат. - Не переусердствуйте с молоком. В возрасте от 1 до 5 лет не позволяйте ребенку выпивать более 24 унций (710 миллилитров) молока в день.
- Повышение абсорбции. Витамин C способствует усвоению пищевого железа.Вы можете помочь своему ребенку усваивать железо, предлагая продукты, богатые витамином С, такие как цитрусовые, дыня, клубника, болгарский перец, помидоры и темно-зеленые овощи.
Следует ли мне проверять ребенка на дефицит железа?
Железодефицитная анемия и железодефицитная анемия обычно диагностируются с помощью анализов крови. Американская академия педиатрии рекомендует проверять всех младенцев на железодефицитную анемию в возрасте от 9 до 12 месяцев, а тем, у кого есть факторы риска дефицита железа, — снова в более старшем возрасте.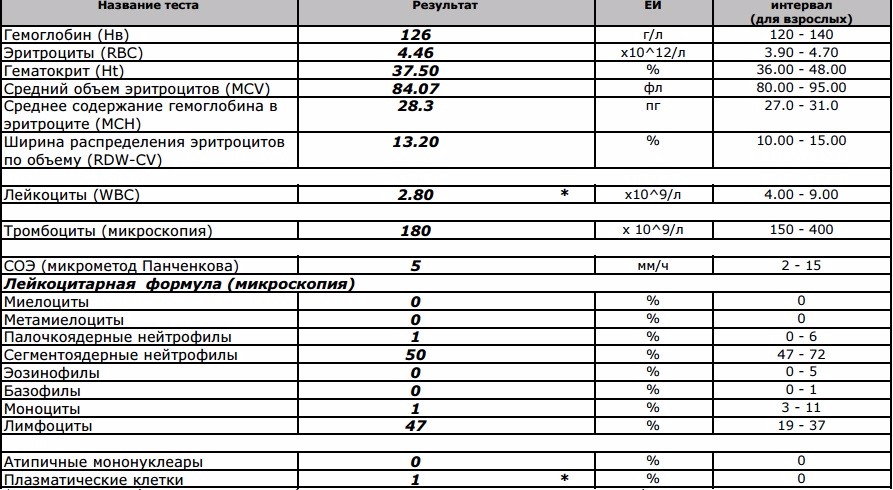 В зависимости от результатов скрининга врач вашего ребенка может порекомендовать пероральный прием добавок железа, ежедневный прием поливитаминов или дальнейшее тестирование.
В зависимости от результатов скрининга врач вашего ребенка может порекомендовать пероральный прием добавок железа, ежедневный прием поливитаминов или дальнейшее тестирование.
Дефицит железа у детей можно предотвратить. Чтобы поддерживать рост и развитие вашего ребенка, предлагайте продукты, богатые железом, во время еды и перекусов и поговорите с врачом вашего ребенка о необходимости обследований и добавок железа.
Получите самую свежую информацию о здоровье от экспертов Mayo Clinic.
Зарегистрируйтесь бесплатно и будьте в курсе достижений в области исследований, советов по здоровью и актуальных тем, касающихся здоровья, таких как COVID-19, а также опыта в области управления здоровьем.
Узнайте больше об использовании данных Mayo Clinic.
Чтобы предоставить вам наиболее актуальную и полезную информацию и понять, какие информация полезна, мы можем объединить вашу электронную почту и информацию об использовании веб-сайта с другая имеющаяся у нас информация о вас.Если вы пациент клиники Мэйо, это может включать защищенную медицинскую информацию. Если мы объединим эту информацию с вашими защищенными информация о здоровье, мы будем рассматривать всю эту информацию как защищенную информацию и будет использовать или раскрывать эту информацию только в соответствии с нашим уведомлением о политика конфиденциальности. Вы можете отказаться от рассылки по электронной почте в любое время, нажав на ссылку для отказа от подписки в электронном письме.
Подписаться!
Спасибо за подписку
Наш электронный информационный бюллетень Housecall будет держать вас в курсе самой последней информации о здоровье.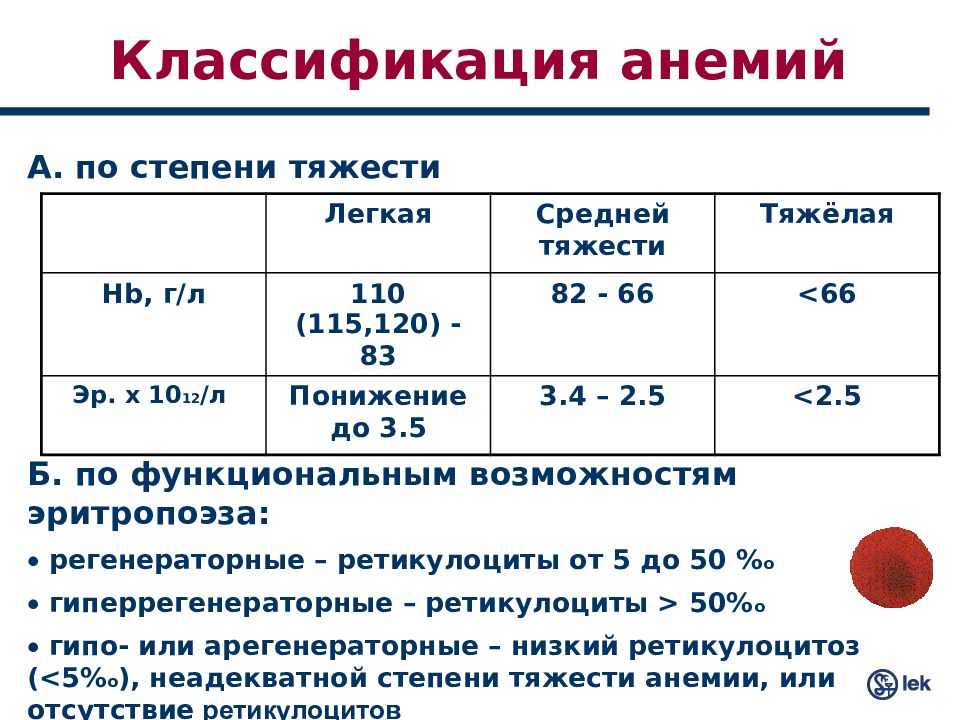
Извините, что-то пошло не так с вашей подпиской
Повторите попытку через пару минут
Повторить
Декабрь07, 2021 Показать ссылки- Пауэрс Дж. М. и др. Дефицит железа у младенцев и детей младше 12 лет: скрининг, профилактика, клинические проявления и диагностика. https://www.uptodate.com/contents/search. По состоянию на 14 октября 2019 г.
- Утюг. Национальные институты здоровья. https://ods.od.nih.gov/factsheets/Iron-HealthProfessional/. По состоянию на 14 октября 2019 г.
- Что такое железодефицитная анемия? Национальный институт сердца, легких и крови. https://www.nhlbi.nih.gov/health-topics/iron-deficiency-anemia.
 По состоянию на 14 октября 2019 г.
По состоянию на 14 октября 2019 г. - Каушанский К. и др., Ред. Дефицит железа и перегрузки. В: Гематология Вильямса. 9 изд. McGraw-Hill Education; 2016. https://accessmedicine.mhmedical.com. По состоянию на 14 октября 2019 г.
- Hay WW, et al., Eds. Амбулаторная и офисная педиатрия. В: Современная диагностика и лечение: педиатрия. 24-е изд. McGraw-Hill Education; 2018. https://accessmedicine.mhmedical.com. По состоянию на 14 октября 2019 г.
- Hoecker JL (экспертное заключение). Клиника Майо.21 октября 2019 г.
.
Железодефицитная анемия | Детская больница CS Mott
Всем нам нужно железо, чтобы сохранять силы! Железо является важной частью гемоглобина, части красных кровяных телец, которые переносят кислород от легких к остальному телу. Ребенок, который не получает достаточно железа, может иметь проблемы с обучением или поведением, поскольку железо важно для энергии, работы мышц и развития мозга.
Сколько железа нужно ребенку?
Количество железа, необходимое ребенку, зависит от его возраста:
ВОЗРАСТ | MILLIGRAMS IRON / ДЕНЬ |
7-12 месяцев | 11 миллиграммов (следует принимать обогащенные железом хлопья и / или формулу |
1-3 года | 7 миллиграммов |
4-8 лет | 10 миллиграммов |
9-13 лет | 8 миллиграммов |
Мальчики подросткового возраста | 11 миллиграммов |
Девочки-подростки | 15 миллиграммов |
Что такое железодефицитная анемия?
Анемия — это уменьшение количества эритроцитов ниже нормы для определенного возраста.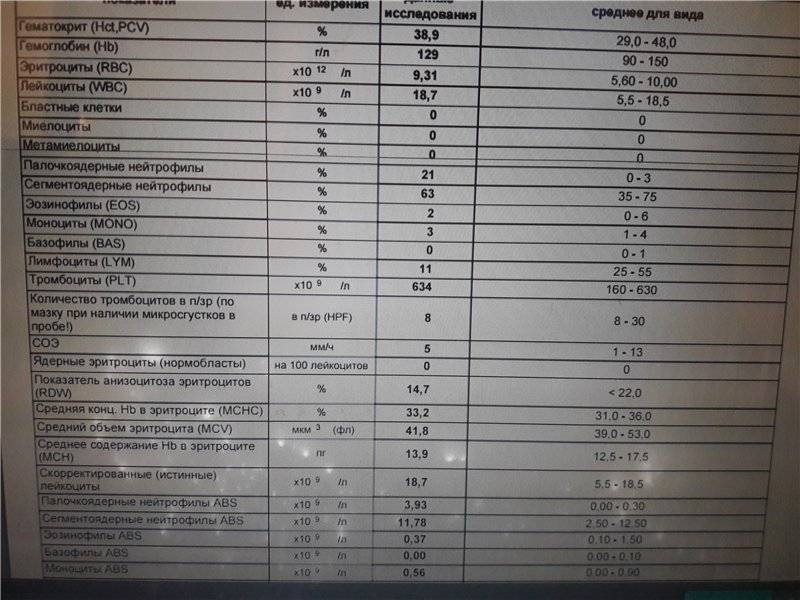
Когда организм не получает достаточно железа, он не может производить гемоглобин. Без достаточного количества гемоглобина будет меньше красных кровяных телец, поэтому меньше кислорода достигает клеток и тканей, составляющих наше тело.
Причины железодефицитной анемии
В развитых странах, таких как США, здоровые дети обычно получают достаточное количество железа в своем рационе через грудное молоко или смесь, обогащенную железом. Когда они начинают есть другие продукты для прикорма, они могут не получать достаточно железа, в зависимости от того, какую пищу они едят.
Коровье молоко затрудняет усвоение железа организмом. У малышей может развиться железодефицитная анемия, если они пьют слишком много коровьего молока (более 24 унций в день) и не едят достаточно продуктов, богатых железом, таких как зеленые листовые овощи и красное мясо.
Дети постарше, которые разборчивы в еде, также могут не получать достаточно железа, особенно те, кто придерживается вегетарианской диеты.
Железодефицитная анемия чаще встречается у девочек-подростков, чем у мальчиков-подростков, потому что их тела не способны накапливать столько железа, помимо потери крови во время менструации.
У мальчиков-подростков быстрый рост, связанный с половым созреванием, может привести к дефициту железа.
Симптомы анемии у детей
Если не устранить дефицит железа, со временем у ребенка с дефицитом железа появятся симптомы анемии. Если ребенок не получает достаточно железа, количество железа в организме будет уменьшаться, в первую очередь влияя на работу мышц и мозга, поскольку организм использует все доступное железо для производства гемоглобина. Когда уровень железа продолжает снижаться, в организме вырабатывается меньше красных кровяных телец, что в конечном итоге приводит к анемии.
Некоторые общие симптомы, связанные с железодефицитной анемией, включают:
- Слабость и чувство усталости
- Бледная кожа, особенно вокруг рук, ногтей и век
- Учащенное сердцебиение или шум в сердце
- Учащенное дыхание
- Раздражительность
- Плохой аппетит
- Дурнота или головокружение
В редких случаях, когда дефицит железа очень серьезен, у ребенка может развиться пика, то есть тяга к еде, не являющейся едой, например, грязь, крошки краски, мел и лед.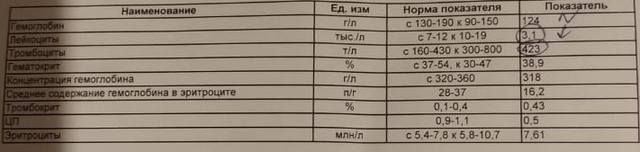
Как диагностируется железодефицитная анемия?
Американская академия педиатрии рекомендует всем младенцам сдавать анализ крови в течение первого года жизни для проверки на анемию, обычно это происходит в возрасте около одного года.
Некоторым младенцам это делают раньше, чем другим, в зависимости от факторов риска анемии, например, недоношенные младенцы или младенцы с очень низкой массой тела при рождении.
У детей старшего возраста врач может проверить анализ крови в зависимости от симптомов, которые испытывает ребенок.Они также могут проверить образец стула, чтобы убедиться, что ребенок не теряет кровь через желудочно-кишечный тракт.
Общие анализы крови, которые используются для проверки на железодефицитную анемию, — это гемоглобин, гематокрит или уровни железа
Как диагностируется железодефицитная анемия?
Если у ребенка обнаруживается железодефицитная анемия, ему обычно требуется ежедневный прием добавок железа внутрь, чтобы повысить уровень железа и гемоглобин до нормального уровня.
- Мультивитамины, содержащие железо, и изменения в диете могут помочь. Однако, если у пациента анемия, этого обычно недостаточно.
- Важно, чтобы добавки железа принимались натощак или с небольшим количеством еды, чтобы они усваивались должным образом. Детям нельзя запивать железом молоко или напитки с кофеином.
- Детям полезно принимать железо с продуктами с высоким содержанием витамина С, такими как апельсиновый сок, клубника, болгарский перец и помидоры.Эти продукты помогут усвоить железо.
- Дети должны начать чувствовать себя лучше в течение нескольких дней после начала приема препаратов железа. Уровни гемоглобина начнут повышаться примерно через месяц, так как вырабатывается больше красных кровяных телец.
- Детям обычно необходимо принимать добавки железа в течение 3–6 месяцев, но иногда требуется более длительное лечение.
Если нет реакции на начальное лечение, возможно, ребенок получает неправильную дозу железа или организм неправильно его усваивает.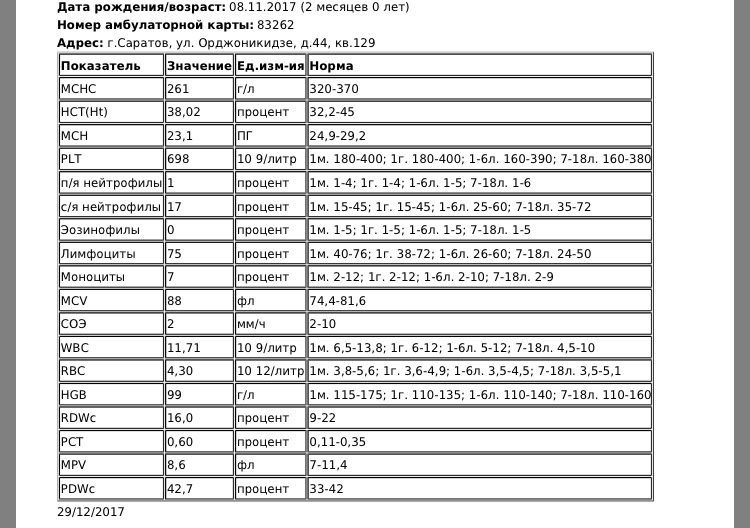 В этих случаях врач захочет повторно проверить уровень в крови и уровень железа, а ребенку может потребоваться посещение детского гематолога, который специализируется на заболеваниях крови.
В этих случаях врач захочет повторно проверить уровень в крови и уровень железа, а ребенку может потребоваться посещение детского гематолога, который специализируется на заболеваниях крови.
Профилактика железодефицитной анемии у детей
- Младенцы младше одного года должны пить только грудное молоко или смеси, содержащие железо. Когда они начинают есть твердую пищу примерно в 6-месячном возрасте, пища должна быть обогащена железом.
- Малыши в возрасте до 2 лет должны есть только 24 унции цельного молока в день.
- Все дети должны есть продукты, богатые железом, например красное мясо, курицу, рыбу, зеленые листовые овощи и бобы.
- Ознакомьтесь с таблицей ниже, в которой показано количество железа в самых разных продуктах питания.
- Ознакомьтесь с другими рекомендациями на сайте Healthychildren.org, чтобы увеличить количество железа в рационе вашего подростка.
Железо из большинства животных источников (гемовое железо) обычно легче усваивается, чем железо из растительных источников пищи (негемовое железо).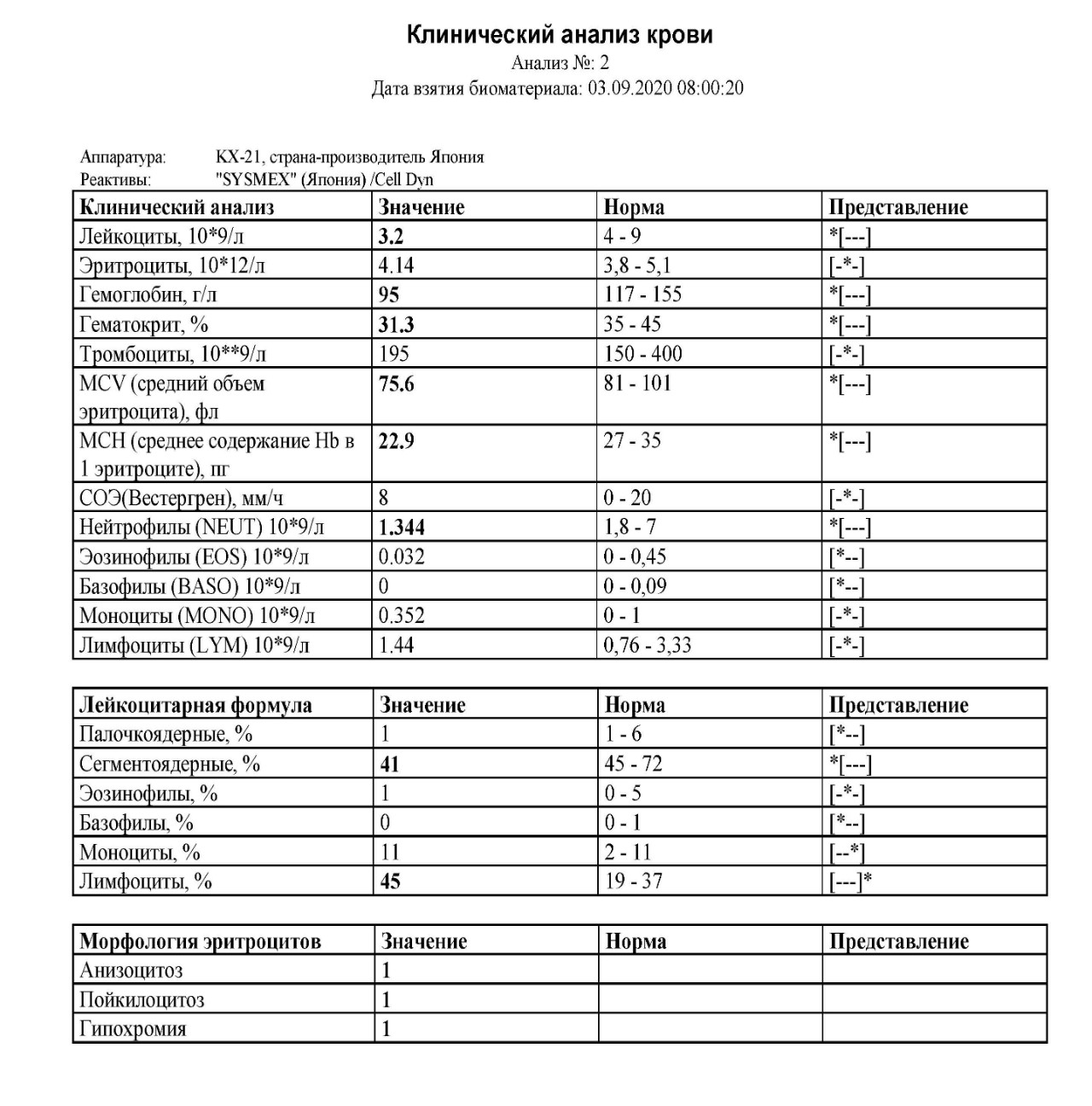
Источники преимущественно гемового железа:
ЕДА | ЖЕЛЕЗНЫЙ (МИЛЛИГРАММЫ) |
Тушеная говяжья печень (3 унции) | 5,8 мг |
Постное филе жареное (3 унции) | 2,9 мг |
Нежирный говяжий фарш, жареный (3 унции) | 1.8 мг |
Куриная грудка без кожи, жареное темное мясо (3 унции) | 1,1 мг |
Куриная грудка без кожи, обжаренное белое мясо (3 унции) | 0,9 мг |
Свинина нежирная, жареная (3 унции) | 0,9 мг |
Лосось, консервированный с косточкой (3 унции) | 0,7 мг |
Источники негемового железа:
ЕДА | ЖЕЛЕЗНЫЙ (МИЛЛИГРАММЫ) |
Обогащенные хлопья для завтрака (1 стакан) | 4. |
Тыквенные семечки (1 унция) | 4,2 мг |
Меласса Blackstrap (1 столовая ложка) | 3,5 мг |
Соевые орехи (1/2 стакана) | 3,5 мг |
Отруби (1/2 стакана) | 3 мг |
Вареный шпинат (1/2 стакана) | 3.2 мг |
Красная фасоль, приготовленная (1/2 стакана) | 2,6 мг |
Чернослив (3/4 стакана) | 2,3 мг |
Лимская фасоль, приготовленная (1/2 стакана) | 2,2 мг |
Тофу твердый (1/2 стакана) | 2 мг |
Рис обогащенный, приготовленный (1/2 стакана) | 1. |
Крендели (1 унция) | 1,2 мг |
Цельнозерновой хлеб (1 ломтик) | 0,9 мг |
Зеленая фасоль, приготовленная (1/2 стакана) | 0,8 мг |
Хлеб белый, обогащенный мукой (1 ломтик) | 0,8 мг |
Яичный желток, большой (1) | 0.6 мг |
Арахисовое масло с кусочками (2 столовые ложки) | 0,6 мг |
Абрикосы сушеные (3) | 0,6 мг |
Вареные кабачки (1/2 стакана) | 0,3 мг |
Клюквенный сок (3/4 стакана) | 0,3 мг |
Рис необогащенный, приготовленный (1/2 стакана) | 0. |
Виноград (1/3 стакана) | 0,1 мг |
Дополнительные ресурсы:
Написано Элис Гросс, MD
Рецензировано Сарой Лауле, MD
Обновлено в сентябре 2017 г.
причин дефицита железа у вашего ребенка — Клиника Кливленда
Автор: Кадаккал Радхакришнан, MD
Клиника Кливленда — некоммерческий академический медицинский центр.Реклама на нашем сайте помогает поддерживать нашу миссию. Мы не поддерживаем продукты или услуги, не принадлежащие Cleveland Clinic. Политика
Железо необходимо для развития вашего ребенка, а дефицит железа может повлиять на здоровье и рост вашего ребенка и даже привести к анемии.
Железодефицитная анемия относительно часто встречается у детей и возникает, когда уровень гемоглобина в крови ниже оптимального. Дефицит железа обычно возникает по трем основным причинам:
- Плохое питание .
 Дети подвержены более высокому риску дефицита железа из-за их более высокой потребности в железе. Проще говоря, диета с низким содержанием железа может привести к его дефициту. И не переусердствуйте с молоком! Диета с избыточным количеством молока, являющегося плохим источником железа, может подвергнуть ребенка риску дефицита железа.
Дети подвержены более высокому риску дефицита железа из-за их более высокой потребности в железе. Проще говоря, диета с низким содержанием железа может привести к его дефициту. И не переусердствуйте с молоком! Диета с избыточным количеством молока, являющегося плохим источником железа, может подвергнуть ребенка риску дефицита железа. - Потеря крови. Причины кровопотери могут варьироваться от язвы желудка (которая редко встречается у детей) до хронического воспаления кишечника и паразитарных заболеваний, таких как нематоды.
- Неспособность усваивать достаточное количество железа из пищи. Это может произойти при таких состояниях, как целиакия или болезнь Крона.
Признаки и симптомы дефицита железа
Несколько признаков могут сигнализировать о том, что у вашего ребенка дефицит железа:
- Общее отсутствие энергии и усталости.
- Бледный вид из-за падения уровня гемоглобина.
- Ногти, которые кажутся хрупкими, язык более красным, чем обычно, и / или трещины на боковой стороне рта.

- Плохой аппетит или желание есть непродовольственные товары, такие как лед, грязь, краска или крахмал.
Дети с дефицитом железа также могут подвергаться более высокому риску отравления свинцом и инфицирования.
Диагностика и лечение
Для диагностики дефицита железа необходимо обследование вашего ребенка педиатром. Оценка включает в себя подробный анамнез, питание, физический осмотр и, наконец, лабораторный анализ, который включает полный анализ крови, включая уровень гемоглобина, оценку статуса железа и запасов в организме, которые включают специальные тесты.
Хотя наиболее частой причиной дефицита железа является недостаточное питание, эти тесты необходимы для точного определения причины дефицита.
Для лечения дефицита железа обычно используются добавки железа, которые могут включать в себя лекарства, отпускаемые по рецепту. На это потребуется до трех месяцев лечения.
В то же время врач, вероятно, оценит и вылечит любое основное заболевание, которое может привести к нарушению всасывания железа или кровопотере.
Хотя реже, в случае, когда уровень гемоглобина у ребенка становится слишком низким, ему или ей может потребоваться переливание крови или терапия с инъекцией железа или внутривенная терапия железом.Это лечение, которое проходит в больнице.
В целом, семьи, страдающие дефицитом железа, могут получить пользу от помощи педиатра-диетолога для улучшения диетического потребления железосодержащих продуктов. Витамин С также может помочь улучшить усвоение железа, поэтому эта добавка может быть полезна в сочетании с продуктами, богатыми железом.
Анемия у детей — состояния и симптомы | Медицинский центр Университета Раша
Анемия — это распространенное заболевание крови, которое возникает, когда у ребенка слишком мало здоровых эритроцитов.Красные кровяные тельца важны, потому что они доставляют кислород ко всем частям тела через белок внутри каждой клетки, называемый гемоглобином. Без достаточного количества кислорода ваш ребенок может чувствовать себя очень усталым, слабым, а его органы и ткани могут быть повреждены.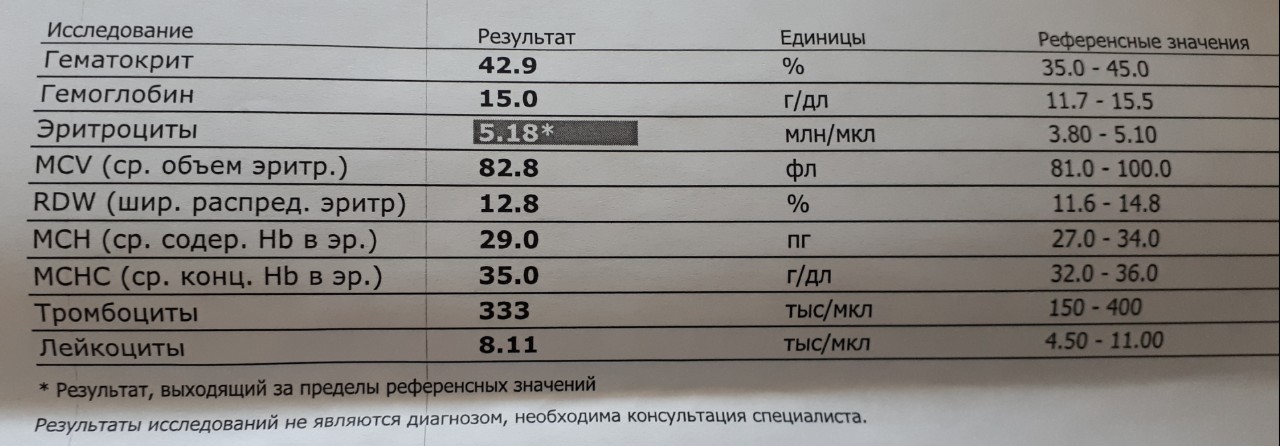
Что такое анемия у детей?
Анемия возникает, когда организм вашего ребенка достаточно быстро разрушает, теряет или не вырабатывает эритроциты. Анемия часто встречается у детей ясельного и подросткового возраста, когда для быстрого роста требуется больше железа и других питательных веществ, чем обычно.
Есть много причин анемии у детей, в том числе генетика, диета с низким содержанием железа или витамина B12, инфекции, некоторые виды рака и лечение, связанное с лекарствами.
Типы анемии у детей
Существует много типов анемии — от обычных до редких:
Апластическая анемияКостный мозг вашего ребенка не вырабатывает достаточно новых красных кровяных телец.
Гемолитическая анемияОрганизм вашего ребенка разрушает эритроциты быстрее, чем обычно, а костный мозг вашего ребенка не может достаточно быстро производить новые замещающие клетки.
Железодефицитная анемия Организму вашего ребенка не хватает железа для выработки гемоглобина, потому что его диета требует больше железа, его организм не усваивает железо или потому что он каким-то образом теряет кровь (например, кровотечение, менструация).
Костный мозг вашего ребенка вырабатывает аномальный гемоглобин, белок, переносящий кислород в красных кровяных тельцах. Обычно круглые и гибкие, эти аномальные клетки липкие, жесткие, хрупкие и изогнутые, как серп.Они закупоривают кровеносные сосуды и препятствуют нормальному притоку кислорода, вызывая болезненные приступы и другие осложнения.
ТалассемияГруппа заболеваний крови (которые вы можете передать своему ребенку), при которых костный мозг вашего ребенка вырабатывает аномальный гемоглобин. Симптомы зависят от типа и степени тяжести, но могут привести к тому, что организм вашего ребенка не вырабатывает достаточно красных кровяных телец или гемоглобина.
Симптомы анемии у детей
- Чувство усталости или слабости
- Одышка
- Головокружение
- Головная боль
- Бледная кожа
Помощь детям с анемией в спешке
Диагностика анемии
Запишитесь на прием к педиатру вашего ребенка, если у вашего ребенка симптомы анемии.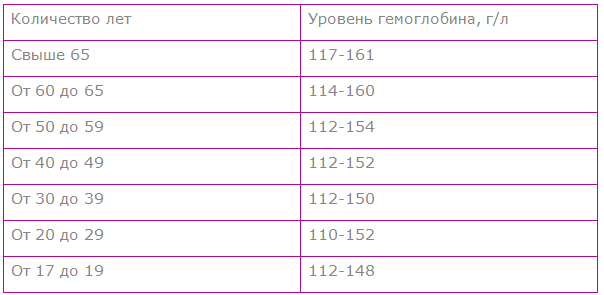
Врач вашего ребенка спросит о симптомах, лекарствах, диете и семейном анамнезе, а также назначит общий анализ крови. И если эти тесты выявляют анемию, врач вашего ребенка может назначить дополнительные тесты, чтобы определить причину. Ваш педиатр также может направить вашего ребенка к детскому гематологу в Rush, который специализируется на заболеваниях крови.
Лечение анемии
Первые шаги к лечению — это выявление причин анемии у вашего ребенка, а затем определение наилучшего способа ее лечения, который часто включает в себя восстановление нормального количества эритроцитов или уровня гемоглобина у вашего ребенка, если это возможно.
Лечение вашего ребенка будет зависеть от того, что вызывает анемию, а также от типа и степени тяжести анемии. Лечение может включать одно или несколько из следующего:
- Корректировки диеты и добавки могут помочь справиться с дефицитом железа или витаминов
- Лекарства могут предотвратить разрушение эритроцитов в организме вашего ребенка или помочь костному мозгу вырабатывать больше.

- Переливание крови может дать вашему ребенку здоровые эритроциты, если у него тяжелая анемия
Rush Excellence в лечении анемии у детей
- Опыт лечения заболеваний крови: Детские гематологи детской больницы Университета Раша специализируются на лечении детей с заболеваниями крови и обеспечивают квалифицированный уход за детьми и их семьями.Многие из них участвуют в клинических и лабораторных исследованиях и имеют доступ к самым передовым методам лечения и самым последним клиническим испытаниям.
- Клинические исследования: Врачи-исследователи в Rush участвуют в клинических испытаниях и исследованиях, которые могут открыть двери для новых эффективных методов лечения различных типов анемии и других заболеваний крови.
- Уход рядом с домом: Детские гематологи из детской больницы Университета Раша готовы принять пациентов в нашем кампусе в Раше в Чикаго, в Медицинском центре Раша Копли в Авроре и в дополнительном центре в Хоффман Эстейтс.

Распространенность анемии у детей в возрасте 6–59 месяцев (%)
Название показателя:
Распространенность анемии у детей в возрасте 6–59 месяцев (%)Краткое название:
Распространенность анемии у детейТема:
Факторы риска
Смертность и бремя болезней
Обоснование:
Анемия широко распространена во всем мире, непропорционально поражая детей и женщин репродуктивного возраста.Анемия связана с плохим когнитивным и двигательным развитием, а также с трудоспособностью. У беременных женщин железодефицитная анемия также связана с неблагоприятными репродуктивными последствиями, такими как преждевременные роды, дети с низкой массой тела при рождении и снижение запасов железа для ребенка, что может привести к нарушению развития. Дефицит железа считается наиболее частой причиной анемии, но есть и другие причины, связанные с питанием и не связанные с питанием. Концентрация гемоглобина в крови используется для диагностики анемии и зависит от многих факторов, включая высоту (в метрах над уровнем моря), курение, триместр беременности, возраст и пол.Когда концентрации гемоглобина в крови используются в сочетании с другими показателями статуса железа, они предоставляют информацию о степени тяжести дефицита железа. Распространенность анемии среди населения может использоваться для классификации значимости проблемы для общественного здравоохранения.
Дефицит железа считается наиболее частой причиной анемии, но есть и другие причины, связанные с питанием и не связанные с питанием. Концентрация гемоглобина в крови используется для диагностики анемии и зависит от многих факторов, включая высоту (в метрах над уровнем моря), курение, триместр беременности, возраст и пол.Когда концентрации гемоглобина в крови используются в сочетании с другими показателями статуса железа, они предоставляют информацию о степени тяжести дефицита железа. Распространенность анемии среди населения может использоваться для классификации значимости проблемы для общественного здравоохранения.Определение:
Процент детей в возрасте 6-59 месяцев с концентрацией гемоглобина менее 110 г / л с поправкой на высоту.Метод измерения
Состояние анемии оценивается по концентрации гемоглобина в крови.Концентрация гемоглобина в крови обычно измеряется в исследованиях с использованием прямого цианметгемоглобинового метода в лаборатории или с помощью портативного фотометра гемоглобина с батарейным питанием (с использованием метода азид-метгемоглобина) в полевых условиях.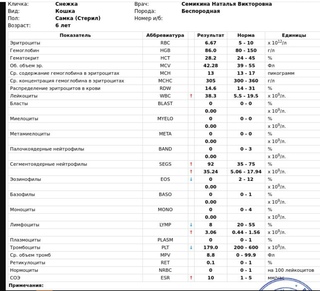
Метод оценки:
Данные о распространенности анемии и / или среднем уровне гемоглобина у женщин репродуктивного возраста, собранные в период с 1995 по 2019 год, были получены из 408 репрезентативных источников данных из 124 стран мира. Байесовская иерархическая модель смеси использовалась для оценки распределения гемоглобина и систематического рассмотрения недостающих данных, нелинейных временных тенденций и репрезентативности источников данных.Полная информация об источниках данных доступна на странице GHO Anemia. Полную информацию о статистических методах можно найти здесь: Finucane MM, Paciorek CJ, Stevens GA EM. Полупараметрическая байесовская оценка плотности с использованием разрозненных источников данных: метаанализ глобального недоедания среди детей. J Am Stat Assoc. 2015; 110 (511): 889–901.Другие возможные источники данных:
Системы видеонаблюдения
Предпочтительные источники данных:
Опросы населения
Ожидаемая частота распространения данных:
Каждые 2-3 годаОжидаемая частота сбора данных:
Источники данных непрерывно собираются из отчетов об исследованиях и рукописей и вводятся в базу данных ВОЗ по микронутриентам, являющуюся частью информационных систем по витаминному и минеральному питанию (VMNIS).

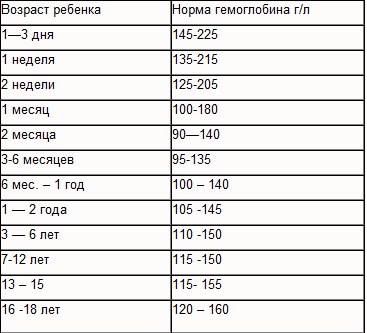


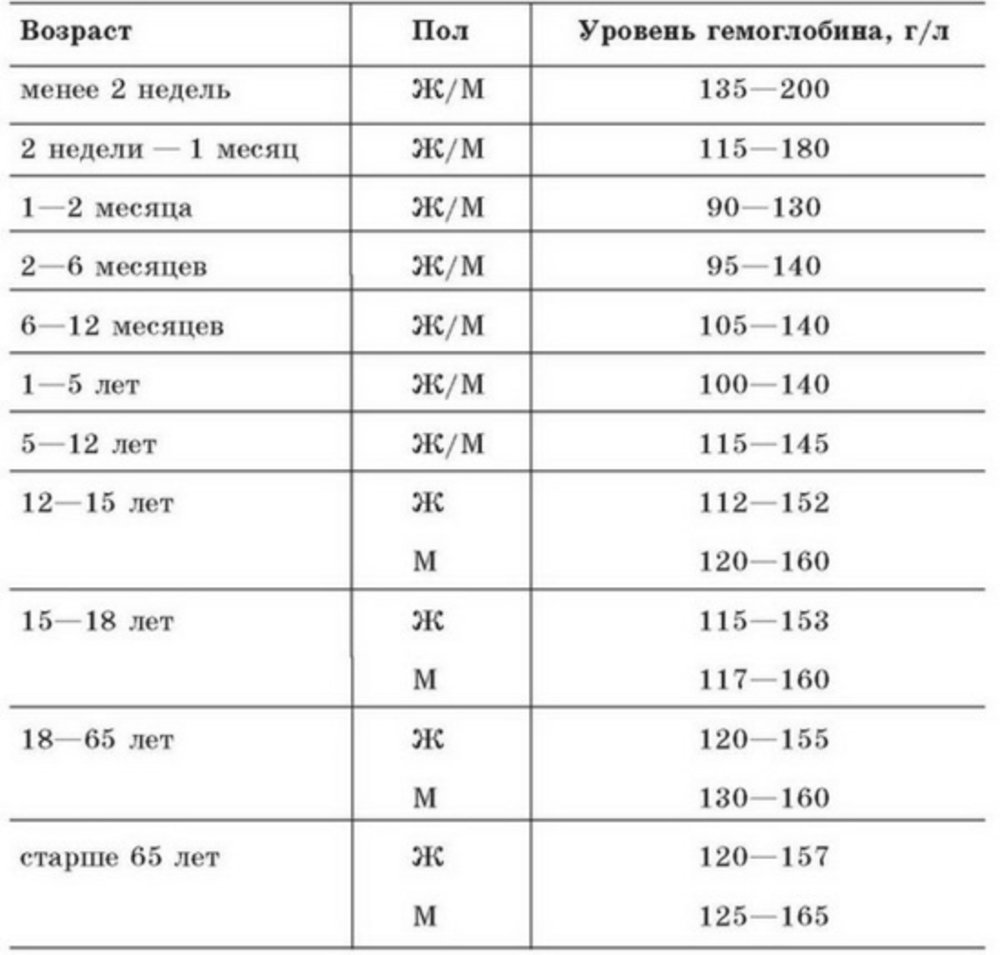


 Если уровень эритроцитов ниже нормы (анемия) организм получает недостаточные количества кислорода. Если уровень эритроцитов выше нормы (полицитемия, или эритроцитоз) имеется высокий риск того, что красные кровные клетки склеятся между собой и заблокируют движение крови по сосудам (тромбоз).
Если уровень эритроцитов ниже нормы (анемия) организм получает недостаточные количества кислорода. Если уровень эритроцитов выше нормы (полицитемия, или эритроцитоз) имеется высокий риск того, что красные кровные клетки склеятся между собой и заблокируют движение крови по сосудам (тромбоз).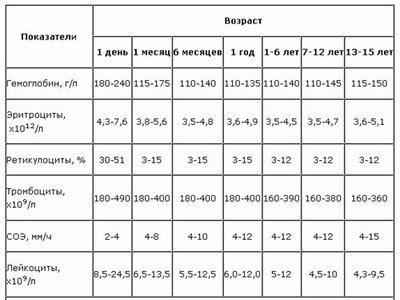 Повышенный гематокрит встречается при эритроцитозах (повышенное количество эритроцитов в крови), а также при обезвоживании организма. Снижение гематокрита указывает на анемию (снижение уровня эритроцитов в крови), либо на увеличение количества жидкой части крови.
Повышенный гематокрит встречается при эритроцитозах (повышенное количество эритроцитов в крови), а также при обезвоживании организма. Снижение гематокрита указывает на анемию (снижение уровня эритроцитов в крови), либо на увеличение количества жидкой части крови. Лейкоциты по размерам превышают эритроциты, однако содержатся в крови в гораздо меньшем количестве. Высокий уровень лейкоцитов говорит о наличии бактериальной инфекции, а снижение числа лейкоцитов встречается при приеме некоторых лекарств, заболеваниях крови и др.
Лейкоциты по размерам превышают эритроциты, однако содержатся в крови в гораздо меньшем количестве. Высокий уровень лейкоцитов говорит о наличии бактериальной инфекции, а снижение числа лейкоцитов встречается при приеме некоторых лекарств, заболеваниях крови и др.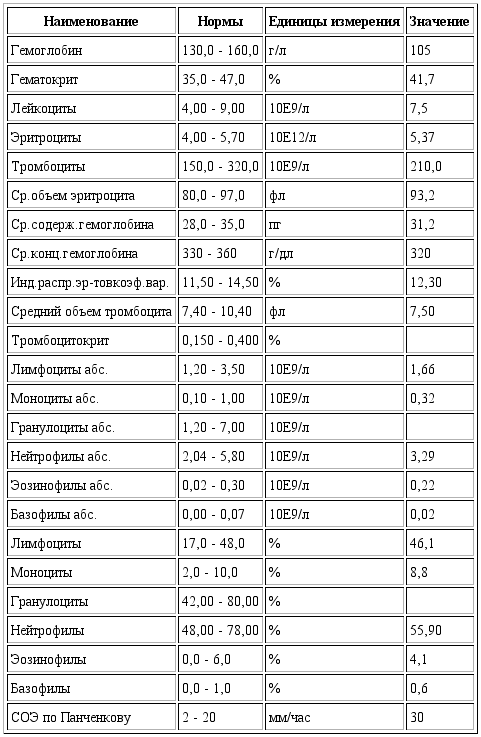 Повышенное содержание моноцитов встречается при некоторых инфекционных заболеваниях (туберкулез) ревматоидном артрите, заболеваниях крови. Снижение уровня моноцитов встречается после тяжелых операций, приема лекарств, подавляющих иммунитет (кортикостероиды и др.).
Повышенное содержание моноцитов встречается при некоторых инфекционных заболеваниях (туберкулез) ревматоидном артрите, заболеваниях крови. Снижение уровня моноцитов встречается после тяжелых операций, приема лекарств, подавляющих иммунитет (кортикостероиды и др.).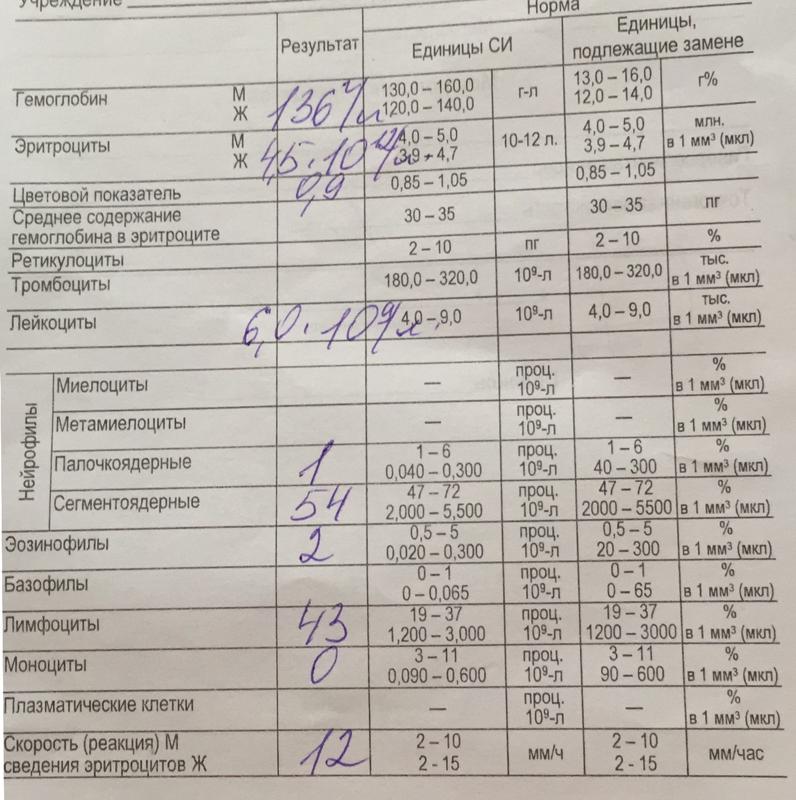

 Симптомы неявные, поэтому человек крайне редко обращается к специалистам на этой стадии заболевания.
Симптомы неявные, поэтому человек крайне редко обращается к специалистам на этой стадии заболевания.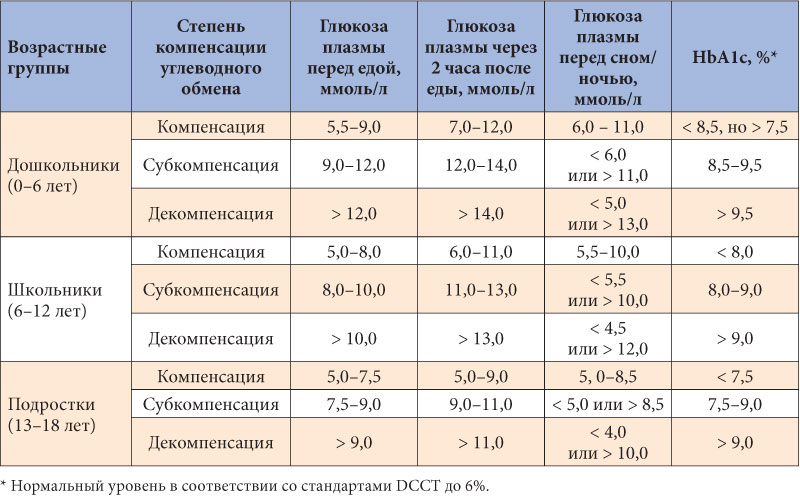 Всего 50 г сушеных грибов в сутки помогут восполнить норму содержания железа в крови. Есть их каждый день могут не все, но периодически включать в свой рацион грибы очень полезно.
Всего 50 г сушеных грибов в сутки помогут восполнить норму содержания железа в крови. Есть их каждый день могут не все, но периодически включать в свой рацион грибы очень полезно.

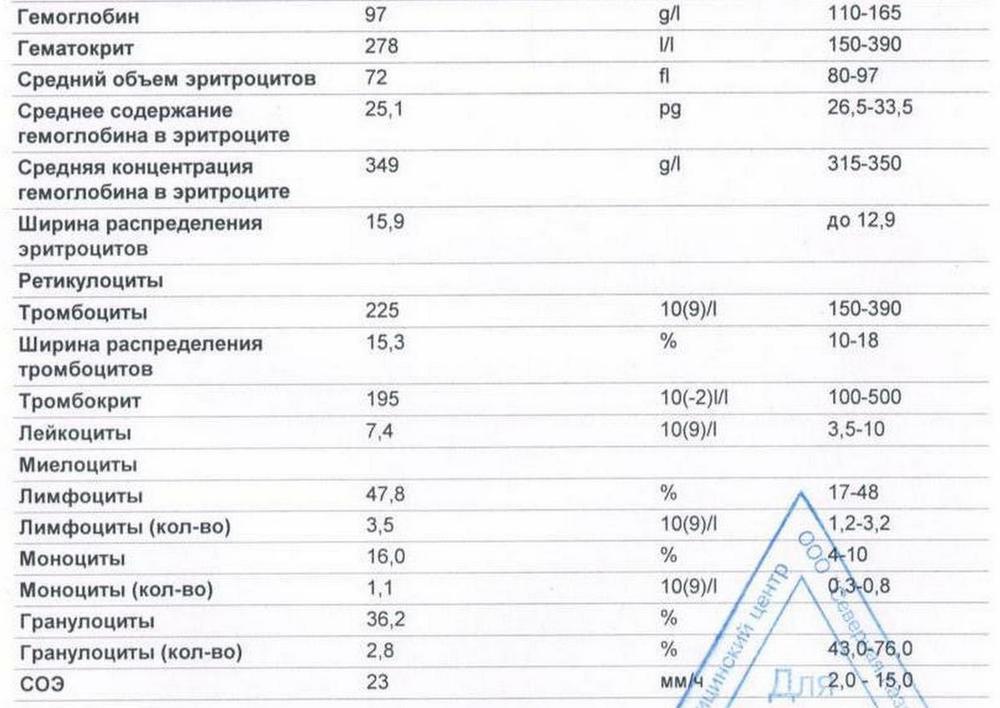 Это происходит, когда красные кровяные тельца становятся слишком большими из-за недостатка фолиевой кислоты или витамина B-12.
Это происходит, когда красные кровяные тельца становятся слишком большими из-за недостатка фолиевой кислоты или витамина B-12.
 Формула с низким содержанием железа может привести к железодефицитной анемии, и ее не следует использовать. См. Выбор формулы .
Формула с низким содержанием железа может привести к железодефицитной анемии, и ее не следует использовать. См. Выбор формулы .  Когда вы начинаете давать ребенку твердую пищу — обычно в возрасте от 4 до 6 месяцев — давайте продукты с добавлением железа, такие как обогащенные железом детские каши, мясное пюре и протертые бобы. Для детей старшего возраста хорошими источниками железа являются красное мясо, курица, рыба, бобы и шпинат.
Когда вы начинаете давать ребенку твердую пищу — обычно в возрасте от 4 до 6 месяцев — давайте продукты с добавлением железа, такие как обогащенные железом детские каши, мясное пюре и протертые бобы. Для детей старшего возраста хорошими источниками железа являются красное мясо, курица, рыба, бобы и шпинат.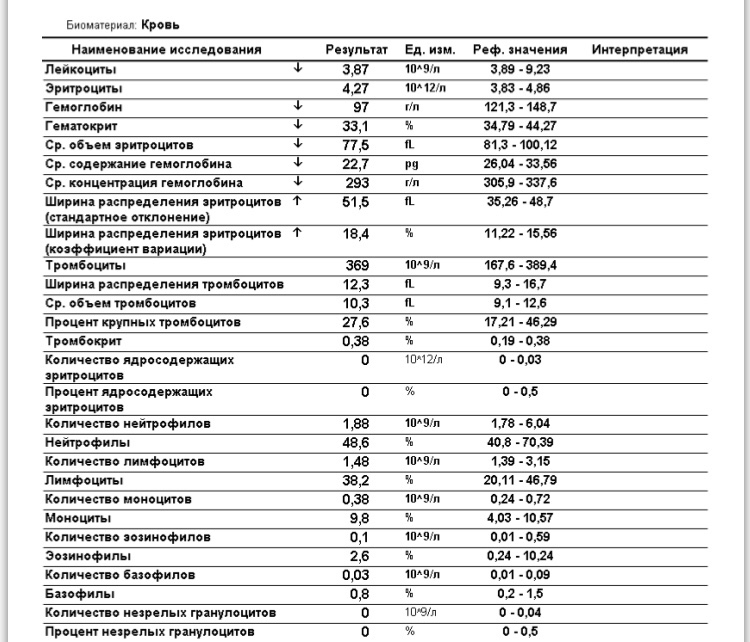 По состоянию на 14 октября 2019 г.
По состоянию на 14 октября 2019 г.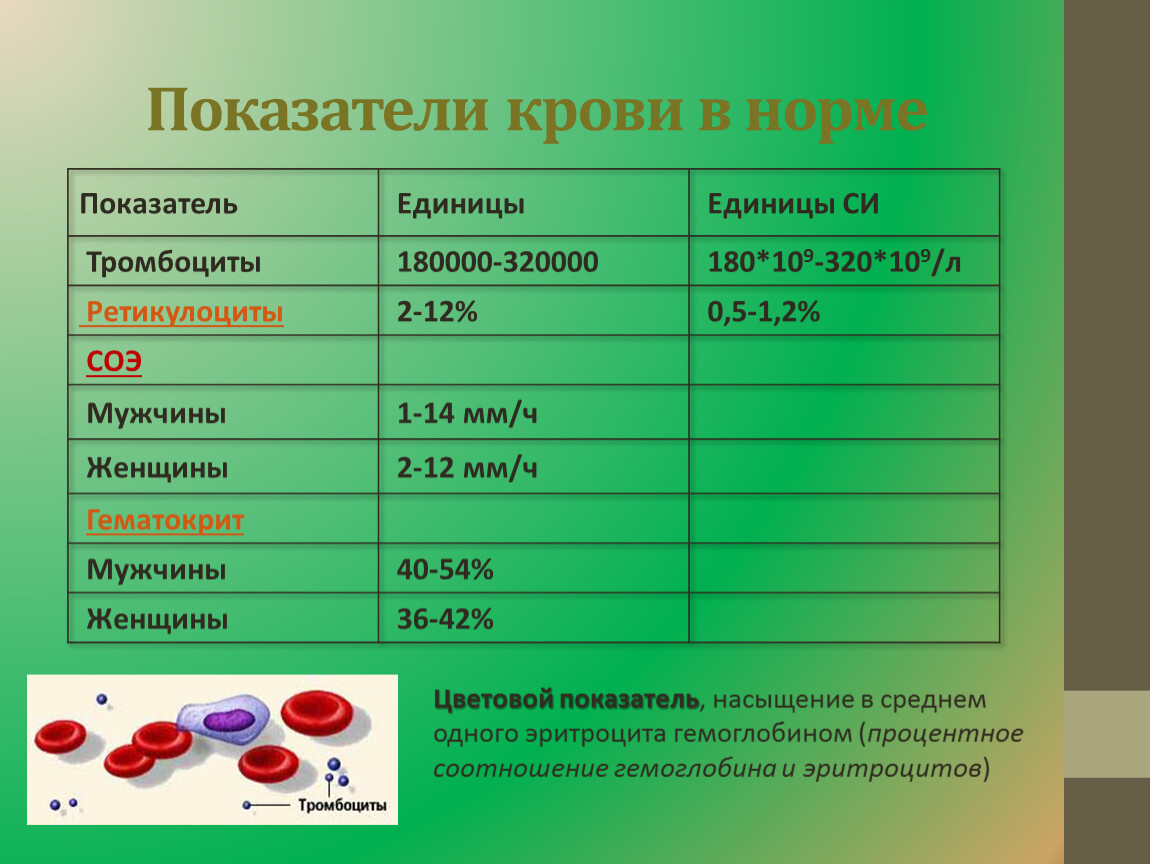 5 мг — 18 мг (в зависимости от злака)
5 мг — 18 мг (в зависимости от злака) 4 мг
4 мг 2 мг
2 мг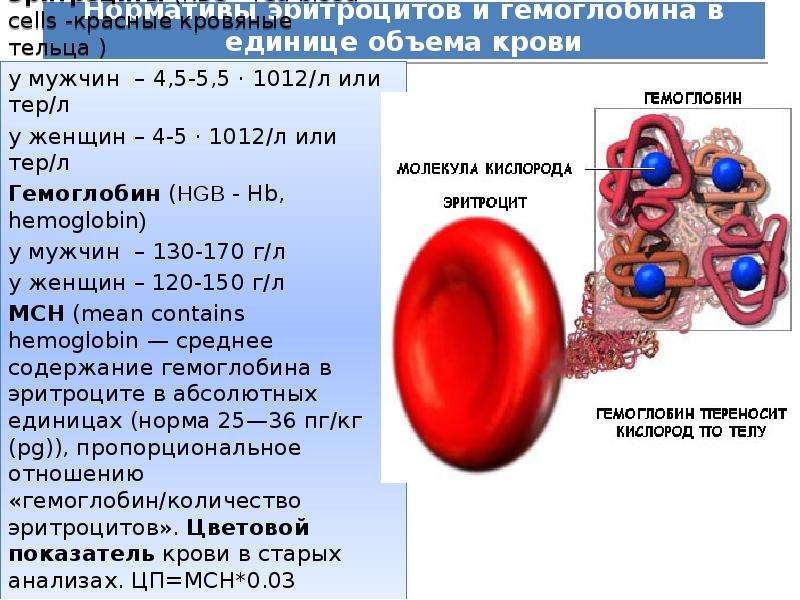 Дети подвержены более высокому риску дефицита железа из-за их более высокой потребности в железе. Проще говоря, диета с низким содержанием железа может привести к его дефициту. И не переусердствуйте с молоком! Диета с избыточным количеством молока, являющегося плохим источником железа, может подвергнуть ребенка риску дефицита железа.
Дети подвержены более высокому риску дефицита железа из-за их более высокой потребности в железе. Проще говоря, диета с низким содержанием железа может привести к его дефициту. И не переусердствуйте с молоком! Диета с избыточным количеством молока, являющегося плохим источником железа, может подвергнуть ребенка риску дефицита железа.

