ЧП в Приморье: дети заболели после пробы Манту из-за передозировки
Мама одного из пострадавших Елена Свиридова рассказала корреспонденту РИА Новости, что ничего не знала ни о том, что ее ребенку будут делать пробу Манту, ни даже о том, что ее ребенок оказался в больнице. По ее словам, на следующий после вакцинации день большинство детей собрали в школе и, не предупреждая родителей, увезли в больницу.
«Нас не предупреждали о приезде врачей и каких-либо прививках. Когда мы попросили объяснений, все школьное руководство сказало о том, что они не знают, откуда и зачем приехали врачи <…> Моего ребенка вечером рвало, у других детей проявлялись разные симптомы, повышенная температура, многие дети не могли уснуть от жара», — говорит Свиридова.
Представитель департамента здравоохранения Приморского края подтвердил РИА Новости, что пробы Манту без согласия родителей — это нарушение установленного порядка, так как родители имеют право отказаться.
«Ситуация очень сложная.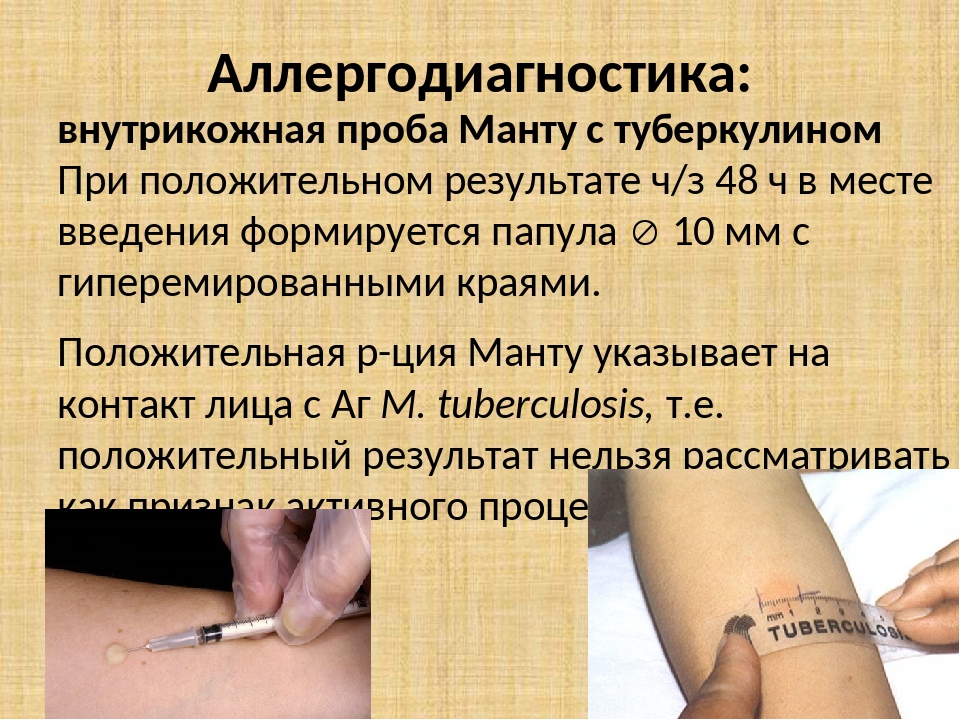
В самой школе получить комментарий не удалось. Представитель школы сообщил РИА Новости, что директор отсутствует на рабочем месте, остальные же сотрудники школы от комментариев отказались.
Прокуратура говорит о передозировке и проверяет качество препарата
По данным прокуратуры края, причиной заболевания детей стало превышение дозы препарата, который им вводили.
«Врач-педиатр Яковлевской центральной районной больницы совместно с медицинской сестрой этой же больницы провели туберкулинодиагностику препаратом «туберкулин» с превышением допустимых доз 45-ти учащихся школы села Новосысоевка», — сообщает прокуратура.
В связи с инцидентом, сообщает ведомство, опрошены проводившие вакцинацию медицинские работники и родители учеников, установлен полный список детей, которым сделали пробу (сначала говорили о 43 школьниках, потом о 45).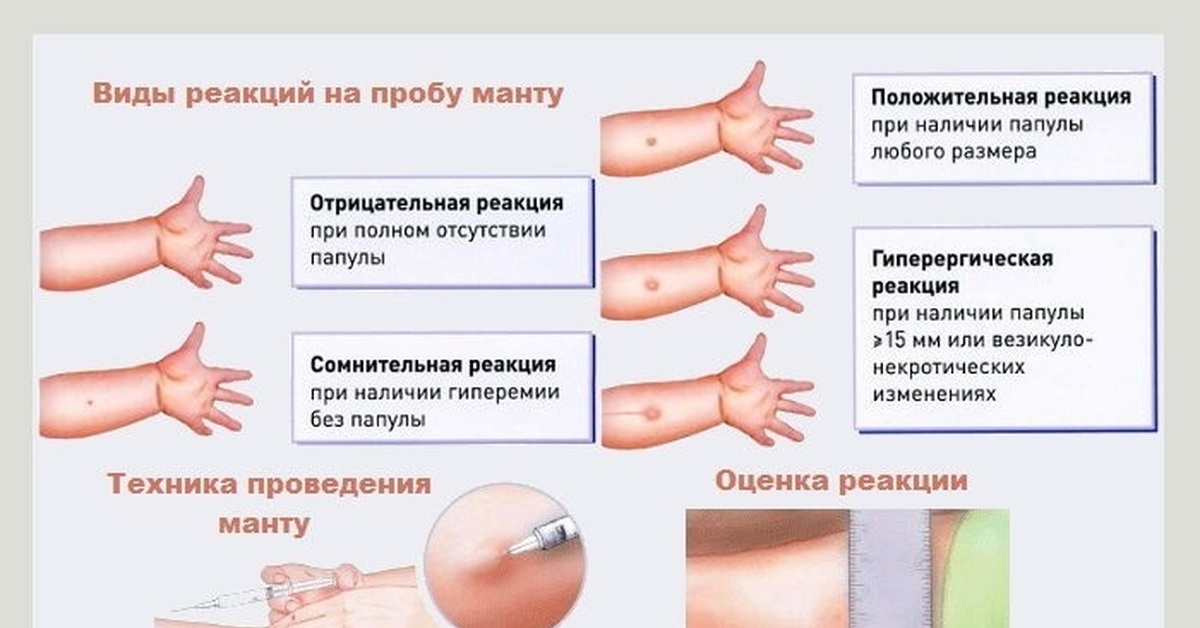
В свою очередь, департамент здравоохранения края проверяет вакцину, которую вводили детям.
«Департамент проводит проверку по факту госпитализации детей после вакцинации традиционным препаратом «туберкулин». Специалисты проверяют качество и ее соответствие, как хранилась и транспортировалась вакцина, так как она могла испортиться из-за этого. Также проверяются действия врача и двух медсестер, которые проводили пробы Манту», — рассказал РИА Новости представитель департамента.
Эксперт Минздрава: проба Манту детям после семи лет уже не нужна — Общество
НЬЮ-ЙОРК, 27 сентября. /ТАСС/. Ребенку, имеющему две вакцинации от туберкулеза к семи годам, проба Манту уже не нужна, достаточно ежегодно проверять Диаскинтестом (инновационный внутрикожный диагностический тест на латентность форм туберкулеза). Об этом ТАСС на полях Генеральной Ассамблеи ООН сообщила главный внештатный фтизиатр Минздрава РФ Ирина Васильева.
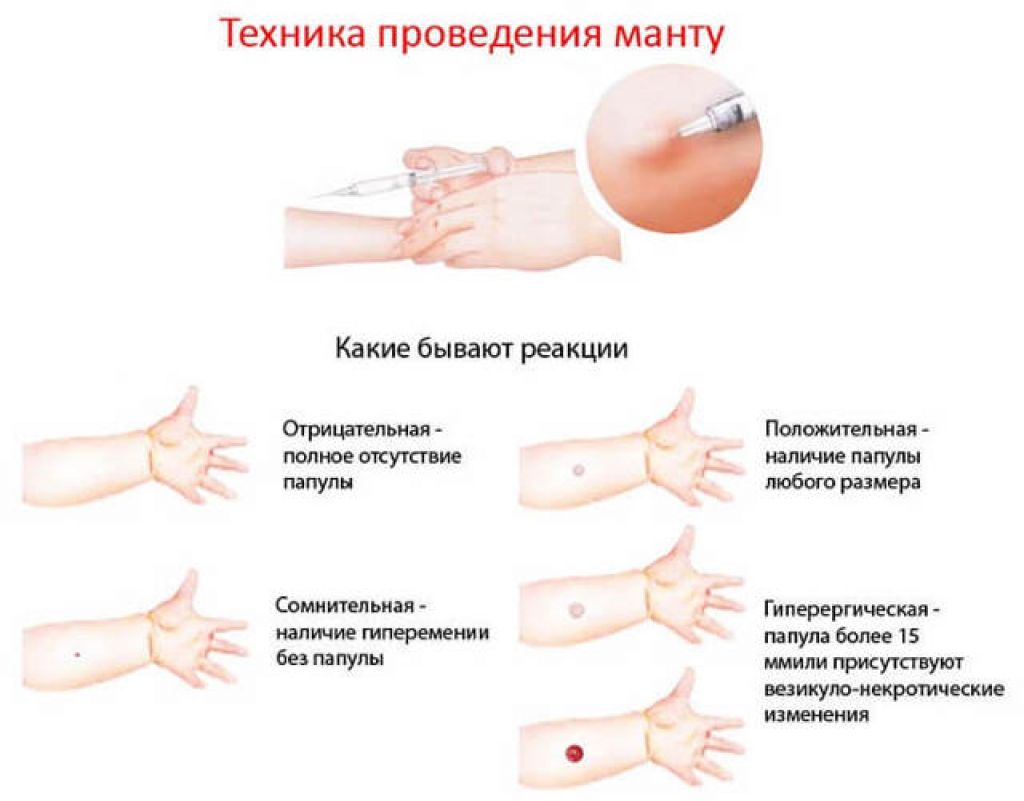
Вакцинируют сейчас детей в РФ два раза — при рождении и в семь лет. «Проба Манту нужна для того, чтобы понять, нужно его ревакцинировать или нет. Больше ни для чего она не нужна», — отметила Васильева.
По ее словам, с 2017 года всех детей в РФ ежегодно проверяют на туберкулез уже Диаскинтестом: «Каждый год проверяют и выясняют, инфицирован ли ребенок. Если инфицирован, то вакцинировать уже не нужно, а если не инфицирован, то вакцинируется в семь лет. Уже после нее проба Манту не нужна».
Проба Манту менее специфична в отличие от Диаскинтеста — наличие выраженной реакции на месте пробы, как правило, говорит о том, что организм борется с каким-то возбудителем. При этом проба Манту может дать ложноположительную реакцию, если у ребенка есть аллергия в активной фазе.
В рамках сессии Генассамблеи в среду состоялось совещание высокого уровня, сопредседателем которого была министр здравоохранения РФ Вероника Скворцова. Министр отметила, что заболеваемость туберкулезом в РФ снизилась на 42% за последние 10 лет, достичь существенных успехов в борьбе с туберкулезом, по ее словам, позволило непрерывное финансирование программ.
Статистика ВОЗ
По данным Всемирной организации здравоохранения, ежегодно в мире заболевают туберкулезом 10 млн человек, каждый десятый — ребенок. По данным за 2017 год, почти полмиллиона человек болеют туберкулезом, имеющим множественную лекарственную устойчивость. Туберкулез остается основной инфекционной причиной смертности в мире, унося ежедневно почти 4,4 тыс. жизней.
Правомерно ли отстранение ребенка от посещения занятий в школе при отказе от проведения пробы Манту?
Ответ: В соответствии со ст. 10 Федерального закона от 30.03.1999 № 52-ФЗ «О санитарно-эпидемиологическом благополучии населения» граждане обязаны выполнять требования санитарного законодательства и не осуществлять действий, влекущих за собой нарушение прав других граждан на охрану здоровья и благоприятную среду обитания.
Санитарно-эпидемиологическими правилами СП 3.1.2.3114-13 «Профилактика туберкулеза» (далее- Правила) определено, что в Российской Федерации основным методом раннего выявления туберкулёза у детей является ежегодная туберкулинодиагностика (внутрикожная аллергическая проба с туберкулином – проба Манту). В целях раннего выявления туберкулёза туберкулинодиагностика проводится детям с 12-месячного возраста и до достижения ими 18 лет (пункт 5.1 Правил). Пробу Манту ставят 1 раз в год независимо от результата предыдущих проб.
В целях раннего выявления туберкулёза туберкулинодиагностика проводится детям с 12-месячного возраста и до достижения ими 18 лет (пункт 5.1 Правил). Пробу Манту ставят 1 раз в год независимо от результата предыдущих проб.
В случае отказа родителей от туберкулинодиагностики для получения заключения о состоянии здоровья ребёнка рекомендуется рентгенологическое обследование органов грудной клетки.
В соответствии со ст.17.3 Федерального закона от 09.01.1996 № 3-ФЗ «О радиационной безопасности населения» гражданин имеет право отказаться от медицинских рентгенорадиологических процедур, за исключением профилактических исследований, проводимых в целях выявления заболеваний, опасных в эпидемиологическом отношении, в т.ч. туберкулёза.
Дети, туберкулинодиагностика которым не проводилась, допускаются в детскую организацию при наличии заключения врача-фтизиатра об отсутствии заболевания (п. 5.7 Правил).
Вышеуказанный пункт Правил не устанавливает ограничений прав на образование в Российской Федерации (решение Верховного Суда Российской Федерации от 17. 12.2015 № АКПИ14-1454 «Об отказе в удовлетворении заявления о признании недействующим пункта 1.3 и абзаца второго пункта 5.7 Санитарно-эпидемиологических правил СП 3.1.2.3114-13 «Профилактика туберкулёза», утв. постановлением Главного государственного санитарного врача Российской Федерации от 22.10.2013 № 60).
12.2015 № АКПИ14-1454 «Об отказе в удовлетворении заявления о признании недействующим пункта 1.3 и абзаца второго пункта 5.7 Санитарно-эпидемиологических правил СП 3.1.2.3114-13 «Профилактика туберкулёза», утв. постановлением Главного государственного санитарного врача Российской Федерации от 22.10.2013 № 60).
В случае отказа родителей от туберкулинодиагностики и невозможности предоставить в образовательную организацию заключение врача-фтизиатра об отсутствии заболевания администрация обязана временно отстранить ребёнка от посещения образовательной организации до предоставления результатов туберкулинодиагностики.
Родители вправе реализовать право ребёнка на получение образования вне организации, осуществляющей образовательную деятельность, в форме семейного образования, самообразования в соответствии со ст. 17 Федерального закона от 29.12.2012 № 273-ФЗ «Об образовании в Российской Федерации». Это подтверждено, в частности, решением Первомайского районного суда города Мурманска от 19.
Допуск детей в образовательную организацию, не прошедших туберкулинодиагностику и не имеющих заключение фтизиатра об отсутствии заболевания туберкулёзом, влечёт за собой нарушение прав других несовершеннолетних на охрану здоровья и благоприятную среду обитания. Подобные действия администрации образовательной организации образуют состав административного правонарушения, ответственность за которое предусмотрена ст. 6.7 Кодекса об административных правонарушениях Российской Федерации.
О пробе Манту — T‑SPOT.TB
Долгое время единственным тестом для скрининга была кожная проба Манту. В настоящее время ее проводят детям до 7 лет, т.к. в 7 лет решается вопрос о повторной ревакцинации БЦЖ и проводится она детям, не инфицированным туберкулезом с отрицательной пробой Манту.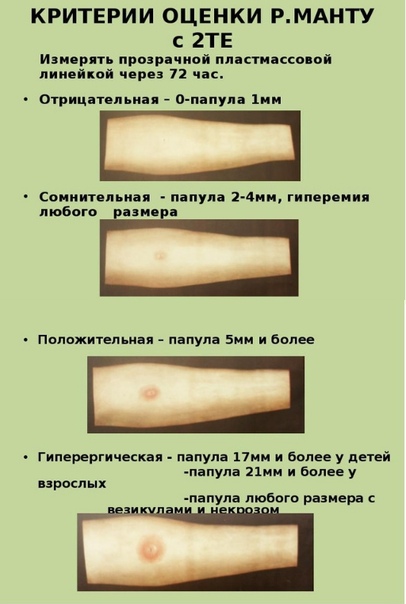
Вакцина БЦЖ (бациллы Кальметта-Герена) существует на протяжении 80 лет и является одной из наиболее широко используемых из всех существующих в настоящее время вакцин, охватывая более 80% новорожденных и детей грудного возраста в странах, где она является компонентом национальной программы иммунизации детей. Вакцина БЦЖ не предотвращает первичного инфицирования и, что более важно, не предотвращает реактивацию латентной легочной инфекции, являющейся основным источником бациллярного распространения среди населения. Вакцина БЦЖ только снижает вероятность перехода инфицирования в болезнь. А основной смысл постановки БЦЖ в том, чтобы инфицированные туберкулезом маленькие дети, в случае если инфицирование перейдет в болезнь, не заболели тяжелейшими формами туберкулеза, такими как туберкулезный менингит и диссеминированный туберкулез, когда в болезнь вовлечен весь организм. Такие формы туберкулеза калечащие, а чаще даже смертельны.
Как и любой иммунологический тест — проба Манту проводится у детей ежегодно.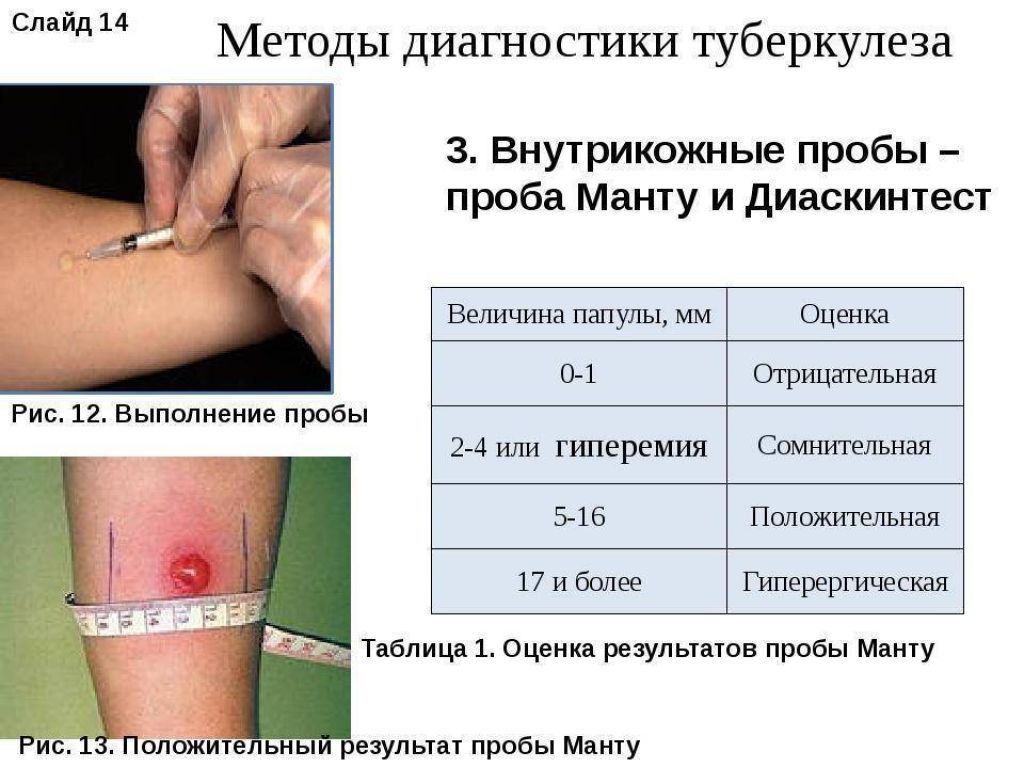
Принцип реакции Манту состоит во внутрикожном введении в человеческий организм малых доз туберкулина — антигена, полученного из микобактерии туберкулеза, и наблюдения за местной реакцией.
В месте введения препарата в кожу возникает специфическое воспаление, вызванное инфильтрацией лимфоцитами. Но в игру вступают не все Т-лимфоциты, а только те, что уже «знакомы» с палочкой Коха.
Противопоказания к проведению реакции Манту:
- кожные заболевания;
- обострение хронических инфекционных заболеваний;
- острые соматические заболевания;
- аллергические реакции и состояния, в том числе бронхиальная астма;
- эпилепсия.
С учетом вышеперечисленных факторов сама по себе положительная реакция Манту не является 100% доказательством инфицирования туберкулезом и имеет ограничения для постановки.
Недостатки кожных туберкулиновых проб:
- требуется два посещения врача;
- на результаты кожных проб влияет предшествующая вакцинация БЦЖ
- наличие иммуносупрессии у пациента может привести к отсутствию кожного иммунного ответа
- субъективность оценки, связанная с техникой выполнения инъекции и последующей интерпретации результатов;
- необходимо соблюдать определенный режим (не рекомендуется соприкосновение с водой) в течение 72 часов;
- частые побочные эффекты, особенно у детей: головная боль и головокружение, подъем температуры до 40°С, лихорадка, рвота, аллергические высыпания на коже, аллергический отек, приступы астмы, зуд в месте инъекции;
- противопоказаны пациентам с распространенными кожными заболеваниями, пациентам с эпилепсией, пациентам при аллергических состояниях и при острых и хронических инфекционных и соматических заболеваниях в стадии обострения.

T-SPOT.TB представляет собой уникальный тест, предназначенный для обследования на туберкулез, который может быть выполнен во время одного посещения врача.
T-SPOT.TB является единственным анализом крови для диагностики туберкулеза, который обладает более чем 95%-ной чувствительностью и специфичностью, а также надежностью в диагностике туберкулезной инфекции у пациентов различных групп, подтвержденными результатами многочисленных клинических исследований.
На результат теста T-SPOT.TB не влияет предшествующая вакцинация БЦЖ и/или наличие иммуносупрессии у пациента.
Сравнение анализа высвобождения интерферона-γ с показаниями туберкулиновой кожной пробы через 48–72 часа и 144–168 часов с использованием 2 коммерческих реагентов | Клинические инфекционные болезни
Аннотация
Справочная информация. Несмотря на широкое распространение, туберкулиновая кожная проба (ТКП) имеет множество ограничений, включая требование о повторном посещении через 48-72 часа. Целью этого исследования было определение надежности показаний TST между 144 и 168 часами.
Целью этого исследования было определение надежности показаний TST между 144 и 168 часами.
Методы. Антиген туберкулина наносили на оба предплечья (аплизол в одной руке и туберсол в другой, из отдельных партий каждого продукта) методом Манту. Образцы крови были взяты для анализа высвобождения интерферона-γ. Субъекты наблюдались через 48–72 часа для первоначального измерения TST (день 2) и возвращались через 144–168 часов для второго измерения (день 7).
Результаты. Всего было изучено 116 субъектов с повышенным риском туберкулеза; 25 (22%) имели положительные результаты на 2-й день с Туберсолом и 27 (23%) имели положительные результаты на 2-й день с Аплизолом.Общее согласие между туберсолом и аплизолом на 2-й день составило 93% (κ = 0,80), а на 7-й день — 94% (κ = 0,76). Общее согласие между 2-м и 7-м днями составило 89% для туберсола и 86% для аплисола. Противоречивые результаты между 2-м и 7-м днями наблюдались в основном у лиц, перенесших в анамнезе вакцинацию против бациллы Кальметта-Герена.
Выводы. Субъекты, которые не явились в течение 48–72 часов для чтения TST, могут все еще иметь надежные показания TST в течение 168 часов. Реагенты аплизол и туберсол дают сопоставимые результаты по сравнению с анализом высвобождения интерферона-γ.
Диагноз скрытой инфекции Mycobacterium tuberculosis служит основой профилактической терапии. Выявление лиц с латентной инфекцией M. tuberculosis имеет решающее значение для цели ликвидации туберкулеза, поскольку развитие активного туберкулеза в этой группе населения можно предотвратить с помощью лечения. Кожная туберкулиновая проба (ТКП) служила основой для скрининга пациентов с риском туберкулеза [1–3]. Это внутрикожная инъекция PPD из бульонной культуры M.туберкулез. Две компании производят туберкулин в США: Parkdale Pharmaceuticals (Aplisol) и Pasteur Mérieux Connaught (Tubersol).
Несмотря на широкое распространение, TST имеет множество ограничений. Недостатками могут быть сложность применения и отсутствие воспроизводимых результатов [4–9].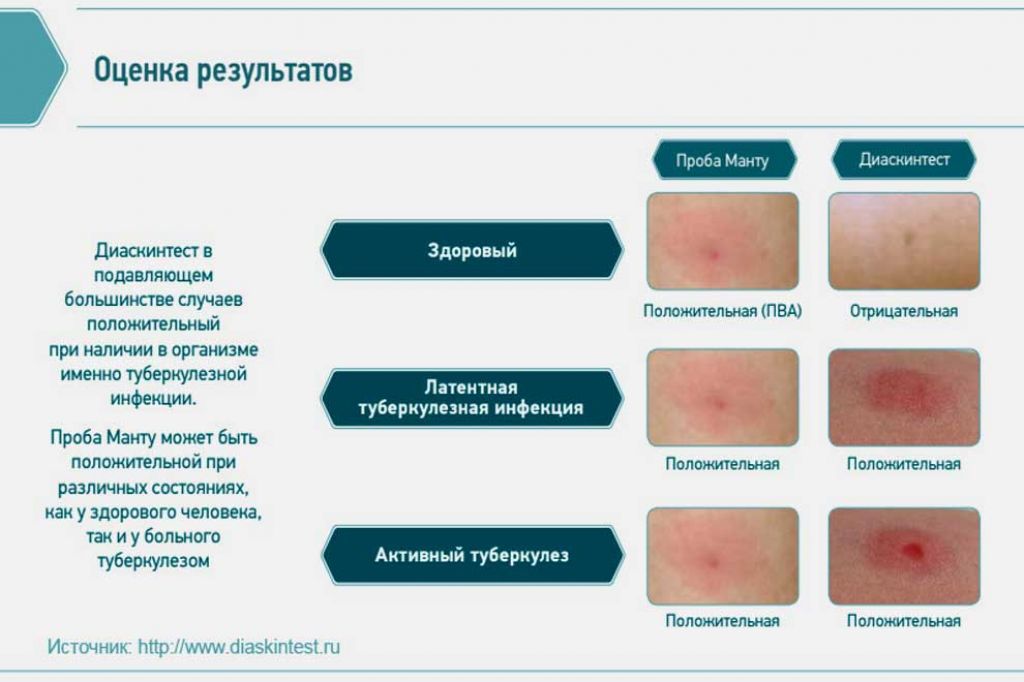 Различия между наблюдателями среди профессионалов здравоохранения также представляют собой серьезную проблему для точной интерпретации результатов ТКП [1, 10, 11]. Ошибка интерпретации и предпочтение цифр могут повлиять на результат TST [2, 12].Источником ложноположительных результатов ТКП является контакт с микобактериями, которые имеют общие антигены с M. tuberculosis [13, 14]. Учитывая степень перекрестной реактивности антигена от разных видов микобактерий, вакцинация против бациллы Кальметта-Герена (БЦЖ) может отрицательно повлиять на специфичность TST [1, 10, 11, 15–18]. Наконец, необходимость оценки туберкулинового ответа через 48–72 ч [2, 3, 19] может вызывать проблемы, особенно у малообеспеченного населения [20]. Из-за этих недостатков было разработано множество тестов для количественной оценки ответа на туберкулезные антигены [12, 15, 21–29].
Различия между наблюдателями среди профессионалов здравоохранения также представляют собой серьезную проблему для точной интерпретации результатов ТКП [1, 10, 11]. Ошибка интерпретации и предпочтение цифр могут повлиять на результат TST [2, 12].Источником ложноположительных результатов ТКП является контакт с микобактериями, которые имеют общие антигены с M. tuberculosis [13, 14]. Учитывая степень перекрестной реактивности антигена от разных видов микобактерий, вакцинация против бациллы Кальметта-Герена (БЦЖ) может отрицательно повлиять на специфичность TST [1, 10, 11, 15–18]. Наконец, необходимость оценки туберкулинового ответа через 48–72 ч [2, 3, 19] может вызывать проблемы, особенно у малообеспеченного населения [20]. Из-за этих недостатков было разработано множество тестов для количественной оценки ответа на туберкулезные антигены [12, 15, 21–29].
QuantiFERON-TB (Cellestis) — это тест, помогающий выявить людей, инфицированных M. tuberculosis. Тест включает инкубацию в течение ночи цельной гепаринизированной крови со стимулирующими антигенами (отрицательный и положительный контроль, M. tuberculosis PPD и Mycobacterium avium PPD) с последующим анализом высвобождения интерферона-γ (IGRA) в надосадочной жидкости плазмы с помощью EIA. . В многочисленных исследованиях IGRA продемонстрировала чувствительность и специфичность, сопоставимую с TST по способности обнаруживать скрытые M.tuberculosis [12, 21–24]. Одним из преимуществ IGRA является то, что он устраняет необходимость повторного посещения для чтения теста. Еще одно преимущество состоит в том, что вакцина БЦЖ менее подвержена влиянию вакцины IGRA и обладает способностью распознавать ответы, вызванные нетуберкулезными микобактериями [12, 15, 24].
tuberculosis PPD и Mycobacterium avium PPD) с последующим анализом высвобождения интерферона-γ (IGRA) в надосадочной жидкости плазмы с помощью EIA. . В многочисленных исследованиях IGRA продемонстрировала чувствительность и специфичность, сопоставимую с TST по способности обнаруживать скрытые M.tuberculosis [12, 21–24]. Одним из преимуществ IGRA является то, что он устраняет необходимость повторного посещения для чтения теста. Еще одно преимущество состоит в том, что вакцина БЦЖ менее подвержена влиянию вакцины IGRA и обладает способностью распознавать ответы, вызванные нетуберкулезными микобактериями [12, 15, 24].
Поскольку ТКП остается экономически эффективным методом выявления лиц с латентной инфекцией M. tuberculosis , ее полное устранение невозможно. В настоящее время три ситуации, связанные с отсроченным считыванием TST (более 72 часов), остаются проблемными.Во-первых, есть люди, которые не возвращаются в течение 48-72 часов, но возвращаются позже, и обнаруживается, что у них нет результатов; от этих людей обычно требуется повторная ТКП. Некоторые данные предполагают, что нереактивное считывание TST в течение 7 дней после размещения, вероятно, даст истинно отрицательный результат [30, 31]. Во-вторых, есть люди, которые не возвращаются для чтения до истечения 72 часов и имеют реактивную ТКП; Считается, что эти люди имеют истинно положительные результаты без повторения ТКП [1–3].В-третьих, несколько человек с инертными результатами через 48–72 часа возвращаются со значительным уплотнением через 72–168 часов. Данных относительно значимости такого события немного, хотя рекомендуется рассматривать этих людей как имеющих положительную реакцию [32].
Некоторые данные предполагают, что нереактивное считывание TST в течение 7 дней после размещения, вероятно, даст истинно отрицательный результат [30, 31]. Во-вторых, есть люди, которые не возвращаются для чтения до истечения 72 часов и имеют реактивную ТКП; Считается, что эти люди имеют истинно положительные результаты без повторения ТКП [1–3].В-третьих, несколько человек с инертными результатами через 48–72 часа возвращаются со значительным уплотнением через 72–168 часов. Данных относительно значимости такого события немного, хотя рекомендуется рассматривать этих людей как имеющих положительную реакцию [32].
Нашей целью было, во-первых, определить надежность чтения TST через 72 часа. Кроме того, мы стремились определить надежность аплисола по сравнению с туберсолом по сравнению с IGRA на 2 разных временных интервалах. Наконец, мы хотели определить любые связанные с предметом переменные, которые могут способствовать несогласованности результатов теста.
Методы
Это исследование проводилось в Дейтонском медицинском центре по делам ветеранов при Медицинской школе государственного университета Райта (Дейтон, Огайо). Одобрение на исследование было получено от институционального наблюдательного совета Государственного университета Райта. Мы набрали 117 человек (50 мужчин и 67 женщин). Мы набрали субъектов, которые считались подверженными повышенному риску латентной инфекции M. tuberculosis (т. Е. Медицинских работников, лабораторный персонал, техников по уходу за пациентами, тех, кто родился в стране с высокой распространенностью туберкулеза, и другой вспомогательный персонал больниц). при контакте с пациентом).Участников исключали, если они были положительными на антитела к ВИЧ, были беременны, страдали злокачественными новообразованиями, имели в анамнезе тяжелую реакцию на ТКП (т. Е. Образование пузырей, рубцевание или анафилаксию) или принимали иммунодепрессанты.
Одобрение на исследование было получено от институционального наблюдательного совета Государственного университета Райта. Мы набрали 117 человек (50 мужчин и 67 женщин). Мы набрали субъектов, которые считались подверженными повышенному риску латентной инфекции M. tuberculosis (т. Е. Медицинских работников, лабораторный персонал, техников по уходу за пациентами, тех, кто родился в стране с высокой распространенностью туберкулеза, и другой вспомогательный персонал больниц). при контакте с пациентом).Участников исключали, если они были положительными на антитела к ВИЧ, были беременны, страдали злокачественными новообразованиями, имели в анамнезе тяжелую реакцию на ТКП (т. Е. Образование пузырей, рубцевание или анафилаксию) или принимали иммунодепрессанты.
После предоставления письменного информированного согласия участники исследования заполнили подробную анкету о факторах риска туберкулеза, включая недавний контакт с туберкулезом, предыдущие результаты TST, предыдущую вакцинацию БЦЖ и критерии исключения.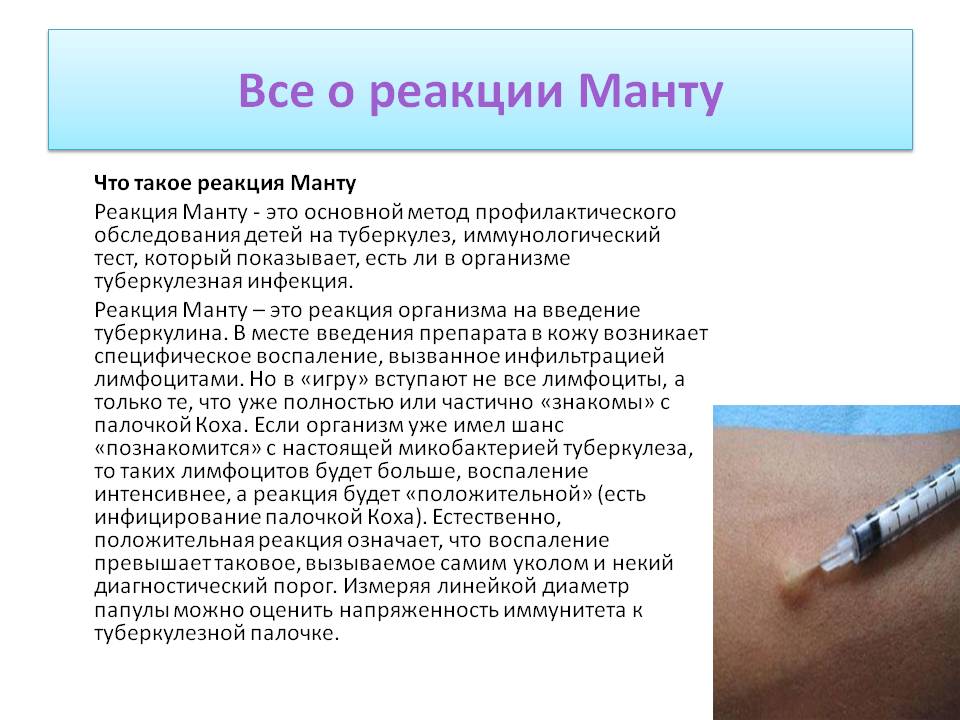 Также регистрировались возраст, место рождения и род занятий.
Также регистрировались возраст, место рождения и род занятий.
Перед введением TST согласившимся субъектам была проведена венепункция для IGRA. Использовали только отдельные партии аплисола и туберсола. Место инъекции каждого из 2 реагентов туберкулина — правое или левое предплечье — рандомизировалось путем подбрасывания монеты. Исследователь, интерпретирующий результаты, не знал, какой реагент использовался для каждого соответствующего предплечья. Поперечное уплотнение в каждом участке TST измеряли через 48–72 ч (день 2) после инъекции с использованием стратифицированной интерпретации уплотнения по риску, как рекомендовано Американским торакальным обществом / Центрами по контролю за заболеваниями [1].Субъекты были проинструктированы вернуться через 144–168 ч (день 7) после инъекции для второго чтения с использованием тех же рекомендаций. Положительная реакция TST определялась как уплотнение диаметром ≥10 мм. Для нашего населения с факторами риска туберкулеза условно положительный результат исследования IGRA считался положительной реакцией.
ИГРА был выполнен и интерпретирован в соответствии с инструкциями производителя [22, 23]. На основе предшествующих исследований положительный результат теста на инфекцию M. tuberculosis определяется процентным соотношением человеческого ответа (человеческий PPD-ответ, деленный на митогенный ответ)> 15% и процентной разницей между птицами (человеческий PPD-ответ минус птичий PPD-ответ. , деленное на человеческий PPD-ответ) -10% или более [21, 23].Кроме того, реактивность M. avium определялась как процентная реакция птиц (ответ PPD птиц, деленная на ответ митогена) ≥20% и процентная разница птиц -10% или меньше. Расчеты и интерпретация выполнялись с помощью калькулятора QuantiFERON-TB (версия 1.51; Cellestis).
Степень согласия между результатами TST и IGRA оценивалась с использованием коэффициентов κ. Значение κ> 0,75 представляет превосходное совпадение, не зависящее от случая, значение κ между .40 и.75 соответствует хорошему или хорошему согласию, а значение κ <0,40 представляет плохое совпадение вне шансов [33]. Тест Макнемара использовался, чтобы определить, различалась ли сила согласия между двумя временными точками. χ 2 критерий независимости и точный критерий Фишера использовались для анализа таблицы сопряженности.
Тест Макнемара использовался, чтобы определить, различалась ли сила согласия между двумя временными точками. χ 2 критерий независимости и точный критерий Фишера использовались для анализа таблицы сопряженности.
Результаты
Одна из 117 субъектов была исключена из анализа, потому что она не появлялась на контрольном приеме для показаний TST.Другой субъект получил второе чтение на 4-й день после инъекции (а не на 7-й день), но был включен в исследуемую группу. Остальные 116 участников состояли из лиц старше 18 лет (средний возраст 38 лет; диапазон 23–69 лет), включая 50 мужчин и 66 женщин. 35 человек родились в странах с высокой распространенностью туберкулеза (> 10 случаев на 100 000 населения) [2, 34] и 28 человек сообщили о получении вакцины БЦЖ (26 из которых родились в странах с высокой распространенностью туберкулеза).
Двадцать пять субъектов (22%), которые прошли ТКП с туберсолом, и 27 (23%), которые прошли тестирование с аплизолом, имели положительный результат на 2-й день. Общее согласие между туберсолом и аплизолом на 2-й день составило 93% (κ =. 80), а на 7-й день — 94% (κ = 0,76). Из 8 субъектов с несовместимыми показаниями между аплизолом и туберсолом TST на 2-й день результаты IGRA согласовывались с аплизолом и туберсолом по 4 раза каждый. Сравнение результатов дня 2 и 7 туберсола показано в таблице 1. Согласие между днем 2 и 7 для аплизола было 86% (κ =.56). Результаты IGRA показаны в сравнении с результатами Tubersol в таблицах 2 и 3. Общее согласие между IGRA и аплизолом на 2-й день составило 88% (κ = 0,67), а на 7-й день — 85% (κ = 0,54). У тринадцати субъектов (11%) были несогласованные показания туберсола между днем 2 и днем 7; из них результаты IGRA совпали с чтением 2-го дня по 8 предметам. У десяти субъектов была положительная реакция на 2-й день и отрицательная на 7-й день; из них результаты IGRA согласуются с чтением на второй день только для 5 предметов.
Общее согласие между туберсолом и аплизолом на 2-й день составило 93% (κ =. 80), а на 7-й день — 94% (κ = 0,76). Из 8 субъектов с несовместимыми показаниями между аплизолом и туберсолом TST на 2-й день результаты IGRA согласовывались с аплизолом и туберсолом по 4 раза каждый. Сравнение результатов дня 2 и 7 туберсола показано в таблице 1. Согласие между днем 2 и 7 для аплизола было 86% (κ =.56). Результаты IGRA показаны в сравнении с результатами Tubersol в таблицах 2 и 3. Общее согласие между IGRA и аплизолом на 2-й день составило 88% (κ = 0,67), а на 7-й день — 85% (κ = 0,54). У тринадцати субъектов (11%) были несогласованные показания туберсола между днем 2 и днем 7; из них результаты IGRA совпали с чтением 2-го дня по 8 предметам. У десяти субъектов была положительная реакция на 2-й день и отрицательная на 7-й день; из них результаты IGRA согласуются с чтением на второй день только для 5 предметов.
Таблица 1
Сравнение результатов туберкулиновой кожной пробы на туберкулиновый антиген через 48–72 ч (2-й день) и 144–168 ч (7-й день) после инъекции.
Таблица 1
Сравнение результатов туберкулиновой кожной пробы на туберкулиновый антиген туберсола через 48–72 ч (2-й день) и 144–168 ч (7-й день) после инъекции.
Таблица 2
Сравнение результатов анализа высвобождения интерферона-γ (IGRA) и туберкулиновой кожной пробы (TST) через 48–72 ч (день 2) и 144–168 ч (день 7) после инъекции.
Таблица 2
Сравнение результатов анализа высвобождения интерферона-γ (IGRA) и туберкулиновой кожной пробы (TST) на туберсоловый антиген через 48–72 ч (день 2) и 144–168 ч (день 7) после инъекции.
Таблица 3
Сравнение субъектов с положительными и отрицательными результатами анализа высвобождения гамма-интерферона (IGRA).
Таблица 3
Сравнение субъектов с положительными и отрицательными результатами анализа высвобождения интерферона-γ (IGRA).
Обсуждение
Основная цель этого исследования состояла в том, чтобы определить достоверность результатов TST, полученных на 7-й день после инъекции. Во-вторых, мы хотели определить, есть ли факторы, коррелирующие с другим показателем на 7-й день по сравнению со 2-м днем.Для удобства многие поставщики медицинских услуг приняли показания ТКП, полученные более чем через 72 часа после инъекции, как достоверную интерпретацию, не зная полностью о последствиях. К сожалению, отсутствие эталона в диагностике латентной инфекции M. tuberculosis затрудняет определение достоверности результатов ТКП, полученных на 7-й день. Общее согласие между результатами IGRA и TST, полученными на 2-й день, было хорошим. Mazurek et al. [12] обнаружили аналогичный уровень согласия в своем анализе лиц, подвергавшихся скринингу на скрытые M.tuberculosis (84,7%; κ = 0,55). Streeton et al. [21] обнаружили немного лучшее общее согласие (91%). Поскольку IGRA подтвердил надежность по сравнению с результатами TST, полученными на 2-й день, его использовали в качестве основы для сравнения результатов 2-го и 7-го дня. Хотя наблюдаемое значение κ в более позднее время немного ниже, чем в более раннее время, 95% доверительные интервалы существенно перекрываются.
Во-вторых, мы хотели определить, есть ли факторы, коррелирующие с другим показателем на 7-й день по сравнению со 2-м днем.Для удобства многие поставщики медицинских услуг приняли показания ТКП, полученные более чем через 72 часа после инъекции, как достоверную интерпретацию, не зная полностью о последствиях. К сожалению, отсутствие эталона в диагностике латентной инфекции M. tuberculosis затрудняет определение достоверности результатов ТКП, полученных на 7-й день. Общее согласие между результатами IGRA и TST, полученными на 2-й день, было хорошим. Mazurek et al. [12] обнаружили аналогичный уровень согласия в своем анализе лиц, подвергавшихся скринингу на скрытые M.tuberculosis (84,7%; κ = 0,55). Streeton et al. [21] обнаружили немного лучшее общее согласие (91%). Поскольку IGRA подтвердил надежность по сравнению с результатами TST, полученными на 2-й день, его использовали в качестве основы для сравнения результатов 2-го и 7-го дня. Хотя наблюдаемое значение κ в более позднее время немного ниже, чем в более раннее время, 95% доверительные интервалы существенно перекрываются. Таким образом, мы делаем вывод, что TST, который не считывается на 2-й день, все же может обеспечить надежное показание TST на 7-й день.В то же время, к показаниям TST на 7-й день следует относиться с осторожностью. Предыдущие исследования показали, что у некоторых людей без значительного уплотнения через 48–72 часа впоследствии развивается уплотнение, а у некоторых людей со значительным уплотнением через 48–72 часа уплотнение отсутствует через 7 дней после инъекции [31, 32]. Мы показали небольшое уменьшение уплотнения между 2-м и 7-м днем. Наблюдалась соответствующая тенденция к тому, что у большего числа испытуемых результаты менялись с положительных на отрицательные, чем с отрицательных на положительные.Несмотря на то, что большее количество субъектов продемонстрировало уменьшение уплотнения со 2-го по 7-й день, мы обнаружили небольшое количество испытуемых с изменением от отрицательного результата TST на 2-й день до положительного результата TST на 7-й день. Результаты IGRA были отрицательными в каждом из них.
Таким образом, мы делаем вывод, что TST, который не считывается на 2-й день, все же может обеспечить надежное показание TST на 7-й день.В то же время, к показаниям TST на 7-й день следует относиться с осторожностью. Предыдущие исследования показали, что у некоторых людей без значительного уплотнения через 48–72 часа впоследствии развивается уплотнение, а у некоторых людей со значительным уплотнением через 48–72 часа уплотнение отсутствует через 7 дней после инъекции [31, 32]. Мы показали небольшое уменьшение уплотнения между 2-м и 7-м днем. Наблюдалась соответствующая тенденция к тому, что у большего числа испытуемых результаты менялись с положительных на отрицательные, чем с отрицательных на положительные.Несмотря на то, что большее количество субъектов продемонстрировало уменьшение уплотнения со 2-го по 7-й день, мы обнаружили небольшое количество испытуемых с изменением от отрицательного результата TST на 2-й день до положительного результата TST на 7-й день. Результаты IGRA были отрицательными в каждом из них. Из этих случаев можно предположить, что это ложноположительные результаты TST на 7 день.
Из этих случаев можно предположить, что это ложноположительные результаты TST на 7 день.
Хотя не было достаточного количества субъектов с несогласованными показаниями между 2 и 7 днями, чтобы можно было провести многофакторный анализ, люди с историей вакцинации БЦЖ (или родившимися в страна с высокой распространенностью туберкулеза) имела высокую несогласованность между показаниями на 2-й и 7-й дни (таблица 4).Предыдущие исследования показали, что вакцинация БЦЖ [16, 35] или воздействие других микобактерий [14] могут повлиять на результаты ТКП. Mazurek et al. [12] предположили, что реактивность к нетуберкулезным микобактериям может быть причиной положительного результата ТКП у одной пятой субъектов, не вакцинированных БЦЖ. Джонсон и др. [15] показали, что вакцинация БЦЖ снижает специфичность TST и IGRA на основе PPD (QuantiFERON-TB), но что IGRA на основе 2 M. tuberculosis — специфических антигенов, ESAT-6 и MPT-64, не затрагивалась. вакцинацией БЦЖ.Этот более специфический анализ цельной крови сейчас коммерчески доступен под торговой маркой QuantiFERON-TB Gold [24], но он не был доступен нам, когда мы планировали текущее исследование.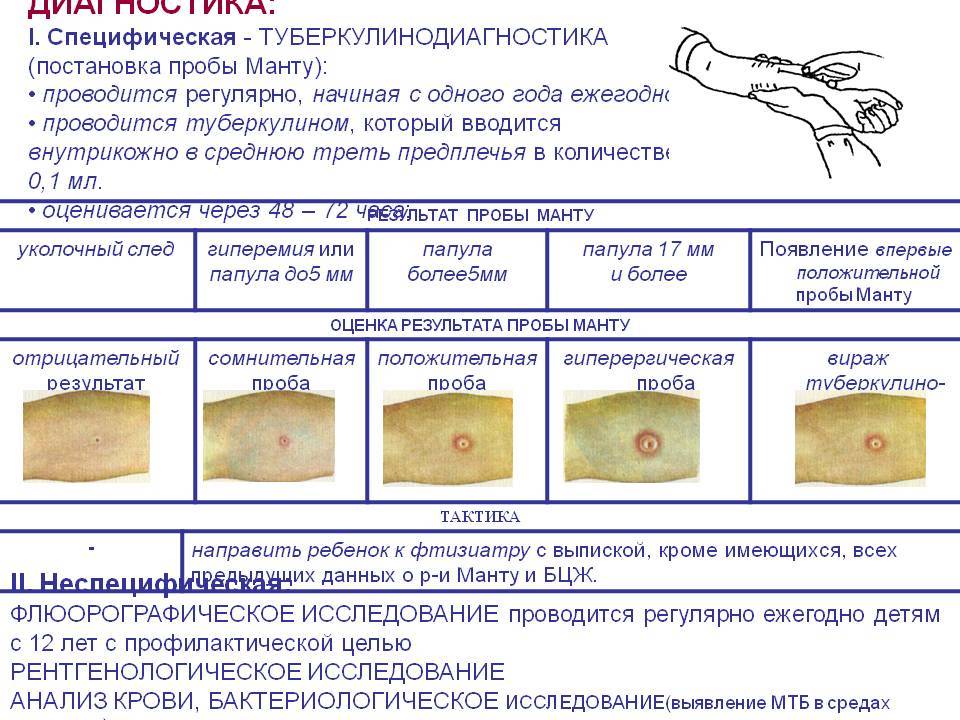
Таблица 4
Сравнение результатов туберкулиновой кожной пробы на туберкулиновый антиген через 48–72 ч (день 2) и 144–168 ч (день 7) после инъекции для субъектов с историей вакцинации против бациллы Кальметта-Герена.
Таблица 4
Сравнение результатов туберкулиновой кожной пробы на туберкулиновый антиген через 48–72 ч (2-й день) и 144–168 ч (7-й день) после инъекции для субъектов, имевших в анамнезе вакцинацию против бациллы Кальметта-Герена.
Некоторые предыдущие исследования показали противоречивые результаты при сравнении аплизола с туберсолом [36–38]. В частности, Grabau et al. [36] обнаружили 40% несоответствие, когда те, у кого были положительные результаты теста с аплизолом, были повторно протестированы с туберсолом. Это несоответствие может быть связано с разным положительным пороговым значением (≥5 мм) для реактивного результата ТКП, а также с различной консистенцией между партиями туберкулина. В настоящем исследовании было выявлено превосходное соответствие между результатами аплисола и туберсола как на 2-й, так и на 7-й день.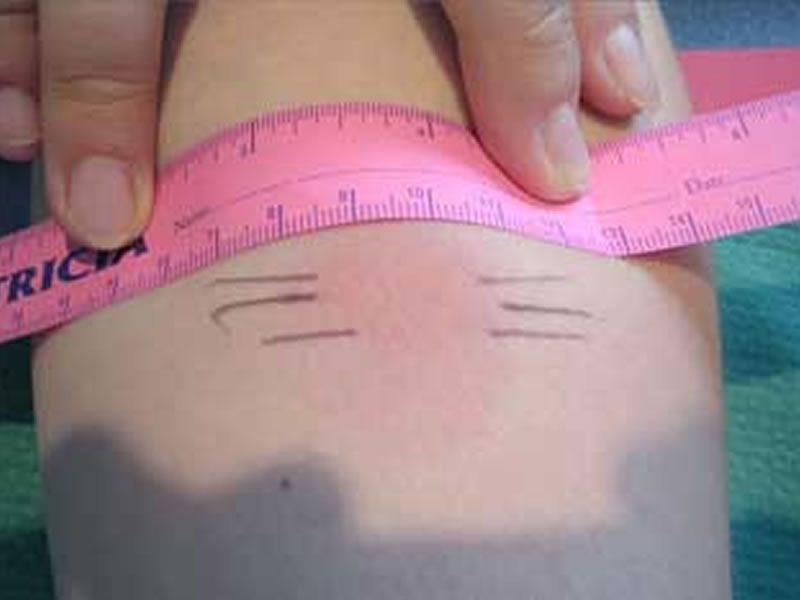 Villarino et al. [39] также обнаружили хорошее соответствие между аплизолом и туберсолом (оценочная специфичность 98,2% и 99,2% соответственно). Мы пришли к выводу, что наиболее противоречивые результаты, которые возникают между аплизолом и туберсолом, скорее всего, происходят случайно или в результате вариации партии.
Villarino et al. [39] также обнаружили хорошее соответствие между аплизолом и туберсолом (оценочная специфичность 98,2% и 99,2% соответственно). Мы пришли к выводу, что наиболее противоречивые результаты, которые возникают между аплизолом и туберсолом, скорее всего, происходят случайно или в результате вариации партии.
Поскольку не существует истинного эталона для выявления скрытой инфекции M. tuberculosis , трудно анализировать результаты IGRA и TST, которые отличаются друг от друга. Возникшие несоответствия могут быть результатом ограничений TST или ограничений IGRA.В настоящем исследовании люди, читающие реакции на ТКП, знали истории болезни пациентов и, возможно, были бессознательно склонны к положительному или отрицательному прочтению. Эти ограничения связаны с размещением и интерпретацией TST в клинических условиях.
Хотя некоторые предыдущие исследования показали несоответствие между результатами Аплизола и Туберсола, мы полагаем, что различия могут быть отнесены на счет случайности.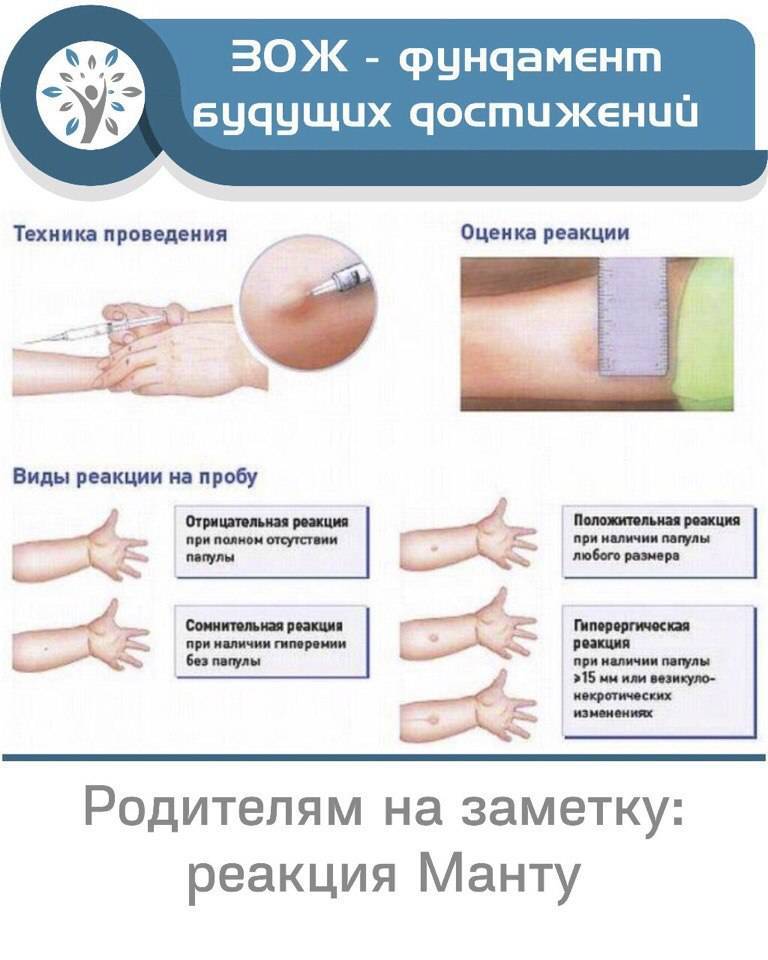 В этом исследовании интерпретация TST на 7-й день более надежна по сравнению с показаниями на 2-й день.Это касается как Аплизола, так и Туберсола. Клинически такая ситуация чаще всего возникает у людей, которые не возвращаются, чтобы пройти тест на анализ на 2-й день. Хотя в большинстве клинических ситуаций интерпретация TST надежна на 7-й день, интерпретация на 2-й день, несомненно, должна оставаться стандартом. Кроме того, интерпретация через более 72 часов после инъекции может быть менее надежной для людей, ранее получавших БЦЖ, чем для других. Однако для этих людей остается неопределенность в отношении интерпретации результатов TST, независимо от того, были ли они получены на 2-й или 7-й день.IGRA — это новый тест, который может разрешить эту неопределенность.
В этом исследовании интерпретация TST на 7-й день более надежна по сравнению с показаниями на 2-й день.Это касается как Аплизола, так и Туберсола. Клинически такая ситуация чаще всего возникает у людей, которые не возвращаются, чтобы пройти тест на анализ на 2-й день. Хотя в большинстве клинических ситуаций интерпретация TST надежна на 7-й день, интерпретация на 2-й день, несомненно, должна оставаться стандартом. Кроме того, интерпретация через более 72 часов после инъекции может быть менее надежной для людей, ранее получавших БЦЖ, чем для других. Однако для этих людей остается неопределенность в отношении интерпретации результатов TST, независимо от того, были ли они получены на 2-й или 7-й день.IGRA — это новый тест, который может разрешить эту неопределенность.
Благодарности
Мы благодарим Гарри Хамиса за помощь в проведении статистического анализа, Джека Бернштейна за предложения по планированию исследования и Сьюзан Марер за административную помощь в реализации этого проекта и обеспечении его бесперебойной работы.
Финансовая поддержка. Дейтонский региональный консорциум последипломного медицинского образования резидентский исследовательский и научный грант.
Возможный конфликт интересов. Все авторы: без конфликтов.
Список литературы
1Медицинское отделение Американского торакального общества Американской ассоциации легких
.Стандарты диагностики и классификация туберкулеза
,Am J Respir Crit Care Med
,2000
, vol.161
(стр.1376
—95
) 2Целевое туберкулиновое тестирование и лечение латентной туберкулезной инфекции
.Американское торакальное общество
,MMWR Recomm Rep
,2000
, vol.49
RR-6
(стр.1
—51
) 3,.Развитие и текущее использование туберкулинового теста
,Clin Infect Dis
,2002
, vol.34
(стр.365
—70
) 4,,,,,.
Нестабильность анергии кожной пробы гиперчувствительности замедленного типа при инфицировании вирусом иммунодефицита человека
,Arch Intern Med
,1995
, vol.155
(стр.2111
—7
) 5,,, et al.Стабильность положительных туберкулиновых проб: действительны ли усиленные реакции?
,Am Rev Respir Dis
,1991
, vol.144
(стр.560
—3
) 6,,,,.Конверсия и реверсия туберкулиновых реакций у жителей домов престарелых
,Am Rev Respir Dis
,1988
, vol.137
(стр.801
—4
) 7,,,.Исследование вариабельности чтения туберкулиновой пробы
,Am Rev Respir Dis
,1964
, vol.90
(стр.913
—9
) 8,,,,.Сравнение чувствительности к двум коммерчески доступным реактивам для туберкулиновых кожных тестов у лиц, недавно перенесших туберкулез
,Clin Infect Dis
,1997
, vol.25
(стр.661
—3
) 9,,.
Использование двойных кожных тестов для оценки туберкулиновых кожных тестовых реакторов от 10 до 14 мм у медицинских работников
,Infect Control Hosp Epidemiol
,2003
, vol.24
(стр.821
—4
) 10,,.Туберкулиновая кожная проба
,Clin Infect Dis
,1993
, vol.17
(стр.968
—75
) 11.Ложные результаты туберкулиновой пробы
,Chest
,1975
, vol.68
(стр.465
—9
) 12,,, et al.Сравнение анализа гамма-интерферона цельной крови с туберкулиновым кожным тестом для выявления скрытой инфекции Mycobacterium tuberculosis
,JAMA
,2001
, vol.286
(стр.1740
—7
) 13,,,,.Туберкулиновая проба. Вариабельность с процедурой Манту
,Am Rev Respir Dis
,1985
, vol.132
(стр.175
—7
) 14,,, et al.Паттерны и последствия естественного иммунного ответа на антигены микобактерий окружающей среды и туберкулеза в северной части Малави
,J Infect Dis
,2001
, vol.
184
(стр.322
—9
) 15« и др.Туберкулин — очищенное производное белка. MPT-64- и ESAT-6 — стимулировали ответы гамма-интерферона у студентов-медиков до и после вакцинации Mycobacterium bovis БЦЖ и у пациентов с туберкулезом
,Clin Diagn Lab Immunol
,1999
, vol.6
(стр.934
—7
) 16,,.Повышение чувствительности к туберкулину среди беженцев из Юго-Восточной Азии
,Am J Respir Crit Care Med
,1994
, vol.149
(стр.1597
—600
) 17« и др.Кинетика гиперчувствительности замедленного типа к туберкулину, вызванной вакцинацией бациллой Кальметта-Герена в северной части Малави
,J Infect Dis
,2002
, vol.186
(стр.807
—14
) 18,,, et al.Влияние вакцинации БЦЖ на реактивность туберкулина и бустерный эффект у сотрудников больниц
,Arch Intern Med
,2001
, vol.161
(стр.1760
—5
) 19.
Измерение отложенных откликов на кожные пробы
,N Engl J Med
,1975
, vol.293
(стр.501
—2
) 20,,,,.Влияние программы стимулирования и обучения на показатели возврата результатов теста PPD у пациентов с ВИЧ-инфекцией
,J Acquir Immune Defic Syndr Hum Retrovirol
,1996
, vol.11
(стр.455
—9
) 21,,.Чувствительность и специфичность анализа крови на гамма-интерферон на туберкулез
,Int J Tuberc Lung Dis
,1998
, vol.2
(стр.443
—50
) 22,.Разработка иммуноферментного анализа человеческого интерферона-γ и сравнение с туберкулиновым кожным тестом для выявления инфекции Mycobacterium tuberculosis
,Clin Diagn Lab Immunol
,1998
, vol.5
(стр.531
—6
) 23,,,.Оценка туберкулинового гамма-интерферона: возможность заменить кожную пробу Манту
,J Clin Microbiol
,1999
, vol.
37
(стр.3229
—32
) 24,,,,.Сравнение туберкулиновой кожной пробы и нового специфического анализа крови у больных туберкулезом
,Am J Respir Crit Care Med
,2004
, vol.170
(стр.65
—9
) 25,,, et al.Оценка анализа высвобождения гамма-интерферона из цельной крови для выявления инфекции Mycobacterium tuberculosis в 2 исследуемых популяциях
,Clin Infect Dis
,2002
, vol.34
(стр.1449
—56
) 26« и др.Оценка Вестерн-блоттинга как потенциального инструмента скрининга профессионального воздействия Mycobacterium tuberculosis у медицинских работников
,J Occup Environ Med
,2000
, vol.42
(стр.64
—8
) 27,.Рекомендации по использованию теста QuantiFERON-TB для диагностики скрытой инфекции Mycobacterium tuberculosis
,MMWR Recomm Rep
,2003
, vol.52
RR-2
(стр.
15
—8
) 28.Является ли анализ высвобождения гамма-интерферона in vitro адекватной заменой туберкулиновой кожной пробы?
,Clin Infect Dis
,2002
, т.34
(стр.1457
—9
) 29,,.Сравнение семи тестов для серологической диагностики туберкулеза
,J Clin Microbiol
,2000
, vol.38
(стр.2227
—31
) 30Бюро исследований туберкулеза Всемирной организации здравоохранения
.Величина туберкулиновой реакции за пять дней подряд
,Bull WHO
,1955
, vol.12
(стр.189
—96
) 31,,.Динамика и усиление туберкулиновых реакторов у жителей домов престарелых
,Am Rev Respir Dis
,1986
, vol.134
(стр.1048
—51
) 32,,,,,.Задержка туберкулиновой реактивности у лиц индокитайского происхождения: значение для профилактической терапии
,Ann Intern Med
,1996
, vol.124
(стр.
779
—84
) 33. ,,,.Измерение межэкспертного согласия
,Статистические методы для ставок и пропорций
,1981
Нью-Йорк
John Wiley & Sons
(стр.212
—36
) 34Всемирная организация здравоохранения
. ,Глобальная борьба с туберкулезом
35,.Влияние вакцинации против бацилл Кальметта-Герена на реактивность туберкулина
,Am Rev Respir Dis
,1992
, vol.145
(стр.621
—5
) 36,,,,.Ложноположительные кожные туберкулиновые пробы в государственной тюремной системе
,Int J Tuberc Lung Dis
,2003
, vol.7
(стр.93
—7
) 37,,,.Тестирование туберкулина в специализированной больнице: вариабельность продуктов
,Инфекционный контроль Hosp Epidemiol
,1994
, vol.15
(стр.758
—60
) 38,,,,,.Ложноположительные результаты туберкулиновой кожной пробы у медицинских работников [письмо]
,JAMA
,2000
, vol.
283
стр.2793
39« и др.Сравнимая специфичность 2 коммерческих туберкулиновых реагентов у лиц с низким риском туберкулезной инфекции
,JAMA
,1999
, vol.281
(стр.169
—71
)© 2005 Американского общества инфекционистов
Туберкулин (внутрикожное введение) Описание и торговые марки
Описание и торговые марки
Информация о лекарствах предоставлена: IBM Micromedex
Торговая марка в США
- Аплисол
- Туберсол
Описания
Очищенное производное туберкулина (PPD) используется в кожных пробах для диагностики туберкулеза (ТБ) у лиц с повышенным риском развития активного заболевания.
Туберкулиновая кожная проба проводится путем инъекции туберкулина PPD в поверхностный слой кожи. Если тест положительный, будет наблюдаться реакция в месте инъекции или прокола и вокруг него. Если тест проводится с помощью инъекции, эта реакция обычно представляет собой твердую приподнятую область с четкими границами. Если тест проводится с использованием устройств для прокола, реакция обычно проявляется в виде опухшего участка в месте прокола. Размер реакции измеряется и записывается, а результаты теста изучаются через 48-72 часа.
Если тест проводится с использованием устройств для прокола, реакция обычно проявляется в виде опухшего участка в месте прокола. Размер реакции измеряется и записывается, а результаты теста изучаются через 48-72 часа.
Это лекарство следует давать только врачом или под его наблюдением.
Этот продукт доступен в следующих лекарственных формах:
Получите самую свежую информацию о здоровье от экспертов клиники Мэйо.
Зарегистрируйтесь бесплатно и будьте в курсе достижений в области исследований, советов по здоровью и актуальных тем, связанных со здоровьем, таких как COVID-19, а также опыта в области управления здоровьем.
Узнайте больше об использовании данных Mayo Clinic.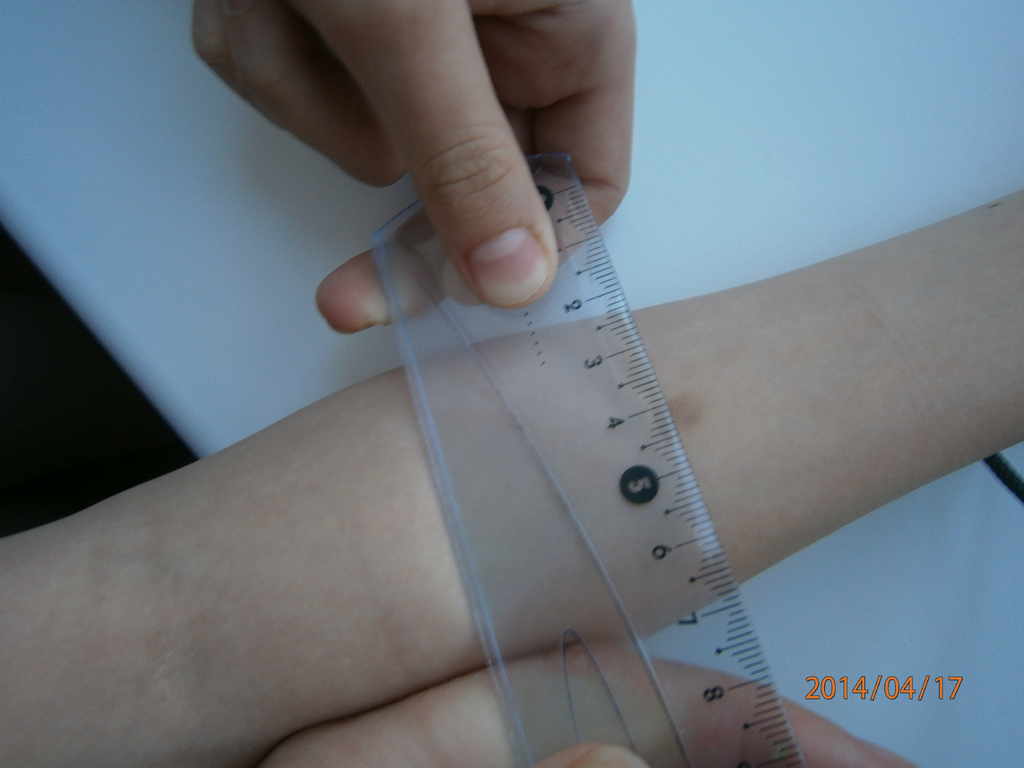
Чтобы предоставить вам наиболее актуальную и полезную информацию и понять, какие информация полезна, мы можем объединить вашу электронную почту и информацию об использовании веб-сайта с другая имеющаяся у нас информация о вас. Если вы пациент клиники Мэйо, это может включать защищенную медицинскую информацию.Если мы объединим эту информацию с вашими защищенными информация о здоровье, мы будем рассматривать всю эту информацию как защищенную информацию и будет использовать или раскрывать эту информацию только в соответствии с нашим уведомлением о политика конфиденциальности. Вы можете отказаться от рассылки по электронной почте в любое время, нажав на ссылку для отказа от подписки в электронном письме.
Подписаться!
Спасибо за подписку
Наш электронный информационный бюллетень Housecall будет держать вас в курсе самой последней информации о здоровье.
Извините, что-то пошло не так с вашей подпиской
Повторите попытку через пару минут
Повторить
Последнее обновление частей этого документа: фев.01, 2021
Авторские права © IBM Watson Health, 2022 г. Все права защищены. Информация предназначена только для использования Конечным пользователем и не может быть продана, распространена или иным образом использована в коммерческих целях.
.
Тестирование на туберкулиновую кожу с помощью инжекторав сравнении с методом Манту в JSTOR
Абстрактный На выборке из 48 учеников младших классов средней школы было проведено исследование надежности введенного из струйного пистолета туберкулина PPD-S в отношении реакции 5 мм.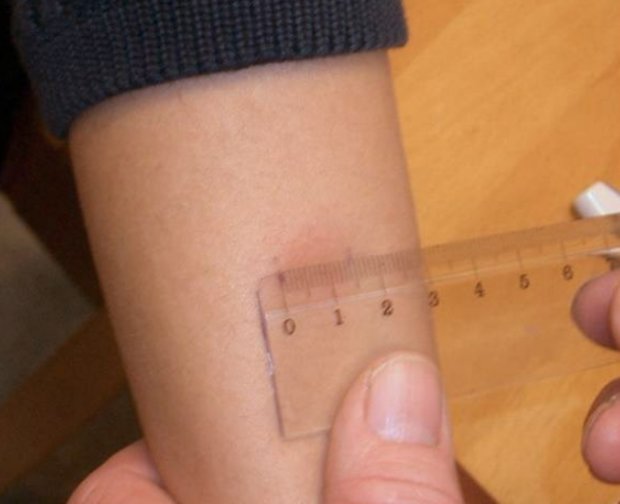 или более по сравнению с туберкулином PPD-S, вводимым шприцем и иглой. Дозировка туберкулина, введенного струей, была стандартизирована для исследования, так что каждый тест с введенным струей туберкулина вызывал внутрикожный волдырь, сравнимый с образованием волдырей, вызванных шприцем и иглой. Выяснилось, что при установке дозировки 0,14 мл. туберкулина при каждом пуске, струйный пистолет, использованный в исследовании, вызывал внутрикожные волдыри, сравнимые с таковыми при инъекции шприцом и иглой 0,1 мл. туберкулина (проба Манту).За некоторыми исключениями, струйный инжекторный пистолет создавал внутрикожные волдыри, которые были более четко очерченными, бледными и стойкими, чем те, которые были получены с помощью шприца и иглы. Принятие студентами было особенно хорошим. Результаты исследования показали, что реакции 5 мм. или более, введенный в струйный пистолет туберкулин PPD-S оказался ненадежным по сравнению с реакциями шприца и иглы (Манту). Шесть из 11 студентов с реакцией форсунки от 5 до 9 мм.
или более по сравнению с туберкулином PPD-S, вводимым шприцем и иглой. Дозировка туберкулина, введенного струей, была стандартизирована для исследования, так что каждый тест с введенным струей туберкулина вызывал внутрикожный волдырь, сравнимый с образованием волдырей, вызванных шприцем и иглой. Выяснилось, что при установке дозировки 0,14 мл. туберкулина при каждом пуске, струйный пистолет, использованный в исследовании, вызывал внутрикожные волдыри, сравнимые с таковыми при инъекции шприцом и иглой 0,1 мл. туберкулина (проба Манту).За некоторыми исключениями, струйный инжекторный пистолет создавал внутрикожные волдыри, которые были более четко очерченными, бледными и стойкими, чем те, которые были получены с помощью шприца и иглы. Принятие студентами было особенно хорошим. Результаты исследования показали, что реакции 5 мм. или более, введенный в струйный пистолет туберкулин PPD-S оказался ненадежным по сравнению с реакциями шприца и иглы (Манту). Шесть из 11 студентов с реакцией форсунки от 5 до 9 мм.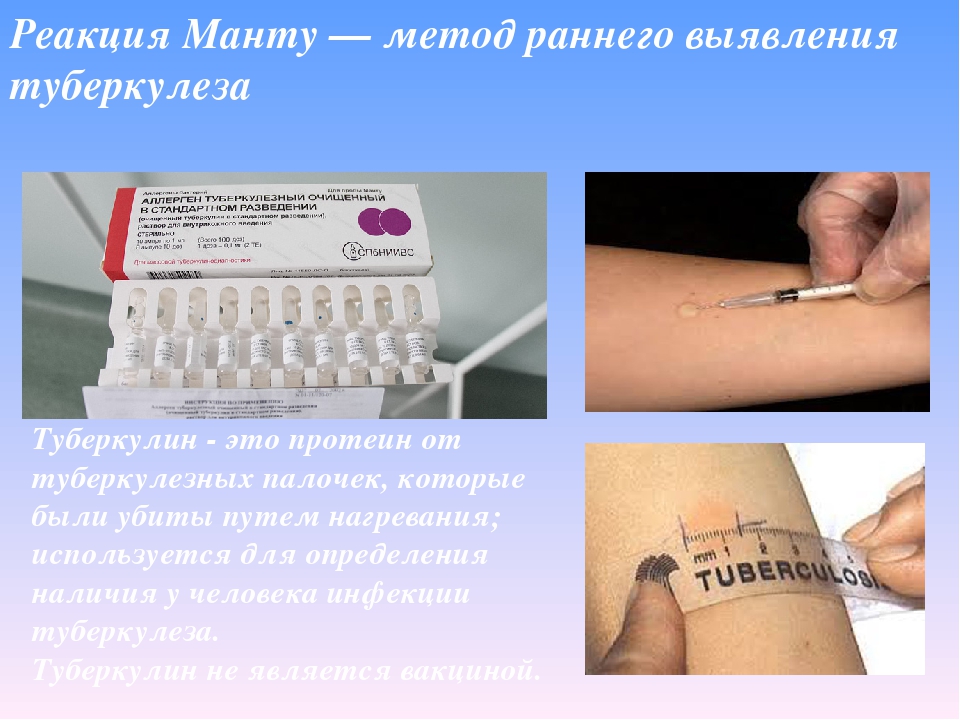 имели положительную пробу Манту (уплотнения 10 мм.или больше). Однако был только один ложноположительный туберкулиновый тест. Из 37 студентов с реакцией форсунки 10 мм. или более, 36 также имели реакцию шприца и иглы (Манту) 10 мм. или больше. Положительные реакции (уплотнения 10 мм и более) на введенный из струйного пистолета туберкулин были надежными по сравнению с положительными реакциями на введенный шприцем и иглой туберкулин.
имели положительную пробу Манту (уплотнения 10 мм.или больше). Однако был только один ложноположительный туберкулиновый тест. Из 37 студентов с реакцией форсунки 10 мм. или более, 36 также имели реакцию шприца и иглы (Манту) 10 мм. или больше. Положительные реакции (уплотнения 10 мм и более) на введенный из струйного пистолета туберкулин были надежными по сравнению с положительными реакциями на введенный шприцем и иглой туберкулин.
Сара Миллер МакКьюн основала SAGE Publishing в 1965 году для поддержки распространения полезных знаний и просвещения мирового сообщества.SAGE — ведущий международный поставщик инновационного высококачественного контента, ежегодно публикующий более 900 журналов и более 800 новых книг по широкому кругу предметных областей. Растущий выбор библиотечных продуктов включает архивы, данные, тематические исследования и видео. Контрольный пакет акций SAGE по-прежнему принадлежит нашему основателю, и после ее жизни она перейдет в собственность благотворительного фонда, который обеспечит дальнейшую независимость компании. Основные офисы расположены в Лос-Анджелесе, Лондоне, Нью-Дели, Сингапуре, Вашингтоне и Мельбурне.www.sagepublishing.com
Основные офисы расположены в Лос-Анджелесе, Лондоне, Нью-Дели, Сингапуре, Вашингтоне и Мельбурне.www.sagepublishing.com
Каким образом проводится туберкулиновая кожная проба Манту с очищенным производным белка (PPD) у пациентов с подозрением на туберкулез (ТБ)?
Автор
Томас Э. Херклайн, доктор медицины Профессор медицины, Государственный университет Райта, Медицинская школа Буншофт; Медицинский консультант, Общественное здравоохранение, Туберкулезная клиника округа Дейтон и Монтгомери (Огайо)
Томас Э. Херклайн, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha, Американского общества инфекционных болезней, Общества инфекционных болезней Огайо
Раскрытие информации: Нечего раскрывать.
Соавтор (ы)
Джудит К. Амороса, доктор медицины, FACR Клинический профессор радиологии и заместитель председателя по развитию профессорско-преподавательского состава и медицинского образования, Медицинская школа Рутгерса Роберта Вуда Джонсона
Джудит К. Амороса, доктор медицины, FACR является членом следующих медицинских обществ: Американский колледж радиологии, Американское общество рентгеновских лучей, Ассоциация университетских радиологов, Радиологическое общество Северной Америки, Общество торакальной радиологии
Амороса, доктор медицины, FACR является членом следующих медицинских обществ: Американский колледж радиологии, Американское общество рентгеновских лучей, Ассоциация университетских радиологов, Радиологическое общество Северной Америки, Общество торакальной радиологии
Раскрытие: Ничего не разглашать.
Главный редактор
Майкл Стюарт Бронз, доктор медицины Дэвид Росс Бойд Профессор и председатель медицинского факультета, кафедра внутренней медицины, кафедра медицины, Научный центр здравоохранения Университета Оклахомы; Магистр Американского колледжа врачей; Научный сотрудник Американского общества инфекционных болезней; Член Королевского колледжа врачей, Лондон
Майкл Стюарт Бронз, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha, Американский колледж врачей, Американская медицинская ассоциация, Ассоциация профессоров медицины, Общество инфекционных болезней Америки, Государственная медицинская ассоциация Оклахомы, Южное общество клинических исследований
Раскрытие информации: нечего раскрывать.
Благодарности
Эрика Банг Медицинский центр государственного университета Нью-Йорка Медицинский центр Колледж
Раскрытие: Ничего не раскрывать.
Диана Брейнард, MD Консультант, Отделение инфекционных заболеваний, Массачусетская больница общего профиля
Раскрытие: Ничего не раскрывать.
Памела С. Чавис, доктор медицины Профессор кафедры офтальмологии и неврологии Медицинского университета Южной Каролины, Медицинский колледж
Памела С. Чавис, доктор медицины, является членом следующих медицинских обществ: Американской академии неврологии, Американской академии офтальмологии и Североамериканского общества нейроофтальмологов
webmd.com»> Раскрытие: Ничего не раскрывать.Дирк М. Элстон, доктор медицины Директор, Академия дерматопатологии Акермана, Нью-Йорк
Дирк М. Элстон, доктор медицины, является членом следующих медицинских обществ: Американская академия дерматологии
Раскрытие: Ничего не раскрывать.
Теодор Дж. Гаэта, DO, MPH, FACEP Доцент кафедры неотложной медицины, Медицинский колледж Вейл Корнелл; Заместитель председателя и программный директор резидентуры по неотложной медицине, Департамент неотложной медицины, Методистская больница Нью-Йорка; Научный руководитель, адъюнкт-профессор кафедры неотложной медицины, медицинский факультет Университета Святого Георгия
Теодор Дж. Гаэта, DO, MPH, FACEP является членом следующих медицинских обществ: Альянса клинического образования, Американского колледжа врачей неотложной помощи, руководителей отделов неотложной медицины, Совета директоров резиденций неотложной медицины, Нью-Йоркской медицинской академии и Общество академической неотложной медицины
webmd.com»> Раскрытие: Ничего не раскрывать.Аарон Глатт, доктор медицины Профессор клинической медицины Нью-Йоркского медицинского колледжа; Президент и генеральный директор, бывший главный врач отделения медицины и инфекционных заболеваний больницы Святого Иосифа (ранее — больница Нью-Айленд)
Аарон Глатт, доктор медицины, является членом следующих медицинских обществ: Американского колледжа грудных врачей, Американского колледжа врачей, Американского колледжа врачей, Американского колледжа врачей-Американского общества внутренней медицины, Американской медицинской ассоциации, Американского общества микробиологов. , Американское торакальное общество, Американская ассоциация венерических заболеваний, Американское общество инфекционных болезней, Международное общество по СПИДу и Общество здравоохранения и эпидемиологии Америки
com»> Раскрытие: Ничего не раскрывать.Саймон К. Лоу, доктор медицины, фармацевт Клинический профессор медицинских наук, кафедра офтальмологии, Глазной институт Жюля Стейна, Калифорнийский университет, Лос-Анджелес, медицинская школа Дэвида Геффена
Саймон К. Лоу, доктор медицинских наук, фармацевт является членом следующих медицинских обществ: Американской академии офтальмологии, Американского общества глаукомы и Ассоциации исследований в области зрения и офтальмологии
Раскрытие: Ничего не раскрывать.
Джон М. Лидом, доктор медицины Почетный профессор медицины Медицинской школы им. Кека Университета Южной Калифорнии
Джон М. Лидом, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha, Американский колледж врачей — Американское общество внутренней медицины, Американское общество микробиологии, Американское общество инфекционных болезней, Международное общество по СПИДу и Phi Beta Kappa
.
Раскрытие: Ничего не раскрывать.
Джеймс Ли, доктор медицины Бывший доцент отделения неотложной медицины Гарвардской медицинской школы; Совет директоров Remote Medicine
Раскрытие: Ничего не раскрывать.
Джеффри Мефферт, доктор медицины Ассистент клинического профессора дерматологии, Школа медицины Техасского университета в Сан-Антонио
Джеффри Мефферт, доктор медицины, является членом следующих медицинских обществ: Американской академии дерматологии, Американской медицинской ассоциации, Ассоциации военных дерматологов и Техасского дерматологического общества
Раскрытие: Ничего не раскрывать.
Монте С. Мельцер, доктор медицины , начальник дерматологической службы, госпиталь Юнион Мемориал
Мельцер, доктор медицины , начальник дерматологической службы, госпиталь Юнион Мемориал
Монте С. Мельцер, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha и Американской академии дерматологии
Раскрытие: Ничего не раскрывать.
Susannah K Mistr, MD Врач-резидент, отделение офтальмологии, Медицинский центр Университета Мэриленда
Сюзанна К. Мистр, доктор медицины, является членом следующих медицинских обществ: Американской академии офтальмологии, Американского колледжа хирургов, Американской медицинской ассоциации, Американской ассоциации студентов-медиков / фонда, Американского общества катарактальной и рефракционной хирургии и Медицинской ассоциации Южной Каролины
. Раскрытие: Ничего не раскрывать.
Кэрол Э. Нейси, доктор философии Адъюнкт-профессор, факультет биологии, Католический университет Америки; Адъюнкт-профессор кафедры тропической медицины и микробиологии, Университет Джорджа Вашингтона
Кэрол Нейси, доктор философии, является членом следующих медицинских обществ: Американской академии микробиологии и Американского общества микробиологии
Раскрытие информации: Sequella, Inc. Доля собственности Занятость; Sequella, Inc. Инвестор долей владения
Джей Джеймс Роузи, доктор медицины Бывший директор службы роговицы, Институт катаракты и лазера Св. Луки
Джеймс Роуси, доктор медицины, является членом следующих медицинских обществ: Американской академии офтальмологии, Американской ассоциации развития науки, Американской медицинской ассоциации, Ассоциации исследований в области зрения и офтальмологии, Флоридской медицинской ассоциации, Панамериканской ассоциации офтальмологов. , Sigma Xi и Южная медицинская ассоциация
, Sigma Xi и Южная медицинская ассоциация
Раскрытие: Ничего не раскрывать.
Hampton Roy Sr, MD Доцент кафедры офтальмологии Медицинского университета Арканзаса
Хэмптон Рой-старший, доктор медицины, является членом следующих медицинских обществ: Американской академии офтальмологии, Американского колледжа хирургов и Панамериканской ассоциации офтальмологов
Раскрытие: Ничего не раскрывать.
Джон Д. Шеппард-младший, доктор медицины, MMSc Профессор офтальмологии, микробиологии и молекулярной биологии, клинический директор, Центр глазной фармакологии Томаса Р. Ли, директор исследовательской программы ординатуры офтальмологии Медицинской школы Восточной Вирджинии; Президент, Virginia Eye Consultants
webmd.com»> Джон Д. Шеппард-младший, доктор медицины, MMSc является членом следующих медицинских обществ: Американской академии офтальмологии, Американского общества микробиологов, Американского общества катарактальной и рефракционной хирургии, Американского общества увеитов и Ассоциации исследований в области зрения и офтальмологииРаскрытие: Ничего не раскрывать.
Ричард Х. Синерт, DO Профессор неотложной медицины, клинический доцент медицины, директор по исследованиям Медицинского колледжа Государственного университета Нью-Йорка; Консультанты, отделение неотложной медицины, госпиталь округа Кингс
Ричард Х. Синерт, доктор медицинских наук, является членом следующих медицинских обществ: Американского колледжа врачей и Общества академической неотложной медицины
Раскрытие: Ничего не раскрывать.
Франсиско Талавера, фармацевт, доктор философии Адъюнкт-профессор, Фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие информации: Medscape Salary Employment
Кейт Цанг, врач-резидент , клинический ассистент инструктора, отделение неотложной медицины, Государственный университет Нью-Йорка, нижний штат Нью-Йорк, больница округа Кингс
Кейт Цанг, доктор медицины, является членом следующих медицинских обществ: Американского колледжа врачей неотложной помощи, Ассоциации резидентов неотложной медицинской помощи и Общества академической неотложной медицины
Раскрытие: Ничего не раскрывать.
Шьям Верма, MBBS, DVD, FAAD Доцент кафедры дерматологии Университета Вирджинии; Адъюнкт-профессор кафедры дерматологии Государственного университета Нью-Йорка в Стоунибруке, адъюнкт-профессор кафедры дерматологии Пенсильванского университета
webmd.com»> Шьям Верма, MBBS, DVD, FAAD является членом следующих медицинских обществ: Американская академия дерматологииРаскрытие: Ничего не раскрывать.
Ричард П. Винсон, доктор медицины Ассистент клинического профессора, кафедра дерматологии, Центр медицинских наук Техасского технического университета, Медицинская школа Пола Л. Фостера; Консультант, Дерматология Маунтин-Вью, PA
Ричард П. Винсон, доктор медицины, является членом следующих медицинских обществ: Американской академии дерматологии, Ассоциации военных дерматологов, Техасского дерматологического общества и Техасской медицинской ассоциации
.Раскрытие: Ничего не раскрывать.
Эрик Л. Вайс, MD, DTM & H Медицинский директор, Управление непрерывности обслуживания и планирования действий в случае бедствий, директор по стипендии, Стипендия по медицине катастроф Медицинского центра Стэнфордского университета, председатель SUMC и LPCH Целевая группа по биотерроризму и готовности к чрезвычайным ситуациям, младший клинический исследователь, Департамент Хирургия (неотложная медицина), Медицинский центр Стэнфордского университета
webmd.com»> Eric L Weiss, MD, DTM & H является членом следующих медицинских обществ: Американский колледж врачей скорой помощи, Американский колледж медицины труда и окружающей среды, Американская медицинская ассоциация, Американское общество тропической медицины и гигиены, Врачи за социальную ответственность, Southeastern Surgical Конгресс, Южная ассоциация онкологии, Южное клиническое неврологическое общество и Общество дикой медициныРаскрытие: Ничего не раскрывать.
Сравнение тестов высвобождения гамма-интерферона с туберкулиновой кожной пробой для выявления латентной туберкулезной инфекции, которая прогрессирует в активный туберкулез: систематический обзор и метаанализ | BMC Infectious Diseases
Процесс идентификации исследования
Из 7 611 идентифицированных записей 515 были отобраны для полнотекстового исследования. Из них 498 записей были исключены. Остальные 17 публикаций вошли в обзор [11–27]. На рис.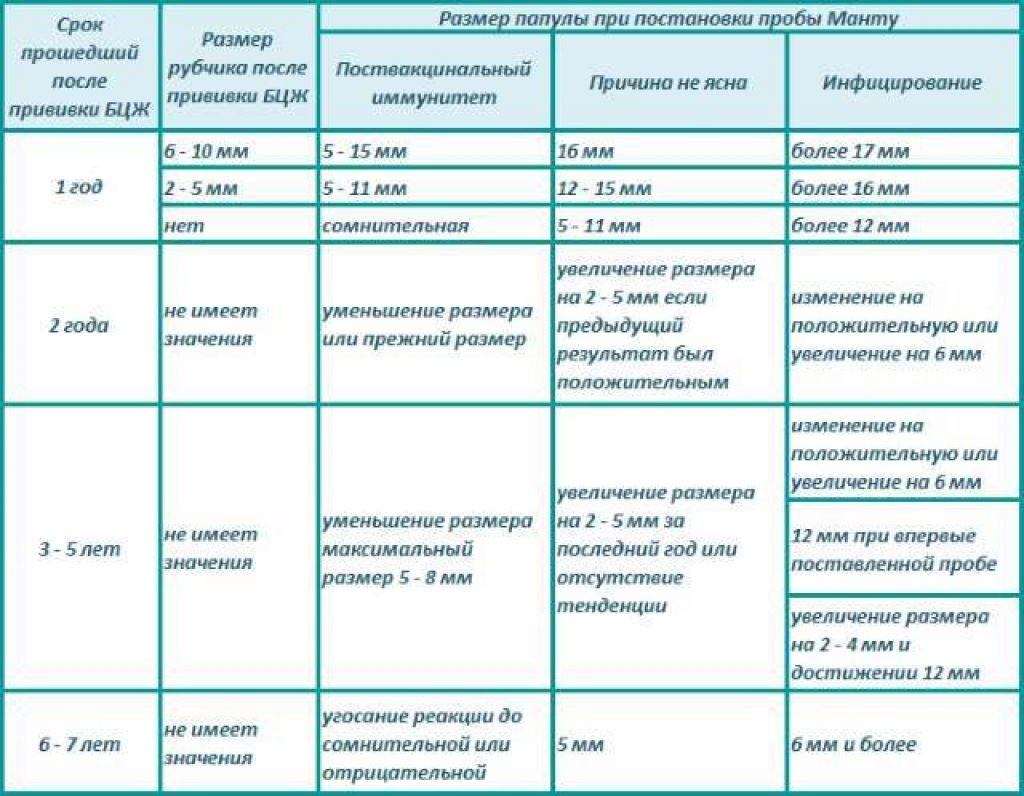 1 показан процесс исследования с причинами исключения, изображенными на блок-схеме PRISMA [28].
1 показан процесс исследования с причинами исключения, изображенными на блок-схеме PRISMA [28].
Характеристики включенных исследований
Из 17 включенных исследований пять были проведены на детях [11, 13–16], 10 — на лицах с ослабленным иммунитетом [12, 17–25] и два исследования [26, 27] были проведены на людях. недавно прибыл из стран с высокой заболеваемостью туберкулезом. Большинство из них были проспективными когортными исследованиями, хотя два [12, 18] (оба с участием людей с ослабленным иммунитетом) были ретроспективными когортами. Более подробная информация об исходных характеристиках включенных исследований представлена в таблице 1.
Таблица 1 Характеристики исследований с участием детей с ослабленным иммунитетом и недавно прибывших иммигрантов из стран с высокой заболеваемостью ТБДети
Пять исследований были проведены в Германии [11], Турции [14], Иране [15], Южной Африке [13] и Южной Корее [16].
Три исследования [11, 13, 16] сравнивали QFT-GIT с TST (5 мм / 10 мм). В одном исследовании [15] QFT-G сравнивался с TST (10 мм). По данным трех исследований, распространенность вакцинации БЦЖ колеблется от 36 до 94% [11, 13, 16].Средняя продолжительность наблюдения за диагнозом активного ТБ варьировала от 1 года [15] до 4 лет [11, 13]. В трех исследованиях [11, 13, 15] четко указаны методы, используемые для диагностики туберкулеза.
Люди с ослабленным иммунитетом
Шесть из 10 исследований были проведены в Южной Корее и Тайване [17–19, 21–23], по одному в Иране [25], Швейцарии [12] и Дании [20], а оставшееся исследование в разных странах Европы [24].
В двух исследованиях участники получали гемодиализ по поводу терминальной стадии почечной недостаточности (ТПН) [19, 25].Два других исследования включали кандидатов на трансплантацию гемопоэтических стволовых клеток [21] и реципиентов трансплантации гемопоэтических стволовых клеток [22]. Остальные шесть исследований включали людей с «ревматическим заболеванием» [18], людей, перенесших трансплантацию почки [17], людей, живущих с вирусом иммунодефицита человека (ЛЖВ) [12], людей, проходящих лечение от воспалительного артрита [23], людей, живущих с лечились от саркоидоза [20], а также участники с различными состояниями и заболеваниями (ЛЖВ, хроническая почечная недостаточность, ревматоидный артрит, трансплантация твердых органов или трансплантация стволовых клеток) [24].
В четырех исследованиях сравнивали T-SPOT.TB с TST (5 мм / 10 мм) [12, 17, 19, 25], в двух исследованиях QFT-G с TST (10 мм) [19] или TST (6 мм / 12 мм). мм) [20], четыре исследования сравнивали QFT-GIT либо с TST (5 мм) [18, 21], либо с TST 10 мм / 15 мм [22, 23]. В исследовании, проведенном Sester и соавторами [24], сравнивались три теста (TST, измеренный на 5 мм, QFT-GIT и T-SPOT.TB). Средняя продолжительность наблюдения в исследованиях варьировала от 1,2 до 5 лет. В семи исследованиях [17–20, 22–24] описаны методы диагностики ТБ.
Люди, недавно прибывшие из стран с высокой заболеваемостью ТБ
Мы выявили только два исследования [26, 27], проведенных с участием людей, недавно прибывших из стран с высокой заболеваемостью ТБ.Эти исследования проводились в Норвегии [26] и Нидерландах [27]. Harstad et al. исследование [26] включало взрослых просителей убежища, а Kik et al. [27] изучают взрослых, недавно перенесших инфекционный туберкулез легких. Большинство участников обоих исследований прибыли из Европы, Африки и Азии. В исследованиях сравнивали QFT-GIT с TST (≥6 мм и ≥15 мм) [26] и QFT-GIT / T-SPOT.TB с TST (≥10 мм и ≥ 15 мм) [27]. О распространенности вакцинации БЦЖ сообщалось только в одном из исследований — 81% [27].Средняя продолжительность наблюдения составила от 2 лет [27] до 3 лет [26]. Только одно исследование предоставило достаточную информацию о методах, используемых для диагностики ТБ, включая рентгенографию грудной клетки, симптомы, результаты мазка и / или посева [27].
В исследованиях сравнивали QFT-GIT с TST (≥6 мм и ≥15 мм) [26] и QFT-GIT / T-SPOT.TB с TST (≥10 мм и ≥ 15 мм) [27]. О распространенности вакцинации БЦЖ сообщалось только в одном из исследований — 81% [27].Средняя продолжительность наблюдения составила от 2 лет [27] до 3 лет [26]. Только одно исследование предоставило достаточную информацию о методах, используемых для диагностики ТБ, включая рентгенографию грудной клетки, симптомы, результаты мазка и / или посева [27].
Оценка риска систематической ошибки
Риск систематической ошибки по областям и в целом представлен в таблице 2. У детей два исследования [14, 15] имели высокий риск, а остальные три исследования — умеренный риск систематической ошибки [11, 13, 16]. В большинстве исследований был умеренный риск систематической ошибки для неправильной классификации людей в отношении построения групп валидности, поскольку не было предоставлено четких определений и методов установления [11, 13, 15].Три исследования с участием людей с ослабленным иммунитетом имели общий высокий [12, 19, 25], а еще три — умеренный риск систематической ошибки [21, 22, 24]. В остальных четырех исследованиях общий риск систематической ошибки был низким [17, 18, 20, 23]. В пяти исследованиях [12, 19, 21, 22, 25] был умеренный / высокий риск систематической ошибки в отношении пунктов участия в исследовании, измерения результатов и искажения результатов исследования.
В остальных четырех исследованиях общий риск систематической ошибки был низким [17, 18, 20, 23]. В пяти исследованиях [12, 19, 21, 22, 25] был умеренный / высокий риск систематической ошибки в отношении пунктов участия в исследовании, измерения результатов и искажения результатов исследования.
Из двух исследований, в которых недавно приехали люди из стран с высоким бременем ТБ, одно исследование имело высокий общий риск систематической ошибки [26], а другое — низкий риск систематической ошибки [27].В исследовании Harstad [26] высокий риск систематической ошибки был отмечен в большинстве областей систематической ошибки (например, участие в исследовании, измерение прогностических факторов, искажение результатов исследования, статистический анализ и области отчетности).
Заболеваемость активным ТБ после тестирования на ЛТБИ по интересующим подгруппам
Подробная информация о заболеваемости активным ТБ по результатам теста на ЛТБИ представлена для интересующих подгрупп в Таблице 3. Оба теста IGRA и TST (5 мм) были значительно эффективны. в исследованиях по выявлению ЛТИ у детей и людей с ослабленным иммунитетом.Среди людей с ослабленным иммунитетом и недавно прибывших из стран с высокой заболеваемостью результаты не были статистически значимыми для TST (10 мм) в прогнозировании прогрессирования до активной формы ТБ. Среди недавних пациентов результаты теста T-SPOT.TB также не были статистически значимо связаны с прогрессированием в активный туберкулез.
Таблица 3 Прогрессирование до ТБ после тестирования на ЛТБИ с помощью IGRA и TST у детей, с ослабленным иммунитетом и недавно прибывших иммигрантовДети
QFT-GIT
Пятьдесят шесть из 3007 (1.86%) QFT-GIT-положительные дети (4 исследования [11, 13, 14, 16]) развили активный ТБ по сравнению с 25 из 5376 (0,46%) QFT-GIT-отрицательных детей (общий общий общий CIR для QFT-GIT : 1,86 / 0,46 = 4,01, 95% ДИ: 2,51, 6,40).
TST (5 мм)
Сорок шесть из 2934 (1,56%) TST (≥5 мм) -позитивных детей (2 исследования [11, 13]) прогрессировали до ТБ по сравнению с 12 из 2414 (0,49%) TST (<5 мм) -отрицательные дети, из которых только 12 (0,49%) перешли в активную форму ТБ (общий общий CIR для TST-5 мм: 1.57 / 0,50 = 3,14, 95% ДИ: 1,68, 5,94).
TST (10 мм)
Двадцать из 711 (2,81%) TST (≥10 мм) -позитивных детей (3 исследования [11, 15, 16]) прогрессировали до ТБ по сравнению с 19 из 2433 (0,78%) TST (<10 мм) -отрицательные дети (общий CIR для TST-10 мм: 2,81 / 0,78 = 3,60, 95% ДИ: 1,93, 6,71).
С ослабленным иммунитетом
IGRA (QFT-GIT и T-SPOT.TB)
В популяции с ослабленным иммунитетом (4 исследования [18, 21, 22, 24]) семь из 232 (3,02%) людей с положительным результатом QFT-GIT перешли в активную форму туберкулеза по сравнению с 13 в 1999 г. (0.65%) QFT-GIT, который дал отрицательный результат (общий CIR для QFT-GIT: 3,02 / 0,65 = 4,65, 95% ДИ: 1,87, 11,51). 34 из 328 (10,37%) людей с положительным результатом T-SPOT.TB (5 исследований [12, 17, 19, 24, 25]) заболели туберкулезом по сравнению с 26 из 1273 (2,04%) T-SPOT.TB, которые прошли тестирование. отрицательный (общий CIR для T-SPOT.TB: 10,37 / 2,04 = 5,08, 95% CI: 3,09, 8,33).
34 из 328 (10,37%) людей с положительным результатом T-SPOT.TB (5 исследований [12, 17, 19, 24, 25]) заболели туберкулезом по сравнению с 26 из 1273 (2,04%) T-SPOT.TB, которые прошли тестирование. отрицательный (общий CIR для T-SPOT.TB: 10,37 / 2,04 = 5,08, 95% CI: 3,09, 8,33).
TST (10 мм)
Четыре из 107 (3,74%) человек с TST (≥10 мм) (5 исследований [19, 20, 22, 23, 25]) развили ТБ по сравнению с 8 из 389 (2,06 %) с TST (<10 мм) (грубый CIR для TST-10 мм: 3.74 / 2,06 = 1,82, 95% ДИ: 0,58, 5,92).
Недавно прибывшие из стран с высокой заболеваемостью туберкулезом
IGRA (QFT-GIT и T-SPOT.TB)
В двух исследованиях [26, 27] 13 из 416 (3,13%) недавно прибывших с положительным результатом QFT-GIT прогрессировал до TB по сравнению с четырьмя из 726 (0,55%), которые дали отрицательный результат (общий CIR для QFT-GIT: 3,13 / 0,55 = 5,69, 95% ДИ: 1,86, 17,28). Шесть из 181 (3,31%) человека, у которых был положительный результат теста на T-SPOT.TB, заболели туберкулезом, по сравнению с двумя из 118 (1,69%), у которых был отрицательный результат (общий CIR для T-SPOT. TB: 3,31 / 1,69 = 1,96, 95% ДИ: 0,40, 9,53).
TB: 3,31 / 1,69 = 1,96, 95% ДИ: 0,40, 9,53).
TST (≥6 мм или ≥10 мм)
В одном исследовании [26] TST (≥6 мм) использовался в качестве порога для положительного результата теста. Результаты показали, что восемь из 415 (1,93%) человек с положительным результатом теста на ТБ прогрессировали по сравнению с одним из 395 (0,25%) человек с отрицательным результатом (общий CIR для TST-6 мм: 1,93 / 0,25 = 7,72, 95% ДИ: 0,96, 60,59). В другом исследовании [27] у 9 из 288 (3,12%) людей с TST (≥10 мм) развился туберкулез, по сравнению с никем из 51 (0%) человека, у которых был отрицательный результат (общий CIR для TST-10). мм: 3.42, 95% ДИ: 0,20, 57,83).
Сравнительное выполнение тестов на выявление скрытой туберкулезной инфекции
Дети
QFT-GIT по сравнению с TST (≥5 мм)
Только два исследования соответствовали критериям включения R-CIR и 95% CI для сравнения QFT-GIT и TST (≥5 мм) [11, 13]. Метааналитическая оценка не была статистически значимой между QFT-GIT и TST (≥5 мм) для выявления LTBI (рис. 2a; объединенный CIR = 1,11, 95% CI: 0,71, 1,74).
2a; объединенный CIR = 1,11, 95% CI: 0,71, 1,74).
Объединенные кумулятивные отношения заболеваемости IGRA по сравнению с TST у детей, с ослабленным иммунитетом и недавно поступивших. a Объединенное кумулятивное соотношение заболеваемости QFT-GIT по сравнению с TST (5 мм) для детской популяции. b Лесной график отношения кумулятивной заболеваемости QFT-GIT по сравнению с TST (10 мм) для детской популяции. c Объединенное кумулятивное соотношение заболеваемости T-SPOT.TB по сравнению с TST (10 мм) для населения с ослабленным иммунитетом. d Лесной график кумулятивного отношения заболеваемости QFT-GIT по сравнению с TST (15 мм) для недавно прибывшей популяции
QFT-GIT vs.TST (≥10 мм)
Отдельные результаты двух исследований склонны к предпочтению IGRA (QFT-GIT) по сравнению с TST (≥10 мм) [11, 16] (рис. 2b). Мы не объединяли R-CIR из-за значительной неоднородности оценок этих исследований ( p = 0,01, I 2 = 83%). Оба исследования имели умеренный риск смещения, поэтому риск смещения с меньшей вероятностью объясняет эту неоднородность. Одним из потенциальных источников неоднородности могла быть разница в бремени заболеваемости туберкулезом между двумя исследованиями.В частности, исследование, которое показало незначительную разницу между IGRA и TST [16], было проведено в районе с высокой заболеваемостью (Южная Корея), в отличие от исследования Diel et al. (2011) [11], который проводился в зоне низкой заболеваемости туберкулезом (Германия). Имеются данные, свидетельствующие о снижении чувствительности и специфичности IGRA в регионах с высоким по сравнению с низким бременем ТБ, где первое представлено высокими показателями вакцинации БЦЖ при рождении [29–33].
2b). Мы не объединяли R-CIR из-за значительной неоднородности оценок этих исследований ( p = 0,01, I 2 = 83%). Оба исследования имели умеренный риск смещения, поэтому риск смещения с меньшей вероятностью объясняет эту неоднородность. Одним из потенциальных источников неоднородности могла быть разница в бремени заболеваемости туберкулезом между двумя исследованиями.В частности, исследование, которое показало незначительную разницу между IGRA и TST [16], было проведено в районе с высокой заболеваемостью (Южная Корея), в отличие от исследования Diel et al. (2011) [11], который проводился в зоне низкой заболеваемости туберкулезом (Германия). Имеются данные, свидетельствующие о снижении чувствительности и специфичности IGRA в регионах с высоким по сравнению с низким бременем ТБ, где первое представлено высокими показателями вакцинации БЦЖ при рождении [29–33].
Люди с ослабленным иммунитетом
T-SPOT.ТБ по сравнению с TST (≥10 мм)
R-CIR были объединены в двух исследованиях, включавших популяцию ESRD (рис. 2c; объединенный R-CIR = 1,01, 95% CI: 0,65, 1,58) [19, 25] . Метааналитическая оценка, сравнивающая эффективность между IGRA (T-SPOT.TB) и TST (≥10 мм), не была статистически значимой. Соответствующие R-CIR для отдельных исследований также были незначительными: 0,38 (95% ДИ: 0,05, 2,87) [19] и 1,07 (95% ДИ: 0,68, 1,68) [25]. Мы не объединили оценки исследования по разным популяциям с ослабленным иммунитетом из-за клинической гетерогенности.
2c; объединенный R-CIR = 1,01, 95% CI: 0,65, 1,58) [19, 25] . Метааналитическая оценка, сравнивающая эффективность между IGRA (T-SPOT.TB) и TST (≥10 мм), не была статистически значимой. Соответствующие R-CIR для отдельных исследований также были незначительными: 0,38 (95% ДИ: 0,05, 2,87) [19] и 1,07 (95% ДИ: 0,68, 1,68) [25]. Мы не объединили оценки исследования по разным популяциям с ослабленным иммунитетом из-за клинической гетерогенности.
Люди, недавно прибывшие из стран с высоким бременем ТБ
QFT-GIT по сравнению с TST (≥15 мм)
В двух исследованиях сравнивали QFT-GIT с TST (≥15 мм) для этой популяции [26, 27]. Как видно на рис. 2d, в Harstad et al. исследование [26], QFT-GIT был в большей степени, чем TST (R-CIR = 6,78, 95% ДИ: 1,91, 24,10). Напротив, в Kik et al. исследование [27], TST была в большей степени, чем QFT-GIT (R-CIR = 0,27, 95% ДИ: 0,07, 0,96). Оценки R-CIR не были объединены из-за значительной неоднородности, вытекающей из противоположных выводов (рис.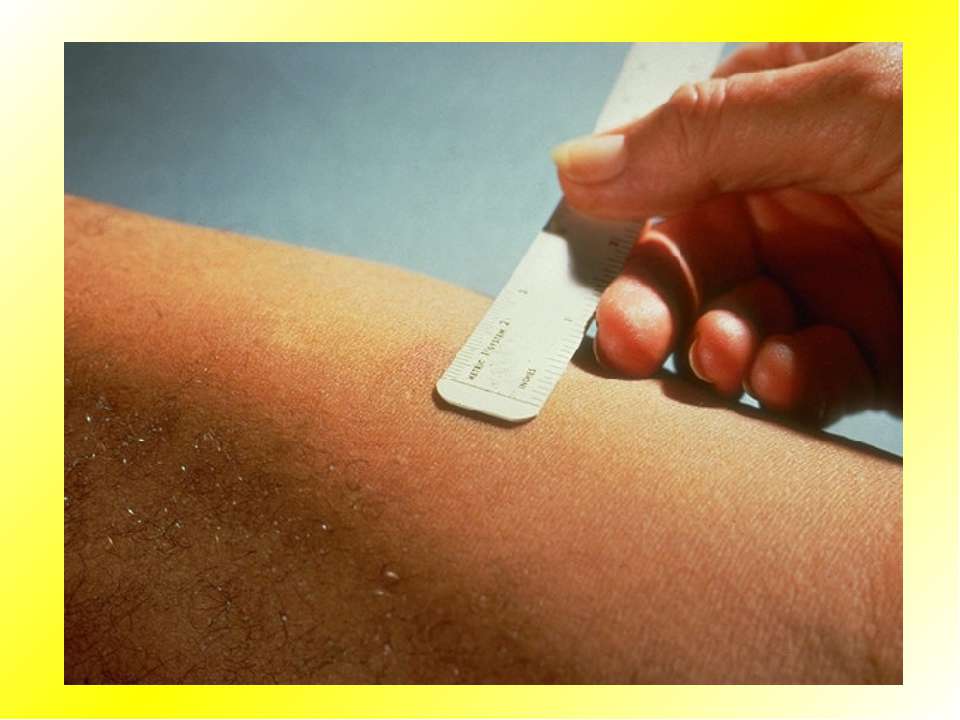 2d; p <0,01, I 2 = 92%). Априори определенные факторы (статус вакцинации БЦЖ, порог ТКП, риск систематической ошибки и распространенность ТБ в стране происхождения) не могли легко объяснить это несоответствие. Обратите внимание, что эти два исследования различались по исследуемым группам лиц, ищущих убежища [26], и иммигрантов, имеющих известный контакт с индексным случаем [27]. Более того, исследование Kik [27] исключило контакты с TST <5 мм, которые могли повлиять на оценку параметров точности теста.
2d; p <0,01, I 2 = 92%). Априори определенные факторы (статус вакцинации БЦЖ, порог ТКП, риск систематической ошибки и распространенность ТБ в стране происхождения) не могли легко объяснить это несоответствие. Обратите внимание, что эти два исследования различались по исследуемым группам лиц, ищущих убежища [26], и иммигрантов, имеющих известный контакт с индексным случаем [27]. Более того, исследование Kik [27] исключило контакты с TST <5 мм, которые могли повлиять на оценку параметров точности теста.
Влияние вакцинации БЦЖ на туберкулиновую кожную пробу | Это имеет значение?
Вакцинация палочкой Кальметта-Герена (БЦЖ) используется для профилактики туберкулеза (ТБ) у людей с 1921 года; около 100 миллионов доз в год вводят детям в 170 странах мира (1).Считается, что вакцина БЦЖ эффективна для предотвращения или облегчения тяжелых осложнений туберкулеза у детей, т. Е. Диссеминированного заболевания или менингита, но ее эффективность в профилактике взрослых форм туберкулеза минимальна (2, 3). Поскольку она мало способствует предотвращению наиболее инфекционных форм ТБ, то есть случаев с положительным мазком, эпидемиологическое влияние БЦЖ на глобальную борьбу с ТБ ограничено. Промышленно развитые страны с низкой заболеваемостью туберкулезом не используют БЦЖ или сократили ее использование, а ревакцинация школьников или молодых людей в большинстве мест прекращена (3).
Поскольку она мало способствует предотвращению наиболее инфекционных форм ТБ, то есть случаев с положительным мазком, эпидемиологическое влияние БЦЖ на глобальную борьбу с ТБ ограничено. Промышленно развитые страны с низкой заболеваемостью туберкулезом не используют БЦЖ или сократили ее использование, а ревакцинация школьников или молодых людей в большинстве мест прекращена (3).
Таким образом, в промышленно развитых странах основной эффект вакцинации БЦЖ в программах борьбы с туберкулезом связан с кожным туберкулиновым тестированием, преобладающим методом выявления латентной туберкулезной инфекции (ЛТИ) у лиц из группы риска и выявления кандидатов на лечение от ЛТИ (4). Вакцинация БЦЖ приводит к реактивным кожным туберкулиновым пробам (ТКП) у многих реципиентов, что создает возможность путаницы при интерпретации; не существует надежного метода, позволяющего отличить истинно-положительный результат теста на инфекцию от ложноположительного результата предыдущей вакцинации (5).Это наиболее актуально в двух ситуациях: ( 1 ) для лиц, родившихся за границей из стран с высокой заболеваемостью, которые эмигрировали в страны с низкой заболеваемостью, но обычно получали предварительную вакцинацию БЦЖ, и ( 2 ) в программах TST, которые используют двухэтапное «усиление» для различения предшествующей и недавней инфекции, т. е. в медицинских учреждениях.
е. в медицинских учреждениях.
Две статьи, опубликованные в этом выпуске журнала Journal , помогают нам проинформировать нас о проблемах, связанных с влиянием вакцинации БЦЖ на ТКП (6, 7).Чи и его коллеги (стр. 958–961) оценили интерпретацию кожных проб у сингапурских школьников, все из которых получали БЦЖ при рождении, и многие из которых, 83% и 36%, были ревакцинированы в возрасте 12 или 16 лет, соответственно, в зависимости от по результатам их инертных (<10 мм) ТСТ (6). Риск развития ТБ через 4 года после прочтения ТКП или ревакцинации у этих двух групп детей был определен путем перекрестного сопоставления результатов ТКП с уведомлениями о ТБ в национальной базе данных.Исследование показало, что у подростков, которым была сделана одна вакцинация БЦЖ при рождении, 10 мм уплотнения было наиболее чувствительным и специфическим порогом для развития туберкулеза, тогда как у тех, кто прошел ревакцинацию, 16 мм были более предсказуемыми.
Сингх и его коллеги (стр. 962–964) оценили двухэтапное усиление ТКП у медицинских работников, не имевших недавнего контакта с ТБ, в Соединенном Королевстве, которым было 21–54 года и которые получали вакцинацию БЦЖ в подростковом или взрослом возрасте 8–12 лет. 40 лет назад (7).У испытуемых были прочитаны тесты TST через 48, 72 и 96 часов, а затем через 1 неделю было проведено повторное тестирование. Был отмечен бустерный эффект со средним увеличением уплотнения на 7,8 мм через 48 часов, но минимальным увеличением или отсутствием увеличения через 72 или 96 часов. Эта разница в усилении привела к более положительным результатам (> 15 мм) после второй TST (19 против 9), когда считывание проводилось через 48 часов, чем через 72 часа (10 против 11).
962–964) оценили двухэтапное усиление ТКП у медицинских работников, не имевших недавнего контакта с ТБ, в Соединенном Королевстве, которым было 21–54 года и которые получали вакцинацию БЦЖ в подростковом или взрослом возрасте 8–12 лет. 40 лет назад (7).У испытуемых были прочитаны тесты TST через 48, 72 и 96 часов, а затем через 1 неделю было проведено повторное тестирование. Был отмечен бустерный эффект со средним увеличением уплотнения на 7,8 мм через 48 часов, но минимальным увеличением или отсутствием увеличения через 72 или 96 часов. Эта разница в усилении привела к более положительным результатам (> 15 мм) после второй TST (19 против 9), когда считывание проводилось через 48 часов, чем через 72 часа (10 против 11).
Каковы последствия этих исследований? Результаты Чи и его коллег подтверждают предыдущие исследования, которые показали, что вакцинация БЦЖ может затруднить интерпретацию ТКП у 0–80% людей и что вакцинация или ревакцинация, проводимые в более позднем возрасте, с большей вероятностью сделают это, чем вакцинация, проводимая в отдаленные сроки. (8).Исследование наглядно демонстрирует, что у тех, кто получил одну прививку в раннем возрасте, 10-миллиметровая граница была предиктором туберкулеза, что характерно для большинства иностранцев, прибывающих в промышленно развитые страны. Кроме того, исследование предполагает, что при принятии решения о лечении ЛТИ среди лиц, получивших более одной вакцинации БЦЖ, возможно использование порогового значения более 10 мм; это может относиться к тем странам, которые использовали ревакцинацию БЦЖ, с нынешней низкой заболеваемостью и программами лечения ЛТИ.Однако многие страны с низкой или снижающейся заболеваемостью туберкулезом, например, Сингапур и несколько стран Восточной Европы, прекратили ревакцинацию БЦЖ (3), и поэтому в будущем это будет иметь все меньшее значение. В развивающихся странах, где вакцинация БЦЖ является обычным явлением (1), лечение ЛТИ широко не применяется, а там, где оно реализуется, основное внимание уделяется контактам в детстве с инфекционными случаями ТБ и лицам, инфицированным вирусом иммунодефицита человека (ВИЧ) (9).
(8).Исследование наглядно демонстрирует, что у тех, кто получил одну прививку в раннем возрасте, 10-миллиметровая граница была предиктором туберкулеза, что характерно для большинства иностранцев, прибывающих в промышленно развитые страны. Кроме того, исследование предполагает, что при принятии решения о лечении ЛТИ среди лиц, получивших более одной вакцинации БЦЖ, возможно использование порогового значения более 10 мм; это может относиться к тем странам, которые использовали ревакцинацию БЦЖ, с нынешней низкой заболеваемостью и программами лечения ЛТИ.Однако многие страны с низкой или снижающейся заболеваемостью туберкулезом, например, Сингапур и несколько стран Восточной Европы, прекратили ревакцинацию БЦЖ (3), и поэтому в будущем это будет иметь все меньшее значение. В развивающихся странах, где вакцинация БЦЖ является обычным явлением (1), лечение ЛТИ широко не применяется, а там, где оно реализуется, основное внимание уделяется контактам в детстве с инфекционными случаями ТБ и лицам, инфицированным вирусом иммунодефицита человека (ВИЧ) (9).
Должны ли мы для принятия решения о лечении ЛТИ у лиц иностранного происхождения, прибывающих в промышленно развитые страны, использовать порог, отличный от рекомендованного в большинстве ситуаций 10 мм? История вакцинации БЦЖ и ревакцинации недавних иммигрантов не всегда точна или доступна.Что еще более важно, большинство положительных результатов ТКП у лиц, родившихся за границей, являются результатом истинной инфекции ТБ (8, 10), а риск-польза от лечения ЛТИ благоприятна для молодых людей, группа, оцененная в Сингапуре. Следовательно, мы должны продолжать следовать текущим рекомендациям, которые используют 10 мм для большинства иностранцев и 5 мм для тех, кто недавно контактировал с людьми с туберкулезом или которые являются ВИЧ-положительными (4). История вакцинации БЦЖ не должна быть фактором при принятии решения о ЛТИ для лиц, родившихся за границей из стран с высокой заболеваемостью.
Исследование Сингх и его коллеги предполагает, что при использовании двухэтапной ТКП для оценки усиления, как это делается во многих медицинских учреждениях, 48 часов могут быть оптимальным временем для чтения ТКП для повышения чувствительности, по крайней мере, у лиц с предыдущим Вакцинация БЦЖ (7). Однако это может быть неприемлемо в тех странах, где BCG не использовалась часто, например в США, и поэтому имеет ограниченное значение для этих ситуаций. Следует отметить разницу в результатах при оценке 15 мм в качестве порогового значения, что повторяет, что в недавних рекомендациях для медицинских работников, у которых нет других известных рисков для ЛТИ, было выбрано 15 мм, а не 10 мм в попытке повысить специфичность TST для этой популяции (4).Напротив, для медицинских работников, которые недавно иммигрировали из стран с высокой заболеваемостью, применяется порог в 10 мм, и, как отмечалось ранее, удаленная вакцинация БЦЖ не должна рассматриваться (5, 6).
Однако это может быть неприемлемо в тех странах, где BCG не использовалась часто, например в США, и поэтому имеет ограниченное значение для этих ситуаций. Следует отметить разницу в результатах при оценке 15 мм в качестве порогового значения, что повторяет, что в недавних рекомендациях для медицинских работников, у которых нет других известных рисков для ЛТИ, было выбрано 15 мм, а не 10 мм в попытке повысить специфичность TST для этой популяции (4).Напротив, для медицинских работников, которые недавно иммигрировали из стран с высокой заболеваемостью, применяется порог в 10 мм, и, как отмечалось ранее, удаленная вакцинация БЦЖ не должна рассматриваться (5, 6).
Проблемы, поднятые в этих исследованиях, также напоминают нам о несовершенстве ТКП и вакцинации БЦЖ как инструментов глобальной борьбы с туберкулезом. Нам нужны более качественные диагностические тесты, чем ТКП, для выявления людей с ЛТИ и, в идеале, тех, кто подвержен наибольшему риску развития ТБ (11). Безусловно, крайне желательна вакцина с большей эффективностью, чем БЦЖ, для профилактики туберкулеза (12). Десять лет назад мы, возможно, считали любую цель недостижимой, но теперь, благодаря значительным достижениям в области технологий и обновлению исследований в области туберкулеза, наши мечты когда-нибудь могут стать реальностью.
Десять лет назад мы, возможно, считали любую цель недостижимой, но теперь, благодаря значительным достижениям в области технологий и обновлению исследований в области туберкулеза, наши мечты когда-нибудь могут стать реальностью.
Ссылки
Раздел:
ВыбратьВверху страницы Ссылки << СТАТЬИ ДЛЯ СИТУАЦИИ| 1. | Fine PEM, Carneiro IAM, Milstien JB, Clements CJ. Вопросы, связанные с использованием БЦЖ в программах иммунизации: документ для обсуждения. Всемирная организация здравоохранения, Женева, Швейцария; 1999; ВОЗ / V & B / 99.23: 1-44. |
| 2. | Colditz GA, Brewer TF, Berkey CS, Wilson ME, Burdick E, Fineberg HV, Mosteller FE Эффективность вакцины БЦЖ в профилактике туберкулеза: метаанализ опубликованной литературы. JAMA 2711994698702 |
| 3. | Всемирная организация здравоохранения, Глобальная программа по туберкулезу и Глобальная программа по вакцинам.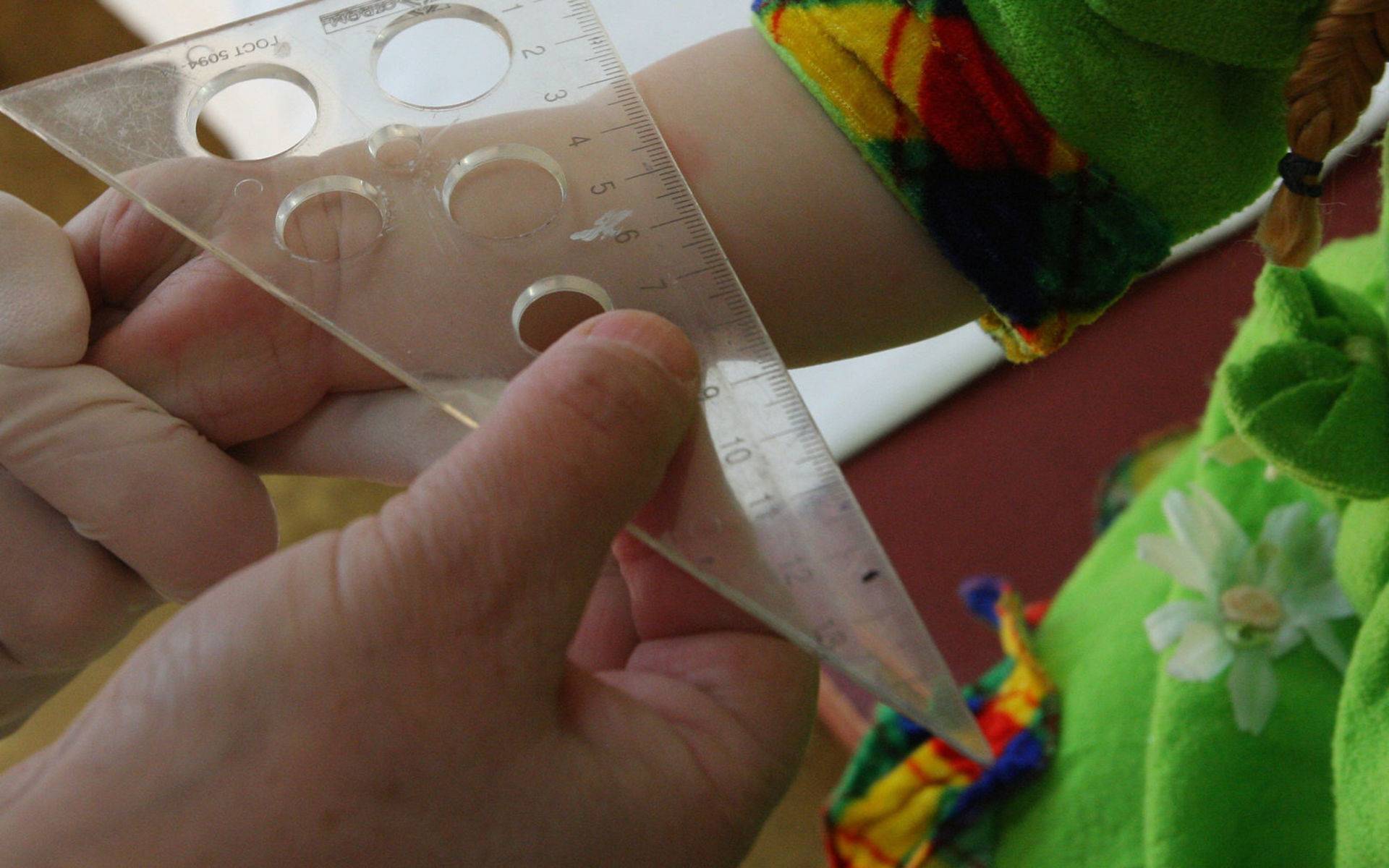 Заявление о ревакцинации БЦЖ для профилактики туберкулеза. Wkly Epidemiol Rec 1995; 72: 229–231. Заявление о ревакцинации БЦЖ для профилактики туберкулеза. Wkly Epidemiol Rec 1995; 72: 229–231. |
| 4. | Американское торакальное общество, Центры по контролю и профилактике заболеваний. Целенаправленное туберкулиновое тестирование и лечение латентной туберкулезной инфекции. Am J Respir Crit Care Med 2000; 161 (Приложение 2): S221 – S243. |
| 5. | Американское торакальное общество, Центры по контролю и профилактике заболеваний. Стандарты диагностики и классификация туберкулеза у взрослых и детей. Am J Respir Crit Care Med 2000; 161: 1376–1395. |
| 6. | Chee CBE, Soh CH, Boudville IC, Chor SS, Wang YT Интерпретация туберкулиновой кожной пробы у Mycobacterium bovis вакцинированных БЦЖ школьников Сингапура. Am J Respir Crit Care Med 1642001958961 |
| 7. | Сингх С.Д., Саттон С.Дж., Вудкок А. А. Повторное тестирование на туберкулин у Mycobacterium tuberculosis Субъекты, вакцинированные БЦЖ, в Великобритании: время бустерного эффекта варьируется в зависимости от времени действия бустера. Am J Respir Crit Care Med 1642001962964 А. Повторное тестирование на туберкулин у Mycobacterium tuberculosis Субъекты, вакцинированные БЦЖ, в Великобритании: время бустерного эффекта варьируется в зависимости от времени действия бустера. Am J Respir Crit Care Med 1642001962964 |
| 8. | Menzies RI. Туберкулиновая кожная проба. В: Райхман Л.Б., Хершфилд Е.С., редакторы. Туберкулез: комплексный международный подход, 2-е изд. Нью-Йорк: Марсель Деккер; 2000. с. 279–322. |
| 9. | Всемирная организация здравоохранения, Международный союз борьбы с туберкулезом и болезнями легких. Профилактическая терапия туберкулеза у ВИЧ-инфицированных: совместное заявление Международного союза борьбы с туберкулезом и болезнями легких (IUATLD) и Глобальной программы по СПИДу и Программы по туберкулезу Всемирной организации здравоохранения (ВОЗ). Tuberc Lung Dis 1994; 75: 96–98. |
| 10. | Menzies R, Vissandjee B, Amyot D Факторы, связанные с реактивностью туберкулина среди рожденных за границей в Монреале. Am Rev Respir Dis 1461992752758 Am Rev Respir Dis 1461992752758 |
| 11. | Barnes PF Диагностика скрытой туберкулезной инфекции: обновление за 100 лет. Am J Respir Crit Care Med 1632001807808 |
| 12. | Институт медицины, Комитет по ликвидации туберкулеза в США.Прекращение пренебрежения; Ликвидация туберкулеза в США. Национальная академия прессы, Вашингтон, округ Колумбия. 2000. |
Ответы на атипичные кожные пробы с туберкулином
Через 24 часа после получения стандартной кожной пробы, содержащей 5 единиц очищенного протеина, производного туберкулина (PPD), у 22-летнего афроамериканца появилась слегка розовая приподнятый твердый налет на месте укола ( A ). Его предыдущие результаты теста PPD были отрицательными. Он отрицал какие-либо конституциональные симптомы и высыпания.В остальном он был здоров, не принимал никаких лекарств и не имел ВИЧ.
Бляшка имела диаметр 20 мм и гранулематозный вид с резкими границами, которые не изменились после 48 часов наблюдения.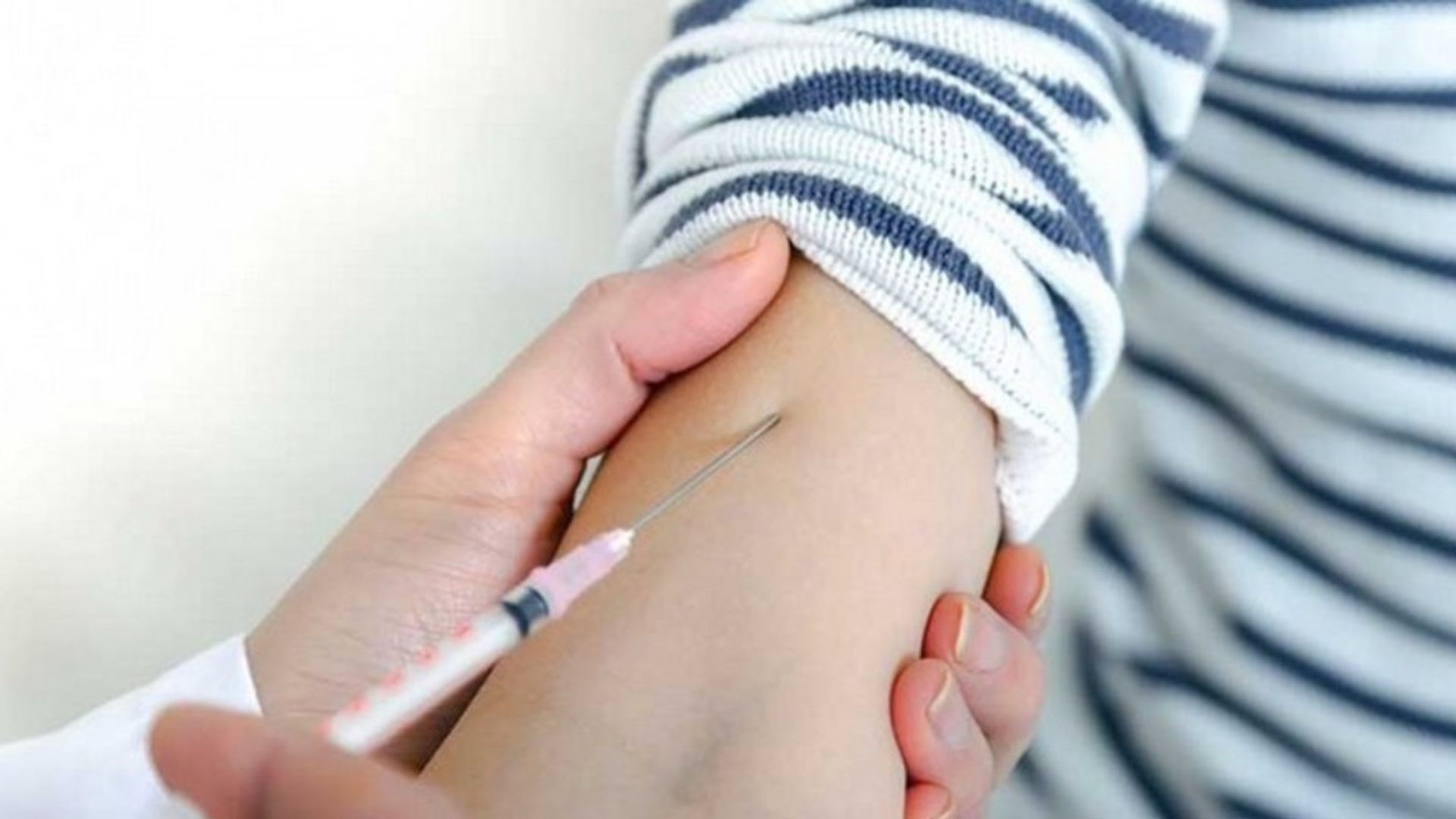 Ударная биопсия поражения показала выраженный спонгиотический дерматит с внутриэпидермальной и субэпидермальной везикуляцией и разбросанными эозинофилами, что соответствует гиперчувствительности туберкулинового типа.
Ударная биопсия поражения показала выраженный спонгиотический дерматит с внутриэпидермальной и субэпидермальной везикуляцией и разбросанными эозинофилами, что соответствует гиперчувствительности туберкулинового типа.
Во время теста PPD (Манту) туберкулиновый антиген вводится внутрикожно.Положительный ответ, который обозначается уплотнением, образованием пузырей или гиперчувствительностью, представляет собой реакцию гиперчувствительности IV типа (замедленного типа). 1 В реакциях типа IV участвуют сенсибилизированные Т-лимфоциты, которые привлекаются к участку PPD, где высвобождаются цитокины, такие как интерферон гамма и фактор некроза опухоли. Последующее уплотнение возникает в результате расширения сосудов, отека, отложения фибрина и привлечения других воспалительных клеток.
Согласно вкладышу в упаковку, атипичные реакции, такие как волдыри, гранулемы и местный некроз, после теста PPD очень редки. 2 Из более чем 5000 туберкулиновых кожных тестов, которые мы провели за последние 5 лет, был только 1 случай образования волдырей на участке PPD ( B ) и 1 гиперчувствительная реакция повышенной чувствительности (см. фото A ) . Тем не менее, местный некроз был зарегистрирован у 2,5% пациентов с положительным ответом. 3
фото A ) . Тем не менее, местный некроз был зарегистрирован у 2,5% пациентов с положительным ответом. 3
Новый анализ на основе сыворотки — QuantiFERON-TB — оказался эффективным инструментом для выявления скрытой инфекции Mycobacterium tuberculosis .Анализ может различать ответы, вызванные нетуберкулезными микобактериями; интерпретация результатов гораздо более объективна, чем при кожной пробе. 4 Ключевой момент: неосложненное уплотнение типично для обычного положительного ответа. Могут возникать местный некроз, образование пузырей и преувеличенные реакции, которые также считаются положительными реакциями.
Мнения или утверждения, содержащиеся в данном документе, являются частной точкой зрения авторов и не могут рассматриваться как официальные или отражающие точку зрения Министерства армии или Министерства обороны.
.

