Реакция на прививку БЦЖ: норма и возможные отклонения
Вы просматриваете раздел Реакция на БЦЖ, расположенный в общем разделе Профилактика туберкулеза
Существуют заболевания, которые проще предупредить или ослабить тяжесть протекания, чем потом заниматься длительным и тяжелым лечением. К таковым можно отнести туберкулез. Эффективной мерой профилактики является вакцинация.
Прививка от туберкулеза не защитит от микобактерии, которые вызывает патологию, но предупредит развитие открытой формы заболевания. БЦЖ прививка считается для организма ребенка довольно сложной, характеризуется длительным периодом заживления со своими особенностями и этапами. Для родителей важно знать, что представляет собой нормальная поствакцинальная реакция, чтобы не пропустить развитие серьезных осложнений.
Что такое реакция на прививку?
Вакцинация против туберкулеза подразумевает введение в организм ребенка ослабленных возбудителей туберкулеза. Делается это уже на 3-5 день жизни младенца, чтобы обезопасить беззащитный организм ребенка от встречи с опасными инфекционными агентами.
После попадания внутрь организма препарата вызывается ответная реакция, от качества которой и зависит успешность формирования иммунитета. При отсутствии соответствующих симптомов можно говорить, что вакцинация прошла безрезультатно и требуется повторное введение препарата.
Нормальная реакция
Реакция на прививку БЦЖ ярче всего и с наиболее выраженными признаками проявляется после первой вакцинации. Длительность формирования иммунитета составляет до полугода, в зависимости от особенностей детского организма продолжительность заживления может доходить до года.
БЦЖ у детей делается в левое плечо, вводится препарат только внутрь кожи.
При нарушении техники введения могут развиться серьезные осложнения, например, абсцесс. Ликвидировать его придется у малыша оперативным путем.
При нормальной реакции организма непосредственно после введения БЦЖ на кожном покрове появляется папула, рассасывающаяся через несколько часов. После вакцинации БЦЖ через несколько дней в качестве ответной реакции можно ожидать небольшое покраснение на месте укола.
Нормальная реакция БЦЖ на фото:
Эти проявления относятся к норме, поэтому мамочкам можно не беспокоиться. Совершенно естественно, если у ребенка незначительно поднимется температура тела. Если малыш плохо переносит температуру, то можно воспользоваться жаропонижающими препаратами.
К нормальной реакции можно отнести появление воспаления с образованием небольшого гнойничка.
Постепенно гнойничок будет прорываться и вновь заполняться гнойным содержимым, все это нормально. Строго запрещается выдавливать гной и обрабатывать ранку антисептическими средствами. Это может нарушить процесс формирования иммунной ответной реакции.
При наблюдении перечисленных симптомов можно судить, что процесс заживления протекает нормально, иммунная система справляется с ослабленными микроорганизмами и формирует способность противостоять активной палочке Коха.
Плохая реакция после БЦЖ
Не у всех деток реакция на прививку адекватная. Бывают отклонения в процессе заживления, поэтому родителям надо знать, какая должна быть норма, и что свидетельствует о патологии.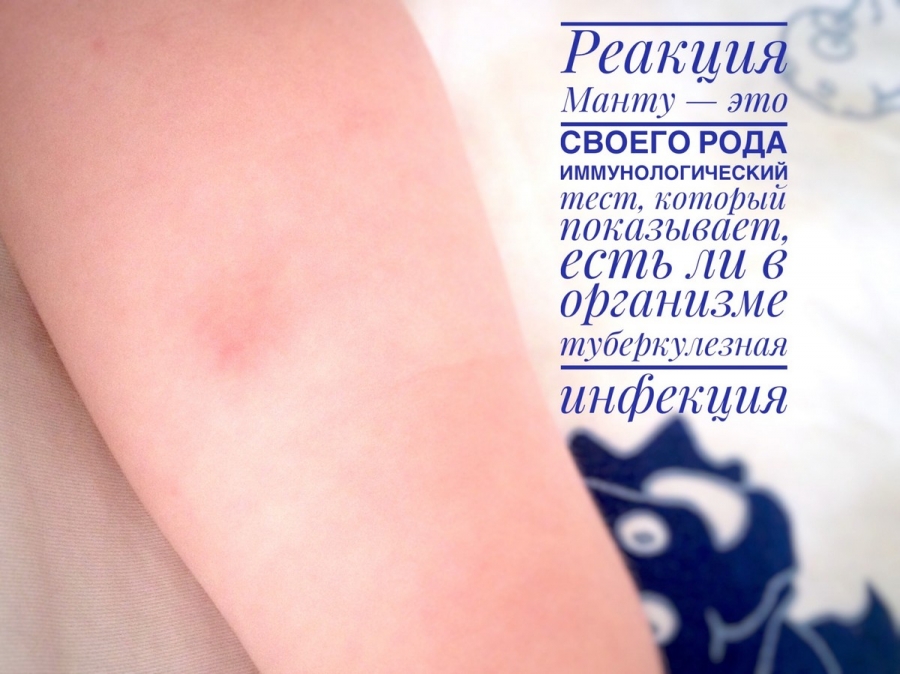
Если после вакцинации через некоторое время появляется на месте укола припухлость и покраснение, которое захватывает не только место введения препарата, но и соседние ткани, то можно говорить об отклонениях в процессе формирования иммунитета.
Нельзя также считать нормой, если процесс воспаления распространяется на рядом лежащие участки кожи. Если образовавшийся гнойничок имеет маленькие размеры и расположен только в месте укола, то это норма. А вот при больших размерах образования, сопровождающиеся сильным отеком и воспалением прилежащих тканей можно говорить, что что-то идет не так и показать ребенка врачу.
О серьезных осложнениях может говорить припухлость не только места инъекции, но и суставов на ручках малыша. Это уже явный симптом развития остеомиелита.
Сильное опухание, подъем температуры тела без явных внешних признаков на месте введения препарата могут говорить о развитии подкожного абсцесса в результате неправильного введения БЦЖ.
Возможные реакции
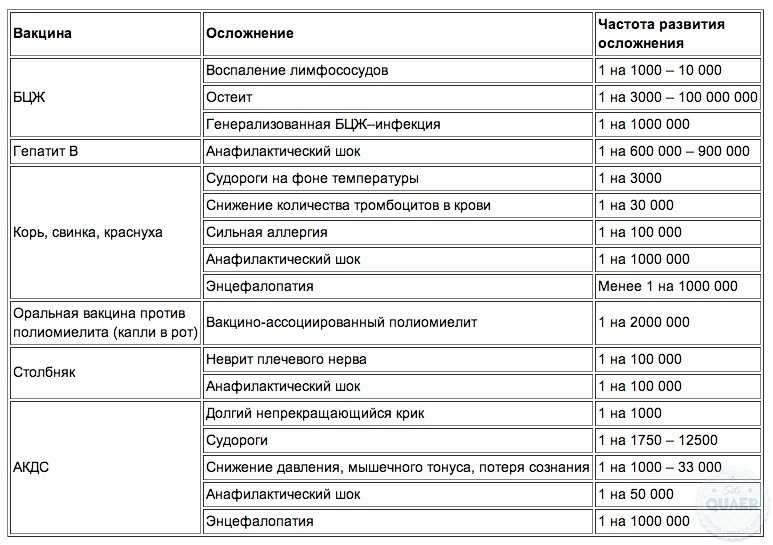
Прививку БЦЖ большинство детей переносят нормально, без серьезных осложнений, но в редких случаях последствия они могут быть. Чаще всего причина кроется в некачественном препарате, нарушении тактики постановки прививки или несоблюдении противопоказаний.
Чаще всего причина кроется в некачественном препарате, нарушении тактики постановки прививки или несоблюдении противопоказаний.
У деток за всю историю вакцинации против туберкулеза были отмечены смертельные случаи, но все малыши оказались ВИЧ инфицированными, то есть не подлежали вакцинации, но это противопоказание почему-то не было учтено.
Все возможные реакции после БЦЖ:
- Покраснение на месте инъекции. Такая реакция соответствует норме, но при условии, что гипертермия не распространяется на соседние участки.
- Опухание места прививки также нормально. Наблюдается, как правило, через несколько дней после вакцинации.
- Зуд. Прививка может чесаться, особенно в период заживления. Это нормально, чтобы не позволить малышу разодрать ее, можно прикрыть место укола салфеткой.
- Появление гнойничка. После этапа покраснения на месте инъекции появляется небольшой пузырек, заполненный гноем. Это норма, но размеры его не должны выходить за границы укола. Если соседние ткани не вовлечены в этот процесс, то все нормально.

- Воспаление места инъекции. После вакцинации БЦЖ это вполне нормально, так организм реагирует на поступление чужеродных микроорганизмов.
- Повышение температуры тела. В норме такой симптом обычно наблюдается в момент появления гнойничка, если показатели на градуснике ползут вверх сразу после прививки, то надо сообщить врачу.
- Воспаление лимфатических узлов не является показателем нормы и развивается при путешествии бактерии по организму. Если увеличиваются подмышечные лимфоузлы, то надо обратиться к врачу.
Главным показателем наличия иммунитета и правильно поставленной БЦЖ является появление небольшого рубца (шрама).
О не сформировавшемся против туберкулеза иммунитете говорит и отсутствие следа на месте укола по прошествии длительного времени.
Если вакцинация прошла безуспешно, то детям делается прививка повторно через некоторое время после пробы Манту.
Вывод
Особенности организма у каждого ребенка индивидуальны, поэтому и реакция на вакцинацию отличается. Но, если знать о признаках нормального процесса заживления после прививки БЦЖ, то можно вовремя распознать отклонения и обратиться к врачу за помощью.
Но, если знать о признаках нормального процесса заживления после прививки БЦЖ, то можно вовремя распознать отклонения и обратиться к врачу за помощью.
Покраснение после прививки
Работаем без выходных и праздников
COVID 19: тесты на антитела
Конечно любая вакцина может вызывать побочные реакции, и покраснение в месте укола – одна из них. В случае с покраснением реакция может быть вызвана как самим фактом грубого вмешательства в тело человека (укол), так и склонностью к аллергии на определенные компоненты вакцины. Чаще всего покраснение возникает после вакцин, содержащих вещества, специально провоцирующие воспаление: АКДС, АДС, от гепатита.
Покраснение относится к местным реакциям, и обычно оно наблюдается вместе с болью припухлостью и отеком в месте инъекции. Хорошая новость — уплотнение и покраснение после прививки держится недолго и проходит само в течение 1-3 дней. Можно сказать, что это всё классические реакции на вакцину, и к ним надо относится спокойно: по статистике покраснение появляется у каждого четвертого ребенка. Если же область покраснения растет или не проходит через 3 дня – это повод обратиться к врачу.
Можно сказать, что это всё классические реакции на вакцину, и к ним надо относится спокойно: по статистике покраснение появляется у каждого четвертого ребенка. Если же область покраснения растет или не проходит через 3 дня – это повод обратиться к врачу.
Какие вакцины вызывают покраснение
Местные побочные реакции в виде боли, уплотнения и отека, покраснения на месте инъекции дают многие вакцины, кроме того, это обычная реакция на укол. Но некоторые вакцины, например, АКДС, дает ярко выраженные реакции – коротко расскажем о них (здесь будут описаны только местные реакции, про повышение температуры, например, рассказывается в другой статье).
Профилактика COVID-19
После прививки от коронавируса возможны обычные местные реакции в легкой форме: отечность, болезненность, покраснение. Все они проходят через 2-3 дня без постороннего вмешательства, но если вы испытываете дискомфорт, можно принять лекарство от аллергии. Это относится ко всем вакцинам от ковида, включая Pfizer/BioNTech, Moderna, Спутник V.
АКДС
АКДС – сложная вакцина, защищающая сразу от нескольких болезней, к тому «славящаяся» наиболее частыми, по сравнению с другими вакцинами, осложнениями. Покраснение не является исключением, и после АКДС встречается довольно часто (вероятность примерно 25%), и более ярко выражено.
Покраснение – нормальная реакция организма на искусственное заражение, свидетельство начал «атаковать» инфицированные клетки. Если речь идет о инактивированных вакцинах, то покраснение небольшое (норма – 2-3 см, не более 6-7 см.), и должно проходить через 2-3 дня. Для «живых» вакцин местные реакции начинают проявляться только через неделю.
Бить тревогу стоит, если область покраснения заметно увеличивается – до 7-8 см, и наблюдается обострение других местных и общих реакций: высокая температура, пульсирующая боль в месте инъекции, красная и горячая кожа, в уплотнении ткань на ощупь мягкая. В таких ситуациях лучше не заниматься самолечением, а сразу обратиться к врачу.
Профилактика коклюша, гепатита В, столбняка, полиомиелита
АДС, АДС-М, Инфанрикс, Пентаксим, Полиорикс, Регевак, Тетраксим могут вызывать боль и покраснение в первые 3 дня.
Профилактика Гепатита А
После вакцин Аваксим, Хавриск и других в первые 3 дня возможны болезненность и покраснение.
Профилактика гриппа
Как и после многих других прививок, вакцины от гриппа (Инфлювак, Ваксигрип и другие) могут дать стандартную местную реакцию в виде болевых ощущений и красноты в месте укола.
Профилактика клещевого энцефалита
Обычные боль и покраснение в месте инъекции в течение первых 3-х дней.
Профилактика менингококковой и пневмококковой инфекции
Также в течение первых 3-х дней возможны болевые ощущение и покраснение после вакцин Превенар, Хиберикс, Менинго А+С и им подобным.
Профилактика ВПЧ
Боль и покраснение после вакцины Гардасил возможно в течение 5 дней.
Профилактика бешенства
Cocav – припухлость, покраснение, зуд, болезненность.
Профилактика желтой лихорадки
Обычные местные реакции в течение 3-х дней.
Профилактика брюшного тифа
Вианвак – боль и покраснение в первые 3 дня.
Наблюдение после вакцинации
Если покраснение небольшое и держится не долее 3-х дней – беспокоиться не о чем. Многие мамы начинают волноваться при разрастании области покраснения или когда оно долго не проходит. Но здесь в первую очередь надо смотреть на самочувствие ребенка: если никаких заметных проблем нет, то и не стоит впадать в панику, даже если покраснение не проходит пару недель.
Чтобы точно знать, какие реакции возможны после прививки, внимательно изучите инструкцию к вакцине. Советуем соблюдать следующие правила после прививки:
- Место укола не мочить и не нагревать, оно должно быть сухим. Выбирайте одежду, чтобы место инъекции не потело.
- Когда моетесь, не трите место укола мочалкой, лучше, если и мыло не будет на него попадать.
- Ничем не обрабатывайте ранку, в том числе мазями, кремами, зеленкой и йодом.
- Не трите и не расчесывайте ранку, не давайте это делать ребенку.
- Одеваться надо в свободную одежду, чтобы место укола не терлось о ткань.
 Лучше выбрать одежду из натуральных тканей, так как синтетика может вызвать аллергическую реакцию.
Лучше выбрать одежду из натуральных тканей, так как синтетика может вызвать аллергическую реакцию.
Как облегчить состояние
Так как покраснение относится к обычным местным реакция на вакцину, настоятельно советуем вам не впадать в панику и избегать самолечения: через 1-3 дня покраснение само пройдет, а неверно выбранные лекарства могут только ухудшить самочувствие. Если ребенок пытается расчесать место укола, можно прикрыть его легкой марлевой повязкой.
Когда пора обратиться к врачу
В подавляющем большинстве случае небольшое покраснение в месте инъекции – совершенно нормальная реакция и она проходит в течение 3-х дней, но иногда реакция затягивается, и это уже повод посоветоваться с врачом:
- диаметр покраснения заметно увеличился вплоть до 8 см.
- реакция не проходит долее 3-х дней
- отек распространяется на соседний сустав
Вакцина БЦЖ: надежда на борьбу с пандемией COVID-19 в условиях кризиса
1. Paules CI, Marston HD, Fauci AS..
Коронавирусные инфекции – больше, чем просто простуда. ДЖАМА. 2020;323(8):707. [опубликовано в Интернете до печати, 23 января 2020 г.]. дои: 10.1001/jama.2020.0757. [PubMed] [CrossRef] [Google Scholar]
Paules CI, Marston HD, Fauci AS..
Коронавирусные инфекции – больше, чем просто простуда. ДЖАМА. 2020;323(8):707. [опубликовано в Интернете до печати, 23 января 2020 г.]. дои: 10.1001/jama.2020.0757. [PubMed] [CrossRef] [Google Scholar]
2. де Вит Э., ван Доремален Н., Фальзарано Д., Мюнстер В.Дж. SARS и MERS: последние сведения о новых коронавирусах. Nature Rev Microbiol. 2016;14(8):523. doi: 10.1038/nrmicro.2016.81. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
3. Малик Ю.С., Сиркар С., Бхат С., Хан С., Дхама К., Дадар М., Тивари Р., Чайкумпа В. Возникающий новый коронавирус (2019-nCoV) — текущий сценарий, эволюционная перспектива, основанная на анализе генома и последних разработках. Вет Квартал. 2020а; 40(1):68–76. дои: 10.1080/01652176.2020.1727993. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
4. Дхама К., Хан С., Тивари Р., Сиркар С., Бхат С., Малик Ю.С., Сингх К.П., Чайкумпа В., Бонилья-Алдана К., Моралес А.Дж.Р. . Коронавирусная болезнь 2019–COVID-19.
5. Отчет ВОЗ о коронавирусной болезни (COVID-19) № 201 (по состоянию на 8-й Август 2020). [по состоянию на август 2020 г. 9]. https://www.who.int/docs/default-source/coronaviruse/situation-reports/20200808-covid-19-sitrep-201.pdf?sfvrsn=121bb855_2
6. Peeri NC, Shrestha N, Rahman MS, Заки Р., Тан З., Биби С., Багбанзаде М., Агамохаммади Н., Чжан В., Хак У. SARS, MERS и новый коронавирус (COVID-19)) эпидемии, новейшие и крупнейшие глобальные угрозы здоровью: какие уроки мы извлекли? Int J Эпидемиол. 2020;dyaa033. [опубликовано в Интернете до печати, 22 февраля 2020 г.]. doi: 10.1093/ije/dyaa033. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
7. Малик Ю.С., Сиркар С., Бхат С., Винодкумар О.Р., Тивари Р., Сах Р., Рабаан А.А., Моралес А.Дж.Р., Дхама К. Возникающая коронавирусная болезнь ( COVID-19), пандемическая чрезвычайная ситуация в области общественного здравоохранения, связанная с животными: текущее обновление статуса.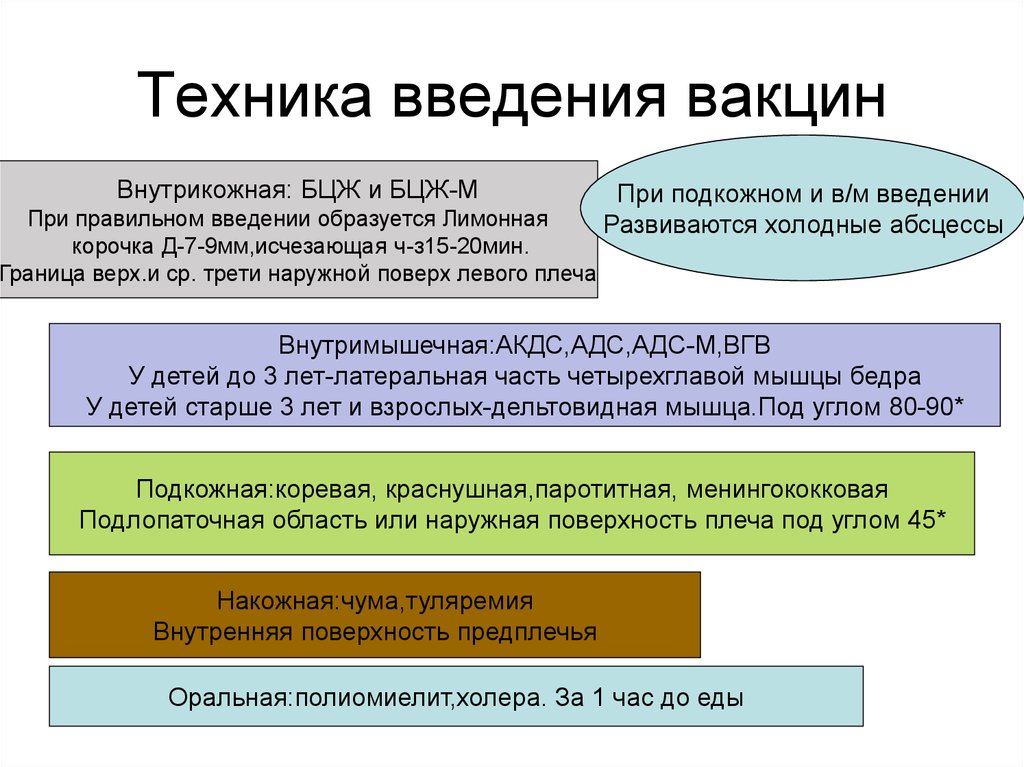 Препринты. 2020b:2020030343. дои: 10.20944/препринты202003.0343.v1. [CrossRef] [Google Scholar]
Препринты. 2020b:2020030343. дои: 10.20944/препринты202003.0343.v1. [CrossRef] [Google Scholar]
8. Chan JF, Yuan S, Kok K-H, To KKW, Chu H, Yang J, Xing F, Liu J, Yip CCY, Poon RWS и др. Семейный кластер пневмонии, связанный с новым коронавирусом 2019 года, указывающий на передачу от человека к человеку: исследование семейного кластера. Ланцет. 2020;395(10223):514–23. doi: 10.1016/S0140-6736(20)30154-9. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
9. Zou L, Ruan F, Huang M, Liang L, Huang H, Hong Z, Yu J, Kang M, Song Y, Xia J и др. др. Вирусная нагрузка SARS-CoV-2 в образцах верхних дыхательных путей инфицированных пациентов. N Engl J Med. 2020;382(12):1177–79. дои: 10.1056/NEJMc2001737. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
10. Young BE, Ong SWX, Kalimuddin S, Low JG, Tan SY, Loh J, Ng O-T, Marimuthu K, Ang LW, Mak TM и др. др. Эпидемиологические особенности и клиническое течение пациентов, инфицированных SARS-CoV-2 в Сингапуре.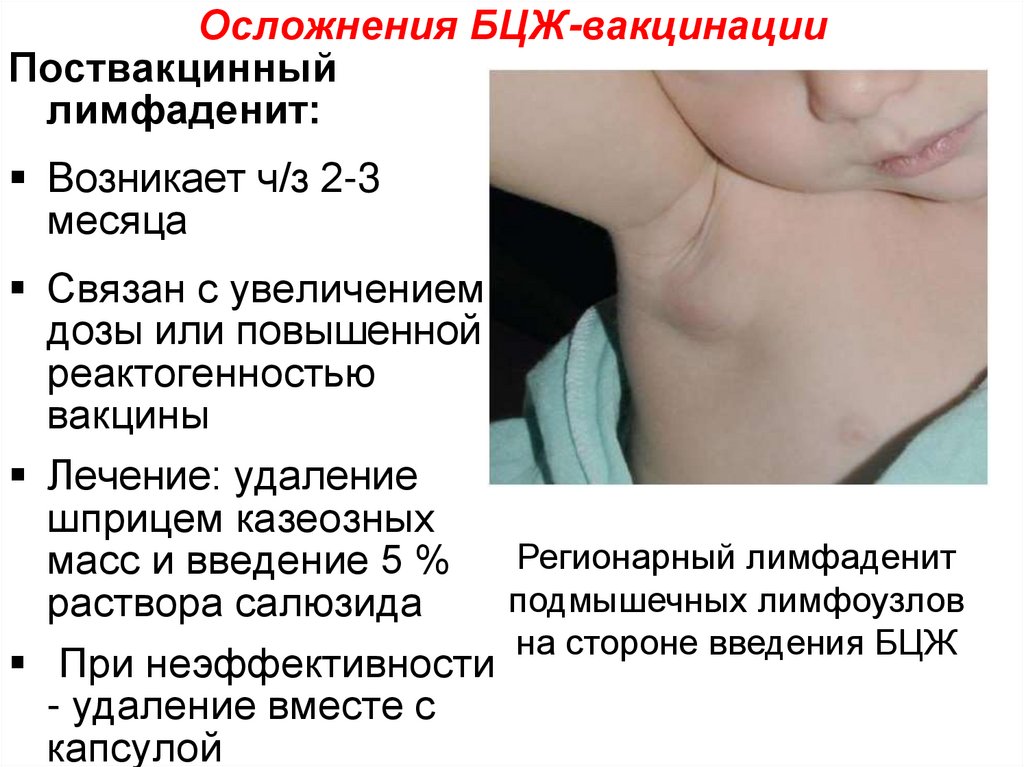 ДЖАМА. 2020;323(15):1488–94. [опубликовано в Интернете до печати, 3 марта 2020 г.] [опубликованное исправление появляется в JAMA. doi: 10.1001/jama.2020.4372]. дои: 10.1001/jama.2020.3204. [Бесплатная статья PMC] [PubMed] [CrossRef] [CrossRef] [Google Scholar]
ДЖАМА. 2020;323(15):1488–94. [опубликовано в Интернете до печати, 3 марта 2020 г.] [опубликованное исправление появляется в JAMA. doi: 10.1001/jama.2020.4372]. дои: 10.1001/jama.2020.3204. [Бесплатная статья PMC] [PubMed] [CrossRef] [CrossRef] [Google Scholar]
11. Peiris JS, Yuen KY, Osterhaus AD, Stöhr K. Тяжелый острый респираторный синдром. N Engl J Med. 2003;349(25):2431–41. дои: 10.1056/NEJMra032498. [PubMed] [CrossRef] [Google Scholar]
12. Дхама К., Шарун К., Тивари Р., Дадар М., Малик Ю.С., Сингх К.П., Чайкумпа В. COVID-19, новая коронавирусная инфекция: достижения и перспективы в разработке и разработка вакцин, иммунотерапевтических и терапевтических средств. Hum Вакцина Иммунотер. 2020;1–7. [опубликовано в Интернете до печати, 18 марта 2020 г.]. дои: 10.1080/21645515.2020.1735227. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
13. Чжан Ю.З., Холмс Э.К. Геномный взгляд на происхождение и появление SARS-CoV-2. Клетка. 2020;181(2):223–27. doi: 10. 1016/j.cell.2020.03.035. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
1016/j.cell.2020.03.035. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
14. Yi Y, Lagniton PNP, Ye S, Li E, Xu RH. COVID-19: что известно и что предстоит узнать о новой коронавирусной болезни. Int J Biol Sci. 2020;16(10):1753–66. Опубликовано 15 марта 2020 г. doi: 10.7150/ijbs.45134. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
15. Shann F. Неспецифические эффекты вакцин и снижение детской смертности. Клин Терапевт. 2013;35(2):109–14. doi: 10.1016/j.clithera.2013.01.007. [PubMed] [CrossRef] [Google Scholar]
16. Moorlag SJCFM, Arts RJW, van Crevel R, Netea MG. Неспецифические эффекты вакцины БЦЖ при вирусных инфекциях. Клин Микробиол Инфект. 2019;25(12):1473–78. doi: 10.1016/j.cmi.2019.04.020. [PubMed] [CrossRef] [Google Scholar]
17. Kleinnijenhuis J, Quintin J, Preijers F, Joosten LAB, Ifrim DC, Saeed S, Jacobs C, van Loenhout J, de Jong D, Stunnenberg HG, et al. Bacille callette-guerin индуцирует NOD2-зависимую неспецифическую защиту от повторного заражения посредством эпигенетического перепрограммирования моноцитов.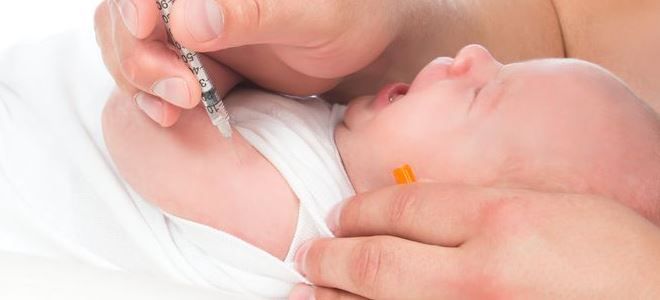 Proc Natl Acad Sci USA. 2012;109(43): 17537–42. doi: 10.1073/pnas.1202870109. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Proc Natl Acad Sci USA. 2012;109(43): 17537–42. doi: 10.1073/pnas.1202870109. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
18. Jin Y, Yang H, Ji W, Wu W, Chen S, Zhang W, Duan G. Вирусология, эпидемиология, патогенез и контроль COVID -19. Вирусы. 2020;12(4):E372. Опубликовано 27 марта 2020 г. doi: 10.3390/v12040372. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
19. Аюб Б.М. Клинические испытания вакцины против COVID-19 должны учитывать многократные дозы БЦЖ. Аптека. 2020;75(4):159. дои: 10.1691/ф.2020.0444. [PubMed] [CrossRef] [Google Scholar]
20. Alakwaa FM, Gilbert JA. Использование диданозина в качестве потенциального средства для лечения COVID-19 с использованием данных секвенирования одноклеточной РНК. Мсистемы. 2020;5(2):e00297–20. doi: 10.1128/mSystems.00297-20. [Статья PMC бесплатно] [PubMed] [CrossRef] [Google Scholar]
21. Zhang TY, Zhong B. Решение потенциальной чрезвычайной глобальной проблемы с поставками лекарств, связанной с гидроксихлорохином для лечения COVID-19. Мед Препарат Дисков. 2020;5:100036. doi: 10.1016/j.medidd.2020.100036. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Мед Препарат Дисков. 2020;5:100036. doi: 10.1016/j.medidd.2020.100036. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
22. Пико С., Марти А., Бьенвену А.Л., Блумберг Л.Х., Дюпуи-Каме Дж., Карневале П., Кано С., Джонс М.К., Даниэль-Рибейро К.Т., Мас-Кома С. и др. Коалиция: пропаганда перспективных клинических испытаний для проверки постэкспозиционного потенциала гидроксихлорохина против COVID-19. Одно Здоровье. 2020;9:100131. [опубликовано в Интернете до печати, 4 апреля 2020 г.]. doi: 10.1016/j.onehlt.2020.100131. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
23. Caly L, Druce JD, Catton MG, Jans DA, Wagstaff KM. Одобренный FDA препарат ивермектин ингибирует репликацию SARS-CoV-2 in vitro. Противовирусный рез. 2020;178:104787. [опубликовано в Интернете до печати, 3 апреля 2020 г.]. doi: 10.1016/j.antiviral.2020.104787. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
24. Патри А., Фабброчини Г. Гидроксихлорохин и ивермектин: синергетическая комбинация для химиопрофилактики и лечения COVID-19?
J Am Acad Дерматол. 2020;S0190-9622(20):30557. [опубликовано в Интернете до печати, 10 апреля 2020 г.]. doi: 10.1016/j.jaad.2020.04.017. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
2020;S0190-9622(20):30557. [опубликовано в Интернете до печати, 10 апреля 2020 г.]. doi: 10.1016/j.jaad.2020.04.017. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
25. Damle B, Vourvahis M, Wang E, Leaney J, Corrigan B. Взгляды клинической фармакологии на противовирусную активность азитромицина и его использование при COVID-19. Клин Фармакол Тер. 2020;108(2):201–11. [опубликовано в Интернете до печати, 17 апреля 2020 г.]. дои: 10.1002/cpt.1857. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
26. Ford N, Vitoria M, Rangaraj A, Norris SL, Calmy A, Doherty M. Систематический обзор эффективности и безопасности антиретровирусных препаратов против SARS, MERS или COVID-19: начальная оценка. J Int AIDS Soc. 2020;23(4):e25489. дои: 10.1002/jia2.25489. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
27. Zhang L, Liu Y. Возможные вмешательства в отношении нового коронавируса в Китае: системный обзор. J Med Virol. 2020;92(5):479–90. doi: 10.1002/jmv.25707. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
doi: 10.1002/jmv.25707. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
28. Явуз С., Юнал С. Противовирусное лечение COVID-19. Турецкий J Med Sci. 2020; 50 (SI–1): 611–19. doi: 10.3906/sag-2004-145. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
29. Salvi R, Patankar P. Новые фармакотерапевтические методы лечения COVID-19. Биомед Фармаколог. 2020. Май;14:110267. doi: 10.1016/j.biopha.2020.110267. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
30. Бачанова В., Епископ М.Р., Дахи П., Долария Б., Групп С.А., Латтин Б.Х., Джанакирам М., Мазиарз Р.Т., МакГирк Д.П., Наступил Л.Дж. CAR T-клеточная терапия во время COVID-19Пандемия. Биол Кровавый Мозг Транс. 2020;26(7):1239–46. doi: 10.1016/j.bbmt.2020.04.008. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
31. Zhao RC. Терапия коронавирусной болезни на основе стволовых клеток 2019. Stem Cells Dev. 2020;29(11):679–81. [опубликовано в Интернете до печати, 17 апреля 2020 г. ]. doi: 10.1089/scd.2020.0071. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
]. doi: 10.1089/scd.2020.0071. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
32. Warren TK, Wells J, Panchal RG, Stuthman KS, Garza NL, Van Tongeren SA, Dong L, Retterer CJ, Eaton BP, Pegoraro G, и другие. Защита от филовирусных заболеваний с помощью нового аналога нуклеозидов широкого спектра действия BCX4430. Природа. 2014. апр 17;508(7496): 402–05. дои: 10.1038/nature13027. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
33. Kawase M, Shirato K, van der Hoek L, Taguchi F, Matsuyama S. Одновременное лечение клеток бронхиального эпителия человека ингибиторами сериновых и цистеиновых протеаз предотвращает проникновение коронавируса тяжелого острого респираторного синдрома. Дж Вирол. 2012. Июнь; 86 (12): 6537–45. doi: 10.1128/ОВИ.00094-12. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
34. Kang S, Peng W, Zhu Y, Lu S, Zhou M, Lin W, Wu W, Huang S, Jiang L, Luo X и др. др. Недавний прогресс в понимании 2019новый коронавирус (SARS-CoV-2), связанный с респираторным заболеванием человека: обнаружение, механизмы и лечение.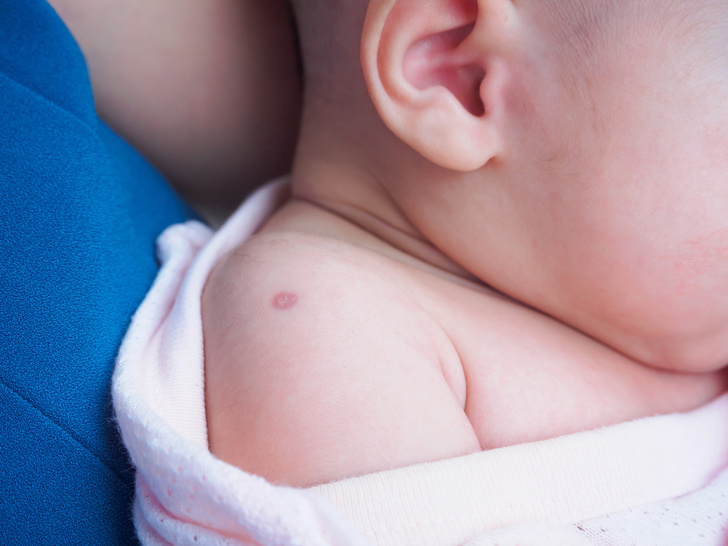 Противомикробные агенты Int J. 2020.
29 марта (5): 105950. doi: 10.1016/j.ijantimicag.2020.105950. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Противомикробные агенты Int J. 2020.
29 марта (5): 105950. doi: 10.1016/j.ijantimicag.2020.105950. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
35. Jiang L, Wang N, Zuo T, Shi X, Poon KM, Wu Y, Gao F, Li D, Wang R, Guo J и др. др. Мощная нейтрализация БВРС-КоВ человеческими нейтрализующими моноклональными антителами к гликопротеину вирусного шипа. Sci Transl Med. 2014. апр 30;6(234):234ra59. doi: 10.1126/scitranslmed.3008140. [PubMed] [CrossRef] [Google Scholar]
36. Jawhara S. Может ли внутривенный иммуноглобулин, полученный от выздоровевших пациентов с коронавирусом, защитить от COVID-19 и укрепить иммунную систему новых пациентов? Int J Mol Sci. 2020;21(7):E2272. Опубликовано 25 марта 2020 г. doi: 10.3390/ijms21072272. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
37. Moderna объявляет о первом участнике, получившем дозу в фазе 1 исследования мРНК-вакцины (мРНК-1273) против нового коронавируса под руководством Национального института здравоохранения
[доступ в мае
19, 2020]. https://investors.modernatx.com/node/8466/pdf
https://investors.modernatx.com/node/8466/pdf
38. Zhu FC, Li YH, Guan XH, Hou L-H, Wang W-J, Li J-X, Wu S-P, Wang B-S, Wang Z, Wang L, et др. Безопасность, переносимость и иммуногенность рекомбинантной аденовирусной векторной вакцины против COVID-19 типа 5: открытое, нерандомизированное, первое испытание на людях с повышением дозы. Ланцет. 2020;395(10240):1845–54. doi: 10.1016/S0140-6736(20)31208-3. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
39. Smith TRF, Patel A, Ramos S, Elwood D, Zhu X, Yan J, Gary EN, Walker SN, Schultheis K, Purwar M, et др. Иммуногенность ДНК-вакцины-кандидата против COVID-19. Нац коммун. 2020;11(1):2601. Опубликовано 20 мая 2020 г. doi: 10.1038/s41467-020-16505-0. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
40. Angelidou A, Diray-Arce J, Conti MG, Smolen KK, van Haren SD, Dowling DJ, Husson RN, Levy O. BCG в качестве примера исследование разработки прецизионных вакцин: уроки гетерогенности вакцин, тренированного иммунитета и иммунного онтогенеза. Фронт микробиол. 2020;11:332. Опубликовано 11 марта 2020 г. doi: 10.3389/fmicb.2020.00332. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Фронт микробиол. 2020;11:332. Опубликовано 11 марта 2020 г. doi: 10.3389/fmicb.2020.00332. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
41. Raviglione MC, Pio A. Эволюция политики ВОЗ по борьбе с туберкулезом, 1948-2001 гг. Ланцет. 2002;359(9308):775–80. doi: 10.1016/s0140-6736(02)07880-7. [PubMed] [CrossRef] [Google Scholar]
42. Hooft van Huijsduijnen R, Kojima S, Carter D, Okabe H, Sato A, Akahata W, Wells TNC, Katsuno K. Переоценка терапевтических антител для забытых и тропических болезней. PLoS Negl Trop Dis. 2020;14(1):e0007860. Опубликовано 30 января 2020 г. doi: 10.1371/journal.pntd.0007860. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
43. Al Abri S, Kasaeva T, Migliori GB, Goletti D, Zenner D, Denholm J, Al Maani A, Cirillo DM, Schön T, Lillebæk T, et al. Инструменты для реализации стратегии Всемирной организации здравоохранения по ликвидации туберкулеза: решение общих проблем в странах с высокой и низкой эндемичностью. Int J Infect Dis. 2020;92S:S60–S68. doi: 10.1016/j.ijid.2020.02.042. [PubMed] [CrossRef] [Google Scholar]
Int J Infect Dis. 2020;92S:S60–S68. doi: 10.1016/j.ijid.2020.02.042. [PubMed] [CrossRef] [Google Scholar]
44. Tsang JS, Dobaño C, VanDamme P, Moncunill G, Marchant A, Othman RB, Sadarangani M, Koff W, Kollmann TR. Улучшение вакциноиндуцированного иммунитета: может ли исходный уровень предсказать исход? Тренды Иммунол. 2020;41(6):457-465. doi: 10.1016/jit.2020.04.001. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
45. Trunz BB, Fine P, Dye C. Влияние вакцинации БЦЖ на детский туберкулезный менингит и милиарный туберкулез во всем мире: метаанализ и оценка экономической эффективности. Ланцет. 2006;367(9517):1173–80. doi: 10.1016/S0140-6736(06)68507-3. [PubMed] [CrossRef] [Google Scholar]
46. Самнер Т., Скриба Т.Дж., Пенн-Николсон А., Хазерилл М., Уайт Р.Г. Потенциальное влияние уровня населения на заболеваемость туберкулезом при использовании теста корреляции риска с характерной экспрессией мРНК для целевой профилактической терапии туберкулеза. Научный представитель 2019 г. ;9(1):11126. Опубликовано 31 июля 2019 г. doi: 10.1038/s41598-019-47645-z. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
;9(1):11126. Опубликовано 31 июля 2019 г. doi: 10.1038/s41598-019-47645-z. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
47. Mangtani P, Abubakar I, Ariti C, Beynon R, Pimpin L, Fine PEM, Rodrigues LC, Smith PG, Lipman M, Whiting PF и др. др. Защита вакциной БЦЖ от туберкулеза: систематический обзор рандомизированных контролируемых испытаний. Клин Инфекция Дис. 2014;58(4):470–80. doi: 10.1093/cid/cit790. [PubMed] [CrossRef] [Google Scholar]
48. Abubakar I, Pimpin L, Ariti C, Beynon R, Mangtani P, Sterne J, Fine P, Smith PG, Lipman M, Elliman D, et al. Систематический обзор и метаанализ текущих данных о продолжительности защиты от туберкулеза при вакцинации бациллой Кальметта-Герена. Оценка медицинских технологий. 2013;17(37):1–vi. дои: 10.3310/hta17370. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
49. Рой П., Векеманс Дж., Кларк А., Сандерсон С., Харрис Р.С., Уайт Р.Г. Потенциальное влияние возраста вакцинации БЦЖ на глобальную детскую смертность от туберкулеза: модельное исследование. Ланцет Глоб Здоровье. 2019;7(12):e1655–e1663. doi: 10.1016/S2214-109X(19)30444-9. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Ланцет Глоб Здоровье. 2019;7(12):e1655–e1663. doi: 10.1016/S2214-109X(19)30444-9. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
50. Zwerling A, Behr MA, Verma A, Brewer TF, Menzies D, Pai M. Атлас мира БЦЖ: база данных глобальных политик вакцинации БЦЖ и практики. ПЛОС Мед. 2011;8(3):e1001012. doi: 10.1371/journal.pmed.1001012. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
51. Буткевичюте Э., Джонс К.Е., Смит С.Г. Гетерологические эффекты вакцинации младенцев БЦЖ: потенциальные механизмы иммунитета. Будущая микробиология. 2018;13(10):1193–208. doi: 10.2217/fmb-2018-0026. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
52. Редельман-Сиди Г. Можно ли использовать БЦЖ для защиты от COVID-19? Нат Рев Урол. 2020:1–2. doi: 10.1038/s41585-020-0325-9. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
53. Кумар Дж., Мина Дж. Демистификация вакцины БЦЖ и COVID-19Отношение. Индийский педиатр. 2020; PII: S097475591600168. [опубликовано в Интернете до печати, 30 апреля 2020 г.] [бесплатная статья PMC] [PubMed] [Google Scholar]
[опубликовано в Интернете до печати, 30 апреля 2020 г.] [бесплатная статья PMC] [PubMed] [Google Scholar]
54. Covián C, Fernández-Fierro A, Retamal-Díaz A, Díaz FE, Vasquez AE, Lay MK, Riedel CA, Gonzalez PA, Bueno SM, Kalergis AM, et al. Индуцированная БЦЖ перекрестная защита и развитие тренированного иммунитета: значение для дизайна вакцины. Фронт Иммунол. 2019;10:2806. Опубликовано 29 ноября 2019 г. doi: 10.3389/fimmu.2019.02806. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
55. Моралес А., Эйдингер Д., Брюс А.В. Внутриполостная бацилла Кальметта-Герена в лечении поверхностных опухолей мочевого пузыря. Дж Урол. 1976;116(2):180–83. doi: 10.1016/S0022-5347(17)58737-6. [PubMed] [CrossRef] [Google Scholar]
56. Редельман-Сиди Г., Гликман М.С., Бохнер Б.Х. Механизм действия БЦЖ-терапии при раке мочевого пузыря — современная перспектива. Нат Рев Урол. 2014;11(3):153–62. doi: 10.1038/nrurol.2014.15. [PubMed] [CrossRef] [Google Scholar]
57. Александрофф А. Б., Джексон А.М., О’Доннелл М.А., Джеймс К. Иммунотерапия БЦЖ рака мочевого пузыря: 20 лет спустя. Ланцет. 1999;353(9165):1689–94. doi: 10.1016/S0140-6736(98)07422-4. [PubMed] [CrossRef] [Google Scholar]
Б., Джексон А.М., О’Доннелл М.А., Джеймс К. Иммунотерапия БЦЖ рака мочевого пузыря: 20 лет спустя. Ланцет. 1999;353(9165):1689–94. doi: 10.1016/S0140-6736(98)07422-4. [PubMed] [CrossRef] [Google Scholar]
58. Kawai K, Miyazaki J, Joraku A, Nishiyama H, Akaza H. Иммунотерапия рака мочевого пузыря Bacillus Calmette-Guerin (BCG): текущее понимание и перспективы инженерной вакцины BCG. Онкологические науки. 2013;104(1):22–27. doi: 10.1111/cas.12075. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
59. Netea MG, Schlitzer A, Placek K, Joosten LAB, Schultze JL. Врожденная и адаптивная иммунная память: эволюционный континуум в ответе хозяина на патогены. Клеточный микроб-хозяин. 2019;25(1):13–26. doi: 10.1016/j.chom.2018.12.006. [PubMed] [CrossRef] [Google Scholar]
60. Van’t Wout JW, Poell R, van Furth R. Роль макрофагов, активированных БЦЖ/ППД, в устойчивости к системному кандидозу у мышей. Сканд Дж. Иммунол. 1992;36(5):713–19. doi: 10.1111/j.1365-3083.1992. tb03132.x. [PubMed] [CrossRef] [Google Scholar]
tb03132.x. [PubMed] [CrossRef] [Google Scholar]
61. Andersen P, Kaufmann SHE. Новые стратегии вакцинации против туберкулеза. Колд Спринг Харб Перспект Мед. 2014;4(6):a018523. doi: 10.1101/cshperspect.a018523. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
62. Bertholet S, Ireton GC, Kahn M, Guderian J, Mohamath R, Stride N, Laughlin EM, Baldwin SL, Vedvick TS, Coler RN, et al. Идентификация антигенов Т-клеток человека для разработки вакцин против микобактерий туберкулеза. Дж Иммунол. 2008;181(11):7948–57. doi: 10.4049/jиммунол.181.11.7948. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
63. O’Neill LAJ, Netea MG. Индуцированный БЦЖ тренированный иммунитет: может ли он обеспечить защиту от COVID-19? Nature Rev. 2020. doi: 10.1038/s41577-020-0337-. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
64. Ван Коойк Ю., Энгеринг А., Леккеркеркер А.Н., Людвиг И.С., Гейтенбек Т.Б. Патогены используют углеводы, чтобы избежать иммунитета, индуцированного дендритными клетками. Курр Опин Иммунол. 2004;16(4):488–93. doi: 10.1016/j.coi.2004.05.010. [PubMed] [CrossRef] [Google Scholar]
Курр Опин Иммунол. 2004;16(4):488–93. doi: 10.1016/j.coi.2004.05.010. [PubMed] [CrossRef] [Google Scholar]
65. Акира С. Врожденный иммунитет и адъюванты. Philos Trans R Soc Lond B Biol Sci. 2011;366(1579):2748–55. doi: 10.1098/rstb.2011.0106. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
66. Ивасаки А., Меджитов Р. Регуляция адаптивного иммунитета врожденной иммунной системой. Наука. 2010;327(5963): 291–95. doi: 10.1126/science.1183021. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
67. Gyssens IC, Netea MG. Гетерологичные эффекты вакцинации и тренированный иммунитет. Клин Микробиол Инфект. 2019;25(12):1457–58. doi: 10.1016/j.cmi.2019.05.024. [PubMed] [CrossRef] [Google Scholar]
68. Tanner R, Villarreal-Ramos B, Vordermeier HM, McShane H. Гуморальный иммунный ответ на вакцинацию БЦЖ. Фронт Иммунол. 2019;10:1317. Опубликовано 11 июня 2019 г. doi: 10.3389/fimmu.2019.01317. [Статья бесплатно PMC] [PubMed] [CrossRef] [Google Scholar]
69. Guerra-Maupome M, Vang DX, McGill JL, Basu J. Аэрозольная вакцинация бациллой calette-guerin вызывает у телят обученный врожденный иммунный фенотип. ПЛОС Один. 2019;14(2):e0212751. Опубликовано 22 февраля 2019 г. doi: 10.1371/journal.pone.0212751. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Guerra-Maupome M, Vang DX, McGill JL, Basu J. Аэрозольная вакцинация бациллой calette-guerin вызывает у телят обученный врожденный иммунный фенотип. ПЛОС Один. 2019;14(2):e0212751. Опубликовано 22 февраля 2019 г. doi: 10.1371/journal.pone.0212751. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
70. Tarancón R, Domínguez-Andrés J, Uranga S, Ferreira AV, Groh LA, Domenech M, Gonzalez-Camacho F, Riksen NP, Aguilo N, Юсте Дж. и др. Новая живая аттенуированная противотуберкулезная вакцина MTBVAC индуцирует тренированный иммунитет и обеспечивает защиту от экспериментальной летальной пневмонии. PLoS Патог. 2020;16(4):e1008404. Опубликовано 2 апреля 2020 г. doi: 10.1371/journal.ppat.1008404. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
71. Рабаан А.А., Аль-Ахмед С.Х., Хак С., Сах Р., Тивари Р., Малик Ю.С., Дхама К., Яту М.И., Бонилья-Алдана Д.К., Родригес-Моралес А.Дж. и др. SARS-CoV-2, SARS-CoV и MERS-COV: сравнительный обзор. Инфез Мед. 2020;28(2):174–84. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
72. Салман С., Салем М.Л. Плановая иммунизация детей может защитить от COVID-19. Мед Гипотезы. 2020;140:109689. doi: 10.1016/j.mehy.2020.109689. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
73. Миллер А., Реанделар М.Дж., Фаскильоне К., Руменова В., Ян Л., Отазу Г.Х. Корреляция между политикой всеобщей вакцинации БЦЖ и снижением заболеваемости и смертности от COVID-19: эпидемиологическое исследование. medRxiv. 2020. doi: 10.1101/2020.03.24.20042937. [CrossRef] [Google Scholar]
74. Iwasaki A, rubau ND. Почему в Японии так мало случаев COVID-19? EMBO Мол Мед. 2020;12(5):e12481. doi: 10.15252/emmm.202012481. [Статья PMC бесплатно] [PubMed] [CrossRef] [Google Scholar]
75. Сингх Б.Р., Гандхарва Р. Являются ли вакцинация БЦЖ, плотность населения, средний возраст и бедность важными детерминантами распространения пандемии COVID-19, заболеваемости и смертности? Исследованиягейт. 2020. doi: 10.13140/RG.2.2.21116.49282. [CrossRef] [Google Scholar]
[CrossRef] [Google Scholar]
76. Iqbal NT, Hussain R. Неспецифический иммунитет вакцины БЦЖ: перспектива иммунотерапии БЦЖ. Испытания Вакцинол. 2014;3:143–49. doi: 10.1016/j.trivac.2014.08.002. [CrossRef] [Google Scholar]
77. Udani PM. Вакцинация БЦЖ в Индии и туберкулез у детей: новые грани. Индийский Дж. Педиат. 1994; 1994 (61): 451–62. дои: 10.1007/BF02751703. [PubMed] [CrossRef] [Google Scholar]
78. Лахария К. Краткая история вакцин и вакцинации в Индии. Индийская J Med Res. 2014;139:491. [Статья бесплатно PMC] [PubMed] [Google Scholar]
79. Курода Н. Спрос на вакцину БЦЖ из-за недоказанных заявлений о ее роли в предотвращении COVID-19 вызывает нехватку вакцин для младенцев в Японии. Pediatr Infect Dis J. 2020: опубликовать до печати. doi: 10.1097/INF.0000000000002724. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
80. O’Connor E, The J, Kamat AM, Lawrentschuk N. Использование вакцины Bacillus Calmette Gu´erin (BCG) в борьбе с COVID-19 — что старое снова новое?
Онкол будущего. 2020;16(19): 1323–25. (Epub перед печатью). doi: 10.2217/fon-2020-0381. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
2020;16(19): 1323–25. (Epub перед печатью). doi: 10.2217/fon-2020-0381. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
81. Лоутон Г. Испытания вакцины БЦЖ проверят на защиту от covid-19. Новая наука. 2020;246(3280):9. doi: 10.1016/S0262-4079(20)30836-8. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
82. Национальная медицинская библиотека США, ClinicalTrials.gov. https://clinicaltrials.gov/ct2/show/{«type»:»clinical-trial»,»attrs»:{«text»:»NCT04348370″,»term_id»:»NCT04348370″}}NCT04348370
Показатели SARS-CoV-2 у вакцинированных БЦЖ и невакцинированных молодых людей | Подростковая медицина | JAMA
Исследовательское письмо
13 мая 2020 г.
Ури Хамиэль, MD 1 ; Эран Козер, MD 1 ; Илан Янгстер, MD, MMSc 1
Принадлежность автора Информация о статье
1 Медицинский факультет им.
 Саклера, Тель-Авивский университет, Тель-Авив, Израиль
Саклера, Тель-Авивский университет, Тель-Авив, Израиль
ДЖАМА. 2020;323(22):2340-2341. дои: 10.1001/jama.2020.8189
Подтвержденные случаи заболевания коронавирусом 2019 (COVID-19) и показатели летальности в разных странах различаются. Одной из причин может быть национальная политика в отношении вакцинации детей БЦЖ, с меньшим числом подтвержденных случаев и более низким числом погибших, зарегистрированных в странах с всеобщим охватом вакцинацией БЦЖ по сравнению с теми, где нет. 1 ,2 На сравнение характеристик вспышек между странами влияют потенциальные искажающие факторы, такие как разные фазы вспышки, средний возраст пострадавшего населения, управление пандемией, количество проводимых тестов, определения смертей, связанных с COVID-19, или занижение данных.
Вакцина БЦЖ регулярно вводилась всем новорожденным в Израиле в рамках национальной программы иммунизации в период с 1955 по 1982 год. В целом уровень принятия вакцины в Израиле высок, более 90% покрытия. С 1982 года вакцину вводят только иммигрантам из стран с высокой распространенностью туберкулеза. Это изменение позволило сравнить показатели и доли инфицирования с тяжелым течением COVID-19 в 2 схожих популяциях с разным статусом БЦЖ: лица, родившиеся в течение 3 лет до и 3 года после прекращения программы универсальной вакцинации БЦЖ.
В целом уровень принятия вакцины в Израиле высок, более 90% покрытия. С 1982 года вакцину вводят только иммигрантам из стран с высокой распространенностью туберкулеза. Это изменение позволило сравнить показатели и доли инфицирования с тяжелым течением COVID-19 в 2 схожих популяциях с разным статусом БЦЖ: лица, родившиеся в течение 3 лет до и 3 года после прекращения программы универсальной вакцинации БЦЖ.
Методы
Текущая политика Министерства здравоохранения Израиля заключается в тестировании на коронавирус тяжелого острого респираторного синдрома 2 (SARS-CoV-2) у каждого пациента с симптомами, которые могут быть совместимы с COVID-19.(кашель, одышка, лихорадка). Мазки из носоглотки были протестированы с помощью полимеразной цепной реакции с обратной транскриптазой в режиме реального времени в утвержденных лабораториях в период с 1 марта по 5 апреля 2020 г. Был включен только 1 тест на пациента. Результаты были стратифицированы по году рождения. Данные о населении по конкретным годам рождения были получены из национального центрального статистического бюро. χ 2 Тесты использовались для сравнения доли и частоты положительных результатов тестов на 100 000 населения среди лиц с симптомами, совместимыми с COVID-19родившиеся с 1979 по 1981 год (возраст 39-41 год) с родившимися с 1983 по 1985 год (возраст 35-37 лет). Двусторонний порог значимости был установлен на уровне P < 0,05. Институциональный наблюдательный совет Медицинского центра Шамир признал исследование исключенным, поскольку все данные были обезличены. Статистический анализ проводили с использованием программного обеспечения R версии 3.5.3 (R Foundation).
Данные о населении по конкретным годам рождения были получены из национального центрального статистического бюро. χ 2 Тесты использовались для сравнения доли и частоты положительных результатов тестов на 100 000 населения среди лиц с симптомами, совместимыми с COVID-19родившиеся с 1979 по 1981 год (возраст 39-41 год) с родившимися с 1983 по 1985 год (возраст 35-37 лет). Двусторонний порог значимости был установлен на уровне P < 0,05. Институциональный наблюдательный совет Медицинского центра Шамир признал исследование исключенным, поскольку все данные были обезличены. Статистический анализ проводили с использованием программного обеспечения R версии 3.5.3 (R Foundation).
Результаты
Из 72060 рассмотренных результатов анализов 3064 были получены от пациентов, родившихся между 1979 и 1981 г. (1,02% когорты рожденных в этот период; 49,2% мужчин; средний возраст 40 лет) и 2869 были среди вероятно непривитых людей, родившихся между 1983 и 1985 гг. (0,96% от общей когорты рождений; 50,8% мужчин; средний возраст, 35 лет). Статистически значимой разницы в доле положительных результатов теста в группе, вакцинированной БЦЖ (361 [11,7%]), по сравнению с невакцинированной группой (299 [10,4%]; разница 1,3%, 95% ДИ, от -0,3% до 2,9%; P = ,09) или в количестве положительных результатов на 100 000 (121 в вакцинированной группе против 100 в невакцинированной группе; разница 21 на 100 000; 95% ДИ, от -10 до 50 на 100 000; P = .15). В каждой группе было 1 случай тяжелого течения заболевания (ИВЛ или госпитализация в реанимационное отделение), летальных исходов не было (таблица).
(0,96% от общей когорты рождений; 50,8% мужчин; средний возраст, 35 лет). Статистически значимой разницы в доле положительных результатов теста в группе, вакцинированной БЦЖ (361 [11,7%]), по сравнению с невакцинированной группой (299 [10,4%]; разница 1,3%, 95% ДИ, от -0,3% до 2,9%; P = ,09) или в количестве положительных результатов на 100 000 (121 в вакцинированной группе против 100 в невакцинированной группе; разница 21 на 100 000; 95% ДИ, от -10 до 50 на 100 000; P = .15). В каждой группе было 1 случай тяжелого течения заболевания (ИВЛ или госпитализация в реанимационное отделение), летальных исходов не было (таблица).
Обсуждение
В этой когорте взрослых израильтян в возрасте от 35 до 41 года вакцинация БЦЖ в детстве ассоциировалась с аналогичным уровнем положительных результатов теста на SARS-CoV-2 по сравнению с отсутствием вакцинации. Из-за небольшого числа тяжелых случаев невозможно сделать вывод о связи между статусом БЦЖ и тяжестью заболевания.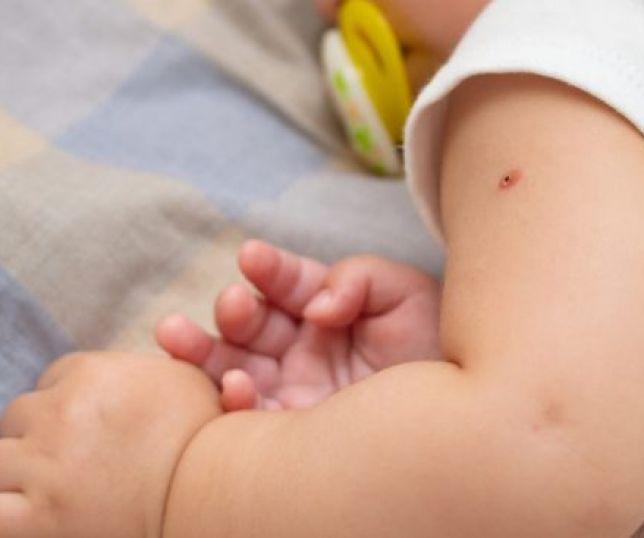 Хотя вакцина БЦЖ вводится для защиты от туберкулеза, было также обнаружено, что она оказывает неспецифическое положительное действие, например защищает от других инфекционных заболеваний 3 и для повышения иммуногенности некоторых вакцин, таких как вакцина против гриппа. 4 Считается, что эти эффекты частично опосредованы гетерологичными эффектами на адаптивный иммунитет, такими как перекрестная реактивность, опосредованная Т-клетками, а также усилением врожденного иммунного ответа. 5
Хотя вакцина БЦЖ вводится для защиты от туберкулеза, было также обнаружено, что она оказывает неспецифическое положительное действие, например защищает от других инфекционных заболеваний 3 и для повышения иммуногенности некоторых вакцин, таких как вакцина против гриппа. 4 Считается, что эти эффекты частично опосредованы гетерологичными эффектами на адаптивный иммунитет, такими как перекрестная реактивность, опосредованная Т-клетками, а также усилением врожденного иммунного ответа. 5
Сильные стороны этого исследования — большая когорта населения и сравнение 2 схожих возрастных групп, что сводит к минимуму искажающие факторы. Основным ограничением является включение населения, не родившегося в Израиле, с неизвестным статусом вакцинации. Однако иммигранты из стран, вакцинирующих БЦЖ, в этих возрастных группах составляют меньшинство (4,9% и 4,6% старшей и младшей групп населения соответственно) и не должны быть чрезмерно представлены в одной группе. 6 Кроме того, показатели на 100 000 человек не отражают уровень положительных результатов в популяции, поскольку лица, прошедшие тестирование, были предварительно отобраны на основе зарегистрированных симптомов.
6 Кроме того, показатели на 100 000 человек не отражают уровень положительных результатов в популяции, поскольку лица, прошедшие тестирование, были предварительно отобраны на основе зарегистрированных симптомов.
В заключение, это исследование не поддерживает идею о том, что вакцинация БЦЖ в детстве имеет защитный эффект от COVID-19 во взрослом возрасте.
Наверх
Информация о статье
Автор, ответственный за переписку: Илан Янгстер, доктор медицины, магистр медицинских наук, отделение детских инфекционных заболеваний, Центр исследования микробиома, Медицинский центр Шамир, Зерифин 70300, Израиль ([email protected]).
Принято к публикации: 30 апреля 2020 г.
Опубликовано в Интернете: 13 мая 2020 г. исследование и берет на себя ответственность за целостность данных и точность анализа данных.
Концепция и дизайн: Hamiel, Youngster.
Сбор, анализ или интерпретация данных: Козер, Юноша.
Составление рукописи: Hamiel, Youngster.
Критическая проверка рукописи на наличие важного интеллектуального содержания: Все авторы.
Статистический анализ: Юноша.
Надзор: Юноша.
Раскрытие информации о конфликте интересов: Нет сообщений.
использованная литература
1.
Миллер А, Реанделар MJ, Фаскильоне К, и другие. Корреляция между политикой всеобщей вакцинации БЦЖ и снижением заболеваемости и смертности от COVID-19: эпидемиологическое исследование. medRxiv . Препринт опубликован 28 марта 2020 г. doi:10.1101/2020.03.24.20042937
2.
Берг
МК, Ю.
Кью, Сальвадор
СЕ,
и другие. Обязательная вакцинация против бациллы Кальметта-Герена (БЦЖ) предсказывает сглаженные кривые распространения COVID-19. medRxiv . Препринт опубликован 4 мая 2020 г. doi:10.1101/2020.04.05.20054163
medRxiv . Препринт опубликован 4 мая 2020 г. doi:10.1101/2020.04.05.20054163
3.
Холлм-Дельгадо МГ, Стюарт ЕА, черный RE. Острая инфекция нижних дыхательных путей у детей, вакцинированных бациллой Кальметта-Герена (БЦЖ). Педиатрия . 2014;133(1):e73-e81. doi:10.1542/peds.2013-2218PubMedGoogle ScholarCrossref
4.
Leentjens Дж, Кокс М, Стокман Р, и другие. Вакцинация БЦЖ повышает иммуногенность последующей вакцинации против гриппа у здоровых добровольцев: рандомизированное плацебо-контролируемое пилотное исследование. J Infect Dis . 2015;212(12):1930-1938. doi:10.1093/infdis/jiv332PubMedGoogle ScholarCrossref
5.
Netea
MG, ван Кревель
Р. Индуцированная БЦЖ защита: влияние на врожденную иммунную память.


 Лучше выбрать одежду из натуральных тканей, так как синтетика может вызвать аллергическую реакцию.
Лучше выбрать одежду из натуральных тканей, так как синтетика может вызвать аллергическую реакцию.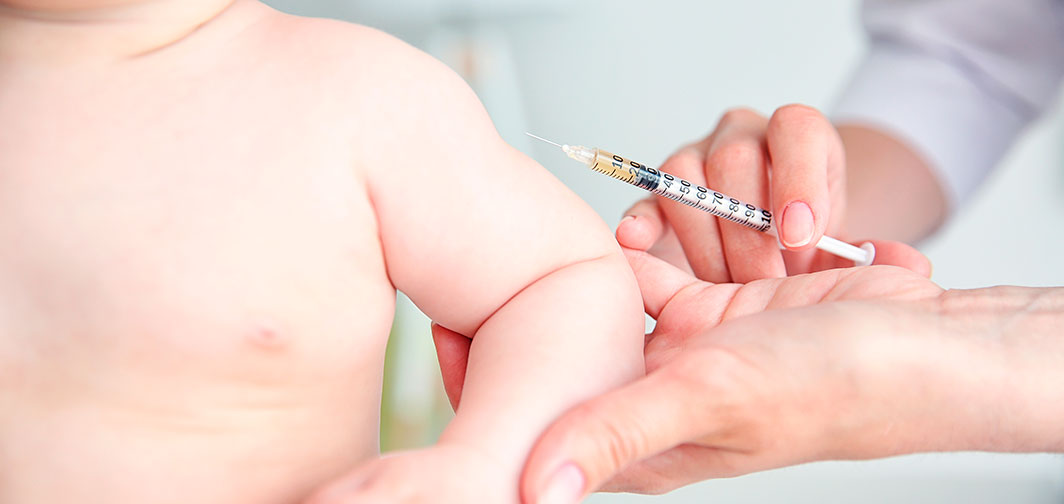 Саклера, Тель-Авивский университет, Тель-Авив, Израиль
Саклера, Тель-Авивский университет, Тель-Авив, Израиль