лиофилизат для приготовления суспензии для внутрикожного введения, 0.05 мг/доза — Энциклопедия лекарств РЛС
Вакцина туберкулезная (БЦЖ) (лиофилизат для приготовления суспензии для внутрикожного введения, 0.05 мг/доза), инструкция по медицинскому применению РУ № Р N001969/01
Дата последнего изменения: 26.07.2018
Содержание
- Действующее вещество
- ATX
- Нозологическая классификация (МКБ-10)
- Фармакологическая группа
- Лекарственная форма
- Состав
- Описание лекарственной формы
- Фармакокинетика
- Фармакодинамика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Отзывы
Действующее вещество
ATX
J07AN01 Туберкулезная живая ослабленная вакцина
Нозологическая классификация (МКБ-10)
Список кодов МКБ-10
Фармакологическая группа
Вакцины, сыворотки, фаги и анатоксины
Лекарственная форма
Лиофилизат для приготовления суспензии для внутрикожного введения
Состав
Одна доза содержит:
Действующее вещество:
Лиофилизат Mycobacterium bovis BCG 0,05 мг
Вспомогательные вещества:
Натрия глутамата моногидрат не более 0,3 мг
Раствор натрия хлорида 0,9% для инъекций до 0,1 мл
Препарат не содержит консервантов
и антибиотиков. Выпускается в комплекте с растворителем — натрия хлорид
растворитель для приготовления лекарственных форм для инъекций 0,9%.
Выпускается в комплекте с растворителем — натрия хлорид
растворитель для приготовления лекарственных форм для инъекций 0,9%.
Описание лекарственной формы
Лиофилизат. Однородная пористая масса, порошкообразная или в виде тонкой ажурной таблетки (колечка) белого или светло-желтого цвета. Гигроскопична.
Фармакокинетика
Вакцина БЦЖ — иммунобиологический препарат, исследования фармакокинетики не проводились.
Фармакодинамика
Вакцина представляет собой культуру микобактерий вакцинного штамма Mycobacterium bovis, субштамм BCG-1 (Russia), лиофилизированную в 1,5% растворе стабилизатора — натрия глутамата моногидрата.
Живые микобактерии вакцинного штамма БЦЖ-1, размножаясь в организме привитого, приводят к развитию длительного иммунитета к туберкулезу.
В норме у вакцинированных на месте
внутрикожного введения вакцины БЦЖ через 4–6 недель последовательно развивается местная
специфическая реакция в виде инфильтрата, папулы, пустулы, язвы размером 5–10
мм в диаметре. Реакция подвергается обратному развитию в течение 2–3 мес.,
иногда и в более длительные сроки. У ревакцинированных местная реакция
развивается через 1–2 недели. У 90–95% вакцинированных на месте прививки
формируется поверхностный рубчик размером до 10 мм.
Реакция подвергается обратному развитию в течение 2–3 мес.,
иногда и в более длительные сроки. У ревакцинированных местная реакция
развивается через 1–2 недели. У 90–95% вакцинированных на месте прививки
формируется поверхностный рубчик размером до 10 мм.
Показания
Активная специфическая профилактика туберкулеза у детей на территориях с показателями заболеваемости туберкулезом, превышающими 80 на 100 тыс. населения, а также при наличии в окружении новорожденного больных туберкулезом.
Противопоказания
Вакцинация
1. Недоношенность — масса тела при рождении менее 2500 г.
2. Внутриутробная гипотрофия III–IV степени.
3. Острые заболевания. Вакцинация
откладывается до окончания острых проявлений заболевания и обострения
хронических заболеваний (внутриутробная инфекция, гнойно-септические
заболевания, гемолитическая болезнь новорожденных среднетяжелой и тяжелой
формы, тяжелые поражения нервной системы с выраженной неврологической
симптоматикой, генерализованные кожные поражения и т.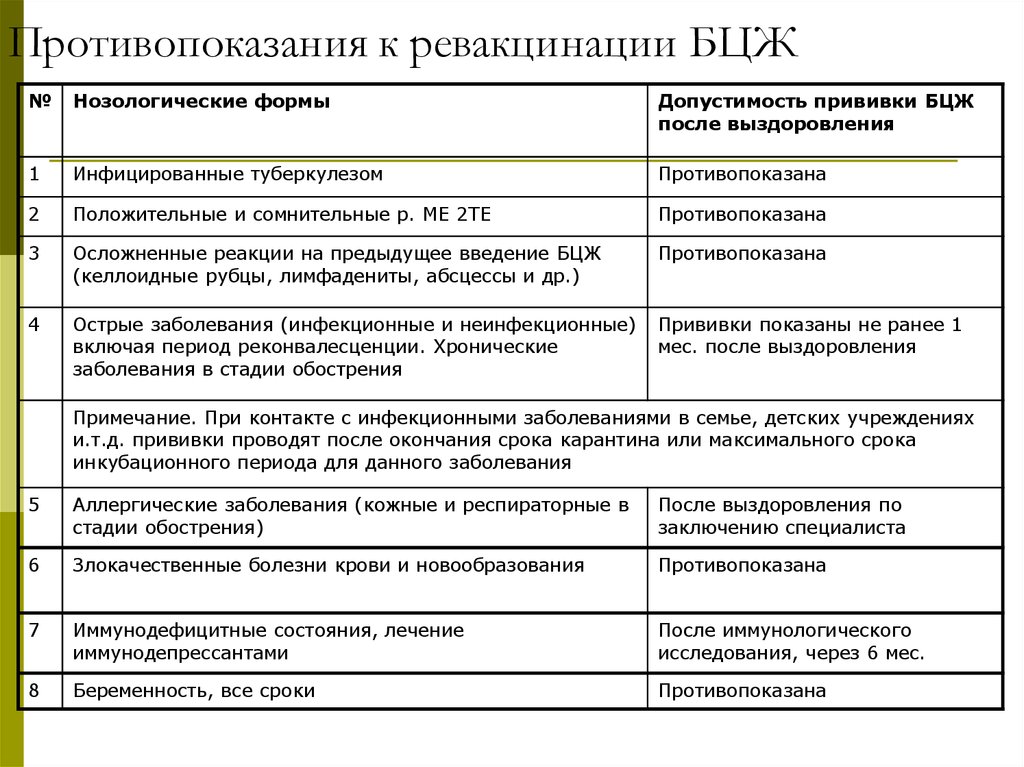
4. Иммунодефицитное состояние (первичное), злокачественные новообразования.
При назначении иммунодепрессантов и лучевой терапии прививку проводят не ранее, чем через 6 мес после окончания лечения.
5. Генерализованная инфекция БЦЖ, выявленная у других детей в семье.
6. Детям, рожденным матерями, необследованными на ВИЧ во время беременности и родов, а также детям, рожденным ВИЧ-инфицированными матерями, не получавшими трехэтапную химиопрофилактику передачи ВИЧ от матери к ребенку, вакцинация не проводится до установления ВИЧ-статуса ребенка в возрасте 18 месяцев.
Вакцинация против туберкулеза детей, рожденных от матерей с ВИЧ-инфекцией и получавших трехэтапную химиопрофилактику передачи ВИЧ от матери к ребенку (во время беременности, родов и в период новорожденности), проводится в родильном доме вакциной туберкулезной для щадящей первичной иммунизации (БЦЖ-М).
Дети, имеющие противопоказания к
иммунизации вакциной БЦЖ, прививаются вакциной БЦЖ-М с соблюдением инструкции к
этой вакцине.
Ревакцинация
1. Острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний, в том числе аллергических. Прививку проводят через 1 мес. после выздоровления или наступления ремиссии.
2. Иммунодефицитные состояния, злокачественные заболевания крови и новообразования.
При назначении иммунодепрессантов и лучевой терапии прививку проводят не ранее, чем через 6 мес. после окончания лечения.
3. ВИЧ-инфекция, обнаружение нуклеиновых кислот ВИЧ молекулярными методами.
4. Больные туберкулезом, лица, перенесшие туберкулез и инфицированные микобактериями.
5. Положительная и сомнительная реакция на пробу Манту с 2 ТЕ ППД-Л.
6. Осложнения на предыдущее введение вакцины БЦЖ.
При контакте с инфекционными
больными в семье, детском учреждении и т.д. прививки проводят по окончании
срока карантина или максимального срока инкубационного периода для данного
заболевания.
Лица, временно освобожденные от прививок, должны быть взяты под наблюдение и учет, и привиты после полного выздоровления или снятия противопоказаний. В случае необходимости проводят соответствующие клинико-лабораторные обследования.
Применение при беременности и кормлении грудью
Не применимо. Препарат используется для вакцинации детей.
Способ применения и дозы
Вакцину БЦЖ применяют внутрикожно в дозе 0,05 мг в 0,1 мл прилагаемого растворителя (раствор натрия хлорида 0,9% для инъекций).
Вакцинацию осуществляют здоровым новорожденным детям на 3–7 день жизни (как правило, в день выписки из родильного дома).
Дети, не привитые в период новорожденности, получают после выздоровления вакцину БЦЖ-М. Детям в возрасте 2 мес. и старше предварительно проводят пробу Манту с 2 ТЕ очищенного туберкулина в стандартном разведении и вакцинируют только туберкулин-отрицательных.
Ревакцинации подлежат дети в
возрасте 7 лет, имеющие отрицательную реакцию на пробу Манту с 2 ТЕ ППД-Л.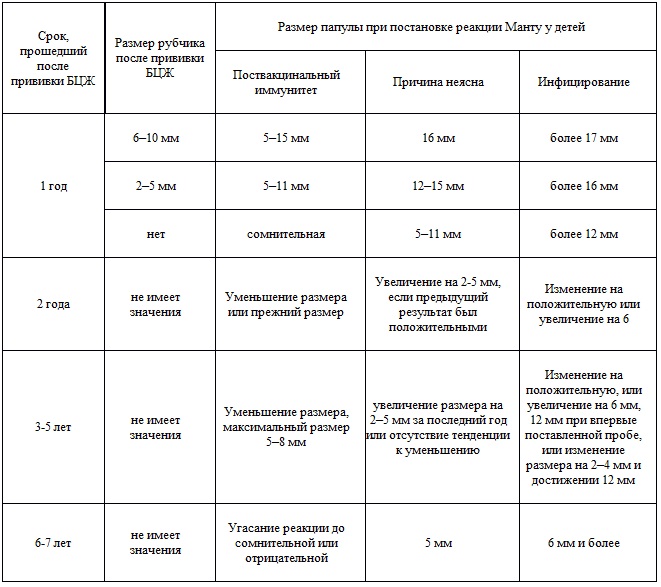 Реакция Манту считается отрицательной при полном отсутствии инфильтрата,
гиперемии или при наличии уколочной реакции (1 мм). Инфицированные микобактериями
туберкулеза дети, имеющие отрицательную реакцию на пробу Манту, ревакцинации не
подлежат. Интервал между постановкой пробы Манту и ревакцинацией должен быть не
менее 3 дней и не более 2 недель.
Реакция Манту считается отрицательной при полном отсутствии инфильтрата,
гиперемии или при наличии уколочной реакции (1 мм). Инфицированные микобактериями
туберкулеза дети, имеющие отрицательную реакцию на пробу Манту, ревакцинации не
подлежат. Интервал между постановкой пробы Манту и ревакцинацией должен быть не
менее 3 дней и не более 2 недель.
Прививки должен проводить
специально обученный и имеющий сертификат медицинский персонал родильных домов
(отделений), отделений выхаживания недоношенных, детских поликлиник или
фельдшерско-акушерских пунктов. Вакцинацию новорожденных проводят в утренние
часы в специально отведенной комнате после осмотра детей педиатром. В
поликлиниках отбор детей на вакцинацию предварительно проводит врач (фельдшер)
с обязательной термометрией в день прививки, учетом медицинских
противопоказаний и данных анамнеза. При необходимости проводят консультацию с
врачами-специалистами, исследование крови и мочи.
Факт выполнения вакцинации (ревакцинации) регистрируют в установленных учетных формах с указанием даты прививки, названия вакцины, предприятия- производителя, номера серии, и срока годности препарата.
Для вакцинации (ревакцинации)
применяют одноразовые стерильные туберкулиновые шприцы вместимостью 1 мл с
тонкими короткими иглами с коротким срезом. Для внесения в ампулу с вакциной
растворителя используют одноразовый стерильный шприц вместимостью 2 мл с
длинной иглой. Запрещается применять шприцы и иглы с истекшим сроком годности и
инсулиновые шприцы, у которых отсутствует градуировка в мл. Запрещается
проводить прививку безигольным инъектором. После каждой инъекции шприц с иглой
и ватные тампоны замачивают в аттестованном дезинфицирующем растворе (следуя
режимам дезинфекции, указанным в инструкции по применению), а затем
централизованно уничтожают. Запрещается применение для других целей
инструментов, предназначенных для проведения прививок против туберкулеза.
Запрещается применение для других целей
инструментов, предназначенных для проведения прививок против туберкулеза.
Вакцину хранят в холодильнике (под замком) в кабинете для прививок. Лица, не имеющие отношения к вакцинации БЦЖ, в помещение, где проводятся прививки (родильный дом) и в прививочный кабинет (поликлиника), в день прививок не допускаются. В день вакцинации (ревакцинации) БЦЖ в прививочном кабинете (комнате) запрещается проводить другие профилактические прививки.
Ампулы с вакциной перед вскрытием тщательно просматривают.
Препарат не подлежит применению при:
— отсутствии маркировки на ампуле или неправильном ее заполнении;
— истекшем сроке годности;
— наличии трещин и насечек на ампуле;
— изменении физических свойств препарата (изменение цвета, сморщенная таблетка и т.д.).
Вакцину растворяют
непосредственно перед употреблением стерильным раствором натрия хлорида 0,9%
для инъекций, приложенным к вакцине. Растворитель должен быть прозрачным,
бесцветным и не иметь посторонних включений.
Растворитель должен быть прозрачным,
бесцветным и не иметь посторонних включений.
Вакцина герметизирована под вакуумом: Шейку и головку ампулы обтирают спиртом. Сначала надпиливают и осторожно, с помощью пинцета, отламывают место запайки. Затем надпиливают и отламывают шейку ампулы, завернув надпиленный конец в стерильную марлевую салфетку.
Вакцина герметизирована под инертным газом: Шейку и головку ампулы обтирают спиртом. Отламывают шейку ампулы по кольцу или точке надлома, завернув головку в стерильную марлевую салфетку.
Для получения дозы 0,05 мг
БЦЖ в 0,1 мл в ампулу, содержащую 20 доз вакцины, переносят стерильным
шприцем 2 мл раствора натрия хлорида 0,9% для инъекций, а в ампулу,
содержащую 10 доз вакцины — 1 мл раствора натрия хлорида 0,9% для
инъекций. Вакцина должна раствориться в течение 1 мин. Допускается наличие
хлопьев, которые должны разбиваться при 2–4-кратном перемешивании с помощью
шприца (не допускается попадание воздуха в шприц). Растворенная вакцина должна
иметь вид грубодисперсной суспензии белого с сероватым или желтоватым оттенком
цвета. При наличии в разведенном препарате крупных хлопьев, которые не
разбиваются при 2–4-кратном перемешивании с помощью шприца, или осадка эту
ампулу с вакциной уничтожают, не используя.
Растворенная вакцина должна
иметь вид грубодисперсной суспензии белого с сероватым или желтоватым оттенком
цвета. При наличии в разведенном препарате крупных хлопьев, которые не
разбиваются при 2–4-кратном перемешивании с помощью шприца, или осадка эту
ампулу с вакциной уничтожают, не используя.
Разведенную вакцину необходимо предохранять от действия солнечного и дневного света (например, цилиндром из черной бумаги). Разведенная вакцина пригодна к применению не более 1 часа после разведения при хранении в асептических условиях, при температуре от 2 до 8 °С. Обязательно ведение протокола с указанием времени разведения препарата и уничтожения ампулы с вакциной.
Для одной прививки в
туберкулиновый шприц набирают 0,2 мл (2 дозы) разведенной вакцины, затем
выпускают через иглу в стерильный ватный тампон примерно 0,1 мл вакцины
для того, чтобы вытеснить воздух и подвести поршень шприца под нужную
градуировку — 0,1 мл. Перед каждым набором вакцину следует аккуратно
перемешивать 2–3 раза с помощью шприца. Одним шприцем вакцина может быть
введена только одному ребенку.
Перед каждым набором вакцину следует аккуратно
перемешивать 2–3 раза с помощью шприца. Одним шприцем вакцина может быть
введена только одному ребенку.
Вакцину БЦЖ вводят строго внутрикожно на границе верхней и средней трети наружной поверхности левого плеча после предварительной обработки кожи 70 ° спиртом. Иглу вводят срезом вверх в поверхностный слой натянутой кожи. Сначала вводят незначительное количество вакцины, чтобы убедиться, что игла вошла точно внутрикожно, а затем всю дозу препарата (всего 0,1 мл). При правильной технике введения должна образоваться папула беловатого цвета диаметром 7–9 мм, исчезающая обычно в течение 15–20 мин.
Побочные действия
После вакцинации и ревакцинации
осложнения отмечаются редко и обычно носят местный характер (лимфадениты,
диаметром более 1 см, — регионарные, чаще подмышечные, иногда над- или
подключичные, реже — подкожные инфильтраты, холодные абсцессы, язвы, келоиды). Крайне редко встречаются персистирующая и диссеминированная БЦЖ-инфекция без
летального исхода (волчанка, оститы и др.), пост-БЦЖ синдром аллергического
характера, который возникает вскоре после прививки (узловатая эритема,
кольцевидная гранулема, сыпи и др.), чрезвычайно редко — генерализованное
поражение БЦЖ при врожденном иммунодефиците. Осложнения выявляются в различные
сроки после прививки — от нескольких недель до года и более.
Крайне редко встречаются персистирующая и диссеминированная БЦЖ-инфекция без
летального исхода (волчанка, оститы и др.), пост-БЦЖ синдром аллергического
характера, который возникает вскоре после прививки (узловатая эритема,
кольцевидная гранулема, сыпи и др.), чрезвычайно редко — генерализованное
поражение БЦЖ при врожденном иммунодефиците. Осложнения выявляются в различные
сроки после прививки — от нескольких недель до года и более.
Взаимодействие
Другие профилактические прививки могут быть проведены с интервалом не менее 1 мес. до и после вакцинации (ревакцинации) БЦЖ (за исключением вакцины против гепатита В, которую вводят в соответствии с Национальным календарем профилактических прививок в РФ).
Передозировка
Случаи передозировки не установлены.
Меры предосторожности
Введение препарата под кожу недопустимо, так как при этом образуется холодный абсцесс.
Запрещается наложение повязки и
обработка йодом и другими дезинфицирующими растворами места введения вакцины
во время развития местной прививочной реакции: инфильтрата, папулы,
пустулы, язвы; место реакции следует предохранять от механического
раздражения, особенно во время водных процедур, о чем следует
обязательно предупредить родителей ребенка.
Более полная информация о проведении вакцинопрофилактики туберкулеза представлена в Приказе Минздрава России № 109 «О совершенствовании противотуберкулезных мероприятий в Российской Федерации» от 21 марта 2003 г.
Особые указания
Неиспользованную вакцину уничтожают кипячением в течение 30 мин, автоклавированием при 126 °С 30 мин или погружением вскрытых ампул в дезинфицирующий раствор в концентрации, эффективной в отношении микобактерий туберкулеза. Концентрацию раствора и время экспозиции определяют в соответствии с инструкцией по применению дезинфицирующего средства.
Влияние на способность управлять транспортными средствами, механизмами
Не применимо. Препарат используется для вакцинации детей.
Форма выпуска
В ампулах, содержащих 0,5 мг
(10 доз) или 1,0 мг препарата (20 доз), в комплекте с растворителем —
раствором натрия хлорида 0,9% для инъекций — по 1 или 2 мл в ампуле,
соответственно.
В одной пачке картонной содержится 5 ампул вакцины БЦЖ (герметизация под вакуумом/герметизация под инертным газом) и 5 ампул раствора натрия хлорида 0,9% для инъекций (5 комплектов).
В одной пачке картонной содержится 5 ампул вакцины БЦЖ (герметизация под инертным газом) и 5 ампул раствора натрия хлорида 0,9% для инъекций в контурных ячейковых упаковках (пять комплектов).
В пачку вкладывают инструкцию по медицинскому применению.
Для ампул ШПВ-6 в пачку дополнительно вкладывают скарификатор ампульный.
Условия отпуска из аптек
Для лечебно-профилактических учреждений.
Условия хранения
Условия хранения
Хранить по СП 3.3.2.3332-16 при температуре от 2 до 8 °С.
Хранить в недоступном для детей месте.
Условия транспортирования
Транспортировать по СП 3.3.2.3332-16 при температуре от 2 до 8 °С.
Срок годности
2 года.
Не применять по истечении срока
годности.
инструкция по применению, доставка на дом
Характеристики
| Для кого | взрослые |
| Тэги | Иммуностимуляторы |
Описание
ИМУРОН-ВАК
(Вакцина БЦЖ для иммунотерапии рака мочевого пузыря)
лиофилизат для приготовления суспензии для внутрипузырного введения
Имурон-вак (Вакцина БЦЖ для иммунотерапии рака мочевого пузыря) лиофилизат для приготовления суспензии для внутрипузырного введения 25 мг или 30 мг, представляет собой живые микобактерии вакцинного штамма БЦЖ-1, лиофилизированные в 1,5 %-ном растворе глутамата натрия.
В одной ампуле Имурон-вак содержится 25 мг или 30 мг микробных клеток БЦЖ и 14,3±0,20 мг стабилизатора глутамата натрия. Препарат не содержит консервантов и антибиотиков.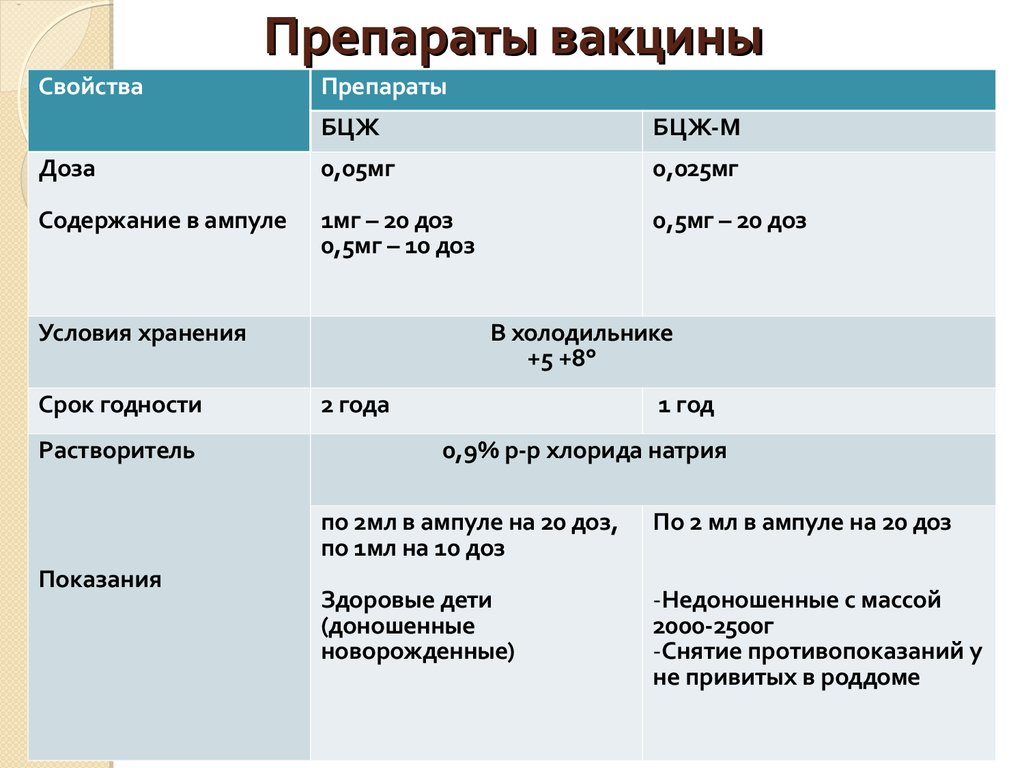
Разовая терапевтическая доза (50 – 100 мг микробных клеток БЦЖ) содержится в двух — четырех ампулах препарата.
Пористая масса, порошкообразная или в виде таблетки светло-желтого цвета. Гигроскопична.
Биологические и иммунобиологические свойства
Живые микобактерии штамма БЦЖ-1 , размножаясь внутриклеточно, приводят к неспецифической стимуляции клеточного иммунного ответа.
Назначение
Препарат предназначен для иммунотерапии поверхностного (Та, Т1, Тis) рака мочевого пузыря или профилактики его рецидивов после трансуретрального удаления опухолей.
Действующие вещества
Вакцина БЦЖ для иммунотерапии рака мочевого пузыря
Форма выпуска
Ампулы
Противопоказания
1. Ранее перенесенный туберкулез.
2. Размер местной реакции на внутрикожное введение туберкулина в дозе 2 ТЕ (проба Манту) 17 мм и более.
3. Иммунодефицитные состояния.
4. Острый цистит или макрогематурия (до исчезнования клинических проявлений).
5. Тяжелые сопутствующие заболевания в стадии декомпенсации.
Травматическая катетеризация или появление крови после катетеризации мочевого пузыря являются противопоказаниями для инстилляции БЦЖ в данный день.
Способ применения и дозы
За 3–11 суток до проведения иммунотерапии больному ставят внутрикожную пробу Манту с 2 ТЕ очищенного туберкулина в стандартном разведении. Постановку пробы и учет ответной реакции проводят в соответствии с инструкцией по применению туберкулина. Пробу Манту выполняют в противотуберкулезном диспансере или сотрудник, имеющий специальную справку-допуск для постановки туберкулиновых проб. Применение Имурон-вак разрешается при размере папулы менее 17 мм в диаметре.
Имурон-вак применяют внутрипузырно.
Внктрипузырные инсталляции рекомендуется начинать не ранее, чем через 3 недели после проведения биопсии при лечении поверхностного рака мочевого пузыря или после трансуретрального удаления опухоли.
При наличии пиурии, бактериурии, дизурии до начала лечения необходимо провести антибактериальную терапию до полной ликвидации клинических симптомов цистита.
Катетеризацию мочевого пузыря проводят эластичным катетером, не травмируя слизистую уретры и мочевого пузыря. После опорожнения мочевого пузыря его следует промыть стерильным раствором натрия хлорида 0,9% для инъекций и убедиться, что в промывной жидкости отсутствует примесь крови. После этого дозу вакцины разводят в 50 мл раствора натрия хлорида 0,9% для инъекций и вводят по катетеру в мочевой пузырь. Больного просят удерживать раствор в мочевом пузыре в течение 2 ч. Желательно, чтобы в течение этого времени пациент менял положение тела для равномерного контакта вакцины со стенками мочевого пузыря. Через 2 ч мочевой пузырь опорожняется в емкость, содержащую не менее 500 мл дезинфицирующего раствора (5% хлорамин), время экспозиции 6 ч.
Рекомендуемая разовая доза вакцины Имурон-вак 50 – 100 мг 1 раз в неделю.
Индукционный курс иммунотерапии состоит из 6 еженедельных инстилляций препарата.
При достижении полной регрессии опухоли целесообразно проведение поддерживающей иммунотерапии в такой же или уменьшенной дозе с интервалами 3 – 6 месяцев на протяжении 1 – 3 лет.
Имурон-вак хранят в специально выделенной комнате в холодильнике под замком. В этой же комнате проводят обработку катетеров и разведение вакцины. Посуду и инструменты, применяемые для БЦЖ-иммунотерапии, категорически запрещается использовать в других целях. Их хранят в отдельном шкафу, под замком.
Разведение вакцины
Ампулы с вакциной перед вскрытием тщательно просматривают.
Препарат не подлежит применению при:
— отсутствии маркировки на ампуле или неправильном ее заполнении;
— истекшем сроке годности;
— при наличии трещин и насечек на ампуле;
— при изменении физических свойств препарата (сморщенная таблетка, изменение цвета) и т.д.).
Сухую вакцину разводят непосредственно перед употреблением стерильным раствором натрия хлорида 0,9% для инъекций. Шейку и головку ампулы обтирают спиртом, место запайки ампулы (головку) надпиливают и осторожно, с помощью пинцета, отламывают. Затем надпиливают и отламывают шейку ампулы, завернув надпиленный конец в стерильную марлевую салфетку. В ампулы с вакциной переносят стерильным шприцем с длинной иглой по 3–4 мл раствора натрия хлорида 0,9% для инъекций. После экспозиции в течение 3–5 мин с последующим 3-кратным перемешиванием с помощью шприца должна образоваться мутная грубодисперсная суспензия светло-желтого цвета. Содержимое ампул тем же шприцем переносят во флакон с раствором натрия хлорида 0,9% для инъекций (общий объем — 50 мл) и тщательно размешивают.
В ампулы с вакциной переносят стерильным шприцем с длинной иглой по 3–4 мл раствора натрия хлорида 0,9% для инъекций. После экспозиции в течение 3–5 мин с последующим 3-кратным перемешиванием с помощью шприца должна образоваться мутная грубодисперсная суспензия светло-желтого цвета. Содержимое ампул тем же шприцем переносят во флакон с раствором натрия хлорида 0,9% для инъекций (общий объем — 50 мл) и тщательно размешивают.
Разведенную вакцину необходимо предохранять от действия дневного солнечного света и употреблять сразу после разведения. Ампулы из-под вакцины, флакон и катетер после процедуры погружают в дезинфицирующий раствор (5% хлорамин) на 6 ч. Допускается дезинфекция инструментария кипячением в течение 40 мин.
Побочные действия
Побочные реакции и осложнения чаще встречаются у больных с малой емкостью мочевого пузыря (менее 150 мл), после проведения лучевой терапии.
Побочные реакции.
а) Локальные:
— Дизурия отмечается у 80%, макрогематурия — у 40% больных. Появляются после 2–3 введений БЦЖ, начинаются через 2–3 ч после инстилляции и продолжаются в течение 1–2 сут. С увеличением количества инстилляций выраженность побочных реакций может нарастать. Проходят, как правило, самостоятельно или может быть проведено симптоматическое лечение.
Появляются после 2–3 введений БЦЖ, начинаются через 2–3 ч после инстилляции и продолжаются в течение 1–2 сут. С увеличением количества инстилляций выраженность побочных реакций может нарастать. Проходят, как правило, самостоятельно или может быть проведено симптоматическое лечение.
б) Системные:
— Повышение температуры тела, не превышающее 38,5 °C, отмечается у 40% больных в день инстилляции. Обычно лихорадка составляет не более 48 ч. Специального лечения не требует или могут быть применены жаропонижающие препараты.
Осложнения
а) Локальные:
— Острый цистит, не проходящий к моменту следующей инстилляции, отмечается у 20% больных. В таких случаях лечение с помощью Имурон-вак должно быть прервано. После исключения бактериального цистита немикобактериальной этиологии назначается терапия противотуберкулезными препаратами до исчезновения симптомов и в течение 2 недель после нормализации состояния. БЦЖ-терапия может быть продолжена в дозе, составляющей от 10 до 30% от первоначальной;
— Симптоматические грануломатозные циститы, простатиты, эпидидимиты у 3–5% больных. При развитии подобных осложнений БЦЖ-терапия прерывается. Проводят терапию изониазидом (300 мг/сут) и рифампицином (600 мг/сут) в течение 3 месяцев. У ряда больных развитие грануломатозных инфильтратов в области устьев мочеточников может привести к нарушению пассажа мочи из верхних мочевых путей и потребовать временного их дренирования;
При развитии подобных осложнений БЦЖ-терапия прерывается. Проводят терапию изониазидом (300 мг/сут) и рифампицином (600 мг/сут) в течение 3 месяцев. У ряда больных развитие грануломатозных инфильтратов в области устьев мочеточников может привести к нарушению пассажа мочи из верхних мочевых путей и потребовать временного их дренирования;
— Грануломатозное поражение паренхимы почки наблюдается редко. Дальнейшая БЦЖ-терапия этим больным противопоказана. Проводят терапию изониазидом (300 мг в сут), рифампицином (600 мг/сут) и этамбутолом (1200 мг в сут) до 6 мес.
б) Системные:
В развитии системных осложнений ведущее значение принадлежит гематогенному распространению БЦЖ. Как правило, они развиваются после грубых травматичных катетеризаций мочевого пузыря с последующим введением БЦЖ. Генерализации инфекции способствует ослабление иммунитета, обусловленное ВИЧ-инфекцией, приемом иммунодепрессантов и другими причинами.
— Аллергические реакции. Отмечаются в виде кожной сыпи, артритов, артралгий менее чем у 1% больных. Иммунотерапия вакциной этим больным должна быть прекращена. Назначают нестероидные противовоспалительные средства, антигистаминные препараты;
Иммунотерапия вакциной этим больным должна быть прекращена. Назначают нестероидные противовоспалительные средства, антигистаминные препараты;
— БЦЖ-сепсис отмечается крайне редко (единичные случаи). Характеризуется острым началом: повышением температуры тела выше 38,5˚C, ознобом, резким ухудшением общего состояния. Иногда отмечается падение артериального давления. Быстро развивается печеночная и почечная недостаточность. При рентгенографии грудной клетки могут выявляться очаговые изменения и инфильтраты в легких. После взятия проб для бактериологических исследований на наличие возбудителя, начинают лечение. Иммунотерапия вакциной должна быть прекращена.
Назначают терапию тремя противотуберкулезными препаратами: изониазид (300 мг в сут), рифампицин (600 мг в сут) и этамбутол (1200 мг в сут). В обязательном порядке добавляют антибиотик широкого спектра действия для лечения возможного уросепсиса не туберкулезной этиологии. Антибактериальную терапию сочетают с применением кортикостероидов: гормональная терапия предотвращает угрожающую жизни гипер-эргическую реакцию. Описаны летальные исходы БЦЖ-сепсиса.
Описаны летальные исходы БЦЖ-сепсиса.
Больной должен быть предупрежден о возможных осложнениях.
Взаимодействие с другими препаратами
Во время курса внутрипузырных инстилляций Имурон-вак следует избегать одновременного назначения средств, к которым чувствительны БЦЖ: противотуберкулезные препараты, фторхинолоны, доксицилин или гентамицин.
Условия хранения
Препарат хранят по СП 3.3.2.1248–03 при температуре от 0 до 8˚C, в недоступном для детей месте.
Транспортируют по СП 3.3.2.1248–03 при температуре от 0 до 8˚C.
Срок годности
2 года. Препарат с истекшим сроком годности применению не подлежит.
Отпуск по рецепту
Да
Вакцинация БЦЖ – Реализация стратегии ВОЗ «Остановить туберкулез»
NCBI Книжная полка. Служба Национальной медицинской библиотеки, Национальных институтов здоровья.
Реализация стратегии ВОЗ «Остановить туберкулез»: руководство для национальных программ борьбы с туберкулезом. Женева: Всемирная организация здравоохранения; 2008.
Женева: Всемирная организация здравоохранения; 2008.
Реализация стратегии ВОЗ «Остановить туберкулез»: Справочник для национальных программ борьбы с туберкулезом.
Показать подробности
- Содержание
Критерий поиска
Охват вакциной БЦЖ > 80% новорожденных и детей грудного возраста в странах, где она является частью национальной программы иммунизации детей. Вакцина БЦЖ показала защитную эффективность против туберкулезного менингита и милиарной диссеминированной болезни у детей (в среднем 86%). Он не предотвращает первичную инфекцию и, что более важно, не предотвращает реактивацию латентной легочной инфекции, основного источника бациллярного распространения в обществе. Влияние вакцинации БЦЖ на передачу 9Таким образом, 0017 M. tuberculosis ограничен.
Рекомендации ВОЗ по применению вакцины БЦЖ
В странах с высоким бременем туберкулеза однократная доза вакцины БЦЖ должна быть введена всем младенцам как можно раньше после рождения.
 Поскольку тяжелые побочные эффекты вакцинации БЦЖ крайне редки, все здоровые новорожденные должны быть вакцинированы БЦЖ, даже в районах, эндемичных по ВИЧ.
Поскольку тяжелые побочные эффекты вакцинации БЦЖ крайне редки, все здоровые новорожденные должны быть вакцинированы БЦЖ, даже в районах, эндемичных по ВИЧ.Вакцинация БЦЖ должна проводиться , а не (i) младенцам и детям со СПИДом, (ii) младенцам и детям, о которых известно, что они ВИЧ-инфицированы, или (iii) детям, о которых известно, что у них есть другие иммунодефициты.
В ситуациях, когда младенцы подверглись воздействию туберкулеза легких с положительным мазком вскоре после рождения, вакцинацию БЦЖ следует отложить до завершения шести месяцев ПЛИ.
Вакцинация медицинского персонала, особенно работников лабораторий, является вариантом в условиях повышенного риска (в частности, если персонал находится в тесном контакте с больными лекарственно-устойчивым ТБ).
Нет доказательств того, что ревакцинация повышает защиту, и ревакцинация не рекомендуется.
Страны с низким бременем ТБ могут решить ограничить вакцинацию БЦЖ новорожденными и детьми грудного возраста из признанных групп высокого риска заболевания или детей старшего возраста с отрицательным результатом ТКП.
 В некоторых группах населения с низким бременем вакцинация 1 БЦЖ была заменена интенсивным выявлением случаев заболевания и контролируемым ранним лечением.
В некоторых группах населения с низким бременем вакцинация 1 БЦЖ была заменена интенсивным выявлением случаев заболевания и контролируемым ранним лечением.
До тех пор, пока не появится улучшенная противотуберкулезная вакцина, усилия по борьбе с распространением болезни будут по-прежнему основываться на доступных в настоящее время средствах, а именно на ранней диагностике и лечении, соответствующем профилактическом лечении и других мерах общественного здравоохранения и инфекционного контроля.
Основные ссылки
Hesseling AC, et al. Риск диссеминированной бациллы Кальметта-Герена (БЦЖ) у ВИЧ-инфицированных детей. вакцина. 2007;25(1):14–18. [PubMed: 16959383]
Вакцина БЦЖ. Еженедельный эпидемиологический отчет. 2004; 4: 27–38. [PubMed: 14768305]
Вопросы, связанные с использованием БЦЖ в программах иммунизации. Женева: Всемирная организация здравоохранения; 1999 г. (WHO/V&B/99.23)
Rieder HL.
 Вмешательства по контролю и ликвидации туберкулеза. Париж: Международный союз по борьбе с туберкулезом и легочными заболеваниями; 2002.
Вмешательства по контролю и ликвидации туберкулеза. Париж: Международный союз по борьбе с туберкулезом и легочными заболеваниями; 2002.Пересмотренные рекомендации по вакцинации БЦЖ для младенцев, подверженных риску заражения ВИЧ. Еженедельный эпидемиологический отчет. 2007; 21: 193–196. [PubMed: 17526121]
Footnotes
- 1
Население с низким бременем определяется как население с (i) годовой частотой регистрации случаев туберкулеза легких с положительным мазком менее 5 на 100 000; или среднегодовая заболеваемость туберкулезным менингитом у детей в возрасте < 5 лет менее 1 на 10 миллионов населения в течение предыдущих пяти лет; или среднегодовой риск туберкулезной инфекции ниже 0,1%.
Авторское право © Всемирная организация здравоохранения, 2008 г.
Все права защищены. Публикации Всемирной организации здравоохранения можно получить в WHO Press, World Health Organization, 20 Avenue Appia, 1211 Geneva 27, Switzerland (тел. : +41 22 791 3264; факс: +41 22 791 4857; электронная почта:
tni.ohw@sredrokoob). Запросы на получение разрешения на воспроизведение или перевод публикаций ВОЗ – будь то для продажи или для некоммерческого распространения – следует направлять в пресс-службу ВОЗ по указанному выше адресу (факс: +41 22 79).1 4806; Эл. адрес:
tni.ohw@snoissimrep).
: +41 22 791 3264; факс: +41 22 791 4857; электронная почта:
tni.ohw@sredrokoob). Запросы на получение разрешения на воспроизведение или перевод публикаций ВОЗ – будь то для продажи или для некоммерческого распространения – следует направлять в пресс-службу ВОЗ по указанному выше адресу (факс: +41 22 79).1 4806; Эл. адрес:
tni.ohw@snoissimrep).
Идентификатор книжной полки: NBK310750
Содержание
- PubReader
- Print View
- CITE на этой стр.
- PDF версия этого названия (1,3 м)
на этой странице
3на этой странице
3на этой странице
3. Вакцина БЦЖ
Другие наименования в этой коллекции
- Руководство ВОЗ, одобренное Комитетом по обзору руководства
Дополнительная информация
- PubMed
Ссылки на PubMed
Последние действия
Ваш просмотр
3
2 Активность пуста. Запись активности отключена.
Включить запись обратно
Подробнее…
Вакцина БЦЖ — Руководство по ресурсам [обновлено в 2023 г.]
Последнее обновление
Вакцина БЦЖ – что это такое?
Вакцина БЦЖ – это специальная вакцина, которая используется для защиты людей от туберкулеза. Туберкулез является заразным заболеванием, которое присутствует во многих странах мира, и вакцина БЦЖ демонстрирует защитный эффект против туберкулеза на 60% и более. 1 Защита, обеспечиваемая вакциной БЦЖ, может длиться несколько десятилетий, в зависимости от человека. Также считается, что вакцина БЦЖ обеспечивает некоторую защиту от менингита и полезна для людей с раком мочевого пузыря. Также проводятся исследования, чтобы выяснить, обеспечивает ли вакцина БЦЖ какой-либо защитный эффект против COVID-19..
Вакцина БЦЖ – кто получает вакцину
Вакцина БЦЖ является одной из наиболее часто используемых вакцин во всем мире. В частности, он широко используется в странах, в которых распространен туберкулез, как способ защиты людей от туберкулеза.
Существует несколько групп людей, для которых следует рассмотреть вопрос о вакцинации БЦЖ (пожалуйста, проконсультируйтесь с Центром по контролю и профилактике заболеваний США для получения текущих рекомендаций): 2
- Дети . Вакцину БЦЖ можно рассмотреть для детей с отрицательным кожным тестом на ТБ и находящихся рядом с нелеченными взрослыми с ТБ или взрослыми с устойчивыми к ТБ штаммами.
- Медицинские работники . Иммунизацию БЦЖ следует рассматривать для медицинских работников, которые подвержены высокому риску воздействия устойчивых к туберкулезу штаммов.
Люди, проживающие в Соединенных Штатах из других стран, часто получают прививку БЦЖ. Вакцина БЦЖ обычно не рекомендуется как часть плановой серии прививок для детей, родившихся в Соединенных Штатах, из-за низкой заболеваемости туберкулезом и вопросов о том, насколько хорошо она работает в условиях активного туберкулеза легких. Вакцинация БЦЖ не должна проводиться во время беременности или людям с ослабленной иммунной системой.
История вакцины БЦЖ
«БЦЖ» в вакцине БЦЖ означает Bacillus Calmette-Guérin. Используемая почти столетие вакцина БЦЖ по оптовой цене менее 1,50 доллара за дозу считается ВОЗ основным лекарством и вводится примерно 100 миллионам детей в год. 3
Введение вакцины БЦЖ
Вакцину БЦЖ вводят людям в странах с высокой распространенностью туберкулеза. Как правило, по возможности новорожденным вводят одну дозу вакцины БЦЖ. Детям и взрослым, пропустившим плановую вакцинацию, также можно вводить вакцину БЦЖ. Перед введением вакцины БЦЖ обычно проводится кожная проба на туберкулез, поскольку лица с положительным результатом кожной пробы на туберкулез не должны получать вакцину БЦЖ. Беременным женщинам также следует избегать вакцинации БЦЖ.
Вакцину БЦЖ вводят в виде инъекции в плечевую мышцу, известную как дельтовидная. Его вводят внутрикожно. После вакцинации БЦЖ очень мало побочных эффектов, если она была введена правильно. Как и у большинства вакцин, наиболее частым побочным эффектом является боль или покраснение в месте введения вакцины БЦЖ. В редких случаях в месте заражения могут возникать более серьезные инфекции. У большинства людей, которым была сделана прививка БЦЖ, на месте прививки будет заметный приподнятый круговой рубец.
В редких случаях в месте заражения могут возникать более серьезные инфекции. У большинства людей, которым была сделана прививка БЦЖ, на месте прививки будет заметный приподнятый круговой рубец.
Людям со слабой иммунной системой не следует делать прививку БЦЖ. В этих ситуациях введение этой противотуберкулезной вакцины может вызвать опасные для жизни заболевания и инфекции.
Вакцина БЦЖ и тестирование на туберкулез
Хотя вакцина БЦЖ обладает защитным действием против туберкулеза, у этой вакцины есть и свои недостатки. Помимо боли, связанной с введением вакцины и последующим рубцеванием, вакцина БЦЖ влияет на любое последующее тестирование, проводимое при обследовании на туберкулез.
Точнее говоря, люди, получившие вакцину БЦЖ, будут иметь ложноположительный результат при распространенной форме скринингового обследования на туберкулез — кожной пробе на туберкулез. Кожная проба на туберкулез считается положительной, если у человека после теста появляется большая приподнятая шишка, а у людей, получивших вакцину БЦЖ, почти всегда будет положительный результат из-за перекрестной реактивности между вакциной БЦЖ и компонентами кожной пробы на туберкулез. Ингредиенты для инъекций. Поскольку контрольным тестом после положительного кожного теста на туберкулез является рентгенография грудной клетки, люди, получившие вакцину БЦЖ в прошлом, подвергаются облучению в результате рентгенограммы грудной клетки каждый раз, когда им необходимо пройти скрининг на туберкулез.
Ингредиенты для инъекций. Поскольку контрольным тестом после положительного кожного теста на туберкулез является рентгенография грудной клетки, люди, получившие вакцину БЦЖ в прошлом, подвергаются облучению в результате рентгенограммы грудной клетки каждый раз, когда им необходимо пройти скрининг на туберкулез.
В последние годы другие способы скрининга на туберкулез упростили дифференциацию того, действительно ли люди, получившие вакцину БЦЖ, подверглись воздействию туберкулеза или нет. Одна инновация в области лабораторных испытаний, известная как анализ крови на туберкулез QuantiFERON-Gold, становится все более актуальной для тестирования людей, получивших вакцину БЦЖ, на туберкулезную инфекцию. Анализ крови QuantiFERON TB ценен для людей, которым была сделана прививка БЦЖ, потому что он может точно определить, подвергался ли человек воздействию туберкулезной инфекции или нет после получения вакцины БЦЖ.
Будущее вакцины БЦЖ
Вакцина БЦЖ играет важную роль в профилактической защите людей с высоким риском заражения туберкулезом, несмотря на неудобства, которые она вызывает.


 В редких случаях в месте заражения могут возникать более серьезные инфекции. У большинства людей, которым была сделана прививка БЦЖ, на месте прививки будет заметный приподнятый круговой рубец.
В редких случаях в месте заражения могут возникать более серьезные инфекции. У большинства людей, которым была сделана прививка БЦЖ, на месте прививки будет заметный приподнятый круговой рубец. Ингредиенты для инъекций. Поскольку контрольным тестом после положительного кожного теста на туберкулез является рентгенография грудной клетки, люди, получившие вакцину БЦЖ в прошлом, подвергаются облучению в результате рентгенограммы грудной клетки каждый раз, когда им необходимо пройти скрининг на туберкулез.
Ингредиенты для инъекций. Поскольку контрольным тестом после положительного кожного теста на туберкулез является рентгенография грудной клетки, люди, получившие вакцину БЦЖ в прошлом, подвергаются облучению в результате рентгенограммы грудной клетки каждый раз, когда им необходимо пройти скрининг на туберкулез.
