Страница не найдена
Размер:
AAA
Цвет: C C C
Изображения Вкл. Выкл.
Обычная версия сайта
RUENBY
Гомельский государственный
медицинский университет
- Университет
- Университет
- История
- Руководство
- Устав и Символика
- Воспитательная деятельность
- Организация образовательного процесса
- Международное сотрудничество
- Система менеджмента качества
- Советы
- Факультеты
- Кафедры
- Подразделения
- Первичная профсоюзная организация работников
- Издания университета
- Гордость университета
- Выпускник-2021
- Первичная организация «Белорусский союз женщин»
- Одно окно
- ГомГМУ в международных рейтингах
- Структура университета
- Абитуриентам
- Приёмная комиссия
- Университетская олимпиада по биологии
- Целевая подготовка
- Заключение, расторжение «целевого» договора
- Льготы для молодых специалистов
- Архив проходных баллов
- Карта и маршрут проезда
- Порядок приёма на 2023 год
- Специальности
- Контрольные цифры приёма в 2022 году
- Стоимость обучения
- Информация о ходе приёма документов
- Приём документов и время работы приёмной комиссии
- Порядок приёма граждан РФ, Кыргызстана, Таджикистана, Казахстана
- Горячая линия по вопросам вступительной кампании
- Студентам
- Первокурснику
- Расписание занятий
- Расписание экзаменов
- Информация для студентов
- Студенческий клуб
- Спортивный клуб
- Общежитие
- Нормативные документы
- Практика
- Стоимость обучения
- Безопасность жизнедеятельности
- БРСМ
- Профком студентов
- Учебный центр практической подготовки и симуляционного обучения
- Многофункциональная карточка студента
- Анкетирование студентов
- Выпускникам
- Интернатура и клиническая ординатура
- Докторантура
- Аспирантура
- Магистратура
- Распределение
- Профессорский консультативный центр
- Факультет повышения квалификации и переподготовки
- Иностранным гражданам
- Факультет иностранных студентов
- Стоимость обучения
- Регистрация и визы
- Полезная информация
- Правила приёма
- Информация о возможностях и условиях приема в 2022 году
- Официальные представители ГомГМУ по набору студентов
- Страхование иностранных граждан
- Приём на Подготовительное отделение иностранных граждан
- Прием иностранных граждан для обучения на английском языке / Training of foreign students in English
- Повышение квалификации и переподготовка для иностранных граждан
- Научная деятельность
- Направления научной деятельности
- Научно-исследовательская лаборатория
- Научно-исследовательская часть
- Инновационные технологии в ГомГМУ
- Научно-педагогические школы
- Конкурсы, гранты, стипендии
- Научные мероприятия
- Работа комитета по этике
- В помощь исследователю
- Совет молодых ученых
- Студенчеcкое научное общество
- Диссертационный совет
- Патенты
- Инструкции на метод
- «Горизонт Европа»
- Госпрограмма (ЧАЭС)
- Главная
Фетоплацентарная недостаточность: проблема современного акушерства | #03/11
Фетоплацентарная недостаточность (ФПН) представляет собой симптомокомплекс, при котором возникают различные нарушения, как со стороны плаценты, так и со стороны плода, вследствие различных заболеваний и акушерских осложнений. Разнообразие вариантов проявления ФПН, частота и тяжесть осложнений для беременной и плода, преобладающее нарушение той или иной функции плаценты зависят от срока беременности, силы, длительности и характера воздействия повреждающих факторов, а также от стадии развития плода и плаценты, степени выраженности компенсаторно-приспособительных возможностей системы «мать–плацента–плод».
Разнообразие вариантов проявления ФПН, частота и тяжесть осложнений для беременной и плода, преобладающее нарушение той или иной функции плаценты зависят от срока беременности, силы, длительности и характера воздействия повреждающих факторов, а также от стадии развития плода и плаценты, степени выраженности компенсаторно-приспособительных возможностей системы «мать–плацента–плод».
Причины возникновения ФПН
ФПН может развиваться под влиянием различных причин. Нарушения формирования и функции плаценты могут быть обусловлены заболеваниями сердца и сосудистой системы беременной (пороки сердца, недостаточность кровообращения, артериальная гипертензия и гипотензия), патологией почек, печени, легких, крови, хронической инфекцией, заболеваниями нейроэндокринной системы (сахарный диабет, гипо- и гиперфункция щитовидной железы, патология гипоталамуса и надпочечников) и целым рядом других патологических состояний. ФПН при анемии обусловлена снижением уровня железа как в материнской крови, так и в самой плаценте, что приводит к угнетению активности дыхательных ферментов и транспорта железа к плоду. При сахарном диабете нарушается метаболизм, выявляются гормональные расстройства и изменения иммунного статуса. Склеротическое поражение сосудов приводит к уменьшению поступления артериальной крови к плаценте. Важную роль в развитии ФПН играют различные инфекционные заболевания, особенно протекающие в острой форме или обостряющиеся во время беременности. Плацента может быть поражена бактериями, вирусами, простейшими и другими возбудителями инфекции.
При сахарном диабете нарушается метаболизм, выявляются гормональные расстройства и изменения иммунного статуса. Склеротическое поражение сосудов приводит к уменьшению поступления артериальной крови к плаценте. Важную роль в развитии ФПН играют различные инфекционные заболевания, особенно протекающие в острой форме или обостряющиеся во время беременности. Плацента может быть поражена бактериями, вирусами, простейшими и другими возбудителями инфекции.
Немаловажное значение в формировании ФПН имеет патология матки: эндометриоз, гипоплазия миометрия, пороки развития матки (седловидная, двурогая). Фактором риска ФПН следует считать миому матки. Однако риск ФПН у беременных с миомой матки различен. К группе с высоким риском относят первородящих в возрасте 35 лет и старше с преимущественно межмышечным расположением миоматозных узлов больших размеров, особенно при локализации плаценты в области расположения опухоли. Группу с низким риском ФПН составляют молодые женщины до 30 лет без тяжелых экстрагенитальных заболеваний, с небольшими миоматозными узлами преимущественно подбрюшинного расположения в дне и теле матки.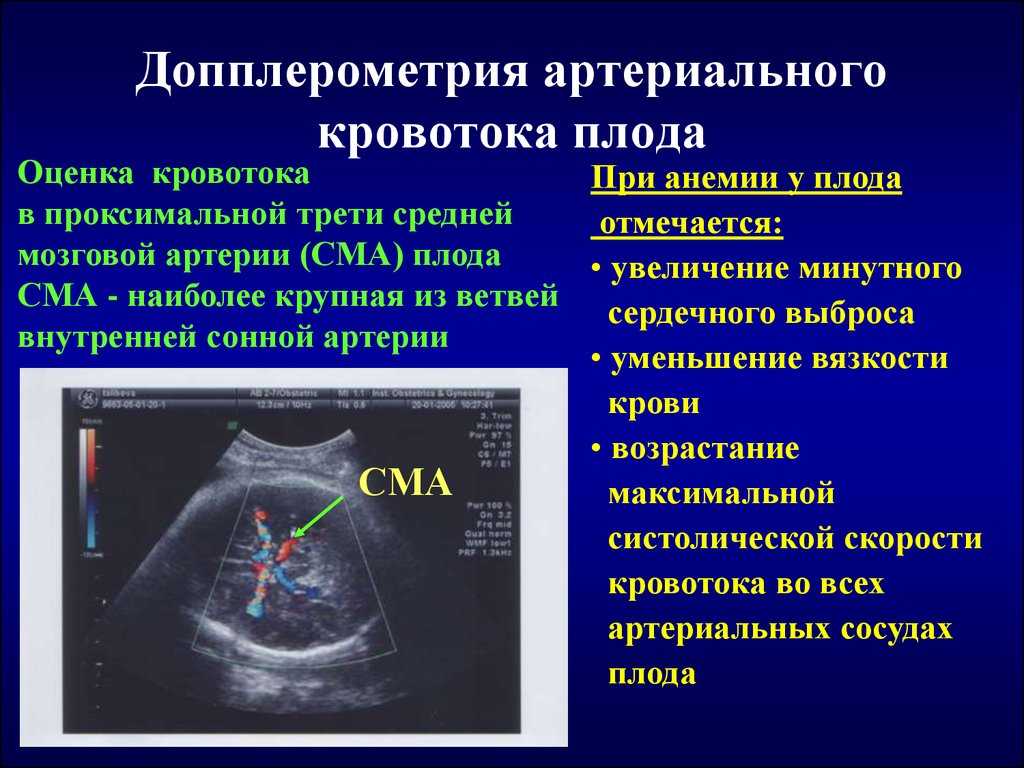
Среди осложнений беременности, наиболее часто сопутствующих ФПН, ведущее место занимает гестоз. Угрозу прерывания беременности следует одновременно рассматривать и как причину, и как следствие ФПН. В связи с различной этиологией ФПН при угрозе прерывания беременности патогенез этого осложнения имеет различные варианты, а прогноз для плода зависит от степени развития защитно-приспособительных реакций. При низком расположении или предлежании плаценты васкуляризация субплацентарной зоны снижена. Более тонкая стенка нижнего сегмента матки не обеспечивает необходимых условий для достаточной васкуляризации плацентарного ложа и его нормального функционирования.
Относительно часто при данной патологии происходит отслойка плаценты, сопровождающаяся кровопотерей. Многоплодная беременность представляет естественную модель ФПН в результате неадекватного обеспечения потребностей двух и более плодов. В основе ФПН при изосерологической несовместимости крови матери и плода чаще всего лежат процессы нарушения созревания плаценты. У плода развивается анемия и гипоксия, возникает задержка развития из-за нарушений процессов синтеза белка и снижения активности ферментов. Функциональное состояние плаценты во многом обусловлено степенью ее развития в соответствии с гестационным сроком и сохранностью защитно-приспособительных механизмов. Соответствие зрелости плаценты гестационному сроку является одним из наиболее важных условий обеспечения адекватного развития плода и его защиты. Несомненно, что поздний возраст беременной (старше 35 лет) или, наоборот, юный возраст (до 17 лет), отягощенный анамнез (аборты, воспалительные заболевания), вредные привычки, воздействие неблагоприятных факторов окружающей среды, плохое питание, социальная незащищенность и бытовая неустроенность также способствуют осложненному формированию плаценты и нарушению ее функции [1].
У плода развивается анемия и гипоксия, возникает задержка развития из-за нарушений процессов синтеза белка и снижения активности ферментов. Функциональное состояние плаценты во многом обусловлено степенью ее развития в соответствии с гестационным сроком и сохранностью защитно-приспособительных механизмов. Соответствие зрелости плаценты гестационному сроку является одним из наиболее важных условий обеспечения адекватного развития плода и его защиты. Несомненно, что поздний возраст беременной (старше 35 лет) или, наоборот, юный возраст (до 17 лет), отягощенный анамнез (аборты, воспалительные заболевания), вредные привычки, воздействие неблагоприятных факторов окружающей среды, плохое питание, социальная незащищенность и бытовая неустроенность также способствуют осложненному формированию плаценты и нарушению ее функции [1].
Клиническая практика и результаты научных исследований свидетельствуют о многофакторной природе ФПН. В связи с этим практически невозможно выделить какой-либо единственный фактор развития данного осложнения. Перечисленные патологические состояния не в одинаковой мере оказывают влияние на развитие ФПН. Чаще всего в развитии этой патологии участвуют несколько этиологических факторов, один из которых может быть ведущим. Патологические изменения, которые происходят при ФПН, приводят к уменьшению маточно-плацентарного и фетоплацентарного кровотока; снижению артериального кровоснабжения плаценты и плода; ограничению газообмена и метаболизма в фетоплацентарном комплексе; нарушению процессов созревания плаценты; снижению синтеза и дисбалансу гормонов плаценты. Все эти изменения подавляют компенсаторно-приспособительные возможности системы «мать–плацента–плод», замедляют рост и развитие плода, обусловливают осложненное течение беременности и родов (угроза преждевременного прерывания беременности, гестоз, преждевременные и запоздалые роды, аномалии родовой деятельности, преждевременная отслойка плаценты и др.) [5].
Перечисленные патологические состояния не в одинаковой мере оказывают влияние на развитие ФПН. Чаще всего в развитии этой патологии участвуют несколько этиологических факторов, один из которых может быть ведущим. Патологические изменения, которые происходят при ФПН, приводят к уменьшению маточно-плацентарного и фетоплацентарного кровотока; снижению артериального кровоснабжения плаценты и плода; ограничению газообмена и метаболизма в фетоплацентарном комплексе; нарушению процессов созревания плаценты; снижению синтеза и дисбалансу гормонов плаценты. Все эти изменения подавляют компенсаторно-приспособительные возможности системы «мать–плацента–плод», замедляют рост и развитие плода, обусловливают осложненное течение беременности и родов (угроза преждевременного прерывания беременности, гестоз, преждевременные и запоздалые роды, аномалии родовой деятельности, преждевременная отслойка плаценты и др.) [5].
В результате воздействия повреждающих факторов и реализации патогенетических механизмов, приводящих к ФПН, закономерно развивается гипоксия плода. На начальных ее этапах у плода активизируются вазопрессорные факторы, повышается тонус периферических сосудов, отмечается тахикардия, увеличивается частота дыхательных движений, повышается двигательная активность, возрастает минутный объем сердца.
На начальных ее этапах у плода активизируются вазопрессорные факторы, повышается тонус периферических сосудов, отмечается тахикардия, увеличивается частота дыхательных движений, повышается двигательная активность, возрастает минутный объем сердца.
Дальнейшее прогрессирование гипоксии приводит к смене тахикардии брадикардией, появляется аритмия, уменьшается минутный объем сердца. Адаптационной реакцией на гипоксию является перераспределение крови в пользу мозга, сердца и надпочечников с одновременным уменьшением кровоснабжения остальных органов. Параллельно угнетается двигательная и дыхательная активность плода [5].
Классификация ФПН
ФПН целесообразно классифицировать с учетом состояния защитно-приспособительных реакций на компенсированную, субкомпенсированную, декомпенсированную [3].
Компенсированная форма ФПН характеризуется начальными проявлениями патологического процесса в фетоплацентарном комплексе. Защитно-приспособительные механизмы активизируются и испытывают определенное напряжение, что создает условия для дальнейшего развития плода и прогрессирования беременности. При адекватной терапии и ведении родов возможно рождение здорового ребенка.
При адекватной терапии и ведении родов возможно рождение здорового ребенка.
Субкомпенсированная форма ФПН характеризуется усугублением тяжести осложнения. Защитно-приспособительные механизмы испытывают предельное напряжение (возможности фетоплацентарного комплекса при этом практически исчерпаны), что не позволяет обеспечить их реализацию в достаточной степени для адекватного течения беременности и развития плода. Увеличивается риск возникновения осложнений для плода и новорожденного.
При декомпенсированной форме ФПН имеет место перенапряжение и срыв компенсаторно-приспособительных механизмов, которые уже не обеспечивают необходимых условий для дальнейшего нормального прогрессирования беременности. В фетоплацентарной системе происходят необратимые морфофункциональные нарушения. Существенно возрастает риск развития тяжелых осложнений для плода и новорожденного (включая их гибель). Клиническая картина ФПН проявляется в нарушениях основных функций плаценты.
Задержка внутриутробного развития плода
Об изменении дыхательной функции плаценты свидетельствуют в основном симптомы гипоксии плода. При этом вначале беременная обращает внимание на повышенную (беспорядочную) двигательную активность плода, затем на ее уменьшение или полное отсутствие. Наиболее характерным признаком хронической ФПН является задержка внутриутробного развития плода. Клиническим проявлением задержки внутриутробного развития плода является уменьшение размеров живота беременной (окружность живота, высота стояния дна матки) по сравнению с нормативными показателями, характерными для данного срока беременности.
При этом вначале беременная обращает внимание на повышенную (беспорядочную) двигательную активность плода, затем на ее уменьшение или полное отсутствие. Наиболее характерным признаком хронической ФПН является задержка внутриутробного развития плода. Клиническим проявлением задержки внутриутробного развития плода является уменьшение размеров живота беременной (окружность живота, высота стояния дна матки) по сравнению с нормативными показателями, характерными для данного срока беременности.
При симметричной форме задержки внутриутробного развития, которая развивается с ранних сроков беременности, отмечается пропорциональное отставание длины и массы тела плода. При этом количественные показатели фетометрии имеют более низкие значения по сравнению с индивидуальными колебаниями, характерными для данного срока беременности.
Асимметричная форма задержки внутриутробного развития характеризуется непропорциональным развитием плода. Эта форма чаще всего возникает во II или в III триместре беременности и проявляется отставанием массы тела плода при нормальной его длине. Преимущественно уменьшаются размеры живота и грудной клетки плода, что связано с отставанием развития паренхиматозных органов (в первую очередь печени) и подкожной жировой клетчатки. Размеры головы и конечностей плода соответствуют показателям, характерным для данного срока беременности.
Преимущественно уменьшаются размеры живота и грудной клетки плода, что связано с отставанием развития паренхиматозных органов (в первую очередь печени) и подкожной жировой клетчатки. Размеры головы и конечностей плода соответствуют показателям, характерным для данного срока беременности.
Нарушения функций плаценты
Отражением нарушений защитной функции плаценты при ослаблении плацентарного барьера является внутриутробное инфицирование плода под действием проникающих через плаценту патогенных микроорганизмов. Возможно также проникновение через плацентарный барьер различных токсичных веществ, также оказывающих повреждающее действие на плод.
Изменение синтетической функции плаценты сопровождается дисбалансом уровня вырабатываемых ею гормонов и снижением синтеза белков, что проявляется задержкой внутриутробного развития плода, гипоксией, патологией сократительной активности матки при беременности и в родах (длительная угроза преждевременного прерывания беременности, преждевременные роды, аномалии родовой деятельности).
Длительное и частое повышение тонуса миометрия приводит к снижению артериального притока крови к плаценте и вызывает венозный застой. Гемодинамические нарушения снижают газообмен между организмом матери и плода, что затрудняет поступление к плоду кислорода, питательных веществ, выведение продуктов метаболизма, способствует нарастанию гипоксии плода.
Нарушение эндокринной функции плаценты может приводить и к перенашиванию беременности. Снижение гормональной активности плаценты вызывает нарушение функции влагалищного эпителия, создавая благоприятные условия для развития инфекции, обострения или возникновения воспалительных заболеваний урогенитального тракта. На фоне расстройства выделительной функции плаценты и околоплодных оболочек отмечается патологическое количество околоплодных вод — чаще всего маловодие, а при некоторых патологических состояниях (сахарный диабет, отечная форма гемолитической болезни плода, внутриутробное инфицирование и др.) — многоводие.
Диагностика ФПН
На начальном этапе развития ФПН перечисленные клинические признаки могут быть выражены слабо или отсутствовать. В связи с этим существенное значение приобретают методы лабораторного и инструментального динамического контроля за состоянием фетоплацентарного комплекса в группе высокого риска по развитию ФПН. Доминирующее положение в клинической картине могут занимать признаки основного заболевания или осложнения, при котором развилась ФПН. Степень выраженности ФПН и нарушения компенсаторно-приспособительных механизмов находятся в прямой зависимости от тяжести основного заболевания и длительности его течения. Наиболее тяжелое течение ФПН приобретает при появлении патологических признаков в срок беременности до 30 недель и ранее. Таким образом, наиболее полную информацию о форме, характере, степени тяжести ФПН и выраженности компенсаторно-приспособительных реакций позволяют получить данные комплексной динамической диагностики [2].
В связи с этим существенное значение приобретают методы лабораторного и инструментального динамического контроля за состоянием фетоплацентарного комплекса в группе высокого риска по развитию ФПН. Доминирующее положение в клинической картине могут занимать признаки основного заболевания или осложнения, при котором развилась ФПН. Степень выраженности ФПН и нарушения компенсаторно-приспособительных механизмов находятся в прямой зависимости от тяжести основного заболевания и длительности его течения. Наиболее тяжелое течение ФПН приобретает при появлении патологических признаков в срок беременности до 30 недель и ранее. Таким образом, наиболее полную информацию о форме, характере, степени тяжести ФПН и выраженности компенсаторно-приспособительных реакций позволяют получить данные комплексной динамической диагностики [2].
С учетом многофакторной этиологии и патогенеза ФПН ее диагностика должна быть основана на комплексном обследовании пациентки. Для установления диагноза ФПН и выявления причин этого осложнения значительное внимание следует уделять правильному сбору анамнеза. При опросе оценивают возраст пациентки (поздний или юный возраст первородящей женщины), особенности ее здоровья, перенесенные экстрагенитальные, нейроэндокринные и гинекологические заболевания, хирургические вмешательства, наличие вредных привычек, выясняют профессию, условия и образ жизни.
При опросе оценивают возраст пациентки (поздний или юный возраст первородящей женщины), особенности ее здоровья, перенесенные экстрагенитальные, нейроэндокринные и гинекологические заболевания, хирургические вмешательства, наличие вредных привычек, выясняют профессию, условия и образ жизни.
Большое значение имеет информация об особенностях менструальной функции, периоде ее становления, количестве и течении предшествующих беременностей. Нарушения менструальной функции являются отражением патологии нейроэндокринной регуляции репродуктивной функции. Важно оценить течение настоящей беременности, характер акушерских осложнений и, главное, наличие заболеваний, на фоне которых развивается беременность (артериальная гипертензия или гипотония, патология почек, печени, сахарный диабет, анемия и др.). Следует обратить внимание на жалобы беременной: увеличение или угнетение двигательной активности плода, боли внизу живота, повышение тонуса матки, появление нетипичных выделений из половых путей, которые могут сопровождаться неприятным запахом и зудом.
При объективном исследовании пальпаторно оценивают состояние тонуса матки. Измеряют высоту стояния дна матки и окружности живота, сопоставляют их с массой тела и ростом беременной, а также уточненным сроком беременности. Такие измерения являются важными и в то же время наиболее простыми показателями для диагностики задержки внутриутробного развития плода, маловодия и многоводия. При наружном осмотре половых органов и при исследовании с помощью зеркал необходимо обратить внимание на наличие признаков воспаления, характер выделений из половых путей, взять материал со стенки влагалища, из цервикального канала и из уретры для микробиологического и цитологического исследования [2].
При эхографическом исследовании определяют размеры плода (размеры головы, туловища и конечностей) и сопоставляют их с нормативными показателями, характерными для предполагаемого гестационного срока. Основой ультразвуковой диагностики для уточнения соответствия размеров плода предполагаемому сроку беременности и выявления задержки внутриутробного развития плода является сопоставление фетометрических показателей с нормативными данными. Непременным условием является оценка анатомических структур плода для выявления аномалий его развития. Эхографическое исследование включает в себя и плацентографию. При этом определяют локализацию плаценты, толщину плаценты, расстояние плаценты от внутреннего зева, соответствие степени зрелости плаценты гестационному сроку, патологические включения в структуре плаценты, расположение плаценты по отношению к миоматозным узлам или рубцу на матке. В процессе исследования проводят оценку объема околоплодных вод, строения пуповины и расположения петель пуповины [4].
Непременным условием является оценка анатомических структур плода для выявления аномалий его развития. Эхографическое исследование включает в себя и плацентографию. При этом определяют локализацию плаценты, толщину плаценты, расстояние плаценты от внутреннего зева, соответствие степени зрелости плаценты гестационному сроку, патологические включения в структуре плаценты, расположение плаценты по отношению к миоматозным узлам или рубцу на матке. В процессе исследования проводят оценку объема околоплодных вод, строения пуповины и расположения петель пуповины [4].
Допплерография представляет собой высокоинформативный, относительно простой и безопасный метод диагностики, который можно использовать для комплексного динамического наблюдения за состоянием кровообращения в системе «мать–плацента–плод» после 18–19 недель беременности, так как к этому времени завершается вторая волна инвазии цитотрофобласта. Характер гемодинамики в артериях пуповины позволяет судить о состоянии фетоплацентарного кровотока и о микроциркуляции в плодовой части плаценты. Для диагностики нарушения маточно-плацентарного кровотока проводят исследования в маточных артериях с двух сторон [4].
Для диагностики нарушения маточно-плацентарного кровотока проводят исследования в маточных артериях с двух сторон [4].
Важной составной частью комплексной оценки состояния плода является кардиотокография (КТГ), которая представляет собой метод функциональной оценки состояния плода на основании регистрации частоты его сердцебиений и их изменений в зависимости от сокращений матки, действия внешних раздражителей или активности самого плода. КТГ значительно расширяет возможности антенатальной диагностики, позволяя решать вопросы рациональной тактики ведения беременности.
Окончательная тактика ведения пациентки должна быть выработана не только на основе оценки отдельных показателей состояния фетоплацентарного комплекса, но и с учетом индивидуальных особенностей конкретного клинического наблюдения (срок и осложнения беременности, сопутствующая соматическая патология, результаты дополнительного комплексного обследования, состояние и готовность организма к родам и т. д.).
Лечение беременных с ФПН
При выявлении ФПН беременную целесообразно госпитализировать в стационар для углубленного обследования и лечения. Исключение могут составлять беременные с компенсированной формой ФПН при условии, что начатое лечение дает положительный эффект и имеются необходимые условия для динамического клинического и инструментального контроля за характером течения беременности и эффективностью проводимой терапии. Ведущее место в проведении лечебных мероприятий занимает лечение основного заболевания или осложнения, при котором возникла ФПН. В настоящее время, к сожалению, не представляется возможным полностью избавить беременную от ФПН какими-либо лечебными воздействиями. Применяемые средства терапии могут способствовать только стабилизации имеющегося патологического процесса и поддержанию компенсаторно-приспособительных механизмов на уровне, позволяющем обеспечить продолжение беременности до возможного оптимального срока родоразрешения.
Исключение могут составлять беременные с компенсированной формой ФПН при условии, что начатое лечение дает положительный эффект и имеются необходимые условия для динамического клинического и инструментального контроля за характером течения беременности и эффективностью проводимой терапии. Ведущее место в проведении лечебных мероприятий занимает лечение основного заболевания или осложнения, при котором возникла ФПН. В настоящее время, к сожалению, не представляется возможным полностью избавить беременную от ФПН какими-либо лечебными воздействиями. Применяемые средства терапии могут способствовать только стабилизации имеющегося патологического процесса и поддержанию компенсаторно-приспособительных механизмов на уровне, позволяющем обеспечить продолжение беременности до возможного оптимального срока родоразрешения.
Основу терапии плацентарной недостаточности составляют мероприятия, направленные на улучшение маточно-плацентарного и фетоплацентарного кровотока. Препараты, применяемые с этой целью, расширяют сосуды, расслабляют мускулатуру матки, улучшают реологические свойства крови в системе «мать–плацента–плод» [2].
Лечение ФПН должно быть направлено на улучшение маточно-плацентарного и фетоплацентарного кровотока; интенсификацию газообмена; коррекцию реологических и коагуляционных свойств крови; устранение гиповолемии и гипопротеинемии; нормализацию сосудистого тонуса и сократительной активности матки; усиление антиоксидантной защиты; оптимизацию метаболических и обменных процессов. Стандартной схемы лечения ФПН существовать не может вследствие индивидуального сочетания этиологических факторов и патогенетических механизмов развития данного осложнения. Подбор препаратов следует проводить индивидуально и дифференцированно в каждом конкретном наблюдении с учетом степени тяжести и длительности осложнения, этиологических факторов и патогенетических механизмов, лежащих в основе этой патологии. Индивидуального подхода требуют дозировка препаратов и продолжительность их применения. Следует обращать внимание на коррекцию побочного действия некоторых лекарственных средств.
В патогенезе плацентарной недостаточности, также как и при гестозе, основным является дисфункция эндотелия. При этом имеется три эндотелиальные системы: матери, плаценты и плода. Поэтому процессы, происходящие в сосудисто-тромбоцитарном звене при плацентарной недостаточности, сходны с теми, которые имеют место при гестозе. А это приводит к метаболическим нарушениям в системе «мать–плацента–плод» и к гипотрофии плода.
При этом имеется три эндотелиальные системы: матери, плаценты и плода. Поэтому процессы, происходящие в сосудисто-тромбоцитарном звене при плацентарной недостаточности, сходны с теми, которые имеют место при гестозе. А это приводит к метаболическим нарушениям в системе «мать–плацента–плод» и к гипотрофии плода.
Потребность в магнии при беременности возрастает в 2–3 раза за счет роста и развития плода и плаценты. Магний, участвующий в более чем 300 ферментативных реакциях, необходим для роста плода. Ионы магния задействованы в синтезе ДНК и РНК. Удачно сочетание магния с пиридоксином, который обеспечивает белковый обмен, являясь катионом более 50 ферментативных реакций, участвуя в синтезе и всасывании аминокислот, способствует образованию гемоглобина в эритроцитах, что особенно важно для растущего эмбриона и плода. Поэтому при наличии плацентарной недостаточности и гипотрофии плода наиболее целесообразно применять препараты магния.
Магний (Магне B6® форте) оказывает положительное действие на маточно-плацентарное кровообращение, поэтому показано его назначение для лечения плацентарной недостаточности и гипотрофии плода. Установлен параллелизм между концентрацией магния в сыворотке крови, в миометрии, в плаценте.
Установлен параллелизм между концентрацией магния в сыворотке крови, в миометрии, в плаценте.
Магне В6® форте хорошо сочетается также с ангиопротекторами, ангиоактивными средствами (Трентал, Курантил, Милдронат, Актовегин и др.), с антиоксидантами — витаминами Е, С, группы В и т. д.
При лечении угрозы прерывания беременности и плацентарной недостаточности магнезиальная терапия может сочетаться с применением витамина Е и других антиоксидантов, с Милдронатом, Актовегином, с блокаторами кальциевых каналов (верапамилом), Эуфиллином, Папаверином, Дибазолом, Но-шпой, антигистаминными препаратами, физиотерапевтическими методами лечения (центральная электроаналгезия, индуктотерапия околопочечной области, гидроионизация и др.).
Лечение ФПН начинают и проводят в стационаре не менее 4 недель с последующим ее продолжением в женской консультации. Общая длительность лечения составляет не менее 6–8 недель. Для оценки эффективности проводимой терапии осуществляют динамический контроль с помощью клинических, лабораторных и инструментальных методов исследования. Важным условием успешного лечения ФПН является соблюдение беременной соответствующего режима: полноценный отдых не менее 10–12 часов в сутки, устранение физических и эмоциональных нагрузок, рациональное сбалансированное питание.
Важным условием успешного лечения ФПН является соблюдение беременной соответствующего режима: полноценный отдых не менее 10–12 часов в сутки, устранение физических и эмоциональных нагрузок, рациональное сбалансированное питание.
Одним из ведущих патогенетических механизмов развития ФПН являются нарушения маточно-плацентарного и фетоплацентарного кровотока, сопровождающиеся повышением вязкости крови, гиперагрегацией эритроцитов и тромбоцитов, расстройством микроциркуляции и сосудистого тонуса, недостаточностью артериального кровообращения. Поэтому важное место в лечении ФПН занимают препараты антиагрегантного и антикоагулянтного действия, а также лекарственные средства, нормализующие сосудистый тонус.
Следует принимать во внимание, что периодическое и длительное повышение тонуса матки способствует нарушению кровообращения в межворсинчатом пространстве вследствие снижения венозного оттока. В связи с этим в курсе терапии ФПН у пациенток с явлениями угрозы прерывания беременности оправдано назначение препаратов токолитического действия.
Таким образом, плацентарная недостаточность развивается при осложненной беременности, что требует проведения лечебно-профилактических мероприятий, направленных на снижение акушерской патологии. Проблема лечения плацентарной недостаточности остается пока до конца не решенной, поэтому коррекция нарушений должна быть начата лучше до наступления беременности, что может позволить снизить частоту осложнений беременности, плода и новорожденного.
Литература
- Федорова М. В. Плацентарная недостаточность // Акушерство и гинекология. 1997. № 6. С. 40–43.
- Серов В. Н. Диагностика и лечение плацентарной недостаточности // РМЖ. 2008. С. 35–40.
- Кузьмин В. Н., Адамян Л. В., Музыкантова В. С. Плацентарная недостаточность при вирусных инфекциях // М.: 2005. С. 103.
- Шаповаленко С. А. Комплексная диагностика и лечение плацентарной недостаточности у беременных на разных стадиях гестации // Вестник Рос. Ассоциации акушер-гинекологов.
 2001. № 2. С. 437.
2001. № 2. С. 437. - Salafia C. M. Placental pathology and fetal growth restriction // Clin.Obstet.Gynecol. 2007. 40. 7409 RU.MPG.11.02.11.
В. Н. Кузьмин, доктор медицинских наук, профессор
МГМСУ, Москва
Контактная информация об авторах для переписки: [email protected]
Плацентарная недостаточность — StatPearls — NCBI Bookshelf
Непрерывное обучение
Плацентарная недостаточность — это состояние, при котором происходит нарушение ремоделирования плацентарных сосудов, что приводит к нарушению образования плаценты, что приводит к ацидозу и гипоксемии плода. Наиболее распространенные последующие последствия этого состояния для плода включают задержку внутриутробного развития, недоношенность или, к сожалению, гибель плода. Чтобы снизить риск заболеваемости и смертности плода, особенно при беременности с высоким риском, следует проводить регулярный пренатальный скрининг с помощью ультразвуковой допплерографии, чтобы увеличить шансы обнаружения и диагностики. В этом мероприятии рассматриваются патофизиология, оценка и возможные методы лечения плацентарной недостаточности, а также подчеркивается роль межпрофессиональной команды в лечении пациентов с этим заболеванием.
В этом мероприятии рассматриваются патофизиология, оценка и возможные методы лечения плацентарной недостаточности, а также подчеркивается роль межпрофессиональной команды в лечении пациентов с этим заболеванием.
Цели:
Рассмотреть факторы риска, связанные с плацентарной недостаточностью.
Опишите типичные результаты ультразвуковой допплерографии, связанные с плацентарной недостаточностью.
Укажите наиболее распространенные нежелательные явления, связанные с плацентарной недостаточностью.
Получите доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Введение
Плацентарная недостаточность связана с различными акушерскими расстройствами, такими как преэклампсия и задержка внутриутробного развития плода, которые предрасполагают к преждевременным родам, основной причине перинатальной заболеваемости и смертности во всем мире. Плохая плацентарная функция чаще всего описывается термином «плацентарная недостаточность» в медицинском сообществе; однако одно исследование выявило проблему отсутствия стандартизированного определения или консенсуса в отношении патогномоничных признаков, относящихся к плацентарной недостаточности.[1]
Плохая плацентарная функция чаще всего описывается термином «плацентарная недостаточность» в медицинском сообществе; однако одно исследование выявило проблему отсутствия стандартизированного определения или консенсуса в отношении патогномоничных признаков, относящихся к плацентарной недостаточности.[1]
Это создает много проблем, когда речь идет об изучении плацентарной недостаточности в литературе, но общее понимание состоит в том, что плацентарная недостаточность представляет собой процесс, при котором происходит прогрессирующее ухудшение функционирования плаценты, так что перенос кислорода и питательных веществ к плоду через плаценту нарушается. уменьшался, достигая высшей точки в декомпенсированной гипоксии и ацидозе.[2][3] Этот процесс приводит к гипоксемии плода, которая затем стимулирует снижение метаболических потребностей плода для сохранения уже доступных питательных веществ, что приводит к ограничению внутриутробного роста плода. С гистопатологической точки зрения плацентарная недостаточность может быть определена при наличии фиброза ворсин хориона, маточно-плацентарного тромбоза, плацентарных инфарктов, отложений фибрина или уменьшения количества и площади поверхности ворсинчатого капиллярного дерева.
Следует отметить, что инфаркты плаценты могут быть нормальным явлением, так как они наблюдаются примерно в 25% нормальных доношенных беременностей; однако было показано, что учащение инфаркта плаценты связано с плацентарной недостаточностью и, следовательно, с задержкой внутриутробного развития (ЗВУР). Как МРТ, так и ультразвуковые исследования, направленные на выявление плацентарной недостаточности, продемонстрировали уменьшение площади и объема плаценты, а также увеличение толщины плаценты в дополнение к плацентам шаровидной формы на МРТ [5].
Этиология
На сегодняшний день основные причины, которые могут привести к плацентарной недостаточности, плохо изучены и все еще изучаются. Известны сопутствующие материнские факторы риска, которые включают преэклампсию или другие гипертензивные расстройства у матери, употребление матерью сигарет, употребление матерью наркотиков, включая кокаин или героин, употребление матерью алкоголя, первородство, преклонный возраст матери и наличие в анамнезе родов с ЗВУР у новорожденного. [2] [6]
[2] [6]
Исследования, анализирующие допплеровские волны в различных плацентарных сосудах матерей, которые курили сигареты во время беременности, продемонстрировали уменьшение волн скорости кровотока, что указывает на то, что воздействие никотина может привести к изменению плацентарной сосудистой сети.[6]
Любое состояние матери, которое может привести к нарушению кровообращения плода, подвергает плод риску развития плацентарной недостаточности. Кроме того, некоторые лекарства, такие как противоопухолевые, противосудорожные или антикоагулянты, могут препятствовать росту плода. Экстремальные значения индекса массы тела матери, включая недоедание матери, также связаны с развитием ЗВУР у новорожденных.[7] Исследования беременностей, осложненных ЗВУР, продемонстрировали неполную трансформацию плацентарной сосудистой сети на ранних сроках беременности, которую можно обнаружить с помощью ультразвуковой допплерографии.
Эпидемиология
Недоношенность является ведущей причиной перинатальной смерти, за которой следует задержка внутриутробного развития плода, осложняющая примерно от 4% до 6% известных беременностей. Плацентарная недостаточность является потенциальной причиной преждевременных родов, преэклампсии, ЗВУР и мертворождения, которые могут возникать в 10–15 % случаев беременности. Для плода с ЗВУР риск спонтанных преждевременных родов в три раза выше по сравнению с плодом без задержки роста, а также в пять-шесть раз выше риск развития перинатальной смерти [2]. К сожалению, примерно у 50% новорожденных ЗВУР выявляют только после родов.
Плацентарная недостаточность является потенциальной причиной преждевременных родов, преэклампсии, ЗВУР и мертворождения, которые могут возникать в 10–15 % случаев беременности. Для плода с ЗВУР риск спонтанных преждевременных родов в три раза выше по сравнению с плодом без задержки роста, а также в пять-шесть раз выше риск развития перинатальной смерти [2]. К сожалению, примерно у 50% новорожденных ЗВУР выявляют только после родов.
Патофизиология
Хотя основная этиология плацентарной недостаточности неизвестна, существуют предполагаемые механизмы. Плацентарная недостаточность связана со снижением кровотока через пупок к плоду, что может быть вторичным по отношению к повышенному сопротивлению пуповинно-плацентарных сосудов. Это повышенное сопротивление можно визуализировать как аномальные допплеровские кривые скорости кровотока в пупочной артерии и оно может быть вторичным по отношению к аномалии прикрепления ворсинок к плацентарной мембране, нарушению перфузии между пупком и плацентой или снижению маточно-плацентарного кровотока. [2] Исследования допплерографии пупочной артерии показали, что степень повреждения плаценты напрямую связана со степенью повреждения плода во время беременности [9].]
[2] Исследования допплерографии пупочной артерии показали, что степень повреждения плаценты напрямую связана со степенью повреждения плода во время беременности [9].]
Основная роль плаценты заключается в том, чтобы служить связующим звеном между кровообращением плода и матери. Для этого необходимо обеспечить прилегание плаценты и ремоделирование артерий матки, чтобы обеспечить доставку питательных веществ к растущему плоду. Отличительной чертой успешной плацентации является ремоделирование маточных артерий. После оплодотворения формируется бластоциста, состоящая из внутренней клеточной массы, которая в конечном итоге станет плодом, и внешней оболочки, называемой трофобластом, которая становится плодной частью плаценты. Чтобы способствовать прилипанию к плаценте, цитотрофобласт, который является внутренним слоем трофобласта, секретирует металлопротеиназы матрикса, которые разрушают блестящую оболочку, а прилипанию способствует образование якорных ворсинок и экспрессия молекул адгезии. Эта инвазия маточно-плацентарных артерий позволяет ремоделировать их в расширенные, неэластичные сосуды с низким сопротивлением, которые лишены материнского вазомоторного контроля, что приводит к увеличению маточно-плацентарной перфузии, что позволяет удовлетворять потребности плода. Любое нарушение процесса ремоделирования может приводить к повышению сопротивления маточно-плацентарных сосудов, что приводит к гипоперфузии плаценты и ее нижестоящим эффектам, включая активацию коагуляции, дисфункцию эндотелиальных клеток, тромбоз плаценты и отложения фибрина, что связано с развитием ЗВУР. .[5][3] Кроме того, если есть потеря фокальной адгезии эндоваскулярных трофобластов, можно увидеть уменьшение площади поверхности плаценты, связанное с плацентарной недостаточностью. Это уменьшение площади плацентарной поверхности, наряду с увеличением толщины плаценты, придает плаценте шаровидный вид, что постулируется как компенсаторный механизм плацентарной недостаточности.
Эта инвазия маточно-плацентарных артерий позволяет ремоделировать их в расширенные, неэластичные сосуды с низким сопротивлением, которые лишены материнского вазомоторного контроля, что приводит к увеличению маточно-плацентарной перфузии, что позволяет удовлетворять потребности плода. Любое нарушение процесса ремоделирования может приводить к повышению сопротивления маточно-плацентарных сосудов, что приводит к гипоперфузии плаценты и ее нижестоящим эффектам, включая активацию коагуляции, дисфункцию эндотелиальных клеток, тромбоз плаценты и отложения фибрина, что связано с развитием ЗВУР. .[5][3] Кроме того, если есть потеря фокальной адгезии эндоваскулярных трофобластов, можно увидеть уменьшение площади поверхности плаценты, связанное с плацентарной недостаточностью. Это уменьшение площади плацентарной поверхности, наряду с увеличением толщины плаценты, придает плаценте шаровидный вид, что постулируется как компенсаторный механизм плацентарной недостаточности.
Внутриутробная среда представляет собой среду с низким содержанием кислорода, поэтому кровообращение плода должно быть гибким, чтобы адаптироваться к любым изменениям, происходящим с маточно-плацентарной функцией. [9] Эта гипоксическая среда стимулирует ангиогенез, в результате чего образуются сосудистые связи между материнским кровообращением и межворсинчатым пространством. Теперь, когда создана сосудистая и питательная сеть поддержки, формируется трофобласт ворсинок, который состоит из материнских микроворсинок и базального слоя плода.[10] Для поддержания функции плаценты требуется большое количество энергии, на что указывает тот факт, что в нормальном физиологическом состоянии плацента потребляет примерно 70% глюкозы и 40% кислорода, которые в норме поступают в матку. Следовательно, для достижения оптимального роста и развития плода доставка питательных веществ в матку должна превышать потребности плаценты, чтобы оставались питательные вещества для использования плодом.[10] Следовательно, любое нарушение доставки питательных веществ в матку влияет на доставку питательных веществ к плоду.
[9] Эта гипоксическая среда стимулирует ангиогенез, в результате чего образуются сосудистые связи между материнским кровообращением и межворсинчатым пространством. Теперь, когда создана сосудистая и питательная сеть поддержки, формируется трофобласт ворсинок, который состоит из материнских микроворсинок и базального слоя плода.[10] Для поддержания функции плаценты требуется большое количество энергии, на что указывает тот факт, что в нормальном физиологическом состоянии плацента потребляет примерно 70% глюкозы и 40% кислорода, которые в норме поступают в матку. Следовательно, для достижения оптимального роста и развития плода доставка питательных веществ в матку должна превышать потребности плаценты, чтобы оставались питательные вещества для использования плодом.[10] Следовательно, любое нарушение доставки питательных веществ в матку влияет на доставку питательных веществ к плоду.
На успешную плацентацию может негативно повлиять латерализация, когда инвазия плаценты происходит в одну сторону, а плацента имплантируется не центрально. Если плацента остается асимметричной до срока, ультразвуковая допплерография продемонстрирует стойкие насечки на неимплантированной стороне, что приведет к относительной плацентарной недостаточности. Латерализация плаценты также была связана с повышенным риском развития материнской преэклампсии и, следовательно, нижестоящей плацентарной недостаточности.][11]
Если плацента остается асимметричной до срока, ультразвуковая допплерография продемонстрирует стойкие насечки на неимплантированной стороне, что приведет к относительной плацентарной недостаточности. Латерализация плаценты также была связана с повышенным риском развития материнской преэклампсии и, следовательно, нижестоящей плацентарной недостаточности.][11]
Анамнез и физикальное исследование
Поскольку задержка внутриутробного развития является одним из основных исходов, связанных с плацентарной недостаточностью, большинство выживших новорожденных поступают либо преждевременно и известны как новорожденные с «экстремально низкой массой тела при рождении» (ЭНМТ), либо в зависимости от когда произошло нарушение кровоснабжения, они могут иметь измененные пропорции тела при рождении. При отторжении плаценты последующие эффекты, такие как ЗВУР, клинически очевидны при допплеровском исследовании примерно на 26-й неделе беременности [9].]
При подозрении на ЗВУР, независимо от того, является ли он вторичным по отношению к плацентарной недостаточности или другой этиологии, плоду будет полезен частый комбинированный мониторинг с использованием как допплеровского, так и биофизического профиля. Эта комбинация методов скрининга позволяет распознать снижение производительности, наблюдаемое, когда ЗВУР связана с плацентарными проблемами. Используя допплеровское исследование, неудачную плацентацию можно визуализировать по зазубринам в маточных артериях, а также по увеличению сопротивления в пупочной артерии с прогрессированием либо до отсутствия, либо до обратного конечно-диастолического объема. Одним из первых признаков, наблюдаемых в биофизическом профиле при подозрении на нарушение плода, является нереактивная запись сердечного ритма плода. Следующее будет либо плохим, либо потерей движений тела плода, дыхательных движений и тонуса. Эти признаки ухудшения допплеровского статуса и плохие биофизические профили типичны при дистрессе плода, который часто встречается при плацентарной недостаточности и может указывать на необходимость родоразрешения.
Эта комбинация методов скрининга позволяет распознать снижение производительности, наблюдаемое, когда ЗВУР связана с плацентарными проблемами. Используя допплеровское исследование, неудачную плацентацию можно визуализировать по зазубринам в маточных артериях, а также по увеличению сопротивления в пупочной артерии с прогрессированием либо до отсутствия, либо до обратного конечно-диастолического объема. Одним из первых признаков, наблюдаемых в биофизическом профиле при подозрении на нарушение плода, является нереактивная запись сердечного ритма плода. Следующее будет либо плохим, либо потерей движений тела плода, дыхательных движений и тонуса. Эти признаки ухудшения допплеровского статуса и плохие биофизические профили типичны при дистрессе плода, который часто встречается при плацентарной недостаточности и может указывать на необходимость родоразрешения.
Оценка
В настоящее время отсутствуют критерии для диагностики плацентарной недостаточности, так как нет и стандартизированных методов диагностики. Частично проблема связана с большим разнообразием терминологии, используемой для описания того, что известно как «плацентарная недостаточность». и плацентарного кровообращения как в здоровом, так и в болезненном состоянии. Было обнаружено, что четыре допплеровских метода являются основными для получения полезной информации о кровообращении плода и матери, включая исследования пупочной артерии, исследования маточных артерий, исследования средней мозговой артерии и исследования венозного протока [9].] Поскольку плод продолжает созревать во время беременности к сроку, происходит множество изменений кровообращения, которые можно оценить с помощью ультразвуковой допплерографии.
Частично проблема связана с большим разнообразием терминологии, используемой для описания того, что известно как «плацентарная недостаточность». и плацентарного кровообращения как в здоровом, так и в болезненном состоянии. Было обнаружено, что четыре допплеровских метода являются основными для получения полезной информации о кровообращении плода и матери, включая исследования пупочной артерии, исследования маточных артерий, исследования средней мозговой артерии и исследования венозного протока [9].] Поскольку плод продолжает созревать во время беременности к сроку, происходит множество изменений кровообращения, которые можно оценить с помощью ультразвуковой допплерографии.
До наступления беременности в маточных артериях наблюдается низкий диастолический кровоток, высокое сопротивление и эластическая тяга, отмеченная в виде ранних диастолических насечек. Успешная плацентация предполагает удаление интимной мышцы из сосудистой сети таким образом, чтобы кровеносные сосуды имели сильный диастолический кровоток, минимальное сопротивление и не обладали эластическими свойствами. При успешной плацентации ультразвуковая допплерография показывает, что ремоделирование происходит быстро, так что к 12 неделе беременности происходит потеря насечки, а резистентность снижается к 20 неделе беременности или ранее. При отторжении плаценты насечка сохраняется, а резистентность остается высокой, что коррелирует с осложнениями у плода, связанными с материнской гипертонией, включая ЗВУР, преэклампсию и гибель плода [9].] Было показано, что использование маточной артерии для допплеровского скрининга для оценки надрезов и сопротивления, чтобы помочь выявить эти ситуации с высоким риском, дает примерно 85% чувствительности для выявления тяжелой ЗВУР и преэклампсии.
При успешной плацентации ультразвуковая допплерография показывает, что ремоделирование происходит быстро, так что к 12 неделе беременности происходит потеря насечки, а резистентность снижается к 20 неделе беременности или ранее. При отторжении плаценты насечка сохраняется, а резистентность остается высокой, что коррелирует с осложнениями у плода, связанными с материнской гипертонией, включая ЗВУР, преэклампсию и гибель плода [9].] Было показано, что использование маточной артерии для допплеровского скрининга для оценки надрезов и сопротивления, чтобы помочь выявить эти ситуации с высоким риском, дает примерно 85% чувствительности для выявления тяжелой ЗВУР и преэклампсии.
По мере увеличения сопротивления плаценты допплеровские исследования пупочной артерии могут показать нормальную, сниженную, отсутствующую или обратную конечно-диастолическую скорость.[12][8] Высокое сопротивление плаценты на ранних сроках беременности является нормальным явлением, и поэтому можно ожидать, что конечная диастолическая скорость будет отсутствовать при допплеровском исследовании до 12–14 недель беременности. Когда плацента успешно прорастает, резистентность падает, а допплеровское исследование пупочной артерии должно демонстрировать непрерывный кровоток к 14–18 неделям беременности.[9]] Стойкое сопротивление пупочной артерии на протяжении всей беременности является показателем повышенного риска плацентарной недостаточности.
Когда плацента успешно прорастает, резистентность падает, а допплеровское исследование пупочной артерии должно демонстрировать непрерывный кровоток к 14–18 неделям беременности.[9]] Стойкое сопротивление пупочной артерии на протяжении всей беременности является показателем повышенного риска плацентарной недостаточности.
В то время как допплеровское исследование пупочной артерии дает важную информацию о возможном поражении плаценты, ценным дополнением является также использование допплеровского исследования средней мозговой артерии (СМА). MCA предоставляет информацию о реакциях системного кровообращения у развивающегося плода, поскольку он представляет сопротивление нижележащей микроциркуляции головного мозга. Нормальная допплерография СМА показывает высокое сопротивление на протяжении всей беременности; тем не менее, плацентарное заболевание можно идентифицировать, когда увеличивается диастолический поток наряду со снижением пульсового индекса. Таким образом, допплеровское исследование СМА может предоставить важную дополнительную информацию, когда есть подозрение на тяжелую ЗВУР, указывая на возможное нарушение плода и необходимость вмешательства.
Другой формой допплерографии, которая дает представление о здоровье плаценты и плода, является венозная допплерография, которая передает информацию, относящуюся к сердечным данным, когда кровообращение плода испытывает стресс. Венозная кривая, которая, как было показано, обеспечивает наилучшие клинические данные, представляет собой венозный проток. Есть много преимуществ использования венозного протока по сравнению с другими венозными волнами, которые включают его реакцию на изменения оксигенации, он является одним из основных регуляторов венозного возврата при аномальном и нормальном кровообращении плода, он не зависит от сердечной функции, он служит прямой канал для просмотра ретроградных пульсовых волн правого предсердия, и, наконец, поскольку он имеет повышенный и фокальный цветной доплеровский сигнал скорости уже с 12 недель беременности до 40 недель беременности, его очень легко визуализировать [9].] Если аномальный венозный проток или ретроградная предсердная волна визуализируются при допплерографии примерно на 12–14 неделе беременности, существует повышенный риск сердечных аномалий плода, и это также служит возможным предвестником, указывающим на тяжелую ЗВУР на основе плаценты.
МРТ позволяет получить дополнительную информацию для обнаружения и диагностики плацентарной недостаточности. Пустоты потока возникают, когда наблюдается потеря сигнала МРТ в кровеносном сосуде, где кровь течет энергично. При использовании Т2-взвешенной визуализации с усилением релаксации (RARE) плацентарная недостаточность может быть обнаружена, когда между плацентой и маткой наблюдаются уменьшенные пустоты потока, поскольку это можно рассматривать как отражение снижения маточно-плацентарной перфузии. Дополнительным преимуществом МРТ является высокая контрастность мягких тканей. Таким образом, плацентарные сосудистые аномалии, в том числе кровоизлияния и инфаркты, могут быть обнаружены на МРТ плаценты, что указывает на высокий риск плацентарной недостаточности и ЗВУР ниже по течению.
Лечение/управление
В настоящее время не существует известного лечения плацентарной недостаточности, кроме родоразрешения, если оно находится в жизнеспособном состоянии. Было показано, что низкие дозы аспирина и использование антиоксидантной терапии, включая витамины С и Е, способствуют улучшению плацентации в тех случаях, когда есть неопределенность в отношении успешной плацентации. [9] Исследования показали, что перинатальная смертность снижается примерно на 38%, когда ранняя допплерография используется для случаев подозрения на ЗВУР во время беременности.[12][13]
[9] Исследования показали, что перинатальная смертность снижается примерно на 38%, когда ранняя допплерография используется для случаев подозрения на ЗВУР во время беременности.[12][13]
Женщинам из группы высокого риска, например женщинам с хронической гипертензией, коагулопатиями или преэклампсией в анамнезе, может быть полезно проведение допплеровского ультразвукового скрининга на сроке от 12 до 14 недель беременности, потому что, если двусторонняя насечка очевидна, следует назначить терапию низкими дозами аспирина следует инициировать.
Исследования in vitro показали, что гепарин может стимулировать неоангиогенез, а также улучшать плацентарную перфузию. Антикоагулянтные свойства гепарина проявляются в его способности мобилизовать фактор тканевого ингибирования в кровообращение, а также в том, что он также усиливает антитромбиновую активность. Дополнительные преимущества гепарина при рассмотрении плацентарной недостаточности и ее последующих последствий заключаются в том, что гепарин способствует пролиферации трофобластов, уменьшает воспаление за счет подавления каскада комплемента, уменьшает апоптоз, а также косвенно действует как фактор роста. [3]
[3]
Было также показано, что гепарин активирует определенные белки, участвующие в плацентарном ангиогенезе и развитии. К ним относятся ангиопоэтин-2, отвечающий за ремоделирование сосудов ворсин хориона, лептин, отвечающий за регуляцию переноса питательных веществ, а также рецептор фактора роста эндотелия сосудов-3, тканевой ингибитор матриксной металлопротеазы-1, фактор некроза опухоли-альфа. и ангиостатин. Основываясь на его свойствах и предварительных данных, некоторые исследования показали, что гепарин может играть роль в профилактическом лечении плацентарной болезни.
Дифференциальный диагноз
Существует много факторов, которые могут способствовать развитию плацентарной недостаточности, и известно, что ЗВУР является серьезным последующим осложнением; однако иногда может быть трудно отличить новорожденного с малым весом для гестационного возраста (SGA) от новорожденного с IUGR. Одно из основных преимуществ допплеровских исследований, особенно пупочной артерии, заключается в том, что допплерографию аномальных пупочных артерий можно использовать для дифференциации между патологической ЗВУР и малым для гестационного возраста новорожденным, таким образом определяя, при какой беременности требуется высокоуровневое наблюдение. по сравнению с рутинным мониторингом.[9][14]
по сравнению с рутинным мониторингом.[9][14]
Если средний расчетный вес плода ниже 10-го процентиля для определенного гестационного возраста, этот плод является SGA. И наоборот, плод с ЗВУР не сможет достичь нормального роста, как правило, вследствие плацентарной недостаточности, генетического заболевания или инфекции.[14] Следовательно, новорожденный с SGA будет физически маленьким, но в целом здоровым, по сравнению с новорожденным с IUGR, который также может быть физически маленьким, но, вероятно, его здоровье будет скомпрометировано.
При рассмотрении дифференциальных диагнозов, которые способствуют плацентарной недостаточности, известны сопутствующие заболевания, включая, помимо прочего, преэклампсию, гипертензивные расстройства у матери, поскольку оба они нарушают плацентарную резистентность и маточно-плацентарный кровоток. Другие заболевания, которые следует учитывать, включают маловодие и недоедание матери или ограничение калорий.
Прогноз
Если новорожденный страдает ЗВУР в результате плацентарной недостаточности и выживает в перинатальном периоде, он подвергается более высокому риску развития когнитивных нарушений в детстве, чем детский церебральный паралич и судорожные расстройства, по сравнению с новорожденным без задержки роста. Пациенты, страдающие плацентарной недостаточностью, часто имеют аномальные кривые скорости кровотока в пупочной артерии (DFVW), и когда в одном исследовании сравнивали DFVW младенцев, у которых была плацентарная недостаточность внутриутробно, с теми младенцами, у которых ее не было, они обнаружили, что младенцы, у которых была аномальная У DFVW также был более низкий IQ, когда им было 5 лет. Имеются также доказательства того, что ЗВУР в младенчестве предрасполагает к хроническим заболеваниям во взрослом возрасте, включая повышенный риск развития ишемической болезни сердца, гипертонии и диабета.[2]
Пациенты, страдающие плацентарной недостаточностью, часто имеют аномальные кривые скорости кровотока в пупочной артерии (DFVW), и когда в одном исследовании сравнивали DFVW младенцев, у которых была плацентарная недостаточность внутриутробно, с теми младенцами, у которых ее не было, они обнаружили, что младенцы, у которых была аномальная У DFVW также был более низкий IQ, когда им было 5 лет. Имеются также доказательства того, что ЗВУР в младенчестве предрасполагает к хроническим заболеваниям во взрослом возрасте, включая повышенный риск развития ишемической болезни сердца, гипертонии и диабета.[2]
Чтобы обеспечить лучший прогноз для новорожденного, приоритет должен быть сосредоточен на вмешательствах, которые позволяют максимально увеличить гестационный возраст при рождении. Подсчитано, что каждая неделя беременности плода между 24-й и 28-й неделями беременности увеличивает выживаемость без сопутствующих осложнений примерно на 10–15 % [3].
Осложнения
Последующие эффекты плацентарной недостаточности на развивающийся плод сложны и многофакторны; однако основными эффектами, как правило, являются плацентарная дыхательная недостаточность и гипоксемия плода, оба из которых способствуют ограничению внутриутробного развития и связанным с ним последствиям, включая недоношенность.
Самым опасным осложнением, очевидно, является полное отсутствие плацентации и, как следствие, выкидыш. Для развивающегося плода степень аномалий пупочной артерии, наблюдаемая при допплерографии, коррелирует с ацидозом, потребностью в реанимации, прессорной поддержке, вентиляционной поддержке, а также полисистемной недостаточностью органов, которая имеет тенденцию возникать при гипоксемии, поскольку это вызывает перераспределение кровотока. у развивающегося плода к основным органам, таким как мозг и сердце, за счет других соответствующих органов, таких как кишечник и почки. Кроме того, когда допплеровские исследования демонстрируют отсутствие или реверсию конечно-диастолического кровотока, у новорожденных повышается частота внутрижелудочковых кровоизлияний [9].]
При повышении резистентности плаценты во время беременности плод с уже ЗВУР подвергается дальнейшему риску гипогликемии, гипоксически-ишемической энцефалопатии, тромбоцитопении, лейкопении и анемии.[8] Кроме того, есть данные, свидетельствующие о том, что у младенцев существует риск развития когнитивного дефицита в детстве, а затем развития хронических заболеваний во взрослом возрасте.
Предупреждение и просвещение пациентов
Крайне важно, чтобы регулярный пренатальный скрининг и ультразвуковое исследование проводились во время беременности женщины, чтобы обеспечить наилучшие возможные результаты для новорожденного. Хотя окончательных профилактических мер для плацентарной недостаточности не существует, после того, как она была распознана с помощью УЗИ, МРТ, плацентарной недостаточности или любой комбинации этих методов, можно начинать такие вмешательства, как терапия гепарином, с надеждой на продление беременности с надеждой на минимизацию ацидоз и гипоксия и, как следствие, ЗВУР, недоношенность или гибель плода. Необходимо провести дальнейшие исследования вмешательств и методов лечения, и во время беременности они принесут наибольшую пользу развивающемуся плоду.
Pearls and Other Issues
Определенного лекарства от плацентарной недостаточности не существует, но последствия можно свести к минимуму, если диагностировать ее на ранней стадии, и мать получает надлежащий дородовой уход. Недавний метаанализ показал, что гепарин может стимулировать рост плода и пролонгировать беременность, если гепарин назначается пациентам с высоким подозрением на плацентарную недостаточность, но не снижает неблагоприятных исходов у новорожденных.
Недавний метаанализ показал, что гепарин может стимулировать рост плода и пролонгировать беременность, если гепарин назначается пациентам с высоким подозрением на плацентарную недостаточность, но не снижает неблагоприятных исходов у новорожденных.
Улучшение результатов работы команды здравоохранения
Согласно допплеровским исследованиям, самые ранние признаки несостоятельности плаценты, вероятно, не будут обнаружены, по крайней мере, после 12 недель беременности, что коррелирует с проспективным когортным исследованием, которое показало, что скрининг плацентарной функции при беременностях с высоким риском во втором триместре по сравнению с первым триместром лучший предиктор неблагоприятных перинатальных исходов.[15]
При обсуждении плацентарной недостаточности будет задействовано как минимум две команды, если не больше, которые будут заниматься уходом за пациентками, так как одна команда будет нести ответственность за наблюдение за матерью и плодом до родов, а другая команда будет заботиться о для новорожденного после родов. Ведение как матери, так и ребенка с задержкой внутриутробного развития требует междисциплинарной команды, состоящей из акушеров-гинекологов, реаниматологов-реаниматологов, медсестер акушерства и отделения интенсивной терапии, респираторных терапевтов, фармацевтов, пульмонологов, а иногда и других специальностей, включая хирургию, инфекционные заболевания или генетику.
Ведение как матери, так и ребенка с задержкой внутриутробного развития требует междисциплинарной команды, состоящей из акушеров-гинекологов, реаниматологов-реаниматологов, медсестер акушерства и отделения интенсивной терапии, респираторных терапевтов, фармацевтов, пульмонологов, а иногда и других специальностей, включая хирургию, инфекционные заболевания или генетику.
У новорожденных с ЗВУР часто развиваются хронические заболевания легких, вторичные по отношению к их недоношенности, и может потребоваться несколько лекарств, а также домашняя оксигенация, или у них могут развиться множественные инфекции, включая некротизирующий энтероколит или поздний сепсис, все из которых требуют координации между вышеупомянутые команды, чтобы обеспечить улучшенные результаты для пациента. Иногда, в зависимости от исхода беременности, важно привлечь комитет по этике или группу паллиативной помощи. Часто семьям легче организовать семейные встречи, на которых присутствует хотя бы один член от каждой специализированной группы, поскольку это улучшает общение между всеми командами и дает семьям возможность задать свои вопросы сразу всем специалистам.
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
Ссылки
- 1.
Хант К., Кеннеди С.Х., Ватиш М. Определения и сообщения о плацентарной недостаточности в биомедицинских журналах: обзор литературы. Eur J Obstet Gynecol Reprod Biol. 2016 окт.; 205:146-9. [PubMed: 27591716]
- 2.
Ганьон Р. Плацентарная недостаточность и ее последствия. Eur J Obstet Gynecol Reprod Biol. 22 сентября 2003 г .; 110 Приложение 1: S99-107. [PubMed: 12965097]
- 3.
Mazarico E, Molinet-Coll C, Martinez-Portilla RJ, Figueras F. Терапия гепарином при плацентарной недостаточности: систематический обзор и метаанализ. Acta Obstet Gynecol Scand. 2020 фев; 99 (2): 167-174. [PubMed: 31519033]
- 4.
Агарвал Р., Тивари А., Вадхва Н., Радхакришнан Г. Гистопатологические данные плаценты при недоношенности/доношенности и раннем/позднем начале малы для гестационного возраста: являются ли они значительными? Индиан Дж.
 Патол Микробиол. 2017 г., апрель-июнь; 60(2):232-235. [В паблике: 28631641]
Патол Микробиол. 2017 г., апрель-июнь; 60(2):232-235. [В паблике: 28631641]- 5.
Ohgiya Y, Nobusawa H, Seino N, Miyagami O, Yagi N, Hiroto S, Munechika J, Hirose M, Takeyama N, Ohike N, Matsuoka R, Sekizawa A, Gokan T. MR Imaging of Плоды для оценки плацентарной недостаточности. Magn Reson Med Sci. 2016;15(2):212-9. [Статья бесплатно PMC: PMC5600058] [PubMed: 26607809]
- 6.
Пинтикан Д., Пойенар А.А., Стрильчук С., Миху Д. Влияние курения матери на васкуляризацию плаценты человека: систематический обзор. Тайвань J Obstet Gynecol. 2019Июль; 58 (4): 454-459. [PubMed: 31307732]
- 7.
Audette MC, Kingdom JC. Скрининг задержки роста плода и плацентарной недостаточности. Semin Fetal Neonatal Med. 2018 апр; 23 (2): 119-125. [PubMed: 29221766]
- 8.
Башат А.А., Харман Ч.Р., Гембрух У. Гематологические последствия плацентарной недостаточности. Arch Dis Child Fetal Neonatal Ed. 2004 Январь;89(1):F94.
 [Бесплатная статья PMC: PMC1721655] [PubMed: 14711871]
[Бесплатная статья PMC: PMC1721655] [PubMed: 14711871]- 9.
Harman CR, Baschat AA. Комплексная оценка состояния плода: какие допплеровские исследования следует провести? Curr Opin Obstet Gynecol. 2003 г., 15 апреля (2): 147–57. [PubMed: 12634607]
- 10.
Башат А.А. Реакция плода на плацентарную недостаточность: обновление. БЖОГ. 2004 г., октябрь; 111 (10): 1031-41. [PubMed: 15383103]
- 11.
Юсуф С., Ахмад А., Кадир С., Гул С., Тали С.Х., Шахин Ф., Ахтар С., Дар Р. Использование плацентарной латеральности и допплеровских аномалий маточных артерий для прогнозирования преэклампсии . J Obstet Gynaecol Индия. 2016 окт; 66 (Приложение 1): 212-6. [Бесплатная статья PMC: PMC5016443] [PubMed: 27651606]
- 12.
Сейам Ю.С., Аль-Махмейд М.С., Аль-Тамими Х.К. Допплерометрия кровотока в пупочной артерии при задержке внутриутробного развития и ее связь с перинатальным исходом. Int J Gynaecol Obstet.
 2002 г., май; 77 (2): 131–137. [PubMed: 12031563]
2002 г., май; 77 (2): 131–137. [PubMed: 12031563]- 13.
Alfirevic Z, Neilson JP. Ультразвуковая допплерография при беременности с высоким риском: систематический обзор с метаанализом. Am J Obstet Gynecol. 1995 г., май; 172(5):1379-87. [PubMed: 7755042]
- 14.
Калаче К.Д., Дюкельманн А.М. Доплер в акушерстве: за пупочной артерией. Клин Обстет Гинекол. 2012 март; 55(1):288-95. [PubMed: 22343245]
- 15.
Коста С.Л., Проктор Л., Додд Дж.М., Тоал М., Окун Н., Джонсон Дж.А., Уиндрим Р., Королевство Дж.К. Скрининг плацентарной недостаточности при беременности высокого риска: лучше ли раньше? Плацента. 2008 декабря; 29 (12): 1034-40. [PubMed: 18930542]
Плацентарная недостаточность — StatPearls — NCBI Bookshelf
Непрерывное обучение
Плацентарная недостаточность — это состояние, при котором происходит нарушение ремоделирования плацентарных сосудов, что приводит к отсутствию плацентации, что приводит к ацидозу и гипоксемии плода. Наиболее распространенные последующие последствия этого состояния для плода включают задержку внутриутробного развития, недоношенность или, к сожалению, гибель плода. Чтобы снизить риск заболеваемости и смертности плода, особенно при беременности с высоким риском, следует проводить регулярный пренатальный скрининг с помощью ультразвуковой допплерографии, чтобы увеличить шансы обнаружения и диагностики. В этом мероприятии рассматриваются патофизиология, оценка и возможные методы лечения плацентарной недостаточности, а также подчеркивается роль межпрофессиональной команды в лечении пациентов с этим заболеванием.
Наиболее распространенные последующие последствия этого состояния для плода включают задержку внутриутробного развития, недоношенность или, к сожалению, гибель плода. Чтобы снизить риск заболеваемости и смертности плода, особенно при беременности с высоким риском, следует проводить регулярный пренатальный скрининг с помощью ультразвуковой допплерографии, чтобы увеличить шансы обнаружения и диагностики. В этом мероприятии рассматриваются патофизиология, оценка и возможные методы лечения плацентарной недостаточности, а также подчеркивается роль межпрофессиональной команды в лечении пациентов с этим заболеванием.
Цели:
Рассмотреть факторы риска, связанные с плацентарной недостаточностью.
Опишите типичные результаты ультразвуковой допплерографии, связанные с плацентарной недостаточностью.
Укажите наиболее распространенные нежелательные явления, связанные с плацентарной недостаточностью.
Получите доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Введение
Плацентарная недостаточность связана с различными акушерскими расстройствами, такими как преэклампсия и задержка внутриутробного развития плода, которые предрасполагают к преждевременным родам, основной причине перинатальной заболеваемости и смертности во всем мире. Плохая плацентарная функция чаще всего описывается термином «плацентарная недостаточность» в медицинском сообществе; однако одно исследование выявило проблему отсутствия стандартизированного определения или консенсуса в отношении патогномоничных признаков, относящихся к плацентарной недостаточности.[1]
Это создает много проблем, когда речь идет об изучении плацентарной недостаточности в литературе, но общее понимание состоит в том, что плацентарная недостаточность представляет собой процесс, при котором происходит прогрессирующее ухудшение функционирования плаценты, так что перенос кислорода и питательных веществ к плоду через плаценту нарушается. уменьшался, достигая высшей точки в декомпенсированной гипоксии и ацидозе. [2][3] Этот процесс приводит к гипоксемии плода, которая затем стимулирует снижение метаболических потребностей плода для сохранения уже доступных питательных веществ, что приводит к ограничению внутриутробного роста плода. С гистопатологической точки зрения плацентарная недостаточность может быть определена при наличии фиброза ворсин хориона, маточно-плацентарного тромбоза, плацентарных инфарктов, отложений фибрина или уменьшения количества и площади поверхности ворсинчатого капиллярного дерева.
[2][3] Этот процесс приводит к гипоксемии плода, которая затем стимулирует снижение метаболических потребностей плода для сохранения уже доступных питательных веществ, что приводит к ограничению внутриутробного роста плода. С гистопатологической точки зрения плацентарная недостаточность может быть определена при наличии фиброза ворсин хориона, маточно-плацентарного тромбоза, плацентарных инфарктов, отложений фибрина или уменьшения количества и площади поверхности ворсинчатого капиллярного дерева.
Следует отметить, что инфаркты плаценты могут быть нормальным явлением, так как они наблюдаются примерно в 25% нормальных доношенных беременностей; однако было показано, что учащение инфаркта плаценты связано с плацентарной недостаточностью и, следовательно, с задержкой внутриутробного развития (ЗВУР). Как МРТ, так и ультразвуковые исследования, направленные на выявление плацентарной недостаточности, продемонстрировали уменьшение площади и объема плаценты, а также увеличение толщины плаценты в дополнение к плацентам шаровидной формы на МРТ [5].
Этиология
На сегодняшний день основные причины, которые могут привести к плацентарной недостаточности, плохо изучены и все еще изучаются. Известны сопутствующие материнские факторы риска, которые включают преэклампсию или другие гипертензивные расстройства у матери, употребление матерью сигарет, употребление матерью наркотиков, включая кокаин или героин, употребление матерью алкоголя, первородство, преклонный возраст матери и наличие в анамнезе родов с ЗВУР у новорожденного. [2] [6]
Исследования, анализирующие допплеровские волны в различных плацентарных сосудах матерей, которые курили сигареты во время беременности, продемонстрировали уменьшение волн скорости кровотока, что указывает на то, что воздействие никотина может привести к изменению плацентарной сосудистой сети.[6]
Любое состояние матери, которое может привести к нарушению кровообращения плода, подвергает плод риску развития плацентарной недостаточности. Кроме того, некоторые лекарства, такие как противоопухолевые, противосудорожные или антикоагулянты, могут препятствовать росту плода. Экстремальные значения индекса массы тела матери, включая недоедание матери, также связаны с развитием ЗВУР у новорожденных.[7] Исследования беременностей, осложненных ЗВУР, продемонстрировали неполную трансформацию плацентарной сосудистой сети на ранних сроках беременности, которую можно обнаружить с помощью ультразвуковой допплерографии.
Экстремальные значения индекса массы тела матери, включая недоедание матери, также связаны с развитием ЗВУР у новорожденных.[7] Исследования беременностей, осложненных ЗВУР, продемонстрировали неполную трансформацию плацентарной сосудистой сети на ранних сроках беременности, которую можно обнаружить с помощью ультразвуковой допплерографии.
Эпидемиология
Недоношенность является ведущей причиной перинатальной смерти, за которой следует задержка внутриутробного развития плода, осложняющая примерно от 4% до 6% известных беременностей. Плацентарная недостаточность является потенциальной причиной преждевременных родов, преэклампсии, ЗВУР и мертворождения, которые могут возникать в 10–15 % случаев беременности. Для плода с ЗВУР риск спонтанных преждевременных родов в три раза выше по сравнению с плодом без задержки роста, а также в пять-шесть раз выше риск развития перинатальной смерти [2]. К сожалению, примерно у 50% новорожденных ЗВУР выявляют только после родов.
Патофизиология
Хотя основная этиология плацентарной недостаточности неизвестна, существуют предполагаемые механизмы. Плацентарная недостаточность связана со снижением кровотока через пупок к плоду, что может быть вторичным по отношению к повышенному сопротивлению пуповинно-плацентарных сосудов. Это повышенное сопротивление можно визуализировать как аномальные допплеровские кривые скорости кровотока в пупочной артерии и оно может быть вторичным по отношению к аномалии прикрепления ворсинок к плацентарной мембране, нарушению перфузии между пупком и плацентой или снижению маточно-плацентарного кровотока.[2] Исследования допплерографии пупочной артерии показали, что степень повреждения плаценты напрямую связана со степенью повреждения плода во время беременности [9].]
Плацентарная недостаточность связана со снижением кровотока через пупок к плоду, что может быть вторичным по отношению к повышенному сопротивлению пуповинно-плацентарных сосудов. Это повышенное сопротивление можно визуализировать как аномальные допплеровские кривые скорости кровотока в пупочной артерии и оно может быть вторичным по отношению к аномалии прикрепления ворсинок к плацентарной мембране, нарушению перфузии между пупком и плацентой или снижению маточно-плацентарного кровотока.[2] Исследования допплерографии пупочной артерии показали, что степень повреждения плаценты напрямую связана со степенью повреждения плода во время беременности [9].]
Основная роль плаценты заключается в том, чтобы служить связующим звеном между кровообращением плода и матери. Для этого необходимо обеспечить прилегание плаценты и ремоделирование артерий матки, чтобы обеспечить доставку питательных веществ к растущему плоду. Отличительной чертой успешной плацентации является ремоделирование маточных артерий. После оплодотворения формируется бластоциста, состоящая из внутренней клеточной массы, которая в конечном итоге станет плодом, и внешней оболочки, называемой трофобластом, которая становится плодной частью плаценты. Чтобы способствовать прилипанию к плаценте, цитотрофобласт, который является внутренним слоем трофобласта, секретирует металлопротеиназы матрикса, которые разрушают блестящую оболочку, а прилипанию способствует образование якорных ворсинок и экспрессия молекул адгезии. Эта инвазия маточно-плацентарных артерий позволяет ремоделировать их в расширенные, неэластичные сосуды с низким сопротивлением, которые лишены материнского вазомоторного контроля, что приводит к увеличению маточно-плацентарной перфузии, что позволяет удовлетворять потребности плода. Любое нарушение процесса ремоделирования может приводить к повышению сопротивления маточно-плацентарных сосудов, что приводит к гипоперфузии плаценты и ее нижестоящим эффектам, включая активацию коагуляции, дисфункцию эндотелиальных клеток, тромбоз плаценты и отложения фибрина, что связано с развитием ЗВУР.
После оплодотворения формируется бластоциста, состоящая из внутренней клеточной массы, которая в конечном итоге станет плодом, и внешней оболочки, называемой трофобластом, которая становится плодной частью плаценты. Чтобы способствовать прилипанию к плаценте, цитотрофобласт, который является внутренним слоем трофобласта, секретирует металлопротеиназы матрикса, которые разрушают блестящую оболочку, а прилипанию способствует образование якорных ворсинок и экспрессия молекул адгезии. Эта инвазия маточно-плацентарных артерий позволяет ремоделировать их в расширенные, неэластичные сосуды с низким сопротивлением, которые лишены материнского вазомоторного контроля, что приводит к увеличению маточно-плацентарной перфузии, что позволяет удовлетворять потребности плода. Любое нарушение процесса ремоделирования может приводить к повышению сопротивления маточно-плацентарных сосудов, что приводит к гипоперфузии плаценты и ее нижестоящим эффектам, включая активацию коагуляции, дисфункцию эндотелиальных клеток, тромбоз плаценты и отложения фибрина, что связано с развитием ЗВУР. .[5][3] Кроме того, если есть потеря фокальной адгезии эндоваскулярных трофобластов, можно увидеть уменьшение площади поверхности плаценты, связанное с плацентарной недостаточностью. Это уменьшение площади плацентарной поверхности, наряду с увеличением толщины плаценты, придает плаценте шаровидный вид, что постулируется как компенсаторный механизм плацентарной недостаточности.
.[5][3] Кроме того, если есть потеря фокальной адгезии эндоваскулярных трофобластов, можно увидеть уменьшение площади поверхности плаценты, связанное с плацентарной недостаточностью. Это уменьшение площади плацентарной поверхности, наряду с увеличением толщины плаценты, придает плаценте шаровидный вид, что постулируется как компенсаторный механизм плацентарной недостаточности.
Внутриутробная среда представляет собой среду с низким содержанием кислорода, поэтому кровообращение плода должно быть гибким, чтобы адаптироваться к любым изменениям, происходящим с маточно-плацентарной функцией.[9] Эта гипоксическая среда стимулирует ангиогенез, в результате чего образуются сосудистые связи между материнским кровообращением и межворсинчатым пространством. Теперь, когда создана сосудистая и питательная сеть поддержки, формируется трофобласт ворсинок, который состоит из материнских микроворсинок и базального слоя плода.[10] Для поддержания функции плаценты требуется большое количество энергии, на что указывает тот факт, что в нормальном физиологическом состоянии плацента потребляет примерно 70% глюкозы и 40% кислорода, которые в норме поступают в матку. Следовательно, для достижения оптимального роста и развития плода доставка питательных веществ в матку должна превышать потребности плаценты, чтобы оставались питательные вещества для использования плодом.[10] Следовательно, любое нарушение доставки питательных веществ в матку влияет на доставку питательных веществ к плоду.
Следовательно, для достижения оптимального роста и развития плода доставка питательных веществ в матку должна превышать потребности плаценты, чтобы оставались питательные вещества для использования плодом.[10] Следовательно, любое нарушение доставки питательных веществ в матку влияет на доставку питательных веществ к плоду.
На успешную плацентацию может негативно повлиять латерализация, когда инвазия плаценты происходит в одну сторону, а плацента имплантируется не центрально. Если плацента остается асимметричной до срока, ультразвуковая допплерография продемонстрирует стойкие насечки на неимплантированной стороне, что приведет к относительной плацентарной недостаточности. Латерализация плаценты также была связана с повышенным риском развития материнской преэклампсии и, следовательно, нижестоящей плацентарной недостаточности.][11]
Анамнез и физикальное исследование
Поскольку задержка внутриутробного развития является одним из основных исходов, связанных с плацентарной недостаточностью, большинство выживших новорожденных поступают либо преждевременно и известны как новорожденные с «экстремально низкой массой тела при рождении» (ЭНМТ), либо в зависимости от когда произошло нарушение кровоснабжения, они могут иметь измененные пропорции тела при рождении. При отторжении плаценты последующие эффекты, такие как ЗВУР, клинически очевидны при допплеровском исследовании примерно на 26-й неделе беременности [9].]
При отторжении плаценты последующие эффекты, такие как ЗВУР, клинически очевидны при допплеровском исследовании примерно на 26-й неделе беременности [9].]
При подозрении на ЗВУР, независимо от того, является ли он вторичным по отношению к плацентарной недостаточности или другой этиологии, плоду будет полезен частый комбинированный мониторинг с использованием как допплеровского, так и биофизического профиля. Эта комбинация методов скрининга позволяет распознать снижение производительности, наблюдаемое, когда ЗВУР связана с плацентарными проблемами. Используя допплеровское исследование, неудачную плацентацию можно визуализировать по зазубринам в маточных артериях, а также по увеличению сопротивления в пупочной артерии с прогрессированием либо до отсутствия, либо до обратного конечно-диастолического объема. Одним из первых признаков, наблюдаемых в биофизическом профиле при подозрении на нарушение плода, является нереактивная запись сердечного ритма плода. Следующее будет либо плохим, либо потерей движений тела плода, дыхательных движений и тонуса. Эти признаки ухудшения допплеровского статуса и плохие биофизические профили типичны при дистрессе плода, который часто встречается при плацентарной недостаточности и может указывать на необходимость родоразрешения.
Эти признаки ухудшения допплеровского статуса и плохие биофизические профили типичны при дистрессе плода, который часто встречается при плацентарной недостаточности и может указывать на необходимость родоразрешения.
Оценка
В настоящее время отсутствуют критерии для диагностики плацентарной недостаточности, так как нет и стандартизированных методов диагностики. Частично проблема связана с большим разнообразием терминологии, используемой для описания того, что известно как «плацентарная недостаточность». и плацентарного кровообращения как в здоровом, так и в болезненном состоянии. Было обнаружено, что четыре допплеровских метода являются основными для получения полезной информации о кровообращении плода и матери, включая исследования пупочной артерии, исследования маточных артерий, исследования средней мозговой артерии и исследования венозного протока [9].] Поскольку плод продолжает созревать во время беременности к сроку, происходит множество изменений кровообращения, которые можно оценить с помощью ультразвуковой допплерографии.
До наступления беременности в маточных артериях наблюдается низкий диастолический кровоток, высокое сопротивление и эластическая тяга, отмеченная в виде ранних диастолических насечек. Успешная плацентация предполагает удаление интимной мышцы из сосудистой сети таким образом, чтобы кровеносные сосуды имели сильный диастолический кровоток, минимальное сопротивление и не обладали эластическими свойствами. При успешной плацентации ультразвуковая допплерография показывает, что ремоделирование происходит быстро, так что к 12 неделе беременности происходит потеря насечки, а резистентность снижается к 20 неделе беременности или ранее. При отторжении плаценты насечка сохраняется, а резистентность остается высокой, что коррелирует с осложнениями у плода, связанными с материнской гипертонией, включая ЗВУР, преэклампсию и гибель плода [9].] Было показано, что использование маточной артерии для допплеровского скрининга для оценки надрезов и сопротивления, чтобы помочь выявить эти ситуации с высоким риском, дает примерно 85% чувствительности для выявления тяжелой ЗВУР и преэклампсии.
По мере увеличения сопротивления плаценты допплеровские исследования пупочной артерии могут показать нормальную, сниженную, отсутствующую или обратную конечно-диастолическую скорость.[12][8] Высокое сопротивление плаценты на ранних сроках беременности является нормальным явлением, и поэтому можно ожидать, что конечная диастолическая скорость будет отсутствовать при допплеровском исследовании до 12–14 недель беременности. Когда плацента успешно прорастает, резистентность падает, а допплеровское исследование пупочной артерии должно демонстрировать непрерывный кровоток к 14–18 неделям беременности.[9]] Стойкое сопротивление пупочной артерии на протяжении всей беременности является показателем повышенного риска плацентарной недостаточности.
В то время как допплеровское исследование пупочной артерии дает важную информацию о возможном поражении плаценты, ценным дополнением является также использование допплеровского исследования средней мозговой артерии (СМА). MCA предоставляет информацию о реакциях системного кровообращения у развивающегося плода, поскольку он представляет сопротивление нижележащей микроциркуляции головного мозга. Нормальная допплерография СМА показывает высокое сопротивление на протяжении всей беременности; тем не менее, плацентарное заболевание можно идентифицировать, когда увеличивается диастолический поток наряду со снижением пульсового индекса. Таким образом, допплеровское исследование СМА может предоставить важную дополнительную информацию, когда есть подозрение на тяжелую ЗВУР, указывая на возможное нарушение плода и необходимость вмешательства.
Нормальная допплерография СМА показывает высокое сопротивление на протяжении всей беременности; тем не менее, плацентарное заболевание можно идентифицировать, когда увеличивается диастолический поток наряду со снижением пульсового индекса. Таким образом, допплеровское исследование СМА может предоставить важную дополнительную информацию, когда есть подозрение на тяжелую ЗВУР, указывая на возможное нарушение плода и необходимость вмешательства.
Другой формой допплерографии, которая дает представление о здоровье плаценты и плода, является венозная допплерография, которая передает информацию, относящуюся к сердечным данным, когда кровообращение плода испытывает стресс. Венозная кривая, которая, как было показано, обеспечивает наилучшие клинические данные, представляет собой венозный проток. Есть много преимуществ использования венозного протока по сравнению с другими венозными волнами, которые включают его реакцию на изменения оксигенации, он является одним из основных регуляторов венозного возврата при аномальном и нормальном кровообращении плода, он не зависит от сердечной функции, он служит прямой канал для просмотра ретроградных пульсовых волн правого предсердия, и, наконец, поскольку он имеет повышенный и фокальный цветной доплеровский сигнал скорости уже с 12 недель беременности до 40 недель беременности, его очень легко визуализировать [9]. ] Если аномальный венозный проток или ретроградная предсердная волна визуализируются при допплерографии примерно на 12–14 неделе беременности, существует повышенный риск сердечных аномалий плода, и это также служит возможным предвестником, указывающим на тяжелую ЗВУР на основе плаценты.
] Если аномальный венозный проток или ретроградная предсердная волна визуализируются при допплерографии примерно на 12–14 неделе беременности, существует повышенный риск сердечных аномалий плода, и это также служит возможным предвестником, указывающим на тяжелую ЗВУР на основе плаценты.
МРТ позволяет получить дополнительную информацию для обнаружения и диагностики плацентарной недостаточности. Пустоты потока возникают, когда наблюдается потеря сигнала МРТ в кровеносном сосуде, где кровь течет энергично. При использовании Т2-взвешенной визуализации с усилением релаксации (RARE) плацентарная недостаточность может быть обнаружена, когда между плацентой и маткой наблюдаются уменьшенные пустоты потока, поскольку это можно рассматривать как отражение снижения маточно-плацентарной перфузии. Дополнительным преимуществом МРТ является высокая контрастность мягких тканей. Таким образом, плацентарные сосудистые аномалии, в том числе кровоизлияния и инфаркты, могут быть обнаружены на МРТ плаценты, что указывает на высокий риск плацентарной недостаточности и ЗВУР ниже по течению.
Лечение/управление
В настоящее время не существует известного лечения плацентарной недостаточности, кроме родоразрешения, если оно находится в жизнеспособном состоянии. Было показано, что низкие дозы аспирина и использование антиоксидантной терапии, включая витамины С и Е, способствуют улучшению плацентации в тех случаях, когда есть неопределенность в отношении успешной плацентации.[9] Исследования показали, что перинатальная смертность снижается примерно на 38%, когда ранняя допплерография используется для случаев подозрения на ЗВУР во время беременности.[12][13]
Женщинам из группы высокого риска, например женщинам с хронической гипертензией, коагулопатиями или преэклампсией в анамнезе, может быть полезно проведение допплеровского ультразвукового скрининга на сроке от 12 до 14 недель беременности, потому что, если двусторонняя насечка очевидна, следует назначить терапию низкими дозами аспирина следует инициировать.
Исследования in vitro показали, что гепарин может стимулировать неоангиогенез, а также улучшать плацентарную перфузию. Антикоагулянтные свойства гепарина проявляются в его способности мобилизовать фактор тканевого ингибирования в кровообращение, а также в том, что он также усиливает антитромбиновую активность. Дополнительные преимущества гепарина при рассмотрении плацентарной недостаточности и ее последующих последствий заключаются в том, что гепарин способствует пролиферации трофобластов, уменьшает воспаление за счет подавления каскада комплемента, уменьшает апоптоз, а также косвенно действует как фактор роста. [3]
Антикоагулянтные свойства гепарина проявляются в его способности мобилизовать фактор тканевого ингибирования в кровообращение, а также в том, что он также усиливает антитромбиновую активность. Дополнительные преимущества гепарина при рассмотрении плацентарной недостаточности и ее последующих последствий заключаются в том, что гепарин способствует пролиферации трофобластов, уменьшает воспаление за счет подавления каскада комплемента, уменьшает апоптоз, а также косвенно действует как фактор роста. [3]
Было также показано, что гепарин активирует определенные белки, участвующие в плацентарном ангиогенезе и развитии. К ним относятся ангиопоэтин-2, отвечающий за ремоделирование сосудов ворсин хориона, лептин, отвечающий за регуляцию переноса питательных веществ, а также рецептор фактора роста эндотелия сосудов-3, тканевой ингибитор матриксной металлопротеазы-1, фактор некроза опухоли-альфа. и ангиостатин. Основываясь на его свойствах и предварительных данных, некоторые исследования показали, что гепарин может играть роль в профилактическом лечении плацентарной болезни.
Дифференциальный диагноз
Существует много факторов, которые могут способствовать развитию плацентарной недостаточности, и известно, что ЗВУР является серьезным последующим осложнением; однако иногда может быть трудно отличить новорожденного с малым весом для гестационного возраста (SGA) от новорожденного с IUGR. Одно из основных преимуществ допплеровских исследований, особенно пупочной артерии, заключается в том, что допплерографию аномальных пупочных артерий можно использовать для дифференциации между патологической ЗВУР и малым для гестационного возраста новорожденным, таким образом определяя, при какой беременности требуется высокоуровневое наблюдение. по сравнению с рутинным мониторингом.[9][14]
Если средний расчетный вес плода ниже 10-го процентиля для определенного гестационного возраста, этот плод является SGA. И наоборот, плод с ЗВУР не сможет достичь нормального роста, как правило, вследствие плацентарной недостаточности, генетического заболевания или инфекции. [14] Следовательно, новорожденный с SGA будет физически маленьким, но в целом здоровым, по сравнению с новорожденным с IUGR, который также может быть физически маленьким, но, вероятно, его здоровье будет скомпрометировано.
[14] Следовательно, новорожденный с SGA будет физически маленьким, но в целом здоровым, по сравнению с новорожденным с IUGR, который также может быть физически маленьким, но, вероятно, его здоровье будет скомпрометировано.
При рассмотрении дифференциальных диагнозов, которые способствуют плацентарной недостаточности, известны сопутствующие заболевания, включая, помимо прочего, преэклампсию, гипертензивные расстройства у матери, поскольку оба они нарушают плацентарную резистентность и маточно-плацентарный кровоток. Другие заболевания, которые следует учитывать, включают маловодие и недоедание матери или ограничение калорий.
Прогноз
Если новорожденный страдает ЗВУР в результате плацентарной недостаточности и выживает в перинатальном периоде, он подвергается более высокому риску развития когнитивных нарушений в детстве, чем детский церебральный паралич и судорожные расстройства, по сравнению с новорожденным без задержки роста. Пациенты, страдающие плацентарной недостаточностью, часто имеют аномальные кривые скорости кровотока в пупочной артерии (DFVW), и когда в одном исследовании сравнивали DFVW младенцев, у которых была плацентарная недостаточность внутриутробно, с теми младенцами, у которых ее не было, они обнаружили, что младенцы, у которых была аномальная У DFVW также был более низкий IQ, когда им было 5 лет. Имеются также доказательства того, что ЗВУР в младенчестве предрасполагает к хроническим заболеваниям во взрослом возрасте, включая повышенный риск развития ишемической болезни сердца, гипертонии и диабета.[2]
Имеются также доказательства того, что ЗВУР в младенчестве предрасполагает к хроническим заболеваниям во взрослом возрасте, включая повышенный риск развития ишемической болезни сердца, гипертонии и диабета.[2]
Чтобы обеспечить лучший прогноз для новорожденного, приоритет должен быть сосредоточен на вмешательствах, которые позволяют максимально увеличить гестационный возраст при рождении. Подсчитано, что каждая неделя беременности плода между 24-й и 28-й неделями беременности увеличивает выживаемость без сопутствующих осложнений примерно на 10–15 % [3].
Осложнения
Последующие эффекты плацентарной недостаточности на развивающийся плод сложны и многофакторны; однако основными эффектами, как правило, являются плацентарная дыхательная недостаточность и гипоксемия плода, оба из которых способствуют ограничению внутриутробного развития и связанным с ним последствиям, включая недоношенность.
Самым опасным осложнением, очевидно, является полное отсутствие плацентации и, как следствие, выкидыш. Для развивающегося плода степень аномалий пупочной артерии, наблюдаемая при допплерографии, коррелирует с ацидозом, потребностью в реанимации, прессорной поддержке, вентиляционной поддержке, а также полисистемной недостаточностью органов, которая имеет тенденцию возникать при гипоксемии, поскольку это вызывает перераспределение кровотока. у развивающегося плода к основным органам, таким как мозг и сердце, за счет других соответствующих органов, таких как кишечник и почки. Кроме того, когда допплеровские исследования демонстрируют отсутствие или реверсию конечно-диастолического кровотока, у новорожденных повышается частота внутрижелудочковых кровоизлияний [9].]
Для развивающегося плода степень аномалий пупочной артерии, наблюдаемая при допплерографии, коррелирует с ацидозом, потребностью в реанимации, прессорной поддержке, вентиляционной поддержке, а также полисистемной недостаточностью органов, которая имеет тенденцию возникать при гипоксемии, поскольку это вызывает перераспределение кровотока. у развивающегося плода к основным органам, таким как мозг и сердце, за счет других соответствующих органов, таких как кишечник и почки. Кроме того, когда допплеровские исследования демонстрируют отсутствие или реверсию конечно-диастолического кровотока, у новорожденных повышается частота внутрижелудочковых кровоизлияний [9].]
При повышении резистентности плаценты во время беременности плод с уже ЗВУР подвергается дальнейшему риску гипогликемии, гипоксически-ишемической энцефалопатии, тромбоцитопении, лейкопении и анемии.[8] Кроме того, есть данные, свидетельствующие о том, что у младенцев существует риск развития когнитивного дефицита в детстве, а затем развития хронических заболеваний во взрослом возрасте.
Предупреждение и просвещение пациентов
Крайне важно, чтобы регулярный пренатальный скрининг и ультразвуковое исследование проводились во время беременности женщины, чтобы обеспечить наилучшие возможные результаты для новорожденного. Хотя окончательных профилактических мер для плацентарной недостаточности не существует, после того, как она была распознана с помощью УЗИ, МРТ, плацентарной недостаточности или любой комбинации этих методов, можно начинать такие вмешательства, как терапия гепарином, с надеждой на продление беременности с надеждой на минимизацию ацидоз и гипоксия и, как следствие, ЗВУР, недоношенность или гибель плода. Необходимо провести дальнейшие исследования вмешательств и методов лечения, и во время беременности они принесут наибольшую пользу развивающемуся плоду.
Pearls and Other Issues
Определенного лекарства от плацентарной недостаточности не существует, но последствия можно свести к минимуму, если диагностировать ее на ранней стадии, и мать получает надлежащий дородовой уход.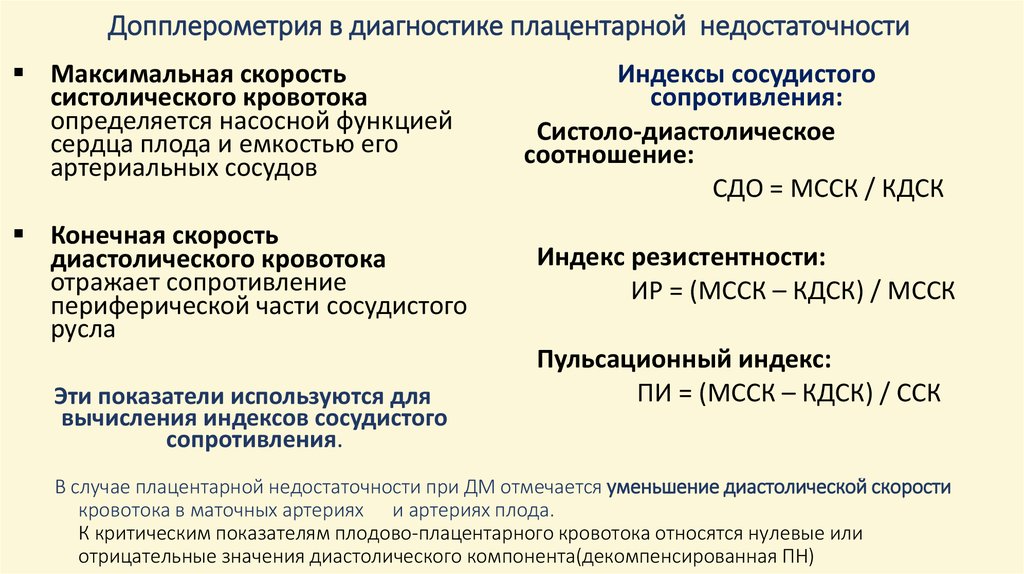 Недавний метаанализ показал, что гепарин может стимулировать рост плода и пролонгировать беременность, если гепарин назначается пациентам с высоким подозрением на плацентарную недостаточность, но не снижает неблагоприятных исходов у новорожденных.
Недавний метаанализ показал, что гепарин может стимулировать рост плода и пролонгировать беременность, если гепарин назначается пациентам с высоким подозрением на плацентарную недостаточность, но не снижает неблагоприятных исходов у новорожденных.
Улучшение результатов работы команды здравоохранения
Согласно допплеровским исследованиям, самые ранние признаки несостоятельности плаценты, вероятно, не будут обнаружены, по крайней мере, после 12 недель беременности, что коррелирует с проспективным когортным исследованием, которое показало, что скрининг плацентарной функции при беременностях с высоким риском во втором триместре по сравнению с первым триместром лучший предиктор неблагоприятных перинатальных исходов.[15]
При обсуждении плацентарной недостаточности будет задействовано как минимум две команды, если не больше, которые будут заниматься уходом за пациентками, так как одна команда будет нести ответственность за наблюдение за матерью и плодом до родов, а другая команда будет заботиться о для новорожденного после родов. Ведение как матери, так и ребенка с задержкой внутриутробного развития требует междисциплинарной команды, состоящей из акушеров-гинекологов, реаниматологов-реаниматологов, медсестер акушерства и отделения интенсивной терапии, респираторных терапевтов, фармацевтов, пульмонологов, а иногда и других специальностей, включая хирургию, инфекционные заболевания или генетику.
Ведение как матери, так и ребенка с задержкой внутриутробного развития требует междисциплинарной команды, состоящей из акушеров-гинекологов, реаниматологов-реаниматологов, медсестер акушерства и отделения интенсивной терапии, респираторных терапевтов, фармацевтов, пульмонологов, а иногда и других специальностей, включая хирургию, инфекционные заболевания или генетику.
У новорожденных с ЗВУР часто развиваются хронические заболевания легких, вторичные по отношению к их недоношенности, и может потребоваться несколько лекарств, а также домашняя оксигенация, или у них могут развиться множественные инфекции, включая некротизирующий энтероколит или поздний сепсис, все из которых требуют координации между вышеупомянутые команды, чтобы обеспечить улучшенные результаты для пациента. Иногда, в зависимости от исхода беременности, важно привлечь комитет по этике или группу паллиативной помощи. Часто семьям легче организовать семейные встречи, на которых присутствует хотя бы один член от каждой специализированной группы, поскольку это улучшает общение между всеми командами и дает семьям возможность задать свои вопросы сразу всем специалистам.
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
Ссылки
- 1.
Хант К., Кеннеди С.Х., Ватиш М. Определения и сообщения о плацентарной недостаточности в биомедицинских журналах: обзор литературы. Eur J Obstet Gynecol Reprod Biol. 2016 окт.; 205:146-9. [PubMed: 27591716]
- 2.
Ганьон Р. Плацентарная недостаточность и ее последствия. Eur J Obstet Gynecol Reprod Biol. 22 сентября 2003 г .; 110 Приложение 1: S99-107. [PubMed: 12965097]
- 3.
Mazarico E, Molinet-Coll C, Martinez-Portilla RJ, Figueras F. Терапия гепарином при плацентарной недостаточности: систематический обзор и метаанализ. Acta Obstet Gynecol Scand. 2020 фев; 99 (2): 167-174. [PubMed: 31519033]
- 4.
Агарвал Р., Тивари А., Вадхва Н., Радхакришнан Г. Гистопатологические данные плаценты при недоношенности/доношенности и раннем/позднем начале малы для гестационного возраста: являются ли они значительными? Индиан Дж.
 Патол Микробиол. 2017 г., апрель-июнь; 60(2):232-235. [В паблике: 28631641]
Патол Микробиол. 2017 г., апрель-июнь; 60(2):232-235. [В паблике: 28631641]- 5.
Ohgiya Y, Nobusawa H, Seino N, Miyagami O, Yagi N, Hiroto S, Munechika J, Hirose M, Takeyama N, Ohike N, Matsuoka R, Sekizawa A, Gokan T. MR Imaging of Плоды для оценки плацентарной недостаточности. Magn Reson Med Sci. 2016;15(2):212-9. [Статья бесплатно PMC: PMC5600058] [PubMed: 26607809]
- 6.
Пинтикан Д., Пойенар А.А., Стрильчук С., Миху Д. Влияние курения матери на васкуляризацию плаценты человека: систематический обзор. Тайвань J Obstet Gynecol. 2019Июль; 58 (4): 454-459. [PubMed: 31307732]
- 7.
Audette MC, Kingdom JC. Скрининг задержки роста плода и плацентарной недостаточности. Semin Fetal Neonatal Med. 2018 апр; 23 (2): 119-125. [PubMed: 29221766]
- 8.
Башат А.А., Харман Ч.Р., Гембрух У. Гематологические последствия плацентарной недостаточности. Arch Dis Child Fetal Neonatal Ed. 2004 Январь;89(1):F94.
 [Бесплатная статья PMC: PMC1721655] [PubMed: 14711871]
[Бесплатная статья PMC: PMC1721655] [PubMed: 14711871]- 9.
Harman CR, Baschat AA. Комплексная оценка состояния плода: какие допплеровские исследования следует провести? Curr Opin Obstet Gynecol. 2003 г., 15 апреля (2): 147–57. [PubMed: 12634607]
- 10.
Башат А.А. Реакция плода на плацентарную недостаточность: обновление. БЖОГ. 2004 г., октябрь; 111 (10): 1031-41. [PubMed: 15383103]
- 11.
Юсуф С., Ахмад А., Кадир С., Гул С., Тали С.Х., Шахин Ф., Ахтар С., Дар Р. Использование плацентарной латеральности и допплеровских аномалий маточных артерий для прогнозирования преэклампсии . J Obstet Gynaecol Индия. 2016 окт; 66 (Приложение 1): 212-6. [Бесплатная статья PMC: PMC5016443] [PubMed: 27651606]
- 12.
Сейам Ю.С., Аль-Махмейд М.С., Аль-Тамими Х.К. Допплерометрия кровотока в пупочной артерии при задержке внутриутробного развития и ее связь с перинатальным исходом. Int J Gynaecol Obstet.


 2001. № 2. С. 437.
2001. № 2. С. 437. Патол Микробиол. 2017 г., апрель-июнь; 60(2):232-235. [В паблике: 28631641]
Патол Микробиол. 2017 г., апрель-июнь; 60(2):232-235. [В паблике: 28631641] [Бесплатная статья PMC: PMC1721655] [PubMed: 14711871]
[Бесплатная статья PMC: PMC1721655] [PubMed: 14711871] 2002 г., май; 77 (2): 131–137. [PubMed: 12031563]
2002 г., май; 77 (2): 131–137. [PubMed: 12031563] Патол Микробиол. 2017 г., апрель-июнь; 60(2):232-235. [В паблике: 28631641]
Патол Микробиол. 2017 г., апрель-июнь; 60(2):232-235. [В паблике: 28631641] [Бесплатная статья PMC: PMC1721655] [PubMed: 14711871]
[Бесплатная статья PMC: PMC1721655] [PubMed: 14711871]