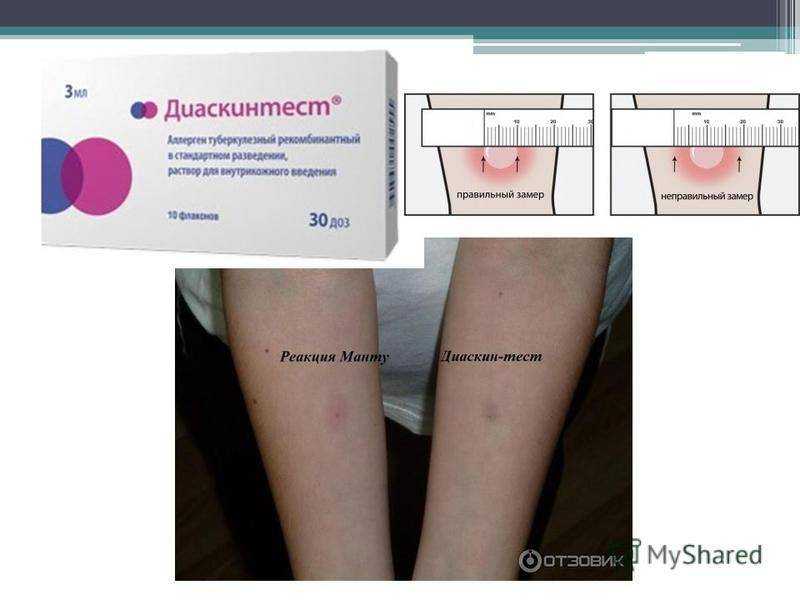
Детей Нур-Султана прививают от коронавируса под прикрытием Манту? Ответ санврача
https://ru.sputnik.kz/20210903/Deti-koronavirus-Mantu-18035303.html
Детей Нур-Султана прививают от коронавируса под прикрытием Манту? Ответ санврача
Детей Нур-Султана прививают от коронавируса под прикрытием Манту? Ответ санврача
Очередная фейковая информация, распространяемая через мессенджеры, взбудоражила некоторых родителей 03.09.2021, Sputnik Казахстан
2021-09-03T12:32+0600
2021-09-03T12:32+0600
2022-09-26T15:56+0600
/html/head/meta[@name=’og:title’]/@content
/html/head/meta[@name=’og:description’]/@content
https://sputnik.kz/img/258/60/2586050_0:249:2757:1799_1920x0_80_0_0_28ae7260c5abcc7e71d0eff0b1a920d1.jpg
новости астаны
Sputnik Казахстан
+74956456601
MIA „Rosiya Segodnya“
2021
Sputnik Казахстан
+74956456601
MIA „Rosiya Segodnya“
Новости
ru_KK
Sputnik Казахстан
media@sputniknews. com
com
+74956456601
MIA „Rosiya Segodnya“
1920
1080
true
1920
1440
true
https://sputnik.kz/img/258/60/2586050_12:0:2743:2048_1920x0_80_0_0_24089982bd780d40432e9ef1766bed70.jpg
1920
1920
true
Sputnik Казахстан
+74956456601
MIA „Rosiya Segodnya“
Sputnik Казахстан
здоровье, общество , вакцинация от коронавируса в казахстане 2021: новости и статистика, новости астаны
здоровье, общество , вакцинация от коронавируса в казахстане 2021: новости и статистика, новости астаны
НУР-СУЛТАН, 3 сен — Sputnik. Главный санитарный врач Нур-Султана Жанна Пралиева опровергла информацию о том, что сейчас детей вакцинируют от коронавируса под прикрытием пробы Манту (ребенку вводят туберкулин, который не является прививкой. Процедура позволяет выяснить, знаком ли организм с туберкулезной палочкой Коха).
В социальных сетях появилась информация о том, что в городе первоклассникам ставят пробу Манту, но некоторые родители пишут отказ в страхе, что их детей под прикрытием Манту вакцинируют против коронавируса.
Сколько вакцинированных астанчан получили положительный ПЦР-тест в августе
«Ежегодно в сентябре проводится ревакцинация первоклассников БЦЖ (вакцина против туберкулеза). На сегодня во всех школах проводится подготовка, составляются списки, и эта компания ежегодно проводится в полном объеме. По поводу того, что детям вколют вакцину против коронавируса, то сейчас детей не вакцинируют. Поэтому вопрос отпадает», – ответила во время брифинга столичный санврач.
Ранее исполняющий обязанности руководителя управления общественного здравоохранения Нур-Султана Алия Рустемова заявила, что столичные дети чаще всего заражаются коронавирусом в семьях, где есть непривитые взрослые.
Вакцина Pfizer получила временную регистрацию в Казахстане: кто получит прививку
По ее словам, рост заболеваемости среди детского населения отмечался летом. С июня дети стали поступать с ярко выраженными клиническими симптомами, такие как интоксикация, лихорадка, высокая температура, катаральные симптомы.
Сейчас с положительным результатом на стационарном лечении находятся 43 ребенка. В отделении реанимации детей нет. Сначала года свыше 10 тысяч детей переболели коронавирусом.
протокол систематического обзора и метаанализа
Туберкулиновые кожные пробы после вакцинации Bacille Calmette Guerin в Африке: протокол для систематического обзора и метаанализа
Chinonyelum Thecla Ezeonu 1 , Richard Chinaza Ikeagwulonu 2 , Uzoma Vivian Asiegbu 1 , Dorathy Chinwe Obu 1 , Datonye Christopher Briggs 3,&
6
1 Кафедра педиатрии, Учебная больница Федерального университета им. Алекса Эквуэме, Абакалики, штат Эбони, Нигерия, 2 Кафедра медицинских лабораторных исследований, Учебная больница Федерального университета им. Алекса Эквуэме, Абакалики, штат Эбони, Нигерия, 3 Кафедра педиатрии, Учебная больница государственного университета Риверс, Порт-Харкорт, штат Риверс, Нигерия
и Автор, ответственный за переписку
Датонье Кристофер Бриггс, кафедра педиатрии, клиническая больница государственного университета Риверс, Порт-Харкорт, штат Риверс, Нигерия
Аннотация
Туберкулиновая реактивность после туберкулиновой кожной пробы, которая является наиболее распространенным показателем эффекта вакцинации бациллой Кальметта-Герена (БЦЖ), оставалась сложной. Этот протокол предназначен для оценки влияния вакцины БЦЖ на кожный туберкулиновый тест в Африке в качестве руководства для лучшего понимания или решения этой сложности. Стратегия поиска разрабатывается с использованием MeSH, ключевых слов, текстовых слов и условий ввода. Поиск будет проводиться в пяти базах данных, включая PubMed, African Journals Online (AJOL), Google Scholar, Research Gate и Cochrane Library. Будут включены только обсервационные исследования, проведенные в странах Африки к югу от Сахары и доступные на английском языке. Первичным измеримым результатом этого исследования является совокупная распространенность положительных туберкулиновых кожных проб. Вторичными результатами являются факторы, влияющие на положительный результат туберкулиновой кожной пробы (ТКП), такие как тип БЦЖ, доза БЦЖ, возраст вакцинации БЦЖ, время/интервал между вакцинацией БЦЖ и ТКП и тип туберкулиновой единицы, используемой для ТКП. Выявленные исследования будут проверены и отобраны на основе критериев включения.
Этот протокол предназначен для оценки влияния вакцины БЦЖ на кожный туберкулиновый тест в Африке в качестве руководства для лучшего понимания или решения этой сложности. Стратегия поиска разрабатывается с использованием MeSH, ключевых слов, текстовых слов и условий ввода. Поиск будет проводиться в пяти базах данных, включая PubMed, African Journals Online (AJOL), Google Scholar, Research Gate и Cochrane Library. Будут включены только обсервационные исследования, проведенные в странах Африки к югу от Сахары и доступные на английском языке. Первичным измеримым результатом этого исследования является совокупная распространенность положительных туберкулиновых кожных проб. Вторичными результатами являются факторы, влияющие на положительный результат туберкулиновой кожной пробы (ТКП), такие как тип БЦЖ, доза БЦЖ, возраст вакцинации БЦЖ, время/интервал между вакцинацией БЦЖ и ТКП и тип туберкулиновой единицы, используемой для ТКП. Выявленные исследования будут проверены и отобраны на основе критериев включения.
Введение
Туберкулез является хроническим заболеванием, представляющим проблему для общественного здравоохранения, особенно в странах с ограниченными ресурсами [1]. В 2017 г. в мире было зарегистрировано около 10 млн новых случаев туберкулеза с 1,6 млн летальных исходов [2]. Однако одним из самых надежных способов предотвращения туберкулеза во всем мире была вакцинация, и вакцина Bacille Calmette Guerin (BCG) широко использовалась на всех континентах. Вакцину БЦЖ обычно вводят для защиты людей, особенно детей, от тяжелых форм туберкулеза [3]. В Африке и в большинстве стран, эндемичных по туберкулезу, вакцину обычно вводят сразу после рождения, чтобы предотвратить тяжелое течение туберкулеза у младенцев. Важно отметить, что бессимптомная латентная туберкулезная инфекция может быть обнаружена с помощью туберкулиновой кожной пробы (ТКП), процедуры, в которой используется очищенное белковое производное (PPD) убитых нагреванием живых культур микобактерий, вводимых внутрикожно в предплечье, чтобы продемонстрировать отсроченную реакцию гиперчувствительности на ППД, которое полностью происходит в течение 48-72 часов [4].
Вакцину БЦЖ обычно вводят для защиты людей, особенно детей, от тяжелых форм туберкулеза [3]. В Африке и в большинстве стран, эндемичных по туберкулезу, вакцину обычно вводят сразу после рождения, чтобы предотвратить тяжелое течение туберкулеза у младенцев. Важно отметить, что бессимптомная латентная туберкулезная инфекция может быть обнаружена с помощью туберкулиновой кожной пробы (ТКП), процедуры, в которой используется очищенное белковое производное (PPD) убитых нагреванием живых культур микобактерий, вводимых внутрикожно в предплечье, чтобы продемонстрировать отсроченную реакцию гиперчувствительности на ППД, которое полностью происходит в течение 48-72 часов [4].
Туберкулиновая реактивность, которая может быть как положительной, так и отрицательной после туберкулиновой кожной пробы, была наиболее распространенной мерой эффекта вакцинации БЦЖ. Положительный туберкулиновый кожный тест был зарегистрирован у лиц, ранее вакцинированных БЦЖ, и в таких обстоятельствах, как недавний контакт с другим человеком, больным ТБ, или постоянное воздействие групп населения с высокой распространенностью ТБ [5,6].
В некоторых исследованиях повышенная туберкулиновая реактивность наблюдалась у лиц, получивших высокие дозы вакцины [24], у лиц, вакцинация или ревакцинация которых была проведена в более позднем возрасте [25-27], а также в случаях бустерного феномена [28].
Цели исследования: 1) для определения общей распространенности положительных кожных туберкулиновых проб в Африке. 2) Определить распространенность положительных кожных туберкулиновых проб в таких подгруппах, как дети, взрослые, ранее вакцинированные БЦЖ и невакцинированные лица в Африке.
3) Для определения факторов, влияющих на положительный результат ТКП, таких как тип БЦЖ, доза БЦЖ, возраст прививки БЦЖ, время/интервал между вакцинацией БЦЖ и ТКП, тип туберкулиновой единицы, используемой для ТКП, сила туберкулиновой единицы, используемой для ТКП. , наличие и отсутствие рубца БЦЖ.
2) Определить распространенность положительных кожных туберкулиновых проб в таких подгруппах, как дети, взрослые, ранее вакцинированные БЦЖ и невакцинированные лица в Африке.
3) Для определения факторов, влияющих на положительный результат ТКП, таких как тип БЦЖ, доза БЦЖ, возраст прививки БЦЖ, время/интервал между вакцинацией БЦЖ и ТКП, тип туберкулиновой единицы, используемой для ТКП, сила туберкулиновой единицы, используемой для ТКП. , наличие и отсутствие рубца БЦЖ.
Контрольные вопросы: 1) какова общая распространенность положительных кожных туберкулиновых проб в Африке? 2) Какова распространенность положительных кожных туберкулиновых проб в таких подгруппах, как дети, взрослые, ранее вакцинированные БЦЖ и невакцинированные лица? 3) Какие факторы влияют на положительный результат ТКП?
Методы
Дизайн исследования: это протокол для систематического обзора и метаанализа обсервационных исследований, в которых сообщается о влиянии вакцины Bacille Calmette Guerin на туберкулиновые кожные пробы в Африке.
Критерии включения: а) обсервационные исследования (когортные, перекрестные, случай-контроль, исторические когорты). б) Исследования всех лет, опубликованные или доступные для поиска на английском языке. в) Исследования, имеющиеся в электронных базах данных. d) Исследования, в которых сообщается о доле положительных случаев туберкулиновой кожной пробы (это первичный критерий исхода) и/или вторичном исходе, которые являются факторами, влияющими на положительный результат ТКП.
Критерии исключения: а) исследования без доли положительных случаев туберкулиновой кожной пробы.
б) Исследования, включающие известные контакты больных активным ТБ.
в) Исследования, в которых участвовали люди с инфекцией или заболеванием ТБ.
г) Описательные обзоры, интервенционные и экспериментальные исследования и письма в редакцию. e) Исследования, о которых не сообщается или которые не могут быть получены на английском языке.
e) Исследования, о которых не сообщается или которые не могут быть получены на английском языке.
Характеристики исследования: PICOS выглядит следующим образом: участниками являются лица, которые прошли кожную туберкулиновую пробу с вакцинацией БЦЖ или без нее в Африке. Вмешательство: нет вмешательства. Компаратор: компаратора нет. Исход: первичным результатом является доля положительных кожных туберкулиновых проб. Поддающиеся измерению вторичные исходы — это факторы, влияющие на положительный результат ТКП. Фильтры, используемые для подгрупп, включают детей, взрослых и лиц, ранее вакцинированных БЦЖ.
Источники информации: при поиске будут использоваться стратегии, основанные на конфиденциальных темах, разработанные для каждой базы данных. Пять баз данных для поиска: PubMed, African Journal Online (AJOL), Google Scholar, Research Gate и Cochrane Library. В ходе исследования будут получены только обсервационные исследования, написанные на английском языке. Нет никаких временных рамок или ограничений на включение публикаций.
Нет никаких временных рамок или ограничений на включение публикаций.
Стратегия поиска: стратегия поиска будет включать термины MeSH, текстовые слова, входные слова и ключевые слова. Используемые стратегии поиска показаны в Таблице 1 .
Извлечение данных: данные будут извлекаться и управляться с использованием следующих инструментов: i). программное обеспечение Zotero, ii) Microsoft Excel и iii) программное обеспечение для комплексного метаанализа (CMA) версии 3.
Скрининг: исследования будут найдены с использованием стратегии поиска. Будет задействовано шесть уровней проверки данных.
Уровень 1: скрининг для выбора только обсервационных исследований, в то время как другие дизайны исследований исключаются.
Уровень 2: просмотр всех выбранных обсервационных исследований по их названиям и рефератам с использованием терминов MeSH, ключевых слов и входных терминов.
Уровень 3: просмотр выбранных исследований путем полнотекстового чтения с использованием той же стратегии. Уровень 4: снежный ком литературы с использованием включенных исследований.
Уровень 5: скрининг первичных и вторичных результатов.
Уровень 6: скрининг риска систематической ошибки с использованием оценки качества NIH для обсервационных исследований и Кокрановского риска систематической ошибки для усиления доказательств.
Уровень 4: снежный ком литературы с использованием включенных исследований.
Уровень 5: скрининг первичных и вторичных результатов.
Уровень 6: скрининг риска систематической ошибки с использованием оценки качества NIH для обсервационных исследований и Кокрановского риска систематической ошибки для усиления доказательств.
Процесс отбора и проверка: пять рецензентов участвуют в этом исследовании. Пара рецензентов будет независимо проверять исследования из каждой базы данных, оценивая исследования на предмет включения или исключения. Конфликты будут разрешаться третьим независимым рецензентом. Все отзывы слепые.
Скрининг и дедупликация будут выполняться в программном обеспечении Zotero. Отобранные исследования будут экспортированы в Microsoft Excel для подготовки к анализу данных. Исследования будут отобраны на основе критериев приемлемости и основного измеримого результата. С авторами исследований, в которых отсутствуют данные, свяжутся по электронной почте и телефону.
Сбор данных: следующие элементы данных будут извлечены из каждого подходящего исследования в Microsoft Excel:
i) Фамилия первого автора, год публикации исследования, год исследования, страна исследования, дизайн исследования
ii) Размер выборки
iii) Тип и доза БЦЖ, возраст на момент вакцинации БЦЖ, интервал между вакцинацией БЦЖ и кожным туберкулиновым тестом, количество субъектов, получивших вакцину БЦЖ, наличие или отсутствие рубца БЦЖ, количество положительных или отрицательных результатов ТКП, тип и сила туберкулиновая проба/используемый антиген, частота ответов/размер волдырей на туберкулиновую пробу определенного диаметра и показания для ТКП. Другими являются изучаемая возрастная группа, возраст, когда проводилась ТКП, возраст, когда вводилась БЦЖ, пол, социально-экономический статус, способы определения прививки БЦЖ, техника нанесения и чтения теста, иммунологический статус испытуемых, наличие заболеваний у испытуемых. изучаемой популяции, такой как рак, сахарный диабет, СПИД. Состояние питания и уровень охвата БЦЖ.
Данные из Microsoft Excel будут экспортированы в программное обеспечение CMA для метаанализа.
Состояние питания и уровень охвата БЦЖ.
Данные из Microsoft Excel будут экспортированы в программное обеспечение CMA для метаанализа.
Риск смещения: риск систематической ошибки во включенных исследованиях будет доступен для отдельных исследований с использованием инструмента оценки качества Национального института здравоохранения (NIH) для обсервационных когортных и перекрестных исследований. Это будет перепроверено с помощью Кокрановского инструмента оценки риска систематической ошибки на предмет убедительности совокупности доказательств.
Исследования с крайней предвзятостью будут исключены после оценки в следующих областях:
1. Метод тестирования и отчетности на уровне результатов.
2. Отчет об исследовании; распространенность с доверительным интервалом или числом положительных случаев/размером выборки, как сообщается на уровне исхода.
3. Неоднородность будет оцениваться на уровне исследования.
4. Систематическая ошибка публикации будет оцениваться на уровне исследования.
Оценка мета-предвзятости: для проверки неоднородности будет использоваться Кокрановское значение Q, I 2 , T 2 . I 2 значения менее 40 % будут считаться низкой неоднородностью, значения от > 40 до ≤ 75 % — умеренными, а значения > 75 % — высокими. В качестве величины эффекта следует использовать распространенность с доверительным интервалом (ДИ, 95%).
Синтез данных: будет проводиться как описательный, так и количественный анализ.
Все исследования, в которых сообщается о первичном исходе с вторичными исходами или без них, будут включены в систематический обзор, при этом все измеримые исходы и размер выборки будут представлены в табличном формате. Исследования с первичными индексами, которые можно преобразовать в распространенность, будут преобразованы в версии 3 программного обеспечения CMA.
Количественные данные будут включать объединенную распространенность, стандартную ошибку и 95% ДИ. Будут оцениваться как случайные модели, так и модели с фиксированными эффектами, и соответствующая модель будет выбрана на основе лесных участков. Анализ подгрупп будет проводиться с использованием категориальных факторов, таких как возраст и статус вакцинации БЦЖ. Мета-регрессия будет выполнена для проверки тенденции распространенности положительных туберкулиновых кожных проб с годами.
Анализ подгрупп будет проводиться с использованием категориальных факторов, таких как возраст и статус вакцинации БЦЖ. Мета-регрессия будет выполнена для проверки тенденции распространенности положительных туберкулиновых кожных проб с годами.
Результаты
Процесс выбора исследования будет представлен в виде блок-схемы в соответствии с Заявлением PRISMA 2015 и контрольным списком PRISMA-P. Будет включена таблица стратегии поиска в различных базах данных, показывающая текстовые слова, MeSH и условия ввода. Список включенных исследований будет сведен в таблицу. Количественные данные, такие как размер эффекта (распространенность), 95% ДИ, значения P и относительные веса, присвоенные исследованиям и тестам на неоднородность, будут включены в лесные участки. Будет включена таблица показателей качества и риска систематической ошибки для каждого подходящего исследования. Будут включены лесные участки для демонстрации анализа подгрупп. Также будет включен кумулятивный метаанализ для проверки тенденций.
Также будет включен кумулятивный метаанализ для проверки тенденций.
Обсуждение
В этом метаанализе будут рассмотрены важные клинические и эпидемиологические вопросы, связанные с интерпретацией ТКП у пациентов с предыдущей вакцинацией БЦЖ, что поможет медицинским работникам обучать пациентов предлагать лечение латентной туберкулезной инфекции в условиях предыдущей вакцинации БЦЖ, положительного кожного теста и нет известных контактов с ТБ. Большие или сильно положительные кожные пробы, скорее всего, связаны с туберкулезной инфекцией, а не с БЦЖ.
Этика и распространение: этическое одобрение не требуется, так как это исследование будет основано на опубликованных данных. Окончательный отчет об этом исследовании будет опубликован в рецензируемом научном журнале.
Конкурирующие интересы
Авторы заявляют об отсутствии конкурирующих интересов.
Вклад авторов
CT задумал проект, CT, RC, UV, DC и DB разработали исследование, RC и UV выполнили поиск, скрининг и обзор в PubMed; UV и DC провели поиск, проверку и обзор AJOL; CT и DC провели поиск ученых в Google, их проверку и обзор; в то время как при поиске в Кокрановской базе данных и поисковых воротах скрининг и обзор выполнялись CT, RC, DC и DB соответственно. Все авторы прочитали и одобрили рукопись к публикации.
Таблица
Таблица 1 : стратегия поиска
Ссылки
- Адебизи Ю.А., Агумаге И., Сильванус Т.Д., Навайла И.Дж., Эквере В.А., Насиру М. и др. . Бремя туберкулеза и проблемы, стоящие перед его искоренением в Западной Африке. Int J Infect. 2019;6(3). Google Scholar
- Всемирная организация здравоохранения. Глобальный отчет по туберкулезу, 2018 г.
 ReliefWeb. По состоянию на 26 июня 2021 г.
ReliefWeb. По состоянию на 26 июня 2021 г. - Андерсен П., Доэрти ТМ. Успех и неудача БЦЖ — последствия для новой противотуберкулезной вакцины. Nat Rev Microbiol. 2005;3(8):656-662. ПабМед | Google Scholar
- Хюбнер Р.Е., Шейн М.Ф., Басс Дж.Б. Кожная туберкулиновая проба. Клин Инфекция Дис. 1993;17(6):968-975. ПабМед | Google Scholar
- Центры по контролю и профилактике заболеваний. Роль вакцины БЦЖ в профилактике и борьбе с туберкулезом в США: совместное заявление консультативного совета по ликвидации туберкулеза и консультативного комитета по практике иммунизации. Атланта, Джорджия. 1996.
- Буджани М., Борраччино А., Мильоре Э., Кароссо А., Пиччони П., Кавальеро М. и др. . Туберкулиновая реактивность у взрослых, вакцинированных БЦЖ: перекрестное исследование. Int J Tuberc Lung Dis. 2003;7(4):320-326. ПабМед | Google Scholar
- Horsburgh CR. Приоритеты лечения латентной туберкулезной инфекции в США.
 N Engl J Med. 2004;350(20):2060-2067. ПабМед | Академия Google
N Engl J Med. 2004;350(20):2060-2067. ПабМед | Академия Google - Miret-Cuadras P, Pina-Gutierrez JM, Juncosa S. Туберкулиновая реактивность у вакцинированных субъектов с бациллой Кальметта-Герена. Туберкулез и болезни легких. 1996;77(1):52-58. ПабМед | Google Scholar
- Куперс Т.А., Петрич Дж.М., Холлоуэй А.В., Гем Дж.В.С. Депрессия туберкулина замедленной гиперчувствительности живым аттенуированным вирусом эпидемического паротита. Журнал педиатрии. 1970;76(5):716-721. ПабМед | Академия Google
- Маес М., Верхаген Л.М., Ортега Д., Санчес Г.Л., Сеговия И., Дель Ногал Б. и др. . Влияние бациллы Кальметта-Герена на туберкулиновые кожные пробы у венесуэльских индейцев в районах с высоким бременем туберкулеза. J Infect Dev Cries. 2014;8(2):176-183. ПабМед | Google Scholar
- Verhagen LM, Hermans PWM, Warris A, de Groot R, Maes M, Villalba JA и др. .
 Гельминты и искаженные профили цитокинов повышают положительную реакцию на туберкулиновые кожные пробы у американских индейцев варао. Туберкулез. 2012;92(6):505-512. ПабМед | Google Scholar
Гельминты и искаженные профили цитокинов повышают положительную реакцию на туберкулиновые кожные пробы у американских индейцев варао. Туберкулез. 2012;92(6):505-512. ПабМед | Google Scholar - Магомед Х., Хокридж Т., Вервер С., Гейтер Л., Хазерилл М., Абрахамс Д.А. и др. . Прогностические факторы латентной туберкулезной инфекции среди подростков в районах с высоким бременем болезни в Южной Африке. Int J Tuberc Lung Dis. 2011;15(3):331-336. ПабМед | Google Scholar
- Линхардт С., Филдинг К., Силла Дж., Тункара А., Донкор С., Манне К. и др. . Факторы риска заражения туберкулезом в странах Африки к югу от Сахары: исследование контактов в Гамбии. Am J Respir Crit Care Med. 2003;168(4):448-455. ПабМед | Google Scholar
- Дханаваде С., Кумбхар С., Гор А., Патил В. Образование рубцов и конверсия туберкулина после вакцинации БЦЖ у младенцев: проспективное когортное исследование. J Family Med Prim Care.
 июль-сентябрь 2015 г.; 4(3):384-7. ПабМед | Google Scholar
июль-сентябрь 2015 г.; 4(3):384-7. ПабМед | Google Scholar - Всемирная организация здравоохранения. Иммунологическая основа для серии иммунизации: модуль 5: туберкулез, обновление 2011 г. По состоянию на 26 июня 2021 г.
- Резаи М.С., Абеди С., Афшари М., Мусазаде М. Оценка реакции кожных туберкулиновых проб у детей и подростков, получивших бациллу Кальметта -Вакцинация Герена при рождении: метаанализ. Osong Public Health Res Perspect. 2017;8(1):3-10. ПабМед | Google Scholar
- Almeida LMD, Barbieri MA, Da Paixão AC, Cuevas LE. Использование очищенного белкового производного для оценки риска заражения детей, находящихся в тесном контакте со взрослыми, больными туберкулезом, в популяции с высоким уровнем охвата бациллами Кальметта-Герена. Pediatr Infect Dis J. 2001;20(11):1061-1065. ПабМед | Google Scholar
- Menzies R, Vissandjee B, Amyot D. Факторы, связанные с реактивностью туберкулина среди родившихся за границей в Монреале.
 Ам преподобный Респир Дис. 1992;146(3):752-756. ПабМед | Google Scholar
Ам преподобный Респир Дис. 1992;146(3):752-756. ПабМед | Google Scholar - Farhat M, Greenaway C, Pai M, Menzies D. Ложноположительные туберкулиновые кожные пробы: каков абсолютный эффект БЦЖ и нетуберкулезных микобактерий? Int J Tuberc Lung Dis. 2006;10(11):1192-1204. ПабМед | Google Scholar
- Wang L. Метаанализ влияния вакцинации Bacille Calmette Guerin на измерения туберкулиновых кожных проб. грудная клетка. 2002;57(9):804-809. ПабМед | Google Scholar
- Густафсон П., Лиссе И., Гомес В., Виейра С.С., Линхардт С., Науклер А. и др. . Факторы риска положительной туберкулиновой кожной пробы в Гвинее-Бисау. Эпидемиология. 2007;18(3):340-347. ПабМед | Google Scholar
- Тернбулл Л., Белл С., Чайлд Ф. Туберкулез (Клиническое руководство NICE 33). Arch Dis Child Educ Pract Ed. 2017;102(3):136-142. ПабМед | Академия Google
- Целевая группа профилактических служб США, Биббинс-Доминго К.
 , Гроссман, округ Колумбия, Карри С.Дж., Бауман Л., Дэвидсон К.В. и др. . Скрининг на латентную туберкулезную инфекцию у взрослых: заявление рабочей группы профилактических служб США. ДЖАМА. 2016;316(9):962-9. ПабМед | Google Scholar
, Гроссман, округ Колумбия, Карри С.Дж., Бауман Л., Дэвидсон К.В. и др. . Скрининг на латентную туберкулезную инфекцию у взрослых: заявление рабочей группы профилактических служб США. ДЖАМА. 2016;316(9):962-9. ПабМед | Google Scholar - Ashley MJ, Siebenmann CO. Туберкулиновая чувствительность кожи после вакцинации БЦЖ вакцинами с высоким и низким числом жизнеспособных клеток. Can Med Assoc J. 1967;97(22):1335-1339. ПабМед | Google Scholar
- Мензис Р. Туберкулиновые кожные пробы. в: Reichman Lb, Hershfield Es, Editors. Туберкулез: комплексный международный подход. 2 и Изд. Нью-Йорк. Марсель Деккер. 2000.
- Караллиедде С., Катугаха Л.П., Урагода К.Г. Туберкулиновая реакция детей из Шри-Ланки после вакцинации БЦЖ при рождении. бугорок. 1987;68(1):33-38. ПабМед | Академия Google
- Sepulveda RL, Burr C, Ferrer X, Sorensen RU. Бустерный эффект туберкулинового тестирования у здоровых 6-летних школьников, привитых бациллой Кальметта-Герена при рождении, в Сантьяго, Чили.
 Pediatr Infect Dis J. 1988;7(8):578-581. ПабМед | Google Scholar
Pediatr Infect Dis J. 1988;7(8):578-581. ПабМед | Google Scholar - Sepulveda RL, Ferrer X, Latrach C, Sorensen RU. Влияние иммунизации бациллой Кальметта-Герена на бустерный эффект туберкулинового тестирования у здоровых молодых людей. Ам преподобный Респир Дис. 1990;142(1):24-28. ПабМед | Google Scholar
- Landi S, Ashley MJ, Grzybowski S. Чувствительность к туберкулину после внутрикожных и множественных пункционных методов вакцинации БЦЖ. Can Med Assoc J. 1967; 97(5):222-225. ПабМед | Google Scholar
Стероиды снижают распространенность положительной туберкулиновой кожной пробы при ревматоидном артрите: влияние на терапию анти-ФНО
На этой странице0003
Туберкулиновая кожная проба использовалась в качестве индикатора латентного туберкулеза у пациентов с ревматоидным артритом (РА) до введения биологических препаратов. Влияние противоревматических препаратов, модифицирующих заболевание (БПВП), и стероидов на результаты туберкулиновой кожной пробы (ТКП) может иметь важное значение при интерпретации результатов этой пробы. Цели . Выявить распространенность положительной ТКП у больных ревматоидным артритом и влияние стандартного лечения на результаты ТКП. Метод . В это перекрестное исследование были включены двести пятьдесят пациентов с РА старше 18 лет, классифицированных с использованием критериев ACR 1987 года для РА, из ревматологического отделения на открытом воздухе. Были зарегистрированы демографические данные, активность заболевания, продолжительность заболевания и терапия. Всем пациентам была проведена ТСТ. Результаты . У 51 (20,4%) больного выявлен туберкулинположительный статус. Прием метотрексата не влиял на положительный результат на туберкулин, но он был значительно ниже у пациентов, недавно принимавших стероиды, по сравнению с пациентами, которые не принимали стероиды в течение последних 3 месяцев (3% против 25%, 9).
Влияние противоревматических препаратов, модифицирующих заболевание (БПВП), и стероидов на результаты туберкулиновой кожной пробы (ТКП) может иметь важное значение при интерпретации результатов этой пробы. Цели . Выявить распространенность положительной ТКП у больных ревматоидным артритом и влияние стандартного лечения на результаты ТКП. Метод . В это перекрестное исследование были включены двести пятьдесят пациентов с РА старше 18 лет, классифицированных с использованием критериев ACR 1987 года для РА, из ревматологического отделения на открытом воздухе. Были зарегистрированы демографические данные, активность заболевания, продолжительность заболевания и терапия. Всем пациентам была проведена ТСТ. Результаты . У 51 (20,4%) больного выявлен туберкулинположительный статус. Прием метотрексата не влиял на положительный результат на туберкулин, но он был значительно ниже у пациентов, недавно принимавших стероиды, по сравнению с пациентами, которые не принимали стероиды в течение последних 3 месяцев (3% против 25%, 9). 0225 P = 0,002). Заключение . Установлено, что распространенность туберкулинпозитивности у больных РА низкая. На результаты не повлиял метотрексат; однако результаты кожных туберкулиновых проб у пациентов, недавно принимавших стероиды, скорее всего, будут отрицательными.
0225 P = 0,002). Заключение . Установлено, что распространенность туберкулинпозитивности у больных РА низкая. На результаты не повлиял метотрексат; однако результаты кожных туберкулиновых проб у пациентов, недавно принимавших стероиды, скорее всего, будут отрицательными.
1. Введение
Связь между ревматоидным артритом (РА) и туберкулезом (ТБ) возникла более девяти десятилетий назад, когда несколько клиницистов в Германии и Форрестье во Франции связали хроническое воспаление туберкулеза с воспалением ревматоидного артрита и таким образом использовали соли золота для лечения РА в 1920s [1, 2] на том основании, что ауротиосульфат натрия эффективен при лечении туберкулеза легких [3]. Бахр и др. даже подчеркивалась роль перекрестно-реактивных микобактериальных антигенов в этиопатогенезе РА [4].
Со временем, когда дальнейшие исследования отрицали этиологическую роль микобактерий в РА, отношения между ними изменились, так что возникновение двух заболеваний вместе не считалось зависимым друг от друга. С появлением стероидов и DMARD для лечения РА исследователи начали обсуждать повышенную заболеваемость туберкулезом при РА из-за иммуносупрессии. В крупном обсервационном когортном исследовании из Японии сообщалось о 3,2-кратном повышении риска туберкулеза у пациентов с РА, получавших стандартную терапию [5]. Подобные результаты были получены в Испании и Швеции еще до эры анти-ФНО, тогда как исследования в США не выявили различий в заболеваемости туберкулезом между населением в целом и больными РА, получающими стандартную терапию [6-8]. Далее, с введением биологических препаратов для лечения РА, проблема связи между ними снова набирает обороты. Различные исследования предполагают увеличение риска реактивации латентного ТБ в 5–10 раз при использовании антител к TNF [9].–12].
С появлением стероидов и DMARD для лечения РА исследователи начали обсуждать повышенную заболеваемость туберкулезом при РА из-за иммуносупрессии. В крупном обсервационном когортном исследовании из Японии сообщалось о 3,2-кратном повышении риска туберкулеза у пациентов с РА, получавших стандартную терапию [5]. Подобные результаты были получены в Испании и Швеции еще до эры анти-ФНО, тогда как исследования в США не выявили различий в заболеваемости туберкулезом между населением в целом и больными РА, получающими стандартную терапию [6-8]. Далее, с введением биологических препаратов для лечения РА, проблема связи между ними снова набирает обороты. Различные исследования предполагают увеличение риска реактивации латентного ТБ в 5–10 раз при использовании антител к TNF [9].–12].
Туберкулиновая кожная проба (ТКП) использовалась в качестве индикатора латентного туберкулеза (ЛТБИ) у пациентов с РА до введения биологических препаратов. Хотя существуют исследования влияния терапии РА на заболеваемость туберкулезом, влияние БПВП, используемых в качестве стандартной терапии у больных РА, на результат туберкулиновой пробы неизвестно. Этот эффект может иметь важное значение для интерпретации результатов туберкулиновой пробы до биологической терапии. Таким образом, это исследование было предпринято с целью определения распространенности положительной ТКП и влияния стандартного лечения (БПВП и стероиды) на результаты ТКП у пациентов с ревматоидным артритом.
Этот эффект может иметь важное значение для интерпретации результатов туберкулиновой пробы до биологической терапии. Таким образом, это исследование было предпринято с целью определения распространенности положительной ТКП и влияния стандартного лечения (БПВП и стероиды) на результаты ТКП у пациентов с ревматоидным артритом.
2. Материал и метод
Пациенты для этого обсервационного, перекрестного и проспективного исследования были набраны из амбулаторного отделения отделения ревматологии Медицинского университета короля Джорджа, Уттар-Прадеш, Лакхнау, Индия. О распространенности туберкулеза в Индии сообщалось Центральным отделом по борьбе с туберкулезом Индии в годовом отчете за 2013 г. о 256 случаях на сто тысяч населения [13]. В различных исследованиях сообщалось, что распространенность латентного туберкулеза в Индии составляет около 38% [14, 15]. Что касается проникновения БЦЖ, то всеобщая вакцинация БЦЖ началась в Индии в конце 50-х годов, и в настоящее время все дети привиты БЦЖ. Исследование было одобрено Институциональным комитетом по этике Медицинского университета KG, Лакхнау. Информированное согласие было получено от всех пациентов перед любой процедурой, связанной с исследованием. Размер выборки рассчитывали, предполагая снижение распространенности туберкулиновой чувствительности у больных РА (25%) по сравнению с общей популяцией (38%) [14, 15]. Пациенты с ревматоидным артритом (РА) как мужского, так и женского пола старше 18 лет, классифицированные по 1987 критериев ACR для РА [16] были зарегистрированы в течение 20 месяцев (с августа 2011 г. по март 2013 г.). Все последовательные пациенты с РА, еще не включенные в наше исследование, посещающие ревматологическую клинику в каждый клинический день нашего отделения, дающие согласие и выполняющие критерии включения и исключения, были включены независимо от приема терапии. Исключались пациенты с любым другим заболеванием соединительной ткани или артритами, кроме РА, любым иммунодепрессивным состоянием и гематологическими злокачественными новообразованиями, пациенты, принимающие биологические препараты, беременные женщины и пациенты с активным туберкулезом или туберкулезом в анамнезе.
Исследование было одобрено Институциональным комитетом по этике Медицинского университета KG, Лакхнау. Информированное согласие было получено от всех пациентов перед любой процедурой, связанной с исследованием. Размер выборки рассчитывали, предполагая снижение распространенности туберкулиновой чувствительности у больных РА (25%) по сравнению с общей популяцией (38%) [14, 15]. Пациенты с ревматоидным артритом (РА) как мужского, так и женского пола старше 18 лет, классифицированные по 1987 критериев ACR для РА [16] были зарегистрированы в течение 20 месяцев (с августа 2011 г. по март 2013 г.). Все последовательные пациенты с РА, еще не включенные в наше исследование, посещающие ревматологическую клинику в каждый клинический день нашего отделения, дающие согласие и выполняющие критерии включения и исключения, были включены независимо от приема терапии. Исключались пациенты с любым другим заболеванием соединительной ткани или артритами, кроме РА, любым иммунодепрессивным состоянием и гематологическими злокачественными новообразованиями, пациенты, принимающие биологические препараты, беременные женщины и пациенты с активным туберкулезом или туберкулезом в анамнезе.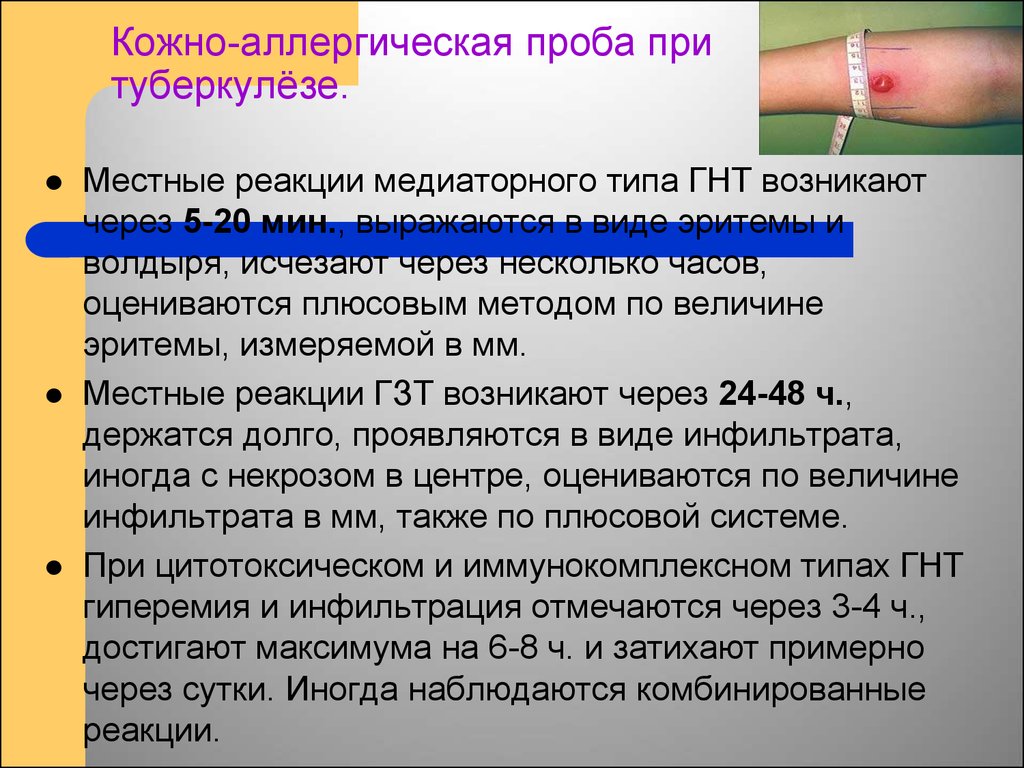
Были зарегистрированы демографические данные, активность заболевания (DAS 28 — показатель СОЭ), продолжительность заболевания и терапия. Оценка по шкале DAS 28 <2,6 была определена как ремиссия, <3,2 — как низкая активность заболевания, <5,1 — как умеренная активность заболевания и ≥5,1 — как высокая активность заболевания. Пациенты, подвергшиеся воздействию табака в форме жевания табака или активного или пассивного курения, были классифицированы как курильщики, а те, кто не подвергался воздействию табака, были классифицированы как некурящие. Все пациенты были обследованы клинически, им была выполнена цифровая рентгенография органов грудной клетки в проекции и проведено необходимое обследование для исключения активного туберкулеза. Всем больным проводилась туберкулиновая кожная проба. Очищенное белковое производное (PPD) 1 TU (0,1 мл) вводили в сгибательную сторону предплечья. Использовался препарат «ППД-РТ-23 с твином 80». Результаты считывали через 72 часа. Туберкулиновая проба считалась положительной, если уплотнение превышало 10 мм. Он считался отрицательным, если он был меньше 5 мм, и сомнительным, если между 5 и 10 мм.
Он считался отрицательным, если он был меньше 5 мм, и сомнительным, если между 5 и 10 мм.
Пациенты были разделены на пять групп в зависимости от приема метотрексата (МТ) в течение последних трех месяцев (контрольный МТ: пациенты, не принимавшие МТ, А-пациенты на мг/нед., В-пациенты на метотрексате –15 мг/нед. , C-пациенты на метотрексате -22,5 мг/нед и D-пациенты на метотрексате мг/нед). В зависимости от приема стероидов пациенты были разделены на три группы (контрольная S-пациенты без приема стероидов в течение последних трех месяцев, I-пациенты с недавним приемом стероидов, определяемым как прием любой дозы стероида в любой форме (перорально, внутримышечно или внутримышечно). -суставной) в течение 1 недели до туберкулиновой пробы, и II-пациенты с историей приема стероидов в течение последних трех месяцев, но не в течение последней недели).
Статистический анализ выполнен с использованием программного обеспечения SPSS 16.0. Критерий хи-квадрат использовался для проверки гипотезы о равенстве пропорций между группами. Точный критерий Фишера применялся, когда ожидаемое значение ячейки было меньше 5. Для сравнения средних значений непрерывных переменных использовался критерий t Стьюдента.
Точный критерий Фишера применялся, когда ожидаемое значение ячейки было меньше 5. Для сравнения средних значений непрерывных переменных использовался критерий t Стьюдента.
3. Результаты
В период с августа 2011 г. по март 2013 г. к участию в исследовании было приглашено 300 пациентов, признанных подходящими для участия в исследовании. Только 256 пациентов дали согласие, из которых 6 пациентов не явились на исследование ТКП. через 72 часа и, таким образом, были исключены, в результате чего общее число участников исследования составило 250. В основном это были пациенты среднего возраста (47,2 ± 10,9лет), женщины (85,2%), некурящие (77,2%) со средней продолжительностью РА 80,8 ± 63,7 мес и умеренной активностью заболевания (43,6%) на момент начала исследования. У 69,2% больных выявлен ревматоидный фактор. Ни один из пациентов не подвергался ТСТ в течение последних двух лет. Демографический профиль различных групп пациентов в зависимости от дозы метотрексата представлен в таблице 1. Демографический профиль пациентов, недавно принимавших стероиды, был аналогичен таковому у пациентов, не принимавших стероиды, по возрасту (, ), статусу курения (хи-квадрат = 0,69, ), положительность ревматоидного фактора (хи-квадрат = 0,09, ), длительность заболевания (, ) и тяжесть заболевания (, ) (табл. 2).
Демографический профиль пациентов, недавно принимавших стероиды, был аналогичен таковому у пациентов, не принимавших стероиды, по возрасту (, ), статусу курения (хи-квадрат = 0,69, ), положительность ревматоидного фактора (хи-квадрат = 0,09, ), длительность заболевания (, ) и тяжесть заболевания (, ) (табл. 2).
Пятьдесят один (20,4%) обследованный пациент был туберкулинположительным, 187 (74,8%) – отрицательным, а 12 (4,8%) имели сомнительные результаты. Хотя прием метотрексата у пациентов не влиял на положительную реакцию на туберкулин (таблица 3), она была значительно ниже у пациентов, недавно принимавших стероиды (группа I) (3), по сравнению с пациентами, не принимавшими стероиды в течение 3 месяцев (контрольная группа S). Достоверной разницы между контролем S и группой II не было (табл. 4).
4. Обсуждение
Согласно отчету ВОЗ, треть населения мира считается носителем латентной туберкулезной инфекции [17]. В округе Анталья, Турция, среди непривитой БЦЖ группы ТКП не было выявлено ни одного в 5-7-летних, 2% в 14-25-летних и 7% в возрастных группах > или = 60 лет [18]. В исследовании, проведенном в 2007 г., распространенность положительной туберкулиновой кожной пробы в Швеции составила 22% [19]. Проспективное исследование серийных туберкулиновых кожных проб, проведенных у 642 пациентов из отделений хронической терапии Госпиталя Управления по делам ветеранов, выявило положительный результат у 23,6% [20]. В исследовании, проведенном на Тайване, 34,2% исследуемой популяции дали положительный результат на ТКП [21]. Из Индии Seal et al. сообщил, что распространенность туберкулезной инфекции составляет 38,9% в 1954 г. [14] и Нариан с соавт. аналогичные цифры сообщали в 1963 г. (38,3%) [15]. Установлено, что распространенность туберкулезной инфекции среди сельского населения Южной Индии в 1968 г. составляла 30% (среди женщин 25% и мужчин 35%) [22]. В нашем исследовании у 20,4% пациентов с ревматоидным артритом была обнаружена положительная ТКП. Исследование было проведено в одном центре в Северной Индии, и, возможно, его потребуется воспроизвести в многоцентровом исследовании.
В исследовании, проведенном в 2007 г., распространенность положительной туберкулиновой кожной пробы в Швеции составила 22% [19]. Проспективное исследование серийных туберкулиновых кожных проб, проведенных у 642 пациентов из отделений хронической терапии Госпиталя Управления по делам ветеранов, выявило положительный результат у 23,6% [20]. В исследовании, проведенном на Тайване, 34,2% исследуемой популяции дали положительный результат на ТКП [21]. Из Индии Seal et al. сообщил, что распространенность туберкулезной инфекции составляет 38,9% в 1954 г. [14] и Нариан с соавт. аналогичные цифры сообщали в 1963 г. (38,3%) [15]. Установлено, что распространенность туберкулезной инфекции среди сельского населения Южной Индии в 1968 г. составляла 30% (среди женщин 25% и мужчин 35%) [22]. В нашем исследовании у 20,4% пациентов с ревматоидным артритом была обнаружена положительная ТКП. Исследование было проведено в одном центре в Северной Индии, и, возможно, его потребуется воспроизвести в многоцентровом исследовании. Сравнивая результаты нашего исследования с доступными популяционными данными, мы можем сделать вывод, что наличие ревматоидного артрита влияет на результаты туберкулиновой пробы в нашей популяции. В исследовании, проведенном в Италии, также было обнаружено, что распространенность латентного туберкулеза с помощью ТКП среди пациентов, страдающих иммуноопосредованными воспалительными заболеваниями, составляет 18,8% [23]. Более низкие показатели положительных результатов ТКП при РА могут быть связаны с самим заболеванием или препаратами, используемыми для его лечения.
Сравнивая результаты нашего исследования с доступными популяционными данными, мы можем сделать вывод, что наличие ревматоидного артрита влияет на результаты туберкулиновой пробы в нашей популяции. В исследовании, проведенном в Италии, также было обнаружено, что распространенность латентного туберкулеза с помощью ТКП среди пациентов, страдающих иммуноопосредованными воспалительными заболеваниями, составляет 18,8% [23]. Более низкие показатели положительных результатов ТКП при РА могут быть связаны с самим заболеванием или препаратами, используемыми для его лечения.
Другим предположением из этого исследования было отсутствие влияния дозы метотрексата на результаты туберкулиновой пробы. Тем не менее, даже низкие дозы недавнего приема стероидов значительно снижают шансы положительного результата на туберкулин. Эти результаты повторяют результаты прошлых исследований. Исследование, проведенное во Флоренции, Италия, показало, что доля положительных результатов ТКП была значительно ниже у пациентов, получавших лечение стероидами, по сравнению с долей положительных результатов у пациентов, не получавших лечения стероидами. В том же исследовании, при рассмотрении влияния каждого класса препаратов с помощью многофакторного анализа, было обнаружено, что использование DMARD не связано с результатами теста, в то время как использование стероидов было связано с более низкой вероятностью TST или Quantiferon-TB Gold In- Трубка (QFT-GIT) положительная оценка [23]. В руководстве Программы борьбы с туберкулезом в Северной Каролине говорится, что ложноотрицательные реакции на ТКП могут быть вызваны высокими дозами стероидов (>15 мг преднизолона или его эквивалента, принимаемого ежедневно в течение одного месяца или дольше) [24]. Шац и др. также выявили, что у пациентов, получавших ежедневные кортикостероиды, туберкулинотрицательность была связана с более высокой дозой кортикостероидов [25]. Напротив, в нашем исследовании среди пациентов, принимавших стероиды в течение последнего месяца, восемь пациентов принимали стероиды, эквивалентные <15 мг преднизолона, и ни у одного из них не было обнаружено туберкулин-положительного результата.
В том же исследовании, при рассмотрении влияния каждого класса препаратов с помощью многофакторного анализа, было обнаружено, что использование DMARD не связано с результатами теста, в то время как использование стероидов было связано с более низкой вероятностью TST или Quantiferon-TB Gold In- Трубка (QFT-GIT) положительная оценка [23]. В руководстве Программы борьбы с туберкулезом в Северной Каролине говорится, что ложноотрицательные реакции на ТКП могут быть вызваны высокими дозами стероидов (>15 мг преднизолона или его эквивалента, принимаемого ежедневно в течение одного месяца или дольше) [24]. Шац и др. также выявили, что у пациентов, получавших ежедневные кортикостероиды, туберкулинотрицательность была связана с более высокой дозой кортикостероидов [25]. Напротив, в нашем исследовании среди пациентов, принимавших стероиды в течение последнего месяца, восемь пациентов принимали стероиды, эквивалентные <15 мг преднизолона, и ни у одного из них не было обнаружено туберкулин-положительного результата. Тем не менее, это не является статистически значимым из-за небольшого числа пациентов, но требует дальнейшего изучения ввиду его клинической значимости.
Тем не менее, это не является статистически значимым из-за небольшого числа пациентов, но требует дальнейшего изучения ввиду его клинической значимости.
В этом исследовании последовательные пациенты с РА, соответствующие критериям включения, были зарегистрированы в амбулаторном отделении, а затем сгруппированы в соответствии с их терапией. Это привело к непропорциональным группам, что является ограничением исследования. Еще одним ограничением исследования является то, что пациенты принимали разные формы и дозы разных кортикостероидов. Иммуносупрессия длительного действия могла повлиять на результаты у некоторых пациентов. Наши данные показывают, что, независимо от дозы или формы принимаемых стероидов, процент положительных результатов ТКП является самым высоким у пациентов, не принимавших стероиды в течение последних трех месяцев (25%), и ниже у тех, кто принимал стероиды в течение последних трех месяцев (16%). , и самый низкий у тех, кто подвергался воздействию стероидов в течение одной недели после тестирования TST (3%). Эта промежуточная степень положительности ТКП в группе, подвергавшейся воздействию стероидов в течение последних 3 месяцев, но не в течение последней 1 недели, может быть связана с различной величиной и продолжительностью иммуносупрессивного эффекта различных форм стероидов, принимаемых пациентами.
Эта промежуточная степень положительности ТКП в группе, подвергавшейся воздействию стероидов в течение последних 3 месяцев, но не в течение последней 1 недели, может быть связана с различной величиной и продолжительностью иммуносупрессивного эффекта различных форм стероидов, принимаемых пациентами.
Несмотря на то, что 2 миллиарда человек имеют латентную форму туберкулеза, лишь небольшая их часть (<10 миллионов в год) заболевает активной формой туберкулеза [26]. Однако у пациентов с РА лечение ингибиторами TNF- α показывает повышенный риск серьезных опасных для жизни инфекций, включая реактивацию латентной туберкулезной инфекции [27]. Таким образом, скрининг на активный ТБ и ЛТБИ стал обязательным до начала терапии TNF [28, 29], а туберкулиновая кожная проба и QFT-GIT остаются широко используемыми тестами [30–33]. Белар и др. показали, что преднизолон серьезно подавляет показатели QFT-GIT и TST, в то время как кортикостероиды длительного действия метотрексат, азатиоприн и 5-ASA не оказывали аналогичного пагубного эффекта, и предложили провести скрининг пациентов на ЛТБИ с помощью QFT-GIT или TST до начала лечения. начало терапии преднизолоном и отрицательные результаты QFT-GIT или TST следует интерпретировать с осторожностью у пациентов, получавших любой кортикостероид [34]. Мы разделяем эту точку зрения и особенно беспокоимся о пациентах с РА, которым планируется лечение ФНО-9.0225 α ингибиторная терапия, так как большинство этих пациентов из-за высокой активности заболевания обычно уже принимают стероиды в той или иной форме. В исследовании ATTRACT около 60% пациентов принимали кортикостероиды в дозе 10 мг или меньше в начале исследования [35]. В такой ситуации нельзя полагаться на ТКП для скрининга латентного туберкулеза. Наше исследование предполагает, что прием стероидов в течение последней 1 недели значительно снижает шансы положительного результата на туберкулин. Поэтому у пациентов с РА перед введением биологических препаратов результаты туберкулиновой пробы следует читать с осторожностью, если в анамнезе имеется недавний прием стероидов.
начало терапии преднизолоном и отрицательные результаты QFT-GIT или TST следует интерпретировать с осторожностью у пациентов, получавших любой кортикостероид [34]. Мы разделяем эту точку зрения и особенно беспокоимся о пациентах с РА, которым планируется лечение ФНО-9.0225 α ингибиторная терапия, так как большинство этих пациентов из-за высокой активности заболевания обычно уже принимают стероиды в той или иной форме. В исследовании ATTRACT около 60% пациентов принимали кортикостероиды в дозе 10 мг или меньше в начале исследования [35]. В такой ситуации нельзя полагаться на ТКП для скрининга латентного туберкулеза. Наше исследование предполагает, что прием стероидов в течение последней 1 недели значительно снижает шансы положительного результата на туберкулин. Поэтому у пациентов с РА перед введением биологических препаратов результаты туберкулиновой пробы следует читать с осторожностью, если в анамнезе имеется недавний прием стероидов.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов в отношении публикации данной статьи.
Финансирование
Эта работа была поддержана Советом по научным и промышленным исследованиям через Грант №. 13(8478-А)/Пул-2011.
Ссылки
H. Mollgaard, «Экспериментальная база для лечения туберкулеза санокризином», Ugeskr Laeger , vol. 86, ст. 1035, 1924.
Посмотреть по адресу:
Google Scholar
Г. Слот, П. М. Девиль, Н. Г. Хилл, Б. Уильямс и М. Х. Фриджон, «Лечение артрита и ревматизма золотом», The Lancet , vol. 223, нет. 5759, стр. 73–76, 1934.
Посмотреть по адресу:
Google Scholar
Дж. Форестье, «Ревматоидный артрит и его лечение солями золота», The Lancet , vol. 224, нет. 5795, стр. 646–648, 1934.
Посмотреть по адресу:
Google Scholar
Г.
 М. Бахр, Г. А. В. Рук, М. Аль-Саффар, Дж. ван Эмбден, Дж. Л. Стэнфорд и К. Бехбехани, «Уровни антител к микобактериям в зависимости от типа HLA: доказательства высоких уровней антител, не связанных с HLA». к белку теплового шока 65 кДа M. bovis при ревматоидном артрите», Clinical and Experimental Immunology , vol. 74, нет. 2, pp. 211–215, 1988.
М. Бахр, Г. А. В. Рук, М. Аль-Саффар, Дж. ван Эмбден, Дж. Л. Стэнфорд и К. Бехбехани, «Уровни антител к микобактериям в зависимости от типа HLA: доказательства высоких уровней антител, не связанных с HLA». к белку теплового шока 65 кДа M. bovis при ревматоидном артрите», Clinical and Experimental Immunology , vol. 74, нет. 2, pp. 211–215, 1988.Посмотреть по адресу:
Google Scholar
T. Yamada, A. Nakajima, E. Inoue et al., «Повышенный риск туберкулеза у пациентов с ревматоидным артритом в Японии », Annals of the Rheumatic Diseases , vol. 65, нет. 12, стр. 1661–1663, 2006.
Посмотреть по адресу:
Сайт издателя | Google Scholar
F. Wolfe, K. Michaud, J. Anderson и K. Urbansky, «Туберкулезная инфекция у пациентов с ревматоидным артритом и эффект терапии инфликсимабом», Arthritis and Rheumatism , vol.
 50, нет. 2, стр. 372–379, 2004.
50, нет. 2, стр. 372–379, 2004.Посмотреть по адресу:
Сайт издателя | Google Scholar
J. Askling, C. M. Fored, L. Brandt et al., «Риск и характеристики случаев туберкулеза при ревматоидном артрите, связанном с антагонистами фактора некроза опухоли в Швеции», Артрит и ревматизм , vol. 52, нет. 7, стр. 1986–1992, 2005.
Посмотреть по адресу:
Сайт издателя | Google Scholar
L. Carmona, C. Hernández-García, C. Vadillo et al., «Повышенный риск туберкулеза у пациентов с ревматоидным артритом», Journal of Rheumatology , vol. 30, нет. 7, pp. 1436–1439, 2003.
Посмотреть по адресу:
Google Scholar
Дж. Дж. Куш, «Обзор безопасности новых противоревматических препаратов, модифицирующих заболевание», Клиники ревматических заболеваний Северной Америки , vol.
 30, нет. 2, стр. 237–255, 2004 г.
30, нет. 2, стр. 237–255, 2004 г.Посмотреть по адресу:
Сайт издателя | Google Scholar
Дж. Кин, С. Гершон, Р. П. Уайз и др., «Туберкулез, связанный с инфликсимабом, фактором некроза опухоли α -нейтрализующим агентом», The New England Journal of Medicine , vol. 345, нет. 15, стр. 1098–1104, 2001.
Посмотреть по адресу:
Сайт издателя | Академия Google
J. J. Gómez-Reino, L. Carmona, V. Rodríguez Valverde, E. M. Mola и MD Montero, «Лечение ревматоидного артрита ингибиторами фактора некроза опухоли может предрасполагать к значительному увеличению риска туберкулеза: отчет о многоцентровом активном наблюдении». Артрит и ревматизм , vol. 48, нет. 8, стр. 2122–2127, 2003.
Посмотреть по адресу:
Сайт издателя | Google Scholar
W.
 G. Dixon, K. L. Hyrich, K. D. Watson et al., «Лекарственный риск туберкулеза у пациентов с ревматоидным артритом, получавших анти-ФНО терапию: результаты из Регистра биологических препаратов Британского общества ревматологии (BSRBR), Annals of the Rheumatic Diseases , vol. 69, нет. 3, стр. 522–528, 2010.
G. Dixon, K. L. Hyrich, K. D. Watson et al., «Лекарственный риск туберкулеза у пациентов с ревматоидным артритом, получавших анти-ФНО терапию: результаты из Регистра биологических препаратов Британского общества ревматологии (BSRBR), Annals of the Rheumatic Diseases , vol. 69, нет. 3, стр. 522–528, 2010.Посмотреть по адресу:
Сайт издателя | Google Scholar
Central TB Division, Government of India, New Delhi, India, TB Epidemiology, TB India 2013, Revised National TB Control Programme, Annual status report: 19.
S. C. Seal, L. M. Bhattacharji, A. K. Banerji , Мазумдар С.М. Туберкулезное обследование сельской местности, находящейся в непосредственной близости от промышленного города, Индийский журнал туберкулеза , том. 1, нет. 3, article 116, 1954.
Посмотреть по адресу:
Google Scholar
Р.
 Нариан, А. Гесер, М. В. Джамбунатан и др., «М. Обследование распространенности туберкулеза в районе Тумкур», Indian Journal of Tuberculosis , vol. 10, article 85, 1963.
Нариан, А. Гесер, М. В. Джамбунатан и др., «М. Обследование распространенности туберкулеза в районе Тумкур», Indian Journal of Tuberculosis , vol. 10, article 85, 1963.Посмотреть по адресу:
Google Scholar
Ф. К. Арнетт, С. М. Эдворти, Д. А. Блох и др., «Американская ассоциация ревматизма, 1987 г., пересмотренные критерии классификации ревматоидного артрита», Артрит и ревматизм , vol. 31, нет. 3, pp. 315–324, 1988.
Посмотреть по адресу:
Google Scholar
Центр СМИ Всемирной организации здравоохранения, «Туберкулез», Информационный бюллетень № 104, 2013 г., http://www.who. int/mediacentre/factsheets/fs104/en/.
Посмотреть по адресу:
Google Scholar
C. Yildirim, A.I. Küçük, G. Ongüt, D.
 Oğünç, D. Colak, and G. Mutlu, «Оценка туберкулиновой реактивности в разных возрастных группах с БЦЖ и без нее вакцинация», Mikrobiyoloji Bülteni , vol. 43, нет. 1, стр. 27–35, 2009 г. (турецкий).
Oğünç, D. Colak, and G. Mutlu, «Оценка туберкулиновой реактивности в разных возрастных группах с БЦЖ и без нее вакцинация», Mikrobiyoloji Bülteni , vol. 43, нет. 1, стр. 27–35, 2009 г. (турецкий).Посмотреть по адресу:
Google Scholar
P. Gustafson, I. Lisse, V. Gomes et al., «Факторы риска для положительных туберкулиновых кожных проб в Гвинее-Бисау», Epidemiology , vol. 18, нет. 3, стр. 340–347, 2007 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
C. Welty, S. Burstin, S. Muspratt, and I.B. Tager, «Эпидемиология туберкулезной инфекции в популяции, получающей хроническую помощь», The American Review of Respiratory Disease , vol. 132, нет. 1, стр. 133–136, 1985.
Посмотреть по адресу:
Google Scholar
Р.
 Дж. Бауэрман, «Туберкулиновые кожные пробы у вакцинированных БЦЖ групп взрослых и детей с высоким риском туберкулеза на Тайване», International Журнал туберкулеза и болезней легких , том. 8, нет. 10, pp. 1228–1233, 2004.
Дж. Бауэрман, «Туберкулиновые кожные пробы у вакцинированных БЦЖ групп взрослых и детей с высоким риском туберкулеза на Тайване», International Журнал туберкулеза и болезней легких , том. 8, нет. 10, pp. 1228–1233, 2004.Посмотреть по адресу:
Google Scholar
Национальный институт туберкулеза, Бангалор, «Туберкулез среди сельского населения южной Индии: пятилетнее эпидемиологическое исследование», Бюллетень Всемирной организации здравоохранения , том. 51, article 473, 1974.
Посмотреть по адресу:
Google Scholar
F. Bartalesi, S. Vicidomini, D. Goletti et al., «QuantiFERON-TB Gold и TST полезны при латентной туберкулезной инфекции. скрининг аутоиммунных заболеваний», European Respiratory Journal , vol. 33, нет. 3, стр. 586–593, 2009 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
NC TB Control Program Policy Manual (Rev.
 02/13), 2:4.
02/13), 2:4.М. Шац, Р. Паттерсон, Р. Клонер и Дж. Фальк, «Распространенность туберкулеза и положительные кожные туберкулиновые пробы в группе больных астмой, получавших стероиды», Annals of Internal Medicine , vol. 84, нет. 3, pp. 261–265, 1976.
Посмотреть по адресу:
Google Scholar
Всемирная организация здравоохранения, Заявление о политике IGRA по тестированию туберкулеза на туберкулез, 2011 г., http://www.who.int/tb/laboratory/ policy_statements/ru.
R. Maini, E.W. St Clair, F. Breedveld et al., «Инфликсимаб (химерный фактор некроза опухоли α моноклональное антитело) по сравнению с плацебо у пациентов с ревматоидным артритом, получающих сопутствующую терапию метотрексатом: рандомизированное исследование фазы III», The Lancet , vol. 354, нет. 9194, стр. 1932–1939, 1999.
Посмотреть по адресу:
Сайт издателя | Google Scholar
M.
 A. Gardam, E. C. Keystone, R. Menzies et al., «Агенты против фактора некроза опухоли и риск туберкулеза: механизмы действия и клиническое лечение», The Lancet Infectious Diseases , том. 3, нет. 3, стр. 148–155, 2003 г.
A. Gardam, E. C. Keystone, R. Menzies et al., «Агенты против фактора некроза опухоли и риск туберкулеза: механизмы действия и клиническое лечение», The Lancet Infectious Diseases , том. 3, нет. 3, стр. 148–155, 2003 г.Посмотреть по адресу:
Сайт издателя | Google Scholar
D. E. Furst, F. C. Breedveld, JR Kalden et al., «Обновленное согласованное заявление о биологических агентах для лечения ревматических заболеваний, 2006 г.», Annals of the Rheumatic Diseases , vol. 65, приложение 3, стр. iii2–iii15, 2006.
Посмотреть по адресу:
Сайт издателя | Google Scholar
Комитет по стандартам медицинской помощи Британского торакального общества, «Рекомендации BTS по оценке риска и лечению инфекции и заболевания Mycobacterium tuberculosis у пациентов, которые должны начать лечение анти-ФНО-9».
 0225 α , Thorax , vol. 60, нет. 10, стр. 800–805, 2005.
0225 α , Thorax , vol. 60, нет. 10, стр. 800–805, 2005.Посмотреть по адресу:
Сайт издателя | Google Scholar
J. E. Fonseca, H. Lucas, H. Canhão et al., «Рекомендации по диагностике и лечению латентной туберкулезной инфекции и активного туберкулеза у пациентов с воспалительными заболеваниями суставов, предложенные для лечения фактором некроза опухоли α ». препараты-антагонисты», Revista Portuguesa de Pneumologia , vol. 12, нет. 5, стр. 603–613, 2006.
Посмотреть по адресу:
Google Scholar
X. Mariette, D. Salmon и RATIO Group, «Французские рекомендации по диагностике и лечению латентного и активного туберкулеза у пациентов с РА, получавших лечение блокаторами TNF», Annals of the Ревматические болезни , том. 62, нет. 8, стр. 791–792, 2003.
Посмотреть по адресу:
Сайт издателя | Google Scholar
C.
 Beglinger, J. Dudler, C. Mottet et al., «Скрининг на туберкулезную инфекцию перед началом анти-TNF- α терапия», Swiss Medical Weekly , vol. 137, нет. 43–44, pp. 621–622, 2007.
Beglinger, J. Dudler, C. Mottet et al., «Скрининг на туберкулезную инфекцию перед началом анти-TNF- α терапия», Swiss Medical Weekly , vol. 137, нет. 43–44, pp. 621–622, 2007.Просмотр по адресу:
Google Scholar
Э. Белар, С. Семб, М. Рувальд и др., «Лечение преднизолоном влияет на эффективность QuantiFERON gold внутрипробирочный тест и туберкулиновый кожный тест у пациентов с аутоиммунными заболеваниями, обследованных на латентную туберкулезную инфекцию», Воспалительные заболевания кишечника , том. 17, нет. 2011. Т. 11. С. 2340–2349.
Посмотреть по адресу:
Сайт издателя | Google Scholar
PE Lipsky, DM van der Heijde, EW St Clair et al., «Инфликсимаб и метотрексат в лечении ревматоидного артрита», The New England Journal of Medicine , vol. 343, нет. 22, стр. 1594–1602, 2000.


 ReliefWeb. По состоянию на 26 июня 2021 г.
ReliefWeb. По состоянию на 26 июня 2021 г. N Engl J Med. 2004;350(20):2060-2067. ПабМед | Академия Google
N Engl J Med. 2004;350(20):2060-2067. ПабМед | Академия Google  Гельминты и искаженные профили цитокинов повышают положительную реакцию на туберкулиновые кожные пробы у американских индейцев варао. Туберкулез. 2012;92(6):505-512. ПабМед | Google Scholar
Гельминты и искаженные профили цитокинов повышают положительную реакцию на туберкулиновые кожные пробы у американских индейцев варао. Туберкулез. 2012;92(6):505-512. ПабМед | Google Scholar  июль-сентябрь 2015 г.; 4(3):384-7. ПабМед | Google Scholar
июль-сентябрь 2015 г.; 4(3):384-7. ПабМед | Google Scholar 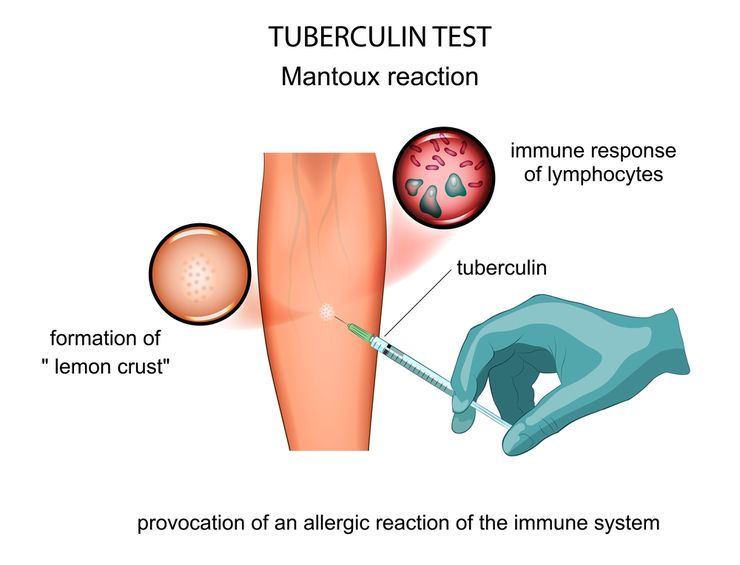 Ам преподобный Респир Дис. 1992;146(3):752-756. ПабМед | Google Scholar
Ам преподобный Респир Дис. 1992;146(3):752-756. ПабМед | Google Scholar  , Гроссман, округ Колумбия, Карри С.Дж., Бауман Л., Дэвидсон К.В. и др. . Скрининг на латентную туберкулезную инфекцию у взрослых: заявление рабочей группы профилактических служб США. ДЖАМА. 2016;316(9):962-9. ПабМед | Google Scholar
, Гроссман, округ Колумбия, Карри С.Дж., Бауман Л., Дэвидсон К.В. и др. . Скрининг на латентную туберкулезную инфекцию у взрослых: заявление рабочей группы профилактических служб США. ДЖАМА. 2016;316(9):962-9. ПабМед | Google Scholar  Pediatr Infect Dis J. 1988;7(8):578-581. ПабМед | Google Scholar
Pediatr Infect Dis J. 1988;7(8):578-581. ПабМед | Google Scholar  М. Бахр, Г. А. В. Рук, М. Аль-Саффар, Дж. ван Эмбден, Дж. Л. Стэнфорд и К. Бехбехани, «Уровни антител к микобактериям в зависимости от типа HLA: доказательства высоких уровней антител, не связанных с HLA». к белку теплового шока 65 кДа M. bovis при ревматоидном артрите», Clinical and Experimental Immunology , vol. 74, нет. 2, pp. 211–215, 1988.
М. Бахр, Г. А. В. Рук, М. Аль-Саффар, Дж. ван Эмбден, Дж. Л. Стэнфорд и К. Бехбехани, «Уровни антител к микобактериям в зависимости от типа HLA: доказательства высоких уровней антител, не связанных с HLA». к белку теплового шока 65 кДа M. bovis при ревматоидном артрите», Clinical and Experimental Immunology , vol. 74, нет. 2, pp. 211–215, 1988. 50, нет. 2, стр. 372–379, 2004.
50, нет. 2, стр. 372–379, 2004. 30, нет. 2, стр. 237–255, 2004 г.
30, нет. 2, стр. 237–255, 2004 г. G. Dixon, K. L. Hyrich, K. D. Watson et al., «Лекарственный риск туберкулеза у пациентов с ревматоидным артритом, получавших анти-ФНО терапию: результаты из Регистра биологических препаратов Британского общества ревматологии (BSRBR), Annals of the Rheumatic Diseases , vol. 69, нет. 3, стр. 522–528, 2010.
G. Dixon, K. L. Hyrich, K. D. Watson et al., «Лекарственный риск туберкулеза у пациентов с ревматоидным артритом, получавших анти-ФНО терапию: результаты из Регистра биологических препаратов Британского общества ревматологии (BSRBR), Annals of the Rheumatic Diseases , vol. 69, нет. 3, стр. 522–528, 2010. Нариан, А. Гесер, М. В. Джамбунатан и др., «М. Обследование распространенности туберкулеза в районе Тумкур», Indian Journal of Tuberculosis , vol. 10, article 85, 1963.
Нариан, А. Гесер, М. В. Джамбунатан и др., «М. Обследование распространенности туберкулеза в районе Тумкур», Indian Journal of Tuberculosis , vol. 10, article 85, 1963. Oğünç, D. Colak, and G. Mutlu, «Оценка туберкулиновой реактивности в разных возрастных группах с БЦЖ и без нее вакцинация», Mikrobiyoloji Bülteni , vol. 43, нет. 1, стр. 27–35, 2009 г. (турецкий).
Oğünç, D. Colak, and G. Mutlu, «Оценка туберкулиновой реактивности в разных возрастных группах с БЦЖ и без нее вакцинация», Mikrobiyoloji Bülteni , vol. 43, нет. 1, стр. 27–35, 2009 г. (турецкий). Дж. Бауэрман, «Туберкулиновые кожные пробы у вакцинированных БЦЖ групп взрослых и детей с высоким риском туберкулеза на Тайване», International Журнал туберкулеза и болезней легких , том. 8, нет. 10, pp. 1228–1233, 2004.
Дж. Бауэрман, «Туберкулиновые кожные пробы у вакцинированных БЦЖ групп взрослых и детей с высоким риском туберкулеза на Тайване», International Журнал туберкулеза и болезней легких , том. 8, нет. 10, pp. 1228–1233, 2004. 02/13), 2:4.
02/13), 2:4. A. Gardam, E. C. Keystone, R. Menzies et al., «Агенты против фактора некроза опухоли и риск туберкулеза: механизмы действия и клиническое лечение», The Lancet Infectious Diseases , том. 3, нет. 3, стр. 148–155, 2003 г.
A. Gardam, E. C. Keystone, R. Menzies et al., «Агенты против фактора некроза опухоли и риск туберкулеза: механизмы действия и клиническое лечение», The Lancet Infectious Diseases , том. 3, нет. 3, стр. 148–155, 2003 г. 0225 α , Thorax , vol. 60, нет. 10, стр. 800–805, 2005.
0225 α , Thorax , vol. 60, нет. 10, стр. 800–805, 2005. Beglinger, J. Dudler, C. Mottet et al., «Скрининг на туберкулезную инфекцию перед началом анти-TNF- α терапия», Swiss Medical Weekly , vol. 137, нет. 43–44, pp. 621–622, 2007.
Beglinger, J. Dudler, C. Mottet et al., «Скрининг на туберкулезную инфекцию перед началом анти-TNF- α терапия», Swiss Medical Weekly , vol. 137, нет. 43–44, pp. 621–622, 2007.