Туберкулинодиагностика в Новосибирске | Медсанчасть-168
Туберкулёз в начале заболевания никак не проявляет себя. В этом то и состоит проблема. Выявить заболевание можно только с помощью тестов. В России самыми распространёнными способами является проба Манту и Диаскинтест.
Многие ошибочно называют процедуру тестирования «вакцинацией». Разберёмся, почему это неправильно.
Большинству детей в первые дни после рождения делают БЦЖ или БЦЖ-М. Это прививка от туберкулёза. В её составе — ослабленные микобактерии туберкулеза.
Реакция организма на введение ослабленных микроорганизмов у всех разная. Для оценки этой реакции и делают пробу Манту. Это внутрикожный тест с очищенным туберкулезным аллергеном.
Проба Манту — это не прививка! Это аллергопроба.
Что же показывает реакция Манту?
- В первые 2 года после БЦЖ реакция Манту показывает, сформировался ли иммунный ответ на вакцинацию.
- После двух лет ежегодную реакцию Манту сравнивают с предыдущим результатом.

- В 7 лет проводит реакцию Манту и по итогам отбирают кандидатов на ревакцинацию БЦЖ.
- Если не было вакцинации БЦЖ, оцениваю, был ли контакт с туберкулезной инфекцией или нет.
После 8 лет можно использовать Диаскинтест. Это тоже внутрикожный тест, но в качестве аллергена выступает рекомбинантный белок.
Диаскинтест отвечает только на вопрос: есть тубифицирование или нет.
Детям с аллергическими реакциями или дерматитами могут рекомендовать провести Диаскинтест.
Использовать Диаскинтест у детей младше 8 лет можно, но надо понимать, что по информативности он уступает реакции Манту. В детском саду или школе могут потребовать у Вас справку от фтизиатра.
Остались вопросы? Нет уверенности, каким тестом провести туберкулинодиагностику? В медсанчасти-168 проводят диагностику двумя способами. Выбор метода доверьте грамотному специалисту. Учитывая возрастные особенности, аллергоанамнез и состояние пациента на момент осмотра педиатр Медсанчасти предложит Вам оптимальный метод диагностики.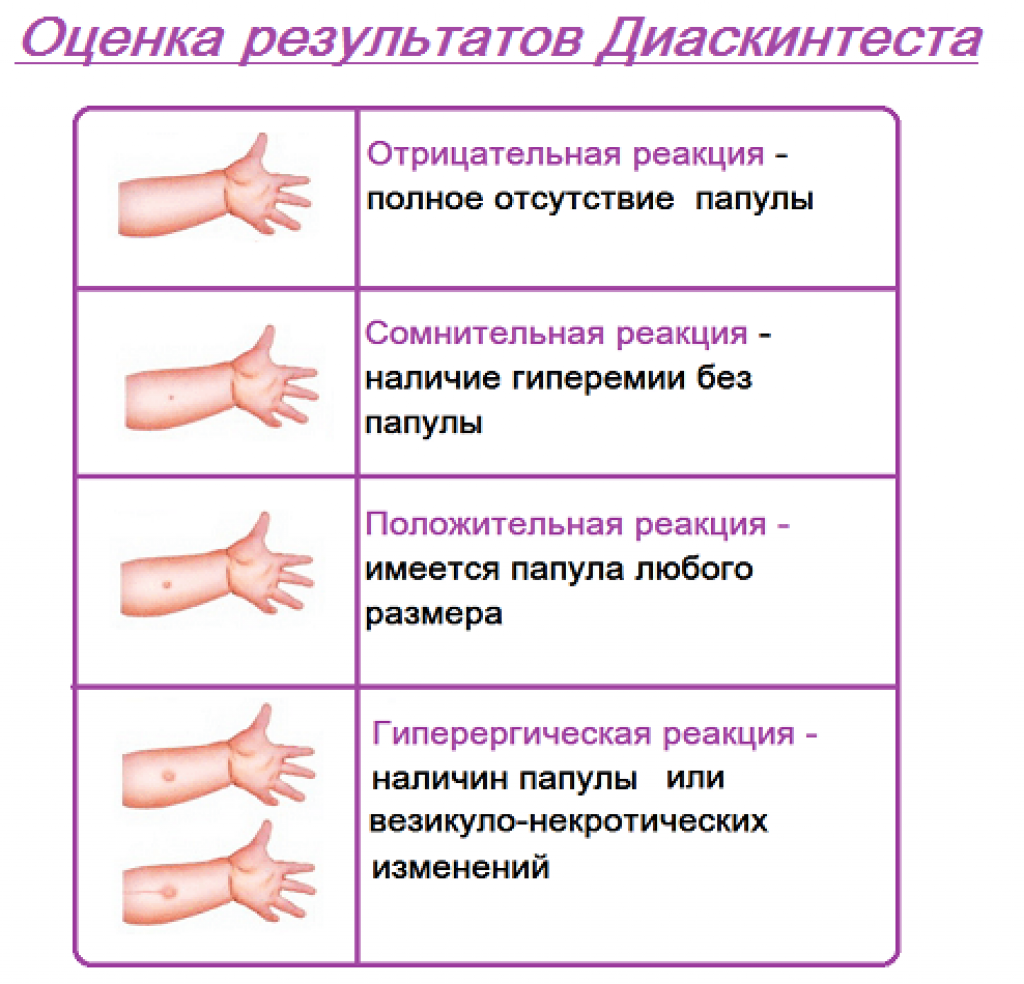
Стоимость консультации перед пробой всего 300р.
Записывайтесь по телефону +7(383)332-05-51
11.08.2021
ДИАСКИН Тест -туберкулинодиагностика
Диаскинтест (Туберкулиновая проба): АЛЛЕРГЕН ТУБЕРКУЛЕЗНЫЙ РЕКОМБИНАНТНЫЙ
Современные российские клиники, начиная с 2009 года, практикуют новые методы определения и диагностирования присутствия бактерий туберкулеза у взрослых и детей. В частности, для наибольшей точности установления диагноза, широкое применение получила методика – Диаскинтест.
Диаскинтест представляет собой инновационный препарат, специально синтезированный для аллергодиагностики туберкулеза. Так называемый аллерген туберкулезный рекомбинантный состав позволяет с наилучшим процентом точности зафиксировать присутствие инфекционного заражения в организме.
В основу препарата вошли два антигена с аббревиатурными номерами CFP10 и ESAT6, которые имеют присутствие в штампах вирулентных бактерий туберкулеза, но по факту являются безопасными элементами, применяемыми для производства сывороток БЦЖ и БЦЖ-М.
При использовании Диаскинтест явные следы истинного инфицирования туберкулезом неизменно себя проявят. Даже если у человека уже была произведена прививка БЦЖ или имеется поствакцинальная аллергия на данный тип прививок, то проведение вакцинации аллерген туберкулезным рекомбинантным составом является приемлемым, поскольку не создает риска заболеть туберкулезом.
Важно осознавать, что Диаскинтест это не полноценная прививка, а специальная форма тестирования, аналогичная форме Манту. Только в отличие от последнего варианта, новый способ многократно точнее отражает реальную картину. В частности, показатель точности пробы Манту составляет 50-70%, а проведение тестирования на основе диаскинтеста составляет не менее 90%.
Основанием к отказу от проведения данного теста может служить лишь острая инфекционная активность в организме пациента или явные признаки эпилепсии.
Диаскинтест — О препарате Диаскинтест: инструкция по применению, дозировка
Диаскинтест® (Аллерген туберкулезный рекомбинантный в стандартном разведении) — инновационный внутрикожный диагностический тест, который представляет собой рекомбинантный белок, содержащий два связанных между собой антигена — ESAT6 и CFP10, характерных для патогенных штаммов микобактерий туберкулеза (Mycobacterium tuberculosis)1. Данные антигены отсутствуют в вакцинном штамме Mycobacterium bovis BCG и у большинства нетуберкулезных микобактерий, поэтому Диаскинтест® вызывает иммунную реакцию только на микобактерии туберкулеза и не дает реакции, связанной с вакцинацией БЦЖ. Благодаря данным качествам, Диаскинтест® обладает практически 100% чувствительностью и специфичностью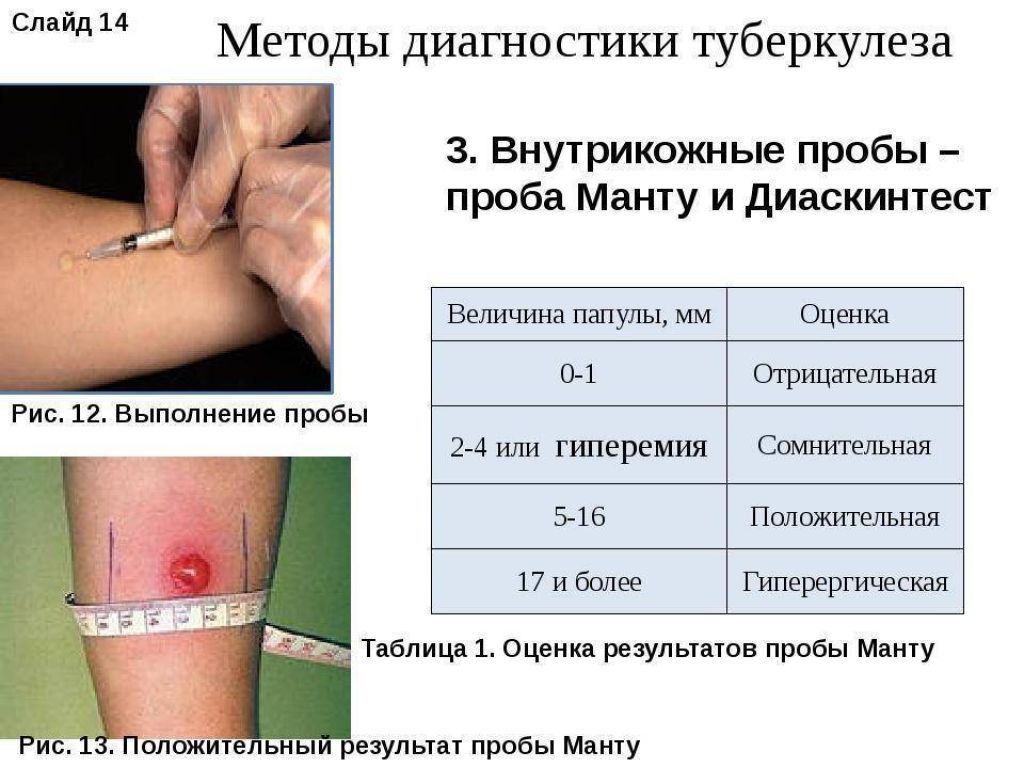 Техника постановки Диаскинтеста и учета результатов идентичны пробе Манту с туберкулином4.
Техника постановки Диаскинтеста и учета результатов идентичны пробе Манту с туберкулином4.
В России использование Диаскинтеста утверждено в 2009 году Приказом МЗ РФ 855 от 29 октября 2009 г.
С 2017 года применение Диаскинтеста в скрининге туберкулеза у детей старше 7 лет и подростков регламентировано Приказом Минздрава России №124н от 21 марта 2017 года5.
Диаскинтест высоко чувствителен и высоко информативен: он позволяет исключить ложноположительные реакции, которые проявляются при проведении пробы Манту у вакцинированных лиц (поствакцинальный иммунитет). По разным оценкам и в разных регионах России чувствительность Диаскинтеста составляет около 96%.
КАК ДОСТИГАЕТСЯ ВЫСОКАЯ ТОЧНОСТЬ ДИАСКИНТЕСТА
Диаскинтест является диагностическим тестом, основанным на формировании реакции гиперчувствительности замедленного типа (ГЧЗТ), проявляющейся в виде уплотнения (папулы) в месте введения при наличии в организме патогенной для организма человека микобактерии туберкулеза с наличием в своей структуре двух антигенов ESAT-6 и CFP-10.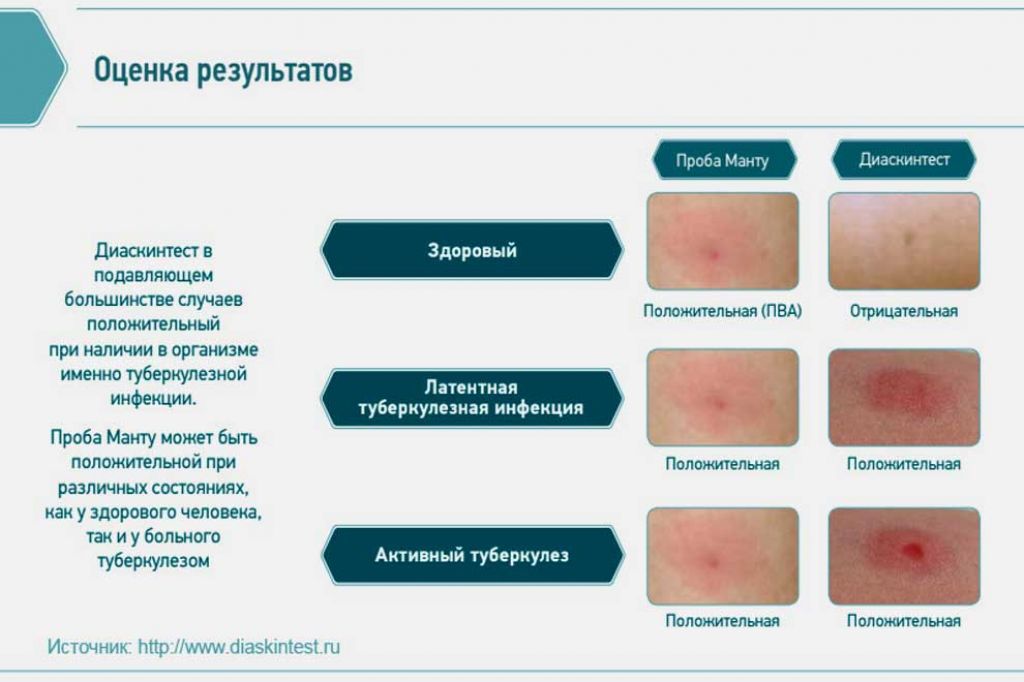
Если человек болен туберкулезом (активная или латентная (скрытая) туберкулезная инфекция), то в месте введения Диаскинтеста формируется уплотнение (папула) – положительный тест. В данном случае необходимо тщательное дообследование для исключения активного туберкулезного поражения. При отсутствии достоверных признаков болезни положительный тест свидетельствует о том, что у человека латентная (скрытая) туберкулезная инфекция и существует высокий риск перехода болезни в активную форму в ближайшее время. Поэтому необходимо проведение специального профилактического лечения противотуберкулезными препаратами.
Если человек здоров, при этом имеет иммунитет от туберкулеза после вакцинации БЦЖ (поствакцинальный иммунитет), то Диаскинтест будет отрицательный.
Для оценки эффективности любой тестовой пробы учитывают две основные характеристики: чувствительность и специфичность. Чем выше эти показатели, тем более качественно тест выявляет инфекцию.
Чувствительность теста – это наличие положительных реакций у лиц с достоверно подтвержденным диагнозом.
Чувствительность Диаскинтеста 96,0%6.
Специфичность же теста – это отрицательная реакция на пробу у абсолютно здоровых людей.
Специфичность Диаскинтеста 99,0%6.
Все это позволило Диаскинтесту стать надежным и высокоинформативным методом диагностики как латентного, так и активного туберкулеза. Высокая точность диагностики позволяет избежать ненужных и зачастую вредных лечебных курсов и исследований.
ПРЕИМУЩЕСТВА ДИАСКИНТЕСТА ПЕРЕД ДРУГИМИ ТЕСТАМИ
- Высокая специфичность и высокая чувствительность;
- Отсутствие ложноположительных результатов в случае вакцинации БЦЖ;
- Не требуется специального лабораторного оборудования;
- Малотравматичен для детей любого возраста;
- Эффективен в любом возрасте: дети, подростки, взрослые.
КОГДА ИСПОЛЬЗУЕТСЯ ДИАСКИНТЕСТ
У детей до 7 лет:
- дифференциальная диагностика поствакцинальной и инфекционной аллергии;
- оценка активности туберкулезного процесса (при обнаружении кальцинатов и следов ранее перенесенной инфекции) в комплексе с другими клинико-лабораторно-рентгенологическими методами;
- дифференциальная диагностика туберкулеза в комплексе с другими клинико-лабораторно-рентгенологическими исследованиями;
- оценка эффективности противотуберкулезного лечения в комплексе с другими методами.

У детей старше 7 лет и подростков:
- диагностика туберкулеза и выявление лиц с высоким риском развития активного туберкулеза (скрининг)7;
- оценка активности туберкулезного процесса;
- дифференциальная диагностика туберкулеза в комплексе с другими клинико-лабораторно-рентгенологическими исследованиями;
- оценка эффективности противотуберкулезного лечения в комплексе с другими методами.
У взрослых:
- диагностика туберкулеза и выявление лиц с высоким риском развития активного туберкулеза;
- оценка активности туберкулезного процесса;
- дифференциальная диагностика туберкулеза в комплексе с другими клинико-лабораторно-рентгенологическими исследованиями;
- оценка эффективности противотуберкулезного лечения в комплексе с другими методами;
- Внимание! Вакцинация БЦЖ не влияет на результаты Диаскинтеста.
КАК ПОДГОТОВИТЬСЯ К ПОСТАНОВКЕ ДИАСКИНТЕСТА
Проба проводится по назначению врача детям, подросткам и взрослым специально обученной медицинской сестрой, имеющей допуск к проведению внутрикожных тестов.
Лицам, у которых в анамнезе имелись проявления неспецифической аллергии, пробу рекомендуется проводить на фоне приема десенсибилизирующих препаратов в течение 7 дней (5 дней до постановки пробы и 2 дня после нее).
УЧЕТ РЕЗУЛЬТАТОВ ДИАСКИНТЕСТА
Результат пробы оценивает врач или обученная медсестра через 72 ч (3 суток) от ее постановки.
Критерии оценки ответной реакции на пробу Диаскинтеста:
Категория реакции | Критерии оценки |
|---|---|
Отрицательная | Полное отсутствие инфильтрата и гиперемии или наличие «уколочной реакции» до 2 мм. |
Сомнительная | Наличие гиперемии без уплотнения (папулы). |
Положительная | Наличие уплотнения (папулы) любого размера. |
Внимание! Лица с сомнительной и положительной реакцией на Диаскинтест® подлежат комплексному обследованию на туберкулез.
Инструкция по применению препарата Диаскинтест®
НОРМАТИВНЫЕ ДОКУМЕНТЫ, РЕГЛАМЕНТИРУЮЩИЕ ПРИМЕНЕНИЕ ДИАСКИНТЕСТА:
- Приказ министерства здравоохранения и социального развития РФ № 855 от 29.10.09 «О внесении изменения в приложение № 4 к приказу Минздрава России № 109 от 21.03.03»
- Федеральные клинические рекомендации по диагностике и лечению латентной туберкулёзной инфекции у детей, утвержденные Российским обществом фтизиатров, под ред. д.м.н. проф. В.А. Аксеновой, 2015г.
- Рекомендации по скринингу и мониторингу туберкулезной инфекции у больных, получающих генно-инженерные биологические препараты, утвержденные Ассоциацией ревматологов РФ 2013 с дополнениями от 2016 г., под ред. Борисова С.Е., Лукиной Г.В..
- Клинические рекомендации «Латентная туберкулезная инфекция (ЛТИ) у детей», 2016
- Клинические рекомендации «Выявление и диагностика туберкулеза у детей, поступающих и обучающихся в образовательных организациях» под ред.
 д.м.н. проф. В.А. Аксеновой, 2017г.
д.м.н. проф. В.А. Аксеновой, 2017г. - Приказ Министерства здравоохранения РФ от 21 марта 2017 г. № 124н “Об утверждении порядка и сроков проведения профилактических медицинских осмотров граждан в целях выявления туберкулеза”
1 Киселев В.И., Барановский П.М., Пупышев С.А. и др. Новый кожный тест для диагностики туберкулеза на основе рекомбинантного белка ESAT-CFP. Мол. мед. -2008. — № 4. — С. 28–34
2 Киселев В.И., Барановский П.М., Рудых И.В. и др. Клинические исследования нового кожного теста «ДИАСКИНТЕСТ®» для диагностики туберкулеза. Пробл. туб. и болезней легких. — 2009. — № 2.- С. 1–8
3 Лебедева Л.В., Грачева С. Г. Чувствительность к туберкулину и инфицированность микобактериями туберкулеза у детей. Пробл. туб. и болезней легких. — 2007. — № 1.- С. 43–49
4 Приказ министерства здравоохранения и социального развития РФ № 855 от 29.10.09 «О внесении изменения в приложение № 4 к приказу Минздрава России № 109 от 21. 03.03»
03.03»
5 Приказ Министерства здравоохранения РФ от 21 марта 2017 г. № 124н “Об утверждении порядка и сроков проведения профилактических медицинских осмотров граждан в целях выявления туберкулеза”
6 Слогоцкая Л.В., Сенчихина О.Ю., Никитина Г.В., Богородская Е.М. Эффективность кожного теста с аллергеном туберкулезным рекомбинантным при выявлении туберкулеза у детей и подростков Москвы в 2013 г. // Педиатрическая фармакология, 2015. – N 1. – С.99-103
7 Приказ Министерства здравоохранения РФ от 21 марта 2017 г. № 124н “Об утверждении порядка и сроков проведения профилактических медицинских осмотров граждан в целях выявления туберкулеза”
Туберкулиновая проба (Манту и Диаскин тест) в Санкт-Петербурге
Туберкулез – хроническая, тяжело протекающая инфекция, возбудителем которой является микобактерия туберкулеза (палочка Коха). Тест на туберкулёз входит в Национальный календарь профилактических прививок, и рекомендован к введению новорожденным (если отсутствуют противопоказания) еще в период пребывания в роддоме. Для закрепления эффекта проводится две плановых ревакцинации, когда ребенку исполняется 7 и 14 лет.
Для закрепления эффекта проводится две плановых ревакцинации, когда ребенку исполняется 7 и 14 лет.
В клинике МЕДИКА используют 2 вида тестирования на туберкулез – проба Манту и Диаскинтест.
Диаскинтест (ДСТ) — это современный тест на туберкулез, результаты которого, в отличие от пробы Манту, не зависят от вакцинации БЦЖ. Положительный ответ на Диаскинтест означает активную фазу туберкулеза, требующую медикаментозного лечения.
Какие обследования должны быть проведены перед постановкой пробы Манту или Диаскинтестом?
- Перед тестом проводится внешний осмотр ребёнка, прослушивание лёгких, осмотр горла, измерение температуры. Врач спрашивает, есть ли у ребёнка жалобы. В медкарте делается запись о проведённом осмотре.
- Накануне и в течение 2-3 суток после прививки не рекомендуется вводить новый прикорм или новые виды пищи. Если ребенок находится на грудном вскармливании – не стоит вводить в рацион питания мамы новые продукты.
 Не нужно употреблять в пищу продукты, часто вызывающие аллергические реакции, — шоколад, клубнику, цитрусовые и др.
Не нужно употреблять в пищу продукты, часто вызывающие аллергические реакции, — шоколад, клубнику, цитрусовые и др. - Рекомендуется искупать ребенка накануне перед прививкой.
Оценка результатов проводится через 72 часа.
Рекомендации после постановки пробы:
Ребенку, которому сделали пробу Манту/Диаскинтест, можно мыть руки, и даже принимать душ и ванну, но при соблюдении некоторых условий:
- Запрещается тереть место укола мочалкой и расчесывать руками.
- Заклеивать место укола пластырем, заматывать пленкой .
- Нельзя мазать место укола кремом, йодом и другими антисептиками.
- Манту нельзя греть.
«ДИАСКИНТЕСТ» — Мамарада
«ДИАСКИНТЕСТ» — аллерген туберкулезный
Препарат для диагностики туберкулеза
Производитель: «Генериум», Россия.
Препарат для диагностики туберкулеза: разработан в 2008 году. Является комплексом рекомбинантных белков CFP-10 и ESAT-6, предназначенных для внутрикожного введения.
Является комплексом рекомбинантных белков CFP-10 и ESAT-6, предназначенных для внутрикожного введения.
Применяется: детям старше 8 лет вместо пробы Манту.
Преимущества диагностики туберкулеза «Диаскинтестом» у детей:
- обладает максимально высокой чувствительностью (98 — 100%)
- обладает максимально высокой специфичностью (90 — 100%)
- большая безопасность и более высокая точность по сравнению с пробой Манту
- более высокая специфичность, чем у импортного аллергена T-Спот
- точная диагностика инфекции, протекающей в скрытой форме
- содержит два антигена, присутствующие в вирулентных штаммах микобактерий туберкулеза и отсутствующие в вакцинном штамме БЦЖ
- при использовании «Диаскинтеста» аллергические реакции практически не возникают
Показания для использования «Диаскинтеста»
«Диаскинтест» используют для проведения внутрикожной пробы у детей старше 8 лет, вместо пробы Манту, с целью диагностики туберкулеза исключительно легочной локализации, проведения оценки активности процесса и выявления пациентов с высоким риском развития активного туберкулезного процесса.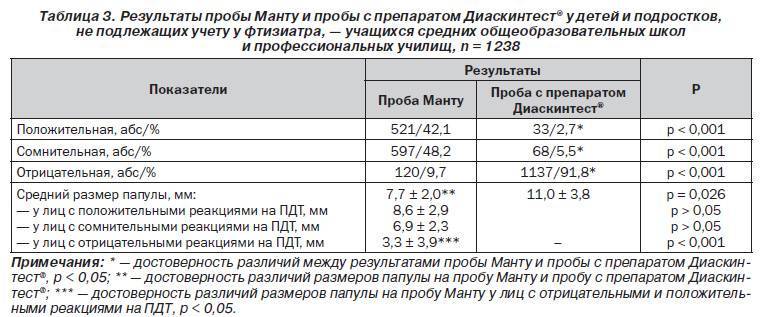 «Диаскинтест» предназначен для постановки внутрикожной пробы со следующими целями:
«Диаскинтест» предназначен для постановки внутрикожной пробы со следующими целями:
- детям из групп высокого риска по заболеванию туберкулезом, не подлежащим диспансерному учету у фтизиатра
- для выявления пациентов с высоким риском развития активного туберкулеза (латентная туберкулeзная инфекция)
- для дифференциальной диагностики поствакцинальной (БЦЖ) и инфекционной аллергии (гиперчувствительности замедленного типа)
- для оценки эффективности противотуберкулезного лечения в сочетании с другими методами
- у пациентов, страдающих сахарным диабетом, язвенной болезнью
- у пациентов с хроническими неспецифическими гнойно-воспалительными заболеваниями бронхолегочной системы и почек
- у ВИЧ-инфицированных пациентов
- у больных, длительно получающих иммуносупрессивную терапию (цитостатики, кортикостероиды, генно-инженерные биологические препараты (ГИБП) и др.)
Принцип действия препарата «Диаскинтест»
Действие препарата «Диаскинтест» основано на выявлении клеточного иммунного ответа на специфические для Mycobacterium tuberculosis антигены. При внутрикожном введении препарата при наличии у лиц с туберкулезной инфекции возникает специфическая кожная реакця, являющаяся проявлением гиперчувствительности замедленного типа.
При внутрикожном введении препарата при наличии у лиц с туберкулезной инфекции возникает специфическая кожная реакця, являющаяся проявлением гиперчувствительности замедленного типа.
Для идентификации (диагностики) туберкулезной инфекции пробу с «Диаскинтест» проводят:
- детям, направленным в противотуберкулезное учреждение для дополнительного обследования на наличие туберкулезного процесса;
- детям, относящимся к группам высокого риска по заболеванию туберкулезом с учетом эпидемиологических, медицинских и социальных факторов риска;
- детям, направленным к фтизиатру по результатам массовой туберкулинодиагностики (Манту).
Важно! Проба с препаратом «Диаскинтест» не может быть использована вместо туберкулинового теста (Манту)для отбора лиц на первичную вакцинацию и ревакцинацию БЦЖ
Оценка результатов пробы с «Диаскинтест»
Результат пробы оценивают врач или обученная медсестра через 72 ч с момента ее проведения путем измерения поперечного (по отношении к оси предплечья) размера гиперемии (покраснения) и инфильтрата (папулы) в миллиметрах прозрачной линейкой.
Гиперемию учитывают только в случае отсутствия инфильтрата.
Ответная реакция на пробу считается:
- отрицательной — при полном отсутствии инфильтрата и гиперемии или при наличии «уколочной реакции» до 2 мм;
- сомнительной — при наличии гиперемии без инфильтрата;
- положительной — при наличии инфильтрата (папулы) любого размера.
Положительные реакции условно различаются по степени выраженности:
- слабо выраженная реакция — при наличии инфильтрата размером до 5 мм;
- умеренно выраженная реакция — при размере инфильтрата 5-9 мм;
- выраженная реакция — при размере инфильтрата 10-14 мм;
- гиперергическая реакция — при размере инфильтрата 15 мм и более, при везикуло-некротических изменениях и (или) лимфангоите, лимфадените независимо от размера инфильтрата.
Лица с сомнительной и положительной реакцией обследуются на туберкулез.
Реакция на Диаскинтест, как правило, отсутствует:
- у лиц, не инфицированных Mycobacterium tuberculosis;
- у лиц, ранее инфицированных Mycobacterium tuberculosis с неактивной туберкулезной инфекцией;
- у больных туберкулезом в период завершения инволюции туберкулезных изменений при отсутствии клинических, рентгено-томографических, инструментальных и лабораторных признаков активности процесса;
- у лиц, излечившихся от туберкулеза;
- у лиц с внелегочной локализацией туберкулеза.

Одновременно проба с препаратом «Диаскинтест» может быть отрицательной у больных туберкулезом с выраженными иммунопатологическими нарушениями, обусловленными тяжелым течением туберкулезного процесса, у лиц на ранних стадиях инфицирования Mycobacterium tuberculosis, на ранних стадиях туберкулезного процесса, у лиц, имеющих сопутствующие заболевания, сопровождающиеся иммунодефицитным состоянием.
Совместимость с другими вакцинами
Здоровым лицам с отрицательным результатом пробы профилактические прививки (кроме БЦЖ) можно проводить непосредственно после оценки и учета результата пробы. Постановку пробы с препаратом «Диаскинтест» следует планировать до проведения профилактических прививок. Если профилактические прививки проведены, то пробу с препаратом осуществляют не ранее, чем через 1 месяц после последней прививки.
Предостережения: применение у беременных и кормящих женщин
Применение препарата возможно только в тех случаях, когда потенциальная польза от результатов пробы для них выше, чем потенциальный вред.
Противопоказания
Только врач может решить, подходит ли «Диаскинтест» для пробы на туберкулез.
Проба «Диаскинтестом» не рекомендуется и не проводится детям в возрасте до 7 лет включительно.
«Диаскинтест» противопоказан лицам с аллергическими и аутоиммунными заболеваниями! Также, применение «Диаскинтеста» противопоказано в следующих случаях:
- Острые заболевания или обострение хронических заболеваний (за исключением случаев, подозрительных на туберкулез).
- Заболевания кожи.
- Эпилепсия.
- В детских коллективах, где имеется карантин по детским инфекциям, проба проводится только после снятия карантина.
Возможные побочные эффекты
У большинства процесс пробы протекает бессимптомно.
Могут наблюдаться головные боли, общая слабость, нарушение сна, повышение температуры тела. У лиц с измененной реактивностью возникают аллергические реакции. Учитывая возможность развития аллергических реакций немедленного типа (анафилактический шок, отек Квинке, крапивница) у особо чувствительных лиц, за привитыми необходимо обеспечить медицинское наблюдение в течение 30 минут.
Учитывая возможность развития аллергических реакций немедленного типа (анафилактический шок, отек Квинке, крапивница) у особо чувствительных лиц, за привитыми необходимо обеспечить медицинское наблюдение в течение 30 минут.
Приходите на прививки в «МАМАРАДА». Полный спектр вакцин для детей и взрослых, семейная вакцинация — по специальной цене!
[Клинические испытания нового кожного теста Диаскинтест для диагностики туберкулеза]
Для скрининговой диагностики туберкулеза и проведения доклинических и клинических испытаний разработан новый реагент для кожной пробы, получивший название Диаскинтест. Доклинические испытания проведены на 315 лабораторных животных (морские свинки, белые мыши). Установлено, что реактив Диаскинтест нетоксичен, не обладает сенсибилизирующими свойствами, безопасен и специфичен, не вызывает положительных реакций у вакцинированных БЦЖ животных и здоровых морских свинок.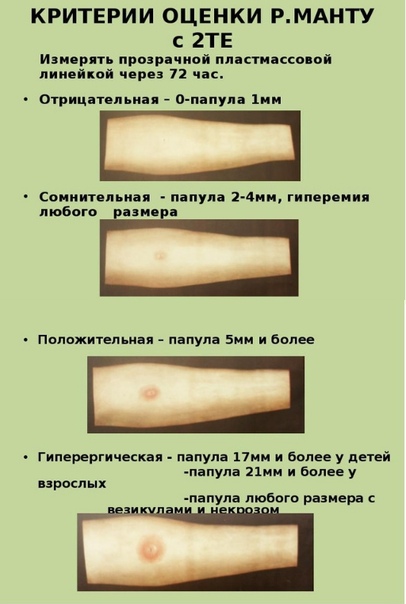 Его удельная активность была сравнима с активностью отечественного эталона — очищенного туберкулина ППД-Л-2. По мере прогрессирования туберкулезного поражения у морских свинок наблюдалась более высокая реакция на диаскинтест в разведении, а у вакцинированных БЦЖ животных реакция на диаскинтест отсутствовала с усилением гиперчувствительности замедленного типа. Клиническое исследование было разрешено Федеральной службой по надзору в сфере здравоохранения и социального развития Российской Федерации. Клинические испытания проводились у 150 человек.Безопасность, специфичность, чувствительность Диаскинтеста впервые изучали в клинических исследованиях и сравнивали его действие с результатами кожной туберкулиновой пробы (проба Манту) с 2 ТЕ ППД Л-2. Установлена высокая чувствительность диаскинтеста при введении в дозе 0,2 мкг в 0,1 мл. У больных активным туберкулезом и новых случаях инфицирования микобактериями туберкулеза возбудитель вызывал положительную кожную реакцию (папула более 10 мм) в 98-100% случаев (p < 0,05).
Его удельная активность была сравнима с активностью отечественного эталона — очищенного туберкулина ППД-Л-2. По мере прогрессирования туберкулезного поражения у морских свинок наблюдалась более высокая реакция на диаскинтест в разведении, а у вакцинированных БЦЖ животных реакция на диаскинтест отсутствовала с усилением гиперчувствительности замедленного типа. Клиническое исследование было разрешено Федеральной службой по надзору в сфере здравоохранения и социального развития Российской Федерации. Клинические испытания проводились у 150 человек.Безопасность, специфичность, чувствительность Диаскинтеста впервые изучали в клинических исследованиях и сравнивали его действие с результатами кожной туберкулиновой пробы (проба Манту) с 2 ТЕ ППД Л-2. Установлена высокая чувствительность диаскинтеста при введении в дозе 0,2 мкг в 0,1 мл. У больных активным туберкулезом и новых случаях инфицирования микобактериями туберкулеза возбудитель вызывал положительную кожную реакцию (папула более 10 мм) в 98-100% случаев (p < 0,05). Агент не вызывал реакции, связанной с вакцинацией БЦЖ.Специфичность теста составила 93-100% при достоверности 95%. Частота избыточных реакций (везикулярно-некротические изменения, лимфангит и лимфаденит) составила 4-14% при достоверности 95%. У больных туберкулезом со значительными иммунопатологическими нарушениями кожная чувствительность к Диаскинтесту может отсутствовать, как и к ППД L-2 (отрицательный тест). Полученные данные обосновывают использование Диаскинтеста при массовых эпидемиологических обследованиях для дифференциальной диагностики туберкулеза и осложнений, связанных с вакцинацией БЦЖ.Препарат также может быть использован для оценки активности процесса у больных туберкулезом и эффективности лечения в сочетании с другими методами и для дифференциальной диагностики туберкулеза.
Агент не вызывал реакции, связанной с вакцинацией БЦЖ.Специфичность теста составила 93-100% при достоверности 95%. Частота избыточных реакций (везикулярно-некротические изменения, лимфангит и лимфаденит) составила 4-14% при достоверности 95%. У больных туберкулезом со значительными иммунопатологическими нарушениями кожная чувствительность к Диаскинтесту может отсутствовать, как и к ППД L-2 (отрицательный тест). Полученные данные обосновывают использование Диаскинтеста при массовых эпидемиологических обследованиях для дифференциальной диагностики туберкулеза и осложнений, связанных с вакцинацией БЦЖ.Препарат также может быть использован для оценки активности процесса у больных туберкулезом и эффективности лечения в сочетании с другими методами и для дифференциальной диагностики туберкулеза.
Диагностическая эффективность новых кожных тестов in vivo на туберкулезную инфекцию по сравнению с туберкулиновыми кожными тестами на основе очищенного белка и анализами высвобождения гамма-интерферона на основе крови in vitro: систематический обзор и метаанализ
Резюме
История вопроса
Новые кожные тесты на туберкулезную инфекцию могут представлять собой подходящую альтернативу существующим тестам; тем не менее, диагностическая эффективность новых тестов по сравнению с кожным тестом очищенного белкового производного туберкулина (TST) или анализом высвобождения интерферона-γ (IGRA) нуждается в систематической оценке.
Методы
В этом систематическом обзоре и метаанализе мы провели поиск в базах данных на английском (Medline OVID), китайском (китайская база данных биомедицинской литературы и национальная инфраструктура знаний Китая) и русском (электронная библиотека) базах данных с момента создания каждой базы данных. до 15 мая 2019 г. (с обновленным поиском в русско-английской базе данных 20 октября 2020 г.) с использованием терминов «ESAT6» ИЛИ «CFP10» И «кожный тест» И «Туберкулез» ИЛИ «C-Tb» ИЛИ «Диаскинтест» . Мы включили исследования, сообщающие о производительности индексных тестов отдельно или по сравнению с компаратором.Критерии включения варьировались в зависимости от целей обзора и результатов работы, но во всех исследованиях требовалось сообщать о пороговых значениях теста для положительности, применяемых к исследуемой популяции. Мы использовали иерархию эталонных стандартов для туберкулезной инфекции, соответствующую системе ВОЗ 2020 г., для оценки эффективности диагностики. Два автора независимо рецензировали названия и рефераты для англо-китайских (LF и MK) и русских исследований (MK и VN). Качество исследования оценивали с помощью QUADAS-2.Совокупные оценки случайных эффектов представлены, когда это необходимо для общей доли согласия, чувствительности в микробиологически подтвержденном туберкулезе и специфичности в когортах с низким риском заражения туберкулезом. Это исследование зарегистрировано в PROSPERO, CRD42019135572.
Два автора независимо рецензировали названия и рефераты для англо-китайских (LF и MK) и русских исследований (MK и VN). Качество исследования оценивали с помощью QUADAS-2.Совокупные оценки случайных эффектов представлены, когда это необходимо для общей доли согласия, чувствительности в микробиологически подтвержденном туберкулезе и специфичности в когортах с низким риском заражения туберкулезом. Это исследование зарегистрировано в PROSPERO, CRD42019135572.
Находки
Нами выявлено 1466 оригинальных статей, из которых 37 (2,5%) исследований, включающих 10 915 человек (7111 Диаскинтест, 2744 C-Tb, 887 КЭ, 173 DPPD), были включены в качественный анализ (29 [78%] исследований Диаскинтеста, пять [15%] исследований C-Tb, два [5%] исследования ЭК-скинтеста и одно [3%] исследования ДППД).В количественный анализ включено 22 (1,5%) исследования, включающих 5810 человек (3143 Диаскинтест, 2129 C-Tb, 538 КЭ-скинтест): 15 (68%) Диаскинтест, 5 (23%) C-Tb, и два (9%) ЭК-скинтеста. Тестируемые подгруппы включали лиц с ВИЧ, детей (0–18 лет) и лиц, подвергшихся воздействию туберкулеза. Исследования были неоднородными с умеренным или высоким риском систематической ошибки. Девять непосредственных исследований индексного теста по сравнению с TST и IGRA позволили провести прямое сравнение и объединение. В смешанной когорте людей с туберкулезом и без туберкулеза суммарная согласованность Диаскинтеста с IGRA составила 87,16% (95% ДИ 79,47–92,24) и 55,45% (46,08–64,45) с ТКП. Отрез 5 мм (TST 5 мм ).Чувствительность диаскинтеста составила 91,18 % (95 % ДИ 81,72–95,98) по сравнению с 88,24 % (78,20–94,01) для ТСТ 5 мм , 89,66 (78,83–95 ·28) для IGRA QuantiFERON и 90,91% (79,95–96,16) для ЦПОТ.ТБ. Согласованность C-Tb с IGRA у лиц с активным туберкулезом составила 79,80% (95% ДИ 76,10–83,07) по сравнению с 78,92% (74,65–82,63) для TST5 мм/15 мм разреза. -выкл. (TST 5 мм/15 мм ). TST 5/15 мм отражает пороговое значение в когортах, в которых применялись стратифицированные пороговые значения: 5 мм для ВИЧ-инфицированных, лиц с ослабленным иммунитетом или лиц, ранее не получавших БЦЖ, и 15 мм для иммунокомпетентных лиц, вакцинированных БЦЖ.
Исследования были неоднородными с умеренным или высоким риском систематической ошибки. Девять непосредственных исследований индексного теста по сравнению с TST и IGRA позволили провести прямое сравнение и объединение. В смешанной когорте людей с туберкулезом и без туберкулеза суммарная согласованность Диаскинтеста с IGRA составила 87,16% (95% ДИ 79,47–92,24) и 55,45% (46,08–64,45) с ТКП. Отрез 5 мм (TST 5 мм ).Чувствительность диаскинтеста составила 91,18 % (95 % ДИ 81,72–95,98) по сравнению с 88,24 % (78,20–94,01) для ТСТ 5 мм , 89,66 (78,83–95 ·28) для IGRA QuantiFERON и 90,91% (79,95–96,16) для ЦПОТ.ТБ. Согласованность C-Tb с IGRA у лиц с активным туберкулезом составила 79,80% (95% ДИ 76,10–83,07) по сравнению с 78,92% (74,65–82,63) для TST5 мм/15 мм разреза. -выкл. (TST 5 мм/15 мм ). TST 5/15 мм отражает пороговое значение в когортах, в которых применялись стратифицированные пороговые значения: 5 мм для ВИЧ-инфицированных, лиц с ослабленным иммунитетом или лиц, ранее не получавших БЦЖ, и 15 мм для иммунокомпетентных лиц, вакцинированных БЦЖ. Чувствительность C-Tb составила 74,52% (95% ДИ 70,39–78,25) по сравнению с чувствительностью 78,18% (67,75–85,94) для TST 5 мм/15 мм , и 71,67% (63,44–78,68) для IGRA. Специфичность составила 97,85% (95% ДИ 93,96–99,25) для C-Tb по сравнению с 93,31% (90,22–95,48) для TST 15 мм отсечки и 99,15% (79 ·66–99·97) для ИГРА. Чувствительность ЭК-кожного теста составила 86,06% (95% ДИ 82,39–89,07).
Чувствительность C-Tb составила 74,52% (95% ДИ 70,39–78,25) по сравнению с чувствительностью 78,18% (67,75–85,94) для TST 5 мм/15 мм , и 71,67% (63,44–78,68) для IGRA. Специфичность составила 97,85% (95% ДИ 93,96–99,25) для C-Tb по сравнению с 93,31% (90,22–95,48) для TST 15 мм отсечки и 99,15% (79 ·66–99·97) для ИГРА. Чувствительность ЭК-кожного теста составила 86,06% (95% ДИ 82,39–89,07).
Интерпретация
Новые кожные тесты на туберкулезную инфекцию, по-видимому, работают так же, как IGRA или ТКП; однако качество исследования варьировалось.Оценка эффективности теста, результатов, важных для пациента, и диагностического использования в текущих клинических алгоритмах будет способствовать внедрению в ключевых группах населения.
Финансирование
StopTB (Рабочая группа по новой диагностике) и FIND.
Переводы
Переводы реферата на китайский и русский языки см. в разделе «Дополнительные материалы».
Сравнение внутрикожной пробы с рекомбинантным аллергеном туберкулеза (диаскинтест) с другими иммунологическими тестами в диагностике туберкулезной инфекции
Сравнение внутрикожного теста с рекомбинантным аллергеном туберкулеза (диаскинтест) с другими иммунологическими тестами в диагностике туберкулезной инфекции – DOAJ Международный журнал микобактериологии
(январь 2018 г.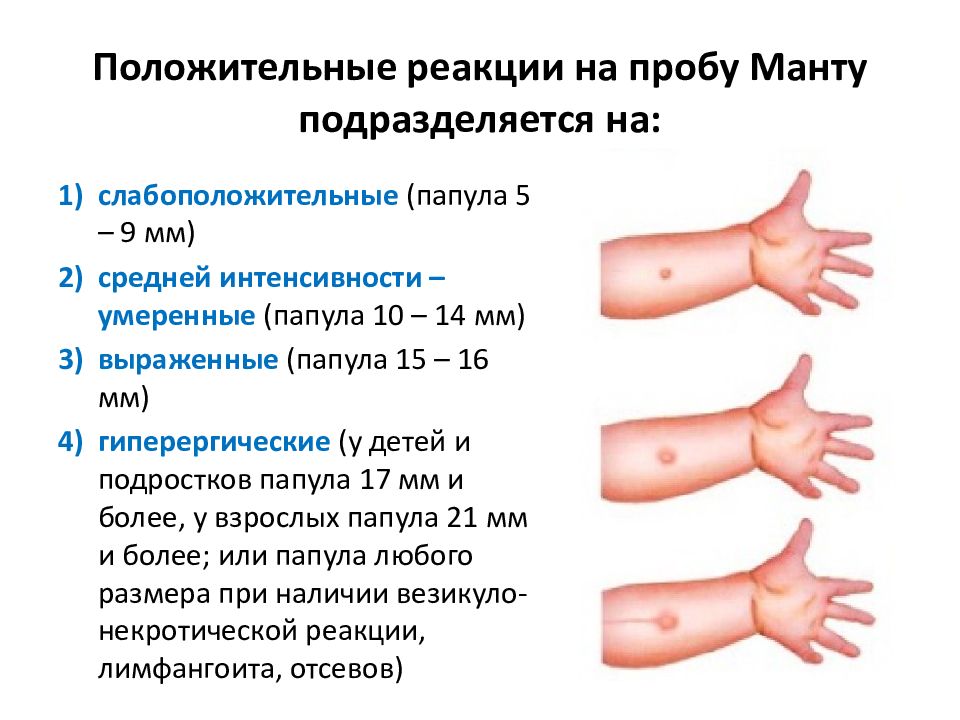 )
)
- Анна Старшинова,
- Вячеслав Журавлев,
- Ирина Довгалюк,
- Александр Пантелеев,
- Вера Манина,
- Юлия Зинченко,
- Евгения Истомина,
- Мария Павлова,
- Петр Яблонский
Принадлежности
- Анна Старшинова
- Вячеслав Журавлев
- Ирина Довгалюк
- Александр Пантелеев
- Вера Манина
- Юлия Зинченко
- Евгения Истомина
- Мария Павлова
- Петр Яблонский
- ДОИ
- https://дои.
 org/10.4103/ijmy.ijmy_17_18
org/10.4103/ijmy.ijmy_17_18 - Том журнала и выпуск
- Том. 7,
нет. 1
стр. 32 – 39
Аннотация
Читать онлайн
Исходная информация: Стратегия ВОЗ по ликвидации туберкулеза (ТБ) к 2035 г. (Стратегия по ликвидации туберкулеза) направлена на раннюю и точную диагностику и последующее эффективное лечение больных туберкулезом.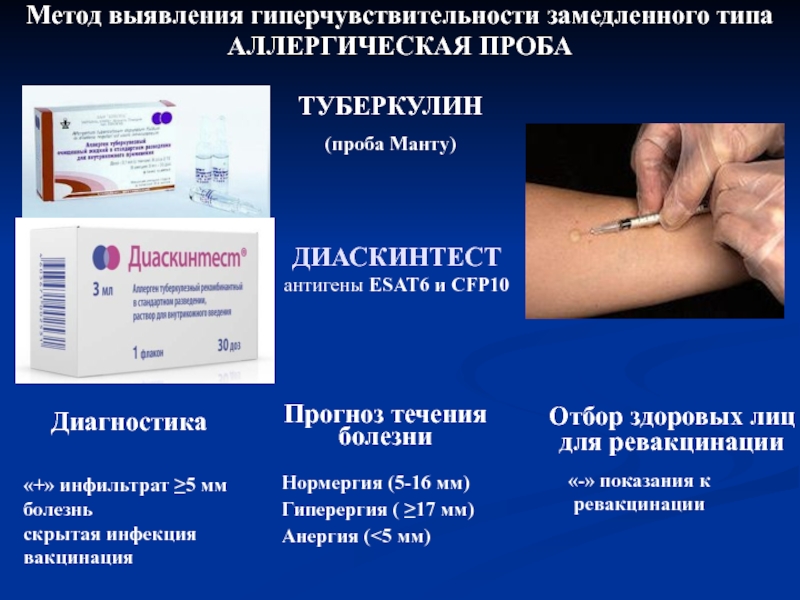 В настоящее время не существует золотого стандарта диагностики латентной туберкулезной инфекции. В этом исследовании оценивались диагностические возможности нового внутрикожного теста с использованием рекомбинантного аллергена ТБ (Диаскинтест) по сравнению с кожным туберкулиновым тестом (ТКП) и коммерческими анализами высвобождения гамма-интерферона ТБ (IGRA). Методы: ретроспективный анализ данных, включавший обследование 860 ВИЧ-отрицательных, вакцинированных бациллой Кальметта-Герена (БЦЖ) лиц в возрасте от 1 года до 65 лет, посетивших противотуберкулезные учреждения Санкт-Петербурга для исключения или подтверждения активного ТБ. велась с 2011 по 2016 год.Результаты. В обследованной детской популяции (n = 696) отмечена высокая степень согласованности результатов диаскинтеста с результатами иммуноферментного теста и QuantiFERON-TB Gold In-Tube test (ELISPOT и QFT) с пороговым значением диаскинтеста ≥ 5 мм: индексы консистенции каппа составили 1,000 и 0,937 для ELISPOT и QFT соответственно.
В настоящее время не существует золотого стандарта диагностики латентной туберкулезной инфекции. В этом исследовании оценивались диагностические возможности нового внутрикожного теста с использованием рекомбинантного аллергена ТБ (Диаскинтест) по сравнению с кожным туберкулиновым тестом (ТКП) и коммерческими анализами высвобождения гамма-интерферона ТБ (IGRA). Методы: ретроспективный анализ данных, включавший обследование 860 ВИЧ-отрицательных, вакцинированных бациллой Кальметта-Герена (БЦЖ) лиц в возрасте от 1 года до 65 лет, посетивших противотуберкулезные учреждения Санкт-Петербурга для исключения или подтверждения активного ТБ. велась с 2011 по 2016 год.Результаты. В обследованной детской популяции (n = 696) отмечена высокая степень согласованности результатов диаскинтеста с результатами иммуноферментного теста и QuantiFERON-TB Gold In-Tube test (ELISPOT и QFT) с пороговым значением диаскинтеста ≥ 5 мм: индексы консистенции каппа составили 1,000 и 0,937 для ELISPOT и QFT соответственно.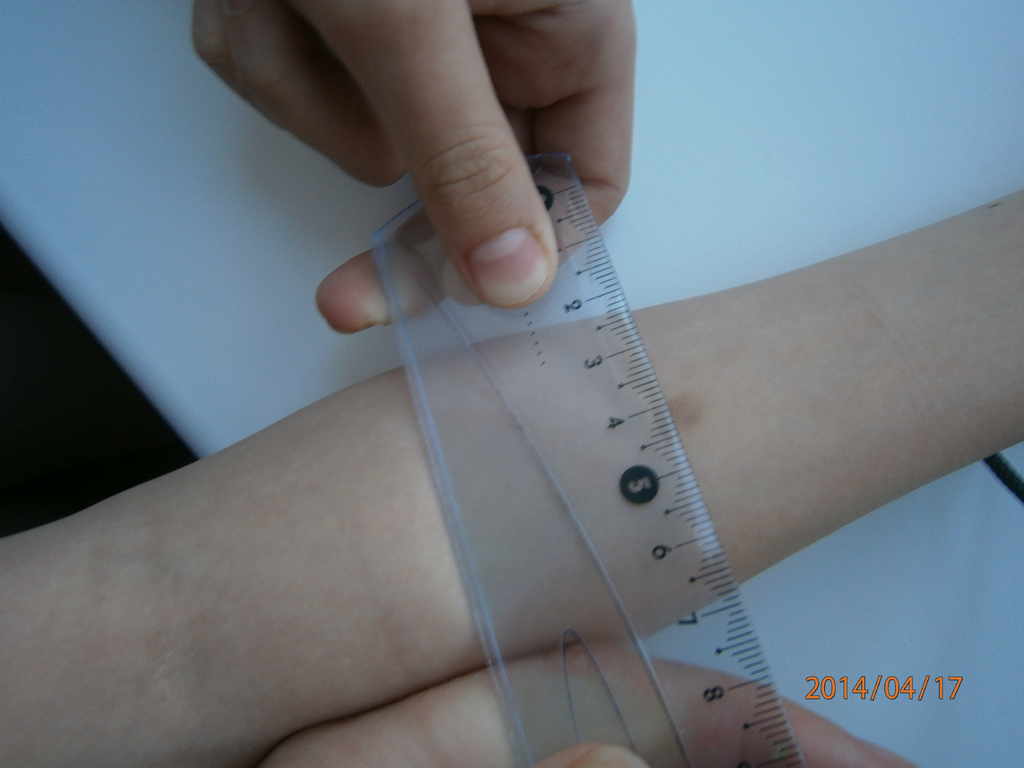 Высокая чувствительность диаскинтеста, сравнимая с тестами IGRA, отмечена у больных с подтвержденным диагнозом туберкулеза во всех возрастных группах. Чувствительность Диаскинтеста у больных группы ТБ/МТБ+ в возрасте 18 лет и старше составила 88.7%; ЭЛИСПОТ, 90,6%; QFT, 87,0%. Проведенный анализ показал высокую конкордантность результатов коммерческих ТБ-тестов у взрослых ВИЧ-негативных пациентов (n = 164) с порогом Диаскинтеста ≥5 мм: каппа-индексы составили 0,805 и 0,636 (Диаскинтест против ELISPOT и QFT соответственно). ) среди привитых БЦЖ. Заключение. Согласно рекомендациям ВОЗ, замена ТКП тестами IGRA не рекомендуется в качестве меры общественного здравоохранения в условиях ограниченных ресурсов, поскольку тесты IGRA являются более дорогостоящими и технически сложными для проведения, чем ТКП.Диаскинтест по сложности сравним с ТКП, а его эффективность близка к эффективности IGRA в популяции, вакцинированной БЦЖ. Таким образом, наше исследование показывает, что замена ТКП диаскинтестом может быть рекомендована в качестве меры общественного здравоохранения в условиях ограниченных ресурсов и всеобщей вакцинации БЦЖ.
Высокая чувствительность диаскинтеста, сравнимая с тестами IGRA, отмечена у больных с подтвержденным диагнозом туберкулеза во всех возрастных группах. Чувствительность Диаскинтеста у больных группы ТБ/МТБ+ в возрасте 18 лет и старше составила 88.7%; ЭЛИСПОТ, 90,6%; QFT, 87,0%. Проведенный анализ показал высокую конкордантность результатов коммерческих ТБ-тестов у взрослых ВИЧ-негативных пациентов (n = 164) с порогом Диаскинтеста ≥5 мм: каппа-индексы составили 0,805 и 0,636 (Диаскинтест против ELISPOT и QFT соответственно). ) среди привитых БЦЖ. Заключение. Согласно рекомендациям ВОЗ, замена ТКП тестами IGRA не рекомендуется в качестве меры общественного здравоохранения в условиях ограниченных ресурсов, поскольку тесты IGRA являются более дорогостоящими и технически сложными для проведения, чем ТКП.Диаскинтест по сложности сравним с ТКП, а его эффективность близка к эффективности IGRA в популяции, вакцинированной БЦЖ. Таким образом, наше исследование показывает, что замена ТКП диаскинтестом может быть рекомендована в качестве меры общественного здравоохранения в условиях ограниченных ресурсов и всеобщей вакцинации БЦЖ.
Ключевые слова
Опубликовано в
International Journal of Mycobacteriology- ISSN
- 2212-5531 (печать)
- 2212-554X (онлайн)
- Издатель
- Публикации Wolters Kluwer Medknow
- Страна издателя
- Индия
- Субъекты LCC
- Наука: микробиология
- Веб-сайт
- http://www.
 ijmyco.org
ijmyco.org
О журнале
QR-код WeChat
Закрывать
Сравнительная чувствительность теста с рекомбинантным туберкулезным аллергеном, содержащим белок ESAT6-CFP10, и пробы Манту с 2 ТЕ ППД-Л у детей и подростков с впервые выявленным туберкулезом в Москве
История вопроса
Группой российских ученых разработан Диаскинтест, содержит Mycobacterium tuberculosis , специфичные рекомбинантные белки CFP10-ESAT6, для кожных тестов (0.2 мкг/0,1 мл).
Цель исследования
Оценить сравнительную чувствительность ТКП с 2 ТЕ ППД-Л и кожной пробы с туберкулезным рекомбинантным аллергеном (Диаскинтест), содержащим белок ESAT6-CFP10, у детей и подростков с впервые выявленным активным туберкулезом при проведении массового обследования в первичная медицинская помощь в москве.
Материалы и методы
Исследование представляло собой комплексное ретроспективное групповое исследование детей и подростков с диагнозом активный туберкулез в Москве в 2013–2016 гг. в возрасте от 0 до 17 лет включительно.
Результаты
Из 441 больного, отобранного для анализа, у 408 пациентов были проведены оба теста (ТКП с 2 ТЕ ППД-Л и Диаскинтест), у 193 пациентов оба теста были проведены одновременно, из них 162 пациента вакцинированы БЦЖ. Сравнительные результаты обоих тестов у 408 больных туберкулезом: при отсечке ≥ 5 мм оба теста имеют одинаковую чувствительность: Диаскинтест 98,3% (95% ДИ 97,0–99,6%), ТКП 98,0% (95% ДИ 96,7–99,4%) , при отсечке ≥10 мм чувствительность снижается для обоих тестов: Диаскинтест 90.0% (95% ДИ 87,0–93,0%), ТКП 88,7% (95% ДИ 85,6–91,9%), но при отсечке ≥ 15 мм снижение чувствительности статистически значимо: для диаскинтеста 61,5% (95% ДИ 56,7–66,3%), а для ТКП 46,3% (95% ДИ 41,4–51,3%), p
Результаты одновременной постановки проб на разных руках у 193 человек (в том числе 162 вакцинированных БЦЖ), не отличаются от результаты для 408 человек.
Корреляция между результатами Диаскинтеста и ТКП была достоверной во всех группах.
Заключение
У детей и подростков с активным туберкулезом Диаскинтест 0.2 мкг/мл и проба Манту с 2 ТЕ ППД-Л имеют высокую чувствительность (98%) при отсечке 5 мм; однако при отсечке ≥ 15 мм чувствительность значительно снижается, причем снижение более выражено в пробе Манту. Преимущество Диаскинтеста в том, что в отличие от пробы Манту он обладает высокой специфичностью в условиях массовой вакцинации БЦЖ. Тест прост в проведении и может использоваться при массовом скрининге.
Кожные тесты для выявления микобактериальных инфекций: достижения, текущие перспективы и последствия для других заболеваний
Алшукаири А.Н., Халид И., Ахмед В.А., Дада А.М., Баюми Д.Т., Малик Л.С., Алтавади С., Игнасио К., Алсалми Х.С. , Al-Abdely HM, Wali GY, Qushmaq IA, Alraddadi BM, Perlman S (2016) Реакция антител и тяжесть заболевания у медицинских работников, переживших MERS.Emerg Infect Dis 22 (6). https://doi.org/10.3201/eid2206.160010
https://doi.org/10.3201/eid2206.160010
Arenas Miras Mdel M, Hidalgo Tenorio C, Jimenez Alonso J (2013) Туберкулез у пациентов с системной красной волчанкой: ситуация в Испании. Реуматол Клин 9(6):369-372. https://doi.org/10.1016/j.reuma.2012.06.011
Статья пабмед Google Scholar
Ариас Гильен М. (2011) Достижения в диагностике туберкулезной инфекции. Арка Бронконеумол 47 (10): 521–530.https://doi.org/10.1016/j.arbres.2011.06.018
Статья пабмед Google Scholar
Badaro R, Machado BAS, Duthie MS, Araujo-Neto CA, Pedral-Sampaio D, Nakatani M, Reed SG (2020) Единственный рекомбинантный белок M. инфицированных больных туберкулезом. АМБ Экспресс 10(1):133. https://doi.org/10.1186/s13568-020-01068-6
CAS Статья пабмед ПабМед Центральный Google Scholar
Bass JB Jr (2003) Насколько хорош туберкулиновый кожный тест? Infect Control Hosp Epidemiol 24(11):797–798. https://doi.org/10.1086/502138
https://doi.org/10.1086/502138
Статья пабмед Google Scholar
Беме К.С., Никол М.П., Набета П., Майкл Дж.С., Готуццо Э., Тахирли Р., Глер М.Т., Блейкмор Р., Вородриа В., Грей К., Хуанг Л., Касерес Т., Мехдиев Р., Рэймонд Л., Уайтлоу А., Сагадеван K, Alexander H, Albert H, Cobelens F, Cox H, Alland D, Perkins MD (2011)Осуществимость, диагностическая точность и эффективность децентрализованного использования теста Xpert MTB/RIF для диагностики туберкулеза и множественной лекарственной устойчивости: многоцентровое внедрение учиться.Ланцет 377 (9776): 1495–1505. https://doi.org/10.1016/S0140-6736(11)60438-8
Статья пабмед ПабМед Центральный Google Scholar
Borsuk S, Newcombe J, Mendum TA, Dellagostin OA, McFadden J (2009) Идентификация белков из очищенного туберкулином белкового производного (PPD) с помощью ЖХ-МС/МС. Туберкулез (Эдинб) 89(6):423–430. https://doi.org/10.1016/j.tube.2009.07.003
https://doi.org/10.1016/j.tube.2009.07.003
CAS Статья Google Scholar
Кэллоу К.А., Парри Х.Ф., сержант М., Тиррелл Д.А. (1990)Временной ход иммунного ответа на экспериментальную коронавирусную инфекцию человека.Epidemiol Infect 105(2):435–446. https://doi.org/10.1017/s0950268800048019
CAS Статья пабмед ПабМед Центральный Google Scholar
Campos-Neto A, Rodrigues-Junior V, Pedral-Sampaio DB, Netto EM, Ovendale PJ, Coler RN, Skeiky YA, Badaro R, Reed SG (2001) Evaluation of DPPD, single recombinant Mycobacterium tuberculosis белок как альтернативный антиген для пробы Манту. Туберкулез (Эдинб) 81(5-6):353–358
CAS Статья Google Scholar
CDC (2013a) Масштабы и последствия периодической нехватки растворов антигенов для туберкулиновых кожных тестов на основе очищенного белка – США, 2013 г. MMWR Morb Mortal Wkly Rep 62(49):1014–1015
MMWR Morb Mortal Wkly Rep 62(49):1014–1015
Google Scholar
CDC (2013b) Нехватка туберкулиновых продуктов на основе очищенного белка в стране. MMWR Morb Mortal Wkly Rep 62(16):312
Google Scholar
CDC (2020) Отдел стратегического плана ликвидации туберкулеза на 2016-2020 гг. По состоянию на 23 августа 2020 г.
Чо Ю.С., Добос К.М., Пренни Дж., Ян Х., Гесс А., Розенкрандс И., Андерсен П., Рю С.В., Бай Г.Х., Бреннан М.Дж., Иззо А., Билефельдт-Оманн Х., Белисл Дж.Т. (2012 ) Расшифровка протеома диагностического реагента in vivo «очищенное белковое производное» микобактерий туберкулеза.Протеомика 12(7):979–991. https://doi.org/10.1002/pmic.201100544
CAS Статья пабмед ПабМед Центральный Google Scholar
Coler RN, Skeiky YA, Ovendale PJ, Vedvick TS, Gervassi L, Guderian J, Jen S, Reed SG, Campos-Neto A (2000) Клонирование гена Mycobacterium tuberculosis , кодирующего очищенный белковый производный белок, который вызывает сильную туберкулёзную специфическую гиперчувствительность замедленного типа. J Infect Dis 182 (1): 224–233.https://doi.org/10.1086/315677
J Infect Dis 182 (1): 224–233.https://doi.org/10.1086/315677
CAS Статья пабмед Google Scholar
Comstock GW, Edwards LB, Philip RN, Winn WA (1964) Сравнение в Соединенных Штатах Америки двух туберкулинов, Ppd-S и Rt 23. Bull World Health Organ 31:161–170
CAS пабмед ПабМед Центральный Google Scholar
Convit J, Sampson C, Zuniga M, Smith PG, Plata J, Silva J, Molina J, Pinardi ME, Bloom BR, Salgado A (1992) Иммунопрофилактическое исследование комбинированной вакцины против лепры Mycobacterium leprae /БЦЖ: предварительные результаты.Ланцет 339(8791):446–450
CAS Статья Google Scholar
Дхармендра (2012) Иммунологические кожные тесты при проказе. Часть I. Выделение белкового антигена Mycobacterium leprae . 1942. Indian J Med Res 136(3):7p после 502
CAS пабмед Google Scholar
Farhat M, Greenaway C, Pai M, Menzies D (2006) Ложноположительные туберкулиновые кожные пробы: каков абсолютный эффект БЦЖ и нетуберкулезных микобактерий? Int J Tuberc Lung Dis 10(11):1192–1204
CAS пабмед Google Scholar
Getahun H, Matteelli A, Chaisson RE, Raviglione M (2015) Латентная инфекция Mycobacterium tuberculosis . N Engl J Med 372 (22): 2127–2135. https://doi.org/10.1056/NEJMra1405427
N Engl J Med 372 (22): 2127–2135. https://doi.org/10.1056/NEJMra1405427
CAS Статья пабмед Google Scholar
Гилленуотер К.А., Сапп С.К., Пирс К., Сиберри Г.К. (2006 г.) Увеличение конверсии туберкулиновых кожных тестов среди медицинских работников после перехода с туберсола на аплисол. Am J Infect Control 34 (10): 651–654. https://doi.org/10.1016/j.ajic.2006.05.288
Статья пабмед Google Scholar
Goldstein S, Perlman DC, Salomon N (1994)Двухэтапный туберкулиновый кожный тест у ВИЧ-инфицированных: предварительный отчет.Гора Синай J Med 61 (4): 337–340
CAS пабмед Google Scholar
Грэм Н.М., Нельсон К.Е., Соломон Л., Бондс М., Риццо Р.Т., Скавотто Дж., Астемборски Дж., Влахов Д. (1992) Распространенность туберкулиновой положительности и анергии кожных проб у ВИЧ-1-серопозитивных и -серонегативных потребителей внутривенных наркотиков . JAMA 267(3):369–373
JAMA 267(3):369–373
CAS Статья Google Scholar
Guld J, Bentzon MW, Bleiker MA, Griep WA, Magnusson M, Waaler H (1958) Стандартизация новой партии очищенного туберкулина (PPD), предназначенного для международного использования.Bull World Health Organ 19(5):845–951
CAS пабмед ПабМед Центральный Google Scholar
Houben RM, Dodd PJ (2016)Глобальное бремя латентной туберкулезной инфекции: переоценка с использованием математического моделирования. PLoS Med 13(10):e1002152. https://doi.org/10.1371/journal.pmed.1002152
Статья пабмед ПабМед Центральный Google Scholar
Huebner RE, Schein MF, Bass JB Jr (1993) Туберкулиновая кожная проба.Clin Infect Dis 17(6):968–975
CAS Статья Google Scholar
Ибаррондо Ф. Дж., Фулчер Дж.А., Гудман-Меза Д., Эллиотт Дж., Хофманн С., Хауснер М.А., Фербас К.Г., Тобин Н.Х., Альдрованди Г.М., Ян О.О. (2020) Быстрый распад антител против SARS-CoV-2 в человек с легкой формой Covid-19. N Engl J Med 383: 1085–1087. https://doi.org/10.1056/NEJMc2025179
Дж., Фулчер Дж.А., Гудман-Меза Д., Эллиотт Дж., Хофманн С., Хауснер М.А., Фербас К.Г., Тобин Н.Х., Альдрованди Г.М., Ян О.О. (2020) Быстрый распад антител против SARS-CoV-2 в человек с легкой формой Covid-19. N Engl J Med 383: 1085–1087. https://doi.org/10.1056/NEJMc2025179
Статья пабмед Google Scholar
Jensen PA, Lambert LA, Iademarco MF, Ridzon R, Cdc (2005) Руководство по предотвращению передачи Mycobacterium tuberculosis в медицинских учреждениях, 2005.MMWR Recomm Rep 54 (RR-17): 1–141
PubMed Google Scholar
Johnson MP, Coberly JS, Clermont HC, Chaisson RE, Davis HL, Losikoff P, Ruff AJ, Boulos R, Halsey NA (1992) Реактивность туберкулинового кожного теста среди взрослых, инфицированных вирусом иммунодефицита человека. J Infect Dis 166(1):194–198
CAS Статья Google Scholar
Kimura M, Comstock GW, Mori T (2005) Сравнение эритемы и уплотнения по результатам туберкулиновых тестов. Int J Tuberc Lung Dis 9(8):853–857
Int J Tuberc Lung Dis 9(8):853–857
CAS пабмед Google Scholar
Landi S, Held HR (1980) Приготовление и характеристика большой партии очищенного от туберкулина белкового производного (PPD-CT68). Энн Склаво 22 (6): 899–907
CAS пабмед Google Scholar
Lifson AR, Watters JK, Thompson S, Crane CM, Wise F (1993) Расхождения в результатах туберкулиновых кожных проб с двумя коммерческими продуктами у группы внутривенных наркоманов.J Infect Dis 168(4):1048–1051
CAS Статья Google Scholar
Liu C, Flamoe E, Chen HJ, Carter D, Reed SG, Campos-Neto A (2004) Экспрессия и очистка иммунологически реактивного DPPD, рекомбинантного Mycobacterium tuberculosis кожного антигена, с использованием Mycobacterium smegmatis и Escherichia coli клетки-хозяева. Can J Microbiol 50(2):97–105
CAS Статья Google Scholar
Длинный QX, Лю Б. З., Дэн Х.Дж., Ву Г.К., Дэн К., Чен Ю.К., Ляо П., Цю Д.Ф., Линь И., Цай С.Ф., Ван Д.К., Ху И., Рен Д.Х., Тан Н., Сюй Ю.Ю., Ю. LH, Mo Z, Gong F, Zhang XL, Tian WG, Hu L, Zhang XX, Xiang JL, Du HX, Liu HW, Lang CH, Luo XH, Wu SB, Cui XP, Zhou Z, Zhu MM, Wang J, Xue CJ, Li XF, Wang L, Li ZJ, Wang K, Niu CC, Yang QJ, Tang XJ, Zhang Y, Liu XM, Li JJ, Zhang DC, Zhang F, Liu P, Yuan J, Li Q, Hu JL , Chen J, Huang AL (2020) Реакция антител на SARS-CoV-2 у пациентов с COVID-19.Nat Med 26 (6): 845–848. https://doi.org/10.1038/s41591-020-0897-1
З., Дэн Х.Дж., Ву Г.К., Дэн К., Чен Ю.К., Ляо П., Цю Д.Ф., Линь И., Цай С.Ф., Ван Д.К., Ху И., Рен Д.Х., Тан Н., Сюй Ю.Ю., Ю. LH, Mo Z, Gong F, Zhang XL, Tian WG, Hu L, Zhang XX, Xiang JL, Du HX, Liu HW, Lang CH, Luo XH, Wu SB, Cui XP, Zhou Z, Zhu MM, Wang J, Xue CJ, Li XF, Wang L, Li ZJ, Wang K, Niu CC, Yang QJ, Tang XJ, Zhang Y, Liu XM, Li JJ, Zhang DC, Zhang F, Liu P, Yuan J, Li Q, Hu JL , Chen J, Huang AL (2020) Реакция антител на SARS-CoV-2 у пациентов с COVID-19.Nat Med 26 (6): 845–848. https://doi.org/10.1038/s41591-020-0897-1
CAS Статья пабмед ПабМед Центральный Google Scholar
Лоннрот К., Равильоне М. (2016 г.) Новая стратегия ВОЗ по ликвидации туберкулеза в период после 2015 г. в эпоху целей устойчивого развития. Trans R Soc Trop Med Hyg 110 (3): 148–150. https://doi.org/10.1093/trstmh/trv108
Статья пабмед ПабМед Центральный Google Scholar
Magill A (2013) Тропическая медицина охотника и возникающие инфекционные заболевания: 99 — Лейшманиоз, 9-е изд. Elsevier
Elsevier
Мамани М., Майзооби М.М., Торабян С., Михан Р., Ализаде К. (2013) Латентный и активный туберкулез: оценка потребителей инъекционных наркотиков. Медицинский центр Красного Полумесяца Ирана J 15(9):775–779. https://doi.org/10.5812/ircmj.6283
Статья пабмед ПабМед Центральный Google Scholar
Маркес М.А., Невес-Феррейра А.Г., да Силвейра Э.К., Валенте Р.Х., Шапоурож А., Пералес Дж., да Силва Бернардес Р., Добос К.М., Спенсер Дж.С., Бреннан П.Дж., Пессолани М.К. (2008) Расшифровка протеомного профиля Оболочка клеток Mycobacterium leprae .Протеомика 8(12):2477–2491. https://doi.org/10.1002/pmic.200700971
CAS Статья пабмед Google Scholar
Mehta SR, MacGruder C, Looney D, Johns S, Smith DM (2009) Различия в реактивности туберкулина, определенные в программе проверки здоровья сотрудников администрации ветеранов. Clin Vaccine Immunol 16(4):541–543. https://doi.org/10.1128/CVI.00375-08
Clin Vaccine Immunol 16(4):541–543. https://doi.org/10.1128/CVI.00375-08
CAS Статья пабмед ПабМед Центральный Google Scholar
Meyers WM, Kvernes S, Binford CH (1975) Сравнение реакций на лепромины человека и броненосца при проказе.Int J Lepr Other Mycobact Dis 43(3):218–225
CAS пабмед Google Scholar
Millar JW, Gannon C, Chan CS (1975) Сравнение реакций Fernandex и Mitsuda у больных проказой с использованием антигенов человека и броненосца. Двойное слепое исследование. Int J Lepr Other Mycobact Dis 43(3):226–233
CAS пабмед Google Scholar
Morrison J, Pai M, Hopewell PC (2008) Туберкулез и латентная туберкулезная инфекция у лиц, тесно контактировавших с больными туберкулезом легких в странах с низким и средним уровнем дохода: систематический обзор и метаанализ. Ланцет Infect Dis 8 (6): 359–368. https://doi.org/10.1016/S1473-3099(08)70071-9
Ланцет Infect Dis 8 (6): 359–368. https://doi.org/10.1016/S1473-3099(08)70071-9
Статья пабмед Google Scholar
Nicol MP, Workman L, Isaacs W, Munro J, Black F, Eley B, Boehme CC, Zemanay W, Zar HJ (2011) Точность теста Xpert MTB/RIF для диагностики туберкулеза легких у госпитализированных детей в больницу в Кейптауне, Южная Африка: описательное исследование. Ланцет Infect Dis 11 (11): 819–824. https://doi.org/10.1016/S1473-3099(11)70167-0
Артикул пабмед ПабМед Центральный Google Scholar
Owusu-Edusei K Jr, Winston CA, Marks SM, Langer AJ, Miramontes R (2017) Использование тестов на туберкулез и медицинские расходы по данным амбулаторных страховых случаев, 2013. Tuberc Res Treat 2017: 3816432–3816439. https://doi.org/10.1155/2017/3816432
Статья пабмед ПабМед Центральный Google Scholar
Pai M, Denkinger CM, Kik SV, Rangaka MX, Zwerling A, Oxlade O, Metcalfe JZ, Cattamanchi A, Dowdy DW, Dheda K, Banaei N (2014) Анализы высвобождения гамма-интерферона для обнаружения Mycobacterium tuberculosis инфекционное заболевание. Clin Microbiol Rev 27 (1): 3–20. https://doi.org/10.1128/CMR.00034-13
Clin Microbiol Rev 27 (1): 3–20. https://doi.org/10.1128/CMR.00034-13
CAS Статья пабмед ПабМед Центральный Google Scholar
Pai M, Behr MA, Dowdy D, Dheda K, Divangahi M, Boehme CC, Ginsberg A, Swaminathan S, Spigelman M, Getahun H, Menzies D, Raviglione M (2016) Туберкулез. Nat Rev Dis Primers 2:16076. https://doi.org/10.1038/nrdp.2016.76
Статья пабмед Google Scholar
Рангака М.Х., Уилкинсон К.А., Глинн Дж.Р., Линг Д., Мензис Д., Мванса-Камбафвиле Дж., Филдинг К., Уилкинсон Р.Дж., Пай М. (2012) Прогностическая ценность анализов высвобождения гамма-интерферона при заболевании активным туберкулезом: систематический обзор и метаанализ.Ланцет Infect Dis 12 (1): 45–55. https://doi.org/10.1016/S1473-3099(11)70210-9
CAS Статья пабмед Google Scholar
Rangel-Frausto MS, Ponce-De-Leon-Rosales S, Martinez-Abaroa C, Haslov K (2001) Туберкулез и качество туберкулина: лучшие намерения, вводящие в заблуждение результаты. Infect Control Hosp Epidemiol 22(8):481–484. https://doi.org/10.1086/501937
Infect Control Hosp Epidemiol 22(8):481–484. https://doi.org/10.1086/501937
CAS Статья пабмед Google Scholar
Reed SG, Badaro R, Masur H, Carvalho EM, Lorenco R, Lisboa A, Teixeira R, Johnson WD Jr, Jones TC (1986) Выбор антигена кожного теста для американского висцерального лейшманиоза.Am J Trop Med Hyg 35 (1): 79–85. https://doi.org/10.4269/ajtmh.1986.35.79
CAS Статья пабмед Google Scholar
Ridley DS, Jopling WH (1966) Классификация лепры по иммунитету. Пятигрупповая система. Int J Lepr Other Mycobact Dis 34(3):255–273
CAS пабмед Google Scholar
Ривуар Б.Л., Гроутхаус Н.А., Терлоу С., Нейпан К.Д., Ранджит С., Сапкота Б.Р., Хадж С., Кунвар С.Б., Макдональд М., Хоксворт Р., Тапа М.Б., Хагге Д.А., Тиббалс М., Смит С., Дуб Т., Она D, Wolff M, Zhou E, Makhene M, Mason R, Sizemore C, Brennan PJ (2014a) Оценка безопасности и эффективности двух новых антигенов для кожных тестов на проказу: рандомизированное двойное слепое клиническое исследование.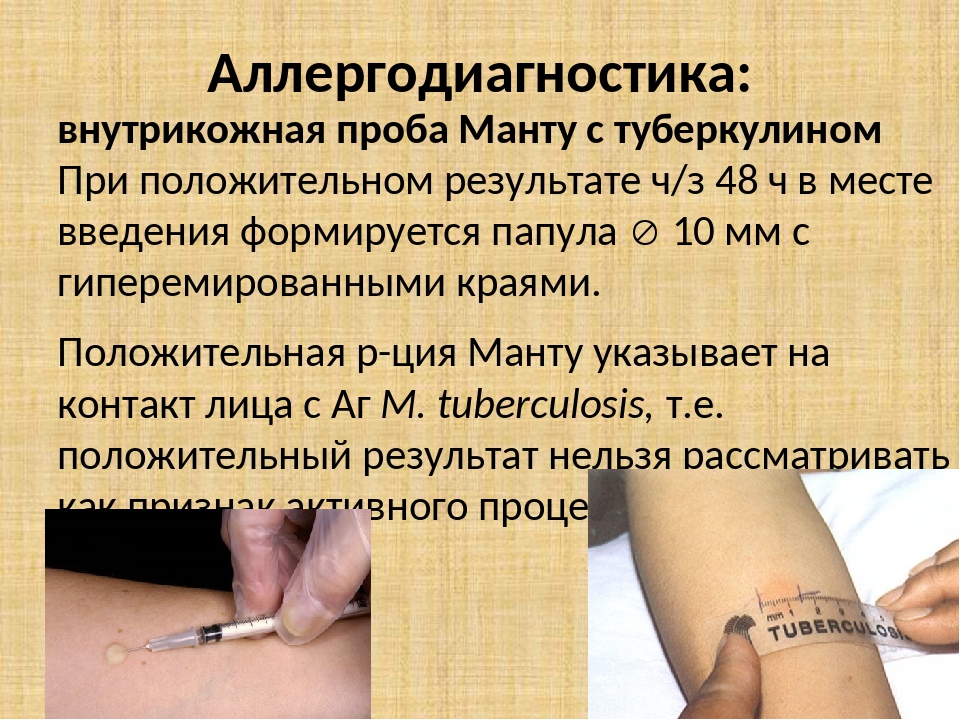 PLoS Negl Trop Dis 8(5):e2811. https://doi.org/10.1371/journal.pntd.0002811
PLoS Negl Trop Dis 8(5):e2811. https://doi.org/10.1371/journal.pntd.0002811
Статья пабмед ПабМед Центральный Google Scholar
Rivoire BL, TerLouw S, Groathouse NA, Brennan PJ (2014b) Задача производства антигенов для кожных тестов с минимальными ресурсами, подходящих для применения человеком против забытой тропической болезни; проказа. PLoS Negl Trop Dis 8(5):e2791. https://doi.org/10.1371/journal.pntd.0002791
CAS Статья пабмед ПабМед Центральный Google Scholar
Роуз Д.Н., Шехтер С.Б., Адлер Дж.Дж. (1995) Интерпретация туберкулиновой кожной пробы.J Gen Intern Med 10(11):635–642
CAS Статья Google Scholar
Сачдева С., Амин С.С., Хан З., Шарма П.К., Бансал С. (2011a) Детская проказа: чтобы не забыть. Trop Dr 41 (3): 163–165. https://doi.org/10.1258/td.2011.100477
Статья Google Scholar
Сачдева С. , Хан З., Ансари М.А., Амин С.С. (2011b) Проказа: вниз, но не наружу. Троп Д-р 41 (1): 28–30.https://doi.org/10.1258/td.2010.100107
, Хан З., Ансари М.А., Амин С.С. (2011b) Проказа: вниз, но не наружу. Троп Д-р 41 (1): 28–30.https://doi.org/10.1258/td.2010.100107
Статья Google Scholar
Sbarbaro J (1978) Антигены кожных тестов: оценка, время которой пришло. Am Rev Respir Dis 118(1-5)
Scollard DM (2004) Классификация лепры: полный цветовой спектр или черно-белый? Int J Lepr Other Mycobact Dis 72(2):166–168
Статья Google Scholar
Seibert F, Glen J (1941) PPD-S состоял примерно из 92 человек.1% белка, 5,9% полисахаридов и 1,2% нуклеиновой кислоты. Am Rev Tuberc 44:9–24
CAS Google Scholar
Shin HS, Kim Y, Kim G, Lee JY, Jeong I, Joh JS, Kim H, Chang E, Sim SY, Park JS, Lim DG (2019) Иммунный ответ на коронавирус ближневосточного респираторного синдрома во время острого фазы выздоровления человека. Clin Infect Dis 68 (6): 984–992. https://doi.org/10.1093/cid/ciy595
Clin Infect Dis 68 (6): 984–992. https://doi.org/10.1093/cid/ciy595
CAS Статья пабмед Google Scholar
Сингал А., Сонталия С., Панди Д. (2011) Детская проказа в больнице третичного уровня в Дели, Индия: переоценка в эпоху после ликвидации.Lepr Rev 82(3):259–269
Статья Google Scholar
Snider DE Jr (1982) Туберкулиновая кожная проба. Am Rev Respir Dis 125 (3 Pt 2): 108–118. https://doi.org/10.1164/arrd.1982.125.3P2.108
Статья пабмед Google Scholar
Старшинова А., Журавлев В., Довгалюк И., Пантелеев А., Манина В., Зинченко Ю., Истомина Е., Павлова М., Яблонский П. (2018) Сравнение внутрикожного теста с рекомбинантным туберкулезным аллергеном (диаскинтест) с другими иммунологическими тестами в диагностика туберкулезной инфекции.Int J Mycobacteriol 7:32–39
CAS Статья Google Scholar
Truman RW, Ebenezer GJ, Pena MT, Sharma R, Balamayooran G, Gillingwater TH, Scollard DM, McArthur JC, Rambukkana A (2014)Броненосец как модель периферической невропатии при проказе. ИЛАР J 54 (3): 304–314. https://doi.org/10.1093/ilar/ilt050
ИЛАР J 54 (3): 304–314. https://doi.org/10.1093/ilar/ilt050
CAS Статья пабмед ПабМед Центральный Google Scholar
Уплекар М., Вейл Д., Лоннрот К., Джарамилло Э., Линхардт С., Диас Х.М., Фальзон Д., Флойд К., Гарджиони Г., Гетахун Х., Гилпин С., Глазиу П., Гшемска М., Мирзаев Ф., Накатани Х., Равильоне M, для WsGTBP (2015) Новая стратегия ВОЗ по ликвидации ТБ.Ланцет 385 (9979): 1799–1801. https://doi.org/10.1016/S0140-6736(15)60570-0
Статья пабмед Google Scholar
Villarino ME, Burman W, Wang YC, Lundergan L, Catanzaro A, Bock N, Jones C, Nolan C (1999) Сопоставимая специфичность двух коммерческих туберкулиновых реагентов у лиц с низким риском туберкулезной инфекции. JAMA 281(2):169–171
CAS Статья Google Scholar
Вилларино М.Е., Бреннан М.Дж., Нолан К.М., Катандзаро А. , Лундерган Л.Л., Бок Н.Н., Джонс С.Л., Ван Ю.С., Бурман В.Дж. (2000) Сравнительное тестирование текущего (PPD-S1) и предлагаемого (PPD-S2) эталона нормы туберкулина.Am J Respir Crit Care Med 161 (4 Pt 1): 1167–1171. https://doi.org/10.1164/ajrccm.161.4.9
, Лундерган Л.Л., Бок Н.Н., Джонс С.Л., Ван Ю.С., Бурман В.Дж. (2000) Сравнительное тестирование текущего (PPD-S1) и предлагаемого (PPD-S2) эталона нормы туберкулина.Am J Respir Crit Care Med 161 (4 Pt 1): 1167–1171. https://doi.org/10.1164/ajrccm.161.4.9
CAS Статья пабмед Google Scholar
Уиттл Х., Эгбога А., Тодд Дж., Морган Г., Рольф М., Сабалли С., Уилкинс А., Корра Т. (1993) Иммунологические реакции гамбийцев в связи с клинической стадией заболевания ВИЧ-2. Clin Exp Immunol 93(1):45–50
CAS Статья Google Scholar
ВОЗ (2010 г.) Усовершенствованная глобальная стратегия дальнейшего снижения бремени болезней, вызываемых проказой: 2011–2015 гг.Всемирная организация здравоохранения, Женева
ВОЗ (2018a) Global Tuberculosis Report 2018. Всемирная организация здравоохранения, Женева
ВОЗ (2018b) Латентная туберкулезная инфекция: обновленное и сводное руководство по программному ведению
2 ВОЗ (2) отчет о туберкулезе 2019 г. , Женева
, Женева
Ян Х., Крух-Гарсия Н.А., Добос К.М. (2012)Очищенные белковые производные туберкулина — прошлое, настоящее и будущее. FEMS Immunol Med Microbiol 66 (3): 273–280.https://doi.org/10.1111/j.1574-695X.2012.01002.x
CAS Статья пабмед ПабМед Центральный Google Scholar
Единственный рекомбинантный белок M.tuberculosis DPPD повышает эффективность кожных проб у ВИЧ-инфицированных больных туберкулезом | AMB Express
Arenas Miras Mdel M, Hidalgo Tenorio C, Jimenez Alonso J (2013) Туберкулез у пациентов с системной красной волчанкой: ситуация в Испании.Реуматол Клин 9(6):369-372. https://doi.org/10.1016/j.reuma.2012.06.011
Артикул пабмед Google Scholar
Ариас Гильен М. (2011) Достижения в диагностике туберкулезной инфекции. Арка Бронконеумол 47 (10): 521–530. https://doi.org/10.1016/j.arbres.2011.06.018
Артикул пабмед Google Scholar
Bass JB Jr (2003) Насколько хорош туберкулиновый кожный тест? Infect Control Hosp Epidemiol 24(11):797–798. https://doi.org/10.1086/502138
https://doi.org/10.1086/502138
Артикул пабмед Google Scholar
Беме К.С., Никол М.П., Набета П., Майкл Дж.С., Готуццо Э., Тахирли Р., Глер М.Т., Блейкмор Р., Вородриа В., Грей К., Хуанг Л., Касерес Т., Мехдиев Р., Рэймонд Л., Уайтлоу А., Сагадеван K, Alexander H, Albert H, Cobelens F, Cox H, Alland D, Perkins MD (2011)Осуществимость, диагностическая точность и эффективность децентрализованного использования теста Xpert MTB/RIF для диагностики туберкулеза и множественной лекарственной устойчивости: многоцентровое внедрение учиться.Ланцет 377 (9776): 1495–1505. https://doi.org/10.1016/S0140-6736(11)60438-8
Артикул пабмед ПабМед Центральный Google Scholar
Borsuk S, Newcombe J, Mendum TA, Dellagostin OA, McFadden J (2009) Идентификация белков из очищенного туберкулином белкового производного (PPD) с помощью ЖХ-МС/МС. Туберкулез (Эдинб) 89(6):423–430. https://doi.org/10.1016/j.tube.2009.07.003
https://doi.org/10.1016/j.tube.2009.07.003
КАС Статья Google Scholar
Кэмерон М.М., Акоста-Серрано А., Берн С., Боэларт М., Ден Бур М., Бурза С., Чепмен Л.А., Часкопулу А., Коулман М., Куртенэ О., Крофт С., Дас П., Дилгер Э., Фостер Г., Гарлапати Р., Хейнс Л., Харрис А., Хемингуэй Дж., Холлингсворт Т.Д., Джервис С., Медли Г., Майлз М., Пейн М., Пикадо А., Поче Р., Готовый П., Роджерс М., Роуленд М., Сундар С., де Влас С.Дж., Уитман Д. (2016) Понимание динамики передачи Leishmania donovani для получения надежных данных о мерах по ликвидации висцерального лейшманиоза в Бихаре, Индия.Векторы-паразиты 9:25. https://doi.org/10.1186/s13071-016-1309-8
КАС Статья пабмед ПабМед Центральный Google Scholar
Campos-Neto A, Rodrigues-Junior V, Pedral-Sampaio DB, Netto EM, Ovendale PJ, Coler RN, Skeiky YA, Badaro R, Reed SG (2001) Evaluation of DPPD, single recombinant Mycobacterium tuberculosis белок как альтернативный антиген для пробы Манту. Туберкулез (Эдинб) 81(5–6):353–358
Туберкулез (Эдинб) 81(5–6):353–358
CAS Статья Google Scholar
CDC (2013a) Масштабы и последствия периодической нехватки растворов антигенов для туберкулиновых кожных тестов на основе очищенного белка – США, 2013 г.MMWR Morb Mortal Wkly Rep 62(49):1014–1015
Google Scholar
CDC (2013b) Нехватка туберкулиновых продуктов на основе очищенного белка в стране. MMWR Morb Mortal Wkly Rep 62(16):312
Google Scholar
CDC (2019 г.) Общенациональный дефицит антигенов туберкулиновых кожных тестов: рекомендации CDC по уходу за пациентами и практике общественного здравоохранения. MMWR Morb Mortal Wkly Rep 68 (24): 552–553.https://doi.org/10.15585/mmwr.mm6824a4
Артикул Google Scholar
Чо Ю.С., Добос К.М., Пренни Дж., Ян Х., Гесс А., Розенкрандс И. , Андерсен П., Рю С.В., Бай Г.Х., Бреннан М.Дж., Иззо А., Билефельдт-Оманн Х., Белисл Дж.Т. (2012) Расшифровка протеома реагента для диагностики in vivo «очищенное белковое производное» из Mycobacterium tuberculosis . Протеомика 12(7):979–991. https://doi.org/10.1002/pmic.201100544
, Андерсен П., Рю С.В., Бай Г.Х., Бреннан М.Дж., Иззо А., Билефельдт-Оманн Х., Белисл Дж.Т. (2012) Расшифровка протеома реагента для диагностики in vivo «очищенное белковое производное» из Mycobacterium tuberculosis . Протеомика 12(7):979–991. https://doi.org/10.1002/pmic.201100544
КАС Статья пабмед ПабМед Центральный Google Scholar
Coler RN, Skeiky YA, Ovendale PJ, Vedvick TS, Gervassi L, Guderian J, Jen S, Reed SG, Campos-Neto A (2000) Клонирование гена Mycobacterium tuberculosis , кодирующего очищенный белковый производный белок, который вызывает сильную туберкулёзную специфическую гиперчувствительность замедленного типа.J Infect Dis 182 (1): 224–233. https://doi.org/10.1086/315677
КАС Статья пабмед Google Scholar
Comstock GW, Edwards LB, Philip RN, Winn WA (1964) Сравнение двух туберкулинов, Ppd-S и Rt 23, в Соединенных Штатах Америки. Bull World Health Organ 31:161–170
Bull World Health Organ 31:161–170
CAS пабмед ПабМед Центральный Google Scholar
Dacso CC (1990) Кожные пробы на туберкулез, том 47.Клинические методы: анамнез, физические и лабораторные исследования, Бостон
Dye C, Glaziou P, Floyd K, Raviglione M (2013) Перспективы ликвидации туберкулеза. Annu Rev Общественное здравоохранение 34: 271–286. https://doi.org/10.1146/annurev-publhealth-031912-114431
Артикул пабмед Google Scholar
Farhat M, Greenaway C, Pai M, Menzies D (2006) Ложноположительные туберкулиновые кожные пробы: каков абсолютный эффект БЦЖ и нетуберкулезных микобактерий? Int J Tuberc Lung Dis 10(11):1192–1204
CAS пабмед Google Scholar
Getahun H, Matteelli A, Chaisson RE, Raviglione M (2015) Латентная инфекция Mycobacterium tuberculosis . N Engl J Med 372 (22): 2127–2135. https://doi.org/10.1056/NEJMra1405427
N Engl J Med 372 (22): 2127–2135. https://doi.org/10.1056/NEJMra1405427
КАС Статья пабмед Google Scholar
Гилленуотер К.А., Сапп С.К., Пирс К., Сиберри Г.К. (2006 г.) Увеличение конверсии туберкулиновых кожных тестов среди медицинских работников после перехода с туберсола на аплисол. Am J Infect Control 34 (10): 651–654. https://doi.org/10.1016/j.ajic.2006.05.288
Артикул пабмед Google Scholar
Goldstein S, Perlman DC, Salomon N (1994)Двухэтапный туберкулиновый кожный тест у ВИЧ-инфицированных: предварительный отчет.Гора Синай J Med 61 (4): 337–340
CAS пабмед Google Scholar
Грэм Н.М., Нельсон К.Е., Соломон Л., Бондс М., Риццо Р.Т., Скавотто Дж., Астемборски Дж., Влахов Д. (1992) Распространенность туберкулиновой положительности и анергии кожных проб у ВИЧ-1-серопозитивных и -серонегативных потребителей внутривенных наркотиков . JAMA 267(3):369–373
JAMA 267(3):369–373
CAS Статья Google Scholar
Houben RM, Dodd PJ (2016)Глобальное бремя латентной туберкулезной инфекции: переоценка с использованием математического моделирования.PLoS Med 13(10):e1002152. https://doi.org/10.1371/journal.pmed.1002152
Артикул пабмед ПабМед Центральный Google Scholar
Huebner RE, Schein MF, Bass JB Jr (1993) Туберкулиновая кожная проба. Clin Infect Dis 17(6):968–975
CAS Статья Google Scholar
Jensen PA, Lambert LA, Iademarco MF, Ridzon R (2005) Руководство по предотвращению передачи Mycobacterium tuberculosis в медицинских учреждениях, 2005.MMWR Recomm Rep 54:1–141
PubMed Google Scholar
Johnson MP, Coberly JS, Clermont HC, Chaisson RE, Davis HL, Losikoff P, Ruff AJ, Boulos R, Halsey NA (1992) Реактивность туберкулинового кожного теста среди взрослых, инфицированных вирусом иммунодефицита человека. J Infect Dis 166(1):194–198
J Infect Dis 166(1):194–198
CAS Статья Google Scholar
Keeler E, Perkins MD, Small P, Hanson C, Reed S, Cunningham J, Aledort JE, Hillborne L, Rafael ME, Girosi F, Dye C (2006) Снижение глобального бремени туберкулеза: вклад улучшенных диагностика.Nature 444(Suppl 1):49–57
Артикул Google Scholar
Kimura M, Comstock GW, Mori T (2005) Сравнение эритемы и уплотнения по результатам туберкулиновых тестов. Int J Tuberc Lung Dis 9(8):853–857
CAS пабмед Google Scholar
Lifson AR, Watters JK, Thompson S, Crane CM, Wise F (1993) Расхождения в результатах туберкулиновых кожных проб с двумя коммерческими продуктами у группы внутривенных наркоманов.J Infect Dis 168(4):1048–1051
CAS Статья Google Scholar
Liu C, Flamoe E, Chen HJ, Carter D, Reed SG, Campos-Neto A (2004) Экспрессия и очистка иммунологически реактивного DPPD, рекомбинантного Mycobacterium tuberculosis кожного тестового антигена, с использованием Mycobacterium smegmatis и Клетки-хозяева Escherichia coli .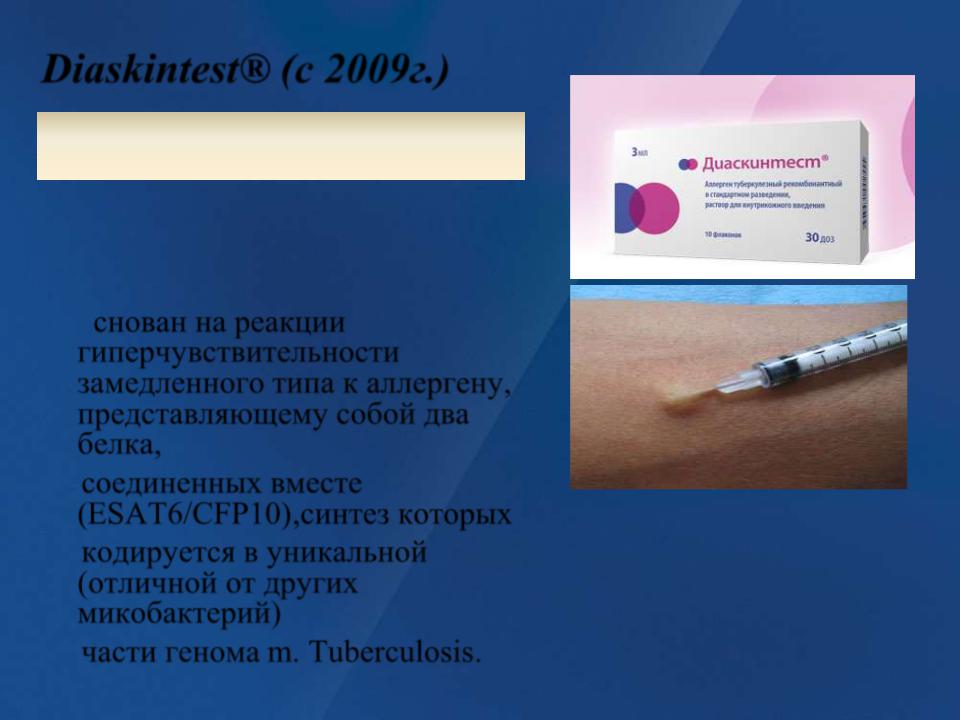 Can J Microbiol 50(2):97–105
Can J Microbiol 50(2):97–105
CAS Статья Google Scholar
Лоннрот К., Равильоне М. (2016 г.) Новая стратегия ВОЗ по ликвидации туберкулеза в период после 2015 г. достижения Целей в области устойчивого развития.Trans R Soc Trop Med Hyg 110 (3): 148–150. https://doi.org/10.1093/trstmh/trv108
Артикул пабмед ПабМед Центральный Google Scholar
Мамани М., Майзооби М.М., Торабян С., Михан Р., Ализаде К. (2013) Латентный и активный туберкулез: оценка потребителей инъекционных наркотиков. Медицинский центр Красного Полумесяца Ирана J 15(9):775–779. https://doi.org/10.5812/ircmj.6283
Артикул пабмед ПабМед Центральный Google Scholar
Mehta SR, MacGruder C, Looney D, Johns S, Smith DM (2009) Различия в реактивности туберкулина, определенные в программе проверки здоровья сотрудников администрации ветеранов. Clin Vaccine Immunol 16(4):541–543. https://doi.org/10.1128/CVI.00375-08
Clin Vaccine Immunol 16(4):541–543. https://doi.org/10.1128/CVI.00375-08
КАС Статья пабмед ПабМед Центральный Google Scholar
Morrison J, Pai M, Hopewell PC (2008) Туберкулез и латентная туберкулезная инфекция у лиц, тесно контактировавших с больными туберкулезом легких в странах с низким и средним уровнем дохода: систематический обзор и метаанализ. Ланцет Infect Dis 8 (6): 359–368. https://doi.org/10.1016/S1473-3099(08)70071-9
Артикул пабмед Google Scholar
Nicol MP, Workman L, Isaacs W, Munro J, Black F, Eley B, Boehme CC, Zemanay W, Zar HJ (2011) Точность теста Xpert MTB/RIF для диагностики туберкулеза легких у госпитализированных детей в больницу в Кейптауне, Южная Африка: описательное исследование.Ланцет Infect Dis 11 (11): 819–824. https://doi.org/10.1016/S1473-3099(11)70167-0
Артикул пабмед ПабМед Центральный Google Scholar
Owusu-Edusei K Jr, Winston CA, Marks SM, Langer AJ, Miramontes R (2017) Использование тестов на туберкулез и медицинские расходы на основе данных амбулаторного страхования, 2013.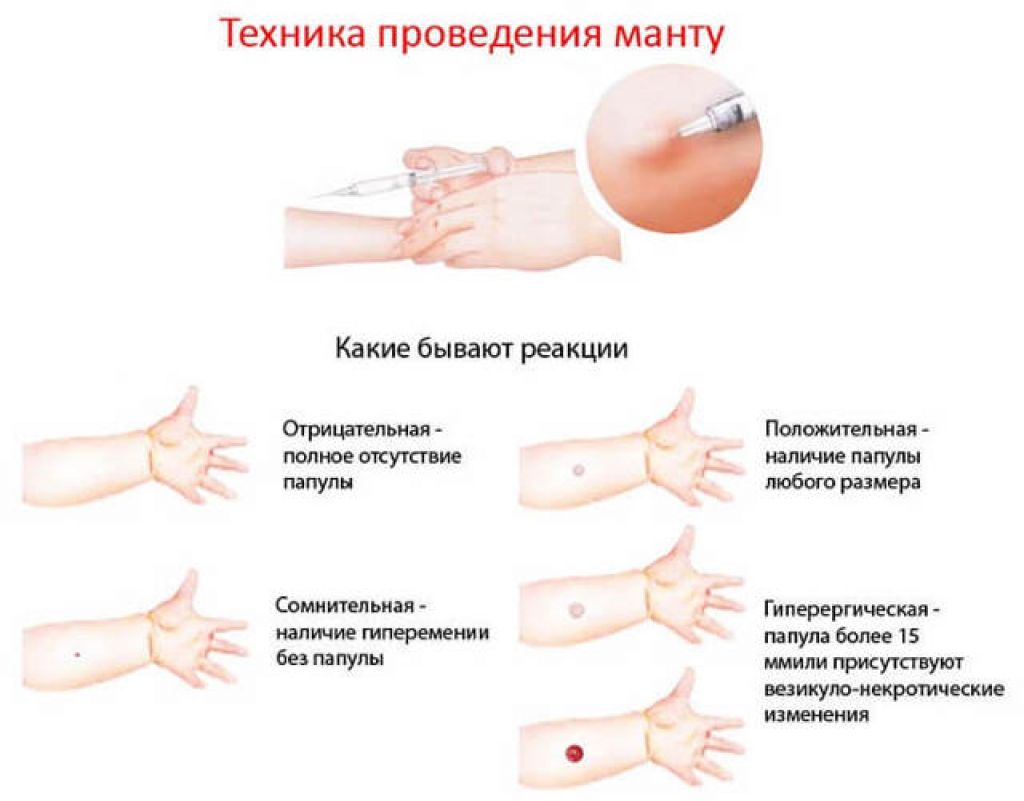 Tuber Res Treat 2017:3816432. https://doi.org/10.1155/2017/3816432
Tuber Res Treat 2017:3816432. https://doi.org/10.1155/2017/3816432
Артикул Google Scholar
Pai M, Denkinger CM, Kik SV, Rangaka MX, Zwerling A, Oxlade O, Metcalfe JZ, Cattamanchi A, Dowdy DW, Dheda K, Banaei N (2014) Анализы высвобождения гамма-интерферона для обнаружения Mycobacterium tuberculosis инфекционное заболевание.Clin Microbiol Rev 27 (1): 3–20. https://doi.org/10.1128/CMR.00034-13
КАС Статья пабмед ПабМед Центральный Google Scholar
Pai M, Behr MA, Dowdy D, Dheda K, Divangahi M, Boehme CC, Ginsberg A, Swaminathan S, Spigelman M, Getahun H, Menzies D, Raviglione M (2016) Туберкулез. Nat Rev Dis Primers 2:16076. https://doi.org/10.1038/nrdp.2016.76
Артикул пабмед Google Scholar
Рангака М.Х., Уилкинсон К.А., Глинн Дж.Р., Линг Д., Мензис Д., Мванса-Камбафвиле Дж. , Филдинг К., Уилкинсон Р.Дж., Пай М. (2012) Прогностическая ценность анализов высвобождения гамма-интерферона при заболевании активным туберкулезом: систематический обзор и метаанализ.Ланцет Infect Dis 12 (1): 45–55. https://doi.org/10.1016/S1473-3099(11)70210-9
, Филдинг К., Уилкинсон Р.Дж., Пай М. (2012) Прогностическая ценность анализов высвобождения гамма-интерферона при заболевании активным туберкулезом: систематический обзор и метаанализ.Ланцет Infect Dis 12 (1): 45–55. https://doi.org/10.1016/S1473-3099(11)70210-9
КАС Статья пабмед Google Scholar
Rangel-Frausto MS, Ponce-De-Leon-Rosales S, Martinez-Abaroa C, Haslov K (2001) Туберкулез и качество туберкулина: лучшие намерения, вводящие в заблуждение результаты. Infect Control Hosp Epidemiol 22(8):481–484. https://doi.org/10.1086/501937
КАС Статья пабмед Google Scholar
Роуз Д.Н., Шехтер С.Б., Адлер Дж.Дж. (1995) Интерпретация туберкулиновой кожной пробы.J Gen Intern Med 10(11):635–642
CAS Статья Google Scholar
Snider DE Jr (1982) Туберкулиновая кожная проба. Am Rev Respir Dis 125 (3 Pt 2): 108–118. https://doi.org/10.1164/arrd.1982.125.3P2.108
https://doi.org/10.1164/arrd.1982.125.3P2.108
Артикул пабмед Google Scholar
Старшинова А., Журавлев В., Довгалюк И., Пантелеев А., Манина В., Зинченко Ю., Истомина Е., Павлова М., Яблонский П. (2018) Сравнение внутрикожного теста с рекомбинантным туберкулезным аллергеном (диаскинтест) с другими иммунологическими тестами в диагностика туберкулезной инфекции.Int J Mycobacteriol 7:32–39
CAS Статья Google Scholar
Уплекар М., Вейл Д., Лоннрот К., Джарамилло Э., Линхардт С., Диас Х.М., Фальзон Д., Флойд К., Гарджиони Г., Гетахун Х., Гилпин С., Глазиу П., Гшемска М., Мирзаев Ф., Накатани Х., Равильоне M, для WsGTBP (2015) Новая стратегия ВОЗ по ликвидации ТБ. Ланцет 385 (9979): 1799–1801. https://doi.org/10.1016/S0140-6736(15)60570-0
Артикул Google Scholar
Villarino ME, Burman W, Wang YC, Lundergan L, Catanzaro A, Bock N, Jones C, Nolan C (1999) Сопоставимая специфичность двух коммерческих туберкулиновых реагентов у лиц с низким риском туберкулезной инфекции. JAMA 281(2):169–171
JAMA 281(2):169–171
CAS Статья Google Scholar
Вилларино М.Е., Бреннан М.Дж., Нолан К.М., Катандзаро А., Лундерган Л.Л., Бок Н.Н., Джонс С.Л., Ван Ю.С., Бурман В.Дж. (2000) Сравнительное тестирование текущего (PPD-S1) и предлагаемого (PPD-S2) эталона нормы туберкулина. Am J Respir Crit Care Med 161 (4 Pt 1): 1167–1171. https://doi.org/10.1164/ajrccm.161.4.9
КАС Статья пабмед Google Scholar
Уиттл Х., Эгбога А., Тодд Дж., Морган Г., Рольф М., Сабалли С., Уилкинс А., Корра Т. (1993) Иммунологические реакции гамбийцев в связи с клинической стадией заболевания ВИЧ-2.Clin Exp Immunol 93(1):45–50
CAS Статья Google Scholar
WHO (2018a) Global Tuberculosis Report 2018. Всемирная организация здравоохранения, Женева
Google Scholar
ВОЗ (2018b) Латентная туберкулезная инфекция: обновленные и сводные рекомендации по программному ведению. Всемирная организация здравоохранения, Женева, Женева
Всемирная организация здравоохранения, Женева, Женева
Google Scholar
Yang H, Kruh-Garcia NA, Dobos KM (2012)Очищенные белковые производные туберкулина – прошлое, настоящее и будущее.FEMS Immunol Med Microbiol 66 (3): 273–280. https://doi.org/10.1111/j.1574-695X.2012.01002.x
КАС Статья пабмед ПабМед Центральный Google Scholar
Заявка на патент США для кожных тестов на туберкулез у лиц с ослабленным иммунитетом Заявка на патент (заявка № 201
479, выданная 23 мая 2019 г.) ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к применению антигенов Mycobacterium tuberculosis для приготовления специфической композиции для кожных тестов с улучшенной диагностической эффективностью в отношении ТБ в M.туберкулез и лица с коинфекцией ВИЧ. Настоящее изобретение обеспечивает композицию, содержащую антигены Mycobacterium tuberculosis (Mtb) для диагностики инфекции Mtb in vivo у лиц с ослабленным иммунитетом или лиц, коинфицированных ВИЧ, где реагент содержит смесь двух антигенов ESAT6 и CFP-10.
Обзор ТБ/PPD
С момента своего открытия в 1908 году Робертом Кохом очищенное от туберкулина производное белка (PPD) использовалось в качестве диагностического теста на латентную инфекцию Mtb.
Использование диагностического теста на латентную инфекцию Mtb для проведения профилактического лечения оказывает существенное влияние на дальнейшее развитие заболевания ТБ. Люди, инфицированные Mtb, не имеют симптомов и нуждаются в более мягком режиме лечения, в то время как у пациентов с активным туберкулезом заболевание протекает тяжело, с высокой смертностью и требует более длительного и сложного лечения. Считается, что ⅓ населения мира инфицировано Mtb, ежегодно у 8 миллионов развивается активный туберкулез, из которых 1,3 миллиона умирают.
При применении в качестве диагностического теста небольшой объем 0.1 мл PPD вводят в верхний слой кожи и через 2-3 дня определяют положительную реакцию, измеряя уплотнение кожи с помощью простой линейки. Иммунологическим фоном кожной реакции PPD является реакция гиперчувствительности замедленного типа IV типа, реакция, опосредованная главным образом PPD-специфичными Т-клетками Th2.
Иммунологическим фоном кожной реакции PPD является реакция гиперчувствительности замедленного типа IV типа, реакция, опосредованная главным образом PPD-специфичными Т-клетками Th2.
PPD при применении в соответствии с описанием Менделя и Манту одобрен Всемирной организацией здравоохранения с 1955 года, а туберкулиновый кожный тест (TST) на основе PPD остается одним из наиболее широко используемых диагностических тестов, каждый из которых проводится более чем по 50 миллионов тестов. год.PPD представляет собой сложный культуральный фильтрат из M.tuberculosis , содержащий более 1000 белковых антигенов в дополнение к липидам и углеводам. Это делает PPD широко распознаваемым людьми, инфицированными Mtb, и он очень иммуногенен, вызывая сильный ответ Т-клеток Th2 в коже. Однако грубый и сложный состав PPD также является причиной проблем с TST PPD. Важно отметить, что множественные антигены в PPD также распознаются регуляторными Т-клетками, CD1-рестриктированными Т-клетками и Th3-клетками, которые могут избирательно ингибировать реакцию типа IV. Кроме того, множественные антигены в PPD также экспрессируются микобактериями окружающей среды и Bacillus Calmette-Guérin (BCG), используемыми для вакцинации против туберкулеза, что делает тест PPD неспецифическим.
Кроме того, множественные антигены в PPD также экспрессируются микобактериями окружающей среды и Bacillus Calmette-Guérin (BCG), используемыми для вакцинации против туберкулеза, что делает тест PPD неспецифическим.
ВИЧ-инфекция и лица с ослабленным иммунитетом.
Еще одной серьезной проблемой при использовании PPD TST является его ненадежность у лиц с ослабленным иммунитетом. Особенно у людей, инфицированных вирусом иммунодефицита человека (ВИЧ), ТКП PPD часто становится невосприимчивой и ложноотрицательной, или она может оказаться ложноположительной из-за применения слишком низкого порога.
Иммунологические предпосылки влияния ВИЧ на способность PPD вызывать кожную реакцию IV типа сложны, однако установлено, что основной причиной является избирательная потеря CD4 Т-клеток ВИЧ-инфекцией. Таким образом, иммунодефицит, вызванный потерей CD4 Т-клеток, является как основным фактором, ведущим к заболеванию оппортунистическими инфекционными вирусами и бактериями (признак ВИЧ/СПИДа), так и неспособностью реагировать на ППД ТКП.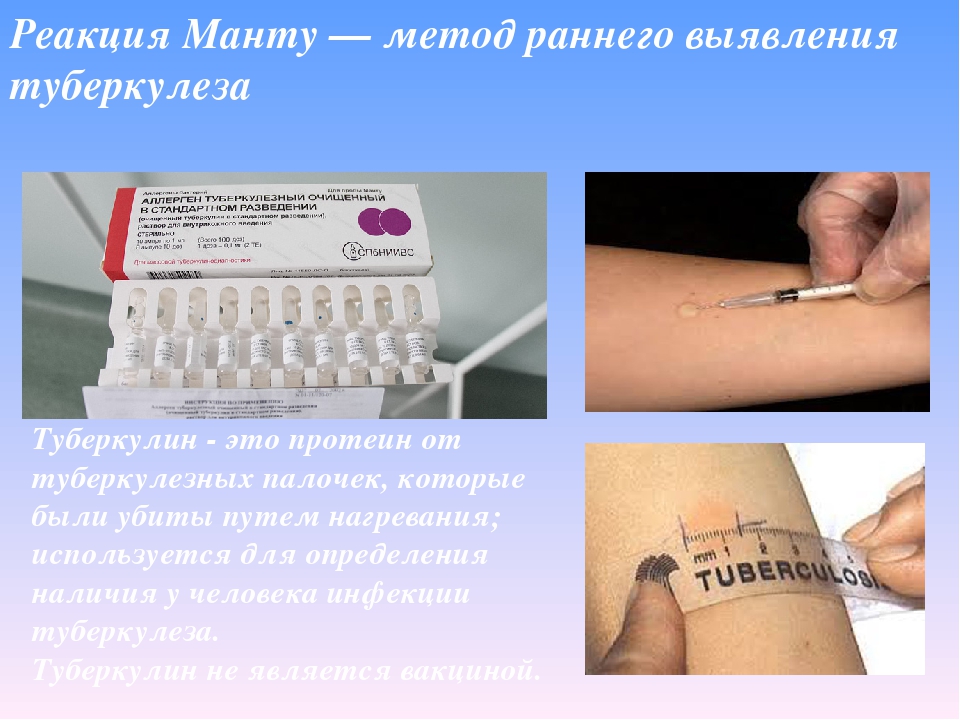
Последствия этой дилеммы могут быть смертельными.Часто ВИЧ-инфекция (или другой иммунодефицит) не диагностируется во время ППД ТКП. Поэтому ответственный врач часто ошибочно полагается на результат ППД ТКП. Это ложное чувство безопасности часто приводит к неправильной диагностике и отсутствию адекватного лечения инфекции Mtb, что приводит к более позднему развитию активной формы туберкулеза. Фактически, Mtb-инфицированные пациенты с ВИЧ/СПИДом имеют 10-процентный ежегодный риск развития ТБ, а ТБ является болезнью, от которой умирает большинство пациентов с ВИЧ/СПИДом.
Решение проблемы перекрестной реактивности к БЦЖ
Как упоминалось выше, перекрестная реактивность к БЦЖ и микобактериям из окружающей среды является основным ограничением ТКП PPD.Перекрестная реактивность ставит под угрозу специфичность и потенциально приводит к чрезмерному лечению из-за ложноположительных ответов. Проблема специфичности может быть решена в некоторой степени, но не полностью, путем увеличения порогового значения для ТКП с 5 мм до 10 мм или даже 15 мм уплотнения, однако увеличение порогового значения ставит под угрозу чувствительность теста.
Особенно для ВИЧ-инфицированных и других больших групп пациентов с самым высоким риском развития ТБ, если не будет предложено адекватное лечение инфекции Mtb, дальнейшая потеря чувствительности может оказаться фатальной.Таким образом, тестирование на ВИЧ перед тестированием PPD TST, например. Вакцинация БЦЖ потребуется для оптимального выполнения PPD TST. Однако из-за ограниченных ресурсов и табу как среди медицинских работников, так и среди пациентов тестирование на ВИЧ часто не предлагается или не принимается лицом, нуждающимся в тесте PPD TST.
Эра специфического тестирования
Открытие специфических иммунодоминантных антигенов Mtb открыло новые важные возможности для диагностики инфекции Mtb. Ранняя работа показала возможность замены PPD TST тестом, который оценивал продукцию интерферона-гамма (IFN-γ) in vitro Т-клетками в ответ на антигены Mtb.Примерно в то же время важным достижением стало открытие высокоиммуногенных антигенов, ранней секретируемой антигенной мишени 6 (ESAT-6) и белка культурального фильтрата 10 (CFP-10), которые значительно улучшили специфичность. Эти антигены кодируются в области различия 1 (RD1) патогена и, следовательно, отсутствуют во всех вакцинных штаммах Bacille Calmette Guerin (BCG) и большинстве нетуберкулезных микобактерий (исключения включают Mycobacterium kansasii, Mycobacterium marinum, Mycobacterium szulgai ). .
Эти антигены кодируются в области различия 1 (RD1) патогена и, следовательно, отсутствуют во всех вакцинных штаммах Bacille Calmette Guerin (BCG) и большинстве нетуберкулезных микобактерий (исключения включают Mycobacterium kansasii, Mycobacterium marinum, Mycobacterium szulgai ). .
Ответы IFN-γ на перекрывающиеся пептиды кодируемых RD1 антигенов ESAT-6 и CFP-10 формируют основу для обнаружения инфекции Mtb в двух коммерчески доступных тестах на высвобождение IFN-γ (IGRA): QuantiFERON-TB Gold (QIAGEN , Германия) и T-SPOT.TB (Oxford Immunotec, Оксфорд, Великобритания).
QuantiFERON-TB Gold (QFT, QIAGEN, Германия), твердофазный иммуноферментный анализ цельной крови (ELISA), имеет европейский знак CE и одобрение Американского управления по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) для выявления как латентной туберкулезной инфекции, так и заболевания.
T-SPOT.TB (Oxford Immunotec, Оксфорд, Великобритания), иммуноферментный анализ пятен (ELISPOT), в котором используются мононуклеарные клетки периферической крови, одобрен Европейским знаком СЕ и одобрен FDA.
Ограничения IGRA
Однако, несмотря на очевидные преимущества IGRA по сравнению с TST, IGRA имеет несколько ограничений:
Тесты IGRA на основе образцов крови требуют забора крови, сложного лабораторного оборудования и обученного персонала для его выполнения. Эти ограничения делают тест практически невозможным для реализации в условиях ограничения ресурсов, где такие тесты пользуются наибольшим спросом.Тесты IGRA также подвержены проблемам на преаналитическом этапе, например. ложноотрицательные ответы из-за задержки начала стадии инкубации.
В отличие от ТКП PPD, диагностическая эффективность тестов IGRA также требует, чтобы у человека, подвергающегося тестированию, был надежный иммунный ответ. Так же, как и для PPD TST, чувствительность IGRA может быть нарушена у лиц с ослабленным иммунитетом. В частности, у пациентов с ВИЧ-инфекцией и низким количеством Т-лимфоцитов CD4 или у пациентов, получающих иммунодепрессанты, часто возникают ложноотрицательные или неопределенные ответы.
Вероятной основной причиной низкой эффективности тестов IGRA у пациентов с иммуносупрессией является их зависимость от обнаружения очень слабого сигнала IFN-γ, который считается положительным (17,5 пг/мл или 6 реактивных Т-клеток на 200 000 РВМС). Такие низкие ответы граничат с уровнями обнаружения наиболее чувствительных анализов, используемых в клинической медицине.
Таким образом, кожный тест, в котором иммунная реакция потенциально может быть вызвана любой специфической Т-клеткой, имеющейся в организме, сам по себе кажется гораздо более надежным по сравнению с диагностическим тестом in vitro, в котором доступное количество Т-клеток ограничено небольшое количество клеток в образце.
В мета-анализе Cattamanchi и коллеги (JAIDS 2011, 56(3) 230-238) показали, что для ВИЧ-инфицированных лиц с активным ТБ (суррогатный эталонный стандарт для ЛТБИ) объединенные оценки чувствительности были неоднородными, но выше для T- Анализ SPOT.TB (72%; 95% ДИ, от 62 до 81%), чем для анализа QFT (61%; 95% ДИ, 47–75%) в странах с низким и средним уровнем дохода. Однако ни один из IGRA не был более чувствительным, чем PPD TST, в прямых сравнениях. Авторы пришли к выводу, что IGRA может меньше зависеть от степени иммуносупрессии, вызванной ВИЧ, по сравнению с PPD TST, но результаты различались в зависимости от географических условий.
Однако ни один из IGRA не был более чувствительным, чем PPD TST, в прямых сравнениях. Авторы пришли к выводу, что IGRA может меньше зависеть от степени иммуносупрессии, вызванной ВИЧ, по сравнению с PPD TST, но результаты различались в зависимости от географических условий.
Потенциально опасные для жизни последствия ложноотрицательных результатов PPD TST и IGRA были описаны Sester et al (Am J Respir Crit Care Med. 2014 Nov 15;190(10):1168-76. doi: 10.1164/rccm.201405- 09670С.). В этом крупном проспективном исследовании, включавшем 768 пациентов с ВИЧ-инфекцией, у восьми пациентов с ВИЧ-инфекцией во время последующего наблюдения развилась активная форма туберкулеза. Пять из 8 пациентов с определенным результатом теста IGRA имели ложноотрицательный результат теста IGRA во время скрининга, и им не было предложено профилактическое лечение.Еще 3 ВИЧ-инфицированных, у которых развился туберкулез, имели неопределенный результат теста IGRA. PPD TST была проведена всем 11 пациентам, у которых развился ТБ. В этой группе только 4 из 11 протестированных были положительными с использованием оптимизированного для ВИЧ порога на 5 мм.
В этой группе только 4 из 11 протестированных были положительными с использованием оптимизированного для ВИЧ порога на 5 мм.
Диаскинтест представляет собой рекомбинантный слитый белок CFP10-ESAT6, полученный в E. coli BL21 (DE3)/pCF-ESAT. Белок экспрессируется в виде 6-кратно меченного гистидином белка и производится компанией «Генериум» в Российской Федерации. Доза составляет 0,2 мкг/0,1 мл. Любой размер уплотнения считается показателем инфекции Mtb.Метка гистидина представляет риск неоэпитопов. Сообщается, что диаскинтест работает с приемлемой специфичностью, но с высокой частотой (4-14%) везикулярно-некротических изменений, лимфангитов и лимфаденитов (Киселев В.И.; Пробл. Туберкулез. Болезн. Легк. 2009; 2:11-6). Повторные инъекции высоких доз антигена могут представлять риск сенсибилизации, что может привести к ложноположительным реакциям, что еще больше увеличивает риск побочных реакций. Диаскинтест является единственным препаратом, находящимся в клинической практике. Несколько исследований изучали эффективность Диаскинтеста у ВИЧ-инфицированных лиц и обнаружили очень сильное негативное влияние ВИЧ-инфекции на эффективность Диаскинтеста.Панкраткова обнаружила чувствительность 42,9% среди ВИЧ-позитивных субъектов по сравнению с 79,7% среди субъектов без ВИЧ-инфекции (Pankratova L et al. European Respiratory Journal 2012, vol 40, Suppl 56/P431), аналогичные важные результаты были получены Литвиновым; 43,5% у ВИЧ-инфицированных по сравнению с 89,7% у ВИЧ-отрицательных (Литвинов и др., Am J Respir Crit Care Med 185; 2012:A4703).
Несколько исследований изучали эффективность Диаскинтеста у ВИЧ-инфицированных лиц и обнаружили очень сильное негативное влияние ВИЧ-инфекции на эффективность Диаскинтеста.Панкраткова обнаружила чувствительность 42,9% среди ВИЧ-позитивных субъектов по сравнению с 79,7% среди субъектов без ВИЧ-инфекции (Pankratova L et al. European Respiratory Journal 2012, vol 40, Suppl 56/P431), аналогичные важные результаты были получены Литвиновым; 43,5% у ВИЧ-инфицированных по сравнению с 89,7% у ВИЧ-отрицательных (Литвинов и др., Am J Respir Crit Care Med 185; 2012:A4703).
Таким образом, ТКП PPD является привлекательным и простым тестом на латентную инфекцию Mtb, однако антигенный компонент PPD неспецифичен, и результаты теста PPD TST у ВИЧ-инфицированных часто бывают ложноотрицательными.Тест IGRA основан на специфических антигенах Mtb ESAT-6 и CFP10 и решает проблемы специфичности теста PPD TST, однако эти тесты сложны в реализации и выполнении, а также часто дают ложноотрицательные результаты у ВИЧ-инфицированных людей.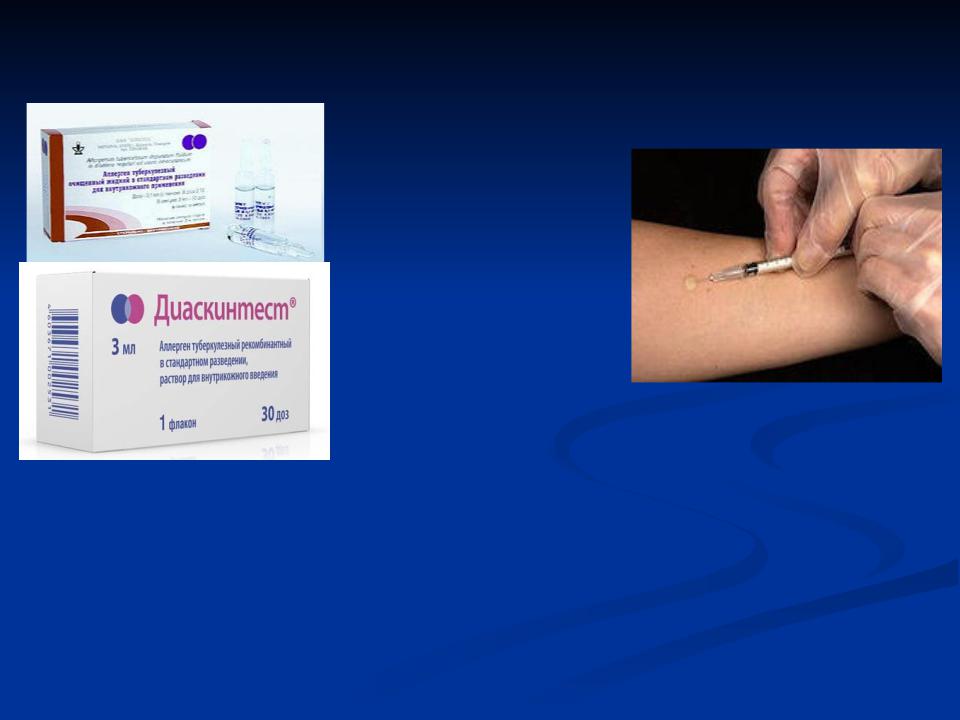 Диаскинтест обеспечивает кожный тест с IGRA-подобной специфичностью, однако эффективность диаскинтеста у ВИЧ-инфицированных сильно снижается, при этом чувствительность снижается наполовину у ВИЧ-инфицированных по сравнению с ВИЧ-неинфицированными. Следовательно, существует потребность в новом диагностическом кожном тесте на инфекцию Mtb с более высокой специфичностью по сравнению с PPD TST и повышенной чувствительностью у ВИЧ-инфицированных.
Диаскинтест обеспечивает кожный тест с IGRA-подобной специфичностью, однако эффективность диаскинтеста у ВИЧ-инфицированных сильно снижается, при этом чувствительность снижается наполовину у ВИЧ-инфицированных по сравнению с ВИЧ-неинфицированными. Следовательно, существует потребность в новом диагностическом кожном тесте на инфекцию Mtb с более высокой специфичностью по сравнению с PPD TST и повышенной чувствительностью у ВИЧ-инфицированных.
Изобретение раскрывает способ диагностики in vivo (кожное тестирование) и диагностические средства для диагностики Mtb у лиц с ослабленным иммунитетом или лиц, коинфицированных ВИЧ, лиц, которые иначе не были бы признаны инфицированными M.tuberculosis из-за недостаточной чувствительности существующих тестов.
Эффект достигается при использовании смеси антигенов M.tuberculosis ESAT6 и CFP10 для приготовления кожного тест-агента, состоящего из смеси этих антигенов. В предпочтительном варианте используют смесь антигенов rdESAT-6 и rCFP-10. Коктейль антигенов C-Tb очень хорошо действует на ВИЧ-инфицированных, демонстрируя общее снижение чувствительности всего на 33% по сравнению с 45% для квантиферона. В отличие от других методов тестирования, C-Tb, по-видимому, поражается ВИЧ-инфекцией только в самых тяжелых случаях с количеством CD4+ T-клеток <100 CD4+ T-клеток/мкл.
В предпочтительном варианте используют смесь антигенов rdESAT-6 и rCFP-10. Коктейль антигенов C-Tb очень хорошо действует на ВИЧ-инфицированных, демонстрируя общее снижение чувствительности всего на 33% по сравнению с 45% для квантиферона. В отличие от других методов тестирования, C-Tb, по-видимому, поражается ВИЧ-инфекцией только в самых тяжелых случаях с количеством CD4+ T-клеток <100 CD4+ T-клеток/мкл.
Настоящее изобретение раскрывает композицию, содержащую антигенов Mycobacterium tuberculosis , для использования в определении in vivo наличия Mtb-инфекции у лиц с ослабленным иммунитетом или лиц, коинфицированных ВИЧ, где агент представляет собой коктейль двух антигенов ESAT6 и CFP-10.
Настоящее изобретение раскрывает применение антигенов Mycobacterium tuberculosis для приготовления диагностического агента для кожных тестов (агента для кожных тестов) для надежной оценки наличия инфекции Mtb у индивидуума, в котором индивидуум является человеком с ослабленным иммунитетом или человеком коинфицированных ВИЧ.
Настоящее изобретение также раскрывает способ диагностики Mtb-инфекции у лиц с ослабленным иммунитетом или у лиц, коинфицированных ВИЧ. Метод диагностики основан на измерении величины кожной реакции, возникающей в ответ на стимуляцию специфических иммунных клеток путем инъекции небольшого объема специфических антигенов Mtb.
Два антигена предпочтительно клонируют, получают и очищают из подходящего организма, например из Lactococcus lactis , rESAT6 и rCFP10, и наиболее предпочтительно двойной ESAT-6 (rdESAT-6; две молекулы ESAT-6, слитые вместе). rdESAT-6 и rCFP10 предпочтительно смешивают в соотношении 1:1 (мас./мас.). Композиция включает два антигена, смешанных в носителе, причем наиболее предпочтительный носитель включает фосфатно-солевой буфер (PBS) с 0,01% полисорбата20 и 0,5% фенола.
Определения
Термин «Туберкулез» относится к клиническому состоянию Туберкулезное заболевание, вызываемое различными штаммами микобактерий, обычно Mycobacterium tuberculosis.
Термин «латентная M.tuberculosis инфекция» относится к субклинической или латентной инфекции M.tuberculosis , которая определяется наличием иммунного ответа на M.tuberculosis без признаков или симптомов активного заболевания .
Термин «ESAT-6» в настоящем изобретении относится к ранней секреторной антигенной мишени 6 кДа, продуцируемой Mycobacterium tuberculosis (esxA), представляет собой секреторный белок и мощный Т-клеточный антиген, локус-метка Rv3875
Термины « CFP10» в настоящем изобретении относится к секретируемому антигену 10 кДа из Mycobacterium tuberculosis , также известному как ESAT-6-подобный белок esxB, или секретируемому антигенному белку MTSA-10, или антигену культурального фильтрата 10 кДа, Rv3874.
Термины «коктейль» и «коктейль антигенов» в настоящем изобретении относятся по меньшей мере к двум белкам вместе в носителе или растворе.
Термин «иммунодефицит», «иммуносупрессия» или «иммуноскомпрометированный» относится к состоянию, при котором способность иммунной системы бороться с инфекционным заболеванием или вызывать иммунный ответ снижена или полностью отсутствует.
Термин «C-Tb» относится к препарату композиции rdESAT-6 и rCFP-10.
Термин «ВИЧ» относится к лентивирусу вируса иммунодефицита человека, который вызывает ВИЧ-инфекцию и со временем может привести к синдрому приобретенного иммунодефицита (СПИД)
Под термином «слитый белок» понимается случайный порядок двух или более иммуногенных полипептиды из М.tuberculosis или его аналоги, слитые вместе с аминокислотным линкером/спейсером (спейсерами) произвольной длины и последовательности или без них. Чтобы избежать агрегации белка при последующем производстве, все цистеины в слитом белке можно заменить любой аминокислотой, но предпочтительным заменителем является серин из-за его высокого структурного сходства с цистеином.
Удивительно улучшенная диагностическая чувствительность ВИЧ-инфицированных, вероятно, достигается за счет совокупности механизмов. Реагент для кожных тестов C-Tb состоит из коктейля антигенов, по сравнению с e. г. Диаскинтест, представляющий собой гибридную конструкцию, содержащую два белка, соединенных линкером. Коктейльный дизайн C-Tb предлагает несколько потенциальных преимуществ, включая лучшее раскрытие эпитопов без вмешательства со стороны линкерных белков. Кроме того, формат кожных тестов имеет преимущества перед форматом IGRA. Длительный инкубационный период позволяет рекрутировать ту же популяцию эффекторных Т-клеток, что и при мониторинге в IGRA, а также рекрутировать популяцию менее дифференцированных клеток.Более широкое привлечение Т-клеток в сочетании с форматом коктейля кожных тестов, вероятно, обеспечило превосходную чувствительность.
г. Диаскинтест, представляющий собой гибридную конструкцию, содержащую два белка, соединенных линкером. Коктейльный дизайн C-Tb предлагает несколько потенциальных преимуществ, включая лучшее раскрытие эпитопов без вмешательства со стороны линкерных белков. Кроме того, формат кожных тестов имеет преимущества перед форматом IGRA. Длительный инкубационный период позволяет рекрутировать ту же популяцию эффекторных Т-клеток, что и при мониторинге в IGRA, а также рекрутировать популяцию менее дифференцированных клеток.Более широкое привлечение Т-клеток в сочетании с форматом коктейля кожных тестов, вероятно, обеспечило превосходную чувствительность.
Диагностический агент для кожного теста содержит два антигена ESAT6 и CFP10. В предпочтительном воплощении реагент для кожных тестов состоит из смеси рекомбинантных вариантов двух антигенов. В наиболее предпочтительном воплощении два антигена представляют собой двойной ESAT-6 (rdESAT-6; две молекулы ESAT-6, слитые вместе) и rCFP-10. Два антигена клонируют, ферментируют и очищают в подходящем организме, т.е.г. из Lactococcus lactis или E. coli . Антигены смешивают в носителе или фармацевтически приемлемом носителе. В наиболее предпочтительном варианте осуществления rdESAT-6 и CFP10 смешивают в соотношении 1:1 (масс./масс.) в растворе фосфатно-солевого буфера (PBS) с 0,01% Polysorbate 20® (и 0,5% фенола). Величина дозы антигена находится в диапазоне 0,25-2,0 мкг/мл каждого антигена. Предпочтительное количество составляет 0,1 мкг/0,1 мл, что соответствует общей концентрации антигенов 1 мкг/мл, что соответствует 0.5 мкг/мл каждого. Этот специфический препарат rdESAT-6 и rCFP-10 называется C-Tb. Реагент не ограничивается только этими антигенами, но может дополнительно включать другие антигены, такие как Rv3615.
Два антигена клонируют, ферментируют и очищают в подходящем организме, т.е.г. из Lactococcus lactis или E. coli . Антигены смешивают в носителе или фармацевтически приемлемом носителе. В наиболее предпочтительном варианте осуществления rdESAT-6 и CFP10 смешивают в соотношении 1:1 (масс./масс.) в растворе фосфатно-солевого буфера (PBS) с 0,01% Polysorbate 20® (и 0,5% фенола). Величина дозы антигена находится в диапазоне 0,25-2,0 мкг/мл каждого антигена. Предпочтительное количество составляет 0,1 мкг/0,1 мл, что соответствует общей концентрации антигенов 1 мкг/мл, что соответствует 0.5 мкг/мл каждого. Этот специфический препарат rdESAT-6 и rCFP-10 называется C-Tb. Реагент не ограничивается только этими антигенами, но может дополнительно включать другие антигены, такие как Rv3615.
Проведение кожной пробы
Кожную пробу проводят путем внутрикожной инъекции небольшого объема C-Tb, например, 0,1 мл на внутреннюю поверхность предплечья.
Инъекцию следует производить туберкулиновым шприцем, срезом иглы вверх. Однако можно использовать и другие способы внутрикожной инъекции.При правильном размещении инъекции C-Tb должно появиться бледное возвышение кожи (волдырь) диаметром от 6 до 10 мм.
Однако можно использовать и другие способы внутрикожной инъекции.При правильном размещении инъекции C-Tb должно появиться бледное возвышение кожи (волдырь) диаметром от 6 до 10 мм.
Реакцию на кожные пробы следует оценивать между 48 и 72 часами после введения. Пациент, который не возвращается в течение 72 часов, должен быть перенесен на другой кожный тест.
Величину кожной реакции можно определить путем измерения уплотнения в миллиметрах (диаметр пальпируемого, приподнятого, затвердевшего участка или припухлости). Диаметр уплотненной области следует измерять поперек предплечья (перпендикулярно длинной оси предплечья).
Уплотнение 5 миллиметров или более, используемое в примере материала, является предпочтительным пределом отсечения, несмотря на то, что могут использоваться другие предельные значения, включая 10, 4, 3, 2, 1, или даже любая реакция выше 0 миллиметров. .
Концепция C-Tb заключается в объединении хорошо известного метода Манту с использованием специфических антигенов из IGRA в специфический кожный тест с единым универсальным порогом индурации 5 мм независимо от вакцинации БЦЖ и ВИЧ-статуса, определяемого через 2- 3 дня для выявления лиц, инфицированных Mtb, доставленных и интерпретированных медицинским или медсестринским персоналом по месту оказания медицинской помощи.
Диагностика
Кожные пробы со специальным реагентом особенно полезны для лиц с иммуносупрессией. ВИЧ представляет собой ключевую группу риска, в которой инфекция Mtb может быстро перейти в активную форму заболевания. ВИЧ-инфицированные лица имеют нарушенную функцию Т-клеток CD4, поэтому кожные тесты с реагентом, нацеленным конкретно на Т-клетки Th2, а не на Th3 или регуляторные Т-клетки, могут оказаться более эффективными.
Целевая группа населения для C-Tb включает лиц, подвергшихся воздействию Mtb, или лиц с признаками или симптомами ТБ, при этом особое внимание уделяется группам с повышенным риском развития ТБ после инфицирования.Эти группы включают, помимо прочего, вновь инфицированных, выявленных в ходе отслеживания контактов, детей в возрасте до 5 лет и ВИЧ-инфицированных.
В настоящем изобретении предложен реагент для кожных тестов для надежной оценки наличия инфекции Mtb у лиц, коинфицированных ВИЧ. Как ясно продемонстрировано в представленных примерах, пример специфического кожного теста (C-Tb) имеет более высокую эффективность, чем PPD TST и IGRA.
rdESAT-6 и CFP10 смешивают в соотношении (вес/вес) в носителе, хотя в предпочтительном варианте соотношение составляет 1:1, другие соотношения вес/вес, включая 1:5, 1:4, 1:3, 1:2; Ожидается, что будут полезны 2:1, 3:1, 4:1, 5:1 и другие соотношения, охватывающие 1:20 и 20:1.
Величина дозы антигена находится в диапазоне 0,25-20,0 мкг/мл каждого антигена. Предпочтительное количество составляет 0,1 мкг/0,1 мл, что соответствует общей концентрации 1 мкг антигенов/мл, что соответствует 0,5 мкг/мл каждого. Ожидается, что большее количество антигена вызовет более сильную реакцию уплотнения кожи, но увеличит риск побочных или излишне сильных реакций. В зависимости от клинических условий, генетического или этнического состава, степени иммуносупрессии или других характеристик испытуемой популяции доза антигена может быть выбрана в пределах 0.25-20,0 0,25-20,0 мкг/мл каждого антигена.
Хотя настоящее изобретение описывает специфический препарат rdESAT-6 и rCFP-10, агент не ограничивается только этими антигенами, но может дополнительно включать другие антигены, такие как espC (Rv3615) или другие специфические антигены, экспрессируемые M. tuberculosis. . Несколько антигенов, о которых известно, что они специфически экспрессируются инфекционными организмами в комплексе M.tuberculosis , могут быть подходящими дополнениями или заменителями ESAT-6 и CFP10 при C-Tb.Эти антигены включают рестриктированные антигены RD1, ассоциированные с RD1 антигены и антигены с иммунодиагностическим потенциалом, такие как Rv2564, Rv3865, Rv3877, Rv2348, Rv3614, Rv3616 и другие, известные специалисту в данной области.
tuberculosis. . Несколько антигенов, о которых известно, что они специфически экспрессируются инфекционными организмами в комплексе M.tuberculosis , могут быть подходящими дополнениями или заменителями ESAT-6 и CFP10 при C-Tb.Эти антигены включают рестриктированные антигены RD1, ассоциированные с RD1 антигены и антигены с иммунодиагностическим потенциалом, такие как Rv2564, Rv3865, Rv3877, Rv2348, Rv3614, Rv3616 и другие, известные специалисту в данной области.
Предпочтительный вариант теста C-Tb предполагает внутрикожную инъекцию. Следует понимать, что инъекция с помощью шприца и иглы является лишь одним из нескольких способов введения. Альтернативные методы включают в себя пушку Хифа (стернидл) и различные другие методы, такие как, помимо прочего, струйный впрыск, доставка снаряда с использованием порошка и золотых частиц (т.например, генный пистолет), твердые пластыри с микроиглами (металлическими или растворяющимися микроиглами), местное добавление C-Tb после предварительной обработки микроиглами, татуировочные пистолеты или технологии, предназначенные для повышения проницаемости кожи в сочетании с пластырем для доставки, например. истирание кожи, ультразвук, электропорация, лазерная порация, химические усилители и термическая абляция.
истирание кожи, ультразвук, электропорация, лазерная порация, химические усилители и термическая абляция.
РИС. 1. Частота положительных результатов C-Tb (черный цвет; пороговое значение 5 мм) и QFT (белый цвет; пороговое значение 0,35 МЕ/мл) среди 534 ВИЧ-отрицательных и 277 ВИЧ-положительных пациентов с подозрением на ТБ.Планка погрешности указывает 95% ДИ.
РИС. 2. Уровень положительных результатов C-Tb (черный) и QFT (белый), стратифицированный в соответствии с количеством CD4 среди 292 пациентов с подозрением на ТБ. Планка погрешности указывает 95% ДИ.
ПРИМЕРЫ Диагностический агент C-Tb был получен путем клонирования, ферментации и очистки рекомбинантных версий двух антигенов rdESAT-6 и rCFP-10 из Lactococcus lactis . Антигены смешивали в эквимолярных количествах ESAT-6 и CFP-10, соответствующих весовому соотношению rdESAT-6 и rCFP-10 1:1 в растворе фосфатно-солевого буфера (PBS) с 0.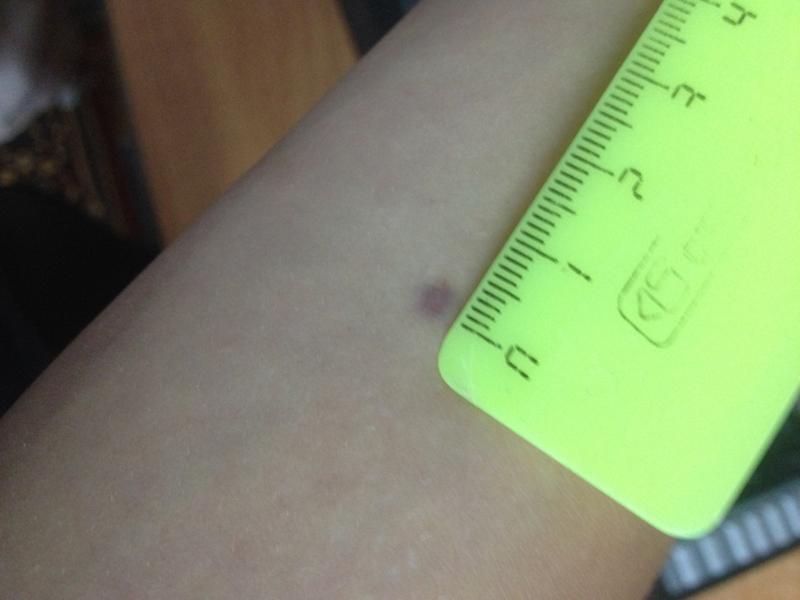 01% Polysorbate 20® (и 0,5% фенола)
01% Polysorbate 20® (и 0,5% фенола)
Диагностическая эффективность C-Tb, PPD и IGRA под названием QuantiFERON®-TB Gold In Tube (QFT) сравнивалась в исследовании фазы III у младенцев и детей младше 5 лет. лет с подозрением на инфекцию Mtb, а также у детей старшего возраста и взрослых с подозрением на туберкулез. Испытание 1190 участников включало 299 ВИЧ-позитивных и 730 ВИЧ-отрицательных. Кровь для QFT-тестирования собирали перед кожным тестированием. C-Tb и PPD вводили дважды вслепую в разные группы в рандомизированном дизайне с разделенным телом.Были включены результаты добровольцев с доступными парными результатами.
Как видно из фиг. 1, C-Tb и QFT показали одинаковую частоту положительных результатов среди ВИЧ-отрицательных: 292/534 (54,7%) были положительными с C-Tb и 285/534 (53,4%) были положительными с QFT. В общей сложности 277 ВИЧ-инфицированных были протестированы обоими тестами. Удивительно, но C-Tb выявил значительно больше инфицированных Mtb, чем тест QFT, 102/277 (36,8%) дали положительный результат на C-Tb и только 80/277 (28,9%) дали положительный результат на QFT (таблица 1, McNemar; P = 0).



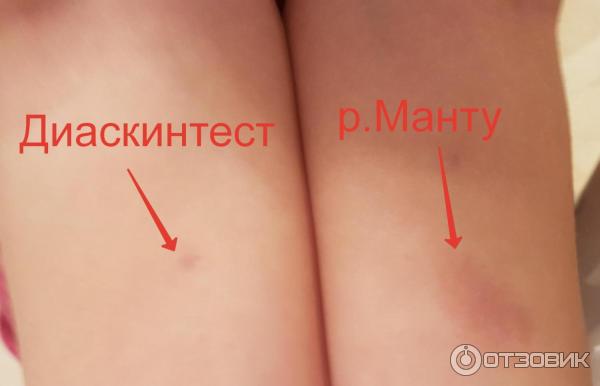
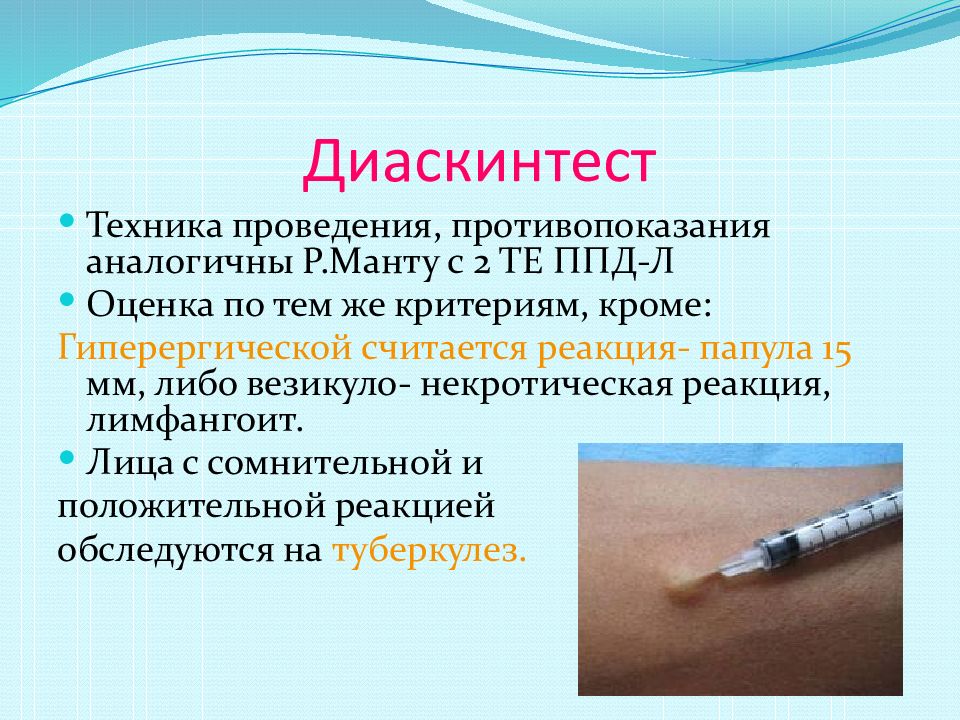
 д.м.н. проф. В.А. Аксеновой, 2017г.
д.м.н. проф. В.А. Аксеновой, 2017г. Не нужно употреблять в пищу продукты, часто вызывающие аллергические реакции, — шоколад, клубнику, цитрусовые и др.
Не нужно употреблять в пищу продукты, часто вызывающие аллергические реакции, — шоколад, клубнику, цитрусовые и др.
 org/10.4103/ijmy.ijmy_17_18
org/10.4103/ijmy.ijmy_17_18 ijmyco.org
ijmyco.org