Рубец после кесарева сечения — WMT клиника высоких технологий в Краснодаре
Количество родов путем кесарева сечения увеличивается каждый год и достигает порядка 40%, поэтому женщины чаще обращаются с проблемой несостоятельного (истонченного) рубца на матке. Основная причина несостоятельности рубца – хронический вялотекущий метроэндометрит, главные симптомы – длительные постменструальные кровомазанья и боли внизу живота.
ДИАГНОСТИКА
Диагностика несостоятельного рубца на матке на этапе планирования беременности особенно сложна, так как только по результатам УЗИ поставить верный диагноз трудно. Поэтому в клинике WMT используется весь комплекс диагностических мероприятий для уточнения диагноза:
- УЗИ малого таза («ниша» в проекции рубца, толщина рубца менее 3 мм, отсутствие васкуляризации при ЦДК указывают на несостоятельность)
- Гидросонография с анэхогенным контрастированием. Исследование проводится на 4-8 день цикла.
 В полость матки вводится физиологический раствор, это позволяет получить объективную информацию о состоянии рубца, характере кровотока в рубце и резерве интактного миометрия.
В полость матки вводится физиологический раствор, это позволяет получить объективную информацию о состоянии рубца, характере кровотока в рубце и резерве интактного миометрия. - Офисная гистероскопия. Выполняется на 4–6-й день менструального цикла, выявляются втяжения в области рубца, отсутствие сосудов, что говорит о выраженном преобладании фиброза. Также позволяет выявить объемные образования в области рубца, эндометриоз рубца и изменения зоны рубца с формированием множественных полостей (ниши) в миометрии.
- МРТ малого таза с оценкой состояния рубца.
ЛЕЧЕНИЕ НЕСОСТОЯТЕЛЬНОГО РУБЦА
При подтверждении диагноза несостоятельного рубца на матке на этапе прегравидарной подготовки хирурги клиники WMT выполняют реконструктивно-пластическую операцию – метропластику. Операция может быть выполнена лапаротомным (открытым), лапароскопическим и влагалищным доступом. Предпочтение отдается лапароскопическому доступу. При оперативном вмешательстве выполняется экономное иссечение соединительнотканного рубца и послойное восстановление стенки матки.
Показания к оперативному лечению:
- Истончение миометрия в зоне рубца 3 мм и менее.
- Истончение рубца на матке в сочетании с эндометриозом и инородных тел (инкапсулированные лигатуры) в структуре.
Оценка состоятельности рубца после метропластики проводится через 1, 3, 6 и 12 месяцев с помощью УЗИ. Только после получения данных об удовлетворительном состоянии рубца, можно планировать беременность.
УЗ-ПРИЗНАКИ ПОЛОЖИТЕЛЬНОГО РЕЗУЛЬТАТА ОПЕРАЦИИ:
- Положение рубца соответствует области операции.
- В зоне рубца отсутствуют деформации, «ниши», участки втяжения со стороны серозной оболочки и полости матки.
- Толщина миометрия в области нижнего маточного сегмента равна толщине передней стенки матки.
- В зоне рубца адекватный кровоток.
ЗАПИСЬ НА ПРИЁМ
Запишитесь на консультацию к врачу-гинекологу клиники WMT по телефону
 или оставьте заявку на сайте.
или оставьте заявку на сайте.Запись на приём
РУБЕЦ НА МАТКЕ ПОСЛЕ ОПЕРАЦИИ КЕСАРЕВА СЕЧЕНИЯ И ОПТИМАЛЬНЫЙ АЛГОРИТМ ДИАГНОСТИКИ ЕГО СОСТОЯНИЯ | Ножницева
1. Guise J.M., Eden K., Emeis C., Denman M.A., Marshall N., Fu R.R., Janik R., Nygren P., Walker M., McDonagh M. Vaginal birth after cesarean: new insights // Evid. Rep. Technol. Assess (Full Rep). 2010. Vol. 191. Р. 1–397.
2. Mathai M., Hofmeyr G.J., Mathai N.E. Abdominal surgical incisions for caesarean section // Cochrane Database Syst Rev. 2013. Vol. 5. CD004453. DOI: 10.1002/14651858.CD004453.pub3.
3. Monteagudo A., Carreno C., Timor-Tritsch I.E. Saline infusion sonohysterographyin nonpregnant women with previous cesarean delivery: the «niche» in the scar // J. Ultrasound. Med. 2001. Vol. 20. Р. 1105–1115.
4. Vervoort A.J., Uittenbogaard L.B., Hehenkamp W.J., Brölmann H.A., Mol B.W., Huirne J.A. Why do niches develop in Caesarean uterine scars? Hypotheses on the aetiology of niche development // Hum. Reprod. 2015. Dec; Vol. 30, No. 12 Р. 2695–2702. DOI: 10.1093/humrep/dev240. Epub 2015 Sep 25. PubMed PMID: 26409016.
Reprod. 2015. Dec; Vol. 30, No. 12 Р. 2695–2702. DOI: 10.1093/humrep/dev240. Epub 2015 Sep 25. PubMed PMID: 26409016.
5. Sholapurkar S.L. Etiology of Cesarean Uterine Scar Defect (Niche): Detailed Critical Analysis of Hypotheses and Prevention Strategies and Peritoneal Closure Debate // J. Clin. Med. Res. 2018 Mar; Vol. 10, No. 3. Р. 166–173. doi: 10.14740/jocmr3271w.
6. Ofili‐Yebovi D., Ben‐Nagi J., Sawyer E., Yazbek J., Lee C., Gonzalez J., Jurkovic D. Deficient lower‐segment Cesarean section scars: prevalence and risk factors // Ultrasound. Obstet. Gynecol. 2008. Vol. 31. Р. 72–77. PMID:18061960.
7. Bij de Vaate A.J., Brolmann H.A., van der Voet L.F., van der Slikke J.W., Veersema S., Huirne J.A. Ultrasound evaluation of the Cesarean scar: relation between a niche and postmenstrual spotting // Ultrasound Obstet. Gynecol. 2011. Vol. 37. Р. 93–99.
8. Vikhareva Osser O., Jokubkiene L., Valentin L. High prevalence of defects in Cesarean section scars at transvaginal ultrasound examination // Ultrasound. Obstet. Gynecol. 2009. Vol. 34. Р. 90–97.
Obstet. Gynecol. 2009. Vol. 34. Р. 90–97.
9. Wang C.B., Chiu W.W., Lee C.Y., Sun Y.L., Lin Y.H., Tseng C.J. Cesarean scar defect: correlation between Cesarean section number, defect size, clinical symptoms and uterine position // Ultrasound Obstet. Gynecol. 2009. Vol. 34. Р. 85–89.
10. Menada Valenzano M., Lijoi D., Mistrangelo E., Costantini S., Ragni N. Vaginal ultrasonographic and hysterosonographic evaluation of the low transverse incision after caesarean section: correlation with gynaecological symptoms // Gynecol. Obstet. Invest. 2006. Vol. 61. Р. 216–222.
11. Regnard C., Nosbusch M., Fellemans C., Benali N., van Rysselberghe M., Barlow P., Rozenberg S. Cesarean section scar evaluation by saline contrast sonohysterography // Ultrasound. Obstet. Gynecol. 2004. Vol. 23. Р. 289–292.
12. Armstrong V, Hansen W.F., Van Voorhis B.J., Syrop C.H. Detection of cesarean scars by transvaginal ultrasound // Obstet. Gynecol. 2003. Vol. 101. Р. 61–65.
13. Burger N. F., Darazs B., Boes E.G. An echographic evaluation during the early puerperium of the uterine wound after caesarean section // J. Clin. Ultrasound. 1982. Vol. 10. Р. 271–274.
F., Darazs B., Boes E.G. An echographic evaluation during the early puerperium of the uterine wound after caesarean section // J. Clin. Ultrasound. 1982. Vol. 10. Р. 271–274.
14. Краснопольский В.И., Логутова Л.С., Буянова С.Н. Несостоятельный рубец на матке после кесарева сечения: причины формирования и лечебная тактика // Акушерство и гинекология. 2013. № 12. С. 28–33.
15. Буянова С.Н., Щукина Н.А., Чечнева М.А., Мгелиашвили М.В., Титченко Ю.П., Пучкова Н.В., Барто Р.А. Современные методы диагностики несостоятельности швов или рубца на матке после кесарева сечения // Российский вестник акушера-гинеколога. 2013. № 1. С. 73–77.
16. Naji O., Abdallah Y., Bij De Vaate A.J., Smith A., Pexsters A., Stalder C., McIndoe A., Ghaem-Maghami S., Lees C., Brölmann H.A., Huirne J.A., Timmerman D., Bourne T. Standardized approach for imaging and measuring Cesarean section scars using ultrasonography // Ultrasound Obstet Gynecol. 2012. Mar. Vol. 39, No. 3. Р. 252–259. DOI: 10.1002/uog. 10077. Review. PubMed PMID: 21858885.
10077. Review. PubMed PMID: 21858885.
17. Vikhareva O.O., Valentin L. Clinical importance of appearance of cesarean hysterotomy scar at transvaginal ultrasonography in nonpregnant women // Obstet. Gynecol. 2011. Vol. 117. Р. 525–532.
18. Valentin L. Prediction of scar integrity and vaginal birth after caesarean delivery // Best Pract. Res. Clin. Obstet. Gynaecol. 2013. Vol. 27. Р. 285–295. DOI: 10.1016/j.bpobgyn.2012.09.003.
19. Цхай В.Б., Леванович Е.В., Ростовцева Е.С. Сравнительный анализ методов диагностики несостоятельного рубца на матке после операции кесарева сечения // Забайкальский медицинский журнал. 2017. № 1. С. 39–42.
Масса матки после кесарева сечения: отчет о двух случаях | BMC Беременность и роды
- История болезни
- Открытый доступ
- Опубликовано:
- Линь-юй Чжоу 1 ,
- Сяо-дань Чжу 1 ,
- Цзянь Цзян 1 и
- …
- Цзянь-анг Тянь-анг 0014 1
BMC Беременность и роды том 20 , Номер статьи: 508 (2020) Процитировать эту статью
1734 доступа
Детали показателей
Abstract
История вопроса
Кесарево сечение (БКШ) — редкое осложнение кесарева сечения и особый тип внематочной беременности.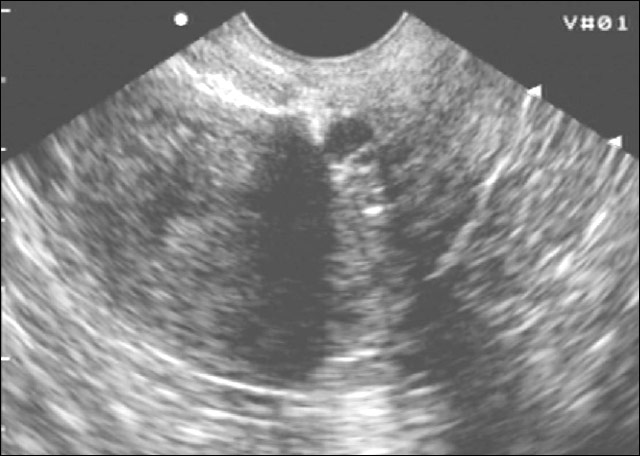 Гестационная трофобластическая неоплазия (ГТН) является редким осложнением беременности. Ранняя диагностика этих двух заболеваний имеет решающее значение, поскольку задержка или неправильный диагноз могут привести к увеличению материнской заболеваемости и смертности.
Гестационная трофобластическая неоплазия (ГТН) является редким осложнением беременности. Ранняя диагностика этих двух заболеваний имеет решающее значение, поскольку задержка или неправильный диагноз могут привести к увеличению материнской заболеваемости и смертности.
Кейс
Мы сообщаем о двух случаях поражения перешейка матки при предшествующем кесаревом сечении (КС). Двум пациентам был поставлен неправильный диагноз на основании первого ультразвукового исследования. Первый случай трофобластической опухоли был первоначально диагностирован как CSP, а второй случай с рубцовой беременностью был ошибочно диагностирован как GTN. Ошибочные диагнозы были связаны с особенностями расположения поражений у двух пациентов, что усложняло диагностику на основе ультразвука и препятствовало ранней клинической диагностике и лечению.
Выводы
Сбор анамнеза, измерение β-ХГЧ и трансвагинальное УЗИ необходимы для ранней диагностики поражений нижней части передней стенки матки.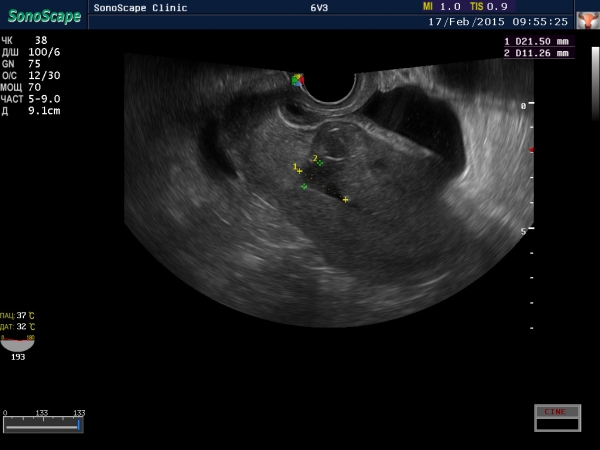 Однако, когда местоположение не может быть определено, можно дополнительно провести магнитно-резонансную томографию (МРТ), чтобы определить, находится ли поражение в рубце на матке. В сочетании со степенью повышенного уровня β-ХГЧ полезно дифференцировать ХСП, миометриальную ГТН или ГТН рубца кесарева сечения.
Однако, когда местоположение не может быть определено, можно дополнительно провести магнитно-резонансную томографию (МРТ), чтобы определить, находится ли поражение в рубце на матке. В сочетании со степенью повышенного уровня β-ХГЧ полезно дифференцировать ХСП, миометриальную ГТН или ГТН рубца кесарева сечения.
Отчеты экспертной оценки
Исходная информация
Всемирная организация здравоохранения (ВОЗ) сообщила, что средняя частота кесарева сечения (КС) в 9 странах Азии в 2010 г. составила 27,3%, а в Китае достигла 46,2% [1]. Распространенность CS различается между странами. Заболеваемость беременностью с рубцом от кесарева сечения (БКШ) в Китае выше, чем в других странах. С изменением политики одного ребенка все больше женщин решили снова забеременеть и, следовательно, столкнутся с риском CSP [2]. CSP — редкое осложнение кесарева сечения и особый тип внематочной беременности. КСП относится к беременности, при которой эмбрион имплантировался в гистеротомный рубец, частично или полностью располагается вне полости матки, окружен миометрием и фиброзной рубцовой тканью [3]. Предполагается, что механизм включает имплантацию бластоцист в крошечные участки расхождения шрама после предшествующего кесарева сечения [4, 5]. Из-за волокнистой природы рубцовой ткани по мере увеличения CSP эти изначально недостаточные места для имплантатов подвергаются риску разрыва, приращения плаценты и кровотечения. Ультразвук является основным методом визуализации для диагностики CSP, хотя точная и ранняя диагностика CSP может быть затруднена [6, 7]. В предыдущих исследованиях примерно в 15% случаев первоначально была ошибочно диагностирована цервикальная внематочная беременность, неполный аборт или низкая имплантация внутриматочной беременности [8, 9].].
Предполагается, что механизм включает имплантацию бластоцист в крошечные участки расхождения шрама после предшествующего кесарева сечения [4, 5]. Из-за волокнистой природы рубцовой ткани по мере увеличения CSP эти изначально недостаточные места для имплантатов подвергаются риску разрыва, приращения плаценты и кровотечения. Ультразвук является основным методом визуализации для диагностики CSP, хотя точная и ранняя диагностика CSP может быть затруднена [6, 7]. В предыдущих исследованиях примерно в 15% случаев первоначально была ошибочно диагностирована цервикальная внематочная беременность, неполный аборт или низкая имплантация внутриматочной беременности [8, 9].].
Несвоевременная диагностика CSP и применение кюретажа могут привести к неконтролируемому кровотечению и разрыву матки, которые являются опасными для жизни осложнениями и могут потребовать гистерэктомии для спасения жизни матери [9, 10].
Однако гестационная трофобластическая болезнь также может возникать в нижней части передней стенки матки, например, в рубцах на матке или на шейке матки, что затрудняет раннюю диагностику [11, 12]. Гестационная трофобластическая неоплазия (ГТН) является редким осложнением беременности. Во всем мире существует значительная вариация заболеваемости GTN, причем самые высокие частоты зарегистрированы в Азии и на Ближнем Востоке [13]. Приблизительно 50% ЗГН развиваются после молярной беременности, и их диагностика относительно проста. Постмолярная ГТН обычно диагностируется с помощью наблюдения за β-ХГЧ и критериев стадии FIGO [14]. Однако диагностика немолярной ГТН, возникающей после самопроизвольного аборта, внематочной или доношенной беременности, относительно сложна. Подобно CSP, клиническая картина в основном включает аномальные вагинальные кровотечения, аборты, внематочную беременность и другие гинекологические заболевания, и это состояние связано с отсутствием специфичности в клинической практике, а также легко диагностируется. Исследования трофобластических опухолей в месте рубца определили набор диагностических критериев для ранней диагностики, чтобы избежать пропущенного диагноза [15].
Гестационная трофобластическая неоплазия (ГТН) является редким осложнением беременности. Во всем мире существует значительная вариация заболеваемости GTN, причем самые высокие частоты зарегистрированы в Азии и на Ближнем Востоке [13]. Приблизительно 50% ЗГН развиваются после молярной беременности, и их диагностика относительно проста. Постмолярная ГТН обычно диагностируется с помощью наблюдения за β-ХГЧ и критериев стадии FIGO [14]. Однако диагностика немолярной ГТН, возникающей после самопроизвольного аборта, внематочной или доношенной беременности, относительно сложна. Подобно CSP, клиническая картина в основном включает аномальные вагинальные кровотечения, аборты, внематочную беременность и другие гинекологические заболевания, и это состояние связано с отсутствием специфичности в клинической практике, а также легко диагностируется. Исследования трофобластических опухолей в месте рубца определили набор диагностических критериев для ранней диагностики, чтобы избежать пропущенного диагноза [15].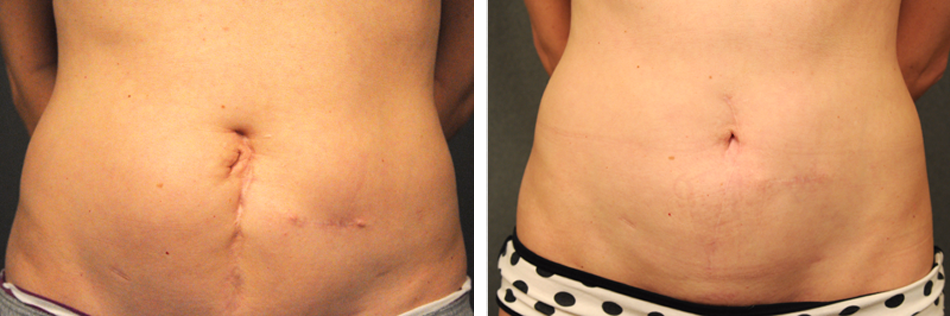
Обе пациентки, описанные здесь, имели в анамнезе шрамовую беременность, и их клиническими проявлениями были нерегулярные вагинальные кровотечения. Более крупные образования можно было обнаружить в нижней части передней стенки матки при УЗИ. В отличие от предыдущих случаев, эти два случая имеют схожие ультразвуковые изображения, показывающие огромное образование в нижней передней стенке матки, но совершенно разные клинические диагнозы. Путем сравнения мы обобщили наши соображения по диагностике и дифференциальной диагностике, основанные на сходных изображениях. Когда трансвагинальное ультразвуковое исследование (ТВС) не может подтвердить конкретную локализацию поражения и диагноз, можно рассмотреть возможность магнитно-резонансной томографии (МРТ) для дальнейшего уточнения взаимосвязи между образованием и рубцом на матке, что помогает поставить окончательный диагноз.
Представление случая
Случай 1
32-летняя женщина с аменореей в течение 2 месяцев и вагинальным кровотечением в течение полумесяца была направлена в нашу больницу. Первая ТВС, проведенная в другой больнице, показала неоднородное образование в передней части нижнего сегмента матки размером 67 * 66 мм, выступающее в полость матки. Внутри наблюдался сигнал кровотока. Массу рассматривали как CSP. Анализы крови, проведенные при поступлении, выявили значение β-ХГЧ более 225 000 МЕ/мл (нормальное значение < 5,3 МЕ/мл). На УЗИ в нашей больнице выявлено неоднородное гипоэхогенное образование размером 90,6 * 6,7 * 8,5 см в нижне-переднем отделе матки. Границы образования были нечеткими, с сотовой структурой в очаге поражения, и образование явно сдавливало полость матки. полость матки. Цветная допплеровская визуализация потока (CDFI) показала обильные сигналы кровотока и низкий индекс сопротивления (RI = 0,4) в очаге поражения. Поражение продемонстрировало периферическое неравномерное усиление в артериальную фазу. Сотовая структура частично демонстрировала гиперусиление на всех этапах экзамена. Заметное отсутствие усиления появилось в центральной области поражения (рис.
Первая ТВС, проведенная в другой больнице, показала неоднородное образование в передней части нижнего сегмента матки размером 67 * 66 мм, выступающее в полость матки. Внутри наблюдался сигнал кровотока. Массу рассматривали как CSP. Анализы крови, проведенные при поступлении, выявили значение β-ХГЧ более 225 000 МЕ/мл (нормальное значение < 5,3 МЕ/мл). На УЗИ в нашей больнице выявлено неоднородное гипоэхогенное образование размером 90,6 * 6,7 * 8,5 см в нижне-переднем отделе матки. Границы образования были нечеткими, с сотовой структурой в очаге поражения, и образование явно сдавливало полость матки. полость матки. Цветная допплеровская визуализация потока (CDFI) показала обильные сигналы кровотока и низкий индекс сопротивления (RI = 0,4) в очаге поражения. Поражение продемонстрировало периферическое неравномерное усиление в артериальную фазу. Сотовая структура частично демонстрировала гиперусиление на всех этапах экзамена. Заметное отсутствие усиления появилось в центральной области поражения (рис. 1). CEUS предположил хориокарциному в качестве диагноза, но не исключалась послеоперационная беременность в сочетании с частичным пузырным заносом. МРТ-обследование также предположило трофобластическую опухоль в качестве диагноза. После профилактической эмболизации маточных артерий при гистероскопии выявлены выраженные опухоли передней стенки перешейка матки, поверхность слизистой интактна, полость матки деформирована компрессией. Явных новообразований в полости матки не обнаружено. После 7 курсов химиотерапии ЭМА и ЭП выполнена лапароскопическая тотальная гистерэктомия и двусторонняя сальпингэктомия. Интраоперационные анатомические препараты включали образования размером 5*5*4 см из перешейка матки. Основная патология показала (в матке) обширный некроз с агрегацией пенистых клеток и воспалительной клеточной инфильтрацией, что соответствует изменениям после химиотерапии, хроническому воспалению слизистой оболочки шейки матки и (двустороннему) ткани фаллопиевых труб. Послеоперационная химиотерапия ЭМА и ЭП была продолжена.
1). CEUS предположил хориокарциному в качестве диагноза, но не исключалась послеоперационная беременность в сочетании с частичным пузырным заносом. МРТ-обследование также предположило трофобластическую опухоль в качестве диагноза. После профилактической эмболизации маточных артерий при гистероскопии выявлены выраженные опухоли передней стенки перешейка матки, поверхность слизистой интактна, полость матки деформирована компрессией. Явных новообразований в полости матки не обнаружено. После 7 курсов химиотерапии ЭМА и ЭП выполнена лапароскопическая тотальная гистерэктомия и двусторонняя сальпингэктомия. Интраоперационные анатомические препараты включали образования размером 5*5*4 см из перешейка матки. Основная патология показала (в матке) обширный некроз с агрегацией пенистых клеток и воспалительной клеточной инфильтрацией, что соответствует изменениям после химиотерапии, хроническому воспалению слизистой оболочки шейки матки и (двустороннему) ткани фаллопиевых труб. Послеоперационная химиотерапия ЭМА и ЭП была продолжена. Последние анализы крови показали значение β-ХГЧ 1,1 МЕ/мл.
Последние анализы крови показали значение β-ХГЧ 1,1 МЕ/мл.
В первом случае поражение демонстрировало периферическое неравномерное гиперусиление в артериальную фазу и более поздние фазы. Внутренняя сотовая структура частично показала гиперусиление. Заметное отсутствие усиления появилось в центральной области поражения
Изображение в полный размер
Второй случай
34-летняя женщина была направлена в нашу больницу по поводу аменореи без очевидной причины 3 месяца назад. При УЗИ в другом стационаре выявлено неравномерно-эхогенное образование размерами 4,1*3,5 см от нижнего отдела матки до передней стенки шейки матки с обильным кровоснабжением. В то время уровень β-ХГЧ составлял 72 587 ЕД/мл (нормальное значение < 5,3 МЕ/мл). После подозрения на внутриматочную беременность выполнена эмболизация маточных артерий. Затем проводят кюретаж под контролем УЗИ. Послеоперационная патология показала внутриутробную плацентарную ткань, продолжалось послеоперационное вагинальное кровотечение. Позже, в нашей больнице, TVS показала, что образование у нижней передней стенки матки было размером примерно 3,8 * 3,2 см. CDFI выявил сигналы периферического богатого кровотока в очаге поражения. Значение β-ХГЧ составило 184,3 мМЕ/мл (нормальное значение < 5,3 МЕ/мл). Первоначальный диагноз был подозрением на трофобластические опухоли при обычном УЗИ. Однако анализ данных МРТ позволил предположить рубцовую беременность. Выполнена лапароскопическая резекция тазового рубца на матке и восстановление матки. Во время операции в части сальника и передней части брюшины образовались плотные мышечные сращения, а в нижней части передней стенки матки вблизи шейки наблюдалось выпячивание 4*3 см. Патология показала некротическую ткань (ткань беременности рубца на матке), волокна, инфильтрацию воспалительных клеток в мышечной ткани и ворсинки в небольшом количестве децидуальной ткани и некротизированной ткани.
Позже, в нашей больнице, TVS показала, что образование у нижней передней стенки матки было размером примерно 3,8 * 3,2 см. CDFI выявил сигналы периферического богатого кровотока в очаге поражения. Значение β-ХГЧ составило 184,3 мМЕ/мл (нормальное значение < 5,3 МЕ/мл). Первоначальный диагноз был подозрением на трофобластические опухоли при обычном УЗИ. Однако анализ данных МРТ позволил предположить рубцовую беременность. Выполнена лапароскопическая резекция тазового рубца на матке и восстановление матки. Во время операции в части сальника и передней части брюшины образовались плотные мышечные сращения, а в нижней части передней стенки матки вблизи шейки наблюдалось выпячивание 4*3 см. Патология показала некротическую ткань (ткань беременности рубца на матке), волокна, инфильтрацию воспалительных клеток в мышечной ткани и ворсинки в небольшом количестве децидуальной ткани и некротизированной ткани.
Обсуждение и выводы
Здесь мы сообщили о двух случаях поражения матки. Двум пациентам был поставлен неправильный диагноз после КС на основании первого ультразвукового исследования. Первый случай трофобластической опухоли был первоначально диагностирован как рубцовая беременность, а второй случай, когда была рубцовая беременность, был ошибочно диагностирован как трофобластическая опухоль. Ошибочные диагнозы были связаны с особенностями локализации поражений у двух пациенток, а именно с нижним передним сегментом матки, что осложняло диагностику на основе УЗИ и в дальнейшем препятствовало ранней клинической диагностике и лечению. Поэтому понимание особенностей рубцовой беременности и трофобластических опухолей очень важно.
Двум пациентам был поставлен неправильный диагноз после КС на основании первого ультразвукового исследования. Первый случай трофобластической опухоли был первоначально диагностирован как рубцовая беременность, а второй случай, когда была рубцовая беременность, был ошибочно диагностирован как трофобластическая опухоль. Ошибочные диагнозы были связаны с особенностями локализации поражений у двух пациенток, а именно с нижним передним сегментом матки, что осложняло диагностику на основе УЗИ и в дальнейшем препятствовало ранней клинической диагностике и лечению. Поэтому понимание особенностей рубцовой беременности и трофобластических опухолей очень важно.
Клиническая ультразвуковая диагностика поражений матки основывается главным образом на характеристиках серого и цветного доплеровского ультразвука [16]. Недавно клиническое исследование под названием TITANIUM было направлено на описание ультразвуковых признаков ЗТН и определение ультразвуковых предикторов резистентности к монохимиотерапии у пациентов с низким риском [17]. Типичные особенности визуализации поражений GTN, расположенных в миометрии, на УЗИ демонстрируют неоднородную эхогенность, губчатую или сотовую форму. CDFI показал повышенную васкуляризацию в массах, что было вызвано наличием внутриочаговых артериовенозных шунтов. При спектральном доплеровском УЗИ сосуды демонстрировали высокоскоростную волну с низким сопротивлением, в основном между 0,2 и 0,4. CDFI может помочь в оценке GTN, поскольку эти поражения имеют артериовенозные связи [18]. В проспективном анализе 246 женщин с полной родинкой допплеровский индекс пульсации показал потенциал в качестве предиктора последующего развития ЗТН [19].]. Однако УЗ-признаки атипичного или особого расположения ЗГТ могут иногда совпадать с признаками внематочной беременности [20].
Типичные особенности визуализации поражений GTN, расположенных в миометрии, на УЗИ демонстрируют неоднородную эхогенность, губчатую или сотовую форму. CDFI показал повышенную васкуляризацию в массах, что было вызвано наличием внутриочаговых артериовенозных шунтов. При спектральном доплеровском УЗИ сосуды демонстрировали высокоскоростную волну с низким сопротивлением, в основном между 0,2 и 0,4. CDFI может помочь в оценке GTN, поскольку эти поражения имеют артериовенозные связи [18]. В проспективном анализе 246 женщин с полной родинкой допплеровский индекс пульсации показал потенциал в качестве предиктора последующего развития ЗТН [19].]. Однако УЗ-признаки атипичного или особого расположения ЗГТ могут иногда совпадать с признаками внематочной беременности [20].
Ультразвук — это метод визуализации первой линии для диагностики CSP. Однако особенности сонографической визуализации CSP сложны. Ранняя диагностика CSP не всегда достигается, и во многих случаях ошибочно диагностируется угроза или пропущенный/неполный выкидыш или просто внутриматочная беременность. Такой ошибочный диагноз может привести к резкому выскабливанию по поводу предполагаемой несостоявшейся беременности, что может закончиться обильным кровотечением и неотложным хирургическим вмешательством, иногда заканчивающимся гистерэктомией. Остаточная ворсинчатая ткань из-за неправильного выскабливания продолжает расти и инфильтрировать миометрий, формируя массы на основе БКШ. Этот вид КСП часто изображают в виде неоднородной массы, состоящей из различных компонентов, в передней стенке нижнего сегмента матки [21]. В этих условиях БКШ трудно дифференцировать от трофобластических опухолей [22]. Во втором случае с помощью TVS была обнаружена сильно васкуляризированная гетерогенная масса, что привело к ошибочному диагнозу трофобластической опухоли, как и в предыдущем исследовании [23].
Такой ошибочный диагноз может привести к резкому выскабливанию по поводу предполагаемой несостоявшейся беременности, что может закончиться обильным кровотечением и неотложным хирургическим вмешательством, иногда заканчивающимся гистерэктомией. Остаточная ворсинчатая ткань из-за неправильного выскабливания продолжает расти и инфильтрировать миометрий, формируя массы на основе БКШ. Этот вид КСП часто изображают в виде неоднородной массы, состоящей из различных компонентов, в передней стенке нижнего сегмента матки [21]. В этих условиях БКШ трудно дифференцировать от трофобластических опухолей [22]. Во втором случае с помощью TVS была обнаружена сильно васкуляризированная гетерогенная масса, что привело к ошибочному диагнозу трофобластической опухоли, как и в предыдущем исследовании [23].
CEUS широко используется в клинической практике и включает микропузырьковое контрастное вещество, вводимое в виде болюса через локтевые вены для определения васкуляризации целевого поражения с очевидными преимуществами в визуализации кровотока [24].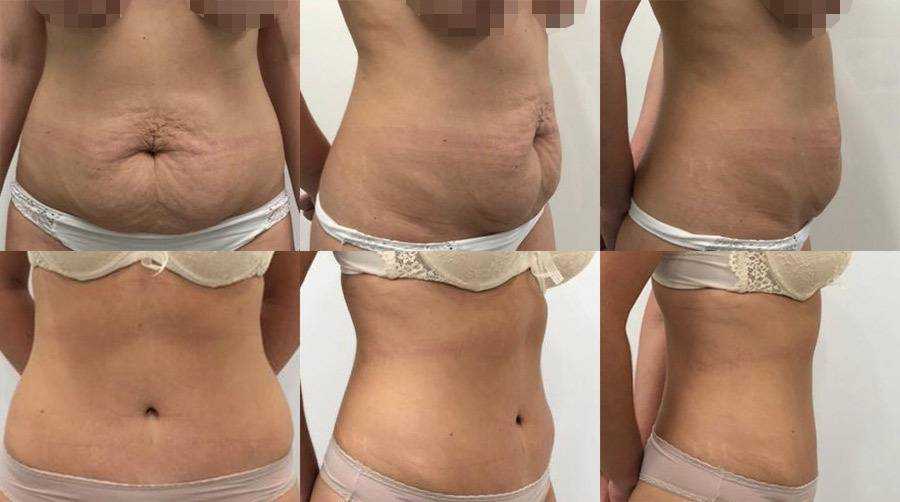 Ультразвуковые изображения CSP показывают образование с периферическим богатым кровотоком в рубце после кесарева сечения. После инъекции контраста поражения могут быть значительно увеличены. Что касается особенностей богатого кровотока, CEUS продемонстрировала более высокую диагностическую и классификационную эффективность для CSP по сравнению с TVS за счет более точного определения местоположения плодного яйца (GS), диапазона, глубины и картины микроциркуляции [25]. В первом случае для обнаружения больших образований в перешейке матки использовалось обычное ультразвуковое исследование, а CDFI показала богатые сигналы кровотока вокруг образований. CEUS показала быстрое усиление области вокруг новообразования в артериальной фазе, в то время как в венозной фазе оно немного отступило, но по-прежнему показало гиперконтрастирование. В сочетании с анамнезом пациента и локализацией поражения КУУЗИ показало высокую вероятность диагноза трофобластической опухоли. К сожалению, второй пациент не был обследован с помощью CEUS.
Ультразвуковые изображения CSP показывают образование с периферическим богатым кровотоком в рубце после кесарева сечения. После инъекции контраста поражения могут быть значительно увеличены. Что касается особенностей богатого кровотока, CEUS продемонстрировала более высокую диагностическую и классификационную эффективность для CSP по сравнению с TVS за счет более точного определения местоположения плодного яйца (GS), диапазона, глубины и картины микроциркуляции [25]. В первом случае для обнаружения больших образований в перешейке матки использовалось обычное ультразвуковое исследование, а CDFI показала богатые сигналы кровотока вокруг образований. CEUS показала быстрое усиление области вокруг новообразования в артериальной фазе, в то время как в венозной фазе оно немного отступило, но по-прежнему показало гиперконтрастирование. В сочетании с анамнезом пациента и локализацией поражения КУУЗИ показало высокую вероятность диагноза трофобластической опухоли. К сожалению, второй пациент не был обследован с помощью CEUS.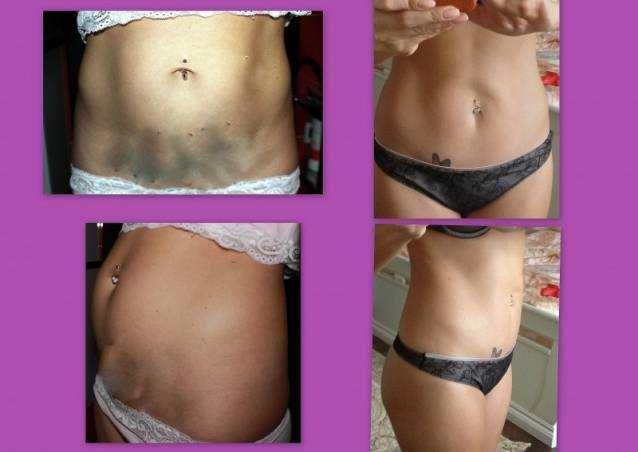 Поскольку у пациентки в анамнезе были нерегулярные вагинальные кровотечения и образование в перешейке матки с богатым сигналом кровотока (рис. 2), после ТВС было ошибочно диагностировано поражение как трофобластическая опухоль.
Поскольку у пациентки в анамнезе были нерегулярные вагинальные кровотечения и образование в перешейке матки с богатым сигналом кровотока (рис. 2), после ТВС было ошибочно диагностировано поражение как трофобластическая опухоль.
Во втором случае образование располагалось в перешейке матки. CDFI выявил сигналы периферического богатого кровотока в поражении
Изображение в натуральную величину
ГТД будет продуцировать избыточный уровень β-ХГЧ, в результате чего уровень в 3-100 раз выше, чем при нормальной беременности, и разница между внематочной беременностью и внематочной беременностью нормальная внутриматочная беременность – это аномально медленное повышение или снижение уровня β-ХГЧ. ГТН следует рассматривать, когда у пациента наблюдается неадекватное снижение уровня β-ХГЧ в сыворотке после выскабливания пузырного заноса или высокий уровень β-ХГЧ, особенно более 100 000 МЕ/л. Диагноз CSP основывается только на положительном тесте на беременность и сонографических критериях [16]. Корреляция с уровнями β-ХГЧ имеет жизненно важное значение для проведения дифференциальной диагностики, которая учитывает другие состояния, которые могут имитировать ЗГТ, такие как миомы, задержка продуктов зачатия, воспалительные заболевания органов малого таза, артериовенозные мальформации и другие злокачественные новообразования матки. Позже оба пациента прошли МРТ-обследование в сочетании с измерением β-ХГЧ для установления правильного диагноза. В настоящее время МРТ может служить дополнительным методом для постановки точного диагноза. Если МРТ по-прежнему не может подтвердить диагноз, необходимо тщательно провести гистероскопию и при необходимости провести профилактическую эмболизацию маточных артерий.
Корреляция с уровнями β-ХГЧ имеет жизненно важное значение для проведения дифференциальной диагностики, которая учитывает другие состояния, которые могут имитировать ЗГТ, такие как миомы, задержка продуктов зачатия, воспалительные заболевания органов малого таза, артериовенозные мальформации и другие злокачественные новообразования матки. Позже оба пациента прошли МРТ-обследование в сочетании с измерением β-ХГЧ для установления правильного диагноза. В настоящее время МРТ может служить дополнительным методом для постановки точного диагноза. Если МРТ по-прежнему не может подтвердить диагноз, необходимо тщательно провести гистероскопию и при необходимости провести профилактическую эмболизацию маточных артерий.
Эти два случая с совершенно разными диагнозами имели чрезвычайно схожие ультразвуковые изображения и клинические проявления, что усложняло клиническую диагностику. Таким образом, в клинической практике у женщин детородного возраста с нерегулярными вагинальными кровотечениями, болями в животе, новообразованиями в малом тазу и аномальными уровнями β-ХГЧ в крови следует учитывать возможность ХСП или ГТН в особых отделах матки при определении дифференциальная диагностика. У пациенток с нерегулярными вагинальными кровотечениями после предшествующего КС, когда ТВС показывает образование в нижней части передней стенки матки, следует учитывать связь между образованием и рубцом на матке. Когда образование слишком велико, чтобы его можно было различить, можно рассмотреть возможность проведения дополнительной МРТ для определения конкретного местоположения образования. Если очаг локализуется в рубце на матке и уровень β-ХГЧ в крови несколько повышен или снижен, можно предположить рубцовую беременность, но если очаг локализуется не в рубце на матке, а в миометрии и аномальное повышение β в крови -Уровни ХГЧ очевидны, следует рассмотреть GTN. Однако, если МРТ показывает, что поражение расположено в рубце на матке, а уровень β-ХГЧ в крови пациентки аномально высок, следует рассматривать более редкое заболевание, такое как ГТН в области кесарева сечения.
У пациенток с нерегулярными вагинальными кровотечениями после предшествующего КС, когда ТВС показывает образование в нижней части передней стенки матки, следует учитывать связь между образованием и рубцом на матке. Когда образование слишком велико, чтобы его можно было различить, можно рассмотреть возможность проведения дополнительной МРТ для определения конкретного местоположения образования. Если очаг локализуется в рубце на матке и уровень β-ХГЧ в крови несколько повышен или снижен, можно предположить рубцовую беременность, но если очаг локализуется не в рубце на матке, а в миометрии и аномальное повышение β в крови -Уровни ХГЧ очевидны, следует рассмотреть GTN. Однако, если МРТ показывает, что поражение расположено в рубце на матке, а уровень β-ХГЧ в крови пациентки аномально высок, следует рассматривать более редкое заболевание, такое как ГТН в области кесарева сечения.
Наличие данных и материалов
Не применимо
Сокращения
- ГТН:
Гестационная трофобластическая неоплазия
- ВОЗ:
Всемирная организация здравоохранения
- ТС:
Кесарево сечение
- CSP:
Кесарево сечение в рубце при беременности
- CDFI:
Цветная доплеровская проточная визуализация
- РИ:
Индекс сопротивления
- CEUS:
УЗИ с контрастированием
- МРТ:
Магнитно-резонансная томография
- ТВС:
Трансвагинальное УЗИ
- Общий номер:
Гестационный мешок
Ссылки
Кали Г., Тимор-Трич И.Е., Паласиос-Харакемада Дж., Монтеагудо А., Бука Д., Форлани Ф., Фамилиари А., Скамбия Г., Ачарья Г., Д’Антонио Ф. Исход кесарева сечения при беременности с рубцом, управляемой выжидательно: систематический обзор и метаанализ. УЗИ Акушерство Гинекол. 2018;51(2):169–75.
Артикул КАС Google Scholar
Раджакумар С., Агарвал С., Халил Х., Фунг Ки Фунг К.М., Шенасса Х., Сингх С.С. Беременность с шрамом от кесарева сечения. J Obstet Gynaecol Can. 2015;37(3):199.
Артикул Google Scholar
«>Tantbirojn P, Crum Crum, Parast M. Патофизиология плаценты: роль децидуальной оболочки и вневорсинчатого трофобласта. Плацента. 2008;29(7):639–45.
Артикул КАС Google Scholar
Миллер Р., Тимор-Трич И., Гьямфи-Баннерман С. Общество медицины матери и плода (SMFM), серия консультаций № 49: Кесарево сечение при беременности с рубцом. Американский журнал акушерства и гинекологии. 2020;222(5):B2–14.
Артикул КАС Google Scholar
Тимор-Трич И., Монтеагудо А., Сантос Р., Цымбал Т., Пинеда Г., Арслан А. Диагностика, лечение и последующее наблюдение за беременностью после кесарева сечения.
 Американский журнал акушерства и гинекологии. 2012;207(1):44.e41-13.
Американский журнал акушерства и гинекологии. 2012;207(1):44.e41-13.Артикул Google Scholar
Ротас М.А., Хаберман С., Левгур М. Внематочная беременность с шрамом от кесарева сечения: этиология, диагностика и лечение. Акушерство Гинекол. 2006;107(6):1373–81.
Артикул Google Scholar
Тимор-Трич И.Е., Монтеагудо А. Непредвиденные последствия увеличения числа кесаревых сечений: раннее приращение плаценты и кесарево рубцовая беременность. Обзор. Am J Obstet Gynecol. 2012;207(1):14–29.
Артикул Google Scholar
Берч Петерсен К., Хоффманн Э., Рифбьерг Ларсен С., Сварре Нильсен Х. Кесарево сечение при рубцовой беременности: систематический обзор исследований по лечению. Фертил Стерил. 2016;105(4):958–67.
Артикул Google Scholar
«>Сорби Ф., Систи Г., Пьералли А., Ди Томмазо М., Ливи Л., Буккольеро А., Фамбрини М. Цервикоистмическая хориокарцинома, имитирующая шрам от кесарева сечения при внематочной беременности. Журнал исследований в области медицинских наук: официальный журнал Исфаханского университета медицинских наук. 2013;18(10):914–7.
Google Scholar
Гольдштейн Д.П., Берковиц Р.С. Современное лечение гестационной трофобластической неоплазии. Hematol Oncol Clin North Am. 2012;26(1):111–31.
Артикул Google Scholar
Комитет FO. Стадии FIGO для гестационной трофобластической неоплазии 2000. Комитет по онкологии FIGO.
 Int J Gynaecol Obstet. 2002;77(3):285–7.
Int J Gynaecol Obstet. 2002;77(3):285–7.Артикул Google Scholar
Wang X, Li Y, Yang J, He Y, Wang M, Wan X, Xiang Y. Выявление и лечение гестационной трофобластической неоплазии, расположенной в кесаревом рубце. Int J Gynaecol Obstet. 2018;141(2):222–7.
Артикул КАС Google Scholar
Тимор-Трич И.Е., Монтеагудо А., Кали Г., Д’Антонио Ф., Каэлин Агтен А. Беременность со шрамом от кесарева сечения: диагностика и патогенез. Obstet Gynecol Clin North Am. 2019;46(4):797–811.
Артикул Google Scholar
Верри Д., Пасчуто Т., Эпштейн Э., Фрушио Р., Масилини Ф., Моро Ф., Скамбия Г., Валентин Л., Теста А.С. ГЕСТАЦИОННАЯ ТРОФОБЛАСТНАЯ НЕОПЛАЗИЯ Ультразвуковая оценка: исследование TITANIUM. Int J Gynecol Рак. 2019;29(7):1216–20.
Артикул Google Scholar
«>Asmar FTC, Braga-Neto AR, de Rezende-Filho J, Villas-Boas JMS, Charry RC, Maesta I. Параметры допплеровской скорости потока маточной артерии для прогнозирования гестационной трофобластической неоплазии после полного пузырного заноса, проспективное когортное исследование. Клиники. 2017;72(5):284–8.
Артикул Google Scholar
Дханда С., Рамани С., Тхакур М. Гестационная трофобластическая болезнь: мультимодальный подход к визуализации, влияющий на диагностику и лечение. Радиол Рес Практ. 2014;2014:842751.
ПабМед ПабМед Центральный Google Scholar
«>Имбар Т., Блум А., Ушаков Ф., Ягель С. Эмболизация маточных артерий для остановки кровотечения после прерывания беременности, имплантированных в рубец после кесарева сечения. J УЗИ Мед. 2003;22(10):1111–5.
Артикул Google Scholar
Weimin W, Wenqing L. Влияние ранней беременности на предыдущий шрам от кесарева сечения в нижнем сегменте. Int J Gynaecol Obstet. 2002;77(3):201–7.
Артикул КАС Google Scholar
Sidhu PS, Cantisani V, Dietrich CF, Gilja OH, Saftoiu A, Bartels E, Bertolotto M, Calliada F, Clevert DA, Cosgrove D, et al. Руководство и рекомендации EFSUMB по клинической практике ультразвукового исследования с контрастным усилением (CEUS) при непеченочных исследованиях: обновление 2017 г.
 (длинная версия). Ультрашалл Мед. 2018;39(2): e2–44.
(длинная версия). Ультрашалл Мед. 2018;39(2): e2–44.Артикул Google Scholar
Wu Y, Zhou L, Chen L, Zhou Q, Zeng T. Эффективность УЗИ с контрастным усилением для диагностики типа беременности с рубцом после кесарева сечения. Медицина. 2019;98(44):e17741.
Артикул Google Scholar
Lumbiganon P, Laopaiboon M, Gulmezoglu AM, Souza JP, Taneepanichskul S, Ruyan P, Attygalle DE, Shrestha N, Mori R, Nguyen DH, et al. Способ родоразрешения и исходы беременности в Азии: глобальное исследование ВОЗ по материнскому и перинатальному здоровью, 2007–2008 гг. Ланцет. 2010;375(9713): 490–9.
Артикул Google Scholar
Кхунда А., Тай Дж. Беременность с шрамом от кесарева сечения. BJOG: международный журнал акушерства и гинекологии. 2007; 114(10):1304. автор ответ 1304.
Статья КАС Google Scholar
Цянь ZD, Чжу XM. Хориокарцинома кесарева сечения: клинический случай и обзор литературы. Евр J Med Res. 2014;19:25.
Артикул Google Scholar
Лин Л.Х., Бернардес Л.С., Хасэ Э.А., Фусида К., Франциско Р.П. Полезна ли ультразвуковая допплерография для оценки гестационной трофобластической болезни? Клиники. 2015;70(12):810–5.
Артикул Google Scholar
Rygh AB, Greve OJ, Fjetland L, Berland JM, Eggebo TM. Артериовенозная мальформация как следствие рубцовой беременности. Acta Obstet Gynecol Scand. 2009;88(7):853–5.
Артикул Google Scholar
Ссылки на скачивание
Благодарности
Неприменимо.
Финансирование
Работа выполнена при поддержке программы Фонда естественных наук провинции Чжэцзян (LZ20h280001). Спонсор не играл никакой роли в разработке исследования и интерпретации данных, а также в написании рукописи.
Информация об авторе
Авторы и организации
Отделение УЗИ, Первая дочерняя больница, Медицинский колледж, Чжэцзянский университет, № 79 Цинчунь Роуд, провинция Чжэцзян, 310003, Ханчжоу, КНР
Линь-Хоу Z , Xiao-dan Zhu, Jian Jiang & Tian-an Jiang
Авторы
- Lin-yu Zhou
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Академия
- Xiao-dan Zhu
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Jian Jiang
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Tian-an Jiang
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
Взносы
LYZ подготовила рукопись; XDZ организовал данные пациента; JJ рассмотрел и отредактировал рукопись; TAJ пересмотрел рукопись.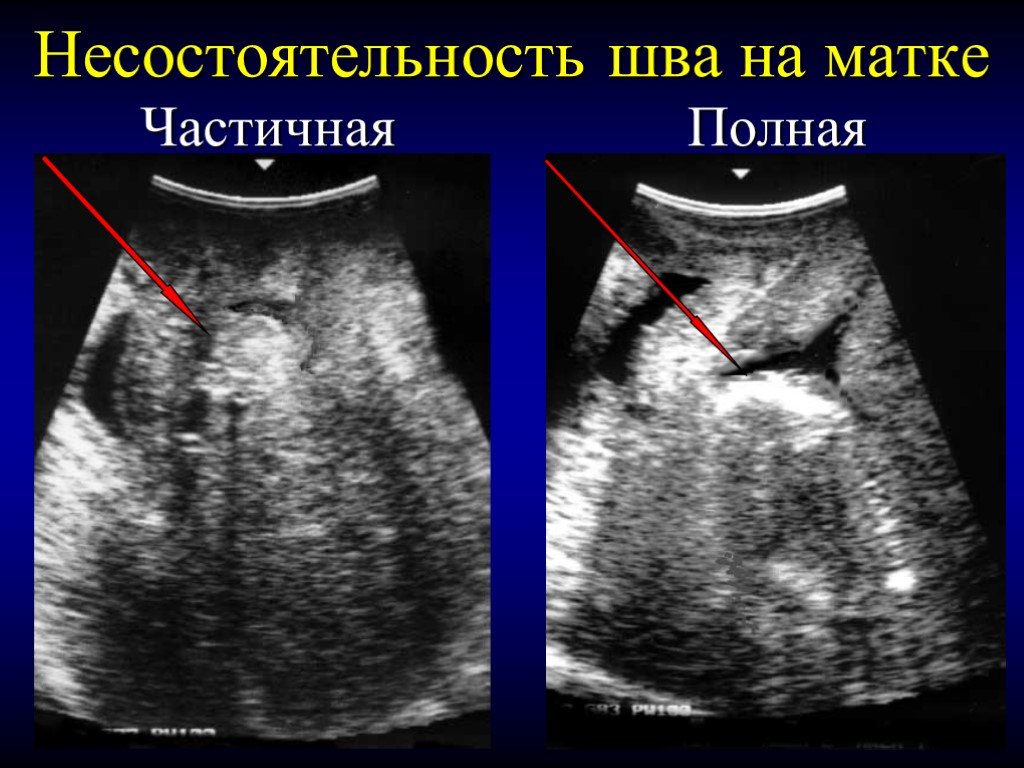 Все авторы прочитали и одобрили окончательный вариант.
Все авторы прочитали и одобрили окончательный вариант.
Автор, ответственный за переписку
Тянь-ань Цзян.
Декларация этики
Одобрение этики и согласие на участие
Неприменимо.
Согласие на публикацию
От пациента было получено письменное информированное согласие на публикацию данного отчета о клиническом случае и любых сопутствующих изображений. Копия письменного согласия доступна для ознакомления редактору этого журнала.
Конкурирующие интересы
Авторы заявляют, что у них нет конкурирующих интересов.
Дополнительная информация
Примечание издателя
Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности.
Права и разрешения
Открытый доступ Эта статья находится под лицензией Creative Commons Attribution 4.0 International License, которая разрешает использование, совместное использование, адаптацию, распространение и воспроизведение на любом носителе или в любом формате, при условии, что вы укажете соответствующую ссылку на оригинальный автор(ы) и источник, предоставьте ссылку на лицензию Creative Commons и укажите, были ли внесены изменения. Изображения или другие сторонние материалы в этой статье включены в лицензию Creative Commons на статью, если иное не указано в кредитной строке материала. Если материал не включен в лицензию Creative Commons статьи, а ваше предполагаемое использование не разрешено законом или выходит за рамки разрешенного использования, вам необходимо получить разрешение непосредственно от правообладателя. Чтобы просмотреть копию этой лицензии, посетите http://creativecommons.org/licenses/by/4.0/. Отказ Creative Commons от права на общественное достояние (http://creativecommons.org/publicdomain/zero/1.0/) применяется к данным, представленным в этой статье, если иное не указано в кредитной линии данных.
Изображения или другие сторонние материалы в этой статье включены в лицензию Creative Commons на статью, если иное не указано в кредитной строке материала. Если материал не включен в лицензию Creative Commons статьи, а ваше предполагаемое использование не разрешено законом или выходит за рамки разрешенного использования, вам необходимо получить разрешение непосредственно от правообладателя. Чтобы просмотреть копию этой лицензии, посетите http://creativecommons.org/licenses/by/4.0/. Отказ Creative Commons от права на общественное достояние (http://creativecommons.org/publicdomain/zero/1.0/) применяется к данным, представленным в этой статье, если иное не указано в кредитной линии данных.
Перепечатки и разрешения
Об этой статье
Эндометриоз после кесарева сечения: симптомы, лечение и рубцы
Кесарево сечение, также известное как кесарево сечение, является фактором риска развития эндометриоза. Эндометриоз после кесарева сечения остается относительно редким, но это потенциальное осложнение, которое женщины должны обсудить со своим врачом.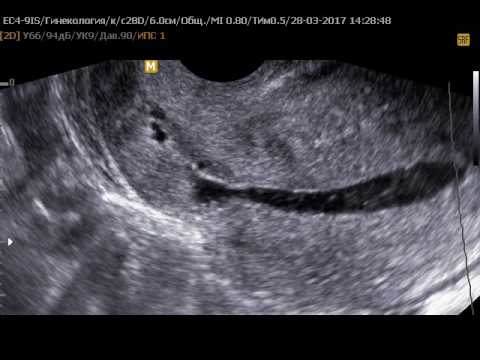
Ткань эндометрия обычно выстилает матку. Классический эндометриоз возникает, когда эндометриоподобная ткань развивается вне матки.
Это может вызвать образование спаек или рубцовой ткани. Они могут разрастаться в большие массы или в полосы, образующиеся между органами.
Когда эндометриоз вызывает либо воспаление, либо рубцовую ткань, у женщины могут быть обильные или болезненные менструации, а также боль между менструациями.
Во время беременности женщина, уже живущая с эндометриозом, может обнаружить, что симптомы эндометриоза временно улучшаются. Это может быть связано с повышением уровня прогестерона в организме во время беременности.
Однако это может быть верно не для каждого человека. В некоторых случаях облегчение боли может быть больше связано с отсутствием менструального цикла во время беременности. Некоторые люди могут не чувствовать облегчения боли во время беременности.
Имеются также данные о том, что эндометриоз может развиться после кесарева сечения у людей, у которых не было этого заболевания до родов.
В этой статье обсуждается эндометриоз после кесарева сечения, в том числе то, как врачи диагностируют и лечат это заболевание.
Эндометриоз может развиться после кесарева сечения, когда он развивается внутри операционного рубца, что известно как послеоперационный эндометриоз.
Инцизионный эндометриоз встречается редко. Частота заболевания составляет всего 0,03-0,45%. Тем не менее, авторы отчета за 2017 год предполагают, что врачи чаще сталкиваются с эндометриозом, связанным с рубцами после кесарева сечения, поскольку количество кесаревых сечений растет.
Число также может быть выше, потому что не все люди могут знать, что у них эндометриоз после кесарева сечения, и могут не сообщать об этом.
Когда хирург выполняет кесарево сечение, ткань эндометрия разрезается и может выйти за пределы матки. Ткань эндометрия может имплантироваться в область послеоперационного рубца.
Затем ткань эндометрия нарастает вдоль рубца, что приводит к болезненным спайкам, которые могут повлиять на фертильность человека или сделать менструации более болезненными. Кроме того, человек может испытывать воспаление, боль и кровотечение из очагов эндометриоза.
Кроме того, человек может испытывать воспаление, боль и кровотечение из очагов эндометриоза.
Хирургия может эффективно лечить многие случаи инцизионного эндометриоза, поскольку она включает удаление воспалительной ткани эндометрия.
Инцизионный эндометриоз может вызывать циклическую боль, отек и коричневые выделения в месте рубца во время менструации. Кроме того, у человека могут наблюдаться стандартные симптомы эндометриоза.
К ним относятся:
- сильная боль во время менструации
- боль или спазмы между менструациями
- боль во время секса
- болезненные движения кишечника
- кровотечение между менструациями0004
- необъяснимая боль в желудке, диарея или запор
- боль в мочевом пузыре, напоминающая инфекцию мочевого пузыря или мочевыводящих путей
Человек, испытывающий любой из этих симптомов, должен обратиться к врачу, чтобы исключить эндометриоз или другое заболевание, которое может вызывать подобные симптомы.
Многие люди с эндометриозом годами ждут постановки диагноза.
Исследование, проведенное в 2017 году, показало, что среднее время между появлением симптомов и постановкой диагноза в США составляет 4,4 года. Молодые женщины, как правило, ждали постановки диагноза дольше, чем женщины старшего возраста.
Однако, по данным Американского фонда эндометриоза, возможна задержка диагностики эндометриоза до 9 лет после появления симптомов. В случаях послеоперационного эндометриоза врачам может потребоваться больше времени, чтобы диагностировать состояние, поскольку оно встречается редко и до сих пор широко не изучено.
Как правило, для обеспечения быстрого и точного диагноза людям, которые подозревают эндометриоз, может потребоваться обратиться к своему гинекологу, в частности спросить о тестах на эндометриоз или обратиться за вторым мнением.
Обычно врачи собирают полную историю болезни и проводят гинекологический осмотр перед тестированием. Затем человеку может потребоваться пройти несколько тестов, чтобы получить точный диагноз.
Во время осмотра врач может почувствовать спайки или разрастания эндометрия, хотя это бывает редко. Если человек испытывает необычную боль во время гинекологического осмотра, это также может быть признаком эндометриоза.
Если гинекологический осмотр заставляет врача заподозрить эндометриоз, другие анализы могут подтвердить диагноз. К ним относятся:
- УЗИ органов малого таза : Во время этой процедуры врач использует звуковые волны для осмотра матки и окружающих органов. Они могут ввести небольшой датчик во влагалище, чтобы лучше рассмотреть его, или использовать датчик только снаружи живота.
- Биопсия : Врач может использовать иглу для удаления небольшого участка ткани эндометрия. Тестирование этого образца может помочь исключить другие проблемы, такие как раковые новообразования.
- Исследовательская хирургия : Хирургия, такая как лапароскопия, является единственным способом, которым врач может точно диагностировать эндометриоз в брюшной стенке.
 Тем не менее, можно диагностировать послеоперационный эндометриоз с помощью УЗИ, МРТ и, как правило, путем выполнения нового разреза на месте старого разреза и удаления ткани. Затем патологоанатом исследует ткань, чтобы подтвердить состояние.
Тем не менее, можно диагностировать послеоперационный эндометриоз с помощью УЗИ, МРТ и, как правило, путем выполнения нового разреза на месте старого разреза и удаления ткани. Затем патологоанатом исследует ткань, чтобы подтвердить состояние.
Эндометриоз — это хроническое заболевание, неизлечимое. В случаях эндометриоза после кесарева сечения наиболее вероятным методом лечения является операция по удалению эндометриоза. Это также более вероятно, если человек хочет снова зачать ребенка.
В целом при эндометриозе операция не всегда является первым методом лечения. Существуют и другие методы лечения, которые могут помочь некоторым людям в зависимости от их конкретных симптомов. Некоторые методы лечения могут также предотвратить ухудшение состояния эндометриоза. Врач может порекомендовать:
- безрецептурные или отпускаемые по рецепту обезболивающие препараты.
- альтернативные методы обезболивания, такие как иглоукалывание или лечебный массаж
- Гормональные противозачаточные таблетки содержат прогестерон, который является гормоном, который может помочь предотвратить рост ткани эндометрия.
 Узнайте больше о противозачаточных средствах при эндометриозе.
Узнайте больше о противозачаточных средствах при эндометриозе. - Гормональные контрацептивы, не содержащие прогестерон, такие как агонисты или антагонисты гонадотропин-высвобождающего гормона (ГнРГ).
В тяжелых случаях люди, которые не хотят забеременеть, могут выбрать гистерэктомию, то есть операцию по удалению матки. Это может также включать двустороннюю сальпингоофорэктомию (БСО), при которой хирург также удаляет яичники.
Узнайте о новых рекомендациях по диагностике и лечению эндометриоза.
Эндометриоз является хроническим заболеванием, но хирургическое и медикаментозное лечение может помочь справиться с симптомами.
Люди, которые использовали лекарства, такие как прогестерон, для контроля эндометриоза, часто испытывают симптомы после прекращения лечения.
Даже у людей, перенесших операцию, эндометриоз может вернуться. Лечение прогестероном или агонистами и антагонистами ГнРГ может снизить риск рецидива или замедлить рост новообразований.
Гистерэктомия сама по себе может значительно снизить риск рецидива. Исследования 2020 года показали, что доля женщин, живущих с эндометриозом и испытывающих боль, после гистерэктомии снизилась на 28%.0037
Тем не менее, более ранние исследования показали, что у 62% участников наблюдались симптомы эндометриоза даже после гистерэктомии, но с сохранением яичников. Это означает, что в некоторых случаях человеку также может потребоваться удаление яичников.
Однако удаление яичников сопряжено с риском для здоровья. Человек должен принять решение о том, нужна ли ему операция и какая операция лучше всего, проконсультировавшись со своим врачом.
Опасен ли рубцовый эндометриоз?
Инцизионный эндометриоз может вызывать боль и дискомфорт. Но это состояние настолько редкое, что недостаточно данных, чтобы указать, опасно ли оно. В крайне редких случаях состояние может стать злокачественным, то есть раковым.
Почему мой шрам от кесарева сечения болит годы спустя?
Через несколько лет после кесарева сечения человек не должен испытывать боли в области рубца.

 В полость матки вводится физиологический раствор, это позволяет получить объективную информацию о состоянии рубца, характере кровотока в рубце и резерве интактного миометрия.
В полость матки вводится физиологический раствор, это позволяет получить объективную информацию о состоянии рубца, характере кровотока в рубце и резерве интактного миометрия.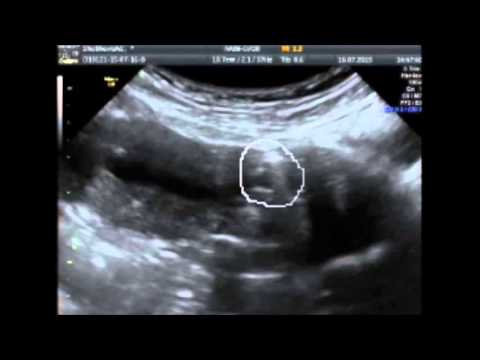 Американский журнал акушерства и гинекологии. 2012;207(1):44.e41-13.
Американский журнал акушерства и гинекологии. 2012;207(1):44.e41-13. Int J Gynaecol Obstet. 2002;77(3):285–7.
Int J Gynaecol Obstet. 2002;77(3):285–7. (длинная версия). Ультрашалл Мед. 2018;39(2): e2–44.
(длинная версия). Ультрашалл Мед. 2018;39(2): e2–44.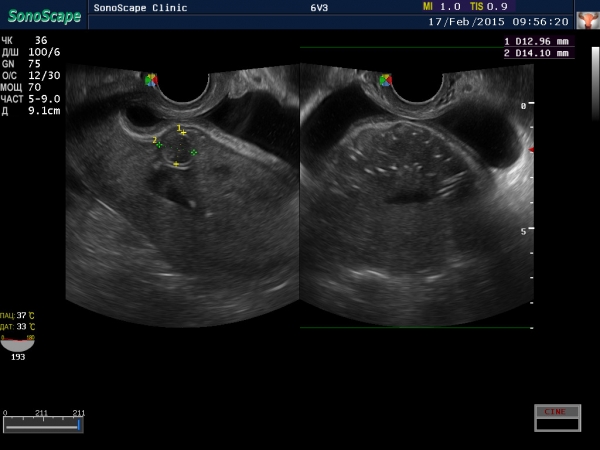 Тем не менее, можно диагностировать послеоперационный эндометриоз с помощью УЗИ, МРТ и, как правило, путем выполнения нового разреза на месте старого разреза и удаления ткани. Затем патологоанатом исследует ткань, чтобы подтвердить состояние.
Тем не менее, можно диагностировать послеоперационный эндометриоз с помощью УЗИ, МРТ и, как правило, путем выполнения нового разреза на месте старого разреза и удаления ткани. Затем патологоанатом исследует ткань, чтобы подтвердить состояние. Узнайте больше о противозачаточных средствах при эндометриозе.
Узнайте больше о противозачаточных средствах при эндометриозе.