Исследование белка в кале
АНМО «Ставропольский краевой клинический консультативно-диагностический центр»:
355017, г. Ставрополь, ул. Ленина 304(8652) 951-951, (8652) 35-61-49 (факс)
(8652) 951-951, (8652) 31-51-51 (справочная служба)
Посмотреть подробнееОбособленное подразделение «Диагностический центр на Западном обходе»:
355029 г. Ставрополь, ул. Западный обход, 64(8652) 951-951, (8652) 31-51-51 (контактный телефон)
(8652) 31-68-89 (факс)
Посмотреть подробнееКлиника семейного врача:
355017 г. Ставрополь, пр. К. Маркса, 110 (за ЦУМом)(8652) 951-951, (8652) 31-51-51 (контактный телефон)
(8652) 31-50-60 (регистратура)
Посмотреть подробнее Невинномысск, ул. Низяева 1
Невинномысск, ул. Низяева 1 (86554) 95-777, 8-962-400-57-10 (регистратура)
Посмотреть подробнееОбособленное структурное подразделение в г. Черкесске :
369000, г. Черкесск, ул. Умара Алиева 318(8782) 26-48-02, +7-988-700-81-06 (контактные телефоны)
Посмотреть подробнееОбособленное структурное подразделение в г. Элисте :
358000, г. Элиста, ул. Республиканская, 478(989) 735-42-07 (контактные телефоны)
Посмотреть подробнееЗАО «Краевой клинический диагностический центр»:
355017 г. Ставрополь, ул. Ленина 304(8652) 951-951, (8652) 35-61-49 (факс)
(8652) 951-951, (8652) 31-51-51 (справочная служба)
Посмотреть подробнееОбособленное структурное подразделение на ул. Савченко, 38 корп. 9:
Савченко, 38 корп. 9:
8 (8652) 316-847 (контактный телефон)
Обособленное структурное подразделение на ул. Чехова, 77 :
355000, г. Ставрополь, ул. Чехова, 778(8652) 951-943 (контактный телефон)
Посмотреть подробнееОбособленное структурное подразделение в г. Михайловске:
358000, г. Михайловск, ул. Ленина, 201 (в новом жилом районе «Акварель»).8(988) 099-15-55 (контактный телефон)
Посмотреть подробнееКальпротектин в кале
Кальпротектин – это белок, вырабатывающийся в лейкоцитах, его концентрация в кале прямо пропорционально числу лейкоцитов, попавших в кишечник. Определение количества кальпротектина в кале – исследование, позволяющее диагностировать воспалительные заболевания кишечника.
Синонимы русские
Фекальный кальпротектин, белок нейтрофилов, маркер кишечного воспаления.
Синонимы английские
Calprotectin, CALPRO, Stool Calprotectin, Calprotectin in human faeces.
Метод исследования
Иммуноферментный анализ (ИФА).
Диапазон определения: 25 — 2500 мкг/г.
Единицы измерения
Мкг/г (микрограмм на грамм).
Какой биоматериал можно использовать для исследования?
Кал.
Как правильно подготовиться к исследованию?
- Специальной подготовки не требуется.
Общая информация об исследовании
В медицинской практике определение количества кальпротектина в кале пациента в совокупности с клиническими проявлениями применяется для диагностики воспалительных заболеваний кишечника.
Анализ рекомендуется проводить при подозрении на воспалительные заболевания кишечника (выявление у пациента спазмов, нарушения моторики кишечника, нерегулярного стула с примесью слизи, потери массы тела, лихорадки, повышенной потливости, общей слабости, повышенной утомляемости, артралгий, обильных выделений крови с калом, патологии перианальной области (свищи, абсцессы), запоров, болей в правом нижнем квадранте живота, вокруг пупка, тошноты, рвоты), при необходимости дифференциальной диагностики с синдромом раздраженного кишечника, другими причинами болей в животе, желудочно-кишечного кровотечения.
Измерение количества кальпротектина в образце стула пациента – это простой, неинвазивный способ диагностики воспалительных заболеваний кишечника, позволяющий врачу отличить эту группу заболеваний от синдрома раздраженного кишечника, при котором воспаление слизистой оболочки желудочно-кишечного тракта отсутствует.
Кальпротектин – это белок нейтрофилов. По сути, это протеин, связанный с кальцием. Он составляет более 60 % от общего количества белков, содержащихся в цитоплазме нейтрофильных гранулоцитов (каждый нейтрофил содержит 25 пикограммов кальпротектина). Кальпротектин высвобождается из активированных лейкоцитов, что приводит к увеличению концентрации этого протеина в фекалиях воспалительных заболеваниях соответствующих органов.
Воспалительные заболевания кишечника (ВЗК) возникают вследствие нарушения иммунного ответа хозяина и кишечной микрофлоры. Основными заболеваниями, относящимися к этой группе, являются язвенный колит и болезнь Крона, при которых может поражаться слизистая оболочка любого отдела желудочно-кишечного тракта.
Существует ряд исследований для подтверждения диагноза воспалительных заболеваний кишечника, но ни один из этих методов не является специфическим, и результаты должны оцениваться специалистом в совокупности с данными обследования и клинической картины. Основным в лечении пациентов, страдающих ВЗК, является поэтапная симптоматическая терапия, направленная на заживление дефектов слизистой оболочки желудочно-кишечного тракта, предотвращение осложнений заболевания.
Для чего используется исследование?
- Для обследования пациентов при подозрении на воспалительные заболевания кишечника;
- для дифференциальной диагностики с синдромом раздраженной кишки, другими причинами болей в животе, желудочно-кишечного кровотечения;
- для профилактического обследования здоровых людей.

Когда назначается исследование?
- При выявлении у пациента спазмов, нарушения моторики кишечника, нерегулярного стула с примесью слизи, потери массы тела, лихорадки, повышенной потливости, общей слабости, повышенной утомляемости, артралгий, задержки развития у детей, обильных выделений крови с калом, патологии перианальной области (свищи, абсцессы), запоров, болей в животе (в правом нижнем квадранте живота, вокруг пупка), тошноте, рвоте.
Что означают результаты?
Референсные значения:
Если уровень кальпротектина в кале пациента находится в пределах референсных значений, значит, у него отсутствуют воспалительные заболевания кишечника.
 Также оно может быть следствием следующих патологических состояний: бактериальных и вирусных инфекций ЖКТ (сальмонеллез, кампилобактериоз, аденовирусы, ротавирусы, норовирусы), новообразований кишечника, дивертикулов, муковисцидоза, аллергии к коровьему молоку, целиакии, кишечного кровотечения.
Также оно может быть следствием следующих патологических состояний: бактериальных и вирусных инфекций ЖКТ (сальмонеллез, кампилобактериоз, аденовирусы, ротавирусы, норовирусы), новообразований кишечника, дивертикулов, муковисцидоза, аллергии к коровьему молоку, целиакии, кишечного кровотечения.Копрограмма
Копрограмма позволяет оценить функциональную деятельность желудка, кишечника, печени и поджелудочной железы, выявить наличие воспалительных процессов и дисбактериоза. Этот анализ дает возможность изучить эффективность пищеварительных процессов организма, оценить скорость прохождения пищи по желудочно-кишечному тракту.
Химический анализ кала в рамках копрограммы включает определение содержания крови, билирубина, стеркобилина, реакции рН.
Реакция рН кала преимущественно зависит от жизнедеятельности микрофлоры кишечника. При преобладании белковой пищи и активации бактерий, расщепляющих белок, образуется много аммиака, придающего калу щелочную реакцию.
Наличие крови в кале свидетельствует о патологических процессах в желудочно-кишечном тракте, сопровождающихся изъязвлением слизистой или распадом опухоли.
Стеркобилин – основной пигмент кала, который придает ему определенную окраску. Отсутствие или резкое уменьшение количества стеркобилина в кале (ахоличный кал) чаще всего свидетельствует об обтурации общего желчного протока камнем, сдавлении его опухолью или резком снижении функции печени (например, при остром вирусном гепатите). Увеличение количества стеркобилина в кале возникает при массивном гемолизе эритроцитов (гемолитическая желтуха) или усиленном желчеотделении. Выявление в кале взрослого человека неизмененного билирубина указывает на нарушение процесса восстановления билирубина в кишечнике под действием микробной флоры. Наиболее частыми причинами этого нарушения являются: подавление жизнедеятельности бактерий кишечника под влиянием больших доз антибиотиков (дисбактериоз кишечника), резкое усиление перистальтики кишечника.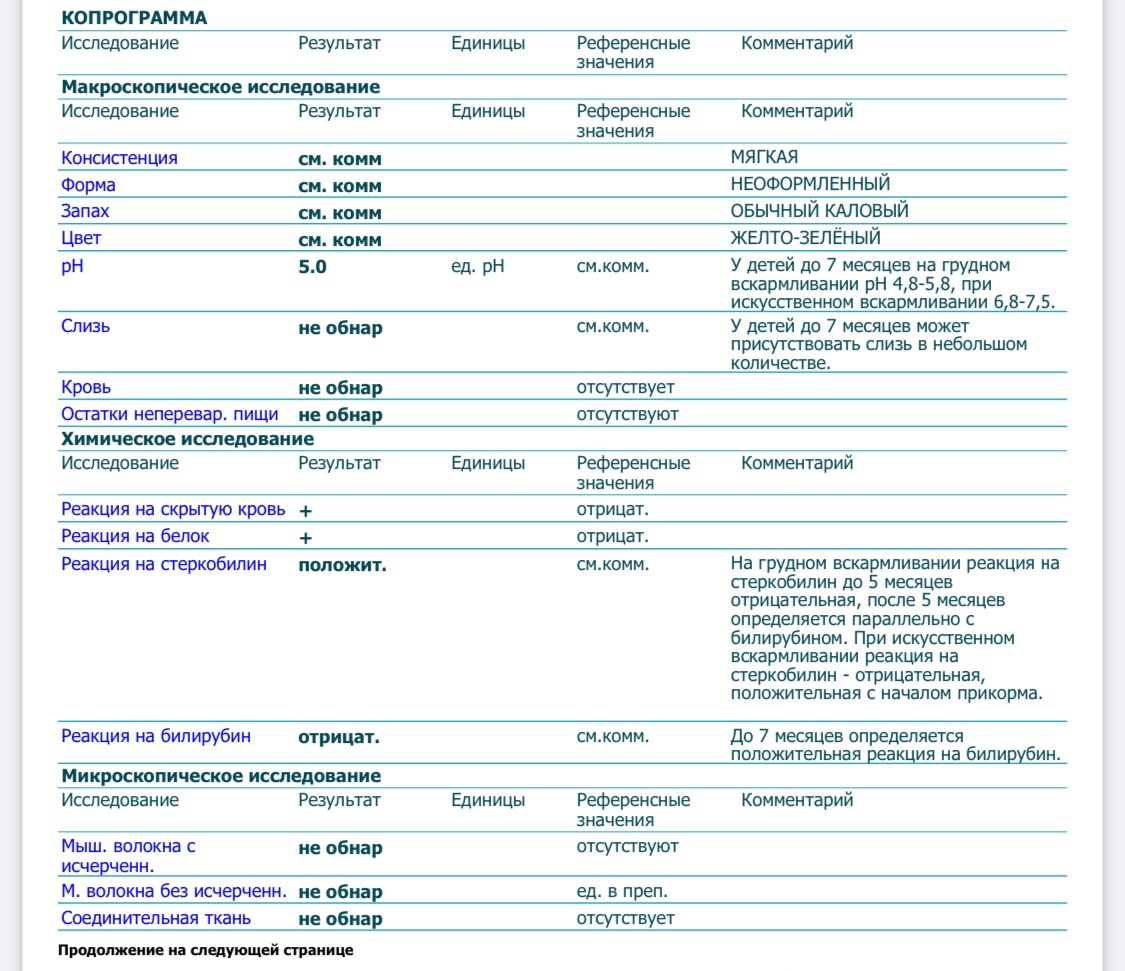
При микроскопическом исследовании в кале можно выявить детрит, остатки пищевых веществ, элементы слизистой оболочки кишечника, клеточные элементы: лейкоциты, эритроциты, макрофаги, опухолевые клетки, кристаллы, яйца гельминтов, паразитирующие в кишечнике простейшие, микроорганизмы. Данные микроскопического исследования могут дать представление о состоянии переваривающей способности кишечника, о состоянии слизистой оболочки (главным образом толстого кишечника).
Детрит составляет основной фон при микроскопии нормального кала, представляет собой остатки пищевых веществ, микроорганизмов, распавшихся клеточных элементов. Он имеет вид аморфных образований мелких размеров, преимущественно зернистой формы.
Слизь в нормальном кале может быть в виде тонкого, малозаметного блестящего налета. При воспалительных процессах обнаруживается в виде тяжей, клочков и плотных, лентовидной формы образований.
Мышечные волокна (остатки белковой пищи) – различают неизмененные и измененные (непереваренные, слабопереваренные, переваренные).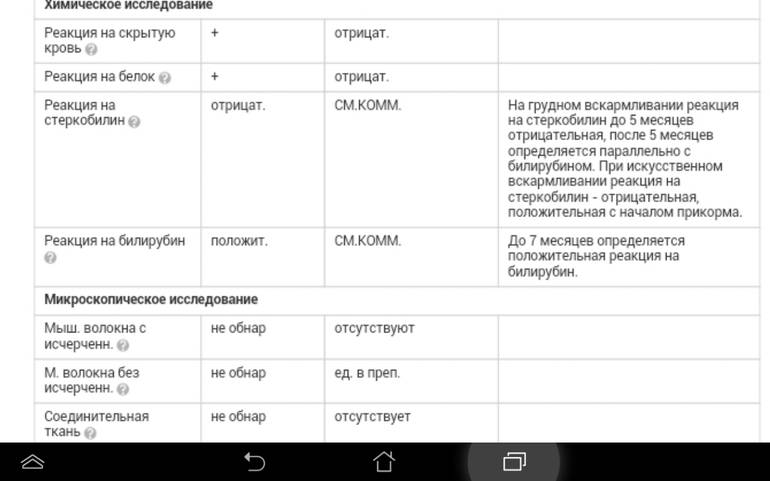 Неизмененные (или непереваренные) волокна желтого цвета, цилиндрической формы с обрезанными концами, имеют поперечную, реже продольную исчерченность. По мере переваривания мышечные волокна теряют исчерченность, поверхность становится гладкой, форма округляется.
Неизмененные (или непереваренные) волокна желтого цвета, цилиндрической формы с обрезанными концами, имеют поперечную, реже продольную исчерченность. По мере переваривания мышечные волокна теряют исчерченность, поверхность становится гладкой, форма округляется.
В нормальном кале немного переваренных мышечных волокон. Большое количество (креаторея) мышечных волокон, особенно непереваренных и слабопереваренных, находят при недостаточности поджелудочной железы, пониженной секреторной функции желудка, ускоренной перистальтике.
Соединительнотканные волокна имеют вид сероватых, преломляющих свет волокон, иногда похожих на тяжи слизи. В нормальном кале не обнаруживаются. Появление их указывает на недостаточность протеолитических ферментов желудка.
Растительная клетчатка и крахмал являются остатками углеводного компонента пищи. Различают два вида клетчатки: перевариваемую и неперевариваемую.
Неперевариваемая клетчатка является опорной клетчаткой (кожица овощей, фруктов, сосуды и волоски растений и т.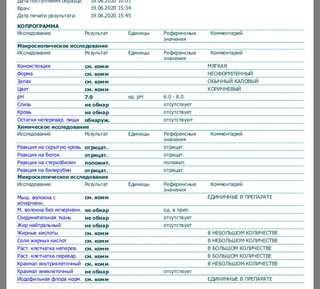 п.), в кишечнике не расщепляется и полностью выделяется с калом. При микроскопии нативных неокрашенных препаратов она имеет разнообразные резкие очертания, правильный рисунок в виде толстых двухконтурных целлюлозных оболочек коричневой, желтой и серой окраски.
п.), в кишечнике не расщепляется и полностью выделяется с калом. При микроскопии нативных неокрашенных препаратов она имеет разнообразные резкие очертания, правильный рисунок в виде толстых двухконтурных целлюлозных оболочек коричневой, желтой и серой окраски.
Перевариваемая клетчатка состоит из округлых больших клеток, имеющих тонкую оболочку и ячеистое строение. При микроскопии перевариваемая клетчатка отличается от неперевариваемой нежными контурами, наличием зерен крахмала или красящих пигментов. В нормальном кале не обнаруживается. Обнаруживается в кале при ускоренной эвакуации.
Крахмал при нормальном пищеварении отсутствует, так как амилолитические ферменты пищеварительного тракта и ферменты бактерий слепой кишки расщепляют крахмал полностью. Присутствие крахмала всегда указывает на недостаточность пищеварения, что бывает при заболеваниях тонкого кишечника и связанной с ними ускоренной эвакуации, при недостаточности поджелудочной железы.
Жир и продукты его расщепления, поступившие с пищей в умеренном количестве, в норме усваиваются почти полностью.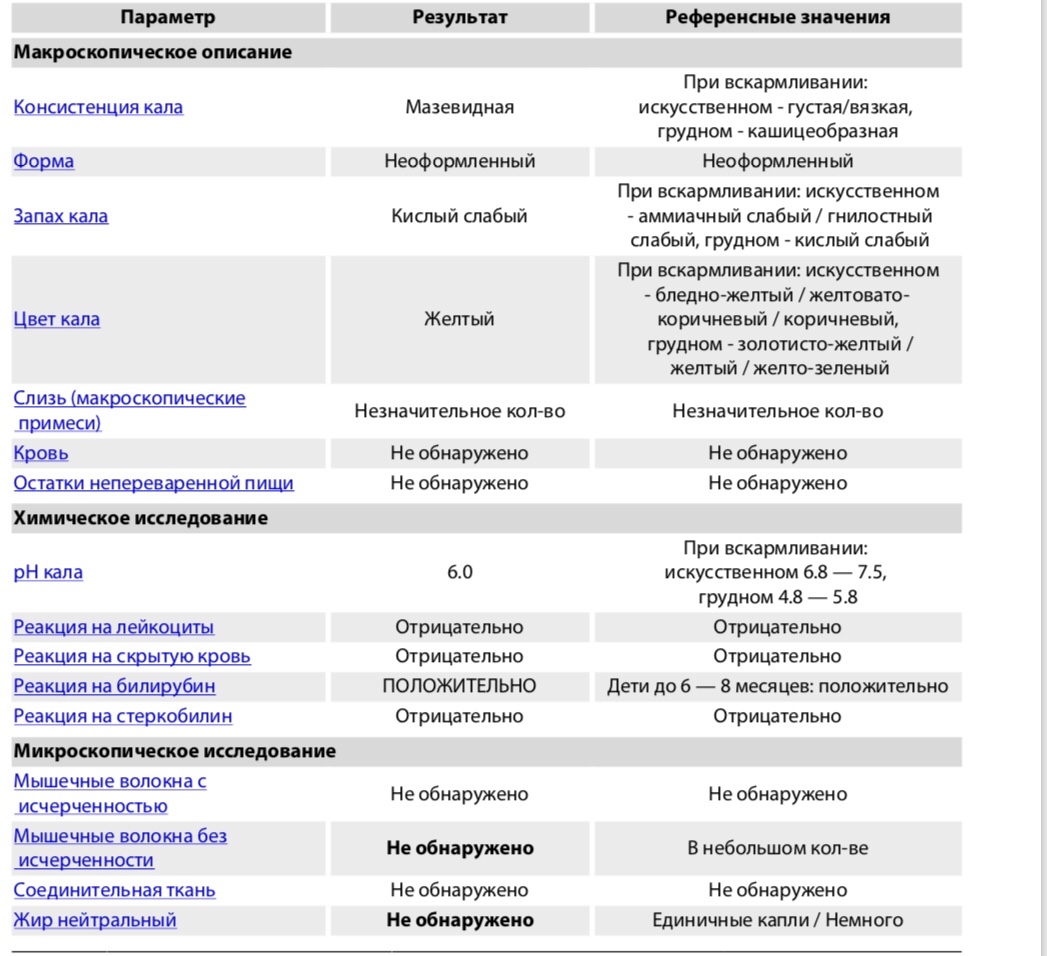 Обнаружение значительного количества нейтрального жира и продуктов его расщепления свидетельствует о нарушении переваривания и всасывании жира. Нейтральный жир в нативных препаратах кала имеет вид бесцветных капель.
Обнаружение значительного количества нейтрального жира и продуктов его расщепления свидетельствует о нарушении переваривания и всасывании жира. Нейтральный жир в нативных препаратах кала имеет вид бесцветных капель.
Жирные кислоты и мыла встречаются в виде глыбок, капель и кристаллов. Кристаллы имеют форму тонких игл, заостренных с двух концов. Часто складываются в небольшие пучки, иногда расположены радиально, окружая венчиком глыбки жирных киcлот. Обнаружение в нативном препарате бесцветных капель, глыбок и игольчатых кристаллов позволяет предположить стеаторею.
Клеточные элементы (кишечный эпителий, клетки крови, макрофаги, клетки опухолей) обнаруживаются в кале, содержащем слизь.
Единичные клетки кишечного эпителия можно встретить и в нормальном кале как следствие физиологического слущивания. Появление этих клеток большими группами, пластами отражает наличие воспаления слизистой оболочки толстого кишечника.
Лейкоциты, располагающиеся в слизи в значительном количестве (скопление), свидетельствуют о воспалительном процессе в толстом кишечнике.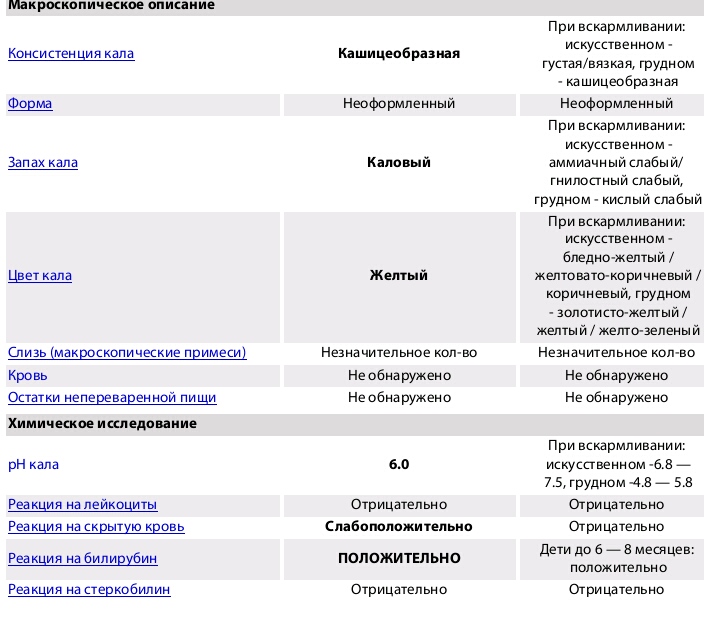 Лейкоциты в слизи, идущей из тонкого кишечника, успевают разрушиться.
Лейкоциты в слизи, идущей из тонкого кишечника, успевают разрушиться.
Эритроциты неизмененные встречаются в кале при кровотечениях из толстого кишечника и прямой кишки. При кровотечении из более высоко лежащих отделов кишечника эритроциты либо совсем разрушаются, либо приобретают характер теней, и распознать их очень трудно.
Макрофаги встречаются при некоторых воспалительных процессах, особенно при бактериальной дизентерии.
Клетки злокачественных опухолей могут попасть в кал при расположении опухоли в прямой кишке. Диагностическое значение имеет нахождение не одиночных клеток, а обрывков ткани, групп клеток, отличающихся характерной атипией.
Кристаллические образования. Кристаллы трипельфосфатов встречаются в резко щелочном кале при усилении гнилостных процессов. Оксалаты кальция обнаруживаются при употреблении в пищу большого количества овощей или при снижении кислотности желудочного сока. Кристаллы Шарко-Лейдена в виде вытянутого ромба часто обнаруживаются в слизи в сочетании с эозинофилами, указывают на аллергическое воспаление кишечника, амебиаз, балантидиаз, глистную инвазию. Кристаллы гематоидина выявляются после кишечного кровотечения при язвенных колитах.
Кристаллы гематоидина выявляются после кишечного кровотечения при язвенных колитах.
белок в кале — 25 рекомендаций на Babyblog.ru
Девочки, всем добрый день!
Нужна Ваша помощь и опыт.
Дочке почти 1,5 месяца. Мы на ГВ
Проблемы с кишечником. Началось все с колик. Но стул при этом был обильный и при каждой смене подгузника в нем было прилично какашек. Но так как в подгузе все впитывается я видела только сухой остаток, а насколько жидкий стул не видела.
А стул жидкий
Далее мы сдаём анализ крови общий, кала (корпорамму) и билирубин (до сих пор не прошла желтушка).
По анализам:
Кровь — повышены эозинофилы и понижены нейтрофилы.
Кал — много слизи и в слизи лейкоцитов 30-35
Билирубин — 138 (при выписке из роддома был 144 — это полтора месяца назад).
Кал на углеводы — 0,1 (норма до 0,25) ЛН исключаем
Ситуация ухудшается и уже дней 5-6 ребёнок почти сам не какает. При смен подгузника в нем какашек по десертной ложке.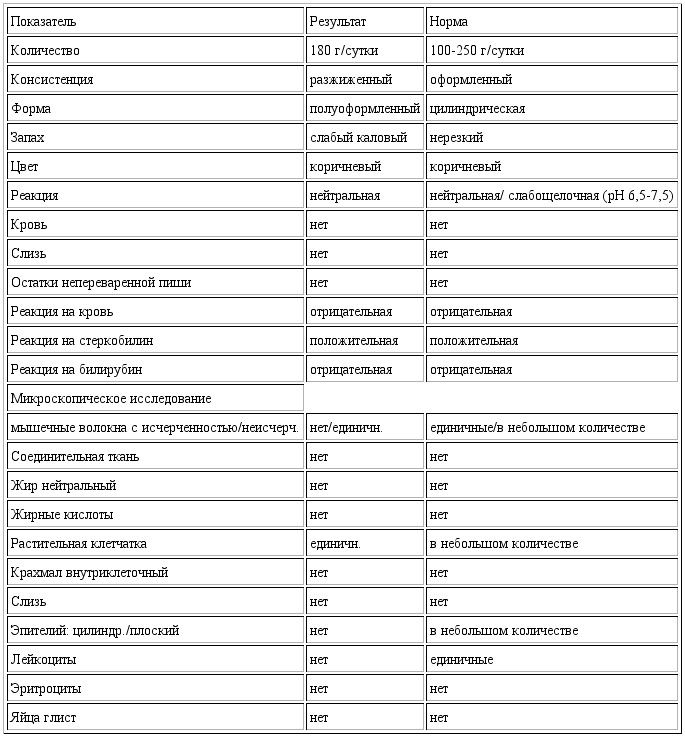 Раньше было очень обильно — по несколько столовых ложек.
Раньше было очень обильно — по несколько столовых ложек.
Утром уже дней 5-6 очень болит животик. Кричит, тужится. Короче ставим трубочку и с газиками выходит оооочень много жидких какашек на пеленку.
Были на приеме у гастроэнтеролога. Она сказала — пищевая аллергия.
Об этом говорит жидкий стул, слизь, повышенные эозинофилы в крови и спрыгивания, которых раньше не было но в последнее время появились.
Ркомендации гастроэнтеролога:
1) Исключить молочный белок. Разрешила только ряженку и йогурт без наполнителя. Предположила что аллергия на молочный белок. Далее понаблюдаем и решим что делать дальше, идти методом тыкв, сдать анализ на аллергены и тд..
2) Пропить курс бактерий — релалайф. До этого пили био гая курс. Прекратили недели 2-3 назад.
3) Урсофальк на 14 дней для снижения билирубина и рекомендовано посетить инфекциониста и исключить инфекции (герпес, цмв и тд). Якобы это может быть причиной высокого билирубина. К инфекционисту идём в субботу.
Диету и до этого соблюдала, но ела молочку. И могла себе позволить блинчик с мясом или кольцо с творогом сладкое.
Вот уже несколько дней ем кашу на воде и пустой чёрной чай с крекером на завтрак.
Одно зеленое яблоко. На обед гречка пустая или макароны с тушеной курицей/индейкой, могу добавить овощи (кабачок, брокколи) и сельдерей или св огурец. На ужин йогурт или стакан ряженки и крекеры.
Жрать хочется пипец как (((. Я готова терпеть, был бы результат но пока его нет.
Прошло 3 дня. Пока ситуация не изменилась. Также какаем обильно утром через трубочку и очень жидко. Все также много слизи. Также болит животик и в последние дни днём беспокойная.
Меня это очень тревожит(((.
Т.к. много запретов по еде несколько недель как подсела на крекеры «Любятово» с солью и за день могу с чаем пачку съесть. Может быть на них аллергия?
Девочки поделитесь может у кого-то была похожая ситуация…
Как вы справились с ситуацией? И через какое время все стабилизировалось?
Может ли билирубин также быть причиной проблем с пищеварением?
Хочу чтобы как можно скорее ребёнок стал какать сам и стул был нормальный!!!
Анализ копрограмма реакция на белок +
Добрый вечер! По данному анализу педиатр ставит нам амебиаз, говорит очень редкое заболевание и незнает чем его лечат в столь раннем возрасте((( Помогите нам пожалуйста.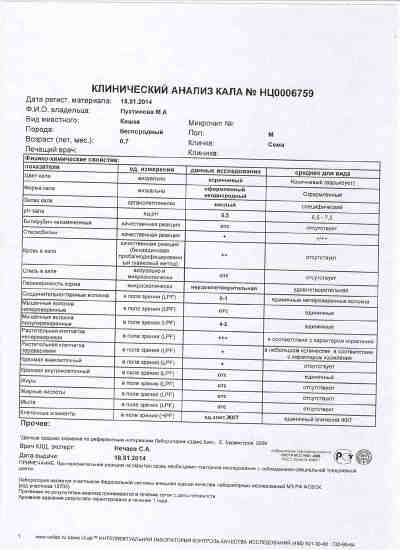 .. Копрограмма: макроскопическое исследование
.. Копрограмма: макроскопическое исследование
Консистенция КАШИЦЕОБРАЗНАЯ
Форма НЕОФОРМЛЕННЫЙ
Запах ОБЫЧНЫЙ КАЛОВЫЙ
Цвет ЖЕЛТО-ЗЕЛЁНЫЙ
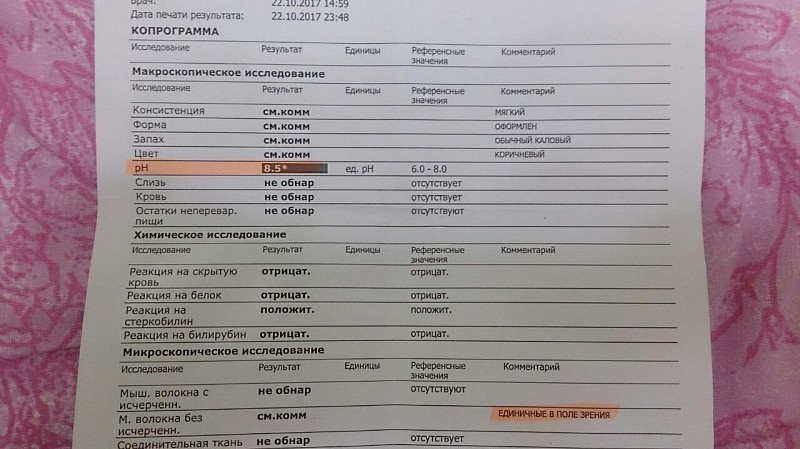
pH 5.0 ед. pH см.комм. У детей до 7 месяцев на грудном вскармливании pH 4,8-5,8, при искусственном
вскармливании 6,8-7,5.
Слизь не обнар см.комм. У детей до 7 месяцев может присутствовать
слизь в небольшом количестве.
Кровь не обнар отсутствует
Остатки неперевар.пищи не обнар отсутствуют Химическое исследование
Реакция на скрытую кровь отрицат. отрицат.
Реакция на белок отрицат. отрицат.
Реакция на стеркобилин положит. см.комм. На грудном вскармливании реакция на
стеркобилин до 5 месяцев
отрицательная, после 5 месяцев определяется
параллельно с билирубином.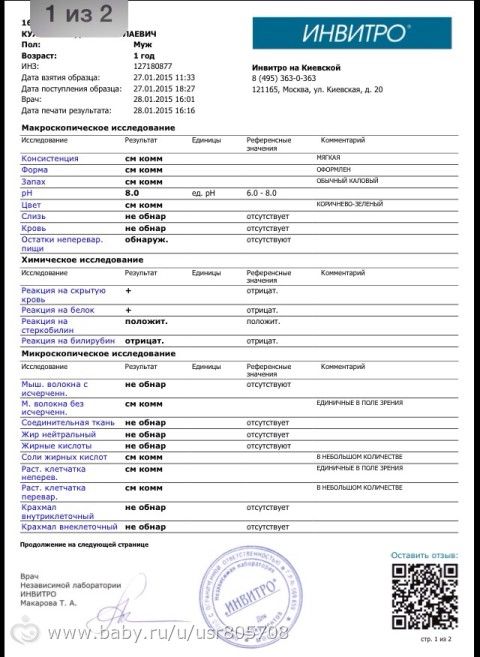 При
При
искусственном вскармливании реакция на
стеркобилин — отрицательная, положительная
с началом прикорма.
Реакция на билирубин отрицат. см.комм. До 7 месяцев определяется положительная
реакция на билирубин.
Микроскопическое исследование
Мыш. волокна с исчерченн. не обнар отсутствуют
М. волокна без исчерченн. не обнар ед. в преп.
Соединительная ткань не обнар отсутствует
Жир нейтральный не обнар отсутствует
Жирные кислоты см.комм ЕДИНИЧНЫЕ В ПОЛЕ ЗРЕНИЯ
Соли жирных кислот см.комм В НЕБОЛЬШОМ КОЛИЧЕСТВЕ
Раст. клетчатка неперев.см.комм В НЕБОЛЬШОМ КОЛИЧЕСТВЕ Раст. клетчатка
перевар.
см.комм В БОЛЬШОМ КОЛИЧЕСТВЕ
Крахмал внутриклеточный не обнар отсутствует
Крахмал внеклеточный не обнар отсутствует
Иодофильная флора норм. не обнар ед. в преп.
не обнар ед. в преп.
Иодофильная флора патол. не обнар отсутствует
Кристаллы см.комм ОКСАЛАТЫ — ЕДИНИЧНЫЕ В ПОЛЕ ЗРЕНИЯ
Слизь см.комм В НЕБОЛЬШОМ КОЛИЧЕСТВЕ
Эпителий цилиндрический см.комм в п/зр. ЕДИНИЧНЫЕ В ПОЛЕ ЗРЕНИЯ
Эпителий плоский см.комм в п/зр. ЕДИНИЧНЫЕ В ПОЛЕ ЗРЕНИЯ
Лейкоциты см.комм в п/зр. ЕДИНИЧНЫЕ В ПОЛЕ ЗРЕНИЯ
Эритроциты не обнар в п/зр. отсутствуют
Простейшие см.комм ОБНАРУЖЕНЫ ЦИСТЫ ENTAMOEBA COLI
Яйца гельминтов не обнар отсутствуют
Дрожжевые грибы см.комм ЕДИНИЧНЫЕ В ПОЛЕ ЗРЕНИЯ
Лабораторные исследования
ИММУНОЛОГИЧЕСКИЕ ИССЛЕДОВАНИЯ
Селективный биохимический скрининг мочи (качественные реакции, тонкослойная хромотография углеводов и аминокислот мочи)
Тонкослойная хроматография углеводов мочи
Реакция на дисахариды мочи (качественная)
Тонкослойная хроматография углеводов сыворотки крови
Тонкослойная хроматография аминокислот мочи
Тонкослойная хроматография аминокислот сыворотки крови
Определение концентрации иммуноглобулинов класса А и G к тканевой трансглутаминидазе методом ИФА
Определение иммуноглобулинов класса М и G к вирусу Эпштейна-Барр методом иммуноблота
Количественное определение экспрессии гена ber-abl типа р190t (9;22) методом Real-time PCR
Количественное определение экспрессии гена ber-abl типа р210t (9;22) методом Real-time PCR
Качественное определение экспрессии гена ber-abl типа р210t (9;22) методом PCR
Качественное определение экспрессии гена ber-abl типа р190t (9;22) методом PCR
Качественное определение экспрессии гена MLL/AF4 t (4;11) методом PCR
Качественное определение экспрессии гена AMLI/ETO t (8;21) методом PCR
Качественное определение экспрессии гена CBFB/MYh21 t (16;16) inv(16;16)методом PCR
Качественное определение делеций в гене дистрофина (регистрация 19 экзонов и промоторной области) методом мультиплексной ПЦР при миодистрофии Дюшенна-Беккера
Качественное определение мутаций в гене CFTR (del 21kb, del F508, del 1507, 1677delTA, 2143delT, 2184insA, 394delTT, 382delT,LI38ins) при муковисцидозе
Количественное определение вальпроевой кислоты в биологических жидкостях (цельная кровь, сыворотка, моча)
Количественное определение метотрексата в биологических жидкостях (цельная кровь, сыворотка, моча)
Определение ХГЧ (хорионический гонодотропин) в сыворотке крови
Определение иммуноглобулинов класса М и G к вирусу простого герпеса 1и2 типов методом ИФА
Авидность Jq G к вирусу простого герпеса 1 и 2 типов методом ИФА
Пренатальный биохимический скрининг с расчетом риска по синдрому Дауна (определение АФП и ХГЧ)
Циркулирующие иммунные комплексы
Фагоцитоз
Определение антител к нативной — ДНК
Определение антител к токсоплазме gondii (Ig; G)
Определение антител к гельминтам (токсокароз, описторхоз, трихинелез, эхинокоокоз)
Тироксин свободный (Т4-св. )
)
Трийодтиронин (Т3 свободный)
Тиреотропный гормон (ТТГ)
Антитела к тиреопероксидазе (ТПО)
Пролактин
17-OH-Прогестерон
Кортизол
Лютеинотропный гормон
Фолликулостим.гормон
Кариотипирование
Определение АФП в сыворотке крови
Гормоны щитовидной железы
Т3 (Трийодтиронин) общ
Т4 (Тироксин) общ
АТ-ТГ (Антитела к тиреоглобулину)
Антитела к рецепторам ТТГ
Т-захват
Кальцитонин
Пролактин (мономер)
Эстрадиол
Прогестерон
Тестостерон
Своб.Тестостерон
CHBG Глобулин, связывающий половые гормоны
ДЭА-S (дигидроэпиандростерона сульфат)
Андростендион
СТГ (Соматотропный гормон)
АКТГ
Дигидротестостерон
Прокальцитонин
Ренин
Антимюллеровский гормон
Альдостерон
Определение ингибина «В»
Аутоиммунная патология :
Анти РЕЗУСНЫЕ а/т
Анти ГРУППОВЫЕ а/т
Анти ФОСФОЛИПИДНЫЕ а/т
Анти СПЕРМАЛЬНЫЕ а/т
Анти ОВАРИАЛЬНЫЕ а/т
Антитела к ткани плаценты
Антитела к Zona pelucida
ENA-скрин (антитела к экстрагируемому нуклеарному антигену)
Антиядерные антитела (антинуклеарный фактор) ANA
Антиперинуклеарный фактор
Антикератиновые антитела
Антитела к базальной мембране клубочка
Антитела к бета-2 гликопротеину
Антитела к виментину
Антитела к кардиолипину
Антитела к миелопероксидазе
Антитела к митохондриям
Антитела к протеиназе 3
Антитела к нуклеосомам
Антитела к цитоплазме нейтрофилов (АНЦА)
Антитела к эндотелию
АЦЦП/anti-CCP (антитела к циклическому цитруллин-содержащему пептиду)
Антитела к тромбоцитам
Антитела к протромбину
Онкомаркеры:
СА-125 (антиген яичников и матки)
СА-15-3 (антиген молочной железы)
СА-19-9 (антиген поджелудочной железы)
СА-72-4(антиген желудка и кишечника)
СА 242 (маркер рака поджелудочной железы, толстого и тонкого кишечника)
РЭА (раковый эмбриональный антиген)
ПСА (простата специфический антиген)
ПСА своб. (Свободный простата спец.антиген)
(Свободный простата спец.антиген)
РАРР-А
Своб. Бета субъединица ХГЧ
Тиреоглобулин
Cyfra 21-1 (маркер рака мочевого пузыря и легких)
NSE (нейронспецифическая енолаза)
ProGRP (маркер мелкоклеточного рака легких)
SСС (маркер рака шейки матки, плоскоклеточных карцином)
НЕ4 (маркер рака яичников)
Белок S-100 (маркер меланомы и повреждения мозга)
Тумор-М2 пируваткиназа(кал) (маркер рака толстого кишечника)
Остеопороз :
Паратгормон
Остеокальцин
Bетта-CrossLaps
Пиридинолин (моча)
25(ОН) Витамин D
P1NP (маркер синтеза кости)
Соматомедин
Исследования кала — копрограмма, анализ на скрытую кровь, анализ на гельминтов. Где сделать платный срочный анализ кала в Москве?
Исследования кала
Исследования кала проводятся для выявления патологий желудочно-кишечного тракта. Общеклиническое исследование кала (копрологическое исследование или копрограмма) позволяет оценить способность органов ЖКТ переваривать пищу. В результате копрологического исследования могут быть обнаружены признаки нарушения функции печени, поджелудочной железы, тонкого кишечника и т.д. Другие виды исследований кала позволяют обнаружить паразитов. Востребованным видом исследования является анализ на скрытую кровь. Наличие скрытой крови в кале может указывать на желудочное или кишечное кровотечение.
В результате копрологического исследования могут быть обнаружены признаки нарушения функции печени, поджелудочной железы, тонкого кишечника и т.д. Другие виды исследований кала позволяют обнаружить паразитов. Востребованным видом исследования является анализ на скрытую кровь. Наличие скрытой крови в кале может указывать на желудочное или кишечное кровотечение.
Кал собирается в чистую и сухую посуду. Женщинам во время месячных сдавать анализ не рекомендуется. Кал должен быть получен без применения слабительных средств или клизмы, путем естественной дефекации. Иногда врач может назначить специальную диету, содержащую определенное содержание белков, жиров и углеводов, которой надо придерживаться в течение нескольких дней до сдачи анализа. При анализе на скрытую кровь за 3 дня до сдачи анализа следует исключить из диеты продукты, которые могут обусловить ложноположительный результат; это – мясо, рыба, зеленые овощи, помидоры, яйца. Если Вы принимаете какие-либо лекарственные препараты, сообщите об этом врачу, – возможно, Вам придется на время прекратить их приём или отложить сдачу анализа.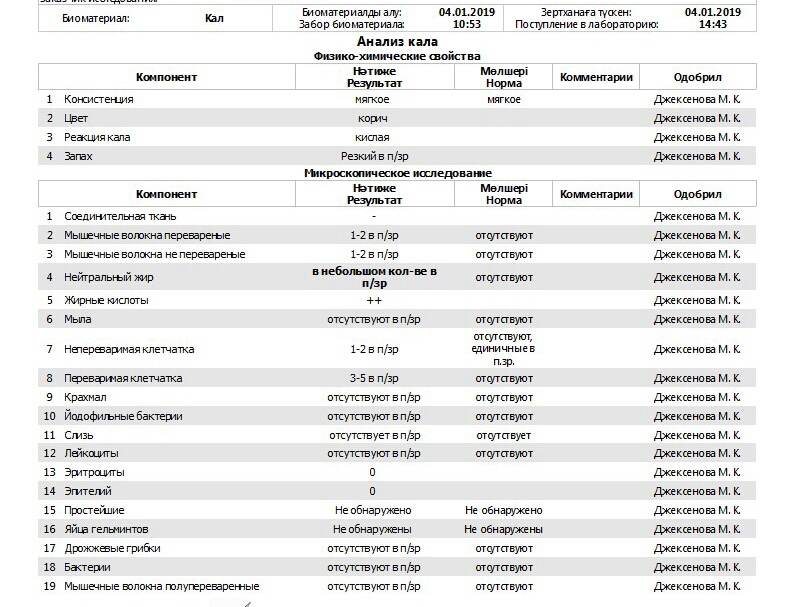
Сдать кал на исследование в Москве Вы можете в любой из поликлиник «Семейного доктора». Сделать срочный анализ кала (в режиме CITO) в Поликлинике № 15 (ст.м. Бауманская). Ниже указаны цены на исследования кала, выполняемые в собственной лаборатории «Семейного доктора».
Уважаемые пациенты!
Обращаем ваше внимание, что указанные цены не являются окончательной стоимостью приёма.
Если манипуляция оказывается на приёме врача, то к стоимости манипуляции добавляется стоимость приёма (соответственно, стоимость приёма увеличивается на стоимость выполненных манипуляций).
Непереносимость белков — StatPearls — NCBI Bookshelf
Программа непрерывного образования
Непереносимость белков — это расстройство, возникающее в результате неблагоприятного воздействия белков пищи. Это вызвано различными механизмами и обычно связано с симптомами, затрагивающими желудочно-кишечный тракт. В этом мероприятии рассматривается оценка и лечение непереносимости белка и подчеркивается роль межпрофессиональной команды в уходе за пациентами с этим заболеванием.
Цели:
Объясните патофизиологию непереносимости белка.
Опишите соответствующую оценку непереносимости белка.
Ознакомьтесь с общими вариантами ведения пациентов с непереносимостью белка.
Обобщить стратегии межпрофессиональной команды по улучшению координации помощи и коммуникации для улучшения ухода за пациентами с непереносимостью белка и улучшения результатов.
Введение
Белковая непереносимость – это расстройство, возникающее в результате неблагоприятного воздействия приема пищевых белков. Он развивается за счет иммунологических, неиммунологических, метаболических, генетических и фармакологических механизмов. Это часто связано с желудочно-кишечными симптомами. При раннем выявлении состояния и вмешательстве расстройство в основном поддается лечению и имеет благоприятный прогноз.
Этиология
Непереносимость белка вызвана неспособностью переваривать или эффективно расщеплять аминокислоты. Когда пищевые белки плохо перевариваются, они могут действовать как антигены, что приводит к аллергии на пищевые белки. Чаще всего причиной пищевой непереносимости в младенчестве являются белки коровьего молока.[1] Синдром энтероколита, вызванный пищевыми белками, также обычно связывают с непереносимостью белков коровьего молока. У пораженных лиц наблюдаются диарея, отеки и гипоальбуминемия. С увеличением возраста и введением различных продуктов непереносимость яичного белка, аллергия на сою и арахис становятся более распространенными.[2]
Когда пищевые белки плохо перевариваются, они могут действовать как антигены, что приводит к аллергии на пищевые белки. Чаще всего причиной пищевой непереносимости в младенчестве являются белки коровьего молока.[1] Синдром энтероколита, вызванный пищевыми белками, также обычно связывают с непереносимостью белков коровьего молока. У пораженных лиц наблюдаются диарея, отеки и гипоальбуминемия. С увеличением возраста и введением различных продуктов непереносимость яичного белка, аллергия на сою и арахис становятся более распространенными.[2]
Непереносимость белка может наблюдаться при следующих состояниях:
Иммунологическая непереносимость пищевого белка: может быть IgE-опосредованной или не-IgE-опосредованной.
IGE Оснащенные условия включают в себя:
Осращенные в IgE Условия включают в себя:
Пищевой белкового белка Энтероколит
Пищевая белка Enteropathey
Пищевой белковочный аллергический проблит
аутоиммунная реакция : Аутоиммунная реакция на белки глютена встречается при глютеновой болезни, чувствительности к глютену без целиакии, аллергии на пшеницу, глютеновой атаксии и герпетиформном дерматите. [3]
[3]
Дефицит ферментов: недостаточность энтерокиназы (энтеропептидазы)
Нарушения обмена веществ:
Генетические/наследственные нарушения: нарушения цикла мочевины, непереносимость лизинурового белка Токсические реакции на биогенные амины:
тирамин в возрасте сыров
гистамин
undefined: синдром раздраженного кишечника
эпидемиология
нетерпимость пищевых продуктов повлияла на 15% до 20% населения.[5] Аллергия на коровье молоко (CMA), реакция на белки в коровьем молоке, является наиболее распространенной пищевой аллергией в раннем возрасте с предполагаемым диапазоном распространенности от 0,5% до 3% в возрасте 1 года.[1][2] ][6] Однако, судя по естественному течению CMA, его разрешение является распространенным явлением, и ожидается, что его распространенность будет ниже у взрослых.
В австралийском исследовании у одного из 10 000 младенцев в возрасте до 2 лет был обнаружен синдром энтероколита, вызванного пищевыми белками (FPIES). Обнаружено, что FPIES встречается преимущественно у младенцев и связан с обычными пищевыми триггерами (белки в коровьем молоке, соя, рис, овес и яйца), но эпидемиологические данные все еще отсутствуют.[7]
Обнаружено, что FPIES встречается преимущественно у младенцев и связан с обычными пищевыми триггерами (белки в коровьем молоке, соя, рис, овес и яйца), но эпидемиологические данные все еще отсутствуют.[7]
Целиакия считается серьезной проблемой общественного здравоохранения, и о ней сообщают во всем мире. Он наиболее распространен в Западной Европе и Соединенных Штатах, но у большинства больных он не диагностируется. Метаанализ, проведенный в 2018 году, показал, что распространенность целиакии составляет 1,4% на основе серологических тестов и 0,7% на основе биопсии.[8]
Хотя предрасположенность к половому признаку неизвестна, FPIES и эозинофильный гастроэнтерит имеют незначительное преобладание у мужчин, в то время как женщины немного чаще страдают глютеновой болезнью.
Патофизиология
Макромолекулы пищевого белка состоят из последовательностей аминокислот, соединенных пептидными связями. Эти связи должны быть гидролизованы и подвергнуты ферментативному воздействию до того, как будут абсорбированы свободные аминокислоты. Процесс переваривания белков начинается в желудке пепсинами с помощью соляной (HCl) кислоты. Затем этот частично переваренный белок достигает двенадцатиперстной кишки, где высокий рН останавливает пептическую активность, а ферменты поджелудочной железы (трипсин, химотрипсин, карбоксипептидазы) берут на себя процесс пищеварения.Небольшие цепочки аминокислот, образующиеся в просвете, теперь подвергаются мембранному перевариванию на щеточной кайме энтероцитов. Мембранные экзопептидазы гидролизуют цепи аминокислот с образованием отдельных аминокислот, которые всасываются в энтероциты и попадают в кровоток для использования в организме.
Процесс переваривания белков начинается в желудке пепсинами с помощью соляной (HCl) кислоты. Затем этот частично переваренный белок достигает двенадцатиперстной кишки, где высокий рН останавливает пептическую активность, а ферменты поджелудочной железы (трипсин, химотрипсин, карбоксипептидазы) берут на себя процесс пищеварения.Небольшие цепочки аминокислот, образующиеся в просвете, теперь подвергаются мембранному перевариванию на щеточной кайме энтероцитов. Мембранные экзопептидазы гидролизуют цепи аминокислот с образованием отдельных аминокислот, которые всасываются в энтероциты и попадают в кровоток для использования в организме.
Непереносимость белка может возникать из-за любых отклонений в процессах пищеварения или метаболизма. Когда пищевые белки не полностью денатурируются желудочной кислотой, это приводит к сенсибилизации белка в кишечнике, что приводит к пищевой аллергии.Гипоацидные состояния, наблюдаемые у пациентов, длительно лечившихся от диспепсических расстройств, часто приводят к развитию аллергии на пищевые белки. [4]
[4]
Анамнез и физикальное исследование
Клинические проявления непереносимости пищевого белка затрагивают различные системы органов и варьируют в зависимости от различных заболеваний. Тем не менее, у пациентов в основном проявляются желудочно-кишечные проявления. При неиммунологической непереносимости пищевого белка количество потребляемой пищи, как правило, более непосредственно связано с тяжестью симптомов.Чрезмерное газообразование в кишечнике, вздутие живота, боль в животе и диарея являются распространенными симптомами. Принимая во внимание, что при иммунологической аллергии на пищевой белок даже следовые количества сенсибилизированного пищевого белка могут вызвать взрывную реакцию и могут поразить кожу и кровеносные сосуды. IgE-опосредованные реакции возникают в течение от нескольких минут до часа после приема пищевого белка, и симптомы варьируют от кожной сыпи, крапивницы, ангионевротического отека, свистящего дыхания до анафилаксии, тогда как не-IgE-опосредованные реакции могут развиваться в течение от нескольких часов до нескольких дней.
Типичным проявлением у младенцев может быть диарея у младенцев в возрасте до 6 месяцев и со временем рвота после кормления молочной смесью в течение нескольких недель. Синдром пищевого проктоколита является распространенным состоянием, при котором у здоровых младенцев возникает диарея, но вес не снижается. Принимая во внимание, что в случае FPIES младенец может обезвоживаться и терять вес.
Вот некоторые симптомы и физические данные, которые наблюдаются при различных нарушениях непереносимости белка:
Синдром оральной аллергии: Реакция в основном возникает из-за перекрестной реактивности между пыльцой и пищей растительного происхождения (фруктами и овощами) и симптомы локализуются на слизистой оболочке полости рта.[9] Симптомы включают зуд и жжение в губах, языке, небе и горле. Возможны ангионевротический отек и рвота.
Немедленная гиперчувствительность ЖКТ: у пациентов появляются тошнота, боль в животе и рвота в течение 1–2 часов после приема сенсибилизированного пищевого белка, часто с последующей диареей. Пораженные люди имеют периодические боли в животе, плохой аппетит и плохую прибавку в весе.
Пораженные люди имеют периодические боли в животе, плохой аппетит и плохую прибавку в весе.
Эозинофильный эзофагит (ЭоЭ): у пациентов возникают затруднения при глотании, застревание твердой пищи, боли в животе, регургитация или рвота и снижение аппетита.У детей младшего возраста могут возникнуть трудности с кормлением и плохая прибавка в весе. Симптомы часто совпадают, и их часто путают с гастроэзофагеальной рефлюксной болезнью (ГЭРБ). Однако у пациентов с ЭоЭ часто обнаруживают в анамнезе и другие аутоиммунные и аллергические состояния.[10]
Эозинофильный гастрит: они обычно проявляются признаками гастрита, такими как боль в животе, постпрандиальная рвота, раннее насыщение, анорексия и задержка развития. Заболевание очень чувствительно к диетическим ограничениям у детей.Примерно 50% этих пациентов также имеют признаки атопии.
Эозинофильный гастроэнтерит: это редкое заболевание с хроническим рецидивирующим течением, характеризующееся инфильтрацией эозинофилами слизистой оболочки желудочно-кишечного тракта.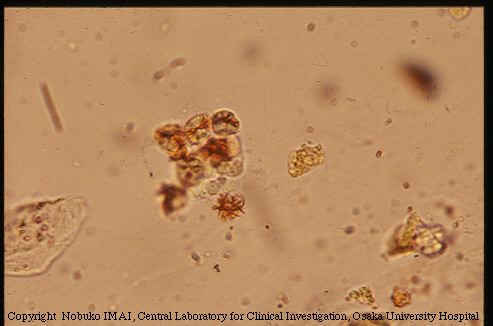 Презентация может быть разной. У детей могут наблюдаться задержка развития, задержка роста, задержка полового созревания или аменорея. Часто у взрослых возникают боли в животе, дисфагия или диарея. Они также могут проявляться признаками энтеропатии с потерей белка, желудочно-кишечными кровотечениями или нарушением всасывания.[11]
Презентация может быть разной. У детей могут наблюдаться задержка развития, задержка роста, задержка полового созревания или аменорея. Часто у взрослых возникают боли в животе, дисфагия или диарея. Они также могут проявляться признаками энтеропатии с потерей белка, желудочно-кишечными кровотечениями или нарушением всасывания.[11]
Синдром энтероколита, вызванного пищевыми белками (FPIES): у пациентов может появиться рвота через один-три часа после еды. У них также может быть вздутие живота, кровавый понос, анемия и потеря веса, и обычно они провоцируются смесями на основе коровьего молока или соевого белка. При физическом осмотре могут быть очевидны признаки обезвоживания. Отсутствуют респираторные симптомы или классические IgE-опосредованные аллергические кожные реакции.
Энтеропатия, вызванная пищевым белком: Пациенты с энтеропатией, вызванной пищевым белком, имеют стеаторею и задержку физического развития в первые несколько месяцев жизни.
Аллергический проктоколит, вызванный пищевым белком: обычно наблюдается у здоровых младенцев, находящихся на грудном вскармливании. У них появляются симптомы стула с прожилками крови в первые несколько месяцев жизни.
У них появляются симптомы стула с прожилками крови в первые несколько месяцев жизни.
Целиакия: у пациентов с целиакией обычно наблюдаются диарея, дурно пахнущий стул, стеаторея, урчание в носу, метеоризм и потеря веса. Больные жалуются на слабость и быструю утомляемость, обычно связанные с неправильным питанием. Могут быть очевидны признаки анемии. Может отмечаться герпетиформный дерматит, зудящая папуловезикулярная сыпь на разгибательных поверхностях конечностей, туловище и ягодицах.
Дефицит энтерокиназы: у младенцев с дефицитом этого фермента с рождения развивается диарея, и они плохо развиваются. При хронической мальабсорбции белка склонны к развитию гипопротеинемических отеков. Пероральное введение экстракта поджелудочной железы приводит к быстрому контролю симптомов и способствует ускорению роста.[12]
Врожденные нарушения обмена веществ: Эти нарушения приводят к накоплению метаболитов перед дефектным ферментом (аминокислоты и/или аммиак), вызывая интоксикацию. Симптомы варьируются в зависимости от пораженных ферментов.
Симптомы варьируются в зависимости от пораженных ферментов.
Токсические реакции на биогенные амины: Проглатывание некоторых биогенных аминов способствует развитию токсических реакций. Пациенты могут жаловаться на головную боль, сердцебиение, рвоту, диарею и аллергию. Установлено, что употребление выдержанного сыра, содержащего тирамин, в сочетании с применением ингибиторов моноаминоксидазы (ИМАО) вызывает головные боли и гипертонический криз.[13] Гистамин более токсичен и может вызывать такие эффекты, как гипотония, раздражение кожи, головная боль, сердцебиение, приступы астмы и т. д.Эта симптоматика известна как «отравление скомброидной рыбой», которое наблюдается после употребления в пищу рыбы из семейств Scombridae и Scomberesocidae (тунец, скумбрия, пеламида, луфарь и т. д.), содержащей высокий уровень гистамина.[14]
Дерматологические проявления:
Белковая непереносимость часто связана с дерматологическими атопическими состояниями. Исследование, проведенное в Италии, показало, что 71% детей с сопутствующей аллергией на коровье молоко имеют сопутствующий атопический дерматит. [15] Другие дерматологические симптомы включают крапивницу, сыпь и ангионевротический отек.
[15] Другие дерматологические симптомы включают крапивницу, сыпь и ангионевротический отек.
Оценка
Не существует специального теста для диагностики непереносимости пищевого белка. Состояние оценивается в первую очередь на основе подробного анамнеза и физического осмотра. Клиницисты должны распознавать и дифференцировать иммунологическую непереносимость пищевого белка от неиммунологической, чтобы предотвратить симптомы и управлять ими. При IgE-опосредованной пищевой аллергии обычно очевидны положительные кожные прик-тесты на пищевые белки наряду с обнаружением специфических пищевых IgE-антител.Однако в большинстве случаев непереносимость пищевых белков не опосредована IgE.
При подозрении на непереносимость пищевого белка в диагностике помогают следующие меры и тесты:
Дневник питания: важно вести дневник питания, поскольку он помогает клиницистам сопоставить симптомы и выяснить взаимосвязь пищи с симптомы пациента.
Кожный прик-тест: Этот тест позволяет выявить IgE-опосредованную аллергию на пищевой белок.
 Хотя положительный результат теста может свидетельствовать о наличии антител IgE, он имеет низкую прогностическую ценность, в то время как отрицательный результат теста имеет высокую прогностическую точность.
Хотя положительный результат теста может свидетельствовать о наличии антител IgE, он имеет низкую прогностическую ценность, в то время как отрицательный результат теста имеет высокую прогностическую точность.Атопический кожный пластырь: Тест используется для выявления отсроченной непереносимости пищевых белков (клеточно-опосредованные реакции).
Анализ сывороточного специфического IgE: Его также проводят для выявления антигенспецифического IgE в сыворотке пациента.
Отказ от диеты: если есть подозрение на непереносимость пищевого белка или аллергию, пациент должен соблюдать диету, свободную от подозреваемого белка, в течение 2–4 недель. Если симптомы улучшаются, в качестве диагностического теста может быть проведен тест на пероральную пищевую провокацию.
Оральный тест на пищевую провокацию: это тест золотого стандарта, который проводится под наблюдением врача для диагностики или исключения пищевой аллергии. Диагноз непереносимости пищевого белка может быть поставлен, когда симптомы исчезают после исключения из рациона соответствующего продукта, а затем симптомы возвращаются после введения того же продукта.
 Реакции и симптомы должны быть воспроизводимы при повторных тестах на исключение диеты и пищевых пробах. Некоторые реакции со стороны желудочно-кишечного тракта могут проявляться с отсроченным началом, вызывая появление симптомов через несколько часов или дней после приема внутрь.
Реакции и симптомы должны быть воспроизводимы при повторных тестах на исключение диеты и пищевых пробах. Некоторые реакции со стороны желудочно-кишечного тракта могут проявляться с отсроченным началом, вызывая появление симптомов через несколько часов или дней после приема внутрь.Радиоаллергосорбентный тест (РАСТ): Этот тест выявляет аллерген-специфические антитела Ig-E с помощью радиоиммуноанализа. Он полезен для определения причин аллергии и часто дает положительный результат при гиперчувствительности немедленного желудочно-кишечного тракта.
Дифференциальный подсчет лейкоцитов: Этот тест подтверждает диагноз аллергического эозинофильного гастрита, аллергического эозинофильного гастроэнтерита и других аллергических состояний, когда наблюдается периферическая эозинофилия.
Анализ кала: Анализ кала может выявить скрытую кровь или фекальные лейкоциты и указать на наличие воспаления.
Биопсия: при аллергическом эозинофильном эзофагите, гастрите и гастроэнтерите биопсия показывает эозинофильную инфильтрацию слизистой и подслизистой оболочки.
 Биопсия тощей кишки при синдроме энтероколита и глютеновой болезни показывает атрофию ворсин и кишечную инфильтрацию лимфоцитами.
Биопсия тощей кишки при синдроме энтероколита и глютеновой болезни показывает атрофию ворсин и кишечную инфильтрацию лимфоцитами.
Лечение/управление
Единственным окончательным методом лечения непереносимости пищевого белка является строгое исключение пищевого белка из рациона. Пациентов следует консультировать по вопросам контроля за составом пищевых продуктов и соблюдения элиминационной диеты.Пациенты, находящиеся на долгосрочной элиминационной диете, также должны иметь доступ к соответствующим диетическим консультациям, в идеале диетологом или диетологом, и к регулярному мониторингу роста, особенно у детей.
Матерям, находящимся на грудном вскармливании, следует рекомендовать избегать коровьего молока и молочных продуктов. В качестве средства выбора для лечения аллергии на коровье молоко, особенно у младенцев и детей младшего возраста, не находящихся на грудном вскармливании, следует рекомендовать интенсивно гидролизованную смесь с подтвержденной гипоаллергенностью. Для пациентов с более тяжелыми симптомами также могут быть рекомендованы формулы аминокислот.[16]
Для пациентов с более тяжелыми симптомами также могут быть рекомендованы формулы аминокислот.[16]
Стероиды являются основным средством лечения IgE-опосредованной иммунологической непереносимости пищевых белков, включая эозинофильные желудочно-кишечные расстройства.[17]
Новорожденных с острым FPIES с легкими симптомами (без вялости, бледности или апатии) можно лечить в домашних условиях с помощью пероральной регидратации. Но при тяжелых симптомах их необходимо лечить в медицинском учреждении с помощью внутривенных вливаний. Внутримышечный адреналин и антигистаминные препараты не играют никакой роли в лечении реакций FPIES.
При подозрении на острые аллергические реакции или анафилаксию следует немедленно отказаться от вероятного продукта питания и оказать неотложную медицинскую помощь.Им могут выписать рецепт на автоинъекционное устройство с адреналином и проинструктировать, как им правильно пользоваться.
Дифференциальный диагноз
Некоторые распространенные дифференциальные диагнозы при непереносимости пищевого белка обсуждаются ниже:
Кишечные инфекции: Кишечные инфекции могут также проявляться симптомами, сходными с непереносимостью белков, или предрасполагать к ним.
 Пациенты с кишечными инфекциями часто имеют признаки инфекции и могут лечиться противомикробными препаратами.
Пациенты с кишечными инфекциями часто имеют признаки инфекции и могут лечиться противомикробными препаратами.Целиакия: Целиакия является широко многофакторным заболеванием с сильным наследственным компонентом и ассоциацией с HLA (DQ2 и DQ8). Они могут проявляться аутоиммунной реакцией на глютеновый белок в пищевых продуктах. Тестирование на сывороточные антитела IgA к тканевой трансглютаминазе (анти-tTG IgA) может помочь в диагностике целиакии или исключить ее как причину непереносимости белка.
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ): у детей наблюдаются такие симптомы, как нарушения сна, рвота, плохой аппетит, плохой рост, хрипы и стридор.Взрослые испытывают изжогу, рвоту и срыгивание. ГЭРБ можно лечить с помощью фармакотерапии и хирургического вмешательства или без них. Они не имеют отношения к тому или иному пищевому белку.
Воспалительные заболевания кишечника (ВЗК): они включают болезнь Крона и язвенный колит, которые могут проявляться обычными желудочно-кишечными симптомами, такими как диарея, ректальное кровотечение и боль в животе.
 Однако важно исключить ВЗК, поскольку они являются системными хроническими заболеваниями и требуют обширного лечения.
Однако важно исключить ВЗК, поскольку они являются системными хроническими заболеваниями и требуют обширного лечения.
Прогноз
Прогноз при многих случаях непереносимости белков благоприятный при соблюдении строгой элиминационной диеты. Многие исследования показали, что прогноз при непереносимости белка коровьего молока благоприятен: у большинства пациентов аллергия перерастает в детстве и раннем подростковом возрасте.[2] Однако у некоторых детей с IgE-опосредованной непереносимостью белков развиваются аллергический риноконъюнктивит и астма.
Осложнения
Белок является важным питательным веществом для здоровья и развития нашего организма.Общие осложнения непереносимости белка, приводящие к дефициту белка, включают потерю мышечной массы, задержку роста, задержку развития и ослабление иммунной системы. У пострадавших людей могут быть такие симптомы, как отеки ног, лица и других частей тела, сухие и ломкие волосы, усталость и частые инфекции.
У взрослых аллергические реакции на белки коровьего молока часто осложняются непереносимостью лактозы, которая усиливается с возрастом. IgE-опосредованные аллергические состояния могут вызывать анафилактические реакции и ангионевротический отек, которые без лечения могут быть опасными для жизни.Диарея и рвота, связанные с FPIES и эозинофильным гастроэнтеритом, могут привести к осложнениям, включая тяжелое обезвоживание и гиповолемический шок.
Сдерживание и обучение пациентов
У здоровых детей грудного возраста рекомендуется обеспечить исключительно грудное вскармливание до 6 месяцев грудного возраста и постепенное введение твердой пищи после 6 месяцев, чтобы предотвратить пищевую аллергию или непереносимость. Младенцы с аллергией на коровье молоко должны избегать молочных смесей и должны находиться на грудном вскармливании.Кормящим матерям желательно исключить из рациона молочные продукты. Если пострадавший младенец не находится на грудном вскармливании, может быть назначена интенсивно гидролизованная смесь. Медицинские работники должны информировать пациентов о важности отмены диеты при подозрении на непереносимость белка или аллергию. Пациентам следует обратить внимание на подозреваемый ингредиент в пищевых продуктах. Пациенты, находящиеся на элиминационной диете, также должны получать соответствующие рекомендации от диетолога или нутрициолога. Пациентам с острыми реакциями гиперчувствительности на пищевые белки в анамнезе следует назначать шприц-ручки с адреналином.
Медицинские работники должны информировать пациентов о важности отмены диеты при подозрении на непереносимость белка или аллергию. Пациентам следует обратить внимание на подозреваемый ингредиент в пищевых продуктах. Пациенты, находящиеся на элиминационной диете, также должны получать соответствующие рекомендации от диетолога или нутрициолога. Пациентам с острыми реакциями гиперчувствительности на пищевые белки в анамнезе следует назначать шприц-ручки с адреналином.
Улучшение результатов работы команды здравоохранения
Белковая непереносимость — это расстройство, которое требует подхода межпрофессиональной команды как для диагностики, так и для лечения. От сбора анамнеза, проведения исследований до постановки правильного диагноза от медицинских работников требуются хорошие коммуникативные и диагностические навыки. Соблюдение со стороны пациента не менее важно в лечении этого состояния. Поскольку отказ от диеты остается основным методом лечения непереносимости белка, необходимо уделять большое внимание регулярным консультациям с диетологом или нутрициологом. Управление индивидуально для каждого пациента. У пациентов, у которых развиваются острые реакции (например, реакции гиперчувствительности при состояниях, опосредованных IgE, тяжелое обезвоживание или шок при FPIES), медсестры и фельдшеры играют жизненно важную роль в межпрофессиональной группе, поскольку они будут контролировать жизненные показатели пациента, вводить жидкости и лекарства, и помочь с образованием пациента и его семьи.
Управление индивидуально для каждого пациента. У пациентов, у которых развиваются острые реакции (например, реакции гиперчувствительности при состояниях, опосредованных IgE, тяжелое обезвоживание или шок при FPIES), медсестры и фельдшеры играют жизненно важную роль в межпрофессиональной группе, поскольку они будут контролировать жизненные показатели пациента, вводить жидкости и лекарства, и помочь с образованием пациента и его семьи.
Аллергологи также играют важную роль в диагностике непереносимости белков, поскольку расстройство часто связано с сенсибилизацией к пищевым белкам.Часто родители или опекуны педиатрических пациентов или сами взрослые пациенты с хронической или тяжелой непереносимостью белков испытывают значительное бремя, беспокойство, беспокойство и стресс, о которых следует заботиться при помощи консультантов, психологов или психиатров, когда это необходимо.
Прогноз при непереносимости белка благоприятный. Надлежащая идентификация возбудителя и его избегание помогает контролировать расстройство. Недавние данные свидетельствуют о том, что сенсибилизацию к коровьему молоку, ведущую к непереносимости и аллергии, можно в первую очередь предотвратить, избегая добавок на основе коровьего молока в течение как минимум первых 3 дней жизни.[18] [Уровень 1] Исследование, проведенное в 2019 году, также успешно продемонстрировало гипоаллергенность новой интенсивно гидролизованной смеси на основе сыворотки, которая содержит два олигосахарида грудного молока.[19] [Уровень 1] Различные текущие исследования добавили новые аспекты в профилактику и лечение непереносимости пищевого белка.
Недавние данные свидетельствуют о том, что сенсибилизацию к коровьему молоку, ведущую к непереносимости и аллергии, можно в первую очередь предотвратить, избегая добавок на основе коровьего молока в течение как минимум первых 3 дней жизни.[18] [Уровень 1] Исследование, проведенное в 2019 году, также успешно продемонстрировало гипоаллергенность новой интенсивно гидролизованной смеси на основе сыворотки, которая содержит два олигосахарида грудного молока.[19] [Уровень 1] Различные текущие исследования добавили новые аспекты в профилактику и лечение непереносимости пищевого белка.
Ссылки
- 1.
- Flom JD, Sicherer SH. Эпидемиология аллергии на коровье молоко. Питательные вещества. 2019 May 10;11(5) [бесплатная статья PMC: PMC6566637] [PubMed: 31083388]
- 2.
- Сэвидж Дж., Джонс С.Б. Пищевая аллергия: эпидемиология и естественное течение. Иммунол Аллергия Клин Норт Ам. 2015 фев; 35 (1): 45-59. [Бесплатная статья PMC: PMC4254585] [PubMed: 25459576]
- 3.

- Ахонди Х., Росс А.Б. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 6 июля 2021 г. Глютен и связанные с ним медицинские проблемы. [PubMed: 30860740]
- 4.
- Untersmayr E. Влияние желудочного пищеварения на развитие пищевой аллергии. Преподобный отец Аллергол (2009).2015 ноябрь;55(7):444-447. [Бесплатная статья PMC: PMC5467726] [PubMed: 28616101]
- 5.
- Lomer MC. Обзорная статья: этиология, диагностика, механизмы и клинические проявления пищевой непереносимости. Алимент Фармакол Тер. 2015 фев; 41 (3): 262-75. [PubMed: 25471897]
- 6.
- Rona RJ, Keil T, Summers C, Gislason D, Zuidmeer L, Sodergren E, Sigurdardottir ST, Lindner T, Goldhahn K, Dahlstrom J, McBride D, Madsen C. Распространенность Пищевая аллергия: метаанализ. J Аллергия Клин Иммунол.2007 г., сен; 120 (3): 638-46. [PubMed: 17628647]
- 7.
- Mehr S, Frith K, Campbell DE. Эпидемиология синдрома энтероколита, вызванного пищевыми белками.
 Курр Опин Аллергия Клин Иммунол. 2014 июнь;14(3):208-16. [Бесплатная статья PMC: PMC4011623] [PubMed: 24686277]
Курр Опин Аллергия Клин Иммунол. 2014 июнь;14(3):208-16. [Бесплатная статья PMC: PMC4011623] [PubMed: 24686277] - 8.
- Сингх П., Арора А., Стрэнд Т.А., Леффлер Д.А., Катасси С., Грин П.Х., Келли С.П., Ахуджа В., Махария Г.К. Глобальная распространенность глютеновой болезни: систематический обзор и метаанализ. Клин Гастроэнтерол Гепатол. 2018 июнь; 16 (6): 823-836.е2. [PubMed: 29551598]
- 9.
- Ивкович-Юрекович И. [Синдром оральной аллергии]. Acta Med Croatica. 2014 июнь; 68 (3): 283-7. [PubMed: 26016219]
- 10.
- Roussel JM, Pandit S. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 14 августа 2021 г. Эозинофильный эзофагит. [PubMed: 2
29]
- 11.
- Ingle SB, Hinge Ingle CR. Эозинофильный гастроэнтерит: необычный тип гастроэнтерита. Мир J Гастроэнтерол. 2013 21 августа; 19 (31): 5061-6.[Бесплатная статья PMC: PMC3746377] [PubMed: 23964139]
- 12.
- Tarlow MJ, Hadorn B, Arthurton MW, Lloyd JK.
 Дефицит кишечной энтерокиназы. Недавно обнаруженное нарушение переваривания белков. Арч Дис Чайлд. 1970 окт; 45 (243): 651-5. [Бесплатная статья PMC: PMC1647492] [PubMed: 5477679]
Дефицит кишечной энтерокиназы. Недавно обнаруженное нарушение переваривания белков. Арч Дис Чайлд. 1970 окт; 45 (243): 651-5. [Бесплатная статья PMC: PMC1647492] [PubMed: 5477679] - 13.
- Сатьянараяна Рао Т.С., Ерагани В.К. Гипертонический криз и сыр. Индийская психиатрия. 2009 Январь; 51 (1): 65-6. [Бесплатная статья PMC: PMC2738414] [PubMed: 19742203]
- 14.
- Tabanelli G. Биогенные амины и качество продуктов питания: новые проблемы и проблемы общественного здравоохранения. Еда. 2020 Jul 01;9(7) [PMC бесплатная статья: PMC7404793] [PubMed: 32630178]
- 15.
- Giannetti A, Cipriani F, Indio V, Gallucci M, Caffarelli C, Ricci G. Влияние атопического дерматита на коровью Аллергия на молоко у детей. Медицина (Каунас). 2019 авг. 10; 55 (8) [бесплатная статья PMC: PMC6723735] [PubMed: 31405131]
- 16.
- Мураро А., Верфель Т., Хоффманн-Зоммергрубер К., Робертс Г., Бейер К., Биндслев-Йенсен К., Кардона В. , Дюбуа А., Дютуа Г.
 , Эйгенманн П., Фернандес Ривас М., Халкен С., Хикштейн Л., Хёст А., Кнол Э., Лак Г., Маркизотто М.Дж., Ниггеманн Б., Нвару Б.И., Пападопулос Н.Г., Поулсен Л.К., Сантос А.Ф., Скайпала И., Шёпфер А., Ван Ри Р., Вентер С., Ворм М., Влиг-Бурстра Б., Панесар С., де Сильва Д., Соарес-Вайзер К., Шейх А., Балмер-Вебер Б.К., Нильссон С., де Йонг Н.В., Акдис К.А., Группа рекомендаций EAACI по пищевой аллергии и анафилаксии. Рекомендации EAACI по пищевой аллергии и анафилаксии: диагностика и лечение пищевой аллергии. Аллергия. 2014 авг;69(8):1008-25. [PubMed: 24
, Эйгенманн П., Фернандес Ривас М., Халкен С., Хикштейн Л., Хёст А., Кнол Э., Лак Г., Маркизотто М.Дж., Ниггеманн Б., Нвару Б.И., Пападопулос Н.Г., Поулсен Л.К., Сантос А.Ф., Скайпала И., Шёпфер А., Ван Ри Р., Вентер С., Ворм М., Влиг-Бурстра Б., Панесар С., де Сильва Д., Соарес-Вайзер К., Шейх А., Балмер-Вебер Б.К., Нильссон С., де Йонг Н.В., Акдис К.А., Группа рекомендаций EAACI по пищевой аллергии и анафилаксии. Рекомендации EAACI по пищевой аллергии и анафилаксии: диагностика и лечение пищевой аллергии. Аллергия. 2014 авг;69(8):1008-25. [PubMed: 246]
- 17.
- Гонсалвес Н. Эозинофильные желудочно-кишечные расстройства. Клин Рев Аллергия Иммунол. 2019 окт;57(2):272-285. [PubMed: 309]
- 18.
- Urashima M, Mezawa H, Okuyama M, Urashima T, Hirano D, Gocho N, Tachimoto H. Первичная профилактика сенсибилизации к коровьему молоку и пищевой аллергии путем отказа от добавок с коровьим молоком при рождении : Рандомизированное клиническое исследование.JAMA Педиатр.
 01 декабря 2019 г.; 173(12):1137-1145. [Бесплатная статья PMC: PMC6806425] [PubMed: 31633778]
01 декабря 2019 г.; 173(12):1137-1145. [Бесплатная статья PMC: PMC6806425] [PubMed: 31633778] - 19.
- Nowak-Wegrzyn A, Czerkies L, Reyes K, Collins B, Heine RG. Подтверждена гипоаллергенность новой интенсивно гидролизованной детской смеси на основе молочной сыворотки, содержащей два олигосахарида грудного молока. Питательные вещества. 2019 Jun 26;11(7) [Бесплатная статья PMC: PMC6682865] [PubMed: 31248026]
Непереносимость белков — StatPearls — NCBI Bookshelf
Continuing Education Activity
Непереносимость белков — это побочное действие, возникающее в результате нарушения приема пищевых белков.Это вызвано различными механизмами и обычно связано с симптомами, затрагивающими желудочно-кишечный тракт. В этом мероприятии рассматривается оценка и лечение непереносимости белка и подчеркивается роль межпрофессиональной команды в уходе за пациентами с этим заболеванием.
Цели:
Объясните патофизиологию непереносимости белка.

Опишите соответствующую оценку непереносимости белка.
Ознакомьтесь с общими вариантами ведения пациентов с непереносимостью белка.
Обобщить стратегии межпрофессиональной команды по улучшению координации помощи и коммуникации для улучшения ухода за пациентами с непереносимостью белка и улучшения результатов.
Введение
Белковая непереносимость – это расстройство, возникающее в результате неблагоприятного воздействия приема пищевых белков. Он развивается за счет иммунологических, неиммунологических, метаболических, генетических и фармакологических механизмов.Это часто связано с желудочно-кишечными симптомами. При раннем выявлении состояния и вмешательстве расстройство в основном поддается лечению и имеет благоприятный прогноз.
Этиология
Непереносимость белка вызвана неспособностью переваривать или эффективно расщеплять аминокислоты.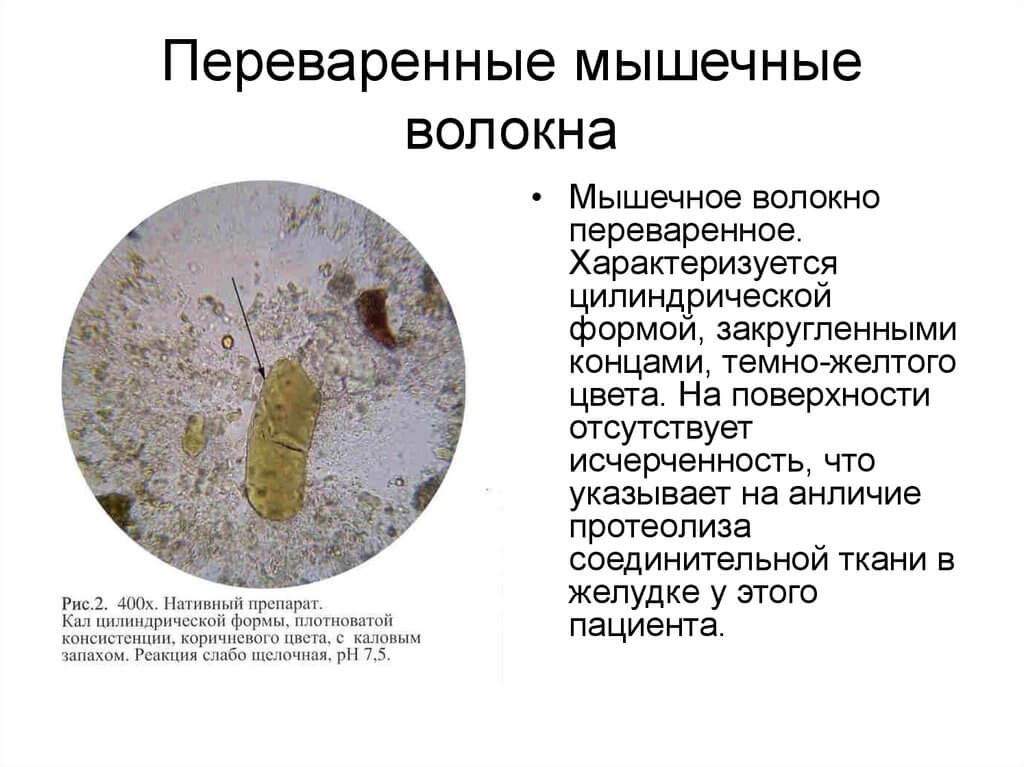 Когда пищевые белки плохо перевариваются, они могут действовать как антигены, что приводит к аллергии на пищевые белки. Наиболее часто белки коровьего молока являются причиной пищевой непереносимости в младенческом возрасте.[1] Синдром энтероколита, вызванный пищевыми белками, также обычно связывают с непереносимостью белков коровьего молока. У пораженных лиц наблюдаются диарея, отеки и гипоальбуминемия. С увеличением возраста и введением различных продуктов непереносимость яичного белка, аллергия на сою и арахис становятся более распространенными.[2]
Когда пищевые белки плохо перевариваются, они могут действовать как антигены, что приводит к аллергии на пищевые белки. Наиболее часто белки коровьего молока являются причиной пищевой непереносимости в младенческом возрасте.[1] Синдром энтероколита, вызванный пищевыми белками, также обычно связывают с непереносимостью белков коровьего молока. У пораженных лиц наблюдаются диарея, отеки и гипоальбуминемия. С увеличением возраста и введением различных продуктов непереносимость яичного белка, аллергия на сою и арахис становятся более распространенными.[2]
Непереносимость белка наблюдается при следующих состояниях:
Иммунологическая непереносимость пищевого белка: может быть IgE-опосредованной или не-IgE-опосредованной.
IGE Оснащенные условия включают в себя:
Осращенные в IgE Условия включают в себя:
Пищевой белкового белка Энтероколит
Пищевая белка Enteropathey
Пищевой белковочный аллергический проблит
аутоиммунная реакция : Аутоиммунная реакция на белки глютена обнаруживается при глютеновой болезни, чувствительности к глютену без целиакии, аллергии на пшеницу, глютеновой атаксии и герпетиформном дерматите. [3]
[3]
Дефицит ферментов: дефицит энтерокиназы (энтеропептидазы)
Метаболические нарушения:
Генетические/наследственные нарушения: нарушения цикла мочевины, непереносимость лизинурического белка Биогенные амины:
тирамин в возрасте сыра
гистамин
undefined: синдром раздраженного кишечника
эпидемиология
Нетерпимость пищевых продуктов повлияла на 15% до 20% населения.[5] Аллергия на коровье молоко (CMA), реакция на белки в коровьем молоке, является наиболее распространенной пищевой аллергией в раннем возрасте с предполагаемым диапазоном распространенности от 0,5% до 3% в возрасте 1 года.[1][2] ][6] Однако, судя по естественному течению CMA, его разрешение является распространенным явлением, и ожидается, что его распространенность будет ниже у взрослых.
В австралийском исследовании у одного из 10 000 младенцев в возрасте до 2 лет был обнаружен синдром энтероколита, вызванного пищевыми белками (FPIES). Обнаружено, что FPIES встречается преимущественно у младенцев и связан с обычными пищевыми триггерами (белки в коровьем молоке, соя, рис, овес и яйца), но эпидемиологические данные все еще отсутствуют.[7]
Обнаружено, что FPIES встречается преимущественно у младенцев и связан с обычными пищевыми триггерами (белки в коровьем молоке, соя, рис, овес и яйца), но эпидемиологические данные все еще отсутствуют.[7]
Целиакия считается серьезной проблемой общественного здравоохранения, и о ней сообщают во всем мире. Он наиболее распространен в Западной Европе и Соединенных Штатах, но у большинства больных он не диагностируется. Метаанализ, проведенный в 2018 году, показал, что распространенность целиакии составляет 1,4% на основе серологических тестов и 0,7% на основе биопсии.[8]
Хотя предрасположенность к половому признаку неизвестна, FPIES и эозинофильный гастроэнтерит имеют незначительное преобладание у мужчин, в то время как женщины немного чаще страдают глютеновой болезнью.
Патофизиология
Макромолекулы пищевого белка состоят из последовательностей аминокислот, соединенных пептидными связями. Эти связи должны быть гидролизованы и подвергнуты ферментативному воздействию до того, как будут абсорбированы свободные аминокислоты. Процесс переваривания белков начинается в желудке пепсинами с помощью соляной (HCl) кислоты. Затем этот частично переваренный белок достигает двенадцатиперстной кишки, где высокий рН останавливает пептическую активность, а ферменты поджелудочной железы (трипсин, химотрипсин, карбоксипептидазы) берут на себя процесс пищеварения.Небольшие цепочки аминокислот, образующиеся в просвете, теперь подвергаются мембранному перевариванию на щеточной кайме энтероцитов. Мембранные экзопептидазы гидролизуют цепи аминокислот с образованием отдельных аминокислот, которые всасываются в энтероциты и попадают в кровоток для использования в организме.
Процесс переваривания белков начинается в желудке пепсинами с помощью соляной (HCl) кислоты. Затем этот частично переваренный белок достигает двенадцатиперстной кишки, где высокий рН останавливает пептическую активность, а ферменты поджелудочной железы (трипсин, химотрипсин, карбоксипептидазы) берут на себя процесс пищеварения.Небольшие цепочки аминокислот, образующиеся в просвете, теперь подвергаются мембранному перевариванию на щеточной кайме энтероцитов. Мембранные экзопептидазы гидролизуют цепи аминокислот с образованием отдельных аминокислот, которые всасываются в энтероциты и попадают в кровоток для использования в организме.
Непереносимость белка может возникать из-за любых отклонений в процессах пищеварения или метаболизма. Когда пищевые белки не полностью денатурируются желудочной кислотой, это приводит к сенсибилизации белка в кишечнике, что приводит к пищевой аллергии.Гипоацидные состояния, наблюдаемые у пациентов, длительно лечившихся от диспепсических расстройств, часто приводят к развитию аллергии на пищевые белки. [4]
[4]
Анамнез и физикальное исследование
Клинические проявления непереносимости пищевого белка затрагивают различные системы органов и варьируют в зависимости от различных заболеваний. Тем не менее, у пациентов в основном проявляются желудочно-кишечные проявления. При неиммунологической непереносимости пищевого белка количество потребляемой пищи, как правило, более непосредственно связано с тяжестью симптомов.Чрезмерное газообразование в кишечнике, вздутие живота, боль в животе и диарея являются распространенными симптомами. Принимая во внимание, что при иммунологической аллергии на пищевой белок даже следовые количества сенсибилизированного пищевого белка могут вызвать взрывную реакцию и могут поразить кожу и кровеносные сосуды. IgE-опосредованные реакции возникают в течение от нескольких минут до часа после приема пищевого белка, и симптомы варьируют от кожной сыпи, крапивницы, ангионевротического отека, свистящего дыхания до анафилаксии, тогда как не-IgE-опосредованные реакции могут развиваться в течение от нескольких часов до нескольких дней.
Типичным проявлением у младенцев может быть диарея у младенцев в возрасте до 6 месяцев и со временем рвота после кормления молочной смесью в течение нескольких недель. Синдром пищевого проктоколита является распространенным состоянием, при котором у здоровых младенцев возникает диарея, но вес не снижается. Принимая во внимание, что в случае FPIES младенец может обезвоживаться и терять вес.
Вот некоторые симптомы и физические данные, которые наблюдаются при различных нарушениях непереносимости белка:
Синдром оральной аллергии: Реакция в основном возникает из-за перекрестной реактивности между пыльцой и пищей растительного происхождения (фруктами и овощами) и симптомы локализуются на слизистой оболочке полости рта.[9] Симптомы включают зуд и жжение в губах, языке, небе и горле. Возможны ангионевротический отек и рвота.
Немедленная гиперчувствительность ЖКТ: у пациентов появляются тошнота, боль в животе и рвота в течение 1–2 часов после приема сенсибилизированного пищевого белка, часто с последующей диареей. Пораженные люди имеют периодические боли в животе, плохой аппетит и плохую прибавку в весе.
Пораженные люди имеют периодические боли в животе, плохой аппетит и плохую прибавку в весе.
Эозинофильный эзофагит (ЭоЭ): у пациентов возникают затруднения при глотании, застревание твердой пищи, боли в животе, регургитация или рвота и снижение аппетита.У детей младшего возраста могут возникнуть трудности с кормлением и плохая прибавка в весе. Симптомы часто совпадают, и их часто путают с гастроэзофагеальной рефлюксной болезнью (ГЭРБ). Однако у пациентов с ЭоЭ часто обнаруживают в анамнезе и другие аутоиммунные и аллергические состояния.[10]
Эозинофильный гастрит: они обычно проявляются признаками гастрита, такими как боль в животе, постпрандиальная рвота, раннее насыщение, анорексия и задержка развития. Заболевание очень чувствительно к диетическим ограничениям у детей.Примерно 50% этих пациентов также имеют признаки атопии.
Эозинофильный гастроэнтерит: это редкое заболевание с хроническим рецидивирующим течением, характеризующееся инфильтрацией эозинофилами слизистой оболочки желудочно-кишечного тракта. Презентация может быть разной. У детей могут наблюдаться задержка развития, задержка роста, задержка полового созревания или аменорея. Часто у взрослых возникают боли в животе, дисфагия или диарея. Они также могут проявляться признаками энтеропатии с потерей белка, желудочно-кишечными кровотечениями или нарушением всасывания.[11]
Презентация может быть разной. У детей могут наблюдаться задержка развития, задержка роста, задержка полового созревания или аменорея. Часто у взрослых возникают боли в животе, дисфагия или диарея. Они также могут проявляться признаками энтеропатии с потерей белка, желудочно-кишечными кровотечениями или нарушением всасывания.[11]
Синдром энтероколита, вызванного пищевыми белками (FPIES): у пациентов может появиться рвота через один-три часа после еды. У них также может быть вздутие живота, кровавый понос, анемия и потеря веса, и обычно они провоцируются смесями на основе коровьего молока или соевого белка. При физическом осмотре могут быть очевидны признаки обезвоживания. Отсутствуют респираторные симптомы или классические IgE-опосредованные аллергические кожные реакции.
Энтеропатия, вызванная пищевым белком: Пациенты с энтеропатией, вызванной пищевым белком, имеют стеаторею и задержку физического развития в первые несколько месяцев жизни.
Аллергический проктоколит, вызванный пищевым белком: обычно наблюдается у здоровых младенцев, находящихся на грудном вскармливании. У них появляются симптомы стула с прожилками крови в первые несколько месяцев жизни.
У них появляются симптомы стула с прожилками крови в первые несколько месяцев жизни.
Целиакия: у пациентов с целиакией обычно наблюдаются диарея, дурно пахнущий стул, стеаторея, урчание в носу, метеоризм и потеря веса. Больные жалуются на слабость и быструю утомляемость, обычно связанные с неправильным питанием. Могут быть очевидны признаки анемии. Может отмечаться герпетиформный дерматит, зудящая папуловезикулярная сыпь на разгибательных поверхностях конечностей, туловище и ягодицах.
Дефицит энтерокиназы: у младенцев с дефицитом этого фермента с рождения развивается диарея, и они плохо развиваются. При хронической мальабсорбции белка склонны к развитию гипопротеинемических отеков. Пероральное введение экстракта поджелудочной железы приводит к быстрому контролю симптомов и способствует ускорению роста.[12]
Врожденные нарушения обмена веществ: Эти нарушения приводят к накоплению метаболитов перед дефектным ферментом (аминокислоты и/или аммиак), вызывая интоксикацию. Симптомы варьируются в зависимости от пораженных ферментов.
Симптомы варьируются в зависимости от пораженных ферментов.
Токсические реакции на биогенные амины: Проглатывание некоторых биогенных аминов способствует развитию токсических реакций. Пациенты могут жаловаться на головную боль, сердцебиение, рвоту, диарею и аллергию. Установлено, что употребление выдержанного сыра, содержащего тирамин, в сочетании с применением ингибиторов моноаминоксидазы (ИМАО) вызывает головные боли и гипертонический криз.[13] Гистамин более токсичен и может вызывать такие эффекты, как гипотония, раздражение кожи, головная боль, сердцебиение, приступы астмы и т. д.Эта симптоматика известна как «отравление скомброидной рыбой», которое наблюдается после употребления в пищу рыбы из семейств Scombridae и Scomberesocidae (тунец, скумбрия, пеламида, луфарь и т. д.), содержащей высокий уровень гистамина.[14]
Дерматологические проявления:
Белковая непереносимость часто связана с дерматологическими атопическими состояниями. Исследование, проведенное в Италии, показало, что 71% детей с сопутствующей аллергией на коровье молоко имеют сопутствующий атопический дерматит. [15] Другие дерматологические симптомы включают крапивницу, сыпь и ангионевротический отек.
[15] Другие дерматологические симптомы включают крапивницу, сыпь и ангионевротический отек.
Оценка
Не существует специального теста для диагностики непереносимости пищевого белка. Состояние оценивается в первую очередь на основе подробного анамнеза и физического осмотра. Клиницисты должны распознавать и дифференцировать иммунологическую непереносимость пищевого белка от неиммунологической, чтобы предотвратить симптомы и управлять ими. При IgE-опосредованной пищевой аллергии обычно очевидны положительные кожные прик-тесты на пищевые белки наряду с обнаружением специфических пищевых IgE-антител.Однако в большинстве случаев непереносимость пищевых белков не опосредована IgE.
При подозрении на непереносимость пищевого белка в диагностике помогают следующие меры и тесты:
Дневник питания: важно вести дневник питания, поскольку он помогает клиницистам сопоставить симптомы и выяснить взаимосвязь пищи с симптомы пациента.
Кожный прик-тест: Этот тест позволяет выявить IgE-опосредованную аллергию на пищевой белок.
 Хотя положительный результат теста может свидетельствовать о наличии антител IgE, он имеет низкую прогностическую ценность, в то время как отрицательный результат теста имеет высокую прогностическую точность.
Хотя положительный результат теста может свидетельствовать о наличии антител IgE, он имеет низкую прогностическую ценность, в то время как отрицательный результат теста имеет высокую прогностическую точность.Атопический кожный пластырь: Тест используется для выявления отсроченной непереносимости пищевых белков (клеточно-опосредованные реакции).
Анализ сывороточного специфического IgE: Его также проводят для выявления антигенспецифического IgE в сыворотке пациента.
Отказ от диеты: если есть подозрение на непереносимость пищевого белка или аллергию, пациент должен соблюдать диету, свободную от подозреваемого белка, в течение 2–4 недель. Если симптомы улучшаются, в качестве диагностического теста может быть проведен тест на пероральную пищевую провокацию.
Оральный тест на пищевую провокацию: это тест золотого стандарта, который проводится под наблюдением врача для диагностики или исключения пищевой аллергии. Диагноз непереносимости пищевого белка может быть поставлен, когда симптомы исчезают после исключения из рациона соответствующего продукта, а затем симптомы возвращаются после введения того же продукта.
 Реакции и симптомы должны быть воспроизводимы при повторных тестах на исключение диеты и пищевых пробах. Некоторые реакции со стороны желудочно-кишечного тракта могут проявляться с отсроченным началом, вызывая появление симптомов через несколько часов или дней после приема внутрь.
Реакции и симптомы должны быть воспроизводимы при повторных тестах на исключение диеты и пищевых пробах. Некоторые реакции со стороны желудочно-кишечного тракта могут проявляться с отсроченным началом, вызывая появление симптомов через несколько часов или дней после приема внутрь.Радиоаллергосорбентный тест (РАСТ): Этот тест выявляет аллерген-специфические антитела Ig-E с помощью радиоиммуноанализа. Он полезен для определения причин аллергии и часто дает положительный результат при гиперчувствительности немедленного желудочно-кишечного тракта.
Дифференциальный подсчет лейкоцитов: Этот тест подтверждает диагноз аллергического эозинофильного гастрита, аллергического эозинофильного гастроэнтерита и других аллергических состояний, когда наблюдается периферическая эозинофилия.
Анализ кала: Анализ кала может выявить скрытую кровь или фекальные лейкоциты и указать на наличие воспаления.
Биопсия: при аллергическом эозинофильном эзофагите, гастрите и гастроэнтерите биопсия показывает эозинофильную инфильтрацию слизистой и подслизистой оболочки.
 Биопсия тощей кишки при синдроме энтероколита и глютеновой болезни показывает атрофию ворсин и кишечную инфильтрацию лимфоцитами.
Биопсия тощей кишки при синдроме энтероколита и глютеновой болезни показывает атрофию ворсин и кишечную инфильтрацию лимфоцитами.
Лечение/управление
Единственным окончательным методом лечения непереносимости пищевого белка является строгое исключение пищевого белка из рациона. Пациентов следует консультировать по вопросам контроля за составом пищевых продуктов и соблюдения элиминационной диеты.Пациенты, находящиеся на долгосрочной элиминационной диете, также должны иметь доступ к соответствующим диетическим консультациям, в идеале диетологом или диетологом, и к регулярному мониторингу роста, особенно у детей.
Матерям, находящимся на грудном вскармливании, следует рекомендовать избегать коровьего молока и молочных продуктов. В качестве средства выбора для лечения аллергии на коровье молоко, особенно у младенцев и детей младшего возраста, не находящихся на грудном вскармливании, следует рекомендовать интенсивно гидролизованную смесь с подтвержденной гипоаллергенностью. Для пациентов с более тяжелыми симптомами также могут быть рекомендованы формулы аминокислот.[16]
Для пациентов с более тяжелыми симптомами также могут быть рекомендованы формулы аминокислот.[16]
Стероиды являются основным средством лечения IgE-опосредованной иммунологической непереносимости пищевых белков, включая эозинофильные желудочно-кишечные расстройства.[17]
Новорожденных с острым FPIES с легкими симптомами (без вялости, бледности или апатии) можно лечить в домашних условиях с помощью пероральной регидратации. Но при тяжелых симптомах их необходимо лечить в медицинском учреждении с помощью внутривенных вливаний. Внутримышечный адреналин и антигистаминные препараты не играют никакой роли в лечении реакций FPIES.
При подозрении на острые аллергические реакции или анафилаксию следует немедленно отказаться от вероятного продукта питания и оказать неотложную медицинскую помощь.Им могут выписать рецепт на автоинъекционное устройство с адреналином и проинструктировать, как им правильно пользоваться.
Дифференциальный диагноз
Некоторые распространенные дифференциальные диагнозы при непереносимости пищевого белка обсуждаются ниже:
Кишечные инфекции: Кишечные инфекции могут также проявляться симптомами, сходными с непереносимостью белков, или предрасполагать к ним.
 Пациенты с кишечными инфекциями часто имеют признаки инфекции и могут лечиться противомикробными препаратами.
Пациенты с кишечными инфекциями часто имеют признаки инфекции и могут лечиться противомикробными препаратами.Целиакия: Целиакия является широко многофакторным заболеванием с сильным наследственным компонентом и ассоциацией с HLA (DQ2 и DQ8). Они могут проявляться аутоиммунной реакцией на глютеновый белок в пищевых продуктах. Тестирование на сывороточные антитела IgA к тканевой трансглютаминазе (анти-tTG IgA) может помочь в диагностике целиакии или исключить ее как причину непереносимости белка.
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ): у детей наблюдаются такие симптомы, как нарушения сна, рвота, плохой аппетит, плохой рост, хрипы и стридор.Взрослые испытывают изжогу, рвоту и срыгивание. ГЭРБ можно лечить с помощью фармакотерапии и хирургического вмешательства или без них. Они не имеют отношения к тому или иному пищевому белку.
Воспалительные заболевания кишечника (ВЗК): они включают болезнь Крона и язвенный колит, которые могут проявляться обычными желудочно-кишечными симптомами, такими как диарея, ректальное кровотечение и боль в животе.
 Однако важно исключить ВЗК, поскольку они являются системными хроническими заболеваниями и требуют обширного лечения.
Однако важно исключить ВЗК, поскольку они являются системными хроническими заболеваниями и требуют обширного лечения.
Прогноз
Прогноз при многих случаях непереносимости белков благоприятный при соблюдении строгой элиминационной диеты. Многие исследования показали, что прогноз при непереносимости белка коровьего молока благоприятен: у большинства пациентов аллергия перерастает в детстве и раннем подростковом возрасте.[2] Однако у некоторых детей с IgE-опосредованной непереносимостью белков развиваются аллергический риноконъюнктивит и астма.
Осложнения
Белок является важным питательным веществом для здоровья и развития нашего организма.Общие осложнения непереносимости белка, приводящие к дефициту белка, включают потерю мышечной массы, задержку роста, задержку развития и ослабление иммунной системы. У пострадавших людей могут быть такие симптомы, как отеки ног, лица и других частей тела, сухие и ломкие волосы, усталость и частые инфекции.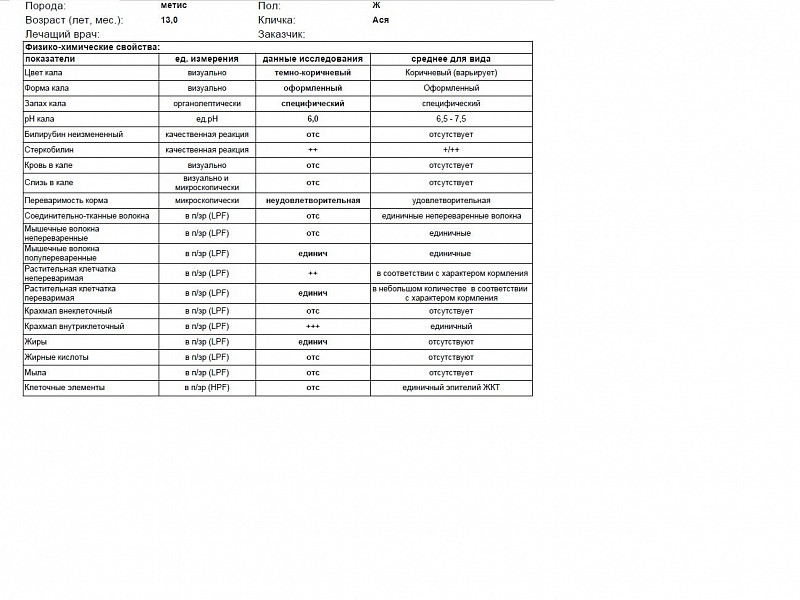
У взрослых аллергические реакции на белки коровьего молока часто осложняются непереносимостью лактозы, которая усиливается с возрастом. IgE-опосредованные аллергические состояния могут вызывать анафилактические реакции и ангионевротический отек, которые без лечения могут быть опасными для жизни.Диарея и рвота, связанные с FPIES и эозинофильным гастроэнтеритом, могут привести к осложнениям, включая тяжелое обезвоживание и гиповолемический шок.
Сдерживание и обучение пациентов
У здоровых детей грудного возраста рекомендуется обеспечить исключительно грудное вскармливание до 6 месяцев грудного возраста и постепенное введение твердой пищи после 6 месяцев, чтобы предотвратить пищевую аллергию или непереносимость. Младенцы с аллергией на коровье молоко должны избегать молочных смесей и должны находиться на грудном вскармливании.Кормящим матерям желательно исключить из рациона молочные продукты. Если пострадавший младенец не находится на грудном вскармливании, может быть назначена интенсивно гидролизованная смесь.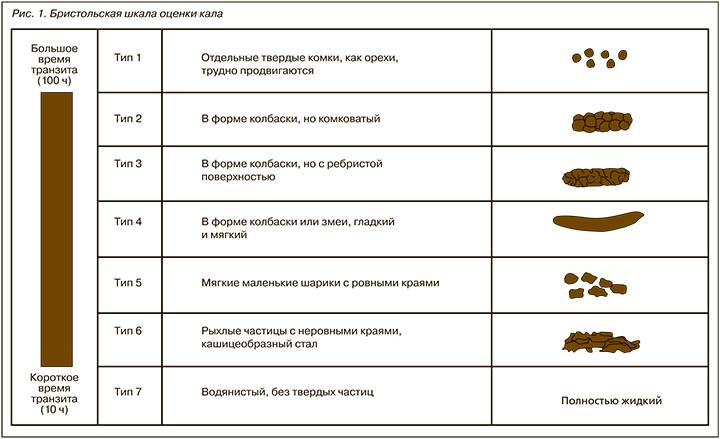 Медицинские работники должны информировать пациентов о важности отмены диеты при подозрении на непереносимость белка или аллергию. Пациентам следует обратить внимание на подозреваемый ингредиент в пищевых продуктах. Пациенты, находящиеся на элиминационной диете, также должны получать соответствующие рекомендации от диетолога или нутрициолога. Пациентам с острыми реакциями гиперчувствительности на пищевые белки в анамнезе следует назначать шприц-ручки с адреналином.
Медицинские работники должны информировать пациентов о важности отмены диеты при подозрении на непереносимость белка или аллергию. Пациентам следует обратить внимание на подозреваемый ингредиент в пищевых продуктах. Пациенты, находящиеся на элиминационной диете, также должны получать соответствующие рекомендации от диетолога или нутрициолога. Пациентам с острыми реакциями гиперчувствительности на пищевые белки в анамнезе следует назначать шприц-ручки с адреналином.
Улучшение результатов работы команды здравоохранения
Белковая непереносимость — это расстройство, которое требует подхода межпрофессиональной команды как для диагностики, так и для лечения. От сбора анамнеза, проведения исследований до постановки правильного диагноза от медицинских работников требуются хорошие коммуникативные и диагностические навыки. Соблюдение со стороны пациента не менее важно в лечении этого состояния. Поскольку отказ от диеты остается основным методом лечения непереносимости белка, необходимо уделять большое внимание регулярным консультациям с диетологом или нутрициологом.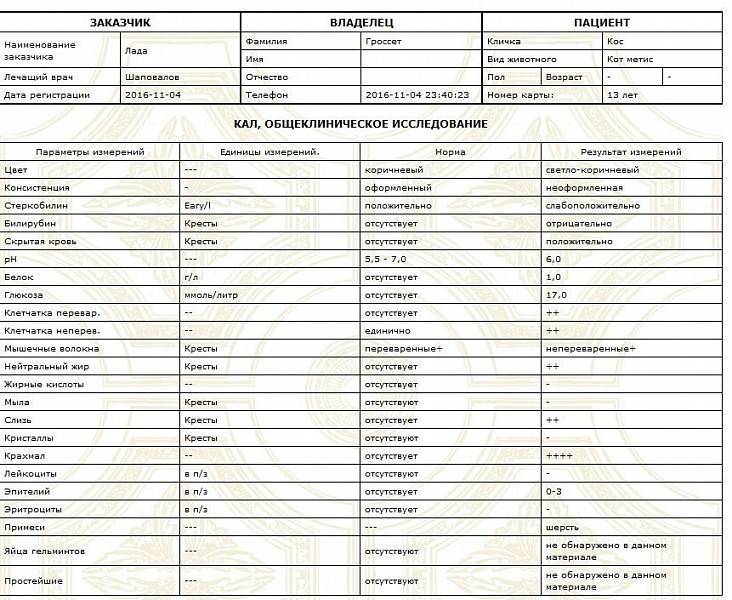 Управление индивидуально для каждого пациента. У пациентов, у которых развиваются острые реакции (например, реакции гиперчувствительности при состояниях, опосредованных IgE, тяжелое обезвоживание или шок при FPIES), медсестры и фельдшеры играют жизненно важную роль в межпрофессиональной группе, поскольку они будут контролировать жизненные показатели пациента, вводить жидкости и лекарства, и помочь с образованием пациента и его семьи.
Управление индивидуально для каждого пациента. У пациентов, у которых развиваются острые реакции (например, реакции гиперчувствительности при состояниях, опосредованных IgE, тяжелое обезвоживание или шок при FPIES), медсестры и фельдшеры играют жизненно важную роль в межпрофессиональной группе, поскольку они будут контролировать жизненные показатели пациента, вводить жидкости и лекарства, и помочь с образованием пациента и его семьи.
Аллергологи также играют важную роль в диагностике непереносимости белков, поскольку расстройство часто связано с сенсибилизацией к пищевым белкам.Часто родители или опекуны педиатрических пациентов или сами взрослые пациенты с хронической или тяжелой непереносимостью белков испытывают значительное бремя, беспокойство, беспокойство и стресс, о которых следует заботиться при помощи консультантов, психологов или психиатров, когда это необходимо.
Прогноз при непереносимости белка благоприятный. Надлежащая идентификация возбудителя и его избегание помогает контролировать расстройство. Недавние данные свидетельствуют о том, что сенсибилизацию к коровьему молоку, ведущую к непереносимости и аллергии, можно в первую очередь предотвратить, избегая добавок на основе коровьего молока в течение как минимум первых 3 дней жизни.[18] [Уровень 1] Исследование, проведенное в 2019 году, также успешно продемонстрировало гипоаллергенность новой интенсивно гидролизованной смеси на основе сыворотки, которая содержит два олигосахарида грудного молока.[19] [Уровень 1] Различные текущие исследования добавили новые аспекты в профилактику и лечение непереносимости пищевого белка.
Ссылки
- 1.
- Flom JD, Sicherer SH. Эпидемиология аллергии на коровье молоко. Питательные вещества. 2019 May 10;11(5) [бесплатная статья PMC: PMC6566637] [PubMed: 31083388]
- 2.
- Сэвидж Дж., Джонс С.Б. Пищевая аллергия: эпидемиология и естественное течение. Иммунол Аллергия Клин Норт Ам. 2015 фев; 35 (1): 45-59. [Бесплатная статья PMC: PMC4254585] [PubMed: 25459576]
- 3.
- Ахонди Х., Росс А.Б. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 6 июля 2021 г. Глютен и связанные с ним медицинские проблемы. [PubMed: 30860740]
- 4.
- Untersmayr E. Влияние желудочного пищеварения на развитие пищевой аллергии. Преподобный отец Аллергол (2009).2015 ноябрь;55(7):444-447. [Бесплатная статья PMC: PMC5467726] [PubMed: 28616101]
- 5.
- Lomer MC. Обзорная статья: этиология, диагностика, механизмы и клинические проявления пищевой непереносимости. Алимент Фармакол Тер. 2015 фев; 41 (3): 262-75. [PubMed: 25471897]
- 6.
- Rona RJ, Keil T, Summers C, Gislason D, Zuidmeer L, Sodergren E, Sigurdardottir ST, Lindner T, Goldhahn K, Dahlstrom J, McBride D, Madsen C. Распространенность Пищевая аллергия: метаанализ. J Аллергия Клин Иммунол.2007 г., сен; 120 (3): 638-46. [PubMed: 17628647]
- 7.
- Mehr S, Frith K, Campbell DE. Эпидемиология синдрома энтероколита, вызванного пищевыми белками. Курр Опин Аллергия Клин Иммунол. 2014 июнь;14(3):208-16. [Бесплатная статья PMC: PMC4011623] [PubMed: 24686277]
- 8.
- Сингх П., Арора А., Стрэнд Т.А., Леффлер Д.А., Катасси С., Грин П.Х., Келли С.П., Ахуджа В., Махария Г.К. Глобальная распространенность глютеновой болезни: систематический обзор и метаанализ. Клин Гастроэнтерол Гепатол. 2018 июнь; 16 (6): 823-836.е2. [PubMed: 29551598]
- 9.
- Ивкович-Юрекович И. [Синдром оральной аллергии]. Acta Med Croatica. 2014 июнь; 68 (3): 283-7. [PubMed: 26016219]
- 10.
- Roussel JM, Pandit S. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 14 августа 2021 г. Эозинофильный эзофагит. [PubMed: 2
29]
- 11.
- Ingle SB, Hinge Ingle CR. Эозинофильный гастроэнтерит: необычный тип гастроэнтерита. Мир J Гастроэнтерол. 2013 21 августа; 19 (31): 5061-6.[Бесплатная статья PMC: PMC3746377] [PubMed: 23964139]
- 12.
- Tarlow MJ, Hadorn B, Arthurton MW, Lloyd JK. Дефицит кишечной энтерокиназы. Недавно обнаруженное нарушение переваривания белков. Арч Дис Чайлд. 1970 окт; 45 (243): 651-5. [Бесплатная статья PMC: PMC1647492] [PubMed: 5477679]
- 13.
- Сатьянараяна Рао Т.С., Ерагани В.К. Гипертонический криз и сыр. Индийская психиатрия. 2009 Январь; 51 (1): 65-6. [Бесплатная статья PMC: PMC2738414] [PubMed: 19742203]
- 14.
- Tabanelli G. Биогенные амины и качество продуктов питания: новые проблемы и проблемы общественного здравоохранения. Еда. 2020 Jul 01;9(7) [PMC бесплатная статья: PMC7404793] [PubMed: 32630178]
- 15.
- Giannetti A, Cipriani F, Indio V, Gallucci M, Caffarelli C, Ricci G. Влияние атопического дерматита на коровью Аллергия на молоко у детей. Медицина (Каунас). 2019 авг. 10; 55 (8) [бесплатная статья PMC: PMC6723735] [PubMed: 31405131]
- 16.
- Мураро А., Верфель Т., Хоффманн-Зоммергрубер К., Робертс Г., Бейер К., Биндслев-Йенсен К., Кардона В. , Дюбуа А., Дютуа Г., Эйгенманн П., Фернандес Ривас М., Халкен С., Хикштейн Л., Хёст А., Кнол Э., Лак Г., Маркизотто М.Дж., Ниггеманн Б., Нвару Б.И., Пападопулос Н.Г., Поулсен Л.К., Сантос А.Ф., Скайпала И., Шёпфер А., Ван Ри Р., Вентер С., Ворм М., Влиг-Бурстра Б., Панесар С., де Сильва Д., Соарес-Вайзер К., Шейх А., Балмер-Вебер Б.К., Нильссон С., де Йонг Н.В., Акдис К.А., Группа рекомендаций EAACI по пищевой аллергии и анафилаксии. Рекомендации EAACI по пищевой аллергии и анафилаксии: диагностика и лечение пищевой аллергии. Аллергия. 2014 авг;69(8):1008-25. [PubMed: 24
6]
- 17.
- Гонсалвес Н. Эозинофильные желудочно-кишечные расстройства. Клин Рев Аллергия Иммунол. 2019 окт;57(2):272-285. [PubMed: 309]
- 18.
- Urashima M, Mezawa H, Okuyama M, Urashima T, Hirano D, Gocho N, Tachimoto H. Первичная профилактика сенсибилизации к коровьему молоку и пищевой аллергии путем отказа от добавок с коровьим молоком при рождении : Рандомизированное клиническое исследование.JAMA Педиатр. 01 декабря 2019 г.; 173(12):1137-1145. [Бесплатная статья PMC: PMC6806425] [PubMed: 31633778]
- 19.
- Nowak-Wegrzyn A, Czerkies L, Reyes K, Collins B, Heine RG. Подтверждена гипоаллергенность новой интенсивно гидролизованной детской смеси на основе молочной сыворотки, содержащей два олигосахарида грудного молока. Питательные вещества. 2019 Jun 26;11(7) [Бесплатная статья PMC: PMC6682865] [PubMed: 31248026]
Непереносимость белков — StatPearls — NCBI Bookshelf
Continuing Education Activity
Непереносимость белков — это побочное действие, возникающее в результате нарушения приема пищевых белков.Это вызвано различными механизмами и обычно связано с симптомами, затрагивающими желудочно-кишечный тракт. В этом мероприятии рассматривается оценка и лечение непереносимости белка и подчеркивается роль межпрофессиональной команды в уходе за пациентами с этим заболеванием.
Цели:
Объясните патофизиологию непереносимости белка.
Опишите соответствующую оценку непереносимости белка.
Ознакомьтесь с общими вариантами ведения пациентов с непереносимостью белка.
Обобщить стратегии межпрофессиональной команды по улучшению координации помощи и коммуникации для улучшения ухода за пациентами с непереносимостью белка и улучшения результатов.
Введение
Белковая непереносимость – это расстройство, возникающее в результате неблагоприятного воздействия приема пищевых белков. Он развивается за счет иммунологических, неиммунологических, метаболических, генетических и фармакологических механизмов.Это часто связано с желудочно-кишечными симптомами. При раннем выявлении состояния и вмешательстве расстройство в основном поддается лечению и имеет благоприятный прогноз.
Этиология
Непереносимость белка вызвана неспособностью переваривать или эффективно расщеплять аминокислоты. Когда пищевые белки плохо перевариваются, они могут действовать как антигены, что приводит к аллергии на пищевые белки. Наиболее часто белки коровьего молока являются причиной пищевой непереносимости в младенческом возрасте.[1] Синдром энтероколита, вызванный пищевыми белками, также обычно связывают с непереносимостью белков коровьего молока. У пораженных лиц наблюдаются диарея, отеки и гипоальбуминемия. С увеличением возраста и введением различных продуктов непереносимость яичного белка, аллергия на сою и арахис становятся более распространенными.[2]
Непереносимость белка наблюдается при следующих состояниях:
Иммунологическая непереносимость пищевого белка: может быть IgE-опосредованной или не-IgE-опосредованной.
IGE Оснащенные условия включают в себя:
Осращенные в IgE Условия включают в себя:
Пищевой белкового белка Энтероколит
Пищевая белка Enteropathey
Пищевой белковочный аллергический проблит
аутоиммунная реакция : Аутоиммунная реакция на белки глютена обнаруживается при глютеновой болезни, чувствительности к глютену без целиакии, аллергии на пшеницу, глютеновой атаксии и герпетиформном дерматите.[3]
Дефицит ферментов: дефицит энтерокиназы (энтеропептидазы)
Метаболические нарушения:
Генетические/наследственные нарушения: нарушения цикла мочевины, непереносимость лизинурического белка Биогенные амины:
тирамин в возрасте сыра
гистамин
undefined: синдром раздраженного кишечника
эпидемиология
Нетерпимость пищевых продуктов повлияла на 15% до 20% населения.[5] Аллергия на коровье молоко (CMA), реакция на белки в коровьем молоке, является наиболее распространенной пищевой аллергией в раннем возрасте с предполагаемым диапазоном распространенности от 0,5% до 3% в возрасте 1 года.[1][2] ][6] Однако, судя по естественному течению CMA, его разрешение является распространенным явлением, и ожидается, что его распространенность будет ниже у взрослых.
В австралийском исследовании у одного из 10 000 младенцев в возрасте до 2 лет был обнаружен синдром энтероколита, вызванного пищевыми белками (FPIES). Обнаружено, что FPIES встречается преимущественно у младенцев и связан с обычными пищевыми триггерами (белки в коровьем молоке, соя, рис, овес и яйца), но эпидемиологические данные все еще отсутствуют.[7]
Целиакия считается серьезной проблемой общественного здравоохранения, и о ней сообщают во всем мире. Он наиболее распространен в Западной Европе и Соединенных Штатах, но у большинства больных он не диагностируется. Метаанализ, проведенный в 2018 году, показал, что распространенность целиакии составляет 1,4% на основе серологических тестов и 0,7% на основе биопсии.[8]
Хотя предрасположенность к половому признаку неизвестна, FPIES и эозинофильный гастроэнтерит имеют незначительное преобладание у мужчин, в то время как женщины немного чаще страдают глютеновой болезнью.
Патофизиология
Макромолекулы пищевого белка состоят из последовательностей аминокислот, соединенных пептидными связями. Эти связи должны быть гидролизованы и подвергнуты ферментативному воздействию до того, как будут абсорбированы свободные аминокислоты. Процесс переваривания белков начинается в желудке пепсинами с помощью соляной (HCl) кислоты. Затем этот частично переваренный белок достигает двенадцатиперстной кишки, где высокий рН останавливает пептическую активность, а ферменты поджелудочной железы (трипсин, химотрипсин, карбоксипептидазы) берут на себя процесс пищеварения.Небольшие цепочки аминокислот, образующиеся в просвете, теперь подвергаются мембранному перевариванию на щеточной кайме энтероцитов. Мембранные экзопептидазы гидролизуют цепи аминокислот с образованием отдельных аминокислот, которые всасываются в энтероциты и попадают в кровоток для использования в организме.
Непереносимость белка может возникать из-за любых отклонений в процессах пищеварения или метаболизма. Когда пищевые белки не полностью денатурируются желудочной кислотой, это приводит к сенсибилизации белка в кишечнике, что приводит к пищевой аллергии.Гипоацидные состояния, наблюдаемые у пациентов, длительно лечившихся от диспепсических расстройств, часто приводят к развитию аллергии на пищевые белки.[4]
Анамнез и физикальное исследование
Клинические проявления непереносимости пищевого белка затрагивают различные системы органов и варьируют в зависимости от различных заболеваний. Тем не менее, у пациентов в основном проявляются желудочно-кишечные проявления. При неиммунологической непереносимости пищевого белка количество потребляемой пищи, как правило, более непосредственно связано с тяжестью симптомов.Чрезмерное газообразование в кишечнике, вздутие живота, боль в животе и диарея являются распространенными симптомами. Принимая во внимание, что при иммунологической аллергии на пищевой белок даже следовые количества сенсибилизированного пищевого белка могут вызвать взрывную реакцию и могут поразить кожу и кровеносные сосуды. IgE-опосредованные реакции возникают в течение от нескольких минут до часа после приема пищевого белка, и симптомы варьируют от кожной сыпи, крапивницы, ангионевротического отека, свистящего дыхания до анафилаксии, тогда как не-IgE-опосредованные реакции могут развиваться в течение от нескольких часов до нескольких дней.
Типичным проявлением у младенцев может быть диарея у младенцев в возрасте до 6 месяцев и со временем рвота после кормления молочной смесью в течение нескольких недель. Синдром пищевого проктоколита является распространенным состоянием, при котором у здоровых младенцев возникает диарея, но вес не снижается. Принимая во внимание, что в случае FPIES младенец может обезвоживаться и терять вес.
Вот некоторые симптомы и физические данные, которые наблюдаются при различных нарушениях непереносимости белка:
Синдром оральной аллергии: Реакция в основном возникает из-за перекрестной реактивности между пыльцой и пищей растительного происхождения (фруктами и овощами) и симптомы локализуются на слизистой оболочке полости рта.[9] Симптомы включают зуд и жжение в губах, языке, небе и горле. Возможны ангионевротический отек и рвота.
Немедленная гиперчувствительность ЖКТ: у пациентов появляются тошнота, боль в животе и рвота в течение 1–2 часов после приема сенсибилизированного пищевого белка, часто с последующей диареей. Пораженные люди имеют периодические боли в животе, плохой аппетит и плохую прибавку в весе.
Эозинофильный эзофагит (ЭоЭ): у пациентов возникают затруднения при глотании, застревание твердой пищи, боли в животе, регургитация или рвота и снижение аппетита.У детей младшего возраста могут возникнуть трудности с кормлением и плохая прибавка в весе. Симптомы часто совпадают, и их часто путают с гастроэзофагеальной рефлюксной болезнью (ГЭРБ). Однако у пациентов с ЭоЭ часто обнаруживают в анамнезе и другие аутоиммунные и аллергические состояния.[10]
Эозинофильный гастрит: они обычно проявляются признаками гастрита, такими как боль в животе, постпрандиальная рвота, раннее насыщение, анорексия и задержка развития. Заболевание очень чувствительно к диетическим ограничениям у детей.Примерно 50% этих пациентов также имеют признаки атопии.
Эозинофильный гастроэнтерит: это редкое заболевание с хроническим рецидивирующим течением, характеризующееся инфильтрацией эозинофилами слизистой оболочки желудочно-кишечного тракта. Презентация может быть разной. У детей могут наблюдаться задержка развития, задержка роста, задержка полового созревания или аменорея. Часто у взрослых возникают боли в животе, дисфагия или диарея. Они также могут проявляться признаками энтеропатии с потерей белка, желудочно-кишечными кровотечениями или нарушением всасывания.[11]
Синдром энтероколита, вызванного пищевыми белками (FPIES): у пациентов может появиться рвота через один-три часа после еды. У них также может быть вздутие живота, кровавый понос, анемия и потеря веса, и обычно они провоцируются смесями на основе коровьего молока или соевого белка. При физическом осмотре могут быть очевидны признаки обезвоживания. Отсутствуют респираторные симптомы или классические IgE-опосредованные аллергические кожные реакции.
Энтеропатия, вызванная пищевым белком: Пациенты с энтеропатией, вызванной пищевым белком, имеют стеаторею и задержку физического развития в первые несколько месяцев жизни.
Аллергический проктоколит, вызванный пищевым белком: обычно наблюдается у здоровых младенцев, находящихся на грудном вскармливании. У них появляются симптомы стула с прожилками крови в первые несколько месяцев жизни.
Целиакия: у пациентов с целиакией обычно наблюдаются диарея, дурно пахнущий стул, стеаторея, урчание в носу, метеоризм и потеря веса. Больные жалуются на слабость и быструю утомляемость, обычно связанные с неправильным питанием. Могут быть очевидны признаки анемии. Может отмечаться герпетиформный дерматит, зудящая папуловезикулярная сыпь на разгибательных поверхностях конечностей, туловище и ягодицах.
Дефицит энтерокиназы: у младенцев с дефицитом этого фермента с рождения развивается диарея, и они плохо развиваются. При хронической мальабсорбции белка склонны к развитию гипопротеинемических отеков. Пероральное введение экстракта поджелудочной железы приводит к быстрому контролю симптомов и способствует ускорению роста.[12]
Врожденные нарушения обмена веществ: Эти нарушения приводят к накоплению метаболитов перед дефектным ферментом (аминокислоты и/или аммиак), вызывая интоксикацию.Симптомы варьируются в зависимости от пораженных ферментов.
Токсические реакции на биогенные амины: Проглатывание некоторых биогенных аминов способствует развитию токсических реакций. Пациенты могут жаловаться на головную боль, сердцебиение, рвоту, диарею и аллергию. Установлено, что употребление выдержанного сыра, содержащего тирамин, в сочетании с применением ингибиторов моноаминоксидазы (ИМАО) вызывает головные боли и гипертонический криз.[13] Гистамин более токсичен и может вызывать такие эффекты, как гипотония, раздражение кожи, головная боль, сердцебиение, приступы астмы и т. д.Эта симптоматика известна как «отравление скомброидной рыбой», которое наблюдается после употребления в пищу рыбы из семейств Scombridae и Scomberesocidae (тунец, скумбрия, пеламида, луфарь и т. д.), содержащей высокий уровень гистамина.[14]
Дерматологические проявления:
Белковая непереносимость часто связана с дерматологическими атопическими состояниями. Исследование, проведенное в Италии, показало, что 71% детей с сопутствующей аллергией на коровье молоко имеют сопутствующий атопический дерматит.[15] Другие дерматологические симптомы включают крапивницу, сыпь и ангионевротический отек.
Оценка
Не существует специального теста для диагностики непереносимости пищевого белка. Состояние оценивается в первую очередь на основе подробного анамнеза и физического осмотра. Клиницисты должны распознавать и дифференцировать иммунологическую непереносимость пищевого белка от неиммунологической, чтобы предотвратить симптомы и управлять ими. При IgE-опосредованной пищевой аллергии обычно очевидны положительные кожные прик-тесты на пищевые белки наряду с обнаружением специфических пищевых IgE-антител.Однако в большинстве случаев непереносимость пищевых белков не опосредована IgE.
При подозрении на непереносимость пищевого белка в диагностике помогают следующие меры и тесты:
Дневник питания: важно вести дневник питания, поскольку он помогает клиницистам сопоставить симптомы и выяснить взаимосвязь пищи с симптомы пациента.
Кожный прик-тест: Этот тест позволяет выявить IgE-опосредованную аллергию на пищевой белок. Хотя положительный результат теста может свидетельствовать о наличии антител IgE, он имеет низкую прогностическую ценность, в то время как отрицательный результат теста имеет высокую прогностическую точность.
Атопический кожный пластырь: Тест используется для выявления отсроченной непереносимости пищевых белков (клеточно-опосредованные реакции).
Анализ сывороточного специфического IgE: Его также проводят для выявления антигенспецифического IgE в сыворотке пациента.
Отказ от диеты: если есть подозрение на непереносимость пищевого белка или аллергию, пациент должен соблюдать диету, свободную от подозреваемого белка, в течение 2–4 недель. Если симптомы улучшаются, в качестве диагностического теста может быть проведен тест на пероральную пищевую провокацию.
Оральный тест на пищевую провокацию: это тест золотого стандарта, который проводится под наблюдением врача для диагностики или исключения пищевой аллергии. Диагноз непереносимости пищевого белка может быть поставлен, когда симптомы исчезают после исключения из рациона соответствующего продукта, а затем симптомы возвращаются после введения того же продукта. Реакции и симптомы должны быть воспроизводимы при повторных тестах на исключение диеты и пищевых пробах. Некоторые реакции со стороны желудочно-кишечного тракта могут проявляться с отсроченным началом, вызывая появление симптомов через несколько часов или дней после приема внутрь.
Радиоаллергосорбентный тест (РАСТ): Этот тест выявляет аллерген-специфические антитела Ig-E с помощью радиоиммуноанализа. Он полезен для определения причин аллергии и часто дает положительный результат при гиперчувствительности немедленного желудочно-кишечного тракта.
Дифференциальный подсчет лейкоцитов: Этот тест подтверждает диагноз аллергического эозинофильного гастрита, аллергического эозинофильного гастроэнтерита и других аллергических состояний, когда наблюдается периферическая эозинофилия.
Анализ кала: Анализ кала может выявить скрытую кровь или фекальные лейкоциты и указать на наличие воспаления.
Биопсия: при аллергическом эозинофильном эзофагите, гастрите и гастроэнтерите биопсия показывает эозинофильную инфильтрацию слизистой и подслизистой оболочки. Биопсия тощей кишки при синдроме энтероколита и глютеновой болезни показывает атрофию ворсин и кишечную инфильтрацию лимфоцитами.
Лечение/управление
Единственным окончательным методом лечения непереносимости пищевого белка является строгое исключение пищевого белка из рациона. Пациентов следует консультировать по вопросам контроля за составом пищевых продуктов и соблюдения элиминационной диеты.Пациенты, находящиеся на долгосрочной элиминационной диете, также должны иметь доступ к соответствующим диетическим консультациям, в идеале диетологом или диетологом, и к регулярному мониторингу роста, особенно у детей.
Матерям, находящимся на грудном вскармливании, следует рекомендовать избегать коровьего молока и молочных продуктов. В качестве средства выбора для лечения аллергии на коровье молоко, особенно у младенцев и детей младшего возраста, не находящихся на грудном вскармливании, следует рекомендовать интенсивно гидролизованную смесь с подтвержденной гипоаллергенностью. Для пациентов с более тяжелыми симптомами также могут быть рекомендованы формулы аминокислот.[16]
Стероиды являются основным средством лечения IgE-опосредованной иммунологической непереносимости пищевых белков, включая эозинофильные желудочно-кишечные расстройства.[17]
Новорожденных с острым FPIES с легкими симптомами (без вялости, бледности или апатии) можно лечить в домашних условиях с помощью пероральной регидратации. Но при тяжелых симптомах их необходимо лечить в медицинском учреждении с помощью внутривенных вливаний. Внутримышечный адреналин и антигистаминные препараты не играют никакой роли в лечении реакций FPIES.
При подозрении на острые аллергические реакции или анафилаксию следует немедленно отказаться от вероятного продукта питания и оказать неотложную медицинскую помощь.Им могут выписать рецепт на автоинъекционное устройство с адреналином и проинструктировать, как им правильно пользоваться.
Дифференциальный диагноз
Некоторые распространенные дифференциальные диагнозы при непереносимости пищевого белка обсуждаются ниже:
Кишечные инфекции: Кишечные инфекции могут также проявляться симптомами, сходными с непереносимостью белков, или предрасполагать к ним. Пациенты с кишечными инфекциями часто имеют признаки инфекции и могут лечиться противомикробными препаратами.
Целиакия: Целиакия является широко многофакторным заболеванием с сильным наследственным компонентом и ассоциацией с HLA (DQ2 и DQ8). Они могут проявляться аутоиммунной реакцией на глютеновый белок в пищевых продуктах. Тестирование на сывороточные антитела IgA к тканевой трансглютаминазе (анти-tTG IgA) может помочь в диагностике целиакии или исключить ее как причину непереносимости белка.
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ): у детей наблюдаются такие симптомы, как нарушения сна, рвота, плохой аппетит, плохой рост, хрипы и стридор.Взрослые испытывают изжогу, рвоту и срыгивание. ГЭРБ можно лечить с помощью фармакотерапии и хирургического вмешательства или без них. Они не имеют отношения к тому или иному пищевому белку.
Воспалительные заболевания кишечника (ВЗК): они включают болезнь Крона и язвенный колит, которые могут проявляться обычными желудочно-кишечными симптомами, такими как диарея, ректальное кровотечение и боль в животе. Однако важно исключить ВЗК, поскольку они являются системными хроническими заболеваниями и требуют обширного лечения.
Прогноз
Прогноз при многих случаях непереносимости белков благоприятный при соблюдении строгой элиминационной диеты. Многие исследования показали, что прогноз при непереносимости белка коровьего молока благоприятен: у большинства пациентов аллергия перерастает в детстве и раннем подростковом возрасте.[2] Однако у некоторых детей с IgE-опосредованной непереносимостью белков развиваются аллергический риноконъюнктивит и астма.
Осложнения
Белок является важным питательным веществом для здоровья и развития нашего организма.Общие осложнения непереносимости белка, приводящие к дефициту белка, включают потерю мышечной массы, задержку роста, задержку развития и ослабление иммунной системы. У пострадавших людей могут быть такие симптомы, как отеки ног, лица и других частей тела, сухие и ломкие волосы, усталость и частые инфекции.
У взрослых аллергические реакции на белки коровьего молока часто осложняются непереносимостью лактозы, которая усиливается с возрастом. IgE-опосредованные аллергические состояния могут вызывать анафилактические реакции и ангионевротический отек, которые без лечения могут быть опасными для жизни.Диарея и рвота, связанные с FPIES и эозинофильным гастроэнтеритом, могут привести к осложнениям, включая тяжелое обезвоживание и гиповолемический шок.
Сдерживание и обучение пациентов
У здоровых детей грудного возраста рекомендуется обеспечить исключительно грудное вскармливание до 6 месяцев грудного возраста и постепенное введение твердой пищи после 6 месяцев, чтобы предотвратить пищевую аллергию или непереносимость. Младенцы с аллергией на коровье молоко должны избегать молочных смесей и должны находиться на грудном вскармливании.Кормящим матерям желательно исключить из рациона молочные продукты. Если пострадавший младенец не находится на грудном вскармливании, может быть назначена интенсивно гидролизованная смесь. Медицинские работники должны информировать пациентов о важности отмены диеты при подозрении на непереносимость белка или аллергию. Пациентам следует обратить внимание на подозреваемый ингредиент в пищевых продуктах. Пациенты, находящиеся на элиминационной диете, также должны получать соответствующие рекомендации от диетолога или нутрициолога. Пациентам с острыми реакциями гиперчувствительности на пищевые белки в анамнезе следует назначать шприц-ручки с адреналином.
Улучшение результатов работы команды здравоохранения
Белковая непереносимость — это расстройство, которое требует подхода межпрофессиональной команды как для диагностики, так и для лечения. От сбора анамнеза, проведения исследований до постановки правильного диагноза от медицинских работников требуются хорошие коммуникативные и диагностические навыки. Соблюдение со стороны пациента не менее важно в лечении этого состояния. Поскольку отказ от диеты остается основным методом лечения непереносимости белка, необходимо уделять большое внимание регулярным консультациям с диетологом или нутрициологом.Управление индивидуально для каждого пациента. У пациентов, у которых развиваются острые реакции (например, реакции гиперчувствительности при состояниях, опосредованных IgE, тяжелое обезвоживание или шок при FPIES), медсестры и фельдшеры играют жизненно важную роль в межпрофессиональной группе, поскольку они будут контролировать жизненные показатели пациента, вводить жидкости и лекарства, и помочь с образованием пациента и его семьи.
Аллергологи также играют важную роль в диагностике непереносимости белков, поскольку расстройство часто связано с сенсибилизацией к пищевым белкам.Часто родители или опекуны педиатрических пациентов или сами взрослые пациенты с хронической или тяжелой непереносимостью белков испытывают значительное бремя, беспокойство, беспокойство и стресс, о которых следует заботиться при помощи консультантов, психологов или психиатров, когда это необходимо.
Прогноз при непереносимости белка благоприятный. Надлежащая идентификация возбудителя и его избегание помогает контролировать расстройство. Недавние данные свидетельствуют о том, что сенсибилизацию к коровьему молоку, ведущую к непереносимости и аллергии, можно в первую очередь предотвратить, избегая добавок на основе коровьего молока в течение как минимум первых 3 дней жизни.[18] [Уровень 1] Исследование, проведенное в 2019 году, также успешно продемонстрировало гипоаллергенность новой интенсивно гидролизованной смеси на основе сыворотки, которая содержит два олигосахарида грудного молока.[19] [Уровень 1] Различные текущие исследования добавили новые аспекты в профилактику и лечение непереносимости пищевого белка.
Ссылки
- 1.
- Flom JD, Sicherer SH. Эпидемиология аллергии на коровье молоко. Питательные вещества. 2019 May 10;11(5) [бесплатная статья PMC: PMC6566637] [PubMed: 31083388]
- 2.
- Сэвидж Дж., Джонс С.Б. Пищевая аллергия: эпидемиология и естественное течение. Иммунол Аллергия Клин Норт Ам. 2015 фев; 35 (1): 45-59. [Бесплатная статья PMC: PMC4254585] [PubMed: 25459576]
- 3.
- Ахонди Х., Росс А.Б. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 6 июля 2021 г. Глютен и связанные с ним медицинские проблемы. [PubMed: 30860740]
- 4.
- Untersmayr E. Влияние желудочного пищеварения на развитие пищевой аллергии. Преподобный отец Аллергол (2009).2015 ноябрь;55(7):444-447. [Бесплатная статья PMC: PMC5467726] [PubMed: 28616101]
- 5.
- Lomer MC. Обзорная статья: этиология, диагностика, механизмы и клинические проявления пищевой непереносимости. Алимент Фармакол Тер. 2015 фев; 41 (3): 262-75. [PubMed: 25471897]
- 6.
- Rona RJ, Keil T, Summers C, Gislason D, Zuidmeer L, Sodergren E, Sigurdardottir ST, Lindner T, Goldhahn K, Dahlstrom J, McBride D, Madsen C. Распространенность Пищевая аллергия: метаанализ. J Аллергия Клин Иммунол.2007 г., сен; 120 (3): 638-46. [PubMed: 17628647]
- 7.
- Mehr S, Frith K, Campbell DE. Эпидемиология синдрома энтероколита, вызванного пищевыми белками. Курр Опин Аллергия Клин Иммунол. 2014 июнь;14(3):208-16. [Бесплатная статья PMC: PMC4011623] [PubMed: 24686277]
- 8.
- Сингх П., Арора А., Стрэнд Т.А., Леффлер Д.А., Катасси С., Грин П.Х., Келли С.П., Ахуджа В., Махария Г.К. Глобальная распространенность глютеновой болезни: систематический обзор и метаанализ. Клин Гастроэнтерол Гепатол. 2018 июнь; 16 (6): 823-836.е2. [PubMed: 29551598]
- 9.
- Ивкович-Юрекович И. [Синдром оральной аллергии]. Acta Med Croatica. 2014 июнь; 68 (3): 283-7. [PubMed: 26016219]
- 10.
- Roussel JM, Pandit S. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 14 августа 2021 г. Эозинофильный эзофагит. [PubMed: 2
29]
- 11.
- Ingle SB, Hinge Ingle CR. Эозинофильный гастроэнтерит: необычный тип гастроэнтерита. Мир J Гастроэнтерол. 2013 21 августа; 19 (31): 5061-6.[Бесплатная статья PMC: PMC3746377] [PubMed: 23964139]
- 12.
- Tarlow MJ, Hadorn B, Arthurton MW, Lloyd JK. Дефицит кишечной энтерокиназы. Недавно обнаруженное нарушение переваривания белков. Арч Дис Чайлд. 1970 окт; 45 (243): 651-5. [Бесплатная статья PMC: PMC1647492] [PubMed: 5477679]
- 13.
- Сатьянараяна Рао Т.С., Ерагани В.К. Гипертонический криз и сыр. Индийская психиатрия. 2009 Январь; 51 (1): 65-6. [Бесплатная статья PMC: PMC2738414] [PubMed: 19742203]
- 14.
- Tabanelli G. Биогенные амины и качество продуктов питания: новые проблемы и проблемы общественного здравоохранения. Еда. 2020 Jul 01;9(7) [PMC бесплатная статья: PMC7404793] [PubMed: 32630178]
- 15.
- Giannetti A, Cipriani F, Indio V, Gallucci M, Caffarelli C, Ricci G. Влияние атопического дерматита на коровью Аллергия на молоко у детей. Медицина (Каунас). 2019 авг. 10; 55 (8) [бесплатная статья PMC: PMC6723735] [PubMed: 31405131]
- 16.
- Мураро А., Верфель Т., Хоффманн-Зоммергрубер К., Робертс Г., Бейер К., Биндслев-Йенсен К., Кардона В. , Дюбуа А., Дютуа Г., Эйгенманн П., Фернандес Ривас М., Халкен С., Хикштейн Л., Хёст А., Кнол Э., Лак Г., Маркизотто М.Дж., Ниггеманн Б., Нвару Б.И., Пападопулос Н.Г., Поулсен Л.К., Сантос А.Ф., Скайпала И., Шёпфер А., Ван Ри Р., Вентер С., Ворм М., Влиг-Бурстра Б., Панесар С., де Сильва Д., Соарес-Вайзер К., Шейх А., Балмер-Вебер Б.К., Нильссон С., де Йонг Н.В., Акдис К.А., Группа рекомендаций EAACI по пищевой аллергии и анафилаксии. Рекомендации EAACI по пищевой аллергии и анафилаксии: диагностика и лечение пищевой аллергии. Аллергия. 2014 авг;69(8):1008-25. [PubMed: 24
6]
- 17.
- Гонсалвес Н. Эозинофильные желудочно-кишечные расстройства. Клин Рев Аллергия Иммунол. 2019 окт;57(2):272-285. [PubMed: 309]
- 18.
- Urashima M, Mezawa H, Okuyama M, Urashima T, Hirano D, Gocho N, Tachimoto H. Первичная профилактика сенсибилизации к коровьему молоку и пищевой аллергии путем отказа от добавок с коровьим молоком при рождении : Рандомизированное клиническое исследование.JAMA Педиатр. 01 декабря 2019 г.; 173(12):1137-1145. [Бесплатная статья PMC: PMC6806425] [PubMed: 31633778]
- 19.
- Nowak-Wegrzyn A, Czerkies L, Reyes K, Collins B, Heine RG. Подтверждена гипоаллергенность новой интенсивно гидролизованной детской смеси на основе молочной сыворотки, содержащей два олигосахарида грудного молока. Питательные вещества. 2019 Jun 26;11(7) [Бесплатная статья PMC: PMC6682865] [PubMed: 31248026]
Маркеры воспаления в фекалиях младенцев с аллергией на коровье молоко
Существует все больше свидетельств того, что воздействие коровьего молока вызывает воспаление в кишечнике младенцев с аллергией на коровье молоко, независимо от симптомов.Чтобы продемонстрировать воспаление и повышенную утечку белка из кишечника во время теста на элиминацию коровьего молока в образцах фекалий младенцев с различными симптомами, указывающими на аллергию на коровье молоко, мы измерили концентрации альфа-1-антитрипсина (АТ), эозинофильного катионного белка (ЭКП). ), иммуноглобулин (Ig) A и специфичные к коровьему молоку антитела IgA в образцах фекалий 208 младенцев со средним возрастом 7 месяцев. Образцы до заражения собирали после среднего 3-недельного периода элиминации, а образцы после заражения получали через 4 дня после начала заражения.Уровни общего IgA до заражения (p = 0,02) и AT после заражения (p = 0,001) в кале были выше у младенцев с положительным заражением. Из этих детей уровни ECP до и после провокации были выше у тех, кто реагировал через 24 часа, чем у тех, кто реагировал в течение 1 часа (p = 0,006 и p = 0,045). Уровни ЕСР до заражения были выше у лиц с кишечными симптомами (p = 0,008), а уровни общего IgA как до, так и после заражения были выше у лиц с IgE-опосредованной реакцией на коровье молоко (p = 0,008).04 и р = 0,008). Независимо от результата провокации, общий IgA увеличивался во время провокации (p < 0,001 как для положительных, так и для отрицательных младенцев) и был выше у тех, кто находился на грудном вскармливании до провокации, чем у тех, кого кормили только смесью (p < 0,01). Следовательно, у младенцев, реагирующих на провокацию коровьим молоком, более высокие уровни фекального IgA до провокации указывают на усиление антигенных стимулов в кишечнике, а более высокие уровни AT после провокации отражают повышенную потерю белка в результате воспаления кишечника.У младенцев с медленно развивающимися желудочно-кишечными симптомами повышенный уровень ЭКБ в кале может помочь отличить пациентов от тех, кто переносит коровье молоко. Индивидуальное серийное наблюдение за фекальными IgA и ECP можно использовать для оценки степени воспаления в кишечнике и подходящего времени для контрольного теста, но они не являются диагностическими инструментами для аллергии на коровье молоко.
Можно ли использовать уровни кальпротектина в кале для мониторинга аллергии на молочный белок у младенцев? | Аллергия, астма и клиническая иммунология
Høst A. Частота аллергии на коровье молоко в детстве. Энн Аллергия Астма Иммунол. 2002; 89 (6 Приложение 1): 33–7.
ПабМед Google Scholar
Гупта Р.С., Дайер А.А., Джайн Н., Гринхот М.Дж. Пищевая аллергия у детей: современная диагностика, лечение и стратегии ведения. Мэйо Клин Proc. 2013;88(5):512–26.
ПабМед Google Scholar
Osborne NJ, Koplin JJ, Martin PE, Gurrin LC, Lowe AJ, Matheson MC, Ponsonby AL, Wake M, Tang ML, Dharmage SC, Allen KJ.Распространенность подтвержденной провокацией IgE-опосредованной пищевой аллергии с использованием популяционной выборки и заранее определенных критериев провокации у младенцев. J Аллергия Клин Иммунол. 2011;127(3):668–76.
КАС пабмед Google Scholar
Гупта Р.С., Спрингстон Э.Е., Уорриер М.Р., Смит Б., Кумар Р., Понграчич Дж., Холл Дж.Л. Распространенность, тяжесть и распространение детской пищевой аллергии в США. Педиатрия. 2011;128(1):e9-17.
ПабМед Google Scholar
Чэнь Дж., Ляо И., Чжан Х.З., Чжао Х., Чен Дж., Ли. Распространенность пищевой аллергии у детей в возрасте до 2 лет в трех городах Китая. Чжунхуа Эр Кэ За Чжи. 2012;50(1):5–9.
ПабМед Google Scholar
Тан Р.А., Коррен Дж. Связь ринита и астмы, синусита, пищевой аллергии и экземы. Иммунол Аллергия Клин Норт Ам. 2011;31(3):481–91.
ПабМед Google Scholar
Соарес-Вайзер К., Таквоенги Ю., Панесар С.С., Мураро А., Верфель Т., Хоффманн-Зоммергрубер К., Робертс Г., Халкен С., Поулсен Л., ван Ри Р., Влиг-Бурстра Б.Дж., Шейх А. Диагноз пищевой аллергии: систематический обзор и метаанализ. Аллергия. 2014;69(1):76–86.
КАС пабмед Google Scholar
Zeng Y, Zhang J, Dong G, Liu P, Xiao F, Li W, Wang L, Wu Q. Оценка симптомов, связанных с коровьим молоком, при раннем выявлении аллергии на белок коровьего молока у китайских младенцев.БМС Педиатр. 2019;19(1):191.
ПабМед ПабМед Центральный Google Scholar
Zhu Q, Li F, Wang J, Shen L, Sheng X. Фекальный кальпротектин у здоровых детей в возрасте 1–4 лет. ПЛОС ОДИН. 2016;11(3):e0150725.
ПабМед ПабМед Центральный Google Scholar
Xiong LJ, Xie XL, Li Y, Deng XZ. Текущее состояние фекального кальпротектина как диагностического или мониторингового биомаркера аллергии к белкам коровьего молока у детей: предварительный обзор, World J Pediatrics: WJP.2020.
Трилло Белисон К., Ортега Паес Э., Медина Кларос А.Ф., Родригес Санчес И., Рейна Гонсалес А., Вера Медиалдеа Р., Рамон Сальгеро Х.М. Фекальный кальпротектин как помощь в диагностике не-IgE-опосредованной аллергии к белкам коровьего молока. Anales de Pediatria (Барселона, Испания: 2003 г.). 2016;84(6):318–23.
Google Scholar
Merras-Salmio L, Kolho KL, Pelkonen AS, Kuitunen M, Mäkelä MJ, Savilahti E. Маркеры воспаления слизистой оболочки кишечника и специфические иммуноглобулины коровьего молока при аллергии на коровье молоко без IgE.Клин Трансл Аллергия. 2014;4(1):8.
ПабМед ПабМед Центральный Google Scholar
Бешер О.Ф., Санджак С., Эркан Т., Кутлу Т., Кокуграш Х., Кокуграш Ф. Можно ли использовать уровень кальпротектина в кале в качестве маркера воспаления при диагностике и последующем наблюдении за аллергией на белок коровьего молока? Аллергия, астма Immunol Res. 2014;6(1):33–8.
Google Scholar
Хан С.Тестирование фекального кальпротектина при синдроме энтероколита, вызванного пищевыми белками. J Investig Allergol Clin Immunol. 2018;28(4):287–8.
КАС пабмед Google Scholar
Zhu Q, Li F, Wang J, Ma J, Sheng X. Активация кальпротектина при легкой IgE-опосредованной гиперчувствительности к овальбумину. Онкотаргет. 2017;8(23):37342–54.
ПабМед ПабМед Центральный Google Scholar
Li F, Ma J, Geng S, Wang J, Liu J, Zhang J, Sheng X. Концентрация кальпротектина в кале у здоровых детей в возрасте 1–18 месяцев. ПЛОС ОДИН. 2015;10(3):e0119574.
ПабМед ПабМед Центральный Google Scholar
Lee YW, Lee KM, Lee JM, Chung YY, Kim DB, Kim YJ, Chung WC, Paik CN. Полезность фекального кальпротектина в оценке активности воспалительного заболевания кишечника. Crit Rev Clin Lab Sci. 2019;34(1):72–80.
КАС Google Scholar
Сантос AF, Броу HA. Использование тестов in vitro для диагностики пищевой аллергии. J Allergy Clin Immunol Pract. 2017;5(2):237–48.
ПабМед ПабМед Центральный Google Scholar
Сато С., Янагида Н., Эбисава М. Как диагностировать пищевую аллергию. Курр Опин Аллергия Клин Иммунол. 2018;18(3):214–21.
КАС пабмед Google Scholar
Камер С., Дешмукх М., Патоле С.Пробиотики при аллергии на белок коровьего молока: систематический обзор рандомизированных контролируемых исследований. Eur J Педиатр. 2019;178(8):1139–49.
КАС пабмед Google Scholar
Payot F, Lachaux A, Lalanne F, Kalach N. Рандомизированное исследование молочной смеси на основе аминокислот у младенцев и детей с тяжелой аллергией на коровье молоко. J Pediatr Gastroenterol Nutr. 2018;66(1):135–40.
КАС пабмед Google Scholar
Longo G, Berti I, Burks AW, Krauss B, Barbi E. IgE-опосредованная пищевая аллергия у детей. Ланцет. 2013;382(9905):1656–64.
КАС пабмед Google Scholar
Томпсон-Чагоян О.К., Виейтес Дж.М., Мальдонадо Дж., Эдвардс С., Гил А. Изменения фекальной микробиоты младенцев с аллергией на белок коровьего молока – испанское проспективное исследование случай-контроль через 6 месяцев. Детская аллергия Иммунол. 2010; 21 (2 часть 2): e394-400.
Google Scholar
Martorell A, Plaza AM, Boné J, Nevot S, García Ara MC, Echeverria L, Alonso E, Garde J, Vila B, Alvaro M, Tauler E, Hernando V, Fernández M. Аллергия на белок коровьего молока. Многоцентровое исследование: клинические и эпидемиологические аспекты. Аллергол Иммунопатол. 2006;34(2):46–53.
Google Scholar
Matthai J, Sathiasekharan M, Poddar U, Sibal A, Srivastava A, Waikar Y, Malik R, Ray G, Geetha S, Yachha SK. Рекомендации по диагностике и лечению аллергии к белкам коровьего молока.Индийский педиатр. 2020;57(8):723–9.
ПабМед Google Scholar
Li F, Ma J, Geng S, Wang J, Ren F, Sheng X. Сравнение различных видов питания по уровню фекального кальпротектина. Ранний Хам Дев. 2014;90(9):471–5.
КАС пабмед Google Scholar
Liu JR, Sheng XY, Hu YQ, Yu XG, Westcott JE, Miller LV, Krebs NF, Hambidge KM. Уровни кальпротектина в кале у сельских китайских младенцев выше, чем у городских, и отрицательно связаны с ростом.БМС Педиатр. 2012;12:129.
ПабМед ПабМед Центральный Google Scholar
Мураро А., Верфель Т., Хоффманн-Зоммергрубер К., Робертс Г., Бейер К., Биндслев-Йенсен С., Кардона В., Дюбуа А., Дютуа Г., Эйгенманн П., Фернандес Ривас М., Халкен С., Хикштейн Л., Хёст А., Кнол Э., Лак Г., Маркизотто М.Дж., Ниггеманн Б., Нвару Б.И., Пападопулос Н.Г., Поульсен Л.К., Сантос А.Ф., Скипала И., Шёпфер А., Ван Ри Р., Вентер С., Червяк М., Влиг-Бурстра Б., Панесар С. , де Сильва Д., Соарес-Вайзер К., Шейх А., Балмер-Вебер Б.К., Нильссон С., де Йонг Н.В., Акдис К.А.Рекомендации EAACI по пищевой аллергии и анафилаксии: диагностика и лечение пищевой аллергии. Аллергия. 2014;69(8):1008–25.
КАС пабмед Google Scholar
Колецко С., Ниггеманн Б., Арато А., Диас Дж. А., Хойшкел Р., Хасби С., Мирин М. Л., Пападопулу А., Рюммеле Ф. М., Стайано А., Шэппи М. Г., Ванденплас Ю. Диагностический подход и лечение коровьего молока аллергия на белок у младенцев и детей: практические рекомендации комитета ESPGHAN GI.J Pediatr Gastroenterol Nutr. 2012;55(2):221–9.
КАС пабмед Google Scholar
Meyer R, Groetch M, Venter C. Когда младенцам с аллергией на белок коровьего молока следует использовать смесь с аминокислотами? Практическое руководство. J Allergy Clin Immunol Pract. 2018;6(2):383–99.
ПабМед Google Scholar
Fiocchi A, Brozek J, Schünemann H, Bahna SL, von Berg A, Beyer K, Bozzola M, Bradsher J, Compalati E, Ebisawa M, Guzman MA, Li H, Heine RG, Keith P, Lack Г., Ланди М., Мартелли А., Рансе Ф., Сэмпсон Х., Штейн А., Терраччано Л., Витс С.Рекомендации Всемирной аллергологической организации (WAO) по диагностике и обоснованию действий по борьбе с аллергией на коровье молоко (DRACMA). Детская аллергия Иммунол. 2010; 21 (Приложение 21): 1–125.
Google Scholar
Палмер Д.Дж., Голд М.С., Макридес М. Влияние потребления вареных и сырых яиц на содержание овальбумина в грудном молоке: рандомизированное двойное слепое перекрестное исследование. Клин Эксперт Аллергия. 2005;35(2):173–178.
КАС пабмед Google Scholar
Dipasquale V, Serra G, Corsello G, Romano C. Стандартные и специализированные детские смеси в Европе: производство, маркетинг и последствия для здоровья. Нутр Клин Практ. 2020;35(2):273–81.
ПабМед Google Scholar
Røseth AG, Fagerhol MK, Aadland E, Schjønsby H. Оценка нейтрофильного доминирующего белка кальпротектина в фекалиях. Методологическое исследование. Scand J Гастроэнтерол. 1992;27(9):793–8.
ПабМед Google Scholar
Риччиуто А., Гриффитс А.М. Клиническое значение фекального кальпротектина. Crit Rev Clin Lab Sci. 2019;56(5):307–20.
КАС пабмед Google Scholar
Khaki-Khatibi F, Qujeq D, Kashifard M, Moein S, Maniati M, Vaghari-Tabari M. Кальпротектин при воспалительных заболеваниях кишечника. Клин Чим Акта. 2020; 510: 556–65.
КАС пабмед ПабМед Центральный Google Scholar
Пэк Э.Ю., Йи Д.Ю., Кан Б., Чхве Б.Х. Фекальный кальпротектин как маркер поражения желудочно-кишечного тракта у детей с пурпурой Шенлейна-Геноха: ретроспективный анализ. БМС Педиатр. 2020;20(1):374.
КАС пабмед ПабМед Центральный Google Scholar
Seo SC, Ahn SH, Ri S, Yoon Y, Byeon JH, Kim SH, Yoon W, Yoo Y. Повышенные уровни фекального кальпротектина связаны с тяжестью атопического дерматита у детей.Азиатская Пак J Аллергия Иммунол. 2018;36(2):82–7.
КАС пабмед Google Scholar
Матиас К.Б., Хобсон С.А., Гарсия-Льорет М., Лоусон Г., Поддиг Д., Фрейшмидт Э.Дж., Син В., Гуриш М.Ф., Чатила Т.А., Оттген Х.К. IgE-опосредованная системная анафилаксия и нарушение толерантности к пищевым антигенам у мышей с усиленной передачей сигналов рецептора IL-4. J Аллергия Клин Иммунол. 2011;127(3):795–805.
КАС пабмед Google Scholar
Kordowski A, Reinicke AT, Wu D, Orinska Z, Hagemann P, Huber-Lang M, Lee JB, Wang YH, Hogan SP, Köhl J. Мыши с рецептором C5a 1 (-/-) защищены от развития IgE- опосредованная экспериментальная пищевая аллергия. Аллергия. 2019;74(4):767–79.
КАС пабмед Google Scholar
Morita H, Nomura I, Matsuda A, Saito H, Matsumoto K. Желудочно-кишечная пищевая аллергия у младенцев. Аллергол Интерн. 2013;62(3):297–307.
КАС пабмед Google Scholar
Baldassarre ME, Laforgia N, Fanelli M, Laneve A, Grosso R, Lifschitz C. Лактобациллы GG улучшают выздоровление детей грудного возраста с кровью в стуле и подозрением на аллергический колит по сравнению с применением только сильно гидролизованной смеси. J Педиатр. 2010;156(3):397–401.
КАС пабмед Google Scholar
Dogan E, Sevinc E. Статус витамина D и уровни эозинофильного катионного белка в сыворотке у младенцев с аллергией на белок коровьего молока.Am J Transl Res. 2020;12(12):8208–15.
КАС пабмед ПабМед Центральный Google Scholar
Li J, Mei X, Cai X, Zhuo Y, Zhang L, Guo H, Yang H, Yang G. Ассоциация эозинофилии крови и недостаточности витамина D у детей раннего возраста с аллергией на коровье молоко. Asia Pac J Clin Nutr. 2019;28(3):550–7.
КАС пабмед Google Scholar
Кан И, Ан XH, О YK, Ли С.Х., Юнг Х.М., Че С.К., Ли Д.Х.Выявление полиморфизмов гена РНКазы 3 и ассоциации с аллергическим ринитом. Eur Arch Оториноларингол. 2010;267(3):391–5.
ПабМед Google Scholar
Райт Б.Л., Фернандес-Бекер Н.К., Камбэм Н., Пурингтон Н., Цао С., Тупа Д., Чжан В., Синдер С.Б., Ранк М.А., Кита Х., Кацка Д.А., Шим К.П., Баннинг Б.Дж., Дойл А.Д., Якобсен Э.А., Цай М., Бойд С.Д., Манохар М., Чинтраджа Р.С. Реакции желудочно-кишечных эозинофилов в продольном рандомизированном исследовании пероральной иммунотерапии арахисом.Клин Гастроэнтерол Гепатол. 2020;19(6):1151–9.
ПабМед Google Scholar
Vanderhoof J, Moore N, de Boissieu D. Оценка смеси на основе аминокислот у младенцев, не реагирующих на смесь с сильно гидролизованным белком. J Pediatr Gastroenterol Nutr. 2016;63(5):531–3.
КАС пабмед ПабМед Центральный Google Scholar
Д’Аурия Э., Сальваторе С., Поцци Э., Мантегацца С., Сарторио МУА, Пенсабене Л., Бальдассарре М.Е., Агости М., Ванденплас Ю., Зуккотти Г.Аллергия на коровье молоко: иммуномодуляция диетическим вмешательством. Питательные вещества. 2019;11(6):1399.
Центральный пабмед Google Scholar
фон Берг А., Филипиак-Питтрофф Б., Кремер Ю., Хоффманн Б., Линк Э., Бекманн С., Хоффманн Ю., Райнхардт Д., Грюбл А., Генрих Дж., Вихманн Х.Е., Бауэр К.П., Колецко С., Бердель Д. , Аллергии у школьников с высоким риском после раннего вмешательства с гидролизатами белков коровьего молока: 10-летние результаты немецкого исследования по вмешательству в питание младенцев (GINI).J Аллергия Клин Иммунол. 2013;131(6):1565–73.
Google Scholar
Roca M, Donat E, Rodriguez Varela A, Carvajal E, Cano F, Armisen A, Ekoff H, Cañada-Martínez AJ, Rydell N, Ribes-Koninckx C. Фекальный кальпротектин и нейротоксин эозинофильного происхождения у детей с не-IgE-опосредованной аллергией на белок коровьего молока. Дж. Клин Мед. 2021;10(8):1595.
КАС пабмед ПабМед Центральный Google Scholar
Olafsdottir E, Aksnes L, Fluge G, Berstad A. Уровни фекального кальпротектина у младенцев с младенческой коликой, здоровых младенцев, детей с воспалительным заболеванием кишечника, детей с рецидивирующей болью в животе и здоровых детей. Акта Педиатр. 2002;91(1):45–50.
КАС пабмед Google Scholar
Сикора Дж., Сиала К., Хумл М., Варваржовска Дж., Шварц Дж., Помахачова Р. Оценка фекального кальпротектина как ценного неинвазивного маркера в различении кишечных патогенов у маленьких детей с острым гастроэнтеритом.Акта Педиатр. 2010;99(9):1389–95.
ПабМед Google Scholar
Границы | Анализ фекальных белков человека-хозяина: реакция на 10-недельное диетическое вмешательство, изменяющее потребление белка с пищей у пожилых мужчин
Введение
Желудочно-кишечный тракт (ЖКТ) координирует сложные задачи пищеварения и всасывания питательных веществ (1, 2). Помимо этих функций, становится все более очевидным, что ЖКТ симбиотически взаимодействует с резидентной популяцией микробиома (3).Учитывая присущую сложность как переваривания питательных веществ, так и поддержания симбиотического микробиома кишечника, ЖКТ требует скоординированного функционирования большой сети иммунных, секреторных и нервных клеток и систем, которые демонстрируют специализацию и скоординированную функциональность на всем протяжении (4). Вся эта система ЖКТ обеспечивает координацию, необходимую для переваривания и/или устранения ошеломляющего разнообразия проглоченных соединений, включая потенциально патогенные микроорганизмы. У большинства людей это происходит при отсутствии дискомфорта или болезни, однако оценки показывают, что до 35% людей старше 65 лет страдают хроническими желудочно-кишечными заболеваниями в США и 25% женщин в исследовании Zurich Cohort (5). ).Сюда входит широкий спектр функциональных желудочно-кишечных расстройств (ФЖР), в том числе функциональная диспепсия (ФД) и синдром раздраженного кишечника (СРК), которые характеризуются на основе различных комбинаций хронических или острых желудочно-кишечных симптомов. Функциональные желудочно-кишечные расстройства определяются отсутствием объяснимых структурных или биохимических нарушений ЖКТ, которые объясняют эту симптоматику. Следовательно, существует постоянная потребность в понимании функции ЖКТ у здоровых людей и механизмов, которые могут лежать в основе развития FGID.
На сегодняшний день для анализа биологического функционирования желудочно-кишечного тракта человека применялись высокопроизводительные методы всестороннего анализа генов и белков микробиоты. Эти методы использовались для всестороннего описания таксономии и функциональных признаков популяции микробиома (6, 7). Меньшее количество исследований было посвящено присущей экспрессии и обилию генетического материала или белков собственного происхождения. Это важно, поскольку вызванное хозяином воспаление и повышенный иммунный ответ являются отличительной чертой заболеваний желудочно-кишечного тракта и дисбактериоза кишечника.Это видно при анализе биомаркеров, включая кальпротектин и лактоферрин (8) в фекалиях. Экспериментальные исследования определили расширяющийся список возможных белков-кандидатов для ассоциации с заболеванием, включая кальпротектин, пируваткиназу, миелопероксидазу и членов семейства белков матриксных металлопротеиназ (8–10). Тем не менее, в то время как эти маркеры имеют потенциал в качестве биомаркеров заболевания (8), эти дискретные белки дают мало информации о сложности нарушений в ЖКТ, обеспечивая очень ограниченное понимание измененного функционирования сложных клеточных систем, лежащих в основе этиологии и патобиологии заболевания.
Современные протеомные методы позволяют измерять тысячи белков. Тем не менее, остаются серьезные проблемы для протеомного применения в образцах фекалий человека. Фекальный протеом по своей природе сложен, поскольку он содержит различные группы белков, которые, соответственно, происходят либо от хозяина, либо от микробиома, либо от остатков протеома из проглоченной пищи (9, 11, 12). Кроме того, зависимый от данных анализ пептидов в масс-спектрометрии часто ограничивается наиболее распространенными пептидами.Затем используется динамическое исключение для предотвращения повторного анализа одного и того же пептида за пределами хроматографического пика (13, 14). Более полный протеом можно получить, используя фракционирование перед ЖХ, что снижает сложность каждого разделения ЖХ и позволяет фрагментировать больше пептидов и, таким образом, идентифицировать их по сравнению с анализом всего образца за один цикл (15). Эти фракции могут быть объединены перед поиском для одновременной идентификации всех соединений. Эта стратегия применяется во многих протеомных анализах (напр.g., протеомика дробовика, которая разделяла пептиды по их ионной силе, а затем по их гидрофобности перед анализом МС/МС) (16). Для фекальной протеомики использовались различные процедуры экстракции, подготовки и фракционирования, которые более полезны для разных частей протеома. В текущем исследовании экстракция SDS использовалась для улучшения экстрагируемости белка из образцов (17).
Особый интерес в регуляции протеома хозяина ЖКТ представляет влияние пищевого белка.Диеты с высоким содержанием белка вызывают значительный интерес, учитывая предполагаемые преимущества для регуляции аппетита, здоровья сердечно-сосудистой системы, гомеостаза глюкозы, состояния тела и потери веса (18). Исследования пожилых людей предполагают потенциальную потребность в большем ежедневном потреблении белка или аминокислот для поддержания массы и функции скелетных мышц (19, 20). Тем не менее, переваривание белка, вероятно, оказывает значительное влияние на ЖКТ. Экспериментальные исследования на грызунах показывают, что изменение белковой диеты влияет на функцию тонкой кишки и бокаловидных клеток с изменением экспрессии белка и секреции слизи (21–24).Точно так же клинический анализ влияния изокалорийной замены мальтодекстрина белком (казеином или соевым белком) выявляет заметные изменения в транскриптоме гена слизистой, полученном из ректальных биопсий (25). В текущем исследовании использовалась нецелевая протеомика открытий, которая позволяет идентифицировать все белки человека вместо подмножества белков животных, как это делалось в предыдущих исследованиях. Этот процесс был использован для идентификации классов протеома фекального хозяина в когорте пожилых самцов, которых кормили либо диетой RDA (0.8 г/кг/день), что включало рекомендуемую диетическую норму в течение 10 недель или 2RDA, содержащую двойную рекомендуемую диетическую норму (1,6 г/кг/день), как описано ранее (26). Мы поняли, что фекальный протеом хозяина будет включать белки, секретируемые в желудочно-кишечный тракт, в том числе ферменты, белки слизи, секреторные, иммунные белки и измельченные клетки (4). Мы также предположили, что диета может влиять на наличие человеческих (собственных) белков после 10-недельной диеты. Хотя наблюдались фрагменты белков пищи и микробиоты, их обсуждение является частью другой работы.
Экспериментальный
Сбор диеты и образцов
Девятнадцать здоровых пожилых мужчин в возрасте 70 лет и старше с ИМТ (кг/м 2 ) в возрасте от 18 до 35 были набраны из местного сообщества для участия в исследовании. Группа RDA имела средний возраст 75,2 ± 4,5 sd. лет и средний ИМТ 27,3 ± 4,7 sd. кг/м 2 . Группа 2RDA имела средний возраст 73,8 ± 3,5 sd. лет и средний ИМТ 28,3 ± 3,3 sd. кг/м 2 . Все были некурящими и не принимали пищевые добавки по крайней мере за 1 месяц до участия в этом испытании.Потенциальные участники были исключены, если они придерживались ограниченной диеты, в том числе вегетарианцы или лица с пищевой аллергией или непереносимостью (например, орехи, рыба, молочные продукты). Дальнейшее исключение применялось к тем, у кого в анамнезе были пищеварительные или сердечно-метаболические заболевания.
Экспериментальный дизайн
Дизайн этого испытания был описан ранее (26). Участники были рандомизированы в две группы, где 9 участников получали контролируемую диету 0.8 г белка/кг/день (RDA) и 10 участников получали контролируемую диету 1,6 г белка/кг/день (2RDA) в течение 10 недель. Было выбрано количество белка, равное удвоенной рекомендуемой диетической норме, потому что данные показали, что белок на этом уровне всасывается задолго до того, как толстая кишка (26). Вся пища, потребляемая участниками, была предоставлена исследователями. Процент энергии, полученной из жира, составил 28–31%, из белков – 11,7% для RDA и 20,6% для 2RDA. Остальную энергию составляли углеводы.Все диеты соответствовали рекомендациям по питанию и активности для Новой Зеландии и соответствовали рекомендациям по потреблению фруктов и овощей (27). Все участники заполнили диетические записи, чтобы убедиться, что вся предоставленная пища была съедена, а выбор продуктов питания был скорректирован в соответствии с предпочтениями участников для поддержания высокого соответствия. Любая потребляемая неисследуемая пища также регистрировалась. Энергетическая ценность интервенционной диеты рассчитывалась индивидуально в соответствии с расчетными энергетическими потребностями участников на основе уравнения Харриса-Бенедикта и корректировалась с учетом физической активности, которая оценивалась с помощью носимых на запястье акселерометров (Fitbit Charge HR).Предполагаемые энергетические потребности были рассчитаны до вмешательства и корректировались каждые две недели на основе сытости участников и поддержания веса, чтобы гарантировать, что участники потребляли достаточное количество белка по сравнению с потреблением энергии. Во время вмешательства участников проинструктировали вести обычный образ жизни, а приготовленную еду доставили на дом. Все испытания проводились в клинике питания и подвижности Оклендского университета.
Сбор и хранение проб
пробы фекалий были собраны в течение 10-й недели исследования после вмешательства.Вкратце, участникам был предоставлен набор для сбора образцов и инструкции по сбору образцов дома. После сбора пробы доставлялись в Институт Лиггинса (Окленд, Новая Зеландия) на льду в течение 3 ч и немедленно хранились при температуре -80°C. Для протеомного анализа из замороженного образца отбирали аликвоты по 1–2 г и помещали на лед для протеомного анализа. Фекалии разделяли на твердые частицы и надосадочную жидкость на основании ранее опубликованных протоколов (17, 28). Гидрохлорид гуанидина добавляли для денатурации белков и ограничения активности бактериальных белков.
Подготовка к протеомике
Схема, показывающая подготовку и анализ образцов для протеомики, показана на рисунке 1. Осадок и супернатант (см. раздел «Сбор и хранение образцов») объединяли в соотношении 1:1. Метанол-хлороформ использовали для экстракции белков и удаления гидрохлорида гуанидина, как описано ранее (29). Осажденный белок ресуспендировали в двух экстракционных буферах: буфере для лизиса и уреатрис-буфере. Что касается буфера для лизиса, осадок ресуспендировали в буфере, содержащем (4% мас./об. дезоксихолата натрия, 50 мМ трис(гидроксиметил)аминометан, рН 8.0 с использованием соляной кислоты). Этот гомогенат нагревали до 95°C в течение 10 мин с последующей гомогенизацией в пробирке из матового стекла в течение 1 мин с помощью ручной электрической дрели (Firebreak 50 Гц P/N 0–2809 об/мин). Для мочевинного буфера осажденные пептиды ресуспендировали в уреатрисовом буфере [8 М мочевина, 100 мМ NaCl и 25 мМ трис(гидроксиметил)аминометан]. Смесь пипетировали вверх и вниз, а затем встряхивали при комнатной температуре в течение ночи. Все экстракты обоих методов затем центрифугировали при 14 100 × 90 129 g 90 130 в течение 10 мин с последующим сбором прозрачных супернатантов.Экстракцию метанолом-хлороформом проводили на образцах, экстрагированных уреатриевым буфером, для удаления мочевины и выделения белков, как описано в Gathercole et al. (30).
Рисунок 1 . Схема, показывающая подготовку образцов фекалий для протеомики, фракционирования, анализа на ЖХ-МС/МС и анализа данных.
Для каждого образца надосадочные жидкости обоих экстрактов объединяли, а затем сушили с помощью скоростного вакуумного концентратора. Белки ресуспендировали в 50 мМ бикарбонате аммония, рН 8.Белки восстанавливали добавлением 1 ммоль трис(2-карбоксиэтил)фосфина при нагревании при 56°С в течение 45 мин с последующим алкилированием 3 ммоль йодацетамида, инкубировали при комнатной температуре в темноте. Белки расщепляли в течение ночи при 37°C после добавления трипсина (~1 мкг трипсина на 133 мкг белка) и конечной концентрации 10% об./об. ацетонитрила. Для прекращения расщепления и осаждения дезоксихолата натрия добавляли муравьиную кислоту до концентрации 1% по объему. После центрифугирования прозрачный супернатант разделяли на две части, сушили и очищали с использованием дисков Empore C18 как в кислой, так и в щелочной среде.Для кислых условий пептиды ресуспендировали в 0,1% об./об. муравьиной кислоте (рН 4,5). Для основных (рН 10) условий пептиды ресуспендировали в 10 мМ формиата аммония (рН 10). Три кондиционированных диска Empore инкубировали в этих растворах в течение 3 часов. Диски Empore элюировали встряхиванием с 75% об./об. ацетонитрилом в течение 1 часа. После удаления дисков растворы пептидов высушивали в скоростном вакуумном концентраторе. Высушенные пептиды ресуспендировали в 100 мкл 0,1% об./об. муравьиной кислоты. Два элюата C18 объединяли 1:1 для каждого образца перед анализом ЖХ-МС/МС.
Анализ ЖХ-МС-МС
Объединенные элюции C18 для каждого образца были проведены в случайном порядке с использованием двух различных методов разделения, а файлы mgf (спектров) были объединены перед поиском белков. Образцы вводили (5 мкл) в колонку ProntoSIL C18AQ Nano trap (5 мкм, 200Å) со скоростью потока 5 мкл/мин. Затем колонку-ловушку подключили к аналитической колонке ProntoSIL C18AQ (внутренний диаметр 100 мкм × 150 мм, 3 мкм, 200 Å) на NanoAdvance LC (Bruker Daltonics) в режиме нанопотока.После разделения аналиты вводили в CaptiveSpray, а затем в масс-спектрометр с ионной ловушкой (Amazon, Bruker Daltonics). Был присоединен Nanobooster (Bruker Daltonics) для введения ацетонитрила в распылитель для улучшения чувствительности. Первый метод разделения проводился при 50°C и включал, начиная с 98 % растворителя А (0,1 % муравьиной кислоты в воде), повышая до 5 % В (0,1 % муравьиной кислоты в ацетонитриле) через 5 мин с последующим увеличением до 25 % В при 65 мин, затем 35% В через 75 мин. Затем колонку очищали, увеличивая до 95% B в течение 80 минут, выдерживая в течение 5 минут и затем повторно уравновешивая при 2% B до конца 90-минутного цикла.Скорость потока была установлена на 800 нл/мин. Второй метод разделения выполняли при температуре колонки 60°C и включали, начиная с 98% растворителя А (0,1% муравьиной кислоты в воде) и 2% растворителя В (0,1% муравьиной кислоты в ацетонитриле), увеличивая до 45% В при 60 мин. Затем колонку очищали, увеличивая до 95% В на 62 мин, выдерживая в течение 3 мин и затем повторно уравновешивая при 2% В до конца 70-минутного цикла. Скорость потока была установлена на 400 нл/мин. Для обоих методов разделения был запущен режим МС с положительным режимом CID для поиска соединений между 350 и 1200 m/z.МС/МС проводили на 10 прекурсорах одновременно. Соединения, проанализированные с помощью МС/МС, исключали после 1 спектра в течение 0,20 мин, если только интенсивность не увеличивалась по крайней мере в 5 раз.
Данные протеомики масс-спектрометрии были депонированы в Консорциум ProteomeXchange через партнерский репозиторий PRIDE (31) с идентификатором набора данных PXD021424.
Идентификация белка
Данные МС были экспортированы в ProteinScape (версия 3.1.0 348; Bruker Daltonics). Файл для обоих методов разделения был объединен в один для каждого образца.Поиск белков проводили с помощью Mascot Server v 2.5.1 (Matrix Science, Великобритания). Поиск спектров проводился в базе данных Swissprot Homo sapiens . Семитрипсин был выбран из-за специфичности фермента, допускающей до двух пропущенных расщеплений. Допустимая погрешность МС была установлена на 0,3 Да, а погрешность МС/МС была установлена на 0,8 Да. Пороговые баллы талисмана пептидов и белков были установлены на 20 и 80 соответственно. Специфика прибора была установлена на ESI-TRAP. Включенные модификации включали карбамидометил (C) в качестве фиксированного и окисление (M), потерю аммиака (N-термин-C), натрий (DE) и дезамидирование (NQ) в качестве переменных модификаций.Для идентификации белков требуется по крайней мере одна уникальная идентификация пептида из списка идентифицированных пептидов для этого белка.
Идентификация белковой группы
Для определения классов и функций белков идентификаторы белков были преобразованы из образцов UNIPROT в названия генов с использованием API преобразования идентификаторов UNIPROT, доступного по адресу (https://www.uniprot.org/help/api_idmapping). Полученные в результате идентификации UNIPROT затем использовались для запроса в базе данных Комитета по номенклатуре генов человека (HUGO) дополнительных аннотаций, включая аннотации гена PANTHER (http://www.pantherdb.org версии 14.0). Термины PANTHER были связаны с родственными образцами с использованием R-пакета PANTHER.db.
Результаты и обсуждение
Протеом человека или хозяина, выделенный из образцов фекалий, может быть полезной стратегией для профилирования адаптивной регуляции сложных физиологических процессов, связанных с перевариванием питательных веществ и гомеостазом микробиома кишечника. Мы предположили, что фекальный протеом хозяина будет включать белки, секретируемые в желудочно-кишечный тракт, в том числе ферменты, белки слизи, секреторные иммунные белки и, возможно, белки из эпителиальных клеток, смещенных вдоль ЖКТ (4).Мы также предположили, что значительно отличающиеся диеты могут изменить фекальный аутопротеом. В текущем исследовании анализ ЖХ-МС был проведен на образцах стула, выделенных после того, как здоровые пожилые мужчины-добровольцы потребляли одну из двух диет, различающихся по общему содержанию белка (26). Диета RDA соответствовала минимальным рекомендациям ВОЗ по пищевым белкам, а диета 2RDA обеспечивала удвоение этого количества белка с компенсирующими изменениями в потреблении углеводов для поддержания энергетического баланса.
Хотя в этой рукописи мы рассмотрели собственный протеом, образцы также включали белки из микробиома и фрагменты пищевых белков.Поскольку масс-спектрометрия не может выбрать только человеческие пептиды в цикле ЖХ-МС/МС, перед разделением ЖХ было проведено фракционирование образцов для увеличения количества пептидов и, следовательно, идентификации белков. Фракционирование позволяет фрагментировать больше пептидов при использовании зависимого от данных анализа с помощью МС. Чтобы ограничить идентификацию пептидов людьми, спектры сравнивали с пептидами человека в базе данных Swissprot, и для идентификации каждого белка требовался уникальный пептид. Хотя белки из пищи и микробиоты будут присутствовать, поиски были ограничены базой данных протеома человека в соответствии с целью этой работы.Список белков, идентифицированных для каждого образца, можно найти в дополнительных материалах.
При изучении различий между двумя диетами белки, идентифицированные в каждой группе, были исследованы на наличие различий с использованием диаграммы Венна (см. Рисунок 2). На первой диаграмме Венна (рис. 2А) показан полный список белков, идентифицированных в 19 образцах. Уникальные белки были обнаружены в рационах RDA и 2RDA, но 30,5% белков (664) были обнаружены в обоих рационах. В образцах рациона 2RDA было идентифицировано большее количество белков человека-хозяина.В среднем 233 ± 11 с.д. белков и 575 ± 28 с.д. пептиды были идентифицированы в образцах белковой диеты RDA, а 266 ± 14 белков и 637 ± 38 пептидов были идентифицированы в каждом из образцов диеты 2RDA. Не было существенной разницы в количестве идентификаций между двумя диетами ( p = 0,07 для белков и p = 0,21 для пептидов). Однако между отдельными людьми наблюдались большие различия. В целом фрагменты из 2181 различных белков-хозяев были идентифицированы в 19 образцах, и 76% этих белков были идентифицированы только в двух или менее образцах.Таким образом, было очень ограниченное перекрытие между людьми для большинства идентифицированных белков. Белком, идентифицированным наиболее последовательно во всех образцах, был член семейства химотрипсиноподобной эластазы 3A (Uniprot ID CEL3A). CEL3A присутствовал во всех образцах диеты 2RDA и отсутствовал только в 1 образце из группы белка RDA. CEL3A, также известная как эластаза 3A, представляет собой сериновую протеазу, которая секретируется поджелудочной железой (32).
Рисунок 2 . Отображение количества всех идентифицированных белков, уникальных для каждой диеты или общих для каждой диеты (A) ; и белки, присутствующие по меньшей мере в 60% одной диетической группы ( n = 6 для обеих диетических групп), наблюдаемые либо в одной, либо в обеих диетических группах (B) .
Чтобы проследить различия в белках, которые более характерны для каждой диеты, на второй диаграмме Венна (рис. 2B) были показаны белки, обнаруженные по крайней мере в 60% образцов с одной и той же диетой (белки перечислены в таблице 1). В диете RDA 14 белков были уникальными белками, обнаруженными в ≥ 60% образцов, и 44 белка были обнаружены только в диете 2RDA. Только 7 белков были обнаружены в 60% образцов для обоих рационов). Ни один из белков не наблюдался во всех 19 образцах.Чтобы увидеть, являются ли какие-либо из этих общих белков уникальными для какой-либо диеты, мы проверили белки по полному списку для другой диеты. Все 51 белок в диете 2RDA были обнаружены по крайней мере в одном образце диеты RDA.
Таблица 1 . Частота белков-хозяев обнаружена не менее чем у 60% ( n = 6) по крайней мере одной из диетических групп и соответствует диаграмме Венна на рис. 2Б.
Было идентифицировано разнообразное количество собственных белков, имеющих отношение к широкому спектру функций.Многие из белков имели более одного функционального класса белков. В обоих рационах ~ 40% всех идентифицированных классов белков были частью белкового класса, состоящего из <1% от общего белка. Приблизительно 20% белков не имели идентификации класса по Panther (см. рис. 3). В обоих рационах все четыре основных класса имели <10% от общего количества белков, и в порядке убывания были связаны связывание нуклеиновых кислот, модуляторы ферментов, белки цитоскелета и факторы транскрипции, которые предполагают наличие сброшенных клеток и/или признаки пролиферации (нуклеиновые кислоты). связывание, белки цитоскелета и факторы транскрипции) в фекалиях.В целом наблюдались ограниченные различия в классах белка между каждой диетой.
Рисунок 3 . Распределение белковых классов составляет >2% прочтений. NA относится к неназначенным белкам. (A) включает 9 участников диеты RDA, а (B) относится к результатам 10 участников диеты 2RDA.
Идентифицированные собственные белки включали те, которые, как ожидается, будут присутствовать в фекалиях, в том числе; ферменты (т.g., химотрипсин), цинковые пальцы, коллаген, белки миозина и белки муцина. В этом исследовании были идентифицированы четыре муцина: MUC4, связанный с мембранами, в одном образце для группы диеты RDA; MUC16 (также известный как CA125) был обнаружен в образцах диеты RDA; MUC5A, секретируемый муцин, обнаружен в одном образце из группы диеты 2RDA, и MUC19, секретируемый белок, который был обнаружен в трех образцах RDA и четырех образцах 2RDA (33, 34). MUC19 помогает поддерживать проницаемость эпителиального слоя кишечника и регулировать иммунные реакции.Присутствие этого белка может указывать на наличие воспаления или другого кишечного заболевания, поскольку ранее не сообщалось об этом белке в здоровом кишечнике человека (35). Все участники этого исследования были здоровы, но дальнейшая работа может быть использована для определения того, является ли это маркером бессимптомного воспаления.
Один белок, K167 (антиген KI-67), был уникальным для образцов из диеты RDA. K167 используется как признак пролиферации в научных исследованиях, в том числе для прогнозирования рака.Было обнаружено, что он действует как поверхностно-активное вещество, помогающее разделять митотические хромосомы после высвобождения в цитоплазму (36), что позволяет предположить, что это могло быть признаком клеточной пролиферации, происходящей в рационе RDA. На веб-сайте Protein Atlas представлены данные о том, что этот белок экспрессируется в желудочно-кишечном тракте, включая железистые клетки толстой кишки, у ряда лиц разного возраста и пола (37, 38).
Классы белков были определены с помощью Panther (39) для всех идентифицированных белков из каждой диеты.Из белков, обнаруженных по крайней мере в 60% одного из рационов (перечисленных на рисунке 2C), 39 белков были классифицированы в соответствии с их функциями у Panther. Наиболее распространенной идентифицированной функцией были белки цитоскелета. Девять из 10 белков наблюдались по крайней мере в 60% образцов из группы диеты 2RDA [включая белок 5, ассоциированный с цитоскелетом (CKAP5) и талин 1 (TLN1)]. Пять функциональных групп были связаны с ДНК и включали белки, связывающие CREB (CBP), лизинметилтрансферазу 2A (KMT2A) и метилтрансферазу 2C (KMT2C).И белки цитоскелета, и белки, связанные с ДНК, участвуют в пролиферации клеток (40, 41) и позволяют предположить, что увеличение потребления белка увеличивает пролиферацию клеток. Этот вероятный эффект подтверждается аналогичными результатами в толстой кишке крыс (42), но не подтверждается наличием K167, признаком пролиферации, обнаруженным только в группе RDA. Отсутствие K167 предполагает, что эти белки могут быть вовлечены в пролиферацию, не идентифицируемую антигеном K167, или увеличение цитоскелетных и связанных с ДНК белков не влияло на пролиферацию клеток в этом исследовании.Работа, проведенная с группой мужчин, которая включала когорту в этом исследовании, показала, что некоторые микроРНК были изменены в диете 2RDA и что диета 2RDA также увеличивала посттранскрипционную регуляцию иммунной системы (43). Кишечник содержит много белков-транспортеров, и в этом списке белков также наблюдались белки с такими функциями, например, рианодиновый рецептор 1 (RYR1) и рианодиновый рецептор 3 (RYR3).
Чтобы дать общее представление о количестве образцов, в которых каждый из белков был обнаружен в двух диетах, 26 лучших белков, наблюдаемых в диете 2RDA (в соответствии с частотой наблюдений), перечислены в таблице 1.Двадцать из этих белков обнаружены в области кишечника согласно Protein Atlas (38). Эти белки имели функции, связанные с пищеварительными ферментами, молекулярными моторами, передачей сигналов и цитоскелетом, включая размещение органелл. Поиски литературы привели к 4 белкам, которые были недавно обнаружены фекальными/кишечными белками. Это были цепи коллагена альфа-1 (VII) (Uniprot ID CO7A1), протокадгерин Fat 3 (Uniprot ID FAT3), белок цинковых пальцев 469 (Uniprot ID ZN496) и тяжелая цепь 8 динеина, аксонемальная (Uniprot ID DYH8).Присутствие этих белков также подтверждает нашу гипотезу о том, что белки, отслаивающиеся от клеток, обнаруженных вдоль кишечной стенки, присутствуют в фекалиях. Ранее это наблюдалось при скрининге колоректального рака, хотя у здоровых людей оно встречалось реже (44).
CO7A1 представляет собой фибриллу, соединяющую наружный эпителий с нижележащей стромой (45). Было показано, что этот белок активируется после добавления TNF-α в культивируемые фибробласты (46), что позволяет предположить, что фибробласты могут продуцировать CO7A1.Слой клеток фибробластов находится под эпителием в кишечнике (47). CO7A1 наблюдался в большинстве проб, в 6 пробах RDA и 9 пробах 2RDA, 90 и 67% соответственно. Это говорит о том, что пептиды этого белка обычно обнаруживаются в фекалиях. Это может быть связано с тем, что белок наблюдается близко к внешнему слою кишечника и может разрушаться во время нормального износа, как мы предполагали.
FAT3 у человека является одним из четырех белков FAT, входящих в семейство белков кадгеринов (48, 49).FAT3 участвует во взаимодействиях с актиновым цитоскелетом. Имеются доказательства того, что FAT3 активирует β-катенин и белки ниже сигнального пути Wnt (50). Это интересно, поскольку два других распространенных белка BCL9 и MACF1, которые были обнаружены 8 раз у участников 2RDA, также являются частью сигнального пути Wnt и ранее наблюдались в кишечной системе (38). Белки пути Wnt участвуют в развитии плода и в гомеостазе у взрослых.Этот процесс устраняет путь деградации, приводящий к увеличению β-катенина как в цитоплазме, так и в ядре клеток и увеличению транскрипции и, таким образом, экспрессии белка, росту клеток и потенциальному участию в межклеточной адгезии. В некоторых ситуациях эта функция может привести к росту опухоли (51) и, возможно, может быть одной из причин того, что мутация в FAT3 приводит к опухолям поджелудочной железы (50). Поскольку FAT3 является частью сигнального пути Wnt, а другие участники этого пути наблюдались в образцах, возможно, этот путь был активен в кишечной системе, что привело к обнаружению фрагментов этих белков в образцах фекалий.
Мало что известно о функции ZN469, за исключением того, что он является фактором транскрипции, как и другие белки с цинковыми пальцами (34). Некоторые исследования показали, что пептид из ZN486 присутствует более чем в два раза больше в ткани серозного рака яичников по сравнению со здоровой тканью эпителия яичника (52). Было высказано предположение, что полиморфизмы ZN486 могут вызывать кератоконус и ухудшать зрение, но исследования в Польше и Саудовской Аравии показали, что это не так (53, 54). Необходимо провести дальнейшие исследования, чтобы теоретизировать и определить точную функцию ZN486 и почему он может присутствовать в фекалиях.
DYH8 представляет собой аксонемный динеин тяжелой цепи. Эти белки тяжелой цепи образуют основную часть молекулярных моторов динеина наряду с белками динеина малой цепи (55, 56). Комплексы Dynein транспортируют биомолекулы по микротрубочкам внутри клеток (56). В исследованиях окрашивания DYH8 показал сильное присутствие в семенниках (38). DYH8 был обнаружен у 70% участников 2RDA, но только у 22% участников RDA. Мы подозреваем, что из-за роли этого белка в транспортировке внутри клеток он мог попасть в кишечную систему через разрушение клеток.
Еще два белка, которые не обнаружены в фекальных/кишечных белках, но обнаружены в мышцах, это рианодиновый рецептор 1 (Uniprot ID RYR1) и рианодиновый рецептор 3 (Uniprot ID RYR3). Рецепторы рианодина входят в состав кальциевых каналов и вызывают сокращение мышц. Есть три из этих рецепторов, каждый из которых доминирует в разных типах мышц. RYR1 доминирует в скелетных мышцах, тогда как RYR3 доминирует в гладких мышцах кишечника. Анализы на антитела показали присутствие RYR3 в кишечнике (38, 57–59).
Перед анализом белки расщепляли трипсином. Сайты расщепления пептидов исследовали на предмет наличия нетриптических расщеплений, свидетельствующих о разрыве белков in situ . Пептид считался трипсином, если он был началом или концом белка или разрывом после лизина или аргинина. В среднем 0,4% пептидов в каждом образце не содержали триптических расщеплений; 8,3% имели триптические расщепления на обоих концах; и 91% имели расщепление трипсином на одном конце пептида.В целом средние сайты расщепления лизина и аргинина составляли 31 и 27% соответственно в обеих диетах. Это говорит о том, что расщепление трипсином является причиной большинства расщеплений, но следует отметить, что трипсин используется для расщепления белков в тонком кишечнике (1), поэтому некоторые расщепления могли произойти на этом этапе расщепления, а не во время подготовки образца. Эта работа включала экстракцию оптимальных белков, а не пептидов из образцов фекалий, что предполагает наличие интактных белков-хозяев в образцах фекалий, которые не полностью перевариваются в пищеварительной системе тонкого кишечника.
Участники были пожилыми мужчинами и, следовательно, могут не отражать вариации популяции, которые могут существовать среди женщин, более молодых популяций или если вариации зависят от возраста. Было показано, что, несмотря на заметно отличающиеся диеты и соблюдение предписанной диеты, в данном случае диеты с высоким содержанием белка, было мало или совсем не было доказательств повышения однородности протеома у здоровых участников. Не было заметного эффекта и от самой диеты.
Таким образом, было бы полезно провести анализ и сравнение между здоровой и определенной нездоровой популяцией, в которой аспекты функции ЖКТ нарушены.Любые исследования в этой области должны быть соответствующим образом масштабированы, чтобы учесть большую степень индивидуальной изменчивости белкового состава фекалий. Добавление образцов перед диетой поможет понять изменчивость до исследования и добавит к пониманию того, какие собственные белки изменяются при удвоении рекомендуемой нормы белка. Эта работа была выполнена с использованием качественного подхода, который позволяет изучать все идентифицированные белки, а не только белки с соответствующей количественной информацией (60).Дальнейшие исследования с использованием количественной масс-спектрометрии без меток могут дополнить имеющуюся у нас информацию о белках человека путем определения различий в концентрации фекальных белков между двумя диетами.
Выводы
В этом исследовании мы идентифицировали человеческие белки, присутствующие в фекалиях пожилых мужчин после 10 недель на здоровой диете, состоящей либо из RDA, либо из удвоенной RDA белка. Мы использовали качественный подход и не обнаружили существенных различий между этими двумя здоровыми диетами, что свидетельствует о том, что увеличение количества белка, использованное в диете 2RDA в этом исследовании, не влияет на отщепление клеток и секрецию пищеварительных ферментов с фекалиями.Мы действительно наблюдали, что протеом фекалий человека-хозяина варьирует в группе людей, соответствующих возрасту и полу. Между диетами наблюдались ограниченные различия в идентифицированных белках и классах белков. Но есть свидетельства того, что белки, связанные с пролиферацией клеток, чаще встречаются в диете 2RDA, чем в диете RDA. Исследования с более высоким содержанием белка или более длительные диеты могут показать дополнительные различия, не наблюдаемые в этой работе. В ходе этого процесса нам удалось показать хозяина-протеома человеческих фекалий этих мужчин.Нет доминирующего класса белков, но связывающие нуклеиновые кислоты и модуляторы ферментов более преобладают в фекалиях этих мужчин, чем другие классы белков Panther. Четыре белка, CO7A1, FAT3, AN469 и DYH8, ранее не идентифицированные в фекалиях, присутствовали по крайней мере в 70% образцов рациона 2RDA. Поскольку в двух диетах наблюдались ограниченные различия, теперь у нас есть основа для сравнения будущих исследований человеческих фекалий. Расширение этой основы, которое рассматривает большее количество участников и особенно принимает во внимание межиндивидуальные различия, было бы полезным.Этот расширенный базовый уровень можно сравнить для дальнейшего понимания кишечных биопутей или поиска маркеров заболевания. Для будущих исследований было бы полезно использовать более экстремальные вариации диетических привычек (всеядные или веганские) или более длительные интервенционные исследования, чтобы увидеть, наблюдаются ли эффекты белка при сравнении экстремальных или более длительных временных рамок. Такие исследования оправданы, поскольку дисфункция желудочно-кишечного тракта является основной причиной плохого состояния здоровья, при этом у многих людей наблюдаются синдромы, симптомы которых разнообразны и часто перекрывают друг друга.
Заявление о доступности данных
Наборы данных, созданные в ходе этого исследования, можно найти в онлайн-репозиториях. Названия репозиториев/репозиториев и регистрационные номера можно найти ниже: PRIDE с идентификатором PXD021424, http://proteomecentral.proteomexchange.org/cgi/GetDataset?ID=PXD021424.
Заявление об этике
Исследования с участием людей были рассмотрены и одобрены Южным комитетом по этике здоровья и инвалидности (Новая Зеландия; 15/STH/236).Пациенты/участники предоставили письменное информированное согласие на участие в этом исследовании.
Вклад авторов
DC-S, CM, JG и AG: концептуализация. DC-S, CM и AM: диетическая методология. EL, AT, JG и AG: анализ кала. CM, AM, SM, NZ, FR и PS: расследование. JG: сбор и написание данных — подготовка первоначального проекта. AM, CM, NZ, FR, PS, SK, NR, AS, K-HW, DC-S и AG: написание — проверка и редактирование. DC-S, NR, SK, AS и K-HW: привлечение финансирования. Все авторы одобрили окончательный вариант рукописи для представления.
Финансирование
Это исследование было поддержано Министерством бизнеса, инноваций и занятости Новой Зеландии, международными отношениями и Европейским союзом (IRSES-318962-BIOAGE), AgResearch Limited через Стратегический научный инвестиционный фонд (контракты A19079 и A21246: Стратегии питания для стареющего населения). ).
Конфликт интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Благодарности
Мы благодарим доктора Мэтта Барнетта за управление контрактами SSIF и отчетность, Петру Хинтерляйтнер, Элизабет Боман, Эвелину Малмквист, Элину Холмстранд, Линнею Линд, Фейт Чеге, Фернандо Тома и Элизу Пеннинг за их помощь в подготовке диеты и сборе данных. Авторы также благодарят Чарльза Хефера за анализ класса белков Panther. Мы хотели бы поблагодарить Келли Армстронг за первоначальную подготовительную работу с образцами для обеспечения безопасного обращения с ними.
Дополнительный материал
Дополнительный материал к этой статье можно найти в Интернете по адресу: https://www.frontiersin.org/articles/10.3389/fnut.2020.595905/full#supplementary-material
Ссылки
1. Эллиотт В.Х., Эллиотт Д.К., редакторы. Биохимия и молекулярная биология. Нью-Йорк, Нью-Йорк: Издательство Оксфордского университета (2001).
Академия Google
2. Singh H, Gallier S. Глава 2 — Переработка пищевых структур в желудочно-кишечном тракте и физиологические реакции. В: Боланд М., Голдинг М., Сингх Х., редакторы. Структура пищи, пищеварение и здоровье .Сан-Диего: Академическая пресса (2014). п. 51–81.
Академия Google
3. Verberkmoes NC, Russell AL, Shah M, Godzik A, Rosenquist M, Halfvarson J, et al. Метапротеомика дробовика микробиоты дистального отдела кишечника человека. Исме Дж. (2009) 3:179–89. doi: 10.1038/ismej.2008.108
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
4. Мартинс душ Сантуш В., Мюллер М., де Вос В.М. Системная биология кишечника: взаимодействие пищи, микробиоты и хозяина на границе слизистой оболочки. Карр Опин Биотехнолог. (2010) 21:539–50. doi: 10.1016/j.copbio.2010.08.003
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
5. Avramidou M, Angst F, Angst J, Aeschlimann A, Rössler W, Schnyder U. Эпидемиология желудочно-кишечных симптомов у молодых и средних швейцарцев: распространенность и сопутствующие заболевания в лонгитудинальной популяционной когорте за 28 лет. ВМС Гастроэнтерол. (2018) 18:21. doi: 10.1186/s12876-018-0749-3
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
6.Ким Дж., Ан Джу, Ким В., Ли С., Чо С. Различия в микробиоте кишечника собак ( Canis lupus Familiaris), получавших натуральный или коммерческий корм, выявленные с помощью платформы Illumina MiSeq. Патог кишечника. (2017) 9:68. doi: 10.1186/s13099-017-0218-5
Полнотекстовая перекрестная ссылка | Академия Google
7. Pan S, Hullar MAJ, Lai LA, Peng H, May DH, Noble WS, et al. Экспрессия кишечного микробного белка в ответ на режим питания в исследовании контролируемого питания: метапротеомный подход. Микроорганизмы. (2020) 8:379. doi: 10.3390/микроорганизмы8030379
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
8. Duvoisin G, Lopez RN, Day AS, Lemberg DA, Gearry RB, Leach ST. Новые биомаркеры и будущий потенциал биомаркеров при воспалительных заболеваниях кишечника. Среднее воспаление. (2017) 2017:1936315. дои: 10.1155/2017/1936315
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
9. Джин П., Ван К., Хуанг С., Nice EC.Разработка фекального протеома: от биомаркеров до персонализированной медицины. Экспертиза протеомики. (2017) 14:445–59. дои: 10.1080/14789450.2017.1314786
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
10. Manceau H, Chicha-Cattoir V, Puy H, Peoc’h K. Фекальный кальпротектин при воспалительных заболеваниях кишечника: обновление и перспективы. Clin Chem Lab Med . (2017) 55:474–83. doi: 10.1515/cclm-2016-0522
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
11.Gavin PG, Mullaney JA, Loo D, Cao K-AL, Gottlieb PA, Hill MM, et al. Кишечная метапротеомика выявляет взаимодействия между хозяином и микробиотой у субъектов с риском развития диабета 1 типа. Лечение диабета. (2018) 41:2178–86. дои: 10.2337/dc18-0777
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
12. Rechenberger J, Samaras P, Jarzab A, Behr J, Frejno M, Djukovic A, et al. Проблемы клинической метапротеомики, выделенные при анализе пациентов с острым лейкозом с колонизацией кишечника полирезистентными энтеробактериями. Протеомы. (2019) 7:2. doi: 10.3390/proteomes7010002
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
13. Чепмен Дж. Д., Гудлетт Д. Р., Масселон К. Д. Мультиплексная и независимая от данных тандемная масс-спектрометрия для глобального профилирования протеома. Масс-спектр. Ред. (2014) 33:452–70. doi: 10.1002/mas.21400
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
14. Hu A, Noble WS, Wolf-Yadlin A. Технические достижения в протеомике: новые разработки в области сбора данных, не зависящих от данных. F1000Res . (2016) 5: F1000 Факультет Rev-1419. doi: 10.12688/f1000research.7042.1
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
16. Di Palma S, Hennrich ML, Heck AJR, Mohammed S. Последние достижения в разделении пептидов с помощью многомерной жидкостной хроматографии для анализа протеома. Дж. Протеомика. (2012) 75:3791–813. doi: 10.1016/j.jprot.2012.04.033
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
17.Zhang X, Li L, Mayne J, Ning Z, Stintzi A, Figeys D. Оценка влияния методов экстракции белка на метапротеомику кишечника человека. Дж. Протеомика. (2018) 180:120–7. doi: 10.1016/j.jprot.2017.07.001
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
18. Wycherley TP, Moran LJ, Clifton PM, Noakes M, Brinkworth GD. Эффекты низкокалорийной диеты с высоким содержанием белка и низким содержанием жира по сравнению со стандартным содержанием белка и низким содержанием жира: метаанализ рандомизированных контролируемых исследований. Am J Clin Nutr. (2012) 96:1281–98. doi: 10.3945/ajcn.112.044321
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
19. Уолранд С., Шорт К.Р., Бигелоу М.Л., Суит А.Дж., Хатсон С.М., Наир К.С. Функциональное влияние высокого потребления белка на здоровых пожилых людей. Am J Physiol Endocrinol Metab. (2008) 295:E921–8. doi: 10.1152/ajpendo..2008
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
20. Брин Л., Филлипс С.М.Метаболизм белков скелетных мышц у пожилых людей: меры по противодействию «анаболической резистентности» старения. Нутр Метаб. (2011) 8:68. дои: 10.1186/1743-7075-8-68
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
21. Lan A, Andriamihaja M, Blouin J-M, Liu X, Descatoire V, Desclée de Maredsous C, et al. Диета с высоким содержанием белка по-разному изменяет характеристики бокаловидных клеток кишечника и экспрессию цитокинов слизистой оболочки подвздошной и толстой кишки. J Nutr Biochem. (2015) 26:91–8. doi: 10.1016/j.jnutbio.2014.09.007
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
22. Kar SK, Jansman AJM, Benis N, Ramiro-Garcia J, Schokker D, Kruijt L, et al. Источники диетического белка по-разному влияют на микробиоту, активность mTOR и транскрипцию сигнальных путей mTOR в тонком кишечнике. ПЛОС ОДИН. (2017) 12:e0188282. doi: 10.1371/journal.pone.0188282
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
23.Zhu Y, Shi C, Niu Q, Wang J, Zhu W. Динамические изменения в морфологии, экспрессии генов и микробиоме в тощей кишке крыс с компенсаторным ростом, вызванные ограничением белка. Микроб Биотехнолог. (2018) 11:734–46. дои: 10.1111/1751-7915.13266
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
24. Meng Y, Li X, Zhang J, Wang C, Lu F. Влияние различных диет на микробиоту слизи тонкой кишки и регуляцию веса у крыс. Научный представитель (2019) 9:8500.doi: 10.1038/s41598-019-44994-7
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
25. Beaumont M, Portune KJ, Steuer N, Lan A, Cerrudo V, Audebert M, et al. Количество и источник пищевого белка влияют на выработку метаболитов кишечной микробиотой и экспрессию генов слизистой оболочки прямой кишки: рандомизированное, параллельное, двойное слепое исследование у людей с избыточным весом. Am J Clin Nutr. (2017) 106:1005–19. doi: 10.3945/ajcn.117.158816
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
26.Митчелл С.Дж., Милан А.М., Митчелл С.М., Зенг Н., Рамзан Ф., Шарма П. и др. Влияние потребления белка с пищей на мышечную массу и мышечную функцию у пожилых мужчин: 10-недельное рандомизированное контролируемое исследование. Am J Clin Nutr. (2017) 106:1375–83. doi: 10.3945/ajcn.117.160325
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
27. Минздрав. Рекомендации по пищевым продуктам и питанию для здоровых пожилых людей: справочный документ. Веллингтон: Министерство здравоохранения (2013 г.).
Академия Google
28. Лихтман Дж.С., Маркобал А., Зонненбург Дж.Л., Элиас Дж.Е. Протеомика стула, ориентированная на хозяина: новая стратегия, ориентированная на реакцию кишечника на микробиоту кишечника. Мол клеточная протеомика. (2013) 12:3310–8. doi: 10.1074/mcp.M113.029967
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
29. Вессель Д., Флюгге У.И. Метод количественного выделения белка в разбавленном растворе в присутствии детергентов и липидов. Анальная биохимия. (1984) 138:141–3. дои: 10.1016/0003-2697(84)
-6
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
30. Gathercole J, Reis MG, Agnew M, Reis MM, Humphrey R, Harris P, et al. Молекулярная модификация, связанная с термической обработкой коровьего молока. Int Dairy J. (2017) 73:74–83. doi: 10.1016/j.idairyj.2017.05.008
Полнотекстовая перекрестная ссылка | Академия Google
31. Перес-Риверол Ю., Чордас А., Бай Дж., Берналь-Ллинарес М., Хевапатирана С., Кунду Д.Дж. и др.База данных PRIDE и связанные с ней инструменты и ресурсы в 2019 году: улучшение поддержки данных количественного анализа. Рез. нуклеиновых кислот. (2019) 47:D442–50. doi: 10.1093/nar/gky1106
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
32. Boros E, Szabó A, Zboray K, Héja D, Pál G, Sahin-Tóth M. Перекрывающаяся специфичность дублированных изоформ эластазы поджелудочной железы человека 3 и архетипической свиной эластазы 1 дает ключ к разгадке эволюции пищеварительных ферментов. J Biol Chem. (2017) 292:2690–702. doi: 10.1074/jbc.M116.770560
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
35. Kumar V, Mack DR, Marcil V, Israel D, Krupoves A, Costea I, et al. Сигнал полногеномного исследования ассоциации в локусе 12q12 для болезни Крона может представлять ассоциации с геном MUC19. Воспаление кишечника Dis. (2013) 19:1254–9. дои: 10.1097/MIB.0b013e318281f454
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
36.Cuylen S, Blaukopf C, Politi AZ, Müller-Reichert T, Neumann B, Poser I, et al. Ki-67 действует как биологический сурфактант для рассеивания митотических хромосом. Природа. (2016) 535:308. doi: 10.1038/nature18610
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
37. Улен М., Фагерберг Л., Халльстрем Б.М., Линдског С., Оксволд П., Мардиноглу А. и соавт. Тканевая карта протеома человека. Наука. (2015) 347:1260419. doi: 10.1126/science.1260419
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
39.Ми Х, Муругануджан А, Томас П.Д. PANTHER в 2013 году: моделирование эволюции функций генов и других свойств генов в контексте филогенетических деревьев. Рез. нуклеиновых кислот . (2013) 41:D377–86. doi: 10.1093/nar/gks1118
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
41. Чжан В., Лю Х.Т. Сигнальные пути МАРК в регуляции клеточной пролиферации в клетках млекопитающих. Сотовый рез. (2002) 12:9. doi: 10.1038/sj.cr.72
Полнотекстовая перекрестная ссылка | Академия Google
43.Рамзан Ф., Митчелл С.Дж., Милан А.М., Ширдинг В., Зенг Н., Шарма П. и др. Всестороннее профилирование реакции циркуляторной микроРНК на диету с высоким содержанием белка у пожилых мужчин: потенциальная роль в модуляции воспалительной реакции. Mol Nutr Food Res. (2019) 63:e1800811. doi: 10.1002/mnfr.201800811
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
45. Sheth J, Mistri M, Patel H, Ankleshwaria C, Parikh A. Аутосомно-доминантная мутация в гене COL7A1, вызывающая дистрофический буллезный эпидермолиз. Мол Цитогенет. (2014) 7:P58. дои: 10.1186/1755-8166-7-S1-P58
Полнотекстовая перекрестная ссылка | Академия Google
46. Takeda H, Kon A, Ito N, Sawamura D, Takagaki K, Hashimoto I, et al. Кератиноцит-специфическая модуляция экспрессии гена коллагена VII типа провоспалительными цитокинами (фактор некроза опухоли-альфа и интерлейкин-1бета). Опыт Дерматол. (2005) 14:289–94. doi: 10.1111/j.0906-6705.2005.00316.x
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
47.Гёке М., Канай М., Подольский Д.К. Кишечные фибробласты регулируют пролиферацию эпителиальных клеток кишечника посредством фактора роста гепатоцитов. Am J Physiol Gastrointest Liver Physiol. (1998) 274:G809–18. doi: 10.1152/ajpgi.1998.274.5.G809
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
49. Сабури С., Хестер И., Гудрич Л., Макнил Х. Функциональные взаимодействия между кадгеринами семейства жиров в морфогенезе тканей и плоской полярности. Развитие. (2012) 139:1806–20.doi: 10.1242/dev.077461
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
50. Zhang X, Liu J, Liang X, Chen J, Hong J, Li L, et al. История и развитие жировых кадгеринов в норме и болезни. Цели Onco Ther. (2016) 9:7337–43. doi: 10.2147/OTT.S111176
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
52. Xu J, Wang X, Xu P, Liu S, Teng F, Liu X, et al. Профилирование пептидома тканей серозного рака яичников человека на основе масс-спектрометрии. Int J Biochem Cell Biol. (2019) 107:53–61. doi: 10.1016/j.biocel.2018.12.004
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
53. Karolak JA, Gambin T, Rydzanicz M, Szaflik JP, Polakowski P, Frajdenberg A, et al. Доказательства того, что ZNF469 является причиной кератоконуса у польских пациентов. Acta Ophthalmologica. (2016) 94:289–94. дои: 10.1111/аос.12968
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
54.Калантан Х., Кондкар А.А., Султан Т., Азад Т.А., Алсабаани Н.А., Аль-Кахтани М.А. и соавт. Полиморфизм rs13334190 в белке цинковых пальцев 469 (ZNF469) не является фактором риска кератоконуса в саудовской когорте. BMC Res Notes. (2017) 10:652. doi: 10.1186/s13104-017-2996-8
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
55. Maiti AK, Mattéi MG, Jorissen M, Volz A, Zeigler A, Bouvagnet P. Идентификация, тканеспецифическая экспрессия и хромосомная локализация нескольких генов тяжелой цепи динеина человека. Eur J Hum Genet. (2000) 8:923–32. doi: 10.1038/sj.ejhg.5200555
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
56. Асаи Д.Дж., Уилкс, Делавэр. Семейство тяжелых цепей динеина1. J Эукариот микробиол. (2004) 51:23–9. doi: 10.1111/j.1550-7408.2004.tb00157.x
Полнотекстовая перекрестная ссылка | Академия Google
57. Stout MA, Raeymaekers L, De Smedt H, Casteels R. Характеристика высвобождения Ca2+ из гетерогенных запасов Ca2+ в саркоплазматическом ретикулуме, выделенном из гладкой мускулатуры артерий и желудка. Can J Physiol Pharmacol. (2002) 80:588–603. doi: 10.1139/y02-083
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
59. Бейкер С.А., Драмм Б.Т., Саур Д., Хенниг Г.В., Уорд С.М., Сандерс К.М. Спонтанные транзиенты Ca2+ в интерстициальных клетках Кахаля, расположенных в глубоком мышечном сплетении тонкой кишки мыши. Ж Физиол. (2016) 594:3317–38. дои: 10.1113/JP271699
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
60.Банчефф М., Ширле М., Свитман Г., Рик Дж., Кастер Б. Количественная масс-спектрометрия в протеомике: критический обзор. Анальный биоанальный хим. (2007) 389:1017–31. doi: 10.1007/s00216-007-1486-6
Реферат PubMed | Полный текст перекрестной ссылки | Академия Google
Аллергический колит | Бостонская детская больница
Что такое аллергический колит?
Аллергический колит — это состояние, при котором иммунная система вашего ребенка чрезмерно реагирует на белки, содержащиеся в коровьем молоке, что приводит к воспалению толстой кишки.
Младенцы различаются по своей чувствительности к молоку. У некоторых очень мало симптомов, а у других может быть кровь в стуле, если у кормящей матери есть даже небольшая капля молока в ее утреннем кофе.
Аллергический колит не редкость; это затрагивает от двух до 3 процентов младенцев. Дети из семей с историей пищевой аллергии, астмы или аллергии на окружающую среду, по-видимому, имеют несколько более высокий риск развития этого состояния.
Аллергический колит часто имеет мало симптомов, но может быть связан с раздражительностью, газообразованием, а кровь или слизь в стуле могут сделать прием пищи очень неудобным для ребенка, поэтому он может не получать необходимое ему питание.
Каковы симптомы аллергического колита?
Хотя симптомы могут не проявляться, пока ребенку не исполнится 6 месяцев, у большинства детей признаки проявляются в течение первых двух месяцев жизни. У большинства детей симптомы выражены слабо, но иногда могут ухудшаться.
Ребенок с аллергическим колитом может быть чрезвычайно беспокойным, его трудно утешить, и у него могут появиться вкрапления или прожилки крови в стуле. У некоторых младенцев также бывает диарея и рвота, а у некоторых могут проявляться другие признаки аллергии, такие как заложенность носа или экзема.Важно помнить, что аллергический колит бывает разным: некоторые дети более чувствительны к молочному белку (и имеют более тяжелые симптомы), чем другие.
Многие дети проходят через период рефлюкса (срыгивания пищи) в первый год жизни, но дети с аллергическим колитом могут особенно тяжело переносить рефлюкс. Лечение колита может привести к улучшению рефлюкса, но некоторые рефлюксы могут быть не связаны с аллергическим процессом.
Каковы причины аллергического колита?
Аллергический колит, по-видимому, вызывается сочетанием изменений иммунной системы матери во время беременности и незрелостью собственной иммунной системы ребенка.Но пока неизвестно, почему у одних детей развивается это заболевание, а у других нет.
Может иметь место наследственный компонент, поскольку дети из семей с историей пищевой аллергии, астмы или аллергии на окружающую среду, по-видимому, чаще страдают аллергическим колитом.
Как диагностируется аллергический колит?
Если ваш ребенок очень раздражителен и вы заметили рвоту и газообразование, рекомендуется записаться на прием к педиатру. Врач проверит наличие крови в стуле вашего ребенка.Это может быть кровь, которую можно увидеть только в микроскоп. При обнаружении крови симптомы, скорее всего, вызваны аллергической реакцией.
Какие существуют варианты лечения аллергического колита?
В большинстве случаев кровь в стуле младенца вызвана аллергией на молоко, которая хорошо поддается лечению. Мать переводят на безмолочную диету (если она кормит грудью) или переводят ребенка на гипоаллергенную смесь. Материнскому грудному молоку требуется до 72 часов, чтобы освободиться от молочного белка, поэтому до тех пор, пока вы снова не будете готовы кормить грудью, вашему ребенку будут давать гипоаллергенную смесь.
Примерно 30 процентов детей с аллергией на белок коровьего молока имеют также аллергию на белок сои, поэтому, если симптомы у вашего ребенка не исчезают, кормящей матери рекомендуется избегать сои, а также молочных продуктов (или использовать соевые бесплатная формула).
Имейте в виду, что даже если ваш ребенок больше не поглощает белки, вызывающие реакции в кишечнике, кишечник все равно нуждается в заживлении. Вот почему вы можете продолжать замечать кровь в стуле в течение трех-четырех недель после начала диеты без молока/сои.Но вы должны заметить, что ваш младенец, кажется, чувствует себя лучше — менее раздражителен и менее склонен к еде, а также может прибавлять в весе, что является хорошим признаком.
Как мы лечим аллергический колит
Отделение гастроэнтерологии, гепатологии и питания Бостонской детской больницы занимается лечением детей с желудочно-кишечными заболеваниями, такими как аллергический колит, уже более 65 лет.
.
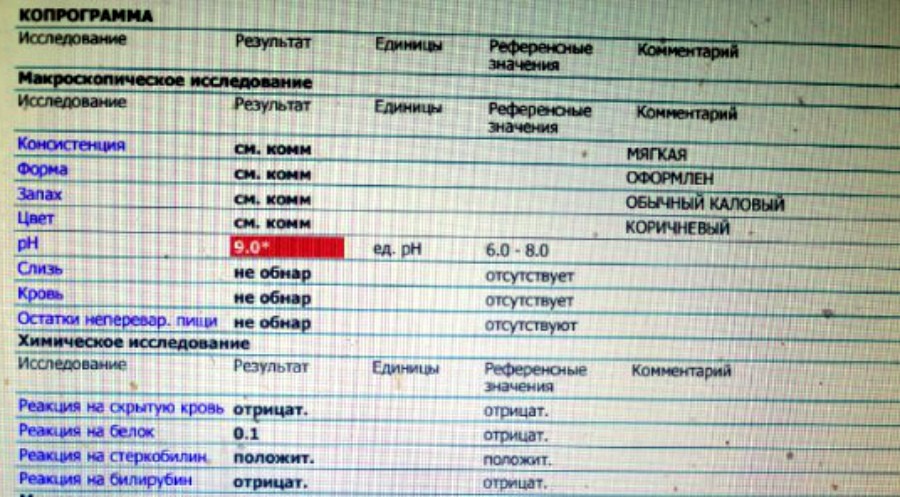
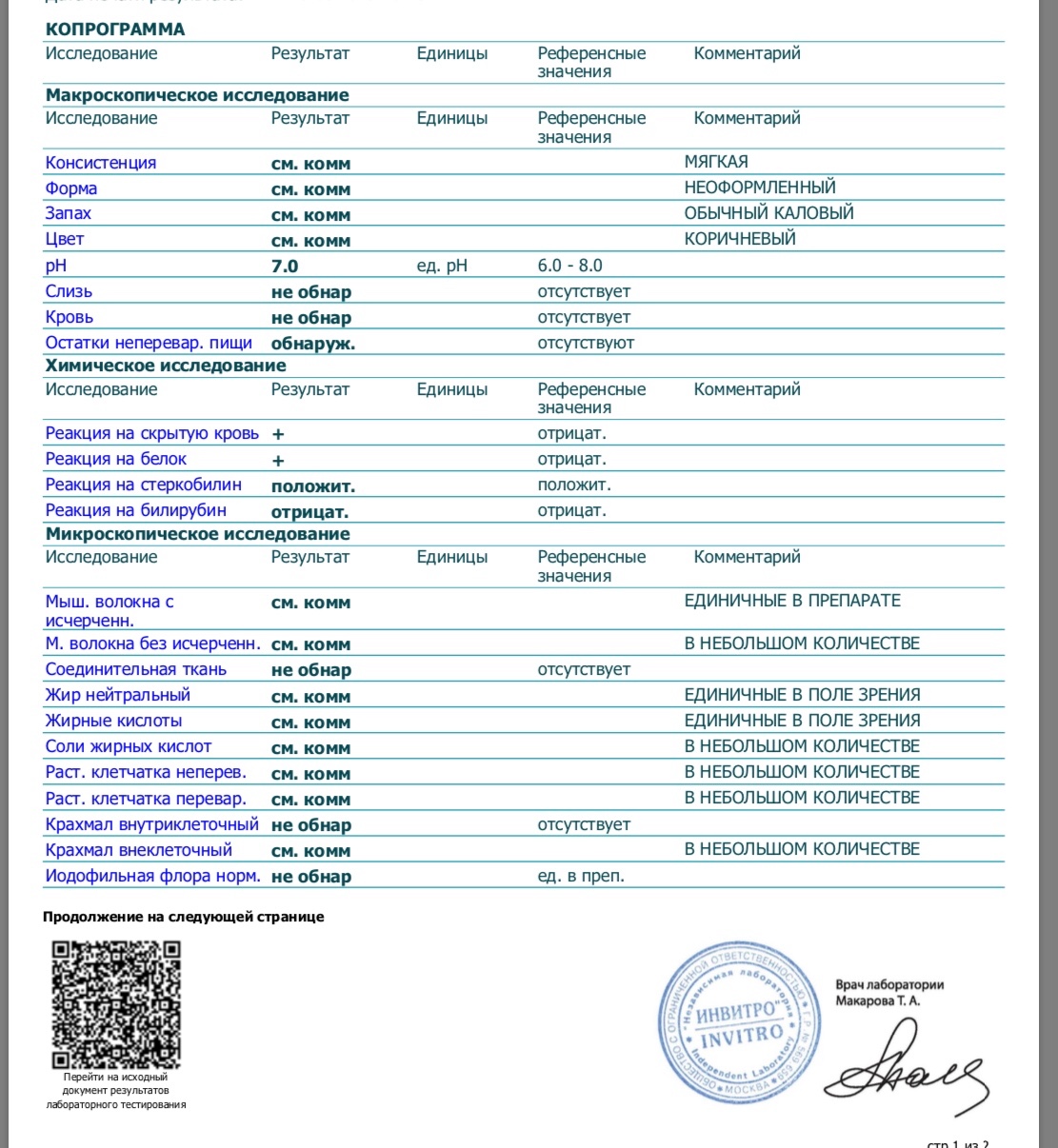 Хотя положительный результат теста может свидетельствовать о наличии антител IgE, он имеет низкую прогностическую ценность, в то время как отрицательный результат теста имеет высокую прогностическую точность.
Хотя положительный результат теста может свидетельствовать о наличии антител IgE, он имеет низкую прогностическую ценность, в то время как отрицательный результат теста имеет высокую прогностическую точность. Реакции и симптомы должны быть воспроизводимы при повторных тестах на исключение диеты и пищевых пробах. Некоторые реакции со стороны желудочно-кишечного тракта могут проявляться с отсроченным началом, вызывая появление симптомов через несколько часов или дней после приема внутрь.
Реакции и симптомы должны быть воспроизводимы при повторных тестах на исключение диеты и пищевых пробах. Некоторые реакции со стороны желудочно-кишечного тракта могут проявляться с отсроченным началом, вызывая появление симптомов через несколько часов или дней после приема внутрь. Биопсия тощей кишки при синдроме энтероколита и глютеновой болезни показывает атрофию ворсин и кишечную инфильтрацию лимфоцитами.
Биопсия тощей кишки при синдроме энтероколита и глютеновой болезни показывает атрофию ворсин и кишечную инфильтрацию лимфоцитами.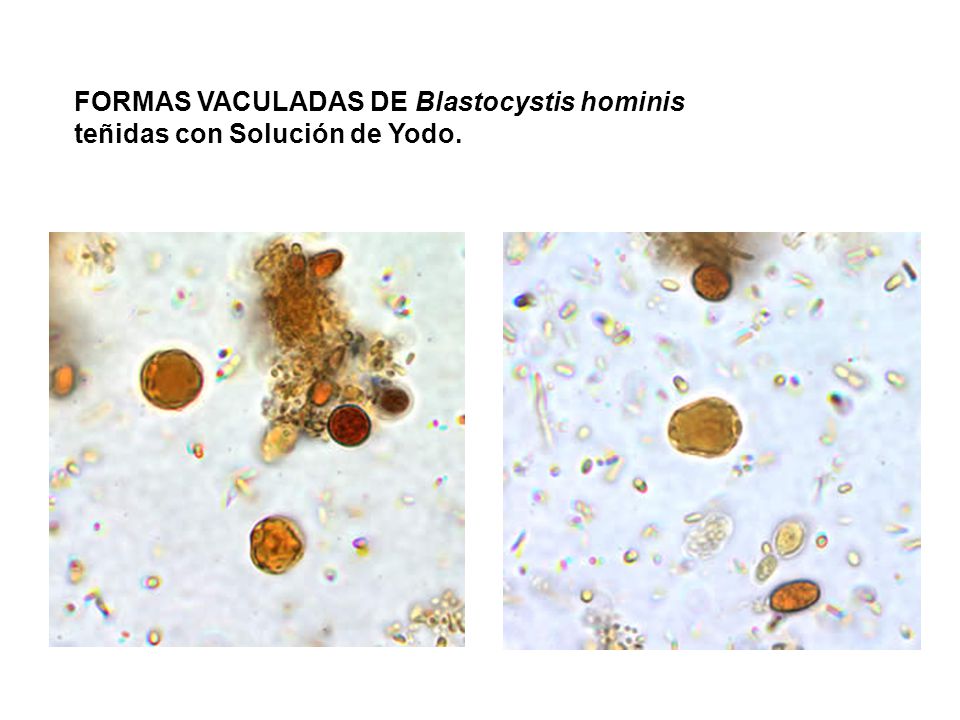 Пациенты с кишечными инфекциями часто имеют признаки инфекции и могут лечиться противомикробными препаратами.
Пациенты с кишечными инфекциями часто имеют признаки инфекции и могут лечиться противомикробными препаратами.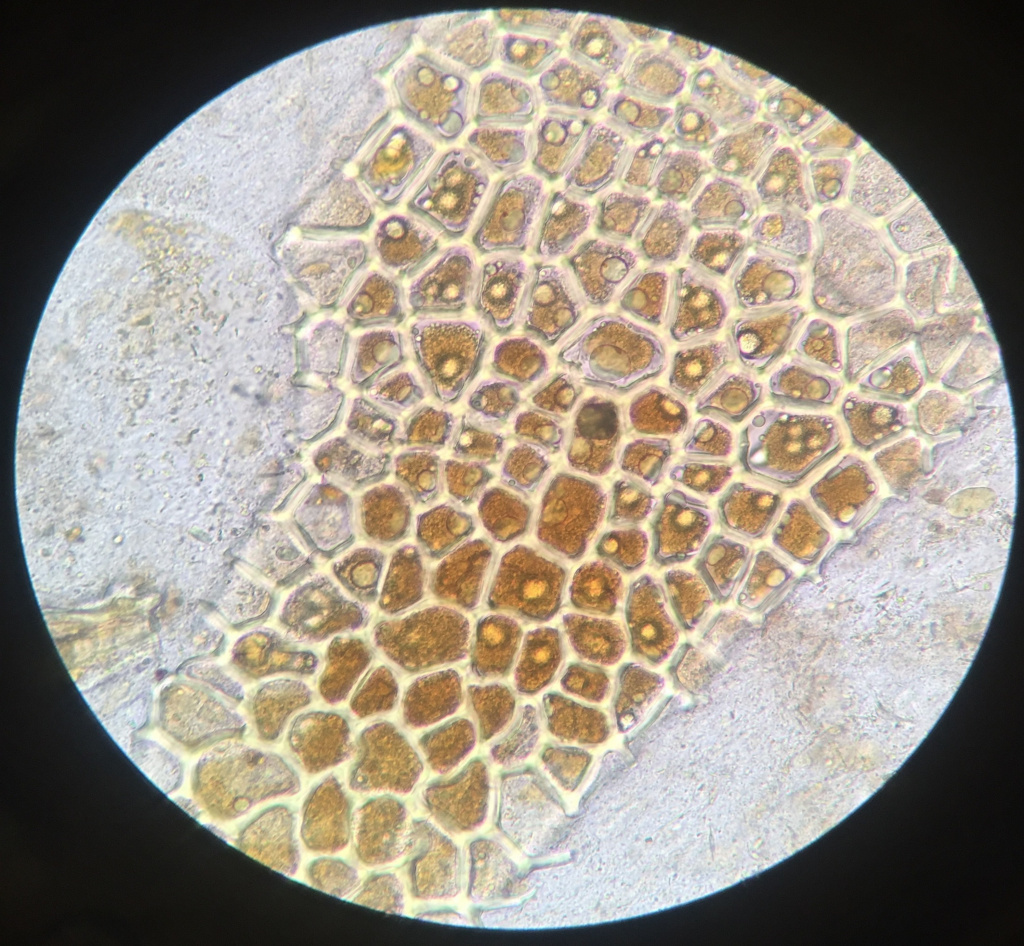 Однако важно исключить ВЗК, поскольку они являются системными хроническими заболеваниями и требуют обширного лечения.
Однако важно исключить ВЗК, поскольку они являются системными хроническими заболеваниями и требуют обширного лечения.
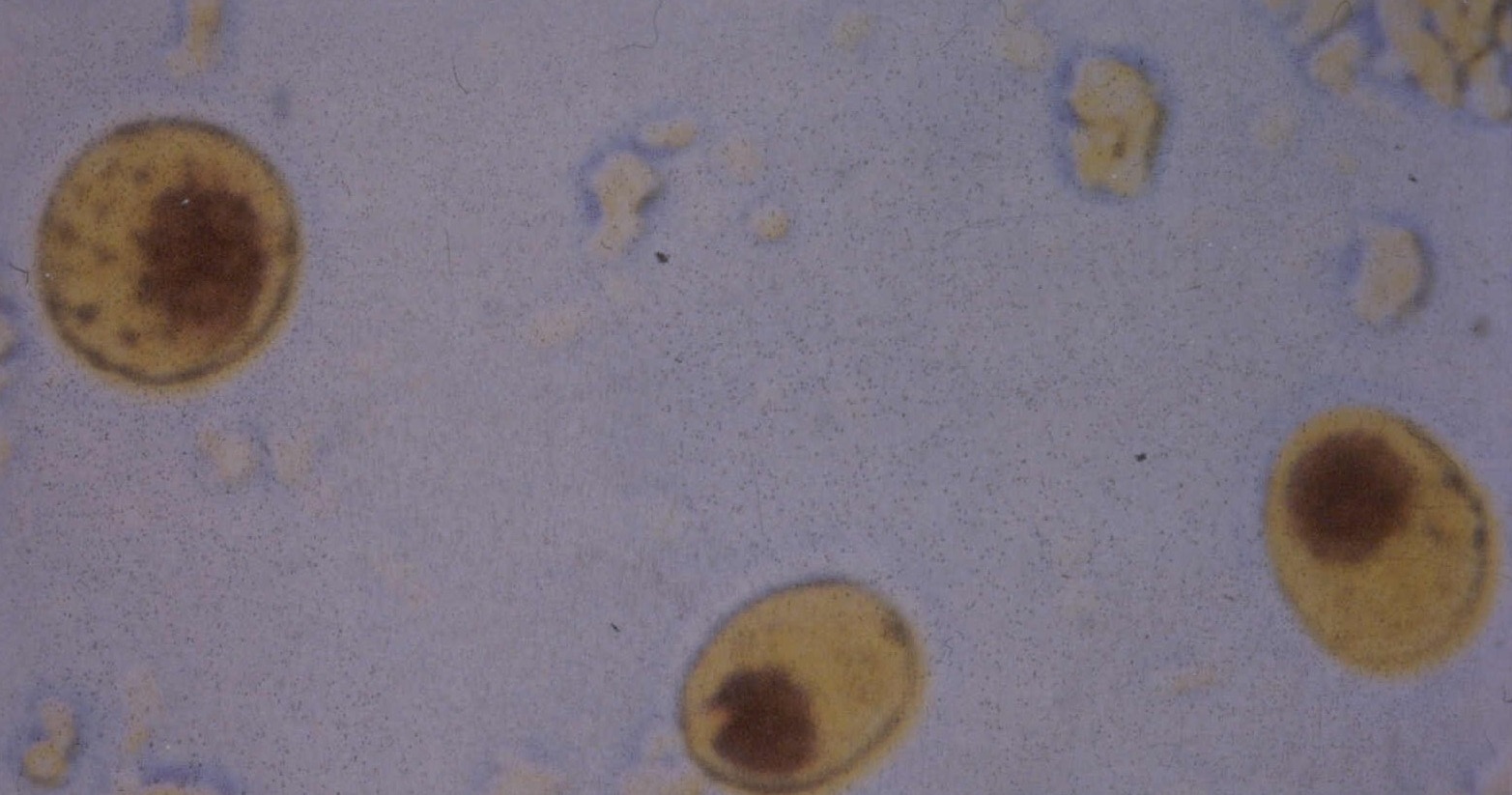 Курр Опин Аллергия Клин Иммунол. 2014 июнь;14(3):208-16. [Бесплатная статья PMC: PMC4011623] [PubMed: 24686277]
Курр Опин Аллергия Клин Иммунол. 2014 июнь;14(3):208-16. [Бесплатная статья PMC: PMC4011623] [PubMed: 24686277] Дефицит кишечной энтерокиназы. Недавно обнаруженное нарушение переваривания белков. Арч Дис Чайлд. 1970 окт; 45 (243): 651-5. [Бесплатная статья PMC: PMC1647492] [PubMed: 5477679]
Дефицит кишечной энтерокиназы. Недавно обнаруженное нарушение переваривания белков. Арч Дис Чайлд. 1970 окт; 45 (243): 651-5. [Бесплатная статья PMC: PMC1647492] [PubMed: 5477679] , Эйгенманн П., Фернандес Ривас М., Халкен С., Хикштейн Л., Хёст А., Кнол Э., Лак Г., Маркизотто М.Дж., Ниггеманн Б., Нвару Б.И., Пападопулос Н.Г., Поулсен Л.К., Сантос А.Ф., Скайпала И., Шёпфер А., Ван Ри Р., Вентер С., Ворм М., Влиг-Бурстра Б., Панесар С., де Сильва Д., Соарес-Вайзер К., Шейх А., Балмер-Вебер Б.К., Нильссон С., де Йонг Н.В., Акдис К.А., Группа рекомендаций EAACI по пищевой аллергии и анафилаксии. Рекомендации EAACI по пищевой аллергии и анафилаксии: диагностика и лечение пищевой аллергии. Аллергия. 2014 авг;69(8):1008-25. [PubMed: 24
, Эйгенманн П., Фернандес Ривас М., Халкен С., Хикштейн Л., Хёст А., Кнол Э., Лак Г., Маркизотто М.Дж., Ниггеманн Б., Нвару Б.И., Пападопулос Н.Г., Поулсен Л.К., Сантос А.Ф., Скайпала И., Шёпфер А., Ван Ри Р., Вентер С., Ворм М., Влиг-Бурстра Б., Панесар С., де Сильва Д., Соарес-Вайзер К., Шейх А., Балмер-Вебер Б.К., Нильссон С., де Йонг Н.В., Акдис К.А., Группа рекомендаций EAACI по пищевой аллергии и анафилаксии. Рекомендации EAACI по пищевой аллергии и анафилаксии: диагностика и лечение пищевой аллергии. Аллергия. 2014 авг;69(8):1008-25. [PubMed: 24 01 декабря 2019 г.; 173(12):1137-1145. [Бесплатная статья PMC: PMC6806425] [PubMed: 31633778]
01 декабря 2019 г.; 173(12):1137-1145. [Бесплатная статья PMC: PMC6806425] [PubMed: 31633778]
 Хотя положительный результат теста может свидетельствовать о наличии антител IgE, он имеет низкую прогностическую ценность, в то время как отрицательный результат теста имеет высокую прогностическую точность.
Хотя положительный результат теста может свидетельствовать о наличии антител IgE, он имеет низкую прогностическую ценность, в то время как отрицательный результат теста имеет высокую прогностическую точность.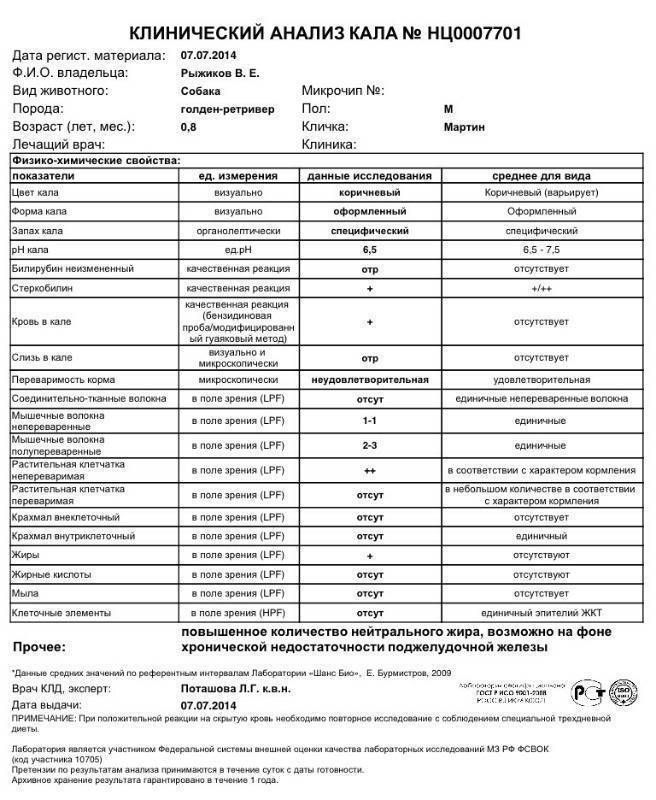 Реакции и симптомы должны быть воспроизводимы при повторных тестах на исключение диеты и пищевых пробах. Некоторые реакции со стороны желудочно-кишечного тракта могут проявляться с отсроченным началом, вызывая появление симптомов через несколько часов или дней после приема внутрь.
Реакции и симптомы должны быть воспроизводимы при повторных тестах на исключение диеты и пищевых пробах. Некоторые реакции со стороны желудочно-кишечного тракта могут проявляться с отсроченным началом, вызывая появление симптомов через несколько часов или дней после приема внутрь. Биопсия тощей кишки при синдроме энтероколита и глютеновой болезни показывает атрофию ворсин и кишечную инфильтрацию лимфоцитами.
Биопсия тощей кишки при синдроме энтероколита и глютеновой болезни показывает атрофию ворсин и кишечную инфильтрацию лимфоцитами.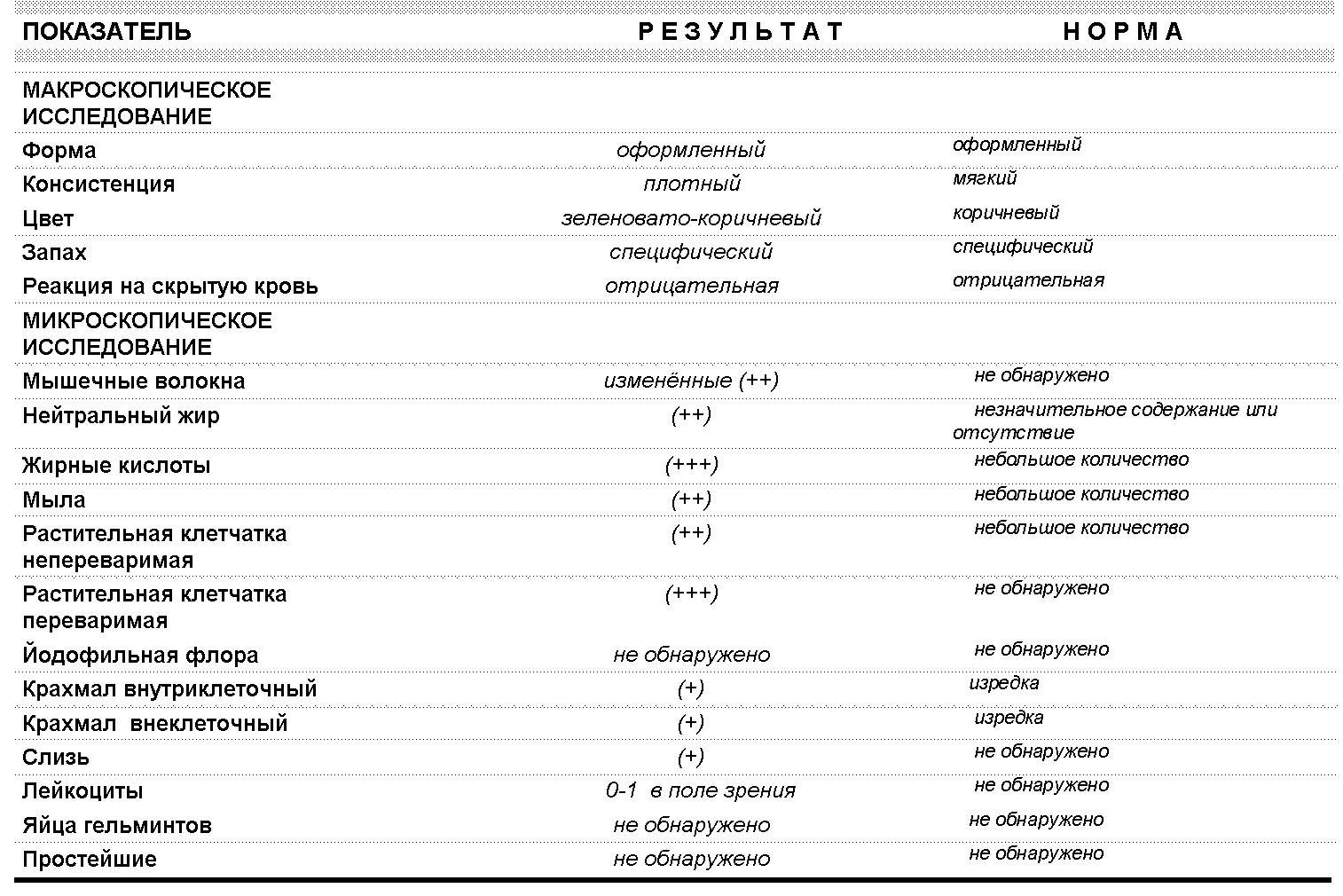 Пациенты с кишечными инфекциями часто имеют признаки инфекции и могут лечиться противомикробными препаратами.
Пациенты с кишечными инфекциями часто имеют признаки инфекции и могут лечиться противомикробными препаратами.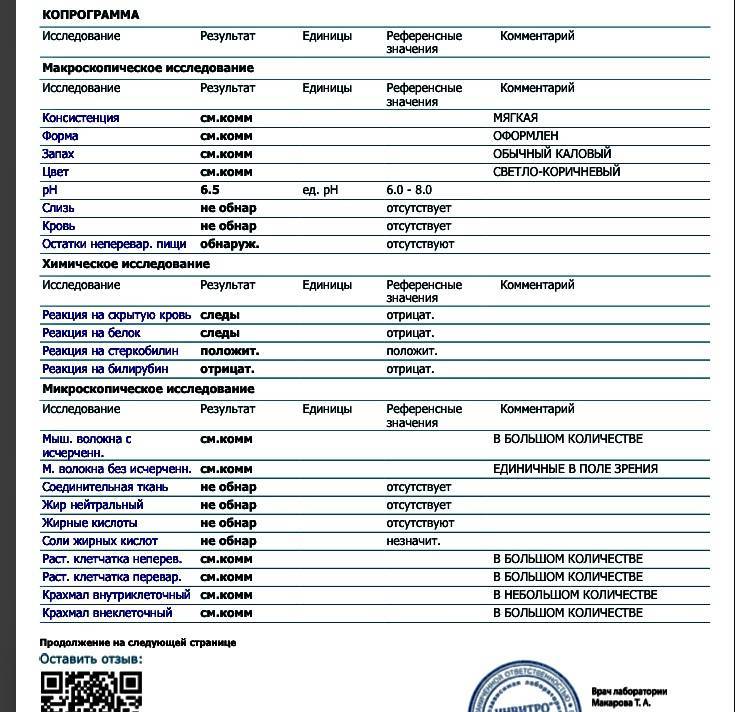 Однако важно исключить ВЗК, поскольку они являются системными хроническими заболеваниями и требуют обширного лечения.
Однако важно исключить ВЗК, поскольку они являются системными хроническими заболеваниями и требуют обширного лечения.