Анэмбриония – беременность или нет?
К сожалению, далеко не все наступившие беременности завершаются деторождением. Репродуктивные потери при этом могут быть обусловлены различными причинами. И одной из них является неразвивающаяся или замершая беременность. Н долю этой патологии приходится до 15-20% репродуктивных потерь. В настоящее время выделяют 2 варианта замершей беременности: гибель эмбриона и анэмбриония. Важно понимать, что дифференциальная диагностика между ними не влияет на последующую лечебную тактику, но учитывается при оценке прогноза. Чаще определяется анэмбриония, причем это состояние во многих случаях не сопровождается самопроизвольным абортом и потому требует искусственного прерывания замершей беременности.
Анэмбриония – что это такое?
Анэмбриония – это отсутствие эмбриона в развивающемся плодном яйце. Такое состояние называют также синдромом пустого плодного яйца. Это отнюдь не редкая патология, которая может быть диагностирована у первобеременных и у женщин, уже имеющих здоровых детей.
В настоящее время выделено достаточно много возможных причин анэмбрионии. К ним относят:
- Генетические аномалии, которые отмечаются почти в 80% патологического состояния. Обычно они связаны с грубыми и/или множественными хромосомными нарушениями. Причем при анэмбрионии такие аномалии носят качественный характер, а при гибели эмбриона и его аборте – преимущественно количественный. Возможны также нежизнеспособные комбинации родительских генов или мутации в ключевых зонах, отвечающих за ранние этапы эмбриогенеза и синтез основных структурных белков клеточных мембран.
- Некоторые острые вирусные и бактериальные заболевания, протекающие на ранних сроках беременности и приводящие к поражению эмбриональных тканей или трофобласта. Наиболее опасны в этом плане ТОРЧ-инфекции, хотя и другие возбудители могут проявлять эмбриотропность.
- Персистирующие вирусно-бактериальные инфекции органов репродуктивной системы, приводящие к развитию хронического эндометрита.
 И в большинстве случаев такая патология протекает без явных клинических симптомов и выявляется уже после замершей беременности.
И в большинстве случаев такая патология протекает без явных клинических симптомов и выявляется уже после замершей беременности. - Экзогенные интоксикации: прием препаратов с эмбриотоксическим действием, наркомания, воздействие некоторых промышленных и сельскохозяйственных ядов (токсинов).
- Эндокринные расстройства у беременной женщины. И наиболее критичным является дефицит прогестерона и нарушения его обмена, что является основной причиной патологии децидуализации эндометрия и аномальной имплантации плодного яйца.
В целом причины возникновения патологии в большинстве случаев остаются не диагностированными. Обычно удается определить лишь предположительную этиологию.
Проведение генетической диагностики абортированных тканей может выявить явные аномалии наследственного материала. Но такое исследование, к сожалению, проводится в очень небольшом проценте случаев.
Анэмбриония является следствием прекращения размножения и дифференцировки эмбриобласта или внутренней клеточной массы – группы клеток, в норме дающих начало тканям плода. И происходит это на самых ранних этапах беременности (обычно на 2-4 неделях гестации), причем без нарушения развития плодных оболочек из трофобласта. В результате образуется так называемое пустое плодное яйцо, которое продолжает расти даже при отсутствии в нем эмбриона.
К патогенетически важным факторам развития заболевания относят:
- Унаследованные от родителей или приобретенные хромосомные аберрации и другие генетические аномалии.

- Избыточное образование в организме женщины циркулирующих иммунных комплексов. Их отложение в стенках мелких сосудов приводит к тромбоэмболиям и другим критическим нарушениям микроциркуляции в зоне имплантирующего яйца. Наибольшее клиническое значение придается антифосфолипидным антителам.
- Чрезмерная активация Т-хелперов с повышением концентрации и агрессии секретируемых ими цитокинов. Эти вещества способны оказывать прямое и опосредованное повреждающее действие на эмбриональные ткани с нарушением их пролиферации и дифференцировки. Фактически плодное яйцо в этом случае выступает мишенью для клеточного звена иммунитета. Причиной такого аномального иммунного ответа организма женщины может быть хроническая инфекция эндометрия, гормональные отклонения, некоторые другие эндогенные факторы.

Важно понимать, что при анэмбрионии в организме женщины вырабатываются вещества, способствующие пролонгации беременности. Поэтому в значительной части случаев самопроизвольный аборт не происходит. У пациентки появляются и поддерживаются признаки беременности, происходит прирост ХГЧ в сыворотке крови. Поэтому базальная температура при анэмбрионии обычно не имеет характерных особенностей. А на первом раннем УЗИ подтверждается факт успешной имплантации плодного яйца в полости матки. Ведь беременность действительно наступает, но развивается она без ключевого компонента – эмбриона.
В последующем возможно отторжение аномального плодного яйца. При этом могут быть диагностированы угроза прерывания беременности (в том числе с образованием отслаивающих ретрохориальных гематом) или самопроизвольный аборт (выкидыш). Но нередко анэмбриония диагностируется лишь при плановом обследовании, в этом случае диагноз является абсолютно неожиданным и шокирующим известием. Такая беременность требует искусственного прерывания.
Как это проявляется?
Анэмбриония не имеет собственных клинических симптомов, все появляющиеся нарушения связаны обычно с угрозой прерывания такой патологической беременности. И к настораживающим признакам можно отнести наличие клинических проявлений относительной прогестероновой недостаточности, что создает предпосылки для самопроизвольного аборта. Поэтому поводом для обращения к врачу могут стать боли внизу живота и кровянистые выделения, при анэмбрионии они могут появиться практически на любом сроке в течение 1-го триместра. Но зачастую об имеющейся патологии женщина узнает лишь при проведении скринингового УЗИ на сроке 10-14 недель.
Диагностика
Как и другие формы замершей беременности, анэмбриония выявляется в первом триместре гестации. И основным диагностическим инструментом при этом является УЗИ, ведь именно это исследование позволяет визуализировать имеющиеся отклонения.
При этом достоверно выявить симптомы можно лишь после 8-ой недели гестации.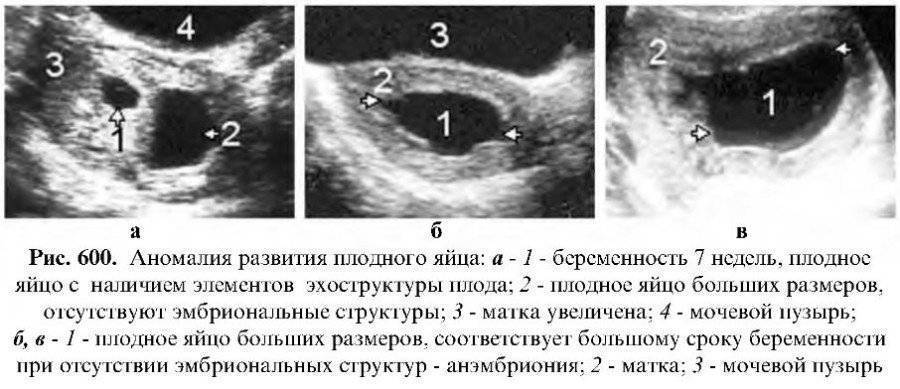 На более ранних сроках визуализация нередко недостаточна вследствие слишком малых размеров плодного яйца, так что не исключен ошибочный диагноз. Поэтому
На более ранних сроках визуализация нередко недостаточна вследствие слишком малых размеров плодного яйца, так что не исключен ошибочный диагноз. Поэтому
Основные эхографические признаки:
- отсутствие желточного мешка при диаметре плодного яйца 8-25мм;
- отсутствие эмбриона в плодном яйце диаметром более 25 мм.
К дополнительным признакам замершей беременности относят неправильную форму плодного яйца, недостаточный прирост его диаметра в динамике, слабую выраженность децидуальной реакции, отсутствие сердцебиения на сроке гестации 7 и более недель.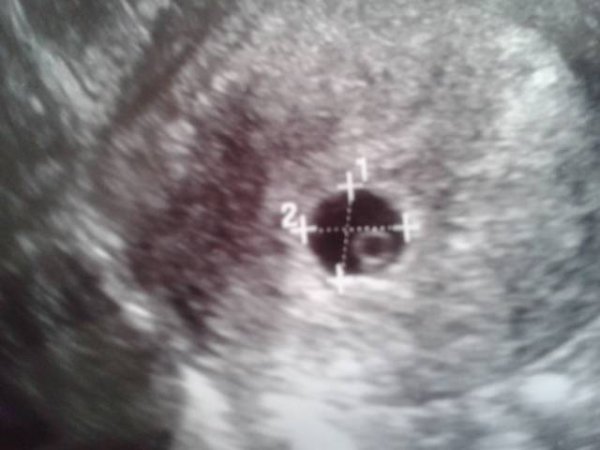
Заподозрить анэмбрионию можно также при динамической оценке уровня ХГЧ в крови. Прирост уровня этого гормона по нижней границе нормы должен быть основанием для дальнейшего обследования женщины с проведением УЗИ. Важно понимать, что ХГЧ вырабатывается и при синдроме пустого плодного яйца. Причем его уровень при этой патологии будет практически нормальным, в отличие замершей беременности с гибелью нормально развивающегося эмбриона. Поэтому отслеживание косвенных признаков беременности и рост ХГЧ при анэмбрионии нельзя отнести к достоверным методам диагностики.
Разновидности
Возможны несколько вариантов синдрома пустого плодного яйца:
- Анэмбриония I типа. Эмбрион и его остатки не визуализируются, размеры плодного яйца и матки не соответствуют предполагаемому сроку беременности. Диаметр яйца составляет обычно не более 2,5 мм, а матка увеличена лишь до 5-7 недели гестации.

- Анэмбриония II типа. Эмбриона нет, но плодное яйцо и матка соответствуют сроку гестации.
- Резорбция одного или нескольких эмбрионов при многоплодной беременности. При этом одновременно визуализируются нормально развивающиеся и регрессирующие плодные яйца. По этому типу нередко протекает анэмбриония после ЭКО, если женщине были подсажены несколько эмбрионов.
Все эти разновидности определяются лишь с помощью УЗИ, характерных клинических особенностей они не имеют.
Что делать?
Подтвержденная анэмбриония является показанием для искусственного прерывания беременности. При этом не учитывается срок гестации, самочувствие женщины и наличие у нее признаков возможного самопроизвольного аборта. Исключение составляет ситуация, когда диагностируется анэмбриония второго плодного яйца при многоплодной беременности. В этом случае предпринимают выжидательную тактику, оценивая в динамике развитие сохранившегося эмбриона.
Прерывание замершей беременности проводится только в стационаре. После процедуры эвакуации плодного яйца женщина должна находиться под врачебным наблюдением. Во многих случаях после неё назначается дополнительное медикаментозное и иногда физиотерапевтическое лечение, направленное на нормализацию гормонального фона, профилактику воспалительных и геморрагических осложнений, ликвидацию выявленной инфекции.
Для проведения медицинского аборта при этой патологии возможно использование нескольких методик. Могут быть использованы:
- медикаментозный аборт – прерывание беременности с помощью гормональных препаратов, провоцирующих отторжение эндометрия вместе с имплантированным плодным яйцом;
- вакуумная аспирация содержимого полости матки;
- выскабливание – операция, включающая механическое удаление плодного яйца и эндометрия специальным инструментом (кюреткой) после принудительного расширения канала шейки матки бужами.
Медикаментозный аборт при анэмбрионии возможен лишь на сроке 6-8 недель. В более поздние сроки гестации предпочтение отдают механическим методам, что требует применения общей анестезии. От выбора способа искусственного аборта зависит, болит ли живот после прерывания беременности, продолжительность реабилитационного периода, вероятность развития ранних и поздних осложнений.
В более поздние сроки гестации предпочтение отдают механическим методам, что требует применения общей анестезии. От выбора способа искусственного аборта зависит, болит ли живот после прерывания беременности, продолжительность реабилитационного периода, вероятность развития ранних и поздних осложнений.
Обследование после искусственного аборта обязательно включает УЗ-контроль. Это позволяет подтвердить полную эвакуацию плодных оболочек и эндометрия, исключить нежелательные последствия аборта в виде гематометры, перфорации и эндометрита.
Прогноз
Может ли повториться анэмбриония? Смогу ли еще иметь детей? Эти вопросы беспокоят всех пациенток, перенесших эту патологию. К счастью, в большинстве случаев состояние не повторяется, женщине в последующем удается благополучно забеременеть и выносить ребенка. Но при этом ее относят к группе риска по возможному развитию осложнений беременности и родов. Поэтому в первом триместре ей обычно назначается динамический УЗИ-контроль развития плодного яйца, определение гормонального профиля и оценка состояния системы гемостаза.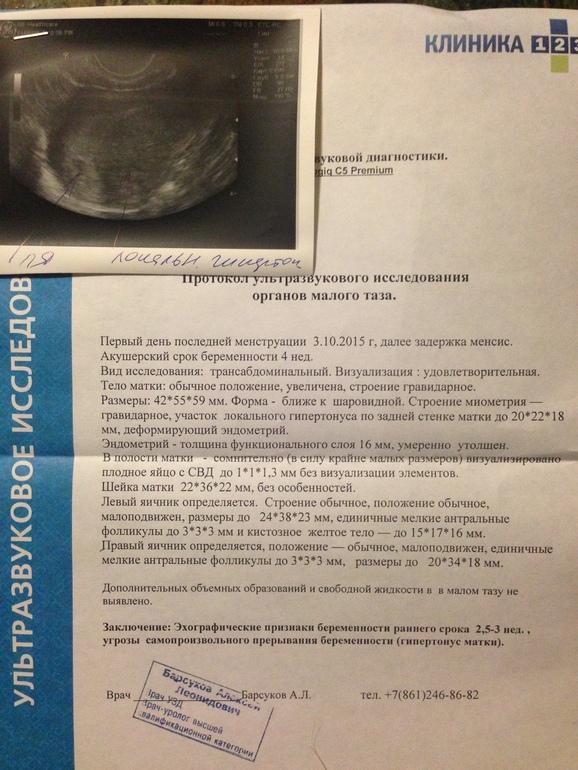
Беременность после анэмбрионии теоретически возможна уже в следующем овариально-менструальном цикле. Но желательно дать организму восстановиться. Поэтому планирование повторного зачатия рекомендуют начинать не ранее, чем через 3 месяца после проведенного искусственного аборта. Если же он протекал с осложнениями, реабилитационный период с соблюдением репродуктивного покоя продлевают на срок до полугода. При выявлении у женщины хронического эндометрита и различных инфекций, через 2 месяца после завершения лечения проводят контрольное обследование и лишь тогда определяют возможные сроки повторного зачатия.
Для предупреждения наступления беременности предпочтение отдают барьерному методу и гормональной контрацепции. Подбор средства при этом осуществляется индивидуально. Внутриматочные спирали сразу после перенесенной замершей беременности не используют во избежание развития эндометрита.
Профилактика
Первичная профилактика анэмбрионии включает тщательное планирование беременности с проведением комплексного обследования. При выявлении отклонений проводится их коррекция. Конечно, такая подготовка не позволяет на 100% исключить вероятность патологии, но снижает риск ее развития.
При выявлении отклонений проводится их коррекция. Конечно, такая подготовка не позволяет на 100% исключить вероятность патологии, но снижает риск ее развития.
Вторичная профилактика проводится при наличии у женщины в анамнезе самопроизвольных абортов и анэмбрионии. Первая беременность с синдромом пустого плодного яйца – повод для последующего обследования женщины на инфекции и нарушения гемостаза. При повторении ситуации показано проведение также генетического обследования супругов для исключения у них аномалий наследственного материала. В некоторых случаях последующее зачатие предпочтительно проводить с помощью ЭКО, что позволит использовать преимплантационную диагностику для выявления у эмбрионов хромосомных нарушений.
Анэмбриония диагностируется достаточно часто. И, к сожалению, в настоящее время пока не удается полностью исключить такую патологию уже на этапе планирования беременности. Ведь она может развиться даже у полностью здоровых и обследованных пациенток. При этом перенесенная замершая беременность не означает невозможность повторного успешного зачатия, большинству женщин после анэмбрионии удается благополучно родить здорового ребенка.
Ультразвуковая диагностика беременности малого срока — 22 ответов на Babyblog
Ультразвуковая диагностика беременности малого срока
Автор: ® Барто Р.А., 2012
При использовании трансвагинального датчика плодное яйцо диаметром 1 мм визуализируется в полости матки через 4 недели и примерно 2 дня после последней менструации при регулярном менструальном цикле. Трансвагинальное ультразвуковое исследование позволяет визуализировать ранние зародышевые структуры на 1 неделю раньше, чем трансабдоминальное УЗИ.
При задержке менструации 5-7 дней и более (срок беременности не менее 5 недель) в полости матки должно четко определяться плодное яйцо. Оно имеет четкую округлую форму с нечетким светлым венчиком по периферии (гиперэхогенный ободок). При этом уровень бета-ХГЧ крови составляет 1000-1500 МЕ/л. При меньшем уровне ХГЧ крови плодное яйцо в полости матки при трансвагинальной эхографии может не определяться. При трансабдоминальном исследовании определение плодного яйца в полости матки возможно при уровне бета-ХГЧ 3000-5000 МЕ/л.
Рис.1 Маточная беременность 4-5 недель.
Примерно с 5,5 недель при трансвагинальном УЗИ в плодном яйце начинает визуализироваться экстраэмбриональная структура — желточный мешок (анг. yolk sac). При этом уровень бета-ХГЧ примерно составляет в среднем 7200 МЕ/л. Поскольку желточный мешок является частью зародышевых структур, его обнаружение позволяет отличить плодное яйцо от простого скопления жидкости в полости матки между листками эндометрия, и в большинстве случаев, дает возможность исключить внематочную беременность. Частота эктопической беременности составляет 1 на 2000 — 3000 беременностей. Риск ее повышается при применении вспомогательных репродуктивных технологий (ВРТ).
Рис.2 Беременность 5,5 недель. Определяется желточный мешок.
С 6 недель беременности (иногда чуть раньше) в плодном яйце можно определить эмбрион, длиной около 3 мм. С этого же срока большинство ультразвуковых аппаратов позволяет определить сердцебиение эмбриона. Если сердцебиение не определяется или нечеткое при длине эмбриона (КТР) 5 мм, показано повторное УЗИ через неделю.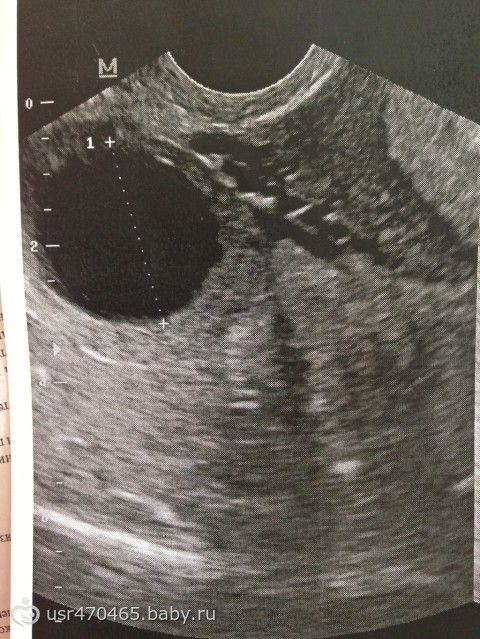 Отсутствие сердечной активности в этом сроке не обязательно является признаком страдания плода или неразвивающейся беременности.
Отсутствие сердечной активности в этом сроке не обязательно является признаком страдания плода или неразвивающейся беременности.
При нормальном течении беременности диаметр плодного яйца увеличивается на 1 мм в сутки. Меньшие темпы роста являются плохим прогностическим признаком. При сроке беременности 6-7 недель диаметр плодного яйца должен быть около 30 мм.
Диагноз анэмбрионии (пустое плодное яйцо) предполагается, если в плодном яйце размером 20 мм не определяется желточный мешок. Или если плодное яйцо диаметром более 25 мм с желточным мешком не содержит эмбриона. А также при размере желточного мешка 10 мм и более. В любом случае при подозрении на анэмбрионию все полученные данные следует трактовать в пользу беременности, и повторить исследование через 7 дней.
Диагноз неразвивающейся беременности не должен выставляться, если при УЗИ плодное яйцо имеет размер меньше 20 мм. При длине эмбриона 5 мм и более в большинстве случаев должно четко определяться сердцебиение.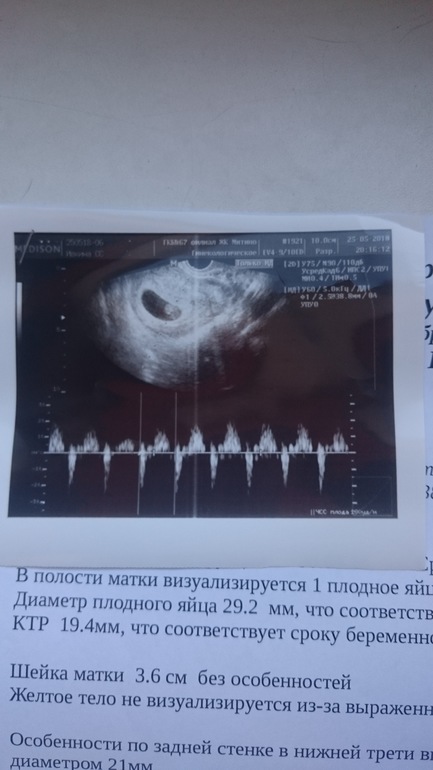 Если эмбрион менее 5 мм, следует повторить УЗИ через неделю. Если при повторном исследовании через неделю при КТР 5-6 мм сердечная деятельность не определяется, беременность является нежизнеспособной. Диагноз неразвивающейся беременности может быть подтвержден по несоответствию уровня бета-ХГЧ эхографическим данным.
Если эмбрион менее 5 мм, следует повторить УЗИ через неделю. Если при повторном исследовании через неделю при КТР 5-6 мм сердечная деятельность не определяется, беременность является нежизнеспособной. Диагноз неразвивающейся беременности может быть подтвержден по несоответствию уровня бета-ХГЧ эхографическим данным.
Следует отметить, что частота прерывания беременности в норме в популяции составляет 15-20% от всех клинически диагностированных беременностей. Однако в действительности, если считать все «химически» диагностированные беременности, определенные по уровню бета-ХГЧ до срока ожидаемых очередных месячных, частота выкидышей может достигать до 60%.
Неразвивающаяся беременность: проблема предгравидарной подготовки и снижения репродуктивных потерь
Невынашивание беременности — проблема, значение которой не только не уменьшается со временем, но, пожалуй, даже возрастает. Население Европы в целом и России в частности достаточно быстро стареет.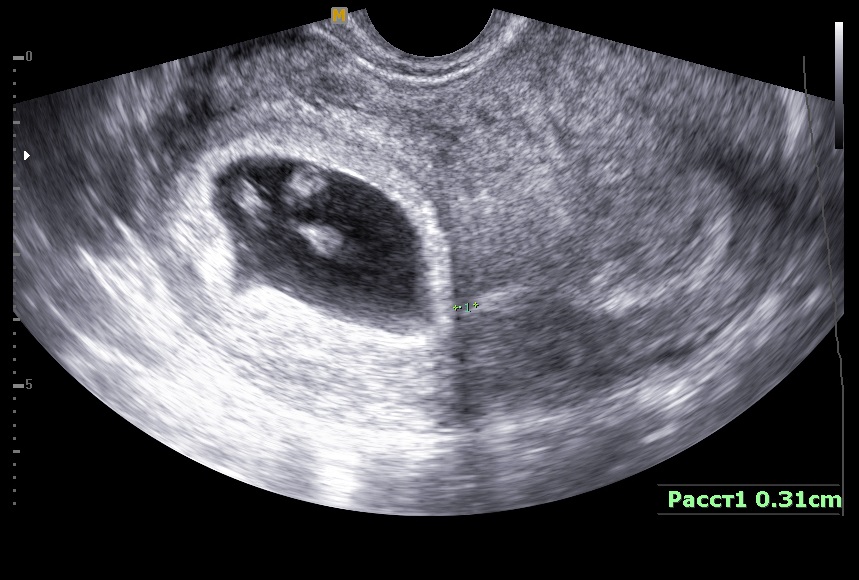 К 2015 г. 46 % женщин будут старше 45 лет [1–3]. При этом если в высокоразвитых странах возрастная разница между средней продолжительностью жизни мужчин и женщин составляет 4–5 лет, то в России в последние годы — 12–14 лет. Таким образом, Россия медленно превращается в страну пожилых одиноких женщин [4].
К 2015 г. 46 % женщин будут старше 45 лет [1–3]. При этом если в высокоразвитых странах возрастная разница между средней продолжительностью жизни мужчин и женщин составляет 4–5 лет, то в России в последние годы — 12–14 лет. Таким образом, Россия медленно превращается в страну пожилых одиноких женщин [4].
В настоящее время, по официальным данным, в России женщины составляют 53 % населения [5]. Из них только 45,7 % (36 млн) находятся в репродуктивном возрасте. Причем поскольку под репродуктивным статистики понимают возрастной диапазон от 15 до 49 лет [5], реальное число женщин, находящихся в активном репродуктивном возрасте, значительно меньше. При этом, по данным Министерства здравоохранения и социального развития РФ за 2004 г., нормальные роды составили лишь 31,2 % [6]. И ситуация вряд ли будет улучшаться, поскольку в первые десятилетия нового века в активную фазу репродукции вступает популяция женщин, имеющая серьезные проблемы с репродуктивным здоровьем [7].
Среди различных форм невынашивания беременности особое место занимает несостоявшийся выкидыш (missed abortion), т.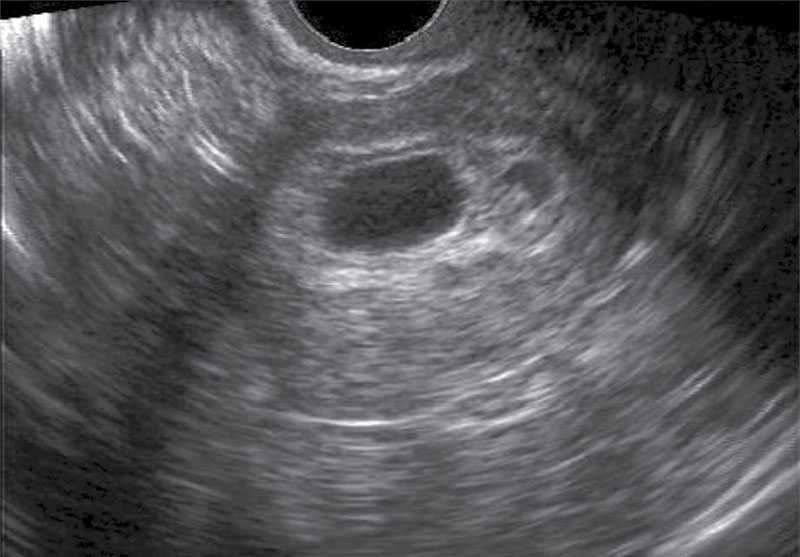 е. гибель эмбриона или плода в раннем сроке с длительной задержкой его в полости матки — неразвивающаяся беременность (НБ).
е. гибель эмбриона или плода в раннем сроке с длительной задержкой его в полости матки — неразвивающаяся беременность (НБ).
В МКБ-10 (1995) введена специальная рубрика «Беременность с абортивным исходом», где выделены формулировка и код отдельных форм ранней патологии беременности. Согласно данной классификации, погибшее плодное яйцо (анэмбриония) (син.: blighted ovum, anembryonic pregnancy, empty sac) представляет собой пустой зародышевый мешок вследствие аплазии или ранней резорбции эмбриобласта. Несостоявшийся выкидыш (missed abortion) — ранняя внутриутробная гибель и задержка плода в полости матки. В научной отечественной литературе в качестве синонимов данных терминов используются понятия «неразвивающаяся» или «замершая беременность».
Удельный вес данной патологии в структуре репродуктивных потерь довольно высок: 10–20 % [8]. В 1847 г. H. Oldham и A. MacClintok впервые для описания внутриутробной гибели плода без его элиминации из полости матки в сроке беременности более 6–7 мес.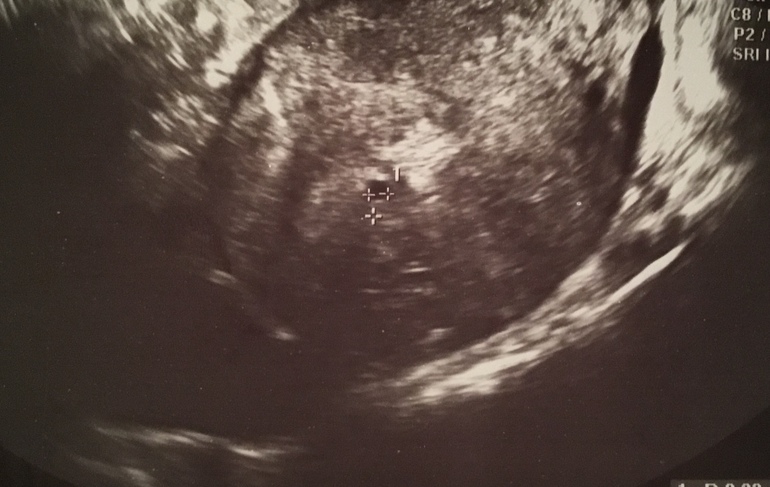 применили термин missed labour, а в 1872 г. был предложен другой термин — missed abortion, используемый акушерами-гинекологами до настоящего времени для обозначения аналогичной ситуации, при которой гестационный срок был менее 6–7 нед. [1]. Внутриутробная задержка погибшего плода или эмбриона является основной причиной возникновения синдрома мертвого плода. Это патологическое состояние, характеризующееся угнетением сократительной деятельности матки и гемостазиологическими нарушениями в организме матери [9–11]. Как правило, в I триместре в 75 % случаев сначала происходит гибель эмбриона и только потом могут наблюдаться явления угрозы прерывания беременности или выкидыш. Для НБ характерно отсутствие каких-либо пролиферативных и метаболических процессов с участием клеточно-тканевых элементов плодного пузыря в связи с их далеко зашедшими дистрофическими и некробиотическими изменениями. Данная ситуация усугубляется ареактивностью матки, которая не отторгает погибший плод. Характерным клиническим признаком замершей беременности является стертая картина субъективных проявлений нарушения беременности на фоне стабилизации размеров матки и их несоответствия сроку беременности.
применили термин missed labour, а в 1872 г. был предложен другой термин — missed abortion, используемый акушерами-гинекологами до настоящего времени для обозначения аналогичной ситуации, при которой гестационный срок был менее 6–7 нед. [1]. Внутриутробная задержка погибшего плода или эмбриона является основной причиной возникновения синдрома мертвого плода. Это патологическое состояние, характеризующееся угнетением сократительной деятельности матки и гемостазиологическими нарушениями в организме матери [9–11]. Как правило, в I триместре в 75 % случаев сначала происходит гибель эмбриона и только потом могут наблюдаться явления угрозы прерывания беременности или выкидыш. Для НБ характерно отсутствие каких-либо пролиферативных и метаболических процессов с участием клеточно-тканевых элементов плодного пузыря в связи с их далеко зашедшими дистрофическими и некробиотическими изменениями. Данная ситуация усугубляется ареактивностью матки, которая не отторгает погибший плод. Характерным клиническим признаком замершей беременности является стертая картина субъективных проявлений нарушения беременности на фоне стабилизации размеров матки и их несоответствия сроку беременности.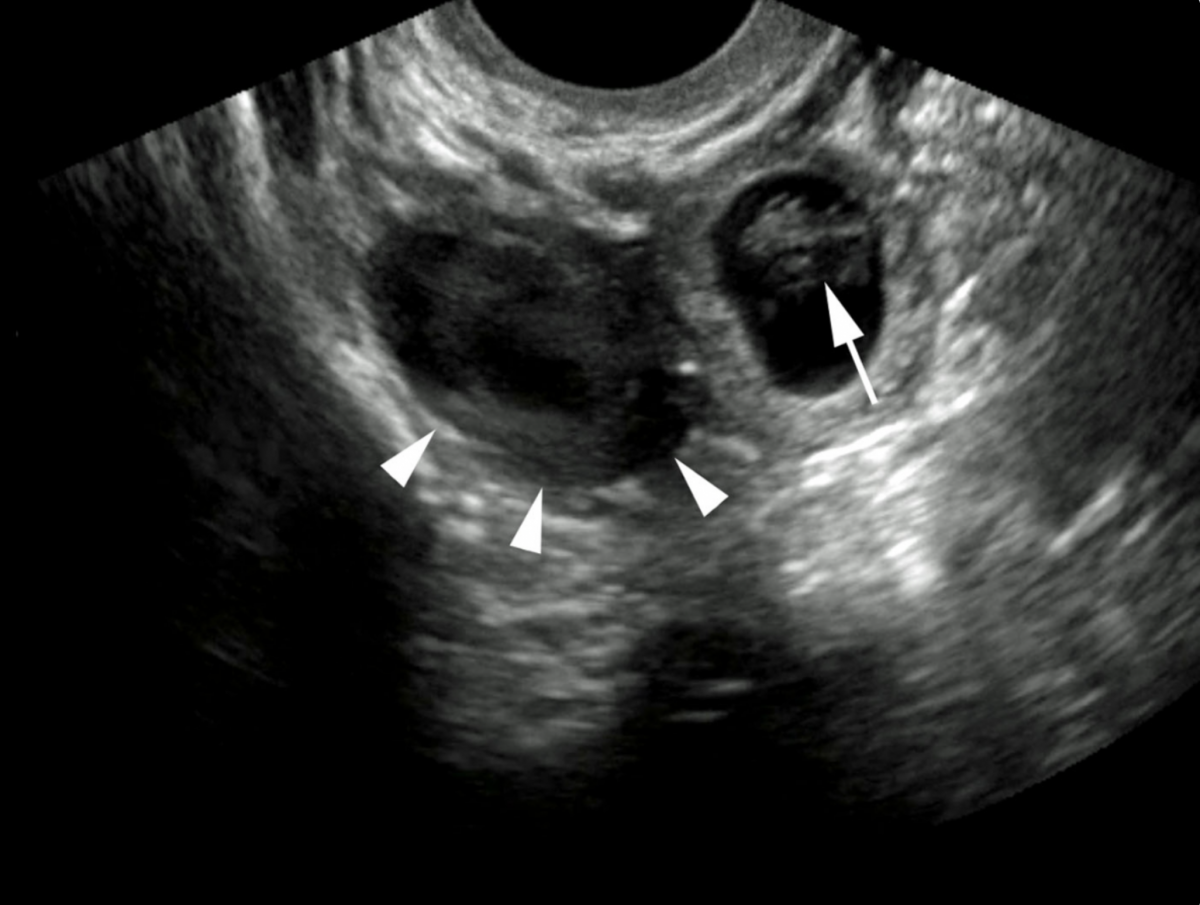
Причины замершей беременности многочисленны и нередко комплексны. В повседневной практике часто бывает трудно установить конкретный фактор, приведший к данной патологии, так как этому мешает мацерация тканей после смерти плода, что затрудняет их генетическое и морфологическое исследование.
Хромосомные аномалии у партнеров — пожалуй, единственная не вызывающая сомнений причина НБ. Гибель эмбриона может быть обусловлена патологическим развитием зиготы, эмбриона, плода или структурными нарушениями в генетической программе развития плаценты [1, 2, 12].
Особая роль в этиологии НБ принадлежит хромосомным аберрациям [3–5]. Основное число эмбрионов с аберрантным кариотипом гибнет в первые недели беременности. Так, в первые 6–7 нед. беременности аномальный кариотип имеют 60–75 % абортусов, в 12–17 нед. — 20–25 %, в 17–28 нед. — только 2–7 %. Среди хромосомных аберраций у абортусов 45–55 % составляют аутосомные трисомии, 20–30 % — моносомия 45ХО, 15–20 % — триплоидия и 5 % — тетраплоидия. Аутосомная трисомия ответственна более чем за половину патологических кариотипов. При этом, как правило, эмбрион отсутствует или имеет множественные пороки развития; хорионическая полость пустая и маленькая [13]. Большинство аутосомных трисомий являются результатом отсутствия расхождения хромосом во время первого митотического деления овоцита, причем частота этого явления возрастает с возрастом матери. Следует отметить, что возраст матери не имеет решающего значения для других хромосомных аномалий, являющихся причиной остановки развития беременности [14]. В 20–25 % наблюдений с патологией кариотипа имеет место моносомия. Моносомия Х вызывает аплазию эмбриона, от которого нередко сохраняется лишь остаток пуповинного тяжа, или же сохранившийся эмбрион находится в состоянии выраженной водянки [13, 14]. При моносомии 98 % беременностей заканчиваются выкидышем и только 2 % — родами ребенка с синдромом Тернера [14]. Триплоидия и тетраплоидия встречаются с умеренной частотой, но те случаи триплоидии, при которых имеет место двойной родительский компонент, обычно приводят к частичному пузырному заносу, клинически проявляющемуся в более поздние сроки беременности.
Аутосомная трисомия ответственна более чем за половину патологических кариотипов. При этом, как правило, эмбрион отсутствует или имеет множественные пороки развития; хорионическая полость пустая и маленькая [13]. Большинство аутосомных трисомий являются результатом отсутствия расхождения хромосом во время первого митотического деления овоцита, причем частота этого явления возрастает с возрастом матери. Следует отметить, что возраст матери не имеет решающего значения для других хромосомных аномалий, являющихся причиной остановки развития беременности [14]. В 20–25 % наблюдений с патологией кариотипа имеет место моносомия. Моносомия Х вызывает аплазию эмбриона, от которого нередко сохраняется лишь остаток пуповинного тяжа, или же сохранившийся эмбрион находится в состоянии выраженной водянки [13, 14]. При моносомии 98 % беременностей заканчиваются выкидышем и только 2 % — родами ребенка с синдромом Тернера [14]. Триплоидия и тетраплоидия встречаются с умеренной частотой, но те случаи триплоидии, при которых имеет место двойной родительский компонент, обычно приводят к частичному пузырному заносу, клинически проявляющемуся в более поздние сроки беременности. Важной структурной патологией хромосом является транслокация (2–10 %), которая может передаваться одним из родителей — сбалансированным носителем. Сбалансированную (компенсированную) транслокацию следует подозревать в тех случаях, когда в анамнезе у супругов есть указания на повторные неразвивающиеся беременности или самопроизвольные выкидыши. Среди прочих видов нарушений кариотипа — различные формы мозаицизма, двойные трисомии и другая редкая патология. Хромосомная патология человека зависит не только от интенсивности мутационного процесса, но и от эффективности отбора. С возрастом отбор ослабевает, поэтому чаще встречаются аномалии развития [13, 14].
Важной структурной патологией хромосом является транслокация (2–10 %), которая может передаваться одним из родителей — сбалансированным носителем. Сбалансированную (компенсированную) транслокацию следует подозревать в тех случаях, когда в анамнезе у супругов есть указания на повторные неразвивающиеся беременности или самопроизвольные выкидыши. Среди прочих видов нарушений кариотипа — различные формы мозаицизма, двойные трисомии и другая редкая патология. Хромосомная патология человека зависит не только от интенсивности мутационного процесса, но и от эффективности отбора. С возрастом отбор ослабевает, поэтому чаще встречаются аномалии развития [13, 14].
В эндометрии увеличивается процент классических естественных киллеров (ЕК) (СD16+) [15]. В децидуальной ткани также увеличивается содержание активированных цитотоксических ЕК (CD57+), продуцирующих эмбриотоксические цитокины, и уменьшается число клеток, продуцирующих трансформирующий фактор роста b2 (ТФР-b2), оказывающий иммуносупрессивное действие [16]. Предполагается, что изменения в субпопуляции клеток СD56+ являются одним из основных механизмов выкидыша с нормальным генотипом [17]. Эндометрий женщин, которые не имели повторных выкидышей, продуцирует Th3 (цитокины ИЛ-4 и ИЛ-6), тогда как цитокины, продуцируемые Th2 (типа ИЛ-2, ИЛ‑12 и ИФН-g), преобладают в эндометрии женщин, страдающих привычным невынашиванием неясной этиологии [18]. Приблизительно у 25 % женщин с необъяснимым привычным выкидышем обнаружено усиление иммунного и воспалительного ответов на трофобластические антигены [19] и преимущественная секреция эмбриотоксических цитокинов Th2 [20]. S. Ho и соавт. [21] показали, что провоспалительные цитокины (ИФН-g и ФНО-a) стимулируют апоптоз ворсинчатого цитотрофобласта. ИЛ-2 может повреждать трофобласт, способствуя превращению ЕК в лимфокинактивированные киллеры. ИФН-g активирует макрофаги к продукции ФНО-a и ИЛ-12, которые, в свою очередь, стимулируют ЕК. Синтезированный макрофагами ИЛ-1 активирует Т-клетки и способствует дальнейшей продукции цитокинов (цитокиновый каскад) моноцитами, макрофагами и эпителиальными клетками.
Предполагается, что изменения в субпопуляции клеток СD56+ являются одним из основных механизмов выкидыша с нормальным генотипом [17]. Эндометрий женщин, которые не имели повторных выкидышей, продуцирует Th3 (цитокины ИЛ-4 и ИЛ-6), тогда как цитокины, продуцируемые Th2 (типа ИЛ-2, ИЛ‑12 и ИФН-g), преобладают в эндометрии женщин, страдающих привычным невынашиванием неясной этиологии [18]. Приблизительно у 25 % женщин с необъяснимым привычным выкидышем обнаружено усиление иммунного и воспалительного ответов на трофобластические антигены [19] и преимущественная секреция эмбриотоксических цитокинов Th2 [20]. S. Ho и соавт. [21] показали, что провоспалительные цитокины (ИФН-g и ФНО-a) стимулируют апоптоз ворсинчатого цитотрофобласта. ИЛ-2 может повреждать трофобласт, способствуя превращению ЕК в лимфокинактивированные киллеры. ИФН-g активирует макрофаги к продукции ФНО-a и ИЛ-12, которые, в свою очередь, стимулируют ЕК. Синтезированный макрофагами ИЛ-1 активирует Т-клетки и способствует дальнейшей продукции цитокинов (цитокиновый каскад) моноцитами, макрофагами и эпителиальными клетками. Активированные макрофаги могут продуцировать NO, токсичный для трофобласта. Однако остается неясным, действительно ли ЕК или макрофаги оказывают цитотоксическое действие на клетки трофобласта [22]. Мишенями для макрофагов и ЕК являются скорее клетки эндотелия, чем трофобласт. Высокие уровни ИЛ-1, ИФН-g и ФНО-a активируют свертывание крови, которой снабжается развивающийся эмбрион [23].
Активированные макрофаги могут продуцировать NO, токсичный для трофобласта. Однако остается неясным, действительно ли ЕК или макрофаги оказывают цитотоксическое действие на клетки трофобласта [22]. Мишенями для макрофагов и ЕК являются скорее клетки эндотелия, чем трофобласт. Высокие уровни ИЛ-1, ИФН-g и ФНО-a активируют свертывание крови, которой снабжается развивающийся эмбрион [23].
Цитокиновый каскад может быть запущен не только инфекционным агентом, но и эндогенными причинами (гипоксия, гормоны и др.). Среди причин замершей беременности следует выделить эндокринные факторы — нарушение образования и гипофункцию желтого тела, связанную с дефицитом прогестерона и слабой децидуализацией стромы эндометрия. Недостаточность первой волны инвазии цитотрофобласта нередко сочетается с хромосомными аномалиями, что является следствием дефекта ответственного за этот процесс гена либо нарушения общей генетической программы развития эмбриона и плаценты [1].
Не при всех эндокринных заболеваниях наблюдается внутриутробная гибель эмбриона (плода). Гиперандрогения (синдром Штейна — Левенталя, адреногенитальный синдром), гипо- и гиперфункция щитовидной железы способствуют недостаточной подготовке эндометрия к беременности и неполноценной имплантации плодного яйца, что требует проведения специфической гормональной коррекции. Нередко гибель эмбриона (плода) возникает при наличии сахарного диабета у матери, что диктует необходимость подготовки к планируемой беременности [24].
Гиперандрогения (синдром Штейна — Левенталя, адреногенитальный синдром), гипо- и гиперфункция щитовидной железы способствуют недостаточной подготовке эндометрия к беременности и неполноценной имплантации плодного яйца, что требует проведения специфической гормональной коррекции. Нередко гибель эмбриона (плода) возникает при наличии сахарного диабета у матери, что диктует необходимость подготовки к планируемой беременности [24].
Одним из вариантов аутоиммунных нарушений является антифосфолипидный синдром (АФС). В I триместре беременности обсуждается роль прямого повреждающего воздействия антифосфолипидных антител на ткань трофобласта с последующим спонтанным прерыванием беременности. Антифосфолипидные антитела изменяют адгезивные характеристики предимплантационной морулы (заряд), усиливают протромботические механизмы и десинхронизируют процессы фибринолиза и фибринообразования, что приводит к дефектам имплантации и снижению глубины децидуальной инвазии трофобласта. Антифосфолипидные антитела напрямую взаимодействуют с синци- тиотрофобластом и цитотрофобластом и ингибируют межклеточное слияние клеток трофобласта. Кроме того, антифосфолипидные антитела подавляют продукцию хорионического гонадотропина и усиливают тромботические тенденции за счет предоставления матриц для реакций свертывания.
Кроме того, антифосфолипидные антитела подавляют продукцию хорионического гонадотропина и усиливают тромботические тенденции за счет предоставления матриц для реакций свертывания.
Для АФС характерна гибель плода после 10 недель беременности. Наличие высокого уровня антител нарушает нормальное формирование синцитиотрофобласта и приводит к прерыванию беременности [12, 25]. При НБ в 13 % случаев в соскобе со стенок полости матки преобладали морфологические изменения: тяжелые реологические нарушения по типу ретроплацентарной гематомы, расслаивающие кровоизлияния с различной давностью их образования [26]. У пациенток с АФС и неблагоприятным исходом беременности отмечено более высокое содержание Т-лимфоцитов, активированных CD8+, В-лимфоцитов и цитотоксических клеток CD57+ и CD16+ [27]. Установлено, что факторами риска развития НБ являются ранний возраст начала половой жизни, воспалительные заболевания гениталий, высокая частота абортов, внутриматочная контрацепция [1, 2].
Другие факторы, приводящие к внутриутробной гибели эмбриона (плода). Лишь 10 % случаев раннего прерывания беременности связаны с заболеваниями матери, например с острой инфекцией. Чаще хронические инфекционные заболевания матери не ведут к внутриутробной гибели плода, но вызывают фетопатии, способствующие внутриутробной смерти под влиянием других факторов. Весьма наглядным в этом плане примером являются пороки сердца.
Лишь 10 % случаев раннего прерывания беременности связаны с заболеваниями матери, например с острой инфекцией. Чаще хронические инфекционные заболевания матери не ведут к внутриутробной гибели плода, но вызывают фетопатии, способствующие внутриутробной смерти под влиянием других факторов. Весьма наглядным в этом плане примером являются пороки сердца.
По данным Н.М. Подзолковой и соавт. [27], у 52,5 % пациенток с неразвивающейся беременностью, согласно результатам полимеразной цепной реакции, выявлена смешанная вирусно-бактериальная флора, в 20 % случаев — моноинфекция, а в остальных случаях — микст-инфекции. При анэмбрионии обнаружено сочетание вируса с мико- и уреаплазмами (42,8 %), гонококками (33,3 %), хламидиями (23,8 %). Отмечается преобладание герпесвирусной инфекции (28 %) над цитомегаловирусной (10,5 %). Обнаружены мико- и уреа- плазмы — 36,6 %, хламидии — 33,3 %, гонококки — 17,5 %, трихомонады — 7 %. Хламидийная инфекция определялась у 51,6–57,1 % пациенток с невынашиванием беременности [28].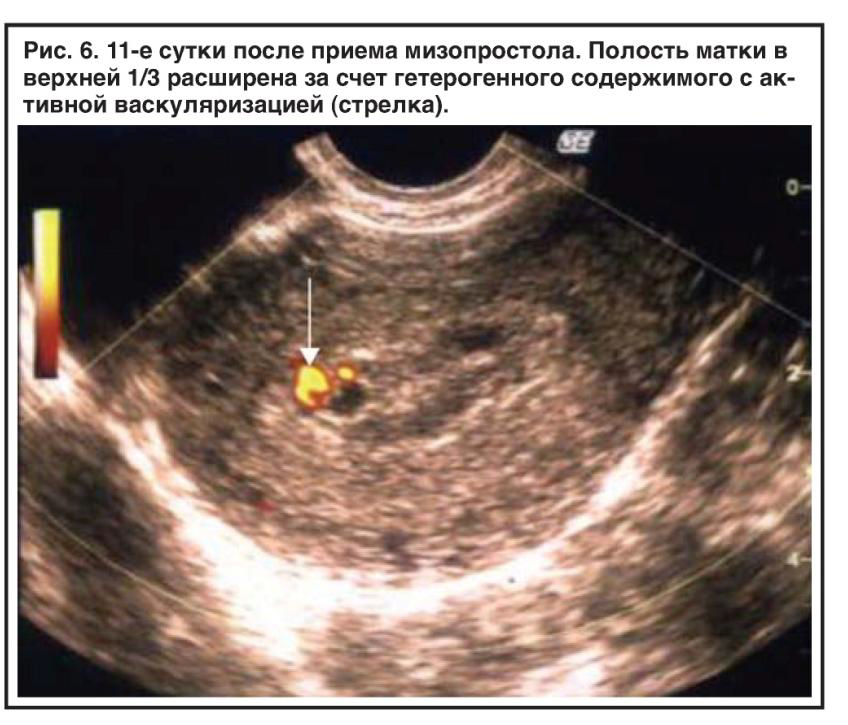
В исследованиях Е.Н. Зарубиной и Е.Н. Фомичевой [29] частота хламидиоза у женщин с привычным невынашиванием была в 2–3 раза выше, чем в общей популяции.
В работах K. Ault и соавт. [30] сообщается о действии хламидий через воспалительные цитокины. У 62,5 % беременных с привычным невынашиванием и НБ в анамнезе обнаружены специфические анти-ЦМВ — иммуноглобулины класса IgM [26, 31]. Особенностью этой инфекции является то, что антитела не предотвращают реактивацию, так же как и при цитомегаловирусной инфекции. У пациенток с прерыванием по типу неразвивающейся беременности хронический эндометрит обусловлен персистенцией вирусов (вирус простого герпеса, цитомегаловирус и др.). Не менее интересна этиологическая связь невынашивания беременности с хронической формой Коксаки-вирусной инфекции. Основным звеном патогенеза этой инфекции считают тканевую гипоксию, показана связь энтеровирусов с развитием аутоиммунных заболеваний с гемостазиологическими изменениями: циркулирующие иммунные комплексы, присутствующие в кровотоке длительное время, вызывают изменения в сосудах, в том числе в плаценте [14].
Среди факторов, приводящих к перинатальной патологии и антенатальной гибели плода, возросла роль эндокринной патологии, в том числе гиперандрогении различного генеза [32–34, 36, 37]. Этиологическим фактором развития заболевания является генетически обусловленная, связанная с системой HLA неполноценность ферментных систем в коре надпочечников и/или яичников либо их одновременное нарушение, обусловленное единством эмбрионального происхождения (из единого зачатка целомического мезотелия). В результате наблюдается снижение уровня нормальных продуктов стероидогенеза и увеличение продукции андрогенов.
Формы гиперандрогении с преимущественным поражением надпочечников, яичников или обоих органов по существу представляют собой проявление клинического полиморфизма единой патологии, зависящей от длительности и глубины патологического процесса и имеющей одну первопричину — нарушение гипоталамо-гипофизарно-надпочечниково-яичниковых взаимоотношений на различных этапах развития женского организма [36].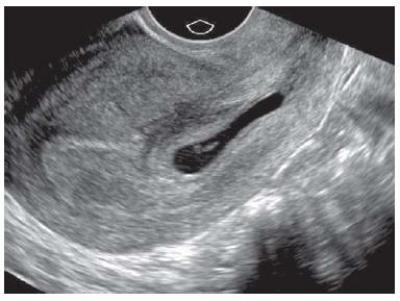
Одной из особенностей клинического проявления гиперандрогении является наличие так называемых стертых форм [38, 39]. Такая неклассическая ее форма присутствует почти у одного процента общей популяции [36]. Клинические проявления в этом случае отсутствуют или крайне незначительны. Частота патологии беременности при гиперандрогении, по данным различных авторов, составляет от 21 до 48 % [33, 35, 36]. По данным ряда авторов, среди гормональных причин прерывания беременности в I триместре основными являются гиперандрогения и гипофункция яичников [40, 41]. 21–32 % случаев невынашивания беременности обусловлены гиперандрогенией. Из них гиперандрогения надпочечникового происхождения — у 30 %, яичникового генеза — у 12,1 % и смешанного генеза — у 57,9 % женщин с НБ. По данным А.Т. Раисовой, В.Г. Орловой (1990) [42], среди женщин с явлениями гирсутизма в 6 раз чаще наблюдали ранние самопроизвольные выкидыши, в 10 раз — НБ. Повышение уровня андрогенов приводит, с одной стороны, к гибели зародыша непосредственно, а с другой стороны — к плацентарной недостаточности [40, 42].
Если оценивать чувствительность эмбриона и плода к повреждающим факторам, то можно сказать, что чем меньше срок беременности, тем эта чувствительность выше. Однако она уменьшается неравномерно на протяжении внутриутробного развития. Выделяют так называемые критические периоды в течении беременности, когда плодное яйцо, эмбрион, плод особенно уязвимы для неблагоприятных условий, в том числе лекарственных: период имплантации (7–12-й день), период эмбриогенеза (3–8-я неделя), период формирования плаценты (до 12 недель), период формирования важнейших функциональных систем плода (20–24-я неделя) [43].
При неразвивающейся беременности определяется стертая картина проявлений нарушения беременности на фоне стабилизации размеров матки и их несоответствия сроку гравидарной аменореи. Матка может иметь нормальные размеры, может быть уменьшена и даже увеличена в случае наличия в полости гематомы. Хорионический гонадотропин находится на предельно низком уровне или даже полностью отсутствует. Постепенно исчезают субъективные признаки беременности (хотя какое-то время после гибели эмбриона или плода пациентка может ощущать себя беременной), периодически отмечаются мажущие кровянистые выделения из половых путей, боли в животе спастического характера. Диагноз неразвивающейся беременности ставится на основании данных ультразвукового сканирования при отсутствии сердцебиения плода. При ультразвуковом исследовании устанавливается несколько вариантов НБ [1, 2, 14].
Постепенно исчезают субъективные признаки беременности (хотя какое-то время после гибели эмбриона или плода пациентка может ощущать себя беременной), периодически отмечаются мажущие кровянистые выделения из половых путей, боли в животе спастического характера. Диагноз неразвивающейся беременности ставится на основании данных ультразвукового сканирования при отсутствии сердцебиения плода. При ультразвуковом исследовании устанавливается несколько вариантов НБ [1, 2, 14].
Наиболее часто встречается анэмбриония, т.е. отсутствие эмбриона в полости плодного яйца после 7 недель беременности. Плодное яйцо имеет меньшие размеры, чем положено по предполагаемому гестационному возрасту, децидуальная оболочка имеет прерывистый контур, эмбрион не визуализируется или же плодное яйцо по размерам соответствует сроку гестации, эмбрион может визуализироваться, но очень маленьких размеров и без сердцебиения. Нередко имеет место ретрохориальная гематома. Если исследование проводится в сроки до 8 недель беременности, то необходимо провести повторное исследование через 7 дней.
Другая эхографическая картина неразвивающейся беременности — замерший плод, при котором визуализируется плодное яйцо и эмбрион обычной формы и размеров без признаков жизнедеятельности плода. При более длительном пребывании погибшего эмбриона в матке визуализация эмбриона невозможна, признаки его жизнедеятельности отсутствуют. Размеры матки отстают от срока беременности, структура плодного яйца резко изменена — отмечаются деформация, нечеткие контуры и форма плодного яйца, наличие множественных перетяжек и отдельных разрозненных эхоструктур.
При ультразвуковом исследовании можно выявить особую форму неразвивающейся беременности — многоплодие в ранние сроки. Нередко у таких женщин отмечается резорбция одного из эмбрионов при нормальном развитии другого. Чаще регресс плодного яйца происходит по типу анэмбрионии, реже — по типу внутриутробной гибели одного из плодов (при дихориальной двойне).
Дифференциальную диагностику при неразвивающейся беременности необходимо проводить с начавшимся самопроизвольным выкидышем и трофобластической болезнью.
Гибель эмбриона (плода) не всегда сопровождается быстрым самопроизвольным изгнанием из матки. Отсутствие каких-либо пролиферативных и метаболических процессов со стороны клеточно-тканевых элементов плодного пузыря в связи с их далеко зашедшими дистрофическими и некробиотическими изменениями усугубляется ареактивностью матки, которая не отторгает погибший плод. Часто наблюдаются случаи, когда погибшее плодное яйцо задерживается в матке на неопределенно долгое время.
Чаще всего происходит постепенное отторжение погибшего плодного яйца с помощью фибринозно-лейкоцитарной экссудативной реакции в ответ на некротизированную ткань. В ходе этого процесса наряду с фибрином и лейкоцитами из сосудов эндометрия выделяются трофобластические, тромбопластические субстанции, эритроциты, что ведет к постоянным мажущим кровянистым выделениям из матки. Тело матки становится мягким, тонус миометрия исчезает, шейка приоткрывается. Все признаки беременности (цианоз влагалища, шейки матки) исчезают.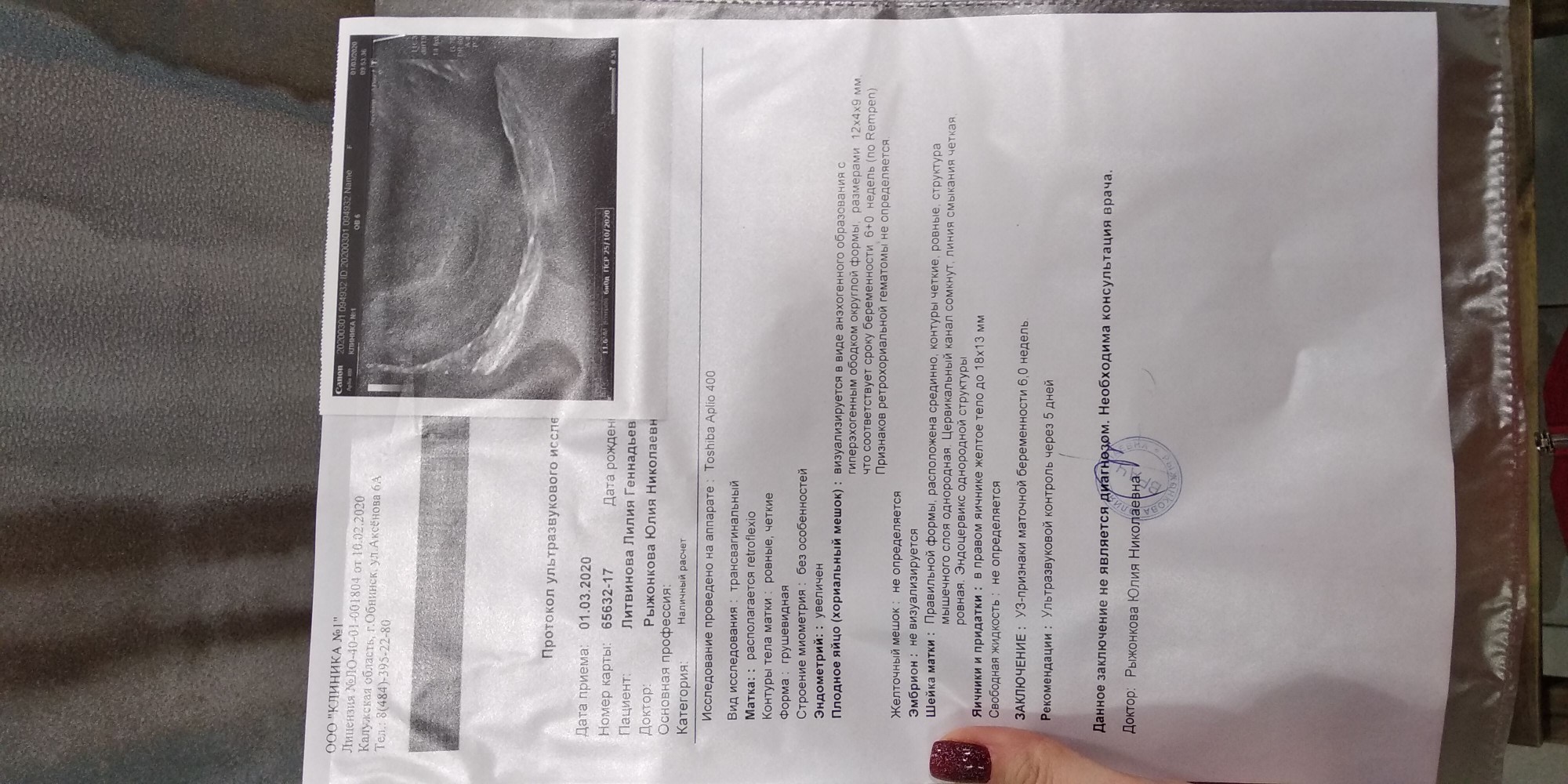
При длительном (2–4 недели и более) нахождении погибшего эмбриона в матке возникает аутолиз, в кровоток пациентки попадают тромбопластические субстанции и развивается ДВС-синдром. Все это является риском развития тяжелого коагулопатического кровотечения при попытке прерывания беременности.
Трудности, возникающие при удалении мертвого плода, могут быть обусловлены предлежанием хориона, плаценты, расположенных в области внутреннего зева матки. Перед выскабливанием матки необходимо исследовать состояние системы гемостаза (развернутая коагулограмма). При выявленных нарушениях (гиперагрегация, гиперкоагуляция, ДВС-синдром) необходима корригирующая терапия (свежезамороженная плазма и другие компоненты). Купированию гемостазиологических нарушений на уровне сосудисто-тромбоцитарного звена способствует применение дицинона и АТФ. В послеоперационном периоде показана антиагрегантная и антикоагулянтная терапия (трентал, курантил, фраксипарин). Энергетический потенциал матки восстанавливают назначением глюкозы, витаминов, хлорида кальция в сочетании со спазмолитическими препаратами.
Задержка погибшего эмбриона в полости матки представляет угрозу не только для здоровья, но и для жизни женщины, поэтому требует активной тактики. Как только поставлен диагноз неразвивающейся беременности, длительное консервативное ведение пациентки рискованно.
После тщательного обследования и соответствующей подготовки женщины (проведение лечебно-профилактических мероприятий, направленных на снижение риска развития возможных осложнений) необходимо прерывание замершей беременности.
В I триместре беременности:
1) расширение шейки матки и вакуумная аспирация;
2) подготовка шейки матки с помощью простагландинов или гидрофильных расширителей и вакуумная аспирация;
3) использование антипрогестагенов в сочетании с простагландинами.
Во II триместре беременности:
1) расширение шейки матки и эвакуация продуктов зачатия с предшествующей подготовкой шейки матки;
2) терапевтический аборт при помощи внутри- и экстраамниотического введения простагландинов или гипертонических агентов;
3) применение антипрогестагена в сочетании с простагландином, изолированное применение простагландинов.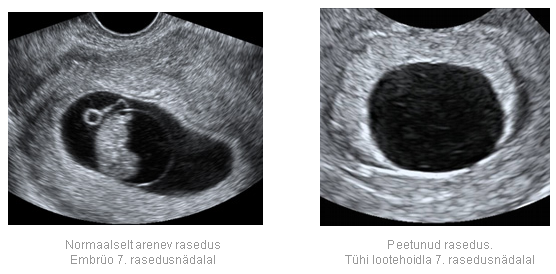
Непосредственно в ходе проведения аборта или сразу после его завершения необходимо выполнить ультразвуковое сканирование, чтобы убедиться в полном удалении частей плода и плаценты. После удаления плодного яйца при неразвивающейся беременности независимо от выбранного метода прерывания целесообразно комплексное противовоспалительное лечение, включая специфическую антибактериальную, иммунокорригирующую и общеукрепляющую терапию.
Каждый случай замершей беременности требует углубленного обследования в отношении генетической, эндокринной, иммунной и инфекционной патологии [44–54].
Тактика ведения пациенток с НБ в анамнезе [52–59]:
1. Выявление наиболее вероятных факторов гибели эмбриона (плода).
2. Проведение предгравидарной подготовки, направленной на устранение или ослабление действия выявленных факторов вне и во время беременности:
— обследование пациенток, планирующих беременность, а также женщин в ранние сроки гестации на урогенитальную инфекцию;
— проведение лечебно-профилактических мероприятий, направленных на ликвидацию инфекционного процесса, проведение специфической противовоспалительной терапии в сочетании с иммунокорректорами;
— анализ маркерных сывороточных белков a-фетопротеина, хорионического гонадотропина в крови в наиболее информативные сроки;
— генетическое консультирование женщин, направленное на выявление групп высокого риска по врожденной и наследственной патологии;
— гормональная терапия при эндокринном генезе замершей беременности;
— определение аутоиммунных нарушений (определение волчаночного антикоагулянта, анти-ХГ, антикардиолипиновых антител и др. ) и индивидуальный подбор антиагрегантов и/или антикоагулянтов и глюкокортикоидов под контролем гемостазиограмм.
) и индивидуальный подбор антиагрегантов и/или антикоагулянтов и глюкокортикоидов под контролем гемостазиограмм.
3. Нормализация психического состояния женщины (седативные средства, пропаганда здорового образа жизни — отказ от курения, алкоголя, наркотиков, отказ от беспорядочных половых связей).
Повторная беременность рекомендуется при устранении известных причин гибели эмбриона (плода) и после проведения противовоспалительной, общеукрепляющей и, по показаниям, гормональной терапии. Необходимо помнить, что особенно опасны повторные неразвивающиеся беременности, приводящие к расстройствам менструальной функции, нарушениям гормональной регуляции, воспалительным заболеваниям половых органов, нарушениям структуры эндометрия, к дисбалансу иммунной системы, прогрессирующему снижению репродуктивной функции, снижению демографических ресурсов. Несомненно, что даже после одной неразвившейся беременности наиважнейшими задачами акушеров-гинекологов являются проведение тщательного клинико-лабораторного обследования пациенток с использованием современных методов диагностики, включая исследование иммунного статуса (общего и локального), для выяснения этиологии и патогенеза неразвивающейся беременности, разработка и проведение эффективной комплексной терапии в предгравидарный период, наблюдение и профилактическое лечение в процессе наступившей беременности.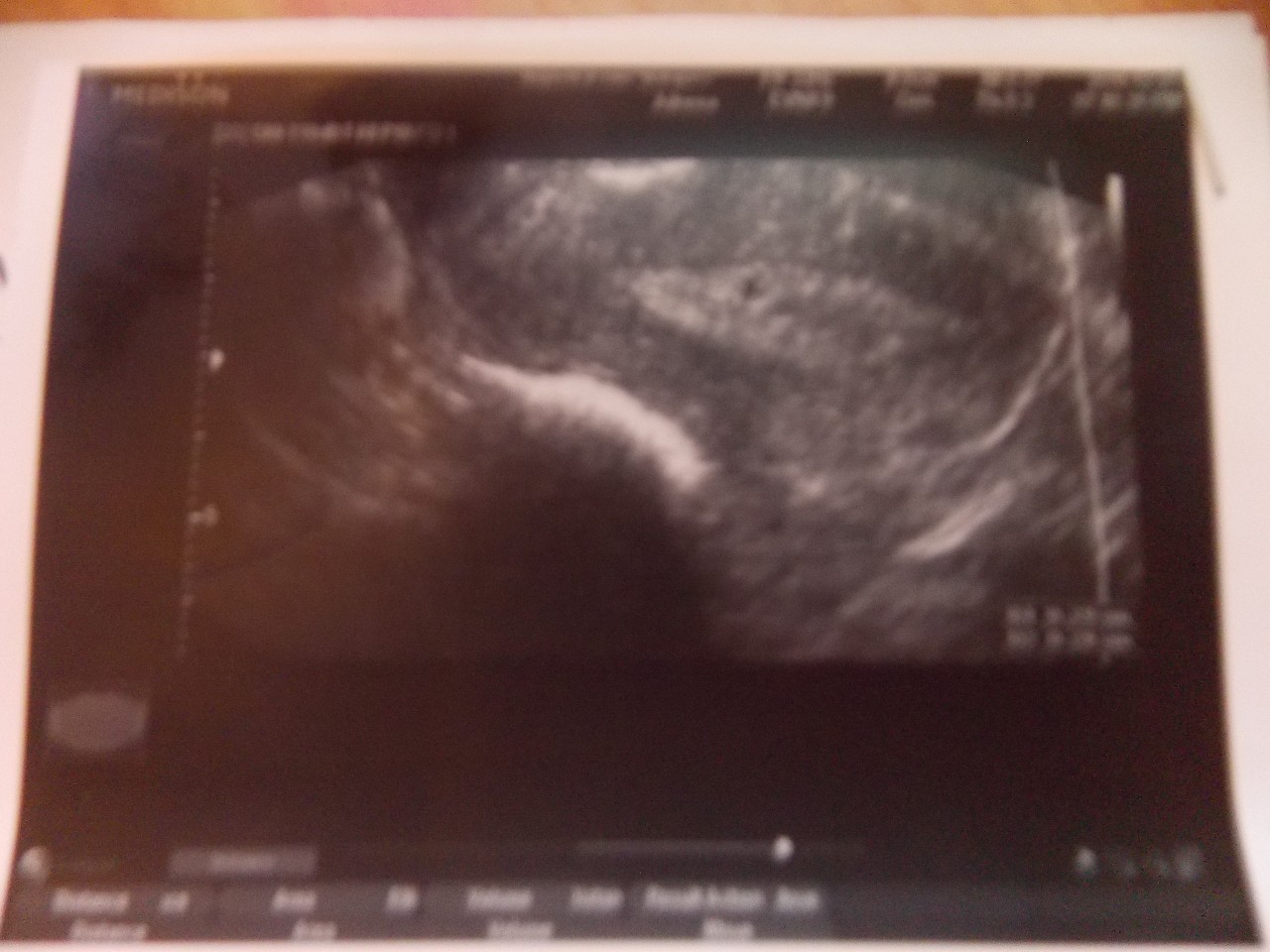
1. Салов И.А. Неразвивающаяся беременность (патогенез, клиника, диагностика, лечение): Автореф. дис… д-ра мед. наук. — Саратов, 1998. — 40 с.
2. Салов И.А., Маринушкин Д.И. Гемостазиологические нарушения при неразвивающейся беременности // Пробл. беременности. — 2000. — № 1. — С. 21-26.
3. Баранов И.И., Серов В.Н. Климактоплан в терапии климактерического синдрома // Русский медицинский журнал. — 2005. — 13. — 1. — 11-14.
4. Сметник В.П. Системные изменения у женщин в климактерии // Русский медицинский журнал. — 2001. — 9. — 9. — 358-361.
5. Кулаков В.И., Серов В.Н., Шарапова О.В., Кира Е.Ф. Этические и правовые аспекты акушерско-гинекологической помощи в современной России // Акуш. и гин. — 2005. — 5. — 3-8.
6. Радзинский В.Е., Запертова Е.Ю., Мисник В.В. Генетические и иммунологические аспекты привычного невынашивания беременности // Акуш. и гин. — 2005. — 6. — 24-29.
7. Ушакова Г.А., Елгина С.И., Назаренко М.Ю. Репродуктивное здоровье современной популяции девочек // Акуш. и гин. — 2006. — 1. — 34-39.
и гин. — 2006. — 1. — 34-39.
8. Доброхотова Ю.Э., Савченко Т.Н. Неразвивающаяся беременность: Учебно-методическое пособие / Под ред. О.В. Макарова. — М.: РГМУ, 2002. — 5-10.
9. Пестрикова Т.Ю. Невынашивание беременности: самопроизвольный аборт, преждевременные роды, неразвивающаяся беременность. Ведение беременности и родов высокого риска. — М.: Релакс, 1994. — 36-71.
10. Lawson H.W., Frye A., Atrach H.K. et al. // Am. J. Obstet. Gynec. — 1994. — 171. — 6. — 1365-1372.
11. Marinov B., Tsachev R., Ruseva R. et al. // Akush. Ginekol. — 1992. — 31. — 2. — 5-7.
12. Серова О.Ф., Милованов А.П. Основные патоморфологические причины неразвивающейся беременности и обоснование прегравидарной терапии женщин // Акуш. и гин. — 2001. — 3. — 19-23.
13. Глуховец Б.И., Глуховец Н.Г. Патоморфологическая диагностика ранних самопроизвольных выкидышей. — СПб., 1999.
14. Сидельникова В.М. Привычная потеря беременности. — М., 2002.
15. Lachapelle M.H., Miron P. // J. Immunol. — 1996. — 156. — 10. — 4027-4034.
// J. Immunol. — 1996. — 156. — 10. — 4027-4034.
16. Coulam C.B., Clark D.A. // Am. J. Reprod. Immunol. — 1997. — 37. — 4. — 279-282.
17. Clark G.F., Oehninger S. et al. // Hum. Reprod. — 1996. — 11. — 3. — 467-473.
18. Lim K.J., Odukoya O.A., Ajjan R.A. et al. // Mol. Hum. Reprod. — 1998. — 4. — 1. — 77-81.
19. Yamada H., Polgar K., Hill J. // Am. J. Obstet. Gynec. — 1994. — 170. — 1. — 13.
20. Hill J.A., Polgar K., Anderson D. // JAMA. — 1995. — 273. — 24. — 1933-1936.
21. Ho S., Winkler-Lowen B. et al. // Placenta. — 1999. — 20. — 5–6. — 423-430.
22. Baines M.G., Duclos A.J. et al. // Am. J. Reprod. Immunol. — 1997. — 37. — 6. — 471-477.
23. Clark D.A., Daya S. // Am. J. Reprod. Immunol. — 1998. — 39. — 65-68.
24. Вербовой А.Ф., Косарева О.В. Клиническая фармакология гипогликемизирующих препаратов. — Самара, 2007. — 70 с.
25. Пономарева И.В., Городничева Ж.А., Сухих Г.Т. и др. // Акуш. и гин. — 2000. — 2. — 12-15.
26. Сухих Г.Т., Ванько Л.В. Иммунология беременности. — М.: РАМН, 2003. — 400 с.
Сухих Г.Т., Ванько Л.В. Иммунология беременности. — М.: РАМН, 2003. — 400 с.
27. Подзолкова Н.М., Бархина Т.Г., Казачков А.Р. и др. Комплексное морфологическое изучение роли инфекционных процессов в этиологии и патогенезе неразвивающейся беременности // Мат-лы 5-го Рос. форума «Мать и дитя». — М., 2003. — 171.
28. Мещерякова А.В. Иммуноморфологические аспекты неразвивающейся беременности первого триместра: Автореф. дис… канд. мед. наук. — М., 2000. — 19.
29. Зарубина Е.Н., Фомичева Е.Н. Влияние урогенитального хламидиоза на течение и исход беременности и родов // Тез. докл. симпозиума «Новое в урологии, андрологии, дерматовенерологии: наука и практика». — Москва — Саратов: СГМУ, 1996. — 11-12.
30. Ault K.A., Taulik O.W. et al. // Am. J. Obstet. Gynec. — 1996. — 175. — 1242-1245.
31. Серов В.Н., Стрижаков А.Н., Маркин С.А. Руководство по практическому акушерству. — М.: МИА, 1997. — 435.
32. Комаров Е.К. Формы надпочечниковой гиперандрогении и значение корригирующей терапии в восстановлении нарушений репродуктивной функции у женщин // Вестник акушер. и гин. — 1997. — № 3. — С. 106-108.
и гин. — 1997. — № 3. — С. 106-108.
33. Лебедев А.С., Якунина Л.В. Истмико-цервикальная недостаточность у женщин с гиперандрогенемией // Проблемы эндокринол. в акуш. и гин.: Мат-лы II съезда Рос. ассоц. врачей акуш. и гин. — М.: Академия, 1997. — С. 69-70.
34. Мурашко Л.Е., Бадоева Ф.С. Перинатальные исходы при хронической плацентарной недостаточности // Акуш. и гин. — 1996. — № 4. — С. 43-45.
35. Орлова О.О. Течение беременности, родов и послеродового периода у женщин после медикаментозной коррекции гормональной недостаточности яичников: Автореф. дис… канд. мед. наук. — СПб., 1996. — С. 15-16.
36. Раисова А.Т. Актуальные проблемы гиперандрогении // Клиницист. — 1995. — № 3. — С. 54-55.
37. Руководство по эндокринной гинекологии / Под ред. Е.М. Вихляевой. — М.: Мед. информ. агентство, 1997. — С. 97-98.
38. Agarval S.К., Buyalos R.P. Corpus luteum function and pregnancy rates witch clomiphene citrate therapy: comparison of human chorionic gonadotrophin — induced versus spontaneous ovulation // Hum. Reprod. — 1995. — Vol. 10, № 2. — P. 328-330.
Reprod. — 1995. — Vol. 10, № 2. — P. 328-330.
39. Barth J.H. Investigations in the assessment and management of patiens witch hirsutism // Curr. Opion. Obstet. Gynec. — 1997. — Vol. 9, № 3. — Р. 187-189.
40. Раисова А.Т. Невынашивание беременности у женщин с гиперандрогенией // Акуш. и гинек. — 1991. — № 6. — С. 28-31.
41. Сидельникова В.М. Гормональные аспекты в клинике невынашивания // Русский медицинский журнал. — 2001. — Т.9, № 19. — С. 817-819.
42. Раисова А.Т., Орлова В.Г. Гиперандрогения в клинике невынашивания беременности // Профилактика, диагностика и лечение женщин с невынашиванием беременности и оказание помощи их детям: Сб. научн. трудов / Под ред. В.М. Сидельниковой. — М., 1990. — С. 35-39.
43. Косарев В.В., Бабанов С.А., Астахова А.В. Фармакология и лекарственная терапия: Справочник / Под ред. чл.-корр. РАМН В.К. Лепахина. — М.: Эксмо, 2009. — 470 с.
44. Вербовой А.Ф., Бабанов С.А., Косарева О.В., Агаркова И.А. Клиническая фармакология препаратов половых гормонов. — Самара: Офорт, 2009. — 60 с.
— Самара: Офорт, 2009. — 60 с.
45. Бакотина И.В. Клинико-морфологические особенности формирования хориона у пациенток с неразвивающейся беременностью: Дис… канд. мед. наук. — М., 2005. — С. 151.
46. Баркаган З.С., Сердюк Г.В. Невынашиваемость беременности и мертворождаемость при нарушениях в системе гемостаза // Гематология и трансфузиология. — 1991. — № 4. — С. 36-41.
47. Винницкий О.И. Вопросы диагностики, клиники, патогенеза неразвивающейся беременности: Автореф. дис… д-ра мед. наук. — Киев, 1988. — 34 с.
48. Вихляева Е.М., Богданова Е.А., Кондриков Н.И. Возрастная патология репродуктивной системы женщины // Акуш. и гинек. — 1994. — № 4. — С. 41-50.
49. Кирющенков П.А. Диагностика и дифференцированная коррекция синдрома диссеминированного внутрисосудистого свертывания крови у беременных с плацентарной недостаточностью: Автореф. дис… канд. мед. наук.— М., 1989. — 21 с.
50. Колесникова И.К. Состояние иммунитета на системном уровне и в эндометрии у женщин с невынашиванием беременности ранних сроков инфекционного и гормонального генеза: Дис… канд.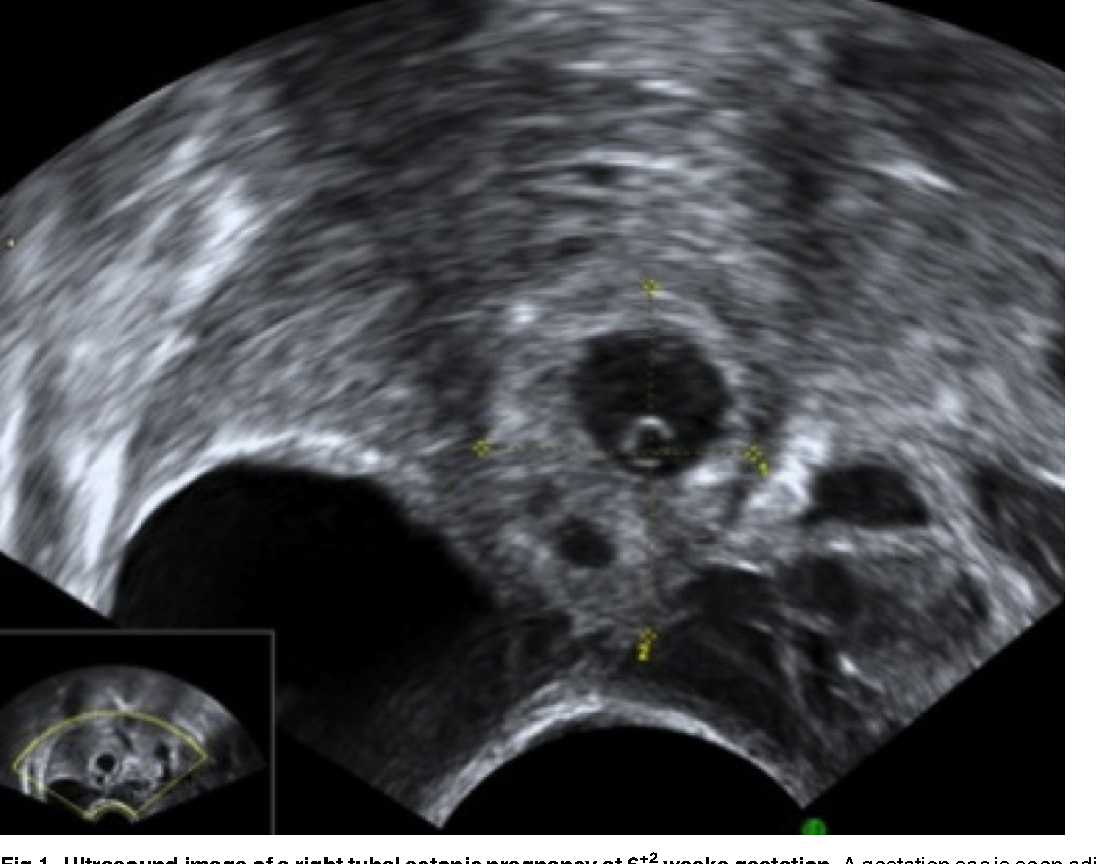 мед. наук. — Иваново, 2004. — С. 151.
мед. наук. — Иваново, 2004. — С. 151.
51. Коробкова Е.С. Реабилитация репродуктивной функции с коррекцией адаптивных программ у женщин, перенесших неразвивающуюся беременность: Дис… канд. мед. наук. — Рязань, 2002. — С. 132.
52. Мещерякова А.В., Демидова Е.М., Старостина Т.А., Волощук И.Н., Нагиева Ф.Г. Иммуноморфологические изменения в децидуальной ткани при неразвивающейся беременности сопутствующей урогенитальной хламидийной инфекции // Акуш. и гинек. — 2001. — № 3. — С. 22-24.
53. Мисник В.В. Генетические и иммунологические причины привычного невынашивания беременности: Дис… канд. мед. наук. — М., 2004. — 151 с.
54. Серова О.Ф. Предгравидарная подготовка женщин с невынашиванием беременности: Автореф. дис… д-ра. мед. наук. — М., 2000. — 40 с.
55. Тетруашвили Н.К. Диагностическая и прогностическая значимость определения цитокинов у больных с привычным невынашиванием беременности: Автореф. дис… канд. мед. наук. — М., 2000. — 28 с.
56. Baszak E., Sikorski R. , Milart P., Wojcik D. Clinical features of missed abortion // Ginekol. Pol. — 2001 Dec. — 72(12). — P. 1069-1072.
, Milart P., Wojcik D. Clinical features of missed abortion // Ginekol. Pol. — 2001 Dec. — 72(12). — P. 1069-1072.
57. Beer A.E., Kwak J. Reproductive medicine program Finch University of Health Science. — Chicago Medical School, 2000. — 96.
58. Raziel A., Kornberg Y., Friedler S., Schachter M., Sela B.A., Ron El.R. Hypercoagulable thrombophilic defects and hyperhomocysteinemia in patients with recurrent pregnancy loss // Am. J. Reprod. Immunol. — 2001 Feb. — 45(2). — P. 5-71.
59. Taylor R.N., Vigne G.L., Zhang P., Hoang P. Effects of progestins and relaxin on glycodelin gene expressions in human endometrial cells // Am. J. Obstet. Gynecol. — 2000. — V. 182, № 4. — P. 841-847.
Ультразвуковая диагностика случая внематочной беременности по типу неполного трубного аборта.
Ультразвуковая диагностика случая внематочной беременности по типу неполного трубного аборта.
Боярчук Е. Д., Гаврелюк С. В., Левенец С. В., Молотов Е. А.
ГУ «ЛНУ имени Тараса Шевченко», Луганск
Вступление. Внематочная беременность является одним из самых серьезных заболеваний репродуктивной сферы молодых женщин, так как требует обязательного и неотложного вмешательства, которое нередко осуществляется по экстренным, а иногда по жизненно важным показаниям. Одной из самых распространенных форм этого заболевания является трубная беременность и составляет, по данным литературы, около 97 % от всех эктопических беременностей. В настоящее время, когда уже практически полностью описан патогенез внематочной беременности, применение современных технологий на аппарате экспертного класса позволило уточнить положение и характер беременности, что дало возможность своевременно прибегнуть к оперативному лечению.
Материалы и методы. В кабинет ультразвуковой диагностики обратилась больная Т., 30 лет, которая на момент обращения находилась на стационарном лечении в отделении гинекологии по поводу нарушения менструального цикла.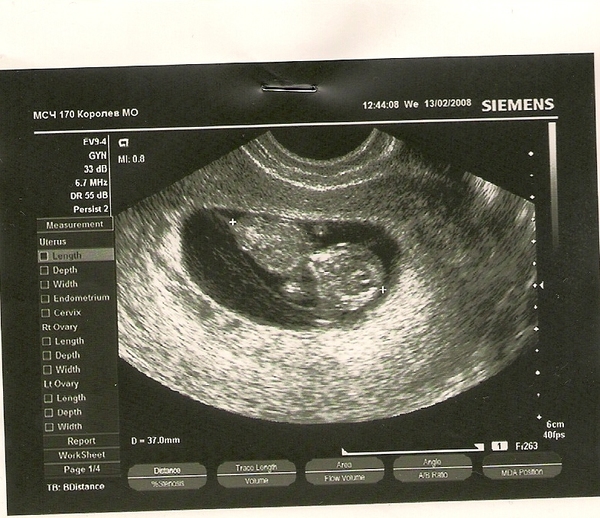 Больная была направлена в лабораторию для повторного анализа крови на уровень хорионического гонадотропина (ХГЧ) и, следуя мимо кабинета ультразвуковой диагностики, самостоятельно решила пройти ультразвуковое исследование (УЗИ). В анамнезе: задержка последних месячных — три недели, за четыре дня до обследования появились метроррагии, по поводу чего была госпитализирована в стационар. При проведении пункции заднего свода была обнаружена свободная жидкость в малом количестве без крови, показатель ХГЧ был определен на уровне 500 ед/л, что соответствует малому сроку беременности. Во время предыдущего ультразвукового исследования, проведенного тремя днями раньше описываемого, было обнаружено желтое тело в левом яичнике, в полости матки плодное яйцо выявлено не было.
Больная была направлена в лабораторию для повторного анализа крови на уровень хорионического гонадотропина (ХГЧ) и, следуя мимо кабинета ультразвуковой диагностики, самостоятельно решила пройти ультразвуковое исследование (УЗИ). В анамнезе: задержка последних месячных — три недели, за четыре дня до обследования появились метроррагии, по поводу чего была госпитализирована в стационар. При проведении пункции заднего свода была обнаружена свободная жидкость в малом количестве без крови, показатель ХГЧ был определен на уровне 500 ед/л, что соответствует малому сроку беременности. Во время предыдущего ультразвукового исследования, проведенного тремя днями раньше описываемого, было обнаружено желтое тело в левом яичнике, в полости матки плодное яйцо выявлено не было.
Результаты. Было проведено трансвагинальное УЗИ на аппарате экспертного класса Toshiba Xario, вагинальным мультичастотным датчиком с рабочими частотами 4,7-7,5 МГц. Данные исследования: матка не увеличена, М-эхо=10,0 мм, не однородное, плодное яйцо в полости матки не визуализируется, шейка обычная, за маткой визуализируется свободная жидкость в объеме до 13 мл, однородной консистенции. Правый яичник обычных размеров, формы и структуры. Левый яичник увеличен (размеры: 47х30х38 мм), имеет неправильную форму по типу треугольной, расположен вершиной вниз. В верхних углах яичника визуализируются жидкостные образования. В латеральном углу – овальной формы, с диаметром до 10 мм. В медиальном углу – округлой формы, с диаметром до 7 мм, окруженное тканью повышенной эхогенности кольцевидной формы, с толщиной по периметру до 3,4 мм. Примечательным было то, что оба жидкостных образования в углах яичника в режиме цветного допплеровского картирования имели кровоток характерный для желтого тела, и с первого взгляда оба были похожи на желтое тело. Следующим этапом ультразвукового исследования был абдоминальный доступ, который не прояснил картину. Лишь повторный осмотр вагинальным датчиком, с применением режимов оптимизации визуализации, позволил сделать правильное заключение. Медиально расположенное жидкостное образование которое прилежало к медиальной стенке яичника, при более детальном исследовании оказалось автономным.
Правый яичник обычных размеров, формы и структуры. Левый яичник увеличен (размеры: 47х30х38 мм), имеет неправильную форму по типу треугольной, расположен вершиной вниз. В верхних углах яичника визуализируются жидкостные образования. В латеральном углу – овальной формы, с диаметром до 10 мм. В медиальном углу – округлой формы, с диаметром до 7 мм, окруженное тканью повышенной эхогенности кольцевидной формы, с толщиной по периметру до 3,4 мм. Примечательным было то, что оба жидкостных образования в углах яичника в режиме цветного допплеровского картирования имели кровоток характерный для желтого тела, и с первого взгляда оба были похожи на желтое тело. Следующим этапом ультразвукового исследования был абдоминальный доступ, который не прояснил картину. Лишь повторный осмотр вагинальным датчиком, с применением режимов оптимизации визуализации, позволил сделать правильное заключение. Медиально расположенное жидкостное образование которое прилежало к медиальной стенке яичника, при более детальном исследовании оказалось автономным.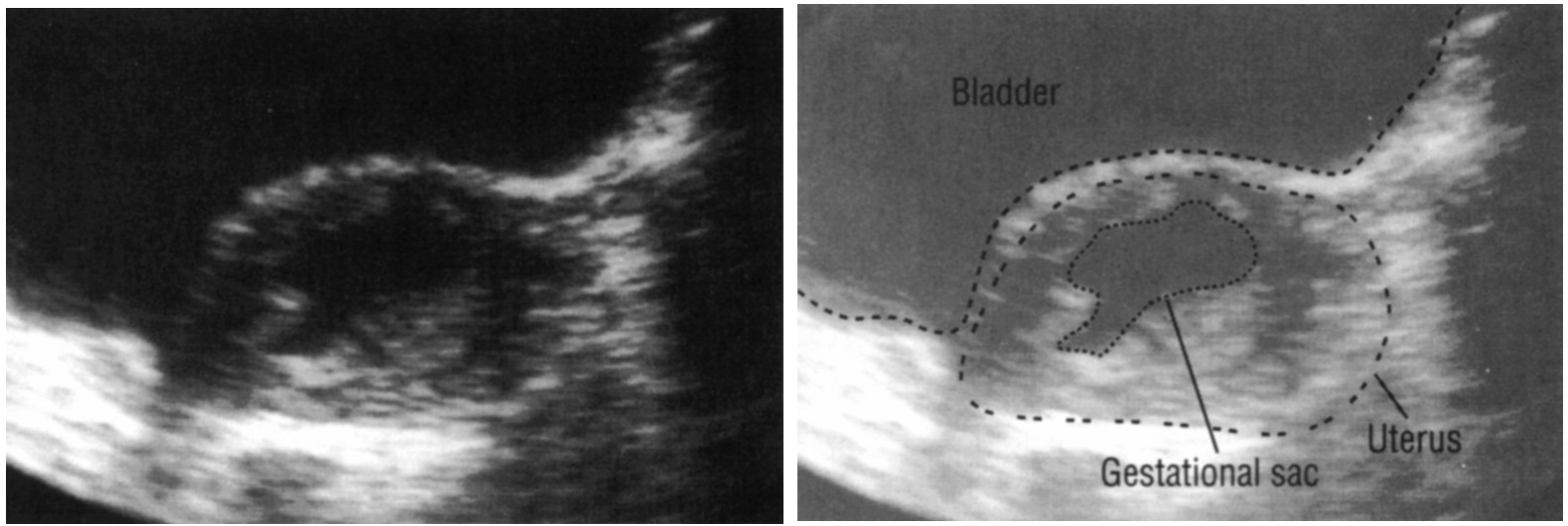 При полипозиционном исследовании в режиме зума в нем визуализировалось жидкостное тонкостенное включение до 2,8 мм в диаметре, которое было идентифицировано, как плодное яйцо с желточным мешком. В пользу прогрессирующей беременности говорило наличие кровоснабжения плодного яйца с желточным мешком, которое регистрировалось в допплеровских режимах. Таким образом, был поставлен единственно правильный диагноз: прогрессирующая внематочная беременность малого срока по типу неполного трубного аборта. Данные УЗИ буквально в течение часа, были подтверждены в операционной.
При полипозиционном исследовании в режиме зума в нем визуализировалось жидкостное тонкостенное включение до 2,8 мм в диаметре, которое было идентифицировано, как плодное яйцо с желточным мешком. В пользу прогрессирующей беременности говорило наличие кровоснабжения плодного яйца с желточным мешком, которое регистрировалось в допплеровских режимах. Таким образом, был поставлен единственно правильный диагноз: прогрессирующая внематочная беременность малого срока по типу неполного трубного аборта. Данные УЗИ буквально в течение часа, были подтверждены в операционной.
Выводы. Применение в практике интракавитальных датчиков с высокой разрешающей способностью дополненных допплеровскими методиками, в сочетании с абдоминальным доступом и полипозиционным исследованием, позволяет идентифицировать малые образования и дифференцировать характер патологических изменений в малом тазу. Это позволяет своевременно выбирать единственно правильную тактику лечения, что во многом способствует применению более щадящих методик лечения и сокращению периода реабилитации.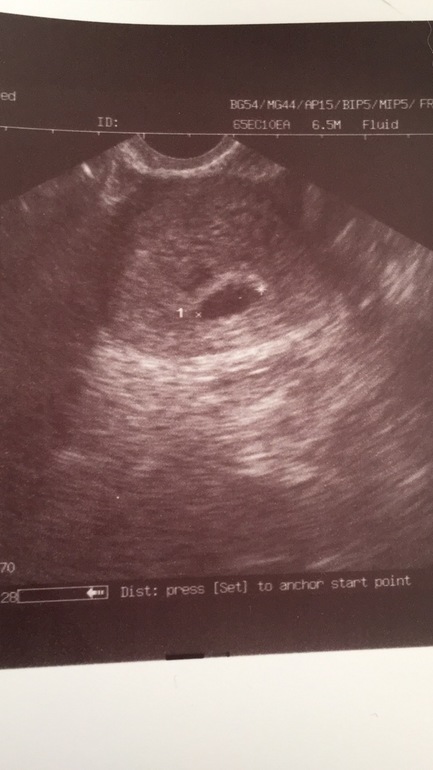
Полость матки – обзор
Физические барьеры
Полость матки защищена от восходящей инфекции несколькими анатомическими структурами. 52 Первую линию защиты обеспечивает уплотнение нормальных половых губ. Оценка строения вульвы и промежности должна быть включена во все предслучные осмотры или оценки на предмет бесплодия. Вульва должна находиться в вертикальном положении на одном уровне с анальным отверстием (рис. 8-1, A ). Половые губы должны быть плотно сжаты, причем большая часть их длины находится ниже седалищного бугра.Половые губы могут раздвигаться в результате предшествующих травм или повреждений (рис. 8-1, B ). У старых повторнородящих кобыл наблюдается тенденция к чрезмерному расслаблению половых губ, особенно во время эструса, а также к наклону дорсальной части вульвы, вызванному расслаблением промежностного тела. В этой ситуации вульва становится горизонтальной, когда ее краниально натягивают на седалищный бугор (рис. 8-1, C ). Эти анатомические изменения предрасполагают кобылу к пневмовагине (засасыванию ветра) и пневмоматке, что в конечном итоге приводит к скоплению мочи в краниальном влагалище и загрязнению матки при открытой шейке матки.Загрязнение фекалиями увеличивает риск заражения.
8-1, C ). Эти анатомические изменения предрасполагают кобылу к пневмовагине (засасыванию ветра) и пневмоматке, что в конечном итоге приводит к скоплению мочи в краниальном влагалище и загрязнению матки при открытой шейке матки.Загрязнение фекалиями увеличивает риск заражения.
Вторым физическим барьером в предотвращении контаминации влагалища и, в конечном счете, матки является вестибуловагинальный сфинктер. У нормальной кобылы вестибуловагинальная область остается закрытой даже при раздвинутых половых губах. Нарушение функции вестибуловагинального сфинктера подозревают, когда воздух всасывается во влагалище или если исследователь может визуализировать вагинальную полость сразу после раскрытия половых губ.Вестибуловагинальный сфинктер может стать скомпрометированным из-за ректовагинальных разрывов и других травм жеребят.
Третьим важным анатомическим барьером для инфекции является шейка матки. Шейка матки открыта во время эструса, поздних сроках беременности и в ближайшем послеродовом периоде. Однако у некоторых кобыл наблюдается нарушенная функция шейки матки, которая может оставаться открытой во время анэструса и даже диэструса. Наиболее частой причиной недостаточности шейки матки является поражение шейки матки вследствие дистоции.
Однако у некоторых кобыл наблюдается нарушенная функция шейки матки, которая может оставаться открытой во время анэструса и даже диэструса. Наиболее частой причиной недостаточности шейки матки является поражение шейки матки вследствие дистоции.
План лечения и профилактики инфекции матки должен включать план восстановления нормальной барьерной функции. Хирургические процедуры, такие как эпизиопластика, вестибуловагинопластика и ректовагинальная коррекция разрыва, следует рассматривать по показаниям.
Проблемы с маткой и фертильностью, бесплодие
(достаточно) нормальная полость матки и слизистая оболочка эндометрия необходимы для зачатия и сохранения беременности.
Существует несколько условий, связанных с полостью или футеровкой, которые могут вызвать проблемы.
- Во время менструации у женщины выделяется эндометриальная выстилка матки и некоторое количество связанной с ней крови. Затем в течение следующих нескольких недель или около того регенерируется новая оболочка, которая в конечном итоге становится восприимчивой к имплантации эмбриона.

- Если эмбрион не имплантируется, ее тело распознает, что она не беременна, сбрасывает слизистую оболочку матки и снова запускает процесс регенерации.
Гистероскопия внутри нормальной полости матки.
Офисная гистероскопия – смотрим вверх от шейки вверх в полость матки.
Устья маточных труб (отверстия фаллопиевых труб в матку) представляют собой темные пятна на 3 и 9 часах.
Ультразвуковые изображения матки с нормальной толщиной эндометрия 11 мм
То же изображение, показывающее внешний контур матки, обведенный красным, и выстилку эндометрия (матки) с «тройной полосой», обведенную зеленым. Цервикальный канал хорошо визуализируется внизу справа.
Проблемы с маткой и слизистой оболочкой матки, которые могут вызывать или способствовать репродуктивным проблемам, таким как бесплодие или привычный выкидыш:
- Полипы матки
- Миома матки (правильная медицинская терминология — миома или лейомиома)
- Внутриматочные спайки – рубцовая ткань в полости матки, также называемая синдромом Ашермана.
 Это может помешать зачатию или увеличить риск выкидыша.
Это может помешать зачатию или увеличить риск выкидыша. - Врожденные пороки развития матки, такие как двурогая матка, Т-образная матка или маточная перегородка
- Дефект лютеиновой фазы – редкое состояние, связанное с неадекватным развитием микроскопических и клеточных изменений в эндометриальной выстилке матки после овуляции и воздействия гормона прогестерона.
- Тонкая выстилка эндометрия – тоже редкость. Нам нравится видеть подкладку толщиной не менее 8 мм при измерении ультразвуком во время максимальной толщины во время цикла (см. выше ультразвуковое изображение 11.подкладка толщиной 2 мм).
Ведутся споры о том, «насколько тонкий — слишком тонкий», а также «насколько толстый — слишком толстый».
- В целом, 8–13 мм — это хорошо, менее 6 — потенциально проблематично, а более 15 или около того может снизить шансы на успешную беременность.
Во время лечения ЭКО слизистая оболочка матки начинает иметь толщину около 3 мм в конце менструального цикла. После достаточного повышения уровня эстрогена слизистая оболочка матки утолщается примерно на 1 мм каждый день во время ЭКО.
После достаточного повышения уровня эстрогена слизистая оболочка матки утолщается примерно на 1 мм каждый день во время ЭКО.
Гистероскопия — это хирургическая процедура, при которой узкий телескопоподобный инструмент вводится через влагалище и шейку матки в полость матки (полость эндометрия). Полость затем расширяется жидкостью (например, соленой водой) и может быть визуализирована через эндоскоп. Эта процедура позволяет увидеть любые дефекты внутри полости.
Полип матки, визуализируемый при гистероскопии
Большой полип матки на «дне» полости матки, визуализируемый при гистероскопии Ультразвук является очень полезным инструментом для оценки таза, матки и ее слизистой оболочки или эндометрия.3D УЗИ, более новая технология, особенно хорошо помогает врачам охарактеризовать форму полости матки.
Нормальная конфигурация матки в сравнении с маточной перегородкой
УЗИ нормальной матки в коронарной плоскости
Полость матки имеет гладкую треугольную форму
Шейка матки внизу изображения
Межматочная перегородка на коронарной плоскости по данным 3D УЗИ
Выстилка эндометрия и полость матки = C
Мышечная часть матки = M
Перегородка «вдавливается» в полость = S
Перегородка как бы лишняя мышца, «продавливающая» сверху в полость.
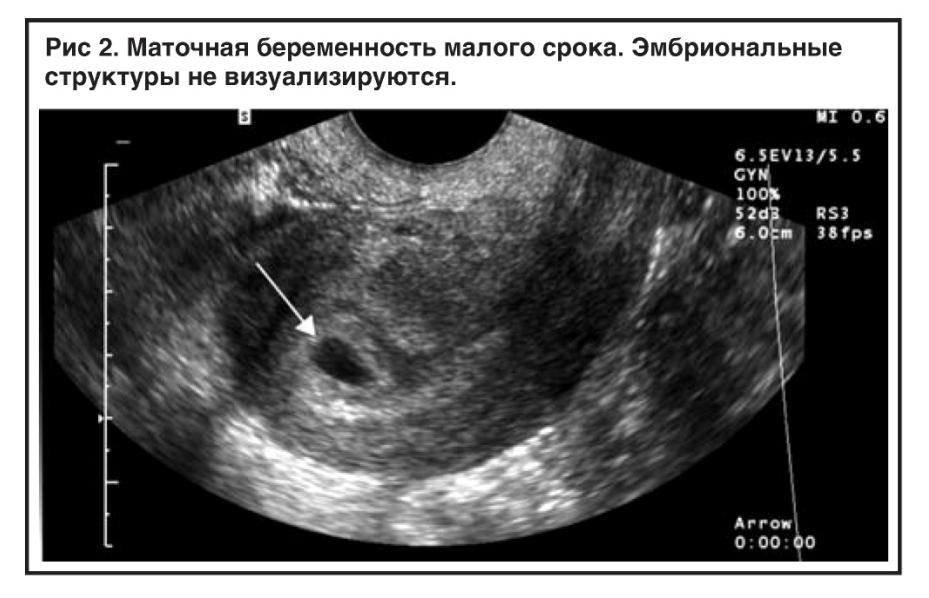
Это ультразвуковое изображение (3D) представляет собой коронарную плоскость, показывающую однорогую матку
. Полость (в букве «С») идет только к одной фаллопиевой трубе (доходит до ее правой трубы)
Другая сторона матки и левая труба врожденно отсутствуют.
Врожденные аномалии матки, такие как однорогая, септированная или двурогая матка, могут вызывать репродуктивные проблемы, такие как выкидыш, преждевременные роды и преждевременные роды.
Снимок офисной гистероскопии перегородки матки, направленной вверх от шейки матки к верхушке матки
Перегородка, разделяющая полость на «S»
Левая сторона ее полости матки находится на «L», правая сторона на «R».
Что такое полость матки? — Размер и разрешение — Видео и стенограмма урока
Структура
Полость матки образована боковыми стенками матки, а также нижней стенкой дна или верхней частью матки.Эти стенки содержат мышечную ткань, известную как миометрий , и слой клеток, выстилающих внешние края, известный как эндометрий .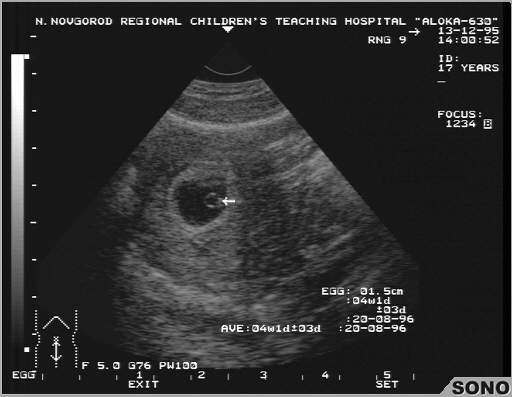 Сама полость в целом имеет Т-образный вид, хотя точность этой формы будет меняться в течение менструального цикла. Ширина полости матки обычно составляет от 27 до 32 мм у женщин до менопаузы, хотя это может варьироваться от человека к человеку. Поскольку матка является местом имплантации оплодотворенных яйцеклеток для беременности, стенки матки будут расти на протяжении всего цикла, и это изменит объем пространства, находящегося в полости матки.
Сама полость в целом имеет Т-образный вид, хотя точность этой формы будет меняться в течение менструального цикла. Ширина полости матки обычно составляет от 27 до 32 мм у женщин до менопаузы, хотя это может варьироваться от человека к человеку. Поскольку матка является местом имплантации оплодотворенных яйцеклеток для беременности, стенки матки будут расти на протяжении всего цикла, и это изменит объем пространства, находящегося в полости матки.
Функция
Матка — это мышечный орган, предназначенный для облегчения некоторых аспектов размножения в женском организме. Во время секса он служит путем для сперматозоидов, направляющихся к яйцеклетке. Он также сокращается во время оргазма, что увеличивает шансы на оплодотворение. Полость матки является ключевым местом, где это происходит. Без этого пространства пути для сперматозоидов не существовало бы, и беременность не наступила бы.
После оплодотворения яйцеклетка имплантируется в слизистую оболочку матки.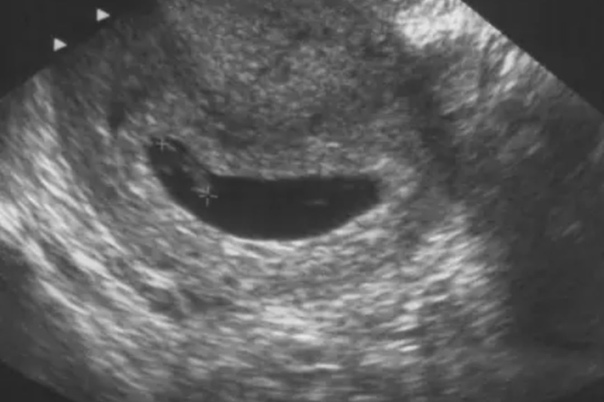 Здесь развивающийся ребенок сможет получать питательные вещества из кровеносных сосудов, находящихся в эндометрии. По мере того, как ребенок продолжает расти, полость матки будет служить пространством, в котором будет размещаться этот рост. Этот рост обычно продолжается примерно девять месяцев или до тех пор, пока ребенок не станет достаточно большим, чтобы прижиматься к шейке матки, расположенной в нижнем конце. Во время родов мышцы миометрия сокращаются, чтобы вытолкнуть ребенка через шейку матки и выйти из полости матки.
Здесь развивающийся ребенок сможет получать питательные вещества из кровеносных сосудов, находящихся в эндометрии. По мере того, как ребенок продолжает расти, полость матки будет служить пространством, в котором будет размещаться этот рост. Этот рост обычно продолжается примерно девять месяцев или до тех пор, пока ребенок не станет достаточно большим, чтобы прижиматься к шейке матки, расположенной в нижнем конце. Во время родов мышцы миометрия сокращаются, чтобы вытолкнуть ребенка через шейку матки и выйти из полости матки.
Итоги урока
Давайте повторим. Полость матки играет важную роль в половом акте, оплодотворении и беременности. Это пространство позволяет сперме двигаться к яйцеклетке, а также позволяет оплодотворенной яйцеклетке имплантироваться и развиваться во время беременности. Поэтому без полости матки процесс размножения внутри женского организма был бы невозможен.
Фаллопиевы трубы | Справочная статья радиологии
Фаллопиевы трубы (TA: tuba uterina 8 ), также известные как маточные трубы или, реже, яйцеводы , представляют собой парные полые трубы, соединяющие каждый яичник и матку и функционирующие для передачи зрелая яйцеклетка от первого ко второму.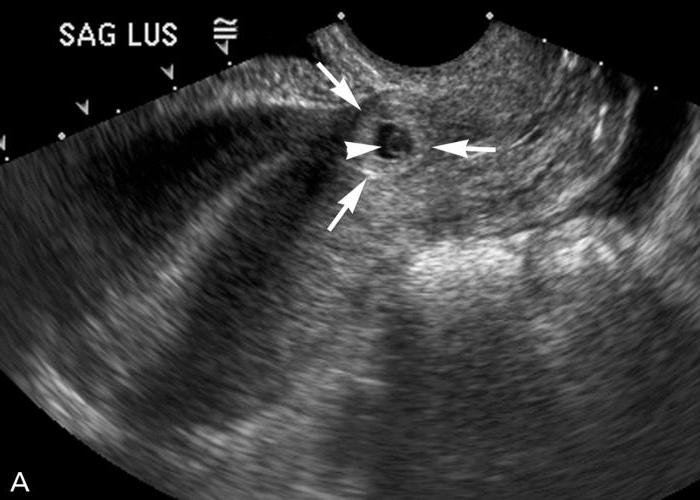 Если происходит зачатие, оно обычно происходит внутри трубы. На него может влиять широкий спектр патологий.
Если происходит зачатие, оно обычно происходит внутри трубы. На него может влиять широкий спектр патологий.
Фаллопиевы трубы имеют длину приблизительно 10-12 см и диаметр 1-4 мм. Он перекрывает промежуток между яичником латерально и маткой медиально. Через него яйцеклетка проходит в полость матки. Брюшинный рефлекс, нависающий над сальпингеями, образует мезосальпинкс.
Фаллопиевы трубы делятся на 5 анатомических сегментов (от латерального к медиальному, по пути яйцеклетки после овуляции):
- фимбрии : ~25 пальцевидных отростков, которые ниспадают на яичник
- фимбрии яичника длиннее других и прикрепляются к трубчатому полюсу яичника
- воронка : воронкообразная боковая часть, которая нависает над яичником с отходящими от него бахромками
- открывается в брюшную полость через отверстие брюшной полости
- ампула : самая широкая и длинная часть, образующая более половины длины, это наиболее распространенное место оплодотворения
- перешеек : непосредственно латеральнее матки, это самый узкий сегмент, как следует из названия
- интерстициальный или интрамуральный сегмент : срез внутри миометрия
См. мнемонику здесь.
мнемонику здесь.
Взаимоотношения
Внематочная часть фаллопиевой трубы проходит между двумя складками широкой связки в ее верхней части 5 .
- на медиальном конце интерстициальный сегмент является продолжением маточно-трубного соединения, продолжением полости эндометрия
- своим латеральным концом воронка открывается в брюшную полость.
Фаллопиевы трубы являются одним из компонентов придатков.
- латеральная треть через лозовидное сплетение к яичниковым венам
- медиально на две трети через маточное сплетение к внутренней подвздошной вене
- через яичниковые сосуды к парааортальным узлам и маточные сосуды к внутренней цепи подвздошной кости
- дренирование также в паховые узлы через круглую связку
- вегетативное кровоснабжение из яичникового и маточного сплетений
- парасимпатическая: блуждающий нерв для латеральной половины, тазовый орган для медиальной половины
- симпатические от грудного и поясничного отделов позвоночника (T10-L1)
- отсутствует односторонний
- гипоплазия односторонняя
- гипоплазия двусторонняя
- аномальное проникновение в тело или дно матки
Как и многие другие мышечные полые трубки, он имеет два слоя мышц (внутренний круговой, наружный продольный) и выстлан смесью реснитчатого и нереснитчатого столбчатого эпителия. Именно первый подталкивает яйцеклетку к матке.
Именно первый подталкивает яйцеклетку к матке.
Нормальная маточная труба не визуализируется при поперечном сечении, если только она не очерчена жидкостью. При наличии перитонеальной жидкости или контрастного вещества фаллопиевы трубы выглядят как парные, тонкие, змеевидные околоматочные структуры, простирающиеся либо кпереди, либо кзади в слепой мешок.
Рентгеноскопия
Контрастные исследования можно выполнить, выполнив гистеросальпингограмму (ГСГ).
История и этимология
Фаллопиевы трубы названы в честь Габриэля Фаллопиуса , итальянского анатома (1523-62).Он тот же анатом, который дал свое имя фаллопиевой связке и фаллопиеву каналу. Несмотря на эпоним, слово «фаллопиевы» чаще всего используется в нижнем регистре.
Гистеросальпингография (Утеросальпингография)
Гистеросальпингография (ГСГ) оценивает форму матки и проверяет, открыты ли фаллопиевы трубы. Он также используется для расследования выкидышей из-за проблем в матке.
Сообщите своему врачу, если вы беременны, и обсудите любые недавние заболевания, состояния здоровья, аллергии и лекарства, которые вы принимаете.Не делайте эту процедуру, если вы подозреваете, что беременны или у вас активная инфекция органов малого таза. Сообщите своему врачу, если у вас аллергия на йодсодержащее контрастное вещество. Сообщите своему врачу, если у вас есть инфекция органов малого таза или невылеченное заболевание, передающееся половым путем (ЗППП). Носите свободную, удобную одежду и оставьте украшения дома. Вам нужно будет надеть халат, как на гинекологический осмотр.
Что такое гистеросальпингография?
HSG — это рентгенологическое исследование матки и фаллопиевых труб.Он использует специальную форму рентгеновского излучения, называемую флюороскопией, и контрастное вещество.
Рентгенологическое исследование помогает врачам диагностировать и лечить заболевания. Он подвергает вас небольшой дозе ионизирующего излучения для получения изображений внутренней части тела. Рентгеновские снимки являются старейшим и наиболее часто используемым видом медицинской визуализации.
Рентгеновские снимки являются старейшим и наиболее часто используемым видом медицинской визуализации.
Ваш врач использует рентгеноскопию, чтобы увидеть ваши внутренние органы в движении. Ваш врач или лаборант наполнит вашу матку и фаллопиевы трубы водорастворимым контрастным веществом.Затем ваш рентгенолог проведет рентгеноскопию, чтобы просмотреть и оценить их.
начало страницы
Каковы наиболее распространенные способы использования этой процедуры?
Врачи в первую очередь используют это обследование, чтобы выяснить, почему у вас могут быть трудности с беременностью. Врач смотрит на раскрытие фаллопиевых труб, форму и структуру матки, а также любые рубцы в матке или близлежащей брюшной (брюшной) полости.
Экзамен также оценивает проходимость фаллопиевых труб и проверяет последствия операции на маточных трубах.Эти эффекты включают в себя:
- Непроходимость фаллопиевых труб вследствие инфекции или рубцевания
- Перевязка маточных труб
- Закрытие фаллопиевых труб при стерилизации и отмене стерилизации
- Повторное открытие фаллопиевых труб после стерилизации или непроходимости, связанной с заболеванием
Экзамен может исследовать повторные выкидыши, вызванные врожденными или приобретенными проблемами матки, такими как:
- Миома матки
- Полипы эндометрия (матки)
- Спайки
- Врожденные аномалии (аномалии матки)
- Опухоли
начало страницы
Как мне подготовиться?
Запланируйте обследование через 7-10 дней после первого дня менструации, но до овуляции.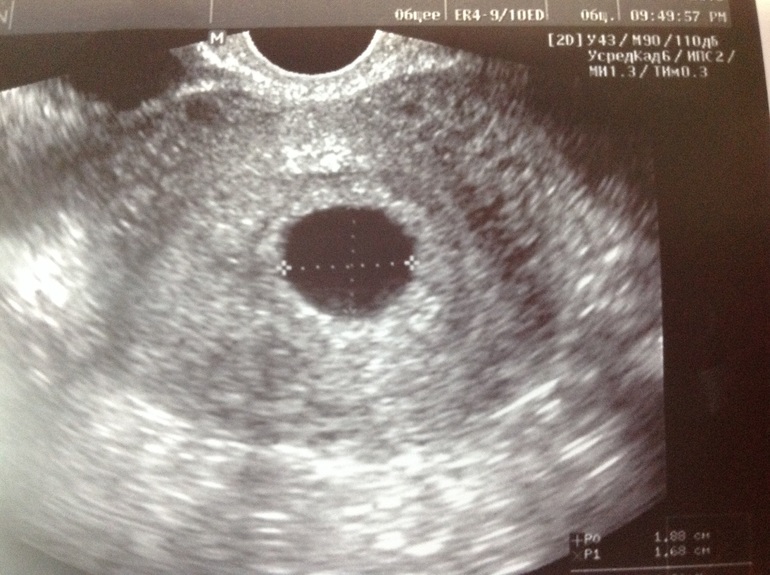 Это лучшее время для экзамена.
Это лучшее время для экзамена.
Не делайте эту процедуру, если у вас активная инфекция органов малого таза. Сообщите своему врачу и лаборанту, если у вас есть какие-либо признаки тазовой инфекции или невылеченного ЗППП. Сообщите своему врачу, если у вас аллергия на йодированный контраст.
Перед процедурой вы можете принять лекарство, отпускаемое без рецепта, чтобы свести к минимуму любой дискомфорт. Некоторые врачи назначают антибиотик до и/или после процедуры.
Расскажите своему врачу обо всех лекарствах, которые вы принимаете.Перечислите любые аллергические реакции, особенно на контрастные вещества с йодом. Расскажите своему врачу о недавних заболеваниях или других заболеваниях.
Вам нужно будет снять часть одежды и надеть халат для экзамена. Удалите любые металлические предметы или одежду в области таза, которые могут мешать получению рентгеновских изображений.
Женщины должны всегда сообщать своему врачу и лаборанту, если они беременны. Врачи не будут проводить много тестов во время беременности, чтобы не подвергать плод риску.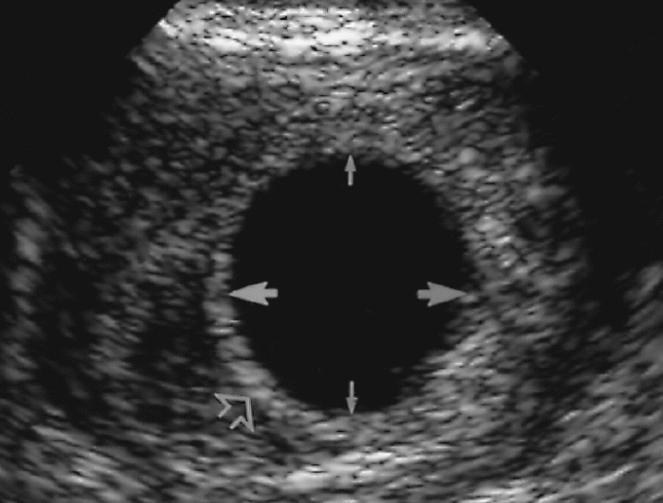 Если рентген необходим, врач примет меры предосторожности, чтобы свести к минимуму облучение ребенка. Дополнительную информацию о беременности и рентгеновских снимках см. на странице «Безопасность при рентгенографии, интервенционной радиологии и процедурах ядерной медицины» .
Если рентген необходим, врач примет меры предосторожности, чтобы свести к минимуму облучение ребенка. Дополнительную информацию о беременности и рентгеновских снимках см. на странице «Безопасность при рентгенографии, интервенционной радиологии и процедурах ядерной медицины» .
начало страницы
Как выглядит оборудование?
В этом исследовании обычно используется рентгенографический стол, одна или две рентгеновские трубки и видеомонитор. Рентгеноскопия преобразует рентгеновские лучи в видеоизображения. Врачи используют его для наблюдения и руководства процедурами. Рентгеновский аппарат и детектор, подвешенный над столом для осмотра, производят видео.
начало страницы
Как работает процедура?
Рентгеновские лучи — это форма излучения, подобная свету или радиоволнам. Рентгеновские лучи проходят через большинство объектов, включая тело. Техник тщательно направляет рентгеновский луч на интересующую область. Аппарат производит небольшую вспышку радиации, которая проходит через ваше тело. Излучение записывает изображение на фотопленку или специальный детектор.
Излучение записывает изображение на фотопленку или специальный детектор.
Рентгеноскопия использует непрерывный или импульсный рентгеновский луч для создания изображений и их проецирования на видеомонитор.На вашем экзамене может использоваться контрастное вещество, чтобы четко определить область интереса. Рентгеноскопия позволяет врачу увидеть суставы или внутренние органы в движении. Экзамен также захватывает неподвижные изображения или видеоролики и сохраняет их в электронном виде на компьютере.
Большинство рентгеновских снимков представляют собой цифровые файлы, хранящиеся в электронном виде. Ваш врач может легко получить доступ к этим сохраненным изображениям для диагностики и управления вашим состоянием.
начало страницы
Как проходит процедура?
Ваш врач, скорее всего, проведет это обследование амбулаторно.
Процедура похожа на гинекологический осмотр. Вы будете лежать на спине на столе для осмотра, согнув колени, или ваши ноги будут поддерживаться стременами.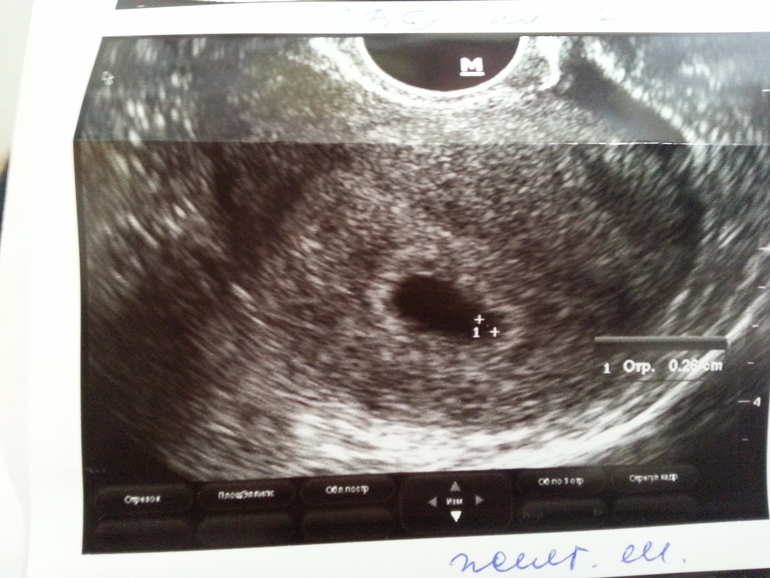 Ваш врач введет зеркало во влагалище, очистит шейку матки и вставит катетер. Врач удалит зеркало и осторожно поместит вас под рентгеноскопическую камеру. Врач заполнит полость матки, фаллопиевы трубы и брюшную полость контрастным веществом через катетер и сделает рентгеноскопические снимки.Врач может попросить вас изменить положение под рентгеноскопической камерой.
Ваш врач введет зеркало во влагалище, очистит шейку матки и вставит катетер. Врач удалит зеркало и осторожно поместит вас под рентгеноскопическую камеру. Врач заполнит полость матки, фаллопиевы трубы и брюшную полость контрастным веществом через катетер и сделает рентгеноскопические снимки.Врач может попросить вас изменить положение под рентгеноскопической камерой.
Когда процедура будет завершена, врач удалит катетер и позволит вам сесть.
Когда обследование будет завершено, лаборант может попросить вас подождать, пока рентгенолог не подтвердит, что у него есть все необходимые снимки.
Экзамен обычно занимает около 30 минут.
начало страницы
Что я испытаю во время и после процедуры?
Это обследование должно вызвать лишь незначительный дискомфорт.
У вас может быть небольшой дискомфорт и спазмы, когда врач устанавливает катетер и вводит контрастное вещество. Это не должно продолжаться долго. Также может быть незначительное раздражение брюшины, слизистой оболочки брюшной полости. Это может вызвать боль внизу живота. Это должно быть минимальным и кратким. Большинство женщин испытывают кровянистые выделения из влагалища в течение нескольких дней после обследования. Это нормально.
Это может вызвать боль внизу живота. Это должно быть минимальным и кратким. Большинство женщин испытывают кровянистые выделения из влагалища в течение нескольких дней после обследования. Это нормально.
начало страницы
Кто интерпретирует результаты и как их получить?
Рентгенолог , врач, обученный контролировать и интерпретировать рентгенологические исследования, будет анализировать изображения.Рентгенолог отправит подписанный отчет вашему основному лечащему врачу или лечащему врачу, который обсудит с вами результаты .
Возможно, вам потребуется повторное обследование. Если это так, ваш врач объяснит, почему. Иногда последующее обследование дополнительно оценивает потенциальную проблему с помощью большего количества изображений или специальной техники визуализации. Он также может увидеть, произошли ли какие-либо изменения в задаче с течением времени. Последующие осмотры часто являются лучшим способом убедиться, что лечение работает или проблема требует внимания.
начало страницы
Каковы преимущества по сравнению с рисками?
Преимущества
- Это минимально инвазивное исследование; осложнения редки.
- Может дать ценную информацию о проблемах с беременностью или вынашиванием плода.
- Он потенциально может открыть закупоренные фаллопиевы трубы, чтобы вы могли забеременеть в будущем.
- После рентгенологического исследования в вашем теле не остается радиации.
- Рентген обычно не имеет побочных эффектов в типичном диагностическом диапазоне для этого исследования.
Риски
- Всегда есть небольшой шанс заболеть раком из-за чрезмерного облучения. Однако, учитывая небольшое количество радиации, используемой в медицинской визуализации, польза от точного диагноза намного перевешивает связанный с этим риск.
- Доза облучения для этой процедуры варьируется. Дополнительную информацию о дозе облучения см. на странице «Доза облучения при рентгенологическом и КТ-обследовании».

- Сообщите врачу и лаборанту, если у вас инфекция органов малого таза, воспалительное заболевание или невылеченное ЗППП.Это поможет вам избежать усугубления любой такой инфекции.
- Женщины должны всегда сообщать своему врачу и рентгенологу, если они беременны. Дополнительную информацию о беременности и рентгеновских снимках см. на странице «Безопасность при рентгенографии, интервенционной радиологии и процедурах ядерной медицины».
Несколько слов о минимизации радиационного облучения
Врачи проявляют особую осторожность во время рентгеновских исследований, чтобы использовать минимально возможную дозу облучения, получая при этом наилучшие изображения для оценки.Национальные и международные организации по защите от радиологии постоянно пересматривают и обновляют стандарты методов, которые используют специалисты в области радиологии.
Современные рентгеновские системы сводят к минимуму паразитное (рассеянное) излучение за счет использования контролируемых рентгеновских лучей и методов контроля дозы.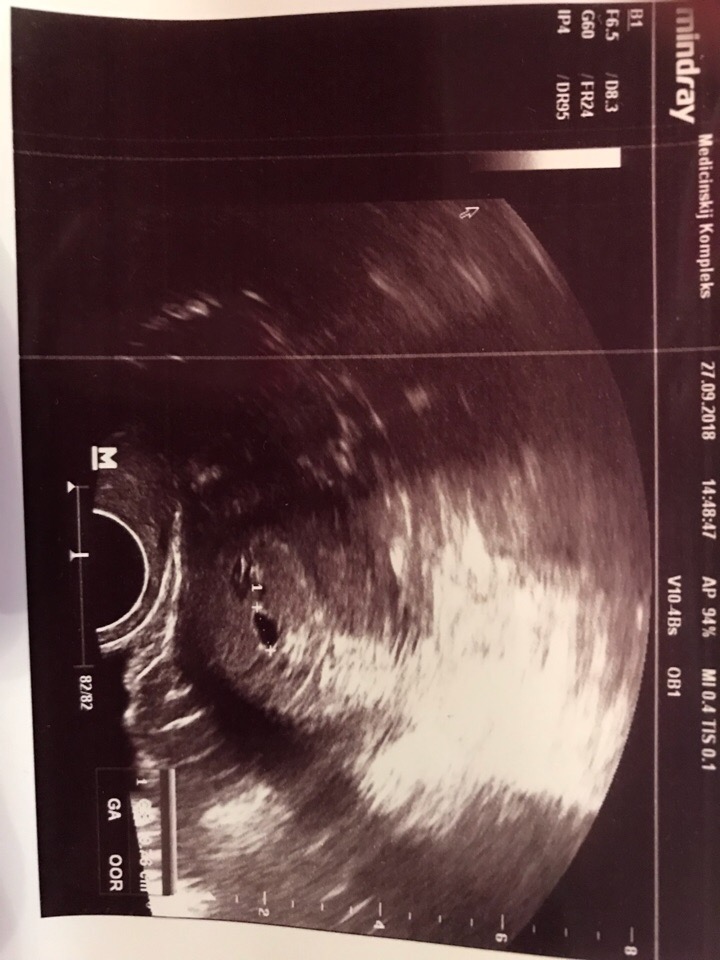 Это гарантирует, что области вашего тела, не отображаемые на изображении, получат минимальное облучение.
Это гарантирует, что области вашего тела, не отображаемые на изображении, получат минимальное облучение.
начало страницы
Каковы ограничения гистеросальпингографии?
Во время этого исследования исследуется только внутренняя часть матки и фаллопиевы трубы.Ваш врач может использовать МРТ или УЗИ для выявления проблем с яичниками, стенкой матки и другими структурами таза. Это обследование не может оценить проблемы бесплодия из-за низкого или аномального количества сперматозоидов или неспособности оплодотворенной яйцеклетки имплантироваться в матку.
начало страницы
Эта страница была проверена 25 ноября 2019 г.
фаллопиевы трубы | Анатомия и функции
маточная труба , также называемая яйцеводом или маточной трубой , любой из пары длинных узких протоков, расположенных в брюшной полости женщины, которые транспортируют мужские сперматозоиды к яйцеклетке, обеспечивают подходящую среду для оплодотворение и транспорт яйцеклетки из яичника, где она образуется, в центральный канал (просвет) матки.
Каждая маточная труба имеет длину 10–13 см (4–5 дюймов) и диаметр 0,5–1,2 см (0,2–0,6 дюйма). Канал трубы выстлан слоем слизистой оболочки, имеющей множество складок и сосочков — мелких конусовидных выростов ткани. Над слизистой оболочкой располагаются три слоя мышечной ткани; самый внутренний слой имеет спирально расположенные волокна, средний слой имеет круглые волокна, а самая внешняя оболочка имеет продольные волокна, которые заканчиваются множеством пальцевидных ответвлений (бамбрий) возле яичников, образуя воронкообразный депозитарий, называемый воронкой.Воронка улавливает и направляет выпущенные яйца; это широкая дистальная (самая внешняя) часть каждой фаллопиевой трубы. Окончания бахромок заходят за яичник; они сокращаются близко к поверхности яичника во время овуляции, чтобы направлять свободную яйцеклетку. От воронки отходит длинная центральная часть фаллопиевой трубы, называемая ампулой. Перешеек представляет собой небольшой участок длиной всего около 2 см (0,8 дюйма), который соединяет ампулу и воронку с маткой.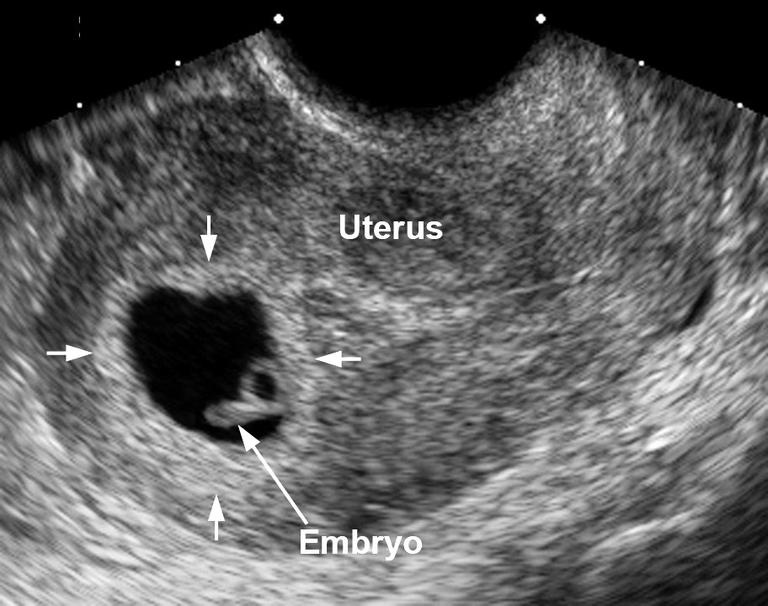 Конечная область фаллопиевой трубы, известная как интрамуральная или маточная часть, расположена в верхней части (дне) матки; это узкая трубка, продолжающаяся с перешейком, и она ведет через толстую стенку матки в полость матки, где обычно прикрепляются и развиваются оплодотворенные яйцеклетки.Канал интрамурального протока является наиболее узкой частью маточной трубы.
Конечная область фаллопиевой трубы, известная как интрамуральная или маточная часть, расположена в верхней части (дне) матки; это узкая трубка, продолжающаяся с перешейком, и она ведет через толстую стенку матки в полость матки, где обычно прикрепляются и развиваются оплодотворенные яйцеклетки.Канал интрамурального протока является наиболее узкой частью маточной трубы.
Британская викторина
Человеческое тело: правда или вымысел?
Насколько глубоки ваши знания о внутреннем устройстве человека? Проверьте это с помощью этого теста.
Слизистая оболочка, выстилающая фаллопиевы трубы, выделяет секрет, который помогает транспортировать сперму и яйцеклетку и поддерживать их жизнь.Основными составляющими жидкости являются кальций, натрий, хлорид, глюкоза (сахар), белки, бикарбонаты и молочная кислота.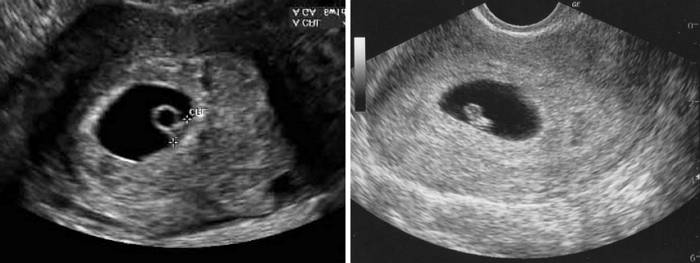 Бикарбонаты и молочная кислота жизненно важны для использования кислорода сперматозоидами, а также помогают яйцеклетке развиваться после ее оплодотворения. Глюкоза является питательным веществом для яйцеклетки и спермы, в то время как остальные химические вещества обеспечивают подходящую среду для оплодотворения.
Бикарбонаты и молочная кислота жизненно важны для использования кислорода сперматозоидами, а также помогают яйцеклетке развиваться после ее оплодотворения. Глюкоза является питательным веществом для яйцеклетки и спермы, в то время как остальные химические вещества обеспечивают подходящую среду для оплодотворения.
Помимо клеток, выделяющих жидкости, слизистая оболочка содержит клетки с тонкими волосовидными структурами, называемыми ресничками; реснички помогают продвигать яйцеклетку и сперматозоид по фаллопиевым трубам.Сперматозоиды, находящиеся в женских половых путях, обычно достигают воронки в течение нескольких часов. Яйцеклетка, независимо от того, оплодотворенная она или нет, достигает полости матки в течение трех-четырех дней. Колебательные движения ресничек и ритмичные мышечные сокращения (перистальтические волны) стенки фаллопиевой трубы работают вместе при перемещении яйцеклетки или сперматозоида.
Аномалии или повреждения фаллопиевых труб могут повлиять на фертильность женщины.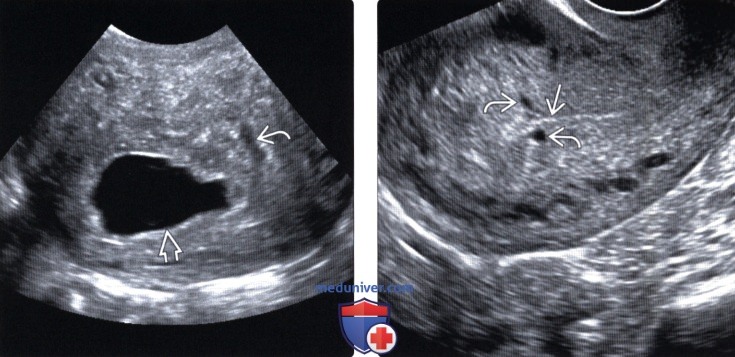 Например, если трубы заблокированы или повреждены, сперматозоиды не могут достичь яйцеклетки или оплодотворенная яйцеклетка не может попасть в матку.Аномалии анатомии и функции фаллопиевых труб имеют различные причины, в том числе инфекции органов малого таза (например, воспалительные заболевания органов малого таза), эндометриоз и врожденные дефекты.
Например, если трубы заблокированы или повреждены, сперматозоиды не могут достичь яйцеклетки или оплодотворенная яйцеклетка не может попасть в матку.Аномалии анатомии и функции фаллопиевых труб имеют различные причины, в том числе инфекции органов малого таза (например, воспалительные заболевания органов малого таза), эндометриоз и врожденные дефекты.
Женская репродуктивная система: Руководство по гистологии
Яйцевод
Яйцевод также известен как маточная или маточная труба. Это проход, по которому яйцеклетка переходит из яичника в полость матки.
Яйцеводы являются частью половых путей.
Имеют стенку из гладких мышц, внутреннюю слизистую оболочку и
наружный слой рыхлой поддерживающей ткани (сероза).
Просвет имеет вид «лабиринта», как вы можете видеть на
поперечное сечение фаллопиевой трубы, показанное ниже.
Проксимальная часть называется воронкой ,
расклешенный и «бахромчатый» (бахромчатый).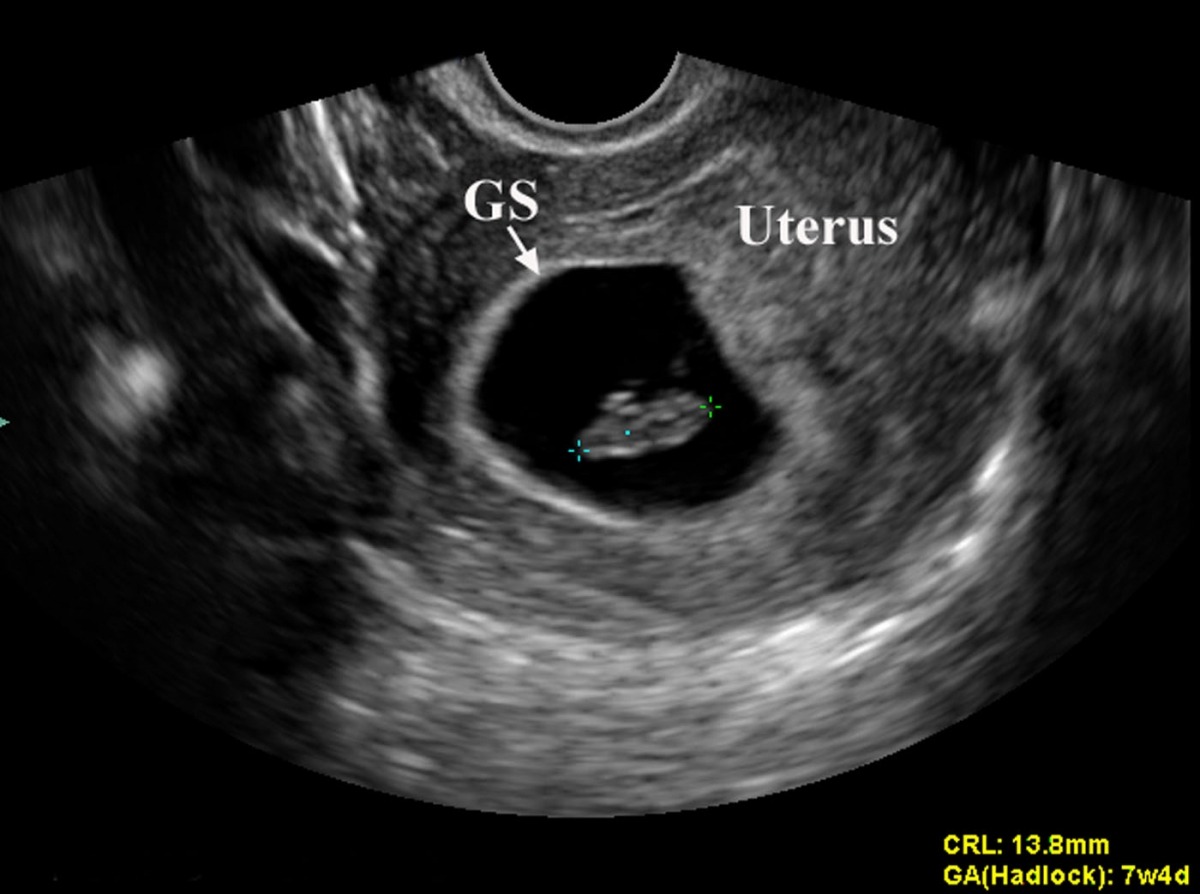
Это ведет к более длинной тонкостенной ампуле ,
имеет первичные, вторичные и третичные продольные складки слизистой оболочки.
Это ведет к короткому толстостенному перешейку ,
имеет меньше продольных складок слизистой оболочки.
Это ведет к внутренней части , которая простирается
через стенку матки и открывается в просвет матки.
Взгляните на это изображение маточной трубы с низким увеличением.
Можете ли вы идентифицировать серозную оболочку (адвентициальный слой), мышечная оболочка слизистой оболочки слой, слизистая оболочка , который очень высоко сложен в продольном направлении, и люмен .В складчатой слизистой оболочке оплодотворяются яйцеклетки.
Маточная труба соединяется со стенкой тела широкой связкой,
который также содержит кровоснабжение серозной оболочки. Вы должны быть
удалось идентифицировать некоторые кровеносные сосуды в серозной оболочке.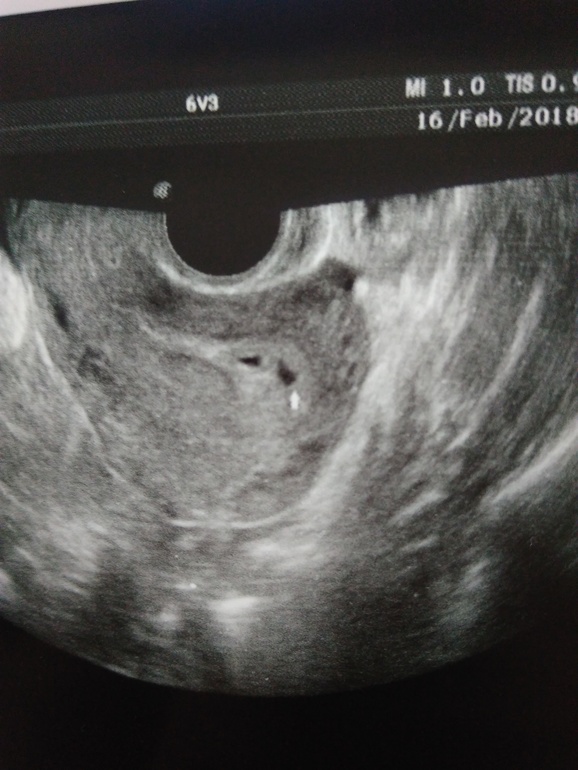
Мышечный слой ( muscolis mucosa ) состоит наружного продольного слоя и внутреннего кольцевого слоя.
Теперь взгляните на это изображение слизистой оболочки с большим увеличением. Может вы идентифицируете богато васкуляризированную lamina propria , базальная мембрана и эпителиальная ячейки .
Существует три типа эпителиальных клеток:
Клетки Peg — нереснитчатые (P). Эти клетки являются секреторными и имеют обширную гольджи, лежащую выше ядра, к апикальной поверхности клетки. Эти клетки выделяют питательный материал для яйцеклетки. Клетки-колышки особенно заметно на 14 день менструального цикла — т.е. примерно в то время овуляции.
Ресничные клетки — Апикальная поверхность реснитчатая,
а некоторые клетки имеют большие скопления гликогена, который окрашивается
темно-красный на этом изображении, окрашенном PAS.

 И в большинстве случаев такая патология протекает без явных клинических симптомов и выявляется уже после замершей беременности.
И в большинстве случаев такая патология протекает без явных клинических симптомов и выявляется уже после замершей беременности.


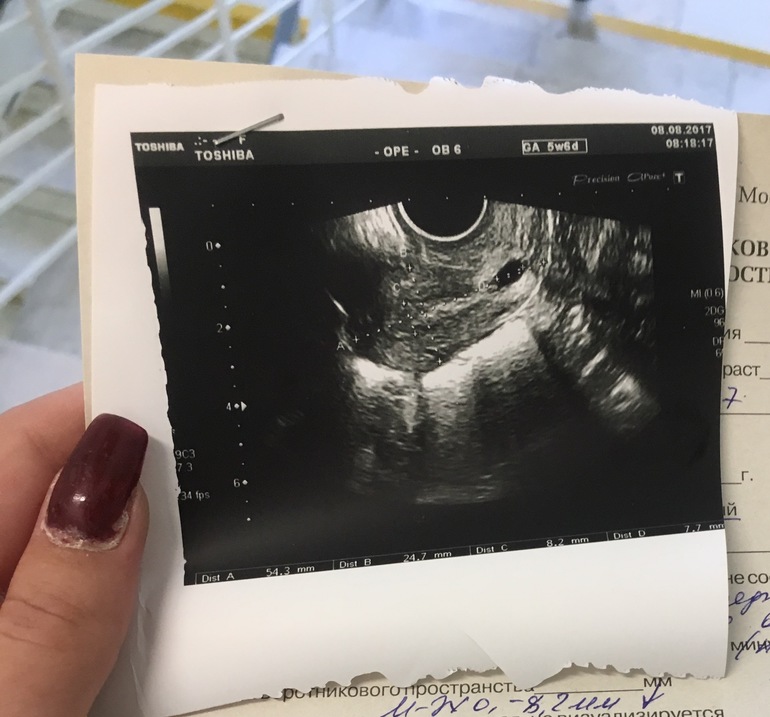
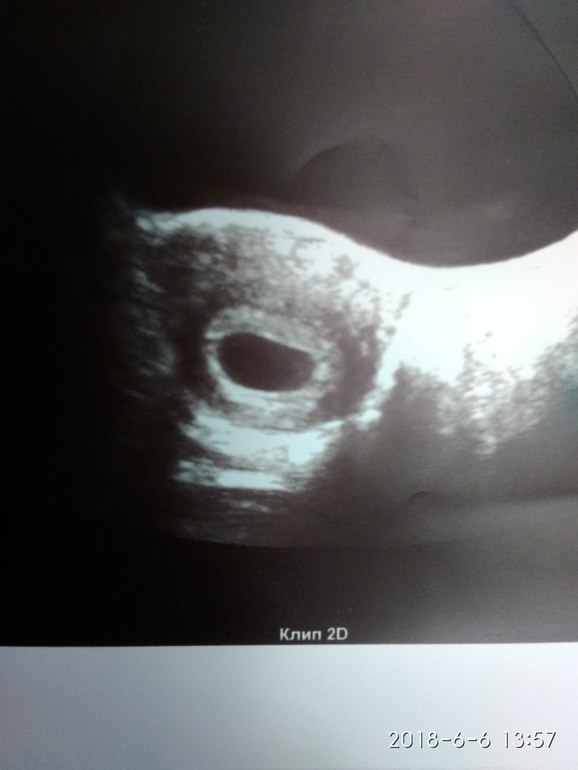 Это может помешать зачатию или увеличить риск выкидыша.
Это может помешать зачатию или увеличить риск выкидыша.