Крис Гоблом — Болезни и прививки — Прививки – Сайт 1796 – гомеопатия и прививки
С любезного разрешения д-ра Криса Гоблома
Оригинал по адресу http://www.whale.to/v/gaublomme2.html
Традиционная вакцина против коклюша является предметом беспокойства в течение всего времени ее существования из-за ее серьезных побочных эффектов. Сотни детей с поражением мозга никогда не останавливали ни производителей вакцины, ни медицинские власти — первые продолжали производить вакцину, а вторые ее использовать. Однако они уже достаточно давно увидели необходимость поиска новой, менее агрессивной вакцины.
Главной идеей было изолировать те антигены, которые необходимы, чтобы вызвать эффективный ответ антител, исключая при этом те, которые ответственны за такие реакции на вакцину как воспаление мозга. Немало лет прошло, пока такая вакцина была сочтена готовой к производству и массовому применению. Япония начала использовать ацеллюлярную вакцину осенью 1981 г. США выдали лицензию на первую ацеллюлярную вакцину для новорожденных и детей в возрасте двух месяцев и старше для первичных серий прививок в июле 1996 г. «Коннот Лэборэториз» выпустила в 1992 г. на рынок трипедию в качестве вакцины для четвертой и пятой ревакцинаций, а в 1996 г. — для первых трех прививок. «Ледерле» выпустила ацельимьюн для четвертой и пятой прививок в 1991 г., а для первых трех доз — в 1996 г.
Эффективность
Трудно доказать эффективность вакцины, если нет согласия даже столь относительно основополагающего понятия как определение болезни, и если никто не знает, какой же уровень антител является защитным. Эта проблема существует в реальности. В опубликованной в 1996 г. статье авторы подчеркивают то же самое: «Не было найдено серологических подтверждений иммунитета», — заявили они (12).
В 1984 г. японцы опубликовали результаты испытания ацеллюлярной вакцины с двумя гемоагглютининами на 5000 детей (1).
Д-р Марк Кэйн из ВОЗ, заявил в августе 1996 г., что новая вакцина не имеет никаких преимуществ в сравнении со старой (3). Исследование вакцины в Сенегале (7) показало даже худшие результаты применения ацеллюлярной вакцины. «С 28-го дня после третей дозы прививки суммарный индекс заболеваемости коклюшем в группе DtaP в сравнении с группой DTwP (RRac/wc) был 1,54 (95 % CI 1,23–1,93)» (7).
«Концентрация антител в крови перед повторной прививкой (в возрасте от 15 до 20 месяцев) была ниже, чем концентрация антител месяц спустя после первичной иммунизации (т.е. в возрасте около 7 месяцев)» (6). Поскольку концентрация антител значительно снижается между 7 и 17 месяцами, почему мы так уверены, что иммунитет длится достаточно долго для того, чтобы защищать в течение всей жизни? Или следующее поколение статей будет убеждать в необходимости повторной прививки каждые 5–10 лет?
Миллер и Эскола, в дебатах по бесклеточной вакцине, пишут в 1998 г.: «Мы согласны, что остается все еще немало вопросов относительно использования ацеллюлярных вакцин. Например, необходимы ли ревакцинации и не ведет ли использование вакцины к снижению времени защиты» (8). Однако производство и широкое использование вакцины началось достаточно давно.
В целом, пятикомпонентные вакцины считаются более эффективными чем двух- или трехкомпонентые в их способности вести к выработке антител. Однако есть противоречащие данные — по некоторым источникам, монокомпонентные вакцины обладают той же эффективностью (10). Поленд (8) заключает из данных исследования Олина с соавт. в Швеции (9), что нет значительной разницы в эффективности клеточной вакцины и трех бесклеточных вакцин при более тяжелых формах коклюша.
Безопасность
Данные по безопасности новой бесклеточной вакцины противоречивы. Исследование в Японии (1), например, упоминает, что «вакцина не имеет существенных побочных эффектов», в то время как введение к той же самой статье сообщает, что «ее токсичность составляет одну десятую токсичности цельноклеточной вакцины…» Как может быть сделано количественное сравнение, если нет «существенных побочных эффектов» вообще? Опровергая это, Поленд (8) сообщает, что в недавнем исследовании в Швеции не было показано никаких преимуществ бесклеточной вакцины в сравнении с цельноклеточной вакциной, как в отношении эффективности, так и в отношении серьезных побочных реакций, включая эпизоды гипотонии и отсутствия ответа на раздражение».
Местные побочные реакции обычно ограничены. Как правило, это покраснение и отек.
Тем не менее иногда случаются и системные реакции. Примеры: повышение температуры, сонливость, возбуждение, длительный пронзительный крик и судороги.
В одном исследовании (4) не было показано разницы со старой вакциной относительно состояния возбуждения, использования жаропонижающих средств, сонливости или анорексии.
Уберол отмечал конвульсии в течение 3 дней после прививки, случавшиеся у одного из 15 912 привитых бесклеточной (DTaP) вакциной (5).
Продолжительный безутешный плач, несомненный симптом воспаления мозга, наблюдался в 1 из 497 случаев применения вакцины (5).
Высокая температура (до 40,50 С) наблюдалась в одном случае на 16 239 использованных доз вакцины (5). Один эпизод гипотонии и отсутствия реакции на раздражения наблюдался у 4 273 реципиентов DTaP (5).
Температура, покраснение места инъекции, опухоль и боль, усиливающаяся по мере увеличения количества уколов (6). «У детей, получающих DTaP четвертой дозой, покраснение места укола и опухоль случаются чаще у детей, ранее получавших DTaP, нежели у получавших ранее DTwP» (6).
Добавки
Производство и хранение новой вакцины против коклюша требует использования определенных веществ, следы которых, соответственно, могут быть обнаружены в небольших количествах в вакцине.
Сульфат аммония использовался в японской вакцине.
Формалин является другим стабилизатором, используемым в производстве вакцины (0,01%). Его токсичность прекрасно известна. Он используется для детоксикации продукта, т.е. для того, чтобы снизить лейкоцитоз и выделение гистамина.
Гидроксид алюминия использовался в качестве адьюванта (0,2 мг/мл) для увеличения продукции антител.
Мертиолят — еще один токсичный продукт, обсуждавшийся в ранее опубликованной статье на эту тему.
Исследования
Одновременное использование нескольких вакцин при том, что изучается и оценивается действие лишь одной из них, является скверной привычкой исследователей вакцин. Естественно, что это ведет к недостоверным результатам.
В раннем японском исследовании, например, токсоиды дифтерии и столбняка были смешаны с коклюшным компонентом, который предстояло изучать (1).
Как и во многих иных исследованиях, время, в течение которого осуществлялся контроль побочных эффектов после прививки, в большинстве исследований по новой вакцине ограничивалось 48–72 часами. Нет необходимости говорить, что многие серьезные побочные эффекты появляются позднее, однако они по определению не могли быть отмечены в этих исследованиях. Тем не менее большинство из этих исследований претендуют на то, чтобы являться доказательными относительно безопасности вакцины.
Дискуссия
Похоже, что бесклеточная вакцина менее токсична, чем ее цельноклеточная предшественница, хотя трудно было бы придумать вакцину более токсичную, чем цельноклеточная вакцина против коклюша. Является ли это достаточным поводом для того, чтобы защищать широкое использование новой вакцины, все еще остается спорным. Национальный Центр информации о прививках (NVIC) требует заменить старую вакцину новой.
Наряду с лучшей статистикой по побочным реакциям в сравнении со старой вакциной, бесклеточная вакцина имеет ряд недостатков. Как указал д-р Марк Кейн из ВОЗ, цена новой вакцины выше, а производство сложнее, при том, что эффективность не больше. Следовательно, он ставит под сомнение использование вакцины для развивающихся стран. Вероятно, по его мнению, более безопасная вакцина важна только для тех, кто может себе ее позволить! Как иронически указывается в статье (3), «… беспокойство относительно побочных реакций характерно исключительно для развитых стран». «Проблема реактогенности АКДС не считается серьезной в развивающихся странах. Потому ли это, что родители и представители здравоохранения более терпимы к небольшим побочным эффектам, или потому, что в менее сутяжническом обществе меньше и адвокатов, но наш опыт расширенной программы иммунизации показывает, что проблема реактогенности АКДС не считается серьезной в развивающихся странах», — заявил Кейн. Еще бы это было проблемой, когда вас выстраивают в ряд и силой заставляют получить прививку!
Прививки взрослым
Вероятно, одним из важных аспектов бесклеточной вакцины является перспектива ее бустерного использования у взрослых.
Довольно странным является то, что цельноклеточная вакцина считается небезопасной для назначения ее для взрослых и детей старше 7 лет, но никто не беспокоится по поводу того, что ее повсеместно получают младенцы.
Сейчас, при наличии «более безопасной» бесклеточной вакцины, готова начаться дискуссия о том, не следует ли назначать ее и взрослым в течение всей жизни. Под заголовком «Управление контроля пищевых продуктов и лекарств (FDA) изучает выполнимость программы прививок против коклюша детям — защита исчезает, и взрослые становятся источниками инфекции для детей», «Новости инфекционных болезней» (Infectious Disease News) начали в Интернете дискуссию в июле 1997 г. Вероятная причина этого беспокойства связана с тем, что прививка против коклюша не дает длительного иммунитета, в то время как создание естественного иммунитета вакцинацией детей невозможно. Результатом этого является увеличение заболеваемости коклюшем взрослых, наблюдаемое в последние годы. «Несмотря на доступность эффективной детской вакцины, случаи коклюша все чаще регистрируются в США. До введения программы прививок против коклюша в 1940-х гг. заболеваемость коклюшем в возрастной группе старше 15 лет была лишь 3 %; это число возросло до 13,5 % между 1989 и 1991 гг., согласно предыдущей статье в ‘Журнале Американской медицинской ассоциации’ (JAMA)» (11).
«Статья в JAMA сообщила о больных до девяти раз посещавших врача из-за кашля, но ни у одного из них не был диагностирован коклюш, и он даже не был включен в дифференциальный диагноз. Тем не менее, согласно этому исследованию, распространенность коклюша среди взрослых равняется 12,4 %».
С другой стороны, в той же самой статье указывается, что тяжелая форма коклюша у взрослых редка, а потому неясно, действительно ли нужно прививать взрослых. Существует вероятность того, что расширение списка прививаемых против коклюша приведет к увеличению группы инфицированных, и, таким образом, еще более усложнит проблему искусственным путем.
Выводы
Несмотря на рекламу и эйфорию в прессе вокруг бесклеточной вакцины против коклюша, огромное количество вопросов и проблем все еще остаются. Резюмируем словами Дж. Поленда: «Хотя сообщается о многочисленных исследованиях, проведенных в разных странах и стоивших миллионы долларов, мы до сих пор не понимаем истинную разницу в эффективности и реактогенности между нынешней и планируемой к использованию вакцинами» (8).
Изучение литературы позволяет нам сделать вывод, что предлагаемая бесклеточная вакцина:
- не более эффективна в предотвращении тяжелых форм коклюша
- не более эффективна в предотвращении серьезных побочных эффектов (хотя здесь данные и противоречивы)
- вызывает меньше местных побочных эффектов, чем цельноклеточная вакцина
- пока что не гарантирует длительного иммунитета
- намного дороже цельноклеточной вакцины
- содержит те же самые токсичные добавки, что и другие вакцины.
Отсюда мы делаем вывод, что новые вакцины имеют серьезное преимущество над старой цельноклеточной вакциной, но его недостаточно для утверждения, что они решили проблемы, столь портившие репутацию старой вакцины.
Соответственно, призыв к массовым прививкам новой вакциной на основании устраненных недостатков старой вакцины и доступности более безопасной вакцины, является ничем не оправданным.
ПРИМЕЧАНИЯ
1. Sato, Y.; Kimura, M.; Fukumi, H.; Development of a pertussis
component vaccine in Japan. Lancet I, 1984; 8369:122–6
2. Aoyama, T.; e.a. Adverse reactions and an antibody response to acellular perlussis vaccine. J
Pediatr 1986; 109:925–30
3. Infectious Diseases in Children:Acellular pertussis vaccines may be impractical for developing
countries. Infectious Diseases in Children Internet Home page, August 1996.
4. Comparison of 13 acellular pertussis vaccines: adverse reactions. Decker MD; et al. Pediatrics 1995; 96:557–66
5. Uberall MA; et al Severe adverse events in a comparative efficacy trial in Germany in infants
receiving either the Lederle/Takeda acellular pertussis component DTP (DTaP) vaccine’ the
Lederle whole-cell component DIP (DIP) or DT vaccine. The Pertussis Vaccine Study Group. Dev Biol
Stand, 1997; 89:83–9
6. Pichichero ME; et al. A safety and immunogenicity comparison of 12 acellular pertussis vaccines
and one whole-cell pertussis vaccine given as a fourth dose in 15-to 20–month–old
children. Pediatrics 1997; 100(5):772–88
7. Simondon F; et al. A randomized double–blind trial comparing a two-component acellular to
a whole-cell pertussis vaccine in Senegal. Vaccine 1977; 15(15): 1606–12
8. Miller, E.; et al. Issues about Pertussis vaccines. Lancet 1998 351:677–9
9. Olin, P.; et al Randomised controlled trial of two-component, three–component and
five-component acellular pertussis vaccines compared with whole–cell pertussis vaccine. Lancet 1997; 350:1569–77
10. Ad Hoc Group for the Study of Pertussis Vaccines. Placebo–controlled trial of two
acellular pertussis vaccines in Sweden — protective efficacy and adverse effects. Lancet 1988; i: 955–60
11. Nennin M, Shinefleld H, Edwards K.. Prevalence and incidence of adult peitussis in an urban
population. JAMA 1996; 275:1672–74.
12. Unanswered questions continue to haunt pertussis vaccine research. Acellular pertussis vaccine
trials showed safety and efficacy, but they did not address other questions. Infectious Diseases
in Children July 1996.
1796web.com
Опыт применения комбинированных вакцин, содержащих ацеллюлярный коклюшный компонент
Опыт применения комбинированных вакцин, содержащих ацеллюлярный коклюшный компонент
А.Ю. Волянский, А.Д. Ярмыш, А.А. Ямчицкая
Центр иммунопрофилактики и иммунореабилитации, г. Харьков
Введение в мире массовой вакцинопрофилактики коклюша в середине прошлого века позволило снизить заболеваемость с 200-400 до 10-20 на 100 тыс. населения [1,4]. На сегодняшний день явно обозначились недостатки клеточного коклюшного компонента, входящего в состав КДС-вакцин, в том числе российской вакцины АКДС, массово применяемой в Украине. Это высокая реактогенность (принято считать, что подавляющее большинство случаев побочных эффектов при введении АКДС обусловлено именно коклюшной составляющей) и довольно низкая эффективность вакцины (по различным данным, уровень сероконверсии — относительного индикатора уровня защищенности — не превышает 65-85% после первичного курса иммунизации [1,4]). Врачи инфекционных отделений детских стационаров наверняка подтвердят тот факт, что среди заболевших коклюшем немалый процент составляют привитые дети (хотя мы не можем исключить и возможность выдачи определенного количества подложных медицинских документов). Гипертрофированная боязнь побочных эффектов, как среди родителей, так и среди педиатров, ведет к неоправданно частому откладыванию введения первой дозы вакцины на второе полугодие жизни ребенка и зачастую, необоснованной замене АКДС на вакцины, не содержащие коклюшный компонент (АДС и АДС-М). В результате, грудные дети, дающие самый высокий процент летальных исходов при коклюше, оказываются беззащитными перед этим опасным заболеванием. Устранить указанные недостатки противококлюшной вакцинопрофилактики может помочь применение недавно появившихся и в Украине комбинированных вакцин с бесклеточным коклюшным компонентом, обладающих более низкой, по сравнению с классической АКДС, реактогенностью и не уступающих своим предшественникам по иммуногенности.
В декабре 1998 года в Украине была зарегистрирована первая АаКДС вакцина, содержащая ацеллюлярный коклюшный компонент (далее АКК). В мае 2003 года процедуру регистрации прошли 4-х и 5-валентные вакцины «Тетраксим» и «Пентаксим» компании «Авентис Пастер» (Франция). Все вышеуказанные вакцины содержат 30 МЕ дифтерийного, 40 МЕ столбнячного и 25 мкг коклюшного анатоксинов, 25 мкг коклюшного филаментозного гемагглютинина в одной дозе. В зависимости от состава, вакцины также содержат ИПВ, рекомбинантную вакцину против гепатита В и конъюгированную вакцину против ХИБ-инфекции в различных комбинациях.
Применение вакцин с бесклеточным коклюшным компонентом сдерживается в Украине высокой ценой и, как следствие, минимальным уровнем бюджетных закупок. Основной сегмент рынка медицинских услуг по вакцинации этими препаратами — частные медицинские центры. В Центре иммунопрофилактики и иммунореабилитации, работающем на базе Института микробиологии и иммунологии им. И.И. Мечникова (г. Харьков), вакцины, содержащие АКК, применяются с сентября 2002 года. В 2002 году было введено 5 доз, в 2003 году — 52 дозы, за 9 месяцев 2004 года — 78 доз. На протяжении двух лет работы с вакцинами, содержащими АКК, мы наблюдаем значительное изменение отношения к этим препаратам со стороны как родителей, так и специалистов, обусловленное, по-видимому, повышением уровня информированности. Если первые случаи применения АаКДС приходились на детей с яркой фоновой патологией (тяжелые атопические дерматиты, пороки сердца, заболевания нервной системы), то на сегодняшний день более половины инъекций этих вакцин проводится здоровым детям из-за закономерного и оправданного желания родителей и врачей свести к минимуму вероятность возникновения каких-либо поствакцинальных реакций.
Нами было проведено изучение реактогенности применяемых в Украине комбинированных вакцин с АКК. Было рассмотрено 100 случаев применения вакцин, содержащих АКК у 51 ребенка (36 детей получали только комбинированные вакцины с АКК, 26 из них — «Пентаксим», 15 детей получали как вакцины с АКК, так и с клеточным коклюшным компонентом (далее ККК)). В качестве контрольной мы использовали группу из 42 детей, получивших 100 инъекций вакцины АКДС. Вакцины вводились в дозе 0,5 мл внутримышечно в переднебоковую область бедра. Предполагалось, что реакциями на дифтерийный, столбнячный анатоксины, ИПВ, вакцины против гепатита В и ХИБ-инфекции можно пренебречь, в силу их редкости и малой выраженности, согласно литературным данным. Вакцины, содержащие мертиолят, не использовались.
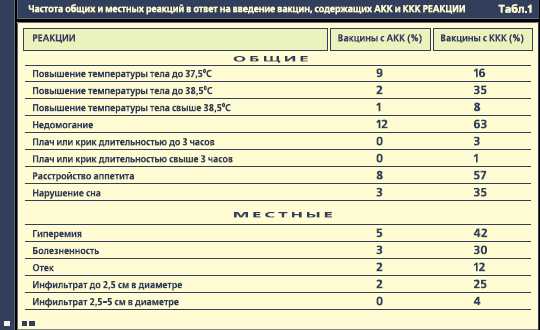
Статистически значимых различий количества и силы реакций между первым, вторым, третьим и четвертым введением одной и той же вакцины не было выявлено для вакцин, содержащих как АКК, так и ККК, поэтому эти данные нами опущены. Непосредственное наблюдение за привитыми велось в течение 30 минут после инъекции, затем проводился контроль общих и местных реакций на исходе первых и вторых суток и далее в течение месяца. В соответствии с общепринятыми методиками, учитывались общие реакции: повышение температуры тела, длительный плач или крик, недомогание, расстройство аппетита, нарушение сна; местные: гиперемия, отечность, местная болезненность, инфильтрат [2].
В ответ на введение вакцин с АКК общие реакции имели место в 12% случаев, из них сильные — в 1%, местные реакции развивались в 5% случаев, все они были слабыми. После применения вакцины с ККК общие реакции отмечались в 63% случаев, из них сильные и чрезмерно сильные — в 8%, местные — в 48% случаев, из них средней интенсивности — в 4%. Дважды инфильтрат в месте инъекции вакцины с ККК сохранялся более 1 месяца, в одном случае имела место чрезмерно высокая гипертермия — до 40,0 оС, купированная к исходу 1 суток после введения ККК-вакцины (Табл.). В целом, можно сказать, что бесклеточные коклюшные вакцины показали очень низкую реактогенность — только в одном случае имела место высокая температурная реакция, все местные реакции (5 случаев) отнесены к слабым и исчезали в течение 2 суток без лечения. Значимых различий между реакциями на коммерческие препараты различных производителей не выявлено. Существенное различие в количестве и силе реакций в ответ на введение вакцин, содержащих АКК и ККК, очевидно, обусловлено именно различиями коклюшного компонента, в первую очередь, наличием липополисахарида в клеточной вакцине. Оценить значимость дополнительного антигена — пертактина можно только после сравнительной оценки клинической эффективности различных вакцин с АКК. Практически же, мы рекомендуем в каждом конкретном случае использовать ту бесклеточную вакцину, которая позволит выдерживать оптимальные интервалы при вакцинации против гепатита В, полиомиелита и гемофильной инфекции. Учитывая то, что высокая цена на сегодняшний день является основным сдерживающим фактором массового использования ацеллюлярных коклюшных вакцин, вакцина «Тетракок», содержащая ККК и не содержащая мертиолят, обладающая высокой иммуногенностью при средней реактогенности, должна оставаться в арсенале центров вакцинации. Также «Тетракок», благодаря наличию в ее составе ИПВ идеально вписывается в украинский календарь вакцинации и позволяет решать задачу прекращения циркуляции вакцинных штаммов полиовирусов.
Литература:
- Учайкин В.Ф., Шамшева О.В. Вакцинопрофилактика. Настоящее и будущее, — М., ГЭОТАР-МЕД, 2001. — 400.
- Медуницын Н.В. Вакцинология, — М., Триада-Х, 1999. — 272.
- Kurstak E. Modern vaccinology. Toronto, 1998. — 373.
- Сanadian immunization guide. Fourth edition — 1999. Reprinted 2001. 153.
© А.Ю. Волянский, А.Д. Ярмыш, А.А. Ямчицкая, 2004
medi.ru
Вакцинация против коклюша. Вакцина АКДС
 Известно, что защита от инфекций, наработанная матерью в течение жизни, передается ребенку через плаценту. Но, к сожалению, против коклюша такую защиту мать передать не может. Поэтому ребенок практически сразу после рождения оказывается абсолютно беззащитным перед грозной инфекцией. В связи с этим огромное значение приобретает своевременная вакцинация детей. Почему вакцинация против коклюша вот уже несколько десятилетий остается актуальной и все попытки отказаться от нее приводили лишь к росту заболеваемости?
Известно, что защита от инфекций, наработанная матерью в течение жизни, передается ребенку через плаценту. Но, к сожалению, против коклюша такую защиту мать передать не может. Поэтому ребенок практически сразу после рождения оказывается абсолютно беззащитным перед грозной инфекцией. В связи с этим огромное значение приобретает своевременная вакцинация детей. Почему вакцинация против коклюша вот уже несколько десятилетий остается актуальной и все попытки отказаться от нее приводили лишь к росту заболеваемости?
Коклюш — инфекция достаточно контагиозная, т.е. очень заразная.
К сожалению, сегодня нельзя сказать, что мы можем полностью ее контролировать. Это связано с тем, что детей вакцинируют лишь в возрасте до 4-х лет. Дети более старшего возраста, подростки и взрослые со временем утрачивают тот иммунитет, который их организм наработал в результате вакцинации. Поэтому заболеваемость коклюшем остается высокой среди школьников и взрослых, которые хоть и болеют значительно более легкими формами коклюша, но все же остаются переносчиками коклюшной инфекции. Если в довакцинальную эру дети заражались в основном от своих сверстников, то сегодня маленькие дети часто заражаются от взрослых, т.е. источником коклюша служат чаще всего старшие братья и сестры, посещающие школу, либо родители.
Вакцинация против коклюша проводится с 60-х годов прошлого века, поэтому современные родители практически не видят тяжелого течения коклюша. С одной стороны, это говорит о высокой эффективности программы вакцинации, а с другой — не дает некоторым родителям достаточно оснований считать коклюш серьезным заболеванием, требующим обязательной вакцинации против него. Однако, коклюш — опасное заболевание, и того, кто слышал коклюшный кашель, не нужно убеждать в необходимости вакцинировать своих детей.
Как сегодня оценивается безопасность вакцины АКДС, известной своей реактогенностью?
Вакцина АКДС (Адсорбированная коклюшно-дифтерийно-столбнячная вакцина) была создана более 50 лет назад. К сожалению, эта вакцина, как и другие цельноклеточные вакцины, вызывает больше всего опасений и нареканий в плане возникающих на нее реакций. Однако именно данная цельноклеточная вакцина, относящаяся к первому поколению коклюшных вакцин, весьма эффективна и дает надежный продолжительный иммунитет. Учитывая эти факторы, и согласно рекомендации ВОЗ, цельноклеточная коклюшная вакцина до сегодняшнего дня остается основным инструментом борьбы с коклюшем.
Что такое цельноклеточная вакцина
Для производства всех АКДС-вакцин используются инактивированные («убитые») коклюшные микробы. Для цельноклеточных используется весь микроб (целой клеткой). Для бесклеточных (ацеллюлярных) — только его фрагменты. Поэтому коклюшный компонент цельноклеточной вакцины содержит около 3000 антигенов, а бесклеточной (ацеллюлярной) — от 2 до 5 антигенов. То есть нагрузка на иммунную систему уменьшается в 1-1,5 тысячи раз.
Что касается реакций, вызываемых вакциной АКДС, то частота и тяжесть их сильно преувеличена. Родители часто путают вероятные осложнения, вызываемые коклюшем, с возможными реакциями на прививку.
К осложнениям относятся тяжелые, стойкие нарушения в состоянии здоровья вследствие профилактических прививок (параличи, судорожный синдром, другие виды неврологических нарушений). Эти ситуации возникают очень редко. Реакции на вакцинацию — это нетяжелые внешние проявления вакцинального процесса (подъем температуры, местные реакции). Важно понимать, что наличие реакции у ребенка не является патологией, это вариант нормы.
Наиболее частой реакцией на вакцину АКДС является подъем температуры (в 30-50 % случаев) и местная реакция в виде уплотнения (инфильтрата) в месте введения вакцины. Возникновение инфильтратов связано с тем, что действующие вещества вакцины (антигены) «насаживаются» на носитель (о чем говорит слово «адсорбированный» в названии вакцины) и поэтому не сразу попадают в кровь, а «сходят» с носителя постепенно.
Медленное поступление антигенов позволяет организму выработать максимальную защиту от инфекции. Кроме того, такой механизм действия делает вакцину более безопасной и эффективной. Но именно из-за того, что антигены не сразу уходят из этого депо, и образуются данные местные реакции.
Они характерны для всех адсорбированных вакцин (АКДС, АДС, АДС-М, АС, зарубежные аналоги АКДС).
Однако, как правило, и температурная, и местная реакции являются нормой.
Такой ответ на введение вакцины развивается не позднее одних суток после прививки и длится не более трех суток.
Реакции, появляющиеся позже и длящиеся дольше, вызваны не прививкой, а, например, ОРЗ, кишечной инфекцией или в результате прорезывающихся у ребенка зубок и т.д.
Причину в этом случае нужно искать вместе с врачом, чтобы исключить тяжелое заболевание. Самой неприятной возможной реакцией на введение цельноклеточной АКДС-вакцины являются неврологические проявления, которые возникают у очень небольшого числа детей (1-2 %).
Например, если у ребенка были проблемы с мышечным тонусом или наблюдалось повышенное внутричерепное давление, после вакцинации эти проблемы могут усугубляться на какой-то период времени. Иногда может наблюдаться задержка в развитии, но, к счастью, благодаря усилиям неврологов и родителей все функции в скором времени восстанавливаются. Однако, безусловно, неприятный осадок от самого существования данных реакций остается не только у родителей, но и у докторов. Судорожные реакции очень редки, могут встречаться на первое поколение АКДС-вакцины.
Эффективность бесклеточной вакцины АКДС
В мире было много дискуссий по поводу соотношения пользы и риска использования АКДС-вакцин первого поколения. Некоторые страны, такие, например, как Швеция и Япония, отказались от вакцинации детей от коклюша и вернулись к государственным вакцинальным про граммам только после создания коклюшных вакцин нового поколения.
На сегодняшний день существуют научные доказательства, что причины возникавших энцефалопатии, которые считались следствием введения АКДС-вакцины, были совершенно другими (инфекционные, генетические заболевания). Было также доказано, что АКДС-вакцина не может вызвать тяжелые повреждения мозга.
В ходе работы над вакциной АКДС нового поколения был модифицирован коклюшный компонент вакцины, в результате чего она стала ацеллюлярной, или бесклеточной. Таким образом, вакцина нового поколения обеспечивает стойкую, надежную защиту от инфекции, при ее применении риски неврологических реакций практически сведены к нулю, а также значительно снижены риски вообще каких-либо реакций. Современное поколение вакцин против коклюша (бесклеточные) содержат от 2 до 5 антигенов.
Для сравнения: вакцина первого поколения (цельноклеточная) содержит 3000 антигенов. Понятно, что вакцины нового поколения более комфортно переносятся детьми. Вакцины нового поколения очень скоро вошли в программы вакцинации всех развитых стран. Но стоимость их, безусловно, гораздо более высокая, чем стоимость вакцины прежнего поколения. Поэтому сегодня по программе государственного обеспечения мы имеем на вооружении только вакцину первого поколения.
Вакцины нового поколения разрешены к применению на территории Российской Федерации и находятся в свободном доступе. Это 4 вакцины (семейства французских и бельгийских вакцин), которые можно привить в условиях коммерческих медицинских центров. В зависимости от входящих в них компонентов они имеют разные коммерческие названия.
Среди них, помимо простой вакцины АКДС, есть вакцины, которые в одном шприце содержат вакцину АКДС и неживую вакцину против полиомиелита или АКДС и вакцину против гемофильной инфекции.
Также существует шестикомпонентная вакцина, в состав которой входит АКДС, инактивированная полиомиелитная вакцина, гемофильная вакцина и вакцина против гепатита В. Причем вакцины, содержащие три компонента, по переносимости идентичны вакцинам, содержащим шесть компонентов.
Сегодня комбинированные вакцины на основе АКДС — это более перспективный и правильный путь, поскольку представляют более щадящий способ защиты от инфекции.
Таким образом, с появлением вакцин нового поколения педиатры обрели возможность без риска серьезных реакций защитить детей с различными тяжелыми заболеваниями от многих опасных инфекций, в частности от коклюша.
Поэтому родители, которые имеют финансовую возможность и понимают разницу между вакцинами нового и первого поколения, могут обратиться в коммерческие медцентры, где их детям сделают прививку.
По какой схеме проводится вакцинация против коклюша
Новорожденные не имеют иммунитета от коклюша, поскольку не получают антител против коклюша в период внутриутробного развития. Это серьезная проблема, и поэтому все вакцинальные программы, которые существуют в мире, предусматривают достаточно раннее начало вакцинации против коклюша — с 2-3-месячного возраста. В России детей от коклюша начинают прививать с 3-х месяцев.
Схема применения АКДС-вакцины состоит из 4 доз. Первые три дозы вводятся с интервалом 1,5 месяца (обычно в 3, 4,5 и 6 месяцев), четвертая доза (ревакцинация) — в 18 месяцев. Данный комплекс прививок защищает детей в течение 5-7 лет, поэтому, к сожалению, к школьному возрасту они утрачивают этот иммунитет.
Родители должны помнить о том, что достойная защита от коклюша вырабатывается лишь через месяц после третьей прививки, поэтому очень важно сделать ее вовремя.
Вообще в мире против коклюша прививают не только детей грудного возраста, но и дошкольников, подростков и взрослых. В развитых странах сегодня очень популярна так называемая кокон-иммунизация, когда вакцинируются все члены семьи, где есть беременная женщина, создавая тем самым некую подушку безопасности вокруг нее и будущего ребенка, у которого в силу возраста еще нет иммунитета против этой болезни. В нашей стране, к сожалению, это сделать пока невозможно.
Что делать, если календарные сроки введения АКДС не соблюдались
Просто продолжить вакцинацию. При любом интервале между дозами АКДС курс прививок продолжается, ничего начинать заново не требуется. Необходимо помнить, что при значительном увеличении интервалов может снижаться эффективность вакцинации. Поэтому без веских причин откладывать проведение прививки не стоит.
Требуется ли какая-нибудь подготовка перед прививкой АКДС?
Для здорового ребенка никаких подготовительных мероприятий не требуется. Если у малыша есть какое-нибудь хроническое заболевание, необходимо обсудить необходимость и объем обследования и медикаментозного «прикрытия». Хотелось бы предостеречь родителей от самостоятельного назначения препаратов. Необходимо знать, что прием противоаллергических препаратов значительно снижает эффективность прививки.
Противопоказания для введения ребенку вакцины АКДС
Противопоказания, конечно, есть.
Именно для этого необходим осмотр педиатра, который определится с наличием противопоказаний к вакцинации. У современного поколения вакцин (ацеллюлярных) противопоказаний существенно меньше, чем у цельноклеточных.
Если у родителей есть вопросы, они могут записаться на прием к специалисту в Городской кабинет иммунопрофилактики и получить квалифицированную консультацию независимо от места прописки. Специалист с учетом особенностей состояния ребенка подберет наиболее эффективные и безопасные вакцины, составит план прививок, согласно которому в дальнейшем можно провести вакцинацию под наблюдением участкового врача.
forsmallbaby.ru
Бесклеточная (ацеллюлярная) вакцина
Бесклеточная (ацеллюлярная) вакцинаПосле смерти двух младенцев от прививки DPT в 1976 г. в Японии срочно начали разрабатывать новую коклюшную вакцину. Она была лицензирована там и стала применяться в 1981 г. Бесклеточная вакцина представляет собой смесь коклюшного анатоксина и антигенов возбудителя болезни, иммунная реакция в ответ на введение которых должна обеспечивать невосприимчивость к болезни. Сам возбудитель в таких вакцинах отсутствует. Эта вакцина выпускается рядом компаний и различается лишь по количеству содержащихся в ней антигенов.
Предполагалось, что за счет «прицельного» выделения антигенов эта вакцина будет свободна от побочных явлений, характерных для ее цельноклеточной (корпускулярной) предшественницы. Однако, похоже, ожидания эти оправдались лишь частично, поскольку и по сей день точно неизвестно, какие именно антигены запускают иммунный ответ, а какие обусловливают тяжелые реакции со стороны нервной системы заболевшего или привитого; потому и антигенный набор вакцины построен больше на гипотезах, чем на точных сведениях. Вслед за введением новой вакцины были отмечены как стандартные местные реакции, так и системные, например конвульсии[528].
После тщательного изучения двух японских вакцин в 1986-1987 г. шведская Национальная бактериологическая лаборатория отказала японцам в продолжении процедуры лицензирования этих вакцин — как вследствие того, что эффективность вакцины оказалась не только не выше, но, вероятно, и ниже, чем у цельноклеточной вакцины, так и вследствие ряда необъяснимых смертей привитых этими вакцинами детей от присоединения бактериальной инфекции (скончались 11 детей из 2800 получивших прививки)[529].
Представитель ВОЗ д-р Марк Кейн заявил в 1996 г., что новая вакцина не имеет никаких преимуществ перед старой в смысле эффективности. Что касается главного своего предназначения — снизить число тяжелых последствий использования коклюшной вакцины — новая вакцина, согласно данным некоторых исследований, не оправдала возлагавшихся на нее надежд. Разницы в количестве случаев СВДС (симптом внезапной детской смерти) и близких к нему состояний, госпитализаций, энцефалопатии и отставания в развитии относительно цельноклеточной вакцины не обнаружилось[530].
Впрочем, другие исследования были более благосклонны к бесклеточной вакцине. Неоднократно цитировавшиеся в этой главе Дэвид и Марк Гейеры исследовали базу данных Системы сообщений о побочных эффектах прививок (VAERS) и обнаружили, что бесклеточная вакцина дает значительно меньшее количество побочных реакций любого рода[531].
Кроме того, в США имелся опыт ее производства еще с 1930-х годов, и он показывал, что бесклеточная вакцина действительно дает меньшее количество тяжелых побочных эффектов. Российские авторы сообщают: «Реактогенность бесклеточных вакцин намного ниже реактогенности корпускулярной вакцины. На введение бесклеточной коклюшной вакцины значительно реже возникают как общие, так и местные реакции (лихорадка — в 7 раз, гипертермия — в 4, отечность — в 5-6, болезненность — в 14 раз»)[532].
Важной для понимания законов, по которым работает прививочный бизнес, будет информация о том, что немалое количество американских компаний разрабатывало, начиная с 1920-х годов, эту, вероятно, более безопасную вакцину. Однако в итоге все они отказались от ее массового производства и маркетинга. Причина? Раз заявив, что располагают новой, более безопасной вакциной, они могли стать объектом судебных исков, в которых истцы бы утверждали, что компании знают, как делать лучший продукт, но в силу тех или иных причин продолжают поставлять на рынок худший, более опасный[533].
В1985 г. американский Институт медицины признал возможность тяжелых неврологических осложнений после прививки DPTH рекомендовал заменить цельноклеточную вакцину против коклюша на бесклеточную (ацеллюлярную). Рекомендация была проигнорирована, а вместо разработки безопасной вакцины производители DPT предпочли тратить деньги на подкуп «независимых экспертов». Однако в 1990-х годах, несмотря на все ухищрения Черри и Ко и их работодателей, ситуация изменилась. Несколько очень крупных исков, после многолетнего разбирательства, были все же выиграны в рамках Национальной программы компенсаций пострадавшим от прививок. Три раза собиравшаяся при Национальном институте здоровья США экспертная группа пришла к выводу о доказанности связи между вакциной DPTH поражением мозга и подчеркнула необходимость перейти на новую, более безопасную вакцину. И, главное, настойчивость японцев и тех, кто их поддерживал (например, групп родителей), поставила на повестку дня вопрос о скором лицензировании бесклеточной вакцины. Чтобы не проиграть сражение за рынок, американские компании вынуждены были отказаться от битой ставки на «мнения экспертов» и начать разрабатывать свои собственные бесклеточные коклюшные вакцины. Сегодня в СШАцельноклеточная вакцина производится только на экспорт, а на внутреннем рынке с 2001 г. используется лишь бесклеточная вакцина.
Помимо прочих сложностей и вопросов известно, что производство новой вакцины значительно сложнее, а цена вакцины в развитых странах 19,43 $, примерно на 9 $ превышает цену старой, что, учитывая необходимость многократного употребления вакцины, в рамках национальных прививочных программ небогатых стран может оказаться совершенно неприемлемой, хотя и утверждается, что при изначально более высокой стоимости бесклеточной вакцины ее применение снижает общемедицинские расходы (уходы за заболевшим после прививки ребенком и особенно выплата компенсаций за инвалидность и смерти привитых цельнокле-точной вакциной)[534].
Вопрос о лучших, более безопасных, но значительно более дорогих вакцинах ждет своего решения. Как и вопрос, нужны ли вообще коклюшные вакцины.
Надеюсь, что в этой главе я дал достаточно сведений для желающих серьезно задуматься о том, совместимы ли прививки против коклюша со здоровьем ребенка и не следует ли держаться как можно дальше от этого очень сомнительного блага. Выбор остается за родителями!
Выводы
Коклюш — болезнь преимущественно детского возраста, бывшая некогда опасной в европейских странах и в Америке и остающаяся таковой для стран третьего мира сегодня. Раз перенесенная болезнь оставляет стойкий, обычно пожизненный иммунитет, который защищает и будущих детей в самом опасном по осложнениям коклюша возрасте.
Коклюшная вакцина (коклюшная составляющая многокомпонентных вакцин) традиционно считается одной из самых малоэффективных и одной из самых опасных из существующих ныне вакцин. Продолжающиеся в национальных масштабах прививочные кампании смещают болезнь в самый опасный, младенческий возраст, лишают женщин возможности приобрести естественный иммунитет и увеличивают число больных стертыми формами коклюша взрослых, которые заражают детей.
Новая бесклеточная (ацеллюлярная) вакцина также отнюдь не свободна от побочных эффектов, хотя, вероятно, более безопасна и эффективна, чем традиционная цельноклеточная. Есть данные, свидетельствующие в пользу высокой эффективности безопасной гомеопатической профилактики коклюша.
В развитых странах для коклюша сегодня характерно мягкое течение; серьезные случаи, осложнения и тем более смерти представляют собой крайне редкое явление и встречаются почти исключительно у детей в возрасте до шести месяцев.
Корь
Дата добавления: 2015-08-09; просмотров: 84 | Нарушение авторских прав
Читайте в этой же книге: Гепатит В — что делать? | Болезнь | Вакцина | Безопасность | Эффективность | Болезнь | Вакцина | Безопасность | Эффективность | Болезнь |
mybiblioteka.su — 2015-2019 год. (0.019 сек.)
mybiblioteka.su
преимущества в безопасности и иммунологическая эффективность – тема научной статьи по медицине и здравоохранению читайте бесплатно текст научно-исследовательской работы в электронной библиотеке КиберЛенинка
■ В. К. Таточенко, М. Д. Бакралзе. Пневмококковая инфЕкиия — недооцениваемая угроза здоровью летей
35. Периодические и географические различия серотипового спектра пневмококков у детей с респираторными заболеваниям и у здоровых носителей / В. К. Таточенко и др. // ЖМЭИ. — 1994.- №3. —С. 3 — 10.
36. Clinical characteristics of children with complicated pneumonia caused by Streptococcus pneumoniae / T. O. Tan et al.// Pediatncs. — 2002. — V. 110 (1). — Р. 1—6.
37. Опыт применения вакцин пневмо и ваксигрипп у инфицированных микобактериями туберкулеза детей из групп риска /
И. Е. Костяная, А. Ф. Мейснер, В. А. Аксенова, А. П. Батуро // Вакцинация. — 2002. — № 1 (19). — С. 10—11.
38. Вакцинация против гриппа, пневмококковой менингококковой и Hib-инфекции часто болеющих детей. — ГУ НЦЗД РАМН, М., 2005.
39. Cost-effectiveness of pneumo coccal vaccine / Evidence frjm the first 5 years of use in the United States in corporating herd effect / T. G. Ray et al. // Pediatr. Infect. Dis.J. — 2006. — V. 25 (6). — Р. 494—501.
Ацеллюлярные коклюшные влшины: преимущества в безопасности и иммунологическая эффективность
О. В. ШАМШЕВА
ГОУ ВПО Российский государственный медицинский университет, Москва
Представлен обзор исследований, посвященных изучению иммуногенности, реактогенности и безопасности комбинированных ацеллюлярных коклюшных вакцин, иммунизирующим компонентом которых является коклюшный анатоксин и филаментозный гемагглютинин.
Ключевые слова: коклюш, вакцинация, иммуногенность, реактогенность УДК 616.921.8-097
ACELLULAR PERTUSSIS VACCINES; ADVANTAGES IN SAFETY AND IMMUNOLOGICAL EFFECTIVENESS
O. V. SHAMSHEVA
Russian Statement MedicaL University, Moscow
The review of studies about immunogenicity, reactogenicity and safety of combined acellular pertussis vaccines, the immunizing component of which is pertussis toxoid and filamentary hemagglutinin is presented.
Key words: pertussis, vaccination, immunogenicity, reactogenicity
За последние 30 лет пройден большой путь в понимании молекулярной микробиологии Bordefella pertussis, эпидемиологии коклюшной инфекции, ее течения и диагностики. Эти успехи реализовались в создании ацел-люлярного компонента коклюшной вакцины (АаКДС), предназначенной как для вакцинации детей (DTaP), так и подростков и взрослых (Tdap).
В допрививочный период коклюшная инфекция характеризовалась циклическими эпидемическими подъемами с периодичностью в 5—10 лет. В 1940-е годы на территории СССР показатели заболеваемости составляли более 300 на 100 тыс. населения, при этом большинство заболевших (93%) составляли дети до 10 лет жизни, в том числе до 10% — дети грудного возраста. Массовая специфическая профилактика коклюша в нашей стране начала проводиться с 1 959—1 960 гг. и уже в следующем десятилетии (с 1972 по 1980 гг.) показатели заболеваемости установились на низком уровне — 5,0—12,3 на 100 тыс. населения и в тысячи раз снизилась летальность. Начиная с 1981 г. показатели охвата прививками детского насе-
Шамшева Ольга Васильевна — д. м. н., проф., зав. каф. инфекционных болезней у детей Московского факультета РГМУ, 117049, Москва, 4 Добрынинский пер., 1, МДГКБ, т. (495) 236-01-55.
ления снизились, и сразу же наблюдался подъем заболеваемости коклюшем, достигший пиков в 1985 и 1994 гг.— 28,7 и 32,9 на 100 тыс. населения соответственно. При этом доля детей до 14 лет жизни среди заболевших составляла 98%, из них более 20% — дети от 1 до 7 лет.
Стабильно высокий уровень охвата прививками против коклюша (АКДС) детей раннего возраста, наблюдавшийся в последнее десятилетие, вновь привел к снижению заболеваемости коклюшем с 19,06 до 5,72 на 100 тыс. населения в 1998 и 2006 гг. соответственно. Анализ возрастной заболеваемости коклюшем, проведенный по материалам официальной статистики, показал, что, несмотря на то, что по-прежнему основной контингент зарегистрированных больных представлен детьми 0—14 лет (95— 98%), самый интенсивный подъем отмечается в возрасте старше 5 лет и до года [1]. Аналогичная картина наблюдается в США, Канаде, Австралии, в странах Западной Европы, где средний возраст заболевших передвинулся на 10—14 лет и старше. Таким образом, очевидно, что необходима новая стратегия борьбы с коклюшем. ВОЗ считает, что в странах с ограниченными ресурсами, где цельноклеточная вакцина пользуется доверием, именно она остается препаратом выбора. Ее высокая профилактическая эффективность продемонстрирована в Японии
■ О. В. шамшева. Ацеллюлярные коклюшныЕ вакцины: преимущества в БЕзопасности и иммунологическая эффективность
(Исомура, 1988; Кимура, 1988; Сато, 1997), когда отказ от массовой вакцинации АКДС в течение 3-х лет привел к увеличению числа случаев коклюша более чем в 100 раз и резкому повышению смертности. В Англии снижение охвата прививками против коклюша с 77 до 30% в 1977—1978 гг. привело к эпидемии с регистрацией 102 500 случаев. Необходимо отметить, что в обеих странах ситуация нормализовалась только после повышения уровня охвата прививками. Однако, несмотря на эффективность вакцинации, циркуляция возбудителя коклюшной инфекции не прекращается, поэтому, для того, чтобы сократить заболеваемость коклюшем к 2010 г. до уровня <1 на 100 тыс. населения согласно рекомендациям Европейского Комитета ВОЗ [2], потребуется не только совершенствование программ вакцинации, но и их существенная модификация. Исследования, проведенные в течение последних 15 лет, велись в трех направлениях [3]:
■ изучение причин продолжительного кашля у подростков и взрослых,
■ оценка иммуногенности вакцин после 2-х кратного и более их введения,
■ изучение заболеваний, характеризующихся продолжительным кашлем, у определенных групп населения.
Прорывом, благодаря которому удалось решить многие вопросы в этой области, стало использование метода иммуноферментного анализа, позволяющего с высокой точностью определять раздельно уровни антител класса IgG и IgA к коклюшному токсину.
Было установлено, что приблизительно в 13—20% случаев причиной кашля у подростков и взрослых в США является Bordetella pertussis. При этом ежегодно инфицируется 1—6,7% лиц разного возраста и 0,37—1,5% из них имеют типичный коклюш (сопровождающийся кашлем). Эти данные позволили предположить, что ежегодно в США коклюшем переболевает от 800 тыс. до 3,3 млн подростков и взрослых. С другой стороны, диагностика коклюша до сих пор вызывает затруднения. Большинство случаев не распознаются и диагностируются как бронхиты или заболевания верхних дыхательных путей. Кроме того, атипичная форма коклюша встречается в 4— 22 раза чаще, чем типичная [3]. На сегодняшний день именно подростки и взрослые с атипичным коклюшем являются основным источником инфекции для детей первых месяцев жизни, у которых заболевание протекает особенно тяжело, и могут наблюдаться летальные исходы. Несмотря на то, что, по-видимому, отсутствует корреляция между уровнем антител и защищенностью против коклюша, данный факт не является бесспорным. В эксперименте на мышах было показано, что антитела и Т-клеточ-ный иммунный ответ ко многим коклюшным антигенам являются протективными [3]. Несомненно, что иммунный ответ на инфекционное заболевание у мышей отличается от такового у людей. И, тем не менее, исследованиями, проведенными 50 лет назад, установлено, что степень за-
щиты от коклюша у детей коррелирует с высокими титрами агглютинирующих антител (агглютининов). Сегодня очевидно, что к антигенам (агглютиногенам), к которым формируются антитела, и которые вызывают агглютинацию, относятся фимбриальный протеин 2 и 3 серотипов, белок пертактин и липополисахариды. Очищенные антигенные комплексы, свободные от компонентов, вызывающих нежелательные реакции, могут быть выделены разными методами из бактериальной массы, а также синтезированы химически или получены с помощью генной инженерии. В состав современных бесклеточных коклюшных вакцин входят коклюшный токсин (КТ), в разных количествах и инактивированный различным путем (анатоксин), филаментозный гемагглютинин (ФГА), белок пертактин (ПРН) и антигены фимбрий типов 2 и 3; максимальное число антигенов в ацеллюлярной коклюшной вакцине — 5.
Безопасность и высокая иммуногенность ацеллюляр-ной коклюшной вакцины в комбинации с дифтерийным и столбнячным анатоксинами была доказана многими клиническими исследованиями [4], а впервые разрешена для прохождения клинических испытаний в Японии. Впоследствии основное внимание было сфокусировано на создании комбинированных вакцин на основе уже существующей АаКДС. При этом в разных комбинациях в препарат вошли вакцина против гепатита В, Хиб-ком-поненты и инактивированная полиовакцина. Были созданы вакцины АаКДС-ГВ, АаКДС/Хиб, АаКДС-ИПВ, АаКДС-ГВ/Хиб, АаКДС-ГВ-ИПВ, АаКДС-ИПВ/Хиб, и, наконец, АаКДС-ГВ-ИПВ/Хиб. Странами, которые первые лицензировали эти вакцины, стали Франция и Германия (табл. 1).
В настоящее время одной только компанией «Sanofi Pasteur» (Франция) производится серия комбинированных препаратов, включающих в свой состав ацеллюляр-ную коклюшную вакцину: Триасел (АаКДС), Тетравак (АаКДС-ИПВ), Пентаксим (АаКДС-ИПВ/Хиб), Актасэль (АаКДС-Хиб), Гексавак (АаКДС-ГВ-ИПВ/Хиб). Комбинированная вакцина Пентаксим, позволяющая за одну инъекцию ввести 5 компонентов, широко используется во Франции для первичной и бустерной иммунизации. Безопасность и низкая реактогенность вакцины подтверждена многими исследователями. Так, Dagan et al. [5] показали, что частота и выраженность побочных реакций на введение вакцины АаКДС-ИПВ/Хиб (Пентаксим) были достоверно меньше, чем на АКДС-ИПВ/Хиб (Пентакок), как после трехкратного ее введения в 2, 4, 6 мес. жизни, так и после бустерного — в 12 мес. (табл. 2).
С другой стороны, частота возникновения и степень выраженности побочных реакций практически не различаются у детей, получивших либо вакцину Пентаксим (АаКДС-ИПВ/Хиб), либо АаКДС/ИПВ и Хиб-вакцину в разные части тела одновременно. В открытом рандомизированном исследовании, проведенном Lagos et al. [6], не выявлено разницы в количестве побочных реакций на
эти вакцины. При этом в общей сложности повышение температуры отмечалось в 4—13% случаев, а местные реакции (слабые и умеренно выраженные) наблюдались менее чем в 30% случаев после всех проведенных прививок на первом году жизни. Сильные реакции в виде уплотнения > 5 см отмечались в 1,3% случаев, гиперемия > 5 см — в 3,6% случаев, ни в одном случае диаметр местных реакций не превышал 7 см. Бустерное введение вакцины Пентаксим также хорошо переносится и детьми 5—6-летнего возраста. По данным Mallet et al. [7] наиболее частыми побочными реакциями у этих детей были болезненность и гиперемия в месте инъекции; реакции развивались, как правило, в течение первых 3 дней после вакцинации, расценивались как легкие или умеренные продолжительностью от 1 до 4-х дней. Повышение температуры выше 39 °С наблюдалось в 0,4%, а до 38,5 °С — в 6% случаев. Hoppenbrouwers et al. [8] показали наличие хотя бы одной местной реакции лишь в 5% случаев, повышение температуры выше 39 °С — в 1,4% случаев. По данным Reinert et al. [9], после введения вакцин с ацеллю-лярным коклюшным компонентом за медицинской помощью в общей сложности обратилось 7,7% детей, из которых связь с вакцинацией была установлена лишь в 0,6% случаев. Безопасность и хорошая переносимость вакцины Пентаксим при введении ее по двум схемам в 2, 4, 6 или в 3 и 5 мес. с ревакцинацией (в обеих схемах) в 12—13 мес. жизни была доказана шведскими исследова-
Таблица 1. Страны и даты первой регистрации вакцин на основе АаКДС
Вакцина Страна 1-ой регистрации Дата включения в календарь
Первичный курс вакцинации Бустер
АаКДС-ИПВ Франция — Август 1996
АаКДС/Хиб Германия Октябрь 1996 Октябрь 1996
АаКДС-ГВ Англия Июль 1997 —
АаКДС-ИПВ/ Хиб Франция Германия Апрель 1998 Июль 1997 Апрель 1998
телями СаНээоп, Оаеээоп, БеЬат et а1. [10]. При этом не было зафиксировано тяжелых вакциноассоциированных осложнений, а число побочных реакций наблюдалось с одинаковой частотой при обеих схемах вакцинации — в 1,8—9,4% случаев при первичной иммунизации и в 1 3,8—1 7% при бустерном введении вакцины (табл. 3).
Изучение иммуногенности комбинированных препаратов, содержащих ацеллюлярную коклюшную вакцину, показало формирование антител в протективных значениях ко всем ее компонентам. При этом более высокие титры антител наблюдались на все 9 входящих в
Таблица 2. Частота побочных реакций у детей первых месяцев жизни на 3-х кратное и бустерное введение вакцин АаКДС-ИПВ/Хиб (Пентаксим), АКДС-ИПВ/Хиб (Пентакок) в 2, 4, 6 и 12 мес. жизни
Побочные эффекты После первых 3-х доз После бустерной дозы
АаКДС-ИПВ/Хиб (n = 286) АКДС-ИПВ/Хиб (n = 276) АаКДС-ИПВ/Хиб (n = 92) АКДС-ИПВ/Хиб (n = 87)
Местные симптомы (%)
Болезненность 15 35* 9 59*
Сильная боль 0 0,7 1,1 17,2*
Гиперемия 9 25* 15 43*
Гиперемия > 2 см 1,7 5,1* 5,4 17,2*
Отек 9 30* 15 47*
Отек > 2 см 2,4 9,4* 1,1 17,2*
Общие симптомы
Температура > 38 °С 22 48* 16 62*
Температура > 39,5 °С 1,4 5,4* 2,2 4,6
Недомогание 28 41* 25 62*
Серьезное недомогание 0,3 0,7 3,3 18,4*
Снижение аппетита 15 24* 15 44*
Потеря аппетита 0,7 0,4 4,3 9,2
* — Статистически достоверно по отношению к АаКДС-ИПВ/Хиб
■ О. В. шамшева. Ацеллюлярные коклюшныЕ вакцины: преимущества в безопасности и иммунологическая эффективность
состав бесклеточных вакцин антигенов, по сравнению с цельноклеточной АКДС-ИПВ/Хиб (табл.4). В исследовании приняли участие 145 детей в возрасте от 15 до 24 мес. жизни, привитые в течение первых месяцев жизни АКДС-ИПВ (Тетракок) трехкратно, а в качестве бустерной дозы (ревакцинация) получившие либо АКДС-ИПВ/Хиб, либо АаКДС-ИПВ/Хиб (Пентаксим), либо АаКДС-ИПВ (+Хиб-вакцину в другую руку). Сыворотка на специфические антитела была исследована на 34 ± 10 день после бустерной вакцинации. Интересно отметить, что титры на введение обеих бесклеточных вакцин были сопоставимы, независимо от того, как вводился Хиб-компонент (в составе вакцины или в другую руку), что свидетельствует об отсутствии интерференции антител на антигены, входящие в состав вакцин. Аналогичные данные получены Lagos et al. [6].
Ведие et а1. [11] показал более высокий иммунный ответ на антигены ацеллюлярной коклюшной вакцины, входящие в состав АаКДС-ИПВ/Хиб (Пентаксим) по сравнению с референс-вакциной АКДС-ИПВ/Хиб, как при их введении в качестве первичной иммунизации в 2, 4, 6 мес, так и в виде бустера в 12 мес. жизни (табл. 5).
Отсутствие каких-либо различий в иммунном ответе, равно как и высокие титры антител при комбинированном и раздельном введении антигенов ацеллюлярных вакцин было показано Hoppenbrouwers et а1. [8] при исследовании детей в Бельгии и Турции. Из 410 человек 138 получили вакцину Пентаксим и 272 — вакцину АаКДС/ ИПВ и Хиб-вакцину в разные части тела. Тенденция к более высокому иммунному ответу была выявлена на Хиб-вакцину при ее отдельном введении. Ревакцинация вызвала бустерный эффект ко всем антигенам.
Таблица 3. Доля детей с местными реакциями и повышением температуры тела в течение 3 дней после прививки (суммарно все дозы)
График вакцинации Возраст n = 236 Доля детей с побочными реакциями (%)
Т>38 °С Т>39 °С Гиперемия > 2 см Отек > 2 см Нет реакций
2, 4, 6, 13 Первая вакцинация 2 мес. 118 3,4 0 0,8 3,4 96,6
3, 5, 12 3 мес. 113 9,7 0,9 0,9 1,3 98,2
2, 4, 6, 13 Вторая вакцинация 4 мес. 117 1,2 0 0,9 3,6 92,9
3, 5, 12 5 мес. 112 5,2 0 4,5 8,6 90,6
2, 4, 6, 13 Третья вакцинация 6 мес. 117 8,5 .,7 6,0 7,7 90,6
2, 4, 6, 13 Ревакцинация 13 мес. 116 5,2 — 9,5 10,3 86,2
3, 5, 12 12 мес. 112 2,7 13,4 12,5 83,0
Таблица 4. Иммунный ответ на бустерное введение вакцин АаКДС-ИПВ/Хиб (Пентаксим), АаКДС-ИПВ+Хиб и АКДС-ИПВ/Хиб у детей в возрасте 15—24 мес. жизни
Вакцина Уровни антител на 34 ± 10 день после бустерной вакцинации
Хиб Диф Ст КТ ФГА ПРН Полиовируса тип
1 2 3
АаКДС-ИПВ/Хиб (n = 56-57) 60,4 5,7 13,3 84,5 505 812 4693 2859 5405
АаКДС-ИПВ+Хиб (n = 37) 60,0 4,8 15,9 73,5 456 790 5261 3853 5161
АКДС-ИПВ/Хиб (n = 42-46) 39,3 3,2 6,9 21,0 156 257 2763 2117 4031
Таблица 5. Уровни антител через месяц после первичной (2, 4, 6 мес. жизни) и бустерной вакцинации (1 2 мес. жизни) вакцинами АаКДС-ИПВ/Хиб (Пентаксим) и АКДС-ИПВ/Хиб
Вакцина Уровни антител через 1 мес. после первичной/бустерной вакцинации
Хиб (mcg/ml) Диф (IU/ml) Столб (IU/ml) КТ (EIU/ml) ФГА (EIU/ml) ПРН (EIU/ml)
АаКДС-ИПВ/Хиб (n = 89-92) 5,1/23 1,2/4,3 2,1/6,1 57/112 149/374 157/525
АКДС-ИПВ/Хиб (n = 80-92) 6,7/14 1,2/3,8 3,0/6,6 16/21 38/107 87/222
В числителе указаны уровни антител после первичной вакцинации, в знаменателе — после бустерной вакцинации
Исследователи используют разные схемы вакцинации, предпочтение отдается 3-х-кратной схеме. При этом оба графика 3, 4, 5 и 2, 4, 6 мес. жизни с последующей ревакцинацией в 12—14 месяцев являются сопоставимыми. В то же время шведскими исследователями Cansson et al. [10] доказана более высокая иммуногенность 3-х-кратной вакцинации АаКДС-ИПВ/Хиб (Пентавак), по сравнению с 2-х-кратной. Тем не менее, перед ревакцинацией наблюдались одинаковые среднегеометрические титры антител к антигенам, введенным по разным схемам, за исключением антител к вирусу полиомиелита 1 и 3 типа, титры к которым были меньше при 2-кратной схеме. Введение бустерной дозы в 12 мес. жизни нивелировало и эти различия.
Исследование было продолжено через 4,5 года после законченной вакцинации: у детей определялись титры антител ко всем антигенам, входящим в состав вакцины. Результаты показали отсутствие различий в показателях се-роконверсии привитых по разным схемам детей. При этом антитела к дифтерийному токсину > 0,01 МЕ/мл сохранились в 89% случаев; к столбнячному токсину > 0,01 МЕ/мл — в 93%; 96—97% детей имели защитные антитела к вирусам полиомиелита 1 —3 типов, 97% — к антигену Хиб. Антитела к коклюшному токсину определялись в 99% случаев методом нейтрализации и 94% детей имели антитела к филаментозному гемагглютинину. Необходимо отметить, что 5-летний опыт использования вакцины Пентавак в 10 областях Швеции привел и к хорошему профилактическому результату — заболеваемость коклюшем снизилась с 224 до 26 случаев на 100 тыс. населения [13]. Mallet et al. [7] также показали длительную циркуляцию специфических антител к компонентам вакцины, сохранявшуюся через 4—5 лет после законченного курса первичной иммунизации. Как и предполагалось, антитела к коклюшному анатоксину отмечались в более низких титрах, что доказывает, что дети не были инфицированы коклюшем за прошедший период.
Заключение
Обобщая представленные данные литературы можно сделать вывод, что, несмотря на наличие вакцин и высокий охват прививками, проблема коклюша до сих пор не решена. Проблема усугубляется еще и тем, что в настоящее время самый интенсивный подъем заболеваемости коклюшем отмечается в возрасте старше 5 лет и в возрасте до года. Цельноклеточная коклюшная вакцина отличается высокой реактогенностью и нередко дает сильные побочные реакции, что является главной причиной отвода от профилактических прививок. Решением проблемы могла бы стать ацеллюлярная коклюшная вакцина, иммунизирующим компонентом которой являются коклюшный анатоксин и филаментозный гемагглютинин (ФГА). Такая вакцина уже находит широкое применение во многих странах Европы. Она отличается высокой им-муногенностью и относительно низкой реактогенностью.
Вакцина показана всем детям раннего возраста, особенно с противопоказаниями к введению цельноклеточной
вакцины или тяжело перенесшим первые вакцинации
цельноклеточной вакциной.
Литература:
1. Таточенко В. К., Федоров A. M. Эпидемические аспекты коклюша в РФ. Особенности вакцинопрофилактики в современных условиях: Пособие для врачей. — М., 2005. — 36 с.
2. Pertussis vaccines. WHO Position Paper // Weekly Epidemiological Record. — 2005. — № 4. — Р. 31—39 // http:www.who.int/ wer/2005/en/wer8004.pdf
3. Cherry IT. D. Immunity to Pertussis //CID. — 2007. — V. 44. — Р. 1278—1279.
4. Tinnion O. N. Acellular vaccines for preventing cough in children / O. N. Tinnion, M. Hanlon // The Cochrane Collaboration review. — The Cochrane Library, 2006. — Issue 1.
5. Safety and immunogenicity of a combined pentavalent diphtheria, tetanus, acelluiar pertussis, inactivated poliovirus and Haemophilus influenzae type b, tetanus conjugate vaccine in infants, compared with a whole cell pertussis pentavalent vaccine / R. Dagan et al. // Pediatr. Infect. Dis. J. —1997. — V. 16. — Р. 1113 — 1121.
6. Clinical acceptability and immunogenicity of a pentavalent parenteral combination vaccine containing diphtheria, tetanus, acellular pertussis, inactivated poliomyelitis and Haemophilus influ-enzae type b conjugate antigens in two-, four- and six-month-old Chilian infants / R. Lagos et al. // Pediatr. Infect. Dis. J. — 1998. — V. 17. — Р. 294—304.
7. Antibody persistence against diphtheria, tetanus, pertussis, poliomyelitis and Haemophilus influenzae type b (Hib) in 5—6 year-old children after primary vaccination and first booster with a pentava-lent combined acellular pertussis vaccine given as a second booster/E. Mallet et al.//Vaccine J. — 2004. — V. 22. — Р. 1415—1422.
8. Priming effect, immunogenicity and safety of an Haemophilus influ-enzae type b-tetanus toxoid conjugate (PRP-T) and diphtheria-teta-nus-acellular pertussis (DTaP) combination vaccine administered to infants in Belgium and Turkey / K. Hoppenprouwers et al. // Vaccine J. — 2004. —V. 22. — Р. 1415—1422.
9. 15th Annual Meeting of the European Society for Pediatric Infectious Diseases abstracts. «Primary or booster immunization with DTaP-IPV vaccine administered either in combination or in association with a Haemophilus influenzae type b (Act-HIB) vaccine: a large-scale safety study / Т. Reinert et al. // 1 5th ESPID. — Paris 1 997. — Abstract 75.
10. Safety and immunogenicity of a combined diphtheria-tetanus-acel-lular pertussis-inactivated polio vaccine — Haemophilus influenzae type b vaccine administered at 2-4-6-13 or 3-5-12 months of age/R. M. Carlsson et al.//Pediatr. Infect. Dis. J. — 1998. — V. 17. — Р. 1026—1033.
11. Immunogenicity and reactogenicity of a booster dose of DTPa-IPV compared to one dose of DT-IPV administered to preadoleseents aged 10—13 / P. Begue et al. // 16 Annual Meeting of the European Society for Peadiatric Infectious Diseases (ESPID). — Bled, Slovenia, 1998. — Р. 52.
12. Antibody persistence in five-year-old children who received a pentavalent combination vaccine in infancy/ R. M. Carlsson et al.// Pediatr. Infect Dis. J. — 2002. — V. 21. — Р. 535—541.
1 3. Effectiveness of the 2-component acellular pertussis combination vaccine Pentavac / Pentaxim: 5 year experience of routine practice in Sweden/L. Hessel et al.//11th ICID, 2004. — Abstract 18.023. — Published in International Infect. Dis. J.— Suppl. 8.— 1 March 2004. — P. 75.
cyberleninka.ru
Бесклеточная (ацеллюлярная) вакцина
Как известно, вакцина АКДС содержит в качестве инактиватора коклюшного и дифтерийного токсинов формальдегид, а в качестве консерванта мертиолят в концентрации 0,01%, и факт наличия этих веществ в вакцинах долгие годы успешно скрывали не только от родителей, но и от врачей.
Публикации в центральной прессе, начавшиеся в 1988-1989 гг., в которых рассказывалось о составе вакцин и о том, в каких условиях они производятся в СССР (инициатором многих таких публикаций была московский вирусолог, к.б.н. Г.П. Червонская), вызвали настоящую бурю возмущения, в первую очередь специалистов, которые прекрасно знали, что означают эти вещества для человеческого организма.
Это возмущение было хорошо отражено в материалах Российского Национального комитета по биоэтике. Вот, например, что писал замдиректора по научной работе НИИ общей и коммунальной гигиены им. А.Н. Сысина АМН СССР, к.м.н. Н.Н. Литвинов: «Устанавливать научно обоснованные безопасные регламенты для недействующих доз — концентраций химических веществ, а тем более ртутных соединений, «разрешенных» 35 лет тому назад для парентерального введения грудным детям, — задача практически неразрешимая.
Необходимо иметь очень серьезные обоснования, жизненные показания, чтобы разрешить многократное введение ребенку подобного дезинфектанта, ртутного пестицида. Кроме того, любые химические добавки, используемые в качестве консервантов, стабилизаторов, наполнителей и т.д., могут менять фармакокинетику основного вещества, в данном случае белков-антигенов, а, следовательно, и их целенаправленное действие.
Я, как специалист, считаю, что в сложившейся ситуации безо всяких промедлений должны быть представлены документы, доказывающие проведение специальных токсикологических исследований на отсутствие тератогенности, эмб-риотоксичности, аллергизирующей активности, мутагенности и канцеро-генности применяемой дозы мертиолята в вакцине АКДС: либо зарубежными фирмами, продающими нам этот пестицид, либо отечественными контролирующими учреждениями — Комитетом вакцин и сывороток или ГИСК им. Л. А Тарасевича.
Неужели вопрос изъятия ртутного вещества из препаратов, используемых с целью профилактики в детской практике здравоохранения, требует каких-то рассуждений, доказательств?.. Так ли необходимо использование комплексного препарата, каким является АКДС, в конце двадцатого века во всех регионах нашей страны, где иммунизация проводится по одной мерке, без учета климатических условий и, как известно, без индивидуального подхода к каждому ребенку и т.д.?
Как учитываются шестнадцать противопоказаний и кто их «успевает» определить? Признаться, я о них услышал и прочитал впервые. Как определяют повышенную чувствительность детей к ртутной соли и формальдегиду? Кому адресовать все эти вопросы по «допущенным», так называемым малым дозам, содержащимся в вакцине? Совершенно несостоятельны ссылки на ВОЗ -мол, ВОЗ требует определенного содержания этих веществ в АКДС. Это отговорка, рассчитанная на дилетанта. К тому же ВОЗ и ее комитеты не могут отвечать за принимаемые у нас в стране решения. Полностью проигнорированы отечественные специалисты и Фармкомитет СССР».
А вот мнение токсиколога, к. м. н. д-ра Н. Н. Михайлова: «…что собой представляет мертиолят? Это — ртутьорганическое соединение, инач? называемое этилртутьтиосалицилат натрия, относится к пестицидам.-Кста-ти, в доступной отечественной литературе сведения о нем весьма скудны, он не зарегистрирован в нашей стране, и я не нашел данных о его глубоком токсикологическом изучении. Мельников Н. Н. в книге «Пестициды: химия, технология и применение», 1987, давая классификацию пестицидам, относит последний к бактерицидам, приводит ДЦ50-40 мг/кг (вызывает 50% гибель крыс в эксперименте), что позволяет отнести мертиолят по степени его опасности, предложенной ВОЗ, к очень опасным веществам.
Это иллюстрирует и такой пример. В «Методических указаниях по применению физико-химических и химических методов контроля медицинских биологических препаратов», М., 1977, утвержденных МЗ СССР (Хлябич, Ковшило), где говорится о приготовлении стандарта, сказано о хранении мертиолята: «ЯД! с притертой пробкой в темном месте». Литературные данные свидетельствуют о том, что органические соединения ртути весьма токсичны для всего живого, могут поражать вегетативную нервную систему, вызывать иммунологические изменения.
Однако мне не встретилось ни одного источника, где бы были отражены сведения по изучению этих отрицательных моментов относительно мертиолята. Вместо этого появились «допустимые» дозы его в медицинских иммунобиологических препаратах (МИБП) -вакцинно-сывороточных средствах, используемых для профилактики и лечения инфекционных заболеваний. Для справки: согласно утвержденному в нашей стране перечню допустимых количеств некоторых консервантов в пищевых продуктах, ртутьсодержа-щие исключены. А мы в плановом порядке вводим «крохотные дозы» этой соли грудным детям…
Я пытался выяснить в свое время, есть ли статья в Государственной фармакопее СССР относительно мертиолята. Нет, в отечественной фармакопее его нет. Есть фундаментальный труд «Руководство по вакцинному и сывороточному делу» под редакцией академика Бургасова П.Н., где очень красиво говорится об основополагающих принципах контроля за качеством МИБП в СССР, который заключается в комплексе мероприятий, обеспечивающих поступление в практику здравоохранения полностью безопасных и эффективных средств специфической профилактики и лечения, диагностики инфекционных заболеваний. В этом же руководстве на стр. 166 читаем: «…должны быть безвредными, стерильными, содержать не более 0,01% консерванта мертиолята… тиомерсал — 100±20 мкг/мл или не содержать консерванта, и иметь следовые количества формальдегида». А в нормативных документах: «должно содержаться 500 мкг/ мл формальдегида».
Но это — не следы, а вполне ощутимое количество! Вообще, когда знакомишься с этим произведением, рассказывающим о том, как должно быть, возникает ощущение сплошных противоречий, многие из которых вызывают удивление: ну почему не обратиться к специалистам в своем отечестве? Ничего не говорится, например, о токсикологии химических веществ, допущенных в биопрепараты. Какие же они… биопрепараты? Совершенно безответственно констатируется факт того, что нечто «допущено» и «безвредно». А проверка такого «безвредно» прошла всего на 2-5 взрослых животных. Наблюдение проведено в течение 14 суток с момента введения препарата. Есть у меня такое подозрение, что так, как изучена АКДС, можно считать, что ее безопасность не проверена!».
Приведу и слова биохимика, ст. н. с. Института иммунобиологии Мин-медпрома, к.б.н. В.Д. Кольцова: «Мертиолят — пестицид. Все пестициды — токсичны. А мертиолят к тому же еще относится к солям тяжелых металлов. Специалистам известно, что последствия одноразового контакта с малыми дозами подобных соединений непредсказуемы. И в данном случае дело не в дозе, а и индивидуальной чувствительности неокрепшего детского организма, да еще на фоне современного состояния окружающей среды, питания, воды и многого другого… Я — родитель двух детей, страдающих аллергией. По специальности биохимик. Не понаслышке мне известно, что такое формальдегид и ртутные соли. Конечно, вводить их парентерально любому ребенку — преступление, а детям, страдающим разными формами аллергии, — вдвойне опасно (а бывают, как известно, и смертельные исходы от введения АКДС). Ртутная соль может быть одной из причин… Уверен, если бы не публикации в центральной прессе, мы бы так и не знали, что вводят поголовно детям в нашей стране в составе так называемых «вакцин».
Кстати говоря, в «Наставлении по применению АКДС» сказано, что инактивация проводится либо формальдегидом, либо мертиолятом. И вдруг узнаем, что они оба входят в состав многих вакцин. Кроме того, вряд ли педиатрам кто-то разъяснил, что мертиолят — ртутьсодержащая соль. Если бы это случилось, то многие бы, наверное, задумались. Отсутствие такой надписи на этикетке — прямое нарушение международных требований об указании в составе лекарственного средства соли ртути!.. Судя по содержанию возражений со стороны чиновников, можно сделать заключение о том, что им абсолютно неизвестны методы изучения безопасности — инактивированных вакцин, в которые входят химические вещества…
Мой отзыв продиктован чувством солидарности с теми специалистами, которые поднимают вопрос о проведении грамотного изучения безопасности вакцин, добавок, содержащихся в них, а также об индивидуальном подходе к ребенку. Качественная прививка — это
а) безопасный препарат и
б) качественный организм ребенка.
И в этом нет никаких новостей. Реакция чиновников, мягко говоря, странная. Вместо того чтобы честно признать недостатки и некачественность АКДС, устранить их (или прекратить производство!), как это должно быть в случае действительной заботы о здоровье детей, они встают в позу незаслуженно оскорбленных. Но такая реакция может быть только у тех, кто либо недопонимает всю опасность своей деятельности (тогда им нечего делать ни в науке, ни в организации здравоохранения), либо осознает опасность препарата и теперь пытается уйти от ответственности, ошельмовав специалистов, сделавших это явным.
Спасибо за обращение к правительству, за то, что нашлись специалисты, взявшие на себя смелость поднять этот очень многогранный вопрос, встав на защиту детей от «охранителей» нашего здоровья. Родители должны знать, что вводят их детям, отчего дети могут стать инвалидами на всю жизнь и кто повинен в этом. Но есть ведь конкретный человек или группа людей, которые дали разрешение на применение ртутной соли в детских препаратах в нашей стране. Кто они?».
Думаю, читатели догадаются, что все эти выступления, все заключения высококвалифированных, действительно независимых специалистов, которые не кормятся от прививочной кормушки, остались гласом вопиющего в пустыне. Никто и не подумал оправдываться, предоставлять им документы (которых, разумеется, никогда не существовало) или объяснять, кто, когда и на основании каких исследований позволил использование ртути в вакцинах, да еще на пару с формальдегидом, и почему этот дикий абсурд продолжается. Но пусть хотя бы об этих фактах станет известно читателям, а соответствующие выводы они сделают сами!
Бесклеточная (ацеллюлярная) вакцина
После смерти двух младенцев от прививки DPT в 1976 г. в Японии срочно начали разрабатывать новую коклюшную вакцину. Она была лицензирована там и стала применяться в 1981 г. Бесклеточная вакцина представляет собой смесь коклюшного анатоксина и антигенов возбудителя болезни, иммунная реакция в ответ на введение которых должна обеспечивать невосприимчивость к болезни. Сам возбудитель в таких вакцинах отсутствует. Эта вакцина выпускается рядом компаний и различается лишь по количеству содержащихся в ней антигенов.
Предполагалось, что за счет «прицельного» выделения антигенов эта вакцина будет свободна от побочных явлений, характерных для ее цельноклеточной (корпускулярной) предшественницы. Однако, похоже, ожидания эти оправдались лишь частично, поскольку и по сей день точно неизвестно, какие именно антигены запускают иммунный ответ, а какие обусловливают тяжелые реакции со стороны нервной системы заболевшего или привитого; потому и антигенный набор вакцины построен больше на гипотезах, чем на точных сведениях. Вслед за введением новой вакцины были отмечены как стандартные местные реакции, так и системные, например конвульсии.
После тщательного изучения двух японских вакцин в 1986-1987 г. шведская Национальная бактериологическая лаборатория отказала японцам в продолжении процедуры лицензирования этих вакцин — как вследствие того, что эффективность вакцины оказалась не только не выше, но, вероятно, и ниже, чем у цельноклеточной вакцины, так и вследствие ряда необъяснимых смертей привитых этими вакцинами детей от присоединения бактериальной инфекции (скончались 11 детей из 2800 получивших прививки).
Представитель ВОЗ д-р Марк Кейн заявил в 1996 г., что новая вакцина не имеет никаких преимуществ перед старой в смысле эффективности. Что касается главного своего предназначения — снизить число тяжелых последствий использования коклюшной вакцины — новая вакцина, согласно данным некоторых исследований, не оправдала возлагавшихся на нее надежд. Разницы в количестве случаев СВДС (симптом внезапной детской смерти) и близких к нему состояний, госпитализаций, энцефалопатии и отставания в развитии относительно цельноклеточной вакцины не обнаружилось.
Впрочем, другие исследования были более благосклонны к бесклеточной вакцине. Неоднократно цитировавшиеся в этой главе Дэвид и Марк Гейеры исследовали базу данных Системы сообщений о побочных эффектах прививок (VAERS) и обнаружили, что бесклеточная вакцина дает значительно меньшее количество побочных реакций любого рода.
Кроме того, в США имелся опыт ее производства еще с 1930-х годов, и он показывал, что бесклеточная вакцина действительно дает меньшее количество тяжелых побочных эффектов. Российские авторы сообщают: «Реактогенность бесклеточных вакцин намного ниже реактогенности корпускулярной вакцины. На введение бесклеточной коклюшной вакцины значительно реже возникают как общие, так и местные реакции (лихорадка — в 7 раз, гипертермия — в 4, отечность — в 5-6, болезненность — в 14 раз»).
Важной для понимания законов, по которым работает прививочный бизнес, будет информация о том, что немалое количество американских компаний разрабатывало, начиная с 1920-х годов, эту, вероятно, более безопасную вакцину. Однако в итоге все они отказались от ее массового производства и маркетинга. Причина? Раз заявив, что располагают новой, более безопасной вакциной, они могли стать объектом судебных исков, в которых истцы бы утверждали, что компании знают, как делать лучший продукт, но в силу тех или иных причин продолжают поставлять на рынок худший, более опасный.
В1985 г. американский Институт медицины признал возможность тяжелых неврологических осложнений после прививки DPTH рекомендовал заменить цельноклеточную вакцину против коклюша на бесклеточную (ацеллюлярную). Рекомендация была проигнорирована, а вместо разработки безопасной вакцины производители DPT предпочли тратить деньги на подкуп «независимых экспертов». Однако в 1990-х годах, несмотря на все ухищрения Черри и Ко и их работодателей, ситуация изменилась. Несколько очень крупных исков, после многолетнего разбирательства, были все же выиграны в рамках Национальной программы компенсаций пострадавшим от прививок. Три раза собиравшаяся при Национальном институте здоровья США экспертная группа пришла к выводу о доказанности связи между вакциной DPTH поражением мозга и подчеркнула необходимость перейти на новую, более безопасную вакцину. И, главное, настойчивость японцев и тех, кто их поддерживал (например, групп родителей), поставила на повестку дня вопрос о скором лицензировании бесклеточной вакцины. Чтобы не проиграть сражение за рынок, американские компании вынуждены были отказаться от битой ставки на «мнения экспертов» и начать разрабатывать свои собственные бесклеточные коклюшные вакцины. Сегодня в СШАцельноклеточная вакцина производится только на экспорт, а на внутреннем рынке с 2001 г. используется лишь бесклеточная вакцина.
Помимо прочих сложностей и вопросов известно, что производство новой вакцины значительно сложнее, а цена вакцины в развитых странах 19,43 $, примерно на 9 $ превышает цену старой, что, учитывая необходимость многократного употребления вакцины, в рамках национальных прививочных программ небогатых стран может оказаться совершенно неприемлемой, хотя и утверждается, что при изначально более высокой стоимости бесклеточной вакцины ее применение снижает общемедицинские расходы (уходы за заболевшим после прививки ребенком и особенно выплата компенсаций за инвалидность и смерти привитых цельнокле-точной вакциной).
Вопрос о лучших, более безопасных, но значительно более дорогих вакцинах ждет своего решения. Как и вопрос, нужны ли вообще коклюшные вакцины.
Надеюсь, что в этой главе я дал достаточно сведений для желающих серьезно задуматься о том, совместимы ли прививки против коклюша со здоровьем ребенка и не следует ли держаться как можно дальше от этого очень сомнительного блага. Выбор остается за родителями!
Выводы
Коклюш — болезнь преимущественно детского возраста, бывшая некогда опасной в европейских странах и в Америке и остающаяся таковой для стран третьего мира сегодня. Раз перенесенная болезнь оставляет стойкий, обычно пожизненный иммунитет, который защищает и будущих детей в самом опасном по осложнениям коклюша возрасте.
Коклюшная вакцина (коклюшная составляющая многокомпонентных вакцин) традиционно считается одной из самых малоэффективных и одной из самых опасных из существующих ныне вакцин. Продолжающиеся в национальных масштабах прививочные кампании смещают болезнь в самый опасный, младенческий возраст, лишают женщин возможности приобрести естественный иммунитет и увеличивают число больных стертыми формами коклюша взрослых, которые заражают детей.
Новая бесклеточная (ацеллюлярная) вакцина также отнюдь не свободна от побочных эффектов, хотя, вероятно, более безопасна и эффективна, чем традиционная цельноклеточная. Есть данные, свидетельствующие в пользу высокой эффективности безопасной гомеопатической профилактики коклюша.
В развитых странах для коклюша сегодня характерно мягкое течение; серьезные случаи, осложнения и тем более смерти представляют собой крайне редкое явление и встречаются почти исключительно у детей в возрасте до шести месяцев.
all159z.narod.ru
Сравнение эффективности цельноклеточной и ацеллюлярной коклюшной вакцины
В настоящее время нет чётких данных и детальных описаний, касающихся необъяснимого снижения иммунной защиты после вакцинации против коклюша. В проведённом в США крупномасштабном когортном исследовании изучалось влияние предшествующей вакцинации с использованием цельноклеточной коклюшной вакцины в сравнении с ацеллюлярной коклюшной вакциной на любые аспекты противококлюшного иммунитета.
В ходе исследования была проанализирована совместная частота большой вспышки коклюша, возникшей после завершения использования цельноклеточной коклюшной вакцины, а также изучена заболеваемость в популяции детей, которые были вакцинированы и цельноклеточной, и ацеллюлярной коклюшной вакциной.
В ходе исследования из общей базы данных выбирались лаборатно-подтверждённые случаи коклюша, а также сведения о вакцинации пациентов в возрасте 8-20 лет.
Из когорты, включающей 263496 пациентов в возрасте от 8 до 20 лет, всего было идентифицировано 904 случая коклюша. У пациентов, которые прошли курс вакцинации против коклюша, получив 5 доз только ацеллюлярной коклюшной вакцины, относительный риск развития коклюша составил 8,57 (p<0,0001) по сравнению с пациентами, которые получили хотя бы одну дозу цельноклеточной коклюшной вакцины. В случае, если вводилось 6 доз ацеллюлярной коклюшной вакцины, относительный риск развития коклюша составил 3,55 (p<0,0001).
Таким образом, в ходе данного крупномасштабного когортного исследования было установлено, что при использовании исключительно ацеллюлярной коклюшной вакцины отмечается увеличение риска возникновения коклюша в общей популяции. Данный риск можно значительно уменьшить, но не элиминировать, введением шестой дозы ацеллюлярной коклюшной вакцины. В то же время получение одной или более доз цельноклеточной коклюшной вакцины значительно увеличивает продолжительность иммунитета после введения последующих доз ацеллюлярной коклюшной вакцины. Таким образом, использование для курса вакцинации полностью только ацеллюлярной коклюшной вакцины является достоверно менее эффективным и приводит к формированию менее продолжительного иммунитета по сравнению с использованием традиционной цельноклеточной коклюшной вакцины.
Witt M.A., Arias L., Katz P.H., Truong E.T., Witt D.J.
Reduced Risk of Pertussis Among Persons Ever Vaccinated With Whole Cell Pertussis Vaccine Compared to Recipients of Acellular Pertussis Vaccines in a Large US Cohort.
Clin Infect Dis. 2013; 56(9): 1248-54.
Источник:
Из импортных цельноклеточных от коклюша в справочнике ЕОК упомянуты Д.Т.Кок, Тетракок, ТетрАкт-ХИБ. Как я понял, в России из них сейчас ничего нет.
klubkom.net
