Анаферон детский защитит ребенка от простуды
Этот детский препарат появился на рынке несколько лет назад и уже успел завоевать доверие мам и педиатров. Лекарство призвано помочь защитить ребенка от простуды или помочь ему переболеть в более легкой форме с меньшим риском развития осложнений. К сожалению, в прохладные весенние дни все еще легко простудиться.
Анаферон детский создан с учетом особенностей растущей иммунной системы специально для детей. Лекарство позволяет усилить защиту от простудных заболеваний, действуя сразу в двух направлениях: блокирует размножение вирусов и активирует работу иммунитета. При этом лекарство бережно воздействует на иммунитет, не вызывая истощения его ресурсов. Препарат не вызывает привыкания, это означает, что организм не «разучится» защищаться от вирусов и после отмены лекарства
Для профилактики вирусных заболеваний ребенку дают по таблетке в день. В каких случаях нужна профилактика, если на дворе весна, и с каждым днем становится все теплее и теплее? В первую очередь в профилактике нуждаются дети, посещающие детский коллектив, в котором кто-нибудь болеет.
При первых признаках простуды дают уже лечебную дозу Анаферона детского, она отличается от профилактической. Малышам таблетку растворяют в чайной ложке воды комнатной температуры. Детям старшего возраста предлагают положить таблетку под язык и подержать до полного растворения (препарат выпускается в форме таблеток для рассасывания). Раз мы упомянули детей грудного возраста, сразу внесем уточнение: лекарство можно давать малышам, начиная с месячного возраста. Лечение рекомендуется продолжать до полного выздоровления. Даже если ребенок уже болеет, все равно есть смысл давать ему Анаферон детский — это может уменьшить риск развития осложнений.
На нашу горячую линию поступают звонки с разными вопросами.
«В январе мы давали ребенку Анаферон детский в течение 3-х недель и это помогло не заболеть. Сейчас у ребенка началось что-то похожее на простуду. Можно ли давать ему Анаферон после 3-х недельного перерыва?»
Да. Можно. Дело в том, что Анаферон не вызывает истощения иммунитета и поэтому его можно применять для профилактики и лечения столько раз, сколько потребуется.
«Мой ребенок заболел какой-то странной инфекцией — у него высокая температура, болит горло и голова, но ко всему этому еще и расстройство желудка и понос. Нам педиатр сказал, что это вирус, и прописал Анаферон детский, а я слышала, что он применяется при гриппе. Поможет ли нам этот препарат?»
Да, поможет. Анаферон является противовирусным препаратом с широким спектром действия. Поэтому он применяется не только при гриппе, но и при других ОРВИ, а также при инфекциях, которые одновременно поражают дыхательную и пищеварительную системы.
Возможно, и у вас будут вопросы по лечению вирусно-респираторных заболеваний с помощью препарата Анаферон детский. В этом случае вы можете посетить наш сайт, на котором есть подборка статей. А еще для вас работает телефон горячей линии: 7 (495) 681-93-00,681-09-30.
В этом случае вы можете посетить наш сайт, на котором есть подборка статей. А еще для вас работает телефон горячей линии: 7 (495) 681-93-00,681-09-30.
Имеются противопоказания, необходимо ознакомиться с инструкцией перед применением.
Информация на сайте имеет справочный характер и не является рекомендацией для самостоятельной постановки диагноза и назначения лечения. По медицинским вопросам обязательно проконсультируйтесь с врачом.
Материалы предоставлены компанией «Материа Медика Холдинг»
https://www.7ya.ru/Bauskas iela 58A — 7RīgaLV-1004Да, тоже сталкивалась с тем, что почему-то считается, что анаферон не проверялся как дожно.Анаферон проходил все положенные проверки и клинические испытания, всю информацию об этом можно найти при желании… я вот удивляюсь, почему у наших людей всегда есть желание поискать доказательства со знаком минус и очень редко — в пользу объекта дискуссии =/ Я в свое время нашла много инфы, именно после того, как мне сказали, что анаферон не помогает, а я на себе и своем сыне увидела, что работает.
Слышала что некоторые говорят пустышка ,вредно ,бесполезно ,не эффективен.Я его даю курсом дочке уже не первый год и всегда помогает и оберегает от нынешних страшных осенне-зимних эпидемий.С мужем Анаферон для взрослых принимаем и у нас в семье о гриппе даже никто и не вспоминает ,как о чем-то страшном и неизбежном.
Всего 2 отзыва Прочитать все отзывы.
04.04.2011
Обновлено 15.01.2021
Лечение ОРВИ у детей. Клиника ИПМ для детей г. Красноярск
Об этом много говорится, но мало соблюдается… Каковы причины? Дело в том, что родители зачастую не понимают как, например, обычное мытье рук может помочь снизить риск заболеваемости. Разберем это по-порядку.
Разберем это по-порядку.
Факты, которые необходимо знать:
- По данным иммунологов, нормальная частота заболеваемости ОРВИ в организованных коллективах — 8 раз в год!
- Риск заболеваемости на 98% зависит от иммунитета и образа жизни ребенка (сон, питание, физическая активность, эмоциональное состояние, бытовые условия).
- 2% — приходится на иммуномодуляторы, противовирусные препараты.
Конечно, ограничить контакт с больными практически невозможно, если ребенок посещает детский сад или школу. Тогда можно пойти другим путем и обезопасить своего ребенка.
Самые частые пути передачи вирусов:
— воздушно-капельный
— контактный
Воздушно-капельный путь передачи инфекции — это заражение через воздух, в который попадают на небольшом расстояние при разговоре, кашле и чихании больных мельчайшие брызги, капли слюны и носовой слизи, содержащие возбудителей болезней. Заражение происходит при вдыхании этих вирусов.
Следовательно, если ребенок заболел, нужно оставить его дома. И соответственно лечить его в домашних условиях.
Также, необходимо одевать маску. Не зря в разгар ОРВИ применяют «масочный режим». Менять маску нужно не реже 1 раза в три-четыре часа.
Вирусы очень длительно сохраняют свою активность в пыльном сухом воздухе, но погибают мгновенно во влажном чистом прохладном воздухе. Чем сильнее воздухообмен, тем меньше вирусов в воздухе, и следовательно, меньше вероятность заболеть. Частое проветривание — самый эффективный способ профилактики. Почему бы не соблюдать это легкое действие: вышли на прогулку — проветрили помещение, пошли покушать на кухню — проветрили спальню и т.д.
Контактный путь путь передачи инфекции:
Вирусы везде: на полу, на бытовых приборах, на ковре, на игрушках, на руках и т.д. Дети в детском саду контактируют целыми днями с этими самыми вирусами.
Соответственно, наши действия какими будут?
- Мытье рук — это первое.
 Часто и тщательно нужно мыть руки, и обязательно научить ребенка этому.
Часто и тщательно нужно мыть руки, и обязательно научить ребенка этому. - Влажная уборка помещения
- Гигиеническая обработка игрушек
Делать эти процедуры необходимо как можно чаще!
Помимо этого профилактика ОРВИ включает в себя:
- Применение иммуномодуляторов (с назначения врача):
— Виферон, Кипферон
— Циклоферон, анаферон
— Бронхо-Мунал, Рибомунил, ИРС-19
— Иммунал
- Питание, богатое витаминами А,В и С
— лимон
— цветная капуста
— шпинат
— киви
— пшеничные отруби
— зеленые и оранжевые овощи и фрукты
— молочные продукты
— рыба
— орехи
— мед, варенье
- Активная физическая нагрузка и практика закаливания (иммунная система буде лучше работать, из-за чего организм сможет противостоять большинству респираторных заболеваний).
- Вакцинация
- Промывание носа солевыми растворами (на заметку: перед детским садом слизистую и крылья носа можно помазать оксалиновой мазью, «Виферон» или «Доктор-Мом», а после десткого сада промыть нос солевым раствором — Аквалор, Аквамарис, Долфин, Квикс, физ.
 раствор и т.д.).
раствор и т.д.).
Для общего укрепления иммунитета разрешается давать детям отвар шиповника, липы и мяты. Они не принесут вреда, а наоборот, будут улучшать защитные силы организма.
Будьте здоровы!
Остались вопросы? Запишитесь на прием к врачу педиатру:
т. (391) 200—50—03
Диагноз: «Аденоиды» — Заболевания: профилактика, лечение, полезные советы — Каталог статей
ДИАГНОЗ: «АДЕНОИДЫ».
Один из наиболее известных диагнозов – «аденоиды». Трудно не утонуть в море информации, разобраться в специальных вопросах и принять правильное решение. При этом часто именно не правильная позиция родителей приводит к нарушению тактики лечения и, соответственно, снижению его эффективности.
Современные родители – люди просвещенные, о многих заболеваниях детского возраста и слышали и читали. Однако знать название болезни далеко не то же самое, что понимать ее суть.
ТРИ СТЕПЕНИ ПРОБЛЕМЫ:
Аденоиды (аденоидные вегетации) – это патологическая гипертрофия третьей (носоглоточной) миндалины.
Причины гипертрофии аденоидной ткани глоточной миндалины связанны с особенностями организма ребенка – конституцией , аллергизацией и частыми инфекционными болезнями.
Различают три степени гипертрофии глоточной миндалины.
1 степень – аденоиды уменьшают дыхательный просвет незначительно и практически не влияют на дыхание.
2 степень – аденоиды прикрывают верхние две трети дыхательного просвета и умеренно затрудняют носовое дыхание.
3 степень – аденоиды прикрывают полностью или почти полностью дыхательный просвет, носовое дыхание при этом сильно затруднено или отсутствует.
ВНЕШНИЕ И ВНУТРЕННИЕ ИЗМЕНЕНИЯ:
Аденоиды закрывая глоточные отверстия евстахиевых (слуховых)труб и нарушая нормальную вентиляцию среднего уха, могут вызвать понижение слуха. Искажается речь, голос становится гнусавым. Дети раннего возраста с трудом овладевают речью. Лицо ребенка приобретает особое выражение, получившее название «аденоидное лицо», или внешний «аденоидизм»: открытый рот, отвисшая нижняя челюсть, сглаженные носогубные складки, вытекающая из углов рта слюна.
Постоянное дыхание через рот приводит к деформации черепа. Иногда отмечают неправильное расположение зубов. Это ведет к неправильному прикусу, иногда – к искривлению носовой перегородки.
Помимо увеличения аденоидов, отрицательное воздействие на организм ребенка может оказывать длительный воспалительный процесс в носоглотке – хронический аденоидит.
ВСЕ СВЯЗАНО:
У детей с аденоидами и аденоидитом отмечается затекание слизи
из носоглотки а ротоглотку, что приводит к упорному кашлю.
Воспалительный процесс распространяется в полость носа, формируя ринит, синусит с обильными выделениями из носа. Затруднение носового дыхания и ограничение подвижности мягкого неба вызывают нарушение речевой функции. Речь у них глухая, отрывистая, с оттенком гнусавости.
Затруднение носового дыхания приводит к дыханию ртом, недостаточному увлажнению, согреванию и очищению вдыхаемого воздуха, постоянному охлаждению полости рта, глотки и нижних дыхательных путей.
Вдыхаемая при ротовом дыхании масса микробов и пылевых частиц оседает на слизистой оболочке гортани, трахеи, что ведет к простудным заболеваниям, частым ангинам, фарингитам, болезням бронхов и легочной ткани.
Существует тесная связь между хроническим аденоидитом и синуситом. В случае первичного острого гнойного синусита патологический секрет транспортируется из пазух непосредственно на глоточную миндалину, которая не может не ответить на эту агрессию воспалением. В итоге синусит приводит к развитию сначала острого, а затем хронического аденоидита.
Нередко осложнение острого аденоидита – евстахиит, отит.
Аденоидные вегетации (разрастания) становятся источниками бактериальной обсемененности и грибковой аллергизации. У 25% детей с аденоидами выявляется аллергический ринит.
КОНСЕРВАТИВНАЯ ТЕРАПИЯ
Лечение аденоидита начинается с консервативной терапии.
Перед применением местных противовоспалительных препаратов необходимо очистить полость носа и носоглотки от патологического содержимого. Для этого применяется отсасывание содержимого, промывание полости носа и носоглотки стерильными солевыми растворами (АкваМарис, Маример).
Для этого применяется отсасывание содержимого, промывание полости носа и носоглотки стерильными солевыми растворами (АкваМарис, Маример).
При густом слизистом отделяемомприменяют разжижающие препараты (Ринофлуимуцил, Ацетилцистеин). Растительным препаратом разжижающим густую слизь в носоглотке и укрепляющим слизистую оболочку, является Синупрет. Он позволяет снять воспаление и отек, повышает защитные силы слизистой носа, помогает бороться с инфекцией.
После очищения полости носа и носоглотки применяют препараты для местной антибактериальной терапии (Изофра, Полидекса). Порядок применения для каждого ребенка определяет только врач.
Перспективным направлением лечения хронических аденоидитов является использование специальных бактериальных
препаратов – иммунокорректоров со свойствами вакцин (ИРС – 19).
Из физиотерапии назначается кварцевое облучение носа и глотки, лазеротерапия, а при обострениях – общая антибактериальная терапия
И антигистаминные (противоаллергические) препараты.
Курсы лечения целесообразно повторять осенью и весной.
В осеннее – зимний период необходимо проводить специфическую противовирусную профилактику – вакцинацию, местное применение противовирусных мазей (Виферон, флореналиевая и оксолиновая мази) и противовирусных препаратов (Анаферон детский).
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
При отсутствии эффекта от консервативной терапии показано хирургическое лечение – аденотомия.
В качестве профилактики развития хронического аденоидита и увеличение аденоидов можно предложить общие мероприятия: закаливание, сбалансированное питание. Даже при начальных симптомах простудных заболеваний не следует посещать детские учреждения.
М.В. Муратов, кандидат медицинских наук
ДГКБ № 5 имени Н.Ф. Филатова
М.В. Муратова, кандидат медицинских наук,
СЗГМУ имени И.И. Мечникова, Санкт-Петербург
Журнал «Для заботливых родителей № 4 2012 года
Клиническое исследование Анаферона для детей Эффективность в профилактике гриппа и других ОРВИ — Полный текст
Дизайн: международное, многоцентровое, двойное слепое, плацебо-контролируемое, рандомизированное исследование в параллельных группах.
В исследование будут включены дети любого пола в возрасте от 1 месяца до 6 лет. Дети могут участвовать в исследовании независимо от частоты перенесенных ОРВИ. Потенциальный участник исследования не должен находиться в инкубационном (если известно), продромальном, остром/подостром периодах любого инфекционного заболевания (кроме периода выздоровления).График набора участников: в период сезонного подъема заболеваемости гриппом/ОРВИ в Российской Федерации и Республике Узбекистан. Скрининг и рандомизация участников будут осуществляться при наличии официальной информации о заболеваемости гриппом/ОРВИ в соответствующем регионе исследования.
Врач совершает первый визит к участнику в медицинском центре или на дому. После того, как родитель/усыновитель подпишет информационный лист (форму информированного согласия), врач оценивает возможность включения участника в исследование.Если ребенок соответствует всем критериям включения и не имеет всех критериев невключения, то он включается в исследование, врач заполняет Бланк клинического исследования. На 1-м визите (1-й день) участника рандомизируют в одну из двух групп: участники 1-й группы будут принимать Анаферон детский по профилактической схеме в течение 12 недель; участники 2-й группы будут принимать Плацебо по схеме Анаферона в течение 12 недель.
На 1-м визите (1-й день) участника рандомизируют в одну из двух групп: участники 1-й группы будут принимать Анаферон детский по профилактической схеме в течение 12 недель; участники 2-й группы будут принимать Плацебо по схеме Анаферона в течение 12 недель.
Всего участник исследования будет наблюдаться 12 недель (скрининг и рандомизация до 1 дня, профилактическое лечение 12 недель).
В период наблюдения в 4 (2-й визит), 8 (3-й визит) и 12 (4-й визит) недель запланировано три визита.
Визиты 2 (неделя 4 ± 3 дня) и 3 (неделя 8 ± 3 дня) проводятся в форме телефонного опроса родителей/усыновителей о состоянии здоровья обследуемого, наличии/отсутствии симптомов гриппа/ОРВИ, возможных применение антибактериальных препаратов и/или госпитализация на фоне курсовой профилактической терапии.
Визит 4 (12 неделя ± 3 дня) проводится на дому или в медицинском центре; врач собирает жалобы, осматривает участника, регистрирует сопутствующую терапию, оценивает соблюдение терапии.
Если в период от 2 до 12 недель участник заболел гриппом/ОРВИ, то он досрочно завершает участие в исследовании (как достигший первичной конечной точки). Участник считается заболевшим гриппом/ОРВИ при выявлении врачом следующих симптомов: фебрильная/субфебрильная температура тела, наличие хотя бы одного гриппоподобного неспецифического симптома (снижение активности/нарушение поведения/слабость; головная боль; озноб) и хотя бы одного респираторный симптом (насморк, заложенность носа, охриплость/хриплый голос, боль в горле, кашель).В этом случае врач совершает внеплановый визит (на дом или в медицинский центр), который является окончательным. Во время визита врач проводит процедуры визита 4. Берется мазок из носоглотки для выявления наиболее частых возбудителей гриппа/ОРВИ.
При возникновении ОРВИ/гриппа в течение первых семи дней от начала профилактической терапии заболевание не регистрируется как нежелательное явление и не учитывается для оценки эффективности исследуемого препарата, поскольку раннее проявление гриппа /ОРВИ может свидетельствовать о включении участника в исследование, когда он находился в инкубационном периоде инфекционного заболевания.
В ходе исследования допускается сопутствующая терапия фоновых хронических состояний, а также плановая вакцинация участника, за исключением препаратов, указанных в разделе «Запрещенное сопутствующее лечение».
Взгляд на механизм действия сильно разведенных биологических препаратов
Ключевые моменты
Сильно разведенные антитела к IFN-γ индуцируют конформационные изменения в IFN-γ.
Высокоразведенные антитела к IFN-γ улучшают связывание IFN-γ с рецептором IFN-γ.
Высокоразведенные антитела к IFN-γ повышают выживаемость мышей с инфекцией гриппа А.
Abstract
Терапевтическое использование АТ в лечении рака, аутоиммунитета, трансплантологии и других областях является одним из основных биофармацевтических достижений 20-го века. Более широкое использование препаратов на основе антител сдерживается высокой стоимостью их производства и частыми побочными эффектами. Одним из многообещающих подходов для преодоления этих ограничений является использование сильно разбавленных АТ, которые получают путем постепенного снижения концентрации АТ до чрезвычайно низкого уровня. Эта технология была использована для создания группы препаратов для лечения различных заболеваний в зависимости от специфичности используемых АТ. Было показано, что высокоразведенные антитела к IFN-γ (hd-анти-IFN-γ) эффективны против гриппа и других респираторных инфекций в различных доклинических и клинических исследованиях. В текущем исследовании мы приводим доказательства возможного механизма действия hd-анти-IFN-γ. Используя спектроскопию ядерного магнитного резонанса высокого разрешения в растворе, мы показываем, что лекарство индуцирует конформационные изменения в молекуле IFN-γ.Изменения химического сдвига произошли в аминокислотах, расположенных в основном на поверхности димера и в С-концевой области IFN-γ. Эти молекулярные изменения могут иметь решающее значение для функции белка, о чем свидетельствует наблюдаемое HD-анти-IFN-γ-индуцированное увеличение специфического связывания IFN-γ с его рецептором в клетках U937, усиленная индуцированная продукция IFN-γ в культуре РВМС человека и повышение выживаемости мышей, инфицированных гриппом А.
Эта технология была использована для создания группы препаратов для лечения различных заболеваний в зависимости от специфичности используемых АТ. Было показано, что высокоразведенные антитела к IFN-γ (hd-анти-IFN-γ) эффективны против гриппа и других респираторных инфекций в различных доклинических и клинических исследованиях. В текущем исследовании мы приводим доказательства возможного механизма действия hd-анти-IFN-γ. Используя спектроскопию ядерного магнитного резонанса высокого разрешения в растворе, мы показываем, что лекарство индуцирует конформационные изменения в молекуле IFN-γ.Изменения химического сдвига произошли в аминокислотах, расположенных в основном на поверхности димера и в С-концевой области IFN-γ. Эти молекулярные изменения могут иметь решающее значение для функции белка, о чем свидетельствует наблюдаемое HD-анти-IFN-γ-индуцированное увеличение специфического связывания IFN-γ с его рецептором в клетках U937, усиленная индуцированная продукция IFN-γ в культуре РВМС человека и повышение выживаемости мышей, инфицированных гриппом А.
Введение
Препараты на основе антител быстро увеличивают свою долю на рынке лекарственных средств.Приблизительно 60 mAb были одобрены для клинического применения (1). Несмотря на растущий спрос, использование терапевтических АТ остается проблематичным из-за ограничений их пероральной доступности, проблем со стабильностью и их побочных эффектов (2, 3). Таким образом, многие исследования были направлены на разработку и усовершенствование фармацевтических препаратов на основе антител с помощью адъювантов, химических модификаций, инкапсуляции и т. д. (4–6).
Одним из многообещающих новых подходов для преодоления этих ограничений является постепенное снижение исходной концентрации Ab для достижения его сверхвысокого разведения (7).Эта платформа успешно используется для производства группы безопасных и эффективных препаратов для лечения различных состояний, включая инфекционные заболевания, эндокринные нарушения, урогенитальную дисфункцию и др. (8–10).
Вышеупомянутая технология была применена к регуляторным молекулам-мишеням, включая цитокин IFN-γ, который участвует в различных физиологических и болезненных состояниях. IFN-γ представляет собой гомодимерный гликопротеин (рис. 1) с плейотропными функциями, продуцируемый преимущественно Т-лимфоцитами и NK-клетками.Он действует как модулятор множества иммунных функций, включая противовирусный иммунный ответ. IFN-γ проявляет эту активность посредством связывания со своим высокоаффинным рецептором, состоящим из α- и β-цепей, что приводит к их объединению в активный комплекс и передаче сигналов через путь JAK/STAT (11).
IFN-γ представляет собой гомодимерный гликопротеин (рис. 1) с плейотропными функциями, продуцируемый преимущественно Т-лимфоцитами и NK-клетками.Он действует как модулятор множества иммунных функций, включая противовирусный иммунный ответ. IFN-γ проявляет эту активность посредством связывания со своим высокоаффинным рецептором, состоящим из α- и β-цепей, что приводит к их объединению в активный комплекс и передаче сигналов через путь JAK/STAT (11).
Антитела против IFN-γ использовались для воздействия на иммунный ответ в экспериментальных моделях (12, 13), но их клиническая разработка не увенчалась успехом, несмотря на демонстрацию некоторых преимуществ (14, 15).Природные аутоантитела к IFN-γ присутствуют у здоровых людей; они увеличивают титр во время инфекций и при некоторых заболеваниях, и было показано, что они нарушают иммуномодулирующую активность цитокина (16). Эти факты побудили нас рассмотреть подход на основе антител для модуляции функций IFN-γ in vivo путем разработки агента на основе сильно разбавленных антител к IFN-γ (hd-анти-IFN-γ). На сегодняшний день уже изучена способность hd-анти-ИФН-γ регулировать функциональную активность и продукцию эндогенных ИФН, модулировать иммунный ответ и влиять на уровень естественных циркулирующих антител к ИФН-γ (17, 18). .Кроме того, противовирусная активность hd-анти-IFN-γ в отношении гриппа и других респираторных инфекций была продемонстрирована в различных доклинических и клинических исследованиях (17, 19–23). Информацию о недавних клинических испытаниях можно найти на сайте ClinicalTrials.gov (https://clinicaltrials.gov/ct2/results?cond=&term=anaferon&cntry=&state=&city=&dist=).
На сегодняшний день уже изучена способность hd-анти-ИФН-γ регулировать функциональную активность и продукцию эндогенных ИФН, модулировать иммунный ответ и влиять на уровень естественных циркулирующих антител к ИФН-γ (17, 18). .Кроме того, противовирусная активность hd-анти-IFN-γ в отношении гриппа и других респираторных инфекций была продемонстрирована в различных доклинических и клинических исследованиях (17, 19–23). Информацию о недавних клинических испытаниях можно найти на сайте ClinicalTrials.gov (https://clinicaltrials.gov/ct2/results?cond=&term=anaferon&cntry=&state=&city=&dist=).
Физико-химические свойства hd-анти-ИФН-γ изучены методами динамического светорассеяния, кондуктометрии, рН-метрии и тензиометрии.Эти результаты показали, что водные растворы сильно разбавленных АТ представляют собой самоорганизующиеся дисперсные системы, в которых формируются нанообъекты (24). Самоорганизация растворов АТ сопровождалась существенным изменением их свойств по сравнению с аналогично обработанной водой. Кроме того, было показано, что раствор hd-анти-ИФН-γ может содержать агрегаты исходных АТ, связанные с газовыми нанопузырьками, которые остаются в многократно разбавленной жидкости за счет флотационного эффекта (25).Эти данные согласуются с ранее продемонстрированным присутствием исходных материалов в форме наночастиц даже в экстремальных разведениях (26).
Кроме того, было показано, что раствор hd-анти-ИФН-γ может содержать агрегаты исходных АТ, связанные с газовыми нанопузырьками, которые остаются в многократно разбавленной жидкости за счет флотационного эффекта (25).Эти данные согласуются с ранее продемонстрированным присутствием исходных материалов в форме наночастиц даже в экстремальных разведениях (26).
С помощью пьезоэлектрического иммуносенсора мы показали, что взаимодействие между IFN-γ и IFN-γ-специфическими антителами изменилось в присутствии hd-анти-IFN-γ (27). Были продемонстрированы конформационные изменения Ag при связывании Ab (28). Подобный аллостерический эффект на антиген также может быть приписан сильно разбавленным антигенам. Таким образом, целью настоящего исследования было выяснить, может ли hd-анти-ИФН-γ вызывать конформационные изменения в молекуле ИФН-γ, влияющие на ее биологическую активность и взаимодействие с другими молекулами (т.д., рецептор IFN-γ).
Материалы и методы
Изготовление экспериментальных образцов
HD-анти–ИФН-γ – активная фармацевтическая субстанция противовирусного коммерческого препарата Анаферон для детей (ООО «НПФ «Материа Медика Холдинг», Москва, Российская Федерация). Аффинно-очищенные кроличьи поликлональные антитела к человеческому rIFN-γ (исходная концентрация 2,5 мг/мл) были произведены в соответствии с действующими требованиями Европейского Союза к GMP для исходных материалов (29) компанией Angel Biotechnology Holdings (Penicuik, U.К.). HD-анти–ИФН-γ были произведены на заводе ООО «НПФ «Материа Медика Холдинг» по технологии, описанной в патенте США 8,535,664 (30). Вкратце, АТ к ИФН-γ (2,5 мг/мл) смешивали с растворителем (этанол–водный раствор) в соотношении 1:100 и подвергали интенсивной вибрационной обработке для получения первого сотенного разведения (т.е. 100-кратного разведения). . Все последующие разведения включали одну часть предыдущего разведения и 99 частей растворителя (этанол-водный раствор для промежуточных разведений и очищенную воду для приготовления конечных разведений) с интенсивной вибрационной обработкой между стадиями разбавления.Наконец, hd-анти-IFN-γ содержит смесь 12-го, 30-го и 50-го сотенных разведений. Теоретический уровень снижения концентрации исходных АТ составляет не менее 1 × 10 24 .
Аффинно-очищенные кроличьи поликлональные антитела к человеческому rIFN-γ (исходная концентрация 2,5 мг/мл) были произведены в соответствии с действующими требованиями Европейского Союза к GMP для исходных материалов (29) компанией Angel Biotechnology Holdings (Penicuik, U.К.). HD-анти–ИФН-γ были произведены на заводе ООО «НПФ «Материа Медика Холдинг» по технологии, описанной в патенте США 8,535,664 (30). Вкратце, АТ к ИФН-γ (2,5 мг/мл) смешивали с растворителем (этанол–водный раствор) в соотношении 1:100 и подвергали интенсивной вибрационной обработке для получения первого сотенного разведения (т.е. 100-кратного разведения). . Все последующие разведения включали одну часть предыдущего разведения и 99 частей растворителя (этанол-водный раствор для промежуточных разведений и очищенную воду для приготовления конечных разведений) с интенсивной вибрационной обработкой между стадиями разбавления.Наконец, hd-анти-IFN-γ содержит смесь 12-го, 30-го и 50-го сотенных разведений. Теоретический уровень снижения концентрации исходных АТ составляет не менее 1 × 10 24 . Таким образом, если не принимать во внимание физические аспекты, упомянутые во Введении , теоретическая концентрация исходных АТ может составлять 2,5 × 10 -24 мг/мл. Это значение упоминается в этой статье только во избежание неправильного понимания уровня разбавления. Высокоразведенные антитела к TNF-α (hd-анти-TNF-α) были приготовлены с использованием аналогичного метода, но исходный раствор содержал аффинно-очищенные поликлональные антитела кролика против человеческого rTNF-α (исходная концентрация 2.5 мг/мл). Плацебо-контроль, не содержащий антител, готовили, применяя ту же процедуру к очищенной воде. В качестве носителя использовали очищенную воду. Все растворы готовили в стеклянных флаконах в стерильных условиях, защищенных от прямого интенсивного света, и хранили при комнатной температуре. Образцы были закодированы производителем и отправлены в исследовательские организации США (Университет Питтсбурга), Бельгии (Euroscreen), Нидерландов (U-CyTech biosciences) и Франции (Apcis), где соответствующие исследования были проведены независимо.
Таким образом, если не принимать во внимание физические аспекты, упомянутые во Введении , теоретическая концентрация исходных АТ может составлять 2,5 × 10 -24 мг/мл. Это значение упоминается в этой статье только во избежание неправильного понимания уровня разбавления. Высокоразведенные антитела к TNF-α (hd-анти-TNF-α) были приготовлены с использованием аналогичного метода, но исходный раствор содержал аффинно-очищенные поликлональные антитела кролика против человеческого rTNF-α (исходная концентрация 2.5 мг/мл). Плацебо-контроль, не содержащий антител, готовили, применяя ту же процедуру к очищенной воде. В качестве носителя использовали очищенную воду. Все растворы готовили в стеклянных флаконах в стерильных условиях, защищенных от прямого интенсивного света, и хранили при комнатной температуре. Образцы были закодированы производителем и отправлены в исследовательские организации США (Университет Питтсбурга), Бельгии (Euroscreen), Нидерландов (U-CyTech biosciences) и Франции (Apcis), где соответствующие исследования были проведены независимо. Образцы тестировались вслепую.
Образцы тестировались вслепую.
Спектроскопия ядерного магнитного резонанса
Кодирующая последовательность человеческого IFN-γ без сигнального пептида (Thermo Fisher Scientific) была клонирована в рамку считывания с N-концевой His6-меткой, за которой следует Strep-метка в pET-28b(+ ) вектор (Novagen). IFN-γ амплифицировали из кДНК в двухэтапной ПЦР с использованием трех праймеров (прямой праймер 1: 5′-CCGCAGTTCGAAAAAGGCGCGCCC CAGGACCCATATGTA -3′; 5′-прямой праймер 2: 5′-TATACATATGG CTAG CTGGAGCCACCCGCAGTTCGAAAAA-3′ ; обратный праймер: 5′-GTG CTAG TCGACGC GGCC GC TTACTGGGATGCTCTTCG -3′) для получения фрагмента, вводящего Strep-метку, а также сайты рестрикции NheI и NotI, необходимые для клонирования в pET-28( б+) вектор.Полную конструкцию трансформировали в компетентные клетки Rosetta(DE3)pLysS (Lucigen). Двойную дрожжевую триптоновую среду (16 г триптона, 10 г дрожжевого экстракта и 5 г NaCl на литр [pH 7,4]), содержащую 50 мкг/мл канамицина, инокулировали глицериновым раствором рекомбинантных клеток и инкубировали в течение ночи при 37°С при встряхивании ( 200 об/мин). Один литр двойной триптоновой среды для дрожжей с 50 мкг/мл канамицина инокулировали ночной культурой с получением исходной OD 600 , равной 0,1. Культуру поровну разделяли на три 2-литровые колбы и инкубировали при 37°С при встряхивании при 160 об/мин до достижения ОП 600 , равной 0.5–0,6. Клетки собирали центрифугированием (3000× g ; 30 мин) и удаляли надосадочную жидкость. Каждый осадок ресуспендировали в 0,3 л минимальной среды М9 (6,6 г Na 2 HPO 4 , 3,0 г KH 2 PO 4 , 0,5 г NaCl, 0,4% глюкозы, 1,0 мМ 0,0 MgSO 4 CaCl 2 , 1,0 мг биотина и 0,5 мг тиамина/л) с добавлением 1,0 г/л 15 N-меченый NH 4 Cl (Cambridge Isotopes), содержащий 50 мкг/мл канамицина и инкубированный при 37°C с встряхивание при 160 об/мин в течение 1 часа.Экспрессию индуцировали добавлением изопропил-β-d-1-тиогалактопиранозида до конечной концентрации 1,0 мМ и инкубировали культуру в течение 4 ч при 37°С при встряхивании со скоростью 160 об/мин.
Один литр двойной триптоновой среды для дрожжей с 50 мкг/мл канамицина инокулировали ночной культурой с получением исходной OD 600 , равной 0,1. Культуру поровну разделяли на три 2-литровые колбы и инкубировали при 37°С при встряхивании при 160 об/мин до достижения ОП 600 , равной 0.5–0,6. Клетки собирали центрифугированием (3000× g ; 30 мин) и удаляли надосадочную жидкость. Каждый осадок ресуспендировали в 0,3 л минимальной среды М9 (6,6 г Na 2 HPO 4 , 3,0 г KH 2 PO 4 , 0,5 г NaCl, 0,4% глюкозы, 1,0 мМ 0,0 MgSO 4 CaCl 2 , 1,0 мг биотина и 0,5 мг тиамина/л) с добавлением 1,0 г/л 15 N-меченый NH 4 Cl (Cambridge Isotopes), содержащий 50 мкг/мл канамицина и инкубированный при 37°C с встряхивание при 160 об/мин в течение 1 часа.Экспрессию индуцировали добавлением изопропил-β-d-1-тиогалактопиранозида до конечной концентрации 1,0 мМ и инкубировали культуру в течение 4 ч при 37°С при встряхивании со скоростью 160 об/мин. Клетки собирали центрифугированием, осадок замораживали при -20°С.
Клетки собирали центрифугированием, осадок замораживали при -20°С.
Затем осадок оттаивали и ресуспендировали в 5 мл буфера А (50 мМ фосфата натрия [pH 8] и 300 мМ NaCl) на 1,0 г свежего веса. Суспензию обрабатывали ультразвуком шестью импульсами по 10 с каждый с 10-секундной паузой на льду между импульсами.Лизат центрифугировали при 5000 × г при 4°C в течение 15 мин, затем осадок ресуспендировали в таком же количестве буфера А. После стадии центрифугирования при 5000 × г при 4°C в течение 15 мин, осадок ресуспендировали в 5 мл буфера Б (100 мМ фосфата натрия [pH 8], 10 мМ Трис и 6,0 М гидрохлорида гуанидина) на 1,0 г сырого веса осадка и перемешивали в течение 1 ч при комнатной температуре. Суспензию центрифугировали при 15 000 × g в течение 30 мин при 4°C, а супернатант наносили на колонку Ni-NTA объемом 5 мл (QIAGEN), уравновешенную пятью объемами колонки буфера B.Колонку промывали 10 колоночными объемами буфера B и 10 колоночными объемами буфера C (100 мМ фосфата натрия [pH 6,3], 10 мМ Трис и 6,0 М гидрохлорида гуанидина) перед элюированием белка четырьмя колоночными объемами элюирующего буфера ( 100 мМ натрий-фосфатного буфера [рН 4,5], 10 мМ Трис и 6,0 М гуанидина гидрохлорида). Всего к элюируемым фракциям по каплям добавляли 350 мл буфера для рефолдинга (150 мМ NaCl, 100 мМ глицина, 20 мМ Трис [pH 8], 100 мМ PMSF и одна таблетка ингибитора протеазы [номер по каталогу 04693132001; Roche]). при комнатной температуре при перемешивании для ускорения рефолдинга белка.Затем раствор оставляли при 4°С на ночь при постоянном перемешивании. На следующий день раствор концентрировали с помощью фильтрующего устройства (отсечка 10 кДа) до объема примерно 5 мл. Концентрированный белок загружали в колонку для гель-фильтрации Superdex 75 (16/60) после уравновешивания колонки 120 мл буфера для гель-фильтрации (10 мМ натрий-фосфатного буфера [pH 7,4], 150 мМ NaCl и одна таблетка ингибитора протеазы). Петлю промывали 15 мл буфера для гель-фильтрации и образец элюировали при скорости потока 1.0 мл/мин с 1,5 объемами колонки того же буфера на фракции элюции по 2,0 мл. Элюированные фракции, содержащие 15 N-меченый IFN-γ, объединяли и концентрировали до 0,4 мМ с использованием концентраторов Amicon для исследований методом ядерного магнитного резонанса (ЯМР) и анализировали при конечной концентрации 50 мкМ.
Всего к элюируемым фракциям по каплям добавляли 350 мл буфера для рефолдинга (150 мМ NaCl, 100 мМ глицина, 20 мМ Трис [pH 8], 100 мМ PMSF и одна таблетка ингибитора протеазы [номер по каталогу 04693132001; Roche]). при комнатной температуре при перемешивании для ускорения рефолдинга белка.Затем раствор оставляли при 4°С на ночь при постоянном перемешивании. На следующий день раствор концентрировали с помощью фильтрующего устройства (отсечка 10 кДа) до объема примерно 5 мл. Концентрированный белок загружали в колонку для гель-фильтрации Superdex 75 (16/60) после уравновешивания колонки 120 мл буфера для гель-фильтрации (10 мМ натрий-фосфатного буфера [pH 7,4], 150 мМ NaCl и одна таблетка ингибитора протеазы). Петлю промывали 15 мл буфера для гель-фильтрации и образец элюировали при скорости потока 1.0 мл/мин с 1,5 объемами колонки того же буфера на фракции элюции по 2,0 мл. Элюированные фракции, содержащие 15 N-меченый IFN-γ, объединяли и концентрировали до 0,4 мМ с использованием концентраторов Amicon для исследований методом ядерного магнитного резонанса (ЯМР) и анализировали при конечной концентрации 50 мкМ.
ЯМР-эксперименты проводились при 25°C на спектрометре Bruker Avance 900 МГц, оборудованном 5-мм криозондом с тройным резонансом и градиентным криозондом z . Двумерные (2D) спектры 1 H– 15 N только для IFN-γ были получены с использованием стандартной последовательности импульсов гетероядерной одиночной квантовой когерентности (HSQC) со 128 сканами в протонном измерении и 128 сканами в азотном измерении. , с задержкой 1 с.Для ЯМР-образцов, содержащих IFN-γ с добавлением сильно разбавленных антител или плацебо, спектры получали при сканировании 2048 × 34. Сбор данных проводили с использованием программного обеспечения TopSpin версии 3.0 (Bruker BioSpin, Billerica, MA). Спектры обрабатывали и анализировали с использованием программного обеспечения NMR View (31) и Sparky (SPARKY 3; Т. Д. Годдард и Д. Г. Кнеллер, Калифорнийский университет, Сан-Франциско). Наблюдаемые резонансы основной цепи были сопоставлены с использованием ранее опубликованных данных ЯМР, которые были получены в аналогичных условиях для конструкции IFN-γ, содержащей остатки 1–133 (всего 143 остатка) (32). Из 133 ожидаемых сигналов амида основной цепи 130 наблюдались в спектре HSQC. Мы однозначно определили 128 из 130 ранее назначенных остатков в нашей выборке. Для назначения был приготовлен более концентрированный образец, чем тот, который использовался для тестирования эффектов hd-анти-IFN-γ, и был подвергнут спектроскопическому анализу 2D 1 H– 15 N HSQC. Этот образец содержал 400 мкМ концентрированного 15 N-меченого IFN-γ в 20 мМ калий-фосфатном буфере (pH 6), содержащем 20 мМ NaCl и 10% D 2 O, который использовали для записи спектров.Для экспериментов ЯМР с участием hd-анти-IFN-γ и плацебо тестируемые образцы добавляли к 50 мкМ 15 N-меченого IFN-γ в 20 мМ калий-фосфатном буфере (pH 6), 20 мМ NaCl и 10 % D 2 O. В каждом случае образцы ЯМР готовили идентичным образом в трех отдельных пробирках: 21,5 мкл IFN-γ плюс 113 мкл буфера (20 мМ K 2 HPO 4 /KH 2 PO 4 плюс 20 мМ NaCl плюс 10% D 2 O, [pH 6]) добавляли к 42 мкл либо плацебо, либо hd-анти-IFN-γ, чтобы получить конечную концентрацию 50 мкМ IFN- γ.
Из 133 ожидаемых сигналов амида основной цепи 130 наблюдались в спектре HSQC. Мы однозначно определили 128 из 130 ранее назначенных остатков в нашей выборке. Для назначения был приготовлен более концентрированный образец, чем тот, который использовался для тестирования эффектов hd-анти-IFN-γ, и был подвергнут спектроскопическому анализу 2D 1 H– 15 N HSQC. Этот образец содержал 400 мкМ концентрированного 15 N-меченого IFN-γ в 20 мМ калий-фосфатном буфере (pH 6), содержащем 20 мМ NaCl и 10% D 2 O, который использовали для записи спектров.Для экспериментов ЯМР с участием hd-анти-IFN-γ и плацебо тестируемые образцы добавляли к 50 мкМ 15 N-меченого IFN-γ в 20 мМ калий-фосфатном буфере (pH 6), 20 мМ NaCl и 10 % D 2 O. В каждом случае образцы ЯМР готовили идентичным образом в трех отдельных пробирках: 21,5 мкл IFN-γ плюс 113 мкл буфера (20 мМ K 2 HPO 4 /KH 2 PO 4 плюс 20 мМ NaCl плюс 10% D 2 O, [pH 6]) добавляли к 42 мкл либо плацебо, либо hd-анти-IFN-γ, чтобы получить конечную концентрацию 50 мкМ IFN- γ.
Анализ насыщения связывания радиолиганда
Анализ проводили путем последовательного добавления следующих реагентов в силиконизированные микроцентрифужные пробирки: 50 мкл буфера для анализа (культуральная среда RPMI 1640 [12–115F; Lonza Bioscience] с добавлением 10% FBS [Ch40160.03 ; Perbio]), 25 мкл [ 125 I]IFN-γ (разбавленного в буфере для анализа с 0,4% азидом натрия в возрастающих концентрациях [3,0, 1,0, 0,3, 0,1, 0,03, 0,01, 0,003 и 0,001 нМ; 285 -IF/CF; R&D Systems; индивидуальная маркировка Perkin Elmer]), и 25 мкл суспензии человеческих моноцитоподобных клеток линии U-937 (85011440; Sigma-Aldrich; 1 миллион клеток на пробирку, разведенных в буфере для анализа без натрия азид; 200 мкг общего белка на точку измерения).Для определения неспецифического связывания в лунку добавляли 50 мкл IFN-γ (285-IF/CF; R&D Systems) (разведенного в буфере для анализа без азида натрия до конечной концентрации 300 нМ) вместо 50 мкл буфера для анализа.
Пробирки инкубировали 150 мин при 4°C и затем центрифугировали. Супернатант удаляли, а осадок клеток промывали один раз 1 мл ледяного буфера для анализа. Пробирки снова центрифугировали, супернатант удаляли, дно пробирки, содержащей осадок клеток, разрезали, помещали в счетные пробирки и затем подсчитывали с помощью счетчика гамма-излучения Cobra (Packard Instrument) в течение 1 мин на пробирку.
Супернатант удаляли, а осадок клеток промывали один раз 1 мл ледяного буфера для анализа. Пробирки снова центрифугировали, супернатант удаляли, дно пробирки, содержащей осадок клеток, разрезали, помещали в счетные пробирки и затем подсчитывали с помощью счетчика гамма-излучения Cobra (Packard Instrument) в течение 1 мин на пробирку.
Значения Kd были рассчитаны с использованием программного обеспечения GraphPad Prism и опции односайтового связывания (гипербола). Данные доза-реакция были проанализированы с помощью программного обеспечения XLfit (IDBS Software Solutions) с использованием нелинейной регрессии, примененной к сигмоидальной модели доза-реакция, как описано в соответствующем руководстве GraphPad для анализа данных связывания радиолиганда (33).
Анализ конкуренции связывания радиолиганда
Анализ проводили путем последовательного добавления следующих реагентов в силиконизированные микроцентрифужные пробирки: 50 мкл hd-анти-IFN-γ ( n = 5), hd-анти-TNF-α ( n = 5), растворитель ( n = 4), буфер ( n = 3) (буфер для анализа без азида натрия) или IFN-γ (разбавленный в буфере для анализа без азида натрия) в возрастающих концентрациях (0 . 001, 0,01, 0,1, 1,0, 10 и 100 нМ), 25 мкл [ 125 I]IFN-γ (разбавленного в буфере для анализа 0,4% азида натрия в концентрации, соответствующей Kd = 0,14 ± 0,05 нМ, как определено с помощью анализа связывания насыщения радиолиганда; дополнительная рис. 1), и 25 мкл клеточной суспензии U-937 (1 миллион клеток на пробирку, разведенных в буфере для анализа без азида натрия; 200 мкг общего белка на данные точку в случае определения общего связывания лиганда). Следующая процедура такая же, как и для анализа связывания насыщения.
001, 0,01, 0,1, 1,0, 10 и 100 нМ), 25 мкл [ 125 I]IFN-γ (разбавленного в буфере для анализа 0,4% азида натрия в концентрации, соответствующей Kd = 0,14 ± 0,05 нМ, как определено с помощью анализа связывания насыщения радиолиганда; дополнительная рис. 1), и 25 мкл клеточной суспензии U-937 (1 миллион клеток на пробирку, разведенных в буфере для анализа без азида натрия; 200 мкг общего белка на данные точку в случае определения общего связывания лиганда). Следующая процедура такая же, как и для анализа связывания насыщения.
Анализ IFN-γ ELISpot
Набор человеческого IFN-γ ELISpot (красная точка; номер по каталогу CT230-PR2; U-CyTech biosciences) использовали для определения эффекта hd-анти-IFN-γ или носителя на генерацию клеток, продуцирующих IFN-γ, в популяции 4 × 10 5 РВМС человека на лунку со стандартным клеточным стимулом. РВМС выделяли из венозной крови одного здорового донора методом центрифугирования в градиенте плотности. Процедура выполнялась в соответствии с инструкциями производителя с некоторыми изменениями. Вкратце, пластины с нижней мембраной из PVDF предварительно смачивали и покрывали захватывающим Ab в течение ночи при 4°C. Перед началом эксперимента культуральную среду лиофилизировали (продолжительность 48 ч). Затем сухое вещество восстанавливали в hd-анти-IFN-γ ( n = 6) или в растворителе ( n = 6) и затем стерилизовали фильтрованием (0,2 мкм). U-CyTech biosciences (Утрехт, Нидерланды) предоставила РВМС человека. Клетки ресуспендировали в культуральной среде, содержащей hd-анти-IFN-γ или носитель, и стимулировали пептидным пулом ICE (пулом из 23 вирусных пептидов вируса гриппа А, CMV и эпитопов EBV, распознаваемых CD8 + Т-клетками). , каталожный номерСТ370; бионауки U-CyTech). Лунки с нестимулированными клетками в среде, восстановленной в носителе, использовали в качестве контроля для подсчета фоновых пятен.
Вкратце, пластины с нижней мембраной из PVDF предварительно смачивали и покрывали захватывающим Ab в течение ночи при 4°C. Перед началом эксперимента культуральную среду лиофилизировали (продолжительность 48 ч). Затем сухое вещество восстанавливали в hd-анти-IFN-γ ( n = 6) или в растворителе ( n = 6) и затем стерилизовали фильтрованием (0,2 мкм). U-CyTech biosciences (Утрехт, Нидерланды) предоставила РВМС человека. Клетки ресуспендировали в культуральной среде, содержащей hd-анти-IFN-γ или носитель, и стимулировали пептидным пулом ICE (пулом из 23 вирусных пептидов вируса гриппа А, CMV и эпитопов EBV, распознаваемых CD8 + Т-клетками). , каталожный номерСТ370; бионауки U-CyTech). Лунки с нестимулированными клетками в среде, восстановленной в носителе, использовали в качестве контроля для подсчета фоновых пятен.
PBMC высевали по 4 × 10 5 клеток на лунку в 100 мкл в трех повторностях. Планшеты ELISpot закрывали крышками и инкубировали при 37°C, 5% CO 2 и 100% влажности в течение примерно 20 часов. После инкубации и промывки основную массу клеток удаляли сильным встряхиванием и в каждую лунку добавляли биотинилированные детектирующие АТ на 1 ч при 37°С.Далее в лунки добавляли раствор стрептавидин-HRP на 1 ч при 37°С, затем субстрат 3-амино-9-этилкарбазол с образованием окрашенной зоны (пятна) на 25 мин при комнатной температуре. Развитие окраски останавливали тщательной промывкой обеих сторон ПВДФ-мембраны деминерализованной водой (собственного производства) и пластины высушивали на воздухе при комнатной температуре. Цветная зона показывает место секреции цитокинов, а клетки, продуцирующие IFN-γ, подсчитывали, анализируя развитие окраски с помощью анализатора изображения ImmunoSpot (CTL, Oberndorf am Neckar, Germany).
После инкубации и промывки основную массу клеток удаляли сильным встряхиванием и в каждую лунку добавляли биотинилированные детектирующие АТ на 1 ч при 37°С.Далее в лунки добавляли раствор стрептавидин-HRP на 1 ч при 37°С, затем субстрат 3-амино-9-этилкарбазол с образованием окрашенной зоны (пятна) на 25 мин при комнатной температуре. Развитие окраски останавливали тщательной промывкой обеих сторон ПВДФ-мембраны деминерализованной водой (собственного производства) и пластины высушивали на воздухе при комнатной температуре. Цветная зона показывает место секреции цитокинов, а клетки, продуцирующие IFN-γ, подсчитывали, анализируя развитие окраски с помощью анализатора изображения ImmunoSpot (CTL, Oberndorf am Neckar, Germany).
Животные и эксперименты in vivo
Мыши.
В исследовании с вирусом h2N1 в возрасте 4–5 недель и массой тела 15–17 г (при заражении вирусом) самки мышей BALB/c (Janvier Labs, Le Genest-Saint-Isle, Франция) были случайным образом распределены в три группы по 20 мышей в каждой. В исследовании с вирусом h4N8 в возрасте 5–7 недель и массой тела 14–18 г (при заражении вирусом) самок мышей BALB/c (лаборатория Чарльза Ривера, Сант-Анджело-Лодиджано, Италия) случайным образом распределяли на четыре группы: по 20 мышей. Мышей содержали по 10 в клетке с высокоэффективными воздушными фильтрами для твердых частиц (лаборатория Чарльза Ривера) в изоляторах уровня биобезопасности 2 в Центре биомедицинских исследований Национальной ветеринарной школы Альфор, Maisons Alfort, Франция.Мышей кормили стерильной поддерживающей диетой для грызунов (A010-Safe, F89 Augy) и негазированной водой (Beaupré). Все исследования с использованием живых вирусов проводились в условиях усиленной защиты 2-го уровня биобезопасности. Исследования на животных проводились в соответствии с применимыми законами и руководствами и соответствовали рекомендациям Национального исследовательского совета (34–36). Исследования были одобрены Институциональным комитетом по этике Центра биомедицинских исследований Национальной ветеринарной школы Альфорт (№ C2EA-16, от октября 2011 г.
В исследовании с вирусом h4N8 в возрасте 5–7 недель и массой тела 14–18 г (при заражении вирусом) самок мышей BALB/c (лаборатория Чарльза Ривера, Сант-Анджело-Лодиджано, Италия) случайным образом распределяли на четыре группы: по 20 мышей. Мышей содержали по 10 в клетке с высокоэффективными воздушными фильтрами для твердых частиц (лаборатория Чарльза Ривера) в изоляторах уровня биобезопасности 2 в Центре биомедицинских исследований Национальной ветеринарной школы Альфор, Maisons Alfort, Франция.Мышей кормили стерильной поддерживающей диетой для грызунов (A010-Safe, F89 Augy) и негазированной водой (Beaupré). Все исследования с использованием живых вирусов проводились в условиях усиленной защиты 2-го уровня биобезопасности. Исследования на животных проводились в соответствии с применимыми законами и руководствами и соответствовали рекомендациям Национального исследовательского совета (34–36). Исследования были одобрены Институциональным комитетом по этике Центра биомедицинских исследований Национальной ветеринарной школы Альфорт (№ C2EA-16, от октября 2011 г. ; Maisons Alfort, Франция).
; Maisons Alfort, Франция).
Вирусный вызов.
Клетки почек собак Madin-Darby инкубировали в полной среде RPMI 1640 с добавлением 5% FCS при 37°C во влажной атмосфере с 5% CO 2 . Запасы вирусов гриппа A A/Equi2/Miami/1/63(h4N8) и A/California [пандемия A/California/07/2009(h2N1)] выращивали в куриных яйцах с эмбрионами (F-38 Grenoble; Lohmann Hatcheries). после возможных пассажей на мышах (2 и 0 соответственно для каждой линии). Все штаммы были получены благодаря любезному предоставлению лаборатории гриппа Института Пастера, Париж, Франция.Вирусные запасы готовили из аллантоисной жидкости и хранили аликвотами при -70°С. Титры вируса штаммов Equi2/Miami/1/63 и A/California/07/2009 (3 × 10 8 БОЕ/мл и 1,4 × 10 8 БОЕ/мл соответственно) определяли с помощью стандартного анализа бляшек. с использованием клеток почек собак Madin-Darby (37). Инфекционность этих вирусных штаммов в нашей мышиной модели титровали путем интраназального заражения 4-кратными серийными разведениями вирусов в Игле MEM для определения LD 50 , после чего дозу заражения корректировали до ближайшего кратного LD 50 , что соответствует расчетному LD 90 во всех экспериментах. Титры LD 50 рассчитывали с использованием метода, описанного Reed и Muench (38). Титрование LD исходного вируса у самок мышей BALB/c в возрасте 7 недель проводили путем интраназальной инокуляции групп из пяти мышей 40 мкл 4-кратного серийно разведенного вируса в PBS (pH 7,2) (Difco Laboratories). Мышей отслеживали на предмет развития признаков, соответствующих гриппозной инфекции, в течение 7 дней и подвергали эвтаназии, если их клиническое состояние соответствовало любому из следующих критериев: потеря 20% массы тела до заражения, развитие любых неврологических или респираторных симптомов или неспособность есть или пить.
Титры LD 50 рассчитывали с использованием метода, описанного Reed и Muench (38). Титрование LD исходного вируса у самок мышей BALB/c в возрасте 7 недель проводили путем интраназальной инокуляции групп из пяти мышей 40 мкл 4-кратного серийно разведенного вируса в PBS (pH 7,2) (Difco Laboratories). Мышей отслеживали на предмет развития признаков, соответствующих гриппозной инфекции, в течение 7 дней и подвергали эвтаназии, если их клиническое состояние соответствовало любому из следующих критериев: потеря 20% массы тела до заражения, развитие любых неврологических или респираторных симптомов или неспособность есть или пить.
Мышей интраназально заражали двумя LD 50 эквивалентами пандемического штамма гриппа A/California/07/2009(h2N1) или пятью LD 50 штамма гриппа A/Equi2/Miami/1/63(h4N8) в 50 мкл стерильного физиологического раствора распределяют поровну между обеими ноздрями. Незараженные мыши получали только разбавитель (PBS). Мышей взвешивали до заражения, а затем каждые 3 дня на протяжении всего эксперимента.
Лечение.
В исследовании h2N1 hd-анти-IFN-γ вводили через зонд два раза в день с 7-часовым интервалом между дозами 0.2 мл/мышь (т.е. 0,4 мл/мышь/день), начиная с 5 дня до и до 21 дня после заражения, как сообщалось ранее (19). Параллельно с желудочным зондом в питьевую воду добавляли hd-анти-ИФН-γ в соотношении 1:3 (замена ежедневно). Принимая во внимание, что среднее поглощение воды мышами составляет 5,7 ± 0,2 мл/30 г массы тела (39), а масса тела мышей в этом эксперименте составляла 18–20 г, поглощение hd-анти-ИФН-γ из поилки было по расчетам составляет ~0,903 мл/мышь/день. В исследовании h4N8 hd-анти-IFN-γ вводили таким же образом, но в течение 26 дней после контрольного заражения и без добавления в питьевую воду.В качестве препарата сравнения использовался осельтамивир, противовирусная активность которого в отношении вируса гриппа была доказана в ходе доклинических исследований (40, 41). Раствор осельтамивира готовили за день до контрольного заражения путем растворения содержимого 75 мг капсулы Тамифлю (осельтамивир; Roche, Welwyn Garden City, UK) в очищенной воде (исследование h2N1) или в 0,9% NaCl (исследование h4N8) до концентрации 0,4 мг/мл. Осельтамивир (10 мг/кг/сут в исследовании h2N1 или 4 мг/кг/сут в исследовании h4N8) вводили через зонд дважды в сутки с 7-часовым интервалом между дозами либо отдельно (оба исследования), либо в комбинации с hd- анти-IFN-γ (в исследовании h2N1) (т.е., 0,4 мл/мышь/день, начиная с 1 часа до 5 дней после заражения). За пять дней до заражения и с 6 по 21 день (исследование h2N1) или 26 день (исследование h4N8) после заражения мыши из этих групп получали воду в том же объеме, но без осельтамивира. Контрольная группа инфицированных мышей получала носитель (питьевая вода) (0,4 мл/мышь/день) с использованием того же режима дозирования, что и группа hd-анти-IFN-γ. Мыши в контрольной группе (оба исследования), в группах, получавших только осельтамивир и осельтамивир плюс hd-анти-IFN-γ (исследование h2N1), получали обычную питьевую воду (заменявшуюся ежедневно) в соответствующих резервуарах для питья во время экспериментов.
Осельтамивир (10 мг/кг/сут в исследовании h2N1 или 4 мг/кг/сут в исследовании h4N8) вводили через зонд дважды в сутки с 7-часовым интервалом между дозами либо отдельно (оба исследования), либо в комбинации с hd- анти-IFN-γ (в исследовании h2N1) (т.е., 0,4 мл/мышь/день, начиная с 1 часа до 5 дней после заражения). За пять дней до заражения и с 6 по 21 день (исследование h2N1) или 26 день (исследование h4N8) после заражения мыши из этих групп получали воду в том же объеме, но без осельтамивира. Контрольная группа инфицированных мышей получала носитель (питьевая вода) (0,4 мл/мышь/день) с использованием того же режима дозирования, что и группа hd-анти-IFN-γ. Мыши в контрольной группе (оба исследования), в группах, получавших только осельтамивир и осельтамивир плюс hd-анти-IFN-γ (исследование h2N1), получали обычную питьевую воду (заменявшуюся ежедневно) в соответствующих резервуарах для питья во время экспериментов.
Следует отметить, что комбинация осельтамивира и hd-анти-IFN-γ тестировалась только против гриппа A [пандемия A/California/07/2009(h2N1)]. Этот штамм вируса, а не A/Equi2/Miami/1/63(h4N8), был выбран потому, что он был ответственен за пандемию свиного гриппа в 2009–2010 гг.
Этот штамм вируса, а не A/Equi2/Miami/1/63(h4N8), был выбран потому, что он был ответственен за пандемию свиного гриппа в 2009–2010 гг.
Тестирование исходных антител к IFN-γ было сочтено неприемлемым, поскольку перорально принимаемые белки и пептиды (и особенно антитела) обычно и без специфических модификаций имеют чрезвычайно низкую биодоступность в диапазоне концентраций около 0–2% (42, 43) .Однако пероральное введение разбавленных белковых растворов может снизить скорость протеолиза белка и ускорить его диффузию через слизистую оболочку кишечника (44).
Терапевтическая эффективность испытанных препаратов на мышах.
В исследовании выживаемости за мышами наблюдали ежедневно в течение 21 или 26 дней после заражения для регистрации уровня смертности (исследования h2N1 и h4N8 соответственно). В исследовании h2N1 мышей взвешивали один раз до (5 дней до заражения) и пять раз после заражения (точно после заражения, а затем на 5, 7, 12 и 19 дни после заражения), всегда через 5 дней. 00 вечера. В исследовании h4N8 мышей взвешивали не менее двух раз в неделю, начиная с 10 дня до инокуляции и до 26 дня после инокуляции, всегда после 17:00.
00 вечера. В исследовании h4N8 мышей взвешивали не менее двух раз в неделю, начиная с 10 дня до инокуляции и до 26 дня после инокуляции, всегда после 17:00.
Статистические методы
Статистический анализ выполнен с использованием SAS 9.4. Описательная статистика была представлена в виде медианы, нижнего и верхнего квартилей (анализ конкуренции связывания радиоолиганда), медианы и межквартильного диапазона (ELISpot), средних значений для выживания (in vivo) и средних значений и стандартных отклонений для весов (in vivo). Приведенные значения p скорректированы для множественных сравнений.Корректировку множественности проводили при анализе каждого эксперимента в отдельности. Данные ELISpot анализировали с использованием точного теста Уилкоксона. Данные анализа конкуренции связывания радиолиганда анализировали с использованием точного теста Уилкоксона с процедурой множественного сравнения Двасса-Стила-Критчлоу-Флигнера. Коррекция множественности значений p для этих данных была выполнена методом Холма (понижающий Bonferroni, PROC MULTTEST). Данные о выживаемости h4N8 и h2N1 анализировали с использованием логарифмического рангового теста (PROC LIFETEST) с поправкой Бонферрони для множественных сравнений.Данные о массе h4N8 и h2N1 анализировали с использованием модели ANOVA с повторными измерениями (PROC MIXED). Были включены групповые, дневные и групповые факторы взаимодействия. Условия применимости смешанной модели оценивались с использованием графика Q–Q для невязок. Попарные сравнения были выполнены с использованием оценок средних по методу наименьших квадратов с методом корректировки множественности Холма.
Данные о выживаемости h4N8 и h2N1 анализировали с использованием логарифмического рангового теста (PROC LIFETEST) с поправкой Бонферрони для множественных сравнений.Данные о массе h4N8 и h2N1 анализировали с использованием модели ANOVA с повторными измерениями (PROC MIXED). Были включены групповые, дневные и групповые факторы взаимодействия. Условия применимости смешанной модели оценивались с использованием графика Q–Q для невязок. Попарные сравнения были выполнены с использованием оценок средних по методу наименьших квадратов с методом корректировки множественности Холма.
Результаты
HD-анти-IFN-γ вызывают конформационные изменения в IFN-γ:
1 H ЯМР-спектроскопия Экспериментальный метод выбора для изучения влияния hd-анти-IFN-γ на структурные свойства IFN-γ используют ЯМР-спектроскопию растворов высокого разрешения.Преимущество ЯМР-спектроскопии по сравнению с другими методами исследования структуры белков, такими как рентгеновская кристаллография и криогенная электронная микроскопия, заключается в том, что она применяется к образцам в среде их водного раствора и позволяет обнаруживать временные взаимодействия между лигандами и белками (45). ). Успех ЯМР-спектроскопии белков основан на том факте, что химические сдвиги ядер в белке очень чувствительны к изменениям в локальном окружении этих ядер. Таким образом, мы можем использовать химические сдвиги в качестве репортеров для потенциальных структурных эффектов hd-анти-IFN-γ на его мишень, IFN-γ (рис.1). Обычно используемые ЯМР-активные ядра в белках включают протон и азот. Естественное содержание 1 H составляет 100%, поэтому спектры протонного ЯМР можно измерять с белками, не обогащенными изотопами (т. е. немечеными). Одномерный (1D) спектр 1 H для одного немеченого IFN-γ, полученный на спектрометре с частотой 900 МГц, показан на рис. 2. Одномерный спектр дает общее представление о профиле IFN-γ и подтверждает осуществимость дальнейших исследований. ЯМР исследования. Вода впитывается на 4.7 ppm, с протонами OH поблизости, тогда как химические сдвиги влево (более высокие значения частей на миллион) преимущественно возникают из-за NH и ароматических протонов, тогда как сдвиги около 0 ppm возникают из-за алифатических боковых цепей.
). Успех ЯМР-спектроскопии белков основан на том факте, что химические сдвиги ядер в белке очень чувствительны к изменениям в локальном окружении этих ядер. Таким образом, мы можем использовать химические сдвиги в качестве репортеров для потенциальных структурных эффектов hd-анти-IFN-γ на его мишень, IFN-γ (рис.1). Обычно используемые ЯМР-активные ядра в белках включают протон и азот. Естественное содержание 1 H составляет 100%, поэтому спектры протонного ЯМР можно измерять с белками, не обогащенными изотопами (т. е. немечеными). Одномерный (1D) спектр 1 H для одного немеченого IFN-γ, полученный на спектрометре с частотой 900 МГц, показан на рис. 2. Одномерный спектр дает общее представление о профиле IFN-γ и подтверждает осуществимость дальнейших исследований. ЯМР исследования. Вода впитывается на 4.7 ppm, с протонами OH поблизости, тогда как химические сдвиги влево (более высокие значения частей на миллион) преимущественно возникают из-за NH и ароматических протонов, тогда как сдвиги около 0 ppm возникают из-за алифатических боковых цепей. На рис. 2А показан полный диапазон 1 H, тогда как на рис. 2В показано увеличение диапазона, содержащего пептидный остов (NH). Мы можем видеть, что существует большое количество различий, наблюдаемых между одним IFN-γ (нижний спектр) и IFN-γ, к которому был добавлен hd-анти-IFN-γ.Несколько пиков изменили свою интенсивность, появились новые пики, а некоторые пропали. В целом пики в контрольном спектре более широкие и, следовательно, менее интенсивные, о чем свидетельствует более низкое отношение сигнал/шум при том же числе сканирований. Области с меньшим перекрытием сигналов в 1D-спектре позволяют идентифицировать основные группы NH остатков E39, W37 и D42 (см. метки на рис. 2B). Очень хорошо видно, как эти три пика изменяют свою относительную интенсивность (увеличиваются) при добавлении hd-анти-IFN-γ.Таким образом, анализ 1D протонной ЯМР-спектроскопии IFN-γ в присутствии и в отсутствие hd-анти-IFN-γ свидетельствует об изменении локального окружения ряда пиков как в основной, так и в боковых цепях аминокислот молекула.
На рис. 2А показан полный диапазон 1 H, тогда как на рис. 2В показано увеличение диапазона, содержащего пептидный остов (NH). Мы можем видеть, что существует большое количество различий, наблюдаемых между одним IFN-γ (нижний спектр) и IFN-γ, к которому был добавлен hd-анти-IFN-γ.Несколько пиков изменили свою интенсивность, появились новые пики, а некоторые пропали. В целом пики в контрольном спектре более широкие и, следовательно, менее интенсивные, о чем свидетельствует более низкое отношение сигнал/шум при том же числе сканирований. Области с меньшим перекрытием сигналов в 1D-спектре позволяют идентифицировать основные группы NH остатков E39, W37 и D42 (см. метки на рис. 2B). Очень хорошо видно, как эти три пика изменяют свою относительную интенсивность (увеличиваются) при добавлении hd-анти-IFN-γ.Таким образом, анализ 1D протонной ЯМР-спектроскопии IFN-γ в присутствии и в отсутствие hd-анти-IFN-γ свидетельствует об изменении локального окружения ряда пиков как в основной, так и в боковых цепях аминокислот молекула. Эти изменения позволяют предположить наличие конформационных изменений в IFN-γ.
Эти изменения позволяют предположить наличие конформационных изменений в IFN-γ.
Трехмерная структура IFN-γ. Использовали код идентификатора (ID) банка данных белков (PDB) 1FG9. IFN-γ имеет 127 а.о. (0–126 а.о.). Мы использовали нумерацию из файла PDB со смещением на 1 для обозначения остатков по всей рукописи.( A ) Атомное представление димера IFN-γ. Каждый мономер показан зеленым и бирюзовым цветом соответственно. ( B ) Представление вторичной структуры димера IFN-γ. Цветовое кодирование и вид как на (A). ( C ) Представление вторичной структуры бирюзового мономера и атомарное представление зеленого мономера. Вид как на (А). ( D ) Обратная сторона (C), с представлением вторичной структуры зеленого мономера и атомным представлением бирюзового мономера.Вид как на (А).
РИСУНОК 2. 1D ЯМР-спектроскопический анализ взаимодействия между hd-анти-IFN-γ и IFN-γ. Сравнение одного немеченого IFN-γ, отрицательного (-) контроля (нижний спектр, обозначенный как -контроль) с образцом немеченого IFN-γ в присутствии hd-анти-IFN-γ (верхний спектр, обозначенный как положительный [+] для добавления hd-анти-IFN-γ). Эксперимент представляет собой в среднем 10 240 сканирований при 25°C. Подавление воды было достигнуто за счет моделирования возбуждения с помощью градиентов. ( A ) Полнодиапазонный спектр протонов, показывающий все протоны в образце.Помимо протонов IFN-γ, имеется несколько буферных пиков высокой интенсивности (за пределами шкалы). ( B ) Увеличение, показывающее диапазон пептидной основы.
Эксперимент представляет собой в среднем 10 240 сканирований при 25°C. Подавление воды было достигнуто за счет моделирования возбуждения с помощью градиентов. ( A ) Полнодиапазонный спектр протонов, показывающий все протоны в образце.Помимо протонов IFN-γ, имеется несколько буферных пиков высокой интенсивности (за пределами шкалы). ( B ) Увеличение, показывающее диапазон пептидной основы.
HD-анти-IFN-γ вызывает конформационные изменения в IFN-γ:
1 H, 15 N-HSQC ЯМР-спектроскопия Из-за ожидаемого перекрытия в одномерных протонных спектрах только три протона могут этот спектр (E39, W37 и D42). Устранение перекрытия требует увеличения размерности и уменьшения количества пиков в спектре ЯМР.Этого можно достичь, комбинируя 1 H ЯМР с одним или несколькими ядрами, такими как углерод или азот, которые также широко распространены в белках. Однако естественное содержание соответствующих ЯМР-активных изотопов невелико, и поэтому их необходимо обогащать в рекомбинантной системе. Поэтому мы экспрессировали IFN-γ в Escherichia coli и очистили его, чтобы включить ЯМР-активное ядро азота, 15 N. Это позволяет применять последовательность импульсов, HSQC, которая выбирает только те протоны, которые связаны с другим ядра, и мы выбрали 15 N.Меньшее количество сигналов и второе измерение спектра позволят разрешить большинство сигналов основной цепи NH IFN-γ. Это было сделано ранее (32), и поэтому мы можем использовать существующее назначение пиков для обозначения всех перекрестных пиков в спектре. Спектр 2D 1 H– 15 N HSQC, зарегистрированный на ЯМР-спектрометре 900 МГц для одного IFN-γ (синий) и для IFN-γ в присутствии hd-анти-IFN-γ или плацебо (красный ) показан на рис. 3А, 3Б соответственно.Мы смогли отнести почти все основные пики NH только к IFN-γ, используя предыдущее распределение (32). Спектр для IFN-γ с hd-анти-IFN-γ или плацебо, соответственно, регистрировали в тех же условиях, что и для одного IFN-γ, за исключением того, что концентрация только IFN-γ была выше, что позволило нам собрать большее количество данных.
Поэтому мы экспрессировали IFN-γ в Escherichia coli и очистили его, чтобы включить ЯМР-активное ядро азота, 15 N. Это позволяет применять последовательность импульсов, HSQC, которая выбирает только те протоны, которые связаны с другим ядра, и мы выбрали 15 N.Меньшее количество сигналов и второе измерение спектра позволят разрешить большинство сигналов основной цепи NH IFN-γ. Это было сделано ранее (32), и поэтому мы можем использовать существующее назначение пиков для обозначения всех перекрестных пиков в спектре. Спектр 2D 1 H– 15 N HSQC, зарегистрированный на ЯМР-спектрометре 900 МГц для одного IFN-γ (синий) и для IFN-γ в присутствии hd-анти-IFN-γ или плацебо (красный ) показан на рис. 3А, 3Б соответственно.Мы смогли отнести почти все основные пики NH только к IFN-γ, используя предыдущее распределение (32). Спектр для IFN-γ с hd-анти-IFN-γ или плацебо, соответственно, регистрировали в тех же условиях, что и для одного IFN-γ, за исключением того, что концентрация только IFN-γ была выше, что позволило нам собрать большее количество данных. количество приращений в измерении азота (см. Материалы и методы ). Это было необходимо для определения всех пиков при сохранении требований к образцу на низком уровне, чтобы обеспечить максимально возможный объем добавления hd-анти-IFN-γ или контроля соответственно.Мы использовали плацебо в качестве контроля, тогда как вода без антител против IFN-γ подвергалась той же обработке, что и образцы, содержащие антитела. Таким образом, этот контроль является более строгим, чем просто буфер, используемый в экспериментах 1D ЯМР, показанных на рис. 2. Сравнение спектров плацебо (записанных в тех же условиях, что и для hd-анти-ИФН-γ; показано на рис. 3А) и только IFN-γ показан на фиг. 3B.
количество приращений в измерении азота (см. Материалы и методы ). Это было необходимо для определения всех пиков при сохранении требований к образцу на низком уровне, чтобы обеспечить максимально возможный объем добавления hd-анти-IFN-γ или контроля соответственно.Мы использовали плацебо в качестве контроля, тогда как вода без антител против IFN-γ подвергалась той же обработке, что и образцы, содержащие антитела. Таким образом, этот контроль является более строгим, чем просто буфер, используемый в экспериментах 1D ЯМР, показанных на рис. 2. Сравнение спектров плацебо (записанных в тех же условиях, что и для hd-анти-ИФН-γ; показано на рис. 3А) и только IFN-γ показан на фиг. 3B.
2D-ЯМР-спектроскопический анализ взаимодействия между hd-анти-IFN-γ и IFN-γ.( A ) Наложение спектров 15 N– 1 H-HSQC IFN-γ в отсутствие (синий) или в присутствии (красный) hd-анти-IFN-γ. Двумерные спектры 1 H– 15 N для одного IFN-γ (синие) были получены с помощью 128 сканирований в протонном измерении и 128 сканирований в азотном измерении при 25°C. Для образцов ЯМР, содержащих IFN-γ с добавленными сильно разбавленными антителами, было получено 2048*34 сканирований (красный). (A I ) Обзор всего спектра; (A II и A III ) расширение локальных областей спектра показано на AI.( B ) Наложение спектров 15 N– 1 H–HSQC IFN-γ в отсутствие (синий) или в присутствии (красный) плацебо. Сбор данных, как в (А). ( C ) Структурное картирование 13 изменений химического сдвига, наблюдаемых в IFN-γ при его взаимодействии с hd-анти-IFN-γ, наряду с их расширенными областями для каждого отдельного остатка (обратите внимание, что каждый остаток появляется на изображении дважды из-за образование димера). Активный димер IFN-γ с заменой домена представлен в виде ленточной диаграммы розового цвета (цепь A) и голубого цвета (цепь B) для выделения отдельных цепей.Сигналы, демонстрирующие изменения химического сдвига в диапазоне 0,01–0,02 и 0,02–0,04 м.
Для образцов ЯМР, содержащих IFN-γ с добавленными сильно разбавленными антителами, было получено 2048*34 сканирований (красный). (A I ) Обзор всего спектра; (A II и A III ) расширение локальных областей спектра показано на AI.( B ) Наложение спектров 15 N– 1 H–HSQC IFN-γ в отсутствие (синий) или в присутствии (красный) плацебо. Сбор данных, как в (А). ( C ) Структурное картирование 13 изменений химического сдвига, наблюдаемых в IFN-γ при его взаимодействии с hd-анти-IFN-γ, наряду с их расширенными областями для каждого отдельного остатка (обратите внимание, что каждый остаток появляется на изображении дважды из-за образование димера). Активный димер IFN-γ с заменой домена представлен в виде ленточной диаграммы розового цвета (цепь A) и голубого цвета (цепь B) для выделения отдельных цепей.Сигналы, демонстрирующие изменения химического сдвига в диапазоне 0,01–0,02 и 0,02–0,04 м. д., представлены синими и красными палочками соответственно (см. Таблицу I). Более слабые изменения наблюдались для V117 и I45 (желтые палочки, черные метки). Соответствующие спектры показаны слева для остатков на границе раздела димеров и справа для остатков вне границы раздела. Горячие точки взаимодействия выделены сеткой (т. Е. Интерфейс димера в зеркальной плоскости двух мономеров и интерфейсы C-концевой цепи).(B I ) Обзор всего спектра; (B II и B III ) расширение локальных участков спектра показано в BI. На вставке показано то же изображение, что и на рис. 1В, чтобы помочь зрителю идентифицировать два мономера в димере. Представление и идентификатор (ID) банка данных белков (PDB), как на рис. 1.
д., представлены синими и красными палочками соответственно (см. Таблицу I). Более слабые изменения наблюдались для V117 и I45 (желтые палочки, черные метки). Соответствующие спектры показаны слева для остатков на границе раздела димеров и справа для остатков вне границы раздела. Горячие точки взаимодействия выделены сеткой (т. Е. Интерфейс димера в зеркальной плоскости двух мономеров и интерфейсы C-концевой цепи).(B I ) Обзор всего спектра; (B II и B III ) расширение локальных участков спектра показано в BI. На вставке показано то же изображение, что и на рис. 1В, чтобы помочь зрителю идентифицировать два мономера в димере. Представление и идентификатор (ID) банка данных белков (PDB), как на рис. 1.
Сначала мы исследуем спектральные изменения, наблюдаемые при добавлении hd-анти-IFN-γ, показанные на рис. 3A. Есть много красных пиков, которые не наблюдаются только у IFN-γ (синие пики), но они лежат за пределами назначенных пиков и могут соответствовать агрегированной конформации, которая сильно отличается от конформации, для которой были назначены пики и структура. Если мы увеличим спектр в области заданных пиков, то увидим, что центры красных сигналов смещены. Например, изменение положения пика аспарагиновой кислоты в положении 42 соответствует изменению локального окружения этой аминокислоты, что подтверждает наши выводы с немеченым IFN-γ в 1D-спектрах протонного ЯМР, показанных на рис. 2. Разрешение и отнесение еще многих пиков позволило выявить ряд дополнительных изменений. В общей сложности 13 пиков сместились после добавления hd-анти-IFN-γ.Явно смещенные пики в спектре IFN-γ плюс hd-анти-IFN-γ были идентифицированы как A9, E39, E40, D42, I45, Q47, I50, F82, F83 и S85, а также V117, A119 и E120 на С-конце (таблица I). Соответствующие изменения не наблюдались при добавлении плацебо-контроля (рис. 3В).
Если мы увеличим спектр в области заданных пиков, то увидим, что центры красных сигналов смещены. Например, изменение положения пика аспарагиновой кислоты в положении 42 соответствует изменению локального окружения этой аминокислоты, что подтверждает наши выводы с немеченым IFN-γ в 1D-спектрах протонного ЯМР, показанных на рис. 2. Разрешение и отнесение еще многих пиков позволило выявить ряд дополнительных изменений. В общей сложности 13 пиков сместились после добавления hd-анти-IFN-γ.Явно смещенные пики в спектре IFN-γ плюс hd-анти-IFN-γ были идентифицированы как A9, E39, E40, D42, I45, Q47, I50, F82, F83 и S85, а также V117, A119 и E120 на С-конце (таблица I). Соответствующие изменения не наблюдались при добавлении плацебо-контроля (рис. 3В).
Наложение всех изменений параметров химического сдвига, которые мы наблюдали при добавлении hd-анти-IFN-γ, но не плацебо, на трехмерную структуру IFN-γ показана на рис. 3C, наряду с увеличенными областями спектров ЯМР. Различные цвета указывают на величину наблюдаемого нами химического сдвига. Наибольшие изменения показаны красным и синим цветом, умеренные изменения — желтым. Розовые и зеленоватые цвета указывают на остатки, расположенные на границе раздела димеров. Для сравнения мы показываем в качестве вставки изображение структуры с рис. 1, чтобы выделить положения двух мономеров в димере. Это сравнение показывает, что многие изменения наблюдаются в этой области интерфейса.Из 13 остатков со смещенными пиками семь расположены на поверхности димера IFN-γ: E39, E40, D42, Q47, F82, V117 и A119 (рис. 3C). Некоторые из пиков со значительным увеличением интенсивности были теми, которые мы уже идентифицировали в спектре 1D 1 H немеченого IFN-γ: E39, W37 и D42 (рис. 2B). Все три идентифицированных пика с повышенной интенсивностью после обработки hd-анти-IFN-γ расположены близко к изгибу между спиралями B и C в центре димерной поверхности раздела IFN-γ.
3C, наряду с увеличенными областями спектров ЯМР. Различные цвета указывают на величину наблюдаемого нами химического сдвига. Наибольшие изменения показаны красным и синим цветом, умеренные изменения — желтым. Розовые и зеленоватые цвета указывают на остатки, расположенные на границе раздела димеров. Для сравнения мы показываем в качестве вставки изображение структуры с рис. 1, чтобы выделить положения двух мономеров в димере. Это сравнение показывает, что многие изменения наблюдаются в этой области интерфейса.Из 13 остатков со смещенными пиками семь расположены на поверхности димера IFN-γ: E39, E40, D42, Q47, F82, V117 и A119 (рис. 3C). Некоторые из пиков со значительным увеличением интенсивности были теми, которые мы уже идентифицировали в спектре 1D 1 H немеченого IFN-γ: E39, W37 и D42 (рис. 2B). Все три идентифицированных пика с повышенной интенсивностью после обработки hd-анти-IFN-γ расположены близко к изгибу между спиралями B и C в центре димерной поверхности раздела IFN-γ. Данные убедительно свидетельствуют о том, что изменение структуры IFN-γ сосредоточено на границе раздела двух мономеров и, таким образом, вероятно, повлияет на равновесие мономер-димер IFN-γ.
Данные убедительно свидетельствуют о том, что изменение структуры IFN-γ сосредоточено на границе раздела двух мономеров и, таким образом, вероятно, повлияет на равновесие мономер-димер IFN-γ.
HD-анти-IFN-γ улучшает связывание IFN-γ с рецептором IFN-γ
Человеческая моноцитоподобная клеточная линия U-937 обильно экспрессирует высокоаффинный рецептор к IFN-γ (46). Чтобы проверить и количественно оценить высокоспецифичное связывание IFN-γ с его рецептором на клетках U-937, мы провели анализ конкурентного связывания.Данные показывают, что существует единственный класс высокоаффинных сайтов связывания с константой ингибирования связывания ( Ки ), равной 1,1 × 10 -9 (0,1–1 × 10 -9 , о которой сообщают van Loon et al. (47) [1991]). Обработка клеток U-937 hd-анти-IFN-γ приводила к значительному увеличению специфического связывания [ 125 I]IFN-γ с рецептором IFN-γ (процент специфического связывания в буферном контроле) по сравнению с как носитель, так и hd-анти-TNF-α ( p < 0. 05): 148,92 (148,20; 155,44) против 119,50 (99,20; 129,64) процента (носитель) и 109,11 (73,22; 143,82) процента (hd-анти-TNF-α).
05): 148,92 (148,20; 155,44) против 119,50 (99,20; 129,64) процента (носитель) и 109,11 (73,22; 143,82) процента (hd-анти-TNF-α).
hd-анти-IFN-γ стимулируют продукцию IFN-γ in vitro МКПК
Ранее мы показали, что продукция IFN-γ значительно увеличивалась в результате лечения животных hd-анти-IFN-γ ( 48). Мы использовали анализ ELISpot для обнаружения и количественной оценки эффектов hd-анти-IFN-γ на клетки, продуцирующие IFN-γ, in vitro. PBMC ресуспендировали в культуральной среде, содержащей hd-анти-IFN-γ или носитель, и стимулировали пулом пептидов ICE.Количество клеток, продуцирующих IFN-γ, в среде, содержащей hd-анти-IFN-γ, было значительно выше (40 пятен [межквартильный размах = 13]) по сравнению с 26 пятнами [межквартильный размах = 4] в носителе [ p < 0,05]) (рис. 4). Нестимулированные клетки в фоновых лунках не проявляли активности (дополнительная рис. 2).
РИСУНОК 4. Обработка hd-анти-IFN-γ усиливает продукцию IFN-γ PBMC, стимулированными пулом пептидов. ELISpot-анализ клеток, продуцирующих IFN-γ, проводили на культуре РВМС человека, стимулированной пулом пептидов ICE в присутствии hd-анти-IFN-γ или носителя.* p <0,05 по сравнению с носителем.
ELISpot-анализ клеток, продуцирующих IFN-γ, проводили на культуре РВМС человека, стимулированной пулом пептидов ICE в присутствии hd-анти-IFN-γ или носителя.* p <0,05 по сравнению с носителем.
Это открытие указывает на то, что hd-анти-IFN-γ участвуют в регуляции уровней IFN-γ, усиливая секрецию IFN-γ и/или индуцируя пролиферацию клеток, продуцирующих IFN-γ. Изображения отдельных чашек можно найти на дополнительном рис. 2. A/h4N8 и лечили перорально hd-анти-IFN-γ (начиная за 5 дней до и до 21 дня или 26 дней после заражения соответственно), носителем (питьевая вода), классическим противовирусным препаратом осельтамивиром (тамифлю), или комбинация hd-анти-IFN-γ и осельтамивира (для h2N1).Смертность и масса тела использовались в качестве конечных точек исследования. Животные, получавшие hd-анти-IFN-γ, демонстрировали повышенную выживаемость (рис. 5). HD-анти-ИФН-γ были по меньшей мере столь же эффективны в снижении смертности, как и осельтамивир, с показателями выживаемости 95 против 75% для h4N8 ( p > 0,05) и 80 против 70% для h2N1 ( p > 0,05). ), статистически значимое различие по сравнению с носителем (20% для h4N8 и 30% для h2N1) было обнаружено для каждой группы лечения ( p < 0.05). Выживаемость при комбинированном лечении анти-ИФН-γ и осельтамивиром составила 75 по сравнению с 70% при лечении одним осельтамивиром для h2N1 ( p > 0,05). В конце исследования потеря массы тела была значительно ниже во всех группах лечения по сравнению с группой, получавшей носитель ( p <0,05) для инфекции h4N8; достоверных различий в потере массы тела в группах животных с инфекцией h2N1 не обнаружено (рис. 6).
), статистически значимое различие по сравнению с носителем (20% для h4N8 и 30% для h2N1) было обнаружено для каждой группы лечения ( p < 0.05). Выживаемость при комбинированном лечении анти-ИФН-γ и осельтамивиром составила 75 по сравнению с 70% при лечении одним осельтамивиром для h2N1 ( p > 0,05). В конце исследования потеря массы тела была значительно ниже во всех группах лечения по сравнению с группой, получавшей носитель ( p <0,05) для инфекции h4N8; достоверных различий в потере массы тела в группах животных с инфекцией h2N1 не обнаружено (рис. 6).
HD-анти-IFN-γ защищает самок мышей BALB/c от заражения гриппом A ( A ) HD-анти-IFN-γ проявляет противовирусную активность против гриппа A [A/California/07/2009 (h2N1) пандемия] с эффективностью, сравнимой с осельтамивиром ( p > 0.05), о чем свидетельствуют повышенные показатели выживаемости по сравнению с таковыми в группе с зараженным носителем ( p <0,05). Кроме того, hd-анти-ИФН-γ в сочетании с осельтамивиром улучшала противовирусную активность препарата сравнения ( p > 0,05). * p < 0,05 по сравнению с носителем, ** p < 0,01 по сравнению с носителем. ( B ) HD-анти-IFN-γ проявлял противовирусную активность против гриппа A [A/Equi2/Miami/1/63(h4N8)] с эффективностью, сравнимой с осельтамивиром ( p > 0.05), о чем свидетельствуют повышенные показатели выживаемости по сравнению с таковыми в группе с зараженным носителем ( p <0,01). ** p <0,01 по сравнению с носителем.
Кроме того, hd-анти-ИФН-γ в сочетании с осельтамивиром улучшала противовирусную активность препарата сравнения ( p > 0,05). * p < 0,05 по сравнению с носителем, ** p < 0,01 по сравнению с носителем. ( B ) HD-анти-IFN-γ проявлял противовирусную активность против гриппа A [A/Equi2/Miami/1/63(h4N8)] с эффективностью, сравнимой с осельтамивиром ( p > 0.05), о чем свидетельствуют повышенные показатели выживаемости по сравнению с таковыми в группе с зараженным носителем ( p <0,01). ** p <0,01 по сравнению с носителем.
HD-анти-IFN-γ улучшает вес самок мышей BALB/c с инфекцией гриппа А. ( A ) HD-анти-IFN-γ проявлял противовирусную активность против гриппа A [пандемия A/California/07/2009(h2N1)] с эффективностью, сравнимой с осельтамивиром ( p > 0,05), о чем свидетельствует увеличение общего живая масса в группе лечения по сравнению с живой массой в группе, получавшей контрольный носитель. Не было обнаружено существенных различий в общей живой массе в группе, получавшей лечение, по сравнению с таковой в группе, получавшей контрольный носитель ( p <0,05). ( B ) HD-анти-IFN-γ проявлял противовирусную активность против гриппа A [A/Equi2/Miami/1/63(h4N8)] с эффективностью, сравнимой с осельтамивиром ( p > 0,05), о чем свидетельствует увеличение общая живая масса в группе лечения по сравнению с таковой в группе, получавшей контрольный носитель ( p <0,05). ** р < 0.01 против автомобиля.
Не было обнаружено существенных различий в общей живой массе в группе, получавшей лечение, по сравнению с таковой в группе, получавшей контрольный носитель ( p <0,05). ( B ) HD-анти-IFN-γ проявлял противовирусную активность против гриппа A [A/Equi2/Miami/1/63(h4N8)] с эффективностью, сравнимой с осельтамивиром ( p > 0,05), о чем свидетельствует увеличение общая живая масса в группе лечения по сравнению с таковой в группе, получавшей контрольный носитель ( p <0,05). ** р < 0.01 против автомобиля.
Обсуждение
В наших предыдущих исследованиях мы показали, что биологические эффекты высоких разведений антител очень специфичны. Например, когда мы оценивали влияние введения сильно разбавленных биопрепаратов in vivo на секрецию цитокинов, мы заметили, что только обработка hd-анти-IFN-γ приводила к увеличению продукции IFN-γ мышиными лимфоцитами, тогда как сильно разведенные антитела к эритропоэтину, hd-анти-TNF-α или плацебо не оказывали значительного эффекта (48). Мы также показали, что аффинность взаимодействия Ag-Ab (IFN-γ и Abs к IFN-γ соответственно) изменялась в присутствии hd-анти-IFN-γ (27).
Мы также показали, что аффинность взаимодействия Ag-Ab (IFN-γ и Abs к IFN-γ соответственно) изменялась в присутствии hd-анти-IFN-γ (27).
Таким образом, специфичность этих эффектов привела нас к гипотезе о том, что сильно разбавленные АТ могут действовать аллостерически непосредственно на антиген-мишень, вызывая конформационные изменения, подобные тем, которые иногда наблюдаются при связывании АТ с АГ. Например, связывание Ab с Ag может вызывать аллостерические эффекты, приводящие к конформационным изменениям Ag (28).Было показано, что mAb, распознающие гормон роста человека, вызывают аллостерические изменения в гормоне, которые влияют на связывание с его рецептором и модифицируют биологическую активность гормона (49).
В текущем исследовании мы оценили влияние hd-анти-IFN-γ на молекулярную структуру и биологические функции IFN-γ. Во-первых, мы использовали ЯМР-спектроскопию высокого разрешения для обнаружения любых конформационных изменений в молекуле IFN-γ, происходящих в присутствии hd-анти-IFN-γ. Зрелый человеческий IFN-γ представляет собой гомодимер из двух субъединиц, каждая из которых состоит из 143 аминокислотных остатков с общей молекулярной массой 45 кДа (50).Мономер IFN-γ состоит из ядра из шести α-спиралей и удлиненной развернутой последовательности в С-концевой области (12, 51). Биологически активный димер образуется путем антипараллельного сшивания двух мономеров. Добавление hd-анти-IFN-γ к образцу IFN-γ вызывало как глобальные, так и специфические изменения в спектре ЯМР. В целом, интенсивность и разрешение спектра улучшились. Мы обнаружили в общей сложности 13 а.о., которые демонстрируют изменение положения или интенсивности при добавлении hd-анти-IFN-γ, но не плацебо.
Зрелый человеческий IFN-γ представляет собой гомодимер из двух субъединиц, каждая из которых состоит из 143 аминокислотных остатков с общей молекулярной массой 45 кДа (50).Мономер IFN-γ состоит из ядра из шести α-спиралей и удлиненной развернутой последовательности в С-концевой области (12, 51). Биологически активный димер образуется путем антипараллельного сшивания двух мономеров. Добавление hd-анти-IFN-γ к образцу IFN-γ вызывало как глобальные, так и специфические изменения в спектре ЯМР. В целом, интенсивность и разрешение спектра улучшились. Мы обнаружили в общей сложности 13 а.о., которые демонстрируют изменение положения или интенсивности при добавлении hd-анти-IFN-γ, но не плацебо.
Семь остатков с изменениями химического сдвига в наших спектрах были отнесены к остаткам, расположенным на границе димера и включающим С-конец IFN-γ. На рис. 2Б отчетливо видно усиление резонансов 1 H в IFN-γ при добавлении hd-анти-IFN-γ. На основании этого результата и высокого разведения анти-ИФН-γ и, следовательно, низких концентраций hd-анти-ИФН-γ мы можем исключить образование комплекса hd-анти-ИФН-γ/ИФН-γ. Такой большой комплекс привел бы к очень широким пикам из-за высокой молекулярной массы комплекса, и было бы невозможно разрешить резонансы с помощью ЯМР.Таким образом, наблюдаемые химические сдвиги обусловлены временным взаимодействием IFN-γ с hd-анти–IFN-γ. Наблюдаемое увеличение интенсивности и резкости резонансов, появление новых пиков свидетельствует об изменении равновесия мономер-димер. Поскольку димер IFN-γ образуется путем замены доменов (см. рис. 1), при котором отдельные элементы вторичной структуры, такие как спирали, занимают соответствующие места в другой структуре, интерфейс распространяется на широкий диапазон структуры, и изменение состояния олигомеризации фактически требует хотя бы частичного развертывания структуры.Таким образом, наиболее общий вывод, который мы можем сделать из изменений химических сдвигов, наблюдаемых с помощью ЯМР-спектроскопии, состоит в том, что существует изменение структуры IFN-γ, вызванное добавлением hd-анти-IFN-γ, с особым акцентом на димер интерфейс.
Такой большой комплекс привел бы к очень широким пикам из-за высокой молекулярной массы комплекса, и было бы невозможно разрешить резонансы с помощью ЯМР.Таким образом, наблюдаемые химические сдвиги обусловлены временным взаимодействием IFN-γ с hd-анти–IFN-γ. Наблюдаемое увеличение интенсивности и резкости резонансов, появление новых пиков свидетельствует об изменении равновесия мономер-димер. Поскольку димер IFN-γ образуется путем замены доменов (см. рис. 1), при котором отдельные элементы вторичной структуры, такие как спирали, занимают соответствующие места в другой структуре, интерфейс распространяется на широкий диапазон структуры, и изменение состояния олигомеризации фактически требует хотя бы частичного развертывания структуры.Таким образом, наиболее общий вывод, который мы можем сделать из изменений химических сдвигов, наблюдаемых с помощью ЯМР-спектроскопии, состоит в том, что существует изменение структуры IFN-γ, вызванное добавлением hd-анти-IFN-γ, с особым акцентом на димер интерфейс. Вероятно, такие стерические изменения в структуре димера потенциально могут влиять на стабильность димера, изменять кинетику олигомеризации IFN-γ и влиять на стехиометрию рецепторного комплекса IFN-γ/IFN-γ. Все эти гипотезы могут быть проверены в будущих углубленных исследованиях состояний и кинетики олигомеризации, как это было сделано ранее для изучения равновесия между мономерными, димерными и олигомерными состояниями в отсутствие hd-анти-IFN-γ. (52).
Вероятно, такие стерические изменения в структуре димера потенциально могут влиять на стабильность димера, изменять кинетику олигомеризации IFN-γ и влиять на стехиометрию рецепторного комплекса IFN-γ/IFN-γ. Все эти гипотезы могут быть проверены в будущих углубленных исследованиях состояний и кинетики олигомеризации, как это было сделано ранее для изучения равновесия между мономерными, димерными и олигомерными состояниями в отсутствие hd-анти-IFN-γ. (52).
Ответы на IFN-γ активируются за счет его взаимодействия с высокоаффинным гетеродимерным рецептором, состоящим из рецептора IFN-γ 1 (IFNGR1) и IFNGR2. Связывание IFN-γ с рецептором активирует путь JAK-STAT. Через свою С-концевую область IFN-γ также связывается (но с меньшей аффинностью) с гликозаминогликановым гепарансульфатом на поверхности клетки. Это взаимодействие ингибирует биологическую активность IFN-γ, а также, возможно, защищает его от протеолитического расщепления и регулирует нацеливание на ткани и локальное накопление (53). Интересно, что внутриклеточный IFN-γ обладает биологической активностью без распознавания внеклеточного домена его высокоаффинного рецептора. Было высказано предположение, что комплекс, состоящий из активированного Stat1a в ассоциации с IFNGR1, подвергается ядерной транслокации в присутствии человеческого IFN-γ, поскольку С-концевой пептид IFN-γ содержит сигнал ядерной локализации (54).
Интересно, что внутриклеточный IFN-γ обладает биологической активностью без распознавания внеклеточного домена его высокоаффинного рецептора. Было высказано предположение, что комплекс, состоящий из активированного Stat1a в ассоциации с IFNGR1, подвергается ядерной транслокации в присутствии человеческого IFN-γ, поскольку С-концевой пептид IFN-γ содержит сигнал ядерной локализации (54).
Таким образом, далее мы исследовали, может ли hd-анти-IFN-γ изменить взаимодействие лиганд-рецептор, принимая во внимание, что биологически активная форма IFN-γ представляет собой димер (50) и IFN-γ связывается с его рецептором как димер (55).Кроме того, С-концевая область молекулы IFN-γ, которая вызывала пространственные изменения, наблюдаемые с помощью ЯМР, играет критическую роль в ее связывании с рецептором IFN-γ и передаче сигналов IFN-γ (54, 56). Результаты анализа конкуренции связывания радиолиганда показали, что hd-анти-IFN-γ усиливает специфическое связывание IFN-γ с его рецептором.
IFN-γ является провоспалительным цитокином и в основном продуцируется NK, NKT, врожденными лимфоидными клетками, CD4 + Th2 и CD8 + CTL, а также профессиональными АПК, такими как макрофаги, дендритные клетки и В-клетки. IFN-γ оказывает защитное действие посредством усиления клеточного иммунитета, активации макрофагов и индукции дифференцировки Th2. Клетки Th2, которые секретируют IFN-γ, стимулируются IFN-γ, IL-12, IL-23 и IL-27 посредством активации STAT1, STAT4 и T-bet. IFN-γ, IL-12 и IL-27 являются частью петли положительной регуляторной обратной связи, которая усиливает продукцию этих цитокинов в клетках того же или разных типов, действуя через цитокин-специфические рецепторы (57). Было обнаружено, что IFN-γ является мощным повышающим регуляторным стимулом для экспрессии собственного гена в PBMC человека (58).Также было показано, что обработка РВМС IFN-γ приводила к секреции IFN-γ через 24–48 часов (59).
IFN-γ оказывает защитное действие посредством усиления клеточного иммунитета, активации макрофагов и индукции дифференцировки Th2. Клетки Th2, которые секретируют IFN-γ, стимулируются IFN-γ, IL-12, IL-23 и IL-27 посредством активации STAT1, STAT4 и T-bet. IFN-γ, IL-12 и IL-27 являются частью петли положительной регуляторной обратной связи, которая усиливает продукцию этих цитокинов в клетках того же или разных типов, действуя через цитокин-специфические рецепторы (57). Было обнаружено, что IFN-γ является мощным повышающим регуляторным стимулом для экспрессии собственного гена в PBMC человека (58).Также было показано, что обработка РВМС IFN-γ приводила к секреции IFN-γ через 24–48 часов (59).
Чтобы изучить влияние hd-анти-IFN-γ на продукцию IFN-γ, мы обработали РВМС человека и измерили количество клеток, секретирующих IFN-γ, с помощью анализа ELISpot. Мы показываем, что hd-анти-IFN-γ положительно регулируют секрецию IFN-γ, индуцированную пулом вирусных пептидов. Возможные механизмы могут включать повышение эффективности презентации АГ или функциональную активацию цитотоксических Т-клеток CD8 + . Кроме того, наши результаты можно рассматривать как косвенное свидетельство того, что hd-анти-IFN-γ регулирует петлю положительной обратной связи посредством активации сигнального пути IFN-γ.
Кроме того, наши результаты можно рассматривать как косвенное свидетельство того, что hd-анти-IFN-γ регулирует петлю положительной обратной связи посредством активации сигнального пути IFN-γ.
IFN-γ играет важную роль во врожденном и адаптивном иммунитете против вирусных и бактериальных инфекций (57). IFN-γ способен напрямую ингибировать репликацию вируса, но, что наиболее важно, цитокин обладает иммуностимулирующим и иммуномодулирующим действием (57). IFN-γ вырабатывается во время острых стадий вирусной инфекции гриппа А и может быть обнаружен в секрете верхних дыхательных путей и в сыворотке крови.Однако, основываясь на данных, полученных на животных моделях [с использованием инъекций нейтрализующих антител против IFN-γ (60) или IFN-γ -/- (61) и IFN-γR -/- (62) мышей], был сделан вывод, что контроль инфекции гриппа А обычно не зависит от IFN-γ. Механизмы уклонения, используемые вирусом гриппа А, играют важную роль в этой неэффективности (63). Интересно, что все же можно было достичь IFN-γ-специфического контроля над вирусом гриппа А на мышиных моделях. В этих случаях животных либо предварительно лечили индуктором IFN полирибоинозиновой-полирибоцитидиловой кислотой (64), либо лечили высокими дозами IFN-γ на ранней стадии инфекции (65).Таким образом, предварительная обработка животных hd-анти-IFN-γ может преодолеть резистентность вируса гриппа А к IFN-γ. В исследовании in vivo мы изучили противовирусную активность hd-анти-IFN-γ против вируса гриппа A на мышиной модели с использованием 5-дневного протокола предварительной обработки. Мы показали, что hd-анти-IFN-γ эффективен против гриппа in vivo. Эти данные согласуются с нашими предыдущими сообщениями (19, 22, 23).
В этих случаях животных либо предварительно лечили индуктором IFN полирибоинозиновой-полирибоцитидиловой кислотой (64), либо лечили высокими дозами IFN-γ на ранней стадии инфекции (65).Таким образом, предварительная обработка животных hd-анти-IFN-γ может преодолеть резистентность вируса гриппа А к IFN-γ. В исследовании in vivo мы изучили противовирусную активность hd-анти-IFN-γ против вируса гриппа A на мышиной модели с использованием 5-дневного протокола предварительной обработки. Мы показали, что hd-анти-IFN-γ эффективен против гриппа in vivo. Эти данные согласуются с нашими предыдущими сообщениями (19, 22, 23).
Ранее был изучен механизм действия лечебного препарата, содержащего в качестве основного компонента высокоразведенные АТ, на β-субъединицу рецептора инсулина.Мы выявили действие препарата на молекулу-мишень (β-субъединицу рецептора инсулина) (66) и расширили исследование для изучения эффектов на уровне организма (67, 68). Кроме того, недавно были опубликованы результаты рандомизированного плацебо-контролируемого двойного слепого клинического исследования эффективности и безопасности этого препарата при сахарном диабете 1 типа (8).
Результаты настоящего исследования позволяют сделать вывод о том, что в отличие от традиционных препаратов на основе антител сильно разведенные антитела действуют, индуцируя конформационные модификации своих мишеней, которые затем влияют на взаимодействие модифицированных мишеней с соответствующими рецепторами и, таким образом, в конечном итоге организуют мишень-зависимый биологический путь.Высокоразведенные биопрепараты предлагают революционный подход к разработке и клиническому применению препаратов на основе антител.
Раскрытие информации
Мы благодарим Николь Мюллер и Джоан Планас-Иглесиас за техническую помощь в подготовке IFN-γ и изображения структуры на рис. 3C соответственно. Авторы заявляют о следующих конкурирующих финансовых интересах: ООО «НПФ «Материа Медика Холдинг» выступило спонсором исследования, провело статистический анализ, приняло решение о публикации работы и покрыло текущие расходы по обработке статьи, а также приняло участие в разработке экспериментов и написание рукописи. МЭБ является учредителем, президентом и мажоритарным акционером ООО «НПФ «Материа Медика Холдинг». S.A.T., E.A.G., E.S.D., A.G.E. и A.L.K. являются научными руководителями ООО «НПФ «Материа Медика Холдинг». Различные технологические варианты hd-анти–ИФН-γ являются субстанциями (отдельно или одним из компонентов) для коммерческих препаратов Анаферон детский, Анаферон, Эргоферон и Полиферон производства или производства и реализации ООО «НПФ «Материа Медика Холдинг». ». Патенты на это вещество и лекарства принадлежат О.т.е. Другие авторы не имеют финансовых конфликтов интересов.
МЭБ является учредителем, президентом и мажоритарным акционером ООО «НПФ «Материа Медика Холдинг». S.A.T., E.A.G., E.S.D., A.G.E. и A.L.K. являются научными руководителями ООО «НПФ «Материа Медика Холдинг». Различные технологические варианты hd-анти–ИФН-γ являются субстанциями (отдельно или одним из компонентов) для коммерческих препаратов Анаферон детский, Анаферон, Эргоферон и Полиферон производства или производства и реализации ООО «НПФ «Материа Медика Холдинг». ». Патенты на это вещество и лекарства принадлежат О.т.е. Другие авторы не имеют финансовых конфликтов интересов.
Благодарности
Мы благодарим Christophe Chaumeil и Maria Myslivetc за техническую помощь, Национальную ветеринарную школу Alfort за руководство мышиными моделями, включая указания по минимизации страданий животных, и членов Euroscreen, SA, Gosselies, Бельгия, за проведение экспериментов с IFN- γ-рецептор.
Сноски
Работа выполнена при поддержке ООО «НПФ «Материа Медика Холдинг», Москва, Российская Федерация.

Сотрудники ООО «НПФ «Материа Медика Холдинг» принимали участие в планировании экспериментов и написании рукописи, проводили статистический анализ и принимали решение о публикации работы.
Электронная версия этой статьи содержит дополнительные материалы.
Сокращения, использованные в этой статье:
- 1D
- одномерный
- 2D
- 2D
- двумерный
- 2D
- HD-IFN-γ
- Высоко разбавленный AB для IFN-γ
- HD-анти –TNF-α
- сильно разбавленные антитела к TNF-α
- HSQC
- гетероядерная одиночная квантовая когерентность
- IFNGR1
- IFN-γ рецептор 1
- ЯМР
- ядерный
- Получено 29 января 2020 г.
- Принято 4 июля 2020 г.
- Качественное исследование FRESH AIR
%PDF-1.
 4
%
1 0 объект
>
эндообъект
11 0 объект /Создатель (Спрингер)
/Заголовок (Рецидивирующие заболевания нижних дыхательных путей у детей раннего возраста в сельской местности Кыргызстана: чрезмерное использование антибиотиков и возможная неправильная диагностика астмы.Качественное исследование FRESH AIR)
/CrossMarkDomains#5B2#5D (springerlink.com)
/Ключевые слова ()
/CrossMarkDomains#5B1#5D (springer.com)
/ModDate (D:20180628102015+02’00’)
/Тема (npj Primary Care Respiratory Medicine, doi:10.1038/s41533-018-0081-y)
/ doi (10.1038/s41533-018-0081-y)
/Автор
/CreationDate (D:20180626170531+05’30’)
>>
эндообъект
2 0 объект
>
эндообъект
3 0 объект
>
эндообъект
4 0 объект
>
эндообъект
5 0 объект
>
эндообъект
6 0 объект
>
/Шрифт >
>>
/DA (/Helv 0 Tf 0 г )
>>
эндообъект
7 0 объект
>
>>
эндообъект
8 0 объект
>
>>
эндообъект
9 0 объект
>
ручей
приложение/pdfdoi:10.1038/s41533-018-0081-y
4
%
1 0 объект
>
эндообъект
11 0 объект /Создатель (Спрингер)
/Заголовок (Рецидивирующие заболевания нижних дыхательных путей у детей раннего возраста в сельской местности Кыргызстана: чрезмерное использование антибиотиков и возможная неправильная диагностика астмы.Качественное исследование FRESH AIR)
/CrossMarkDomains#5B2#5D (springerlink.com)
/Ключевые слова ()
/CrossMarkDomains#5B1#5D (springer.com)
/ModDate (D:20180628102015+02’00’)
/Тема (npj Primary Care Respiratory Medicine, doi:10.1038/s41533-018-0081-y)
/ doi (10.1038/s41533-018-0081-y)
/Автор
/CreationDate (D:20180626170531+05’30’)
>>
эндообъект
2 0 объект
>
эндообъект
3 0 объект
>
эндообъект
4 0 объект
>
эндообъект
5 0 объект
>
эндообъект
6 0 объект
>
/Шрифт >
>>
/DA (/Helv 0 Tf 0 г )
>>
эндообъект
7 0 объект
>
>>
эндообъект
8 0 объект
>
>>
эндообъект
9 0 объект
>
ручей
приложение/pdfdoi:10.1038/s41533-018-0081-y - Рецидивирующие заболевания нижних дыхательных путей среди детей младшего возраста в сельской местности Кыргызстана: чрезмерное использование антибиотиков и возможная гиподиагностика астмы.
 Качественное исследование FRESH AIR
Качественное исследование FRESH AIR - Марианна Штуббе Остергорд
- Йеспер Кьергор
- Метте Мари Кристенсен
- Сюзанна Ревентлоу
- Аня Поульсен
- Эльвира Исаева
- Азамат Акылбеков
- Талант Сооронбаев
- Спрингер США
- npj Респираторная медицина первичной медико-санитарной помощи, doi:10.1038/с41533-018-0081-й 10.1038/s41533-018-0081-yhttp://dx.doi.org/10.1038/s41533-018-0081-yjournalnpj Респираторная медицина первой помощи© 2018, Автор(ы)2055-101010.1038/s41533-018-0081-y
- springer.com
- springerlink.com 2010-04-23True10.1038/s41533-018-0081-y
- springer.com
- springerlink.com Springer2018-06-28T10:20:15+02:002018-06-26T17:05:31+05:302018-06-28T10:20:15+02:00TrueiText® 5.
- converteduuid: 4b34c411-0486-4f50-b8fc-c6b254f3ae9econverted в PDF / A- 2bpdfToolbox2018-06-26T17:06:19+05:30 2B
- Марианна Стуббе Остергаардhttp://orcid.org/0000-0002-4284-5867
- Йеспер Кьергорhttp://orcid.org/0000-0003-2181-4743
- Эльвира Исаеваhttp://orcid.org/0000-0002-4165-5156
- http://нс.adobe.com/pdf/1.3/pdfAdobe PDF Schema
- internalОбъект имени, указывающий, был ли документ изменен для включения информации треппингаTrappedText
- http://ns.adobe.com/pdfx/1.3/pdfxpdfx
- внутренний идентификатор стандарта PDF/XGTS_PDFXVersionText
- внутренний уровень соответствия стандарту PDF/XGTS_PDFXConformanceText
- internalCompany создает PDFCompanyText
- internalDate, когда документ был последний раз измененSourceModifiedText
- externalMirrors crossmark:CrosMarkDomainsCrossMarkDomainsSeq Text
- перекрестие внутренних зеркал: DOIdoiText
- http://нс.
 adobe.com/xap/1.0/mm/xmpMMXMP Media Management Schema
adobe.com/xap/1.0/mm/xmpMMXMP Media Management Schema - внутренний идентификатор на основе UUID для конкретного воплощения документаInstanceIDURI
- internalОбщий идентификатор для всех версий и представлений документа.OriginalDocumentIDURI
- http://www.aiim.org/pdfa/ns/id/pdfaidPDF/A ID Schema
- internalPart of PDF/A standardpartInteger
- внутреннее изменение стандарта PDF/A amdText
- внутренний уровень соответствия стандарту PDF/A, текст
- http://crossref.org/crossmark/1.0/crossmarkcrossmark
- internalCrossMarkDomainsCrossMarkDomainsSeq Text
- internalCrossmarkDomainExclusiveCrossmarkDomainExclusiveText
- внутреннийОбычно то же, что и prism:doiDOIText
- externalThe дата публикации публикации.
 MajorVersionDateText
MajorVersionDateText - http://prismstandard.org/namespaces/basic/2.0/prismPrism
- внешнийТип агрегации указывает единицу агрегации для коллекции контента.Комментарий PRISM рекомендует использовать управляемый словарь агрегации PRISM для предоставления значений для этого элемента. Примечание. PRISM не рекомендует использовать значение #other, разрешенное в настоящее время в этом контролируемом словаре. Вместо использования #other, пожалуйста, обратитесь в группу PRISM по адресу [email protected], чтобы запросить добавление вашего термина в словарь контролируемого типа агрегации. агрегатионтипетекст
- externalАвторское право CopyrightText
- externalЦифровой идентификатор объекта для статьи.DOI также может использоваться в качестве идентификатора dc:identifier. При использовании в качестве dc:identifier форма URI должна быть захвачена, а голый идентификатор также должен быть захвачен с помощью prism:doi.
 Если в качестве требуемого dc:identifier используется альтернативный уникальный идентификатор, то DOI следует указывать как голый идентификатор только в пределах prism:doi.
Если необходимо указать URL-адрес, связанный с DOI, то prism:url можно использовать вместе с prism:doi для предоставления конечной точки службы (т. е. URL-адреса).
доитекст
Если в качестве требуемого dc:identifier используется альтернативный уникальный идентификатор, то DOI следует указывать как голый идентификатор только в пределах prism:doi.
Если необходимо указать URL-адрес, связанный с DOI, то prism:url можно использовать вместе с prism:doi для предоставления конечной точки службы (т. е. URL-адреса).
доитекст - externalISSN для электронной версии выпуска, в котором встречается ресурс.Разрешает издателям включать второй ISSN, идентифицирующий электронную версию выпуска, в котором встречается ресурс (поэтому e(lectronic)Issn. Если используется, prism:eIssn ДОЛЖЕН содержать ISSN электронной версии. См. prism:issn. исснтекст
- externalНазвание журнала или другого издания, в котором был/будет опубликован ресурс.
Обычно это будет использоваться для предоставления названия журнала, в котором статья появилась в качестве метаданных для статьи, а также такой информации, как название статьи, издатель, том, номер и дата обложки.
 Примечание. Название публикации можно использовать, чтобы различать печатный журнал и онлайн-версию, если названия различаются, например «magazine» и «magazine.com».
публикацияNameText
Примечание. Название публикации можно использовать, чтобы различать печатный журнал и онлайн-версию, если названия различаются, например «magazine» и «magazine.com».
публикацияNameText - externalЭтот элемент содержит URL-адрес статьи или единицы контента. Платформа атрибутов необязательно разрешена для ситуаций, в которых необходимо указать несколько URL-адресов. PRISM рекомендует использовать в сочетании с этим элементом подмножество значений платформы PCV, а именно «мобильный» и «веб-сайт».ПРИМЕЧАНИЕ. PRISM не рекомендует использовать значение #other, разрешенное в словаре, контролируемом платформой PRISM. Вместо использования #other обратитесь к группе PRISM по адресу [email protected], чтобы запросить добавление вашего термина в словарь, контролируемый платформой. URL-текст
- http://springernature.com/ns/xmpExtensions/2.0/snSpringer Nature Схема ORCID
- Информация о внешнем авторе: содержит имя каждого автора и его/ее ORCID (ORCiD: Open Researcher and Contributor ID).
 ORCID — это постоянный идентификатор (непатентованный буквенно-цифровой код), позволяющий однозначно идентифицировать научных и других академических авторов. authorInfoBag AuthorInformation
ORCID — это постоянный идентификатор (непатентованный буквенно-цифровой код), позволяющий однозначно идентифицировать научных и других академических авторов. authorInfoBag AuthorInformation - Указывает типы информации об авторе: имя и ORCID автора. http://springernature.com/ns/xmpExtensions/2.0/authorInfo/authorAuthorInformation
- Указывает имя автора.nameText
- Выдает ORCID автора.orcidURI
- http://www.niso.org/schemas/jav/1.0/javNISO
- externalValues for Journal Article Version — одно из следующих: АО = Авторский оригинал SMUR = Представленная рукопись находится на рассмотрении AM = принятая рукопись П = Доказательство VoR = версия записи CVoR = исправленная версия записи EVOR = расширенная версия Recordjournal_article_versionClosed Выбор текста конечный поток эндообъект 10 0 объект > эндообъект 12 0 объект > эндообъект 13 0 объект > ручей HWRG}-G_1vl1@a,»${WE4_»تTb(KK bMb0tO7}3^2{ǹ*U0%9NR!XSSBqN 7 O&G!$_WMKfttЂۤӶ`hX0s)dCCс)&52
- Грипп.
- ОРВИ.
- Профилактика развития осложнений гриппа и простудных заболеваний.
- Профилактика и терапия инфекции у пациентов с ослабленным иммунитетом.
- Хронические цитомегаловирусные и герпетические инфекционные патологии.
- Совместное лечение смешанных бактериальных инфекций.
- «Ремантадин».
- «Арбидол».
- «Кагоцел» (мощный аналог, справляющийся с хламидозами и энтеровирусами).
- «Виферон» (самый дешевый аналог «Анаферона», продается в свечах).
- Оцилококцинум.
- «Афлубин» (дешевый аналог детского «Анаферона»).
- «Энгистол».
- «Амизон».
- «Гриппферон».
- Интерферон.
- Тамифлю.
- Новирин.
- Исмижен.
- «Гроприносин».
- «Милистан».
- кишечных инфекциях
- ОРВИ,
- герпесвирусные инфекции,
- грипп,
- нейроинфекция,
- острые респираторные заболевания, спровоцированные вирусными возбудителями;
- грипп;
- профилактика всевозможных осложнений, которые могут развиться при ОРВИ;
- цитомегаловирусная инфекция;
- герпетическая инфекция в хронической или острой фазе.
 Часто назначение Анаферона требуется при генитальном герпесе, инфекционном мононуклеозе, аденовирусе, ветряной оспе;
Часто назначение Анаферона требуется при генитальном герпесе, инфекционном мононуклеозе, аденовирусе, ветряной оспе; - в составе комплексной терапии смешанных и бактериальных инфекций;
- лечение инфекций, развившихся на фоне иммунодефицитных состояний, а также профилактика таких заболеваний.
 3,5 © 2000-2012 1T3XT BVBA (AGPL-версия) VoRuuid: 963054b6-a803-4827-ad10-64f961885d67uuid: 9650f781-eed1-44c5-bd69-98198905e35bdefault1
3,5 © 2000-2012 1T3XT BVBA (AGPL-версия) VoRuuid: 963054b6-a803-4827-ad10-64f961885d67uuid: 9650f781-eed1-44c5-bd69-98198905e35bdefault1Детские таблетки пингвина, как они есть называется.
 «Анаферон» (детский): Комаровский отзывы, применение, аналоги
«Анаферон» (детский): Комаровский отзывы, применение, аналогиПростуда и грипп – одни из самых распространенных заболеваний в мире. Именно из-за респираторной вирусной инфекции происходит максимальное количество обращений к терапевту и педиатру. По статистике, здоровый взрослый человек заболевает ОРВИ не менее 3-4 раз в год, а количество эпизодов простудных заболеваний у детей может быть в три, а иногда и в четыре раза выше. И тяжесть заболевания, и частота инфекций во многом, если не во всем, зависят от состояния иммунной системы человека: чем выше иммунный ответ, тем легче протекает простуда.Основной принцип действия многих профилактических и лечебных противопростудных препаратов, в том числе Анаферона, также основан на иммуностимулирующем эффекте.
Анаферон – популярное российское средство для лечения и профилактики респираторных вирусных инфекций у взрослых и детей: как гриппа, так и ОРВИ, независимо от вида возбудителя, вызвавшего заболевание. Идея его создания была предложена отечественной компанией, производящей гомеопатические препараты — Материа Медика. В перечне ее продукции, помимо детского и взрослого Анаферона, есть множество других гомеопатических средств, в том числе Агри и Агри Детский с противовирусными свойствами, гомеопатические таблетки от боли в горле Фарингомед, а также инновационный препарат для лечения вирусных инфекций. Эргоферон.Кроме того, в портфолио Материа Медика также входят гомеопатические лекарства от кашля в таблетках и раствор Ренгалин. Каждый из этих препаратов можно использовать при простуде и гриппе, и все же наибольшей популярностью пользуются пастилки Анаферон.
В перечне ее продукции, помимо детского и взрослого Анаферона, есть множество других гомеопатических средств, в том числе Агри и Агри Детский с противовирусными свойствами, гомеопатические таблетки от боли в горле Фарингомед, а также инновационный препарат для лечения вирусных инфекций. Эргоферон.Кроме того, в портфолио Материа Медика также входят гомеопатические лекарства от кашля в таблетках и раствор Ренгалин. Каждый из этих препаратов можно использовать при простуде и гриппе, и все же наибольшей популярностью пользуются пастилки Анаферон.
Слава Анаферона настолько велика, что до 2012 года он входил в Российский Перечень жизненно необходимых для здоровья человека лекарственных средств. Почему этот препарат заслужил такое высокое признание отечественных медицинских деятелей, рядовых врачей, а главное, самих пациентов – об этом мы и расскажем в этой статье.А заодно разберем пошагово, как Анаферон влияет на иммунный ответ, как и сколько дней его принимать.
Рождение нового
И начнем знакомство с истории создания наркотиков. В начале 90-х, когда рухнули барьеры между отечественной и западной фармацевтикой, на территории постсоветского пространства резко возросла популярность доселе малодоступных альтернативных лекарств и БАДов, в том числе гомеопатических средств.Одной из первых на волну времени отреагировала молодая российская компания Материа Медика, специалисты которой вплотную занялись разработкой и внедрением комплексных гомеопатических препаратов.
В начале 90-х, когда рухнули барьеры между отечественной и западной фармацевтикой, на территории постсоветского пространства резко возросла популярность доселе малодоступных альтернативных лекарств и БАДов, в том числе гомеопатических средств.Одной из первых на волну времени отреагировала молодая российская компания Материа Медика, специалисты которой вплотную занялись разработкой и внедрением комплексных гомеопатических препаратов.
К началу XXI века холдинг «Материа Медика» разработал потенциально новый класс лекарственных средств, не имеющих аналогов не только в Российской Федерации, но и во всем мире. Они содержали сверхмалые дозы природных антител и, по словам разработчиков, обладали уникальными свойствами.
В 2002 году на рынок вышел первый представитель этих препаратов Анаферон Детский.
Потребители с восторгом приняли дебютанта. Продажи Анаферона для детей били все рекорды, а мамы не уставали давать своим детям сладковатые и совершенно безопасные таблетки. Производитель, вдохновленный успехом первенца, через два года запустил Анаферон для взрослых. Сегодня препарат зарегистрирован не только в России, но и во многих странах бывшего СССР.Интересно, что в 2009 году в США был запатентован и Анаферон, хотя за рубежом он не смог снискать российской славы, несмотря на громкие заявления Материа Медика об инновационных разработках и уникальном составе. Кстати, пора с ним познакомиться.
Производитель, вдохновленный успехом первенца, через два года запустил Анаферон для взрослых. Сегодня препарат зарегистрирован не только в России, но и во многих странах бывшего СССР.Интересно, что в 2009 году в США был запатентован и Анаферон, хотя за рубежом он не смог снискать российской славы, несмотря на громкие заявления Материа Медика об инновационных разработках и уникальном составе. Кстати, пора с ним познакомиться.
>> Рекомендуем: если вас интересуют эффективные методы избавления от хронических ринитов, фарингитов, тонзиллитов, бронхитов и затяжных простудных заболеваний, то после прочтения этой статьи обязательно загляните на страницу этого сайта .Информация основана на личном опыте автора и помогла многим, надеемся поможет и вам. Теперь возвращаемся к статье.
Состав Анаферона: расшифровываем инструкцию по применению
Если человек без медицинского образования захочет разобраться в тонкостях инструкции по применению, то в разделе «Состав» он, скорее всего, споткнется о непонятные термины. Давайте разберемся с информационным туманом, в который производитель заводит неискушенного читателя.
Давайте разберемся с информационным туманом, в который производитель заводит неискушенного читателя.
Итак, Анаферон содержит антитела к гамма-интерферону человека. И не просто антитела, а так называемая смесь гомеопатических разведений. Неудивительно, что эта формулировка сбивает с толку потребителей.
Что такое антитела?
Начнем с того, что антитела — это особые белки, которые вырабатывает организм человека. Они располагаются на поверхности лейкоцитов, В-лимфоцитов, а также в сыворотке и тканевой жидкости. Антитела «умеют» распознавать особые молекулы, которые есть у каждого микроорганизма или вируса — антигены.После «узнавания» антитела образуют прочный комплекс с антигенами, способный полностью нейтрализовать бактерию или вирус. Кроме того, «гениальные» белки также стимулируют иммунный ответ.
Однако антитела, содержащиеся в Анафероне, направлены не на создание комплекса антитело-чужеродный антиген, а на стимуляцию выработки интерферона, другого вещества, значение которого не всегда понятно рядовому потребителю.
Что такое интерферон?
Следует отметить, что Анаферон содержит не антитела к патогенным возбудителям, а белки, стимулирующие выработку интерферона гамма.Это еще один термин, требующий «расшифровки». Интерфероны, как и антитела, представляют собой особые белки. Они вырабатываются в организме в ответ на вирусные инфекции. Три типа человеческого интерферона — альфа, бета и гамма — вступают в бой и побеждают врага, помогая клетке стать полностью невосприимчивой к вирусу. Антитела стимулируют выработку гамма-интерферона, что в конечном итоге усиливает иммунный ответ.
Что такое гомеопатическое разведение?
Принцип действия гомеопатии основан на стимуляции собственных защитных сил организма под действием ничтожно малых доз препарата.Для достижения «гомеопатической» дозировки препарат разводят в инертных растворителях. Причем разводят в таком количестве, что в конечном продукте, как правило, не остается ни одной молекулы исходного, неразбавленного вещества. В Анафероне используются разведения С12, С30 и С200. Это означает, что он включает сотые (стократные) разведения антител к интерферону гамма, повторенные 12, 30 и 200 раз соответственно.
В Анафероне используются разведения С12, С30 и С200. Это означает, что он включает сотые (стократные) разведения антител к интерферону гамма, повторенные 12, 30 и 200 раз соответственно.
Как производится?
Согласно заявлениям компании «Материя Медика», технология производства таблеток Анаферон основана на иммунизации кроликов гамма-интерфероном человека, после чего в организме животного начинают массово вырабатываться антитела.Затем с помощью так называемой аффинной очистки из сыворотки крови кролика выделяют образовавшиеся полезные белки, которые впоследствии разводят в многократных сотенных разведениях водно-спиртовым раствором. По данным производителя, в 1 грамме взрослого Анаферона содержится не более 10-24 антител к гамма-интерферону, что можно смело приравнять к нулю.
«Но если масса действующего вещества не превысила нулевую отметку, то каков состав препарата?» — спросит читатель.Конечно, вспомогательные вещества в какой-то мере в данном случае играют роль основных. В своем качестве Анаферон, как и большинство других гомеопатических препаратов, использует целлюлозу, стеарат магния и, самое главное, лактозу, или молочный сахар. Это его нейтральное сладковатое послевкусие вы чувствуете, когда рассасываете гомеопатические таблетки. При этом масса таблетки равна массе молочного сахара в ее составе — ведь действующее вещество в гомеопатии почти эфемерно и не имеет собственного веса.Кстати, наличие лактозы следует учитывать людям с дефицитом фермента лактазы, расщепляющего молочный сахар. Но подробнее об этом нюансе мы поговорим в разделе «Противопоказания». Теперь попробуем разобраться, помогает ли Анаферон и как он действует?
В своем качестве Анаферон, как и большинство других гомеопатических препаратов, использует целлюлозу, стеарат магния и, самое главное, лактозу, или молочный сахар. Это его нейтральное сладковатое послевкусие вы чувствуете, когда рассасываете гомеопатические таблетки. При этом масса таблетки равна массе молочного сахара в ее составе — ведь действующее вещество в гомеопатии почти эфемерно и не имеет собственного веса.Кстати, наличие лактозы следует учитывать людям с дефицитом фермента лактазы, расщепляющего молочный сахар. Но подробнее об этом нюансе мы поговорим в разделе «Противопоказания». Теперь попробуем разобраться, помогает ли Анаферон и как он действует?
Как действует Анаферон?
Препарат относится к группе иммуностимулирующих профилактических средств. Стимулирует иммунный ответ, а также оказывает противовирусное действие.На фоне приема таблеток Анаферон увеличивается выработка антител и образование всех трех видов интерферона – альфа, бета и гамма. По словам производителя, при лечении Анафероном снижается концентрация вирусных частиц в пораженных тканях, что ускоряет выздоровление и в конечном итоге снижает вероятность осложнений от простуды.
Однако у многих потребителей, познакомившихся с особенностями состава и производства лекарств, возникает вполне резонный вопрос: как может действовать лекарство, если оно не содержит ни одной молекулы действующего вещества – ведь молочный сахар неспособны стимулировать иммунный ответ? Давайте разберемся.
Подводные камни гомеопатии
Гомеопатия не является официальным лечением. Это альтернативная форма медицины, которая с момента своего появления подвергалась жесткой критике со стороны приверженцев традиционного направления. Основной принцип гомеопатии — лечить подобное подобным.
Согласно концепции создателя гомеопатии немецкого врача Самуэля Ганемана, вещества, применяемые в качестве лечебных средств у здоровых людей, вызывают симптомы, сходные с проявлениями болезни.
Если следовать этой теории, здоровый человек, принимающий Анаферон, должен ощущать признаки простуды.
По утверждениям врачей-гомеопатов, лекарства, содержащие настолько ничтожные дозы активных веществ, что обнаружить их невозможно даже с помощью современных инновационных технологий, могут работать за счет некой «памяти». Скажем, его усваивают водой для разведения в процессе приготовления лекарства. Мы не будем оспаривать эту теорию или соглашаться с ней — это задача ученых.Кстати, свое веское слово они уже сказали, причислив действие гомеопатических средств к действию лекарства-пустышки, то есть плацебо.
Скажем, его усваивают водой для разведения в процессе приготовления лекарства. Мы не будем оспаривать эту теорию или соглашаться с ней — это задача ученых.Кстати, свое веское слово они уже сказали, причислив действие гомеопатических средств к действию лекарства-пустышки, то есть плацебо.
Однако в этой связи не помешает упомянуть, что эффект плацебо, по некоторым данным, может достигать 50%. Не все препараты, признанные официальной медициной, могут похвастаться таким впечатляющим результатом. Поэтому многие специалисты придерживаются нейтральной позиции: если гомеопатические препараты помогают больному, пусть и дальше лечится ими.Если человек не чувствует никаких изменений, все равно стоит обратиться к официальной медицине.
Кстати, специалисты Всемирной организации здравоохранения настаивают на том, что гомеопатические препараты нельзя применять для лечения тяжелых заболеваний, в том числе инфекционных. Однако гомеопатия была и остается одной из самых популярных форм альтернативной медицины. Гомеопатические препараты широко используются во многих развитых странах мира, в том числе в Германии и Франции. В странах бывшего СССР гомеопатические средства также пользуются большим спросом.Их применяют для лечения самых разных заболеваний, в том числе и простудных.
Гомеопатические препараты широко используются во многих развитых странах мира, в том числе в Германии и Франции. В странах бывшего СССР гомеопатические средства также пользуются большим спросом.Их применяют для лечения самых разных заболеваний, в том числе и простудных.
Показания к приему Анаферона
Анаферон – универсальный препарат, который применяется при ряде различных заболеваний. Перечислим наиболее распространенные показания к назначению:
Применение Анаферона при ветряной оспе может способствовать более легкому течению заболевания, а также ускорить выздоровление.
Анаферон и часто болеющие дети: лекарство-находка или …?
Важной и трудноразрешимой (или практически неразрешимой) проблемой как для педиатров, так и для родителей является регулярность возникновения респираторных инфекций у определенной группы детей, попадающих в категорию «часто болеющих».В то время как большинство малышей болеют ОРВИ 6–8 раз в год, что считается абсолютной нормой, люди часто болеют простудой или гриппом хотя бы раз в месяц, а иногда и чаще. В этом случае часто начинается вирусная инфекция, но не заканчивается, и на первых порах довольно невинное ОРВИ превращается в грозную бактериальную инфекцию, требующую немедленной антибактериальной терапии.
В этом случае часто начинается вирусная инфекция, но не заканчивается, и на первых порах довольно невинное ОРВИ превращается в грозную бактериальную инфекцию, требующую немедленной антибактериальной терапии.
Причина столь высокой подверженности множеству «детских» болезней чаще всего кроется в нарушении иммунного ответа.Во время нечастых ремиссий педиатры делают все возможное, чтобы нормализовать иммунный статус ребенка. Препараты эхинацеи, свечи и капли с интерфероном, бактериальные лизаты (например, Бронхо-Мунал или ИРС-19) – используются все доступные на рынке иммуномодуляторы. Нередко схема комплексной терапии пополняется гомеопатическими препаратами, среди которых Энгистол, Грипп-Хелем, Лимфомиозот и, конечно же, Анаферон детский. Насколько оправдано и безопасно назначение последних в таких случаях?
Скажем прямо: главным преимуществом назначения профилактических (и даже лечебных) схем терапии Анафероном является высокий профиль безопасности препарата.Он не способен провоцировать какие-либо побочные эффекты или вступать в реакцию с какими-либо другими препаратами.
Это весомое «за» в пользу применения детского Анаферона как метода профилактики респираторных инфекций для всех взрослых и детей в возрасте от 1 месяца, в том числе часто болеющих. При этом лекарственная нагрузка на организм минимальна, если не нулевая: вспомните дозировку «действующего вещества» в таблетках лактозы и метилцеллюлозы. Поэтому родители, дающие Анаферон своим детям на любой, даже самый длительный срок, могут спать спокойно и не переживать за страдающие печень, желудок и другие внутренние органы ребенка: дозы лекарства они точно не «заметят», т.к. включая ударные.
В то же время следует отметить, что многие специалисты крайне скептически относятся к терапевтическим возможностям Анаферона, причисляя его к известному списку так называемых фуфломицинов.
Мы не будем оценивать эффективность препарата: это задача врачей, а не медицинских журналистов. Однако, даже если предположить, что Анаферон полностью и бесповоротно неэффективен, нельзя отрицать факт его безопасности. А значит, как говорят скептики, «хуже точно не будет.Для родителей, порой отчаявшихся в поисках путей, которые привели бы к долгожданному детскому здоровью, этого факта достаточно, чтобы иметь возможность сказать Анаферону «да» и дать своему ребенку столько, сколько позволяет инструкция. теперь поговорим о том, как принимать препарат детям, и как пить взрослому
А значит, как говорят скептики, «хуже точно не будет.Для родителей, порой отчаявшихся в поисках путей, которые привели бы к долгожданному детскому здоровью, этого факта достаточно, чтобы иметь возможность сказать Анаферону «да» и дать своему ребенку столько, сколько позволяет инструкция. теперь поговорим о том, как принимать препарат детям, и как пить взрослому
Как принимать Анаферон
Схема лечения и профилактики одинакова для любого возраста — назначают только детям (старше 1 месяца) детская форма препарата и взрослая, соответственно взрослая.
За один раз необходимо рассасывать не более одной таблетки препарата.
Лечение ОРВИ
Терапию вирусных инфекций следует начинать при первых признаках заболевания. При этом, как и в случае с любыми другими гомеопатическими средствами, лечение начинают с ударной дозы.
В первые два часа после начала заболевания таблетки необходимо рассасывать каждые полчаса. После этого двухчасового «марафона» принимают еще три таблетки Анаферона, распределяя их поровну на остаток дня.
Со второго дня переходят на «спокойный» режим: по 1 таблетке 3 раза в день. Терапию продолжают до полного выздоровления.
Лечение герпетической инфекции (генитальной)
При рецидиве генитального герпеса можно попробовать облегчить состояние Анафероном. Схема терапии, как и при ОРВИ, начинается с ударной дозы.
В первые трое суток после появления сыпи по одной таблетке принимают 8 раз, а с четвертого дня терапии рассасывают по одной таблетке 4 раза.Продолжительность лечения не должна быть менее трех недель.
Профилактика ОРВИ
Профилактический курс прост и понятен: по заверениям производителя, прием одной таблетки три раза в день в течение от 1 до 3 месяцев способствует снижению риска заражения респираторными инфекциями и вирусами герпеса. Кстати, профилактические свойства Анаферона можно использовать для предотвращения заражения ветряной оспой в случае эпидемии или карантина в детских учреждениях (детских садах или школах).
Профилактика рецидивов генитального герпеса
Генитальный герпес — крайне неприятная инфекция, которую невозможно вылечить раз и навсегда. Целью лечения в таких случаях является поддержание иммунного статуса больного, что позволяет увеличить продолжительность безрецидивного периода. Анаферон можно применять для профилактики рецидивов генитального герпеса по схеме: по одной таблетке три раза в день в течение длительного времени (до полугода, а иногда и дольше).
Целью лечения в таких случаях является поддержание иммунного статуса больного, что позволяет увеличить продолжительность безрецидивного периода. Анаферон можно применять для профилактики рецидивов генитального герпеса по схеме: по одной таблетке три раза в день в течение длительного времени (до полугода, а иногда и дольше).
Как правильно пить гомеопатические препараты?
Для пациентов, начинающих принимать Анаферон или решивших лечить им своих детей, важно знать правила применения гомеопатических препаратов.От их соблюдения во многом зависит конечный результат терапии или профилактики.
Итак, все гомеопатические средства следует рассасывать во рту, а именно под языком. Это требование объясняется тем, что лекарство, доставляемое сублингвально (то есть сублингвально), всасывается непосредственно в кровоток, минуя пищеварительный тракт. Подъязычная область имеет разветвленную капиллярную сеть, расположенную близко к поверхности слизистой оболочки. Именно в эти капилляры проникает препарат.
Некоторых потребителей интересует, можно ли принимать гомеопатические препараты, в том числе Анаферон, как обычно, внутрь. Отвечаем: можно, однако результат такой терапии, скорее всего, будет приближаться к нулю.
Так вот предельно малые дозы действующих веществ (веществ), содержащихся в гомеопатических препаратах, проходя через «жернова» пищеварительного тракта, просто «теряются», а в кишечнике всасывается только лактоза и другие вспомогательные вещества.
Еще одним важным требованием является то, что гомеопатические препараты нельзя пить одновременно с едой. они просто не будут всасываться в кровь. «Правильное» дозирование следует проводить либо через час после еды, либо за полчаса до еды.
Что правильно давать детям?
И еще один вопрос, требующий подробного освещения: как давать Анаферон маленьким детям, которые еще не могут нормально растворять таблетки во рту?
Производитель рекомендует растворять лекарство в небольшом количестве очищенной или кипяченой воды и давать ребенку. Если малыш может удерживать растворенное лекарство во рту несколько секунд или минут, прекрасно. В противном случае препарат все же будет всасываться, но, возможно, в несколько меньшей концентрации.
Если малыш может удерживать растворенное лекарство во рту несколько секунд или минут, прекрасно. В противном случае препарат все же будет всасываться, но, возможно, в несколько меньшей концентрации.
Обращаю внимание родителей, что Анаферон не рекомендуется растворять в соках, молоке и других напитках: из-за этого уменьшится всасывание препарата. Единственным надежным растворителем является обычная вода.
Анаферон или …?
Теперь поговорим об одной из самых актуальных тем, волнующих потребителей: что лучше? Что лучше, Анаферон или Арбидол (Кагоцел, Виферон, Эргоферон, Энгистол, Ремантадин и так далее)? На самом деле, на этот вопрос почти невозможно ответить.А все потому, что Анаферон – оригинальное лекарство, не имеющее других, более дешевых (равно как и более дорогих) аналогов.
Среди всех перечисленных выше препаратов ближайшим «родственником» Анаферона является Эргоферон – гомеопатические таблетки производства той же компании Материа Медика. Наряду с антителами к интерферону гамма Эргоферон содержит еще два типа антител, обладающих дополнительным противовоспалительным и противоаллергическим действием. Эргоферон назначают взрослым и детям (в отличие от Анаферона только с шестимесячного возраста) для лечения и профилактики респираторно-вирусных инфекций и гриппа.Нельзя с уверенностью сказать, какой из препаратов «лучше» или «хуже», и единственное, что можно посоветовать колеблющимся потребителям, — проверить эффективность экспериментально. Кстати, по безопасности Эргоферон ничем не уступает Анаферону, поэтому о побочных эффектах можно не беспокоиться.
Эргоферон назначают взрослым и детям (в отличие от Анаферона только с шестимесячного возраста) для лечения и профилактики респираторно-вирусных инфекций и гриппа.Нельзя с уверенностью сказать, какой из препаратов «лучше» или «хуже», и единственное, что можно посоветовать колеблющимся потребителям, — проверить эффективность экспериментально. Кстати, по безопасности Эргоферон ничем не уступает Анаферону, поэтому о побочных эффектах можно не беспокоиться.
Вопрос сравнения Анаферона с любыми другими противовирусными препаратами вообще некорректен — настолько они разные.
Единственным свойством, которое в какой-то степени делает препараты из приведенного нами перечня, является отсутствие четких доказательств эффективности с точки зрения доказательной медицины.Вот почему ни один из этих препаратов не используется в западных странах. Но можно с уверенностью сказать, что Анаферон (как и другие гомеопатические препараты) является одним из самых безопасных препаратов.
Побочные действия и противопоказания
Как мы уже говорили, Анаферон очень хорошо переносится. Единственным возможным побочным действием препарата является проявление индивидуальной чувствительности (то есть аллергии) к его компонентам, то есть к лактозе и другим вспомогательным веществам.
Единственным возможным побочным действием препарата является проявление индивидуальной чувствительности (то есть аллергии) к его компонентам, то есть к лактозе и другим вспомогательным веществам.
Безопасность Анаферона настолько высока, что его часто назначают при беременности или кормлении грудью, хотя в инструкции по применению препарата для этих категорий пациентов упоминается достаточно осторожно.Прежде чем назначать лекарство будущим или состоявшимся кормящим матерям, производитель рекомендует врачам взвесить соотношение риска и пользы.
И последнее: Анаферон разрешен к применению детям с 1 месяца и взрослым. Препятствием к его приему могут стать только два противопоказания: индивидуальная чувствительность и непереносимость лактозы. Во всех остальных случаях сомнений быть не может: Анаферон не нанесет вреда. Но будет ли это полезно, во многом зависит и от правильной дозировки и применения, и от тяжести заболевания, и от восприимчивости организма к гомеопатическим средствам.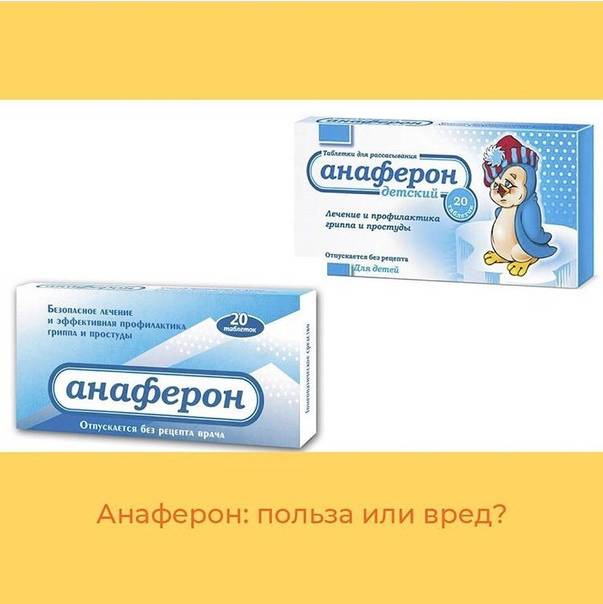
«Анаферон», от чего помогает этот противовирусный иммуномодулятор? Гомеопатическое лекарство активирует гуморальный и клеточный иммунитет. Препарат «Анаферон» инструкция по применению советует принимать при насморке, герпесе, ангине и голове.
Форма выпуска и состав
Выпускается в форме подъязычных таблеток. Продается в ячейковых упаковках по 20 штук. Таблетки «Анаферон», от которых лекарство помогает при симптомах гриппа и простуды, включают антитела к гамма-интерферону человека в объеме 3 мг и вспомогательные вещества.
Фармакологические свойства
Согласно информации, предоставленной инструкцией и Википедией, «Анаферон» применяется для лечения гриппа и простудных заболеваний. Это эффективное гомеопатическое средство с противовирусными и иммуномодулирующими свойствами.
После приема препарата в организме повышается уровень антител, активируется клеточный и гуморальный иммунитет, синтезируется гамма-интерферон, улучшается фагоцитарное действие макрофагов и цитокинов.
Таблетки «Интерферон», улучшающие самочувствие больного при ОРВИ и гриппозных проявлениях, быстро купируют признаки интоксикации и респираторные симптомы.Применение средства снижает вероятность суперинфекции и влияния бактерий на организм, образования гнойных осложнений.
Препарат «Интерферон»: от чего помогает
Показания к применению включают следующие заболевания и симптомы:
Средство назначают лицам с ослабленными защитными силами организма, часто в местах большого скопления людей, в условиях повышенного риска заражения.
Противопоказания
Инструкция запрещает применение «Анаферона» только при непереносимости его состава. Осторожность при лечении требуется женщинам, ожидающим рождения ребенка.
Осторожность при лечении требуется женщинам, ожидающим рождения ребенка.
Препарат «Анаферон»: инструкция по применению
Таблетки необходимо держать во рту до полного растворения.Лекарство принимают вне зависимости от диеты. Терапию начинают при первых симптомах заболевания. В течение первых 2 часов принимайте по 1 таблетке каждые полчаса. Затем до конца дня равномерно используют еще 3 таблетки. В последующие дни пьют по 1 таблетке 3 раза в день до полного выздоровления.
Профилактика болезней
В качестве профилактики инструкция по применению предписывает принимать «Анаферон» в течение 1-3 месяцев. Суточная доза составляет 1 таблетку. Если больного укусил клещ, то необходимо применять средство в течение 3 недель по 1 таблетке 3 раза в день.Это мероприятие предотвратит развитие клещевого энцефалита.
Как пить при герпесе
При появлении признаков генитального герпеса лекарство пьют по следующей схеме. Первые 3 дня принимают по 8 таблеток через равные промежутки времени. В последующие 2 дня дозу снижают до 7 драже, еще 2 дня применяют по 6 капсул. Следующие 2 дня — по 5 и еще 2 дня — по 4 таблетки. Затем переходят на 3 капсулы в день в течение декады.
В последующие 2 дня дозу снижают до 7 драже, еще 2 дня применяют по 6 капсул. Следующие 2 дня — по 5 и еще 2 дня — по 4 таблетки. Затем переходят на 3 капсулы в день в течение декады.
«Анаферон детский»: инструкция по применению
Для профилактики заболеваемости ОРВИ и гриппом детям дают по 1 таблетке в течение месяца.После месячного перерыва профилактическую обработку можно повторить.
Побочные эффекты
Применение препарата «Анаферон» вызывает негативные реакции организма в редких случаях. При повышенной чувствительности к медикаменту могут быть проявления аллергии на коже: зуд, покраснение.
специальные инструкции
При отсутствии улучшения состояния в течение трех дней после приема препарата следует обратиться к врачу. При совместном применении с анальгетиками и нестероидными противовоспалительными средствами дозировку последних можно уменьшить.Кроме того, прием лекарства может сократить продолжительность терапии.
Аналоги препарата «Анаферон»
Аналогов препарата по действующему веществу нет. Аналогичным действием обладают лекарства:
Аналогичным действием обладают лекарства:
Что лучше: Анаферон или Эргоферон?
Аналог обладает выраженным противовирусным действием, а также противоаллергическим действием. Лекарство может назначаться по более широкому кругу показаний.
Что лучше: Анаферон или Афлубин?
Этот аналог обладает, помимо иммуномодулирующего действия, терморегуляторными, дезинтоксикационными, противовоспалительными свойствами.Лекарство имеет разный состав и назначается исходя из целесообразности применения.
Для детей, беременных и кормящих
Детям после 1 месяца от рождения назначают «Анаферон детский». В связи с отсутствием сведений о влиянии препарата на плод и новорожденного лечение данным средством нежелательно.
Цена
В Москве можно купить Анаферон в таблетках по 195 руб.
Цена в Киеве 50-60 гривен.
В Минске — 6-8 BYN. рублей.
По Казахстану — 1100 тенге.
«Анаферон» детский в форме таблеток предлагается маленьким пациентам в период заболеваний органов дыхания и для их профилактики. Сейчас этот препарат назначают многие врачи без исключения, хотя отзывы о нем довольно противоречивы. Сама православная медицина скептически относится к гомеопатическим средствам, в том числе к Анаферону. И, тем не менее, педиатры предлагают малышам «Анаферон».Мнение Комаровского по этому поводу однозначно: «Анаферон», как иммуномодулирующее средство, совершенно бесполезен.
Почему главный педиатр СНГ так категоричен? На это есть объективные причины. Комаровский уверен, что врачи прекрасно понимают, что этот препарат малоэффективен, и максимум, чего от него можно ожидать, — это эффекта плацебо, о чем свидетельствуют многочисленные отзывы. С другой стороны, «Анаферон» безопасен и не представляет угрозы для здоровья ребенка, а значит, его можно назначать, не беспокоясь о последствиях.Так фармацевты зарабатывают свои копейки, и так родители малышей успокаивают себя тем, что делают все возможное для здоровья ребенка.
Комаровский уверен, что врачи прекрасно понимают, что этот препарат малоэффективен, и максимум, чего от него можно ожидать, — это эффекта плацебо, о чем свидетельствуют многочисленные отзывы. С другой стороны, «Анаферон» безопасен и не представляет угрозы для здоровья ребенка, а значит, его можно назначать, не беспокоясь о последствиях.Так фармацевты зарабатывают свои копейки, и так родители малышей успокаивают себя тем, что делают все возможное для здоровья ребенка.
Мнение Комаровского по поводу Анаферона поддерживают многие специалисты. Но говорить об этом открыто не хотят — ведь фармрынок «кормит» тех же врачей.
Показания к применению
Для чего нужен Анаферон? Согласно инструкции по применению назначают при:
При этом производители подчеркивают, что данный состав лучше использовать в комплексе с другими препаратами. Видимо, из-за того, что вне комплексной терапии «Анаферон» не действует.
Видимо, из-за того, что вне комплексной терапии «Анаферон» не действует.
Некоторые пациенты, испробовавшие средство, оставляют положительные отзывы, говоря, что почувствовали его благотворное действие, и на 3-5-й день приема симптомы исчезли. Комаровский отвечает, что в нормальных условиях любые респираторные недуги за это время пройдут самостоятельно, по крайней мере симптомы острой формы утихнут.
В качестве профилактики герпесвирусной инфекции рекомендуется применять Анаферон в течение полугода.Комаровский предупреждает, что даже гомеопатические средства нельзя использовать так долго.
Отзывы педиатров
Как известно из многих программ, Комаровский выражает недовольство гомеопатическими препаратами и приводит реальные аргументы в пользу отказа от них. Концентрация активного вещества в одной таблетке настолько мала, что не может оказать никакого влияния на здоровье человека. Цифра производителя 10-16 нг/г смешна. А вот количество сахара в виде моногидрата лактозы зашкаливает. На самом деле именно сахаром производители Анаферона пытаются лечить детей.
На самом деле именно сахаром производители Анаферона пытаются лечить детей.
Состав
Активные компоненты: аффинно очищенные антитела к гамма-интерферону человека — 0,003 г *
Вспомогательные вещества: лактоза, целлюлоза микрокристаллическая, магния стеарат.
* вводится в виде водно-спиртовой смеси активной формы действующего вещества 1
1 Активная форма действующего вещества — активная форма с содержанием не более 10 -15 нг/г активного вещества.
Описание
Таблетки плоскоцилиндрической формы, с риской и фаской, от белого до почти белого цвета. На плоской стороне с каракулями надпись MATERIA MEDICA, на другой плоской стороне надпись ANAFERON.
Фармакотерапевтическая группа
Иммуномодуляторы. Противовирусные агенты.
Коды АТХ L03, J05AX
фармакологический эффект
При профилактическом и лечебном применении препарат оказывает иммуномодулирующее и противовирусное действие. Экспериментально и клинически установлена эффективность в отношении вирусов гриппа (в том числе гриппа птиц), парагриппа, вирусов простого герпеса 1 и 2 типов (лабиальный герпес, генитальный герпес), других вирусов герпеса (ветряная оспа, инфекционный мононуклеоз), энтеровирусов, клещевого вируса энцефалит, ротавирус, коронавирус, калицивирус, аденовирус, респираторно-синцитиальный (РС-вирус). Препарат снижает концентрацию вируса в пораженных тканях, влияет на систему эндогенных интерферонов и связанных с ними цитокинов, индуцирует образование эндогенных «ранних» интерферонов (ИФН α/β) и интерферона гамма (ИФН-у).
Экспериментально и клинически установлена эффективность в отношении вирусов гриппа (в том числе гриппа птиц), парагриппа, вирусов простого герпеса 1 и 2 типов (лабиальный герпес, генитальный герпес), других вирусов герпеса (ветряная оспа, инфекционный мононуклеоз), энтеровирусов, клещевого вируса энцефалит, ротавирус, коронавирус, калицивирус, аденовирус, респираторно-синцитиальный (РС-вирус). Препарат снижает концентрацию вируса в пораженных тканях, влияет на систему эндогенных интерферонов и связанных с ними цитокинов, индуцирует образование эндогенных «ранних» интерферонов (ИФН α/β) и интерферона гамма (ИФН-у).
Стимулирует гуморальный и клеточный иммунный ответ. Повышает продукцию антител (в т.ч. секреторного IgA), активирует функции Т-эффекторов, Т-хелперов (Тх), нормализует их соотношение. Повышает функциональный резерв Th и других клеток, участвующих в иммунном ответе. Является индуктором смешанного Txl и Th3-типа иммунного ответа: увеличивает продукцию цитокинов Txl (ИФН?, ИЛ-2) и Th3 (ИЛ-4, 10), нормализует (модулирует) баланс Th2/Th3 виды деятельности. Повышает функциональную активность фагоцитов и натуральных клеток-киллеров (ЕК-клеток).Обладает антимутагенными свойствами.
Повышает функциональную активность фагоцитов и натуральных клеток-киллеров (ЕК-клеток).Обладает антимутагенными свойствами.
Показания к применению
Профилактика и лечение острых респираторных вирусных инфекций (включая грипп).
Комплексная терапия инфекций, вызванных вирусами герпеса (инфекционный мононуклеоз, ветряная оспа, лабиальный герпес, генитальный герпес).
Комплексная терапия и профилактика рецидивов хронической герпесвирусной инфекции, в том числе лабиального и генитального герпеса.
Комплексная терапия и профилактика других острых и хронических вирусных инфекций, вызванных вирусом клещевого энцефалита, энтеровирусом, ротавирусом, коронавирусом, калицивирусом.
Применение в комплексной терапии бактериальных инфекций Комплексная терапия вторичных иммунодефицитных состояний различной этиологии, в том числе профилактика и лечение осложнений вирусных и бактериальных инфекций.
Противопоказания
Повышенная индивидуальная чувствительность к компонентам препарата. Детям и лицам до 18 лет показано применение препарата Анаферон детский.
Детям и лицам до 18 лет показано применение препарата Анаферон детский.
Беременность и лактация
Безопасность применения Анаферона беременными и в период лактации не изучалась.При необходимости приема препарата следует учитывать соотношение риск/польза.
Способ применения и дозировка
Внутри. За один раз — 1 таблетка (держать во рту до полного растворения — не во время еды).
ОРВИ, грипп, кишечные инфекции, герпесвирусные инфекции, нейроинфекции. Лечение следует начинать как можно раньше – при появлении первых признаков острой вирусной инфекции по следующей схеме: в первые 2 часа препарат принимают каждые 30 минут, затем в течение первых суток принимают еще 3 дозы в регулярные отрезки.Со второго дня принимать по 1 таблетке 3 раза в день до полного выздоровления. При отсутствии улучшения на третий день лечения препаратом при ОРВИ и гриппе следует обратиться к врачу. В эпидемический сезон с профилактической целью препарат принимают ежедневно 1 раз в сутки в течение 1-3 мес.
Генитальный герпес. При острых проявлениях генитального герпеса препарат принимают через равные промежутки времени по следующей схеме: 1-3 день — по 1 таблетке 8 раз в день, затем по 1 таблетке 4 раза в день в течение не менее 3 недель.Для профилактики рецидивов хронической герпесвирусной инфекции — по 1 таблетке в сутки. Рекомендуемая продолжительность профилактического курса определяется индивидуально и может составлять до 6 мес.
При применении препарата для лечения и профилактики иммунодефицитных состояний, в комплексной терапии бактериальных инфекций — по 1 таблетке в сутки.
При необходимости препарат можно комбинировать с другими противовирусными и симптоматическими средствами.
Побочный эффект
При применении препарата по указанным показаниям и в указанных дозировках побочных эффектов не выявлено.
Возможны проявления повышенной индивидуальной чувствительности к компонентам препарата.
Передозировка
Случаев передозировки пока не зарегистрировано. При случайной передозировке возможны диспептические явления из-за входящих в состав препарата наполнителей.
При случайной передозировке возможны диспептические явления из-за входящих в состав препарата наполнителей.
Взаимодействие с другими лекарственными средствами
На сегодняшний день случаев несовместимости с другими препаратами не выявлено.
При необходимости препарат можно комбинировать с другими противовирусными, антибактериальными и симптоматическими средствами.
специальные инструкции
Препарат содержит лактозу, в связи с чем его не рекомендуется назначать пациентам с врожденной галактоземией, синдромом мальабсорбции глюкозы или врожденной лактазной недостаточностью.
Форма выпуска
Леденцы. По 20 таблеток в блистере из поливинилхлоридной пленки и алюминиевой фольги. Каждый блистер вместе с инструкцией по медицинскому применению помещен в картонную пачку.
Условия хранения
В сухом, защищенном от света месте при температуре не выше 25°С.Хранить в недоступном для детей месте.
Срок годности
3 года.
Не использовать после истечения срока годности.
Условия отпуска из аптек
Без рецепта.
инструкция по применению, цена, отзывы, аналоги таблеток Анаферон
Таблетки Анаферон для взрослых относятся к группе гомеопатических средств, обладающих иммуномодулирующим действием и выраженным противовирусным действием. С помощью активации определенных звеньев иммунной системы человека происходит естественное образование гамма — интерферона, стимулирующего работу иммунитета, направленную на борьбу с инфекцией вирусной природы.Это свойство препарата способствует быстрому купированию симптомов простуды, избавлению от заложенности носа, кашля, болей в горле, слезотечения и ринита. При попадании на слизистые оболочки полости рта Анаферон проявляет выраженное противовирусное действие. Параллельно снижается вероятность присоединения бактериальной инфекции, а также возникновения суперинфекции. Обычно при сочетании препарата Анаферон с другими противовоспалительными или жаропонижающими средствами их дозу уменьшают. Доказана эффективность Анаферона при лечении и профилактике различных заболеваний органов дыхания. Чаще всего препарат назначают против вирусов герпеса, гриппа, энтеровирусов. Средство активно в отношении вирусов клещевого энцефалита и коронавируса, а также вируса птичьего гриппа.
Доказана эффективность Анаферона при лечении и профилактике различных заболеваний органов дыхания. Чаще всего препарат назначают против вирусов герпеса, гриппа, энтеровирусов. Средство активно в отношении вирусов клещевого энцефалита и коронавируса, а также вируса птичьего гриппа.
Форма выпуска и состав
Анаферон выпускается в форме таблеток. Блистер содержит 20 таблеток. Упакован в индивидуальную картонную упаковку, содержащую данные о серии и сроке годности.Помимо блистера в упаковке есть инструкция с описанием препарата. Используйте средство путем медленного рассасывания в полости рта.
Таблетки Анаферонсодержат очищенные гамма-антитела к интерферону организма человека в виде водно-спиртовой смеси, содержащей активные вещества. В качестве дополнительных веществ также включены стеарат магния, лактоза и микрокристаллическая целлюлоза.
Показания к применению
Анаферон показан при следующих заболеваниях:
Противопоказания
Для лечения детей в возрасте до 18 лет применяют Анаферон детский. Анаферон для взрослых разрешен к применению лицам, достигшим указанного возраста.Основным противопоказанием является имеющаяся повышенная чувствительность к какому-либо компоненту препарата или дополнительному веществу, указанному в инструкции. В период грудного вскармливания или лактации требуется разрешение лечащего врача.
Дозирование и введение
Взрослым препарат следует применять путем длительного рассасывания в полости рта строго между приемами пищи. Держите таблетку во рту до растворения. Схема лечения при заболеваниях разной этиологии отличается. Неизменной остается только дозировка препарата – 1 таблетка под язык.
Неизменной остается только дозировка препарата – 1 таблетка под язык.
При лечении ОРВИ, нейроинфекций, кишечных заболеваний, спровоцированных вирусами, при гриппе лечение следует начинать как можно раньше. В первые 2 часа нужно применять Анаферон каждые полчаса. После этого в течение первых дней болезни проводят еще 3 приема препарата примерно через такие же промежутки времени. Со второго дня до полного выздоровления рекомендуется принимать по 1 таблетке под язык 3 раза в день. Если видимый эффект не наступает через 3 дня применения по схеме, следует немедленно обратиться к врачу для уточнения диагноза.Профилактику вышеперечисленных заболеваний можно проводить в течение 3 месяцев в неблагоприятный эпидемиологический период. С целью профилактики прием снижают до 1 таблетки в сутки. Минимальная ставка 30 дней. После курса лечения Анафероном следующее его назначение допускается не ранее, чем через 1 мес.
Лечение генитального герпеса осуществляется по другой схеме. При его обострении в первые 3 дня следует принимать 8 раз в день по 1 таблетке под язык. Дальнейший курс не должен быть менее 3 недель.В этот период необходимая дозировка составляет 1 таблетка 4 раза в течение 24 часов.
Дальнейший курс не должен быть менее 3 недель.В этот период необходимая дозировка составляет 1 таблетка 4 раза в течение 24 часов.
При необходимости профилактики возможных обострений герпетических заболеваний Анферон принимают 1 раз в сутки по 1 таблетке. Длительность терапии определяет врач. Иногда профилактический курс занимает около полугода.
Профилактику и терапию иммунодефицитных состояний проводят по схеме 1 доза в сутки однократно. Длительность курса определяет врач.
Для экстренной профилактики, например, после укуса клеща, следует пройти курс препарата Анаферон продолжительностью 21 день. Необходимая дозировка – по 1 таблетке трижды в сутки.
При необходимости возможен совместный прием с другими симптоматическими или противовирусными препаратами.
Побочные эффекты
Продукт считается безопасным; возможны редкие реакции индивидуального характера в виде повышенной чувствительности к компонентам. Возможно развитие диспепсических осложнений на фоне увеличения рекомендованной в инструкции дозировки. Небольшой слабительный эффект обусловлен наличием в составе таблеток дополнительных компонентов.
Небольшой слабительный эффект обусловлен наличием в составе таблеток дополнительных компонентов.
специальные инструкции
При наличии у больного врожденной галактоземии Анаферон лучше не применять. Ограничения применения также распространяются на людей с недостаточной усвояемостью лактазы, галактозы или глюкозы, синдромом мальабсорбции. Информация о безопасности Анаферона у кормящих матерей и женщин, вынашивающих ребенка, отсутствует. Данным группам лиц разрешено применять препарат только в медицинских целях.
Несовместимость компонентов препарата с другими средствами отсутствует, поэтому допускается параллельное применение Анаферона с другими препаратами.
Анаферон не влияет на концентрацию. Ограничений по вождению нет.
Условия хранения
Анаферон следует хранить в темном и сухом месте, желательно в оригинальной упаковке, в недоступном для детей месте. Подходящий температурный режим не может превышать 25 градусов Цельсия. Хранение Анаферона разрешено в течение 3 лет. Праздники без рецепта.
Праздники без рецепта.
Аналоги Анаферона
Анаферон – гомеопатический препарат. На фармацевтическом рынке представлен огромный ассортимент других препаратов, обладающих противовирусным действием. Наиболее известны и эффективны Кагоцел, Арбидол и Афлубин. Состав этих препаратов не идентичен. Назначение подходящего метода лечения находится в компетенции врача.
Цены Анаферон Взрослый
Анаферон пастилки, 20 шт.- от 185 руб.
Оцените Анаферон по 5-бальной шкале:
Антибиотик для лечения бактериальных инфекций
Азифар: антибиотик для лечения бактериальных инфекций
Производитель
Мекофар.
Ингредиент
Каждая упаковка: азитромицина дигидрат, эквивалентный азитромицину 100 мг или 200 мг.
Описание
Aziphar 100: порошок цвета или цвета слоновой кости, фруктовый аромат, сладкий вкус.
Фармакодинамический
Фармакотерапевтическая группа: Системные антибиотики.
Код УВД: J01FA10
Азитромицин — новый антибиотик широкого спектра действия из группы макролидов, известный как азалид. Препарат оказывает сильное бактерицидное действие за счет связывания с рибосомами болезнетворных бактерий, препятствуя синтезу ими белка.
Азитромицин хорошо действует на грамположительные бактерии, такие как стрептококки, пневмококки, золотистый стафилококк, коринебактерии дифтерии, клостридии перфрингенс; Грамотрицательные бактерии, такие как Haemophilus influenza, Moraxella catarrhalis, Neisseria gonorrhoeae, Acinetobacter, Yersinia, Legionella… Кроме того, этот антибиотик также эффективен против Listeria monocytogenes, Mycobacterium avium, Mycoplasma pneumonia и hominins, Toxoplasma Gondi, Chlamydia trachomatis,…
Фармакокинетика
После приема внутрь азитромицин широко распределяется в организме, биодоступность составляет около 40%. После приема пиковые концентрации в плазме достигаются в течение 2-3 часов. Препарат распределяется преимущественно в тканях: легкие, миндалины, предстательная железа, гранулоциты, макрофаги. .. намного выше в крови.
.. намного выше в крови.
Небольшое количество азитромицина деметилируется в печени и выводится с желчью в неизмененном виде и частично в виде метаболитов. Приблизительно 6% пероральной дозы выводится с мочой в течение 72 часов в неизмененном виде.
Дозировка и введение
Хорошо встряхнуть перед использованием.
Принимать 1 раз в день за 1 час до еды или через 2 часа после еды.
Формат упаковки:
Положите порошок в стакан с водой, хорошо перемешайте и выпейте.
Формат бутылки:
Аккуратно постучите по флакону, чтобы растворить порошок. Снимите крышку бутылки.
Добавляйте питьевую воду медленно, пока объем не станет ниже отметки (обычный объем для бутылки 15 г составляет 15 мл; для бутылки 22,5 г составляет 22,5 мл), закройте бутылку и хорошо встряхните. Добавьте воды до указанного объема. потрясен. Объем препарата во флаконе достиг установленной отметки, а содержание азитромицина составило 200 мг/5 мл. Используйте воду комнатной температуры. Не используйте горячую или теплую воду.
Используйте воду комнатной температуры. Не используйте горячую или теплую воду.
Хранить суспензию после восстановления при температуре ниже 30°C.Не храните в холодильнике, так как это может усилить горький вкус лекарства.
После разведения суспензию можно использовать в течение 10 дней.
Дозировка: По назначению врача.
Рекомендуемая доза:
Дети: 10 мг/кг в первый день, затем 5 мг/кг/день со 2-го по 5-й день или 10 мг/кг/день в течение 3 дней.
Взрослые и дети > 45 кг: в первый день принимают в дозе 500 мг, следующие 4 дня принимают однократно в дозе 250 мг/сут или 500 мг/сут, применяют в течение 3 дней.
Взрослые лечат заболевания, передающиеся половым путем, такие как цервицит, уретрит, вызванные инфекцией Chlamydia trachomatis, однократной дозой 1 г.
Пожилые люди: доза равна дозе для молодых людей.
Осторожно
Соответствующая коррекция дозы азитромицина требуется для пациентов с почечной недостаточностью и клиренсом креатинина менее 40 мл/мин.
Не используйте это лекарство у людей с заболеваниями печени, поскольку азитромицин выводится в основном печенью.
Следует соблюдать осторожность при использовании азитромицина и других макролидов, поскольку возможность аллергических реакций, таких как ангионевротический отек и анафилаксия, очень опасна (хотя и редко).
Как и при применении других антибиотиков, при применении препарата следует наблюдать за признаками суперинфекции нечувствительными к препарату бактериями, в том числе грибками.
Соблюдайте осторожность при управлении автомобилем или работе с механизмами, поскольку препарат может вызвать головокружение, сонливость.
Передозировка
Нет данных о передозировке азитромицина.Типичными симптомами передозировки макролидными антибиотиками являются: потеря слуха, тошнота, рвота и диарея.
Лечение: при появлении симптомов передозировки следует немедленно обратиться в ближайшее медицинское учреждение, чтобы медицинский персонал мог подобрать соответствующие методы лечения, такие как промывание желудка и поддерживающая терапия.
Активно следите за своевременными мерами по исправлению положения.
Противопоказания
Не применять пациентам с повышенной чувствительностью к азитромицину или антибиотикам группы макролидов или другим компонентам препарата.
Применение у беременных и кормящих женщин
Беременность и лактация: применять только при отсутствии других подходящих препаратов.
Интерактивный
Поскольку пища снижает биодоступность препарата до 50%, азитромицин следует принимать только за 1 час до или через 2 часа после еды.
Не используйте азитромицин одновременно с производными спорыньи из-за потенциальной токсичности.
Азитромицин следует принимать не менее чем за 1 час до или через 2 часа после приема антацидов.
При одновременном применении азитромицина с циклоспорином или дигоксином следует контролировать концентрации циклоспорина или дигоксина и соответствующим образом корректировать дозу.
Фармакокинетические исследования на здоровых добровольцах не выявили значительных эффектов при одновременном применении азитромицина с карбамазепином или метилпреднизолоном.
На фармакокинетику азитромицина не влияет однократный прием циметидина за 2 часа до введения азитромицина.
Никакого влияния на фармакокинетику азитромицина и теофиллина не наблюдалось при одновременном применении азитромицина и теофиллина у здоровых добровольцев, но при одновременном применении этих двух препаратов необходимо контролировать концентрацию теофиллина.
Азитромицин не влиял на антикоагулянтный эффект в фармакокинетических исследованиях у здоровых добровольцев, получавших однократную дозу варфарина 15 мг. Эти два препарата можно применять одновременно, но время свертывания крови у пациента все же следует контролировать.
Несовместимость
Поскольку исследования несовместимости не проводились, этот препарат нельзя смешивать с другими препаратами.
Побочные реакции на лекарства (НЛР)
Часто
Желудочно-кишечный тракт: тошнота, рвота, боль в животе, диарея.
Слух: обратимая тугоухость при длительном применении высоких доз.
Реже
Все тело: утомляемость, головная боль, головокружение, сонливость и т. д.
Пищеварение: метеоризм, диспепсия, снижение аппетита.
Кожа: сыпь, зуд.
Другие эффекты: вагинит, цервицит,…
Редко
Тело в целом: анафилактическая реакция.
Кожа: ангионевротический отек.
Печень: повышенные трансаминазы.
Кровь: транзиторная нейтропения.
Консервация
Хранить в сухом, защищенном от света месте при температуре не выше 30°С.
Внешний вид и упаковка
Порошок для пероральной суспензии 100 мг: коробка из 10 упаковок по 2 штуки.5г; 200мг: коробка 12 упаковок по 5г, коробка 1 флакон 15г, коробка 1 флакон 22,5г.
Ртутная фармацевтическая корпорация
Следующие положения и условия применяются к покупке продуктов у Mercury Drug через онлайн-сервис заказа на ее веб-сайте.
Согласие/соглашение о конфиденциальности данных
Получая доступ к онлайн-заказу и используя его, вы принимаете и соглашаетесь соблюдать положения и условия Политики конфиденциальности данных компании Mercury Drug в целях использования ее услуг, администрирования вашей учетной записи, обработки любых транзакций с использованием вашей онлайн-учетной записи, и для других разумных целей, связанных с вашей онлайн-учетной записью.
Размещение заказа
Вы должны предоставить всю запрашиваемую информацию для обработки вашего заказа. Компания Mercury Drug оставляет за собой право в любое время запросить у вас дополнительную информацию, чтобы мы могли выполнить ваш заказ и/или выполнить требования государственных нормативных актов. Прием заказа осуществляется при наличии заказанного товара. Также в каждой аптеке «Меркурий» ассортимент продукции может различаться. Размещая заказ, вы подтверждаете, что данные, указанные вами на странице заказа, являются верными и правильными во всех отношениях.Система отобразит страницу подтверждения, подтверждающую успешное получение вашего заказа.
Подтверждение вашего заказа
После того, как мы получим ваш заказ, вы получите электронное письмо с информацией о стоимости заказанных вами продуктов. После того, как вы подтвердите свой заказ, вы получите еще одно электронное письмо, в котором будут содержаться инструкции о том, как заявить права на приобретенный товар в выбранном вами аптеке Mercury.
Цены на продукты
Цены на товары указаны в филиппинских песо по их обычной цене, включая налог на добавленную стоимость (НДС).Ценовые котировки могут быть изменены в любое время без предварительного уведомления.
В случае скидок, будь то рекламные или санкционированные государством, применимая скидка будет рассчитана во время обслуживания заказа при условии предоставления необходимых документов и удостоверения личности в обслуживающем магазине. Все заработанные скидки будут зачислены на ваш личный счет и будут зачислены при следующей покупке.
Условия оплаты
Оплата вашего заказа должна быть произведена с помощью онлайн-способа оплаты.С вас будет взиматься плата на основе обычной цены приобретенных продуктов, включая налог на добавленную стоимость (НДС), как указано в ценовом предложении. Мы управляем вашими данными с помощью безопасного способа оплаты, чтобы защитить вас от мошенничества.
Подача вашего заказа
Все транзакции, совершенные с помощью этого онлайн-сервиса, должны обрабатываться в соответствии со стандартным филиппинским временем.
Товар(ы), приобретенные в Интернете, должны быть востребованы или поданы только в аптеке Mercury, которую вы выбрали в форме заказа, строго в пользу назначенного вами получателя после того, как вы получите электронное письмо с подтверждением того, что ваши приобретенные продукты готовы к отправке. поднимать.
Оформление заказов осуществляется в соответствии с обычными часами работы действующей аптеки Mercury, сведения о которых должны быть предоставлены в электронном письме, подтверждающем наличие ваших продуктов, или которые вы можете проверить на нашем веб-сайте www.mercurydrug.com. .
Назначение вашего получателя, уполномоченного получать/заявлять права на продукты, приобретенные через Интернет, остается в силе и действует до тех пор, пока оно не будет отозвано или аннулировано раньше, и до тех пор, пока компания Mercury Drug не будет должным образом уведомлена в письменной форме или по электронной почте об отзыве, отмене или изменении получателя до доставка/выдача купленных товаров. Любое уведомление об отзыве, аннулировании или изменении получателя требует времени обработки не менее 24 часов с момента получения уведомления компанией Mercury Drug.
Любое уведомление об отзыве, аннулировании или изменении получателя требует времени обработки не менее 24 часов с момента получения уведомления компанией Mercury Drug.
При запросе продукта(ов) назначенный вами получатель должен предъявить хотя бы одно действительное удостоверение личности. как удостоверение личности. Настоящим понимается, что указание вами получателя также дает ему/ей право назначать или назначать своего представителя в случае, если он/она не может лично заявить права на товар/продукты. В таком случае назначенный вами получатель должен оформить доверенность в пользу своего представителя, которую необходимо предъявить при получении товара/продуктов.Ваш назначенный получатель или его/ее представитель, в зависимости от обстоятельств, должны подписать форму приемки, подтверждающую получение продукта/ов от вашего имени. Квитанция об операции выдается при подаче/выдаче продукции.
В отношении лекарств, отпускаемых по рецепту, и транзакций, касающихся пожилых людей или лиц с ограниченными возможностями (PWD), назначенный вами получатель или его/ее представитель должен предъявить действительный рецепт врача и другие требования, установленные государством, во время подачи заявки на продукт(ы). Mercury Drug оставляет за собой право приостановить выпуск любого продукта или отказать в предоставлении любой скидки в случае, если назначенный вами получатель или его/ее представитель не соблюдает вышеуказанные требования.
Mercury Drug оставляет за собой право приостановить выпуск любого продукта или отказать в предоставлении любой скидки в случае, если назначенный вами получатель или его/ее представитель не соблюдает вышеуказанные требования.
Все подтвержденные заказы должны быть запрошены назначенным получателем или его/ее представителем в течение 7 дней с даты уведомления о наличии вашего заказа.
Отмена заказа
Любая отмена заказа должна быть произведена в течение 24 часов после подтверждения вашего заказа, но до того, как товар/ы будут доставлены/выданы назначенному вами получателю или его/ее представителю.Mercury Drug оставляет за собой право отклонить любой запрос на отмену, сделанный после указанного периода. Все запросы на аннулирование и отмену списаний с кредитной карты должны быть представлены компанией Mercury Drug в банк-эмитент для обработки и утверждения в соответствии с банковскими правилами и положениями.
Несмотря на вышеизложенное, Mercury Drug оставляет за собой право отменить любую транзакцию на законных и обоснованных основаниях.
Отказ от ответственности и возмещение ущерба
Используя средство онлайн-заказа Mercury Drug, вы соглашаетесь возместить убытки и ограждать компанию Mercury Drug, ее директоров, должностных лиц, сотрудников, аффилированных лиц, агентов, подрядчиков и лицензиаров (совместно именуемые MDC) от любых без исключения обязательств, убытков и убытки в случае сбоя системы онлайн-заказа по причинам, не зависящим от компании Mercury Drug, таким как, помимо прочего, форс-мажор и/или случайное событие, или которые могут возникнуть в результате того, что вы не уведомили компанию Mercury Drug своевременно об отзыве, отмене или изменении получателя.
Общий
Настоящие Положения и условия использования представляют собой полное соглашение между вами и Mercury Drug и регулируют использование вами онлайн-сервиса заказов Mercury Drug. Настоящее соглашение регулируется законами Республики Филиппины.
Размещая заказ онлайн, вы подтверждаете, что прочитали и поняли все положения и условия, изложенные в настоящем документе, и добровольно соглашаетесь соблюдать все применимые законы, уставы и правила.

 Часто и тщательно нужно мыть руки, и обязательно научить ребенка этому.
Часто и тщательно нужно мыть руки, и обязательно научить ребенка этому. раствор и т.д.).
раствор и т.д.). 
 4
%
1 0 объект
>
эндообъект
11 0 объект /Создатель (Спрингер)
/Заголовок (Рецидивирующие заболевания нижних дыхательных путей у детей раннего возраста в сельской местности Кыргызстана: чрезмерное использование антибиотиков и возможная неправильная диагностика астмы.Качественное исследование FRESH AIR)
/CrossMarkDomains#5B2#5D (springerlink.com)
/Ключевые слова ()
/CrossMarkDomains#5B1#5D (springer.com)
/ModDate (D:20180628102015+02’00’)
/Тема (npj Primary Care Respiratory Medicine, doi:10.1038/s41533-018-0081-y)
/ doi (10.1038/s41533-018-0081-y)
/Автор
/CreationDate (D:20180626170531+05’30’)
>>
эндообъект
2 0 объект
>
эндообъект
3 0 объект
>
эндообъект
4 0 объект
>
эндообъект
5 0 объект
>
эндообъект
6 0 объект
>
/Шрифт >
>>
/DA (/Helv 0 Tf 0 г )
>>
эндообъект
7 0 объект
>
>>
эндообъект
8 0 объект
>
>>
эндообъект
9 0 объект
>
ручей
приложение/pdfdoi:10.1038/s41533-018-0081-y
4
%
1 0 объект
>
эндообъект
11 0 объект /Создатель (Спрингер)
/Заголовок (Рецидивирующие заболевания нижних дыхательных путей у детей раннего возраста в сельской местности Кыргызстана: чрезмерное использование антибиотиков и возможная неправильная диагностика астмы.Качественное исследование FRESH AIR)
/CrossMarkDomains#5B2#5D (springerlink.com)
/Ключевые слова ()
/CrossMarkDomains#5B1#5D (springer.com)
/ModDate (D:20180628102015+02’00’)
/Тема (npj Primary Care Respiratory Medicine, doi:10.1038/s41533-018-0081-y)
/ doi (10.1038/s41533-018-0081-y)
/Автор
/CreationDate (D:20180626170531+05’30’)
>>
эндообъект
2 0 объект
>
эндообъект
3 0 объект
>
эндообъект
4 0 объект
>
эндообъект
5 0 объект
>
эндообъект
6 0 объект
>
/Шрифт >
>>
/DA (/Helv 0 Tf 0 г )
>>
эндообъект
7 0 объект
>
>>
эндообъект
8 0 объект
>
>>
эндообъект
9 0 объект
>
ручей
приложение/pdfdoi:10.1038/s41533-018-0081-y Качественное исследование FRESH AIR
Качественное исследование FRESH AIR adobe.com/xap/1.0/mm/xmpMMXMP Media Management Schema
adobe.com/xap/1.0/mm/xmpMMXMP Media Management Schema MajorVersionDateText
MajorVersionDateText Если в качестве требуемого dc:identifier используется альтернативный уникальный идентификатор, то DOI следует указывать как голый идентификатор только в пределах prism:doi.
Если необходимо указать URL-адрес, связанный с DOI, то prism:url можно использовать вместе с prism:doi для предоставления конечной точки службы (т. е. URL-адреса).
доитекст
Если в качестве требуемого dc:identifier используется альтернативный уникальный идентификатор, то DOI следует указывать как голый идентификатор только в пределах prism:doi.
Если необходимо указать URL-адрес, связанный с DOI, то prism:url можно использовать вместе с prism:doi для предоставления конечной точки службы (т. е. URL-адреса).
доитекст Примечание. Название публикации можно использовать, чтобы различать печатный журнал и онлайн-версию, если названия различаются, например «magazine» и «magazine.com».
публикацияNameText
Примечание. Название публикации можно использовать, чтобы различать печатный журнал и онлайн-версию, если названия различаются, например «magazine» и «magazine.com».
публикацияNameText ORCID — это постоянный идентификатор (непатентованный буквенно-цифровой код), позволяющий однозначно идентифицировать научных и других академических авторов. authorInfoBag AuthorInformation
ORCID — это постоянный идентификатор (непатентованный буквенно-цифровой код), позволяющий однозначно идентифицировать научных и других академических авторов. authorInfoBag AuthorInformation Часто назначение Анаферона требуется при генитальном герпесе, инфекционном мононуклеозе, аденовирусе, ветряной оспе;
Часто назначение Анаферона требуется при генитальном герпесе, инфекционном мононуклеозе, аденовирусе, ветряной оспе;