Стеркобилин качеств. проба (кал) > Качественное определение стеркобилина в кале > MedElement
Стеркобилин качеств. проба (кал) > Качественное определение стеркобилина в кале > MedElementТакже: Качественное определение стеркобилина в кале
Категория: Стеркобилин (кал)
Единица измерения: .
Краткое описание
- Версия для печати
В норме стеркобилин присутствует в кале. Нарушение поступления билирубина в кишечник при заболеваниях печени или механическом препятствии оттоку желчи в результате закупорки или сдавления общего желчного протока приводит к снижению или полному отсутствию стеркобилина в кале, что отражается на окраске испражнений. Полное отсутствие стеркобилина можно установить только при химическом исследовании.
Подробное описание
Унифицированный метод с двухлористой ртутью (проба Шмидта).
В результате реакции стеркобилина с двухлористой ртутью образуется соединение, имеющее розовое окрашивание. Применяются следующие реактивы: раствор двухлористой ртути (HgCl2 — хлорид ртути, сумма), 70 г/л раствора.Растворяют при кипячении, после охлаждения фильтруют.
Комочек кала величиной с лесной орех растирают в фарфоровой чашечке или пробирке с 3—4 мл раствора двухлористой ртути, закрывают крышкой или пробкой и оставляют при комнатной температуре в вытяжном шкафу на сутки. Контрольную пробу ставят так же, как опытную, но вместо двухлористой ртути берут воду.
 Оценку результатов можно провести немедленно, если подогревать пробирки с опытной и контрольными пробами на пламени горелки. При наличии билирубина образуется зеленое окрашивание. В норме реакция положительная.
Оценку результатов можно провести немедленно, если подогревать пробирки с опытной и контрольными пробами на пламени горелки. При наличии билирубина образуется зеленое окрашивание. В норме реакция положительная.Метод с применением треххлористого железа.
Необходимые реактивы
1. Реактив Фуше — раствор треххлористого железа (FeCl3) 1 : 5 мл воды.
2. Концентрированная соляная кислота.
В стеклянный сосуд помещают 1 г фекальных масс, хорошо смешанных с 10 мл дистиллированной воды. Затем 5 мл из этой эмульсии фекальных масс смешивают с 5 мл концентрированной соляной кислоты и нагревают в течение 5 мин до 50 °С. После охлаждения под водопроводом к этой смеси добавляют 2—3 капли треххлористого железа. Реакция может регистрироваться немедленно — в присутствии стеркобилина появляется красная окраска.
Метод с применением ацетата цинка.
Необходимый реактив: Насыщенный раствор ацетата цинка (10 г ацетата цинка в 100 мл этилового спирта).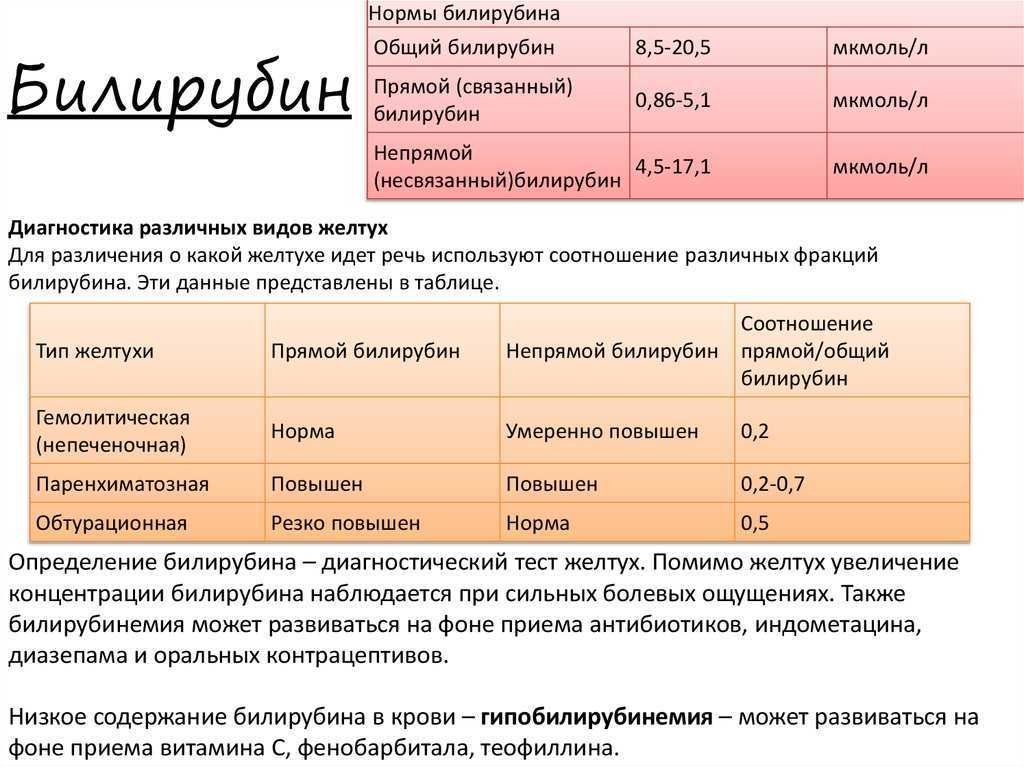
В пробирке смешивают до полной однородности 2—3 г фекальных масс и 100 мл насыщенного спиртового раствора ацетата цинка. В эту смесь добавляют 2—4 капли спиртового раствора йода и затем смесь фильтруют. Спустя 24 ч реакция регистрируется: в присутствии желчных пигментов фильтрат приобретает зеленую окраску.
Разделы Закрыть список разделов
На главную- Краткое описание
- Подробное описание
- Источники и литература
Набор реагентов для клинического анализа кала, Россия — ВЛ-Медиа
Набор реагентов для клинического анализа кала
Принцип реакции:
Морфологическое и химическое исследования кала дают суммарное представление о функции важнейших пищеварительных желез, оно отражает степень переваривания принятой пищи и состояние слизистой кишечного тракта.
Определение скрытой крови. В присутствии гемоглобина крови бензидин реагирует с перекисью водорода с образованием в течение первых 2 минут соединений, окрашенных в зеленый, сине-зеленый или синий цвет. Интенсивность окраски пропорциональна количеству крови в кале.
Определение стеркобилина. Стеркобилин взаимодействует с уксуснокислым цинком в присутствии раствора Люголя с образованием соединений, дающих зеленую флюоресценцию.
Определение билирубина.
Билирубин, поступающий в кишечник с желчью, под влиянием кишечной флоры восстанавливается, в результате чего образуется уробилин (стеркобилин) — нормальный пигмент кала и уробилиноген — продукт более полного восстановления.
Билирубин под действием реактива Фуше превращается в зеленый биливердин; интенсивность окраски пропорциональна количеству билирубина в кале.
Реагенты:
- Бензидин – 1 флакон (1,0 г)
- Уксусная кислота (50%) – 1 флакон (100 мл)
- Гидроперит – 1 упаковка
- Уксусная кислота (30 %) – 1 флакон (100 мл)
- Уксуснокислый цинк (10%) – 1 фл (100 мл)
- Раствор Люголя – 1 флакон (50 мл)
- Реактив Фуше — 1 флакон (100 мл)
- Раствор судана III (2%) – 1 флакон (100 мл)
- Глицерин – 1 флакон (130 г)
- Метиленовый синий (2%) – 1 флакон (20 мл)
Оборудование.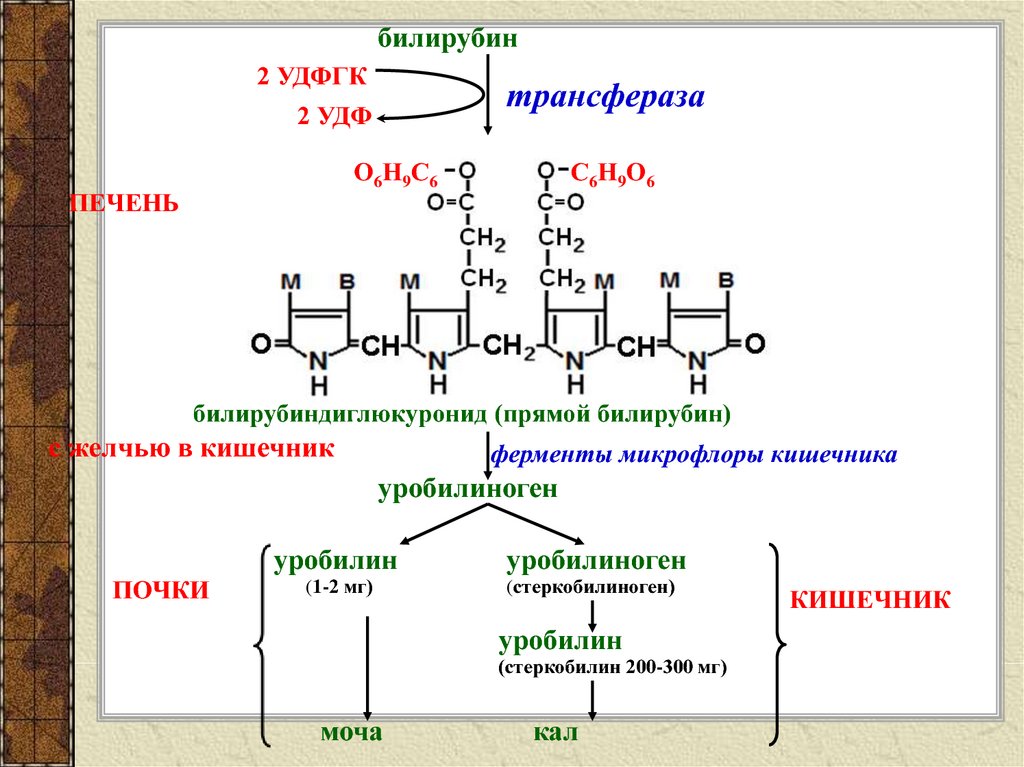
—фарфоровые ступки; -стеклянные палочки;
-чашки Петри; -воронки;
-предметные стекла; -покровные стекла;
-пробирки; -штативы;
-горелка; -весы;
-микроскоп; -бумага фильтровальная;
-перчатки резиновые.
Приготовление нативных препаратов.
Кусочек кала величиной с лесной орех помещают в ступку, добавляют немного водопроводной воды и растирают до консистенции жидкой кашицы. Капли приготовленной эмульсии стеклянной палочкой наносят на предметные стекла и готовят не менее 6 препаратов: нативный, с раствором Люголя, с метиленовым синим, с суданом III, с 30% уксусной кислотой и глицерином.
Проведение определения:
- Определение скрытой крови
Приготовление 3% раствора перекиси водорода. Растворить 3 таблетки гидроперита в 50 мл дистиллированной воды. Раствор стабилен при хранении в посуде из темного стекла и температуре 2-8 С в течении 3 месяцев.
Приготовление раствора бензидина. Перед употреблением немного бензидина (~500 мг) растворяют в 5 мл 50% уксусной кислоты до полного растворения. Раствор годен к употреблению, нестойкий.
Ход определения.
Неразведенный кал наносят толстым слоем на предметное стекло, добавляют 2-3 капли раствора бензидина в уксусной кислоте и столько же перекиси водорода. Перемешивают стеклянной палочкой. Положительная реакция на кровь дает зеленое или сине-зеленое окрашивание в течение первых 2 мин. Окрашивание, наступившее позже, чем через 2 мин, не учитывают.
- Определение билирубина
Приготовление эмульсии кала: кусочек кала помещают в фарфоровую ступку и растирают в небольшом количестве дистиллированной воды или изотоническим растворе хлорида натрия.
Эмульсию кала поместить в 2 пробирки по 1-2 мл, в опытную пробирку добавить по каплям реактив Фуше (объем реактива не должен быть больше эмульсии кала). В присутствии билирубина появляется зеленое или зеленоватое окрашивание.
Сравнить опытную и контрольную окраску в проходящем свете.
- Определение стеркобилина
Приготовление эмульсии кала: кусочек кала помещают в фарфоровую ступку и растирают в небольшом количестве дистиллированной воды или изотоническим растворе хлорида натрия.
Приготовление рабочего раствора Люголя. Разбавить раствор Люголя дистиллированной водой в соотношении 1:1.
Эмульсию кала внести в пробирку в количестве 1-2 мл, добавить 1-2 мл раствора уксуснокислого цинка (предварительно взболтать) и 1 каплю рабочего раствора Люголя.
Полученную смесь профильтровать в стеклянную пробирку, при наличии стеркобилина (положительная реакция) раствор дает зеленую флюоросценцию, видную на темном фоне.
- Исследование нативного препарата.
При микроскопическом исследование нативного препарата различают следующие элементы: детрит, остатки пищи, элементы слизистой оболочки кишечника, кристаллические образования, флору, мышечные волокна, нейтральный жир в виде бесцветных капель, жирные кислоты и мыла. растительную клетчатку и крахмал, микроорганизмы, яйца гельминтов, кристаллы.
- Исследование кала с суданом III
Капли нейтрального жира и капли жирных кислот окрашиваются в оранжевый цвет. Нагревание такого препарата ведет к расщеплению мыл (если они есть) и образованию капель жирных кислот, которые также окрашиваеются в оранжевый цвет.
На предметное стекло стеклянной палочкой нанести 1-2 капли эмульсии кала или жидкой каловой массы, внести в препарат 1-2 капли раствора судана III, эмульсия и реактив смешивают краем покровного стекла и рассматривают сначала под малым (8х10), а затем под большим (40х10) увеличением.
- Исследование кала с метиленовым синим
Для получения 0,5% раствора метиленового синего, перед использованием, 2% раствор метиленового синего разбавить дистиллированной водой в соотношении 1:3.
При обнаружении жира в виде капель микроскопируют препарат с метиленовым синим, капли нейтрального жира бесцветны, капли жирных кислот окрашены в голубой или синий цвет.
На предметное стекло стеклянной палочкой нанести 1-2 капли эмульсии кала или жидкой каловой массы, внести в препарат 1-2 капли раствора метиленового синего (0,5%), эмульсия и реактив смешивают краем покровного стекла и рассматривают сначала под малым (8х10), а затем под большим (40х10) увеличением.
- Исследование кала с глицерином
Глицерин очищает от бактерий и калового дейтрита яйца гельминтов, «просветляет» препарат и помогает установить принадлежность обнаруженных яиц. При обнаружении яиц гельминтов необходимо провести специальное исследование по Като.
На предметное стекло стеклянной палочкой нанести 1-2 капли эмульсии кала или жидкой каловой массы, внести в препарат 1-2 капли глицерина, эмульсия и глицерин смешивают краем покровного стекла и рассматривают сначала под малым (8х10), а затем под большим (40х10) увеличением.
- Исследование кала с нагреванием.
Дифференцирует жирные кислоты от мыл. При обнаружении глыбок и игл нативный препарат подогревают (не доводя до кипения) и тотчас микроскопируют. Образование капель после нагревания указывает на наличие жирных кислот, при остывании препарата капли вновь превращаются в глыбки (препарат можно подогреть повторно. Если при нагревании капель не образовалось, а иглы и глыбки остаются , нагревают препарат с уксусной кислотой.
- Исследование с 30% раствором уксусной кислоты
Глыбки и кристаллы мыл сплавляются в капли после нагрева (до кипения) препарата с уксусной кислотой . Уксусная кислота расщепляет мыла и освобождает жирные кислоты, которые плавятся, образуя капли.
Уксусная кислота расщепляет мыла и освобождает жирные кислоты, которые плавятся, образуя капли.
СОЕДИНЕНИЕ ДЛЯ БОЧЕК: c05793
СОЕДИНЕНИЕ ДЛЯ БОЧКОВ: c05793
» Японская версия | Все ссылки Путь (1) ПУТЬ КЕГА (1) Химическое вещество (5) ПабХим (1) ЧЭБИ (1) 3ДМЕТ (1) ХМДБ (1) НИККАДЖИ (1) Химическая реакция (1) РЕАКЦИЯ В БОЧКЕ (1) Все базы данных (7) |
DBGET интегрированная поисковая система базы данных
Стеркобилин (SB) ИФА набор | Abbexa Ltd
- Набор для ИФА на стеркобилин (SB)
Описание Публикации и обзоры (0)
Стеркобилин (SB) ELISA Kit представляет собой набор ELISA для количественного измерения in vitro концентраций стеркобилина (SB) в сыворотке, плазме, стуле и других биологических жидкостях.
| Цель | Стеркобилин (СБ) |
| Реактивность | Общий (все виды) |
| Протестированные приложения | ИФА |
| Рекомендуемые разведения | Оптимальные разведения/концентрации должны определяться конечным пользователем. |
| Хранение | Поставляется при температуре 4 °C. После получения храните набор в соответствии с инструкциями по хранению в руководстве к набору. После получения храните набор в соответствии с инструкциями по хранению в руководстве к набору. |
| Срок действия | Срок действия данного комплекта 6 месяцев. |
| Стабильность | Стабильность набора определяется скоростью потери активности. Потери составляют менее 5% в течение срока годности при соответствующих условиях хранения. Чтобы свести к минимуму колебания производительности, необходимо строго контролировать рабочие процедуры и лабораторные условия. Также настоятельно рекомендуется, чтобы весь анализ выполнялся одним и тем же пользователем. |
| Испытательный полигон | 1,23 нг/мл — 100 нг/мл |
| Чувствительность | |
| Стандартная форма | Лиофилизированный |
| Метод обнаружения | Колориметрический |
| Тип анализа | Конкурентный |
| Данные анализа | Количественный |
| Тип образца | Сыворотка, плазма, стул и другие биологические жидкости.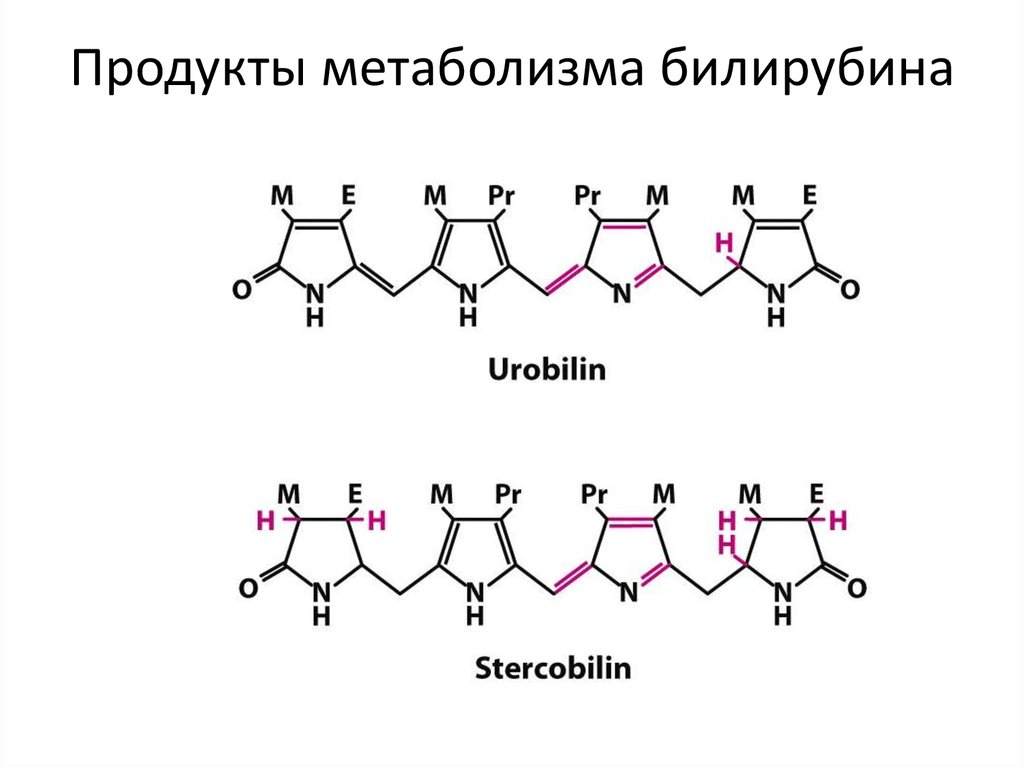 |
| Тип цели | Антиген |
| Принцип анализа | Этот набор основан на конкурентной технологии твердофазного иммуноферментного анализа. Антитело предварительно наносят на 96-луночный планшет. Стандарты, тестовые образцы и реагент, конъюгированный с биотином, добавляют в лунки и инкубируют. Реакция конкурентного ингибирования происходит между меченым биотином SB и немеченым SB на предварительно покрытом антителе. Затем добавляют реагент, конъюгированный с HRP, и весь планшет инкубируют. Несвязавшиеся конъюгаты удаляют с помощью промывочного буфера на каждом этапе. Субстрат TMB используется для количественного определения ферментативной реакции HRP. После добавления субстрата TMB только лунки, содержащие достаточное количество SB, будут давать продукт синего цвета, который затем меняется на желтый после добавления кислого стоп-раствора. Интенсивность желтого цвета обратно пропорциональна количеству SB, связанного на пластине. OD измеряют спектрофотометрически при 450 нм в ридере для микропланшетов, по которому можно рассчитать концентрацию SB. Интенсивность желтого цвета обратно пропорциональна количеству SB, связанного на пластине. OD измеряют спектрофотометрически при 450 нм в ридере для микропланшетов, по которому можно рассчитать концентрацию SB. |
| Комплект компонентов | Перечисленные компоненты комплекта приведены только для справки. Руководство по продукту может незначительно отличаться. Изделие следует использовать в соответствии с инструкциями, прилагаемыми к изделию и поставляемыми вместе с ним.
|
| Необходимый материал, но не предоставляется |
|
| Приготовление реагентов | Эта процедура предназначена только для справки. Руководство по продукту может незначительно отличаться. Изделие следует использовать в соответствии с инструкциями, прилагаемыми к изделию и поставляемыми вместе с ним.
|
| Процедура анализа | Эта процедура предназначена только для справки. Руководство по продукту может незначительно отличаться. Изделие следует использовать в соответствии с инструкциями, прилагаемыми к изделию и поставляемыми вместе с ним.
|
| Протокол | Эта процедура предназначена только для справки. Руководство по продукту может незначительно отличаться. Изделие следует использовать в соответствии с инструкциями, прилагаемыми к изделию и поставляемыми вместе с ним.
|
| Расчет результатов | Этот анализ является конкурентным, поэтому существует обратная корреляция между концентрацией SB в образце и измеренной абсорбцией. Создайте график с логарифмом стандартной концентрации (ось Y) и средней измеренной абсорбции (ось X). Примените наиболее подходящую линию тренда через стандартные точки. Концентрацию SB в образцах можно интерполировать по стандартной кривой. |
| Точность анализа | Precision Intra-assay (Прецизионность внутри анализа): 3 образца с низким, средним и высоким уровнями стеркобилина (SB) были протестированы 20 раз на одном планшете соответственно. Прецизионность между анализами (прецизионность между анализами): 3 образца с низким, средним и высоким уровнями стеркобилина (SB) были протестированы на 3 разных планшетах, по 8 повторов в каждом планшете. CV (%) = (стандартное отклонение / среднее значение) × 100 Внутри анализа: CV Между анализами: CV |
| Наличие | Отправка в течение 5-7 рабочих дней. |
| Примечание | Этот продукт предназначен только для исследовательских целей. Диапазон и чувствительность могут быть изменены. Пожалуйста, свяжитесь с нами для получения последней информации о продукте. Для получения точных результатов концентрации пробы должны быть разбавлены до средней концентрации набора. |

 198J
198J 9276 -17.1540
9276 -17.1540 
 5 ml tubes
5 ml tubes

 Рекомендуется построить стандартную кривую для каждого теста.
Рекомендуется построить стандартную кривую для каждого теста.