Анализы в KDL. Антитела к вирусу простого герпеса I, II типов (Herpes simplex virus I, II), IgM
Герпесом называют вирусное заболевание, при котором на коже и слизистых появляются болезненные элементы — везикулы. Позже на этом месте образуются корочки. Простой герпес (HSV-1) поражает в основном область рта, губы, лицо, глаза и шею, генитальный (HSV-2) вызывает поражение кожи и слизистых в области половых органов.
Герпес считается одной из самых распространенных инфекций в мире, в РФ им инфицированы более 80% населения. Однажды попав в организм, вирус сохраняется на всю жизнь: полностью избавиться от него невозможно. Здоровый иммунитет подавляет вирус и не дает инфекции рецидивировать. Герпетическая инфекция представляет угрозу для людей с ослабленным иммунитетом (например, при наличии ВИЧ-инфекции, приеме иммунодепрессантов и т. д.).
Заражение может происходить контактным (через кожу, при поцелуях и т. д.), бытовым (через предметы обихода), половым путем, воздушно-капельным и от матери плоду при беременности или во время родов.
При подозрении на первую встречу с инфекцией назначают анализ на антитела класса IgM к вирусу герпеса I и II типа.
Антитела классов IgM и IgG вырабатываются организмом в ответ на инфекцию и для борьбы с ней. Сначала появляются IgM — их можно обнаружить уже через несколько дней после заражения, они являются маркером острой инфекции и держатся в крови до нескольких недель, после чего пропадают. IgG появляются позже, спустя 2–3 недели, и сохраняются в организме в течение всей жизни.
В каких случаях обычно назначают исследовани
е- Для подтверждения диагноза при подозрении на первичное инфицирование вирусом герпеса.

- В период подготовки к беременности и во время беременности.
Что именно определяют в процессе анализа
Проводят определение концентрации антител класса IgM к вирусу герпеса I и II типа в крови методом ИФА (иммуноферментный анализ).
Что означают результаты теста
Отрицательный результат говорит об отсутствии антител класса IgM к герпесу. Положительный результат указывает на текущую инфекцию. Обычно исследуют одновременно наличие антител класса IgM и класса IgG к герпесу I и II типов.
У пациентов с другими инфекциями, вызванными вирусами группы герпеса (ветрянка, ЦМВ-инфекция и т. д.), у беременных возможно получение ложноположительного результата при определении иммуноглобулинов IgM к герпесу. Это связано с невысокой специфичностью иммуноглобулинов класса М и схожестью биологической структуры вирусов группы герпеса между собой. Поэтому результаты лабораторного теста должен оценивать врач с учетом клинических признаков и результатов других исследований.
Сроки выполнения теста
Результат исследования можно получить спустя 3–4 дня после сдачи анализа.
Подготовка к анализу
Следует придерживаться общих правил подготовки к взятию крови из вены. Кровь можно сдавать не ранее чем через 3 часа после приема пищи в течение дня или утром натощак. Чистую воду можно пить в обычном режиме.
ToRCH-комплекс (комплекс анализов «Антитела к инфекциям, беременность») (определение уровня в крови)
Для чего это нужно
Токсоплазма, краснуха, цмв, герпес 1 и 2 типов, парвовирус В19, ветряная оспа и БЕРЕМЕННОСТЬ До или на ранних сроках беременности желательно комплексное определение антител к ToRCH-инфекциям. Эти показатели входят в блок анализов ToRCH-комплекс (читается как торч-комплекс)
Значение анализов
Токсоплазма, краснуха, цмв, герпес 1 и 2 типов, парвовирус В19, ветряная оспа и БЕРЕМЕННОСТЬ
До или на ранних сроках беременности желательно комплексное определение антител к ToRCH-инфекциям. Эти показатели входят в блок анализов ToRCH-комплекс (читается как торч-комплекс).
Эти показатели входят в блок анализов ToRCH-комплекс (читается как торч-комплекс).
| Антитела класса IgG к краснухе (rubella) | Антитела класса IgG к токсоплазмам (toxoplasma) | Антитела класса IgG к ВПГ 2 типа (HSV 2) |
| Антитела класса IgM к краснухе (rubella) | Антитела класса IgM к токсоплазмам (toxoplasma) | Антитела класса IgM к ВПГ 2 типа (HSV 2) |
| Антитела класса IgG к ЦМВ (цитомегаловирусу, CMV) | Антитела класса IgG к ВПГ 1 типа (HSV 1) | Антитела класса IgG к парвовирусу В19 (В19 V) |
| Антитела класса IgM к ЦМВ (цитомегаловирусу, CMV) | Антитела класса IgM к ВПГ 1 типа (HSV 1) | Антитела класса IgM к парвовирусу В19 (В19 V) |
| Антитела класса IgG к вирусу ветряной оспы (VZV, Varicella Zoster Virus) |
| |
| Антитела класса IgM к вирусу ветряной оспы (VZV, Varicella Zoster Virus) | ||
Определяется два вида антител — IgG и IgM, по которым судят о встрече с инфекционным агентом, а также о времени этой встречи.
Варианты заключений:
- IgG положительный, IgG отрицательный, IgG слабо-положительный (анализ количественный!)
- IgM положительный, IgM отрицательный, IgM слабо-положительный (анализ количественный!)
Подробнее читайте в статье ToRCH-инфекции и беременность
Как расшифровывается ToRCH?
В 1971 году введена аббревиатура ToRCH (торч)- для объединения группы инфекций, связанных с беременностью. Понятие ToRCH-инфекций используется как собирательный термин группы инфекций, связанных с патологией во время беременности.
Toxoplasma (токсоплазмы)
Other (другие)
Rubella (краснуха)
Cytomegalovirus (цитомегаловирус, ЦМВ)
Herpes (герпес)
Другие обозначения анализов:
| Антитела класса IgG к краснухе (rubella) | Анти-rubella, anti rubella, АТ к краснухе |
| Антитела класса IgM к краснухе (rubella) | |
| Антитела класса IgG к ЦМВ (цитомегаловирусу,CMV) | Анти-ЦМВ, anti CMV, АТ к ЦМВ, к цитомегаловирусной инфекции, CMV IgG/IgM |
| Антитела класса IgM к ЦМВ (цитомегаловирусу,CMV) | |
| Антитела класса IgG к ВПГ 2 типа (HSV 2) | Анти HSV, anti HSV, антитела к герпесу |
| Антитела класса IgM к ВПГ 2 типа (HSV 2) | |
| Антитела класса IgG к ВПГ 1 типа (HSV 1) | |
| Антитела класса IgM к ВПГ 1 типа (HSV 1) | |
| Антитела класса IgG к парвовирусу В19 (ПВ В19) | Антитела к ПВ В19 |
| Антитела класса IgM к парвовирусу В19 (ПВ В19) | |
| Антитела класса IgG к токсоплазмам (toxoplasma) | Anti toxo, антитела к токсоплазме |
| Антитела класса IgM к токсоплазмам (toxoplasma) | |
| Антитела класса IgG к вирусу ветряной оспы (VZV, Varicella Zoster Virus) | Антитела к ветряной оспе
Антитела к ветрянке Антитела к опоясывающему лишаю Антитела к VZV Антитела к Varicella Zoster Virus |
- женщинам во время подготовки к беременности
- беременным на ранних сроках
- новорожденным для диагностики врожденного инфицирования
- в течение беременности сдаются те анализы, которые требуют регулярного контроля
Часто пациенты получают неопределенный результат — «серая» или «неопределенная» зона. И им рекомендуют пересдать анализ через 2 недели. Это можно себе позволить,
И им рекомендуют пересдать анализ через 2 недели. Это можно себе позволить,
если вы только готовитесь к беременности. НО: при беременности ждать нельзя! Такие анализы должны сразу пересматриваться более точными методами!
Специфические антитела класса IgM, в частности, антитела к краснухе, относятся к факторам, циркулирующим в крови экстремально низких концентрациях. Поэтому анализы не в цифрах (количественно), а в виде положительности (=реактивности) или отрицательности (=отсутствии реактивности). Отрицательный и положительный результаты отделяет друг от друга так называемый порог отсечки (cutoff). Цифры показателя выше данного порога считаются положительными, а ниже порога — отрицательными. Зона значений порог ± 10%) является „зоной неопределенности».
Для анализа антител используются два способа: подтверждающие анализы методом иммуноблот и анализ на авидность антител IgG.
Если Вы сдаете эти анализы, исчезает необходимость ЖДАТЬ 2 недели плюс дни готовности анализа.
1. ПОДТВЕРЖДАЮЩИЕ АНАЛИЗЫ на токсоплазму, краснуху, цмв методом иммуноблот:
Используются рекомбинантные антигены
- Высокочувствительный и специфичный тест!
- Чувствительность 97 %
- Специфичность 99 %
- Высокая разрешающая способность между отрицательным и положительным результатами!
- Более точное выявление срока заражения
Будьте уверены в анализе!
Зачем это нужно:
точное и своевременное выявление позволит правильно определить тактику ведения беременности нет необходимости терять время на ожидание следующего анализа.
Тактика врача определяется в каждом конкретном случае по-разному (подготовка к беременности, начало беременности, период новорожденности и т.д.)
Подробнее о методе иммуноблот
2. АВИДНОСТЬ АНТИТЕЛ IgG, индекс авидности
Определить время, когда произошло инфицирование можно и по авидности антител IgG.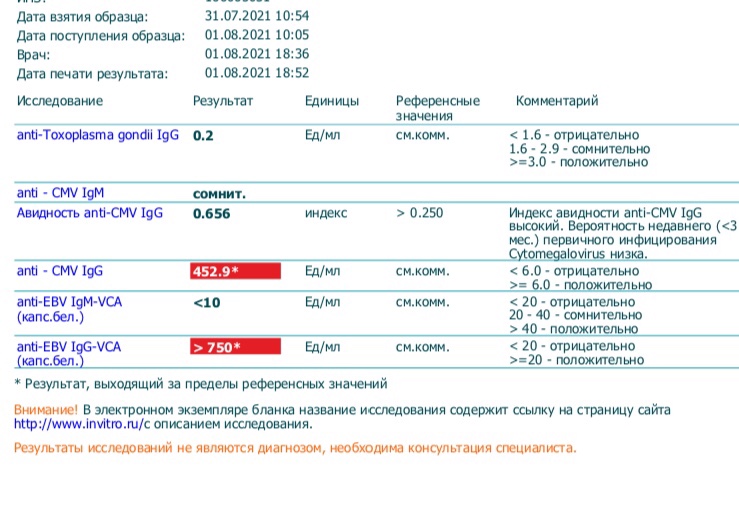 Низкоавидные антитела встречаются при острой, недавно развившейся инфекции. Высокоавидные антитела — если встреча с инфекцией состоялась давно. Определение авидности проводится для трех инфекцией:
Низкоавидные антитела встречаются при острой, недавно развившейся инфекции. Высокоавидные антитела — если встреча с инфекцией состоялась давно. Определение авидности проводится для трех инфекцией:
Результат анализа представлен в виде индекса авидности.
Подробнее Авидность антител IgG
Дополнительная справка: если анализы сданы во время беременности|
| Токсоплазма, краснуха | Цитомегаловирус (ЦМВ) |
|---|---|---|
| IgG в высоких титрах, IgM отрицательные | Иммунитет есть, дальнейшие исследования не нужны | Иммунитет есть. Но при беременности имеет значение и активация инфекции, поэтому требуется наблюдение (пересдача IgM в течение беременности). |
| IgG в низких титрах или «серая зона», IgM отрицательные | Сдача анализов:
— IgG методом иммуноблот — авидность антител IgG | Сдача анализов:
— IgG методом иммуноблот — авидность антител IgG |
| IgG положительные, IgM положительные | Иммунитет есть, дальнейшие исследования не нужны | Сдача анализов:
— IgM методом иммуноблот |
| IgG отрицательные, IgM отрицательные | Требуется наблюдение (пересдача IgM в течение беременности). | Требуется наблюдение (пересдача IgM в течение беременности). |
| IgG отрицательные, IgM в высоком титре или «серая зона» | Сдача анализов:
— IgM методом иммуноблот | Сдача анализов:
— IgM методом иммуноблот |
| В середине беременности (первая сдача антител) IgG положительные, IgM положительные | Сдача анализов:
— IgG методом иммуноблот — авидность антител IgG — IgM методом иммуноблот | Сдача анализов:
— IgG методом иммуноблот — авидность антител IgG — IgM методом иммуноблот |
Парвовирусная инфекция и беременность
Частота инфицирования беременных женщин B 19 V составляет приблизительно 1 случай на 400 беременностей. При этом у большинства беременных женщин инфекция протекает бессимптомно (!) Поэтому точный диагноз можно установить только с помощью серологического тестирования (определение IgG и IgM в крови). Инфекция B 19 V не является причиной для прерывания беременности, так как этот вирус не оказывает тератогенного действия. Однако достаточно часто B 19 V может быть причиной развития серьезных осложнений во время беременности — анемии плода, анасарки (водянка плода), внутриутробной гибели плода. Читать дальше…
Инфекция B 19 V не является причиной для прерывания беременности, так как этот вирус не оказывает тератогенного действия. Однако достаточно часто B 19 V может быть причиной развития серьезных осложнений во время беременности — анемии плода, анасарки (водянка плода), внутриутробной гибели плода. Читать дальше…
Основные сведения о цитомегаловирусе (ЦМВ)
Цитомегаловирусная инфекция или цитомегаловирус представляет собой один из видов герпесвирусов, к которым кроме него относятся также простой вирус герпеса человека 1-ого и 2-ого типов, вирус Варицелла-Зостер, вирус Эпштайна-Барр и герпесвирусы человека 6-ого, 7-ого и 8-ого типов.
ЦМВ человека относится к вирусам, вызывающим схожие заболевания у различных животных. Все эти заболевания связаны с появлением характерных увеличенных клеток — отсюда и название цитомегаловирус (цито — клетка, мегало — большая). Вирус ЦМВ может размножаться в различных клетках организма человека, но предпочтительно этими клетками являются фибробласты (клетки соединительной ткани).
Читать дальше…
Анализы
Вирус простого герпеса (HSV, herpes simplex virus) и беременность
В конце 2006 г. в ведущем американском журнале по акушерству и гинекологии начали печататься итоги обследования нескольких тысяч женщин на антитела к вирусу простого герпеса. Оказалось, что вопреки общепринятым взглядам огромный процент женского населения репродуктивного возраста не имел антител к герпесу вообще, т. е. никогда не сталкивалось с вирусом. Именно эти пациентки попадают в группу риска по внутриутробному герпесу во время беременности и по тяжелым герпетическим инфекциям у новорожденных, поскольку у них отсутствуют защитные антитела (IgG), которые защищают внутриутробный плод, переходя через плаценту из крови матери, а новорожденного — переходя из крови в материнское молоко. Практически все случаи тяжелых герпетических инфекций у детей, возникающие внутриутробно или сразу после родов — это дети женщин, никогда до беременности не болевших герпесом.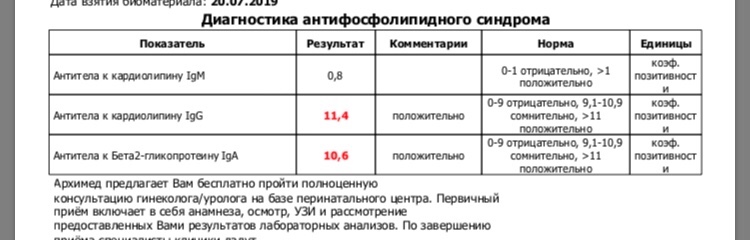
Анализы:
Краснуха и беременность, нужна ли прививка от краснухи
Проблемная инфекция в России, так как очень многие женщины непривиты. Если не было прививки, возможно заражение во время беременности. Такой вирус, как краснуха при беременности опасен для ребенка, поэтому до беременности рекомендуется сделать прививку. Если антитела к краснухе не обнаружены при наступлении беременности, необходимо проводить исследования каждый месяц.
Анализы на краснуху до беременности:
антитела IgG к краснухе положительные — опасности нет, так как нет риска первичного инфицирования.
Антитела IgG к краснухе отрицательные — рекомендуется вакцинация (прививка от краснухи)
Анализы на краснуху во время беременности:
Антитела IgM к краснухе положительные — не исключено первичное инфицирование
Анализы:
Токсоплазмы (Toxoplasma gondii) и беременностьБольшая часть беременных женщин не имеет антител к токсоплазмам. Вероятность заражения во время беременности — 1 из 20 (при отсутствии антител к токсоплазмам). Необходимо проводить профилактические мероприятия: термическая обработка мяса (главный источник инфекции — свинина), не есть сырое сало, не покупать еду в магазинах быстрого питания на улице, соблюдать правила гигиены при приготовлении пищи, не встречаться с котятами (животными до года).
Вероятность заражения во время беременности — 1 из 20 (при отсутствии антител к токсоплазмам). Необходимо проводить профилактические мероприятия: термическая обработка мяса (главный источник инфекции — свинина), не есть сырое сало, не покупать еду в магазинах быстрого питания на улице, соблюдать правила гигиены при приготовлении пищи, не встречаться с котятами (животными до года).
Анализы:
Ветряная оспа и беременность
VZV вызывает два заболевания: при первичном заражении – ветряную оспу, при реактивации – опоясывающий лишай. Все женщины при планировании беременности должны проходить обследование на наличие антител к вирусу ветряной оспы, желательно даже в тех случаях, когда в детской карте есть запись о перенесенной ветряной оспе. При отсутствии антител может быть рекомендована вакцинация. Подробнее читайте «Ветряная оспа и беременность»
Цитомегаловирусная инфекция (ЦМВИ), токсоплазма, ВПГ 1 и 2 типов, парвовирус В19, краснуха, в Лабораториях ЦИР:
- Сдать анализы (антитела к инфекциям, авидность IgG и подтверждающие тесты) можно 7 дней в неделю
- Получение результатов: с курьером, лично , по электронной почте.

- Стоимость анализов
- Скачайте и заполните направление на антитела к инфекциям
Читайте также:
Условия сдачи анализа
Кровь из вены, рекомендуется 8 часов голода, но допустимо и не менее 3 часов после легкого приема пищи.Цитомегаловирусная инфекция (ЦМВ), краснуха, токсоплазмы, парвовирус В19, вирус простого герпеса и беременность
Материал составлен на основе фундаментальных трудов западных ученых.
Токсоплазма, краснуха, цитомегаловирус и беременность
При беременности назначают анализы на антитела к инфекциям — токсоплазме, цитомегаловирусу и краснухе. Определяется два вида антител – IgG и IgM, по которым судят о встрече с инфекционным агентом, а также о времени этой встречи. Самое страшное – заражение во время беременности (краснуха, токсоплазма, ЦМВ) или активация инфекции (ЦМВ).
Часто пациенты получают неопределенный результат – «серая» или «неопределенная» зона. И им рекомендуют пересдать анализ через 2 недели. Это можно себе позволить, если вы только готовитесь к беременности. Но: при беременности ждать нельзя! Такие анализы должны сразу пересматриваться более точными методами. .
И им рекомендуют пересдать анализ через 2 недели. Это можно себе позволить, если вы только готовитесь к беременности. Но: при беременности ждать нельзя! Такие анализы должны сразу пересматриваться более точными методами. .
Специфические антитела класса IgM, в частности, антитела к краснухе, относятся к факторам, циркулирующим в крови экстремально низких концентрациях. Поэтому анализы не в цифрах (количественно), а в виде положительности (=реактивности) или отрицательности (=отсутствии реактивности). Отрицательный и положительный результаты отделяет друг от друга так называемый порог отсечки (cutoff). Цифры показателя выше данного порога считаются положительными, а ниже порога — отрицательными. Зона значений порог ± 10%) является „зоной неопределенности”.
Быстрые уточняющие методы диагностики
Используются два способа: подтверждающие анализы методом иммуноблот и анализ на авидность антител IgG.
Если Вы сдаете эти анализы, исчезает необходимость ЖДАТЬ 2 недели плюс дни готовности анализа.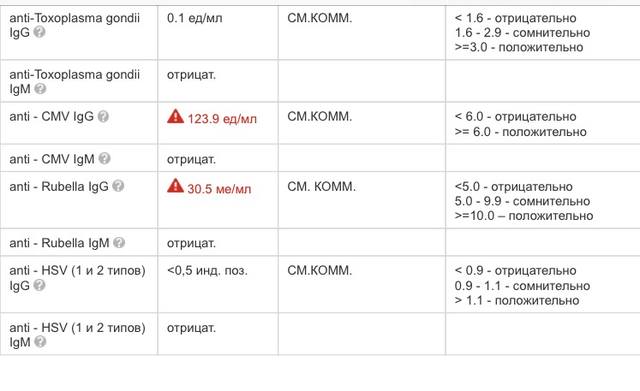 Вы получаете сведения о своем состоянии ВОВРЕМЯ.
Вы получаете сведения о своем состоянии ВОВРЕМЯ.
Подтверждающие анализы на токсоплазму, краснуху, ЦМВ методом иммуноблот:
Используются рекомбинантные антигены
- Высокочувствительный и специфичный тест!
- Чувствительность 97 %
- Специфичность 99 %
- Высокая разрешающая способность между отрицательным и положительным результатами!
- Более точное выявление срока заражения
Используется для подтверждения результатов скрининговых исследований, таких как ИФА (ELISA) или иммунофлуоресцентный анализ (IFA).
Будьте уверены в анализе!
Зачем это нужно:
- точное и своевременное выявление позволит правильно определить тактику ведения беременности
- нет необходимости терять время на ожидание следующего анализа
Тактика врача определяется в каждом конкретном случае по-разному (подготовка к беременности, начало беременности, период новорожденности и т. д.)
д.)
Авидность антител IgG
Определить время, когда произошло инфицирование можно и по авидности антител IgG. Этот анализ менее точен по срокам, чем подтверждающий анализ методом иммуноблот.
Низкоавидные антитела встречаются при острой, недавно развившейся инфекции
Высокоавидные антитела – если встреча с инфекцией состоялась давно.
Определение авидности антител помогает врачу оценить ситуацию по инфекции и решить вопрос о дальнейших действиях.
Кому нужно полное обследование на инфекции?
- женщинам во время подготовки к беременности
- беременным
- новорожденным для диагностики врожденного инфицирования
Дополнительная справка: если анализы сданы во время беременности
| Токсоплазма, краснуха | ЦМВ | |
|---|---|---|
| IgG в высоких титрах, IgM отрицательные | Иммунитет есть, дальнейшие исследования не нужны | Иммунитет есть.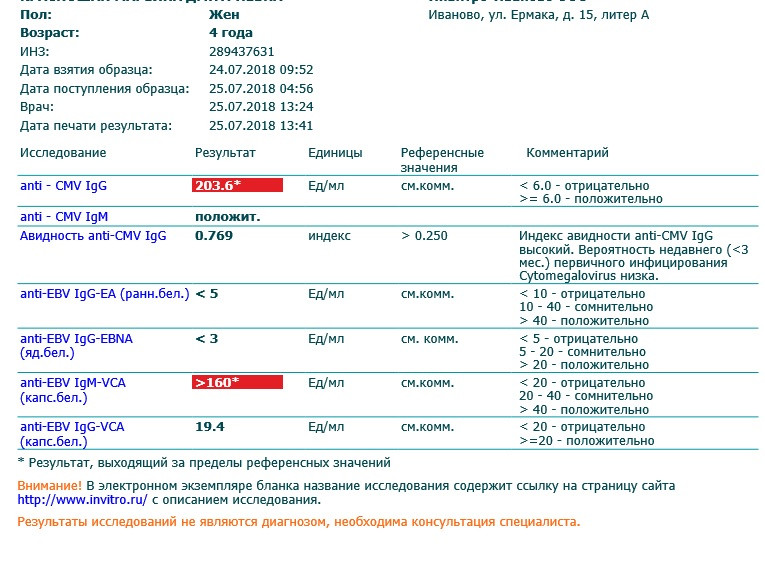 Но при беременности имеет значение и активация инфекции, поэтому требуется наблюдение (пересдача IgM в течение беременности). Но при беременности имеет значение и активация инфекции, поэтому требуется наблюдение (пересдача IgM в течение беременности). |
| IgG в низких титрах или «серая зона», IgM отрицательные | Сдача анализов:
— IgG методом иммуноблот — авидность антител IgG | Сдача анализов:
— IgG методом иммуноблот — авидность антител IgG |
| IgG положительные, IgM положительные | Иммунитет есть, дальнейшие исследования не нужны | Сдача анализов:
— IgM методом иммуноблот |
| IgG отрицательные, IgM отрицательные | Требуется наблюдение (пересдача IgM в течение беременности). | Требуется наблюдение (пересдача IgM в течение беременности). |
| IgG отрицательные, IgM в высоком титре или «серая зона» | Сдача анализов:
— IgM методом иммуноблот | Сдача анализов:
— IgM методом иммуноблот |
| В середине беременности (первая сдача антител) IgG положительные, IgM положительные | Сдача анализов:
— IgG методом иммуноблот — авидность антител IgG — IgM методом иммуноблот | Сдача анализов:
— IgG методом иммуноблот — авидность антител IgG — IgM методом иммуноблот |
Основные сведения о цитомегаловирусе (ЦМВ)
Цитомегаловирус представляет собой один из видов герпесвирусов, к которым кроме него относятся также простой вирус герпеса человека 1-ого и 2-ого типов, вирус Варицелла-Зостер, вирус Эпштайна-Барр и герпесвирусы человека 6-ого, 7-ого и 8-ого типов.
ЦМВ человека относится к вирусам, вызывающим схожие заболевания у различных животных. Все эти заболевания связаны с появлением характерных увеличенных клеток — отсюда и название цитомегаловирус (цито — клетка, мегало — большая). Вирус может размножаться в различных клетках организма человека, но предпочтительно этими клетками являются фибробласты (клетки соединительной ткани).
В добавок к тому, что ЦМВ вызывает тяжелые врожденные дефекты, он может привести к целому ряду заболеваний у детей и взрослых.
Существует три основных клинических вида цитомегаловируса:
- Генитальная ЦМВ инфекция может привести к гепатоспленомегалии (увеличению печени и селезенки), ретиниту (воспаление сетчатки), появлению сыпи и поражению центральной нервной системы.
- У около 10 процентов детей и взрослых первичная цитомегаловирусная инфекция вызывает мононуклеозный синдром с лихорадкой, общим недомоганием, атипичным лимфоцитозом и фарингитом.
- Пациенты с трансплантантатами и ВИЧ-инфицированные люди могут заболеть угрожающим жизни заболеванием, которое охватывает легкие, желудочно-кишечный тракт, сетчатку, печень и центральную нервную систему.

Существует предположение, что вирус обладает онкогенным эффектом и в редких случаях может трансформировать фибробласты.
Эпидемиология цитомегаловирусной инфекции (ЦМВ)
Цитомегаловирус распространен по всему миру, но проживание в плохих социальных условиях и не соблюдение правил личной гигиены сильно способствует передаче микроба. Часто встречаются инфекции у новорожденных и маленьких детей. Вирус можно обнаружить в молоке, слюне, фекалиях и моче. Была прослежена передача вируса от маленького ребенка к его беременной матери, и затем к развивающемуся плоду. К счастью, вирус плохо передается при случайных контактах, так как для его передачи необходимо время. ЦМВ часто передается половым путем, его выделяют из семени или цервикальной слизи. Однажды заразившись, человек, возможно, будет носителем данного вируса в течение всей жизни.
Заболевания, вызываемые ЦМВ, и их клинические проявления
Генитальная цитомегаловирусная инфекция (ЦМВ)
Инфекции у плода варьируются от легких форм до тяжелых и диссеминированных. Петехии (точечные кровоизлияния), гепатоспленомегалия и желтуха — наиболее часто встречаемые проявления. Микроцефалия с (или без) церебральной кальцификации, внутриматочная задержка роста и преждевременное развитие встречаются (что это такое????) в 30-50 процентах случаев. Лабораторные аномалии включают повышение уровня аланинаминотрансферазы, тромбоцитопению (уменьшенное число тромбоцитов), гипербилирубинемию (повышение уровня билирубина в крови), гемолиз (разрушение клеток крови) и увеличение уровня белка спинномозговой жидкости. Прогнозы для новорожденных с тяжелыми формами заболевания весьма печальны: процент смертности очень велик, а те, кому удается преодолеть болезнь, в будущем встречаются с трудностями в интеллектуальном развитии и развитии слуха.
Петехии (точечные кровоизлияния), гепатоспленомегалия и желтуха — наиболее часто встречаемые проявления. Микроцефалия с (или без) церебральной кальцификации, внутриматочная задержка роста и преждевременное развитие встречаются (что это такое????) в 30-50 процентах случаев. Лабораторные аномалии включают повышение уровня аланинаминотрансферазы, тромбоцитопению (уменьшенное число тромбоцитов), гипербилирубинемию (повышение уровня билирубина в крови), гемолиз (разрушение клеток крови) и увеличение уровня белка спинномозговой жидкости. Прогнозы для новорожденных с тяжелыми формами заболевания весьма печальны: процент смертности очень велик, а те, кому удается преодолеть болезнь, в будущем встречаются с трудностями в интеллектуальном развитии и развитии слуха.
Зачастую генитальный цитомегаловирус никак не проявляется у новорожденных, а потому не лечится своевременно, что приводит к отклонениям у таких детей в различных системах, которые проявляются в течение первых лет их жизни.
Перинатальная ЦМВ инфекция
Новорожденные могут заразиться ЦМВ при прохождении родового канала или при последующем контакте с материнским молоком или другими выделениями. Огромное количество случаев инфицирования новорожденных протекает асимптоматически. Однако длительная интерстициальная пневмония связана с цитомегаловирусом. Иногда она сопровождается присоединением других инфекций, таких как Chlamidia trachomatis или Ureaplasma urealyticum. Медленное набирание веса, аденопатия, сыпь, гепатит, анемия и атипичный лимфоцитоз также могут сопутствовать заболеванию.
Огромное количество случаев инфицирования новорожденных протекает асимптоматически. Однако длительная интерстициальная пневмония связана с цитомегаловирусом. Иногда она сопровождается присоединением других инфекций, таких как Chlamidia trachomatis или Ureaplasma urealyticum. Медленное набирание веса, аденопатия, сыпь, гепатит, анемия и атипичный лимфоцитоз также могут сопутствовать заболеванию.
Мононуклеозный синдром
Этот синдром возникает у 10 процентов первично зараженных людей, у оставшихся первичная инфекция протекает бессимптомно. Для пациентов с этим синдромом характерно наличие лихорадки, общего недомогания, атипичного лимфоцитоза и, в редких случаях, цервикальной аденопатии или гепатита.
Большинство пациентов выздоравливают без последствий, хотя послевирусная астения может продолжаться в течение нескольких месяцев.
ЦМВ и трансплантация органов
Считается, что ЦМВ является одним из основных патогенов, осложняющих трансплантацию органов. У пациентов, которым пересаживают почку, сердце, легкие и трансплантаты печени, ЦМВ вызывает множество синдромов, включающих лихорадку и лейкопению, гепатит, пневмонит, эзофагит, гастрит, колит и ретинит. Период максимального риска находится между первым и четвертым месяцами после трансплантации.
У пациентов, которым пересаживают почку, сердце, легкие и трансплантаты печени, ЦМВ вызывает множество синдромов, включающих лихорадку и лейкопению, гепатит, пневмонит, эзофагит, гастрит, колит и ретинит. Период максимального риска находится между первым и четвертым месяцами после трансплантации.
ЦМВ у людей с поражениями иммунной системы.
Цитомегаловирус признан важным паразитом у ВИЧ-инфицированных людей, у которых он вызывает ретинит или диссиминированные (охватывающие весь организм) заболевания. Хотя случаи серьезных ЦМВ заболеваний снизились, установление высокоактивного режима приема антиретровирусных препаратов иногда вызывает острые вспышки ЦМВ-ого ретинита в течение первых нескольких недель терапии.
Диагностика цитомегаловируса
Диагностику ЦМВ инфекции невозможно убедительно провести только по клиническим проявлениям. Необходимо выделение вируса или определение цитомегаловирусных антигенов или ДНК из клинических образцов. Кроме того, важно проследить рост уровня антител в крови. Вирус легко определяется в культуре фибробластов. Если содержание вируса велико, что зачастую имеет место при генитальной ЦМВ инфекции, характерные изменения в клетках будут видны в течение нескольких дней. Но если содержание вируса мало, как при цитомегаловирусном мононуклеозе, такая диагностика может занять несколько недель. Многие лаборатории применяют метод, включающий в себя центрифугирование и определение антител к раннему ЦМВ- антигену. Такое исследование может дать результат раньше, чем метод культур.
Вирус легко определяется в культуре фибробластов. Если содержание вируса велико, что зачастую имеет место при генитальной ЦМВ инфекции, характерные изменения в клетках будут видны в течение нескольких дней. Но если содержание вируса мало, как при цитомегаловирусном мононуклеозе, такая диагностика может занять несколько недель. Многие лаборатории применяют метод, включающий в себя центрифугирование и определение антител к раннему ЦМВ- антигену. Такое исследование может дать результат раньше, чем метод культур.
| Госпитальный | ВИЧ (антитела и антигены) | 1 400 р. |
| Реакция пассивной гемагглютинации на сифилис (РПГА), качественно | ||
| Поверхностный антиген вируса гепатита В (австралийский антиген, HbsAg) | ||
| Антитела к вирусу гепатита С, суммарные (Anti-HCV) | ||
| Госпитальный терапевтический | Клинический анализ крови с лейкоцитарной формулой (5DIFF) | 3 400 р. |
| СОЭ | ||
| Общий белок | ||
| Аланинаминотрансфераза (АЛТ) | ||
| Глюкоза | ||
| Аспартатаминотрансфераза (АСТ) | ||
| Мочевина | ||
| Креатинин | ||
| Билирубин общий | ||
| Поверхностный антиген вируса гепатита В (австралийский антиген, HbsAg) | ||
| Антитела к вирусу гепатита С, суммарные (Anti-HCV) | ||
| Микрореакция на сифилис качественно (RPR) | ||
| ВИЧ (антитела и антигены) | ||
| Госпитальный хирургический | Клинический анализ крови с лейкоцитарной формулой (5DIFF) | 4 700 р. |
| СОЭ | ||
| Группа крови | ||
| Резус-фактор | ||
| Фибриноген | ||
| Протромбин (время, по Квику, МНО) | ||
| АЧТВ | ||
| Общий белок | ||
| Мочевина | ||
| Креатинин | ||
| Аланинаминотрансфераза (АЛТ) | ||
| Аспартатаминотрансфераза (АСТ) | ||
| Билирубин общий | ||
| Глюкоза | ||
| Поверхностный антиген вируса гепатита В (австралийский антиген, HbsAg) | ||
| Антитела к вирусу гепатита С, суммарные (Anti-HCV) | ||
| Микрореакция на сифилис качественно (RPR) | ||
| ВИЧ (антитела и антигены) | ||
| Биохимический анализ крови, базовый | Общий белок | 1 800 р. |
| Мочевина | ||
| Креатинин | ||
| Аланинаминотрансфераза (АЛТ) | ||
| Аспартатаминотрансфераза (АСТ) | ||
| Холестерин общий | ||
| Билирубин общий | ||
| Железо | ||
| Глюкоза | ||
| Биохимический анализ крови | Общий белок | 2 500 р. |
| Мочевина | ||
| Креатинин | ||
| Билирубин общий | ||
| Аланинаминотрансфераза (АЛТ) | ||
| Аспартатаминотрансфераза (АСТ) | ||
| Щелочная фосфатаза | ||
| Альфа-амилаза | ||
| Гамма-глутамилтрансфераза (ГГТ ) | ||
| Железо | ||
| Мочевая кислота | ||
| Холестерин общий | ||
| Триглицериды | ||
| Кальций общий | ||
| Глюкоза | ||
| Коагулограмма, скрининг | АЧТВ | 1 200 р. |
| Протромбин (время, по Квику, МНО) | ||
| Тромбиновое время | ||
| Фибриноген | ||
| Липидный профиль, базовый | Холестерин общий | 1 100 р. |
| Холестерин липопротеидов высокой плотности (ЛПВП, LDL) | ||
| Холестерин липопротеидов низкой плотности (ЛПНП, HDL) | ||
| Холестерин липопротеидов очень низкой плотности (ЛПОНП), (включает определение триглицеридов, код 4.5.A1.201) | ||
| Коэффициент атерогенности | ||
| Липидный профиль, расширенный | Холестерин общий | 3 100 р. |
| Холестерин липопротеидов высокой плотности (ЛПВП, LDL) | ||
| Холестерин липопротеидов низкой плотности (ЛПНП, HDL) | ||
Холестерин липопротеидов очень низкой плотности (ЛПОНП), (включает определение триглицеридов,
код 4. 5.A1.201) 5.A1.201) | ||
| Коэффициент атерогенности | ||
| Аполипопротеин А1 | ||
| Аполипопротеин В | ||
| Липопротеин (а) | ||
| Кардиологический | Протромбин (время, по Квику, МНО) | 3 800 р. |
| Фибриноген | ||
| Натрий, калий, хлор (Na/K/Cl) | ||
| Креатинкиназа-МВ | ||
| Лактатдегидрогеназа (ЛДГ) | ||
| Тропонин I | ||
| Холестерин общий | ||
| Холестерин липопротеидов низкой плотности (ЛПНП, HDL) | ||
| Гомоцистеин | ||
| С-реактивный белок ультрачувствительный | ||
| Тиреотропный гормон (ТТГ) | ||
| Обследование печени, базовый | Аланинаминотрансфераза (АЛТ) | 1 500 р. |
| Аспартатаминотрансфераза (АСТ) | ||
| Билирубин общий | ||
| Билирубин прямой | ||
| Щелочная фосфатаза | ||
| Гамма-глутамилтрансфераза (ГГТ ) | ||
| Обследование печени | Протромбин (время, по Квику, МНО) | 2 500 р. |
| Общий белок | ||
| Белковые фракции | ||
| Билирубин общий | ||
| Билирубин прямой | ||
| Аланинаминотрансфераза (АЛТ) | ||
| Аспартатаминотрансфераза (АСТ) | ||
| Щелочная фосфатаза | ||
| Гамма-глутамилтрансфераза (ГГТ ) | ||
| Холестерин общий | ||
| Холинэстераза | ||
| Альфа-фетопротеин (АФП) | ||
| Диагностика гепатитов, скрининг | Антитела к вирусу гепатита А, IgM (Anti-HAV IgM) | 2 500 р. |
| Антитела к вирусу гепатита А, IgG (Anti-HAV IgG) | ||
| Поверхностный антиген вируса гепатита В (австралийский антиген, HbsAg) | ||
| Антитела к поверхностному антигену вируса гепатита В (Anti-HBs) | ||
| Антитела к ядерному (cor) антигену вируса гепатита В, суммарные (Anti-HBc) | ||
| Антитела к вирусу гепатита С, суммарные (Anti-HCV) | ||
| Нефрологический, биохимический | Альбумин | 1 500 р. |
| Креатинин | ||
| Мочевина | ||
| Натрий, калий, хлор (Na/K/Cl) | ||
| Кальций общий | ||
| Магний | ||
| Фосфор неорганический | ||
| Ревматологический, расширенный | Мочевая кислота | 4 900 р. |
| Антистрептолизин-О | ||
| С-реактивный белок | ||
| Ревматоидный фактор | ||
| Антитела к циклическому цитруллиновому пептиду (ACCP, anti-CCP) | ||
| Антинейтрофильные цитоплазматические антитела, IgG (ANCA), Combi 6 | ||
| Антинуклеарные антитела, иммуноблот (аутоантитела класса IgG к 14 различным антигенам: nRNP/Sm, Sm, SS-A (SS-A нативный и Ro-52), SS-B, Scl-70, Jo-1, PM-Scl, протеин B центромера, PCNA, dsDNA, нуклеосомы, гистоны, рибосомальный белок P, AMA-M2) | ||
| Антитела к хламидии (Chlamydia trachomatis), IgG | ||
| Маркеры остеопороза, биохимический | Фосфор неорганический | 4 500 р. |
| 25-OH витамин D, суммарный (кальциферол) | ||
| Паратгормон | ||
| Кальцитонин | ||
| Остеокальцин | ||
| С-концевые телопептиды коллагена I типа (Beta-Cross laps) | ||
| Кальций ионизированный | ||
| Диагностика диабета, биохимический | Глюкоза | 2 900 р. |
| Гликированный гемоглобин А1с | ||
| Инсулин | ||
| C-пептид | ||
| Антитела к инсулину (IAA) | ||
| Антитела к бета-клеткам поджелудочной железы (ICA) | ||
| Инсулинорезистентность | Глюкоза | 1 100 р. |
| Инсулин | ||
| Индекс HOMA | ||
| Индекс CARO | ||
| Фитнес. Физические нагрузки | Клинический анализ крови с лейкоцитарной формулой (5DIFF) | 2 900 р. |
| Мочевина | ||
| Креатинин | ||
| Аланинаминотрансфераза (АЛТ) | ||
| Аспартатаминотрансфераза (АСТ) | ||
| Креатинкиназа (КФК) | ||
| Миоглобин | ||
| Молочная кислота (лактат) | ||
| Гастрокомплекс | Пепсиноген I | 2 500 р. |
| Пепсиноген II | ||
| Пепсиноген I/Пепсиноген II (соотношение) | ||
| Гастрин | ||
| Антитела к хеликобактеру (Helicobacter pylori), IgG | ||
| Дифференциальная диагностика заболеваний ЖКТ | Панкреатическая эластаза 1 в кале | 4 900 р. |
| Кальпротектин (в кале) | ||
| Опухолевая пируваткиназа Тu M2 (в кале) | ||
| Определение гемоглобина в кале количественным иммунохроматографическим методом (FOB Gold Test) | ||
| Гематологический (диагностика анемий) | Клинический анализ крови с лейкоцитарной формулой (5DIFF) | 3 900 р. |
| Ретикулоциты | ||
| Билирубин общий | ||
| Билирубин прямой | ||
| Железо | ||
| Ферритин | ||
| Трансферрин | ||
| Латентная железосвязывающая способность сыворотки (ЛЖСС) | ||
| Витамин В9 (фолиевая кислота) | ||
| Витамин В12 (цианкобаламин) | ||
| Обследование щитовидной железы, скрининг | Тиреотропный гормон (ТТГ) | 1 800 р. |
| Тироксин свободный (Т4 свободный) | ||
| Трийодтиронин свободный (Т3 свободный) | ||
| Антитела к тиреоглобулину (Анти-ТГ) | ||
| Антитела к микросомальной тиреопероксидазе (Анти-ТПО) | ||
| Обследование щитовидной железы | Тиреотропный гормон (ТТГ) | 3 300 р. |
| Тироксин свободный (Т4 свободный) | ||
| Трийодтиронин свободный (Т3 свободный) | ||
| Антитела к микросомальной тиреопероксидазе (Анти-ТПО) | ||
| Тиреоглобулин | ||
| Антитела к тиреоглобулину (Анти-ТГ) | ||
| Антитела к рецепторам тиреотропного гормона (АТ рТТГ) | ||
| Кальцитонин | ||
| Гормональный профиль для мужчин | Тиреотропный гормон (ТТГ) | 1 800 р. |
| Фолликулостимулирующий гормон (ФСГ) | ||
| Лютеинизирующий гормон (ЛГ) | ||
| Пролактин | ||
| Тестостерон свободный | ||
| Гормональный профиль для женщин | Тиреотропный гормон (ТТГ) | 3 300 р. |
| Лютеинизирующий гормон (ЛГ) | ||
| Фолликулостимулирующий гормон (ФСГ) | ||
| Эстрадиол | ||
| Пролактин | ||
| Дегидроэпиандростерон сульфат (ДГЭА-сульфат) | ||
| Кортизол | ||
| Тестостерон свободный | ||
| Андростендион | ||
| Гидроксипрогестерон (17-OH-прогестерон) | ||
| Планирование беременности, базовый | Фолликулостимулирующий гормон (ФСГ) | 1 500 р. |
| Лютеинизирующий гормон (ЛГ) | ||
| Пролактин | ||
| Эстрадиол | ||
| Планирование беременности (гормоны) — лютеиновая фаза | Тиреотропный гормон (ТТГ) | 2 500 р. |
| Гидроксипрогестерон (17-OH-прогестерон) | ||
| Прогестерон | ||
| Тестостерон свободный (включает определение тестостерона общего и свободного, ГСПГ (SHBG), расчет индекса свободных андрогенов) | ||
| Дегидроэпиандростерон сульфат (ДГЭА-сульфат) | ||
| Диагностика нарушений функции яичников | Антимюллеров гормон (АМГ, АМН, MiS) | 1 500 р. |
| Антитела к стероид-продуцирующим клеткам яичника (АСКП-Ovary) | ||
| Исследование стероидного профиля крови методом тандемной масспектрометрии | Кортизон | 5 900р. |
| Кортизол | ||
| Кортикостерон | ||
| Прогестерон | ||
| 21-дезоксикортизол | ||
| 17-гидроксипрогестерон | ||
| Дезоксикортикостерон | ||
| Тестостерон | ||
| Дегидроэпиандростерон | ||
| Андростендион | ||
| Аyтифосфолипидный синдром (АФС) | Волчаночный антикоагулянт (скрининг) | 1 900 р. |
| Антитела к кардиолипину (суммарные) | ||
| Антитела к бета2-гликопротеину | ||
| Онкологический для мужчин, биохимический | Альфа-фетопротеин (АФП) | 3 200 р. |
| Раково-эмбриональный антиген (РЭА) | ||
| Антиген CA 19-9 | ||
| Простатоспецифический антиген (ПСА) общий | ||
| Антиген СА 72-4 | ||
| Общий бета-ХГЧ (диагностика беременности, онкомаркер) | ||
| Онкологический для женщин, биохимический | Альфа-фетопротеин (АФП) | 3 900 р. |
| Раково-эмбриональный антиген (РЭА) | ||
| Антиген CA 19-9 | ||
| Антиген СА 125 | ||
| Антиген CA 15-3 | ||
| Антиген СА 72-4 | ||
| Антиген плоскоклеточной карциномы (SCCA) | ||
| Диагностика рака молочной железы | (2-OHE1+2+OHE2)/16a-OHE1 | 6 900 р. |
| 4-гидроксиэстрон (4-OHE1) | ||
| 2-OHE1/2-OMeE1 | ||
| 2-гидроксиэстрон (2-OHE1) | ||
| 2-гидроксиэстрадиол (2-OHE2) | ||
| 2-OHE1+2-OHE2 | ||
| 16a-гидроксиэстрон (16a-OHE1) | ||
| 2-метоксиэстрон (2-OMeE1) | ||
| 4-метоксиэстрон (4-OMeE2) | ||
| Прегнадиол | ||
| Эстриол | ||
| Эстрон | ||
| TORCH-комплекс, скрининг | Антитела к токсоплазме (Toxoplasma gondii), IgG | 1 800 р. |
| Антитела к вирусу краснухи, IgG | ||
| Антитела к вирусу простого герпеса (Herpes simplex virus, ВПГ) II типа, IgG | ||
| Антитела к цитомегаловирусу (Cytomegalovirus, CMV), IgG | ||
| TORCH- комплекс, базовый | Антитела к токсоплазме (Toxoplasma gondii), IgM | 2 800 р. |
| Антитела к токсоплазме (Toxoplasma gondii), IgG | ||
| Антитела к вирусу краснухи, IgM | ||
| Антитела к вирусу краснухи, IgG | ||
| Антитела к цитомегаловирусу (Cytomegalovirus), IgM | ||
| Антитела к цитомегаловирусу (Cytomegalovirus), IgG | ||
| Антитела к вирусу простого герпеса I, II типов (Herpes simplex virus I, II), IgM | ||
| Антитела к вирусу простого герпеса I, II типов (Herpes simplex virus I, II), IgG | ||
| TORCH-комплекс, расширенный | Антитела к токсоплазме (Toxoplasma gondii), IgM | 3 800 р. |
| Антитела к токсоплазме (Toxoplasma gondii), IgG | ||
| Антитела к вирусу краснухи, IgM | ||
| Антитела к вирусу краснухи, IgG | ||
| Антитела к цитомегаловирусу (Cytomegalovirus, CMV), IgM | ||
| Антитела к цитомегаловирусу (Cytomegalovirus, CMV), IgG | ||
| Антитела к вирусу простого герпеса (Herpes simplex virus, ВПГ) I,II типов, IgM | ||
| Антитела к вирусу простого герпеса (Herpes simplex virus, ВПГ) I,II типов, IgG | ||
| Антитела к хламидии (Chlamydia trachomatis), IgA | ||
| Антитела к хламидии (Chlamydia trachomatis), IgG | ||
| Антитела к листерии (Listeria monocytogenes) | ||
| Инфекции, передающиеся половым путем (кровь) | ВИЧ (антитела и антигены) | 3 200 р. |
| Антитела к бледной трепонеме (Treponema pallidum), суммарные | ||
| Поверхностный антиген вируса гепатита В (австралийский антиген, HbsAg) | ||
| Антитела к ядерному (cor) антигену вируса гепатита В, суммарные (Anti-HBc) | ||
| Антитела к вирусу гепатита С, суммарные (Anti-HCV) | ||
| Антитела к хламидии (Chlamydia trachomatis), IgA | ||
| Антитела к хламидии (Chlamydia trachomatis), IgG | ||
| Антитела к микоплазме (Mycoplasma hominis), IgА | ||
| Антитела к микоплазме (Mycoplasma hominis), IgG | ||
| Антитела к уреаплазме (Ureaplasma urealyticum), IgА | ||
| Антитела к уреаплазме (Ureaplasma urealyticum), IgG | ||
| Антитела к вирусу простого герпеса (Herpes simplex virus, ВПГ) I,II типов, IgG | ||
Антитела к трихомонаде (Trichomonas vaginalis), IgG. | ||
| Диагностика паразитарных заболеваний | Клинический анализ крови с лейкоцитарной формулой (5DIFF) | 2 900 р. |
| Антитела к хеликобактеру (Helicobacter pylori), IgG | ||
| Антитела к лямблиям (Lamblia intestinalis), суммарные | ||
| Антитела к описторхисам (Opisthorchis felineus), IgG | ||
| Антитела к токсокарам (Toxocara canis), IgG | ||
| Антитела к трихинеллам (Trichinella spiralis), IgG | ||
| Антитела к эхинококкам (Echinococcus granulosus), IgG | ||
| Антитела к токсоплазме (Toxoplasma gondii), IgG | ||
| Антитела к аскаридам (Ascaris lumbricoides), IgG | ||
| Иммуноглобулин E (IgE) | ||
| Диагностика описторхоза | ДНК Описторхисов | 1 100 р. |
| Антитела к антигенам описторхисов, IgG | ||
| Скрининговая диагностика ВИЧ | РНК ВИЧ | 2 100 р. |
| ВИЧ (антитела и антигены) |
почему они так важны в борьбе с COVID-19 — РБК
Коронавирус — новая инфекция, поэтому тесты на антитела к нему только начинают производить. О близкой готовности тестов сразу несколько лабораторий и компаний заявили еще в середине марта. Но попытка массового проведения серологических исследований в Великобритании оказалась неудачной. В марте Борис Джонсон поставил задачу делать по 100 тыс. тестов в день — главным образом медицинским работникам и сотрудникам жизненно важных отраслей. Эти люди продолжают работать в карантин, у них больше шансов встретиться с вирусом, и переболевшие среди них особенно полезны экономике. Тесты были произведены и закуплены (заметная доля — в Китае, лидере всех «коронавирусных» производств), однако ни один из них не был одобрен контрольными лабораториями в Оксфордском университете, и теперь Великобритания пытается вернуть бюджетные деньги, потраченные на закупки миллионов тестов.
В США FDA выдало первое разрешение тесту на антитела 2 апреля, но для эпидемиологического, а не диагностичеcкого применения. Дело в том, что антитела могут появиться не сразу при попадании вируса в организм, то есть недавно заболевший может дать положительный ПЦР-тест и отрицательный антительный. Поэтому американские тесты можно делать только в лабораториях, а не на приеме у врача для установления диагноза.
Читайте на РБК Pro
В этом сейчас главная проблема: трудно перейти от эпидемиологических исследований к принятию решения о здоровье конкретного человека. Если нам нужно определить общее количество переболевших для установления летальности, ошибка в 10% может считаться приемлемой и компенсироваться охватом. Однако 10% врачей и медсестер, получивших ложно положительный тест и на этом основании работающих без дефицитных средств защиты, рискуют жизнью.
Первые результаты
На самом деле массовое тестирование на антитела имеет смысл, только если переболело значительное количество людей. И хотя существование скрытых инфекций не подвергается сомнению, они все же не охватили существенную часть населения, считают американские эксперты. А немецкие ученые, проведя тестирование в городке Гангельт в Северном Рейне-Вестфалии — одном из ранних очагов эпидемии в стране, обнаружили антитела лишь у 15% жителей. Даже в Ухане эта доля составила лишь 19,1%. Определить, какой процент населения должен переболеть для достижения коллективного иммунитета довольно трудно, нужно знать, сколько человек заражает один больной — а эта цифра для коронавируса не определена точно. Большинство экспертов указывают интервал от 65% до 80%.
И хотя существование скрытых инфекций не подвергается сомнению, они все же не охватили существенную часть населения, считают американские эксперты. А немецкие ученые, проведя тестирование в городке Гангельт в Северном Рейне-Вестфалии — одном из ранних очагов эпидемии в стране, обнаружили антитела лишь у 15% жителей. Даже в Ухане эта доля составила лишь 19,1%. Определить, какой процент населения должен переболеть для достижения коллективного иммунитета довольно трудно, нужно знать, сколько человек заражает один больной — а эта цифра для коронавируса не определена точно. Большинство экспертов указывают интервал от 65% до 80%.
Коронавирус
Россия Москва Мир
0 (за сутки)
Заразились
0
0 (за сутки)
Умерли
0 (за сутки)
Заразились
0
0 (за сутки)
Умерли
0 (за сутки)
Заразились
0
0 (за сутки)
Умерли
Источник: JHU, федеральный и региональные оперштабы по борьбе с вирусом
Важные результаты может дать исследование очагов инфекции в Италии. Мэр городка Нембро в провинции Бергамо Клаудио Канчелли призвал провести тестирование на антитела всех горожан. Из 11 616 жителей Нембро за март потерял 121. Не все эти смерти официально зарегистрированы как смерти от коронавируса, но годом ранее, в марте 2019-го, там умерли всего 11 человек. Таким образом, городок потерял 1% населения, поэтому, говорит мэр, коллективный иммунитет уже достигнут, и это хорошо бы проверить антительным тестом. Впрочем, такая гигантская смертность уникальна и не повторялась ни в одном из больших городов.
Мэр городка Нембро в провинции Бергамо Клаудио Канчелли призвал провести тестирование на антитела всех горожан. Из 11 616 жителей Нембро за март потерял 121. Не все эти смерти официально зарегистрированы как смерти от коронавируса, но годом ранее, в марте 2019-го, там умерли всего 11 человек. Таким образом, городок потерял 1% населения, поэтому, говорит мэр, коллективный иммунитет уже достигнут, и это хорошо бы проверить антительным тестом. Впрочем, такая гигантская смертность уникальна и не повторялась ни в одном из больших городов.
В России тест на антитела предлагают Федеральное медико-биологическое агентство и новосибирский центр «Вектор», но о его надежности ничего не известно. Роспотребнадзор сообщил, что антитела найдены у 3% сопровождавших «Сапсаны» Москва — Санкт-Петербург медиков, но это слишком маленькая группа людей, чтобы по ней судить о реальной распространенности иммунитета.
Координировать усилия по выявлению переболевших взялась ВОЗ. Организация объявила программу Solidarity по распределенным клиническим испытаниям лекарств — кандидатов против вируса. Программа Solidarity II создана по ее образу и подобию и призвана собирать и обобщать информацию из разных стран и помогать обеспечивать ее качество и стандартизацию.
Программа Solidarity II создана по ее образу и подобию и призвана собирать и обобщать информацию из разных стран и помогать обеспечивать ее качество и стандартизацию.
Строго говоря, уверенности в успехе нет. Наука не знает, как устроен человеческий иммунитет к коронавирусу и устойчив ли он — возбудитель COVID-19 живет с нами слишком мало времени. Из Кореи и Китая поступают отдельные сообщения, что вирус возвращается к выздоровевшим больным, а у некоторых из них антитела в крови не определяются. Но пока эксперты склонны относить такие случаи к последствиям неточного тестирования. Во всем мире уже выздоровели почти 450 тыс. пациентов, и их массового повторного заражения не наблюдается.
Скорость распространения коронавируса в мире
Случаев за сутки
Источник: JHU
Данные по миру i
Авидность материнских IgG, IgM и ультразвуковые отклонения: комбинированный метод выявления врожденной цитомегаловирусной инфекции с последствиями
Hyde TB, Schmid DS, Cannon MJ . Показатели сероконверсии цитомегаловируса и факторы риска: последствия для врожденного ЦМВ. Rev Med Virol 2010; 20 : 311–326.
Показатели сероконверсии цитомегаловируса и факторы риска: последствия для врожденного ЦМВ. Rev Med Virol 2010; 20 : 311–326.
Артикул Google Scholar
Пекхэм С.С. Цитомегаловирусная инфекция: врожденные и неонатальные заболевания. Scand J Infect Dis Suppl 1991; 80 : 82–87.
КАС пабмед Google Scholar
Фаулер К.Б., Стагно С., Пасс РФ, Бритт В.Дж., Болл Т.Дж., Алфорд К.А. Исход врожденной цитомегаловирусной инфекции в зависимости от статуса материнских антител. N Engl J Med 1992; 326 : 663–667.
КАС Статья Google Scholar
Pass RF, Fowler KB, Boppana SB, Britt WJ, Stagno S .Врожденная цитомегаловирусная инфекция после инфицирования матери в первом триместре: симптомы при рождении и исход. Дж Клин Вирол 2006; 35 : 216–220.
Артикул Google Scholar
Лаззаротто Т., Герра Б., Габриэлли Л., Ланари М., Ландини М.П. Актуальная информация о профилактике, диагностике и лечении цитомегаловирусной инфекции во время беременности. Clin Microbiol Infect 2011; 17 : 1285–1293.
КАС Статья Google Scholar
Stagno S, Pass RF, Cloud G, Britt WJ, Henderson RE, Walton PD и др. . Первичная цитомегаловирусная инфекция при беременности: заболеваемость, передача плоду и клинический исход. ЯМА 1986; 256 : 1904–1984.
КАС Статья Google Scholar
Adler SP, Finney JW, Manganello AM, Best AM .Профилактика передачи цитомегаловируса беременным от ребенка к матери. J Pediatr 2004; 145 : 485–491.
Артикул Google Scholar
Гера Б.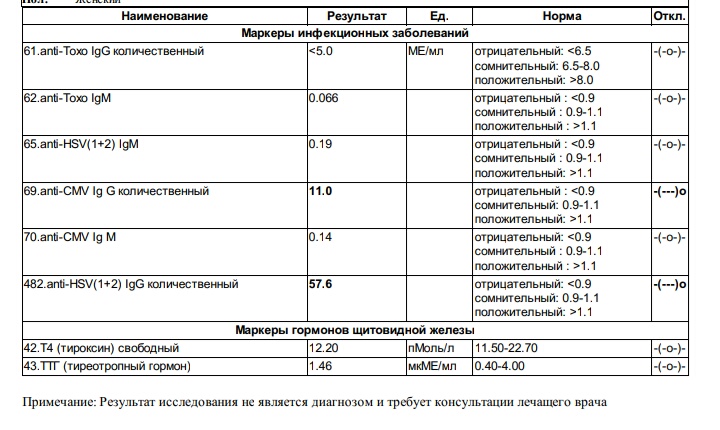 , Симонацци Г., Пуччетти С., Ланари М., Фарина А., Лаззаротто Т. и др. . Ультразвуковой прогноз симптоматической врожденной цитомегаловирусной инфекции. Am J Obstet Gynecol . 2008 г.; 198 (4): 380 е1–е7.
, Симонацци Г., Пуччетти С., Ланари М., Фарина А., Лаззаротто Т. и др. . Ультразвуковой прогноз симптоматической врожденной цитомегаловирусной инфекции. Am J Obstet Gynecol . 2008 г.; 198 (4): 380 е1–е7.
Кеннесон А., Кэннон М.Дж.Обзор и метаанализ эпидемиологии врожденной цитомегаловирусной инфекции. Rev Med Virol 2007; 17 : 253–276.
Артикул Google Scholar
Ревелло М.Г., Герна Г. . Диагностика и лечение цитомегаловирусной инфекции человека у матери, плода и новорожденного. клин. микробиол. 2002 г.; 15 : 680–715.
Артикул Google Scholar
Лаззаротто Т., Гера Б., Ланари М., Габриэлли Л., Ландини М.П.Новые достижения в диагностике врожденной цитомегаловирусной инфекции. Дж Клин Вирол 2008; 41 : 192–197.
КАС Статья Google Scholar
Блэкберн Н. К., Бесселаар Т.Г., Шоуб Б.Д., О’Коннелл К.Ф. Дифференциация первичной цитомегаловирусной инфекции от реактивации с помощью теста денатурации мочевины для измерения авидности антител. J. Med. Вирол 1991; 33 : 6–9.
К., Бесселаар Т.Г., Шоуб Б.Д., О’Коннелл К.Ф. Дифференциация первичной цитомегаловирусной инфекции от реактивации с помощью теста денатурации мочевины для измерения авидности антител. J. Med. Вирол 1991; 33 : 6–9.
КАС Статья Google Scholar
Лаззаротто Т., Габриэлли Л., Ланари М., Герра Б., Беллуччи Т., Сасси М. и др. .Врожденная цитомегаловирусная инфекция: последние достижения в диагностике материнской инфекции. Хум Иммунол 2004; 65 : 410–415.
КАС Статья Google Scholar
Munro SC, Hall B, Whybin LR, Leader L, Robertson P, Maine GT и др. . Диагностика и скрининг цитомегаловирусной инфекции у беременных. J клин. Микробиол 2005; 43 (9): 4713–4718.
КАС Статья Google Scholar
Picone O, Vauloup-Fellous C, Cordier AG, Châtelet IPD, Senat MV, Frydman R и др. .Двухлетнее исследование цитомегаловирусной инфекции во время беременности во французской больнице. БДЖОГ 2009; 116 : 818–823.
.Двухлетнее исследование цитомегаловирусной инфекции во время беременности во французской больнице. БДЖОГ 2009; 116 : 818–823.
КАС Статья Google Scholar
Леруэ-Виль М., Селье Ю., Саломон Л.Дж., Штирнеманн Ю.Дж., Жакмар Ф., Вилле Ю. . Прогнозирование инфицирования плода при цитомегаловирусном иммуноглобулине М в первом триместре беременности: ретроспективная когорта. Clin Infect Dis 2013; 56 : 1428–1435.
КАС Статья Google Scholar
Бенуа Г., Саломон Л.Дж., Мохло М., Суарес Б., Жакмар Ф., Вилле Ю. . Прогностическое значение ультразвуковых отклонений и биологических показателей в крови плодов, инфицированных цитомегаловирусом. БДЖОГ 2008; 115 : 823–829.
КАС Статья Google Scholar
Эндерс Г., Бедер У., Линдеманн Л. , Шаласта Г., Даймингер А. .Пренатальная диагностика врожденной цитомегаловирусной инфекции у 189 беременностей с известным исходом. Пренатальная диагностика 2001; 21 : 362–377.
, Шаласта Г., Даймингер А. .Пренатальная диагностика врожденной цитомегаловирусной инфекции у 189 беременностей с известным исходом. Пренатальная диагностика 2001; 21 : 362–377.
КАС Статья Google Scholar
Биндер Н.Д., Бакмастер Дж.В., Бенда Г.И. Исход для плода с асцитом и цитомегаловирусной инфекцией. Педиатрия 1988; 82 : 100–103.
КАС пабмед Google Scholar
Крино JP .Ультразвуковая и фетальная диагностика перинатальной инфекции. Clin Obstet Gynecol 1999; 42 : 71–80.
КАС Статья Google Scholar
Линч Л., Даффос Ф., Эмануэль Д., Джовангранди Ю., Майзель Р., Форестье Ф. и др. . Пренатальная диагностика цитомегаловирусной инфекции плода. Am J Obstet Gynecol 1991; 165 : 714–718.
КАС Статья Google Scholar
Доллард СК, Гросс С. Д., Росс Д.С.Новая оценка распространенности неврологических и сенсорных последствий и смертности, связанной с врожденной цитомегаловирусной инфекцией. Rev Med Virol 2007; 17 : 355–363.
Д., Росс Д.С.Новая оценка распространенности неврологических и сенсорных последствий и смертности, связанной с врожденной цитомегаловирусной инфекцией. Rev Med Virol 2007; 17 : 355–363.
Артикул Google Scholar
Нумадзаки К., Фуджикава Т. . Хронологические изменения заболеваемости и прогноза у детей с бессимптомной врожденной цитомегаловирусной инфекцией в Саппоро, Япония. BMC Infect Dis 2004; 4 : 22.
Артикул Google Scholar
Тагава М., Минематус Т., Масузаки Х., Ишимару Т., Мориучи Х. . Сероэпидемиологическое обследование цитомегаловирусной инфекции среди беременных в г. Нагасаки, Япония. Pediatr Int 2010; 52 : 459–462.
Артикул Google Scholar
Vaulup-Fellous C, Picone O, Cordier AG, Parent-du-Chatelet I, Senat MV, Frydman R et al . Влияет ли консультирование по гигиене на частоту первичной ЦМВ-инфекции во время беременности? Результаты 3-летнего проспективного исследования во французской больнице. Дж Клин Вирол 2009; 46S : S49–S53.
Влияет ли консультирование по гигиене на частоту первичной ЦМВ-инфекции во время беременности? Результаты 3-летнего проспективного исследования во французской больнице. Дж Клин Вирол 2009; 46S : S49–S53.
Артикул Google Scholar
Модель множественной регрессии для прогнозирования высокого уровня авидности иммуноглобулина G цитомегаловируса у беременных с положительным результатом на IgM
https://doi.org/10.1016/j.ijid.2020.08.034Get rights and contentМатематическая модель, представленная в этом исследовании, может прогнозировать вероятность того, что беременные женщины будут иметь высокую авидность CMV IgG с высоким уровнем точности (~97%).
Эта модель чрезвычайно точна в прогнозировании высокого уровня ИИ IgG, что позволяет нам с высокой степенью достоверности заверить беременных женщин, которые мы идентифицировали как низкий риск, сразу после того, как они были протестированы как IgM-положительные.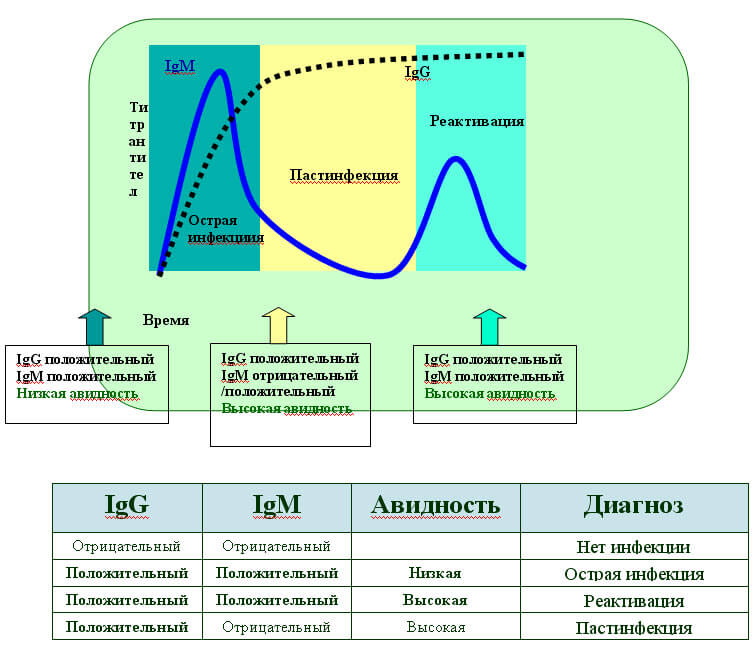
Титр IgM ЦМВ и беременных с одним паритетом были независимыми прогностическими факторами высокой авидности IgG ЦМВ.
Резюме
Цель
Создать модель для прогнозирования высокого индекса авидности (AI) иммуноглобулина (Ig)G цитомегаловируса (ЦМВ) с использованием клинической информации, чтобы способствовать психическому здоровью беременных женщин с положительным результатом на ЦМВ-IgM.
Методы
Мы исследовали 371 женщину с положительной реакцией на IgM на сроке беременности ≤14 недель. Собирали информацию о возрасте, паритете, роде занятий, клинических признаках, значениях IgM и G и IgG AI. Пороговое значение IgG AI для диагностики врожденной инфекции рассчитывали на основе анализа кривой рабочих характеристик приемника. Межгрупповые различия оценивали с помощью критерия Манна-Уитни U или анализа χ 2 . Факторы, предсказывающие высокий AI IgG, определяли с помощью множественной логистической регрессии.
Результаты
Женщины были разделены на группы с высоким и низким уровнем IgG AI на основе порогового значения IgG AI 31,75. Существовали значительные различия в уровнях IgG и IgM, возрасте, клинических признаках и количестве женщин с одним паритетом между двумя группами. В множественном логистическом регрессионном анализе IgM и количество женщин с одним родом были независимыми предикторами. Этот результат помог нам создать математическую модель, которая правильно классифицировала уровень IgG AI для 84,6% женщин.
Заключение
Мы создали высокоэффективную модель для прогнозирования высокого уровня IgG AI сразу после демонстрации положительного результата IgM.
Ключевые слова
Тревога
Цитомегаловирус
Иммуноглобулин М
Беременность
Скрининг
Рекомендованные статьиЦитирование статей (0)
9020 ©. Опубликовано Elsevier Ltd от имени Международного общества инфекционных заболеваний.Рекомендуемые статьи
Ссылки на статьи
Трехлетний обзор крупного ирландского родильного дома третичного уровня
Ретроспективный аудит был проведен для всех акушерских пациенток, у которых в период с января 2012 г. по декабрь 2014 г. были получены положительные результаты IgM ЦМВ в больнице Ротонда. , Ирландия.Всего было проведено 622 положительных теста на CMV IgM на образцах от 572 пациентов. Тридцать семь пациентов имели положительный результат CMV IgM (5,9%) в системе Architect в рамках начального скрининга. Три пациентки были исключены, так как они не были акушерскими пациентами. Из 34 беременных женщин с положительными результатами IgM ЦМВ при первоначальном скрининге у 16 (47%) положительный результат на IgM ЦМВ был подтвержден на второй платформе (VIDAS), а у 18 (53%) — нет. Из 16 пациентов с подтвержденными положительными результатами CMV IgM у четырех (25%) была острая инфекция, у двух (12.5 %) имели инфекцию в неопределенное время, а 10 (62,5 %) имели инфекцию более чем за три месяца до отбора проб, что определялось индексом авидности CMV IgG. У двух из четырех новорожденных женщин с низкой авидностью IgG ДНК ЦМВ была обнаружена в моче. Оба этих случая имели серьезные неврологические повреждения, и показанием для тестирования их матерей было то, что бипариетальный диаметр (ДПР) был меньше 5-го процентиля при обычном 20-недельном сканировании аномалий беременности.
по декабрь 2014 г. были получены положительные результаты IgM ЦМВ в больнице Ротонда. , Ирландия.Всего было проведено 622 положительных теста на CMV IgM на образцах от 572 пациентов. Тридцать семь пациентов имели положительный результат CMV IgM (5,9%) в системе Architect в рамках начального скрининга. Три пациентки были исключены, так как они не были акушерскими пациентами. Из 34 беременных женщин с положительными результатами IgM ЦМВ при первоначальном скрининге у 16 (47%) положительный результат на IgM ЦМВ был подтвержден на второй платформе (VIDAS), а у 18 (53%) — нет. Из 16 пациентов с подтвержденными положительными результатами CMV IgM у четырех (25%) была острая инфекция, у двух (12.5 %) имели инфекцию в неопределенное время, а 10 (62,5 %) имели инфекцию более чем за три месяца до отбора проб, что определялось индексом авидности CMV IgG. У двух из четырех новорожденных женщин с низкой авидностью IgG ДНК ЦМВ была обнаружена в моче. Оба этих случая имели серьезные неврологические повреждения, и показанием для тестирования их матерей было то, что бипариетальный диаметр (ДПР) был меньше 5-го процентиля при обычном 20-недельном сканировании аномалий беременности.
1. Введение
Врожденный ЦМВ (цЦМВ) может иметь разрушительные последствия для пораженных младенцев и их семей, поскольку инфекция может привести к глухоте, серьезным неврологическим нарушениям, а также трудностям в обучении.Крупный систематический обзор сенсоневральной тугоухости показал, что 10–20% случаев были связаны с врожденной ЦМВ, и, таким образом, она оказывает значительное влияние на экономику [1]. Недавно Кимберлин и его коллеги сообщили о преимуществах, связанных с ранним противовирусным лечением ЦМВ, в частности, при потере слуха [2]. Это лечение увеличивает потребность в надежном методе скрининга, чтобы можно было выявить детей, инфицированных ЦМВ при рождении. Было показано, что неонатальный скрининг на ЦМВ-инфекцию с использованием полимеразной цепной реакции (ПЦР) мочи или слюны экономически эффективен при использовании целенаправленного подхода [3–6].Как и в большинстве больниц, мы традиционно использовали систему тестирования на сероконверсию ЦМВ у определенных групп пациентов (например, выкидыш во втором триместре и внутриутробная смерть или дети, рожденные ВИЧ-инфицированными женщинами или женщинами, получавшими иммуносупрессию во время беременности), но у нас нет общая политика дородового или неонатального скрининга.
Недавнее исследование в другом родильном доме в Дублине, Ирландия, показало, что врожденная заболеваемость ЦМВ составила 0,19% при тестировании слюны новорожденных [7].Таким образом, можно рассчитать ожидаемое количество инфицированных младенцев в нашем учреждении и выяснить, сколько из этих случаев было выявлено в рамках нашей текущей программы тестирования. Наша гипотеза заключается в том, что очень мало случаев врожденного ЦМВ выявляется с помощью антенатального серологического тестирования и что многие дети не выявляются в неонатальном периоде, таким образом упуская возможность получить противовирусное лечение.
2. Материалы и методы
Это был ретроспективный аудит всех акушерских пациенток, у которых были положительные результаты CMV IgM в период с января 2012 г. по декабрь 2014 г. в больнице Ротонда, Дублин, Ирландия.Цель состояла в том, чтобы определить показания для первоначального тестирования CMV IgM, а также неонатальный исход. Вторичная цель заключалась в том, чтобы определить, какой процент ожидаемых случаев врожденного ЦМВ был диагностирован с помощью материнской серологии. Основываясь на исследовании Уотерса и его коллег, в нашей больнице ожидается 51 (0,19% × 26 862 живорожденных > 500 г) ребенок с цМВ в течение периода исследования.
Основываясь на исследовании Уотерса и его коллег, в нашей больнице ожидается 51 (0,19% × 26 862 живорожденных > 500 г) ребенок с цМВ в течение периода исследования.
Больница «Ротонда» является специализированным родильным домом третичного уровня, в котором за исследуемый период было зарегистрировано 26 862 живорождений > 500 g.Больница обслуживает разнообразное по этническому признаку население, и в 2012 и 2013 годах 64% и 73% рожавших пациентов, соответственно, были ирландцами. Единственным критерием включения был положительный результат IgM ЦМВ у акушерской пациентки, которую тестировали либо во время беременности, либо сразу после родов (т. е. в условиях выкидыша или внутриутробной смерти). Критериев исключения не было. Пациенты находились под наблюдением до родов, чтобы можно было зарегистрировать исход плода. Для матерей с подтвержденным обнаруживаемым ЦМВ-специфическим IgM регистрировали результаты анализа мочи на ДНК ЦМВ у новорожденного.Это считалось подтверждением ЦМВ у новорожденного, если оно проводилось в первые 21 день жизни.
Положительные результаты CMV IgM были выявлены после электронного поиска в Лабораторной информационной системе больницы Ротонда, которую посещали пациенты. Серологическое тестирование проводилось в Национальной справочной лаборатории по вирусам в Ирландии (NVRL). Тестирование CMV IgM сначала проводилось на системе Architect (Abbott Diagnostics), а затем подтверждалось на VIDAS (BioMerieux, Франция).Это был стандартный алгоритм, действовавший во время тестирования всех клинических образцов. Анализ мочи на ДНК ЦМВ проводили с использованием набора Artus на системе ABI 7500 FAST Real-Time PCR. Все тесты проводились в соответствии с инструкциями производителей.
В соответствии с больничными рекомендациями, тестирование на IgM цитомегаловируса проводят во всех случаях аномальных результатов антенатального ультразвукового исследования, таких как задержка внутриутробного развития, эхогенность кишечника, микроцефалия и сердечные аномалии.Его также обычно запрашивают в необъяснимых случаях внезапной внутриутробной смерти; у женщин с выкидышами во втором триместре; и у некоторых пациентов с трансаминитом. Диагностическими критериями ЦМВ-инфекции у матери считались подтвержденные положительные результаты CMV IgM в двух различных анализах (Architect и VIDAS), как указано выше. Образцы, показавшие положительные результаты на Architect, но не подтвержденные на Vidas, были исключены из исследования. После подтверждения результата CMV IgM было проведено тестирование авидности CMV IgG (VIDAS, BioMerieux).Диагноз недавней (определяемой как в течение трех месяцев с даты взятия пробы) ЦМВ-инфекции ставился, если индекс авидности составлял ≤0,4. Считалось, что пациенты с индексом авидности ≥0,65 были инфицированы более чем за три месяца до отбора проб, в то время как пациенты с сомнительным индексом авидности (между 0,4 и 0,6) считались инфицированными ЦМВ в какой-то момент, но время могло измениться. не определяться.
Диагностическими критериями ЦМВ-инфекции у матери считались подтвержденные положительные результаты CMV IgM в двух различных анализах (Architect и VIDAS), как указано выше. Образцы, показавшие положительные результаты на Architect, но не подтвержденные на Vidas, были исключены из исследования. После подтверждения результата CMV IgM было проведено тестирование авидности CMV IgG (VIDAS, BioMerieux).Диагноз недавней (определяемой как в течение трех месяцев с даты взятия пробы) ЦМВ-инфекции ставился, если индекс авидности составлял ≤0,4. Считалось, что пациенты с индексом авидности ≥0,65 были инфицированы более чем за три месяца до отбора проб, в то время как пациенты с сомнительным индексом авидности (между 0,4 и 0,6) считались инфицированными ЦМВ в какой-то момент, но время могло измениться. не определяться.
У новорожденных инфицирование цМВ считалось подтвержденным, если ДНК ЦМВ обнаруживалась с помощью ПЦР в моче в первый 21 день жизни.Для целей данного исследования у новорожденных, рожденных от матерей с положительными результатами IgM ЦМВ, были зарегистрированы только результаты ДНК ЦМВ мочи.
Данные записывались в электронном виде в Microsoft Excel, выполнялась только описательная статистика. Статистику хи-квадрат проводили для сравнения статуса паритета с использованием программного обеспечения MedCalc, версия 15.6.1.
3. Результаты
За период исследования с января 2012 г. по декабрь 2014 г. было зарегистрировано 26 862 живорождений >500 g.Разбивка результатов CMV IgM показана в таблице 1. Всего было проведено 622 положительных теста CMV IgM на образцах от 572 пациентов. Было 37 пациентов с положительным результатом CMV IgM (5,9%) на системе Architect в рамках начального скрининга. Три пациентки были исключены, поскольку они не были акушерскими больными: из оставшихся 34 было 32 одноплодные беременности и 2 многоплодные беременности.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Средний возраст 34 пациентов с обнаруживаемым ЦМВ IgM составил 30 лет с межквартильным диапазоном 25–34 года (диапазон 19–43 года). Из 34 пациентов 22 были белыми ирландцами (65%), шесть (17%) были белыми неирландцами, двое (6%) были небелыми азиатами и четверо (12%) были неизвестны. Медиана беременности при тестировании составляла 28 недель с межквартильным диапазоном от 17 до 33 недель (диапазон 6–41 неделя). Срок беременности на момент родов был доступен для 30 из 34 матерей со средним сроком беременности 37 недель и межквартильным диапазоном 31–38 недель (диапазон 15–41 недель). Семь (21,8%) из 32 женщин были первородящими, а у двух женщин предыдущая акушерская история не была доступна.По сравнению с больничной статистикой за 2013 год, в которой 3689 из 8648 (42,7%) женщин были нерожавшими, у женщин с положительным результатом IgM ЦМВ был статистически значимо более высокий уровень многоплодия (= 4,81, ). Наиболее распространенной причиной подозрения на ЦМВ-инфекцию была задержка внутриутробного развития (ЗВУР) (1), наблюдаемая при антенатальном сканировании, за которой следовали повышенные ферменты печени (2) и внутриутробная гибель (4) (Таблица 2).
Из 34 пациентов 22 были белыми ирландцами (65%), шесть (17%) были белыми неирландцами, двое (6%) были небелыми азиатами и четверо (12%) были неизвестны. Медиана беременности при тестировании составляла 28 недель с межквартильным диапазоном от 17 до 33 недель (диапазон 6–41 неделя). Срок беременности на момент родов был доступен для 30 из 34 матерей со средним сроком беременности 37 недель и межквартильным диапазоном 31–38 недель (диапазон 15–41 недель). Семь (21,8%) из 32 женщин были первородящими, а у двух женщин предыдущая акушерская история не была доступна.По сравнению с больничной статистикой за 2013 год, в которой 3689 из 8648 (42,7%) женщин были нерожавшими, у женщин с положительным результатом IgM ЦМВ был статистически значимо более высокий уровень многоплодия (= 4,81, ). Наиболее распространенной причиной подозрения на ЦМВ-инфекцию была задержка внутриутробного развития (ЗВУР) (1), наблюдаемая при антенатальном сканировании, за которой следовали повышенные ферменты печени (2) и внутриутробная гибель (4) (Таблица 2).
+
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Клинические результаты дети 34 женщин показан в Таблице 1. Из этих 34 пациентов у 16 (47%) положительный результат на IgM ЦМВ был подтвержден на второй платформе (VIDAS), а у 18 (53%) — нет. Из 16 пациентов с подтвержденными положительными результатами CMV IgM у четырех (25%) была острая инфекция, у двух (12,5%) инфекция была неопределенной по времени, и у десяти (62,5%) была инфекция более чем за три месяца до отбора проб, как определено Индекс авидности CMV IgG.
Из этих 34 пациентов у 16 (47%) положительный результат на IgM ЦМВ был подтвержден на второй платформе (VIDAS), а у 18 (53%) — нет. Из 16 пациентов с подтвержденными положительными результатами CMV IgM у четырех (25%) была острая инфекция, у двух (12,5%) инфекция была неопределенной по времени, и у десяти (62,5%) была инфекция более чем за три месяца до отбора проб, как определено Индекс авидности CMV IgG.
У двух из четырех новорожденных женщин с низкой авидностью IgG ДНК ЦМВ была обнаружена в моче. Оба этих случая имели серьезные неврологические повреждения, и показанием для тестирования их матерей было то, что бипариетальный диаметр (ДПР) был меньше 5-го процентиля при обычном 20-недельном сканировании аномалий беременности.В двух случаях у матерей с низкой авидностью CMV IgG, но без ДНК CMV, обнаруженной в неонатальной моче, оба плода имели BPD выше 30-го центиля при 20-недельном сканировании аномалий. Показаниями для тестирования у матерей этих двух здоровых детей были материнская просьба, а асимметричная ЗВУР была отмечена при рутинном антенатальном УЗИ на 31 неделе беременности. У трех из четырех новорожденных, рожденных от матерей с высокой авидностью CMV IgG, были проведены ПЦР-тесты мочи на ЦМВ, и все они были отрицательными у этих здоровых живорожденных детей.
У трех из четырех новорожденных, рожденных от матерей с высокой авидностью CMV IgG, были проведены ПЦР-тесты мочи на ЦМВ, и все они были отрицательными у этих здоровых живорожденных детей.
4. Заключение
Это исследование показало, что за трехлетний период, в течение которого было зарегистрировано 26 862 живорождений > 500 г, при условии, что заболеваемость ирландской цМВ-инфекцией составляет 0,19% [7], тогда только двое из ожидаемых 51 врожденно инфицированных младенцев выявлено за период исследования. Примечательно, что у двух матерей врожденно инфицированных младенцев IgM были положительными в первые 15 недель беременности. Это подчеркивает тот факт, что, поскольку заражение ЦМВ в первом триместре обычно протекает наиболее тяжело, ранняя инфекция во время беременности, скорее всего, будет обнаружена на основе клинически направленного целевого скрининга, как это в настоящее время имеет место в нашей больнице.
Два основных ограничения этого исследования заключаются в том, что оно является ретроспективным и что показания к тестированию не соответствуют рекомендациям по тестированию. Например, рекомендуется проводить скрининг на врожденный ЦМВ при невынашивании беременности во втором триместре. Было бы интересно изучить этих пациентов в будущем, чтобы попытаться определить роль, если таковая имеется, ЦМВ в выкидыше или внутриутробной смерти. В результате может быть чрезмерная представленность внутриутробных смертей среди изученных пациенток. Кроме того, две матери в исследовании, у которых были подтверждены положительные результаты CMV IgM, были потеряны для последующего наблюдения, и неясно, каковы были неонатальные исходы у этих пациенток.В течение периода исследования иммуноблот CMV IgM не проводился для окончательной классификации случаев, и это можно было бы сделать в рамках будущих исследований, чтобы помочь определить, представляют ли случаи новую инфекцию или реактивацию. Поскольку это было ретроспективное исследование, использовался алгоритм тестирования, существовавший в то время, хотя в настоящее время могут быть доступны другие алгоритмы тестирования. Также повторное тестирование CMV IgG не проводилось у всех пациентов для демонстрации сероконверсии.
Например, рекомендуется проводить скрининг на врожденный ЦМВ при невынашивании беременности во втором триместре. Было бы интересно изучить этих пациентов в будущем, чтобы попытаться определить роль, если таковая имеется, ЦМВ в выкидыше или внутриутробной смерти. В результате может быть чрезмерная представленность внутриутробных смертей среди изученных пациенток. Кроме того, две матери в исследовании, у которых были подтверждены положительные результаты CMV IgM, были потеряны для последующего наблюдения, и неясно, каковы были неонатальные исходы у этих пациенток.В течение периода исследования иммуноблот CMV IgM не проводился для окончательной классификации случаев, и это можно было бы сделать в рамках будущих исследований, чтобы помочь определить, представляют ли случаи новую инфекцию или реактивацию. Поскольку это было ретроспективное исследование, использовался алгоритм тестирования, существовавший в то время, хотя в настоящее время могут быть доступны другие алгоритмы тестирования. Также повторное тестирование CMV IgG не проводилось у всех пациентов для демонстрации сероконверсии.
Результаты, показанные в этом исследовании, показывают, что необходима альтернатива текущему подходу, если все или, по крайней мере, большая часть случаев ЦМВ должны быть выявлены в неонатальном периоде, что позволяет при необходимости проводить раннее противовирусное лечение.Низкая частота выявления случаев cCMV, описанных здесь, разочаровывает. Универсальное тестирование мочи или слюны на ДНК ЦМВ у новорожденных в послеродовых отделениях повысит уровень выявления случаев ЦМВ.
Следует проявлять осторожность при попытке распространить эти результаты на другие группы населения, поскольку необходимо учитывать фоновую серопозитивность ЦМВ, а также этническую принадлежность. Известно, что показатели распространенности ЦМВ среди беременных женщин в Ирландии низкие по международным стандартам [7].По мере улучшения лечения cCMV становится более важным раннее выявление новорождённых и возможность уменьшения или сведения к минимуму любой потери слуха. Существующий подход к обнаружению cCMV является субоптимальным, и необходимо изучить другие потенциальные методы скрининга, такие как анализ ДНК ЦМВ мочи/слюны новорожденных.
Этическое одобрение
Это исследование было одобрено Советом по этике больницы Ротонда (REC-2014-012).
Раскрытие информации
Для этого проекта не было получено финансирования, и лабораторные исследования проводились в рамках плановой клинической помощи.
Конфликт интересов
Ни у кого из авторов нет конфликта интересов в отношении данного проекта.
Благодарности
Авторы хотели бы поблагодарить сотрудников лаборатории больницы Ротонда и Национальной справочной лаборатории по вирусам за их помощь.
| Случай 60-80% инфицированы ЦМВ в развитых странах и почти 100% в развивающихся странах. Внутриутробная инфекция встречается в Европе в 0,5-2% случаев, а у 10-15% врожденно инфицированных новорожденных будут симптомы. Приблизительно 10-20% умирают, и по крайней мере две трети будут иметь неврологические нарушения. Нарушения слуха можно увидеть у младенцев бессимптомно при рождении.  ЕСЛИ МАТЬ ЗАРАЖАЕТСЯ ПЕРВИЧНОЙ ИНФЕКЦИЕЙ ЦМВ ЕСЛИ МАТЬ ЗАРАЖАЕТСЯ ПЕРВИЧНОЙ ИНФЕКЦИЕЙ ЦМВ Материнские симптомы: Инкубационный период 4-8 недель. Наиболее распространенные бессимптомные или мононуклеозоподобные симптомы могут развиваться, особенно у матерей с иммунодефицитом. Внутриутробные инфекции после первичных инфекций возникают в 33% случаев в первом триместре и в 44% — в третьем триместре. У 7% женщин с первичной инфекцией плод будет сильно поврежден с врожденным ЦМВ. ЦМВ может присутствовать в грудном молоке, при этом от 25% до 70% серопозитивных женщин выделяют ЦМВ на той или иной стадии. ЦМВ редко обнаруживается в молозиве. Если ЦМВ выделяется в молоке, риск заражения высок (50 процентов), но последствия для ребенка незначительны. При врожденной цитомегаловирусной инфекции у половины матерей первичная инфекция. Более половины матерей имеют антитела против ЦМВ. Заразен только при интимном контакте (поцелуй, половой акт, роды, кормление грудью и др.  ) Выделение ЦМВ со слюной и мочой в детских садах от 10-80 %. ) Выделение ЦМВ со слюной и мочой в детских садах от 10-80 %. Зараженный младенец выделяет вирус со слюной и мочой в течение нескольких лет. Трансмиссия: Более вероятны те, у кого ЦМВ выделяется из шейки матки или влагалища во время родов, и, по оценкам, 50% детей, рожденных от этих матерей, могут заразиться инфекцией.Повторное заражение младенца при следующей беременности крайне редко. Послеродовые инфекции безвредны. Крайне недоношенные дети были определены как риск тяжелых инфекций. Ультразвуковые маркеры: Церебральная вентрикуломегалия. Микроцефальная гиперэхогенная гепатоспленомегалия кишечника, асцит, внутричерепная кальцификация, ЗВУР, но нормальное УЗИ не исключает неонатальную аномалию. У половины детей с симптомами синдром цитомегалических включений, состоящий из:

Обнаружение вируса (культура вируса, CMV-ANA (ПЦР) или CMV-IgM) (моча, кровь, ткань) в первые 2 недели после родов указывает на врожденную инфекцию.  Обычно требуется от одного до трех дней инкубации, чтобы получить ответ для культуры. Обычно требуется от одного до трех дней инкубации, чтобы получить ответ для культуры. CMV-IgM может быть продемонстрирован у 70% детей с врожденным ЦМВ и у всех, у кого позже разовьются осложнения. Тем не менее, подтверждающая вирусная культура все же должна быть проводится из-за ложноположительных и ложноотрицательных возникают результаты. ДНК ЦМВ с помощью ПЦР, вероятно, идентифицирует младенцев, за которыми необходимо наблюдать для неврологической оценки и потери слуха. ПРОФИЛАКТИКА Отсутствие риска для персонала при соблюдении норм гигиены. Не целуйте других детей в губы и не пробуйте ложку во время кормления. Не ешьте остатки детского питания. Лечение: Лечение не рекомендовано, но были обнаружены многообещающие результаты по предотвращению высокого процента поздней потери слуха при лечении новорожденных ганцикловиром. Перспективно использование анти-ЦМВ гипериммунного глобулина для лечения и профилактики врожденной инфекции.  Валганцикловер и иммуноглобулин кажутся многообещающими, если признаки со стороны ЦНС присутствуют при рождении, такие как ретинит, потеря слуха, сепсис и рефрактерная тромбоцитопения. Каталожные номера: (1) Аллан Маклин и др. Инфекция и беременность, RCOG Press, 2001. (2) Дафф, П. Продуманный алгоритм для точной диагностики первичной ЦМВ-инфекции во время беременности. Am J Obstet Gynecol 2007 (3) Guerra B. Влияние диагностических и подтверждающих тестов и дородового консультирования на частоту прерывания беременности среди женщин с положительными титрами антител к иммуноглобулину М цитомегаловируса. Am J Obstet Gynecol 2007 (4) www.infpreg.com (5) www.uptodate.com 2007 г. Не стесняйтесь, пишите мне веб-мастеру, доктору Ларсу Крэгу Мёллеру, если у вас есть исправления, которые могут улучшить руководство. |
Проблемы со скринингом матери на врожденную цитомегаловирусную инфекцию — ScienceDaily
Цитомегаловирус человека (ЦМВ) является распространенным вирусом, встречающимся во всем мире. Когда ЦМВ поражает плод, это может вызвать серьезные осложнения, такие как проблемы со слухом и умственная отсталость у пораженных младенцев.Группа исследователей впервые оценила эффективность универсального материнского скрининга с использованием тестов на авидность IgG ЦМВ для врожденной ЦМВ-инфекции, а также выявила проблемы с текущими методами скрининга материнского ЦМВ.
Когда ЦМВ поражает плод, это может вызвать серьезные осложнения, такие как проблемы со слухом и умственная отсталость у пораженных младенцев.Группа исследователей впервые оценила эффективность универсального материнского скрининга с использованием тестов на авидность IgG ЦМВ для врожденной ЦМВ-инфекции, а также выявила проблемы с текущими методами скрининга материнского ЦМВ.
Исследование проводили профессор ЯМАДА Хидето (кафедра акушерства и гинекологии Высшей школы медицины Университета Кобе), доцент ТАНИМУРА Кендзи (Центр перинатальной помощи больницы Университета Кобе), профессор проекта МОРИОКА Итиро (Высшая школа медицины, кафедра педиатрии) и доктор МИНЕМАЦУ Тошио (директор Исследовательского центра по контролю заболеваний больницы Айсенкай Нитинан).
Риск передачи ЦМВ плоду наиболее высок у матерей, впервые заразившихся вирусом во время беременности (первичная инфекция), но результаты этого исследования показывают, что ряд матерей, имеющих инфицированные плоды, уже были инфицированы ранее беременность (не первичная инфекция). Методы скрининга, которые направлены только на выявление женщин с первичной инфекцией во время беременности, могут не учитывать эти случаи. Эти результаты были опубликованы в Clinical Infectious Diseases 20 июля.
Методы скрининга, которые направлены только на выявление женщин с первичной инфекцией во время беременности, могут не учитывать эти случаи. Эти результаты были опубликованы в Clinical Infectious Diseases 20 июля.
В последнее время неврологические осложнения, вызванные врожденной ЦМВ-инфекцией у пораженных младенцев, успешно лечили противовирусными препаратами, но ранняя диагностика врожденной инфекции жизненно важна для эффективности этого лечения. Для выявления первичной ЦМВ-инфекции широко используют анализы крови матери на ЦМВ-специфические антитела иммуноглобулина (Ig) М (CMV IgM). Однако тесты на CMV IgM могут оставаться положительными в течение многих лет после первичной инфекции, поэтому положительный результат на CMV IgM не всегда указывает на первичную инфекцию во время беременности.Тест на авидность CMV IgG также используется для выявления недавней инфекции. Это исследование было направлено на определение эффективности тестов на авидность CMV IgG в качестве универсального скрининга матери на врожденную ЦМВ-инфекцию.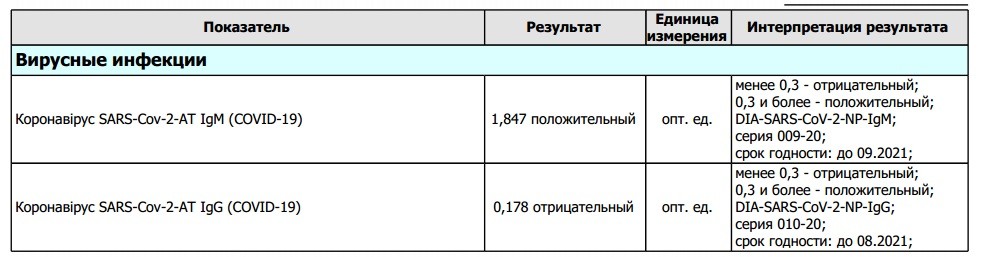
В исследовательскую группу были включены 2193 беременных женщины. Они проводили тесты на антитела CMV IgG (CMV IgG) до 22 недель беременности (GW), и если тесты были отрицательными, женщинам говорили, как избежать заражения ЦМВ, и снова тестировали на CMV IgG в 34-36 GW. Если они давали положительный результат на CMV IgG во втором тесте, считалось, что у них была первичная инфекция во время беременности.
Женщинам с положительным результатом теста на CMV IgG были проведены тесты на авидность CMV IgG. При индексе авидности 45% и менее добавляли тесты на CMV IgM, а при индексе авидности менее 35% и/или положительном результате на CMV IgM считали, что у женщины первичное инфицирование во время беременности. Если их индекс авидности превышал 45%, это расценивали как хроническую инфекцию (заражение до беременности). Они также измерили CMV IgM в хранящихся образцах сыворотки, чтобы сравнить эффективность материнского скрининга с использованием тестов на авидность и с помощью тестов на CMV IgM.
Из 2193 субъектов у 10 младенцев была врожденная ЦМВ-инфекция. В общей сложности у 93 женщин была выявлена первичная ЦМВ-инфекция во время беременности. Среди этих субъектов 3 родили младенцев с врожденной инфекцией. С другой стороны, среди 1287 человек с непервичной инфекцией было 7 случаев с врожденной инфекцией. Скрининг с использованием теста на авидность имел такой же уровень диагностической точности, как и скрининг с использованием CMV IgM.
Эти результаты показывают, что стандартные методы материнского скрининга, которые выявляют беременных женщин с первичной ЦМВ-инфекцией во время беременности, могут предсказать только 3 случая врожденной инфекции, а остальные 7 случаев не учитывались.
Для выявления всех младенцев с врожденной ЦМВ-инфекцией при рождении существуют ограничения на современные методы скрининга, используемые для беременных женщин. Нам нужно изменить нашу стратегию, например, используя ПЦР-тесты, которые нацелены на всех новорожденных, обнаруживая вирус в их моче. Основываясь на этих выводах, исследователи планируют разработать более комплексный метод скрининга врожденной ЦМВ-инфекции, позволяющий раннее выявление и лечение заболевания.
Основываясь на этих выводах, исследователи планируют разработать более комплексный метод скрининга врожденной ЦМВ-инфекции, позволяющий раннее выявление и лечение заболевания.
Источник истории:
Материалы предоставлены Университетом Кобе . Примечание. Содержимое можно редактировать по стилю и длине.
Транзиторный волчаночный антикоагулянт и ложноположительный результат Тесты на антитела к цитомегаловирусу в Эпсте-ин-Барр Вирус инфекционного мононуклеоза
Ann Hematol Oncol. 2019; 6(1): 1227.
* Автор, ответственный за переписку: Zafer Bicakci, Департамент Детская гематология и онкология, Университет им. Кафки, Медицинский факультет, Карс, Турция
Поступила в редакцию: 03 декабря 2018 г.; Принято: 21 января 2019 г .; Опубликовано: 28 января 2019 г.
Аннотация
Инфекционный мононуклеоз может быть связан с вирусом Эпштейна-Барра (EBV),
а также цитомегаловирус (ЦМВ) и может привести к развитию
Волчаночный антикоагулянт (LA) или антитела к кардиолипину. Белки ЦМВ могут
также реагируют с антителами IgM против ВЭБ во время ферментативно-связанной
Иммуносорбентный анализ (ИФА). Может быть трудно дифференцировать
инфекции, вызванные любым вирусом, поскольку они имеют очень похожее клиническое течение
с аналогичными результатами лабораторных испытаний. В данном исследовании мы представляем трехлетнего
девочка с ВЭБ-индуцированным инфекционным мононуклеозом. Лабораторные исследования показали
наличие транзиторного волчаночного антикоагулянта (длительное АЧТВ) и привело к
ложноположительный результат на антитела к цитомегаловирусу.У нее была гепатоспленомегалия,
повышение активности трансаминаз, атипичный лимфоцитоз (78%), длительный частичный
Тромбопластиновое время (аЧТВ) и лабораторный тест на ЛА были положительными. То
лабораторные исследования на выявление вирусов показали CMV IgM (+), CMV ПЦР (-), EBV VCA
IgM (+) и EBV VCA IgG (+). Примерно через месяц после начала заболевания
повышение трансаминаз и пролонгация АЧТВ нормализовались,
и гепатоспленомегалия разрешилась.
Белки ЦМВ могут
также реагируют с антителами IgM против ВЭБ во время ферментативно-связанной
Иммуносорбентный анализ (ИФА). Может быть трудно дифференцировать
инфекции, вызванные любым вирусом, поскольку они имеют очень похожее клиническое течение
с аналогичными результатами лабораторных испытаний. В данном исследовании мы представляем трехлетнего
девочка с ВЭБ-индуцированным инфекционным мононуклеозом. Лабораторные исследования показали
наличие транзиторного волчаночного антикоагулянта (длительное АЧТВ) и привело к
ложноположительный результат на антитела к цитомегаловирусу.У нее была гепатоспленомегалия,
повышение активности трансаминаз, атипичный лимфоцитоз (78%), длительный частичный
Тромбопластиновое время (аЧТВ) и лабораторный тест на ЛА были положительными. То
лабораторные исследования на выявление вирусов показали CMV IgM (+), CMV ПЦР (-), EBV VCA
IgM (+) и EBV VCA IgG (+). Примерно через месяц после начала заболевания
повышение трансаминаз и пролонгация АЧТВ нормализовались,
и гепатоспленомегалия разрешилась.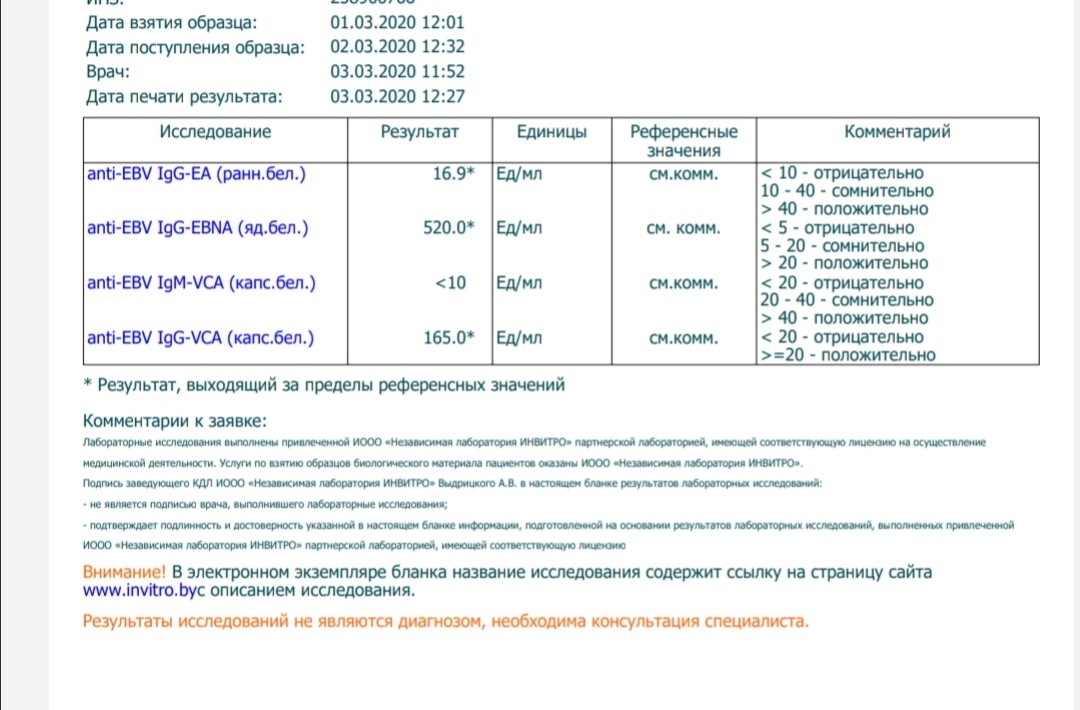 Примерно через пять месяцев после
В начале заболевания волчаночный антикоагулянт и CMV IgM не были положительными.Нет
таких осложнений, как тромбоз или кровотечение, не наблюдалось. В заключении;
поликлональная активация В-лимфоцитов при инфекционном мононуклеозе ВЭБ может привести к
в развитии преходящего волчаночного антикоагулянта (длительного АЧТВ), а также
ложноположительные тесты на антитела к цитомегаловирусу из-за антигенного сходства
между этими двумя вирусами.
Примерно через пять месяцев после
В начале заболевания волчаночный антикоагулянт и CMV IgM не были положительными.Нет
таких осложнений, как тромбоз или кровотечение, не наблюдалось. В заключении;
поликлональная активация В-лимфоцитов при инфекционном мононуклеозе ВЭБ может привести к
в развитии преходящего волчаночного антикоагулянта (длительного АЧТВ), а также
ложноположительные тесты на антитела к цитомегаловирусу из-за антигенного сходства
между этими двумя вирусами.
Ключевые слова: вирус Эпштейна-Барр; Инфекционный мононуклеоз; волчанка антикоагулянт; Цитомегаловирус
Введение
Вирус Эпштейна-Барр (ВЭБ) и цитомегаловирус (ЦМВ),
члены семейства вирусов герпеса, являются наиболее распространенными вирусами
которые вызывают инфекционный мононуклеоз (ЭМ), характеризующийся лихорадкой,
фарингит и лимфаденопатия.Не менее 90% мировых
население инфицировано ВЭБ/ЦМВ. Болезнь может трансформироваться
в латентную форму после первичной инфекции и может реактивироваться
после многих лет в состояниях, связанных с иммунодефицитами. Первичная инфекция может также возникнуть вскоре в младенчестве после
элиминация материнских антител. ВЭБ является наиболее распространенным
Причина инфекционного мононуклеоза в детском возрасте. Первичный ЦМВ
инфекции составляют 7% синдромов мононуклеоза, проявляющихся
симптомы настолько похожи на EBV-индуцированный мононуклеоз, что
практически невозможно провести дифференциальный диагноз [1].
Первичная инфекция может также возникнуть вскоре в младенчестве после
элиминация материнских антител. ВЭБ является наиболее распространенным
Причина инфекционного мононуклеоза в детском возрасте. Первичный ЦМВ
инфекции составляют 7% синдромов мононуклеоза, проявляющихся
симптомы настолько похожи на EBV-индуцированный мононуклеоз, что
практически невозможно провести дифференциальный диагноз [1].
Известно, что вирусные инфекции вызывают появление антифосфолипидные антитела (аФЛ) у взрослых и детей [2]. АФЛ часто преходящие, особенно у детей после перенесенного вирусного инфекций [3]. Сообщалось, что уровни APL столь же высоки, как 30-60% при острых инфекциях, вызванных вирусом Эпштейна-Барра (ВЭБ) [4]. Преходящий волчаночный антикоагулянт может быть обнаружен из-за поликлонального Индуцированная ВЭБ-инфекцией активация В-лимфоцитов [5].
Циркулирующие волчаночные антикоагулянты (LA) вместе с анти-
Антитела к кардиолипину (aCL) образуют подмножество гетерогенных
группа аутоантител, называемая антифосфолипидными антителами (аФЛ). Эти
вырабатываются антитела против фосфолипидзависимых белков плазмы,
в основном протромбин или β2-гликопротеин I, и ингибируют некоторые
vitro фосфолипидзависимые реакции свертывания крови (обычно
превращение протромбина в тромбин), что приводит к длительному
активированное частичное тромбопластиновое время (аЧТВ). APL также были
сообщалось в связи с несколькими клиническими состояниями, включая
вирусные инфекции, аутоиммунные заболевания и злокачественные новообразования; а также
у здоровых на вид лиц (первичный антифосфолипидный синдром)
[2].
Эти
вырабатываются антитела против фосфолипидзависимых белков плазмы,
в основном протромбин или β2-гликопротеин I, и ингибируют некоторые
vitro фосфолипидзависимые реакции свертывания крови (обычно
превращение протромбина в тромбин), что приводит к длительному
активированное частичное тромбопластиновое время (аЧТВ). APL также были
сообщалось в связи с несколькими клиническими состояниями, включая
вирусные инфекции, аутоиммунные заболевания и злокачественные новообразования; а также
у здоровых на вид лиц (первичный антифосфолипидный синдром)
[2].
LA или aCL могут встречаться как при EBV, так и при ЦМВ-инфекциях.
[2]. Клинические проявления цитомегаловирус-ассоциированного
мононуклеозоподобный синдром имеет много общих клинических черт с
классического ВЭБ-индуцированного инфекционного мононуклеоза. Кроме
аналогичные гематологические и печеночные данные при инфекциях, вызванных
обоих этих вирусов, первичная инфекция EBV также может индуцировать
появление перекрестной реакции с низкими титрами ЦМВ-IgM [6].
В этом случае мы хотели представить трехлетнюю девочку. пациенты с ВЭБ-индуцированным инфекционным мононуклеозом, у которых выявлены транзиторный волчаночный антикоагулянт (пролонгированное АЧТВ) и ложноположительные тесты на антитела к цитомегаловирусу.
Отчет о болезни
Трехлетнюю девочку госпитализировали в другую больницу
в течение четырех дней из-за высокой температуры, усталости, тонзиллита и отека в
веки. Лабораторные данные включали количество лейкоцитов.
8500×109/л и количество тромбоцитов 192×109/л. Уровни
гемоглобин и гематокрит были 12,5 г/дл и 37% соответственно.
Следующие лабораторные значения включали АСТ 85 ЕД/л, АЛТ 98 ЕД/л,
Общий билирубин (T.bil) 0,57 мг/дл и прямой билирубин (D.bil) 0,28
мг/дл.Анализ мочи на белок отрицательный. После оценки
клинико-лабораторных данных больному поставлен диагноз
с тонзиллитом. Поскольку жалобы больной продолжались, она была
поступил в нашу больницу через день со следующими результатами
в том числе легкий отек век, отек миндалин, миндалины
экссудат крипт, гепатомегалия (расширение на 2 см книзу под последним
ребро справа) и спленомегалия (расширение на 1 см под последним
ребро слева).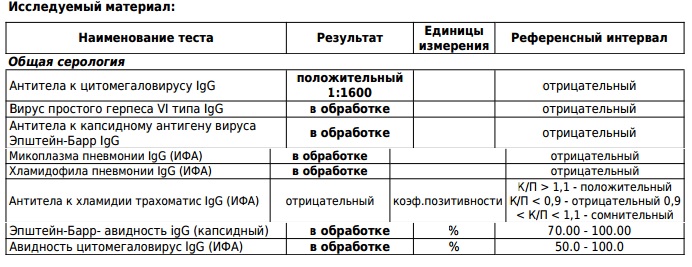 В периферических венах обнаруживаются атипичные лимфоциты.
мазок и повышенный уровень трансаминаз присутствовали.Инфекционный
В диагнозе учитывался мононуклеоз. Следующие результаты
были обнаружены в том числе ЦМВ IgG (+), ЦМВ IgM (+), ПЦР ЦМВ (-),
EBV VCA IgM (+) и EBV VCA IgG (+). Обычные тесты на коагуляцию
показали пролонгированное АЧТВ, однако уровни фибриногена и D-димера
были нормальными. Пролонгированный уровень АЧТВ определяли в разведении 1:1.
плазмы пациента нормальной человеческой плазмой. Анализ смешивания
не улучшали АЧТВ, что свидетельствует о присутствии антикоагулянтов в
кровообращение, исключающее дефицит фактора свертывания крови.Уровни
факторы свертывания крови, которые потенциально могли повлиять на АЧТВ
(VIII, IX, XI и XII) также были в норме. Тесты на внутреннюю коагуляцию
ингибиторы фактора были отрицательными. Волчаночный антикоагулянт – 112,6 сек.
(<44), скрининг на волчанку составил 112,6 с (
В периферических венах обнаруживаются атипичные лимфоциты.
мазок и повышенный уровень трансаминаз присутствовали.Инфекционный
В диагнозе учитывался мононуклеоз. Следующие результаты
были обнаружены в том числе ЦМВ IgG (+), ЦМВ IgM (+), ПЦР ЦМВ (-),
EBV VCA IgM (+) и EBV VCA IgG (+). Обычные тесты на коагуляцию
показали пролонгированное АЧТВ, однако уровни фибриногена и D-димера
были нормальными. Пролонгированный уровень АЧТВ определяли в разведении 1:1.
плазмы пациента нормальной человеческой плазмой. Анализ смешивания
не улучшали АЧТВ, что свидетельствует о присутствии антикоагулянтов в
кровообращение, исключающее дефицит фактора свертывания крови.Уровни
факторы свертывания крови, которые потенциально могли повлиять на АЧТВ
(VIII, IX, XI и XII) также были в норме. Тесты на внутреннюю коагуляцию
ингибиторы фактора были отрицательными. Волчаночный антикоагулянт – 112,6 сек.
(<44), скрининг на волчанку составил 112,6 с (
Цитомегаловирус — американский семейный врач
1.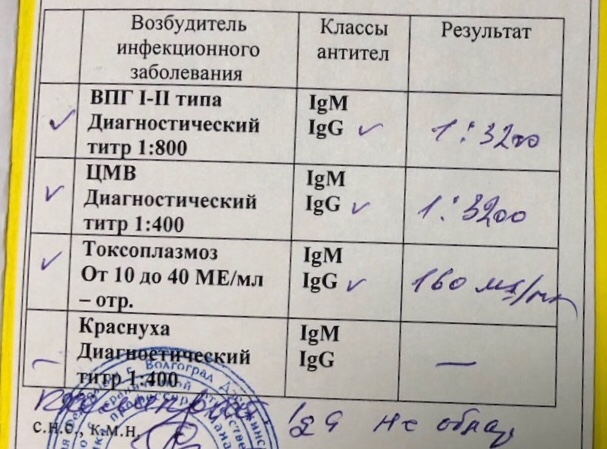 de Jong MD,
Галассо Г.Дж.,
Газзар Б,
Полиция Гриффитса,
Джабс Д.А.,
Керн ER,
Спектор СА.
Итоги II Международного симпозиума по цитомегаловирусу. Противовирусный рез .
1998; 39: 141–62 ….
de Jong MD,
Галассо Г.Дж.,
Газзар Б,
Полиция Гриффитса,
Джабс Д.А.,
Керн ER,
Спектор СА.
Итоги II Международного симпозиума по цитомегаловирусу. Противовирусный рез .
1998; 39: 141–62 ….
2. Бэйл Дж. Ф. Младший, Петерам С.Дж., Соуза ИП, Мерф младший. Цитомегаловирусная реинфекция у детей раннего возраста. J Педиатр . 1996; 128:347–52.
3. Адлер СП. Цитомегаловирус и детский сад. Доказательства повышенного уровня инфицирования среди работников дневного ухода. N Английский J Med . 1989; 321:1290–6.
4. Бэйл Дж. Ф. младший, Циммерман Б, Доусон Дж.Д., Соуза ИП, Петерам С.Дж., Мерф младший.Передача цитомегаловируса в детских домах. Arch Pediatr Adolesc Med . 1999; 153:75–79.
5. Балкарек КБ,
Бэгли Р,
Облачная ГА,
Пройти РФ.
Цитомегаловирусная инфекция среди сотрудников детской больницы.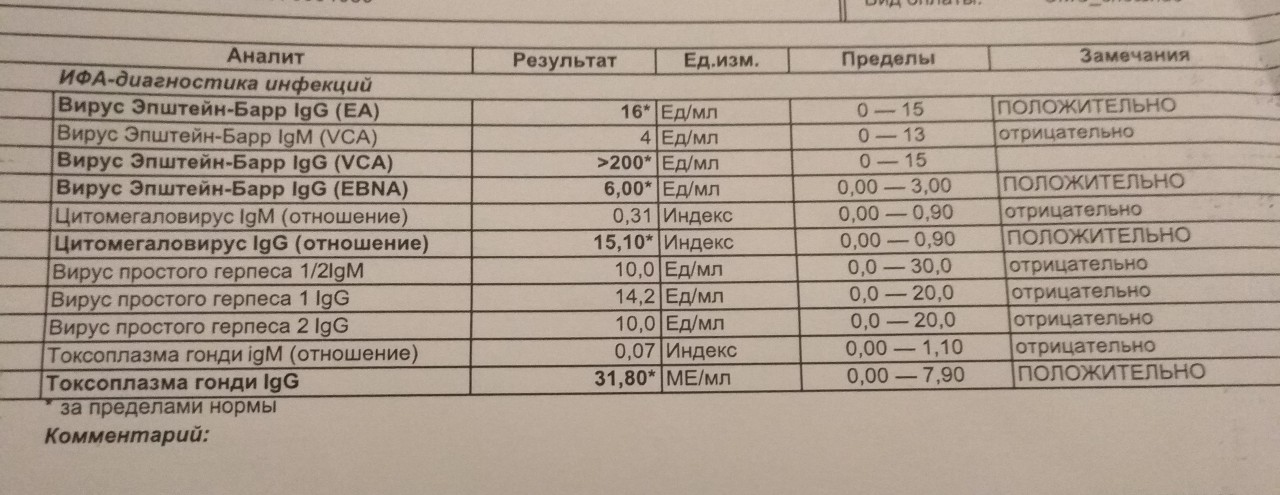 Нет доказательств повышенного риска, связанного с уходом за пациентом. ЯМА .
1990; 263:840–4.
Нет доказательств повышенного риска, связанного с уходом за пациентом. ЯМА .
1990; 263:840–4.
6. Эванс А.С. Инфекционный мононуклеоз и родственные синдромы. Am J Med Sci . 1978; 276: 325–39.
7. Клемола Э., Каариайнен Л. Цитомегаловирус как возможная причина заболевания, напоминающего инфекционный мононуклеоз. Бр Мед J . 1965; 5470: 1099–102.
8. Джордан М.С., Руссо В, Стюарт Дж.А., Благородный ГР, Чин ТД. Спонтанный цитомегаловирусный мононуклеоз. Энн Интерн Мед . 1973; 79: 153–60.
9. Драго Ф., Арагон М.Г., Лугани С, Ребора А. Цитомегаловирусная инфекция у здоровых людей и людей с ослабленным иммунитетом.Обзор. Дерматология . 2000; 200:189–95.
10. Кано Ю.,
Шиохара Т.
Современные представления о цитомегаловирусной инфекции у иммунокомпетентных лиц. J Dermatol Sci . 2000; 22:196–204.
2000; 22:196–204.
11. Хорвиц, Калифорния, Хенле В, Хенле Г. Диагностические аспекты синдрома цитомегаловирусного мононуклеоза у ранее здоровых лиц. Постград Мед . 1979; 66: 153–158.
12. Райт Дж.Г. Тяжелая тромбоцитопения, вторичная по отношению к бессимптомной цитомегаловирусной инфекции у иммунокомпетентного хозяина. Дж Клин Патол . 1992; 45:1037–1038.
13. Филипс Калифорния, Фаннинг В.Л., Гамп Д.В., Филлипс CF. Цитомегаловирусный энцефалит у иммунологически нормальных взрослых. Успешное лечение видарабином. ЯМА . 1977; 238: 2299–300.
14. Эддлстон М., Павлин С, Можжевельник М, Уоррелл Д.А. Тяжелая цитомегаловирусная инфекция у иммунокомпетентных пациентов. Клин Infect Dis . 1997; 24:52–6.
15. Цапарас Ю.Ф.,
Бригден М.Л.,
Матиас Р,
Томас Э,
Рабуд Дж,
Дойл П. Доля положительных результатов на вирус Эпштейна-Барр, цитомегаловирус, вирус герпеса человека 6, токсоплазму и вирус иммунодефицита человека типов 1 и 2 у гетерофил-отрицательных пациентов с абсолютным лимфоцитозом или инструментально-генерируемым атипичным лимфоцитом. Медицинская лаборатория Arch Pathol .
2000; 124:1324–30.
Доля положительных результатов на вирус Эпштейна-Барр, цитомегаловирус, вирус герпеса человека 6, токсоплазму и вирус иммунодефицита человека типов 1 и 2 у гетерофил-отрицательных пациентов с абсолютным лимфоцитозом или инструментально-генерируемым атипичным лимфоцитом. Медицинская лаборатория Arch Pathol .
2000; 124:1324–30.
16. Маттес FM, Маклафлин Дж. Э., Эмери В.К., Кларк Д.А., Полицейское управление Гриффитса.Гистопатологическое обнаружение включений глаза совы по-прежнему специфично для цитомегаловируса в эпоху человеческих герпесвирусов 6 и 7. J Clin Pathol . 2000;53:612–4.
17. Болярд Э.А., Таблан ОС, Уильямс ВВ, Пирсон М.Л., Шапиро КН, Дейчман С.Д. Руководство по инфекционному контролю среди медицинского персонала, 1998 г. Infect Control Hosp Epidemiol . 1998; 19: 407–63.
18. Гувер Д.Р.,
Саа А.Дж.,
Бацеллар Х,
Фэйр Дж,
Детельс Р,
Андерсон Р,
и другие. Клинические проявления СПИДа в эпоху профилактики пневмоцистоза. N Английский J Med .
1993; 329:1922–6.
Клинические проявления СПИДа в эпоху профилактики пневмоцистоза. N Английский J Med .
1993; 329:1922–6.
19. Дейтон Дж. Р., Уилсон П, Сабин КА, Дэйви СиСи, Джонсон М.А., Эмери В.К., и другие. Изменения течения цитомегаловирусного ретинита после введения высокоактивной антиретровирусной терапии. СПИД . 2000; 14:1163–70.
20. Холланд Г., Туфайл А., Джордон М.Цитомегаловирусные заболевания. В: Pepose JS, Holland GN, Wilhelmus KR, eds. Глазная инфекция и иммунитет. Сент-Луис: Мосби, 1996:1088.
21. Уиткап С.М. Цитомегаловирусный ретинит в эпоху высокоактивной антиретровирусной терапии. ЯМА . 2000; 283: 653–7.
22. Долин Р., Мазур Х., Сааг М.С. терапия СПИДа. Philadelphia: Churchill Livingstone, 1999.
23. Имплантат ганцикловира плюс пероральный ганцикловир по сравнению с парентеральным цидофовиром для лечения цитомегаловирусного ретинита у пациентов с синдромом приобретенного иммунодефицита: исследование ганцикловира цидофовира цитомегаловирусного ретинита.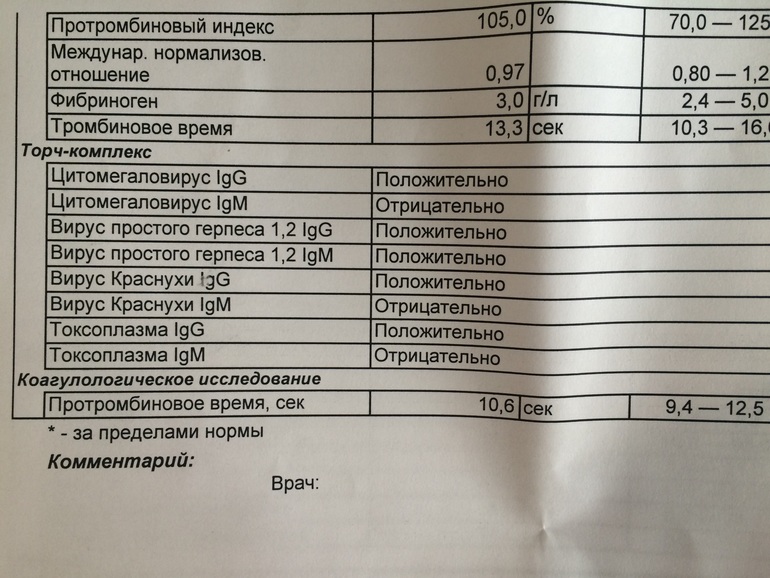


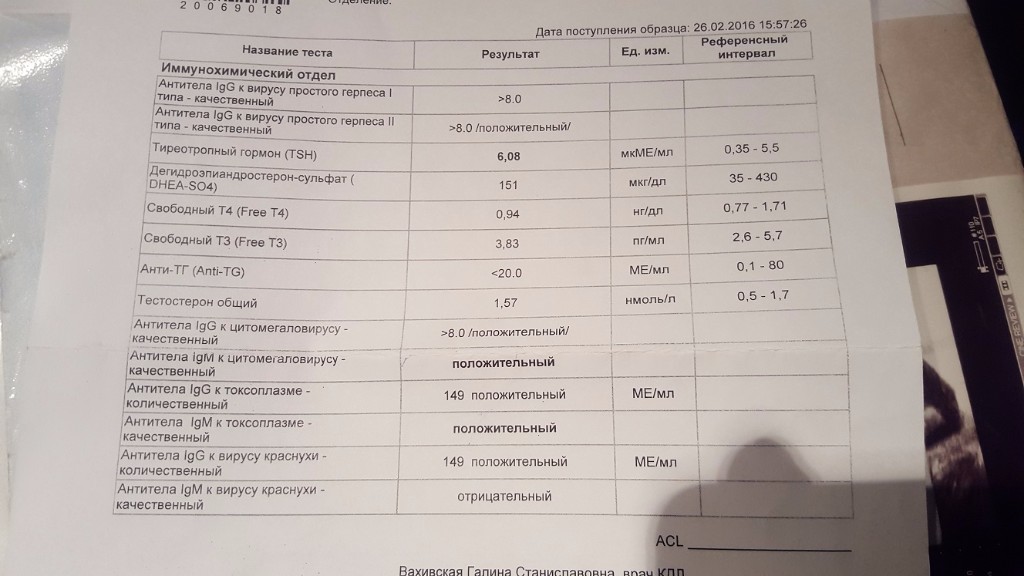

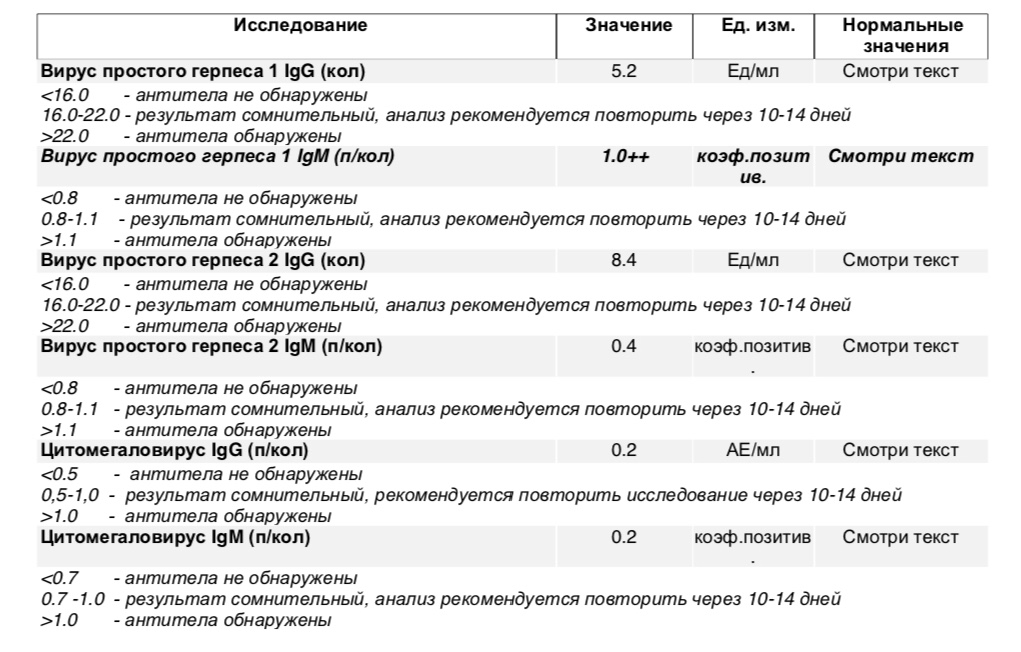
 4
4  г. микроцефалия, двигательная инвалидность, хориоретинит, перивентрикулярная лейкомаляция и кальцификаты, гидранэнцефалия, атрофия зрительного нерва, вялость, дистресс и судороги)
г. микроцефалия, двигательная инвалидность, хориоретинит, перивентрикулярная лейкомаляция и кальцификаты, гидранэнцефалия, атрофия зрительного нерва, вялость, дистресс и судороги)