Вакцинация против туберкулеза | Министерство здравоохранения Чувашской Республики
Следующая по очереди – вакцинация против туберкулеза. Её выполняют при выписке из роддома на 3-7 день жизни.
Туберкулез – инфекция, вызываемая микобактерией туберкулёза человека. Поражаются лёгкие, другие внутренние органы, кожа, кости, позвоночник. Наиболее тяжёлой формой заболевания является туберкулёзный менингит (воспаление мозговых оболочек). На заболеваемость туберкулёзом влияет ряд социальных факторов: недостаточное питание, скученность в помещениях, где живёт ребёнок и контакты с больными туберкулёзом взрослыми. Но болеют и социально благополучные люди, нередко туберкулёз выявляют у пожилых людей. Вакцинация новорожденных вакциной БЦЖ спасает от наиболее тяжёлых форм туберкулёза (туберкулёзного менингита, диссеминированных форм). От инфицирования самой туберкулёзной палочкой она не защищает, но защищает от смертельных и инвалидизирующих форм туберкулёза.
Вакцина БЦЖ существует на протяжении 80 лет и является одной из наиболее широко используемых в мире. ВОЗ рекомендует начинать вакцинацию БЦЖ сразу после рождения ребенка. В странах, где заболеваемость туберкулёзом очень низкая (США, Германия, Швеция, Израиль и другие), прививку БЦЖ проводят только в группах риска (людям, приехавшим из стран, где распространен туберкулёз).
Россия относится к странам с очень высокой заболеваемостью туберкулёзом, в том числе лекарственноустойчивым. В России прививка против туберкулёза жизненно необходима новорожденному.
Вакцина БЦЖ содержит как живые, так и неживые микробные клетки.
В вакцине БЦЖ-М доля живых клеток выше, а доза в 2 раза меньше, что позволяет меньшей дозой получить удовлетворительный результат и снизить частоту нежелательных реакций.
Обе вакцины из субштамма М. bovis (коровий) — БЦЖ (BCG-1 Russia) и оба препарата отвечают требованию ВОЗ.
В календарь данная вакцинация введена в 1953 году.
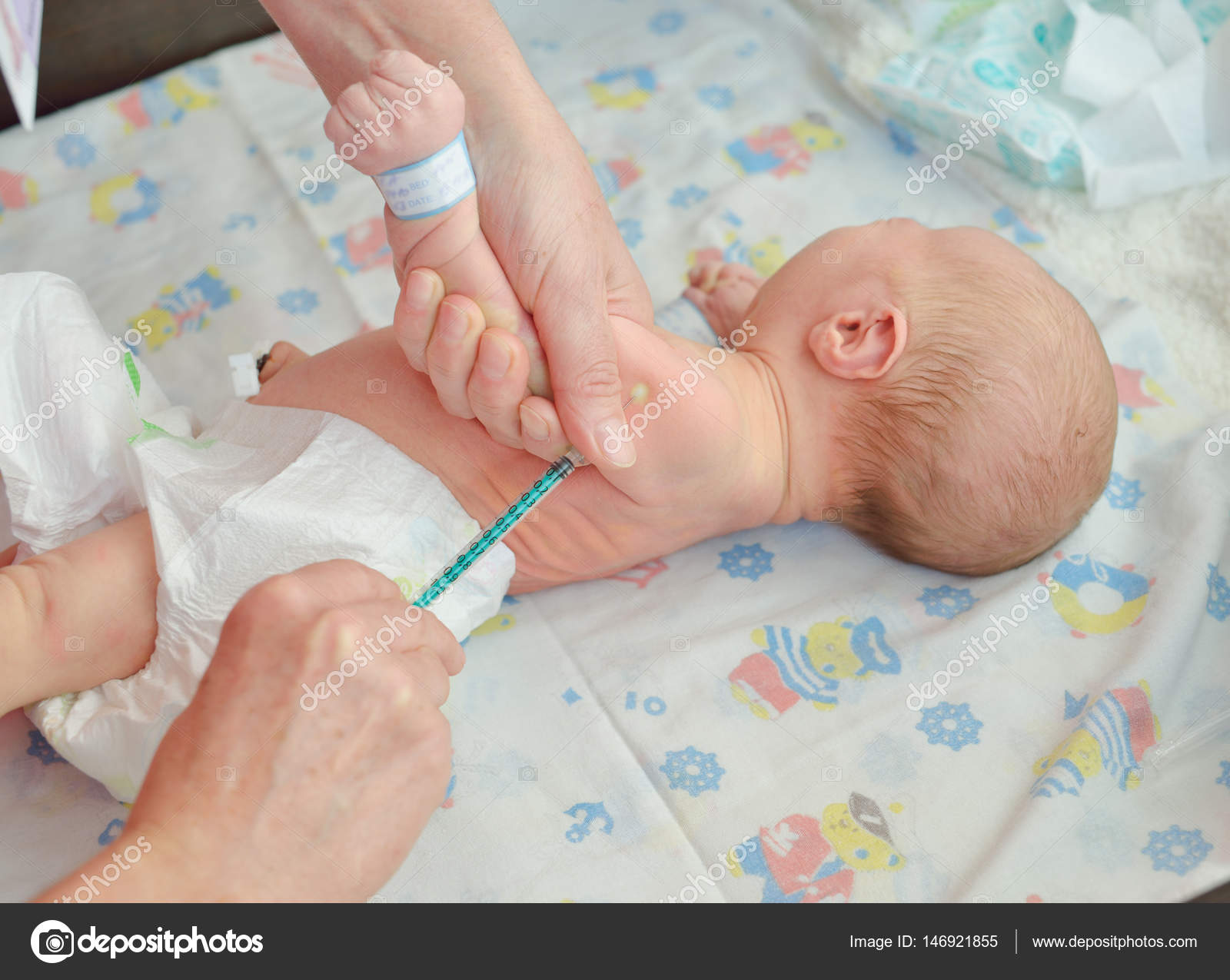
Вакцинация проводится практически здоровым новорожденным вакциной БЦЖ-М в возрасте 3-7 дней внутрикожно в верхнюю треть плеча. Вакцина БЦЖ используется у новорожденных в субъектах РФ с показателями заболеваемости выше 80 на 100 тыс. населения, а также при наличии в окружении больных туберкулёзом.
Вакцина БЦЖ используется у новорожденных в субъектах РФ с показателями заболеваемости выше 80 на 100 тыс. населения, а также при наличии в окружении больных туберкулёзом.
Ревакцинация проводится туберкулиноотрицательным детям в возрасте 7лет.
Скворцова: наличие прививки БЦЖ может влиять на уровень заболеваемости при коронавирусе — Общество
МОСКВА, 7 апреля. /ТАСС/. Показатель вакцинации БЦЖ среди населения может иметь определенную взаимосвязь с уровнем заболеваемости и смертности от коронавирусной инфекции. Об этом сообщила глава Федерального медико-биологического агентства Вероника Скворцова во вторник в интервью телеканалу «Россия-24».
«В международных обзорах это действительно сейчас широко обсуждается, причем различия там не в два раза, а в десять раз, на порядок, и заболеваемости, и смертности от коронавирусной инфекции. Много домыслов, каким образом одно увязать с другим. Но то, что это может иметь определенное значение, наверно может,.
Согласно исследованию американских эпидемиологов, скорость распространения и уровня смертности от коронавирусной инфекции в разных странах может быть связана с тем, как давно и насколько широко в них применялась вакцина БЦЖ, предназначенная для борьбы с туберкулезом.
Эту вакцину разработали вирусологи Альбер Кальмет и Камиль Герен в 1921 году. Она до сих пор остается главным средством борьбы с туберкулезом. Однако вакцинация эффективна только для тех людей, кто ранее не болел туберкулезом. Защитное действие БЦЖ длится около 5-7 лет, после чего нужно делать прививку повторно.
Многие ученые сомневаются в эффективности БЦЖ, особенно для вакцинирования взрослых людей. Поэтому, в отличие от России и других стран бывшего социалистического лагеря, в США и некоторых странах Европы массовое вакцинирование БЦЖ не проводили.
Кроме туберкулеза вакцину использовали для лечения рака мочевого пузыря, однако ее эффективность подтверждает лишь небольшое количество наблюдений.
Ранее профессор Новосибирского НИИ туберкулеза Наталия Ставицкая в разговоре с корреспондентом ТАСС подчеркивала, что сейчас нет оснований считать БЦЖ средством от коронавирусной инфекции. Она пояснила, что при анализе данных не учитывается влияние многих факторов, таких как контагиозность вируса (способность передаваться от больных людей к здоровым), и эпидемиологических факторов.
Российские ученые выявили пользу прививки от туберкулеза в борьбе с COVID — РБК
Как утверждают ученые, в странах, где массовая БЦЖ-вакцинация никогда не проводилась или прекратилась более 20 лет назад, в частности в США, Бельгии, Нидерландах, Италии, а также на западе Германии, уровень смертности намного выше.
Исследователи предположили, что вакцина БЦЖ запускает тренированный иммунитет, который дополнительно активирует клетки, мобилизующие защитные силы организма. А вырабатываемые после БЦЖ-вакцинации медиаторы могут способствовать менее тяжелому течению заболевания.
Читайте на РБК Pro
 В. Ломоносова Алексей Аграновский в беседе с РБК заявил, что разговоры о том, что прививка от туберкулеза может снизить скорость распространения COVID-19 и облегчить его течение, идут еще с весны, когда пришла первая волна эпидемии. «Достоверно сказать, что прививка от туберкулеза, БЦЖ, ограничивает коронавирусную инфекцию, нельзя, но так вполне может быть. Тема еще требует изучения. Некоторые объясняют это тренировкой иммунитета. Звучит несколько поверхностно, но этого нельзя исключить», — сказал он.
В. Ломоносова Алексей Аграновский в беседе с РБК заявил, что разговоры о том, что прививка от туберкулеза может снизить скорость распространения COVID-19 и облегчить его течение, идут еще с весны, когда пришла первая волна эпидемии. «Достоверно сказать, что прививка от туберкулеза, БЦЖ, ограничивает коронавирусную инфекцию, нельзя, но так вполне может быть. Тема еще требует изучения. Некоторые объясняют это тренировкой иммунитета. Звучит несколько поверхностно, но этого нельзя исключить», — сказал он.Ранее, как отметил вирусолог, появлялись сообщения о том, что на территории бывшей ГДР, где прививали людей от туберкулеза, заболеваемость была меньше, чем на территории Западной Германии, где такая прививка не делалась, хотя там проживает один народ. «Призываю всех относиться к данным внимательно, не верить всему заранее. Это предмет будущих исследований», — заключил Аграновский.
 Ф.Гамалеи, академик РАН Феликс Ершов в разговоре с РБК заявил, что связь между уровнем смертности от COVID-19 в разных странах и вакцинацией БЦЖ действительно существует. Возможно, именно с этим связан феномен относительно благополучной эпидемиологической ситуации в России, странах Азии и Южной Америки, где принята поголовная вакцинация детей БЦЖ: там смертность от COVID-19 значительно ниже, чем в Италии, Испании, Франции и США, где вакцинация БЦЖ была необязательной.
Ф.Гамалеи, академик РАН Феликс Ершов в разговоре с РБК заявил, что связь между уровнем смертности от COVID-19 в разных странах и вакцинацией БЦЖ действительно существует. Возможно, именно с этим связан феномен относительно благополучной эпидемиологической ситуации в России, странах Азии и Южной Америки, где принята поголовная вакцинация детей БЦЖ: там смертность от COVID-19 значительно ниже, чем в Италии, Испании, Франции и США, где вакцинация БЦЖ была необязательной.Как отметил Ершов, из этого следует два важных вывода: во-первых, Россия благодаря обязательным прививкам БЦЖ надежно защищена от коронавируса, во-вторых, опыт России с поголовной вакцинацией детей БЦЖ можно использовать в мире для защиты людей от коронавируса.
Коронавирус
Россия Москва Мир
0 (за сутки)
Заразились
0
0 (за сутки)
Умерли
0 (за сутки)
Заразились
0
0 (за сутки)
Умерли
0 (за сутки)
Заразились
0
0 (за сутки)
Умерли
Источник: JHU, федеральный и региональные оперштабы по борьбе с вирусом
Новая вакцина от туберкулеза повышает результативность лечения на 50-60% — Российская газета
Доклинические (биомедицинские) испытания на лабораторных животных успешно прошла новая противотуберкулезная вакцина. Она разработана ведущими научными медицинскими институтами страны — Санкт-Петербургским НИИ фтизиопульмонологии и НИИ гриппа имени А.А. Смородинцева. Вакцина векторная, как и знаменитая «Спутник-V».
Она разработана ведущими научными медицинскими институтами страны — Санкт-Петербургским НИИ фтизиопульмонологии и НИИ гриппа имени А.А. Смородинцева. Вакцина векторная, как и знаменитая «Спутник-V».
Необходимость в создании новой вакцины назрела давно. Вакцина БЦЖ (а другой пока и нет), которой прививали еще наших бабушек, была создана в 1921 году французскими медиками Кальметом и Гереном на основе штамма ослабленной туберкулезной палочки — палочки Коха. То есть ровно сто лет назад. Через четыре года БЦЖ была передана в нашу страну, а с 1928-го началась массовая вакцинация.
БЦЖ остается единственной вакциной для специфической защиты от туберкулеза поныне. При всех своих плюсах вакцина имеет недостатки. В их числе — ограниченная защита от туберкулеза у подростков и взрослых, а также снижение защиты в раннем подростковом возрасте. К тому же из-за того, что БЦЖ содержит живой штамм, есть риск заболевания туберкулезом тех, кто заражен ВИЧ-инфекцией. В некоторых странах ведутся работы по созданию нового кандидата в вакцины. Так, три года назад в ЮАР прошла вторую фазу клинических испытаний на добровольцах новая вакцина. Но, как выяснилось, ее эффективность меньше.
Так, три года назад в ЮАР прошла вторую фазу клинических испытаний на добровольцах новая вакцина. Но, как выяснилось, ее эффективность меньше.
— Мы разработали вакцину, которая может вводиться через нос, то есть в виде аэрозоля. Специально выбрали столь щадящий способ введения, который более оптимален для детей. Да и для взрослых — тоже. Сравните укол и просто «пшик» в нос. Второй вариант введения вакцины — под язык, — пояснила главный научный сотрудник НИИ фтизиопульмонологии Татьяна Виноградова,
Вакцина создана на основе генно-инженерных конструкций с использованием вируса гриппа. Это векторная вакцина, как и «Спутник-V», но с той разницей, что для «Спутника» в качестве средства доставки брали аденовирус.
— Мы же используем ослабленный вирус гриппа А, совершенно безопасный для человека. Заболеть гриппом от вакцины невозможно. Вирус доставит в организм человека определенные белки палочки Коха, с которыми связано формирование защиты от активного туберкулеза, — уточнила Марина Стукова, заведующая лабораторией векторных вакцин НИИ гриппа имени А. А. Смородинцева.
А. Смородинцева.
Преимущество разработки перед вакциной БЦЖ, которая, как мы помним, вводится подкожно, является формированием иммунного ответа в респираторном тракте. Этот подход оптимален для защиты от инфекций, передающихся аэрозольным путем, в том числе туберкулеза.
Планируется создание как профилактического варианта, так и вакцины для специфической иммунотерапии туберкулеза, которая будет повышать эффективность лечения противотуберкулезными препаратами. На моделях экспериментального туберкулеза уже доказано повышение результативности лечения на 50-60 процентов. Причем это касается и туберкулеза, вызванного микобактериями с множественной лекарственной устойчивостью. Это важный фактор, поскольку лекарственно-устойчивый туберкулез — проблема номер один в современной фтизиатрии.
Предложенная вакцина повышает результативность лечения на 50-60 процентов
Что касается профилактического варианта вакцины, то спектр ее применения обширен. Но прежде всего она может подойти для детей и подростков, которым показана ревакцинация, персоналу учреждений, работающих с туберкулезными больными. Также в группу возможных вакцинированных входят больные ревматоидным артритом, другими системными и онкологическими заболеваниями.
Также в группу возможных вакцинированных входят больные ревматоидным артритом, другими системными и онкологическими заболеваниями.
Вакцина особенно показана ВИЧ-инфицированным, людям с пересаженными органами, больным, получающим иммуносупрессивные препараты, а также пожилым. Всем тем, у кого риск заболеть, причем тяжело, значительно выше. На данном этапе замена БЦЖ новой вакциной не планируется. Новая вакцина предназначена для поддержания стойкой и длительной защиты от туберкулеза при угасании противотуберкулезного иммунитета, то есть она может делаться спустя какое-то время после БЦЖ. Конкретные рекомендации появятся после клинических испытаний. Их проведение пока упирается в финансирование.
вакцин | Основные факты о туберкулезе | ТБ
Противотуберкулезная вакцина (БЦЖ)
Бацилла Кальметта-Герена (БЦЖ) представляет собой вакцину против туберкулеза (ТБ). Эта вакцина не используется широко в Соединенных Штатах, но ее часто вводят младенцам и маленьким детям в других странах, где распространен туберкулез. БЦЖ не всегда защищает людей от заражения туберкулезом.
БЦЖ не всегда защищает людей от заражения туберкулезом.
Рекомендации БКГ
В Соединенных Штатах БЦЖ следует рассматривать только для очень избранных людей, которые соответствуют определенным критериям и после консультации со специалистом по ТБ.Медицинским работникам, рассматривающим вопрос о вакцинации БЦЖ для своих пациентов, рекомендуется обсудить это вмешательство с программой борьбы с ТБ в их районе.
Дети
Вакцинация БЦЖ должна рассматриваться только для детей с отрицательным результатом теста на туберкулез, которые постоянно контактируют с больными, и не может быть отделена от взрослых, которые
- Не лечатся или лечатся неэффективно по поводу туберкулеза, и ребенку не может быть назначено длительное первичное профилактическое лечение туберкулезной инфекции; или
- Заболевание ТБ, вызванное штаммами, устойчивыми к изониазиду и рифампину.
Медицинские работники
Вакцинация БЦЖ медицинских работников должна рассматриваться на индивидуальной основе в условиях, когда
- Высокий процент больных ТБ инфицирован штаммами ТБ, устойчивыми как к изониазиду, так и к рифампину;
- Продолжается передача лекарственно-устойчивых штаммов ТБ медицинским работникам, и вероятно последующее заражение; или
- Были приняты всесторонние меры по борьбе с инфекцией туберкулеза, но они не увенчались успехом.

Медицинские работники, которым предлагается вакцинация БЦЖ, должны быть проинформированы о рисках и преимуществах, связанных как с вакцинацией БЦЖ, так и с лечением латентной туберкулезной инфекции.
Тестирование на ТБ у людей, вакцинированных БЦЖ
Многие люди, родившиеся за пределами США, были привиты БЦЖ.
Людям, ранее вакцинированным БЦЖ, может быть сделана кожная проба на туберкулез для проверки на туберкулезную инфекцию. Прививка БЦЖ может вызвать положительную реакцию на кожную пробу на туберкулез.Положительная реакция на кожную пробу на туберкулез может быть связана с самой вакциной БЦЖ или с заражением бактериями туберкулеза.
Анализ крови на туберкулез (IGRA), в отличие от кожного теста на туберкулез, не зависит от предшествующей вакцинации БЦЖ, и ожидается, что он не даст ложноположительного результата у людей, получивших БЦЖ.
Для детей в возрасте до пяти лет кожная проба на туберкулез предпочтительнее, чем анализы крови на туберкулез.
Положительный кожный тест на туберкулез или анализ крови на туберкулез говорит только о том, что человек инфицирован бактериями туберкулеза.Он не говорит о том, есть ли у человека латентная инфекция ТБ или заболевание прогрессировало до ТБ. Другие тесты, такие как рентген грудной клетки и образец мокроты, необходимы, чтобы определить, болен ли человек туберкулезом.
Узнайте о тестировании и диагностике.
БКГ
Формулировка международных требований к производству и контролю вакцины БЦЖ была впервые рассмотрена Экспертным комитетом ВОЗ по биологической стандартизации в его тринадцатом докладе. В своем четырнадцатом докладе Комитет просил ВОЗ как можно скорее принять меры для формулирования таких требований.Эти требования были одобрены Экспертным комитетом ВОЗ по биологической стандартизации на его восемнадцатом совещании и опубликованы в Приложении 1 к его отчету.
Mycobacterium tuberculosis (Mtb), этиологический агент туберкулеза (ТБ), является основной причиной заболеваний и смерти человека, особенно в развивающихся странах.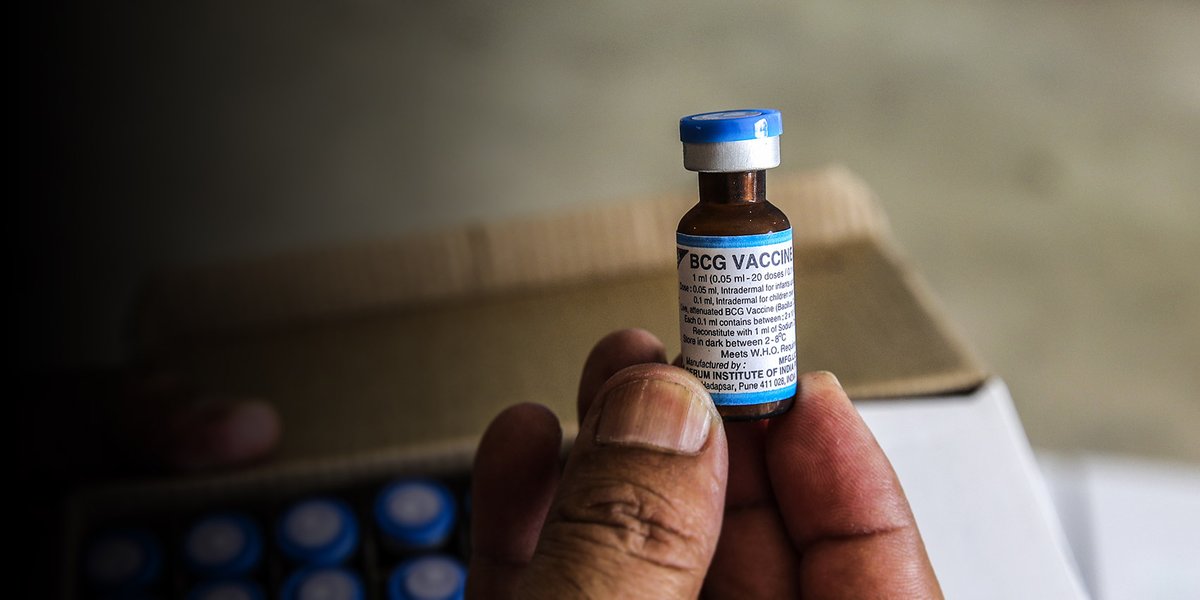 В глобальном контексте ТБ тесно связан с бедностью, а борьба с ТБ в конечном счете является вопросом справедливости и прав человека. В некоторых районах с высоким бременем туберкулеза существующие стратегии борьбы с туберкулезом в настоящее время не работают из-за растущего числа случаев заболевания туберкулезом, возникающих параллельно с пандемией ВИЧ/СПИДа или с ней.Возникающая резистентность микобактерий к лекарственным препаратам еще больше усложняет ситуацию. После десятилетий неуклонного снижения заболеваемость ТБ также растет в промышленно развитых странах, главным образом в результате вспышек в особо уязвимых группах.
В глобальном контексте ТБ тесно связан с бедностью, а борьба с ТБ в конечном счете является вопросом справедливости и прав человека. В некоторых районах с высоким бременем туберкулеза существующие стратегии борьбы с туберкулезом в настоящее время не работают из-за растущего числа случаев заболевания туберкулезом, возникающих параллельно с пандемией ВИЧ/СПИДа или с ней.Возникающая резистентность микобактерий к лекарственным препаратам еще больше усложняет ситуацию. После десятилетий неуклонного снижения заболеваемость ТБ также растет в промышленно развитых странах, главным образом в результате вспышек в особо уязвимых группах.
Вакцина против бациллы Кальметта-Герена (БЦЖ) существует уже 80 лет и является одной из наиболее широко используемых из всех современных вакцин, прививка >80% новорожденных и детей грудного возраста в странах, где она является частью национальной программы иммунизации детей.Вакцина БЦЖ имеет задокументированный защитный эффект против менингита и диссеминированного туберкулеза у детей.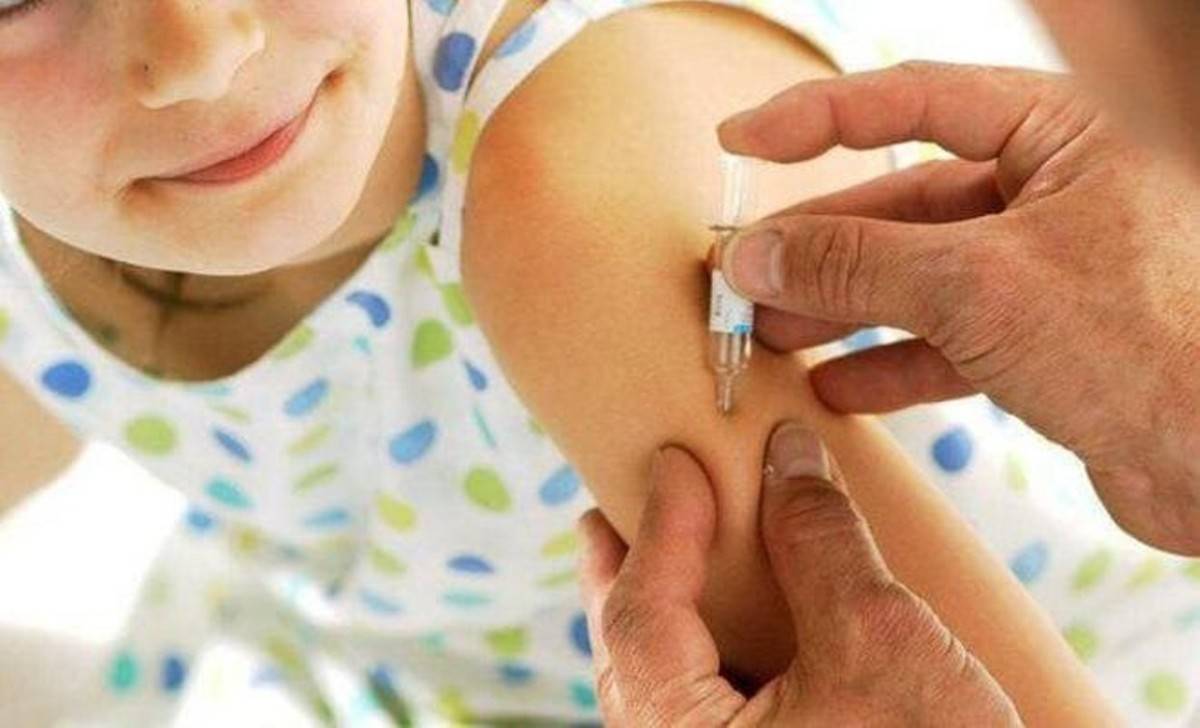 Он не предотвращает первичную инфекцию и, что более важно, не предотвращает реактивацию латентной легочной инфекции, основного источника бациллярного распространения в обществе. Таким образом, влияние вакцинации БЦЖ на передачу Mtb ограничено.
Он не предотвращает первичную инфекцию и, что более важно, не предотвращает реактивацию латентной легочной инфекции, основного источника бациллярного распространения в обществе. Таким образом, влияние вакцинации БЦЖ на передачу Mtb ограничено.
Биологическое взаимодействие между Mtb и человеком-хозяином является сложным и изучено лишь частично. Недавние достижения в таких областях, как микобактериальная иммунология и геномика, стимулировали исследования многочисленных новых экспериментальных вакцин, но маловероятно, что какая-либо из этих остро необходимых вакцин будет доступна для рутинного использования в ближайшие несколько лет.Тем временем рекомендуется оптимальное использование БЦЖ.
Вакцинация БЦЖ: 90 лет прошло, а еще так много предстоит узнать…
История вакцинации против туберкулеза изобилует примерами научных открытий и повторных открытий. В конце 19-го и начале 20-го века, после объявления Робертом Кохом об открытии им Mycobacterium tuberculosis в 1882 году, ученые всего мира, в том числе и сам Кох, решили изобрести вакцину против туберкулеза. В 1908 году Леон Кальметт, бактериолог, и Камиль Герен, ветеринар из Института Пастера, Лилль, начали эксперимент по разработке вакцины путем ослабления штамма Mycobacterium bovis до тех пор, пока он не потерял свою вирулентность. Тринадцать лет и 230 пассажей спустя они смогли показать, что штамм обладал защитным действием на животных моделях и больше не вызывал болезни, которая, как впоследствии было обнаружено, в первую очередь связана с потерей генов в области различия 1 (RD1) области геном M bovis .1 В том же году ребенку, контактировавшему с больным туберкулезом, была введена первая доза живой аттенуированной вакцины M bovis Bacille Calmette-Geurin (БЦЖ). Теперь, когда ввели более 3 миллиардов доз, БЦЖ является наиболее широко используемой вакциной во всем мире.
В 1908 году Леон Кальметт, бактериолог, и Камиль Герен, ветеринар из Института Пастера, Лилль, начали эксперимент по разработке вакцины путем ослабления штамма Mycobacterium bovis до тех пор, пока он не потерял свою вирулентность. Тринадцать лет и 230 пассажей спустя они смогли показать, что штамм обладал защитным действием на животных моделях и больше не вызывал болезни, которая, как впоследствии было обнаружено, в первую очередь связана с потерей генов в области различия 1 (RD1) области геном M bovis .1 В том же году ребенку, контактировавшему с больным туберкулезом, была введена первая доза живой аттенуированной вакцины M bovis Bacille Calmette-Geurin (БЦЖ). Теперь, когда ввели более 3 миллиардов доз, БЦЖ является наиболее широко используемой вакциной во всем мире.
С момента своего первого применения 90 лет назад БЦЖ была рекомендована в качестве вакцины из-за ее частичного защитного действия против активного туберкулеза и смерти, хотя и с большей эффективностью против диссеминированных и менингеальных заболеваний у детей, чем легочных заболеваний у подростков и взрослых. 2 3 Это, вместе с исследованиями аутопсии, предполагающими, что БЦЖ уменьшает размер очагов туберкулеза в легких, тем самым ограничивая размножение и распространение бактерий4, и модели животных, где вакцинация БЦЖ снижает бактериальную нагрузку после заражения М.tuberculosis , но не защищает от инфекции, привели к давней догма о том, что БЦЖ защищает от распространения и болезней, но не от инфекций. Всего 5 лет назад первое сообщение5 о способности БЦЖ защищать от инфекции изменило наше представление о том, как действует БЦЖ.Вывод о том, что БЦЖ может действовать на ранней стадии пути передачи инфекции от туберкулеза к заболеванию (рис. 1), впоследствии был подтвержден исследованиями контактов взрослых и детей в сообществе в Гамбурге6 и двумя исследованиями школьных вспышек туберкулеза в Великобритании. 7 последний из которых опубликован в текущем выпуске Thorax ( , см. стр. 1067 ).8 Исследуя вспышку точечного туберкулеза в детском саду, Эриксен и его коллеги обнаружили, что вакцинированные БЦЖ дети значительно более вероятно инфицирование, судя по результатам анализа высвобождения гамма-интерферона (IGRA), чем невакцинированные дети.
2 3 Это, вместе с исследованиями аутопсии, предполагающими, что БЦЖ уменьшает размер очагов туберкулеза в легких, тем самым ограничивая размножение и распространение бактерий4, и модели животных, где вакцинация БЦЖ снижает бактериальную нагрузку после заражения М.tuberculosis , но не защищает от инфекции, привели к давней догма о том, что БЦЖ защищает от распространения и болезней, но не от инфекций. Всего 5 лет назад первое сообщение5 о способности БЦЖ защищать от инфекции изменило наше представление о том, как действует БЦЖ.Вывод о том, что БЦЖ может действовать на ранней стадии пути передачи инфекции от туберкулеза к заболеванию (рис. 1), впоследствии был подтвержден исследованиями контактов взрослых и детей в сообществе в Гамбурге6 и двумя исследованиями школьных вспышек туберкулеза в Великобритании. 7 последний из которых опубликован в текущем выпуске Thorax ( , см. стр. 1067 ).8 Исследуя вспышку точечного туберкулеза в детском саду, Эриксен и его коллеги обнаружили, что вакцинированные БЦЖ дети значительно более вероятно инфицирование, судя по результатам анализа высвобождения гамма-интерферона (IGRA), чем невакцинированные дети. Эффективность вакцины против инфекции оценивалась в 66%, но, учитывая небольшой размер исследования, доверительные интервалы достаточно широки, чтобы перекрываться со снижением ОР на 38%7 и 24%5, наблюдавшимся в предыдущих более крупных исследованиях. В совокупности эти данные убедительно свидетельствуют о том, что по крайней мере часть защитного эффекта БЦЖ связана с защитой от инфекции, что имеет существенное значение для разработки и оценки новых противотуберкулезных вакцин, а также роли БЦЖ в программах борьбы с ТБ.Действительно, Эриксен и его коллеги обсуждают вопрос о пересмотре порога вакцинации БЦЖ в регионах с разным уровнем заболеваемости туберкулезом. Тем не менее, к выводам о причинной роли БЦЖ в защите от инфекции следует относиться с осторожностью, учитывая нерандомизированный характер обсервационных исследований на сегодняшний день, хотя совокупные данные из множества эпидемиологически различных условий делают доводы в пользу причинной роли БЦЖ все более частыми. неотразимый.
Эффективность вакцины против инфекции оценивалась в 66%, но, учитывая небольшой размер исследования, доверительные интервалы достаточно широки, чтобы перекрываться со снижением ОР на 38%7 и 24%5, наблюдавшимся в предыдущих более крупных исследованиях. В совокупности эти данные убедительно свидетельствуют о том, что по крайней мере часть защитного эффекта БЦЖ связана с защитой от инфекции, что имеет существенное значение для разработки и оценки новых противотуберкулезных вакцин, а также роли БЦЖ в программах борьбы с ТБ.Действительно, Эриксен и его коллеги обсуждают вопрос о пересмотре порога вакцинации БЦЖ в регионах с разным уровнем заболеваемости туберкулезом. Тем не менее, к выводам о причинной роли БЦЖ в защите от инфекции следует относиться с осторожностью, учитывая нерандомизированный характер обсервационных исследований на сегодняшний день, хотя совокупные данные из множества эпидемиологически различных условий делают доводы в пользу причинной роли БЦЖ все более частыми. неотразимый.
Схема защитного действия БЦЖ на различных стадиях естественного течения туберкулеза.Серые стрелки представляют эффекты БЦЖ, обнаруженные за последние 5 лет, а черные стрелки представляют исторически известные эффекты.
В этом выпуске Thorax мы также узнаем о другом до сих пор неизвестном эффекте БЦЖ, который, по-видимому, заключается в ее способности способствовать разрешению лечения у пациентов с активным заболеванием. Jeremiah и его коллеги сообщают о результатах лонгитюдного исследования 546 взрослых пациентов с обычно высоким исходным бактериальным обсеменением мокроты, проходящих лечение от туберкулеза легких в Танзании ( , см. стр. 1072 )9; 5.5% результатов посева мокроты не стали отрицательными через 2 месяцев лечения, что является общепризнанным маркером риска рецидива после завершения лечения. При многофакторном анализе отсутствие рубца после введения БЦЖ было связано с весьма значимым трехкратным увеличением риска неудачной конверсии посева мокроты. Пациенты с самой высокой исходной бактериальной нагрузкой мокроты имели пятикратно повышенный риск неудачной конверсии мокроты в течение 2 месяцев, как и ожидалось, в то время как ВИЧ-статус, количество CD4 и индекс массы тела не были значимо связаны с неудачной конверсией мокроты.Эти результаты намекают на возможную роль БЦЖ в содействии клиренсу большой бациллярной нагрузки во время лечения. Учитывая, что БЦЖ не защищает от развития туберкулеза легких в условиях высокой нагрузки, ее связь с микробиологической реакцией на лечение является неожиданной и удивительной. Тем не менее, возможно, что противотуберкулезные антибиотики и иммунный ответ хозяина каким-то образом взаимодействуют, чтобы уменьшить микобактериальную нагрузку in vivo, но вклад иммунного ответа хозяина сам по себе трудно установить наряду с мощным эффектом противотуберкулезного лечения у больных с лекарственной чувствительностью. болезнь.Тем не менее, значительные показатели спонтанного выздоровления больных туберкулезом в доантибиотическую эру в санаториях10 и недавние данные на животных моделях11 предполагают значительную роль реакции хозяина в микробиологическом излечении.
Пациенты с самой высокой исходной бактериальной нагрузкой мокроты имели пятикратно повышенный риск неудачной конверсии мокроты в течение 2 месяцев, как и ожидалось, в то время как ВИЧ-статус, количество CD4 и индекс массы тела не были значимо связаны с неудачной конверсией мокроты.Эти результаты намекают на возможную роль БЦЖ в содействии клиренсу большой бациллярной нагрузки во время лечения. Учитывая, что БЦЖ не защищает от развития туберкулеза легких в условиях высокой нагрузки, ее связь с микробиологической реакцией на лечение является неожиданной и удивительной. Тем не менее, возможно, что противотуберкулезные антибиотики и иммунный ответ хозяина каким-то образом взаимодействуют, чтобы уменьшить микобактериальную нагрузку in vivo, но вклад иммунного ответа хозяина сам по себе трудно установить наряду с мощным эффектом противотуберкулезного лечения у больных с лекарственной чувствительностью. болезнь.Тем не менее, значительные показатели спонтанного выздоровления больных туберкулезом в доантибиотическую эру в санаториях10 и недавние данные на животных моделях11 предполагают значительную роль реакции хозяина в микробиологическом излечении. Таким образом, по крайней мере вероятно, что иммунитет хозяина играет роль в бактериальном клиренсе мокроты, но неизвестно, как этот иммунитет позитивно и долговременно модулируется вакцинацией БЦЖ много лет назад. Кроме того, вызывает недоумение тот факт, что предположительно иммунологически опосредованные эффекты БЦЖ на микробиологический ответ на лечение могли быть настолько сильными, когда ВИЧ-статус и количество CD4 не оказывали существенного влияния на скорость конверсии мокроты.В статье Jeremiah et al. отсутствует информация о чувствительности инфекционных штаммов к антибиотикам, которая является основным фактором, определяющим время конверсии мазка мокроты и посева, но, учитывая сообщения о низкой распространенности туберкулеза с множественной лекарственной устойчивостью в Танзании,12 это маловероятно. запутать выводы. К этому замечательному первому сообщению о связи вакцинации БЦЖ с выздоровлением следует относиться с осторожностью, пока дальнейшие исследования не подтвердят это наблюдение; тем не менее, результаты должны стимулировать дальнейшие исследования в том же духе, расширенные на детей, внелегочные заболевания и устойчивые к лекарствам организмы.
Таким образом, по крайней мере вероятно, что иммунитет хозяина играет роль в бактериальном клиренсе мокроты, но неизвестно, как этот иммунитет позитивно и долговременно модулируется вакцинацией БЦЖ много лет назад. Кроме того, вызывает недоумение тот факт, что предположительно иммунологически опосредованные эффекты БЦЖ на микробиологический ответ на лечение могли быть настолько сильными, когда ВИЧ-статус и количество CD4 не оказывали существенного влияния на скорость конверсии мокроты.В статье Jeremiah et al. отсутствует информация о чувствительности инфекционных штаммов к антибиотикам, которая является основным фактором, определяющим время конверсии мазка мокроты и посева, но, учитывая сообщения о низкой распространенности туберкулеза с множественной лекарственной устойчивостью в Танзании,12 это маловероятно. запутать выводы. К этому замечательному первому сообщению о связи вакцинации БЦЖ с выздоровлением следует относиться с осторожностью, пока дальнейшие исследования не подтвердят это наблюдение; тем не менее, результаты должны стимулировать дальнейшие исследования в том же духе, расширенные на детей, внелегочные заболевания и устойчивые к лекарствам организмы. Интересно, что этот отчет расширил данные о защитном действии БЦЖ, идентифицировав другой гораздо более поздний момент в естественном течении туберкулезной инфекции, когда БЦЖ, по-видимому, действует (рис. 1).
Интересно, что этот отчет расширил данные о защитном действии БЦЖ, идентифицировав другой гораздо более поздний момент в естественном течении туберкулезной инфекции, когда БЦЖ, по-видимому, действует (рис. 1).
Наряду с растущим количеством данных о том, что БЦЖ влияет на несколько отдельных моментов в естественном течении туберкулеза, все больше данных указывают на благотворное влияние БЦЖ на другие заболевания, помимо туберкулеза, включая проказу13, астму14, детскую пневмонию15 и младенческую смертность от всех причин.16 17 Таким образом, несмотря на то, что мы используем БЦЖ уже почти столетие, только совсем недавно база эпидемиологических данных постепенно выявляет плейотропные эффекты БЦЖ на туберкулез и другие серьезные заболевания. Несмотря на недавний прогресс в распознавании множественных эффектов БЦЖ, ее иммунологические механизмы действия, а также причины ее неспособности последовательно предотвращать туберкулез легких у взрослых остаются неясными.18 Это серьезный недостаток, учитывая исключительную важность такого понимания для разработка и оценка новых и улучшенных противотуберкулезных вакцин с большей защитной эффективностью.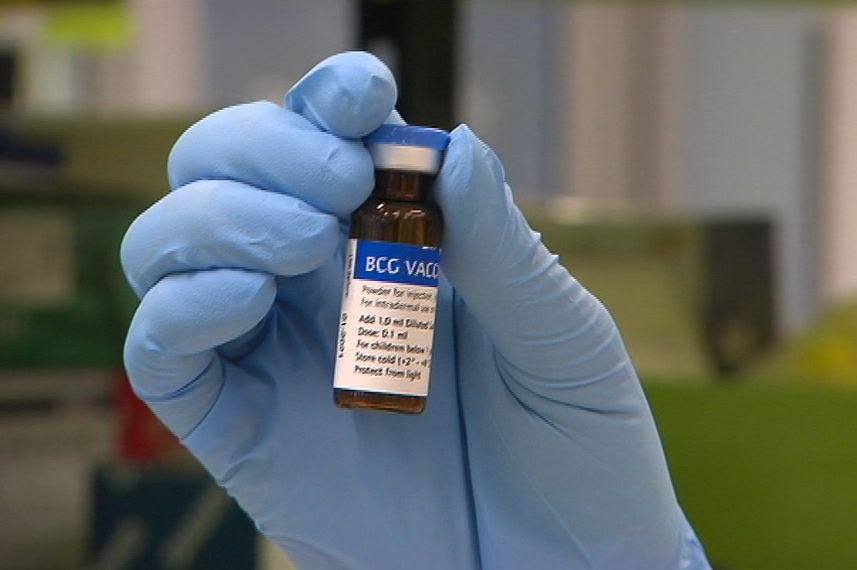 Более того, в клинических испытаниях находится не менее двенадцати экспериментальных вакцин-кандидатов, большинство из которых оцениваются на предмет их способности усиливать иммунный ответ, первоначально вызванный БЦЖ. Проблема в том, что мы до сих пор не знаем, какой из иммунных ответов, индуцированных БЦЖ, опосредует или коррелирует с защитой от туберкулезной инфекции или заболевания. Хотя полифункциональные CD4 и CD8 Т-клетки, специфичные к антигенам М. tuberculosis , все чаще рассматриваются как потенциальные корреляты или медиаторы защитного иммунитета в испытаниях вакцин и индуцируются новыми вакцинами,19, 20 БЦЖ-специфические полифункциональные Т-клетки не коррелируют с защитой от туберкулёз.21
Более того, в клинических испытаниях находится не менее двенадцати экспериментальных вакцин-кандидатов, большинство из которых оцениваются на предмет их способности усиливать иммунный ответ, первоначально вызванный БЦЖ. Проблема в том, что мы до сих пор не знаем, какой из иммунных ответов, индуцированных БЦЖ, опосредует или коррелирует с защитой от туберкулезной инфекции или заболевания. Хотя полифункциональные CD4 и CD8 Т-клетки, специфичные к антигенам М. tuberculosis , все чаще рассматриваются как потенциальные корреляты или медиаторы защитного иммунитета в испытаниях вакцин и индуцируются новыми вакцинами,19, 20 БЦЖ-специфические полифункциональные Т-клетки не коррелируют с защитой от туберкулёз.21
Значительная трудность в интерпретации результатов обеих статей, опубликованных в этом выпуске Thorax , и, действительно, всех обсервационных исследований, изучающих защитные эффекты и основные механизмы БЦЖ, заключается в том, что они полагаются на образование рубцов в качестве суррогатного маркера БЦЖ. вакцинация. Зависимость от образования рубца при выводе о вакцинации осложняется высокой распространенностью (20–50%) реципиентов, неспособных сформировать рубец22–24, и влиянием метода вакцинации на развитие рубца.16 Более того, образование рубца не коррелирует с БЦЖ-индуцированным развитием адаптивных клеточных иммунных ответов.25, 26 Эта нерешенная связь между образованием рубца и вакцинацией БЦЖ затрудняет оценку истинного защитного действия вакцины, независимо от рубца, у пациентов. эпоха, когда рандомизированные испытания БЦЖ по сравнению с плацебо неэтичны. Таким образом, вопрос состоит в том, опосредована ли частичная защита от различных стадий пути от воздействия туберкулеза до заболевания, вызванного вакцинацией БЦЖ, иммунными реакциями, которые не зависят от реакции, необходимой для рубцевания, или иммунными реакциями, которые также вызывают рубцевание.Третья возможность заключается в том, что рубцовая реакция на внутрикожное введение БЦЖ является суррогатным маркером людей, у которых ранее существовал врожденный защитный иммунитет против туберкулеза, не индуцированный вакцинацией БЦЖ.
вакцинация. Зависимость от образования рубца при выводе о вакцинации осложняется высокой распространенностью (20–50%) реципиентов, неспособных сформировать рубец22–24, и влиянием метода вакцинации на развитие рубца.16 Более того, образование рубца не коррелирует с БЦЖ-индуцированным развитием адаптивных клеточных иммунных ответов.25, 26 Эта нерешенная связь между образованием рубца и вакцинацией БЦЖ затрудняет оценку истинного защитного действия вакцины, независимо от рубца, у пациентов. эпоха, когда рандомизированные испытания БЦЖ по сравнению с плацебо неэтичны. Таким образом, вопрос состоит в том, опосредована ли частичная защита от различных стадий пути от воздействия туберкулеза до заболевания, вызванного вакцинацией БЦЖ, иммунными реакциями, которые не зависят от реакции, необходимой для рубцевания, или иммунными реакциями, которые также вызывают рубцевание.Третья возможность заключается в том, что рубцовая реакция на внутрикожное введение БЦЖ является суррогатным маркером людей, у которых ранее существовал врожденный защитный иммунитет против туберкулеза, не индуцированный вакцинацией БЦЖ. Продольные иммуноэпидемиологические исследования с клиническими конечными точками, которые наблюдают за лицами, вакцинированными БЦЖ, у которых есть и у которых нет рубцов, необходимы, чтобы распутать иммунологические отношения между триадой вакцинации, образованием рубцов и защитой. Примечательно, что крупные клинические испытания вакцин с конечной точкой, предназначенные для усиления БЦЖ новыми вакцинами, могут предоставить возможность решить этот сложный вопрос и выявить истинные корреляты защитного иммунитета, вызванные вакцинами.
Продольные иммуноэпидемиологические исследования с клиническими конечными точками, которые наблюдают за лицами, вакцинированными БЦЖ, у которых есть и у которых нет рубцов, необходимы, чтобы распутать иммунологические отношения между триадой вакцинации, образованием рубцов и защитой. Примечательно, что крупные клинические испытания вакцин с конечной точкой, предназначенные для усиления БЦЖ новыми вакцинами, могут предоставить возможность решить этот сложный вопрос и выявить истинные корреляты защитного иммунитета, вызванные вакцинами.
Подобно прекрасному вину, которое с возрастом становится только лучше, спустя 90 лет после его первой прививки людям мы все еще изучаем различные аспекты применения БЦЖ при туберкулезе и за его пределами. По иронии судьбы, масштабы глобальной пандемии туберкулеза, сами по себе отчасти являющиеся результатом неспособности БЦЖ полностью защитить от туберкулеза, вынуждают нас настойчиво пытаться разгадать механизмы, ответственные за частичную эффективность БЦЖ, одновременно продвигаясь вперед с клиническими испытаниями вакцины. новые экспериментальные вакцины.Таким образом, прививка от туберкулеза, по-видимому, имеет много общего с самой жизнью, как предположил Серен Кьеркегор: « Жизнь можно понять только в обратном направлении, но ее нужно прожить вперед ».
новые экспериментальные вакцины.Таким образом, прививка от туберкулеза, по-видимому, имеет много общего с самой жизнью, как предположил Серен Кьеркегор: « Жизнь можно понять только в обратном направлении, но ее нужно прожить вперед ».
Обязательная вакцинация против бациллы Кальметта-Герена (БЦЖ) предсказывает сглаженные кривые распространения COVID-19
ВВЕДЕНИЕ
Пандемия коронавирусной болезни 2019 (COVID-19) началась в декабре 2019 года в Ухане, Китай. С тех пор он быстро распространился по всему миру.В настоящее время не видно конца. Настоящая работа мотивирована предыдущими данными о том, что вакцинация против бациллы Кальметта-Герена (БЦЖ) (обычно вводимая при рождении и/или в детстве) обеспечивает длительный защитный эффект не только против туберкулеза (предполагаемая цель БЦЖ), но также против различных другие инфекционные болезни ( 1 – 3 ). Недавние предположения изобилуют тем, что БЦЖ может быть эффективным инструментом в борьбе с COVID-19. Однако существующим межнациональным анализам препятствуют методологические недостатки.По большей части не было предпринято никаких усилий, чтобы исключить возможные последствия предвзятости в отчетности. Потенциальная польза от универсальных политик BCG требует тщательной оценки. Чтобы восполнить этот пробел, мы сосредоточились на темпах роста как подтвержденных случаев, так и смертей в ранний период вспышек в странах и проверили, может ли этот темп быть медленнее в странах, где вакцинация БЦЖ обязательна как минимум до 2000 г., по сравнению с теми, что нет. Вакцина БЦЖ используется против туберкулеза ( 4 ).Один обзор показал, что вакцинация БЦЖ снижает риск заболевания туберкулезом на 50% ( 5 ). Продолжение более раннего клинического испытания БЦЖ, проведенного на коренных американцах, показывает, что БЦЖ защищает людей как от туберкулеза, так и от рака легких на срок до нескольких десятилетий на протяжении всей жизни каждого человека ( 2 , 3 ). Более поздний метаанализ более широкого круга обсервационных исследований и клинических испытаний ( 1 ) предполагает, что эффективность БЦЖ может распространяться на смертность от всех причин.
Однако существующим межнациональным анализам препятствуют методологические недостатки.По большей части не было предпринято никаких усилий, чтобы исключить возможные последствия предвзятости в отчетности. Потенциальная польза от универсальных политик BCG требует тщательной оценки. Чтобы восполнить этот пробел, мы сосредоточились на темпах роста как подтвержденных случаев, так и смертей в ранний период вспышек в странах и проверили, может ли этот темп быть медленнее в странах, где вакцинация БЦЖ обязательна как минимум до 2000 г., по сравнению с теми, что нет. Вакцина БЦЖ используется против туберкулеза ( 4 ).Один обзор показал, что вакцинация БЦЖ снижает риск заболевания туберкулезом на 50% ( 5 ). Продолжение более раннего клинического испытания БЦЖ, проведенного на коренных американцах, показывает, что БЦЖ защищает людей как от туберкулеза, так и от рака легких на срок до нескольких десятилетий на протяжении всей жизни каждого человека ( 2 , 3 ). Более поздний метаанализ более широкого круга обсервационных исследований и клинических испытаний ( 1 ) предполагает, что эффективность БЦЖ может распространяться на смертность от всех причин. В нескольких контролируемых исследованиях получены последовательные результаты, показывающие, что снижение смертности связано с защитой от респираторных инфекций, а также неонатального сепсиса ( 6 – 8 ). В совокупности имеющиеся данные свидетельствуют о том, что БЦЖ оказывает благотворное влияние на иммунитет против ряда инфекций, связанных с легкими, которые выходят за рамки туберкулеза, что делает ее многообещающим кандидатом для защиты от COVID-19. Что касается механизмов, то недавняя экспериментальная работа ( 9 ) показала, что вакцинация БЦЖ вызывает полногеномное эпигенетическое перепрограммирование моноцитов человека, что, в свою очередь, предсказывает защиту от экспериментальной вирусной инфекции.
В нескольких контролируемых исследованиях получены последовательные результаты, показывающие, что снижение смертности связано с защитой от респираторных инфекций, а также неонатального сепсиса ( 6 – 8 ). В совокупности имеющиеся данные свидетельствуют о том, что БЦЖ оказывает благотворное влияние на иммунитет против ряда инфекций, связанных с легкими, которые выходят за рамки туберкулеза, что делает ее многообещающим кандидатом для защиты от COVID-19. Что касается механизмов, то недавняя экспериментальная работа ( 9 ) показала, что вакцинация БЦЖ вызывает полногеномное эпигенетическое перепрограммирование моноцитов человека, что, в свою очередь, предсказывает защиту от экспериментальной вирусной инфекции. За последнее столетие многие страны приняли всеобщую политику обязательной вакцинации БЦЖ для борьбы с туберкулезом, который в то время представлял серьезную угрозу. С тех пор многие страны придерживались такой политики, по крайней мере, до недавнего времени (например, Китай, Ирландия, Финляндия и Франция). Некоторые другие страны прекратили эту политику, поскольку туберкулез перестал представлять угрозу (например, Австралия, Испания и Эквадор). Следует отметить, что в некоторых странах вакцинация БЦЖ никогда не была обязательной (например, США, Италия и Ливан).Таким образом, существует достаточная вариабельность наличия или отсутствия такой политики, распределенной по разным регионам мира, чтобы можно было проводить систематические сравнения.
Некоторые другие страны прекратили эту политику, поскольку туберкулез перестал представлять угрозу (например, Австралия, Испания и Эквадор). Следует отметить, что в некоторых странах вакцинация БЦЖ никогда не была обязательной (например, США, Италия и Ливан).Таким образом, существует достаточная вариабельность наличия или отсутствия такой политики, распределенной по разным регионам мира, чтобы можно было проводить систематические сравнения.
 Чтобы исключить любое систематическое влияние межнациональных различий в предвзятости отчетности, мы сосредоточились на темпах роста как случаев, так и смертей. Эти показатели не подвержены ошибкам в отчетах до тех пор, пока эти ошибки остаются стабильными в течение тестируемого периода. Таким образом, чтобы избежать каких-либо систематических изменений в предвзятости отчетности, важно изучить короткий начальный период роста.В то же время для получения достоверных оценок скорости роста необходима проверка достаточно длительного периода. Чтобы одновременно удовлетворить эти два конкурирующих требования, мы решили изучить первые 30 дней начала вспышек в стране в основном анализе, за которым последовала проверка устойчивости, проверяющая еще более короткий 15-дневный период. Кроме того, в последующем анализе мы приняли меру предвзятости отчетности по странам и соответственно взвесили данные. Кроме того, мы также контролировали доступность тестов.Сначала мы проверили, будут ли темпы роста значительно ниже в странах, которые продолжали обязательную вакцинацию БЦЖ по крайней мере до 2000 года, по сравнению со странами, которые в настоящее время не требуют ее.
Чтобы исключить любое систематическое влияние межнациональных различий в предвзятости отчетности, мы сосредоточились на темпах роста как случаев, так и смертей. Эти показатели не подвержены ошибкам в отчетах до тех пор, пока эти ошибки остаются стабильными в течение тестируемого периода. Таким образом, чтобы избежать каких-либо систематических изменений в предвзятости отчетности, важно изучить короткий начальный период роста.В то же время для получения достоверных оценок скорости роста необходима проверка достаточно длительного периода. Чтобы одновременно удовлетворить эти два конкурирующих требования, мы решили изучить первые 30 дней начала вспышек в стране в основном анализе, за которым последовала проверка устойчивости, проверяющая еще более короткий 15-дневный период. Кроме того, в последующем анализе мы приняли меру предвзятости отчетности по странам и соответственно взвесили данные. Кроме того, мы также контролировали доступность тестов.Сначала мы проверили, будут ли темпы роста значительно ниже в странах, которые продолжали обязательную вакцинацию БЦЖ по крайней мере до 2000 года, по сравнению со странами, которые в настоящее время не требуют ее.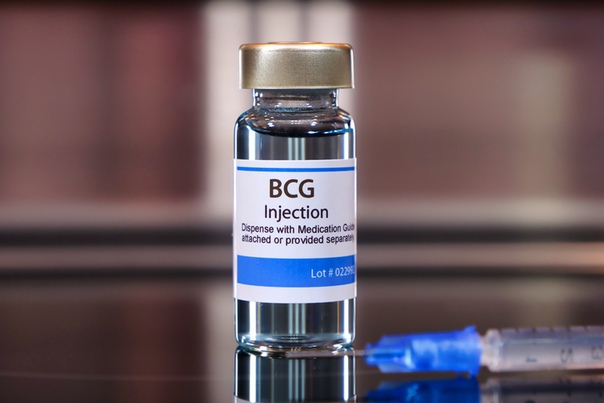 Этот год (2000 г.) был выбран, поскольку вакцинация может стать эффективной на уровне популяции только тогда, когда подавляющее большинство [от 70 до 80%, согласно моделированию, представленному в ( 11 ), при условии, что репродуктивное число (R0) для COVID-19 больше 3 ( 12 )] становится устойчивым к целевому вирусу, явление, известное как «коллективный иммунитет» ( 13 ).В странах, где вакцинация БЦЖ обязательна при рождении, по крайней мере, до 2000 года, подавляющее большинство взрослых должны были стать устойчивыми к вирусным инфекциям, связанным с легкими. Мы также исследовали, может ли быть какая-то разница между теми, у кого никогда не было такой политики, и теми, у кого она была в 20-м веке, но прекратила ее как минимум два десятилетия назад. В качестве дополнительной проверки надежности мы проверили, могут ли группы стран, которые различаются по статусу политики BCG, различаться по различным культурным параметрам, таким как индивидуализм и коллективизм ( 14 ).
Этот год (2000 г.) был выбран, поскольку вакцинация может стать эффективной на уровне популяции только тогда, когда подавляющее большинство [от 70 до 80%, согласно моделированию, представленному в ( 11 ), при условии, что репродуктивное число (R0) для COVID-19 больше 3 ( 12 )] становится устойчивым к целевому вирусу, явление, известное как «коллективный иммунитет» ( 13 ).В странах, где вакцинация БЦЖ обязательна при рождении, по крайней мере, до 2000 года, подавляющее большинство взрослых должны были стать устойчивыми к вирусным инфекциям, связанным с легкими. Мы также исследовали, может ли быть какая-то разница между теми, у кого никогда не было такой политики, и теми, у кого она была в 20-м веке, но прекратила ее как минимум два десятилетия назад. В качестве дополнительной проверки надежности мы проверили, могут ли группы стран, которые различаются по статусу политики BCG, различаться по различным культурным параметрам, таким как индивидуализм и коллективизм ( 14 ).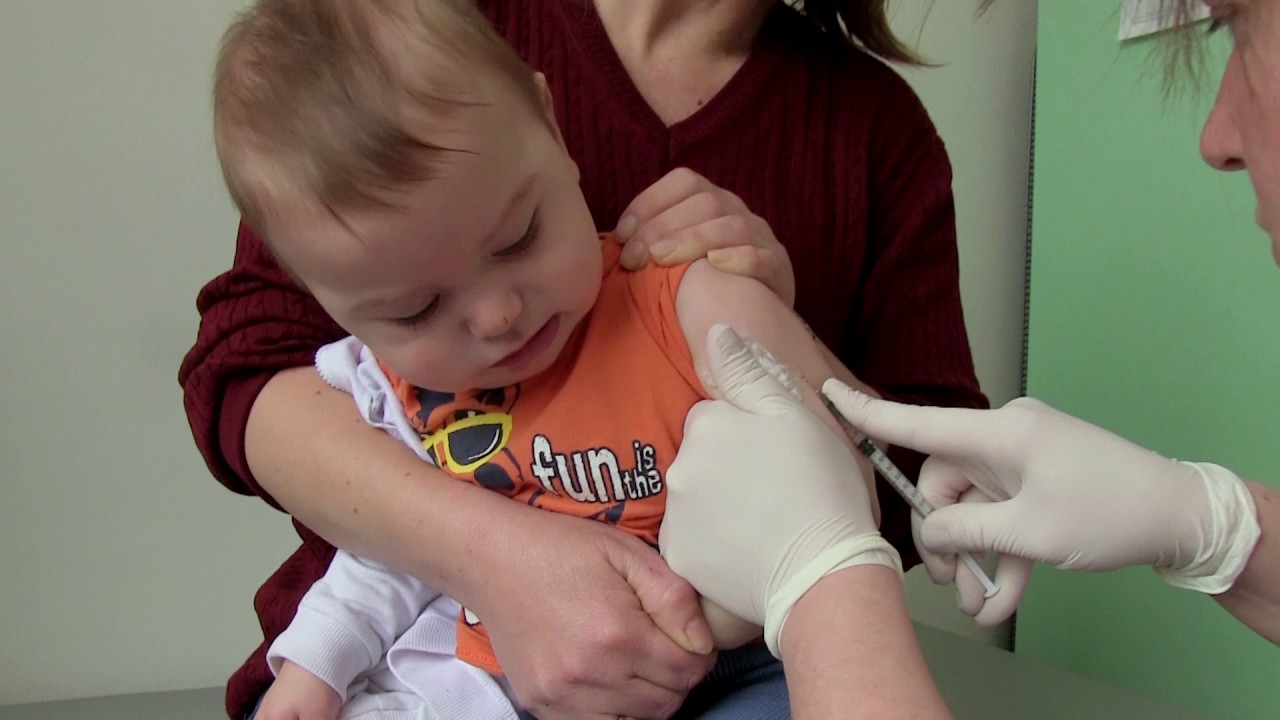
РЕЗУЛЬТАТЫ
Подтвержденные случаи
Все страны, в которых за последние 15 дней было зарегистрировано не менее 100 подтвержденных случаев, и которые имели доступные данные о политике БЦЖ и ковариатах (средний возраст, валовой внутренний продукт на душу населения, плотность населения, численность населения, и коэффициент чистой миграции) (всего 134 страны). Для каждой страны день 1 был установлен как первый день не менее 100 подтвержденных случаев. См. столбец 2 таблицы S1 для даты первого дня для каждой включенной страны.
Чтобы смоделировать экспоненциальный рост подтвержденных случаев, мы оценили линейную смешанную модель естественного логарифмически преобразованного числа подтвержденных случаев. Мы ввели два противопоставления, обозначающие статус полиса BCG [текущий по сравнению с (прошлым и отсутствующим) в совокупности и прошлый по сравнению с отсутствием]. Влияние статуса полиса BCG на скорость роста отражается взаимодействием между днем и контрастом статуса каждого полиса BCG.
| A. Случаи | B. ТНТ | |||||||
|---|---|---|---|---|---|---|---|---|
| Predictor | б | т | Р | б | т | П | ||
| 42.165 | <0,001 | 2,445 | 8,284 | <0,001 | ||||
| День | 0,114 | 12,218 | <0,001 | 0,139 | 9,236 | <0,001 | ||
| Средний возраст | 0. 219 219 | 2.164 | 0.034 | 0.224 | 0.224 | 1.363 | 0.176 | |
| ВВП на душу населения | 0.163 | 1.586 | 0.115 | 0.145 | 0.145 | 0.930 | 0.354 | 0.354 |
| -0.099 | -1.715 | -1.79 | -0.012 | -0.135 | -0.135 | 0.893 | ||
| Чистый курс миграции | 0.111 | 1.242 | 0.217 | 0,217 | 0.050 | 0.368 | 0.368 | 0.713 |
| Население | 0. 518 518 | 8.533 | <0,001 | 0.679 | 7.281 | <0.001 | ||
| BCG Прошло против Never | 0.136 | 0,415 | 0,679 | -0.164 | -0.322 | -0.322 | 0.748 | |
| BCG Ток против не текущих | -0.633 | -3.388 | 0.001 | -0.993 | -0.993 | -3.437 | 0.001 | |
| День × Средний возраст | 0,008 | 1.442 | 0,153 | 0.020 | 2.631 | 0,010 | ||
| день × ВВП на душу | 0,010 | 1,951 | 0,053 0,011 1,515 | |||||
| Плотность населения день × | -0,001 -0,390 0,697 | -0. 003 003 | -0.674 | -0.674 | 0.502 | |||
| День × Чистая скорость миграции | 0,005 | 1.051 | 0.295 | 0.003 | 0.492 | 0.623 | ||
| населения Дэй × 0,030 | 9,617 <0,001 | 0,037 | 8,860 | <0,001 | ||||
| день × БЦЖ в прошлом по сравнению с никогда | -0,009 -0,511 | 0,610 | -0.007 | -0.291 | 9 -0.2910.772 | |||
| день × BCG ток против не тока | -0.039 | -3.978 | — 0.059 | -4.530 | <0,001 | |||
Таблица 1. Таблицы регрессии, предсказывающие рост (A) случаев и (B) смертей. Day центрирован по среднему значению, а переменные политики BCG имеют контрастное кодирование.
Таблицы регрессии, предсказывающие рост (A) случаев и (B) смертей. Day центрирован по среднему значению, а переменные политики BCG имеют контрастное кодирование.
Население подвергается естественному логарифмическому преобразованию, и все ковариаты стандартизированы. Этот анализ основан на 134 и 135 странах по заболеваемости и смертности соответственно. ВВП, валовой внутренний продукт.
Рис. 1 Кривые роста числа случаев COVID-19 и смертей в зависимости от страновой политики БЦЖ.
( A и B ) случаев и ( C и D ) смертей, представленных в линейной (A и C) и логарифмической (B и D) шкалах.
Рис. 2 Кривые роста числа случаев COVID-19 и смертей в зависимости от страновой политики БЦЖ.
Темпы роста корректируются с учетом среднего возраста, ВВП на душу населения, плотности населения, общей численности населения (логарифмически преобразованной) и коэффициента чистой миграции. Для каждой группы нанесены средние значения и стандартная ошибка.
Страны, которые когда-то проводили такую политику, но отменили ее до 2000 г., существенно не отличались по темпам роста от тех, которые никогда не вводили обязательную вакцинацию БЦЖ, b = −0.009, Р = 0,610. С точки зрения контрольных переменных, больший размер популяции предсказывал более высокие темпы роста подтвержденных случаев. См. таблицу S2 для корреляционной таблицы всех переменных-предикторов.
Влияние статуса политики БЦЖ на случаи COVID-19 оставалось неизменным при взвешивании стран по качеству отчетности (дополнительный анализ 1) и при контроле общего количества тестов (дополнительный анализ 2). Следовательно, предвзятость в тестировании и отчетности, явно распространенная в разных странах, практически не повлияла на влияние универсальной политики БЦЖ на темпы роста.Более того, этот эффект также не изменился при использовании 15-дневного временного окна (дополнительный анализ 3), что добавило дополнительные доказательства того, что основной анализ вряд ли связан с какими-либо систематическими изменениями в отчетных погрешностях в течение 30-дневного периода. Кроме того, эффект БКГ имел мало общего с культурными аспектами индивидуализма по сравнению с коллективизмом или дистанцированием от власти (дополнительный анализ 4).
Кроме того, эффект БКГ имел мало общего с культурными аспектами индивидуализма по сравнению с коллективизмом или дистанцированием от власти (дополнительный анализ 4).
Смерти
В этот анализ были включены все страны, которые сообщили о хотя бы одной смерти от COVID-19 в течение 15 дней и располагали доступными данными о политике БЦЖ и ковариатах (всего 135 стран).Для каждой страны день 1 был установлен как первый день хотя бы одной подтвержденной смерти. См. столбец 3 таблицы S1 для даты первого дня для каждой включенной страны.
Мы оценили линейную смешанную модель естественного логарифмически преобразованного количества смертей, контролируя те же контрольные переменные, что и выше. Как и при анализе подтвержденных случаев, мы обнаружили значительный основной эффект дня, b = 0,139, P Таблица 1B). Это увеличение было обусловлено значительной взаимосвязью между днем и статусом полиса BCG.В частности, темпы роста числа смертей, связанных с COVID-19, были значительно ниже в странах с обязательной вакцинацией БЦЖ по крайней мере до 2000 г. по сравнению со странами без обязательной вакцинации БЦЖ до 2000 г., b = -0,059, P С и Д). На рис. 2В показано распределение коэффициентов регрессии по странам.
по сравнению со странами без обязательной вакцинации БЦЖ до 2000 г., b = -0,059, P С и Д). На рис. 2В показано распределение коэффициентов регрессии по странам.Страны, которые когда-то имели такую политику, но отменили ее до 2000 г., по темпам роста не отличались от тех, которые никогда не вводили обязательную БКГ, b = −0.007, Р = 0,772. С точки зрения контрольных переменных, большая численность населения и более высокий средний возраст предсказывали более высокие темпы роста смертности от COVID-19.
Влияние статуса политики БЦЖ на смертность, связанную с COVID-19, оставалось неизменным при использовании 15-дневного временного окна (дополнительный анализ 3), что свидетельствует о надежности основного анализа. Кроме того, эффект БЦЖ не был связан с упомянутыми выше культурными аспектами (дополнительный анализ 4).
ОБСУЖДЕНИЕ
Наш анализ показывает, что обязательная вакцинация БЦЖ связана со сглаживанием кривой распространения COVID-19. Эффект, который мы демонстрируем, весьма значителен. Например, согласно нашей модели, общее число смертей, связанных с COVID-19, в Соединенных Штатах по состоянию на 29 марта 2020 года составило бы 468 (19% от фактического числа (2467)), если бы Соединенные Штаты ввели обязательную вакцинацию БЦЖ. вакцинация несколькими десятилетиями ранее (см. Дополнительный анализ 5).
Эффект, который мы демонстрируем, весьма значителен. Например, согласно нашей модели, общее число смертей, связанных с COVID-19, в Соединенных Штатах по состоянию на 29 марта 2020 года составило бы 468 (19% от фактического числа (2467)), если бы Соединенные Штаты ввели обязательную вакцинацию БЦЖ. вакцинация несколькими десятилетиями ранее (см. Дополнительный анализ 5).
 Мы обошли эти проблемы тремя способами.Во-первых, мы сосредоточились на темпах роста как числа случаев, так и смертей, на которые не должны влиять ошибки в отчетности, если эти ошибки стабильны в течение периода исследования. Чтобы выполнить это требование, мы сосредоточились на коротком периоде (либо первые 30 дней, либо 15 дней). Во-вторых, мы использовали наилучшую доступную оценку предвзятости отчетности по странам в качестве веса в нашем анализе. В-третьих, мы контролировали доступность тестирования. Примечательно, что кривые роста были такими же крутыми в странах, где политика BCG была обязательной только в 20-м веке (т.е., те, которые прекратили политику до 2000 г.), как и те, которые никогда не требовали вакцинации. Вакцинация БЦЖ может стать эффективной только тогда, когда значительная часть населения становится устойчивой к вирусу. Другими словами, распространение вируса можно замедлить только при наличии коллективного иммунитета, препятствующего легкому распространению вируса среди населения [см.
Мы обошли эти проблемы тремя способами.Во-первых, мы сосредоточились на темпах роста как числа случаев, так и смертей, на которые не должны влиять ошибки в отчетности, если эти ошибки стабильны в течение периода исследования. Чтобы выполнить это требование, мы сосредоточились на коротком периоде (либо первые 30 дней, либо 15 дней). Во-вторых, мы использовали наилучшую доступную оценку предвзятости отчетности по странам в качестве веса в нашем анализе. В-третьих, мы контролировали доступность тестирования. Примечательно, что кривые роста были такими же крутыми в странах, где политика BCG была обязательной только в 20-м веке (т.е., те, которые прекратили политику до 2000 г.), как и те, которые никогда не требовали вакцинации. Вакцинация БЦЖ может стать эффективной только тогда, когда значительная часть населения становится устойчивой к вирусу. Другими словами, распространение вируса можно замедлить только при наличии коллективного иммунитета, препятствующего легкому распространению вируса среди населения [см. симуляцию в ( 11 )]. Обратите внимание, что до тех пор, пока другие получают вакцинацию, любой отдельный человек будет защищен без вакцинации, что приведет к искушению безбилетника (т.е., не вакцинированные). Следовательно, в отсутствие обязательной вакцинации, навязанной государством, культурные нормы, подчеркивающие просоциальную взаимозависимую ориентацию ( 33 , 34 ), могут оказаться решающими для успеха БЦЖ в предотвращении будущих вспышек COVID-19 ( 11 , 35 ). Хотя текущий анализ не предоставил никаких доказательств, эта возможность должна быть рассмотрена в будущей работе. Необходимо признать некоторые ограничения наших усилий. Во всех национальных стратегиях БЦЖ вводится в раннем возрасте, обычно при рождении.Остается неясным, может ли вакцинация БЦЖ быть эффективной при введении взрослым, а также неизвестно, как долго вакцинация БЦЖ может обеспечивать иммунитет к COVID-19, хотя она эффективна против туберкулеза и рака легких в течение нескольких десятилетий ( 2 , 3 ).
симуляцию в ( 11 )]. Обратите внимание, что до тех пор, пока другие получают вакцинацию, любой отдельный человек будет защищен без вакцинации, что приведет к искушению безбилетника (т.е., не вакцинированные). Следовательно, в отсутствие обязательной вакцинации, навязанной государством, культурные нормы, подчеркивающие просоциальную взаимозависимую ориентацию ( 33 , 34 ), могут оказаться решающими для успеха БЦЖ в предотвращении будущих вспышек COVID-19 ( 11 , 35 ). Хотя текущий анализ не предоставил никаких доказательств, эта возможность должна быть рассмотрена в будущей работе. Необходимо признать некоторые ограничения наших усилий. Во всех национальных стратегиях БЦЖ вводится в раннем возрасте, обычно при рождении.Остается неясным, может ли вакцинация БЦЖ быть эффективной при введении взрослым, а также неизвестно, как долго вакцинация БЦЖ может обеспечивать иммунитет к COVID-19, хотя она эффективна против туберкулеза и рака легких в течение нескольких десятилетий ( 2 , 3 ). ). Кроме того, неясно, может ли БЦЖ иметь какие-либо побочные эффекты при введении тем, кто уже инфицирован COVID-19. Существует острая необходимость в рандомизированных клинических испытаниях. Наконец, темпы экспоненциального роста показали существенную вариабельность в странах, в которых вакцинация БЦЖ обязательна (рис.2, А и Б). Следовательно, БЦЖ ни в коем случае не является волшебным средством, обеспечивающим безопасность от COVID-19. По всей вероятности, существуют некоторые социальные переменные, которые смягчают этот эффект. Это изменение должно быть учтено в дальнейшей работе. Несмотря на все эти ограничения, текущие данные впервые убедительно демонстрируют значительное преимущество универсальной политики БЦЖ в снижении распространения COVID-19, тем самым оправдывая тщательное исследование достоинств обязательной вакцинации БЦЖ в борьбе с COVID-19. .
). Кроме того, неясно, может ли БЦЖ иметь какие-либо побочные эффекты при введении тем, кто уже инфицирован COVID-19. Существует острая необходимость в рандомизированных клинических испытаниях. Наконец, темпы экспоненциального роста показали существенную вариабельность в странах, в которых вакцинация БЦЖ обязательна (рис.2, А и Б). Следовательно, БЦЖ ни в коем случае не является волшебным средством, обеспечивающим безопасность от COVID-19. По всей вероятности, существуют некоторые социальные переменные, которые смягчают этот эффект. Это изменение должно быть учтено в дальнейшей работе. Несмотря на все эти ограничения, текущие данные впервые убедительно демонстрируют значительное преимущество универсальной политики БЦЖ в снижении распространения COVID-19, тем самым оправдывая тщательное исследование достоинств обязательной вакцинации БЦЖ в борьбе с COVID-19. .Влияние вакцинации БЦЖ на провоспалительные реакции у пожилых людей
. 2021 авг. 4;7(32):eabg7181.
doi: 10.1126/sciadv.abg7181.
Печать 2021 авг.
2021 авг. 4;7(32):eabg7181.
doi: 10.1126/sciadv.abg7181.
Печать 2021 авг.Принадлежности Расширять
Принадлежности
- 1 ICMR — Национальный институт исследований туберкулеза, Ченнаи, Индия[email protected] [email protected].
- 2 ICMR — Национальный институт исследований туберкулеза, Ченнаи, Индия.
- 3 ICMR — Национальный институт исследований туберкулеза — Международный центр передового опыта в области исследований, Ченнаи, Индия.

- 4 ICMR-Национальный институт эпидемиологии, Ченнаи, Индия.
- 5 ICMR — Национальный институт исследований туберкулеза — Международный центр передового опыта в области исследований, Ченнаи, Индия[email protected] [email protected].
Элемент в буфере обмена
Нателла Паван Кумар и соавт. Научная реклама .
Бесплатная статья ЧВК Показать детали Показать вариантыПоказать варианты
Формат АннотацияPubMedPMID
. 2021 авг. 4;7(32):eabg7181.
doi: 10.1126/sciadv.abg7181.
Печать 2021 авг.
2021 авг. 4;7(32):eabg7181.
doi: 10.1126/sciadv.abg7181.
Печать 2021 авг.Принадлежности
- 1 ICMR — Национальный институт исследований туберкулеза, Ченнаи, Индия. [email protected].на [email protected].
- 2 ICMR — Национальный институт исследований туберкулеза, Ченнаи, Индия.
- 3 ICMR — Национальный институт исследований туберкулеза — Международный центр передового опыта в области исследований, Ченнаи, Индия.
- 4 ICMR-Национальный институт эпидемиологии, Ченнаи, Индия.

- 5 ICMR — Национальный институт исследований туберкулеза — Международный центр передового опыта в области исследований, Ченнаи, Индия[email protected] [email protected].
Элемент в буфере обмена
Полнотекстовые ссылки Параметры отображения цитированияПоказать варианты
Формат АннотацияPubMedPMID
Абстрактный
Мы исследовали влияние вакцинации бациллой Кальметта-Герена (БЦЖ) на нестимулированные уровни в плазме широкого набора цитокинов, хемокинов, белков острой фазы (АРР), матриксных металлопротеиназ (ММП) и факторов роста в группе здоровых пожилых людей. лицам (возраст от 60 до 80 лет) в начале исследования (до вакцинации) и через 1 месяц после вакцинации в рамках нашего клинического исследования по изучению влияния БЦЖ на COVID-19.Наши результаты показали, что вакцинация БЦЖ приводила к снижению уровней в плазме крови типов 1, 2 и 17 и других провоспалительных цитокинов и интерферонов типа 1. Вакцинация БЦЖ также приводила к снижению уровней в плазме СС, хемокинов СХС, АРР, ММР и факторов роста. Плазменные уровни вышеупомянутых параметров были значительно ниже у вакцинированных лиц по сравнению с невакцинированными контрольными людьми. Таким образом, наше исследование демонстрирует иммуномодулирующие свойства вакцинации БЦЖ и предполагает ее потенциальную полезность в неспецифической вакцинации против COVID-19 путем подавления патогенных воспалительных реакций.
лицам (возраст от 60 до 80 лет) в начале исследования (до вакцинации) и через 1 месяц после вакцинации в рамках нашего клинического исследования по изучению влияния БЦЖ на COVID-19.Наши результаты показали, что вакцинация БЦЖ приводила к снижению уровней в плазме крови типов 1, 2 и 17 и других провоспалительных цитокинов и интерферонов типа 1. Вакцинация БЦЖ также приводила к снижению уровней в плазме СС, хемокинов СХС, АРР, ММР и факторов роста. Плазменные уровни вышеупомянутых параметров были значительно ниже у вакцинированных лиц по сравнению с невакцинированными контрольными людьми. Таким образом, наше исследование демонстрирует иммуномодулирующие свойства вакцинации БЦЖ и предполагает ее потенциальную полезность в неспецифической вакцинации против COVID-19 путем подавления патогенных воспалительных реакций.
Copyright © 2021 Авторы, некоторые права защищены; эксклюзивный лицензиат Американской ассоциации содействия развитию науки. Претензий к оригинальным работам правительства США нет. Распространяется по лицензии Creative Commons Attribution License 4.0 (CC BY).
Претензий к оригинальным работам правительства США нет. Распространяется по лицензии Creative Commons Attribution License 4.0 (CC BY).
Цифры
Рис.1. Прививка БЦЖ снижает…
Рис. 1. Вакцинация БЦЖ приводит к снижению уровня про- и противовоспалительных цитокинов в плазме крови.
Рис. 1. Вакцинация БЦЖ приводит к снижению уровня про- и противовоспалительных цитокинов в плазме крови. ( A ) Уровни в плазме цитокинов типа 1, семейства IL-1 и IFN типа 1 у предварительно вакцинированных БЦЖ (M0) ( n = 82) и M1 после вакцинации ( n = 82) и уровни в плазме показаны цитокины 1-го типа, семейство IL-1 и IFN 1-го типа у невакцинированных БЦЖ (UVC) ( n = 55) и поствакцинированных (M1) ( n = 82). ( B ) Уровни провоспалительных цитокинов в плазме у предвакцинированных БЦЖ (М0) ( n = 82) и М1 после вакцинации ( n = 82) и уровни провоспалительных цитокинов в плазме у невакцинированных БЦЖ (УВК) ( n = 55) и поствакцинированные (М1) ( n = 82) особи. ( C ) Уровни противовоспалительных цитокинов в плазме у предвакцинированных БЦЖ (М0) ( n = 82) и М1 после вакцинации ( n = 82) и уровни противовоспалительных цитокинов в плазме у невакцинированных БЦЖ ( UVC) ( n = 55) и поствакцинированные (M1) ( n = 82) особи.Данные представлены в виде точечных диаграмм, где каждый кружок представляет одного человека. Для анализа M0 и M1 было рассчитано значений P с использованием парного критерия Уилкоксона с поправкой Холма на множественные сравнения; для анализа между UVC и M1 значений P были рассчитаны с использованием критерия Манна-Уитни с поправкой Холма на множественные сравнения.
( B ) Уровни провоспалительных цитокинов в плазме у предвакцинированных БЦЖ (М0) ( n = 82) и М1 после вакцинации ( n = 82) и уровни провоспалительных цитокинов в плазме у невакцинированных БЦЖ (УВК) ( n = 55) и поствакцинированные (М1) ( n = 82) особи. ( C ) Уровни противовоспалительных цитокинов в плазме у предвакцинированных БЦЖ (М0) ( n = 82) и М1 после вакцинации ( n = 82) и уровни противовоспалительных цитокинов в плазме у невакцинированных БЦЖ ( UVC) ( n = 55) и поствакцинированные (M1) ( n = 82) особи.Данные представлены в виде точечных диаграмм, где каждый кружок представляет одного человека. Для анализа M0 и M1 было рассчитано значений P с использованием парного критерия Уилкоксона с поправкой Холма на множественные сравнения; для анализа между UVC и M1 значений P были рассчитаны с использованием критерия Манна-Уитни с поправкой Холма на множественные сравнения.
Рис. 2. Прививка БЦЖ снижает…
2. Прививка БЦЖ снижает…
Рис. 2. Вакцинация БЦЖ приводит к снижению уровня хемокинов в плазме.
Рис. 2. Вакцинация БЦЖ приводит к снижению уровня хемокинов в плазме. ( A ) Уровни хемокинов СС в плазме у предвакцинированных БЦЖ (М0) ( n = 64) и М1 после вакцинации ( n = 82) и уровни хемокинов СС в плазме у невакцинированных БЦЖ (УВК) ( n = 55) и поствакцинированные (М1) ( n = 82) особи.( B ) Уровни хемокинов СХС в плазме у предвакцинированных БЦЖ (М0) ( n = 82) и М1 после вакцинации ( n = 82) и уровни хемокинов СХС в плазме у невакцинированных БЦЖ (УВК) ( n = 55) и поствакцинированные (М1) ( n = 82) особи. Данные представлены в виде точечных диаграмм, где каждый кружок представляет одного человека.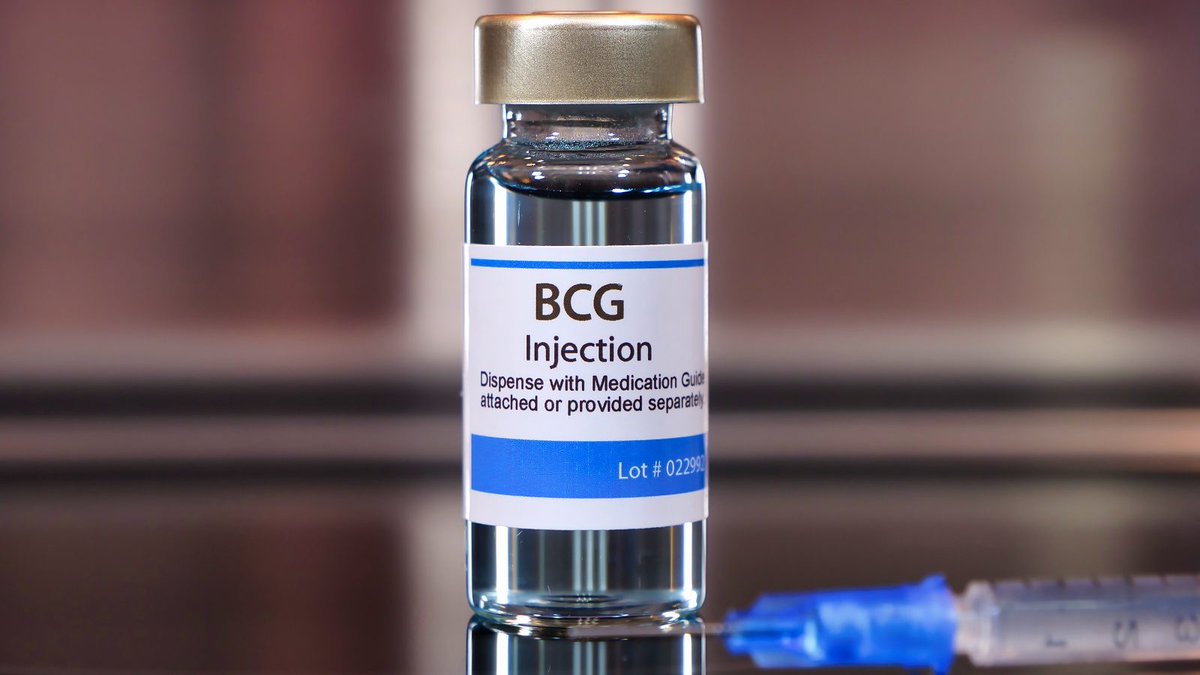 Для анализа M0 и M1 было рассчитано значений P с использованием парного критерия Уилкоксона с поправкой Холмса для множественных сравнений; для анализа между UVC и M1 значений P были рассчитаны с использованием критерия Манна-Уитни с поправкой Холма на множественные сравнения.
Для анализа M0 и M1 было рассчитано значений P с использованием парного критерия Уилкоксона с поправкой Холмса для множественных сравнений; для анализа между UVC и M1 значений P были рассчитаны с использованием критерия Манна-Уитни с поправкой Холма на множественные сравнения.
Рис. 3. Прививка БЦЖ приводит к снижению…
Рис. 3. Вакцинация БЦЖ приводит к снижению уровня АРР в плазме крови.
Инжир.3. Вакцинация БЦЖ приводит к снижению уровня АРР в плазме. Показаны уровни АРР в плазме у предварительно вакцинированных БЦЖ (М0) ( n = 82) и М1 после вакцинации ( n = 82). Данные отображаются в виде линейных диаграмм, где каждая линия представляет одного человека. Значения P были рассчитаны с использованием тестов Уилкоксона на согласованные пары с поправкой Холма для множественных сравнений. Также показаны уровни APP в плазме у невакцинированных БЦЖ (UVC) ( n = 55) и поствакцинированных (M1) ( n = 82) лиц.Данные представлены в виде точечных диаграмм, где каждый кружок представляет одного человека. Значения P рассчитывали по критерию Манна-Уитни с поправкой Холма на множественные сравнения.
Данные отображаются в виде линейных диаграмм, где каждая линия представляет одного человека. Значения P были рассчитаны с использованием тестов Уилкоксона на согласованные пары с поправкой Холма для множественных сравнений. Также показаны уровни APP в плазме у невакцинированных БЦЖ (UVC) ( n = 55) и поствакцинированных (M1) ( n = 82) лиц.Данные представлены в виде точечных диаграмм, где каждый кружок представляет одного человека. Значения P рассчитывали по критерию Манна-Уитни с поправкой Холма на множественные сравнения.
Рис. 4. Прививка БЦЖ приводит к снижению…
Рис.4. Вакцинация БЦЖ приводит к снижению уровня ММП в плазме крови.
Рис. 4. Вакцинация БЦЖ приводит к снижению уровня ММП в плазме крови.
4. Вакцинация БЦЖ приводит к снижению уровня ММП в плазме крови. Показаны уровни ММП в плазме у предварительно вакцинированных БЦЖ (М0) ( n = 82) и М1 после вакцинации ( n = 82). Данные отображаются в виде линейных диаграмм, где каждая линия представляет одного человека. Значения P были рассчитаны с использованием тестов Уилкоксона на согласованные пары с поправкой Холма для множественных сравнений.Также показаны уровни ММР в плазме у невакцинированных БЦЖ (УВК) ( n = 55) и поствакцинированных (М1) ( n = 82) лиц. Данные представлены в виде точечных диаграмм, где каждый кружок представляет одного человека. Значения P рассчитывали по критерию Манна-Уитни с поправкой Холма на множественные сравнения.
Рис.5. Прививка БЦЖ снижает…
Рис. 5. Вакцинация БЦЖ приводит к снижению уровня факторов роста в плазме.
5. Вакцинация БЦЖ приводит к снижению уровня факторов роста в плазме.
Показаны уровни факторов роста в плазме у предварительно вакцинированных БЦЖ (М0) ( n = 82) и М1 после вакцинации ( n = 82).Данные показаны линейными диаграммами, где каждая линия представляет одного человека. Значения P были рассчитаны с использованием тестов Уилкоксона на согласованные пары с поправкой Холма для множественных сравнений. Также показаны уровни ММР в плазме у невакцинированных БЦЖ (УВК) ( n = 55) и поствакцинированных (М1) ( n = 82) лиц. Данные представлены в виде точечных диаграмм, где каждый кружок представляет одного человека. Значения P рассчитывали по критерию Манна-Уитни с поправкой Холма на множественные сравнения.
Похожие статьи
- Вакцинация БЦЖ и риск заражения COVID-19: возможная взаимосвязь.

Ахмед С.М., Наср М.А., Эльшенави С.Е., Хусейн А.Е., Эль-Бетар А.Х., Мохамед Р.Х., Эль-Бадри Н. Ахмед С.М. и др. Вирусология. 2022 2 января; 565: 73-81. doi: 10.1016/j.virol.2021.10.003. Epub 2021 28 октября.Вирусология. 2022. PMID: 34742127 Бесплатная статья ЧВК.
- История вакцинации БЦЖ связана со снижением серораспространенности SARS-CoV-2 среди различных групп медицинских работников.
Ривас М.Н., Эбингер Дж.Е., Ву М., Сун Н., Браун Дж., Собхани К., Ван Эйк Дж.Е., Ченг С., Ардити М. Ривас М.Н. и соавт. Джей Клин Инвест. 2021 19 января; 131 (2): e145157. DOI: 10.1172/JCI145157.Джей Клин Инвест. 2021. PMID: 33211672 Бесплатная статья ЧВК.
- Вакцинация БЦЖ вызывает повышенную частоту дендритных клеток и изменение уровня интерферонов типа I и типа III в плазме у пожилых людей.

Кумар Н.П., Падмаприядарсини С., Раджаманикам А., Бхавани П.К., Нэнси А., Джеядипа Б., Селварадж Н., Ашокан Д., Ренджи Р.М., Венкатарамани В., Трипати С., Бабу С.Кумар Н.П. и соавт. Int J Infect Dis. 2021 сен; 110: 98-104. doi: 10.1016/j.ijid.2021.07.041. Epub 2021 22 июля. Int J Infect Dis. 2021. PMID: 34302964 Бесплатная статья ЧВК.
- Ревакцинация БЦЖ медицинских работников в Бразилии для улучшения врожденного иммунного ответа против COVID-19: структурированное резюме протокола исследования для рандомизированного контролируемого исследования.
Junqueira-Kipnis AP, Dos Anjos LRB, Barbosa LCS, da Costa AC, Borges KCM, Cardoso ADRO, Ribeiro KM, Rosa SBA, Souza CC, das Neves RC, Saraiva G, da Silva SM, Silveira EA, Rabahi MF, Conte MB , Кипнис А.Junqueira-Kipnis AP, et al. Испытания. 2020 26 октября; 21 (1): 881. doi: 10.
 1186/s13063-020-04822-0.
Испытания. 2020.
PMID: 33106170
Бесплатная статья ЧВК.
Клиническое испытание.
1186/s13063-020-04822-0.
Испытания. 2020.
PMID: 33106170
Бесплатная статья ЧВК.
Клиническое испытание. - Вакцина БЦЖ от COVID-19: первый вердикт и дальнейшие направления.
Гонсалес-Перес М., Санчес-Тархуэло Р., Шор Б., Нистал-Виллан Э., Очандо Х. Гонсалес-Перес М. и соавт. Фронт Иммунол.2021 8 марта; 12:632478. doi: 10.3389/fimmu.2021.632478. Электронная коллекция 2021. Фронт Иммунол. 2021. PMID: 33763077 Бесплатная статья ЧВК. Обзор.
использованная литература
- Тай М. З., Пох С. М., Рения Л., МакЭри П. А., Нг Л. Ф. П., Троица COVID-19: иммунитет, воспаление и вмешательство.Нац. Преподобный Иммунол. 20, 363–374 (2020).
 —
ЧВК
—
пабмед
—
ЧВК
—
пабмед
- Тай М. З., Пох С. М., Рения Л., МакЭри П. А., Нг Л. Ф. П., Троица COVID-19: иммунитет, воспаление и вмешательство.Нац. Преподобный Иммунол. 20, 363–374 (2020).
- Бенн К. С., Нетеа М. Г., Селин Л. К., Ааби П., Маленький укол — большой эффект: неспецифическая иммуномодуляция вакцинами. Тренды Иммунол. 34, 431–439 (2013). — пабмед
- Биринг-Соренсен С., Ааби П., Лунд Н., Монтейро И., Дженсен К. Дж., Эриксен Х. Б., Шальц-Бухгольц Ф., Jorgensen A.S.P., Rodrigues A.
 , Fisker A.B., Benn C.S., Early BCG-Дания и неонатальная смертность среди младенцев с массой тела <2500 г: рандомизированное контролируемое исследование. клин. Заразить. Дис. 65, 1183–1190 (2017).
-
ЧВК
-
пабмед
, Fisker A.B., Benn C.S., Early BCG-Дания и неонатальная смертность среди младенцев с массой тела <2500 г: рандомизированное контролируемое исследование. клин. Заразить. Дис. 65, 1183–1190 (2017).
-
ЧВК
-
пабмед
- Биринг-Соренсен С., Ааби П., Лунд Н., Монтейро И., Дженсен К. Дж., Эриксен Х. Б., Шальц-Бухгольц Ф., Jorgensen A.S.P., Rodrigues A.
- Гарли М.L., Martins C.L., Bale C., Balde M.A., Hedegaard K.L., Gustafson P., Lisse I.M., Whittle HC, Aaby P., БЦЖ-рубец и положительная туберкулиновая реакция связаны со снижением детской смертности в Западной Африке. Неспецифический положительный эффект БЦЖ? Вакцина 21, 2782–2790 (2003 г.). — пабмед
- Немес Э.
 , Гелденхейс Х., Розот В., Рутковски К.Т., Ратанджи Ф., Билек Н., Мабве С., Махете Л., Эразмус М., Тофи А., Муленга Х., Ханеком В.А., Селф С.Г., Беккер Л.- Г., Райалл Р., Гурунатан С., ДиазГранадос К.А., Андерсен П., Кроманн И., Эванс Т., Эллис Р.Д., Лэндри Б., Хоки Д.А., Хопкинс Р., Гинзберг А.М., Скриба Т.Дж., Хазерилл М.; C-040-404 Исследовательская группа, Профилактика инфекции M.tuberculosis с помощью вакцины h5:IC31 или ревакцинации БЦЖ. Н. англ. Дж. Мед. 379, 138–149 (2018).
—
ЧВК
—
пабмед
, Гелденхейс Х., Розот В., Рутковски К.Т., Ратанджи Ф., Билек Н., Мабве С., Махете Л., Эразмус М., Тофи А., Муленга Х., Ханеком В.А., Селф С.Г., Беккер Л.- Г., Райалл Р., Гурунатан С., ДиазГранадос К.А., Андерсен П., Кроманн И., Эванс Т., Эллис Р.Д., Лэндри Б., Хоки Д.А., Хопкинс Р., Гинзберг А.М., Скриба Т.Дж., Хазерилл М.; C-040-404 Исследовательская группа, Профилактика инфекции M.tuberculosis с помощью вакцины h5:IC31 или ревакцинации БЦЖ. Н. англ. Дж. Мед. 379, 138–149 (2018).
—
ЧВК
—
пабмед
- Немес Э.
Показать все 35 ссылок
Типы публикаций
- Поддержка исследований, не-U.
 С. Правительство
С. Правительство
термины MeSH
- Вакцина БЦЖ / введение и дозировка*
- Воспаление/иммунология
- Воспаление/обмен веществ
- Воспаление/профилактика и контроль*
- Медиаторы воспаления/метаболизм*
Укажите
КопироватьФормат: ААД АПА МДА НЛМ
Защита от SARS-CoV-2 с помощью вакцинации БЦЖ не подтверждается эпидемиологическими анализами
По состоянию на 13 июня 2020 г. во всем мире было подтверждено 7 713 571 человек, инфицированных CoV-2.Интересно, что в настоящее время на https://clinicaltrials. gov зарегистрировано 17 клинических испытаний по оценке вакцинации БЦЖ от COVID-19 (таблица 1). Семь испытаний начаты в странах, где в настоящее время действует универсальная политика БЦЖ (Египет, Мексика, Южная Африка, Колумбия, Индия и Бразилия; таблица 1). Четыре испытания проводятся в странах, где в прошлом применялась универсальная политика вакцинации БЦЖ (Австралия, Дания и Франция), и 6 испытаний — в Нидерландах и США, двух странах, где никогда не проводилась универсальная политика вакцинации БЦЖ (таблица 1).Крупнейшее исследование, основанное на количестве участников, проводится в Австралии для изучения влияния вакцинации БЦЖ на заболеваемость, продолжительность и тяжесть заболевания COVID-19.
gov зарегистрировано 17 клинических испытаний по оценке вакцинации БЦЖ от COVID-19 (таблица 1). Семь испытаний начаты в странах, где в настоящее время действует универсальная политика БЦЖ (Египет, Мексика, Южная Африка, Колумбия, Индия и Бразилия; таблица 1). Четыре испытания проводятся в странах, где в прошлом применялась универсальная политика вакцинации БЦЖ (Австралия, Дания и Франция), и 6 испытаний — в Нидерландах и США, двух странах, где никогда не проводилась универсальная политика вакцинации БЦЖ (таблица 1).Крупнейшее исследование, основанное на количестве участников, проводится в Австралии для изучения влияния вакцинации БЦЖ на заболеваемость, продолжительность и тяжесть заболевания COVID-19.
Заинтригованные большим количеством начатых клинических испытаний, мы хотели проанализировать имеющиеся в настоящее время данные, чтобы проверить связь между политикой вакцинации БЦЖ и скоростью распространения CoV-2 и связанной с ним смертностью. Информация о политике вакцинации БЦЖ доступна для 158 стран (дополнительная таблица S1). В Бельгии, Нидерландах, Канаде, Италии, Ливане и Соединенных Штатах Америки никогда не применялась универсальная политика вакцинации БЦЖ, однако все эти страны предлагают вакцинацию для подгрупп высокого риска (медицинские работники и дети родителей из стран с высоким риском) («Никогда не применять универсальную политику вакцинации БЦЖ» ‘, Инжир.1а). В 18 странах в прошлом применялась универсальная политика БЦЖ, включая многие европейские страны, Австралию, Эквадор и Израиль («Универсальная политика БЦЖ в прошлом», рис. 1а). В настоящее время в 134 странах действует политика всеобщей вакцинации БЦЖ, включая большинство стран Центральной Америки, Южной Америки, Африки и Азии («Текущая политика универсальной вакцинации БЦЖ», рис. 1a). Во-первых, мы проанализировали заболеваемость туберкулезом во всех странах, где имеется информация о политике BCG. В двух странах с информацией о политике BCG не было данных о заболеваемости туберкулезом, перечисленных в Мировом атласе BCG, и поэтому они не были включены в наш анализ.
В Бельгии, Нидерландах, Канаде, Италии, Ливане и Соединенных Штатах Америки никогда не применялась универсальная политика вакцинации БЦЖ, однако все эти страны предлагают вакцинацию для подгрупп высокого риска (медицинские работники и дети родителей из стран с высоким риском) («Никогда не применять универсальную политику вакцинации БЦЖ» ‘, Инжир.1а). В 18 странах в прошлом применялась универсальная политика БЦЖ, включая многие европейские страны, Австралию, Эквадор и Израиль («Универсальная политика БЦЖ в прошлом», рис. 1а). В настоящее время в 134 странах действует политика всеобщей вакцинации БЦЖ, включая большинство стран Центральной Америки, Южной Америки, Африки и Азии («Текущая политика универсальной вакцинации БЦЖ», рис. 1a). Во-первых, мы проанализировали заболеваемость туберкулезом во всех странах, где имеется информация о политике BCG. В двух странах с информацией о политике BCG не было данных о заболеваемости туберкулезом, перечисленных в Мировом атласе BCG, и поэтому они не были включены в наш анализ. Наш анализ показал, что в странах с активной политикой универсальной БЦЖ заболеваемость туберкулезом выше, чем в странах, где в прошлом применялась универсальная БЦЖ (рис. 1b). У нас были полные данные по 74 странам для изучения связи политики вакцинации БЦЖ с распространением и смертностью от COVID-19. Скорость распространения COVID-19 была значительно снижена в странах с действующей политикой универсальной вакцинации БЦЖ по сравнению со странами, где никогда не применялась или применялась в прошлом универсальная политика вакцинации БЦЖ (рис. 1c).
Наш анализ показал, что в странах с активной политикой универсальной БЦЖ заболеваемость туберкулезом выше, чем в странах, где в прошлом применялась универсальная БЦЖ (рис. 1b). У нас были полные данные по 74 странам для изучения связи политики вакцинации БЦЖ с распространением и смертностью от COVID-19. Скорость распространения COVID-19 была значительно снижена в странах с действующей политикой универсальной вакцинации БЦЖ по сравнению со странами, где никогда не применялась или применялась в прошлом универсальная политика вакцинации БЦЖ (рис. 1c).
Скорость распространения COVID-19 в странах с четкой национальной политикой вакцинации БЦЖ.( a ) На картах мира показаны страны, в которых никогда не проводилась национальная политика вакцинации БЦЖ (выделено красным), страны, в которых в прошлом проводилась политика всеобщей вакцинации БЦЖ (зеленый цвет), и страны, в которых в настоящее время действует политика всеобщей вакцинации БЦЖ (синий цвет). ). ( b ) Заболеваемость ТБ на 100 000 жителей, показанная как среднее ± SEM для всех трех групп политики вакцинации БЦЖ (никогда (красный), прошлая (зеленый) и текущая (синий) политика вакцинации БЦЖ). Был выполнен однофакторный дисперсионный анализ с посттестом Тьюки. ( c ) Скорость распространения CoV-2 показана для всех трех групп политик вакцинации БЦЖ (никогда (красный), прошлая (зеленый) и текущая (синий) политика вакцинации БЦЖ).Данные представлены в виде медианы ± межквартильный размах. Карты были созданы с использованием следующего веб-сайта: https://mapchart.net/world.html.
). ( b ) Заболеваемость ТБ на 100 000 жителей, показанная как среднее ± SEM для всех трех групп политики вакцинации БЦЖ (никогда (красный), прошлая (зеленый) и текущая (синий) политика вакцинации БЦЖ). Был выполнен однофакторный дисперсионный анализ с посттестом Тьюки. ( c ) Скорость распространения CoV-2 показана для всех трех групп политик вакцинации БЦЖ (никогда (красный), прошлая (зеленый) и текущая (синий) политика вакцинации БЦЖ).Данные представлены в виде медианы ± межквартильный размах. Карты были созданы с использованием следующего веб-сайта: https://mapchart.net/world.html.
Введенный вакцинный штамм БЦЖ не приводил к более высокой смертности на 100 000 жителей (дополнительный рисунок S1a). В Испании и Швеции была высокая смертность на 100 000 жителей, и в обеих странах в прошлом применялась универсальная политика БЦЖ. Основываясь на этом наблюдении, мы проанализировали, коррелирует ли год прекращения вакцинации БЦЖ со смертностью.Мы обнаружили, что смертность на 100 000 жителей не коррелировала со временем прекращения универсальной политики БЦЖ (дополнительный рисунок S1b). Затем мы проанализировали смертность в странах с действующей универсальной политикой БЦЖ. Не наблюдалось корреляции между смертностью на 100 000 жителей и временем, прошедшим с момента введения всеобщей политики БЦЖ (дополнительный рисунок S1c). Данные о охвате БЦЖ были доступны для 51 страны, что дает оценку доступа и соблюдения политики БЦЖ в каждой стране (дополнительная таблица S2).За исключением Украины, где охват составляет 15–45%, в большинстве стран охват превышает 90%.
Затем мы проанализировали смертность в странах с действующей универсальной политикой БЦЖ. Не наблюдалось корреляции между смертностью на 100 000 жителей и временем, прошедшим с момента введения всеобщей политики БЦЖ (дополнительный рисунок S1c). Данные о охвате БЦЖ были доступны для 51 страны, что дает оценку доступа и соблюдения политики БЦЖ в каждой стране (дополнительная таблица S2).За исключением Украины, где охват составляет 15–45%, в большинстве стран охват превышает 90%.
Несмотря на то, что мы наблюдали снижение скорости распространения COVID-19 в странах с политикой всеобщей вакцинации БЦЖ, этот анализ фундаментально ограничен степенью, в которой страны способны проводить тестирование на CoV-2 для количественной оценки распространения COVID-19. Сравнение скорости распространения COVID-19 и частоты тестирования дало сильную положительную корреляцию 0,68 ( p значение = 4,2 × 10 –11 ) (рис.2а). Показатели тестирования на CoV-2 значительно различались между странами с различной политикой вакцинации БЦЖ (рис. 2b). При включении только стран с «высоким уровнем тестирования на CoV-2» с 10 или более тестами на тысячу, что приводит к эквивалентному распределению показателей тестирования на CoV-2 по странам с разными политиками БЦЖ, скорость распространения COVID-19 больше не связана с политикой БЦЖ (рис. . 2с). В соответствии с этим многофакторный анализ показал, что частота тестирования, но не политика вакцинации БЦЖ, была связана со скоростью распространения COVID-19 (рис.2г). Чтобы оценить, могут ли дополнительные факторы мешать анализу, мы проанализировали связь плотности населения (население/км 2 ), долю населения старше 65 лет, долю населения, проживающего в городских районах (городское население), на душу населения. ВВП, уровень курения, распространенность диабета и смертность, связанная с сердечно-сосудистыми заболеваниями (ССЗ), как с политикой вакцинации БЦЖ (рис. 2e), так и со скоростью распространения COVID-19 (рис. 2f). Выполнение многофакторного анализа переменных, в значительной степени связанных как с политикой вакцинации БЦЖ, так и со скоростью распространения COVID-19, показало, что частота тестирования и уровень смертности от сердечно-сосудистых заболеваний были независимо связаны с увеличением скорости распространения COVID-19 (рис.
2b). При включении только стран с «высоким уровнем тестирования на CoV-2» с 10 или более тестами на тысячу, что приводит к эквивалентному распределению показателей тестирования на CoV-2 по странам с разными политиками БЦЖ, скорость распространения COVID-19 больше не связана с политикой БЦЖ (рис. . 2с). В соответствии с этим многофакторный анализ показал, что частота тестирования, но не политика вакцинации БЦЖ, была связана со скоростью распространения COVID-19 (рис.2г). Чтобы оценить, могут ли дополнительные факторы мешать анализу, мы проанализировали связь плотности населения (население/км 2 ), долю населения старше 65 лет, долю населения, проживающего в городских районах (городское население), на душу населения. ВВП, уровень курения, распространенность диабета и смертность, связанная с сердечно-сосудистыми заболеваниями (ССЗ), как с политикой вакцинации БЦЖ (рис. 2e), так и со скоростью распространения COVID-19 (рис. 2f). Выполнение многофакторного анализа переменных, в значительной степени связанных как с политикой вакцинации БЦЖ, так и со скоростью распространения COVID-19, показало, что частота тестирования и уровень смертности от сердечно-сосудистых заболеваний были независимо связаны с увеличением скорости распространения COVID-19 (рис. 2г). Процент смертности от COVID-19 был значительно ниже между странами, в которых в настоящее время проводится универсальная политика БЦЖ, по сравнению со странами, в которых никогда не проводилась универсальная политика БЦЖ (значение p = 0,01) (рис. 3a). Однако однофакторный анализ показал, что возраст искажает результаты анализа (рис. 3b). С поправкой на возраст процент смертности от CoV-2 не отличается в странах с разной политикой вакцинации против вируса гепатита В, хотя возраст остается статистически связанным с процентом смертности ( P = 0,001) (рис.3с). Повторение этих анализов с использованием политики вакцинации БЦЖ в качестве бинарной переменной, то есть текущей универсальной политики по сравнению с отсутствием текущей универсальной политики, дало эквивалентные результаты, за исключением того, что больше не было значимой связи между политикой вакцинации БЦЖ и смертностью от COVID-19 (дополнительное приложение). Рисунок S2).
2г). Процент смертности от COVID-19 был значительно ниже между странами, в которых в настоящее время проводится универсальная политика БЦЖ, по сравнению со странами, в которых никогда не проводилась универсальная политика БЦЖ (значение p = 0,01) (рис. 3a). Однако однофакторный анализ показал, что возраст искажает результаты анализа (рис. 3b). С поправкой на возраст процент смертности от CoV-2 не отличается в странах с разной политикой вакцинации против вируса гепатита В, хотя возраст остается статистически связанным с процентом смертности ( P = 0,001) (рис.3с). Повторение этих анализов с использованием политики вакцинации БЦЖ в качестве бинарной переменной, то есть текущей универсальной политики по сравнению с отсутствием текущей универсальной политики, дало эквивалентные результаты, за исключением того, что больше не было значимой связи между политикой вакцинации БЦЖ и смертностью от COVID-19 (дополнительное приложение). Рисунок S2).
Показатели тестирования на SARS-CoV-2 влияют на наблюдаемую пользу политики вакцинации БЦЖ. ( a ) График корреляции общей скорости распространения COVID-19 и тестов на тысячу жителей.Врезка представляет собой коэффициент корреляции Спирмена (ρ). ( b ) Тесты/1000 показаны для всех трех групп политик вакцинации БЦЖ (никогда (красный), прошлая (зеленый) и текущая (синий) политика вакцинации БЦЖ) при сравнении высокой и низкой частоты тестирования. Данные показаны как медиана с межквартильным диапазоном. Крускала-Уоллиса с апостериорным тестом Данна. ( c ) Скорость распространения CoV-2 показана для всех трех групп политик вакцинации БЦЖ (никогда (красный), прошлая (зеленый) и текущая (синий) политика вакцинации БЦЖ) при сравнении высокой и низкой частоты тестирования.Данные показаны как медиана с межквартильным диапазоном. Крускала-Уоллиса с апостериорным тестом Данна. ( d ) Многофакторный регрессионный анализ скорости распространения CoV-2 показывает коэффициенты и p-значений для тестов на 1000 жителей. ( e ) Одномерный анализ ассоциаций с политикой вакцинации БЦЖ показывает коэффициенты и скорректированные значения p для смертности от сердечно-сосудистых заболеваний (ССЗ), плотности населения с диабетом (плотность населения), уровня курения, городского населения (городское население.
( a ) График корреляции общей скорости распространения COVID-19 и тестов на тысячу жителей.Врезка представляет собой коэффициент корреляции Спирмена (ρ). ( b ) Тесты/1000 показаны для всех трех групп политик вакцинации БЦЖ (никогда (красный), прошлая (зеленый) и текущая (синий) политика вакцинации БЦЖ) при сравнении высокой и низкой частоты тестирования. Данные показаны как медиана с межквартильным диапазоном. Крускала-Уоллиса с апостериорным тестом Данна. ( c ) Скорость распространения CoV-2 показана для всех трех групп политик вакцинации БЦЖ (никогда (красный), прошлая (зеленый) и текущая (синий) политика вакцинации БЦЖ) при сравнении высокой и низкой частоты тестирования.Данные показаны как медиана с межквартильным диапазоном. Крускала-Уоллиса с апостериорным тестом Данна. ( d ) Многофакторный регрессионный анализ скорости распространения CoV-2 показывает коэффициенты и p-значений для тестов на 1000 жителей. ( e ) Одномерный анализ ассоциаций с политикой вакцинации БЦЖ показывает коэффициенты и скорректированные значения p для смертности от сердечно-сосудистых заболеваний (ССЗ), плотности населения с диабетом (плотность населения), уровня курения, городского населения (городское население. ), больничных коек на 1000 жителей, валового внутреннего продукта (ВВП), возраста и анализов на 1000 жителей. ( f ) Одномерный анализ ассоциаций со скоростью распространения CoV-2 показывает коэффициенты и скорректированные значения p для смертности от сердечно-сосудистых заболеваний (ССЗ), плотности населения с диабетом (плотность населения), уровня курения, городского населения (городское население). .), больничных коек на 1000 жителей, валового внутреннего продукта (ВВП), возраста и анализов на 1000 жителей. ( г ) Многофакторный регрессионный анализ скорости распространения CoV-2 для переменных, значимых в 2e и 2f.
), больничных коек на 1000 жителей, валового внутреннего продукта (ВВП), возраста и анализов на 1000 жителей. ( f ) Одномерный анализ ассоциаций со скоростью распространения CoV-2 показывает коэффициенты и скорректированные значения p для смертности от сердечно-сосудистых заболеваний (ССЗ), плотности населения с диабетом (плотность населения), уровня курения, городского населения (городское население). .), больничных коек на 1000 жителей, валового внутреннего продукта (ВВП), возраста и анализов на 1000 жителей. ( г ) Многофакторный регрессионный анализ скорости распространения CoV-2 для переменных, значимых в 2e и 2f.
Распределение смертности от COVID-19 и политика вакцинации БЦЖ. ( a ) Смертность от CoV-2 показана для всех трех групп политик вакцинации БЦЖ (никогда (красный), прошлая (зеленый) и текущая (синий) политика вакцинации БЦЖ). Данные представлены в виде медианы ± межквартильный размах. ( b ) Одномерный анализ смертности от CoV-2 показывает коэффициенты и скорректированные значения p для политики вакцинации БЦЖ (BCG Vac.), смертности от диабета, сердечно-сосудистых заболеваний (ССЗ), тестов на 1000 жителей, плотности населения (население .плотность населения), больничные койки на 1000 жителей, уровень курения, валовой внутренний продукт (ВВП), городское население (городское население) и возраст. ( c ) Многофакторный регрессионный анализ доли населения старше 65 лет и политики вакцинации БЦЖ с процентной смертностью от COVID19.
( b ) Одномерный анализ смертности от CoV-2 показывает коэффициенты и скорректированные значения p для политики вакцинации БЦЖ (BCG Vac.), смертности от диабета, сердечно-сосудистых заболеваний (ССЗ), тестов на 1000 жителей, плотности населения (население .плотность населения), больничные койки на 1000 жителей, уровень курения, валовой внутренний продукт (ВВП), городское население (городское население) и возраст. ( c ) Многофакторный регрессионный анализ доли населения старше 65 лет и политики вакцинации БЦЖ с процентной смертностью от COVID19.
Чтобы еще больше подтвердить наши наблюдения, мы затем повторили наш анализ только в европейских странах, стремясь повысить однородность популяционной генетики и демографических характеристик, чтобы улучшить качество наших сравнений.При первоначальном анализе мы по-прежнему наблюдали отчетливые демографические различия между странами с текущей политикой вакцинации БЦЖ и без нее (дополнительный рисунок S3a). Чтобы решить эту проблему, мы выполнили кластеризацию K-средних на основе демографических дескрипторов (за исключением политики вакцинации БЦЖ), разделив Европу на два кластера (дополнительный рисунок S3b). Все страны в Кластере 2 имели политику вакцинации БЦЖ, но в Кластере 1 было 3 страны без политики вакцинации БЦЖ (Бельгия, Италия и Нидерланды).Анализ только Кластера 1 не выявил демографических особенностей (плотность населения, доля населения старше 65 лет, доля населения, проживающего в городских районах, больничные койки на душу населения, ВВП на душу населения, уровень курения, распространенность диабета или смертность, связанная с сердечно-сосудистыми заболеваниями). быть связанным с политикой вакцинации БЦЖ (дополнительный рисунок S3c). В странах кластера 1 политика вакцинации БЦЖ не была связана с изменением скорости распространения COVID-19 (нескорректированное значение P = 0.86) (Дополнительный рисунок S3d). Хотя никакие демографические признаки не достигли P < 0,05 после поправки на множественные сравнения, тесты на 1000 жителей и курение имели нескорректированные значения P < 0,05. Выполнение многофакторного регрессионного анализа с использованием этих двух параметров показало, что оба они, вероятно, независимо связаны с увеличением наблюдаемой скорости распространения COVID-19 (дополнительный рисунок S3e).
Все страны в Кластере 2 имели политику вакцинации БЦЖ, но в Кластере 1 было 3 страны без политики вакцинации БЦЖ (Бельгия, Италия и Нидерланды).Анализ только Кластера 1 не выявил демографических особенностей (плотность населения, доля населения старше 65 лет, доля населения, проживающего в городских районах, больничные койки на душу населения, ВВП на душу населения, уровень курения, распространенность диабета или смертность, связанная с сердечно-сосудистыми заболеваниями). быть связанным с политикой вакцинации БЦЖ (дополнительный рисунок S3c). В странах кластера 1 политика вакцинации БЦЖ не была связана с изменением скорости распространения COVID-19 (нескорректированное значение P = 0.86) (Дополнительный рисунок S3d). Хотя никакие демографические признаки не достигли P < 0,05 после поправки на множественные сравнения, тесты на 1000 жителей и курение имели нескорректированные значения P < 0,05. Выполнение многофакторного регрессионного анализа с использованием этих двух параметров показало, что оба они, вероятно, независимо связаны с увеличением наблюдаемой скорости распространения COVID-19 (дополнительный рисунок S3e). Анализ одномерной связи процентной смертности от COVID-19 в странах из Кластера 1 показал, что и ВВП, и Тесты/1000 значительно ( P прил. < 0,05), связанные с более низким процентом смертности, тогда как возраст был значим только до поправки на множественные сравнения (дополнительный рисунок S3f). Многофакторный регрессионный анализ с использованием трех параметров показал, что распространенность курения и количество тестов на 1000 жителей, вероятно, независимо связаны с увеличением и снижением смертности от COVID-19 соответственно (дополнительный рисунок S3g).
Анализ одномерной связи процентной смертности от COVID-19 в странах из Кластера 1 показал, что и ВВП, и Тесты/1000 значительно ( P прил. < 0,05), связанные с более низким процентом смертности, тогда как возраст был значим только до поправки на множественные сравнения (дополнительный рисунок S3f). Многофакторный регрессионный анализ с использованием трех параметров показал, что распространенность курения и количество тестов на 1000 жителей, вероятно, независимо связаны с увеличением и снижением смертности от COVID-19 соответственно (дополнительный рисунок S3g).
Систематический обзор политики вакцинации БЦЖ среди групп высокого риска в странах с низким бременем туберкулеза: последствия для стратегии вакцинации коренных общин Канады | BMC Public Health
Диаграмма результатов скрининга PRISMA [24] показана на рис.1 .
Характеристики исследований
Из 49 включенных исследований 32 были первичными (оригинальными исследованиями), 12 представляли собой отчеты о политике и 5 представляли собой обзоры. Первичные исследования имели различные дизайны, включая РКИ ( n = 4), исследования случай-контроль или когортные исследования ( n = 3), квазиэкспериментальные исследования ( n = 5), перекрестные секционные исследования ( n = 8), ретроспективные или проспективные когортные или наблюдательные исследования ( n = 7), моделирующие исследования ( n = 4) и один клинический случай.
Первичные исследования имели различные дизайны, включая РКИ ( n = 4), исследования случай-контроль или когортные исследования ( n = 3), квазиэкспериментальные исследования ( n = 5), перекрестные секционные исследования ( n = 8), ретроспективные или проспективные когортные или наблюдательные исследования ( n = 7), моделирующие исследования ( n = 4) и один клинический случай.
Среди 12 докладов о политике и 32 первичных исследований с точки зрения стран проведения (все из которых должны были иметь уровень заболеваемости ТБ < 100 случаев на миллион населения в качестве критерия для включения), большинство было проведено в европейских странах ( ФРАНЦИЯ N = 6, Великобритания N = 6, Дания N = 4, Швеция N = 3, Нидерланды N = 2, Финляндия N = 2, Норвегия N = 2, чеш Республика n = 2 и Ирландия n = 1).Дальнейшие исследования проводились в Канаде ( n = 3), США ( n = 3), Австралии ( n = 3), Саудовской Аравии ( n = 1), Объединенных Арабских Эмиратах ( n = 1) и Египет ( n = 1). Остальные 4 исследования охватили несколько стран (одно из которых включало США, Канаду и Гренландию , сноска 1 ), в то время как другие предоставили информацию о вакцинации БЦЖ в странах с низким уровнем заболеваемости в целом. 5 обзоров касались либо Великобритании ( n = 1), Франции ( n = 1), либо общих условий с низкой заболеваемостью ( n = 3).
Остальные 4 исследования охватили несколько стран (одно из которых включало США, Канаду и Гренландию , сноска 1 ), в то время как другие предоставили информацию о вакцинации БЦЖ в странах с низким уровнем заболеваемости в целом. 5 обзоров касались либо Великобритании ( n = 1), Франции ( n = 1), либо общих условий с низкой заболеваемостью ( n = 3).
Из 32 первичных исследований в 16 сообщалось об эффективности вакцины или заболеваемости ТБ при различных стратегиях вакцинации БЦЖ, в 15 сообщалось о побочных эффектах, связанных с использованием БЦЖ, или предоставлялись другие рекомендации в отношении политики вакцинации (14 исследований и один клинический случай) и 1 в исследовании сообщалось об обоих [10].
Обзор политики вакцинации в зависимости от заболеваемости ТБ в включенных в исследование странах
Краткое изложение рекомендаций по политике в включенных в исследование странах в разбивке по национальной заболеваемости ТБ представлено в таблице 2 . Поскольку включенные исследования сообщают о различных стратегиях и показателях заболеваемости в зависимости от даты публикации, текущие политики в этой сводной таблице взяты из Мирового атласа BCG [4], который последний раз обновлялся в 2017 г., если не указано иное. Национальные показатели заболеваемости на 100 000 населения для каждой страны были рассчитаны на основе оценок заболеваемости ВОЗ за 2016 г., тогда как показатели заболеваемости в конкретных целевых группах риска (при наличии), а также политические рекомендации, основанные на наблюдениях, взяты из отдельных исследований, включенных в текущий обзор.
Поскольку включенные исследования сообщают о различных стратегиях и показателях заболеваемости в зависимости от даты публикации, текущие политики в этой сводной таблице взяты из Мирового атласа BCG [4], который последний раз обновлялся в 2017 г., если не указано иное. Национальные показатели заболеваемости на 100 000 населения для каждой страны были рассчитаны на основе оценок заболеваемости ВОЗ за 2016 г., тогда как показатели заболеваемости в конкретных целевых группах риска (при наличии), а также политические рекомендации, основанные на наблюдениях, взяты из отдельных исследований, включенных в текущий обзор.
Как показано в таблице 2, показатели заболеваемости в странах, включенных в исследование, варьировались от 0,7/100 000 населения/год (в ОАЭ) до 9,8/ 100 000 населения в год (в Великобритании) (в соответствии с критериями исключения из обзора включены только страны с заболеваемостью < 10/100 000 (т. е. < 100/1 000 000)). Хотя почти все из 15 стран ранее в какой-то момент применяли массовую или плановую вакцинацию, сегодня массовая вакцинация продолжается только в 4 из этих стран (Египет, Саудовская Аравия, ОАЭ и, в некоторых регионах, Ирландия).С тех пор все 11 оставшихся стран перешли на целевую вакцинацию отдельных групп риска вместо всеобщей вакцинации. Интересно отметить, что хотя три из четырех стран, продолжающих массовую вакцинацию, имеют относительно высокие показатели заболеваемости по сравнению с другими странами с низким бременем (Саудовская Аравия: 9,3/100 000, Египет: 8,6/100 000, Ирландия: 6,8/100 000 населения в год). четвертая, ОАЭ, продолжает массовую вакцинацию, несмотря на самый низкий уровень заболеваемости туберкулезом среди всех 15 стран (0,7/100 000 населения в год).
е. < 100/1 000 000)). Хотя почти все из 15 стран ранее в какой-то момент применяли массовую или плановую вакцинацию, сегодня массовая вакцинация продолжается только в 4 из этих стран (Египет, Саудовская Аравия, ОАЭ и, в некоторых регионах, Ирландия).С тех пор все 11 оставшихся стран перешли на целевую вакцинацию отдельных групп риска вместо всеобщей вакцинации. Интересно отметить, что хотя три из четырех стран, продолжающих массовую вакцинацию, имеют относительно высокие показатели заболеваемости по сравнению с другими странами с низким бременем (Саудовская Аравия: 9,3/100 000, Египет: 8,6/100 000, Ирландия: 6,8/100 000 населения в год). четвертая, ОАЭ, продолжает массовую вакцинацию, несмотря на самый низкий уровень заболеваемости туберкулезом среди всех 15 стран (0,7/100 000 населения в год).
В странах, где в настоящее время проводится целевая вакцинация, в группы риска, определенные для таргетной вакцинации, чаще всего входили дети, чьи родители были из эндемичных по ТБ стран, или дети с семейным анамнезом ТБ или контактировавшие с больным ТБ, у которых была нереактивная ТКП. Общими причинами перехода от всеобщей к целевой программе вакцинации были низкий риск заражения среди населения в целом и, следовательно, большое количество прививок, необходимых для предотвращения одного случая в контексте условий с низкой заболеваемостью (например, 21 699–25 125 прививок, необходимых среди норвежского подросткового населения для предотвращения одного случая) [11, 34], и концентрации большинства случаев среди определенной группы риска [36].В странах, где массовая вакцинация все еще считалась оправданной, причины для продолжения массовой вакцинации включали низкую частоту серьезных побочных эффектов, связанных с вакциной [28], и результаты, касающиеся значительной корреляции охвата вакцинацией БЦЖ со снижением заболеваемости ТБ и заболеваемостью ТБ. сопутствующие показатели смертности (в Египте) [45].
Общими причинами перехода от всеобщей к целевой программе вакцинации были низкий риск заражения среди населения в целом и, следовательно, большое количество прививок, необходимых для предотвращения одного случая в контексте условий с низкой заболеваемостью (например, 21 699–25 125 прививок, необходимых среди норвежского подросткового населения для предотвращения одного случая) [11, 34], и концентрации большинства случаев среди определенной группы риска [36].В странах, где массовая вакцинация все еще считалась оправданной, причины для продолжения массовой вакцинации включали низкую частоту серьезных побочных эффектов, связанных с вакциной [28], и результаты, касающиеся значительной корреляции охвата вакцинацией БЦЖ со снижением заболеваемости ТБ и заболеваемостью ТБ. сопутствующие показатели смертности (в Египте) [45].
Примечательно, что среди исследований в странах, которые перешли от всеобщей к целевой вакцинации, все сочли это изменение политики целесообразным и не рекомендовали повторное введение всеобщей вакцинации, однако также подчеркивались возможные опасности отмены массовой вакцинации.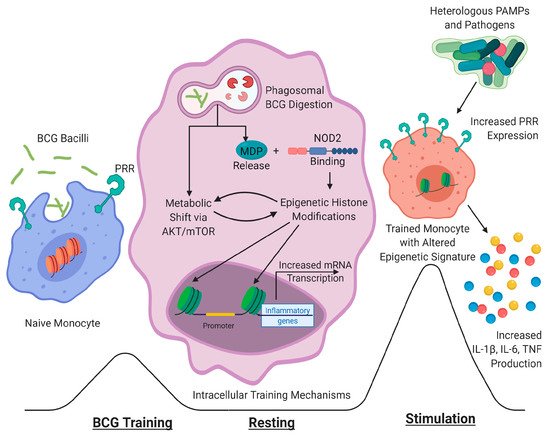 К ним относился не только потенциальный рост заболеваемости туберкулезом (как это произошло, например, в Чехии, где рост заболеваемости туберкулезом наблюдался в регионе, в котором массовая вакцинация была прекращена в 1986 г. [9]), но и озабоченность неполным охватом групп риска после отмены всеобщей вакцинации [35]. Таким образом, было достигнуто общее согласие в том, что для успешной отмены всеобщей вакцинации необходимо эффективное выявление детей из группы высокого риска и строгое соблюдение руководящих принципов в отношении их вакцинации [14, 35], а также сильная программа борьбы с ТБ (включая достаточные стратегии скрининга и диагностики) должны быть на месте до вывода [19, 32].
К ним относился не только потенциальный рост заболеваемости туберкулезом (как это произошло, например, в Чехии, где рост заболеваемости туберкулезом наблюдался в регионе, в котором массовая вакцинация была прекращена в 1986 г. [9]), но и озабоченность неполным охватом групп риска после отмены всеобщей вакцинации [35]. Таким образом, было достигнуто общее согласие в том, что для успешной отмены всеобщей вакцинации необходимо эффективное выявление детей из группы высокого риска и строгое соблюдение руководящих принципов в отношении их вакцинации [14, 35], а также сильная программа борьбы с ТБ (включая достаточные стратегии скрининга и диагностики) должны быть на месте до вывода [19, 32].
Эффективность вакцины БЦЖ и влияние политики вакцинации на заболеваемость туберкулезом
Результаты исследований, касающиеся эффективности вакцины и влияния изменений политики вакцинации на заболеваемость туберкулезом, представлены в таблице 3 (сгруппированы по странам). Хотя двухгрупповые исследования, сравнивающие вакцинированные и невакцинированные группы (или районы с более высоким и более низким охватом вакцинацией), обычно сообщают о более высокой заболеваемости туберкулезом в невакцинированных (или с низким охватом) группах по сравнению с вакцинированными (или с высоким охватом) группы [8, 30, 42, 55, 56]. Несмотря на это, сообщаемая эффективность вакцины, тем не менее, широко варьировалась в разных исследованиях: от 49% (95% ДИ: 14–62%) в исследовании азиатских детей, живущих в Великобритании [53], до 87,5% (95% ДИ: 30–98%) в исследовании населения Франции в целом [50]. Выводы, которые поддерживали целевую вакцинацию среди отдельных групп риска, а не всеобщую вакцинацию, включали большое количество вакцинаций, необходимых для предотвращения одного случая ТБ в районах с низким бременем [34], наряду с потенциально высоким числом побочных эффектов на один предотвращенный случай [52]. и сохраняющийся низкий риск заражения в условиях низкой заболеваемости, делающий массовую вакцинацию ненужной [10, 11, 13].Также было подчеркнуто, что еще одним преимуществом прекращения массовой вакцинации в странах с низким уровнем заболеваемости было восстановление диагностической полезности ТКП для выявления ЛТБИ [10]; это важное соображение, учитывая, что выявление и профилактика ЛТБИ по-прежнему является компонентом борьбы с туберкулезом в контексте коренных народов Канады [57], а также потому, что тесты на высвобождение гамма-интерферона не являются широко доступными [58].
Несмотря на это, сообщаемая эффективность вакцины, тем не менее, широко варьировалась в разных исследованиях: от 49% (95% ДИ: 14–62%) в исследовании азиатских детей, живущих в Великобритании [53], до 87,5% (95% ДИ: 30–98%) в исследовании населения Франции в целом [50]. Выводы, которые поддерживали целевую вакцинацию среди отдельных групп риска, а не всеобщую вакцинацию, включали большое количество вакцинаций, необходимых для предотвращения одного случая ТБ в районах с низким бременем [34], наряду с потенциально высоким числом побочных эффектов на один предотвращенный случай [52]. и сохраняющийся низкий риск заражения в условиях низкой заболеваемости, делающий массовую вакцинацию ненужной [10, 11, 13].Также было подчеркнуто, что еще одним преимуществом прекращения массовой вакцинации в странах с низким уровнем заболеваемости было восстановление диагностической полезности ТКП для выявления ЛТБИ [10]; это важное соображение, учитывая, что выявление и профилактика ЛТБИ по-прежнему является компонентом борьбы с туберкулезом в контексте коренных народов Канады [57], а также потому, что тесты на высвобождение гамма-интерферона не являются широко доступными [58].
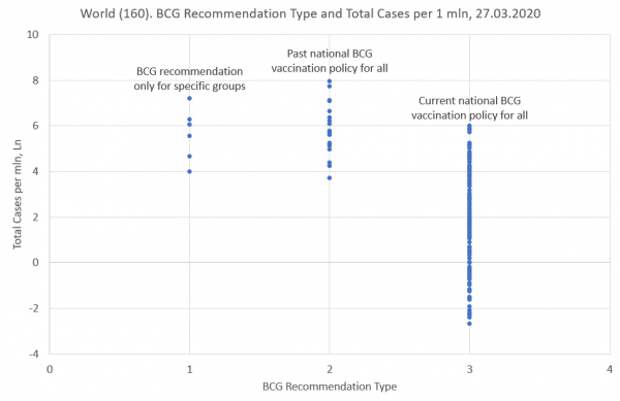 Не было обнаружено значимой связи между применением БЦЖ и психомоторным развитием ребенка [39] или заболеваемостью ВЗК [40], нетуберкулезными инфекциями [59] или астмой [61], в то время как частота атипичных микобактериальных заболеваний была ниже [62]. и более низкое использование лекарств от экземы [61] в группах, получавших БЦЖ, по сравнению с теми, кто этого не делал.
Не было обнаружено значимой связи между применением БЦЖ и психомоторным развитием ребенка [39] или заболеваемостью ВЗК [40], нетуберкулезными инфекциями [59] или астмой [61], в то время как частота атипичных микобактериальных заболеваний была ниже [62]. и более низкое использование лекарств от экземы [61] в группах, получавших БЦЖ, по сравнению с теми, кто этого не делал.Общие рекомендации в обзорах и отчетах о политике
Сводка рекомендаций из 12 включенных отчетов о политике представлена в таблице 5 . В целом массовая вакцинация не рекомендовалась в странах с низким уровнем заболеваемости, где вместо этого стратегия борьбы с ТБ должна быть сосредоточена на выявлении и быстром лечении активных случаев, а также на контроле ЛТБИ [29]. Кроме того, во многих отчетах подчеркивалось, что для готовности к отказу от лечения необходима сильная система эпиднадзора за ТБ, позволяющая своевременно оценивать последствия политики [6, 19, 32], и должен быть обеспечен всесторонний охват выбранных групп высокого риска [65]. .Повторная вакцинация не рекомендовалась ни в одном отчете из-за отсутствия доказательств ее эффективности [6, 32, 36, 65].
.Повторная вакцинация не рекомендовалась ни в одном отчете из-за отсутствия доказательств ее эффективности [6, 32, 36, 65].
Из 5 включенных обзоров 3, которые дали рекомендации для общих условий с низкой заболеваемостью, пришли к выводу, что политика всеобщей вакцинации имеет ограниченную ценность в странах с низкой вместо этого рекомендуются группы риска [5, 67, 68]. Два оставшихся обзора были посвящены конкретно Соединенному Королевству и Франции, и оба они были опубликованы до прекращения массовой вакцинации в обеих странах, при этом во французском обзоре утверждалось, что массовая вакцинация в то время (2003 г.) по-прежнему была оправдана, исходя из количества новых случаев туберкулезного менингита, хотя точное пороговое значение числа случаев, при которых вакцинация больше не будет считаться полезной, не было установлено [69], в то время как британское исследование показало, что (по состоянию на 1988 г. ) рутинная вакцинация 10–14 лет в рамках британских школьных программ по-прежнему оправдано, но эта политика подлежит пересмотру в последующие годы [70].Как упоминалось ранее, политика массовой вакцинации в обеих странах с тех пор была пересмотрена в пользу принятия целенаправленной вакцинации [12, 13].
) рутинная вакцинация 10–14 лет в рамках британских школьных программ по-прежнему оправдано, но эта политика подлежит пересмотру в последующие годы [70].Как упоминалось ранее, политика массовой вакцинации в обеих странах с тех пор была пересмотрена в пользу принятия целенаправленной вакцинации [12, 13].
Оценка риска систематической ошибки
Риск систематической ошибки во включенных РКИ ( n = 4) оценивался с использованием Инструмента оценки качества для контролируемых интервенционных исследований Национального института сердца, легких и крови (NHLBI) [25]. Включенные РКИ, как правило, имели низкий риск систематической ошибки, поскольку риск перекрестного заражения (т.е. вакцинация в невакцинированной группе) была низкой, размер выборки был оправданным, а распределение по группам в большинстве исследований было надлежащим образом рандомизированным. Однако потенциальные источники систематической ошибки во включенных РКИ включают тот факт, что из-за характера вмешательства (т. е. проведения вакцинации) исследовательский персонал не мог быть ослеплен при распределении по группам, а распределение по группам не могло быть скрыто от участников. Результаты оценки риска систематической ошибки для включенных РКИ показаны на рис. 2.
е. проведения вакцинации) исследовательский персонал не мог быть ослеплен при распределении по группам, а распределение по группам не могло быть скрыто от участников. Результаты оценки риска систематической ошибки для включенных РКИ показаны на рис. 2.
Оценка риска систематической ошибки для включенных рандомизированных контролируемых испытаний. * Размер выборки достаточен для выявления различий между группами в основном исходе с мощностью не менее 80%.
Обсервационные и кросс-секционные исследования ( n = 15) (оценка с помощью инструмента оценки качества NHLBI для обсервационных когортных и кросс-секционных исследований [25]) также в целом имели высокое методологическое качество, отвечающее большинству критериев оценки качества . Тем не менее, отсутствие ослепления оценщиков результатов (или отсутствие сообщения об этом) было потенциальным источником систематической ошибки в большинстве исследований, и в большинстве исследований были неадекватные или нечеткие отчеты о поправке на вмешивающиеся факторы, как показано на рис. 3 ниже. Во включенных исследованиях «случай-контроль» и «случай-когорт» ( n = 3) (оцененных с использованием инструмента оценки качества NHLBI для исследований случай-контроль [25]) также недостаточно сообщалось об ослеплении экспертов по оценке результатов статусом участников (как случаев или контроля), хотя во всех исследованиях должным образом учитывались и другие источники систематической ошибки, такие как предоставление четких определений случаев и их четкое отличие от контроля. Риск систематической ошибки в исследованиях случай-контроль показан на рис.4 .
3 ниже. Во включенных исследованиях «случай-контроль» и «случай-когорт» ( n = 3) (оцененных с использованием инструмента оценки качества NHLBI для исследований случай-контроль [25]) также недостаточно сообщалось об ослеплении экспертов по оценке результатов статусом участников (как случаев или контроля), хотя во всех исследованиях должным образом учитывались и другие источники систематической ошибки, такие как предоставление четких определений случаев и их четкое отличие от контроля. Риск систематической ошибки в исследованиях случай-контроль показан на рис.4 .
Оценка риска систематической ошибки для включенных обсервационных исследований
Рис. 4Оценка риска систематической ошибки для включенных исследований случай-контроль
В случае квазиэкспериментальных исследований ( n = 5), которые оценивались с использованием Контрольного списка критической оценки JBI для квазиэкспериментальных исследований [26 ], существенными источниками систематической ошибки был тот факт, что большинство исследований не предоставили достаточной информации об исходных характеристиках участников и о том, были ли какие-либо существенные различия в этих характеристиках у подвергшихся воздействию и у тех, кто подвергался воздействию. неэкспонированные группы, а также недостаточное или отсутствующее сравнение характеристик участников, выбывших из-под наблюдения, по сравнению с теми, кто завершил исследование. На рис. 5 показана оценка риска систематической ошибки для включенных квазиэкспериментальных исследований, а также баллы отдельных исследований для каждого критерия оценки качества на рис. 2, 3, 4, 5 представлены в дополнительном файле 2.
неэкспонированные группы, а также недостаточное или отсутствующее сравнение характеристик участников, выбывших из-под наблюдения, по сравнению с теми, кто завершил исследование. На рис. 5 показана оценка риска систематической ошибки для включенных квазиэкспериментальных исследований, а также баллы отдельных исследований для каждого критерия оценки качества на рис. 2, 3, 4, 5 представлены в дополнительном файле 2.
Оценка риска систематической ошибки для включенных квазиэкспериментальных исследований
Отчет о клиническом случае [63] был оценен с использованием контрольного списка JBI Critical Appraisal Checklist for Case Reports [26], и было обнаружено, что он имеет низкий риск систематической ошибки , так как он четко описывал демографические характеристики пациента и историю болезни, а также текущее состояние пациента, проведенные диагностические тесты и результаты лечения.
Наконец, 4 включенных модельных исследования были оценены с использованием Принципов надлежащей практики ISPOR для аналитического моделирования решений в оценке здравоохранения [27].




 1186/s13063-020-04822-0.
Испытания. 2020.
PMID: 33106170
Бесплатная статья ЧВК.
Клиническое испытание.
1186/s13063-020-04822-0.
Испытания. 2020.
PMID: 33106170
Бесплатная статья ЧВК.
Клиническое испытание. —
ЧВК
—
пабмед
—
ЧВК
—
пабмед , Fisker A.B., Benn C.S., Early BCG-Дания и неонатальная смертность среди младенцев с массой тела <2500 г: рандомизированное контролируемое исследование. клин. Заразить. Дис. 65, 1183–1190 (2017).
-
ЧВК
-
пабмед
, Fisker A.B., Benn C.S., Early BCG-Дания и неонатальная смертность среди младенцев с массой тела <2500 г: рандомизированное контролируемое исследование. клин. Заразить. Дис. 65, 1183–1190 (2017).
-
ЧВК
-
пабмед , Гелденхейс Х., Розот В., Рутковски К.Т., Ратанджи Ф., Билек Н., Мабве С., Махете Л., Эразмус М., Тофи А., Муленга Х., Ханеком В.А., Селф С.Г., Беккер Л.- Г., Райалл Р., Гурунатан С., ДиазГранадос К.А., Андерсен П., Кроманн И., Эванс Т., Эллис Р.Д., Лэндри Б., Хоки Д.А., Хопкинс Р., Гинзберг А.М., Скриба Т.Дж., Хазерилл М.; C-040-404 Исследовательская группа, Профилактика инфекции M.tuberculosis с помощью вакцины h5:IC31 или ревакцинации БЦЖ. Н. англ. Дж. Мед. 379, 138–149 (2018).
—
ЧВК
—
пабмед
, Гелденхейс Х., Розот В., Рутковски К.Т., Ратанджи Ф., Билек Н., Мабве С., Махете Л., Эразмус М., Тофи А., Муленга Х., Ханеком В.А., Селф С.Г., Беккер Л.- Г., Райалл Р., Гурунатан С., ДиазГранадос К.А., Андерсен П., Кроманн И., Эванс Т., Эллис Р.Д., Лэндри Б., Хоки Д.А., Хопкинс Р., Гинзберг А.М., Скриба Т.Дж., Хазерилл М.; C-040-404 Исследовательская группа, Профилактика инфекции M.tuberculosis с помощью вакцины h5:IC31 или ревакцинации БЦЖ. Н. англ. Дж. Мед. 379, 138–149 (2018).
—
ЧВК
—
пабмед С. Правительство
С. Правительство