Что такое БЦЖ?
Что такое туберкулез?
Туберкулез – это хроническая бактериальная инфекция, которая занимает одно из первых мест в мире по показателям заболеваемости и смертности. Заражение происходит воздушно-капельным путем от больных, которые выделяют палочку туберкулеза с мокротой при чихании, кашле, разговоре. Возбудитель туберкулеза способен поразить многие органы и системы организма: легкие, мозг, почки, кости, глаза, кожу, лимфатическую систему. Наиболее тяжелые формы туберкулеза возникают у новорожденных детей.
Что такое вакцина БЦЖ?
Вакцина БЦЖ — это живые возбудители туберкулеза, которые после специальной обработки, утратили способность вызывать заболевание, но не утратили способность создавать противотуберкулёзный иммунитет. Кроме того, существует вакцина БЦЖ-М которая используется для щадящей вакцинации ослабленных детей. Прививку БЦЖ (БЦЖ-М) осуществляют в родильном отделении здоровым доношенным детям на 3-7 сутки жизни и недоношенным детям по достижении массы тела 2,5кг.
Если по каким-то причинам ребенок не был привит в родильном доме, то его вакцинируют после снятия противопоказаний в стационаре (в случае перевода малыша в больницу из родильного дома) или в поликлинике. В поликлинике противотуберкулезная прививка детям старше 2-х месяцев возможна только после проведения пробы Манту, которая покажет возможное заражение ребенка к этому возрасту.
В возрасте 7, 14 лет делается повторная прививка против туберкулеза.
Что такое рубчик БЦЖ?
Через какое-то время в месте вакцинации образуется ранка, покрытая корочкой. Позже корочка отпадает, ранка открывается. Постепенно ранка заживает, образуя рубчик. Как — то обрабатывать, пытаться лечить эту ранку, заклеивать ее пластырем при купании не нужно. Ничего страшного, если вода попадает на нее! Ранку только нельзя травмировать и тереть!!! Если вас все же что-то беспокоит, спросите совета у врача педиатра.
Чем опасен отказ родителей от вакцинации БЦЖ?
Прививка существенно снижает риск инфицирования и заболевания туберкулёзом. Это означает, что привитой ребенок с хорошим поствакцинальным иммунитетом при встрече с микобактериями либо не инфицируется вовсе, либо перенесет инфекцию в легкой форме.
Это означает, что привитой ребенок с хорошим поствакцинальным иммунитетом при встрече с микобактериями либо не инфицируется вовсе, либо перенесет инфекцию в легкой форме.
Дети, не получившие прививку БЦЖ, могут заболеть туберкулезом, в том числе и самыми тяжелыми формами (поражение головного мозга, костей и др.)
Именно поэтому, для контроля состояния противотуберкулезного иммунитета и выявления момента первичного инфицирования детям ежегодно проводят пробу Манту.
Министерство здравоохранения Пермского края
ГБУЗ ПК «ПКД «Фтизиопульмонология»
Пермь, 2013
Почему привитые люди тоже болеют туберкулёзом
Согласитесь, что это достаточно хороший уровень защиты. Что касается тяжелых форм туберкулёза, от которых можно умереть (иногда они протекают столь молниеносно, что не успевают даже поставить верный диагноз), то здесь уровень защиты БЦЖ еще выше: 90-92%.
Что касается тяжелых форм туберкулёза, от которых можно умереть (иногда они протекают столь молниеносно, что не успевают даже поставить верный диагноз), то здесь уровень защиты БЦЖ еще выше: 90-92%.
Также советскими исследователями было отмечено, что после внедрения всеобщей вакцинации БЦЖ в 60-х годах прошлого века, течение туберкулёза легких стало менее тяжелым и осложненным — реже стала встречаться вторичная генерализация процесса по разным органам, туберкулёзные плевриты и распад легочной ткани.
Тем не менее, вакцина БЦЖ не идеальна — во-первых, ее защита длится всего несколько лет и, соответственно, не действует на взрослых. Во-вторых, защитный эффект от заболевания не максимальный. Много десятилетий подряд ведутся работы по созданию новых вакцин, однако ни одна из них еще не зарегистрирована, поскольку не удается создать преимущественно лучший вариант, чем БЦЖ. В настоящее время основные вакцины-кандидаты являются бустерными. То есть, предполагается, что они будут усиливать и продлевать эффект БЦЖ, но не заменят ее полностью».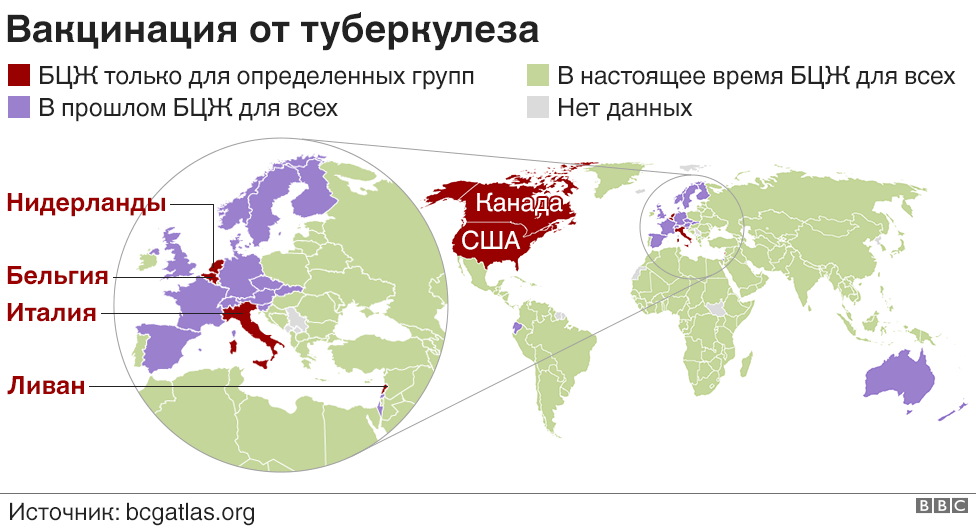
Вакцинация БЦЖ в Казахстане
Для профилактики тяжелых форм туберкулёза все здоровые новорожденные дети, согласно Национальному календарю прививок, получают свою первую вакцину БЦЖ на 2-4 сутки после рождения. Весь список противопоказаний к вакцинации описан в Приказе №214 о профилактике туберкулёза. До вакцинации все матери новорожденных должны пройти флюорографию в роддоме, чтобы исключить туберкулёз. Также пройти флюорографию обязаны все, кто будет проживать в одном доме с новорожденным, если ребенок не получил БЦЖ вакцину по медицинским противопоказаниям или родители подписали отказ от прививки. Только после предоставления необходимых справок маму с ребенком могут выписать из роддома.
Защиты вакцины БЦЖ хватает, в среднем, на 5-6 лет — все зависит от иммунитета каждого ребенка. Именно поэтому казахстанским детям в 6-летнем возрасте ставится вторая прививка БЦЖ. Ревакцинация проводится только после отрицательной пробы Манту и не позднее двух недель после нее. В случае, если проба Манту дала сомнительную реакцию, то она повторяется через 3 месяца. Если реакция Манту положительная, то вероятность инфицирования ребенка проверяется с помощью Диаскинтеста (АТР – прим. V). Если ребенок до 6 лет переболел туберкулёзом, вторая прививка ему уже не ставится. По статистике до ревакцинации доходят менее ⅔ тех, кто получил прививку БЦЖ в роддоме. По данным за 2020 год в роддоме БЦЖ получили 92,8% новорожденных, а охват ревакцинацией среди 6-летних детей в этом же году составил 58,7%.
Если реакция Манту положительная, то вероятность инфицирования ребенка проверяется с помощью Диаскинтеста (АТР – прим. V). Если ребенок до 6 лет переболел туберкулёзом, вторая прививка ему уже не ставится. По статистике до ревакцинации доходят менее ⅔ тех, кто получил прививку БЦЖ в роддоме. По данным за 2020 год в роддоме БЦЖ получили 92,8% новорожденных, а охват ревакцинацией среди 6-летних детей в этом же году составил 58,7%.
По итогам исследований, опубликованных в 2018 году, ревакцинация не приводит к какому-либо видимому эффекту, но специалисты в области вакцинопрофилактики не исключают, что, возможно, не все факторы еще до конца изучены. В большинстве стран СНГ, где туберкулёз не сдает своих позиций, дети по-прежнему получают вторую прививку в 6-7 лет. Российским опытом ревакцинации с нами поделилась Ольга Винокурова, а также тем, насколько, по ее мнению, имеет смысл вторая прививка:
«Ревакцинация БЦЖ действительно имеет достаточно слабый защитный эффект. Количество ревакцинированных детей с каждым годом уменьшается и мы планомерно движемся к отмене ревакцинации как малоэффективной меры, как и рекомендует ВОЗ. В моей практике никаких показательных случаев на эту тему не было, и я отношусь к этому вопросу спокойно — я не против ревакцинации, если родители желают дополнительно защитить ребенка, но предсказать, насколько действенна будет эта защита — трудно, поэтому мы честно говорим о том, что не стоит многого от нее ожидать».
В моей практике никаких показательных случаев на эту тему не было, и я отношусь к этому вопросу спокойно — я не против ревакцинации, если родители желают дополнительно защитить ребенка, но предсказать, насколько действенна будет эта защита — трудно, поэтому мы честно говорим о том, что не стоит многого от нее ожидать».
В Казахстане вакцинация БЦЖ проводится только в роддомах и государственных поликлиниках. Частные медицинские и прививочные центры вакцину БЦЖ не ставят. Техника вакцинации БЦЖ отличается от других прививок и, по правилам, требуется отдельный прививочный кабинет. В 2021 году в Казахстане используется вакцина индийского производителя Serum Institute of India Pvt.Ltd., прошедшая преквалификацию ВОЗ.
В следующем материале мы разберем вопросы, связанные с поствакцинальными осложнениями после БЦЖ и диагностику туберкулёза у детей с помощью проб Манту и АТР.
«БЦЖ или не БЦЖ, вот в чем вопрос!». Проблема вакцинации БЦЖ: почему мы не можем сделать это правильно?
1. Консультативный совет по ликвидации туберкулеза (ACET) и Консультативный комитет по практике иммунизации Роль вакцины БЦЖ в профилактике и борьбе с туберкулезом в Соединенных Штатах. ММВР. 1996; 45:1–18. [PubMed] [Google Scholar]
Консультативный совет по ликвидации туберкулеза (ACET) и Консультативный комитет по практике иммунизации Роль вакцины БЦЖ в профилактике и борьбе с туберкулезом в Соединенных Штатах. ММВР. 1996; 45:1–18. [PubMed] [Google Scholar]
2. Национальный консультативный комитет по иммунизации Вакцина БЦЖ. Сектор народонаселения и общественного здравоохранения. В: Центр профилактики и контроля инфекционных заболеваний, изд. Национальное руководство по иммунизации. 6-е изд. Оттава: Канадская медицинская ассоциация; 2002. стр. 71–6. [Академия Google]
3. Министерство здравоохранения Канады. Туберкулез в Канаде, 2000 г. Оттава: Министерство здравоохранения Канады; (в печати)
4. Туберкулез в общинах коренных народов . Оттава: Министерство здравоохранения Канады; 1999.
5. Старке Дж. Р. Туберкулез центральной нервной системы у детей. Семин Педиатр Нейрол. 1999; 6: 318–31. [PubMed] [Академия Google]
Туберкулез центральной нервной системы у детей. Семин Педиатр Нейрол. 1999; 6: 318–31. [PubMed] [Академия Google]
6. Мелкий ПЭМ. Вакцины Bacille Calmette-Guerin: приблизительное руководство. Клин Инфекция Дис. 1995; 20:11–4. [PubMed] [Google Scholar]
7. Родригес Л.С., Диван В.К., Уилер Дж.Г. Защитный эффект БЦЖ против туберкулезного менингита и милиарного туберкулеза: метаанализ. Int J Эпидемиол. 1993; 22:1154–8. [PubMed] [Google Scholar]
8. Colditz GA, Berkey S, Mosteller F, et al. Эффективность вакцинации новорожденных и детей грудного возраста бациллой Кальметта-Герена в профилактике туберкулеза: метаанализ опубликованной литературы. Педиатрия. 1995;96:29–35. [PubMed] [Google Scholar]
9. Colditz GA, Brewer TF, Berkey CS, et al. Эффективность вакцины БЦЖ в профилактике туберкулеза. ДЖАМА. 1994; 271: 698–702. [PubMed] [Google Scholar]
10. Ponnighaus JM, Fine PE, Sterne JA, et al. Эффективность вакцины БЦЖ против проказы и туберкулеза в северной части Малави. Ланцет. 1992; 339: 636–9. [PubMed] [Google Scholar]
Ланцет. 1992; 339: 636–9. [PubMed] [Google Scholar]
11. Исследовательская группа профилактики каронга Рандомизированное контролируемое исследование одной БЦЖ, повторной БЦЖ или комбинированной БЦЖ и убитых 9Вакцина 0023 Mycobacterium leprae для профилактики лепры и туберкулеза в Малави. Ланцет. 1996; 348:611. [PubMed] [Google Scholar]
12. Fordham von Reyn C, Vuola JM. Новые вакцины для профилактики туберкулеза. Клин Инфекция Дис. 2002; 35: 465–74. [PubMed] [Google Scholar]
13. Аронсон Д.Д. Защитная вакцинация против туберкулеза с особым упором на вакцинацию БЦЖ. Ам преподобный Туберк. 1948; 48: 255–81. [PubMed] [Google Scholar]
14. Ferguson RG, Simes AB. Вакцинация БЦЖ новорожденных индийцев в Саскачеване. бугорок. 1949;30:5–11. [PubMed] [Google Scholar]
15. Rosenthal SR, Loewinsohn E, Graham ML, Liveright D, Thorne MG, Johnson V. Вакцинация БЦЖ в семьях, больных туберкулезом. Ам преподобный Респир Дис. 1960; 84: 690–704. [PubMed] [Google Scholar]
16. Rosenthal SR, Loewinsohn E, Graham ML, et al. Вакцинация БЦЖ против туберкулеза в Чикаго: статистический анализ двадцатилетнего исследования. Педиатрия. 1961; 28: 622–41. [PubMed] [Google Scholar]
Rosenthal SR, Loewinsohn E, Graham ML, et al. Вакцинация БЦЖ против туберкулеза в Чикаго: статистический анализ двадцатилетнего исследования. Педиатрия. 1961; 28: 622–41. [PubMed] [Google Scholar]
17. Хьюстон С., Фаннинг А., Соскольн К.Л., Фрейзер Н. Эффективность вакцинации бациллой Кальметта-Герена (БЦЖ) против туберкулеза. Am J Эпидемиол. 1990;131:340–8. [PubMed] [Google Scholar]
18. Behr MA, Wilson MA, Gill WP, et al. Сравнительная геномика вакцин БЦЖ с помощью полногеномного ДНК-микрочипа. Наука. 1999; 284:1520–3. [PubMed] [Google Scholar]
19. Young T, Hershfield E. Исследование случай-контроль для оценки эффективности массовой вакцинации новорожденных БЦЖ среди канадских индейцев. Am J Общественное здравоохранение. 1986; 76: 783–6. [Бесплатная статья PMC] [PubMed] [Google Scholar]
20. Turnbull FM, McIntyre PB, Achat HM, et al. Национальное исследование побочных реакций после вакцинации бациллой Кальметта-Герена. Клин Инфекция Дис. 2002; 34: 447–53. [PubMed] [Академия Google]
[PubMed] [Академия Google]
21. Kroger L, Korppi M, Brander E, et al. Остеит, вызванный вакцинацией Bacille Calmette-Guerin: ретроспективный анализ 222 случаев. J заразить дис. 1995; 172: 574–6. [PubMed] [Google Scholar]
22. Albot EA, Perkins MD, Silva SFM, Frothingham R. Диссеминированная болезнь Bacille Calmette-Guerin после вакцинации: история болезни и обзор. Клин Инфекция Дис. 1997; 24:1139–46. [PubMed] [Google Scholar]
23. Hutmacher M, Scheifel D, Law B, Halperin S. Госпитализация в связи с осложнениями вакцины БЦЖ: больницы IMPACT, 1993–2001. Резюме P20, 5-я Канадская национальная конференция по иммунизации; Виктория, Британская Колумбия. 1–3 декабря 2002 г. [Google Scholar]
24. Romanus V, Svensson A, Hallander HO. Влияние изменения охвата вакцинацией БЦЖ на заболеваемость туберкулезом среди детей шведского происхождения в период с 1969 по 1989 год. Tuber Lung Dis. 1992; 73: 150–61. [PubMed] [Google Scholar]
25. Romanus V, Hallander HO, Wahlen P, Olinder-Nielsen AM, Magnusson PH, Juhlin I. Атипичные микобактерии при внелегочных заболеваниях у детей. Заболеваемость в Швеции с 1969 по 1990 год, в связи с изменением охвата вакцинацией БЦЖ. Tuber Lung Dis. 1995; 76: 300–10. [PubMed] [Google Scholar]
Атипичные микобактерии при внелегочных заболеваниях у детей. Заболеваемость в Швеции с 1969 по 1990 год, в связи с изменением охвата вакцинацией БЦЖ. Tuber Lung Dis. 1995; 76: 300–10. [PubMed] [Google Scholar]
История вакцины БЦЖ — PMC
Maedica (Bucur). 2013 март; 8(1): 53–58.
a и a, b
Информация об авторе Примечания к статье Информация об авторских правах и лицензии Отказ от ответственности
Туберкулез (ТБ) по-прежнему является причиной 2 миллионов смертей каждый год, несмотря на то, что он является излечимым инфекционным заболеванием, передающимся воздушно-капельным путем. Термины «чахотка» и «туберкулез» исторически использовались для описания туберкулеза, который был причиной каждой четвертой смерти в 19 веке.век. Из-за своей инфекционной природы, хронического течения и длительного лечения туберкулез является тяжелым бременем для общества. Более того, появление ТБ с множественной лекарственной устойчивостью и текущая эпидемия ТБ-ВИЧ вызывают еще большую обеспокоенность. Лечение и профилактика туберкулеза стали постоянной проблемой с древних времен. Бацилла Кальметта-Герена (БЦЖ) — единственная доступная на сегодняшний день вакцина, которая используется уже более 90 лет с поразительными показателями безопасности. Однако его эффективность остается спорной. Не существует универсальной политики вакцинации БЦЖ, при этом некоторые страны просто рекомендуют ее использование, а другие внедрили программы иммунизации. В этой статье мы рассмотрим несколько важных вех разработки вакцины БЦЖ с момента открытия до сегодняшнего дня.
Лечение и профилактика туберкулеза стали постоянной проблемой с древних времен. Бацилла Кальметта-Герена (БЦЖ) — единственная доступная на сегодняшний день вакцина, которая используется уже более 90 лет с поразительными показателями безопасности. Однако его эффективность остается спорной. Не существует универсальной политики вакцинации БЦЖ, при этом некоторые страны просто рекомендуют ее использование, а другие внедрили программы иммунизации. В этой статье мы рассмотрим несколько важных вех разработки вакцины БЦЖ с момента открытия до сегодняшнего дня.
Ключевые слова: Туберкулез, БЦЖ, вакцина, история, обзор
Люди были инфицированы M.tuberculosis (Mtb) на протяжении тысячелетий. Туберкулезная инфекция характеризуется сложным иммунологическим ответом, который приводит к уникальному взаимодействию хозяина и патогена, что затрудняет лечение и контроль. Кроме того, ТБ является болезнью, связанной с бедностью, и имеет серьезные социальные последствия. Внедрение бациллы Кальметта-Герена (БЦЖ) и химиотерапии в прошлом столетии знаменует собой важный прогресс в истории туберкулеза (ТБ), который объясняет оптимизм в борьбе с болезнью, особенно в эндемичных районах. На сегодняшний день БЦЖ остается наиболее широко используемой вакциной во всем мире, она была введена более чем 4 миллиардам человек с поразительными показателями безопасности (1,2). Помимо БЦЖ, нет других доступных вакцин для лечения туберкулеза, и из многих новых кандидатов, находящихся в стадии разработки, ни одна не близка к использованию на рынке. В этом обзоре мы обсудим основные вехи в истории ТБ и БЦЖ.
На сегодняшний день БЦЖ остается наиболее широко используемой вакциной во всем мире, она была введена более чем 4 миллиардам человек с поразительными показателями безопасности (1,2). Помимо БЦЖ, нет других доступных вакцин для лечения туберкулеза, и из многих новых кандидатов, находящихся в стадии разработки, ни одна не близка к использованию на рынке. В этом обзоре мы обсудим основные вехи в истории ТБ и БЦЖ.
Ранняя история туберкулеза
Mtb, внутриклеточный патоген, вызывающий туберкулез, был открыт в 1882 г. Робертом Кохом и является причиной большего количества смертей среди людей, чем какой-либо другой отдельный патоген сегодня (3-5). В начале прошлого века существовала надежда, что ТБ можно победить с помощью вакцинации недавно разработанной вакциной M. bovis БЦЖ, выделенной и названной в честь Кальметта и Герена в Лилле, Франция (6). Эти надежды были еще больше подкреплены разработкой первых противотуберкулезных препаратов во время Второй мировой войны Сельманом Ваксманом, который обнаружил бактериостатическую активность стрептомицина в отношении Mtb (7). Первоначально лечение стрептомицином казалось очень эффективным, но ситуация изменилась, когда быстро развилась лекарственная устойчивость, что является ранним свидетельством способности Mtb приобретать лекарственную устойчивость при лечении одним антибиотиком. Несмотря на эту раннюю запись на стене, ошибочное представление о том, что туберкулез можно победить с помощью антибиотиков и вакцинации БЦЖ, привело к самоуспокоенности на несколько десятилетий. Ситуация резко изменилась только в начале 1990-е годы, когда Всемирная организация здравоохранения (ВОЗ) объявила туберкулез глобальной чрезвычайной ситуацией (8). С этого времени ученые-фтизиатры, которые сосредоточили большую часть своих усилий на других областях исследований и разработок из-за отсутствия интереса к ТБ и финансирования, смогли переориентировать усилия и инициировать значительные мероприятия по изучению ТБ (9). ). Появление туберкулеза с множественной лекарственной устойчивостью (МЛУ-ТБ), вызванного эпидемией ВИЧ, стало причиной такого смещения интереса.
Первоначально лечение стрептомицином казалось очень эффективным, но ситуация изменилась, когда быстро развилась лекарственная устойчивость, что является ранним свидетельством способности Mtb приобретать лекарственную устойчивость при лечении одним антибиотиком. Несмотря на эту раннюю запись на стене, ошибочное представление о том, что туберкулез можно победить с помощью антибиотиков и вакцинации БЦЖ, привело к самоуспокоенности на несколько десятилетий. Ситуация резко изменилась только в начале 1990-е годы, когда Всемирная организация здравоохранения (ВОЗ) объявила туберкулез глобальной чрезвычайной ситуацией (8). С этого времени ученые-фтизиатры, которые сосредоточили большую часть своих усилий на других областях исследований и разработок из-за отсутствия интереса к ТБ и финансирования, смогли переориентировать усилия и инициировать значительные мероприятия по изучению ТБ (9). ). Появление туберкулеза с множественной лекарственной устойчивостью (МЛУ-ТБ), вызванного эпидемией ВИЧ, стало причиной такого смещения интереса. Вскоре исследователи определили последовательность генома Mtb и начали анализировать иммунологию туберкулеза и клеточную биологию (10).
Вскоре исследователи определили последовательность генома Mtb и начали анализировать иммунологию туберкулеза и клеточную биологию (10).
2012 — 91 год вакцинации БЦЖ
В 1900 году Альберт Кальметт и Камиль Герен начали свои исследования противотуберкулезной вакцины в Институте Пастера в Лилле. Они культивировали бациллы туберкулеза на глицериновой и картофельной среде, но им было трудно получить гомогенную суспензию бацилл. Пытаясь противодействовать их склонности к слипанию, они попытались добавить в среду бычью желчь и, к своему удивлению, отметили, что пересев приводит к снижению вирулентности организма. Именно это случайное наблюдение привело их к осуществлению долгосрочного проекта по производству вакцины из этой аттенуированной туберкулезной палочки (11).
В 1908 году, начав с вирулентного бычьего штамма туберкулезной палочки, предоставленного Нокардом (первоначально выделенного им в 1902 году из вымени больной туберкулезом коровы), они культивировали его на своей желчной, глицериновой и картофельной среде, а затем приступили к пересеву в примерно три недельных интервала. К 1913 году они были готовы начать испытание вакцины на крупном рогатом скоте, которое было прервано началом Первой мировой войны. Субкультивирование продолжалось на протяжении всей немецкой оккупации Лилля, несмотря на значительно возросшую стоимость картофеля и трудности с получением подходящей бычьей желчи на скотобойне. . Тем не менее, им удалось получить это по милости ветеринаров немецких оккупационных войск. К 1919, после примерно 230 пересевов, проведенных в течение предыдущих 11 лет, у них была туберкулезная палочка, которая не вызывала прогрессирующего туберкулеза при введении морским свинкам, кроликам, крупному рогатому скоту или лошадям. По предложению Герена они назвали его Bacille Bilie Calmette-Guerin; позже они опустили «Bilie», и так родилась БЦЖ (11).
К 1913 году они были готовы начать испытание вакцины на крупном рогатом скоте, которое было прервано началом Первой мировой войны. Субкультивирование продолжалось на протяжении всей немецкой оккупации Лилля, несмотря на значительно возросшую стоимость картофеля и трудности с получением подходящей бычьей желчи на скотобойне. . Тем не менее, им удалось получить это по милости ветеринаров немецких оккупационных войск. К 1919, после примерно 230 пересевов, проведенных в течение предыдущих 11 лет, у них была туберкулезная палочка, которая не вызывала прогрессирующего туберкулеза при введении морским свинкам, кроликам, крупному рогатому скоту или лошадям. По предложению Герена они назвали его Bacille Bilie Calmette-Guerin; позже они опустили «Bilie», и так родилась БЦЖ (11).
В 1921 году Кальметт решил, что пришло время испытать вакцину на людях. Первое введение БЦЖ человеку было осуществлено Бенджамином Вайль-Халле (1875-1919 гг.).58) ассистировал Раймон Турпин (1895-1988) в госпитале Шарите, Париж. Женщина умерла от туберкулеза через несколько часов после рождения здорового ребенка. 18 июля 1921 года Вайль-Халле и Терпин дали младенцу перорально дозу БЦЖ. Нежелательных последствий не было. Пероральный путь был выбран, поскольку Кальметт считал желудочно-кишечный тракт обычным путем естественного заражения туберкулезной палочкой. Затем Weill-Halle попробовал подкожный и накожный пути введения другим младенцам, но родители возражали против местных реакций, и поэтому пероральный метод был продолжен с использованием эмульсии БЦЖ, приготовленной Боке и Негре. К 1924 они смогли сообщить о серии из 664 оральных вакцинаций БЦЖ младенцев (12). Институт Пастера в Лилле начал массовое производство вакцины БЦЖ для медицинских работников. С 1924 по 1928 год 114 000 младенцев были вакцинированы без серьезных осложнений (13). В 1928 году Кальметт позвал Герена присоединиться к нему в Париже, поскольку не считал необходимым, чтобы Герен продолжал эксперименты с БЦЖ на животных в Лилле. К 1931 году появилась специальная лаборатория по приготовлению БЦЖ, заведующей которой был назначен Герен.
Женщина умерла от туберкулеза через несколько часов после рождения здорового ребенка. 18 июля 1921 года Вайль-Халле и Терпин дали младенцу перорально дозу БЦЖ. Нежелательных последствий не было. Пероральный путь был выбран, поскольку Кальметт считал желудочно-кишечный тракт обычным путем естественного заражения туберкулезной палочкой. Затем Weill-Halle попробовал подкожный и накожный пути введения другим младенцам, но родители возражали против местных реакций, и поэтому пероральный метод был продолжен с использованием эмульсии БЦЖ, приготовленной Боке и Негре. К 1924 они смогли сообщить о серии из 664 оральных вакцинаций БЦЖ младенцев (12). Институт Пастера в Лилле начал массовое производство вакцины БЦЖ для медицинских работников. С 1924 по 1928 год 114 000 младенцев были вакцинированы без серьезных осложнений (13). В 1928 году Кальметт позвал Герена присоединиться к нему в Париже, поскольку не считал необходимым, чтобы Герен продолжал эксперименты с БЦЖ на животных в Лилле. К 1931 году появилась специальная лаборатория по приготовлению БЦЖ, заведующей которой был назначен Герен.
Таким образом, метод вакцинации БЦЖ оказался безопасным. Но не менее важным был вопрос о его эффективности. Статистика Calmette и Guerin показала снижение смертности от туберкулеза среди восприимчивых детей, привитых БЦЖ. За пределами Франции вакцинация БЦЖ также применялась, особенно в Барселоне Луисом Сайе; а в скандинавских странах Арвид Валлгрен в Гётеборге (14) и Йоханнес Хеймбек в Осло (15) первыми применили кожное введение БЦЖ. Однако в Великобритании по-прежнему сохранялся значительный скептицизм, и статистика Кальметта и Герена подверглась резкой критике в 1919 г.28 профессора М. Гринвуда (16). Более того, в Соединенных Штатах Петрофф и его коллеги из санатория Трюдо сообщили в 1929 г., что в образце БЦЖ, предоставленном Кальметтом, были выделены вирулентные туберкулезные бациллы, что поставило под серьезное сомнение утверждение Кальметта о том, что БЦЖ является «вирусным лекарством» (17). . Несмотря на эти тревожные сообщения, Кальметт и Герен были уверены, что BCG безопасна, пока не произошла «катастрофа в Любеке».
Любекская катастрофа (1930 г.)
В 1930 г. трагическая катастрофа в Любеке подорвала доверие к BCG. В этом городе на севере Германии профессор Дейке, директор больницы общего профиля Любека, и доктор Альштедт, главный врач Любекского департамента здравоохранения, разработали схему вакцинации новорожденных. БЦЖ поставлялась из Института Пастера в Париже, но была подготовлена для введения в туберкулезной лаборатории в Любеке, и использовался пероральный путь введения. Через четыре-шесть недель у большого числа детей развился туберкулез. Из 250 вакцинированных 73 человека умерли в первый год и еще 135 были инфицированы, но выздоровели. Правительство Германии организовало расследование, которое возглавили профессор Бруно Ланге из Института Роберта Коха в Берлине и профессор Людвиг Ланге из Министерства здравоохранения Германии. Через 20 месяцев в их отчете БЦЖ была оправдана как причина катастрофы, которую они приписали небрежному заражению вакцины вирулентными туберкулезными бациллами в лабораториях Любека (18). Двое из пострадавших врачей были приговорены к тюремному заключению.
Двое из пострадавших врачей были приговорены к тюремному заключению.
Когда новости о катастрофе в Любеке распространились по всему миру, Кальметт и Герен стали объектами серьезной критики, и оба они испытали сильное напряжение. В августе 1930 года на собрании Международного союза борьбы с туберкулезом в Осло Кальметт защищался и получил бурные овации. Хотя отчет немецкого расследования реабилитировал БЦЖ как причину катастрофы, доверие к вакцине было подорвано.
Первые исследования БЦЖ
К концу 19В 40-х годах появилось несколько исследований, доказывающих полезность БЦЖ для защиты от туберкулеза. Туберкулез стал серьезной проблемой после Второй мировой войны, и использование БЦЖ поощрялось, в частности, ЮНИСЕФ, недавно созданной Всемирной организацией здравоохранения (ВОЗ) и Скандинавскими обществами Красного Креста. В течение следующего десятилетия кампании распространились на развивающиеся страны. Также в 1950-х годах Совет по медицинским исследованиям в Соединенном Королевстве и Служба общественного здравоохранения США организовали крупные испытания. Вскоре стало очевидно, что процедура, используемая в Соединенном Королевстве (копенгагенский штамм БЦЖ, вводимый туберкулин-отрицательным 13-летним детям), очень эффективна против туберкулеза (19).), в то время как в Соединенных Штатах (штамм Tice, назначаемый туберкулинотрицательным людям разного возраста) практически не давал защиты (20). На основании этих результатов соответствующие органы общественного здравоохранения рекомендовали БЦЖ в качестве рутинной процедуры для туберкулин-негативных подростков в Соединенном Королевстве, тогда как БЦЖ не рекомендовалась для рутинного использования в Соединенных Штатах, но ограничивалась определенными группами высокого риска. Большинство стран мира последовали примеру Европы и ВОЗ и ввели рутинную вакцинацию БЦЖ по различным графикам (например, при рождении, поступлении в школу, выпуске из школы), в то время как Нидерланды и США отказались от рутинного использования БЦЖ и основывали свои стратегия борьбы с туберкулезом при отслеживании контактов и использовании туберкулина для выявления лиц для профилактического лечения.
Вскоре стало очевидно, что процедура, используемая в Соединенном Королевстве (копенгагенский штамм БЦЖ, вводимый туберкулин-отрицательным 13-летним детям), очень эффективна против туберкулеза (19).), в то время как в Соединенных Штатах (штамм Tice, назначаемый туберкулинотрицательным людям разного возраста) практически не давал защиты (20). На основании этих результатов соответствующие органы общественного здравоохранения рекомендовали БЦЖ в качестве рутинной процедуры для туберкулин-негативных подростков в Соединенном Королевстве, тогда как БЦЖ не рекомендовалась для рутинного использования в Соединенных Штатах, но ограничивалась определенными группами высокого риска. Большинство стран мира последовали примеру Европы и ВОЗ и ввели рутинную вакцинацию БЦЖ по различным графикам (например, при рождении, поступлении в школу, выпуске из школы), в то время как Нидерланды и США отказались от рутинного использования БЦЖ и основывали свои стратегия борьбы с туберкулезом при отслеживании контактов и использовании туберкулина для выявления лиц для профилактического лечения.
Эффективность БЦЖ
Ранее были выдвинуты две гипотезы, объясняющие несопоставимые результаты, наблюдаемые при различных оценках БЦЖ. Один объяснил различия различиями между штаммами БЦЖ (21). На самом деле БЦЖ никогда не клонировали и пассировали в разных условиях, в разных лабораториях с момента ее первоначального получения в 1920-х годах. Было признано, что штаммы, произведенные разными производителями, различаются по микробиологическим свойствам (22), и, следовательно, вполне разумно предположить, что это может отражаться в различиях в иммуногенности (23). Альтернативная гипотеза возникла вокруг испытаний USPHS, в которых отмечалось, что плохие результаты наблюдались в Алабаме, Джорджии и Пуэрто-Рико среди населения, которое, как известно, подвергалось воздействию многих различных «экологических» микобактерий. Таким образом, изначально Палмер и его коллеги предположили, что воздействие различных микобактерий из окружающей среды может само по себе обеспечивать некоторую защиту от туберкулеза и различными способами влиять на иммунную систему, и что БЦЖ не может значительно улучшиться на этом фоне (24).
Чтобы сделать выбор между этими точками зрения, в районе Чинглпут в Южной Индии, начиная с 1968 г., было организовано большое исследование при содействии Индийского совета медицинских исследований, ВОЗ и Службы общественного здравоохранения США (25). . План состоял в том, чтобы сравнить два разных штамма БЦЖ (парижский/пастеровский против датского), каждый в двух дозах, в районе, который, как известно, имеет очень высокую распространенность воздействия микобактерий из окружающей среды. Сопутствующее испытание планировалось провести в районе на севере Индии с небольшим воздействием микобактерий из окружающей среды, но, к сожалению, отчасти из-за политических волнений, оно так и не было начато. Результаты судебного процесса над Чинглпутом были обнародованы в 1979, и они показали, что ни одна из вакцин не обеспечивает никакой защиты от туберкулеза легких (25). Подробные результаты этого испытания странны по нескольким причинам. Риск заболевания среди лиц, считавшихся «туберкулинотрицательными» в начале, был намного ниже, чем предсказывалось вначале, и оказалось, что на самом деле было больше случаев среди вакцинированных, чем среди контрольной группы, в течение короткого времени после вакцинации (хотя статистическая значимость это наблюдение сомнительно). Хотя два семинара, организованных ВОЗ, рассмотрели исследование и пришли к выводу, что результаты нельзя отнести к методологической ошибке (26), полностью подробное представление результатов этого масштабного исследования так и не появилось, а без подробных данных трудно точно понять что случилось. Неожиданные результаты исследования Chingleput привели к серии обсервационных исследований, направленных на оценку использования БЦЖ в различных популяциях мира (27). Хотя большинство исследований показали некоторую степень защиты, общее впечатление состоит в большом разнообразии, для которого до сих пор нет общепризнанного объяснения.
Хотя два семинара, организованных ВОЗ, рассмотрели исследование и пришли к выводу, что результаты нельзя отнести к методологической ошибке (26), полностью подробное представление результатов этого масштабного исследования так и не появилось, а без подробных данных трудно точно понять что случилось. Неожиданные результаты исследования Chingleput привели к серии обсервационных исследований, направленных на оценку использования БЦЖ в различных популяциях мира (27). Хотя большинство исследований показали некоторую степень защиты, общее впечатление состоит в большом разнообразии, для которого до сих пор нет общепризнанного объяснения.
ВАКЦИНЫ БЦЖ сегодня
В настоящее время используется несколько вакцин БЦЖ. Основными производителями для международного рынка являются Pasteur-Merieux-Connaught, Датский институт сывороток Statens, Evans Medeva (который взял на себя старую вакцину Glaxo) и Японская лаборатория БЦЖ в Токио. Каждая из этих вакцин БЦЖ производится по-своему, и признано, что они различаются по различным качествам, таким как доля жизнеспособных клеток на дозу (22). Штаммы БЦЖ, полученные из исходного штамма Paris после 1925 (например, нынешние штаммы Pasteur, Copenhagen, Glaxo-Evans) не имеют области генома, известной как RD-2, которая все еще присутствует в штаммах, полученных ранее этой даты [представлена нынешними бразильскими (Moreau), японскими и российские штаммы] (28,29).
Штаммы БЦЖ, полученные из исходного штамма Paris после 1925 (например, нынешние штаммы Pasteur, Copenhagen, Glaxo-Evans) не имеют области генома, известной как RD-2, которая все еще присутствует в штаммах, полученных ранее этой даты [представлена нынешними бразильскими (Moreau), японскими и российские штаммы] (28,29).
Фенотипические различия между этими вакцинными штаммами БЦЖ были впервые обнаружены в 1920-х годах, а совсем недавно молекулярные исследования определили их геномные различия. Хотя несколько исследований на животных и людях предполагают, что конкретный вакцинный штамм БЦЖ, используемый для иммунизации, влияет на микобактериальный специфический иммунный ответ, в настоящее время недостаточно данных, чтобы отдать предпочтение или рекомендовать один вакцинный штамм БЦЖ.
Тем не менее, большинство населения мира обеспечено вакциной БЦЖ, закупленной ЮНИСЕФ (Детским фондом Организации Объединенных Наций) от имени Глобального альянса по вакцинам и иммунизации. ЮНИСЕФ использует только четырех поставщиков вакцины БЦЖ, которые производят только три различных вакцинных штамма БЦЖ: БЦЖ-Дания, производимая Государственным институтом сывороток в Дании, БЦЖ-Россия (генетически идентичная БЦЖ-Болгария) производства Bulbio (BB-NCIPD) в Болгарии и Институтом сыворотки в Индии и БЦЖ-Япония, произведенная Японской лабораторией БЦЖ.
На людях было проведено три исследования защитной эффективности, вызванной различными вакцинными штаммами БЦЖ (вставка ref). В двух исследованиях (с последующим наблюдением от 4 до 50 лет) БЦЖ Пастера ассоциировалась со статистически значимо большей защитной эффективностью, чем БЦЖ-Фиппс или БЦЖ-Глаксо (30). В третьем исследовании (с последующим наблюдением в течение 15 лет) вакцина БЦЖ-Дания показала большую защитную эффективность, чем БЦЖ-Пастер (25 и 17% соответственно) (31).
Эти исследования дают лишь ограниченную информацию о защитной эффективности вакцинных штаммов БЦЖ, наиболее часто используемых в настоящее время, поскольку БЦЖ-Фиппс и БЦЖ-Глаксо больше не используются, а БЦЖ-Пастер используется в очень немногих странах, в которых определен оптимальный вакцинный штамм БЦЖ имеет серьезные последствия.
Во-первых, принимая во внимание большую популяцию младенцев, получающих вакцину БЦЖ каждый год, даже небольшое повышение защитного иммунитета в результате использования определенного штамма БЦЖ приведет к усилению защиты от ТБ для большого числа детей. Во-вторых, разрабатывается ряд новых противотуберкулезных вакцин, в том числе вакцины, предназначенные для замены БЦЖ, и вакцины, предназначенные для бустерной вакцинации БЦЖ (5). Наиболее продвинутыми являются бустерные вакцины на основе субъединиц или живых векторов, предназначенные для использования после введения примирующей дозы существующей вакцины БЦЖ. Поэтому по-прежнему важно определить, какой штамм вакцины БЦЖ индуцирует наилучший первичный иммунный ответ против туберкулеза для последующей бустерной вакцинации.
Во-вторых, разрабатывается ряд новых противотуберкулезных вакцин, в том числе вакцины, предназначенные для замены БЦЖ, и вакцины, предназначенные для бустерной вакцинации БЦЖ (5). Наиболее продвинутыми являются бустерные вакцины на основе субъединиц или живых векторов, предназначенные для использования после введения примирующей дозы существующей вакцины БЦЖ. Поэтому по-прежнему важно определить, какой штамм вакцины БЦЖ индуцирует наилучший первичный иммунный ответ против туберкулеза для последующей бустерной вакцинации.
Одно из недавних исследований Н. Ритц и Ко. (32) пришли к выводу, что существуют значительные различия в иммунном ответе, индуцированном различными вакцинными штаммами БЦЖ у новорожденных. Иммунизация БЦЖ-Дания или БЦЖ-Япония индуцировала более высокие частоты микобактериально-специфических полифункциональных и цитотоксических Т-клеток и более высокие концентрации цитокинов Th2, чем иммунизация БЦЖ-Россия. Эти результаты могут иметь важные последствия для глобальной политики противотуберкулезной иммунизации и будущих испытаний противотуберкулезной вакцины. ❑
❑
Хотя эффективность вакцины БЦЖ остается спорной, живая аттенуированная БЦЖ по-прежнему является единственной вакциной, используемой для профилактики туберкулеза у людей. Он эффективен против тяжелых форм туберкулеза, и его использование ежегодно предотвращает большое количество смертей, которые в противном случае были бы вызваны туберкулезом. Выбор штамма БЦЖ для вакцинации остается важным вопросом. В настоящее время трудно определить, какой штамм следует использовать, и дальнейший подробный анализ геномики и иммуногенности подштаммов БЦЖ может дать ответ на этот важный вопрос. Всемирная организация здравоохранения и Международный союз по борьбе с туберкулезом и болезнями легких могут определить подштаммы БЦЖ, обеспечивающие наилучшую защиту, и рекомендовать их для вакцинации в будущем.
Авторы благодарят Matthias I.P. Gröschel, Медицинский центр Гронингена, Нидерланды, за пересмотр этой статьи.
КОНФЛИКТ ИНТЕРЕСОВ
не объявлено.
ФИНАНСОВАЯ ПОДДЕРЖКА
не заявлено.
1. McShane H. Туберкулезные вакцины: Beyond Bacille Calmette-Guerin. Philos Trans R Soc Lond B Biol Sci. 2011; 366: 2782–9. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2. Ottenhoff THM, Kaufmann SHE. Вакцины против туберкулеза: где мы и куда нам нужно идти? Читнис К.Э., редактор. PLoS Патог. 2012;8:e1002607–12. [Бесплатная статья PMC] [PubMed] [Google Scholar]
3. Оттенхофф ТГМ. Преодоление глобального кризиса: «да, мы можем», но и для туберкулеза … ? Евр Дж Иммунол. 2009;39:2014–20. [PubMed] [Google Scholar]
4. Kaufmann SHE, Winau F. От бактериологии к иммунологии: дуализм специфичности. Нац. Иммунол. 2005; 6: 1063–6. [PubMed] [Google Scholar]
5. Kaufmann SH, Hussey G, Lambert P-H. Новые вакцины от туберкулеза. Ланцет. 2010;375:2110–9. [PubMed] [Google Scholar]
6. Calmette A, Guerin C, Boquet A, et al. Париж: Массон и др.; 1927. Профилактическая вакцинация против туберкулеза с использованием «БЦЖ». [Google Scholar]
7. Ваксман С.А. Победа над туберкулезом. Первое издание. Калифорнийский университет Press. 1965 [Google Scholar]
Ваксман С.А. Победа над туберкулезом. Первое издание. Калифорнийский университет Press. 1965 [Google Scholar]
8. Всемирная организация здравоохранения. Туберкулез: глобальная чрезвычайная ситуация; 1994 год; Женева, Швейцария. [Google Scholar]
9. Kaufmann SHE, Parida SK. Изменение моделей финансирования борьбы с туберкулезом. Нат Мед. 2007; 13: 299–303. [PubMed] [Google Scholar]
10. Cole ST, Brosch R, Parkhill J, et al. Расшифровка биологии Mycobacterium Tuberculosis из полной последовательности генома. Нат Мед. 1998;393:537–44. [PubMed] [Google Scholar]
11. Calmette A. 1922. Бактериальная инфекция и туберкулез у человека и у животных. [Google Scholar]
12. Calmette A, Guerin C, Weill-Halle B. Bull Acad Med. Том. 91. Париж: 1924. Очерк иммунизации против туберкулезной инфекции. стр. 787–96. [Google Scholar]
13. Calmette A, Guerin C, Negre L, et al. Энн Инст Пастер. Том. 41. Лилль: 1927 год. О профилактической вакцинации новых детей против туберкулеза с помощью БЦЖ. стр. 201–32. [Академия Google]
стр. 201–32. [Академия Google]
14. Валлгрен А. Ценность Кальметта. Вакцинация в профилактике туберкулеза в детском возрасте. ДЖАМА. 1934; 103: 1341–5. [Google Scholar]
15. Heimbeck J. Туберкулез у медсестер. Туберк. 1936: 18–18. [Google Scholar]
16. Гринвуд М. Статистическое исследование вакцинации БЦЖ профессором Кальметтом. БМЖ. 1928; 1: 793–5. [Бесплатная статья PMC] [PubMed] [Google Scholar]
18. Lange B. Weitere Untersuchungen zur Klärung der Ursachen der Unglücksfälle в Любеке. Туберк. 1931; 62: 335–51. [Google Scholar]
19. Hart PD, Sutherland I. Вакцины БЦЖ и Bacillus полевки в профилактике туберкулеза в подростковом и раннем взрослом возрасте. БМЖ. 1977; 2: 293–5. [Бесплатная статья PMC] [PubMed] [Google Scholar]
20. Comstock GW, Palmer CE. Долгосрочные результаты вакцинации БЦЖ на юге США.
21. Осборн Т.В. Изменения штаммов БЦЖ. Туберк. 1983; 64: 1–13. [PubMed] [Google Scholar]
22. Milstien JB, Gibson JJ. Контроль качества вакцины БЦЖ ВОЗ: обзор факторов, которые могут влиять на эффективность и безопасность вакцины. Бык. Всемирный орган здравоохранения. 1990; 68: 93–108. [Бесплатная статья PMC] [PubMed] [Google Scholar]
23. Hart PD. Эффективность и применимость Mass B.C.G. Вакцинация в борьбе с туберкулезом. БМЖ. 1967; 1: 587–9.2. [Бесплатная статья PMC] [PubMed] [Google Scholar]
24. Palmer CE, Long MW. Влияние инфекции атипичными микобактериями на вакцинацию БЦЖ и туберкулез. Ам преподобный Респир Дис. 1966; 94: 553–68. [PubMed] [Google Scholar]
25. Бейли Г.В. Испытание по профилактике туберкулеза, Мадрас. Индийская J Med Res. 1980; 72: 1–74. [PubMed] [Google Scholar]
26. Прививка от туберкулеза. Отчет научной группы ICMR/ВОЗ. Представитель World Health Organ Tech Rep. 1980; 651:1–21. [PubMed] [Академия Google]
1980; 651:1–21. [PubMed] [Академия Google]
27. Смит П.Г. Ретроспективная оценка эффективности вакцинации БЦЖ против туберкулеза методом случай-контроль. Туберк. 1982; 63: 23–35. [PubMed] [Google Scholar]
28. Mahairas GG, Sabo PJ, Hickey MJ, et al. Молекулярный анализ генетических различий между Mycobacterium Bovis BCG и Virulent M. Bovis. Журнал бактериологии. 1996; 178:1274–82. [Бесплатная статья PMC] [PubMed] [Google Scholar]
29. Corbel MJ, Fruth U, Griffiths E, et al. Отчет о консультации ВОЗ по характеристике штаммов БЦЖ, Имперский колледж, Лондон. вакцина. 2004; 22: 2675–80. [PubMed] [Академия Google]
30. Аронсон Н.Е., Сантошам М., Комсток Г.В. и др. Долгосрочная эффективность вакцины БЦЖ у американских индейцев и коренных жителей Аляски: 60-летнее последующее исследование. ДЖАМА. 2004; 291:2086–91. [PubMed] [Google Scholar]
31. Центр исследования туберкулеза (ICMR), Ченнаи. Пятнадцатилетнее наблюдение за испытаниями вакцин БЦЖ в Южной Индии для профилактики туберкулеза.
