Тромбоциты и их норма у женщин по возрасту в таблице
Тромбоциты — это маленькие безъядерные и бесцветные кровяные клетки. Их основная функция — участие в свертывании крови. Отслеживание количества этих клеток в крови человека, соответствие его норме, помогает выявлять на ранних стадиях проблемы со здоровьем.
Зачем нужны тромбоциты
Кровяные клетки тромбоциты выполняют несколько важных функций в организме:
- необходимы для процесса свертывания крови, на месте травмы они образуют кровяной сгусток, который потом превращается в плотную «заплатку», позволяя избежать потери крови через рану;
- воздействуют на поврежденный кровеносный сосуд, создавая в нем спазм, из-за этого ток крови по нему снижается, что тоже приводит к уменьшению потерь крови;
- поддерживают здоровое состояние внутренней стенки сосуда — они снижают его проницаемость, подпитывают его;
- при начале болезни активируют воспалительную реакцию, подавая иммунным клеткам сигнал действовать.

Образуются тромбоциты в красном костном мозге, а разрушаются в селезенке и частично в печени.
Норма тромбоцитов у женщин
Норма тромбоцитов у женщин зависит от возраста и физиологического состояния женщины (менструация, беременность). В анализе показатель тромбоцитов обозначается как PLT. Измеряют его в тысячах на 1 микролитр (тыс./мкл).
Тромбоциты: норма у женщин по возрасту, таблица
| Возраст женщины | Минимум, тыс./мкл | Максимум, тыс./мкл |
|---|---|---|
| До 16 лет | 160 | 390 |
| 16-25 | 180 | 380 |
| 26-35 | 400 | |
| 36-60 | 180 | 340 |
| От 60 и старше | 180 | 320 |
В период менструаций показатели количества тромбоцитов у женщин могут падать до 150 тыс. /мкл. Плотность крови в эти дни снижена, чтобы эндометрий отторгался и выходил, для предотвращения застойных явлений в матке.
/мкл. Плотность крови в эти дни снижена, чтобы эндометрий отторгался и выходил, для предотвращения застойных явлений в матке.
Во время беременности объем крови в организме женщины увеличивается, а тромбоциты не успевают вырабатываться в нужном количестве. Поэтому во время беременности допускается небольшое снижение тромбоцитов относительно нормы. Показатели нормального количества тромбоцитов для беременных лежат в пределах от 150 тыс./мкл до 320 тыс./мкл.
Что такое тромбокрит
Анализируя состояние количества тромбоцитов в крови, врачи выделяют еще один показатель, который называется тромбокритом. Тромбокрит показывает, в каком соотношении тромбоциты содержатся в общем объеме крови, которая еще не разделена на плазму и другие элементы. Тромбокрит в анализе обозначают как РСТ и указывают в процентах.
Тромбокрит: норма у женщин по возрасту, таблица
| Возраст женщины | РСТ, % |
|---|---|
| От 15 до 18 | 0,18-0,34 |
| От 18 до 60 лет | 0,1-0,4 |
| Во время беременности или менструации | 0,07-0,2 |
Заложенный природой механизм защиты от тромбоза во время беременности приводит к тому, что у будущих мам уровень тромбокрита может снижаться на половину от нормы. Во время месячных уровень тромбокрита также меньше нормы.
Во время месячных уровень тромбокрита также меньше нормы.
В целом, тромбокрит — это более узкий и специфичный показатель уровня тромбоцитов в организме.
Причины повышенного уровня тромбоцитов
Когда у пациента повышается уровень тромбоцитов, у него развивается тромбоцитоз. Такое состояние опасно возможной закупоркой сосудов и образованием тромбов.
Причины повышения:
- физическая нагрузка;
- воспалительный процесс;
- анемии различных видов;
- эритремия;
- удаление селезенки;
- послеоперационный период;
- злокачественная опухоль.
Причины пониженного уровня тромбоцитов
Состояние, в котором у человека диагностируют пониженный уровень тромбоцитов, называется тромбоцитопенией. Оно возникает при повышенном разрушении тромбоцитов, снижении выработки их костным мозгом и нездоровой задержкой их в селезенке.
Причины понижения:
- болезни костного мозга;
- тромбоз;
- тромбоцитопения из-за определенных лекарств;
- ДВС-синдром;
- инфекционные заболевания;
- заболевания щитовидки;
- апластическая анемия;
- острое поражение печени;
- гемофилия;
- аутоиммунные патологии кровеносной системы.

Тромбоцитопения выражается в длительных и обильных месячных, синяках и кровоподтеках на теле, возникающих без причин. Для такого состояния характерны частая кровоточивость носа, десен, долгое заживление ран и порезов.
Если вы сдали анализ крови и увидели, что количество тромбоцитов отклоняется от нормы, не нужно паниковать и пытаться поставить себе диагноз самостоятельно. Важно, чтобы расшифровка анализов проводилась квалифицированным специалистом, который назначит, при необходимости, дополнительные обследования и терапию.
Относитесь бережно к своему организму и будьте здоровы!
0
0
44233
Мой мир
Вконтакте
Одноклассники
норма у женщин по возрасту (таблица). Причины отклонений от нормы
Тромбоциты — это клетки крови, которые участвуют в процессе тромбоза и гемостаза. Они выполняют важную роль в организме, защищая от повреждений сосудов и кровотечений. Поэтому нужно регулярно проходить обследование и своевременно обращаться за помощью к врачу в случае обнаружения отклонений от установленных норм. Анализы, с помощью которых определяют тромбоциты, норма у женщин по возрасту, таблица показателей у них и у детей, норма у мужчин, причины отклонений представлены в этом материале.
Поэтому нужно регулярно проходить обследование и своевременно обращаться за помощью к врачу в случае обнаружения отклонений от установленных норм. Анализы, с помощью которых определяют тромбоциты, норма у женщин по возрасту, таблица показателей у них и у детей, норма у мужчин, причины отклонений представлены в этом материале.
Роль тромбоцитов в организме
Тромбоциты — это клетки, которые по форме напоминают небольшие пластинки. Основная их роль в организме — защита от кровопотери. Когда происходит повреждение сосуда, тромбоциты моментально направляются к поврежденному участку. Соединяясь между собой, они образовывают барьер, препятствуя кровотечению.
Помимо такой защитной функции, тромбоциты обеспечивают жидкое состояние крови, а также растворяют образовавшиеся тромбы.
Именно поэтому важно регулярно проводить анализ на тромбоциты в крови. Норма, повышенные, пониженные значения, а также причины образования отклонений показателей этих клеток крови описаны ниже.
Анализы для определения количества тромбоцитов
Простая клиническая диагностика крови способна определить количество тромбоцитов. Если результаты отклонены от норм, то врач может рекомендовать пациенту пройти более глубокое обследование — коагулограмму. Для общего анализа забор материала проводится из пальца, дополнительная диагностика предполагает сбор венозной крови. Для расшифровки результата применяется установленная норма тромбоцитов у мужчин, женщин, детей.
Перед любым из указанных анализов следует соблюдать общие правила подготовки к сдаче крови:
- за трое суток необходимо воздержаться от употребления алкогольных напитков, жирной и жареной пищи;
- сдается кровь натощак;
- желательно провести исследование в утреннее время.
Тромбоциты: норма у женщин по возрасту (таблица)
Для большинства людей нормой считаются такие показатели количества тромбоцитов в крови: от 200 до 400 тыс./мкл. Но у женщин при интерпретации результатов анализа следует учитывать дополнительные факторы, такие как день менструального цикла, возраст и даже время суток. Потому что от этих состояний зависит скорость, с которой организм вырабатывает тромбоциты.
Потому что от этих состояний зависит скорость, с которой организм вырабатывает тромбоциты.
Норма у женщин по возрасту (таблица) представлена ниже.
| Возраст | Количество тромбоцитов (тыс./мкл) |
| 15–18 лет | от 180 до 340 |
| 18–80 лет | от 180 до 320 |
Кроме возраста, на показатели количества тромбоцитов в крови у женщины влияют такие факторы, как беременность и менструация. В первом случае в организме увеличивается объем крови, тромбоциты не успевают восстанавливаться в необходимом количестве, поэтому небольшое снижение показателей в результате анализа является нормой.
Во время ежемесячных женских выделений происходит потеря объема крови в организме, что также приводит к снижению количества тромбоцитов. Поэтому при вышеуказанных состояниях допустимо временное снижение показателей до 150 тыс./мкл — это норма тромбоцитов у женщин. Отклонение от нормы будет установлено в том случае, если в результатах анализа указано количество тромбоцитов ниже 150 единиц на микролитр, а также в том случае, если такие показатели остаются постоянными.
В период менструаций и во время беременности считается нормой количество тромбоцитов в пределах 150–320 тыс./мкл крови. Женщинам необходимо регулярно обследоваться у врача, следовать его рекомендациям. В том случае, если помимо обнаружения пониженного уровня тромбоцитов в результате анализа присутствуют еще и жалобы пациента на состояние здоровья, в срочном порядке следует провести дополнительные диагностические процедуры с целью исключения серьезных патологических состояний.
Расшифровка результатов
В бланке результата анализа на определение количества тромбоцитов указываются разные медицинские аббревиатуры. Что они обозначают? Расшифровка в таблице:
- MPV (mean platelet volume) — это значение указывает на средний объем тромбоцитов в крови человека.
- PDW — обозначает приблизительную ширину распространения тромбоцитов.
- PCT (platelet crit) — тромбокрит.
- Тромбоциты PLT — нормы в крови у мужчин, женщин и детей обычно указываются именно в показателе PLT.
 Эта цифра обозначает количество данных клеток в крови человека. При обнаружении в этом показателе отклонений врач может назначить повторное обследование.
Эта цифра обозначает количество данных клеток в крови человека. При обнаружении в этом показателе отклонений врач может назначить повторное обследование.
Норма для мужчин
У мужчин при нормальном протекании процесса кроветворения тромбоциты обновляются с постоянной регулярностью. В норме показатели должны соответствовать 180–320 тыс./мкл. Если в женском организме возможны допустимые отклонения в показателях количества тромбоцитов, то у мужчин такие отступления недопустимы. При расшифровке анализа специалист может либо подтвердить норму, либо указать на возможную патологию в работе кровеносной системы.
Показатели тромбоцитов у детей
В детском возрасте нормы показателей тромбоцитов в крови зависят от возраста малыша. У новорожденного, в зависимости от общего состояния, допускается широкий диапазон показателей, которые могут считаться в каждом конкретном случае нормой. Относительно стабильной выработка организмом тромбоцитов становится в возрасте старше 4 лет.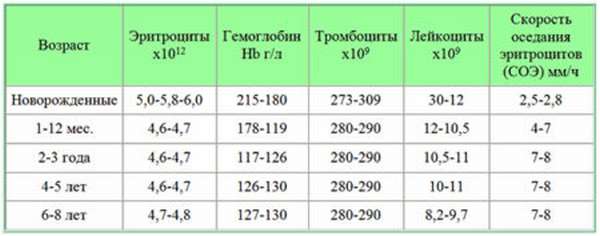
Таблица, представленная ниже, помогает расшифровать результат анализа у детей.
| Возраст ребенка | Нормы показателей тромбоцитов (тыс./мкл) |
| Новорожденный | 100–420 |
| от 2 месяцев до 1 года | 120–350 |
| от 1 года до 4 лет | 150–320 |
Причины повышенных показателей
Итак, мы узнали, что означают повышенные тромбоциты в крови. И причины возникновения такого состояния будут далее представлены вашему вниманию. Если результат анализа на определение таких клеток крови выявил отклонения от нормы, врач может лишь заподозрить определенную проблему со здоровьем. Для постановки диагноза требуется повторное или более глубокое дополнительное исследование.
В случае если при повторной сдаче анализа были обнаружены завышенные показатели тромбоцитов, то специалист может заподозрить (подтвердить) следующие нарушения в состоянии здоровья исследуемого пациента:
- Первичный тромбоз (или нарушение работы клеток костного мозга).

- Инфекционные заболевания (вирусного, бактериального и грибкового происхождения).
- Воспалительные процессы в организме.
- Обширный некроз тканей.
- Прием пациентом некоторых медицинских препаратов.
- Открытые травмы, кровотечения.
- Онкологическое заболевание.
- После хирургического вмешательства (например, при удалении селезенки) количество тромбоцитов увеличивается.
Причины низких показателей
Состояние, при котором в крови содержится пониженное количество тромбоцитов, называется тромбоцитопенией. Часто такое заболевание наблюдается у недоношенных новорожденных, что связано с недоразвитостью отдельных систем и органов малыша. Результат анализа показал, что тромбоциты ниже нормы у ребенка? Причины могут быть следующие:
- внутриутробное инфицирование плода некоторыми заболеваниями;
- несовместимость по группе крови плода и организма матери;
- асфиксия в процессе родовой деятельности;
- врожденная анемия.

У детей старше 4 лет и взрослых причины такого состояния могут быть следующие:
- инфекционные заболевания;
- интоксикация организма;
- проведение процедуры гемодиализа;
- серьезные аллергические реакции;
- онкозаболевание крови;
- кровотечение;
- заболевания аутоиммунной системы;
- прием некоторых медицинских препаратов.
Расшифровать результат анализа может только специалист. Следует учитывать, что многие факторы влияют на то, в каком объеме организм вырабатывает тромбоциты. Норма у женщин по возрасту, таблица установленных показателей у детей, а также уровень этих клеток в крови у мужчин должны быть известны каждому гематологу.
При обнаружении отклонений от установленных норм необходимо пройти повторное обследование. Только в таком случае врач может утвердить диагноз и назначить необходимое лечение. Для профилактики заболеваний, связанных с нарушением выработки тромбоцитов, следует следить за питанием, регулярно заниматься кардионагрузками (такими как бег, плавание, езда на велосипеде и другое), организовывать полноценный отдых.
причины появления, при каких заболеваниях возникает, диагностика и способы лечения
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Определение
Тромбоциты – клетки крови, которые участвуют в процессе ее свертывания. Их основная роль – образование тромба, или сгустка крови, закрывающего рану при кровотечении.
Тромбообразование является естественным процессом защиты от массивной кровопотери при любых травмах.
Избыточное количество тромбоцитов в крови называют тромбоцитозом — данное состояние часто протекает бессимптомно и может быть опасным для жизни.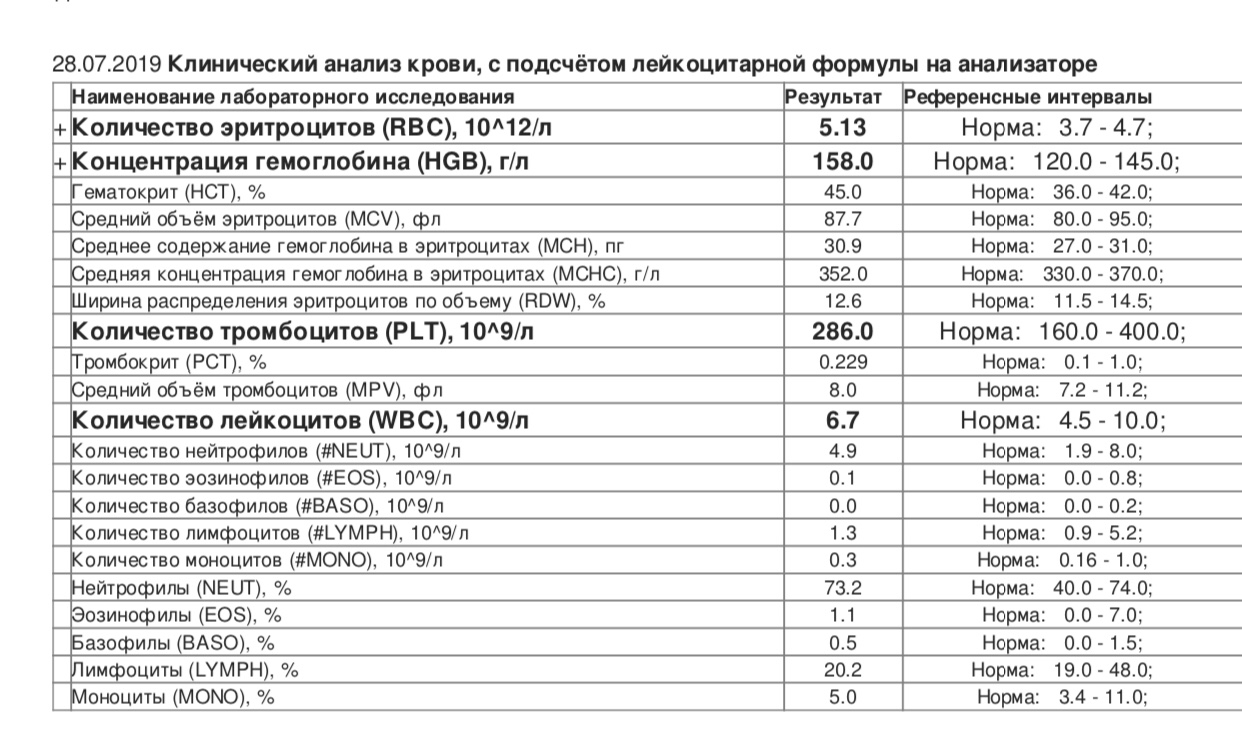
Разновидности тромбоцитозов
Под тромбоцитозом в широком смысле понимают увеличение количества тромбоцитов в периферической крови выше 400 тыс./мкл.
С точки зрения патологического процесса тромбоцитоз подразделяют на первичный и реактивный.
Реактивный тромбоцитоз возникает вследствие патологического процесса без участия гемопоэтических (кроветворных) стволовых клеток, часто это нормальная реакция на кровотечение.
Первичный тромбоцитоз развивается в результате нарушения системы кроветворения и деления стволовых клеток в костном мозге.
Возможные причины тромбоцитоза
В норме большое количество тромбоцитов может встречаться у новорожденных и у грудных детей.
В редких случаях тромбоцитоз сохраняется и во взрослом возрасте.Патологические механизмы, приводящие к развитию тромбоцитоза, многообразны и требуют дифференциального подхода к диагностике.
Реактивное повышение количества тромбоцитов наблюдается в следующих случаях:
- Инфекционно-воспалительные заболевания — одна из самых частых причин реактивного тромбоцитоза.
 Количество тромбоцитов в периферической крови увеличивается при пневмонии, сепсисе, остеомиелите, а также после хирургических вмешательств и травм. При системных воспалительных заболеваниях соединительной ткани, например при
Количество тромбоцитов в периферической крови увеличивается при пневмонии, сепсисе, остеомиелите, а также после хирургических вмешательств и травм. При системных воспалительных заболеваниях соединительной ткани, например при - Железодефицитная анемия – распространенное заболевание, которое встречается во всех возрастных группах.
Если дефицит железа развился на фоне хронической кровопотери, при обследовании выявляется тромбоцитоз.
- Спленэктомия (операция по удалению селезенки) – еще одна причина реактивного тромбоцитоза. Уровень тромбоцитов растет в течение первых 3 недель после оперативного вмешательства. Это происходит за счет того, что до удаления селезенки часть тромбоцитов находилась в тромбоцитарном депо (резервуаре) селезенки и не учитывалась в анализе крови.

При повышении уровня тромбоцитов до 600–800 тыс./мкл возрастает риск артериальных тромбозов и, как следствие, инфарктов и инсультов.
- Нарушение функции селезенки (аспления), приводящее к тромбоцитозу, может происходить в результате травм, опухолевых процессов в селезенке, при серповидно-клеточной анемии и тромбозах сосудов селезенки.
- Злокачественные новообразования меняют баланс цитокинов (белков, которые вырабатывают клетки иммунной системы при воспалении) с увеличением образования тромбоцитов. Тромбоциты в данном случае участвуют в образовании метастазов, создавая связь между собой и опухолевыми клетками. Наряду с этим механизмом развития тромбоцитоза злокачественные опухоли проходят стадию распада, которая характеризуется кровопотерей и реактивным тромбоцитозом.
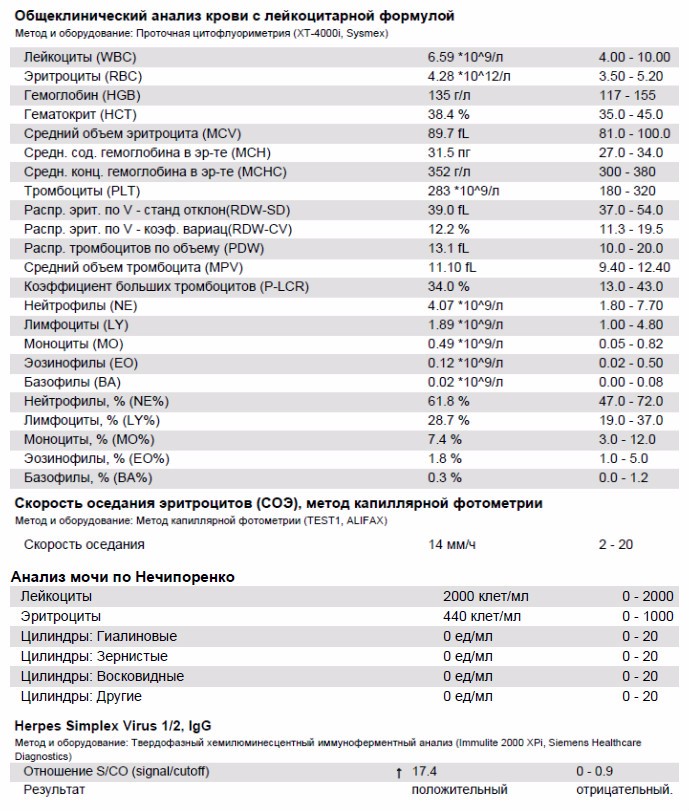
Тромбоцитоз в некоторых случаях ассоциирован с мутациями, характерными для миелопролиферативных заболеваний: истинной полицитемии, идеопатического миелофиброза и эссенциальной полицитемии. В данном случае прослеживается наследственный характер заболевания (у родственников диагностированы миелопролиферативные патологии). В костном мозге активируется деление стволовых клеток вследствие генетического дефекта. Симптомы зависят от основного заболевания и напрямую с ним связаны.
К каким врачам обращаться при тромбоцитозеТромбоцитоз выявляется с помощью лабораторных методов исследования и требует обращения к терапевту или врачу общей практики. В случае необходимости терапевт назначит консультацию гематолога, ревматолога, хирурга, онколога.
Диагностика и обследования при тромбоцитозе
При выявлении тромбоцитоза в клиническом анализе крови врач назначит комплекс лабораторно-инструментальных методов обследования с целью установления причины, вызвавшей данное состояние.
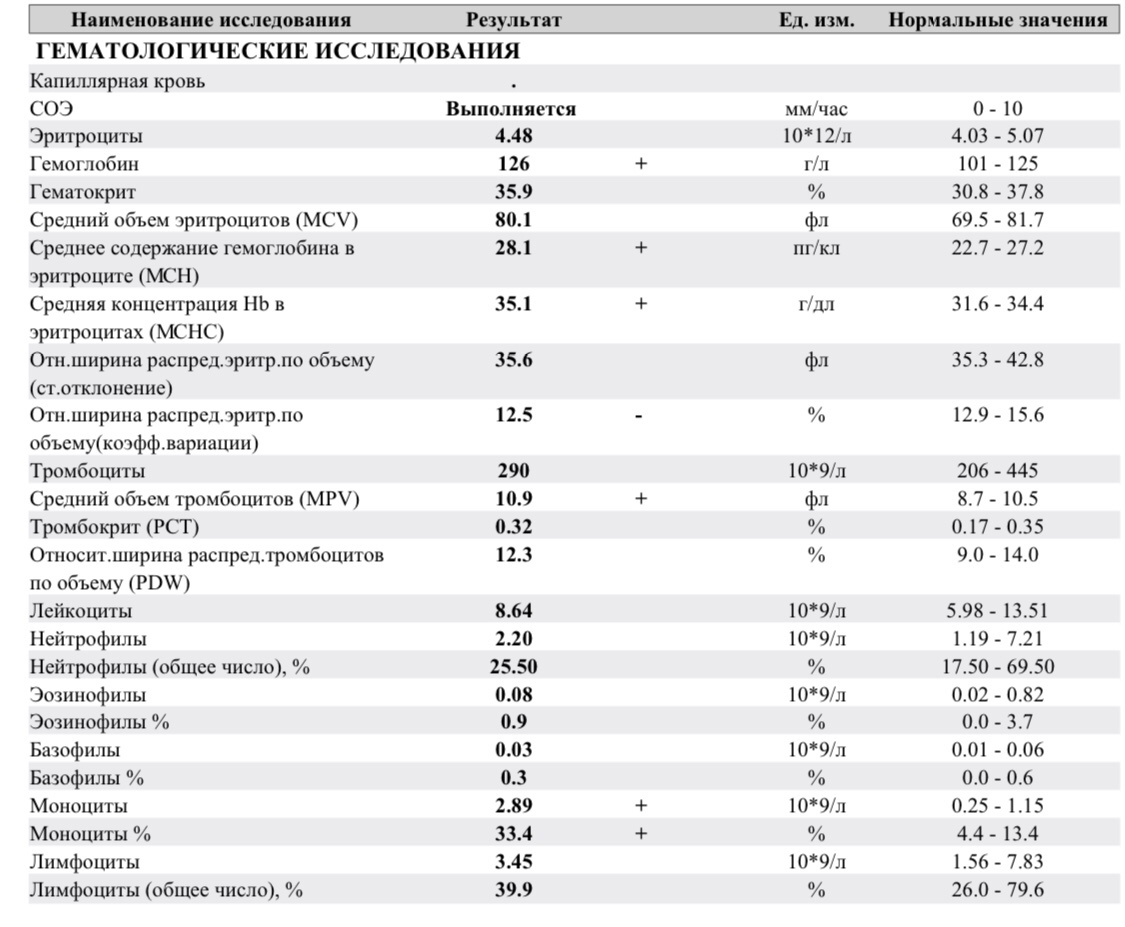
- Клинический анализ крови: общий анализ с подсчетом тромбоцитов, лейкоформула, СОЭ (с микроскопией мазка крови при наличии патологических сдвигов).
Тромбоциты — норма в крови, чем опасны повышенные и пониженные значения
Обновлено 11 сентября 2021 Просмотров: 111 368 Автор: Дмитрий Петров- Тромбоциты — это…
- Как определяют их уровень в крови
- Норма тромбоцитов у женщин, детей и мужчин
- О чем говорят повышенные тромбоциты
- Причины пониженных значений
Здравствуйте, уважаемые читатели блога KtoNaNovenkogo.ru. Людей, с нормально функционирующей системой кровообращения можно смело выделить из общей толпы.
Именно слаженное функционирование и необходимый баланс всех многочисленных компонентов, входящих в состав крови, обеспечивают человеку отличный настрой, бодрость, активность, полноту сил и энергии.
Рассмотрим особенности тромбоцитов, входящих в тройку основных форменных компонентов в составе крови – зачем они ей нужны и к чему может привести их дисбаланс.
Тромбоциты — это…
Тромб — это сгусток крови (в переводе с греческого языка), основой которого являются тромбоциты.
Тромбоцит же представляет собой маленькую, бесцветную, кровяную пластинку сферической формы (бляшки Биццоцеро). Формируются пластинки из плазменной структуры (мегакариоцитов – плазменных клеток) костного мозга. Тромбоциты не имеют ядра, но снабжены обильным количеством гранул (более 200).
Ценность грануляций обусловлена высоким содержанием особых компонентов тромбоцитарного роста (тромбоксана, тромбина, аденозиндифосфората и пр.факторов), обеспечивающих образование аминокислот и ферментов (что это такое?), разрушающих мембраны бактериальных клеток, предотвращая проникновение в кровь болезнетворных патогенов.
Размер тромбоцитарных пластин варьируется в пределах их возраста (юного, среднего, зрелого), от 2-х до 5-ти мкм.
Однако при соприкосновении тромбоцита с поверхностью, не соответствующей внутреннему эндотелию сосудов или полости сердечного перикарда, пластинки активируются, выпуская до 10 ложноножек (отростков) в десятки раз превышающих размер самой пластинки.
Такая особенность позволяет тромбоцитам служить своеобразной «заплаткой», закрывающей при необходимости раневые поверхности сосудов, не допуская кровотечений.
Именно ложноножки обеспечивают продвижение пластин по кровеносной системе. Тромбоциты обладают способностью прилипания к инородным агентам, захватыванию их и уничтожению, формируют сгусток тромба путем агрегации (склеивания пластин между собой) для предотвращения геморрагических процессов (кровотечений).
Основная роль тромбоцитов – активное участие в процессе свертывания крови (гемостаза).
Они обеспечивают транспортную функцию, доставляя питательные компоненты к тканям (эндотелию), выстилающих внутреннюю полость сосудистых стенок. Они сохраняют жизнедеятельность до 10 дней, после чего разрушаются в различных органах (в селезенке, легких, либо печени).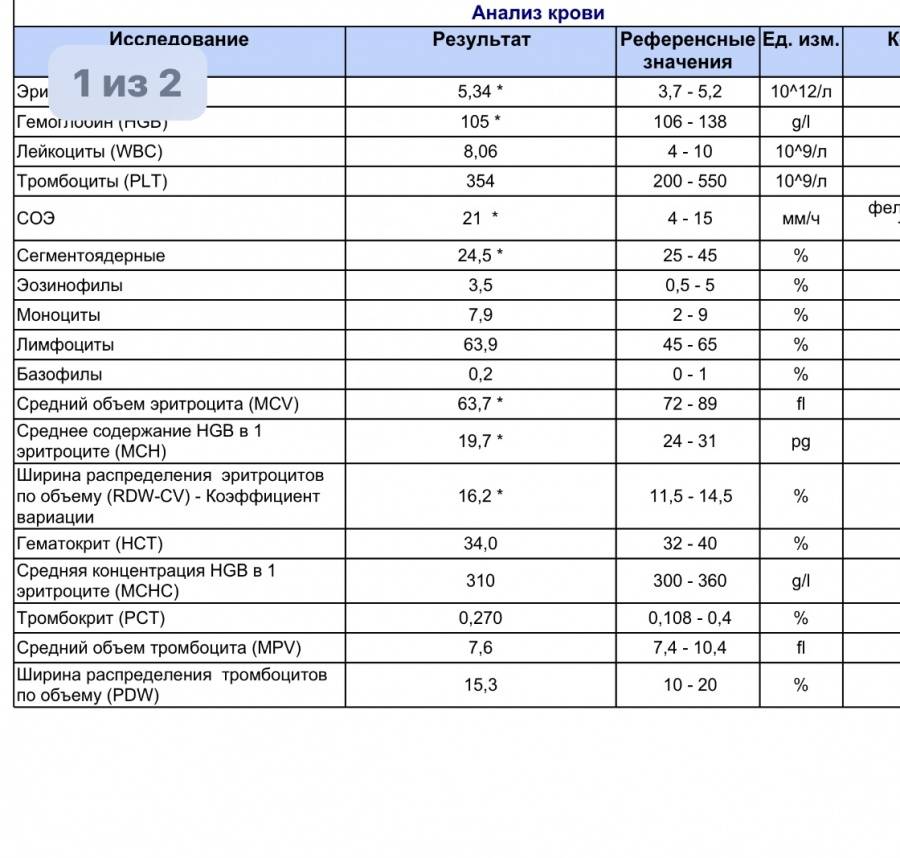
Последние разработки японских ученых доказали, что мегакариоциты не единственные источники образования бляшек Бицоцерро (тромбоцитов). Им удалось получить тромбоциты из собственных стволовых клеток пациента.
Данные исследования повышают успешность проведения трансплантации, так как при наличии таких тромбоцитов не вызывается отторжения организмом донорских органов.
Как участвуют тромбоциты в процессе гемостаза можно рассмотреть на схеме:
Оценив по достоинству основные функции тромбоцитов, можно понять, чем чреват их дисбаланс в организме и какими могут быть негативные последствия.
Любой дисбаланс активности и количества тромбоцитов в медицине называется тромбоцитопатией.
- Снижение концентрации тромбоцитарных пластин называют тромбоцитопенией.
- А повышенную концентрацию – тромбоцитозом.
- Нарушение функции их активности диагностируют, как тромбостению.
Как определяют их уровень
Сразу отметим, что, как такового, отдельного анализа на определение тромбоцитарных пластин – нет.
Оценку их функций и состояние проводят в комплексе с общим анализом клиники крови, отображая результат аббревиатурой – PLT (обязательный показатель) и измерением тромбокрита – РСТ (уровня их концентрации в общем объеме крови).
При данном анализе не учитывается соотношение возрастных групп и форм тромбоцитов (раздражения и дегенерации).
Более детальный анализ тромбоцитарных свойств определяется при определенных состояниях (перед операцией, при кровотечениях и пр.критических состояниях) методом гемостазиограммы (коагулограммы) с использованием скрининговых тестов, определяющих состоятельность процесса гемостаза.
Норма тромбоцитов в крови у женщин, детей и мужчин
Референсный, средний уровень тромбоцитарных пластин в анализе клиники крови зависит от возраста пациента.
Для анализа на тромбоциты забор капиллярной или венозной крови берется на пустой желудок. Концентрация отображается в единицах тыс/мкл.
Концентрация отображается в единицах тыс/мкл.
Приведем примеры нормальной концентрации тромбоцитарных «клеток» для различных возрастных групп пациентов, согласно европейским стандартам.
Для детей:
Для женщин:
В период менструальных кровотечений, снижение в крови концентрации тромбоцитарных пластин считается нормальным явлением.
Сниженный уровень тромбоцитов – частое явление при беременности, что обусловлено увеличением общего объема крови при отсутствии полноценного питания беременной женщины. Во всех иных случаях, сниженная норма, это весомый повод для обращения за врачебной помощью.
Допустимые значения для мужчин варьируются от 200 до 400 тыс. ед/мкл.
Данные исследования позволяют вовремя выявить процессы воспаления в организме, различные формы гематологических заболеваний, нарушения в процессе кроветворения, аллергические реакции и провести оценку состоятельности иммунитета.
Любое проявление дисбаланса тромбоцитов в биоматериале может спровоцировать тромбообразование, либо увеличить риски развития кровотечений.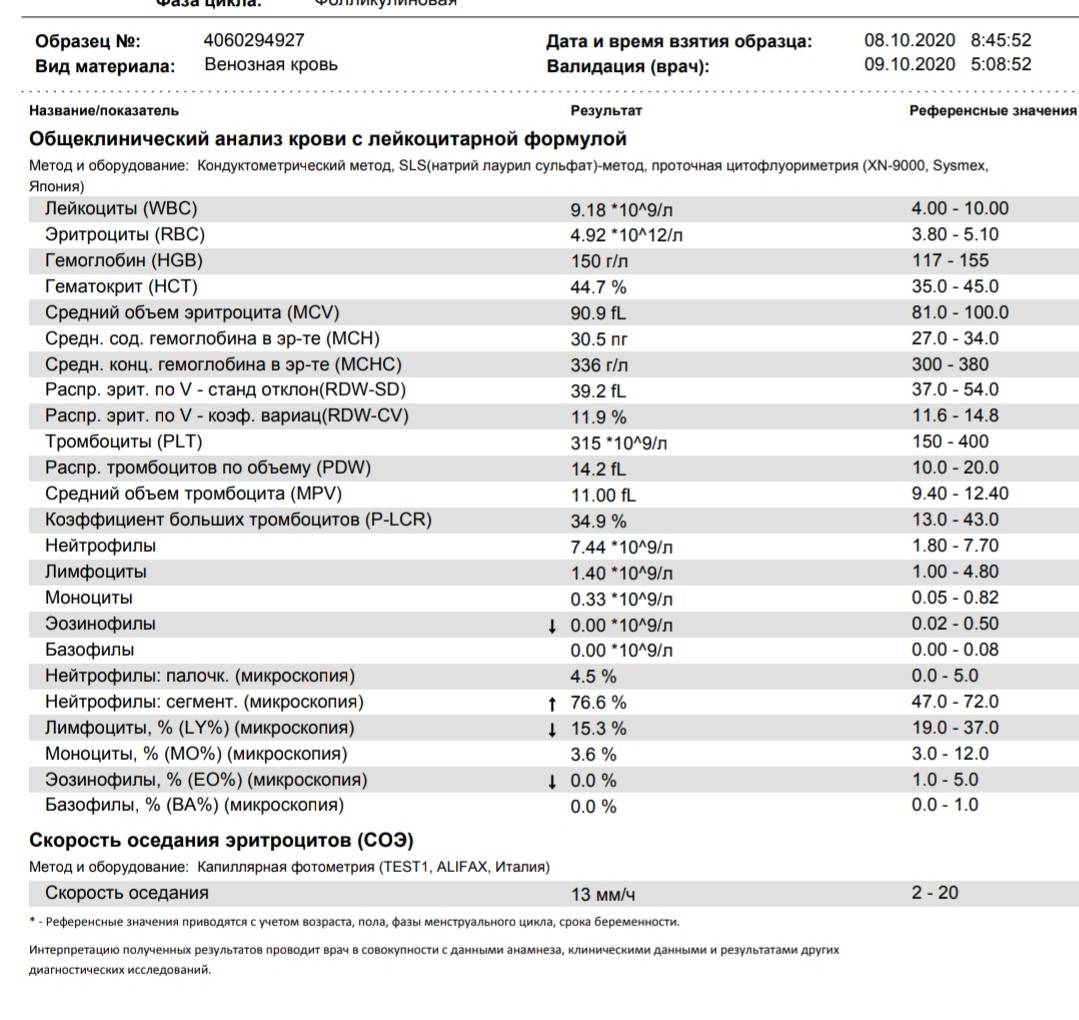
О чем говорят повышенные тромбоциты
Увеличение концентрации бляшек Биццоцеро может предупредить о наличии в организме различных патологических процессов – развитии туберкулезной инфекции, рака крови (лейкозе), онкологических заболеваний различных органов, лимфоме Ходжкина.
Тромбоцитоз (повышение тромбоцитов) – неизменный спутник:
- эритроцитоза;
- воспалительных кишечных и суставных патологий;
- хронической формы миелолейкоза;
- острого течения инфекционных заболеваний;
- внутрисосудистого гемолиза и анемии .
К увеличению количества тромбоцитов приводят сильные стрессы, общая интоксикация организма и кровопотери, что в конечном итоге может привести к развитию тромбоцитамии и несостоятельности функций стволовых клеток в костном мозге.
Как ни странно, но значительные кровопотери не снижают концентрацию тромбоцитарных пластин, а наоборот – увеличивают. Что обусловлено наличием компенсированных свойств организма, способного восполнять потери тромбоцитов.
Что обусловлено наличием компенсированных свойств организма, способного восполнять потери тромбоцитов.
Не важно по каким причинам тромбоциты выходят за границы нормативных значений. При такой ситуации необходима врачебная оценка с проведением соответствующей терапии.
Причины пониженных тромбоцитов
Снижение уровня тромбоцитарных пластин провоцирует множество факторов.
Тромбоцитопению диагностируют при:
- самовольном и не правильном приеме медикаментозных препаратов;
- наличии различных форм патологии печени и щитовидной железы;
- развитии анемии мегалобластного характера либо лейкемии;
- алкогольной зависимости и иных заболеваниях.
Тромбоцитопению способны спровоцировать кровотечения из носа и десен (гингивит), кровопотери при затяжных менструациях, даже небольшие порезы либо манипуляции по экстракции зубов (удаление).
При тромбоцитопении снижается эластичность сосудистых стенок, что вызывает их повышенную хрупкость. Снижение уровня тромбоцитарных пластин в крови лечится фармакологическими средствами либо переливанием тромбоцитарных масс.
Снижение уровня тромбоцитарных пластин в крови лечится фармакологическими средствами либо переливанием тромбоцитарных масс.
При обнаружении дисбаланса тромбоцитов в крови, необходима консультация гематолога. Самолечение недопустимо, так как неверное определение причинного фактора способно обернуться непредвиденными последствиями – вызвать процессы внутреннего кровоизлияния.
Автор статьи: детский врач-хирург Ситченко Виктория Михайловна
Удачи вам! До скорых встреч на страницах блога KtoNaNovenkogo.ru
Эта статья относится к рубрикам:
таблица, причины повышенныя, как понизить plt
Тромбоциты являются важной составляющей крови, которая отвечает за коагуляцию при ранениях. Норма тромбоцитов в крови у женщин должна соответствовать таблицам состава крови.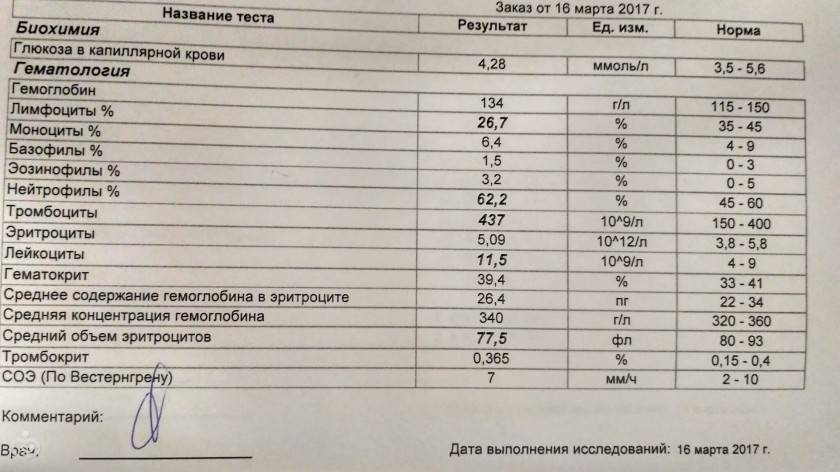 При любых отклонениях в этом показателе в организме женщины могут начать развиваться различные опасные патологии, которые на поздних стадиях трудно поддаются лечению. В каком возрасте особенно важно контролировать количество тромбоцитов у женщин, и какие симптомы могут указать на отклонение от нормальных показателей?
При любых отклонениях в этом показателе в организме женщины могут начать развиваться различные опасные патологии, которые на поздних стадиях трудно поддаются лечению. В каком возрасте особенно важно контролировать количество тромбоцитов у женщин, и какие симптомы могут указать на отклонение от нормальных показателей?
Анализ на тромбоциты
Первым анализом на определение количества тромбоцитов является общее исследование крови. Для него пациенту необходимо сдать кровь из пальца. При обнаружении отклонений женщине нужно сдать дополнительный анализ — коагулограмму. Для этого исследования нужно уже венозная кровь. Это исследование дает врачам более точную картину состояния женщины и определяет соотношение всех компонентов крови относительно друг друга.
Сегодня врачи используют определение уровня тромбоцитов по Фонио. Этот анализ подразумевает забор капиллярной крови. После сдачи анализа, кровь смешивают с реактивом и при помощи увеличителя определяют количественное содержание этих клеток в крови. Расшифровкой анализа должен заниматься только профессиональный врач. Сегодня таблица показателей данного анализа включает в себя следующие пункты:
Расшифровкой анализа должен заниматься только профессиональный врач. Сегодня таблица показателей данного анализа включает в себя следующие пункты:
- PLT в крови — количественный уровень тромбоцитов. Норма plt зависит от возрастной категории и пола пациента.
- MPV — средний объем тромбоцитов.
- PDW — область распространения тромбоцитов.
- PCT — уровень тромбокрита.
Какая норма тромбоцитов в крови у женщин? Показатели этих кровяных телец в женском организме могут меняться в зависимости от возраста пациентки. Также на уровень тромбоцитов может влиять вынашивание ребенка или менструация. Для каждой пациентки врач определяет норму индивидуально, с учетом всех факторов, которые могут повлиять на результаты анализа. Средние нормальные показатели для женщин составляют:
| Возраст | Средние нормы |
|---|---|
| Девушки от 15 до 18 лет | 180-350 тыс./мкл. |
| Женщины после 18 лет | 180-320 тыс.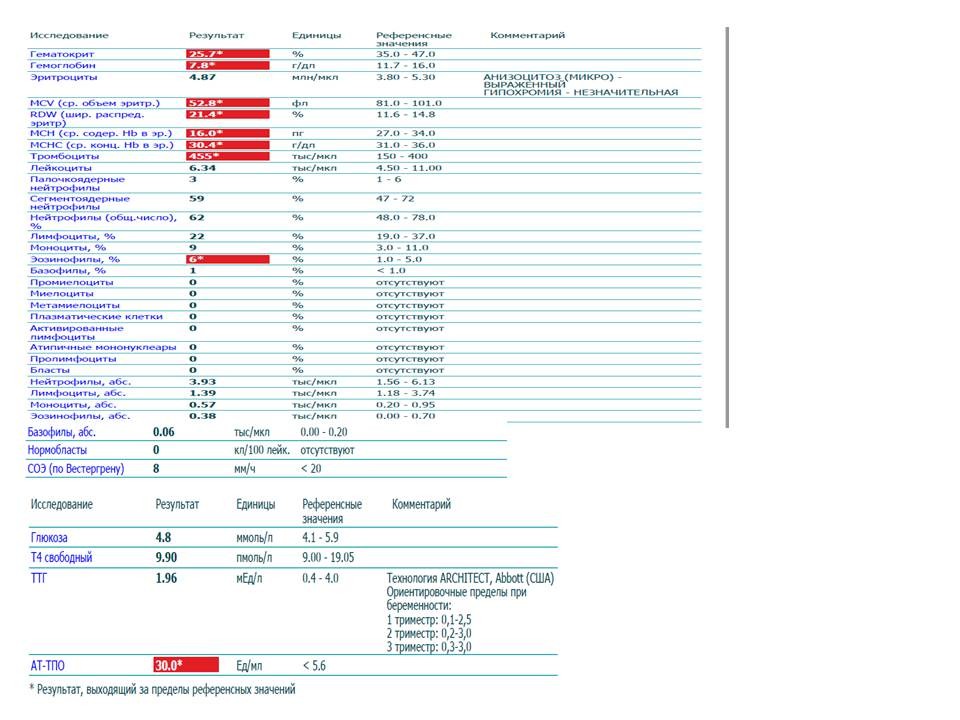 /мкл. /мкл. |
| Беременные женщины | 150-320 тыс./мкл. |
Уровень тромбоцитов в крови – показатель относительно стабильный. Продолжительность существования этой клетки составляет от 7 до 10 дней. После этого срока тромбоцит разрушается и утилизируется. На его место приходят новые клетки. Если процесс утилизации нарушен, возникает накопление тромбоцитов в крови, что может привести к образованию тромбов. Норма у женщин по возрасту может незначительно колебаться. Какая должна быть норма именно у вас, должен рассчитать врач с учетом всех сторонних факторов.
Если же нарушается процесс выработки этих клеток, наблюдается их недостаток в крови у женщины, что ведет к возникновению внутренних кровотечений и нарушению свертываемости крови. Оба этих отклонения могут спровоцировать развитие опасных патологических состояний. Помимо этого наличие отклонений в анализе может свидетельствовать об уже имеющемся заболевании, которое стало причиной нарушения.
Когда нужно сдать анализ
Тромбоциты нормы для женщин нужно проверять в следующих случаях:
- Заболевания печени.

- Болезни ССС.
- Перенесенный инфаркт.
- Перенесенный инсульт.
- Перед терапией антикоагулянтами.
- Менопауза.
Контролировать показатели тромбоцитов нужно всем женщинам после 30 лет один раз в год. Женщины после 40 лет должны сдавать этот анализ не реже 2 раз в год. Также важно контролировать уровень после 60 лет, когда уровень может значительно повышаться и есть большой риск развития инфарктов и инсультов. Особую важность контроль тромбоцитов имеет при беременности.
О чем свидетельствует повышение показателей
Повышенные тромбоциты в крови у женщин вызывают такое заболевание как тромбоцитоз. При этом показатель превышает 320 тыс./мкл. Тромбоциты выше нормы могут быть следствием следующих заболеваний:
- Онкологические заболевания.
- Воспалительные заболевания в хронической форме.
- Анемия.
- Травмы с кровопотерей.
Помимо этого повышены тромбоциты в крови могут быть в послеоперационном периоде, при лечении определенными группами лекарственных препаратов, после родов, при обильных менструациях и т. д.
д.
Тромбоцитоз может иметь как первичную, так и вторичную форму. Первичная форма возникает на фоне нарушения работы костного мозга. Именно там формируются тромбоциты, после чего попадают в кровь. При данной патологии высокий уровень тромбоцитов наблюдается не только в крови, но и в печени, а также в селезенке.
Обычно эта патология развивается в пожилом возрасте.
Вторичный тромбоцитоз развивается при хронических заболеваниях воспалительного или онкологического характера. Эта патология может возникать, не зависимо от возраста пациентки. Лечение вторичной формы заключается в устранении основного заболевания.
Для того чтобы снизить уровень тромбоцитов в крови врачи рекомендуют прием антикоагулянтов. Эта терапия должна проводиться под четким контролем лечащего врача, ведь неадекватное лечение может привести к нарушению уровня в обратную сторону. Помимо лекарств пациентке может быть назначена корректировка питания. Благоприятно влияют на снижение уровня тромбоцитов следующие продукты:
- Натуральные соки или чистая не газированная вода 2л.
 в сутки.
в сутки. - Зеленые и листовые овощи.
- Фрукты зеленого цвета.
- Имбирь.
- Свежие или свежемороженые ягоды.
Если тромбоциты в крови повышены, важно отказаться от жирной и жареной пищи, которая вызывает их превышение. Готовить еду лучше на пару или методом запекания. Также следует следить за жирностью молочных продуктов. По возможности таким пациенткам рекомендуется исключить любой повышающий тромбоциты продукт питания. Правильное питание с юности позволит избежать проблем в будущем. Каждая девушка должна следить за своим рационом. Это позволит не только избежать многих заболеваний, но и подарит красоту и стройную фигуру без необходимости диет и косметических процедур.
О чем свидетельствует понижение уровня
Пониженное содержание тромбоцитов в крови может нести в себе опасность внутренних кровотечений и большую потерю крови при травмах или хирургическом вмешательстве. В этом случае значительно снижается свертываемость крови, которая просто не останавливается от любого повреждения сосудов.
Пониженные тромбоциты в крови могут свидетельствовать о наличии следующих заболеваний:
- Лейкоз.
- Цирроз печени.
- Патологии селезенки.
- Онкология костного мозга.
- Заболевания инфекционного характера.
- Гепатит.
- Вирусные заболевания.
- Интоксикация.
При тромбоцитопении важно своевременно выявить причины отклонения, особенно если показатели в анализе крови значительно ниже нормы. Заподозрить, что у вас понижены тромбоциты, можно при появлении следующих симптомов:
- Частые кровоизлияния из носа.
- Повышенная кровоточивость при чистке зубов.
- Менструации более 5-ти дней с большой кровопотерей.
- Мелкие кровоподтеки на теле в виде красных точек.
- Появление синяков при легком ушибе.
- Плохая свертываемость крови.
Все эти симптомы говорят о том, что у пациента, скорее всего низкий уровень тромбоцитов. Лечение данного отклонения невозможно без установки истинной причины нарушения.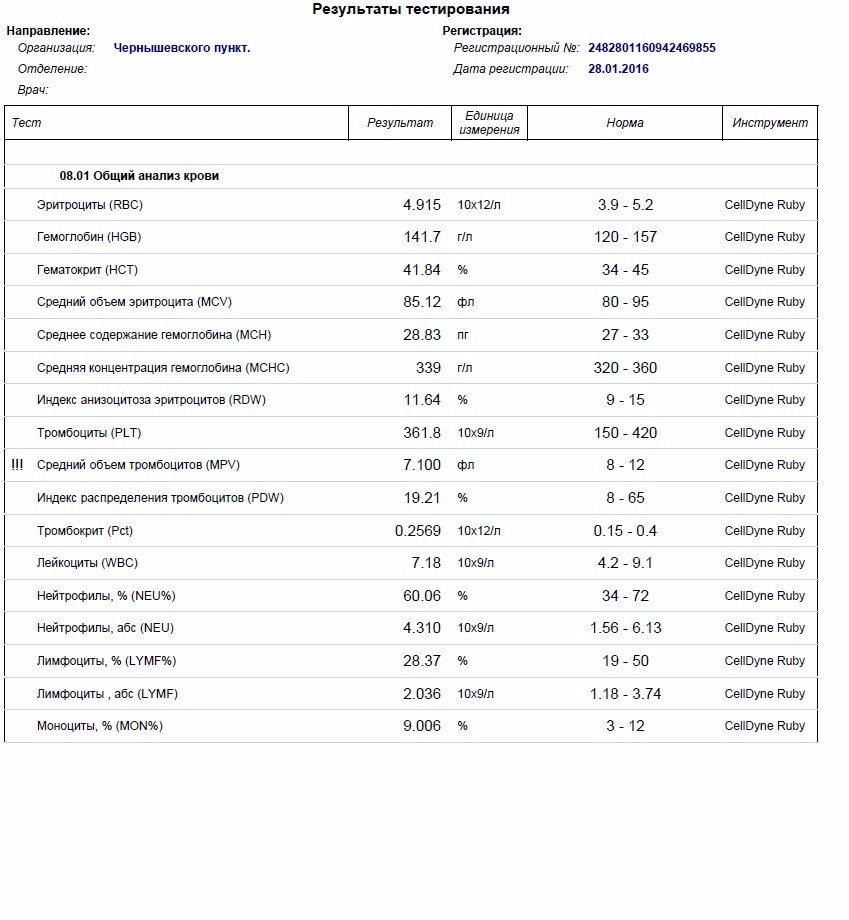 В отличие от случаев, когда тромбоциты повышены, и их можно снизить таблетками, для повышения уровня нет специфичных медикаментозных препаратов. При неэффективности лечения пациенту может быть рекомендовано удаление селезенки.
В отличие от случаев, когда тромбоциты повышены, и их можно снизить таблетками, для повышения уровня нет специфичных медикаментозных препаратов. При неэффективности лечения пациенту может быть рекомендовано удаление селезенки.
Профилактика нарушений
Для того чтобы поддерживать нормальный уровень тромбоцитов, важно вести здоровый образ жизни.
Нужно питаться полезной и разнообразной едой, заниматься спортом и чаще бывать на свежем воздухе.
Эти несложные правила помогут сохранить здоровья женщины на долгие годы. Также женский организм особенно нуждается в тщательном контроле. Ведь почему женщины чаще сталкиваются с тромбозом и тромбоцетопинией, чем мужчины? Все просто, женский организм в течение всей жизни испытывает колоссальные нагрузки. Это беременность, роды, грудное вскармливание и наконец, менопауза. Все эти гормональные перестройки истощают женское тело, и если не следить за своим здоровьем, можно заработать массу болезней.
Каждая женщина должна помнить, что только она сама может поддерживать свое здоровье и уберечь себя от различных патологий.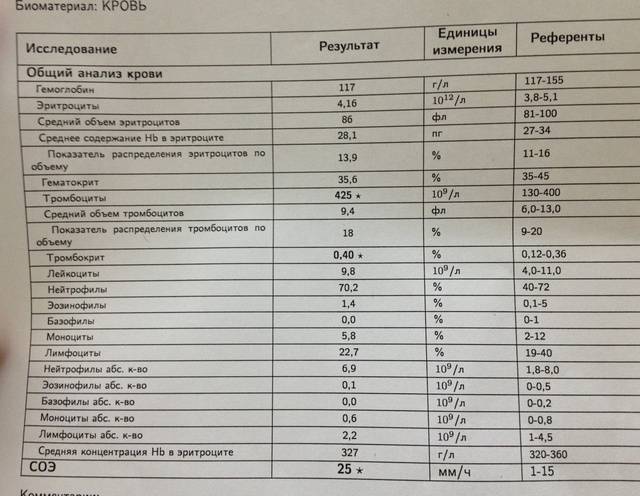 Для этого нужно просто 1 раз в год сдавать анализ крови и посещать нескольких специалистов для профилактического осмотра. В этом случае все недуги будут выявляться на ранних стадиях, когда их лечение не займет много времени и сил. Будьте здоровы и берегите себя!
Для этого нужно просто 1 раз в год сдавать анализ крови и посещать нескольких специалистов для профилактического осмотра. В этом случае все недуги будут выявляться на ранних стадиях, когда их лечение не займет много времени и сил. Будьте здоровы и берегите себя!
Вконтакте
Google+
Одноклассники
Диагностический центр МЕДЛАЙФ-БИО
Общий анализ крови – набор тестов, направленных на определение количества различных клеток крови (эритроцитов, лейкоцитов, тромбоцитов), их характеристик и соотношения. Общий анализ крови – наиболее часто назначаемый вид лабораторных исследований. Данный тест применяют как для общей оценки состояния здоровья при плановых обследованиях, перед хирургическими вмешательствами, а также для диагностики, определения возможной причины, и оценки эффективности лечения анемий (малокровия), инфекций и воспалительных процессов, нарушений свертывания крови, лейкозов (лейкемий), аллергии.Поводом для обращения к врачу и назначения общего анализа крови могут стать следующие симптомы:
— слабость, быстрая утомляемость, одышка при незначительной или умеренной нагрузке, сердцебиения, головная боль, шум в ушах, нарушения сна, аппетита, полового влечения – признаки анемии;
— боль в пораженном органе, покраснение и припухлось кожи, повышение температуры тела, ознобы, головная боль, ломота в суставах, снижение аппетита – признаки инфекционных и воспалительных процессов;
— закупорка кровеносных сосудов и, наоборот, повышенная кровоточивость – признаки нарушения свертывания крови;
— анемия, повышенная кровоточивость, и инфекционные осложнения – могут иметь место при лейкозах;
— приступы удушья, насморк, воспаление глаз, покраснение и отек кожи, расстройство желудка – признаки аллергии.
Учитывая высокую ценность общего анализа крови для диагностики широкого перечня заболеваний, его результаты должны удовлетворять высоким требованиям надежности. Следует отметить, что исследования крови, выполняемые «ручными» методами, имеют большие погрешности, и часто вызывают обоснованные нарекания, как врачей, так и пациентов. Именно с точки зрения надежности полученных результатов, автоматизированные гематологические анализаторы обладают рядом преимуществ перед «ручным» исследованием.
Главные из них:
— анализ большого количества клеток: более 10 тысяч, по сравнению с 100-200 клетками при визуальном способе подсчета,
— стандартизация каждого этапа анализа,
— минимизация «человеческого фактора».
Большинство функционирующих в лабораториях Украины гематологических анализаторов определяют до 18 параметров общего анализа крови, и не способны выполнять полный анализ лейкоцитарной формулы. В диагностическом центре «Глобал-Диагностик» общий анализ крови выполняется с помощью сложной аналитической системы Sysmex ХS-1000i (Япония), которая определяет 24 параметра общего анализа крови, и позволяет получить целый ряд дополнительных характеристик клеток, которые невозможно оценить при визуальном анализе мазка крови. Анализатор Sysmex ХS-1000i не только выполняет развернутый анализ крови с дифференцировкой лейкоцитов на 5 подтипов, но и строит графики распределения лейкоцитов, эритроцитов и тромбоцитов по размерам. Анализ этих графиков позволяет получить дополнительную диагностически ценную информацию.
Уникальной особенностью данного анализатора является возможность обнаружения незрелых лейкоцитов, бластов, атипичных и патологических лимфоцитов. Присутствие даже 1% таких клеток в образце может быть признаком серьезной патологии, между тем, когда в мазке анализируется только 100 клеток, их можно «пропустить».
Анализатор Sysmex ХS-1000i не только выполняет развернутый анализ крови с дифференцировкой лейкоцитов на 5 подтипов, но и строит графики распределения лейкоцитов, эритроцитов и тромбоцитов по размерам. Анализ этих графиков позволяет получить дополнительную диагностически ценную информацию.
Уникальной особенностью данного анализатора является возможность обнаружения незрелых лейкоцитов, бластов, атипичных и патологических лимфоцитов. Присутствие даже 1% таких клеток в образце может быть признаком серьезной патологии, между тем, когда в мазке анализируется только 100 клеток, их можно «пропустить».
Однако роль врача-лаборанта в выполнении данного исследования также очень важна. О любых отклонениях от нормы, а также находках, требующих дополнительных исследований, анализатор «выдает» специальное сообщение, и эти образцы затем аналируются «визуально» квалифицированным специалистом для подтверждения и уточнения патологических находок.
Для анализа может использоваться как венозная, так и капиллярная кровь.
Клинико-диагностическое значение показателей общего анализа крови
Гематокрит (HCT) – процентное соотношение клеток крови (форменных элементов) к жидкой ее части; используется в комплексной оценке анемий и состояний, при которых количество форменных элементов, наоборот, увеличивается (эритроцитозы, лейкемии), помогает принять решение о необходимости переливания крови и оценить результаты этой процедуры.
Гемоглобин (HGB) – основной компонент эритроцитов, с помощью которого они транспортируют кислород от легких к тканям и органам, а углекислый газ – от тканей и органов к легким. Концентрация гемоглобина в крови – важный показатель для оценки тяжести анемии или эритроцитоза и для контроля за эффективностью терапии этих состояний.
Эритроциты (RBC) – клетки, содержащие гемоглобин и транспортирующие кислород и углексилый газ в крови человека. Определение количества эритроцитов необходимо для диагностики анемии или эритроцитоза и дифференцировки между различными типами анемий.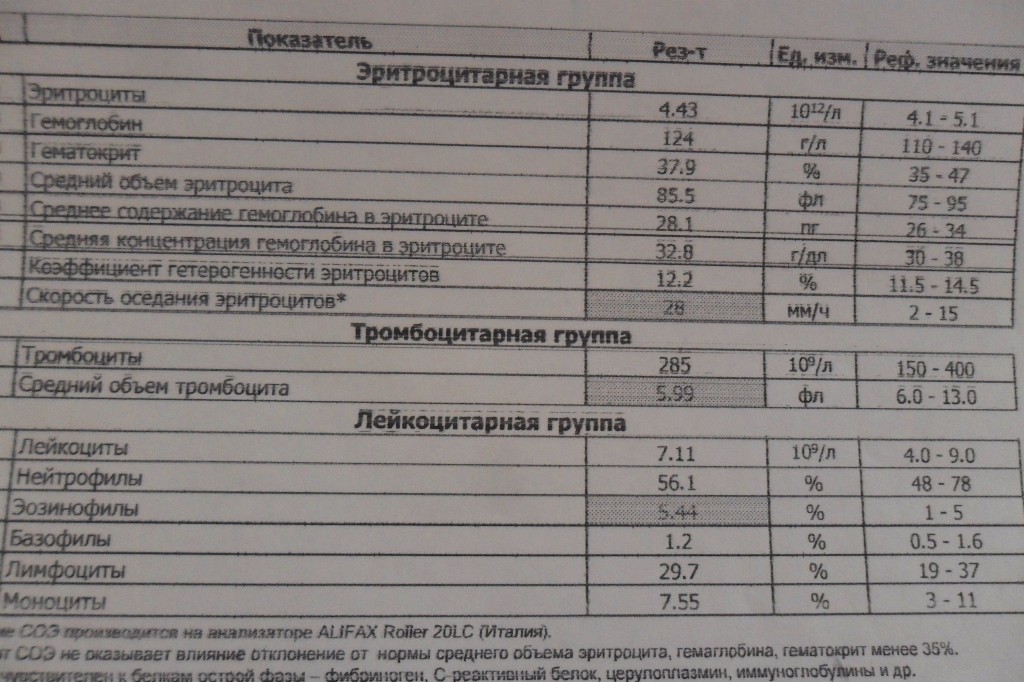
Эритроцитарные индексы: предоставляют информацию о размерах эритроцитов и содержании в них гемоглобина.
• средний объем эритроцита (MCV) – характеризует размер этих клеток; он необходим для определения причины анемии. Так, например, при дефиците витамина B12 размер эритроцитов увеличивается, при дефиците железа – уменьшается.
• среднее содержание гемоглобина в эритроците (MCH) и средняя концентрация гемоглобина в эритроците (MCHC) дополняют друг друга и используются вместо устаревшего и менее информативного цветового показателя. Эти индексы позволяют определить причину анемии. Так, например, при дефиците витамина B12 в увеличенных эритроцитах содержание и концентрция гемоглобина повышены, а при дефиците железа – снижены.
• ширина распределения эритроцитов по объёму (RDW) – показатель, определяющий степень различия эритроцитов пациента по размеру. Имеет значение в ранней диагностике анемий, поскольку часто меняется раньше, чем размер эритроцитов.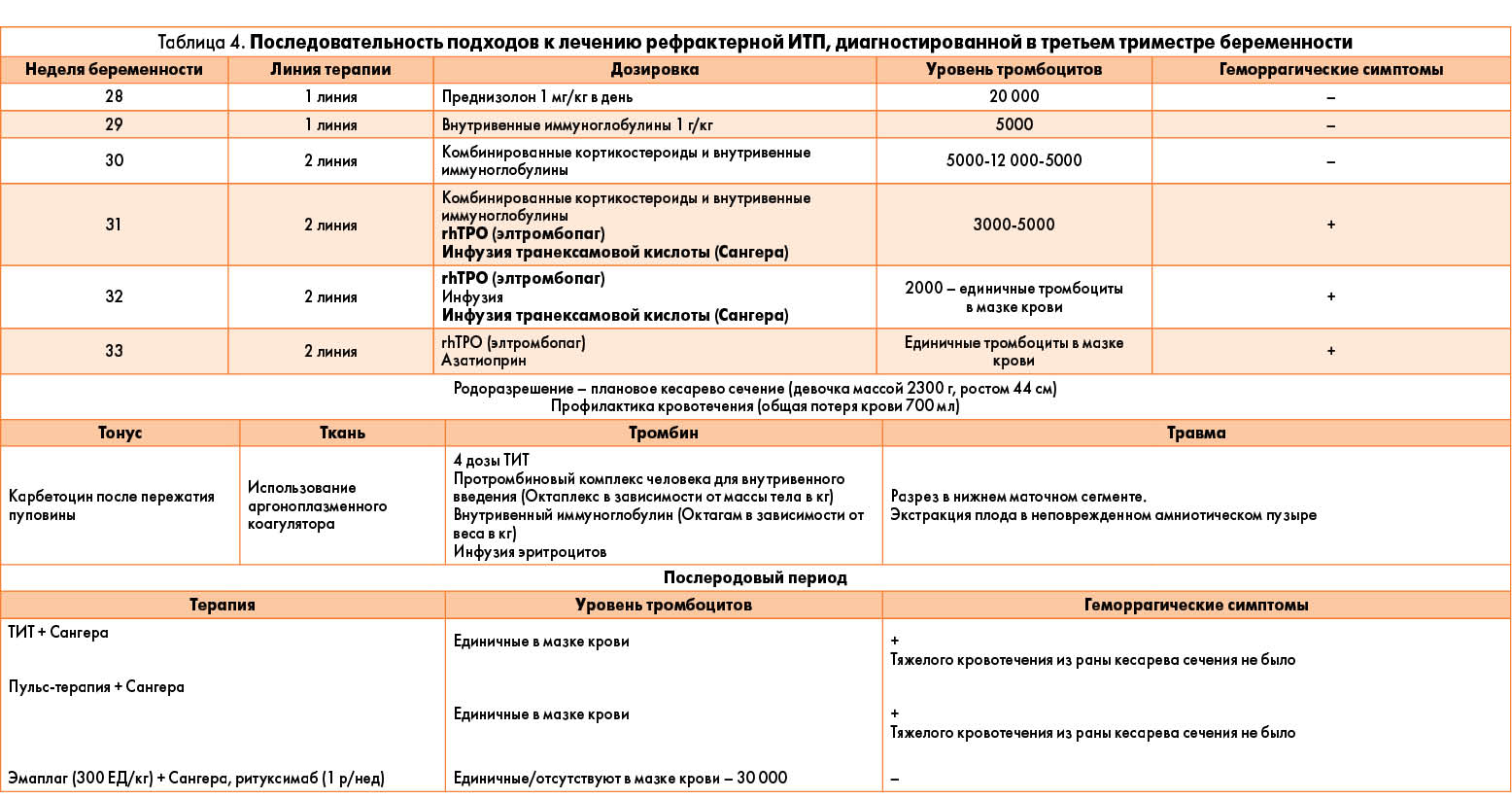 Позволяет оценить эффективность лечения анемии.
Позволяет оценить эффективность лечения анемии.
Лейкоциты (WBC) – группа клеток, главная задача которых – обнаруживать чужеродные агенты (бактерии, вирусы) в организме и уничтожать их. Определение количества лейкоцитов необходимо для диагностики инфекций, повреждения тканей организма, злокачественных опухолей, заболеваний костного мозга.
Лейкоцитарная формула – относительное (%) и абсолютное количество лейкоцитов разных видов: нейтрофилов, лимфоцитов, моноцитов, эозинофилов, базофилов. Если подсчет общего количества лейкоцитов позволяет узнать суммарное количество этих клеток, то лейкоцитарная формула – количество клеток каждого типа в отдельности. Эта информация имеет огромное значение для диагностики заболеваний, поскольку каждый тип лейкоцитов выполняет специфическую функцию.
Нейтрофилы – наиболее многочисленные из лейкоцитов – первыми начинают бороться с возбудителями бактериальных и грибковых инфекций и первыми появляются в месте повреждения тканей (инфаркты органов, ожоги, травмы, операции)./123/123.jpg) Увеличение количества нейтрофилов – один из основных лабораторных признаков любого нагноительного процесса. Снижение количества нейтрофилов может указывать на первичное поражение костного мозга или его истощение, и является неблагоприятным прогностическим признаком, так как повышает риск развития инфекции.
Увеличение количества нейтрофилов – один из основных лабораторных признаков любого нагноительного процесса. Снижение количества нейтрофилов может указывать на первичное поражение костного мозга или его истощение, и является неблагоприятным прогностическим признаком, так как повышает риск развития инфекции.
При многих тяжёлых инфекциях, септических и гнойных процессах, злокачественных опухолях, заболеваниях костного мозга лейкоцитарная формула изменяется за счёт увеличения процентного содержания молодых форм нейтрофилов: палочкоядерных, метамиелоцитов, миелоцитов и промиелоцитов. Такое изменение лейкоцитарной формулы называется сдвиг влево. Анализатор Sysmex ХS-1000i автоматически определяет наличие и подсчитывает даже самое незначительное (менее 0,5%) количество этих незрелых форм нейтрофилов.
Эозинофилы – обеспечивает защиту организма от паразитов, а также принимают активное участие в аллергических реакциях. Поэтому пристутвие в организме паразитов или такие аллергические заболевания как ринит, коньюнктивит, астма, экзема сопровождаются повышением количества эозинофилов в крови.
Базофилы – в норме участвуют в регуляции проницаемости сосудистой стенки, а при патологии – в развитии аллергических реакций немедленного типа, воспалительных процессах. Поэтому при аллергии на пищу или лекарственные прапараты количество этих клеток в крови может увеличиваться. Также увеличение количества базофилов может указывать на заболевания костного мозга.
Лимфоциты – главные клетки иммунной системы, их основная функция состоит в распознавании опасных для организма молекул (антигенов) и специфическом ответе на них. В результате адекватного ответа на антигенную стимуляцию происходит увеличение количества лимфоцитов, при неадекватном ответе количество лимфоцитов может снижаться. Лимфоциты активно участвуют в развитии иммунодефицитных состояний, инфекционных, аллергических, онкологических заболеваний, отторжения трансплантированных органов, а также аутоиммунных процессов. При перечисленных процессах количество лимфоцитов в крови может существенно меняться.
Моноциты – клетки, участвующие в защитных реакциях организма.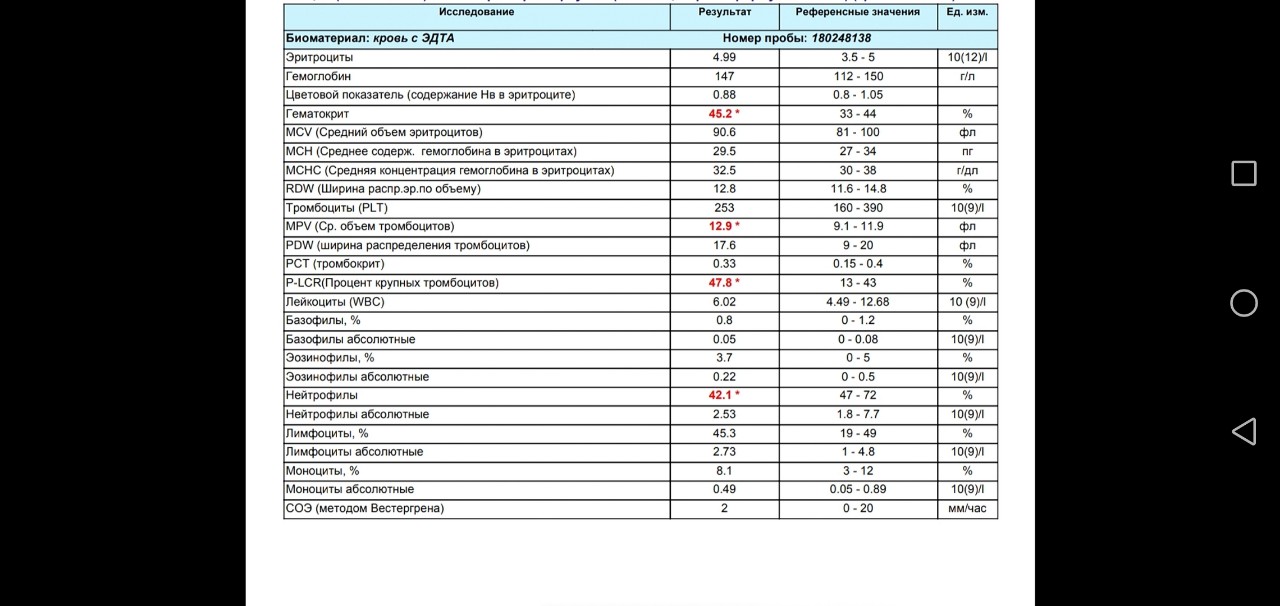 Они удаляют из организма путем поглощения (фагоцитоза) отмирающие клетки и бактерии. Увеличение количества моноцитов в крови может быть следствием заболеваний костного мозга или антигенного раздражения.
Они удаляют из организма путем поглощения (фагоцитоза) отмирающие клетки и бактерии. Увеличение количества моноцитов в крови может быть следствием заболеваний костного мозга или антигенного раздражения.
Тромбоциты – клетки, играющие важную роль в свертывании крови. Если у человека снижено количество тромбоцитов, риск кровотечения и образования синяков у него повышен.
Количество тромбоцитов (PLT) – зачастую определяет вероятность развития тромбоза или кровоточивости. Причинами изменения количества тромбоцитов могут быть заболевания костного мозга, злокачественные опухоли, инфекции, воспалительные заболевания.
Тромбокрит (PCT) – доля объема цельной крови, занимаемая тромбоцитами.
Тромбоцитарные индексы
Средний объем тромбоцита (MPV) и процент крупных тромбоцитов (P-LCR) характеризуют размер этих клеток, свидетельствуют об их активности и скорости образования в костном мозге.
Ширина распределения тромбоцитов по объёму (PDW) – показатель, определяющий степень различия тромбоцитов пациента по размеру, что может помочь определить причину изменения количества этих клеток.
Скорость оседания эритроцитов (СОЭ)
Данная методика измеряет скорость оседания эритроцитов на дно капилляра под действием силы тяжести. Склеивание эритроцитов ведет к образованию скоплений (агрегатов) этих клеток, вес которых значительно выше, чем отдельно взятого эритроцита, и которые поэтому оседают быстрее.
Величина СОЭ зависит от двух главных составляющих. Первая ? наличие и уровень в плазме белков-глобулинов, количество которых повышается при воспалительных процессах вследствие инфекции, а также при повреждениях тканей организма (инфаркт, ожог, и тд). Эти белки фиксируются на поверхности эритроцитов и стимулируют их склеивание друг с другом. Вторая составляющая – вязкость крови, которая, в первую очередь, зависит от количества самих эритроцитов (меньшее количество эритроцитов – выше СОЭ, и наоборот).
К сожалению, очень часто результаты определения СОЭ традиционным для нашей страны методом (Панченкова) не соответствует клинической картине.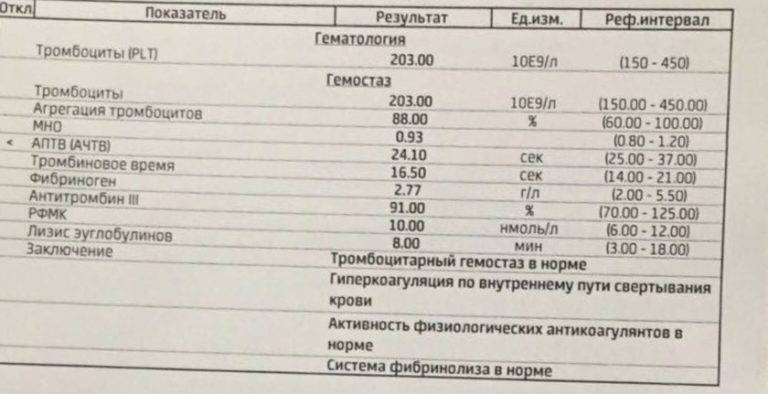 И это не удивительно, поскольку данный метод не поддается контролю качества и не может быть стандартизирован!
И это не удивительно, поскольку данный метод не поддается контролю качества и не может быть стандартизирован!
Прежде всего, новозможно стандартизировать процедуру получения капиллярной крови. Каждый, кто хотя бы пару раз сдавал кровь из пальца на анализ, согласится, что для получения достаточного количества крови лаборанту приходится чрезмерно сжимать место узкого прокола. В результате этого, во-первых, может разрушаться часть эритроцитов, а во-вторых, в образец крови попадает тканевая жидкость, богатая белками-глобулинами. Между тем, именно эти две составляющие и определяют величину СОЭ.
Кроме того, на величину СОЭ влияет целый ряд неспецифических факторов: качество капилляра, правильность разведения крови цитратом натрия перед проведением исследования, качество цитрата натрия.
Следует отметить, что в развитых странах для «ручного» определения СОЭ пользуются методом Вестергрена, который рекомендован Всемирной организацией здравоохранения. Отличия методов Вестергрена и Панченкова – в строении капилляра. Все методические документы Международного комитета по стандартизации в гематологии (ICSH) и Всемирного общества здравоохранения строго регламентируют, что внутренний диаметр капилляра должен составлять не менее 2,55 мм, однако внутренний диаметр капилляра Панченкова – только 1 мм. Если образуются крупные скопления эритроцитов, то при таком узком просвете, они могут блокировать свое собственное оседание. В результате скорость оседания эритроцитов искусственно снижается.
Все методические документы Международного комитета по стандартизации в гематологии (ICSH) и Всемирного общества здравоохранения строго регламентируют, что внутренний диаметр капилляра должен составлять не менее 2,55 мм, однако внутренний диаметр капилляра Панченкова – только 1 мм. Если образуются крупные скопления эритроцитов, то при таком узком просвете, они могут блокировать свое собственное оседание. В результате скорость оседания эритроцитов искусственно снижается.
Международные стандарты также регламентируют, что длина рабочей градуированной поверхности капилляра для определения СОЭ должна быть не менее 200 мм. Капилляр Панченкова имеет длину рабочей поверхности 100 мм, что резко ограничивает уровень максимальных значений СОЭ.
Однако метод Вестергрена не идеален, и также имеет целый ряд недостатков, которые затрудняют его эффективное применение, а именно:
1. Длительность получения результатов: 60 минут, в то время как остальные показатели общего анализа крови могут быть получены через 60 секунд.
2. Несмотря на стандартизацию, вариабельность результатов определения СОЭ сохраняется на высоком уровне – разница может достигать более 15%.
3. Когда лаборант одновременно работает с десятками образцов, очень трудно Затруднения при работе с сериями образцов. На загрузку каждого образца в штатив для определения СОЭ требуется около 30 секунд. Если необходимо загрузить 10 образцов для анализа СОЭ, то от постановки первого капилляра до последнего проходит в среднем 5 минут, следовательно, если последний капилляр мы будем оценивать через 60 минут, то первый через 65 минут после постановки. При этом, если учесть, что СОЭ между 60 и 66 минутами может изменяться на 10 мм, то результаты в первом капилляре будут ложно завышены.
4. Сложность стандартизации температурного режима выполнения измерения СОЭ. Согласно рекомендациям ICSH, анализ СОЭ должен проводиться при постоянной температуре с колебаниями не более 1оС. Это требование связано с тем, что изменение температуры на один градус по Цельсию приводит к изменению СОЭ на 3%.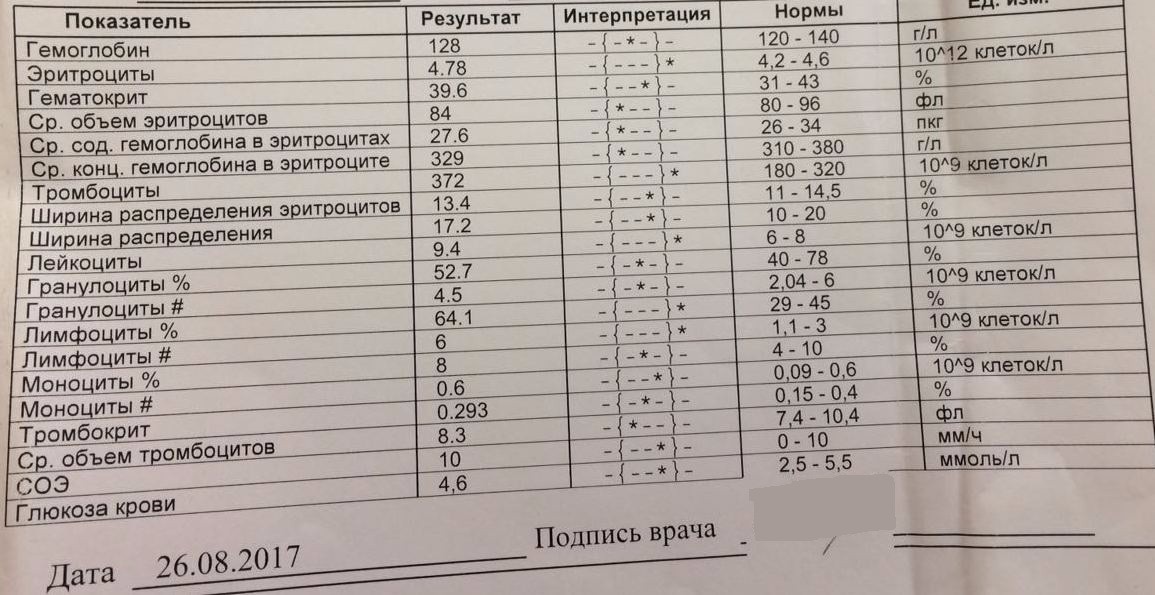
5. Классический метод Вестергрена практически не поддается автоматизации.
6. Одно из главных ограничений метода Вестергрена – невозможность включения данного метода в систему контроля качества, что делает результаты, полученные при помощи данного метода, ориентировочными и малодостоверными.
Наличие вышеперечисленных ограничений классического метода определения СОЭ по Вестергрену заставило научно-исследовательские лаборатории ведущих производителей в области лабораторного оборудования искать новые методы его определения, которые удовлетворяли бы всем методическим и клиническим потребностям современных лабораторий. Результатом разработок в этой области стали полностью автоматизированные аналитические системы измерения СОЭ типа Roller компании Alifax (Италия). Уникальный метод определения СОЭ, реализованный в данном приборе, позволил решить все проблемы, присущие классическому методу Вестергрена, при этом корреляция с референсным методом составляет 95–99%.
Согласно методологии референсного метода Вестергрена, результат оседания эритроцитов оценивается один раз через 60 минут после постановки, т.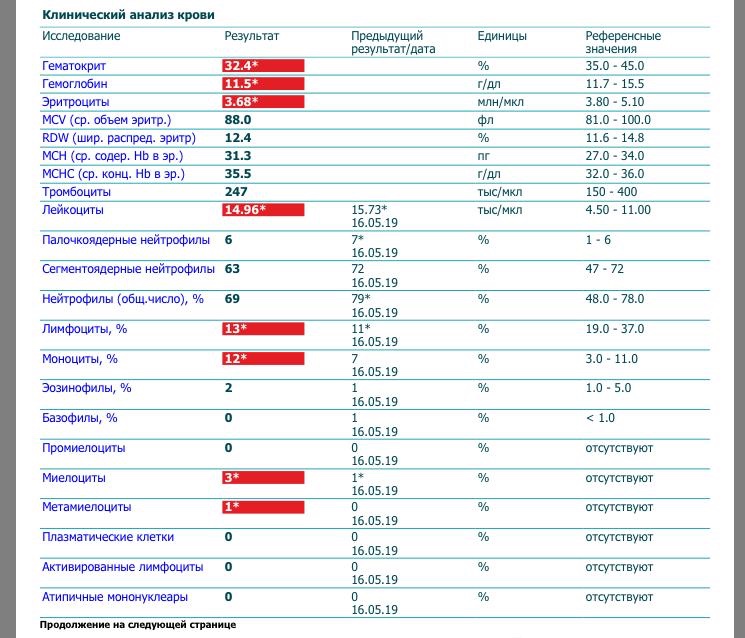 е. он оценивает не скорость оседания, а величину осаждения эритроцитов за 1 час. Принцип работы анализатора Roller основан на измерении кинетики агрегации эритроцитов, что достигается путем многократной оценки (1000 измерений) оптической плотности исследуемой пробы в специальном капилляре в течение 20 секунд. Это означает, что данные анализаторы действительно измеряют скорость процесса. Кроме того, анализаторы, предлагаемые компанией Alifax, оценивают самую специфическую фазу процесса оседания эритроцитов, а именно фазу агрегации.
е. он оценивает не скорость оседания, а величину осаждения эритроцитов за 1 час. Принцип работы анализатора Roller основан на измерении кинетики агрегации эритроцитов, что достигается путем многократной оценки (1000 измерений) оптической плотности исследуемой пробы в специальном капилляре в течение 20 секунд. Это означает, что данные анализаторы действительно измеряют скорость процесса. Кроме того, анализаторы, предлагаемые компанией Alifax, оценивают самую специфическую фазу процесса оседания эритроцитов, а именно фазу агрегации.
Внедрение в практику автоматических анализаторов СОЭ позволило элиминировать ограничения, связанные с классическим методом Вестергрена, а именно:
1. Время проведения одного исследования СОЭ составляет 20 секунд, что позволяет в течение 1 минуты получать полный общий анализ крови, включающий результаты подсчета клеток крови, дифференцировку формулы и СОЭ.
2. В качестве биологического материала для исследования СОЭ в анализаторе Roller используется цельная кровь с ЭДТА, что дает возможность определять СОЭ и выполнять автоматический гематологический анализ из одной пробирки.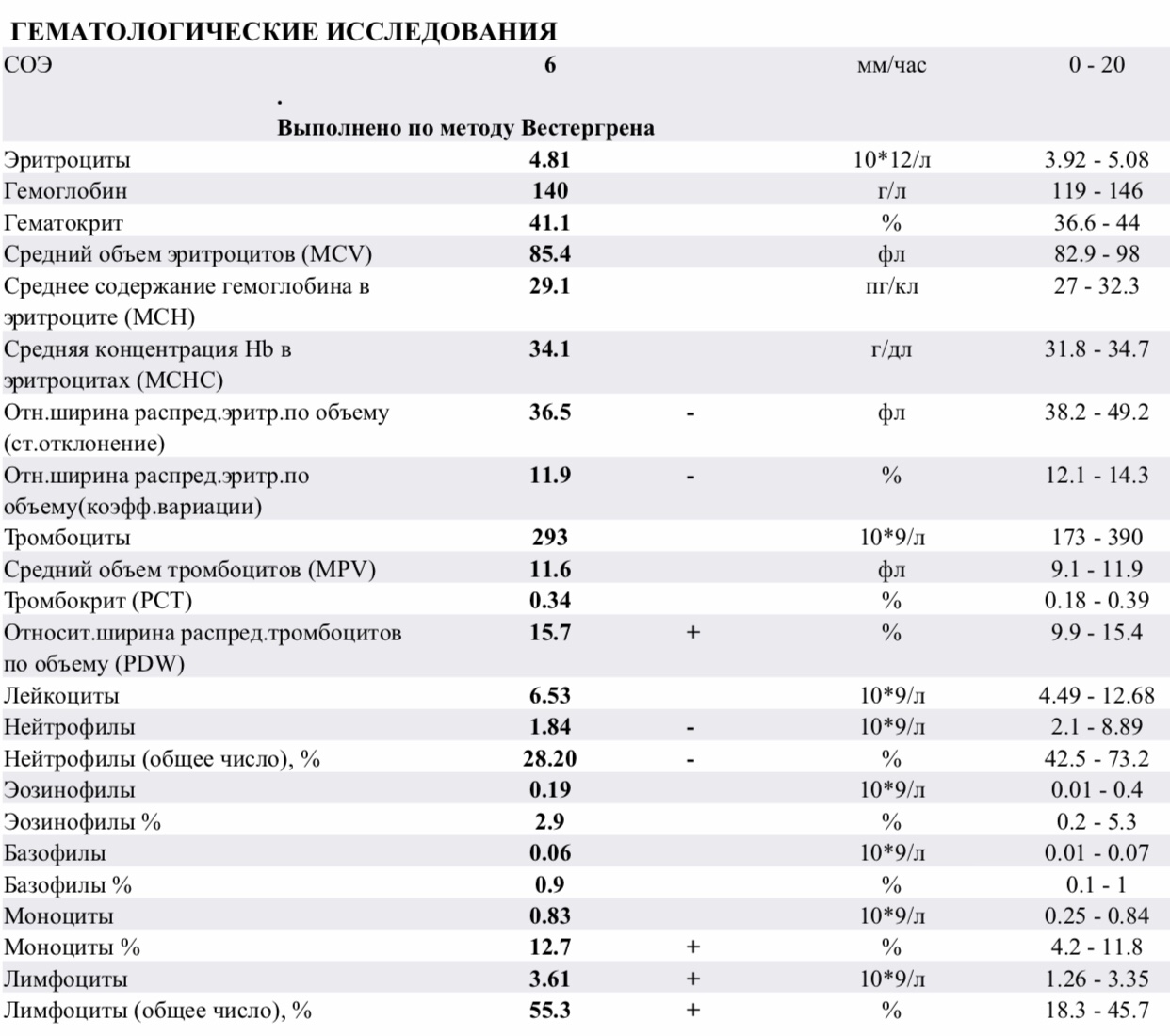 При этом исключается необходимость собирать кровь отдельно с цитратом натрия, а это значительно упрощает процесс сбора крови, уменьшает затраты (нет необходимости использовать специальные вакуумные пробирки с цитратом натрия) и элиминирует дополнительный источник ошибок, связанный с разведением крови и качеством цитрата натрия (в случае, если специальные пробирки не применяются).
3. Анализаторы Alifax не чувствительны к влиянию таких свойств образца как высокий/низкий гематокрит MCV, а также к колебаниям температуры окружающей среды.
При этом исключается необходимость собирать кровь отдельно с цитратом натрия, а это значительно упрощает процесс сбора крови, уменьшает затраты (нет необходимости использовать специальные вакуумные пробирки с цитратом натрия) и элиминирует дополнительный источник ошибок, связанный с разведением крови и качеством цитрата натрия (в случае, если специальные пробирки не применяются).
3. Анализаторы Alifax не чувствительны к влиянию таких свойств образца как высокий/низкий гематокрит MCV, а также к колебаниям температуры окружающей среды.
Одним из главных преимуществ анализаторов СОЭ, которые предлагает компания Alifax, является возможность включения исследований СОЭ в систему контроля качества. Разработаны специальные трехуровневые контрольные материалы, которые позволяют проводить контроль качества определения СОЭ на анализаторе и Roller согласно всем стандартам.
До настоящего времени накоплено достаточное количество материала для того, чтобы сделать вывод о хорошей диагностической эффективности применения результатов определения СОЭ, полученных при помощи анализатора Roller.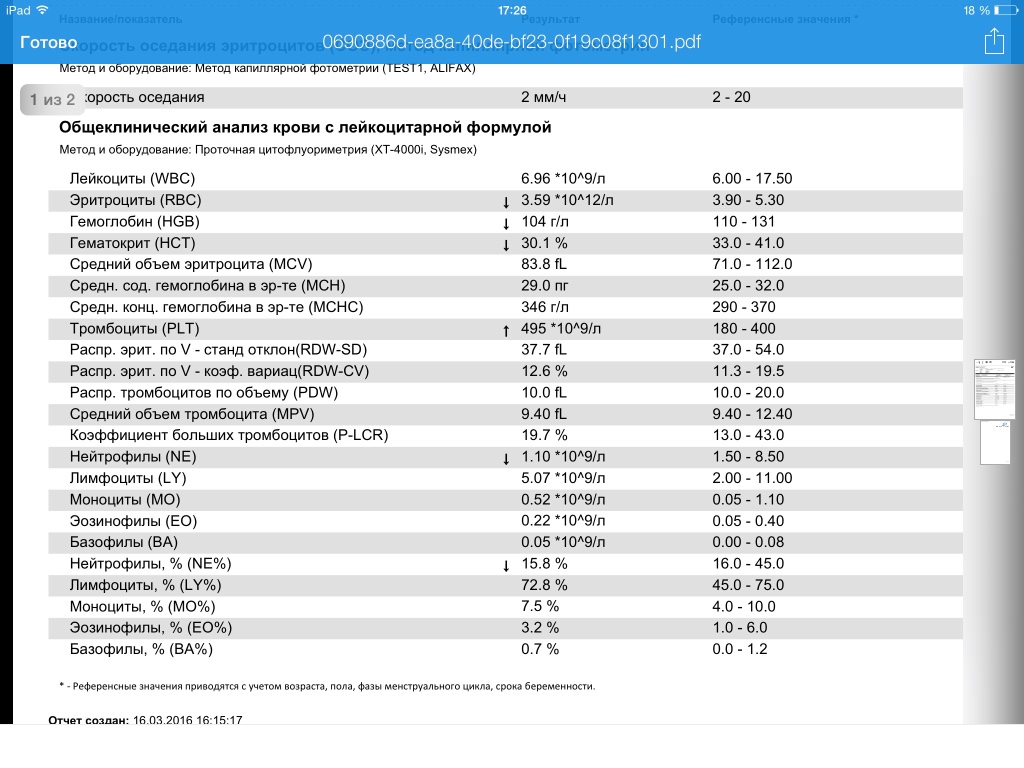 Некоторые публикации свидетельствуют о большей чувствительности результата измерения СОЭ, по сравнению с классическим методом Вестергрена, для оценки активного воспаления у пациентов онкологического профиля, а также пациентов с аутоиммунными заболеваниями и инфекциями.
Некоторые публикации свидетельствуют о большей чувствительности результата измерения СОЭ, по сравнению с классическим методом Вестергрена, для оценки активного воспаления у пациентов онкологического профиля, а также пациентов с аутоиммунными заболеваниями и инфекциями.
Диапазон клинического применения СОЭ: старые и новые возможности.
Известным фактом является зависимость значений СОЭ от возраста, пола, расы (табл. 8).
Таблица 8. Референсные значения СОЭ для различных клинических групп.
| Клиническая группа | Значения СОЭ,мм/час |
| Беременные[16] | |
| Первый триместр | 4 — 57 |
| Второй триместр | 7 — 47 |
| Третий триместр | 13 – 70 |
| Взрослые до 50 лет[17] | |
| Мужчины | |
| Женщины | |
| Взрослые > 50 лет [17] | |
| Мужчины | |
| Мужчины |
 Приведенные выше референсные значения, разработанные для метода Вестергрена, применимы для интерпретации результатов определения СОЭ, полученных при помощи анализатора Roller.
Приведенные выше референсные значения, разработанные для метода Вестергрена, применимы для интерпретации результатов определения СОЭ, полученных при помощи анализатора Roller.Применение определения СОЭ для скрининга в общей популяции людей без клинических симптомов заболевания в настоящее время не рекомендуется. В то же время данный тест может быть полезен в совокупности с результатами физикального осмотра и сбора анамнеза для выявления патологических состояний у пациентов с клиническими проявлениями. Продемонстрировано, что в 68% случаев полученные высокие значения СОЭ подтверждали клиническую гипотезу врача, предварительно сформированную на анамнестических данных и данных осмотра. Согласно рекомендациям некоторых авторов показатель СОЭ может быть использован в качестве так называемого «индекса болезненности» в группе госпитализированных пациентов. Например, процент выявления новых заболеваний среди пациентов с уровнем СОЭ до 20 мм/час составил 7%, а при уровне СОЭ более 50 мм/час этот показатель увеличивался до 66%.
Особое внимание необходимо уделить интерпретации значений СОЭ выше 100 мм/час. Ввиду ограничений метода Панченкова, отечественные клиницисты не знакомы с правилами интерпретации уровня СОЭ более 80 мм/час. На основании многочисленных клинических исследований показано, что специфичность теста для патологических состояний растет пропорционально росту значений СОЭ, а при уровнях более 100 мм/час число ложноположительных результатов сводится к нулю. Наиболее частыми причинами таких высоких значений СОЭ является туберкулез, метастазирующие опухоли и парапротеинемии. Направление дальнейшего диагностического поиска зависит от других клинических данных. Например, если у пациента старше 50 лет без клинических признаков воспаления уровень СОЭ более 100 мм/час, то следующим диагностическим шагом является проведение электрофореза белков сыворотки крови с целью обнаружения моноклонального компонента. Кроме того, СОЭ может быть дополнительным критерием для дифференциальной диагностики между множественной миеломой (СОЭ > 50 мм/час) и доброкачественной моноклональной гаммапатией (CОЭ За последние 20 лет появилось много публикации, свидетельствующих о возможности эффективного использования показателя СОЭ для диагностики и мониторинга терапии различных патологических состояний.
 Например, в одном исследовании продемонстрировано, что обнаружение СОЭ > 40 мм/час и С-реактивного белка > 60 мг/л у женщин с подозрением на воспалительное заболевание органов малого таза подтверждало диагноз в 70%. Причем степень роста СОЭ коррелировала с тяжестью патологического процесса. В другом исследовании показано, что уровень СОЭ более 37 мм/час у пациентов с раком простаты свидетельствует о высоком риске прогрессии болезни и смерти. Была изучена эффективность применение анализа СОЭ в диагностике и оценке прогноза коронарных и цереброваскулярных осложнений атеросклероза. Установлено, что значения СОЭ выше 22 мм/час в группе пациентов 45-65 лет ассоциированы с высоким риском развития сердечно-сосудистых осложнений атеросклероза. У пациентов с ишемическим инсультом нормальный уровень СОЭ свидетельствовал о быстром восстановлении неврологического дефицита, а значения СОЭ более 28 мм/час были связаны с плохим прогнозом.
Например, в одном исследовании продемонстрировано, что обнаружение СОЭ > 40 мм/час и С-реактивного белка > 60 мг/л у женщин с подозрением на воспалительное заболевание органов малого таза подтверждало диагноз в 70%. Причем степень роста СОЭ коррелировала с тяжестью патологического процесса. В другом исследовании показано, что уровень СОЭ более 37 мм/час у пациентов с раком простаты свидетельствует о высоком риске прогрессии болезни и смерти. Была изучена эффективность применение анализа СОЭ в диагностике и оценке прогноза коронарных и цереброваскулярных осложнений атеросклероза. Установлено, что значения СОЭ выше 22 мм/час в группе пациентов 45-65 лет ассоциированы с высоким риском развития сердечно-сосудистых осложнений атеросклероза. У пациентов с ишемическим инсультом нормальный уровень СОЭ свидетельствовал о быстром восстановлении неврологического дефицита, а значения СОЭ более 28 мм/час были связаны с плохим прогнозом. Для чего используется анализ
- профилактическое обследование
- острые и хронические воспалительные процессы,
- инфекционные заболевания
- онкологические заболевания
- аутоиммунные заболевания (диагноз, прогноз).

Причины повышения СОЭ
- Инфекционные заболевания (чаще бактериальной этиологии).
- Воспалительные заболевания.
- Болезни соединительной ткани (ревматоидный артрит, системная красная волчанка, системная склеродермия, васкулиты).
- Воспалительные заболевания кишечника (болезнь Крона, неспецифический язвенный колит).
- Онкологические заболевания (миеломная болезнь, лимфогранулематоз, рак различных локализаций).
- Инфаркт миокарда.
- Анемии.
- Ожоги, травмы.
- Амилоидоз
- Беременность
Причины снижения СОЭ
- Болезни, сопровождающиеся изменением формы эритроцитов, такие как серповидно-клеточная анемия или наследственный сфероцитоз
- Полицитемия и состояния, которые к ней приводят, такие как, например, хроническая сердечная недостаточность или заболевания легких.
- Гипофибриногенемия.
- Обезвоживание.

Критические значения показателей общего анализа крови
Сильное отклонение некоторых лабораторных показателей от референсных значений в ту или другую сторону может привести к серьезным последствиям для пациента, в том числе угрожать его жизни. Такие значения лабораторных показателей называют критическими. Лаборатории обязаны информировать своих пациентов и их врачей о получении таких результатов незамедлительно. В лаборатории «Глобал-Диагностик» принят перечень критических значений в общем анализе крови, приведенный в таблице ниже (табл. 9). В случае получения критического значения лабораторного показателя специалисты лаборатории в кратчайшие сроки связываются с пациентом или его лечащим врачом и оповещают о результатах анализа.
Таблица 9. Критические значения в общем анализе крови
| Компоненты анализа | Возраст | Нижний предел | Верхний предел | Ед имерения |
| Лейкоциты | > 50 | ?10^9 | ||
| Гематокрит | > 60 | % | ||
| Гемоглобин | > 240 | г/л | ||
| > 2 мес | > 200 | г/л | ||
| Тромбоциты | > 1000 | ?10^9 | ||
| Бласты | Впервые выявленные бласты | %, ?10^9 | ||
Краткая расшифровка общего анализа крови (CBC) в Израиле : Armedical
CBC (Complete Blood Count) – общий анализ крови. Общий анализ крови является важным инструментом в диагностике заболеваний общего функционирования организма человека. В Тель-Авивской больнице Ихилов общий анализ крови выполняется в компьютеризованных лабораторных условиях. Общий анализ крови обеспечивает количественную и качественную информацию об условиях снижения эритроцитов, что говорит об анемии, инфекции и различных расстройствах.
Общий анализ крови является важным инструментом в диагностике заболеваний общего функционирования организма человека. В Тель-Авивской больнице Ихилов общий анализ крови выполняется в компьютеризованных лабораторных условиях. Общий анализ крови обеспечивает количественную и качественную информацию об условиях снижения эритроцитов, что говорит об анемии, инфекции и различных расстройствах.
В лаборатории больницы Ихилов в большинстве случаев берут образец крови из вены, в некоторых случаях – из пальца, это в том случае когда нужно за короткий период времени получить результаты анализа крови.
Эритроциты (RBC) – красные кровяные тельца, переносящие гемоглобин. Главная функция эритроцитов транспортировка кислорода из лёгких ко всем тканям и двуокись углерода – от тканей обратно в лёгкие. Мало эритроцитов – мало гемоглобина. Мало гемоглобина – мало эритроцитов. Они взаимосвязаны.
Эритроциты в норме: от 4,2 до 5,6 (число клеток на микролитр крови)
Недостаток красных кровяных телец – один из признаков анемии (малокровие).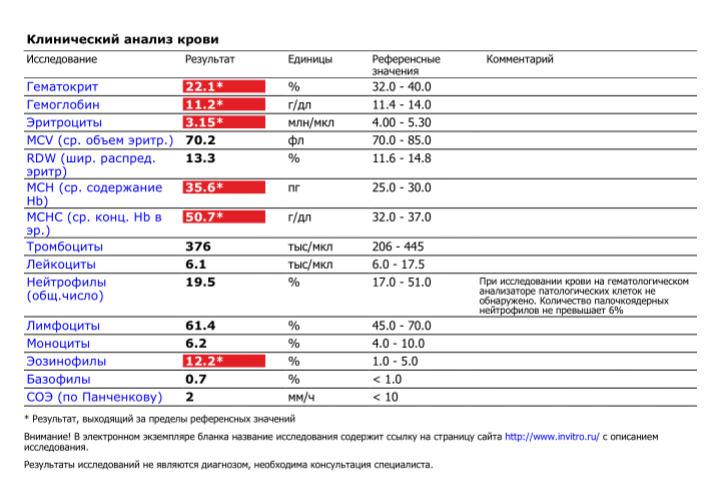 Причинами анемии может быть дефицитом железа. Избыток эритроцитов называется полицитемия. Полицитемия может быть вызвана с нарушением производства красных кровяных телец в костном мозге.
Причинами анемии может быть дефицитом железа. Избыток эритроцитов называется полицитемия. Полицитемия может быть вызвана с нарушением производства красных кровяных телец в костном мозге.
Гемоглобин (HGB) – Белок, содержащийся в эритроцитах и отвечающий за перенос молекул кислорода к клеткам организма. Гемоглобин – железосодержащий комплекс, окружающий белок. Уровень гемоглобина не является постоянной величиной и зависит от возраста, пола, этнической принадлежности, заболевания, курения, у женщин – от беременности и т.д.
Гемоглобин в норме: 11,7 – 17,0 гр.дл. (г на 100 мл крови). Есть варианты, зависящие от пола и возраста.
Снижение уровня гемоглобина – выраженная анемия. Анемия может быть вызвана существенным недостатком красных кровяных телец, острой или хронической кровопотерей. Это связано с недостатком фолиевой кислоты В9 и витамином В12. Гемолиз (повышенное разрушение оболочек эритроцитов) от аутоиммунных состояний, инфекций и наследственных заболеваний кровообразования.
Средний объём гемоглобина (MCH) – среднее количество гемоглобина в отдельном эритроците: в красных кровяных тельцах.
Норма: 27-31pg.
Исключение: Пониженное количество гемоглобина в красных клетках крови. Анемии и другие гематологические проблемы.
Гематокрит (HCT) – показывает в процентах индекс объёма эритроцитов к объёму всего образца крови.
Норма (HCT): мужчины 42%-52%, женщины – от 36% до 48%
Исключение: Пониженный гематокрит говорит об анемии (полицитемия). Повышенный гематокрит – эритремия.
Средний объём эритроцита (MCV) – индекс среднего объёма эритроцитов.
Норма (MCV): 80-94. Значения зависят от возраста.
Исключение: Аномально низкое значение называется микроцитоз. Это может быть связано с дефицитом железа, всасыванием железа в кишечнике, заболеваниях почек, талассемией, генетических причинах и кровопотерями. Аномально высокое значение называется макроцитоз.
Недостаток витаминов В9 и В12, нарушение работы щитовидной железы.
Ширина распределения эритроцитов в процентах (RDW) – различие эритроцитов по размерам.
Норма (RDW): 9%- 14.5%
Исключение: Аномальные уровни могут указывать на нарушение кроветворения.
Лейкоциты (WBC) – белые или бесцветные клетки крови различных размеров. Основная функция лейкоцитов – противодействовать инфекциям, вирусам, бактериям и т.д. Лейкоциты делятся на 5 типов: нейтрофилы, лимфоциты, моноциты, эозинофилы и базофилы.
Норма (WBC): 4,50 до 11,0 (от 4 500 до 11 000 кубических клеток на мКл крови)
Исключение: значительное увеличение или значительное понижение лейкоцитов указывают на воспалительный процесс. На характер инфекции указывают тип лейкоцитов.
Нейтрофилы (NEUT) – Процентное содержание нейтрофилов в крови. Нейтрофилы генерируются в костном мозге. Срок их службы в крови длится несколько часов. Нейтрофилы уничтожают микробы (фагоцитоз).
Нейтрофилы уничтожают микробы (фагоцитоз).
Норма (NEUT): 40%-75% (количество нейтрофилов в 100 лейкоцитах). Нормальные значения зависят от возраста.
Исключение: Повышенное количество нейтрофилов указывает на воспаления и инфекции.
Лимфоциты (LYM) – основные клетки иммунной системы человека. Лимфоциты – один из видов белых кровяных клеток, который производится в лимфатической системе и костном мозге. По своим функциям лимфоциты делятся на В – лимфоциты, вырабатывающие антитела, Т-лимфоциты, которые борются с инфекциями и NK лимфоциты, контролирующие качество клеток организма.
Норма (LYMLYMPH): от 20% до 40% (количество лимфоцитов в 100 лейкоцитах). Нормальное значение варьируется в зависимости от возраста (особенно у детей).
Исключение: Повышенное количество лимфоцитов может быть вызвано различными заболеваниями, особенно вирусными инфекциями.
Эозинофилы (EOSEOSIN) – белые клетки крови, характеризуются специфическим оранжевым цветом. Они принимают участие в иммунной системе. Повышаются при инфекциях паразитами. Существует тенденция к появлению при аллергие и астме.
Они принимают участие в иммунной системе. Повышаются при инфекциях паразитами. Существует тенденция к появлению при аллергие и астме.
Норма (EOS): от 0% до 6% (количество эозинофилов в 100 лейкоцитах)
Исключение: Увеличение процента эозинофилов является признаком наличия факторов аллергии или глистных инвазий.
Моноциты (MONO) – один из видов фагоцитов, самый крупный вид лейкоцитов. Моноциты образуются в костном мозге. Эти клетки участвуют в регулировании и дифференцировании кроветворения, затем уходят в ткани организма и там превращаются в макрофаги. Моноциты имеют большое значение, так как отвечают за начальную активацию всей иммунной системы человека.
Норма (MONO): от 3% до 7% (от общего числа белых клеток крови)
Исключение: Увеличение процента моноцитов является признаком развития различных вирусных заболеваний.
Базофилы (BASO) – одна из крупных форм лейкоцитов в крови, относящихся к иммунной системе.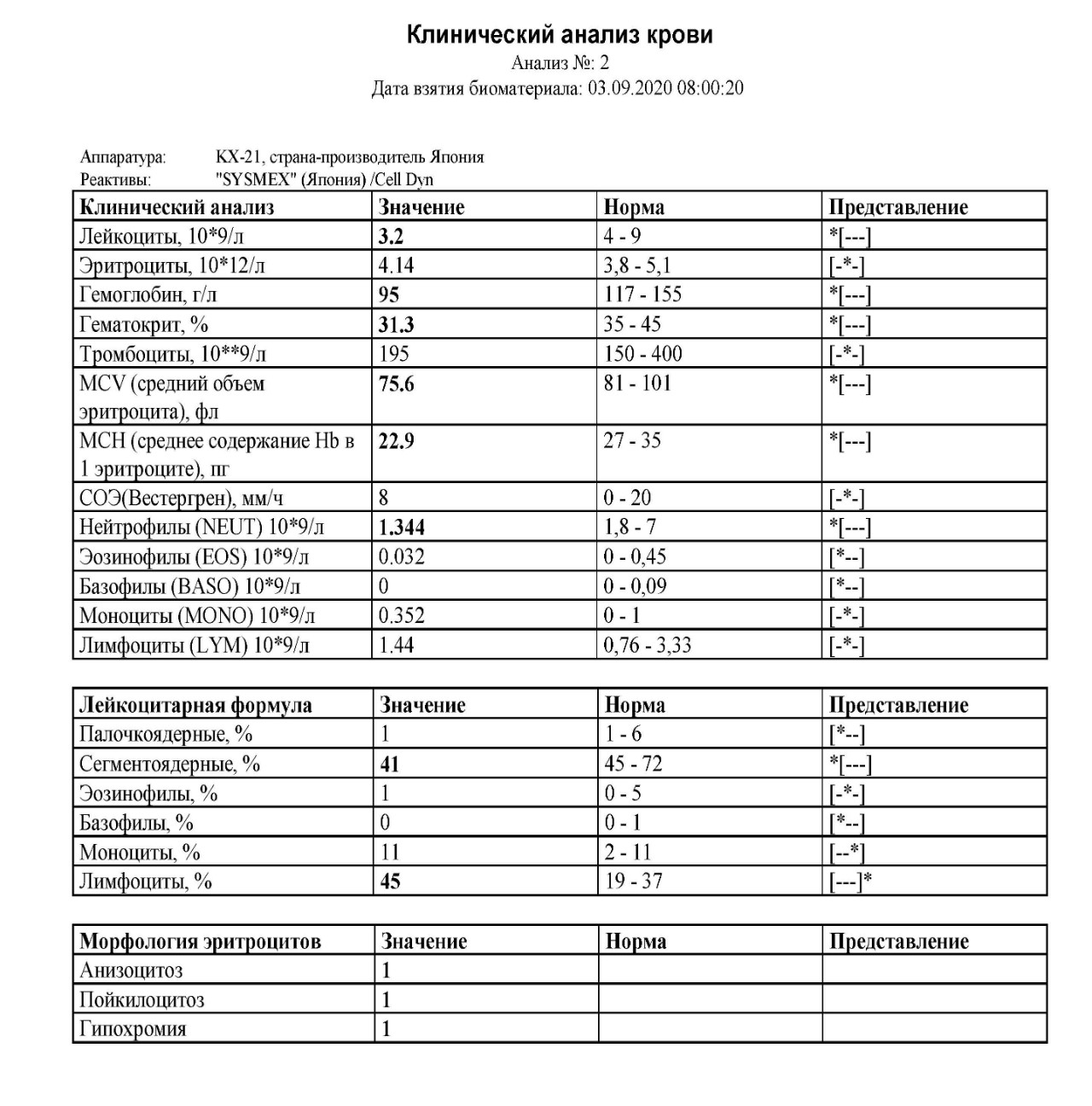 Основная функция – расширение кровеносных сосудов во время инфекции.
Основная функция – расширение кровеносных сосудов во время инфекции.
Норма (BASO): от 0% до 2% (от общего числа белых клеток крови)
Исключение: Увеличение процента клеток базофилов является признаком инфекции или различных вирусных инфекций.
Тромбоциты (PLT) – Клетки, влияющие на процессы свёртывания крови. Тромбоциты отвечают за гемостаз, заживление ран и остановку кровотечения. Анализ тромбоцитов важен при болезнях костного мозга, в котором они образуются. Самые крупные клетки костного мозга называются Мегакариоцит.
Норма (PLT): 150 000 – 450 000 (на микролитр крови)
Исключение: Низкие значения (менее 50 тысяч) может указывать на риск кровотечения или вирусную инфекцию. Иногда снижение тромбоцитов может привести к образованию тромбов.
Средний объём тромбоцитов (MPV) – индекс среднего объёма тромбоцитов.
Норма (MPV): 7-11 FL
Исключение: Повышенный объём тромбоцитов может указывать на разрушение старых тромбоцитов и формирование новых тромбоцитов.
Практический бюллетень № 166: Тромбоцитопения при беременности: акушерство и гинекология
Общие сведения
Функция тромбоцитов
В отличие от других нарушений свертываемости крови, при которых синяки часто являются начальным клиническим проявлением, нарушения тромбоцитов, такие как тромбоцитопения, обычно приводят к кровотечениям в слизистые оболочки.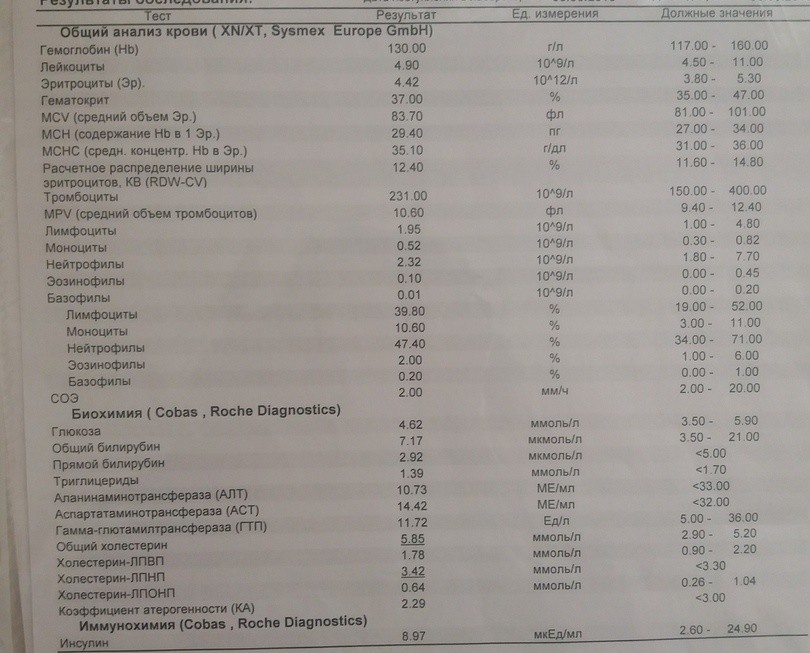 Наиболее частыми проявлениями тромбоцитопении являются петехии, экхимозы, носовые кровотечения, кровоточивость десен и менометроррагия. Кровоизлияния в суставы обычно не бывает. Хотя опасные для жизни кровотечения встречаются редко, когда они происходят, они связаны с гематурией, желудочно-кишечными кровотечениями и редко внутричерепными кровоизлияниями.
Наиболее частыми проявлениями тромбоцитопении являются петехии, экхимозы, носовые кровотечения, кровоточивость десен и менометроррагия. Кровоизлияния в суставы обычно не бывает. Хотя опасные для жизни кровотечения встречаются редко, когда они происходят, они связаны с гематурией, желудочно-кишечными кровотечениями и редко внутричерепными кровоизлияниями.
Определение тромбоцитопении
Нормальный диапазон количества тромбоцитов у небеременных составляет 165–415 x 10 9 /л ( 1 ).Традиционно тромбоцитопения у беременных определялась как число тромбоцитов менее 150 x 10 9 /л ( 2, 3 ). Лабораторный диапазон количества тромбоцитов у беременных варьирует в зависимости от триместра с постепенным снижением по мере развития беременности. У женщин на последнем месяце беременности средний уровень тромбоцитов значительно ниже, чем у небеременных женщин ( 1, 3 ). Определение тромбоцитопении несколько произвольно и не обязательно имеет клиническое значение.В двух проспективных обсервационных исследованиях с участием более чем 11 000 беременных женщин 95% доверительный интервал установил нижние пределы количества тромбоцитов от 116 x 10 9 /л до 123 x 10 9 /л ( 3, 4 ). ). Значительное кровотечение обычно ограничивается пациентами с чрезвычайно низким уровнем тромбоцитов, которым предстоит серьезное хирургическое вмешательство. Для снижения риска спонтанного кровотечения в консенсусных руководствах рекомендуется переливание тромбоцитов у взрослых с числом тромбоцитов менее 10 x 10 ovid.com/mrws/1.0″> 9 /л и у лиц, перенесших обширное хирургическое вмешательство, с числом тромбоцитов менее 50 x 10 9 /л. 5 ).
У женщин на последнем месяце беременности средний уровень тромбоцитов значительно ниже, чем у небеременных женщин ( 1, 3 ). Определение тромбоцитопении несколько произвольно и не обязательно имеет клиническое значение.В двух проспективных обсервационных исследованиях с участием более чем 11 000 беременных женщин 95% доверительный интервал установил нижние пределы количества тромбоцитов от 116 x 10 9 /л до 123 x 10 9 /л ( 3, 4 ). ). Значительное кровотечение обычно ограничивается пациентами с чрезвычайно низким уровнем тромбоцитов, которым предстоит серьезное хирургическое вмешательство. Для снижения риска спонтанного кровотечения в консенсусных руководствах рекомендуется переливание тромбоцитов у взрослых с числом тромбоцитов менее 10 x 10 ovid.com/mrws/1.0″> 9 /л и у лиц, перенесших обширное хирургическое вмешательство, с числом тромбоцитов менее 50 x 10 9 /л. 5 ).
Дифференциальная диагностика тромбоцитопении
Тромбоцитопения вызывается повышенным разрушением тромбоцитов или снижением продукции тромбоцитов. Во время беременности большинство случаев связано с повышенным разрушением тромбоцитов, которое может быть вызвано иммунологической деструкцией, аномальной активацией тромбоцитов или потреблением тромбоцитов в результате чрезмерного кровотечения или воздействия на аномальные сосуды. Снижение продукции тромбоцитов во время беременности встречается реже и обычно связано с заболеваниями костного мозга или дефицитом питательных веществ ( 6 ).Наиболее частой причиной тромбоцитопении во время беременности является гестационная тромбоцитопения, на долю которой приходится 80% случаев ( ovid.com/mrws/1.0″> 2–4 ) (см. вставку 1).
Коробка 1.
Причины тромбоцитопении при беременности
- Гестационная тромбоцитопения
- Артериальная гипертензия при беременности
- Преэклампсия
- HELLP-синдром
- Первичная иммунная тромбоцитопения
- Вторичная иммунная тромбоцитопения
- Антифосфолипидный синдром
- Системная красная волчанка
- Инфекция (например, вирус иммунодефицита человека, гепатит С, цитомегаловирус, Helicobacter pylori )
- Лекарственная тромбоцитопения (например, гепарины, противомикробные препараты, противосудорожные препараты, анальгетики)
- Связь с системными заболеваниями
- Диссеминированное внутрисосудистое свертывание крови
- Тромботическая тромбоцитопения/гемолитический уремический синдром
- Секвестрация селезенки
- Заболевания костного мозга
- Дефицит питательных веществ
- Врожденная тромбоцитопения
Аббревиатура: HELLP, гемолиз, повышенный уровень ферментов печени и низкий уровень тромбоцитов.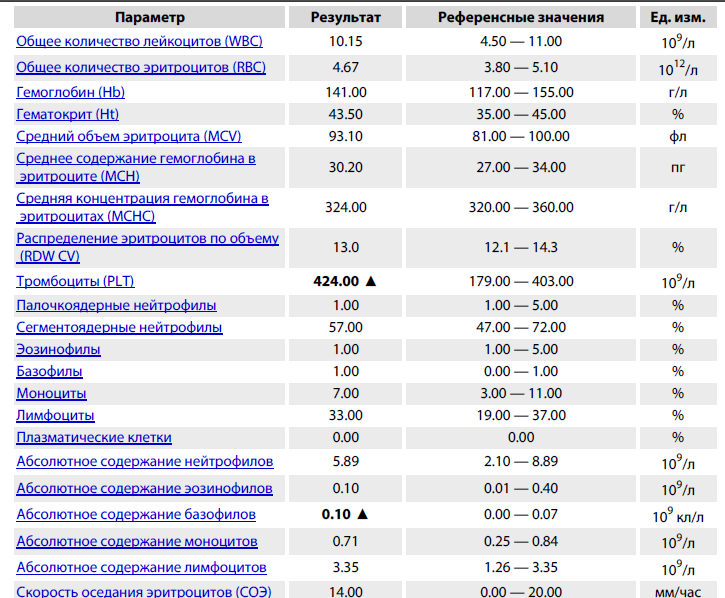
Гестационная тромбоцитопения
Гестационная тромбоцитопения, также называемая случайной тромбоцитопенией беременных, на сегодняшний день является наиболее частой причиной тромбоцитопении во время беременности и поражает 5–11% беременных женщин ( 2–4 ). Хотя ее патогенез неясен, гестационная тромбоцитопения может быть результатом различных процессов, включая гемодилюцию и усиленный клиренс ( 7 ). Существует несколько характеристик гестационной тромбоцитопении ( 6 ).Во-первых, начало заболевания приходится на середину второго-третьего триместров, при этом в большинстве случаев количество тромбоцитов превышает 75 x 10 9 /л ( 0″> 3, 4 ). Однако были описаны некоторые случаи с количеством тромбоцитов всего 43 x 10 9 /л ( 8 ). Во-вторых, женщины с гестационной тромбоцитопенией протекают бессимптомно, без кровотечения в анамнезе. В-третьих, женщины не имеют истории тромбоцитопении вне беременности. В-четвертых, количество тромбоцитов обычно возвращается к норме в течение 1–2 месяцев после родов.Хотя небольшое проспективное обсервационное исследование показало, что гестационная тромбоцитопения может рецидивировать при последующих беременностях, риск рецидива неизвестен ( 9 ). Наконец, частота фетальной или неонатальной тромбоцитопении на фоне гестационной тромбоцитопении низка. Частота неонатальной тромбоцитопении, определяемая по количеству тромбоцитов в пуповинной крови у женщин с гестационной тромбоцитопенией, колеблется от 0,1% до 1,7% ( ovid.com/mrws/1.0″> 2, 4 ).Таким образом, женщины с гестационной тромбоцитопенией не подвержены риску кровотечений у матери или плода или кровотечений. Специфических лабораторных тестов для подтверждения гестационной тромбоцитопении не существует, и диагноз ставится методом исключения. Гестационная тромбоцитопения должна спонтанно разрешиться после родов.
Преэклампсия
Преэклампсия является этиологией в 5–21% случаев материнской тромбоцитопении ( 2–4 ). Гематологическим диагностическим критерием преэклампсии является число тромбоцитов менее 100 х 10 9 /л во время беременности при впервые возникшей гипертензии ( 10 ).Клинические кровотечения встречаются редко, если только у пациента не развивается диссеминированная внутрисосудистая коагулопатия.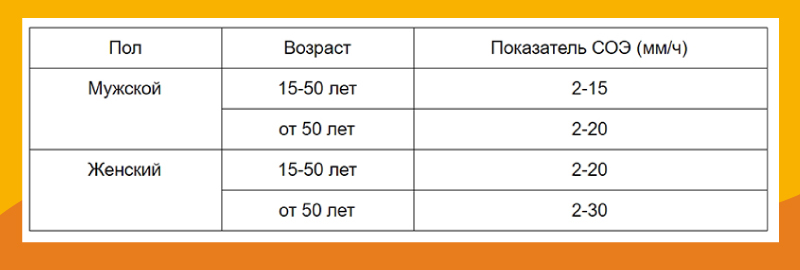 В некоторых случаях микроангиопатическая гемолитическая анемия и повышенные печеночные пробы связаны с тромбоцитопенией у беременных с преэклампсией. Считается, что у таких людей гемолиз, повышенный уровень ферментов печени и синдром низкого количества тромбоцитов (HELLP) ( 11 ).
В некоторых случаях микроангиопатическая гемолитическая анемия и повышенные печеночные пробы связаны с тромбоцитопенией у беременных с преэклампсией. Считается, что у таких людей гемолиз, повышенный уровень ферментов печени и синдром низкого количества тромбоцитов (HELLP) ( 11 ).
Происхождение тромбоцитопении у женщин с преэклампсией неизвестно.Заболевание связано с состоянием потребления и активации тромбоцитов ( 12 ). Функция тромбоцитов также может быть нарушена у женщин с преэклампсией, даже если количество тромбоцитов у них нормальное. Примечательно, что количество тромбоцитов может снижаться до того, как станут очевидными другие клинические проявления преэклампсии ( 13 ).
Может быть повышенный риск (1,8%) тромбоцитопении у новорожденных от женщин с тромбоцитопенией, связанной с гипертоническими расстройствами беременности ( ovid.com/mrws/1.0″> 2 ).Однако исследованные младенцы были рождены «до срока» (гестационный возраст не указан), и 60% младенцев имели массу тела при рождении, малую для гестационного возраста ( 2 ). Недоношенность и задержка роста плода связаны с повышенной вероятностью неонатальной тромбоцитопении, независимо от количества тромбоцитов у матери ( 14 ). Другие крупные обсервационные исследования женщин в сроке не выявили случаев неонатальной тромбоцитопении у женщин с преэклампсией, связанной с материнской тромбоцитопенией ( 3, 4 ).
Тромбоцитопения на иммунологической основе
Тромбоцитопения с иммунологической основой во время беременности может быть широко классифицирована как два расстройства: 1) фетально-неонатальная аллоиммунная тромбоцитопения и 2) материнская первичная иммунная тромбоцитопения (ИТП), аутоиммунное состояние. Фетально-неонатальная аллоиммунная тромбоцитопения не влияет на женщину, но может быть причиной большего числа случаев внутричерепного кровоизлияния, связанного с тромбоцитопенией, чем все другие первичные материнские тромбоцитопенические состояния вместе взятые.Напротив, ИТП может поражать женщин и плод, но при надлежащем лечении результат для обоих является превосходным.
Фетально-неонатальная аллоиммунная тромбоцитопения не влияет на женщину, но может быть причиной большего числа случаев внутричерепного кровоизлияния, связанного с тромбоцитопенией, чем все другие первичные материнские тромбоцитопенические состояния вместе взятые.Напротив, ИТП может поражать женщин и плод, но при надлежащем лечении результат для обоих является превосходным.
Материнская иммунная тромбоцитопения
Иммунная тромбоцитопения характеризуется сложными процессами, в которых играют роль нарушение образования тромбоцитов и эффекты, опосредованные Т-клетками ( 7 ). Для ИТП нет патогномоничных признаков, симптомов или диагностических тестов, что делает его диагнозом исключения. Он характеризуется изолированной тромбоцитопенией (количество тромбоцитов менее 100 x 10 9 /л) при отсутствии других этиологических факторов ( ovid.com/mrws/1.0″> 7 ).Международная рабочая группа по гематологии разработала согласованные определения ИТП ( 15 ). Первичная ИТП определяется как приобретенное иммуноопосредованное заболевание, характеризующееся изолированной тромбоцитопенией при отсутствии какой-либо очевидной инициирующей или основной причины тромбоцитопении. Термин «вторичная» ИТП используется для обозначения всех форм иммуноопосредованной тромбоцитопении, возникающих вследствие основного заболевания или воздействия лекарств. Иммунная тромбоцитопения классифицируется по продолжительности на впервые диагностированную, персистирующую (продолжительность 3–12 месяцев) и хроническую (продолжительность 12 месяцев и более) ( 7, 15 ).Оценки частоты ИТП во время беременности сильно различаются, затрагивая 1 из 1000–10 000 беременностей ( ovid.com/mrws/1.0″> 7 ).
Влияние беременности на течение ИТП до конца не изучено, поскольку большинство данных основано на ретроспективных обсервационных исследованиях. В двух исследованиях 237 беременностей с ИТП 66–91% беременностей не имели симптомов кровотечения, а среди беременностей с кровотечением 92% считались легкими или умеренными (т. , 17 ).Половина беременностей показала снижение количества тромбоцитов не менее чем на 30% с первого триместра до родов, при этом медиана количества тромбоцитов при родах колебалась от 85 x 10 9 /л до 110 x 10 9 /л ( ). 16, 17 ). Антитромбоцитарные антитела материнского иммуноглобулина G могут проникать через плаценту, подвергая плод и новорожденного риску тромбоцитопении. Ретроспективные тематические исследования ИТП во время беременности показывают, что почти у четверти детей, рожденных женщинами с ИТП, число тромбоцитов будет ниже 150 x 10 ovid.com/mrws/1.0″> 9 /л ( 16, 17 ).Никакой связи между числом тромбоцитов у матери при родах и количеством тромбоцитов у младенцев при рождении не выявлено ( 16 ). От 8% до 15% новорожденных будут лечить тромбоцитопению на основании таких факторов, как количество тромбоцитов, признаки и симптомы кровотечения или необходимость инвазивных вмешательств ( 16, 17 ). Несмотря на эту заболеваемость, риск тромбоцитопении плода, связанной с ИТП, приводящей к тяжелым геморрагическим осложнениям, встречается редко (менее 1%) ( 16, 17 ).Количество тромбоцитов у новорожденных с тромбоцитопенией обычно снижается после родов, причем надир приходится на первые 2 недели жизни ( ovid.com/mrws/1.0″> 16 ).
Фетально-неонатальная аллоиммунная тромбоцитопения
Фетально-неонатальная аллоиммунная тромбоцитопения является тромбоцитарным эквивалентом гемолитической (Rh) болезни новорожденных и развивается в результате аллоиммунизации матери антигенами тромбоцитов плода с трансплацентарным переносом тромбоцитарно-специфических антител и последующей деструкцией тромбоцитов.Крупные проспективные скрининговые исследования сообщают, что это состояние встречается у 1 из 1000–3000 живорожденных и может быть серьезным и потенциально опасным для жизни ( 18, 19 ). В отличие от аллоиммунизации эритроцитов, аллоиммунная тромбоцитопения плода и новорожденного может повлиять на первую беременность. Большая часть клинически очевидных случаев фетально-неонатальной аллоиммунной тромбоцитопении выявляется у первого живорожденного ребенка ( ovid.com/mrws/1.0″> 20 ).
В типичном случае непредвиденной фетально-неонатальной аллоиммунной тромбоцитопении женщина здорова и имеет нормальное количество тромбоцитов, а ее беременность, роды и роды неотличимы от таковых у других акушерских пациенток с низким риском.Однако новорожденный рождается с признаками глубокой тромбоцитопении или у нее развивается симптоматическая тромбоцитопения в течение нескольких часов после рождения. У пораженного младенца часто проявляются генерализованные петехии или экхимозы над предлежащей частью плода. Кровоизлияние во внутренние органы и кровотечение после обрезания или венепункции также могут иметь место. Наиболее серьезным осложнением фетально-неонатальной аллоиммунной тромбоцитопении является внутричерепное кровоизлияние, которое возникает у 15% новорожденных с числом тромбоцитов менее 50 x 10 9 /л ( 0″> 18, 21 ).Внутриутробное кровоизлияние плода из-за аллоиммунной тромбоцитопении плода и новорожденного может произойти внутриутробно, и половина (52%) может быть обнаружена с помощью УЗИ до начала родов ( 22 ). Результаты УЗИ могут включать внутрижелудочковое, перивентрикулярное или паренхиматозное кровоизлияние ( 22 ). Эти наблюдения контрастируют с неонатальным внутричерепным кровоизлиянием из-за ИТП, которое встречается чрезвычайно редко и обычно возникает в неонатальном периоде.
Несколько полиморфных диаллельных антигенных систем, находящихся на гликопротеинах мембран тромбоцитов, ответственны за фетально-неонатальную аллоиммунную тромбоцитопению. Многие из этих антигенных систем имеют несколько названий, потому что они были идентифицированы одновременно в разных частях мира. Была принята единая номенклатура, которая описывает эти антигены как человеческие тромбоцитарные антигены (HPA), с номерами, идентифицирующими определенные антигенные группы и аллели, обозначенными как «a» или «b» ( ovid.com/mrws/1.0″> 23 ).В настоящее время существует более 15 официально признанных тромбоцитарно-специфических антигенов ( 23 ). Ряд различных антигенов может вызывать сенсибилизацию и тяжелые заболевания плода, но большинство зарегистрированных случаев у представителей европеоидной расы и большинство тяжелых случаев произошли в результате сенсибилизации против HPA-1a, ранее известного как Pl A1 и Zw a ( 23, 24 ).
Тромбоцитопения плода из-за сенсибилизации HPA-1a имеет тенденцию быть тяжелой и может возникать на ранних сроках беременности.В когортном исследовании 107 плодов с фетально-неонатальной аллоиммунной тромбоцитопенией (97 с несовместимостью HPA-1a), изученных in utero до получения какой-либо терапии, у 50% исходное количество тромбоцитов было менее 20 x 10 ovid.com/mrws/1.0″> 9 /л ( 25 ). Этот процент включал 21 из 46 плодов, протестированных до 24 недель беременности. Кроме того, это исследование показало, что количество тромбоцитов плода может снижаться со скоростью более 10 х 10 9 /л в неделю при отсутствии терапии, хотя эта скорость снижения может быть неравномерной или предсказуемой.
Риск рецидива фетально-неонатальной аллоиммунной тромбоцитопении чрезвычайно высок и приближается к 100% в случаях, связанных с HPA-1a, если последующий родной брат несет соответствующий антиген ( 25 ). Таким образом, риск рецидива связан с зиготностью самца. Как и в случае аллоиммунизации эритроцитами, заболевание имеет тенденцию быть столь же тяжелым или прогрессировать при последующих беременностях.
Клинические соображения и рекомендации
ovid.com/mrws/1.0″> • Какое обследование необходимо для выявления материнской тромбоцитопении?
Дифференциальный диагноз тромбоцитопении беременных включает гестационную тромбоцитопению, псевдотромбоцитопению, вирусную инфекцию, лекарственную тромбоцитопению, преэклампсию, HELLP-синдром, тромботическую тромбоцитопеническую пурпуру, гемолитико-уремический синдром, диссеминированное внутрисосудистое свертывание крови, системную красную волчанку, антифосфолипидный синдром и врожденную тромбоцитопению. 6 ).Эти расстройства обычно можно определить на основе подробного медицинского и семейного анамнеза и физического осмотра с учетом текущего приема лекарств, артериального давления, спленомегалии, вирусной серологии и дополнительных лабораторных исследований по мере необходимости.
Общий анализ крови и исследование мазка периферической крови обычно показаны при оценке материнской тромбоцитопении.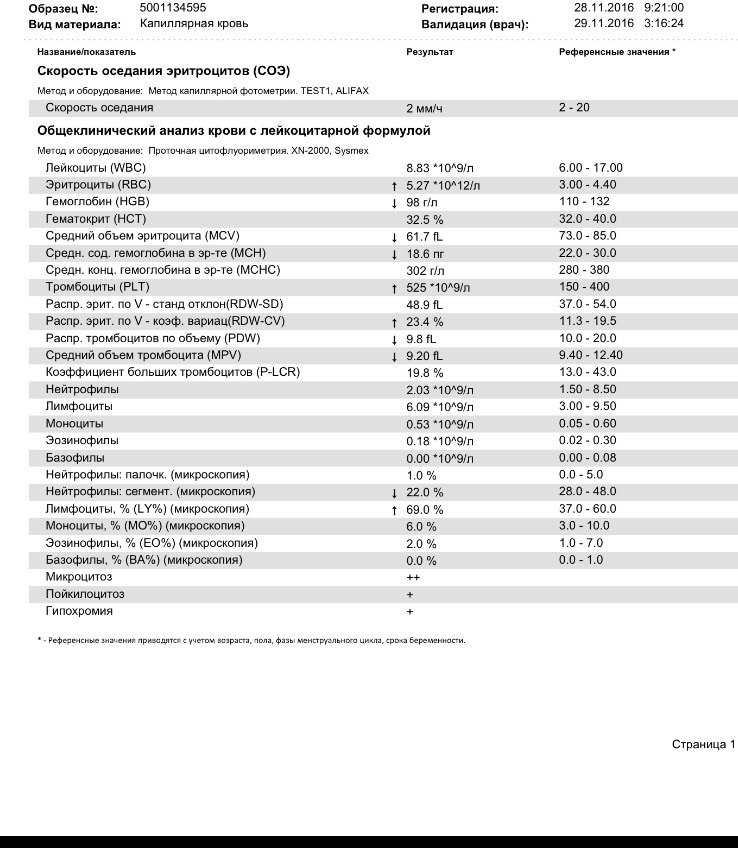 ОАК помогает исключить панцитопению. Оценка мазка периферической крови позволяет исключить скопление тромбоцитов, которое может быть причиной псевдотромбоцитопении.Биопсия костного мозга редко требуется при обследовании беременных с тромбоцитопенией, чтобы отличить недостаточное образование тромбоцитов от повышенного оборота тромбоцитов. Был разработан ряд анализов для ассоциированных с тромбоцитами (прямых) антител и циркулирующих (непрямых) антитромбоцитарных антител. Хотя многие люди с ИТП будут иметь повышенный уровень антител, ассоциированных с тромбоцитами, а иногда и циркулирующих антитромбоцитарных антител, эти тесты не рекомендуются для рутинной оценки материнской тромбоцитопении ( 6 ).Тесты на антитромбоцитарные антитела неспецифичны, плохо стандартизированы и подвержены значительной межлабораторной вариации ( 7 ). Кроме того, гестационная тромбоцитопения и ИТП не могут быть дифференцированы на основании анализа на антитела к тромбоцитам ( ovid.com/mrws/1.0″> 7 ).
ОАК помогает исключить панцитопению. Оценка мазка периферической крови позволяет исключить скопление тромбоцитов, которое может быть причиной псевдотромбоцитопении.Биопсия костного мозга редко требуется при обследовании беременных с тромбоцитопенией, чтобы отличить недостаточное образование тромбоцитов от повышенного оборота тромбоцитов. Был разработан ряд анализов для ассоциированных с тромбоцитами (прямых) антител и циркулирующих (непрямых) антитромбоцитарных антител. Хотя многие люди с ИТП будут иметь повышенный уровень антител, ассоциированных с тромбоцитами, а иногда и циркулирующих антитромбоцитарных антител, эти тесты не рекомендуются для рутинной оценки материнской тромбоцитопении ( 6 ).Тесты на антитромбоцитарные антитела неспецифичны, плохо стандартизированы и подвержены значительной межлабораторной вариации ( 7 ). Кроме того, гестационная тромбоцитопения и ИТП не могут быть дифференцированы на основании анализа на антитела к тромбоцитам ( ovid.com/mrws/1.0″> 7 ).
Если исключить лекарственные препараты и другие медицинские расстройства, наиболее вероятным диагнозом в первом и втором триместрах будет гестационная тромбоцитопения или ИТП. Следует отметить, что хотя гестационная тромбоцитопения может возникать в первом триместре, обычно она проявляется позже во время беременности ( 6 ).В целом материнская тромбоцитопения между 100 x 10 9 /л и 149 x 10 9 /л у бессимптомных беременных женщин без проблем с кровотечением в анамнезе обычно связана с гестационной тромбоцитопенией. Количество тромбоцитов менее 100 x 10 9 /л более характерно для ИТП, а количество тромбоцитов менее 50 x 10 0″> 9 /л почти наверняка связано с ИТП ( 6, 15 ). В третьем триместре или послеродовом периоде внезапное начало значительной тромбоцитопении у матери должно привести к подозрению на преэклампсию, тромботическую тромбоцитопеническую пурпуру, гемолитико-уремический синдром, острую жировую дистрофию печени или диссеминированное внутрисосудистое свертывание крови, хотя ИТП также может проявляться таким образом.
• Какое акушерское лечение целесообразно при гестационной тромбоцитопении?
Беременность с гестационной тромбоцитопенией, как правило, не связана с повышенным риском кровотечений у матери или тромбоцитопении плода ( 2–4 ). Таким образом, такие вмешательства, как кесарево сечение и определение количества тромбоцитов у плода, не показаны пациенткам с этим состоянием. Женщинам с гестацион- ной тромбоцитопенией не требуется никаких дополнительных обследований или специализированной помощи, за исключением последующего контроля числа тромбоцитов.Доказательств, позволяющих определить частоту подсчета тромбоцитов, нет, поэтому график последующих лабораторных исследований должен основываться на клинических данных. Во многих случаях диагноз ставится во время родов. Однако, если диагноз поставлен в дородовом периоде, экспертное мнение предполагает, что количество тромбоцитов следует проверять еженедельно, начиная с 34-й недели беременности ( 6 ). После родов количество тромбоцитов следует повторить через 1–3 месяца после родов, чтобы определить, произошло ли разрешение тромбоцитопении ( 6 ).
Женщинам с гестацион- ной тромбоцитопенией не требуется никаких дополнительных обследований или специализированной помощи, за исключением последующего контроля числа тромбоцитов.Доказательств, позволяющих определить частоту подсчета тромбоцитов, нет, поэтому график последующих лабораторных исследований должен основываться на клинических данных. Во многих случаях диагноз ставится во время родов. Однако, если диагноз поставлен в дородовом периоде, экспертное мнение предполагает, что количество тромбоцитов следует проверять еженедельно, начиная с 34-й недели беременности ( 6 ). После родов количество тромбоцитов следует повторить через 1–3 месяца после родов, чтобы определить, произошло ли разрешение тромбоцитопении ( 6 ).
• Необходимо ли лечение тромбоцитопении, связанной с преэклампсией?
Первичным лечением материнской тромбоцитопении (количество тромбоцитов менее 100 x 10 ovid.com/mrws/1.0″> 9 /л), связанной с тяжелыми признаками преэклампсии или HELLP-синдрома, являются роды ( 10 ). Несмотря на то, что сообщалось о реверсировании тромбоцитопении до родов с помощью медикаментозной терапии, этот курс лечения не является обычным ( 11 ).Что еще более важно, основная патофизиология преэклампсии разрешится только после родов. Таким образом, помимо медикаментозной стабилизации, влияние кортикостероидов на зрелость легких плода или, в особых случаях преждевременной беременности, тромбоцитопения вследствие преэклампсии является показанием к родоразрешению. Способ родоразрешения должен определяться гестационным возрастом плода, предлежанием плода, состоянием шейки матки и состоянием матери и плода ( 10 ).
Обильные кровотечения нечасты у пациенток с преэклампсией, но незначительные кровотечения, такие как просачивание операционного поля во время кесарева сечения, распространены.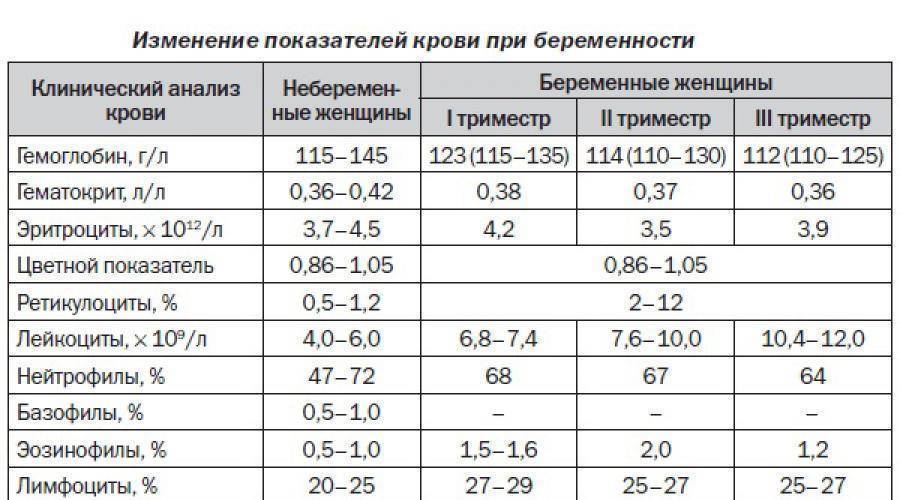 Иногда требуется переливание тромбоцитов для улучшения гемостаза у пациентов с числом тромбоцитов менее 50 x 10 9 /л или подозрением на диссеминированное внутрисосудистое свертывание крови. Однако у этих женщин трансфузии менее эффективны из-за ускоренного разрушения тромбоцитов. Таким образом, переливание тромбоцитов лучше всего проводить у пациентов с тромбоцитопенией и активным кровотечением. Исключение составляет пациентка, перенесшая кесарево сечение. В консенсусных рекомендациях рекомендуется переливание тромбоцитов для повышения количества тромбоцитов у матери до более чем 50 x 10 9 /л перед серьезной операцией ( 5 ).
Иногда требуется переливание тромбоцитов для улучшения гемостаза у пациентов с числом тромбоцитов менее 50 x 10 9 /л или подозрением на диссеминированное внутрисосудистое свертывание крови. Однако у этих женщин трансфузии менее эффективны из-за ускоренного разрушения тромбоцитов. Таким образом, переливание тромбоцитов лучше всего проводить у пациентов с тромбоцитопенией и активным кровотечением. Исключение составляет пациентка, перенесшая кесарево сечение. В консенсусных рекомендациях рекомендуется переливание тромбоцитов для повышения количества тромбоцитов у матери до более чем 50 x 10 9 /л перед серьезной операцией ( 5 ).
Количество тромбоцитов часто снижается в течение 24–48 часов после рождения, после чего следует быстрое восстановление. У большинства пациенток уровень тромбоцитов превышает 100 x 10 9 /л в течение 2–6 дней после родов ( 26, 27 ). Хотя редко, тромбоцитопения может продолжаться в течение длительного периода и часто связана с другими патологическими состояниями ( 28 ). Хотя тромбоцитопения, связанная с тяжелыми признаками преэклампсии или HELLP-синдрома, может уменьшиться после лечения кортикостероидами или выскабливания матки, никаких различий в материнской смертности или заболеваемости при этих методах лечения отмечено не было ( 29, 30 ).
• Когда женщины с иммунной тромбоцитопенией должны получать медикаментозное лечение?
Целью медикаментозной терапии во время беременности у женщин с ИТП является минимизация риска геморрагических осложнений при регионарной анестезии и родах, связанных с тромбоцитопенией. Поскольку функция тромбоцитов у этих пациентов обычно нормальная, нет необходимости поддерживать их количество в нормальном диапазоне. Текущие согласованные руководства рекомендуют, чтобы, за исключением периода родов, показания к лечению для беременных были аналогичны тем, которые в настоящее время рекомендуются для любого пациента ( 7, 31 ).Рекомендации по ведению ИТП во время беременности в основном основаны на клиническом опыте и консенсусе экспертов. Нет данных о пороге тромбоцитов, при котором следует лечить беременных с ИТП ( 31 ). Лечение начинают, когда у пациента появляется симптоматическое кровотечение, когда количество тромбоцитов падает ниже 30 x 10 9 /л, или для повышения количества тромбоцитов до уровня, который считается безопасным для процедур ( 7 ). Во время родов ведение ИТП основано на оценке риска кровотечения у матери, связанного с родами, эпидуральной анестезией и минимальном количестве тромбоцитов, рекомендуемом для проведения этих процедур (80 x 10 9 /л при эпидуральном введении и 50 x 10 9 /л для кесарева сечения) ( 5, 31, 32 ).
• Какую терапию следует использовать для лечения иммунной тромбоцитопении во время беременности?
Кортикостероиды, внутривенный иммуноглобулин (ВВИГ) или оба препарата являются препаратами первой линии для лечения материнской ИТП ( 7, 31 ). Хотя любой подход приемлем, по мнению экспертов, кортикостероиды рекомендуются в качестве стандартного начального лечения курсами до 21 дня ( 7, 31 ). Лечение должно быть адаптировано к индивидуальному пациенту, принимая во внимание возникновение и тяжесть кровотечения, скорость желаемого увеличения количества тромбоцитов и возможные побочные эффекты.Отсутствуют данные, определяющие последовательность лечения пациентов с рецидивирующей или стойкой тромбоцитопенией, связанной с кровотечением, после начального курса лечения ( 31 ).
Преднизолон в дозе 0,5–2 мг/кг в день рекомендован в качестве начального лечения ИТП у взрослых ( 7, 31 ). Хотя имеется мало данных, позволяющих различать лечение ИТП у беременных и небеременных женщин, общепринятые рекомендации при беременности заключаются в том, что преднизолон следует назначать вначале в низкой дозе (10–20 мг/день), а затем корректировать до минимальной дозы, вызывающей адекватное увеличение количества тромбоцитов ( 7 ).Первоначальный ответ обычно возникает в течение 4–14 дней и достигает пика в течение 1–4 недель ( 15 ). Рекомендуется назначать кортикостероиды в течение не менее 21 дня, а затем снижать дозу ( 31 ). Дозу можно снижать до достижения минимальной дозы, необходимой для поддержания количества тромбоцитов, предотвращающего большое кровотечение.
Внутривенный иммуноглобулин является подходящей терапией для случаев, невосприимчивых к кортикостероидам, когда при применении кортикостероидов возникают значительные побочные эффекты или когда необходимо более быстрое увеличение тромбоцитов.Внутривенный иммуноглобулин следует вводить первоначально в дозе 1 г/кг однократно, но при необходимости его можно повторить ( 31 ). Первоначальный ответ обычно возникает в течение 1–3 дней и достигает пика в течение 2–7 дней ( 15 ). Лечение с помощью ВВИГ является дорогостоящим и имеет ограниченную доступность. При рассмотрении вопроса об использовании ВВИГ целесообразно обратиться за консультацией к врачу, имеющему опыт работы в таких случаях.
Спленэктомия — это вариант лечения пациентов с ИТП, у которых лечение первой линии оказалось неэффективным ( 7 ).Спленэктомия остается единственным методом лечения, обеспечивающим длительную ремиссию в течение 1 года и дольше у значительной доли пациентов с ИТП ( 31 ). Процедуры обычно избегают во время беременности из-за риска для плода и технических трудностей на поздних сроках беременности. Однако при необходимости спленэктомия может быть безопасно выполнена во время беременности, в идеале во втором триместре. Данные о степени риска, а также об идеальном типе хирургического доступа (открытый или лапароскопический) отсутствуют ( 31 ).
Переливание тромбоцитов следует использовать только как временную меру для остановки опасного для жизни кровотечения или для подготовки пациента к операции. Большую, чем обычно, дозу тромбоцитов (в 2-3 раза) следует вводить с внутривенными высокими дозами кортикостероидов или ВВИГ от каждых 30 минут до 8 часов ( 7, 31 ). Влияние на количество тромбоцитов оказывается кратковременным ( 31 ). Другие терапевтические варианты, используемые для лечения ИТП, такие как цитотоксические агенты (циклофосфамид или алкалоиды барвинка), иммуноглобин Rh D или иммунодепрессанты (азатиоприн или ритуксимаб), не были должным образом оценены во время беременности и могут иметь потенциальные неблагоприятные эффекты на плод ( 7). , 31 ).
• Какую дополнительную специализированную помощь должны получать женщины с иммунной тромбоцитопенией?
Бессимптомным беременным с ИТП требуется мало специализированной помощи. Мнение экспертов предполагает, что последовательную оценку количества тромбоцитов у матери следует проводить каждый триместр у бессимптомных женщин в стадии ремиссии и чаще у женщин с тромбоцитопенией ( 6 ). Беременных женщин с ИТП следует проинструктировать избегать нестероидных противовоспалительных средств, салицилатов и травм.Пациент, перенесший спленэктомию, должен быть иммунизирован против пневмококка, Haemophilus influenzae и менингококка. Если поставлен диагноз ИТП, уместны консультация и постоянная оценка с врачом, имеющим опыт в таких вопросах.
• Можно ли предотвратить внутричерепное кровоизлияние у плода или новорожденного при беременности, осложненной иммунной тромбоцитопенией?
Хотя внутричерепные кровоизлияния у плода или новорожденного встречаются редко в случаях ИТП у матери, логично сделать вывод, что методы лечения, повышающие количество тромбоцитов у матери у пациенток с ИТП, также улучшают количество тромбоцитов у плода.Однако медикаментозная терапия, такая как ВВИГ и стероиды, не может надежно предотвратить тромбоцитопению плода или улучшить исход плода ( 33 ). Поскольку некоторые из этих методов лечения (например, ВВИГ) не были должным образом протестированы в соответствующих исследованиях, недостаточно данных, чтобы рекомендовать медикаментозное лечение матери при показаниях для плода.
Нет никаких доказательств того, что кесарево сечение безопаснее вагинальных родов для плода с тромбоцитопенией у матери, вызванной ИТП ( 7, 31 ).Многочисленные обсервационные исследования, в которых оценивали более 800 новорожденных, рожденных женщинами с ИТП, показали, что частота внутричерепных кровоизлияний составляет менее 1%, а геморрагические осложнения у новорожденных с тромбоцитопенией не связаны со способом родоразрешения ( 16, 17, 34 ). Большинство неонатальных кровотечений происходит через 24–48 часов после родов при самом низком уровне тромбоцитов ( 34 ). Учитывая очень низкий риск серьезных неонатальных кровотечений, способ родоразрешения при беременности, осложненной ИТП, следует определять только на основании акушерских соображений ( 7, 31 ).
• Какие тесты или характеристики можно использовать для прогнозирования тромбоцитопении плода при беременности, осложненной иммунной тромбоцитопенией?
Никакие материнские тесты или клинические характеристики не могут надежно предсказать тяжесть тромбоцитопении у детей, рожденных женщинами с ИТП. Серология у матери, предыдущая спленэктомия, количество тромбоцитов и наличие ассоциированных с тромбоцитами антител плохо коррелируют с неонатальной тромбоцитопенией ( 34, 35 ).
• Есть ли какая-либо роль в определении количества тромбоцитов плода при иммунной тромбоцитопении?
Нет данных в поддержку рутинного использования интранатального подсчета тромбоцитов плода ( 31 ). Взятие проб кожи головы чревато неточностями и техническими трудностями, а кордоцентез сопряжен с риском потери плода 1,3% или выше в зависимости от показаний, гестационного возраста и проникновения плаценты ( 36 ).Низкая частота внутричерепных кровоизлияний и отсутствие продемонстрированной разницы в неонатальных исходах между родами через естественные родовые пути и путем кесарева сечения подтверждают мнение о том, что определение числа тромбоцитов у плода необоснованно для ИТП ( 7, 31 ).
• Какова соответствующая неонатальная помощь детям, рожденным от беременностей, осложненных иммунной тромбоцитопенией?
Независимо от способа родоразрешение должно осуществляться в условиях, где доступный клиницист, знакомый с расстройством, может лечить любые неонатальные осложнения и иметь доступ к лекарствам, необходимым для лечения.При родах следует определить количество тромбоцитов пуповинной крови путем венепункции пуповинного сосуда. Внутримышечные инъекции (например, витамина К) следует отложить до тех пор, пока не станет известно число тромбоцитов. Младенцы должны находиться под клиническим наблюдением и контролироваться гематологическими параметрами, поскольку количество тромбоцитов имеет тенденцию достигать надира между 2 и 5 днями после рождения ( 7 ).
• Можно ли проводить регионарную анестезию пациенту с тромбоцитопенией?
Ни в одном исследовании не оценивали нижний предел количества тромбоцитов для безопасной эпидуральной анестезии.Нет данных в поддержку определенного минимального количества тромбоцитов для регионарной анестезии, и каждый случай должен рассматриваться индивидуально. Литература предлагает только ограниченные и ретроспективные данные по этому вопросу, но недавний обзор медицинской литературы и международных руководств предлагает безопасный счет для введения и удаления эпидуральной или спинальной анестезии. Эпидуральная или спинальная анестезия считается приемлемой у пациентов с числом тромбоцитов, превышающим или равным 80 x 10 9 /л, при условии, что уровень тромбоцитов стабилен, нет другой приобретенной или врожденной коагулопатии, функция тромбоцитов в норме и пациент не получает антитромбоцитарную или антикоагулянтную терапию ( 32 ).Более низкое количество тромбоцитов также может быть приемлемым, но в настоящее время недостаточно опубликованных данных, чтобы давать рекомендации. Для пациента с числом тромбоцитов менее 75 x 10 9 /л следует принимать индивидуальное решение, основанное на рисках и преимуществах.
• Когда следует начинать обследование на предмет возможной аллоиммунной тромбоцитопении плода и новорожденного и какие тесты полезны для постановки диагноза?
Следует заподозрить фетально-неонатальную аллоиммунную тромбоцитопению в случаях необъяснимой фетальной или неонатальной тромбоцитопении, кровоизлияния или данных УЗИ, свидетельствующих о внутричерепном кровотечении.Лабораторная диагностика включает определение типа HPA и зиготности обоих родителей и подтверждение материнских антитромбоцитарных антител со специфичностью к отцовским (или фетально-неонатальным) тромбоцитам и несовместимому антигену. Типирование тромбоцитов можно определить серологически или путем генотипирования, поскольку уже идентифицированы гены и полиморфизмы, ответственные за большинство случаев фетально-неонатальной аллоиммунной тромбоцитопении. Это полезно, когда отец является гетерозиготным по соответствующему антигену, потому что типирование фетального антигена тромбоцитов может быть выполнено с использованием амниоцитов.Теоретически этот метод также должен быть применим для взятия проб ворсин хориона, хотя при использовании этого метода высказывались опасения из-за возможности повышенной сенсибилизации в случаях, когда поражен плод ( 23, 37 ). Лабораторная оценка фетально-неонатальной аллоиммунной тромбоцитопении может быть сложной, результаты могут быть неоднозначными, а антигенную несовместимость не всегда можно идентифицировать. Соответственно, тестирование на фетально-неонатальную аллоиммунную тромбоцитопению следует проводить в опытной региональной лаборатории, которая имеет особый интерес и опыт в области фетально-неонатальной аллоиммунной тромбоцитопении ( 23 ).
Существует теоретическая польза популяционного скрининга на несовместимость антигенов тромбоцитов. Неясно, будет ли такая программа клинически полезной или рентабельной ( 38 ). Другой областью разногласий является пациентка, у сестры которой была беременность, осложненная фетально-неонатальной аллоиммунной тромбоцитопенией. Возможно, стоит обследовать этих пациентов на несовместимость антигена тромбоцитов или фенотип человеческого лейкоцитарного антигена ( 25 ).Тем не менее, теоретические преимущества тестирования этих женщин должны быть сопоставлены с потенциальным беспокойством, стоимостью и заболеваемостью, связанной с лечением, без определенной пользы.
• Как определить количество тромбоцитов у плода при беременности, осложненной фетально-неонатальной аллоиммунной тромбоцитопенией?
Как и в случае с ИТП, адекватных непрямых методов определения количества тромбоцитов у плода не существует. Титры материнских антитромбоцитарных антител плохо коррелируют с тяжестью заболевания.Кроме того, такие характеристики, как исход ранее пораженных братьев и сестер (например, количество тромбоцитов при рождении или внутричерепное кровоизлияние, обнаруженное после родов), не позволяют надежно предсказать тяжесть тромбоцитопении плода ( 25 ). В настоящее время единственным точным способом оценки числа тромбоцитов плода является его непосредственное измерение путем чрескожного забора пуповинной крови ( 36 ). Сообщалось о серьезных осложнениях до 8% процедур забора крови плода в условиях фетально-неонатальной аллоиммунной тромбоцитопении ( 39 ).
• Какое акушерское лечение аллоиммунной тромбоцитопении у плода и новорожденного является подходящим?
Основной целью акушерского ведения беременностей, осложненных фетально-неонатальной аллоиммунной тромбоцитопенией, является предотвращение внутричерепного кровоизлияния и связанных с ним осложнений. Однако, в отличие от ИТП, более высокая частота внутричерепных кровоизлияний, связанных с фетально-неонатальной аллоиммунной тромбоцитопенией, оправдывает более агрессивные вмешательства.Кроме того, стратегии, направленные на предотвращение внутричерепного кровоизлияния, должны быть начаты антенатально из-за риска внутриутробного внутричерепного кровоизлияния.
Оптимальное ведение плодов с риском внутриутробно-неонатальной аллоиммунной тромбоцитопении (с положительным результатом теста на несовместимый антиген или с отцом, гомозиготным по этому антигену) остается неопределенным. Ведущие решения в этих случаях должны быть индивидуальными, и перед началом любого плана лечения женщины следует проконсультироваться с акушерскими и педиатрическими специалистами, знакомыми с этим расстройством.Недавние подходы, основанные на консенсусе экспертов в этой области исследований, рекомендовали стратифицированное лечение ( 39 ). Женщин с фетально-неонатальной аллоиммунной тромбоцитопенией подразделяют на группы в зависимости от наличия или отсутствия внутричерепного кровоизлияния при ранее перенесенной беременности и гестационного возраста манифестации. Интенсивность материнского наблюдения и терапии корректируется соответствующим образом.
В попытке увеличить количество тромбоцитов плода и избежать внутричерепного кровоизлияния использовалось несколько методов лечения, включая лечение матери внутривенным иммуноглобулином со стероидами или без них ( 40, 41 ) и переливание тромбоцитов плода ( 42 ).При беременности, определяемой как «высокий риск» внутричерепного кровоизлияния (количество тромбоцитов плода в пробе пуповинной крови на сроке 20 недель гестации менее 20 x 10 9 /л или у родного ребенка с перинатальным внутричерепным кровоизлиянием), материнские ВВИГ в сочетании с преднизолон более эффективен, чем монотерапия ВВИГ, в отношении удовлетворительного ответа тромбоцитов плода. Принимая во внимание, что при беременности «стандартного риска» (отсутствие внутричерепного кровоизлияния в анамнезе у ранее пораженного брата или сестры и начальное количество тромбоцитов у плода выше 20 x 10 9 /л на 20-й неделе беременности) терапия ВВИГ или преднизолоном эффективна, без существенного преимущество одного метода лечения перед другим ( 41 ).Однако ни один из этих методов лечения не эффективен во всех случаях. Прямое введение ВВИГ плоду не приводит к достоверному улучшению количества тромбоцитов у плода, хотя сообщалось о нескольких случаях ( 43, 44 ). Трансфузии тромбоцитов материнскими тромбоцитами стабильно эффективны для увеличения числа тромбоцитов у плода. Однако короткий период полураспада перелитых тромбоцитов требует еженедельных процедур и может ухудшить аллоиммунизацию ( 42 ).
Традиционно забор крови плода был включен в лечение фетально-неонатальной аллоиммунной тромбоцитопении для определения необходимости и эффективности терапии.На основании результатов проспективных исследований лечебных вмешательств при фетально-неонатальной аллоиммунной тромбоцитопении было установлено, что ранний кордоцентез не является необходимым ( 40, 45 ). В консенсусных рекомендациях в настоящее время предлагается раннее эмпирическое начало терапии на основании риска рецидива внутричерепного кровоизлияния у плода ( 39 ). Лечение должно основываться на анамнезе пациента и наличии материнских антитромбоцитарных антител и соответствующего тромбоцитарного антигена на клетках плода.Женщинам, планирующим вагинальные роды, рекомендуется откладывать забор крови плода до 32 недель беременности. В этих случаях будет проведен забор пуповинной крови, чтобы документально подтвердить, что реакция тромбоцитов плода на терапию была адекватной для безопасного проведения вагинальных родов, но на достаточно позднем сроке беременности, чтобы родить жизнеспособного новорожденного, если какое-либо осложнение приведет к экстренному родоразрешению.
Роды и вагинальные роды не противопоказаны плодам с числом тромбоцитов выше 50 x 10 9 /л, но кесарево сечение рекомендуется для плодов с числом тромбоцитов ниже этого уровня.Родоразрешение должно осуществляться в условиях, оборудованных для надлежащего ухода за новорожденным с тяжелой тромбоцитопенией.
Сводка рекомендаций
Следующие рекомендации основаны на ограниченных или непоследовательных научных доказательствах (уровень B):
- • материнская тромбоцитопения между 100 x 10 9 / L и 149 x 10
9 9
/ л в бессимптомные беременные женщины без проблем с кровотечением в анамнезе обычно связаны с гестационной тромбоцитопенией. - • Учитывая очень низкий риск серьезных неонатальных кровотечений, способ родоразрешения при беременности, осложненной ИТП, следует определять только на основании акушерских соображений.
- • При беременности, определяемой как «высокий риск» внутричерепного кровоизлияния (количество тромбоцитов плода в пробе пуповинной крови на 20-й неделе гестации менее 20 x 10 9 /л, или родной брат с перинатальным внутричерепным кровоизлиянием ), материнский ВВИГ в сочетании с преднизоном более эффективен, чем один ВВИГ, в отношении получения удовлетворительного ответа тромбоцитов у плода.Принимая во внимание, что при беременности «стандартного риска» (отсутствие внутричерепного кровоизлияния в анамнезе у ранее пораженного брата или сестры и начальное количество тромбоцитов у плода выше 20 x 10 9 /л на 20-й неделе беременности) терапия ВВИГ или преднизолоном эффективна, без существенного преимущества одного вида терапии перед другим.
Следующие рекомендации основаны главным образом на консенсусе и мнении экспертов (уровень C): /л перед серьезной операцией. База данных MEDLINE, Кокрановская библиотека и собственные внутренние ресурсы и документы Американского колледжа акушеров и гинекологов были использованы для проведения поиска литературы с целью поиска соответствующих статей, опубликованных в период с января 1985 г. по январь 2015 г. Поиск был ограничен статьями, опубликованными в английский язык. Приоритет отдавался статьям, сообщающим о результатах оригинальных исследований, хотя также использовались обзорные статьи и комментарии.Тезисы исследований, представленные на симпозиумах и научных конференциях, не были сочтены подходящими для включения в этот документ. Руководства, опубликованные такими организациями или учреждениями, как Национальные институты здравоохранения и Американский колледж акушеров и гинекологов, были проанализированы, а дополнительные исследования были обнаружены путем просмотра библиографий выявленных статей. При отсутствии надежных исследований использовались экспертные заключения акушеров-гинекологов. Исследования были проанализированы и оценены на качество в соответствии с методом, изложенным в U.S. Целевая группа профилактических услуг: На основе самого высокого уровня доказательств, обнаруженных в данных, рекомендации предоставляются и классифицируются в соответствии со следующими категориями: Уровень A — рекомендации основаны на достоверных и непротиворечивых научных данных. Уровень B — рекомендации основаны на ограниченных или противоречивых научных данных. Уровень C — рекомендации основаны главным образом на консенсусе и мнении экспертов. Данную главу следует цитировать следующим образом: Непрерывный учебник по женской медицине, серия – Модуль акушерства Том 8 Здоровье матери и расстройства во время беременности Редактор тома: клинический доцент Сандра Лоу , Университет Нового Южного Уэльса, Австралия Глава Гематологические нормальные диапазоны при беременности Впервые опубликовано: февраль 2021 г. Адам Мортон Акушерство, Mater Health, Южный Брисбен, Квинсленд, Австралия Вариант оценки исследования Ответив на 4 вопроса с несколькими вариантами ответов (случайно выбранных) после изучения этой главы, читатели могут претендовать на Награды за непрерывное профессиональное развитие от FIGO плюс a Сертификат об окончании обучения от GLOWM Интерпретация лабораторных исследований основывается на контрольных интервалах.Физиологические изменения во время беременности могут привести к значительным изменениям нормальных значений многих гематологических анализов, и поэтому такие результаты могут быть ошибочно истолкованы как отклонения от нормы или маскировать патологическое состояние. Существуют значительные различия между лабораториями в зависимости от метода тестирования, используемого анализа и популяционных факторов. Везде, где это возможно, клиницисты должны использовать референтный интервал, характерный для лаборатории, проводившей тест. Здоровая беременность связана со снижением уровня гемоглобина (Hb) и гематокрита из-за того, что увеличение объема плазмы превышает увеличение массы эритроцитов и происходит на более ранних сроках беременности (таблица 1).Объем плазмы начинает увеличиваться с 6-й недели беременности, примерно на 10% выше уровня до беременности в начале второго триместра, затем быстро увеличивается, достигая уровней более чем на 50% выше уровня до беременности к 26 неделе беременности, затем стабилизируется до конца беременности. Объем плазмы начинает снижаться с 6-го дня после родов, достигая небеременных уровней через 6 недель после родов. 1 Масса эритроцитов не увеличивается примерно до 20 недель беременности и увеличивается примерно на 30% по сравнению с небеременным состоянием.Масса эритроцитов также возвращается к нормальному уровню через 6 недель после родов. 1 1 Референтные интервалы образцов для гематологических анализов при здоровой беременности. Baseline первого триместра второго триместра третий триместр Hemoglobin (HB) (G / DL) 2 12–16 11.5-14 10-15 9.5-15 35-44 31-41 30-39 28-40 28-40 9 / L) 2 4-10 6-16 6-16 6-16 тромбоцитов (× 10 9 / L) 2 150-400 170-390 150-400 145-400 эритропоэтин (EPO) (U / L) 2 4-27 12-25 8-67 14-222 Активируемая часть Время EAL тромбопластина (APTT) (S) 3 30-40 26-42 24-36 26-35 Thrombin Время (S ) 3 12–14 11.7-17 10-16 11.1-1-15.944 11.1-15.5 3 11-15 9.7-12.5 8.5-13.2 80052 8,6-12.4 3 80-120 72-120 68-125 56–119 Фибриноген (г/л) 3 1.5-4.0 2.38-4.44 2,8-59 2 Белок C (%) 3 70-140 80 -120 83-138 67-135 70-140 21-133 19–113 20–165 D-димер (мкг/мл) 3 0.01-0.31 0.05-0.73 0.14-2.82 2 Von Willebrand Factor (VWF): AG (U / DL) 4 60- 95 90-150 90-150 100-175 135-245 фактор VIII: C (U / DL) 4 110-160 125-200 160-230 90-230 Adamsts13 (% Activity) 122 ± 34 — — — 118 ± 29 Скорость оседания эритроцитов (СОЭ), мм/ч 5 0–20 7-47 (19) 13-70 (32) 6 10-150 14- 133 (32) 7-130 (18) 5-110 (21) Transferrin SAT (%) 6 12-45 12 -54 10-56 5-65 5-65 Общая емкость для привязки железа (TIBC) (MMOL / L) 6 41-77 40 -84 52-100 52-100 54-120 Религиозный рецептор передачи 6 1.9-4.4 0,4-2,0 0.4-2.0 1.2-3.0 2,3-52 Total Vitamin B12 (PMOL / L) 7 130-650 60-320 (230) 50-360 (170) 60-390 (170) Active Vitamin B12 (PMOL / L) 7 35 -260 35-260 (79) 35-260 (79) 35-190 (76) 30-260 (79) сывороточный фолат (NMOL / L) 8 10-45 10-45 7-30 (14) 6-20 (10) 5-20 (10) Флаулты красных крови (MMOL / L) 8 0.5-1.4 0.5-1.4 (0,84) 0,45-1,3 (0,75) Лактат дегидрогеназа (LDH) (U / L) 2 115-211 115-211 70052 9104 80-447 82-524 82-524 Haptoglobin (G / L) 9 0,3 –2,0 0,44–0.49 (0.47) 0.24-0.32 (0.28) 0.27-0.36 (0.32) Total Bilirobin (MMOL / L) 2 5-22 2–7 2–14 2–19 Несоедин. Билирубин (ммоль / л) 2 3-15 2-7 2-7 2-8 нб.Эти контрольные интервалы включены исключительно для иллюстрации тенденций изменений во время беременности. Это , а не , которые следует использовать в качестве эталонных интервалов для диагностики и лечения пациентов. Клиницисты должны использовать эталонные интервалы в соответствии с лабораторией, в которой проводилось тестирование. Анемия во время беременности определяется Всемирной организацией здравоохранения (ВОЗ) как уровень гемоглобина менее 110 г/дл в первом и третьем триместрах и менее 105 г/дл во втором триместре. По оценкам, анемией страдают 30% женщин детородного возраста и более 40% беременных женщин во всем мире.Наибольшая распространенность анемии у беременных в Юго-Восточной Азии (48,7%) и Африке (46,3%). 10 Средний объем эритроцитов (MCV) увеличивается в среднем на 4 фл во время беременности у здоровых женщин, получающих достаточное количество железа. 11 У женщин, не получающих препараты железа, средний корпускулярный Hb (MCH) снижается с конца второго триместра с дальнейшим значительным снижением после родов, а средняя корпускулярная концентрация Hb (MCHC) постепенно снижается до конца третьего триместра. 11 У женщин, получающих достаточное количество железа, MCH и MCHC не изменяются во время беременности. Наиболее частой причиной микроцитоза (MRC) во время беременности является дефицит железа, за которым следует признак талассемии. Как правило, снижение MCV при дефиците железа пропорционально снижению Hb, тогда как при талассемии снижение MCV пропорционально больше, чем снижение Hb. Скрининг гемоглобинопатии с помощью электрофореза гемоглобина рекомендуется всем женщинам африканского, средиземноморского, ближневосточного, юго-восточного азиатского или западно-индийского происхождения. 12 Электрофорез гемоглобина также рекомендуется всем другим женщинам с низким MCH или MCV при скрининге общего анализа крови. В швейцарском исследовании предложен целевой скрининг несерповидной гемоглобинопатии у беременных женщин без анемии с MCV <80 фл, MCH <27,5 пг или MRC >3%, а также у женщин с анемией с MCV <76 фл, MCH <24 пг или MRC> 10%. 13 Материнская анемия во время беременности связана с повышенной частотой преждевременных родов, низкой массой тела при рождении, отслойкой плаценты, преэклампсией и послеродовыми кровотечениями. 14 , 15 , 16 , 17 , , 18 , 19 , 20 Сильная анемия связана с повышенным риском смерти материнской аОР 2.36). 21 Дополнительные материнские эффекты с анемией во время беременности включают повышенную восприимчивость к инфекции, повышенную вероятность переливания крови и повышенный риск послеродовой депрессии. 18 Неблагоприятные исходы анемии матери для плода включают задержку роста и развития, нарушение психомоторного и умственного развития, повышенный риск когнитивных и поведенческих отклонений, а также повышенную перинатальную и неонатальную смертность. 22 , 23 Железодефицитная анемия на поздних сроках беременности связана с нарушением слухового созревания новорожденных. 24 Уровни иммунореактивного эритропоэтина (ЭПО) в сыворотке остаются неизменными по сравнению со значениями до зачатия в первом триместре, абсолютные значения постепенно увеличиваются примерно в 2–4 раза во втором и третьем триместрах. 25 , 26 Однако уровни ЭПО ниже расчетного значения гематокрита в первом и втором триместрах, в целом согласуясь со значениями гематокрита в третьем триместре и после родов. Анемия часто встречается у женщин с инфекцией, вызванной вирусом иммунодефицита человека (ВИЧ), особенно у женщин с прогрессирующим заболеванием или у женщин, принимающих антиретровирусные препараты, такие как зидовудин. У большинства людей с ВИЧ наблюдается неадекватное повышение уровня ЭПО в сыворотке для данной степени анемии. 27 Деформируемость эритроцитов снижена в первом триместре по сравнению с небеременными контрольными женщинами и еще больше снижается во втором и третьем триместре. Кроме того, деформируемость эритроцитов при преэклампсии значительно ниже, чем при здоровой беременности в третьем триместре. 28 Малярия является важной причиной тяжелой анемии. Диагноз малярии основывается на обнаружении паразитов в толстом и тонком мазках крови, а также на экспресс-тестах диагностики малярии. В районах, где малярия эндемична и беременные женщины могут иметь высокий фоновый уровень иммунитета, инфекция, как правило, не связана с лихорадкой, но может быть связана с тяжелой анемией. Периферические мазки часто отрицательны, несмотря на плацентарную инфекцию. 29 Чувствительность высокочувствительных экспресс-тестов, обычных экспресс-тестов и световой микроскопии для выявления малярии в образцах периферической крови у беременных женщин в условиях низкой передачи инфекции составила 86%, 83% и 77% соответственно. 30 Количество лейкоцитов значительно увеличивается при здоровой беременности из-за нейтрофильного лейкоцитоза. Типичные референтные интервалы во время беременности составляют 6–16 × 10 9 /л. 31 , 2 Количество лейкоцитов заметно возрастает во время нормальных родов со средним числом лейкоцитов 10–16 × 10 9 /л и верхним уровнем 29 × 10 9 /л. 32 , 33 Введение бетаметазона для содействия созреванию легких плода приводит к среднему увеличению количества нейтрофилов на 35% и снижению количества лимфоцитов на 45%, общее количество лейкоцитов увеличивается в среднем до 13.5 × 10 9 /л, при этом максимальные значения лейкоцитов обычно составляют менее 20 × 10 9 /л. 34 , 35 Как правило, нейтрофильный лейкоцитоз достигает пика через 24 часа после введения кортикостероидов, хотя повышение сохраняется не менее 5 дней. 36 Незрелые формы лейкоцитов, такие как миелоциты и метамиелоциты, могут быть обнаружены в мазке периферической крови здоровых женщин во время беременности. 37 Количество лимфоцитов уменьшается в первом и втором триместре, а затем увеличивается в третьем триместре.Уровни моноцитов увеличиваются в первом триместре, затем снижаются по мере развития беременности. Количество эозинофилов и базофилов остается неизменным во время беременности. 38 Связанные с беременностью изменения лейкоцитов сохраняются в течение 6–8 недель после родов. Лейкоцитоз не является отличительным признаком у беременных женщин с поражением печени, характерным для острого жирового гепатоза беременных (ОЖЖП), тяжелой преэклампсии (ПЭТ)/гемолиза, повышенного уровня печеночных ферментов и синдрома низкого количества тромбоцитов (HELLP), сепсиса и тромботическая тромбоцитопеническая пурпура / гемолитико-уремический синдром (ТТП-ГУС). Исследования, изучающие изменения количества тромбоцитов во время нормальной беременности, дали противоречивые результаты. В семи лонгитюдных исследованиях сообщалось об уменьшении количества тромбоцитов во время беременности, а в четырех — об отсутствии изменений. 39 Тромбоцитопения, определяемая как количество тромбоцитов менее 150 × 10 9 /л, осложняет примерно 8–10% беременностей. 40 , 41 При неосложненной беременности и родах у 1% женщин число тромбоцитов было менее 100 × 10 9 /л. 41 Годовое проспективное исследование беременных индийских женщин с количеством тромбоцитов менее 100 × 10 9 /л показало, что 12% случаев произошли до 20 недель беременности, 24% были диагностированы между 20 и 29 неделями беременности, и 64% произошли между 30 неделями беременности и сроком. 42 Примерно в 75% случаев причиной является гестационная тромбоцитопения, в 21% — ПЭТ/HELLP, а в 4% — иммунная тромбоцитопения (ИТП). Менее распространенные причины включают системную красную волчанку, антифосфолипидный синдром, TTP-HUS, острую жировую дистрофию печени беременных (AFLP), диссеминированное внутрисосудистое свертывание крови (DIC), ВИЧ-инфекцию, гиперспленизм и медикаментозное лечение.При отсутствии ранее ненормального результата может быть трудно дифференцировать ИТП от гестационной тромбоцитопении. Характеристики гестационной тромбоцитопении включают относительно легкую тромбоцитопению (>70 000 × 10 9 /л), отсутствие в анамнезе тромбоцитопении до зачатия или на ранних сроках беременности, возвращение количества тромбоцитов к нормальному диапазону в течение 12 недель после родов и отсутствие кровотечения в анамнезе. Нет единого мнения относительно количества тромбоцитов, выше которого безопасно проводить нейроаксиальную анестезию.Руководящие принципы Британского комитета по стандартам в гематологии рекомендуют количество тромбоцитов выше 80 × 10 9 /л для нейроаксиальной блокады у женщин с ИТП. 43 Тромбоэластография (ТЭГ) одновременно измеряет коагуляцию и фибринолиз и может быть лучшим тестом, чем анализ функции тромбоцитов у беременных женщин с тромбоцитопенией. 44 Во время беременности ТЭГ демонстрирует повышенную свертываемость и снижение фибринолиза по сравнению с 8 нед после родов. 45 Гемостаз происходил на 20–35% быстрее, и было продемонстрировано незначительное увеличение прочности сгустка. В одной серии случаев предполагалось, что нейроаксиальная блокада может быть выполнена у беременных женщин с числом тромбоцитов более 56 × 10 9 /л и нормальной тромбоэластографией. 46 TTP-HUS и синдром HELLP имеют общие признаки тромбоцитопении, гемолиза, нарушения функции печени и могут осложняться острым повреждением почек и судорогами. Крайне важно дифференцировать TTP-HUS от HELLP, поскольку TTP-HUS обычно следует за полиорганной недостаточностью, приводящей к смерти без плазмафереза (таблица 2).Гемолиз при ТТП-ГУС обычно тяжелый с фрагментированными эритроцитами/шистоцитами в мазке крови, заметно повышенным уровнем лактатдегидрогеназы (ЛДГ), повышенным непрямым билирубином, низким уровнем гаптоглобина и гемоглобинурией. Функциональные пробы печени обычно слегка повышены при TTP-HUS по сравнению с более выраженным повышением при HELLP. В одном исследовании было обнаружено, что соотношение ЛДГ: аспартатаминотрансферазы (АСТ) выше 22,12 является диагностическим признаком TTP-HUS, а не HELLP-синдрома. 47 Активность ADAMS-TS 13 обычно составляет <10% при TTP-HUS, в то время как средняя активность ADAMS-TS 13 составляет 31% при HELLP. 48 При здоровой беременности активность ADAMTS13 прогрессивно снижалась с 12 до 16 недель беременности, достигая среднего уровня 52% (диапазон 22–89) в конце раннего послеродового периода. 49 2 Дифференциальный гемолиз, повышенный уровень ферментов печени и низкий уровень тромбоцитов (HELLP) от тромботической тромбоцитопенической пурпуры (ТТП). Характеристика HELLP ТТП тромбоцитопения Переменная Среднее число тромбоцитов 25 × 10 9 / л 25% + Редкие Неврологическое участие Редкие эклампсии 75% Повышенные трансаминаз Сильной Mild Острое повреждение почек 7– 36% 80-90% 9039 Common Переменная Уровни антитробин III 60-80% 85- 120% (нормальный) LDH: AST Соотношение <22 > 22 Среднее 31% <10% 9039 Диссерированные внутрисосудистые коагуляции (DIC) 5-13% Reedumber по сравнению с небеременными женщинами, рассмотрение костного мозга здоровых беременных женщин повышение клеточности во второй половине беременности и первые 8 дней после родов, увеличение нормобластического эритропоэза лейкоз с повышенным количеством ядерных эритроцитов, повышенным гранулопоэзом и небольшим увеличением плазматических клеток и клеток фагоцитарного ретикулума. 50 Активированное частичное тромбопластиновое время (АЧТВ), протромбиновое время (ПВ) и тромбиновое время снижаются на 10–20 % с момента зачатия до третьего триместра здоровой беременности. 51 , 52 52 52 , 53 , 54 , , 3 , 55 Авторы цитируют ссылочные интервалы 8,5-11,05, 8,5-12,4 и 9,5-12,6 s для PT в третьем триместре.Продолжительное ПТ является практически универсальным признаком AFLP. 56 Исследования, изучающие возможные физиологические изменения антитромбина III (ATIII) во время неосложненной беременности, дали противоречивые результаты. В нескольких исследованиях не было описано никаких изменений ATIII на протяжении всей беременности по сравнению со значениями до зачатия. 52 , 57 57 57 , 58 , 59 , , 60 Другие авторы сообщили о падении в Atiii из Мидтримера, третий триместр ценностей на 13% -20% ниже беременные значения. 3 , 61 , 62 Снижение уровня ATIII во время беременности было больше при многоплодной беременности, чем при одноплодной. 62 Сразу после родов уровни ATIII снижаются, достигая надира (средний уровень ATIII 76%) через 12 часов после родов, прежде чем вернуться к исходному уровню через 72 часа после родов. 61 Активность ATIII ниже при преэклампсии, чем при неосложненной беременности, со средним уровнем от 60% до 85% в пяти исследованиях. 63 , , 64 64 , 65 , 66 , , , 67 , , 68 64 , 66 , 67 , 69 Считается, что низкий уровень ATIII при синдроме HELLP возникает в первую очередь в результате повышенного потребления, а не увеличения потерь мочи. 70 Уровень ATIII считается полезным для дифференциации AFLP от HELLP. Обзор 61 случая в литературе женщин с диагнозом AFLP показал, что средний уровень ATIII составляет 16,1% (диапазон 0–69%). 56 ATIII может быть низким при AFLP из-за сниженного печеночного синтеза, измененного коэффициента транскапиллярного потока, коагулопатии потребления и потери мочи с протеинурией. 71 , 72 При здоровой беременности наблюдается значительное снижение уровней общего и свободного белка S с первого по второй триместр. 73 Описана большая вариабельность изменений протеина С, при этом в некоторых исследованиях обнаружено увеличение протеина С, а в других исследованиях никаких изменений по сравнению с небеременными взрослыми. Резистентность к активированному протеину С оставалась постоянной на протяжении всей беременности. Обследование беременных женщин с тромбоэмболическими осложнениями на дефицит протеина S следует отложить до 3 месяцев после родов. Распространенность антикардиолипиновых антител, анти-β2 гликопротеина 1 и волчаночного антикоагулянта при здоровой беременности составляет 1,6–11%, 2–3,9% и 7–8% соответственно. 74 , , 75 75 , 76 , , 77 77 Уровни фибриногена значительно во время беременности значительно возникают во время беременности, а использование небеременных референс-интервалов может недооценивать распространенность распространенной внутрисосудистой коагуляции (DIC) . 78 , 79 Уровень фибриногена менее 3 г/л вместе с количеством тромбоцитов менее 50 и удлиненным ПВ и АЧТВ согласуется с ДВС-синдромом при беременности.Модифицированная шкала беременности, учитывающая физиологические изменения протромбинового времени, фибриногена и тромбоцитов, показала чувствительность 88% и специфичность 96% для диагностики ДВС-синдрома (таблица 3). 80 ДВС-синдром осложняет 0,03% беременностей. Причины включают отслойку плаценты (37%), послеродовое кровотечение (29%), ПЭТ/HELLP (14%), AFLP (8%), сепсис (6%) и эмболию околоплодными водами (6%). Коагулопатия/ДВС-синдром гораздо реже встречается при HELLP-синдроме, чем при AFLP. Шесть исследований описали ДВС-синдром, осложняющий 5.6–13% случаев HELLP-синдрома. 69 , 81 81 , 82 , , 83 , , 84 , 85 20-летний обзор обнаружил, что DIC сложно только 0,2% случаев тяжелого домашнего животного . 86 Серия случаев AFLP сообщала о ДВС-синдроме у 16–77% пациентов. 56 Уровень D-димера неуклонно повышается во время беременности. 87 , 88 Исследования показали, что уровни D-димера превышают порог отсутствия беременности у 15–50% женщин в первом триместре, 67–78% во втором триместре и 96–100% в третьем триместре. 88 , 89 , 90 Уровни D-димера заметно повышены во время родов, быстро снижаясь в течение первых 3 дней после родов, хотя нормализация может наступить только через 4 недели после родов. 91 Были предложены пороговые значения D-димера для беременных; однако валидированные пороговые значения для исключения тромбоэмболии отсутствуют. Роль оценки клинической вероятности в диагностическом ведении беременных неясна.Руководства профессиональных обществ содержат противоречивые рекомендации. Пока не будут проведены дальнейшие валидационные исследования, алгоритмы, основанные на измерении D-димера, не следует использовать для исключения легочной эмболии во время беременности или после родов. 3 Модифицированный показатель синдрома диссеминированного внутрисосудистого свертывания крови (ДВС-синдром) при беременности. 74 Ссылки
1. Аббасси-Ганавати М., Грир Л.Г., Каннингем Ф.Г. Беременность и лабораторные исследования: справочная таблица для клиницистов [опубликованные опечатки появляются в Obstet Gynecol 2010;115:387]. Obstet Gynecol 2009;114:1326–31.
2. Берроуз Р.Ф., Келтон Дж.Г. Фетальная тромбоцитопения и ее связь с материнской тромбоцитопенией. N Engl J Med 1993;329:1463–6.
3. Бёлен Ф., Холфельд П., Экстерманн П., Пернегер Т.В., де Мёрлуз П.Количество тромбоцитов при доношенной беременности: переоценка порога. Obstet Gynecol 2000;95:29–33.
4. Сайнио С., Кекомаки Р., Рииконен С., Терамо К. Тромбоцитопения у матери в срок: популяционное исследование. Acta Obstet Gynecol Scand 2000;79:744–9.
5. Кауфман Р.М., Джулбегович Б., Гернсхаймер Т., Клейнман С., Тинмут А.Т., Капочелли К.Е. и соавт. Переливание тромбоцитов: руководство по клинической практике от AABB. Ann Intern Med 2015; 162: 205–13.
6. Гернсхаймер Т., Джеймс А.Х., Стази Р.Как я лечу тромбоцитопению при беременности. Кровь 2013; 121:38–47.
7. Прован Д., Стази Р., Ньюленд А.С., Бланшетт В.С., Болтон-Маггс П., Бассел Дж.Б. и соавт. Международный консенсусный отчет по исследованию и лечению первичной иммунной тромбоцитопении. Кровь 2010; 115: 168–86.
8. Берроуз Р.Ф., Келтон Дж.Г. Тромбоцитопения при родах: проспективное исследование 6715 родов. Am J Obstet Gynecol 1990;162:731–4.
9. Руджери М., Скьявотто К., Кастаман Г., Тосетто А., Родегьеро Ф.Гестационная тромбоцитопения: проспективное исследование. Гематология 1997;82:341–2.
10. Американский колледж акушеров и гинекологов. Гипертония при беременности. Вашингтон, округ Колумбия: Американский колледж акушеров и гинекологов; 2013.
11. Сибай Б.М. Диагностика, противоречия и лечение синдрома гемолиза, повышенных ферментов печени и низкого количества тромбоцитов. Obstet Gynecol 2004;103:981–91.
12. Чайворапонгса Т., Чемсайтонг П., Йео Л., Ромеро Р.Преэклампсия, часть 1: современные представления о ее патофизиологии. Nat Rev Nephrol 2014; 10: 466–80.
13. Ромеро Р., Мазор М., Локвуд С.Дж., Эмамиан М., Беланже К.П., Хоббинс Дж.С. и соавт. Клиническое значение, распространенность и естественное течение тромбоцитопении при артериальной гипертензии, вызванной беременностью. Ам Дж. Перинатол 1989; 6: 32–8.
14. Стэнворт С.Дж. Тромбоцитопения, кровотечения и переливание тромбоцитов у больных новорожденных. Гематология Am Soc Hematol Educ Program 2012; 2012: 512–6.15. Родегьеро Ф., Стази Р., Гернсхаймер Т., Мишель М., Прован Д., Арнольд Д.М. и соавт. Стандартизация терминологии, определений и критериев результатов при иммунной тромбоцитопенической пурпуре у взрослых и детей: отчет международной рабочей группы. Кровь 2009; 113: 2386–93.
16. Веберт К.Е., Миттал Р., Сигуин С., Хеддл Н.М., Келтон Дж.Г. Ретроспективный 11-летний анализ акушерских пациенток с идиопатической тромбоцитопенической пурпурой. Кровь 2003; 102: 4306–11.
17.Лусто В., Дебувери О., Кануи-Пуатрин Ф., Байли Л., Хеллаф М., Тубул С. и др. Влияние беременности на течение иммунной тромбоцитопении: ретроспективное исследование 118 беременностей у 82 женщин. Бр Дж. Гематол 2014; 166:929–35.
18. Кьелдсен-Краг Дж., Килли М.К., Томтер Г., Голебёвска Э., Ранден И., Хауге Р. и соавт. Программа скрининга и вмешательства, направленная на снижение смертности и серьезных осложнений, связанных с тяжелой неонатальной аллоиммунной тромбоцитопенией. Кровь 2007; 110: 833–9.
19.Тернер М.Л., Бессос Х., Фагге Т., Харкнесс М., Рентул Ф., Сеймур Дж. и др. Проспективное эпидемиологическое исследование результатов и экономической эффективности антенатального скрининга для выявления неонатальной аллоиммунной тромбоцитопении, вызванной анти-HPA-1a. Переливание 2005; 45: 1945–56.
20. Уильямсон Л.М., Хакетт Г., Ренни Дж., Палмер К.Р., Макивер С., Хэдфилд Р. и соавт. Естественная история фето-материнской аллоиммунизации тромбоцит-специфическим антигеном HPA-1a (PlA1, Zwa), определяемая антенатальным скринингом.Кровь 1998; 92: 2280–7.
21. Найт М., Пирс М., Аллен Д., Куринчук Дж.Дж., Спарк П., Робертс Д.Дж. и др. Заболеваемость и исходы фетоматеринской аллоиммунной тромбоцитопении: национальное исследование Великобритании с использованием трех источников данных. Бр Дж. Хэматол 2011; 152:460–8.
22. Тиллер Х., Камфуис М.М., Флодмарк О., Пападогианнакис Н., Дэвид А.Л., Сайнио С. и соавт. Внутричерепные кровоизлияния у плода, вызванные аллоиммунной тромбоцитопенией у плода и новорожденного: обсервационное когортное исследование 43 случаев из международного многоцентрового регистра.BMJ Open 2013;3(3):e002490.
23. Берковиц Р.Л., Бассел Дж.Б., МакФарланд Дж.Г. Аллоиммунная тромбоцитопения: современное состояние, 2006 г. Am J Obstet Gynecol 2006;195:907–13.
24. Спенсер Дж. А., Берроуз РФ. Фето-материнская аллоиммунная тромбоцитопения: обзор литературы и статистический анализ. Aust NZ J Obstet Gynaecol 2001;41:45–55.
25. Бассел Дж. Б., Забуски М. Р., Берковиц Р. Л., МакФарланд Дж. Г. Аллоиммунная тромбоцитопения плода. N Engl J Med 1997; 337: 22–6.
26.Нейгер Р., Contag SA, Coustan DR. Разрешение тромбоцитопении, связанной с преэклампсией. Obstet Gynecol 1991;77:692–5.
27. Мартин Дж. Н. мл., Блейк П.Г., Лоури С.Л., Перри К.Г. мл., Файлз Дж. С., Моррисон Дж. К. Беременность, осложненная преэклампсией-эклампсией с синдромом гемолиза, повышением активности печеночных ферментов, снижением количества тромбоцитов: насколько быстро происходит послеродовое восстановление? Obstet Gynecol 1990;76:737–41.
28. Кац В.Л., Торп Дж.М. мл., Розас Л., Боуз В.А. мл. Естественная история тромбоцитопении, связанной с преэклампсией.Am J Obstet Gynecol 1990;163:1142–3.
29. Вудстра Д.М., Чандра С., Хофмейр Г.Дж., Доусвелл Т. Кортикостероиды при синдроме HELLP (гемолиз, повышенный уровень ферментов печени, низкий уровень тромбоцитов) при беременности. Кокрановская база данных систематических обзоров, 2010 г., выпуск 9. Ст. №: CD008148. DOI: 10.1002/14651858.CD008148.pub2.
30. Рагаб А., Года Х., Рагиб М., Баракат Р., Эль-Самануди А., Бадави А. Ускоряет ли немедленное послеродовое выскабливание эндометрия выздоровление от преэклампсии-эклампсии? Рандомизированное контролируемое исследование.Arch Gynecol Obstet 2013; 288:1035–8.
31. Нойнерт С., Лим В., Кроутер М., Коэн А., Сольберг Л. мл., Кроутер М. А. Американское общество гематологов, 2011 г., основанное на фактических данных практическое руководство по иммунной тромбоцитопении. Американское общество гематологов. Кровь 2011; 117:4190–207.
32. Ван Вин Дж. Дж., Нокес Т. Дж., Макрис М. Риск спинномозговой гематомы после нейроаксиальной анестезии или люмбальной пункции у лиц с тромбоцитопенией. Бр Дж. Хэматол 2010; 148:15–25.
33.Каплан С., Даффос Ф., Форестье Ф., Терциан Г., Кэтрин Н., Понс Дж. К. и др. Тромбоциты плода при тромбоцитопенической беременности. Ланцет 1990; 336: 979–82.
34. Пейн С.Д., Резник Р., Мур Т.Р., Хедриана Х.Л., Келли Т.Ф. Материнские характеристики и риск тяжелой неонатальной тромбоцитопении и внутричерепного кровоизлияния при беременности, осложненной аутоиммунной тромбоцитопенией. Am J Obstet Gynecol 1997;177:149–55.
35. Берроуз Р.Ф., Келтон Дж.Г. Низкий риск для плода при беременности, связанной с идиопатической тромбоцитопенической пурпурой.Am J Obstet Gynecol 1990;163:1147–50.
36. Берри С.М., Стоун Дж., Нортон М.Е., Джонсон Д., Бергелла В. Забор крови плода. Общество медицины матери и плода (SMFM). Am J Obstet Gynecol 2013;209:170–80.
37. Макфарланд Дж. Г., Астер Р. Х., Бассел Дж. Б., Джанопулос Дж. Г., Дербес Р. С., Ньюман П. Дж. Пренатальная диагностика неонатальной аллоиммунной тромбоцитопении с использованием аллель-специфических олигонуклеотидных зондов. Кровь 1991; 78: 2276–82.
38. Камфуис М.М., Паридаанс Н., Порселейн Л., Де Хаас М., Ван Дер Шут С.Э., Бренд А и др.Скрининг беременных на аллоиммунную тромбоцитопению плода или новорожденного: систематический обзор. БДЖОГ 2010; 117:1335–43.
39. Пачеко Л.Д., Берковиц Р.Л., Мойзе К.Дж. младший, Бассел Дж.Б., МакФарланд Дж.Г., Сааде Г.Р. Аллоиммунная тромбоцитопения плода и новорожденного: алгоритм ведения, основанный на стратификации риска. Obstet Gynecol 2011;118:1157–63.
40. Бассель Дж. Б., Берковиц Р. Л., Хунг С., Колб Э. А., Виссерт М., Примиани А. и соавт. Внутричерепное кровоизлияние при аллоиммунной тромбоцитопении: стратифицированное ведение для предотвращения рецидива у последующего пораженного плода.Am J Obstet Gynecol 2010;203:135.e1–14.
41. Берковиц Р.Л., Колб Э.А., МакФарланд Дж.Г., Виссерт М., Примани А., Лессер М. и соавт. Параллельные рандомизированные исследования риск-ориентированной терапии аллоиммунной тромбоцитопении плода. Obstet Gynecol 2006;107:91–6.
42. Каплан С., Даффос Ф., Форестье Ф., Кокс В.Л., Лион-Кан Д., Дюпюи-Монбрун М.С. и соавт. Лечение аллоиммунной тромбоцитопении: антенатальная диагностика и внутриутробное переливание материнских тромбоцитов. Кровь 1988; 72: 340–3.
43.Боуман Дж., Харман С., Ментиголоу С., Поллок Дж. Внутривенное переливание иммуноглобулина плоду при аллоиммунной тромбоцитопении. Ланцет 1992;340:1034–5.
44. Циммерманн Р., Хуч А. Внутриутробно-фетальная терапия иммуноглобулином при аллоиммунной тромбоцитопении. Ланцет 1992;340:606.
45. Берковиц Р.Л., Лессер М.Л., МакФарланд Дж.Г., Виссерт М., Примиани А., Хунг С. и соавт. Дородовое лечение без раннего кордоцентеза при аллоиммунной тромбоцитопении стандартного риска: рандомизированное контролируемое исследование.Obstet Gynecol 2007;110:249–55. Гематологические нормальные диапазоны при беременности | Статья
Мортон А, Глоб. библиотека женская медицина .,
ISSN: 1756-2228; DOI 10.3843/GLOWM.413403 АВТОРЫ
Подробности см. в конце главы ВВЕДЕНИЕ
КОЛИЧЕСТВО ЭРИТРИЦ
38 2 9102 3 905 9005) (0,65) КОЛИЧЕСТВО ЛЕЙКоцитов
PLATELET COUNT
гемолиза Переменные Тяжелые + Лихорадка Отсутствует желтуха 5-10% 9
9
Аспирация костного мозга
ПРОФИЛЬ КОАГУЛЯЦИИ
Параметры | ||
Количество тромбоцитов (× 10 9 / L) | <50 = 1 | |
50-100 = 2 | ||
100-18562 100-185 = 2 | ||
> 185 = 0 | ||
Время протромбина (пациента / нормальное значение) | 0.5-1 = 5 | |
1.0-1.5362 1.0-1.5 = 12 | ||
> 1.5 = 25 | ||
фибриноген (G / L) | ≤3,0 = 25 | |
3.0-4.0 = 6 | ||
4.0-4.5 = 1 | ||
> 4.5 = 0 | ||
Общая оценка | > 26 = высокая вероятность DIC |
Уровни фактора фон Виллебранда (ФВ) увеличиваются примерно в 2 раза от периода до зачатия до третьего триместра, достигая пика незадолго до рождения как у здоровых женщин, так и у лиц с болезнью фон Виллебранда (БВ). 4 Активность фактора Виллебранда после родов и активность фактора VIII (FVIII : C) остаются на более высоком уровне в течение 2 дней, а затем начинают снижаться на третий день после родов. 92 У 32 женщин с болезнью Виллебранда типа 1 активность ФВ: Ag и фактора VIII (FVIII : C) нормализовалась во время беременности, кофактор ристоцетина фон Виллебранда (ФВ : RCo) оставался ниже нормального уровня для небеременных только у трех пациенток. . 93 В четырех из девяти беременностей у женщин с болезнью Виллебранда 2 типа все факторы свертывания нормализовались в третьем триместре.Однако качественные отклонения у женщин с болезнью Виллебранда 2 типа будут сохраняться, и тромбоцитопения может ухудшиться. Для регионарной анестезии, родоразрешения и, по крайней мере, в течение первых 5 дней после родов уровни фактора Виллебранда и фактора VIII: C следует поддерживать на уровне более 50 МЕ/мл. Низкий FVIII : C, по-видимому, является наиболее важным фактором, определяющим послеродовое кровотечение. Уровни фактора Виллебранда могут быстро падать после родов, а чрезмерное кровотечение может возникнуть уже через 21 день после родов.
РЕАКТИВЫ ОСТРОЙ ФАЗЫ
В большинстве исследований сообщается, что уровни С-реактивного белка (СРБ) остаются неизменными во время здоровой беременности, хотя в первые 2 дня после родов уровни повышаются в четыре раза. 94 , 95 , 96 , 97
Скорость оседания эритроцитов (СОЭ) В исследовании с участием 1019 женщин референтный диапазон 95% у женщин без анемии вырос с 4–57 мм/ч в первом триместре до 13–70 мм/ч в третьем триместре. Соответствующие значения у женщин с анемией составляли 8–83 мм/ч во втором триместре и 12–91 мм/ч в третьем триместре. 5
Таким образом, СРБ предпочтительнее, чем СОЭ, как индикатор воспаления или инфекции во время беременности.
ИССЛЕДОВАНИЯ ЖЕЛЕЗА
Уровень ферритина в сыворотке обычно достаточен для диагностики дефицита железа, за исключением случаев активного воспаления, поскольку ферритин действует как реагент острой фазы. Диагностические пороги дефицита железа во время беременности значительно различаются. В то время как ВОЗ определяет железодефицитную анемию на основе сывороточного ферритина <15 нг/мл, беременные женщины с сывороточным уровнем ферритина <30 нг/мл считаются подверженными риску железодефицитной анемии в Соединенном Королевстве, а в Дании предполагается, что женщинам с сывороточным ферритином <70 г/мл следует назначить препараты железа. 98 Сывороточный ферритин постепенно снижается с первого триместра и достигает надира к третьему триместру примерно на 50% от значений до зачатия, независимо от баланса железа. 99
Исследования, связывающие наличие или отсутствие окрашиваемого железа в костном мозге с сывороточным ферритином, показали, что уровень <30 нг/мл имеет 92% чувствительность и 98% специфичность для диагностики дефицита железа, тогда как сывороточный ферритин менее 10 нг /мл имеет только 25% чувствительность при выявлении дефицита железа. 100 , 101
В условиях острого воспаления может быть полезным измерение насыщения трансферрина (TS). TS менее 16% считается маркером функционального дефицита железа.
Использование микроцитоза при скрининге приводит к недооценке распространенности железодефицитной анемии, так как снижение уровня гемоглобина обычно предшествует снижению среднего объема эритроцитов. 102 Микроцитоз присутствовал только у 27,5–65% пациентов с дефицитом железа. 103 , 104 Уровни растворимых рецепторов трансферрина увеличиваются при дефиците железа и не зависят от воспаления. Метаанализ 10 исследований показал, что уровни растворимых рецепторов трансферрина имеют чувствительность 86% и специфичность 75% при выявлении дефицита железа. 105 Анализ не стандартизирован и не широко доступен. Гепсидин регулирует системную биодоступность железа, определяя, насколько хорошо железо всасывается при пероральном приеме. Уровни гепсидина падают во время беременности, женщины с неопределяемым уровнем передают плоду больше железа, поступившего от матери, чем женщины с определяемым уровнем гепсидина.Оценивается полезность уровней гепсидина в качестве биомаркера дефицита железа, одно недавнее исследование показало, что сывороточный гепсидин превосходит гемоглобин, сывороточное железо, сывороточный ферритин, TS и способность связывать железо трансферрина в качестве показателя ЖДА у беременных женщин. 106 Гепсидин может быть особенно полезен при выявлении дефицита железа при инфекционных или воспалительных заболеваниях.
На основании показателей эритроцитарного и ретикулоцитарного индексов, включая содержание Hb в ретикулоцитах и процент гипохромных эритроцитов и микроцитарных эритроцитов, Demmers et al. пришел к выводу, что, в отличие от небеременных женщин с дефицитом железа, низкие концентрации ферритина у беременных женщин не связаны с функциональным дефицитом железа. 98 Метаболизм железа может по-разному регулироваться для оптимального роста и развития плода, несмотря на низкие запасы железа у матери.
Уровни железа в сыворотке остаются относительно стабильными во время беременности. Уровень трансферрина в сыворотке увеличивается примерно на 10%. Насыщение трансферрина несколько падает. Железосвязывающая способность трансферрина постепенно увеличивается с первого триместра. 107
ВИТАМИН B12
Содержание общего витамина B12 в сыворотке значительно снижается во время беременности из-за снижения уровня хологаптокоррина. 108 Голотранскобаламин (активный B12), фракция B12, проникающая через плаценту, не изменяется и должна использоваться для диагностики дефицита B12 во время беременности. 7 Метилмалоновая кислота является наиболее специфическим функциональным индикатором статуса B12, поскольку гомоцистеин также определяется статусом фолиевой кислоты и других витаминов группы B. 109 Уровни витамина B12 значительно различаются у представителей разных национальностей, поэтому референтные интервалы во время беременности должны зависеть от популяции и лаборатории. Женщины южноазиатского происхождения, проживающие в Ванкувере, продемонстрировали значительно более низкие уровни витамина B12 и более высокие показатели дефицита и неадекватности витамина B12 в первом триместре, чем женщины европейского происхождения. 110 Сообщаемая распространенность дефицита B12 на ранних сроках беременности составляет до 70% в Индии по сравнению с 5–17% в Северной Америке.
ФОЛАТ
У женщин, не получавших добавки, уровни фолиевой кислоты в плазме и эритроцитах постепенно снижались с 16–18 недель беременности до 8 недель после родов, что сопровождалось реципрокным повышением уровня гомоцистеина в плазме. 8 , 111
МАРКЕРЫ ГЕМОЛИЗА
Некоторые авторы сообщают, что уровень ЛДГ может повышаться по сравнению с таковым в первом триместре, при этом значения у здоровых женщин в третьем триместре вдвое превышают значения до беременности. 2 Другие авторы сообщают об отсутствии изменений ЛДГ. 112 Исследования изоферментов ЛДГ у девяти женщин с HELLP-синдромом показали, что преобладающим типом является изофермент ЛДГ 5 (печень, скелетные мышцы) с относительным снижением изоферментов ЛДГ 1 и 2 (эритроциты, сердечная мышца). 113 Таким образом, общая ЛДГ не является надежным маркером внутрисосудистого гемолиза при синдроме HELLP.
Уровни гаптоглобина падают примерно на 25% по сравнению со значениями в первом триместре, достигая надира на 24–27 неделе беременности, а затем снова повышаются к концу здоровой беременности. 97 , 9 Одно исследование выявило низкий уровень гаптоглобина у 39% из 220 здоровых беременных женщин с прямой зависимостью между низким уровнем гаптоглобина и концентрацией гемоглобина. Авторы пришли к выводу, что причиной низких значений гаптоглобина, вероятно, была гемодилюция и повышение концентрации эстрогенов в крови во время беременности. 114 В клиническом случае также описаны неопределяемые уровни гаптоглобина на 31 неделе беременности без других признаков гемолиза, сывороточный гаптоглобин возвращается к нормальным значениям в течение 3 дней после родов. 115
Нет никаких изменений в субпопуляциях ретикулоцитов и зрелости между небеременными женщинами и женщинами в первом триместре. Со второго триместра происходит изменение зрелости ретикулоцитов со значительным увеличением числа незрелых ретикулоцитов и уменьшением числа зрелых ретикулоцитов. 116 , 117 Индекс зрелости ретикулоцитов резко снижается через 1–4 недели после родов, опускаясь до уровня небеременных женщин через 5 недель после родов.У курильщиков абсолютное количество ретикулоцитов в третьем триместре ниже, чем у некурящих. Могут быть значительные этнические различия в количестве ретикулоцитов при здоровой беременности, анемичные гречанки и итальянки демонстрируют значительно более высокое количество ретикулоцитов, чем англо-саксонские женщины. 118 Обычно, если количество ретикулоцитов превышает 3% при анемии, механизмом является гемолиз или кровопотеря, тогда как количество ретикулоцитов менее 3% указывает на гипопролиферативный костный мозг.
На протяжении всей беременности наблюдается легкое снижение верхней границы референтного интервала для общего и несвязанного билирубина. 119
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
- Физиологические изменения во время беременности могут привести к значительным изменениям нормальных значений многих гематологических анализов возможно, клиницисты должны использовать референтный интервал, характерный для лаборатории, проводившей тест.
КОНФЛИКТ ИНТЕРЕСОВ
Автор(ы) этой главы заявляют, что у них нет интересов, противоречащих содержанию главы.
Обратная связь
Примечание издателя: Мы постоянно стараемся обновлять и улучшать главы этой серии. Поэтому, если у вас есть какие-либо конструктивные комментарии по поводу этой главы, поделитесь ими с нами, выбрав ссылку «Ваш отзыв» в левой колонке.
ССЫЛКИ
1 | Morrison J PM.Анемия, связанная с беременностью. Glob Libr Women’s Med 2016. |
2 | Abbassi-Ghanavati M, Greer LG, Cunningham FG. Беременность и лабораторные исследования: справочная таблица для клиницистов. Obstet Gynecol 2009;114:1326–31. DOI: 10.1097/AOG.0b013e3181c2bde8. |
3 | Цуй С., Ян С., Чжан Дж., и др. Референсные интервалы коагуляции и антикоагуляции для здоровой беременности в зависимости от триместра. Thromb Res 2017; 156:82–6. DOI: 10.1016/j.thromres.2017.05.021. |
4 | Epiney M, Boehlen F, Boulvain M, et al. Уровни D-димера во время родов и после родов. J Thromb Haemost 2005;3:268–71. DOI: 10.1111/j.1538–7836.2004.01108.x. |
5 | Харам К., Аугенсен К., Эльсайед С. Характер белков сыворотки при нормальной беременности с особым упором на острофазовые реагенты. Br J Obstet Gynaecol 1983; 90:139–45. |
6 | Шекхар С., Дидди Г. Болезнь печени при беременности. Тайвань J Obstet Gynecol 2015; 54: 475–82. DOI: 10.1016/j.tjog.2015.01.004. |
7 | Моркбак А.Л., Хвас А.М., Мильман Н., и др. Голотранскобаламин остается неизменным во время беременности. Продольные изменения кобаламинов и связывающих их белков во время беременности и после родов. Haematologica 2007;92:1711–2. DOI: 10.3324/гематол.11636. |
8 | Мильман Н, Быг К.Е., Хвас А.М., и др. Фолиевая кислота в эритроцитах, фолиевая кислота в плазме и гомоцистеин в плазме при нормальной беременности и после родов: лонгитюдное исследование с участием 404 датских женщин. Eur J Haematol 2006;76:200–5. DOI: 10.1111/j.1600–0609.2005.00606.x. |
9 | Хэмм В., Ричардсен Г., Свитковски Р.Изоферменты лактатдегидрогеназы у больных с синдромом HELLP. Z Geburtshilfe Neonatol 1996;200:115–8. |
10 | Организация WH. Всемирная организация здравоохранения, Распространенность анемии в мире, 1993–2005 гг.: Глобальная база данных ВОЗ по анемии, 2008 г. |
11 | Мильман Н., Быг К.Е., Аггер А.О. Показатели гемоглобина и эритроцитов во время нормальной беременности и после родов у 206 женщин с добавками железа и без них. Acta Obstet Gynecol Scand 2000; 79:89–98. |
12 | Комитет G. Мнение Комитета № 691: Скрининг носителей генетических заболеваний. Obstet Gynecol 2017;129:e41–55. DOI: 10.1097/AOG.0000000000001952. |
13 | Бенцайова Г., Дапото К., Циммерманн Р., и др. Параметры эритроцитов при скрининге антенатальной несерповидной гемоглобинопатии. Int J Womens Health 2015; 7:379–84.DOI: 10.2147/IJWH.S73362. |
14 | Шолл ТО. Статус железа во время беременности: подготовка к матери и ребенку. Am J Clin Nutr 2005;81:1218S–22S. DOI: 10.1093/ajcn/81.5.1218. |
15 | Арнольд Д.Л., Уильямс М.А., Миллер Р.С., и др. Железодефицитная анемия, курение сигарет и риск отслойки плаценты. J Obstet Gynaecol Res 2009;35:446–52.DOI: 10.1111/j.1447–0756.2008.00980.x. |
16 | Виллар Дж., Мериальди М., Гулмезоглу А.М., и др. Вмешательства в области питания во время беременности для профилактики или лечения материнской заболеваемости и преждевременных родов: обзор рандомизированных контролируемых исследований. J Nutr 2003;133:1606S–25S. DOI: 10.1093/jn/133.5.1606S. |
17 | Сурьянараяна Р., Чандраппа М., Сантурам А.Н., и др. Проспективное исследование распространенности анемии беременных женщин и его исходов: исследование на базе сообщества. J Family Med Prim Care 2017;6:739–43. DOI: 10.4103/jfmpc.jfmpc_33_17. |
18 | Рахмати С., Милад Азами, Паризад Н., и др. Взаимосвязь материнской анемии во время беременности с преждевременными родами: систематический обзор и метаанализ. J Matern Fetal Neonatal Med 2018:1–151. DOI: 10.1080/14767058.2018.1555811. |
19 | Фигейреду А., Гомеш-Фильо И.С., Силва Р.Б., и др. Материнская анемия и низкий вес при рождении: систематический обзор и метаанализ. Питательные вещества 2018;10. DOI: 10.3390/nu10050601. |
20 | Chen C, Grewal J, Betran AP, et al. Тяжелая анемия, серповидно-клеточная анемия и талассемия как факторы риска гипертензивных расстройств во время беременности в развивающихся странах. Гипертензия беременных 2018;13:141–7. DOI: 10.1016/j.preghy.2018.06.001. |
21 | Дару Дж., Замора Дж., Фернандес-Феликс Б.М., и др. Риск материнской смертности у женщин с тяжелой анемией во время беременности и после родов: многоуровневый анализ. Lancet Glob Health 2018;6:e548&ndashe54. DOI: 10.1016/S2214–109X(18)30078–0. |
22 | Ауэрбах М., Джеймс С.Е., Николетти М., и др. Результаты первого американского проспективного исследования внутривенного введения железа беременным с дефицитом железа при пероральной непереносимости железа. Am J Med 2017; 130:1402–7. DOI: 10.1016/j.amjmed.2017.06.025. |
23 | Рахман М.М., Абэ С.К., Рахман М.С., и др. Материнская анемия и риск неблагоприятных исходов родов и здоровья в странах с низким и средним уровнем дохода: систематический обзор и метаанализ. Am J Clin Nutr 2016;103:495–504.DOI: 10.3945/ajcn.115.107896. |
24 | ElAlfy MS, El-Farrash RA, Taha HM, et al. Слуховая реакция ствола головного мозга у доношенных новорожденных, рожденных от матерей с железодефицитной анемией: связь с тяжестью заболевания. J Matern Fetal Neonatal Med 2018: 1–8. DOI: 10.1080/14767058.2018.1533940. |
25 | Бегин Ю., Липсей Г., Орис Р., и др. Сывороточный иммунореактивный эритропоэтин при беременности и в раннем послеродовом периоде. BrJ Haematol 1990;76:545–9. |
26 | Макмаллин М.Ф., Уайт Р., Лаппин Т., и др. Гемоглобин во время беременности: связь с эритропоэтином и кроветворным статусом. Eur J Haematol 2003; 71:44–50. |
27 | Henry DH, Beall GN, Benson CA, et al. Рекомбинантный человеческий эритропоэтин в лечении анемии, связанной с инфекцией, вызванной вирусом иммунодефицита человека (ВИЧ), и терапией зидовудином.Обзор четырех клинических испытаний. Ann Intern Med 1992;117:739–48. |
28 | Мицуи Ю., Эгучи К., Хирамацу Ю., и др. Изменения деформируемости эритроцитов при нормально протекающей беременности и гипертензии, вызванной беременностью, по данным электронного спинового резонанса. Acta Med Okayama 1994; 48:1–5. DOI: 10.18926/AMO/31133. |
29 | Шульман К.Э., Дорман Э.К., Балмер Дж.Н.Малярия как причина тяжелой анемии беременных. Ланцет 2002;360:494. DOI: 10.1016/s0140–6736(02)09662–9. |
30 | Васкес А.М., Медина А.С., Тобон-Кастано А., и др. Проведение высокочувствительного экспресс-теста (HS-RDT) для выявления малярии в образцах периферической и плацентарной крови беременных женщин в Колумбии. PLoS One 2018;13:e0201769. DOI: 10.1371/journal.pone.0201769. |
31 | Райли Л.К., Руперт Дж.Оценка пациентов с лейкоцитозом. Am Fam Physician 2015;92:1004–11. |
32 | Джеймс Д., Стир П., Вайнер С., и др. Беременность и лабораторные исследования: справочная таблица для врачей. Obstet Gynecol 2010;115:868; ответ автора 868–9. DOI: 10.1097/AOG.0b013e3181d7131e. |
33 | Пайдас М., Хоссейн Н. Гематологические изменения во время беременности. Гемостаз и тромбоз в акушерстве и гинекологии . Wiley, 2011, стр. 1–11. |
34 | Уоллес Э.М., Эккель К., Коттер Т., и др. Гематологические эффекты лечения бетаметазоном на поздних сроках беременности. Aust NZ J Obstet Gynaecol 1998;38:396–8. |
35 | Каданали С., Ингеч М., Кучукозкан Т., и др. Изменения количества лейкоцитов, гранулоцитов и лимфоцитов после антенатального введения бетаметазона беременным женщинам. Int J Gynaecol Obstet 1997; 58:269–74. |
36 | Bauer ME, Price LK, MacEachern MP, et al. Материнский лейкоцитоз после антенатального введения кортикостероидов: систематический обзор и метаанализ. J Obstet Gynaecol 2018;38:210–6. DOI: 10.1080/01443615.2017.1342614. |
37 | Каралис I, Надар СК, Аль-Йемени Э., и др. Активация тромбоцитов при артериальной гипертензии, вызванной беременностью. Thromb Res 2005; 116:377–83. DOI: 10.1016/j.thromres.2005.01.009. |
38 | Эдельстам Г., Лоубир К., Крал Г., и др. Новые референтные значения для стандартных образцов крови и нейтрофильного липокалина человека во время беременности в третьем триместре. Scand J Clin Lab Invest 2001;61:583–92. |
39 | Риз Дж. А., Пек Дж. Д., Макинтош Дж. Дж., и др. Количество тромбоцитов у женщин с нормальной беременностью: систематический обзор. Am J Hematol 2017;92:1224–32. DOI: 10.1002/ajh.24829. |
40 | Леви Дж.А., Мерфи Л.Д. Тромбоцитопения при беременности. J Am Board Fam Pract 2002;15:290–7. |
41 | Риз Дж.А., Пек Дж.Д., Дешам Д.Р., и др. Количество тромбоцитов во время беременности. N Engl J Med 2018; 379:32–43. DOI: 10.1056/NEJMoa1802897. |
42 | Пандей А. СР.Тромбоцитопения во время беременности: институциональное проспективное исследование продолжительностью один год. Международный журнал исследований в области медицинских наук 2017; 5:3502–5. |
43 | van Veen JJ, Nokes TJ, Makris M. Риск гематомы позвоночника после нейроаксиальной анестезии или люмбальной пункции у пациентов с тромбоцитопенией. Br J Haematol 2010; 148:15–25. DOI: 10.1111/j.1365–2141.2009.07899.x. |
44 | Бейлин Ю., Арнольд И., Хоссейн С.Оценка анализатора функции тромбоцитов (PFA-100) по сравнению с тромбоэластограммой (ТЭГ) у роженицы. Int J Obstet Anesth 2006; 15:7–12. DOI: 10.1016/j.ijoa.2005.04.013. |
45 | Карлссон О., Спорронг Т., Хилларп А., и др. Проспективное лонгитюдное исследование тромбоэластографии и стандартных гемостатических лабораторных тестов у здоровых женщин при нормально протекающей беременности. Anesth Analg 2012;115:890–8. ДОИ: 10.1213/АНЭ.0b013e3182652a33. |
46 | Huang J, McKenna N, Babins N. Полезность тромбоэластографии во время нейроаксиальной блокады у рожениц с тромбоцитопенией. AANA J 2014; 82: 127–30. |
47 | Кейзер С.Д., Бойд К.В., Реберг Дж.Ф., и др. Высокое отношение ЛДГ к АСТ помогает дифференцировать связанную с беременностью тромботическую тромбоцитопеническую пурпуру (ТТП) от HELLP-синдрома. J Matern Fetal Neonatal Med 2012;25:1059–63. DOI: 10.3109/14767058.2011.619603. |
48 | Латтуада А., Росси Э., Кальзаросса С., и др. Снижение уровня протеазы, расщепляющей фактор фон Виллебранда (ADAMTS-13), от легкой до умеренной у беременных с микроангиопатическим синдромом HELLP. Haematologica 2003; 88:1029–34. |
49 | Санчес-Лусерос А., Фариас К.Э., Амарал М.М., и др. Активность протеазы, расщепляющей фактор фон Виллебранда (ADAMTS13), у нормальных небеременных женщин, беременных женщин и женщин после родов. Thromb Haemost 2004;92:1320–6. DOI: 10.1160/TH03–11–0683. |
50 | Ловенштейн Л., Брэмлидж, Калифорния. Костный мозг при беременности и послеродовом периоде. Кровь 1957; 12: 261–77. |
51 | Хань Л., Лю С., Ли Х., и др. Показатели свертывания крови и индексы тромбоцитов: изменения при нормальной и преэклампсии при беременности и прогностические значения преэклампсии. PLoS One 2014;9:e114488. DOI: 10.1371/journal.pone.0114488. |
52 | Чернека Ф., Риччи Г., Симеоне Р., и др. Изменения коагуляции и фибринолиза при нормальной беременности. Повышенный уровень прокоагулянтов и сниженный уровень ингибиторов во время беременности вызывают состояние гиперкоагуляции в сочетании с реактивным фибринолизом. Eur J Obstet Gynecol Reprod Biol 1997;73:31–6. |
53 | Лю Дж., Юань Э., Ли Л.Специфические для гестационного возраста референтные интервалы для рутинных анализов гемостаза при нормальной беременности. Clin Chim Acta 2012; 413:258–61. DOI: 10.1016/j.cca.2011.09.046. |
54 | Гонг Дж.М., Шэнь И., Хе И.С. Референтные интервалы рутинных анализов коагуляции во время беременности и послеродового периода. J Clin Lab Anal 2016;30:912–7. DOI: 10.1002/jcla.21956. |
55 | Хуэй С., Лили М., Либин С., и др. Изменения коагуляции и гемодинамики при беременности: проспективное продольное исследование 58 случаев. Arch Gynecol Obstet 2012;285:1231–6. DOI: 10.1007/s00404–011–2137-x. |
56 | Мортон А., Лори Дж. Физиологические изменения беременности и критерии Суонси в диагностике острого жирового гепатоза беременных. Obstet Med 2018;11:126–31. DOI: 10.1177/1753495X18759353. |
57 | Шривастава М., Бали С., Пандей Дж., и др. Гипертония, вызванная беременностью, и антитромбин-III. Indian J Pathol Microbiol 1995; 38:257–60. |
58 | Сюй К.Г., Чжоу Л., Шонг С.Г., и др. Активность антитромбина III у китайских женщин с преэклампсией. Thromb Res 1990; 59: 401–6. |
59 | Гранинджер В., Татра Г., Пирич К., и др. Низкий уровень антитромбина III и высокий уровень фибронектина в плазме при преэклампсии. Eur J Obstet Gynecol Reprod Biol 1985;19:223–9. |
60 | Weenink GH, Treffers PE, Kahle LH, et al. Антитромбин III при нормальной беременности. Thromb Res 1982; 26: 281–7. |
61 | Джеймс А.Х., Ри Э., Темз Б., и др. Характеристика уровней антитромбина при беременности. Thromb Res 2014; 134:648–51. DOI: 10.1016/j.thromres.2014.07.025. |
62 | Цунода Т., Окучи А., Изуми А., и др. Активность антитромбина III и количество тромбоцитов с большей вероятностью снижаются при беременности двойней, чем при беременности одноплодной. Acta Obstet Gynecol Scand 2002;81:840–5. |
63 | Weiner CP, Kwaan HC, Xu C, et al. Активность антитромбина III у женщин с артериальной гипертензией во время беременности. Obstet Gynecol 1985;65:301–6. |
64 | Патерностер Д.М., Стелла А., Симиони П., и др. Параметры коагуляции и фибронектина плазмы при HELLP-синдроме. Int J Gynaecol Obstet 1995;50:263–8. |
65 | Демир С, Дилек И. Естественные ингибиторы свертывания крови и резистентность к активному протеину с при преэклампсии. Клиники (Сан-Паулу) 2010;65:1119–22.DOI: 10.1590/s1807–5 10001100011. |
66 | де Бур К., Буллер Х.Р., тен Кейт Дж.В., и др. Исследования коагуляции при синдроме гемолиза, повышенных ферментах печени и низких тромбоцитах. Br J Obstet Gynaecol 1991; 98:42–7. |
67 | Мариэтта М., Симони Л., Педрацци П., и др. Снижение уровня антитромбина в плазме связано с ухудшением течения преэклампсии. Int J Lab Hematol 2009; 31:227–32. DOI: 10.1111/j.1751–553X.2008.01031.x. |
68 | Chen Y, Lin L. Потенциальное значение параметров коагуляции для предположения о преэклампсии во время третьего триместра беременности. Am J Med Sci 2017; 354:39–43. DOI: 10.1016/j.amjms.2017.03.012. |
69 | Vigil-De Gracia P. Острая жировая дистрофия печени и HELLP-синдром: два различных расстройства беременности. Int J Gynaecol Obstet 2001;73:215–20. |
70 | Вайнер ЧП, Бонсиб СМ. Взаимосвязь между гистологией почек и активностью антитромбина III в плазме у женщин с ранним началом преэклампсии. Am J Perinatol 1990;7:139–43. DOI: 10.1055/s-2007–999466. |
71 | Канфер А. Факторы свертывания крови при нефротическом синдроме. Am J Nephrol 1990;10(1):63–8. ДОИ: 10.1159/000168196. |
72 | Knot E, Ten Cate JW, Drijfhout HR, и др. Метаболизм антитромбина III у пациентов с заболеваниями печени. Дж. Клин Патол 1984; 37: 523–30. DOI: 10.1136/jcp.37.5.523. |
73 | Кристофферсен А.Х., Петерсен П.Х., Рораас Т., и др. Оценка внутрисубъектной биологической изменчивости протеина С, антитромбина, свободного протеина S, активности протеина S и резистентности к активированному протеину С у беременных женщин. Clin Chem 2017;63:898–907. DOI: 10.1373/clinchem.2016.265900. |
74 | Рой-Грин К., Фредерик Дж., Уорф Г., и др. Антифосфолипидные и другие аутоантитела в когорте привычных абортов и здоровых повторнородящих женщин на Ямайке. Hum Antibodies 2011; 20:1–5. DOI: 10.3233/HAB20110236 |
75 | Faden D, Tincani A, Tanzi P, et al. Антитела к бета-2 гликопротеину I в общей акушерской популяции: предварительные результаты по распространенности и корреляции с исходом беременности. Антитела к бета2-гликопротеину I связаны с некоторыми акушерскими осложнениями, в основном с преэклампсией-эклампсией. Eur J Obstet Gynecol Reprod Biol 1997;73:37–42. |
76 | Аводу О.А., Эджеле О.А., Шокунби В.А., и др. Распространенность волчаночного антикоагулянта у повторнородящих женщин в Бенин-Сити, Нигерия. Niger Postgrad Med J 2003; 10:19–22. |
77 | Рикс П., Стентофт Дж., Ауншолт Н.А., и др. Волчаночный антикоагулянт и антикардиолипиновые антитела в акушерской популяции. Acta Obstet Gynecol Scand 1992;71:605–9. |
78 | Адлер Г., Духинский Т., Ясинская А., и др. Фракции фибриногена в третьем триместре беременности и в послеродовом периоде. Thromb Res 2000; 97: 405–10. |
79 | Manten GT, Franx A, Sikkema JM, и др. Фибриноген и высокомолекулярный фибриноген во время и после нормально протекающей беременности. Thromb Res 2004; 114:19–23. DOI: 10.1016/j.thromres.2004.04.008. |
80 | Эрез О., Новак Л., Беер-Вайзел Р., и др. Шкала ДВС-синдрома у беременных – популяционная модификация шкалы Международного общества тромбоза и гемостаза. PLoS One 2014;9:e | . DOI: 10.1371/journal.pone.00.
81 | Windsperger K, Lehner R. Соотношение фибриноген/CRP как новый параметр для диагностики диссеминированного внутрисосудистого свертывания крови у пациентов с HELLP-синдромом и как прогностический фактор неонатального исхода. Am J Obstet Gynecol 2013;208:118 e111–7. DOI: 10.1016/j.ajog.2012.11.025. |
82 | Челик С., Гезгинч К., Алтынтепе Л., и др. Результаты беременностей с синдромом HELLP. Рен Фэйл 2003; 25: 613–8. DOI: 10.1081/jdi-120022553. |
83 | Зубери Н.Ф., Ариф К., Хан Ф.М., и др. Сравнение тяжелой преэклампсии/эклампсии у пациенток с HELLP-синдромом и без него. J Pak Med Assoc 1998; 48:29–32. |
84 | Хаддад Б., Бартон Дж. Р., Ливингстон Дж. К., и др. Синдром HELLP (гемолиз, повышенный уровень ферментов печени и низкий уровень тромбоцитов) по сравнению с тяжелой преэклампсией: начало в < или =28.0 недель беременности. Am J Obstet Gynecol 2000;183:1475–9. |
85 | Ван Дам П.А., Ренье М., Бэкеландт М., и др. ДВС-синдром и синдром гемолиза, повышение активности печеночных ферментов и низкий уровень тромбоцитов при тяжелой преэклампсии. Obstet Gynecol 1989;73:97–102. |
86 | Рэттрей Д.Д., О’Коннелл К.М., Баскетт Т.Ф. Острое диссеминированное внутрисосудистое свертывание крови в акушерстве: обзор населения третичного центра (с 1980 по 2009 год). J Obstet Gynaecol Can 2012;34:341–7. DOI: 10.1016/S1701–2163(16)35214–8. |
87 | Van der Pol LM, Mairuhu AT, Tromeur C, et al. Использование правил клинического прогнозирования и тестов на D-димер в диагностическом ведении беременных с подозрением на острую легочную эмболию. Blood Rev 2017; 31:31–6. DOI: 10.1016/j.blre.2016.09.003. |
88 | Клайн Дж.А., Уильямс Г.В., Эрнандес-Нино Дж.Концентрации D-димера при нормальной беременности: необходимы новые диагностические пороги. Clin Chem 2005; 51:825–9. DOI: 10.1373/clinchem.2004.044883. |
89 | Ковач М., Микович З., Ракичевич Л., и др. Использование D-димера с новой отсечкой может быть полезным в диагностике венозной тромбоэмболии у беременных. Eur J Obstet Gynecol Reprod Biol 2010;148:27–30. DOI: 10.1016/j.ejogrb.2009.09.005. |
90 | Ван М., Лу С., Ли С., и др. Референтные интервалы D-димера в период беременности и послеродового периода на коагуляционном анализаторе STA-R evolution. Clin Chim Acta 2013; 425:176–80. DOI: 10.1016/j.cca.2013.08.006. |
91 | Друри-Стюарт Д.Н., Ланнерт К.В., Чанг Д.В., и др. Комплексные изменения параметров, связанных с фактором фон Виллебранда, приобретаются при неосложненной беременности. PLoS One 2014;9:e112935. DOI: 10.1371/журнал.поне.0112935. |
92 | Huq FY, Kulkarni A, Agbim EC, et al. Изменения уровня фактора VIII и фактора фон Виллебранда в послеродовом периоде. Гемофилия 2012;18:241–5. DOI: 10.1111/j.1365–2516.2011.02625.x. |
93 | Delbruck C, Miesbach W. Курс активности фактора фон Виллебранда и фактора VIII у пациентов с болезнью фон Виллебранда во время беременности. Acta Haematol 2019:1–8. DOI: 10.1159/000496820. |
94 | Nielsen FR, Bek KM, Rasmussen PE, et al. С-реактивный белок при нормально протекающей беременности. Eur J Obstet Gynecol Reprod Biol 1990;35:23–7. |
95 | Гаврилишин П., Бернштейн П., Миллиган Дж. Э., и др. Преждевременный разрыв плодных оболочек: роль С-реактивного белка в прогнозировании хориоамнионита. Am J Obstet Gynecol 1983;147:240–6. |
96 | Watts DH, Krohn MA, Wener MH, et al. С-реактивный белок при нормально протекающей беременности. Obstet Gynecol 1991;77:176–80. |
97 | Ван ден Бро Н.Р., Лецкий Е.А. Беременность и скорость оседания эритроцитов. BJOG 2001; 108:1164–7. |
98 | Деммерс М.В., Ниенс М., ван дер Хаар Г., и др. Маркеры функционального дефицита железа отсутствуют во время беременности, несмотря на признаки низкого уровня запасов железа. Энн Клин Биохим 2019:4563219837290. DOI: 10.1177/0004563219837290. |
99 | M R. Нормальные значения. В: Джеймс Д. С.П., Вайнер С.П., Гоник Б., Кроутер К.А., Робсон С.К. (ред.) Беременность с высоким риском: варианты ведения . 4-е изд. Saunders/Elsevier, 2011. |
100 | Ауэрбах М.Комментарий: Дефицит железа при беременности – новый подход с внутривенным введением железа. Reprod Health 2018;15:96. DOI: 10.1186/s12978–018–0536–1. |
101 | Koenig MD, Tussing-Humphreys L, Day J, et al. Гепсидин и гомеостаз железа во время беременности. Питательные вещества 2014;6:3062–83. DOI: 10.3390/nu6083062. |
102 | Джолобе ОМП. Предостережения в лечении железодефицитной анемии. Eur J Intern Med 2018;48:e38. DOI: 10.1016/j.ejim.2017.07.032. |
103 | Петросян И., Блейсон Г., Андрес Э., и др. Анемия у пожилых людей: этиологический профиль проспективной когорты из 95 госпитализированных пациентов. Eur J Intern Med 2012;23:524–8. DOI: 10.1016/j.ejim.2012.03.013. |
104 | Фрэнсис Дж., Шеридан Д., Саманта А., и др. Железодефицитная анемия при хронических воспалительных ревматических заболеваниях: низкий средний клеточный гемоглобин является лучшим маркером, чем низкий средний клеточный объем. Энн Реум Дис 2005; 64: 787–8. DOI: 10.1136/ard.2004.025890. |
105 | Инфузино I, Брага Ф, Дольчи А, и др. Рецептор растворимого трансферрина (sTfR) и индекс sTfR/log ферритина для диагностики железодефицитной анемии. Метаанализ. Am J Clin Pathol 2012;138:642–9.DOI: 10.1309/AJCP16NTXZLZFAIB. |
106 | Заман Б., Расул С., Джасим С., и др. Гепсидин как диагностический биомаркер железодефицитной анемии во время беременности. J Matern Fetal Neonatal Med 2019:1–241. DOI: 10.1080/14767058.2019.1635112. |
107 | Курхаде Г.А., Ханоркар С.В., Пураник Б.М., и др. Уровень железа и трансферрина в сыворотке крови при беременности и в послеродовом периоде. Indian J Physiol Pharmacol 1994; 38:34–8. |
108 | Мильман Н., Быг К.Е., Бергхолт Т., и др. Статус кобаламина при нормальной беременности и послеродовом периоде: лонгитюдное исследование, включающее 406 датских женщин. Eur J Haematol 2006;76:521–5. DOI: 10.1111/j.0902–4441.2006.t01–1-EJh3550.x. |
109 | Шредер Т.Х., Тан А., Маттман А., и др. Референтные интервалы концентрации общего витамина B12 и холотранскобаламина в сыворотке крови и точки их изменения в зависимости от концентрации метилмалоновой кислоты для оценки статуса витамина B12 на ранних и средних сроках беременности. Clin Chem Lab Med 2019. DOI: 10.1515/cclm-2018–1337. |
110 | Schroder TH, Sinclair G, Mattman A, et al. Беременные женщины южноазиатского происхождения в Канаде имеют значительно более низкий уровень витамина B12 по сравнению с беременными женщинами европейского происхождения. Бр Ж Нутр 2017;118:454–62. DOI: 10.1017/S0007114517002331. |
111 | Брюинс Х.В., ван ден Берг Х.Изменения уровня некоторых витаминов во время и после нормальной беременности. Eur J Obstet Gynecol Reprod Biol 1995;61:31–7. |
112 | Каттоццо Г., Калоначи А., Албени С., и др. Референтные значения для аланинаминотрансферазы, альфа-амилазы, аспартатаминотрансферазы, гамма-глутамилтрансферазы и лактатдегидрогеназы, измеренные в соответствии со стандартом IFCC при неосложненной беременности. Clin Chem Lab Med 2013;51:e239–41.DOI: 10.1515/cclm-2013–0371. |
113 | Ларссон А., Палм М., Ханссон Л.О., и др. Референтные значения альфа-1-кислого гликопротеина, альфа-1-антитрипсина, альбумина, гаптоглобина, С-реактивного белка, IgA, IgG и IgM при беременности. Acta Obstet Gynecol Scand 2008;87:1084–8. DOI: 10.1080/00016340802428146. |
114 | Арекул С., Китиани У., Укоскит К. Гаптоглобины сыворотки при беременности. Юго-Восточная Азия J Trop Med Public Health 1975;6:567–72. |
115 | Гацка С., Бремерих Д., Кауфманн М., и др. [Изолированное снижение гаптоглобина при беременности: диагноз случайный или патологический? ]. Централбл Гинакол 2002;124:120–2. DOI: 10.1055/s-2002–24234. |
116 | Чой Дж.В., Пай Ш.Х. Изменение эритропоэза с гестационным возрастом при беременности. Энн Хематол 2001; 80: 26–31. |
117 | Mercelina-Roumans PE, Ubachs JM, van Wersch JW. Количество ретикулоцитов и их субфракций у курящих и некурящих беременных. Eur J Clin Chem Clin Biochem 1995;33:263–5. |
118 | Трейл ЛМ. Ретикулоциты при здоровой беременности. Med J Aust 1975; 2: 205–6. |
119 | Ю Ф, Чжоу В, Инь М, и др. Проспективное и лонгитюдное исследование показателей метаболизма железа при нормальной беременности у китайских женщин. Clin Lab 2019;65. DOI: 10.7754/Clin.Lab.2018.180928. |
Вариант оценки онлайн-исследования
Все читатели, являющиеся квалифицированными врачами или смежными медицинскими работниками, теперь могут автоматически получить 2 кредита непрерывного профессионального развития от FIGO плюс a сертификат о завершении исследования от GLOWM за успешные ответы на 4 вопроса с несколькими вариантами ответов (выбранных случайным образом) на основе по изучению этой главы.
Студенты-медики могут получить только сертификат об окончании обучения .
(Чтобы узнать больше о программе непрерывного профессионального развития FIGO, НАЖМИТЕ ЗДЕСЬ)
Я хочу продолжить оценку исследования для этой главы
Гипертензивные расстройства беременных – Американский семейный врач
2.Абалос Э, Дулей Л, Стейн ДВ. Антигипертензивная медикаментозная терапия легкой и умеренной артериальной гипертензии во время беременности. Кокрановская база данных Syst Rev . 2014;(2):CD002252.
3. Анкумах Н.А., Канту Дж, Яук В, и другие. Риск неблагоприятных исходов беременности у женщин с легкой хронической гипертонией до 20 недель беременности. Акушерство Гинекол . 2014;123(5):966–972.
4. Маги Л.А., Дулей Л.Пероральные бета-адреноблокаторы при легкой и умеренной артериальной гипертензии во время беременности. Кокрановская база данных Syst Rev . 2003; (3): CD002863.
5. фон Дадельзен П., член парламента Орнштейна, Бык СБ, и другие. Падение среднего артериального давления и задержка роста плода при артериальной гипертензии беременных: метаанализ. Ланцет . 2000;355(9198):87–92.
6. Отчет рабочей группы Национальной образовательной программы по высокому кровяному давлению по высокому кровяному давлению у беременных. Am J Obstet Gynecol . 2000;183(1):S1–S22.
7. Национальный сотрудничающий центр здоровья женщин и детей; Национальный институт здравоохранения и передового опыта. Гипертония во время беременности: лечение гипертонических расстройств во время беременности. Лондон, Великобритания: Королевский колледж акушеров и гинекологов; 2011.
8. Черчилль Д., Биверс ГД, Мехер С, и другие. Диуретики для профилактики преэклампсии. Кокрановская база данных Syst Rev .2007; (1): CD004451.
9. Комитет по акушерской практике. Заключение комитета №. 623: неотложная терапия острого начала тяжелой гипертензии во время беременности и в послеродовом периоде. Акушерство Гинекол . 2015;125(2):521–525.
10. Шекхар С, Шарма С, Такур С, и другие. Пероральный нифедипин или внутривенный лабеталол при неотложной гипертензии во время беременности: рандомизированное контролируемое исследование. Акушерство Гинекол .2013;122(5):1057–1063.
11. Бартон Дж. Р., О’Брайен Дж. М., Бергауэр Н.К., и другие. Легкая гестационная гипертензия на отдаленных сроках: прогрессирование и исход. Am J Obstet Gynecol . 2001;184(5):979–983.
12. Дэвисон Дж. М., Хомут В, Джеябалан А, и другие. Новые аспекты патофизиологии преэклампсии. J Am Soc Нефрол . 2004;15(9):2440–2448.
13.Макмастер МТ, Чжоу Ю, Фишер СДж. Аномальная плацентация и синдром преэклампсии. Семин Нефрол . 2004;24(6):540–547.
14. Ван А, Рана С, Каруманчи С.А. Преэклампсия: роль ангиогенных факторов в ее патогенезе. Физиология (Bethesda) . 2009; 24:147–158.
15. Лин Дж., Август П. Генетические тромбофилии и преэклампсия: метаанализ. Акушерство Гинекол .2005;105(1):182–192.
16. Колуччи Ф., Буленуар С, Кикбуш Дж, и другие. Как изменчивость генов иммунной системы влияет на плацентацию? Плацента . 2011;32(8):539–545.
17. Джордж Э.М., Грейнджер Дж.П. Эндотелин: ключевой медиатор гипертонии при преэклампсии. Am J Hypertens . 2011;24(9):964–969.
18. Дакитт К., Харрингтон Д. Факторы риска преэклампсии при дородовом обследовании: систематический обзор контролируемых исследований. БМЖ . 2005;330(7491):565.
19. Милн Ф., Редман С, Уокер Дж, и другие. Рекомендации сообщества по преэклампсии (PRECOG): как проводить скрининг и обнаруживать начало преэклампсии в сообществе. БМЖ . 2005;330(7491):576–580.
20. Кенни Л.С., Черная Ма, Постон Л, и другие. Предсказание преэклампсии на ранних сроках беременности у нерожавших женщин, сочетающее клинический риск и биомаркеры: международное когортное исследование Screening for Pregnancy Endpoints (SCOPE). Гипертония . 2014;64(3):644–652.
21. Лиман Л., Дресанг Л, Фонтейн П. Глава B: Медицинские осложнения беременности. ТАКЖЕ Учебный план провайдера . Февраль 2015 г .: 1–38.
22. Родригес-Томпсон Д., Либерман Э.С. Использование случайного соотношения белка и креатинина в моче для диагностики значительной протеинурии во время беременности. Am J Obstet Gynecol . 2001;185(4):808–811.
23.Сибай БМ. Профилактика сульфатом магния при преэклампсии: данные рандомизированных исследований. Клин Акушерство Гинекол . 2005;48(2):478–488.
24. Альтман Д, Карроли Г, Дулей Л, и другие. Полезен ли сульфат магния женщинам с преэклампсией и их детям? The Magpie Trial: рандомизированное плацебо-контролируемое исследование. Ланцет . 2002;359(9321):1877–1890.
25. Купманс С.М., Бийленга Д, Гроен Х, и другие.Индукция родов по сравнению с выжидательным мониторингом гестационной гипертензии или легкой преэклампсии после 36 недель беременности (HYPITAT). Ланцет . 2009;374(9694):979–988.
26. Губка CY, Мерсер БМ, Далтон М, и другие. Сроки указанных поздних преждевременных и преждевременных родов. Акушерство Гинекол . 2011; 118 (2 п. 1): 323–333.
27. Броекхейсен К., ван Баарен Г.Дж., ван Пампус MG, и другие.; Учебная группа HYPITAT-II. Немедленные роды по сравнению с выжидательным мониторингом гипертензивных расстройств или беременности между 34 и 37 неделями беременности (HYPITAT-II): открытое рандомизированное контролируемое исследование. Ланцет . 2015;385(9986):2492–2501.
28. Дилды Г.А. Осложнения преэклампсии. В: Акушерство интенсивной терапии. 4-е изд. Малден, Массачусетс: Блэквелл; 2004.
29. Дулей Л., Гюльмезоглу А.М., Хендерсон-Смарт диджей, и другие.Сульфат магния и другие противосудорожные средства для женщин с преэклампсией. Кокрановская база данных Syst Rev . 2010;(11):CD000025.
30. Дулей Л., Гюльмезоглу А.М., Чоу Д. Сульфат магния против литического коктейля при эклампсии. Кокрановская база данных Syst Rev . 2010;(9):CD002960.
31. Дулей Л., Хендерсон-Смарт диджей, Чоу Д. Сульфат магния против фенитоина при эклампсии. Кокрановская база данных Syst Rev .2010;(10):CD000128.
32. Дулей Л., Хендерсон-Смарт диджей, Уокер Г.Дж., и другие. Сульфат магния в сравнении с диазепамом при эклампсии. Кокрановская база данных Syst Rev . 2010;(12):CD000127.
33. Сибай Б.М. Диагностика, профилактика и лечение эклампсии. Акушерство Гинекол . 2005;105(2):402–410.
34. Сибай Б.М. Профилактика сульфатом магния при преэклампсии: уроки, извлеченные из недавних испытаний. Am J Obstet Gynecol . 2004;190(6):1520–1526.
35. Мартин Дж. Н. мл., Тигпен БД, Мур РЦ, и другие. Инсульт и тяжелая преэклампсия и эклампсия: сдвиг парадигмы с акцентом на систолическое артериальное давление. Акушерство Гинекол . 2005;105(2):246–254.
36. Дулей Л., Мехер С, Джонс Л. Препараты для лечения очень высокого кровяного давления во время беременности. Кокрановская база данных Syst Rev .2013;(7):CD001449.
37. Сибай Б.М. Диагностика и лечение гестационной гипертензии и преэклампсии. Акушерство Гинекол . 2003;102(1):181–192.
38. Бартон Дж. Р., Сибай БМ. Диагностика и лечение гемолиза, повышенных ферментов печени и синдрома низких тромбоцитов. Клин Перинатол . 2004;31(4):807–833, vii.
39. Сибай Б.М. Диагностика, противоречия и лечение синдрома гемолиза, повышенных ферментов печени и низкого количества тромбоцитов. Акушерство Гинекол . 2004; 103 (5 пт. 1): 981–991.
40. Черчилль Д., Дулей Л, Торнтон Дж.Г., и другие. Вмешательство в сравнении с выжидательной тактикой при тяжелой преэклампсии между 24 и 34 неделями беременности. Кокрановская база данных Syst Rev . 2013;(7):CD003106.
41. Сибай Б.М., Рамадан МК, Уста я, и другие. Материнская заболеваемость и смертность при 442 беременностях с гемолизом, повышенным уровнем ферментов печени и низким уровнем тромбоцитов (синдром HELLP). Am J Obstet Gynecol . 1993;169(4):1000–1006.
42. Вайнштейн Л. Синдром гемолиза, повышенный уровень печеночных ферментов и низкий уровень тромбоцитов: тяжелое последствие артериальной гипертензии во время беременности. Am J Obstet Gynecol . 1982;142(2):159–167.
43. Практический бюллетень ACOG: тромбоцитопения при беременности. № 6, сентябрь 1999 г. Клинические рекомендации по ведению акушеров-гинекологов. Int J Gynaecol Obstet . 1999;67(2):117–128.
44. О’Брайен Дж. М., Шумате С.А., Сатчвелл С.Л., и другие. Польза терапии кортикостероидами для матери у пациентов с синдромом HELLP (гемолиз, повышенный уровень ферментов печени и низкий уровень тромбоцитов): влияние на скорость регионарной анестезии. Am J Obstet Gynecol . 2002;186(3):475–479.
45. Вудстра Д.М., Чандра С, Хофмейр Г.Дж., и другие. Кортикостероиды при синдроме HELLP (гемолиз, повышенный уровень ферментов печени, низкий уровень тромбоцитов) у беременных. Кокрановская база данных Syst Rev . 2010;(9):CD008148.
46. Маттар Ф., Сибай БМ. Эклампсия. VIII. Факторы риска материнской заболеваемости. Am J Obstet Gynecol . 2000;182(2):307–312.
47. Курей С.Д., Эдмондс С.М., Тонг С, и другие. Характеристика симптомов, непосредственно предшествующих эклампсии. Акушерство Гинекол . 2011;118(5):995–999.
48. Майя С.Б., Кац Л, Нето КН, и другие.Сокращенная (12-часовая) и традиционная (24-часовая) послеродовая терапия сульфатом магния при тяжелой преэклампсии. Int J Gynaecol Obstet . 2014;126(3):260–264.
49. Маги Л., фон Дадельсен П. Профилактика и лечение послеродовой гипертензии. Кокрановская база данных Syst Rev . 2013;(4):CD004351.
50. Дулей Л., Хендерсон-Смарт диджей, Мехер С, и другие. Антиагреганты для профилактики преэклампсии и ее осложнений. Кокрановская база данных Syst Rev . 2007; (2): CD004659.
51. Целевая группа профилактических служб США. Окончательное изложение рекомендации: низкие дозы аспирина для предотвращения преэклампсии: профилактическое лечение, сентябрь 2014 г. -и-смертность-от-преэклампсии-профилактическое-лекарство. По состоянию на 15 ноября 2015 г.
52. Hofmeyr GJ, Лори Т.А., Аталла А.Н., и другие.Добавки кальция во время беременности для предотвращения гипертонических расстройств и связанных с ними проблем. Кокрановская база данных Syst Rev . 2014;(6):CD001059.
53. Вернер Э.Ф., Хауспург АК, Роуз диджей. Анализ эффективности затрат на профилактику низкими дозами аспирина для предотвращения преэклампсии в Соединенных Штатах. Акушерство Гинекол . 2015;126(6):1242–1250.
54. Лиман Л., Фонтейн П. Гипертонические расстройства беременности. Семейный врач . 2008;78(1):93–100.
Обзор | NIH
Рекомендации по использованию антиретровирусных препаратов во время беременности: обзор
| Рекомендации комиссии |
|---|
|
В этом разделе представлен обзор ключевых клинических и фармакокинетических (ФК) вопросов, имеющих отношение к выбору специфических антиретровирусных (АРВ) препаратов для применения во время беременности. Дополнительные рекомендации для беременных с ВИЧ, которые никогда не получали антиретровирусную терапию (антиретровирусная терапия [АРТ]-наивные), беременных, которые в настоящее время получают АРТ, а также для тех, кто ранее получал АРТ или принимал АРВ-препараты для профилактики, можно найти в другие разделы, следующие за этим обзором.В таблице 4 представлена конкретная информация о рекомендуемых АРВ-препаратах при начале АРТ у беременных, ранее не получавших АРТ. В таблице также приведены рекомендации по выбору и модификации схемы АРВ-терапии у беременных, которые уже проходили лечение, и у тех, кто пытается забеременеть. Рекомендации по применению АРВ-препаратов у людей детородного возраста, которые активно не пытаются забеременеть, см. в Руководстве по применению антиретровирусных препаратов у взрослых и подростков, живущих с ВИЧ.
В Таблице 5 сведены рекомендации по использованию АРВ-препаратов у людей с ВИЧ во время зачатия и беременности для конкретных ситуаций в одной таблице для удобства пользования. Таблица 5 включает рекомендации по применению АРВ-препаратов в следующих ситуациях:
- Начало АРТ у беременных, которые никогда не получали АРВ-препараты;
- Продолжение АРТ у людей, которые забеременели во время полностью супрессивной схемы, которая хорошо переносилась;
- Возобновление АРТ у беременных, получавших АРТ или АРВ-препараты для профилактики в прошлом;
- Переход на новый режим АРВТ у беременных, чья текущая АРТ плохо переносится и/или не приводит к подавлению вируса; и
- Начало или модификация АРТ у людей, которые пытаются забеременеть.
В Таблице 11 и Приложении B представлена информация об отдельных препаратах, включая данные о дозировке и фармакокинетике при беременности.
Беременных часто исключают из первоначальных клинических испытаний на ВИЧ. В результате данные о ФК, безопасности лекарств и эффективности новых АРВ часто ограничиваются небеременными взрослыми. 1 , 2 Эффективность АРВ-препаратов для лечения беременных можно экстраполировать на основании данных об эффективности у небеременных взрослых, если прямая фармакокинетическая оценка у беременных показывает воздействие препарата во время беременности, которое находится в пределах эффективного диапазона у небеременных Взрослые.Точно так же схемы АРТ, которые приводят к подавлению вируса на протяжении всей беременности, вероятно, будут эффективны для предотвращения вертикальной передачи ВИЧ. Напротив, безопасность АРТ нельзя экстраполировать, и ее следует оценивать непосредственно у беременных. Тем не менее, препараты с известной пользой для небеременных людей не следует отменять во время беременности, за исключением случаев, когда известно, что они оказывают неблагоприятное воздействие на беременных, плод или младенца, и эти побочные эффекты перевешивают пользу для беременных, или если адекватные уровни лекарственного средства не установлены. может быть достигнута во время беременности.Беременность и возможность наступления беременности не должны исключать использование оптимальных схем приема лекарств. Решение о том, какие АРВ-препараты использовать во время беременности, пациентки должны принимать после обсуждения известных и потенциальных преимуществ и рисков для себя и своего плода со своими поставщиками медицинских услуг (см. Приложение C: Консультативное руководство по антиретровирусной терапии для медицинских работников). 3
Группа по лечению ВИЧ во время беременности и профилактике перинатальной передачи ВИЧ (Группа) анализирует данные клинических испытаний, опубликованные в рецензируемых журналах, и данные, подготовленные производителями для U.S. Обзор Управления по санитарному надзору за качеством пищевых продуктов и медикаментов, связанный с лечением взрослых женщин с ВИЧ, как беременных, так и небеременных. Долговечность, переносимость и простота схемы лечения особенно важны для обеспечения приверженности и сохранения вариантов лечения в будущем. Выбор режима должен основываться на нескольких факторах, которые применимы ко всем беременным, а также на факторах, которые будут различаться у отдельных пациенток.
Факторы, связанные с беременностью, включают:
- Потенциальные краткосрочные и долгосрочные неблагоприятные воздействия на плод или новорожденных, такие как возможный риск тератогенности, преждевременные роды или влияние на рост и развитие.
- Имеющиеся данные о безопасности и результатах применения препарата во время беременности, включая связь с неблагоприятными исходами беременности, такими как преждевременные роды;
- Изменения ПК при беременности; и
- Возможные побочные эффекты для пациента, особенно те, которые могут усугубиться во время беременности.
Факторы индивидуального уровня включают—
- Возможные лекарственные взаимодействия с другими лекарствами;
- Результаты тестирования на резистентность и предшествующее воздействие АРВ-препаратов на пациента;
- Сопутствующие заболевания;
- Способность пациента соблюдать режим; и
- Удобство и предпочтения пациента.
Группа использует информацию из нескольких источников для разработки рекомендаций по конкретным лекарствам или режимам лечения беременных. Эти источники включают —
- Данные рандомизированных клинических испытаний и проспективных когортных исследований, которые демонстрируют стойкую вирусную супрессию во время беременности, а также иммунологические и клинические улучшения;
- Уровень заболеваемости и описания краткосрочной и долгосрочной лекарственной токсичности АРВ-схем;
- Данные клинических исследований риска материнской токсичности, тератогенности, неблагоприятных исходов беременности и неблагоприятных исходов у младенцев;
- Специальные знания о переносимости лекарств и упрощенных режимах дозирования;
- Известная эффективность схем приема АРВ-препаратов в снижении перинатальной передачи ВИЧ при наличии данных, доказательств высоких показателей подавления вирусной нагрузки во время беременности или доказательств высоких показателей подавления вирусной нагрузки у небеременных пациенток с данными фармакокинетики (лекарственное воздействие) во время беременности, демонстрирующими воздействие аналогично таковым у небеременных пациентов;
- Данные о фармакокинетике (лекарственное воздействие) во время беременности;
- Данные исследований тератогенности на животных; и
- Данные регистра антиретровирусных препаратов при беременности и другие данные постмаркетингового наблюдения. 4
АРВ-препараты и комбинации препаратов для применения во время беременности подразделяются на следующие категории:
- Предпочтительный номер : Лекарства или комбинации препаратов обозначены как Предпочтительный номер для терапии беременных, когда данные клинических испытаний у взрослых продемонстрировали эффективность и долговечность при приемлемой токсичности и простоте использования, а также когда доступны данные о фармакокинетике для беременных. для руководства дозированием. Кроме того, имеющиеся данные должны свидетельствовать о благоприятном соотношении риска и пользы для препарата или комбинации препаратов по сравнению с другими вариантами АРВ-препаратов; оценка рисков и преимуществ должна включать результаты для беременных, плодов и младенцев.Некоторые предпочтительных препаратов или схем могут иметь минимальные риски токсичности или тератогенности, которые компенсируются другими преимуществами для людей с ВИЧ, которые беременны или пытаются забеременеть.
- Альтернатива : Лекарства или комбинации препаратов обозначаются как Альтернатива вариантов терапии беременных, когда данные клинических испытаний у взрослых показывают эффективность, а данные у беременных в целом благоприятны, но ограничены. Большинство препаратов или схем Альтернативные связаны с большим количеством проблем с ФК, дозировкой, переносимостью, составом, введением или взаимодействием, чем те, что относятся к категории Предпочтительных , но они приемлемы для использования во время беременности.Некоторые Альтернативные препараты или схемы могут иметь известные риски токсичности или тератогенности, которые компенсируются другими преимуществами для людей с ВИЧ, которые беременны или пытаются забеременеть.
- Недостаточно данных для рекомендации : Препараты и комбинации препаратов этой категории одобрены для применения у взрослых, но данные о фармакокинетике или безопасности для беременных слишком ограничены, чтобы давать рекомендации по применению у беременных. В некоторых случаях может быть целесообразным продолжать использование этих препаратов или их комбинаций у пациенток, забеременевших на фоне хорошо переносимой АРТ.
- Не рекомендуется, за исключением особых обстоятельств: Хотя некоторые препараты не рекомендуются для начальной АРТ у ранее не получавших АРТ людей из-за особых соображений безопасности или очень ограниченных данных о безопасности и эффективности при беременности, могут быть обстоятельства, при которых людям, ранее получавшим АРТ, начать или продолжить использование определенных препаратов для достижения или поддержания вирусной супрессии.
- Не рекомендуется : Лекарства и комбинации лекарств, перечисленные в этой категории, не рекомендуются для использования во время беременности из-за низкой вирусологической эффективности или потенциально серьезных проблем с безопасностью для матери или плода.Препараты, не рекомендуемые для начальной терапии в популяциях, ранее не получавших АРВ-препараты, также классифицируются как , не рекомендуется при беременности. В эту категорию входят препараты или комбинации препаратов, для которых данные фармакокинетики демонстрируют низкие уровни препаратов и риск повторного заражения вирусом во время беременности. Уровни этих препаратов часто бывают низкими на поздних сроках беременности (во время второго и третьего триместров), когда высок риск перинатальной передачи в случае материнской виремии. В некоторых ситуациях может быть целесообразным продолжать использование этих препаратов или комбинаций препаратов у людей, забеременевших на полностью супрессивной АРТ, которая хорошо переносилась, хотя в таких случаях следует чаще проводить мониторинг вирусной нагрузки.См. раздел «Беременные с ВИЧ, которые в настоящее время получают антиретровирусную терапию и мониторинг во время беременности».
Выбор АРВ-препаратов должен быть индивидуализирован в соответствии с анамнезом АРВ-препаратов беременной пациентки, результатами тестов на лекарственную устойчивость и наличием сопутствующих заболеваний, а также индивидуальными предпочтениями пациентки в отношении баланса между известными и неизвестными рисками и преимуществами. Людям, которые беременны или пытаются забеременеть, рекомендуется АРТ, включающая не менее трех препаратов.Для людей, ранее не получавших АРВ-препараты, предпочтительна схема АРВ-терапии, включающая два нуклеозидных ингибитора обратной транскриптазы (НИОТ) и ингибитор переноса цепи интегразы (ИНСТИ) или усиленный ритонавиром (РТВ) ингибитор протеазы (ИП) (таблица 4).
В общем, люди , которые уже находятся на полностью супрессивном режиме, когда наступает беременность, должны продолжать свои режимы. Ключевые исключения включают схемы, включающие препараты, которые не рекомендуются для применения у взрослых из-за высокого риска токсичности (например,например, диданозин [ddI], индинавир [IDV], ставудин [d4T] и лечебная доза RTV) или с меньшей вирусологической эффективностью (нелфинавир [NFV]), а также препараты, которые не следует использовать во время беременности из-за проблем с ФК (см. Таблица 4). Для пациентов, у которых была достигнута вирусная супрессия и которые забеременели при применении схем с потенциально повышенным риском вирусологической неудачи во время беременности из-за проблем с фармакокинетикой (например, схемы, усиленные кобицистатом (COBI)), или которые получают схемы с недостаточными данными во время беременности ( е.например, биктегравир [BIC], дораварин [DOR] или инъекционный каботегравир и рилпивирин длительного действия [CAB/RPV]), клиницисты должны рассмотреть вопрос о продолжении или изменении схемы АРВ-терапии, см. Беременные с ВИЧ, которые в настоящее время получают антиретровирусные препараты. Терапия. Изменение режима несет риск повторного заражения вирусом во время перехода. 5 Если с пациентом принято решение продолжать тот же режим, следует чаще контролировать вирусную нагрузку (т. е. каждые 1–2 месяца).
Людей, которые не полностью подавлены и которые в настоящее время принимают АРТ, следует тщательно обследовать на предмет приверженности и резистентности, прилагая все усилия для достижения быстрого и полного подавления вирусной нагрузки посредством вмешательств, направленных на соблюдение режима лечения, или смены лекарств (см. Антиретровирусная терапия).При лечении пациентов, которые ранее получали АРВ-препараты, но в настоящее время не принимают АРВ-препараты, клиницисты должны будут принимать во внимание предыдущие схемы лечения и возможность генотипической резистентности. Конкретные рекомендации для каждого типа пациентов описаны в таблице 5 и в следующих разделах: беременные с ВИЧ, которые никогда не получали антиретровирусные препараты, беременные с ВИЧ, которые в настоящее время получают антиретровирусную терапию, и беременные с ВИЧ, которые ранее получали антиретровирусные препараты. Лечение или профилактика, но в настоящее время не получают никаких антиретровирусных препаратов.
Баланс между рисками и преимуществами АРТ в условиях ограниченности данных
Важно взвесить имеющиеся данные о рисках и преимуществах всех агентов Preferred и Alternative . Эти препараты включают долутегравир (DTG), атазанавир/ритонавир (ATV/r), дарунавир/ритонавир (DRV/r) и ралтегравир (RAL) (, предпочтительный ), а также эфавиренз (EFV) и рилпивирин (RPV) ( Альтернатива ) и базовые препараты НИОТ, включая абакавир (ABC), ламивудин (3TC), эмтрицитабин (FTC), тенофовира дизопроксилфумарат (TDF), тенофовира алафенамид (TAF) (все Предпочтительно ) и зидовудин (ZDV) ( Альтернатива ).Из них данные систематического наблюдения за рождаемостью доступны только для TDF, FTC, 3TC, EFV и DTG. 6 , 7 Хотя ранние данные вызывали опасения по поводу риска дефектов нервной трубки (ДНТ) при применении DTG, и подобные опасения не высказывались для других агентов, данные слишком ограничены для выявления или расчета конкретных рисков редких врожденные дефекты, такие как ДНТ, связанные с применением других АРВ-препаратов до зачатия или в период до зачатия или их применением на ранних сроках беременности (см. Тератогенность, Долутегравир, Элвитегравир, Ралтегравир и Биктегравир).Чтобы определить, несет ли препарат повышенный риск редкого события, такого как ДНТ, необходимо отслеживать более 2000 воздействий в период до зачатия, чтобы исключить трехкратное увеличение риска. Врачам рекомендуется предоставлять в регистр Antiretroviral Premancy Registry данные обо всех пациентках, забеременевших во время приема АРВ-препаратов или получающих АРВ-препараты во время беременности.
Также следует учитывать риск других неблагоприятных исходов беременности, многие из которых встречаются чаще, чем врожденные дефекты.Например, использование ИП, особенно лопинавира/ритонавира (LPV/r), было связано с повышенным риском преждевременных родов, что может привести к увеличению младенческой заболеваемости и смертности. 6-8 Кроме того, необходимы данные о важных клинических исходах беременности, таких как артериальная гипертензия и увеличение веса (см. Схемы приема антиретровирусных препаратов и Исходы для матери и новорожденного). В исследовании Tsepamo в Ботсване риски неблагоприятных исходов беременности, кроме ДНТ, были одинаковыми для женщин, получавших схемы на основе DTG, и женщин, получавших схемы на основе EFV. 9-11 В целом данные о рисках, связанных с использованием других предпочтительных и альтернативных АРВ-препаратов до зачатия или на очень ранних сроках беременности, крайне ограничены; это отсутствие данных не указывает ни на наличие, ни на отсутствие риска при использовании препаратов, отличных от DTG и EFV. Чрезвычайно важно консультировать всех пациентов о потенциальных рисках и преимуществах АРВ-препаратов, чтобы способствовать принятию информированных индивидуальных решений (см. Приложение C: Консультативное руководство по антиретровирусной терапии для медицинских работников). 12
Фармакокинетические аспекты антиретровирусных препаратов
Физиологические изменения, происходящие во время беременности, могут влиять на всасывание, распределение, биотрансформацию и элиминацию лекарств; это также влияет на требования к дозировке лекарств и, потенциально, увеличивает риск вирусологической неудачи или токсичности лекарств. 13-15 Во время беременности время транзита через желудочно-кишечный тракт увеличивается, а количество воды и жира в организме увеличивается на протяжении всей беременности. Эти изменения сопровождаются увеличением сердечного выброса, вентиляции, печеночного и почечного кровотока.Концентрации белков плазмы также снижаются, что может снижать общие уровни лекарственного средства в плазме, но не обязательно уровни свободного или несвязанного лекарственного средства в плазме. Кроме того, увеличивается реабсорбция натрия в почках и происходят изменения в клеточных транспортерах и ферментах, метаболизирующих лекарственные препараты, в печени и кишечнике. Плацентарный транспорт лекарств, компартментализация лекарств в эмбрионе/плоде и плаценте, биотрансформация лекарств плодом и плацентой и элиминация лекарств плодом также могут влиять на фармакокинетику лекарств у беременной женщины.В целом, фармакокинетика НИОТ и ненуклеозидных ингибиторов обратной транскриптазы (ННИОТ) у беременных и небеременных женщин одинакова (хотя данные о фармакокинетике этравирина [ETR] ограничены). ФК ИП и ИНСТИ более вариабельны, особенно во втором и третьем триместрах. Имеющиеся в настоящее время данные о ФК и дозах АРВ-препаратов при беременности перечислены для каждого препарата ниже и обобщены в Таблице 11.
Нуклеозидные ингибиторы обратной транскриптазы
Предпочтительными комбинациями НИОТ для применения у беременных женщин, ранее не получавших АРВ-препараты, являются абакавир (АВС), применяемый в комбинации с ламивудином (3TC), и тенофовира дизопроксила фумарат (TDF) или тенофовир алафенамид (TAF), используемый в комбинации с эмтрицитабином (FTC). или 3ТС.
Абакавир плюс ламивудин является компонентом НИОТ в некоторых схемах Preferred для небеременных взрослых. Его преимущество в том, что его принимают один раз в день, и он хорошо переносится во время беременности. 16 Тестирование на аллель HLA-B*5701 должно быть выполнено и задокументировано как отрицательное до начала ABC, и женщины должны быть информированы о симптомах реакций гиперчувствительности. Клиницисты должны определить, есть ли у пациента коинфекция вирусом гепатита В (ВГВ)/ВИЧ; для женщин с коинфекцией ВГВ/ВИЧ следует выбрать два НИОТ, которые активны в отношении ВГВ (например,например, TDF с FTC или 3TC) вместо ABC плюс 3TC (см. Коинфекция ВГВ/ВИЧ).
Тенофовира дизопроксила фумарат или тенофовира алафенамид плюс эмтрицитабин или ламивудин являются компонентами НИОТ в некоторых схемах Preferred для небеременных взрослых. Эти комбинации имеют несколько преимуществ, включая обнадеживающие фармакокинетические данные, большой опыт применения во время беременности, дозировку один раз в сутки, повышенную активность против ВГВ и меньшую токсичность, чем ZDV плюс ламивудин. 17-19 Эффективность и токсичность TDF и TAF у беременных схожи.В исследовании International Mother Pediatric Adolescent AIDS Clinical Trials (IMPAACT) 2010 не наблюдалось различий в подавлении вируса, нежелательных явлениях степени 3 или выше или расчетном клиренсе креатинина среди людей, рандомизированных для начала TDF/FTC (n = 215) по сравнению с TAF/ FTC (n = 217) с DTG в гестационном возрасте >14 недель. В этом исследовании при схеме TAF/FTC наблюдалось меньше неблагоприятных исходов родов, чем при схемах TDF/FTC (24% против 33%, разница абсолютного риска -8,8%; 95% доверительный интервал (ДИ), -17.от 3% до -0,3%), 19 , что может быть связано с более высокой долей женщин с низкой прибавкой массы тела во время беременности в группе TDF/FTC (15,0% против 23,6%). 20 Однако у большего числа женщин в группе TAF/FTC наблюдался высокий гестационный набор веса, чем в группе TDF/FTC. Высокая прибавка массы тела во время беременности не была связана с неблагоприятными исходами в этом исследовании, но моделирование предполагает, что со временем избыточная прибавка массы тела при схемах, содержащих TAF и DTG, может привести к увеличению массы тела до беременности и неблагоприятным исходам беременности, связанным с ожирением. 21 Кроме того, были опасения по поводу аномалий роста костей и роста у младенцев, подвергшихся воздействию TDF внутриутробно , но продолжительность и клиническая значимость результатов исследования требуют дальнейшей оценки (см. Тенофовира дизопроксила фумарат). 22
Зидовудин плюс ламивудин представляет собой комбинацию Альтернатива НИОТ для беременных, ранее не получавших АРВ-препараты. Несмотря на доказанную эффективность в предотвращении перинатальной передачи ВИЧ и обширный опыт применения во время беременности, эта комбинация НИОТ классифицируется как Альтернатива , а не Предпочтительная , поскольку требует приема два раза в день и связана с более высокой частотой побочных эффектов легкой и средней степени тяжести. эффекты, включая тошноту, головную боль и обратимую анемию и нейтропению у матери и новорожденного (см. Зидовудин).
Беременных, получающих диданозин или ставудин , следует перевести на предпочтительные или альтернативные препараты.
Ингибиторы переноса цепей Integrase
Долутегравир (DTG) является предпочтительным ИИ для беременных, поскольку имеется достаточно данных о фармакокинетике, эффективности и безопасности DTG при его применении во время беременности. Группа рассмотрела все данные, доступные по состоянию на октябрь 2021 года, относительно использования DTG до зачатия или в течение первого триместра беременности.На основании этих данных DTG считается предпочтительным препаратом для использования во время беременности и для людей, которые пытаются забеременеть (см. Руководство по антиретровирусным препаратам для взрослых и подростков).
Эффективность и переносимость. DTG связан с более высокими показателями вирусной супрессии, более быстрыми темпами снижения вирусной нагрузки, лучшей переносимостью и более высоким генетическим барьером для лекарственной устойчивости, чем другие агенты Preferred и Alternative . 9 , 10 , 23 Два рандомизированных клинических испытания, в которых сравнивали DTG плюс два НИОТ с EFV плюс два НИОТ у женщин, не получавших АРТ, которые начали терапию во время беременности, показали, что АРТ на основе DTG вызывала более быстрое вирусное подавление, при этом большая часть женщин достигает неопределяемой вирусной нагрузки (<50 копий/мл) во время родов. 11, 24 Более высокие показатели вирусной супрессии не приводили к статистически значимо более низким показателям наблюдаемой вертикальной передачи при использовании DTG по сравнению с EFV, даже несмотря на то, что показатели передачи были низкими при использовании обеих схем, а исследования не позволяли выявить небольшие различия. 11, 25, 26 Программные данные из Бразилии также указывают на более высокие показатели подавления вирусной нагрузки при родах с помощью DTG, чем с ATV/r. 27
Безопасность . Крупное исследование наблюдения за рождаемостью Tsepamo в Ботсване показало, что риск ДНТ ниже, чем сообщалось ранее в предварительных данных исследования. 6 В этом исследовании воздействие DTG во время зачатия было связано с небольшим, но статистически значимым увеличением распространенности ДНТ у младенцев в Ботсване; см. Тератогенность.В самом последнем анализе распространенность DTG в периконцепционный период (0,15%) была выше, чем распространенность NTD у детей, рожденных женщинами, получавшими EFV (0,06%), и женщинами без ВИЧ (0,07%), распространенность значительно не увеличилась. по сравнению с женщинами с ВИЧ, получающими любую схему АРВ-препаратов без DTG при зачатии (0,10%, разница в распространенности [разница 0,06%]; 95% ДИ, от 0,03% до 0,20%) 28 (см. Тератогенность).
Если существует причинно-следственная связь между применением DTG и возникновением ДНТ, механистическая этиология остается неизвестной, в том числе вопрос о том, является ли дефицит фолиевой кислоты опосредующим фактором (таким образом, будет ли риск снижаться за счет приема фолиевой кислоты) и может ли аналогичный риск существуют для других INTI.Не было установлено никакой связи между использованием DTG и нарушением метаболизма фолиевой кислоты, 29 , 30 , а также не существует доказательств того, что фолиевая кислота предотвращает связанные с DTG NTD. Известно, что фолиевая кислота предотвращает ДНТ у населения в целом. 31 , 32 Всем беременным и людям, которые могут забеременеть, следует ежедневно принимать не менее 400 мкг фолиевой кислоты.
Фармакокинетика s . Хотя некоторые фармакокинетические исследования показали, что уровни DTG в течение третьего триместра ниже предварительно определенного целевого уровня 33 и ниже уровней, оцененных после родов, 34 другие исследования показали, что эти изменения не были клинически значимыми, 19 и данные относительно переноса через плаценту и сравнения с уровнями у небеременных взрослых показывают, что коррекция дозы во время беременности не требуется (см. Долутегравир).Кроме того, уровни несвязанного DTG в плазме у беременных женщин соответствовали предложенной 90% ингибирующей концентрации для несвязанного DTG. 15
Последствия для здоровья матери. По мере накопления опыта применения DTG во время беременности и в послеродовом периоде важным фактором является увеличение массы тела матери во время и после беременности. Значительное увеличение веса при схемах на основе DTG наблюдалось у небеременных групп населения, особенно среди женщин и среди людей, также получающих TAF. 35 , 36 Во время беременности также наблюдалось увеличение массы тела, связанное с приемом ДТГ, но это может отражать лучшее состояние здоровья матери (например,g., более низкие показатели недостаточного набора веса или потери веса во время беременности с помощью АРТ на основе DTG). В некоторых исследованиях наблюдалось большее увеличение веса во время беременности при приеме TAF/FTC/DTG (0,08 кг в неделю) 37 и TDF/FTC/DTG (0,03–0,05 кг в неделю) 37 , 38 , чем при приеме TDF /FTC/EFV, в то время как другие не обнаружили повышенного набора веса во время беременности с DTG. 39 Однако еженедельная прибавка веса во время беременности у женщин, получавших АРТ на основе DTG или EFV, оставалась меньше, чем у женщин без ВИЧ, 38 меньше, чем рекомендуется для населения в целом. 37 Меньше неблагоприятных исходов при родах было при использовании DTG, что может быть объяснено меньшим недостаточным набором веса при схемах на основе DTG. Послеродовая прибавка массы тела была выше у женщин, получавших DTG, чем у женщин, получавших АРТ на основе EFV, но была аналогична прибавке массы тела у женщин в послеродовом периоде без ВИЧ-инфекции в перинатальном исследовании DolPHIN-2 (долутегравир у беременных ВИЧ-инфицированных матерей и их новорожденных). 40 , 41
Ралтегравир (RAL) является предпочтительным ИС для использования у беременных, ранее не получавших АРВ, на основании ФК, безопасности и других данных об использовании RAL во время беременности. 42-46 Клинические испытания и программные данные демонстрируют более быстрое разрушение вируса и большую долю вирусной супрессии при родах при использовании RAL, чем при использовании EFV или усиленных ИП. 27, 47, 48, 49-51
Хотя лекарственная форма RAL для приема один раз в день одобрена для применения у небеременных взрослых, фармакокинетические данные указывают на низкие уровни препарата при приеме один раз в день во время беременности 52, 53 ; дозирование два раза в день остается рекомендуемым графиком дозирования.
Элвитегравир/кобицистат (EVG/c) представляет собой ИИ, для которого данные об использовании во время беременности в настоящее время ограничены. 54-56 Данные исследования P1026 и исследования PANNA позволяют предположить, что совместное введение EVG и COBI приводило к значительно более низким уровням обоих препаратов в третьем триместре, чем в послеродовом периоде (уровни в третьем триместре были ниже уровней, которые ожидается, что это приведет к подавлению вируса). 57 Прорывы вируса действительно имели место в исследовании P1026, и только 74% женщин сохраняли вирусную супрессию при родах. 58, 59 На основании этих данных EVG/c не рекомендуется для первоначального использования во время беременности.В ретроспективной когорте из 134 женщин в девяти центрах третичной медицинской помощи в США, которые получали ЭВГ в любой период беременности, вирусная супрессия при родах составила 81% (88% среди тех, кто начал ЭВГ до беременности), а общая перинатальная передача ВИЧ была ниже. 0,8%. 56,60 У людей, уже получающих EVG/c, которые забеременели и имеют вирусную супрессию, можно рассмотреть продолжение режима с частым мониторингом вирусной нагрузки во втором и третьем триместре (например, каждые 1–2 месяца), или режим может быть переключен на другой режим Предпочтительный режим во время беременности.Если беременность планируется, EVG/c можно изменить, а вирусную супрессию по новому режиму подтвердить до зачатия.
Биктегравир (BIC) — это ИИ, который рекомендуется для первоначального применения у небеременных взрослых. Данные о фармакокинетике BIC при беременности не опубликованы, а данные о клинических исходах при беременности крайне ограничены; в аннотации, представленной производителем BIC, не было зарегистрировано ДНТ среди 18 женщин с проспективными сообщениями о воздействии в период до зачатия. 61
Каботегравир (КАБ) — это ИИ, который является частью полной схемы АРТ с двумя препаратами, доступной для использования в виде инъекционной формы длительного действия (в сочетании с инъекционным RPV длительного действия) у небеременных взрослых с уровнем РНК <50 копий/мл в течение не менее 3 месяцев, получают стабильный режим антиретровирусной (АРВ) терапии, не имеют в анамнезе неэффективного лечения и не имеют известной или предполагаемой резистентности.Таким образом, CAB Не рекомендуется для беременных или небеременных людей, начинающих или возобновляющих АРТ, или для тех, чья текущая схема плохо переносится и/или не полностью подавляет. Недостаточно данных для людей, забеременевших на КАБ, или тех, кто планирует забеременеть, поскольку доступные данные о фармакокинетике беременности ограничены (n = 3), а данные о клинических исходах во время беременности крайне ограничены. 62 Группа рекомендует людям, забеременевшим при приеме инъекционных КАБ длительного действия и RPV, перейти на пероральную схему АРТ, рекомендованную для использования во время беременности; время перехода должно учитывать длительный период полувыведения инъекционной формы длительного действия (медиана 5.6–11,5 нед) с персистенцией препарата до 12 мес. 63 При текущем графике дозирования ежемесячных внутримышечных (IM) инъекций переход на пероральный режим должен происходить в течение 4 недель после последних внутримышечных доз CAB и RPV. 64 Рекомендации по дозировке, включая руководство по переходу на пероральный режим, можно найти в инструкциях по применению 63, 65 и в Руководстве по антиретровирусной терапии для взрослых и подростков.
Ингибиторы протеазы
Атазанавир/ритонавир (ATV/r) и дарунавир/ритонавир (DRV/r) являются предпочтительными ИП для применения у беременных, ранее не получавших АРВ-препараты, на основании исследований эффективности у взрослых и опыта применения во время беременности.Как и в случае с RAL, BIC и EVG/c, данные ограничены для понимания риска редких врожденных дефектов, таких как ДНТ, при применении этих АРВ-препаратов. Факторы, влияющие на решение о том, какое лекарство использовать, могут включать ограничения в одновременном назначении антацидов, блокаторов h3 или ингибиторов протонной помпы (для ATV/r) и необходимость приема дважды в день (для DRV/r). Хотя применение DRV/r один раз в сутки одобрено для небеременных взрослых, данных о фармакокинетике недостаточно для поддержки его применения во время беременности. 66
Атазанавир (ATV) связан с повышением уровня непрямого билирубина, что теоретически может повышать риск гипербилирубинемии у новорожденных; однако до настоящего времени в исследованиях не наблюдалось патологических возвышений. 67 В анализах педиатрического когортного исследования ВИЧ/СПИДа (PHACS) и исследования надзорного мониторинга токсичности АРВТ (SMARTT) внутриутробное воздействие атазанавира было связано с небольшим, но статистически значимым снижением языковых и социально-эмоциональных показателей. по сравнению с воздействием других наркотиков. 68 Воздействие АТВ также ассоциировалось с риском позднего появления языка через 12 месяцев, но уже не было значительным через 24 месяца. 69, 70 Клиническое значение этих результатов, связанных с воздействием in utero ATV, неизвестно.
Лопинавир/ритонавир (LPV/r) вместо Не рекомендуется для начала беременности, за исключением особых обстоятельств . Имеются обширный клинический опыт и данные о фармакокинетике применения LPV/r во время беременности, но во время беременности он требует приема два раза в день и часто вызывает тошноту и диарею; он также был связан с повышенным риском преждевременных родов и рождения детей с малым весом для гестационного возраста (см. Схемы антиретровирусной терапии и Исходы для матери и новорожденного).Людям, забеременевшим на супрессивной, хорошо переносимой схеме, включающей LPV/r, следует продолжать эту схему.
Дарунавир/кобицистат (DRV/c) и атазанавир/кобицистат (ATV/c) являются Не рекомендуется для использования во время беременности. 59, 71, 72 Фармакокинетические исследования показывают, что низкие уровни как DRV, так и COBI наблюдаются на поздних сроках беременности, а высокие показатели вирусологической неудачи наблюдаются на поздних сроках беременности среди женщин, вирусная супрессия которых наблюдалась на ранних сроках беременности.Уровни ATV были аналогичным образом ниже во втором и третьем триместрах; 59 Ожидается, что вирусологические и трансмиссивные исходы при применении ATV/c будут аналогичны наблюдаемым при применении DRV/c и EVG/c. Кроме того, однократная суточная доза DRV составляет Не рекомендуется для начальной терапии во время беременности. Людям, которые забеременели во время приема DRV/c или ATV/c и имеют вирусную супрессию, режим может быть продолжен с частым мониторингом вирусной нагрузки в течение второго и третьего триместров (например,g., каждые 1-2 месяца), или схема может быть изменена на другую схему Preferred во время беременности. Как для DRV, так и для ATV, COBI можно заменить на RTV в качестве фармакологического усилителя, но особое внимание следует уделить дозировке ATV (более высокая при использовании с TDF или антацидами) и DRV (дозировка два раза в день).
Текущие данные свидетельствуют о том, что при стандартной дозировке для взрослых концентрации LPV, ATV и DRV в плазме снижаются во втором и/или третьем триместре. Коррекция дозы рекомендуется для LPV/r и может быть рассмотрена для ATV/r, но коррекция дозы не рекомендуется для DRV/r (см. Таблицу 11). 73 Конкретные рекомендации по дозированию зависят от ИП, опыта лечения конкретного пациента и использования (если таковые имеются) сопутствующих препаратов, которые могут взаимодействовать с другими препаратами. 73-81 Клиницисты могут рассмотреть возможность терапевтического мониторинга лекарств в определенных ситуациях.
Некоторые старые ИП — IDV, NFV, RTV (в качестве единственного ИП) и небустированные саквинавир или типранавир — не рекомендуются для применения у взрослых, а другие — усиленный или небустированный фосампренавир, саквинавир/ритонавир и типранавир/ритонавир — не рекомендуются для начальной терапии у взрослых.Эти препараты являются Нерекомендуемыми и не должны использоваться у беременных из-за опасений, которые включают более низкую эффективность, токсичность, изменения фармакокинетики во время беременности, а также ограниченные данные и опыт применения при беременности. Подробную информацию об отдельных АРВ-препаратах, комбинациях АРВ-препаратов и схемах АРВ-терапии, которые не рекомендуются или не должны использоваться у взрослых, см. в Таблице 4, а также в Таблицах «Что не следует использовать» и в Таблице 11 Руководства по антиретровирусной терапии для взрослых и подростков.
Ненуклеозидные ингибиторы обратной транскриптазы
Не существует Предпочтительных ННИОТ для использования у беременных, ранее не получавших АРВ-препараты.
Скрининг на антенатальную и послеродовую депрессию рекомендуется всем беременным. Поскольку использование некоторых ННИОТ может увеличить риск депрессии и суицидальных наклонностей, этот скрининг особенно важен для пациентов, получающих схемы, содержащие EFV и RPV. 82-84
Эфавиренз (EFV) — это Альтернатива ННИОТ для беременных и небеременных, ранее не получавших АРВ-препараты. EFV может быть подходящим для людей, которые хотят принимать один раз в день комбинированный режим с фиксированными дозами и которые переносят EFV без побочных эффектов.Хотя данные об использовании EFV во время беременности обнадеживают в отношении NTD и предотвращения вертикальной передачи ВИЧ, при применении TDF/TDF/ FTC/EFV по сравнению с TAF/FTC/DTG. 11 Кроме того, к побочным эффектам, связанным с EFV, относятся головокружение, утомляемость, редкая и иногда тяжелая гепатотоксичность, яркие сновидения и/или ночные кошмары, а также повышенный риск суицидальных наклонностей. 9,83,85-89
Хотя первоначально считалось, что EFV также связан с повышенным риском ДНТ, крупные мета-анализы и данные из Ботсваны, описанные выше, убеждают в том, что риск ДНТ у младенцев, принимавших EFV в первом триместре, не превышает риск в общее население. 7,9,85,86,90 В результате Перинатальные рекомендации не ограничивают использование EFV во время беременности или у людей, которые планируют забеременеть; это согласуется с рекомендациями Британской ассоциации по ВИЧ и рекомендациями Всемирной организации здравоохранения, в которых отмечается, что EFV можно использовать на протяжении всей беременности 91 (см. Тератогенность и беременные с ВИЧ, которые в настоящее время получают антиретровирусную терапию).Обсервационное исследование сообщило о двукратном повышении риска микроцефалии среди детей, рожденных от 141 женщины, получавшей EFV, по сравнению с женщинами, получавшими другие АРВ-препараты в США; хотя другие факторы, такие как употребление алкоголя, незапланированная беременность, гестационный возраст на момент начала АРТ, изменения в практике АРВ-терапии с течением времени и небольшое число женщин, принимающих недавно рекомендованные АРВ-препараты в качестве препаратов сравнения (например, DTG [n = 52], RAL [n = 167] и DRV [n = 254]) — возможно, способствовали этой связи.Важно отметить, что Группа рекомендует, чтобы женщины, забеременевшие на супрессивных схемах, содержащих EFV , продолжали использовать эти схемы, как это рекомендуется для большинства схем 92 (см. Таблицу 4 и Таблицу 5).
Рилпивирин (RPV) (перорально) может использоваться как часть схемы АРТ для небеременных взрослых с РНК ВИЧ до лечения <100 000 копий/мл и количеством Т-лимфоцитов CD4 (CD4) >200 клеток/мм 3 . Имеются достаточные данные об использовании во время беременности, чтобы рекомендовать пероральный RPV в качестве агента Альтернатива для беременных, которые соответствуют тем же критериям количества CD4 и вирусной нагрузки. 5,56,93 Хотя фармакокинетические данные показывают, что концентрация RPV в плазме снижается во втором и третьем триместрах, это снижение меньше, чем снижение, наблюдаемое при EVG/c или DRV/c, и у большинства женщин будет адекватная экспозиция 5 ; однако возможны вирусные прорывы. Дозы RPV, превышающие стандартные, не изучались, поэтому данных недостаточно, чтобы рекомендовать изменение дозировки во время беременности. RPV следует принимать во время еды, что может затруднить его переносимость во время беременности.При стандартных дозах вируса чумы КРС необходимо часто контролировать вирусную нагрузку (например, каждые 1–2 месяца; см. Мониторинг состояния женщины и плода во время беременности).
Инъекционный RPV длительного действия, используемый в сочетании с инъекционным CAB длительного действия, Не рекомендуется для беременных, начинающих или возобновляющих АРТ, или чей текущий режим плохо переносится и/или не полностью подавляет (см. раздел о каботегравире выше). Недостаточно данных для тех, кто забеременел от инъекционного RPV длительного действия или для тех, кто планирует забеременеть, поскольку данные о фармакокинетике беременности ограничены, а данных о клинических исходах во время беременности очень мало.Группа рекомендует людям, забеременевшим при приеме инъекционных КАБ длительного действия и RPV, перейти на пероральную схему АРТ, рекомендованную для использования во время беременности; время перехода должно учитывать длительный период полувыведения инъекционного RPV длительного действия (в среднем 13–28 недель). 63 При текущем графике дозирования ежемесячных в/м инъекций переход на пероральный режим должен происходить в течение 4 недель после последних в/м доз CAB и RPV. 64 Рекомендации по дозировке, включая руководство по переходу на пероральный режим, можно найти в инструкции по применению 63,65 и в Руководстве по антиретровирусной терапии для взрослых и подростков.
Невирапин является Не рекомендуется для начальной АРТ у беременных, ранее не получавших АРВ-препараты, или у небеременных взрослых из-за большей вероятности побочных эффектов, сложного начального дозирования и низкого барьера резистентности. Этравирин является Не рекомендуется для беременных, ранее не получавших АРВ-препаратов, поскольку он не рекомендуется для небеременных пациентов, ранее не получавших АРВ-препаратов, а также из-за недостаточности данных о безопасности и фармакокинетике применения ETR во время беременности.Имеющиеся данные о фармакокинетике у женщин, получавших ЭТР в рамках клинической помощи, позволяют предположить, что стандартная доза для взрослых подходит во время беременности; в отличие от других АРВ-препаратов, воздействие ЭТР увеличивается во время беременности. 34,94 Тем не менее, может быть уместно начать прием любого из этих АРВ-препаратов в особых обстоятельствах, или может быть целесообразно продолжить их использование у людей, ранее получавших АРТ, которые забеременели на хорошо переносимых, полностью подавляющих схемах, включающих эти наркотики.
Применение доравирина при беременности еще не изучалось; данных недостаточно, чтобы рекомендовать его использование во время беременности.
Ингибиторы проникновения, прикрепления и слияния
Энфувиртид и маравирок (MVC) относятся к Не рекомендуется для начальной АРТ у беременных, поскольку они не рекомендуются для начальной АРТ у небеременных взрослых, а данные по безопасности и фармакокинетике этих препаратов при беременности ограничены. Имеющиеся данные о фармакокинетике у женщин, получавших MVC в рамках клинической терапии, позволяют предположить, что во время беременности уместна стандартная доза для взрослых, несмотря на снижение воздействия MVC во время беременности (см. Маравирок). 95 Использование этих препаратов может быть рассмотрено для беременных, у которых наблюдалась вирусологическая неудача при применении некоторых других классов АРВ-препаратов, а также для людей, которые забеременели на фоне хорошо переносимых подавляющих схем, включающих эти препараты; однако данных недостаточно для информирования о безопасности или рекомендациях по дозировке для их использования во время беременности, эти препараты следует использовать только после консультации со специалистами по ВИЧ и акушерством.
Ибализумаб представляет собой гуманизированное моноклональное антитело к рецептору CD4. Фостемсавир является ингибитором прикрепления. Оба препарата показаны пациентам с ВИЧ с множественной лекарственной устойчивостью, для которых не может быть доступных терапевтических альтернатив. Однако данных о применении этих препаратов во время беременности нет.
Фармакологические бустеры
Низкая доза ритонавира в качестве фармакологического бустерного препарата для других ИП, как описано выше, в настоящее время является предпочтительным фармакологическим бустером для использования при беременности. Cobicistat- усиленные АРВ-препараты (ATV, DRV или EVG) Не рекомендуется для использования во время беременности.Как отмечалось выше, было обнаружено, что уровни EVG, DRV, ATV и COBI значительно ниже в третьем триместре, чем в послеродовом периоде. 59,71,72 Тем не менее, для людей, которые забеременели во время лечения COBI-стимулированными схемами и имеют вирусную супрессию, схема может быть продолжена с частым мониторингом вирусной нагрузки в течение второго и третьего триместра (например, каждые 1-2 месяца) , или режим может быть переключен на другой режим Preferred во время беременности. См. раздел «Беременные с ВИЧ, которые в настоящее время получают антиретровирусную терапию и мониторинг во время беременности», чтобы узнать о вопросах, которые следует решать пациентам при принятии решения о переходе на другой режим АРВ-терапии или продолжении текущего режима с частым мониторингом вирусной нагрузки.
Ссылки
- Рабочая группа PHASES. Преодоление пробела в доказательствах для беременных женщин в отношении ВИЧ и сопутствующих инфекций: призыв к действию. Чапел-Хилл, Северная Каролина: 2020. Доступно по адресу: http://www.hivpregnancyethics.org.
- Абрамс Э.Дж., Мофенсон Л.М., Позняк А. и др. Расширенное и своевременное исследование АРВ-препаратов для использования беременными женщинами. J Приобретенный иммунодефицитный синдром . 2020 г. (онлайн перед печатью). Доступно по ссылке: https://www.ncbi.nlm.nih.gov/pubmed/33298793.
- Литвин Л., Семенюк Р.А., Дилмитис С. и соавт.Ценности и предпочтения женщин, живущих с ВИЧ, беременных, родильниц или планирующих забеременеть в отношении выбора антиретровирусной терапии во время беременности. BMJ Открытый . 2017;7(9):e019023. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/288.
- Руководящий комитет регистра антиретровирусных препаратов для беременных. Международный промежуточный отчет Антиретровирусного реестра беременных за 1 января 1989 г. – 31 января 2021 г. Уилмингтон, Северная Каролина: Координационный центр реестра; 2021. Доступно по адресу: http://www.apegistry.com.
- Frange P, Tubiana R, Sibiude J, et al. Рилпивирин у ВИЧ-1-позитивных женщин, начинающих беременность: переходить или не переходить? J Antimicrob Chemother . 2020;75(5):1324-1331. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/32157283.
- Заш Р., Холмс Л., Дисеко М. и др. Обновленная информация о дефектах нервной трубки при антиретровирусном воздействии в исследовании Tsepamo, Ботсвана. Представлено на: Международной конференции по СПИДу. 2020.
- Заш Р., Холмс Л., Дисеко М. и др.Дефекты нервной трубки и схемы антиретровирусного лечения в Ботсване. N Английский J Med . 2019;381(9):827-840. Доступно по ссылке: https://www.ncbi.nlm.nih.gov/pubmed/31329379.
- Tshivuila-Matala COO, Honeyman S, Nesbitt C, Kirtley S, Kennedy SH, Hemelaar J. Неблагоприятные перинатальные исходы, связанные со схемами антиретровирусной терапии: систематический обзор и сетевой метаанализ. СПИД . 2020;34(11):1643-1656. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/32701581.
- Заш Р., Якобсон Д.Л., Дисеко М. и др.Сравнительная безопасность антиретровирусного лечения на основе долутегравира или эфавиренца, начатого во время беременности в Ботсване: обсервационное исследование. Ланцет Глоб Здоровье . 2018;6(7):e804-e810. Доступно по ссылке: https://www.ncbi.nlm.nih.gov/pubmed/29880310.
- Venter WDF, Moorhouse M, Sokhela S, et al. Долутегравир плюс два разных пролекарства тенофовира для лечения ВИЧ. N Английский J Med . 2019;381(9):803-815. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/31339677.
- Локман С., Браммель С.С., Зиемба Л. и др.Эффективность и безопасность долутегравира с эмтрицитабином и тенофовир алафенамид фумаратом или тенофовира дизопроксил фумаратом, а также эфавиренцем, эмтрицитабином и тенофовиром дизопроксилфумаратом схемы антиретровирусной терапии ВИЧ, начатые во время беременности (IMPAACT 2010/VESTED): многоцентровое, открытое, рандомизированное, контролируемое, испытание 3 фазы. Ланцет . 2021;397(10281):1276-1292. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/33812487.
- Редфилд Р.Р., Моди С., Мур К.А., Делани А., Хонейн М.А., Томлинсон Х.Л.Автономия здравоохранения женщин, живущих с ВИЧ. N Английский J Med . 2019;381(9):798-800. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/31339674.
- Мирочник М., Каппарелли Э. Фармакокинетика антиретровирусных препаратов у беременных. Клин Фармакокинета . 2004;43(15):1071-1087. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/15568888.
- Roustit M, Jlaiel M, Leclercq P, Stanke-Labesque F. Фармакокинетика и терапевтический мониторинг антиретровирусных препаратов у беременных женщин. Бр Дж Клин Фармакол . 2008;66(2):179-195. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/18537960.
- Боллен П., Фрериксен Дж., Конопницкий Д. и соавт. Влияние беременности на фармакокинетику общего и несвязанного долутегравира и его основного метаболита у женщин, живущих с вирусом иммунодефицита человека. Клин Заражение Дис . 2020; ciaa006. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/32103260.
- Шапиро Р.Л., Хьюз М.Д., Огву А. и соавт. Антиретровирусные схемы при беременности и кормлении грудью в Ботсване. N Английский J Med . 2010;362(24):2282-2294. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/20554983.
- Момпер Дж., Бест Б., Ван Дж. и др. Фармакокинетика тенофовира алафенамида с кобицистатом и без него при беременности. Представлено на: 22-й Международной конференции по СПИДу; 2018. Амстердам, Нидерланды.
- Брукс К., Пинилла М., Шапиро Д. и др. Фармакокинетика тенофовира алафенамида в дозе 25 мг с бустерами фармакокинетики во время беременности и после родов. Представлено на семинаре по клинической фармакологии ВИЧ, гепатита и других противовирусных препаратов; 2019.Нордвейк, Нидерланды.
- Боллен П., Фрериксен Дж., Конопницкий Д. и соавт. Влияние беременности на фармакокинетику общего и несвязанного долутегравира и его основного метаболита у женщин, живущих с вирусом иммунодефицита человека. Клин Заражение Дис . 2021;72(1):121-127. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/32103260.
- Хоффман Р.М., Зиемба Л., Браммель С., Чинула Л., Нематадзира Т.Г., Накаива Ф. Прибавка в весе до родов и неблагоприятные исходы беременности в ударе 2010 г.Резюме 176. Представлено: Конференция по ретровирусам и оппортунистическим инфекциям; 2021. Виртуальная конференция. Доступно по адресу: https://www.natap.org/2021/CROI/croi_83.htm.
- Baxevanidi EE, Asif S, Qavi A, et al. Предсказал долгосрочные неблагоприятные исходы родов и здоровья ребенка в исследовании ADVANCE. Резюме 572. Представлено на: конференции по ретровирусам и условно-патогенным инфекциям; 2021. Виртуальная конференция. Доступно по адресу: https://www.croiconference.org/abstract/predicted-long-term-adverse-birth-and-child-health-outcomes-in-the-advance-trial.
- Siberry GK, Jacobson DL, Kalkwarf HJ, et al. Более низкое содержание минералов в костях новорожденных связано с применением матерью тенофовира дизопроксила фумарата во время беременности. Клин Заражение Дис . 2015;61(6):996-1003. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/26060285.
- Заш Р., Раф К., Джейкобсон Д.Л. и др. Влияние гестационного возраста при начале терапии тенофовиром, эмтрицитабином и эфавирензом на неблагоприятные исходы родов в Ботсване. J Pediatric Infect Dis Soc . 2018;7(3):e148-e151.Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/29688554.
- Кинту К., Малаба Т.Р., Накибука Дж. и др. Долутегравир в сравнении с эфавиренцем у женщин, начинающих терапию ВИЧ на поздних сроках беременности (DolPHIN-2): открытое рандомизированное контролируемое исследование. Ланцет ВИЧ . 2020;7(5):e332-e339. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/32386721.
- Дэйви Д.Л.Дж., Беккер Л.Г., Машеле Н., Горбач П., Коутс Т.Дж., Майер Л. Сохранение и назначение PrEP для беременных женщин во время изоляции от COVID-19 в Южной Африке. Ланцет ВИЧ . 2020;е735. Доступно по ссылке: https://pubmed.ncbi.nlm.nih.gov/32758479.
- Малаба Т.Р., Накатудде И., Кинту К. и др. Окончательные результаты DolPHIN2: долутегравир по сравнению с эфавирензом на поздних сроках беременности и через 72 недели после родов. Представлено на: конференции по ретровирусам и условно-патогенным инфекциям; 2021. Виртуальная конференция. Доступно по адресу: https://www.croiconference.org/abstract/dolphin2-final-results-dolutegravir-vs-efavirenz-in-late-pregnancy-to-72w-postpartum/?utm_source=rss&utm_medium=rss&utm_campaign=dolphin2-final- результаты-долутегравир-против-эфавиренц-в-поздней-беременности-до-72н-послеродовой&utm_source=rss&utm_medium=rss&utm_campaign=dolphin2-final-results-долутегравир-против-эфавиренз-в-поздней-беременности-до-72н-послеродовой.
- Pascom ARP, Fonseca FF, Pinho RGG, Perini FB, Pereira G, Avelino-Silva VI. Влияние антиретровирусного режима на подавление вирусной нагрузки у беременных женщин, живущих с ВИЧ, в Бразилии. Int J STD AIDS . 2020;31(9):903-910. Доступно по ссылке: https://www.ncbi.nlm.nih.gov/pubmed/32702281.
- Заш Р., Холмс Л.Б., Дисеко М. и др. Обновленная информация о дефектах нервной трубки при антиретровирусном воздействии в исследовании Tsepamo, Ботсвана. Аннотация PEBLB14. Представлено в: ИАС; 2021. Виртуальная конференция Доступно по адресу: https://www.ias2021.org/wp-content/uploads/2021/07/IAS2021_Abstracts_web.pdf
- Мохан Х., Ленис М.Г., Лоретт Э.Ю. и др. Применение долутегравира у беременных мышей связано с повышенной частотой дефектов плода при терапевтических, но не сверхтерапевтических дозах. EBioMedicine . 2021;63:103167. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/33341441.
- Chandiwana NC, Chersich M, Venter WDF, et al. Неожиданные взаимодействия между долутегравиром и фолатом: данные рандомизированного исследования из Южной Африки. СПИД . 2021;35(2):205-211. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/33086234.
- Zamek-Gliszczynski MJ, Zhang X, Mudunuru J, et al. Клиническая экстраполяция эффектов долутегравира и других ингибиторов интегразы ВИЧ на пути транспорта фолиевой кислоты. Препарат Метаб Dispos . 2019;47(8):890-898. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/31167838.
- Кабрера Р.М., Соудер Дж.П., Стил Дж.В. и др. Антагонизм долутегравира к рецепторам фолиевой кислоты: снижение токсического воздействия на развитие путем приема фолиевой кислоты. СПИД . 2019;33(13):1967-1976. Доступно по ссылке: https://www.ncbi.nlm.nih.gov/pubmed/31259764.
- Уэйтт С., Оррелл С., Валимва С. и др. Безопасность и фармакокинетика долутегравира у беременных с ВИЧ-инфекцией и их новорожденных: рандомизированное исследование (исследование ДолФИН-1). ПЛОС Мед . 2019;16(9):e1002895. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/31539371.
- Mulligan N, Best BM, Wang J, et al. Фармакокинетика долутегравира у беременных и родильниц, живущих с ВИЧ. СПИД . 2018;32(6):729-737. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/262.
- Venter F, Sokhela S, Fairlie L, Serenata C. Исследование ADVANCE: Фаза 3, рандомизированное сравнение TAF/FTC+DTG, TDF/FTC+DTG или TDF/FTC/EFV для лечения первой линии ВИЧ-1-инфекции . Представлено на Международной виртуальной конференции по СПИДу; 2020. Доступно по адресу: https://www.natap.org/2020/IAC/IAC_84.htm.
- Куанфак С., Санчес Т., Ванджи М. и др. Долутегравир по сравнению со схемами на основе низких доз эфавиренца для начального лечения инфекции ВИЧ-1 в Камеруне: результаты 96-й недели исследования ANRS 12313 NAMSAL.Представлено на Международной виртуальной конференции по СПИДу; 2020.
- Чинула Л., Бруммель С.С., Зимба Л., Страникс-Чибанда Л., Колетти А., Кротье Цеа. Безопасность и эффективность DTG по сравнению с EFV и TDF по сравнению с TAF при беременности: исследование Impaact 2010. Представлено на: конференции по ретровирусам и условно-патогенным инфекциям; 2020. Бостон, Массачусетс.
- Caniglia EC, Shapiro R, Diseko M, et al. Увеличение веса во время беременности у женщин, начинающих прием долутегравира, в Ботсване. EClinicalMedicine . 2020;29-30:100615.Доступно по ссылке: https://www.ncbi.nlm.nih.gov/pubmed/33437946.
- Джао, Дж. Классная антиретровирусная терапия и увеличение массы тела во время беременности: результаты PHACS SMARTT. Представлено на: конференции по ретровирусам и условно-патогенным инфекциям; 2021. Виртуальная конференция.
- Джао Дж., Сунь С., Легбедзе Дж. и др. Использование долутегравира связано с более высоким весом в послеродовом периоде по сравнению с эфавирензом. Представлено на: конференции по ретровирусам и условно-патогенным инфекциям; 2020. Бостон, Массачусетс. Доступно по адресу: https://www.croiconference.org/abstract/dolutegravir-use-is-associated-with-higher-postpartum-weight-compared-to-efavirenz.
- Малаба Т.Р., Чен Т., Кинту К. и др. Послеродовые изменения веса у женщин, начинающих прием DTG по сравнению с EFV во время беременности: dolPHIN-2. Представлено на: конференции по ретровирусам и условно-патогенным инфекциям; 2020. Бостон, Массачусетс. Доступно по адресу: https://www.croiconference.org/abstract/postpartum-weight-changes-in-women-initiating-dtg-vs-efv-in-pregnancy-dolphin-2.
- McKeown DA, Rosenvinge M, Donaghy S, et al.Высокие неонатальные концентрации ралтегравира после трансплацентарного переноса у ВИЧ-1 положительных беременных женщин. СПИД . 2010;24(15):2416-2418. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/20827058.
- Пиннетти С., Барончелли С., Виллани П. и др. Быстрое снижение уровня РНК ВИЧ после добавления ралтегравира и тенофовира к текущей высокоактивной антиретровирусной терапии у женщины с высокой виремией ВИЧ на 38-й неделе беременности. J Antimicrob Chemother .2010;65(9):2050-2052. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/20630894.
- Яворский Д., Томпсон С., Юдин М.Х. и соавт. Использование более новых антиретровирусных препаратов, дарунавира и этравирина с ралтегравиром или без него, при беременности: отчет о двух случаях. Антивир Тер . 2010;15(4):677-680. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/20587860.
- Блонк М., Колберс А., Идальго-Тенорио С. и др. Ралтегравир у беременных с ВИЧ-1: фармакокинетика, безопасность и эффективность. Клин Заражение Дис . 2015;61(5):809-816. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/254.
- Watts DH, Stek A, Best BM и др. Фармакокинетика ралтегравира при беременности. J Приобретенный иммунодефицитный синдром . 2014;67(4):375-381. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/25162818.
- Жоао Э.К., Моррисон Р.Л., Шапиро Д.Е. и др. Ралтегравир в сравнении с эфавирензом у беременных женщин, живущих с ВИЧ, ранее не получавших антиретровирусную терапию (NICHD P1081): открытое, рандомизированное, контролируемое исследование 4 фазы. Ланцет ВИЧ . 2020;7(5):e322-e331. Доступно по ссылке: https://www.ncbi.nlm.nih.gov/pubmed/32386720.
- Бритес С., Нобрега И., Лус Э., Травассос А.Г., Лоренцо С., Нетто Э.М. Ралтегравир в сравнении с лопинавиром/ритонавиром для лечения ВИЧ-инфицированных беременных с поздним обращением. Клинические испытания ВИЧ . 2018;19(3):94-100. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/29629852.
- Чжэн Ю., Хирт Д., Дельмас С. и др. Влияние беременности на концентрацию несвязанного ралтегравира в исследовании ANRS 160 RalFe. Антимикробные агенты Chemother . 2020;64(10). Доступно по ссылке: https://www.ncbi.nlm.nih.gov/pubmed/32661003.
- Benamor Teixeira ML, Fuller TL, Fragoso Da Silveira Gouvea MI, et al. Эффективность трех режимов антиретровирусной терапии, начатых во время беременности: клинический опыт в Рио-де-Жанейро. Антимикробные агенты Chemother . 2020;64(12). Доступно по ссылке: https://www.ncbi.nlm.nih.gov/pubmed/33020151.
- Иллан Рамос М., Мазариегос Орельяна Д., Прието Тато Л.М., Наварро Гомес М.Л., Муньос Галлиго Э., Рамос Амадор Х.Т.Эффективность и безопасность ингибиторов интегразы у ВИЧ-инфицированных беременных женщин, наблюдаемых в Мадридской когорте. Мед Клин (Барк) . 2020;155(10):441-444. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/32473739.
- Bukkems VE, Post TM, Colbers AP, Burger DM, Svensson EM. Популяционный фармакокинетический анализ, оценивающий воздействие ралтегравира в дозе 1200 мг один раз в сутки на беременных женщин, живущих с ВИЧ. CPT Pharmacometrics Syst Pharmacol . 2021;10(2):161-172. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/33369217.
- ван дер Галиен Р., Тер Хайне Р., Греупинк Р. и др. Фармакокинетика ингибиторов ВИЧ-интегразы во время беременности: механизмы, клинические последствия и пробелы в знаниях. Клин Фармакокинета . 2018;58(3):309-323. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/291.
- Pain JB, Le MP, Caseris M, et al. Фармакокинетика долутегравира у недоношенных новорожденных после интенсификации лечения ВИЧ во время беременности. Антимикробные агенты Chemother .2015;59(6):3660-3662. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/25845873.
- Рахангдейл Л., Кейтс Дж., Поттер Дж. и др. Ингибиторы интегразы на поздних сроках беременности и быстрое снижение вирусной нагрузки ВИЧ. Am J Obstet Gynecol . 2016;214(3):385 e381-387. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/26
4. - Патель К., Хуо Ю., Джао Дж. и др. Подавление вируса при родах и исходах родов у беременных женщин, живущих с ВИЧ, с помощью долутегравира в США: сравнительный анализ эффективности и безопасности.Представлено на: AIDS 2020; 2020. Виртуально. Доступно по адресу: http://programme.aids2020.org/Abstract/Abstract/1174.
- Bukkems V, Necsoi C, Tenorio CH, et al. Клинически значимое более низкое воздействие элвитегравира в третьем триместре беременных, живущих с ВИЧ: данные исследования PANNA. Клин Заражение Дис . 2020; ciaa488. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/32330231.
- Момпер Дж., Бест Б.М., Ван Дж. и др. Фармакокинетика элвитегравира/кобицистата у беременных и родильниц с ВИЧ. СПИД . 2018;32(17):2507-2516. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/30134297.
- Бойд С.Д., Сэмпсон М.Р., Вишванатан П., Струбл К.А., Арья В., Шерват А.И. Антиретровирусные схемы, содержащие кобицистат, не рекомендуются во время беременности: точка зрения. СПИД . 2019;33(6):1089-1093. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/303.
- Badell ML, Sheth AN, Momplaisir F, et al. Многоцентровый анализ применения элвитегравира во время беременности на подавление вируса ВИЧ и перинатальные исходы. Открыть форум, заразить Dis . 2019;6(4):ofz129. Доступно по ссылке: https://www.ncbi.nlm.nih.gov/pubmed/31037241.
- Фэрроу Т., Дитон С., Нгуен Н. и др. Совокупный обзор безопасности использования элвитегравира и биктегравира во время беременности и риска дефектов нервной трубки. Аннотация P030. Представлено на: Лекарственная терапия ВИЧ; 2018. Глазго, Великобритания. Доступно по адресу: http://hivglasgow.org/wp-content/uploads/2018/11/P030-4.pdf.
- Патель П., С. Тиагараджа, С. Форд и др. Фармакокинетический хвост каботегравира при беременности и неонатальных исходах.Резюме 775. Представлено на: Конференция по ретровирусам и оппортунистическим инфекциям 2020. Бостон, Массачусетс. Доступно по ссылке: https://www.croiconference.org/abstract/cabotegravir-pharmacokinetic-tail-in-pregnancy-and-neonatal-outcomes.
- Cabenuva (суспензия для инъекций каботегравира пролонгированного действия; суспензия рилпивирина для инъекций пролонгированного действия), в одной упаковке для внутримышечного применения [вкладыш]. Управление по контролю за продуктами и лекарствами. 2021. Доступно по адресу: https://www.accessdata.fda.gov/drugsatfda_docs/label/2021/212888s000lbl.пдф.
- Группа по антиретровирусным рекомендациям для взрослых и подростков. Оптимизация антиретровирусной терапии в условиях подавления вирусной нагрузки. 2021. Доступно по адресу: https://clinicalinfo.hiv.gov/en/guidelines/adult-and-adolescent-arv/optimizing-antiretroviral-therapy-setting-virologic-suppression.
- Vocabria (каботегравир) [вкладыш]. Управление по контролю за продуктами и лекарствами. 2021. Доступно по адресу: https://www.accessdata.fda.gov/drugsatfda_docs/label/2021/212887s000lbl.pdf.
- Schalkwijk S, Ter Heine R, Colbers A, et al.Оценка режимов дозирования дарунавира/ритонавира для ВИЧ-позитивных беременных женщин с использованием полумеханистического фармакокинетического моделирования. J Антимикроб Chemother . 2019;74(5):1348-1356. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/30715324.
- Флоридия М., Равизза М., Масуэлли Г. и др. Профиль атазанавира и лопинавира у беременных женщин с ВИЧ: переносимость, активность и исходы беременности в обсервационном национальном исследовании. J Antimicrob Chemother . 2014;69(5):1377-1384.Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/24370933.
- Caniglia EC, Patel K, Huo Y, et al. Воздействие атазанавира внутриутробно и развитие нервной системы у младенцев: сравнительное исследование безопасности. СПИД . 2016;30(8):1267-1278. Доступно по ссылке: https://www.ncbi.nlm.nih.gov/pubmed/26867136.
- Райс М.Л., Зельдоу Б., Сиберри Г.К. и др. Оценка риска позднего появления речи после внутриутробного воздействия антиретровирусных препаратов у неинфицированных младенцев, подвергшихся воздействию ВИЧ. Pediatr Infect Dis J .2013;32(10):e406-413. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/24067563.
- Sirois PA, Huo Y, Williams PL, et al. Безопасность перинатального воздействия антиретровирусных препаратов: исходы развития у младенцев. Pediatr Infect Dis J . 2013;32(6):648-655. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/23340561.
- Crauwels HM, Osiyemi O, Zorrilla C, Bicer C, Brown K. Уменьшение воздействия дарунавира и кобицистата на ВИЧ-1-инфицированных беременных женщин, получающих лечение на основе дарунавира/кобицистата. ВИЧ Мед . 2019;20(5):337-343. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/30873741.
- Момпер Дж., Стек А., Ван Дж. и др. Фармакокинетика атазанавира, усиленная кобицистатом, во время беременности и после родов. Представлено на семинаре по клинической фармакологии ВИЧ, гепатита и других противовирусных препаратов; 2019. Нордвейк, Нидерланды.
- Le MP, Mandelbrot L, Descamps D, et al. Фармакокинетика, безопасность и эффективность усиленного ритонавиром атазанавира (300/100 мг один раз в сутки) у беременных женщин, инфицированных ВИЧ-1. Антивир Тер . 2015;20(5):507-513. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/25599649.
- Реатаз (атазанавир) вкладыш [вкладыш]. Управление по контролю за продуктами и лекарствами. 2018. Доступно по адресу: https://www.accessdata.fda.gov/drugsatfda_docs/label/2018/021567s042,206352s007lbl.pdf.
- Стек А.М., Мирочник М., Каппарелли Э. и др. Снижение воздействия лопинавира во время беременности. СПИД . 2006;20(15):1931-1939. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/16988514.
- Виллани П., Флоридия М., Пирилло М.Ф. и др. Фармакокинетика нелфинавира у ВИЧ-1-инфицированных беременных и небеременных женщин. Бр Дж Клин Фармакол . 2006;62(3):309-315. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/16
7.
- Брайсон Ю.Дж., Мирочник М., Стек А. и др. Фармакокинетика и безопасность нелфинавира при применении в комбинации с зидовудином и ламивудином у ВИЧ-инфицированных беременных женщин: протокол группы клинических исследований по СПИДу у детей (PACTG) 353. HIV Clin Trials .2008;9(2):115-125. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/18474496.
- Мирочник М., Бест Б.М., Стек А.М. и др. Воздействие лопинавира в повышенной дозе во время беременности. J Приобретенный иммунодефицитный синдром . 2008;49(5):485-491. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/18989231.
- Read JS, Best BM, Stek AM и др. Фармакокинетика новой лекарственной формы нелфинавира 625 мг во время беременности и после родов. ВИЧ Мед . 2008;9(10):875-882. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/18795962.
- Буйон-Пишо М., Жюльен В., Азрия Э. и др. Популяционный анализ изменений фармакокинетики лопинавира, связанных с беременностью, и их возможных последствий для коррекции дозы. J Antimicrob Chemother . 2009;63(6):1223-1232. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/115.
- Бест Б.М., Стек А.М., Мирочник М. и др. Фармакокинетика лопинавира в таблетках при повышенной дозе во время беременности. J Приобретенный иммунодефицитный синдром .2010;54(4):381-388. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/20632458.
- Форд Н., Шуббер З., Позняк А. и др. Сравнительная безопасность и психоневрологические нежелательные явления, связанные с применением эфавиренца в качестве антиретровирусной терапии первой линии: систематический обзор и метаанализ рандомизированных исследований. J Приобретенный иммунодефицитный синдром . 2015;69(4):422-429. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/25850607.
- Джонс Д.Л., Родригес В.Дж., Алкайд М.Л., Вайс С.М., Пельтцер К.Использование эфавиренца во время беременности связано с суицидальными мыслями у женщин в послеродовом периоде в сельской местности Южной Африки. Поведение при СПИДе . 2019;23(1):126-131. Доступно по ссылке: https://www.ncbi.nlm.nih.gov/pubmed/29959721.
- Миллс А.М., Антинори А., Клотет Б. и др. Неврологическая и психиатрическая переносимость рилпивирина (TMC278) по сравнению с эфавиренцем у ранее не получавших лечения ВИЧ-1-инфицированных пациентов через 48 недель. ВИЧ Мед . 2013;14(7):391-400. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/23298380.
- Ford N, Calmy A, Mofenson L. Безопасность эфавиренца в первом триместре беременности: обновленный систематический обзор и метаанализ. СПИД . 2011;25(18):2301-2304. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/211.
- Ford N, Shubber Z, Jao J, Abrams EJ, Frigati L, Mofenson L. Безопасность котримоксазола при беременности: систематический обзор и метаанализ. J Приобретенный иммунодефицитный синдром . 2014;66(5):512-521. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/24853309.
- Заш Р., Макема Дж., Шапиро Р.Л. Дефекты нервной трубки при лечении долутегравиром с момента зачатия. N Английский J Med . 2018;379(10):979-981. Доступно по ссылке: https://www.ncbi.nlm.nih.gov/pubmed/30037297.
- Martinez de Tejada B, Европейская группа по совместному исследованию беременных и детей с ВИЧ. Врожденные дефекты после применения антиретровирусной терапии на основе эфавиренца при зачатии/первом триместре беременности: многогрупповой анализ. J Приобретенный иммунодефицитный синдром . 2019;80(3):316-324. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/30570524.
- Бхаттачарья Д., Гупта А., Тирни С. и др. Гепатотоксичность и смертность, связанная с поражением печени, у женщин детородного возраста, живущих с ВИЧ, и с высоким уровнем CD4, начавших лечение по схемам, содержащим эфавиренз. Клин Заражение Дис . 2020; ciaa244. Доступно по ссылке: https://www.ncbi.nlm.nih.gov/pubmed/32161944.
- Эфавиренц (Сустива) [вкладыш]. Управление по контролю за продуктами и лекарствами.2019. Доступно по адресу: https://www.accessdata.fda.gov/drugsatfda_docs/label/2019/020972s057,021360s045lbl.pdf.
- Британская ассоциация ВИЧ. Руководство Британской ассоциации ВИЧ по ведению ВИЧ-инфекции во время беременности и после родов, 2018 г. (третье промежуточное обновление 2020 г.). 2020. Доступно по адресу: https://www.bhiva.org/file/5f1aab1ab9aba/BHIVA-Pregnancy-guidelines-2020-3rd-interim-update.pdf.
- Williams PL, Yildirim C, Chadwick EG, et al. Связь применения антиретровирусных препаратов матерями с микроцефалией у детей, подвергшихся воздействию ВИЧ, но не инфицированных (SMARTT): проспективное когортное исследование. Ланцет ВИЧ . 2019;7(1):e49-e58. Доступно по ссылке: https://www.ncbi.nlm.nih.gov/pubmed/31740351.
- Schalkwijk S, Colbers A, Konopnicki D, et al. Снижение экспозиции рилпивирина в третьем триместре беременности у ВИЧ-1-позитивных женщин. Клин Заражение Дис . 2017;65(8):1335-1341. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/285.
- Ramgopal M, Osiyemi O, Zorrilla C, et al. Фармакокинетика общего и несвязанного этравирина у беременных с ВИЧ-1. J Приобретенный иммунодефицитный синдром . 2016;73(3):268-274. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/27159225.
- Колберс А., Бест Б., Шалквейк С. и др. Фармакокинетика маравирока у беременных с ВИЧ-1. Клин Заражение Дис . 2015;61(10):1582-1589. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/26202768.
Лечение меноррагии у женщин с тромбоцитопенией с помощью тромбоцитов или тромбоцитов и гормонов — полнотекстовый просмотр
Низкий уровень тромбоцитов может возникать в результате заболеваний крови, таких как недостаточность костного мозга, или в результате прохождения таких процедур, как химиотерапия или трансплантация стволовых клеток.Основным осложнением низкого уровня тромбоцитов у женщин репродуктивного возраста является маточное кровотечение, которое может быть опасным для жизни. Иногда это кровотечение начинается при нормальном менструальном цикле, но может начаться неожиданно. В любом случае для остановки маточного кровотечения требуются не только препараты крови, включая тромбоциты, но и гормональное лечение.
Гормоны эстроген или прогестерон могут помочь в этом случае, предположительно, стимулируя эндометриальный ангиогенез. Было показано, что непрерывные оральные контрацептивы (ОК) очень эффективны в лечении обильных менструальных кровотечений у здоровых женщин, но было проведено мало исследований у женщин с низким уровнем тромбоцитов.Кроме того, они имеют мало побочных эффектов и являются противозачаточными. Высокие дозы премарина внутривенно также полезны, но только в течение нескольких дней, после чего последует сильное кровотечение. Гормоны прогестина так же эффективны и также являются контрацептивами.
Оральные контрацептивы обычно используются для остановки маточных кровотечений при тромбоцитопении, вторичной по отношению к недостаточности костного мозга, химиотерапии и/или трансплантации стволовых клеток, во время эпизодов тяжелой тромбоцитопении. В настоящее время нет данных, подтверждающих необходимость использования гормональной терапии в дополнение к переливанию тромбоцитов.Мы ожидаем показать, что использование непрерывного КОК в дополнение к переливаниям тромбоцитов приведет к лучшему и более быстрому контролю маточного кровотечения, чем только переливания тромбоцитов.
Подходящие субъекты должны быть гемодинамически стабильными, менструирующими женщинами в возрасте от 12 до 55 лет, у которых имеется недостаточность костного мозга или которые проходят химиотерапию и/или трансплантацию стволовых клеток по поводу других заболеваний с уровнем тромбоцитов менее 50 000/мкл и имеют тяжелое менструальное кровотечение, которое ожидается, что продлится не менее 2 недель.Субъекты будут рандомизированы для непрерывного приема ОКФ (Ло-оврал) по 1 таблетке два раза в день или плацебо два раза в день в течение одной недели. Все субъекты получат переливание тромбоцитов, чтобы поддерживать уровень тромбоцитов выше 20 000 на микролитр на протяжении всего исследования. Через неделю все субъекты, у которых продолжаются кровотечения, будут непрерывно получать по 1 таблетке ОК два раза в день. Те, у кого остановилось кровотечение, будут непрерывно получать 1 таблетку ОК в день. Лечение будет сравниваться по доле тех, кто останавливает вагинальное кровотечение через 7 и 14 дней после начала лечения.
Увеличение объема плазмы при здоровой беременности: систематический обзор и метаанализ продольных исследований | BMC Беременность и роды
- 1.
Miller JR, Keith MN, Rowntree LG. Плазма и объем крови при беременности. ДЖАМА. 1915; 65 (9): 779–82.
Артикул Google Scholar
- 2.
Раунтри Л.Г., Браун Г.Э., Рот Г.М. Объем крови и плазмы в норме и при патологии. Филадельфия: компания WB Saunders; 1929 г.
Google Scholar
- 3.
Dieckmann JW, Wegner CR. Кровь при нормальной беременности: объемы крови и плазмы. Arch Intern Med. 1934; 53 (1): 71–86.
КАС Статья Google Scholar
- 4.
Scholten RR, Lotgering FK, Hopman MT, Van Dijk A, Van de Vlugt M, Janssen MCH, Spaanderman MEA. Низкий объем плазмы у нормотензивных женщин с ранее преэклампсией предрасполагает к артериальной гипертензии.Гипертония. 2015;66(5):1066–72.
КАС пабмед Статья ПабМед Центральный Google Scholar
- 5.
Scholten RR, Sep S, Peeters L, Hopman MTE, Lotgering FK, Spaanderman MEA. Низкий объем плазмы до беременности и предрасположенность к преэклампсии и задержке роста плода. Акушерство Гинекол. 2011;117(5):1085–93.
ПабМед Статья ПабМед Центральный Google Scholar
- 6.
Аарденбург Р., Спаандерман М.Е.А., Экхарт Т.Х., ван Эйндховен Х.В., ван дер Хейден О.В.Х., Петерс Л.Л.Х. Низкий объем плазмы после беременности, осложненной преэклампсией, предрасполагает к гипертонической болезни при следующей беременности. Br J Obstet Gynaecol. 2003;110(11):1001–6.
Артикул Google Scholar
- 7.
Stekkinger E, Scholten RR, Heidema WM, Spaanderman MEA. Рецидивирующая преэклампсия у женщин с метаболическим синдромом и низким объемом плазмы: ретроспективное когортное исследование.Br J Obstet Gynaecol. 2015; 122(13):1773–80.
КАС Статья Google Scholar
- 8.
Campbell DM, MacGillivray I. Сравнение материнской реакции при первой и второй беременности в зависимости от веса ребенка. J Obstet Gynaecol Br Commonw. 1972;79(8):684–93.
КАС пабмед Статья ПабМед Центральный Google Scholar
- 9.
Duffus GM, Macgillivray I, Dennis KJ.Взаимосвязь между весом ребенка и изменениями электролитов, белков и эстриола в моче. J Obstet Gynaecol Br Commonw. 1971; 78 (2): 97–104.
КАС Статья Google Scholar
- 10.
Pirani BBK, Campbell DM, MacGillivray I. Объем плазмы при нормальной первой беременности. J Obstet Gynaecol Br Commonw. 1973; 80 (10): 884–7.
КАС пабмед Статья Google Scholar
- 11.
Rajalakshmi K, Raman L. Изменения объема плазмы у индийских женщин с нормальной беременностью. J Obstet Gynaecol Br Emp. 1985; 82: 521–7.
КАС Google Scholar
- 12.
Cope I. Изменения объема плазмы и крови на поздних и пролонгированных сроках беременности. J Obstet Gynaecol Br Emp. 1958; 65 (6): 877–94.
КАС пабмед Статья ПабМед Центральный Google Scholar
- 13.
Гибсон ХМ. Объем плазмы и скорость клубочковой фильтрации при беременности и их связь с различиями в росте плода. J Obstet Gynaecol Br Commonw. 1973; 80 (12): 1067–74.
КАС пабмед Статья ПабМед Центральный Google Scholar
- 14.
Hytten FE, Paintin DB. Увеличение объема плазмы при нормальной беременности. J Obstet Gynaecol Br Emp. 1963; 70: 402–7.
КАС пабмед Статья ПабМед Центральный Google Scholar
- 15.
Whittaker PG, Macphail S, Lind T. Серийные гематологические изменения и исход беременности. Акушерство Гинекол. 1996;88(1):33–9.
КАС пабмед Статья ПабМед Центральный Google Scholar
- 16.
Мильман Н., Келд-Эрик Б., Аггер А.О. Показатели гемоглобина и эритроцитов во время нормальной беременности и после родов у 206 женщин с добавками железа и без них. Acta Obstet Gynecol Scand. 2000; 79: 89–98.
КАС пабмед Статья ПабМед Центральный Google Scholar
- 17.
Breymann C. Оценка и дифференциальная диагностика железодефицитной анемии во время беременности. Клин по расследованию наркотиков. 2000;19(6):21–7.
КАС Статья Google Scholar
- 18.
Критерии CDC для анемии у детей и женщин детородного возраста. Еженедельный отчет о заболеваемости и смертности, Центры по контролю и профилактике заболеваний (CDC). 1989 год; 38:400–404. Проверено 16 июля 2017 г. В . , том. 38.
- 19.
Tuttle S, Aggett PJ, Campbell D, MacGillivray I. Питание цинком и медью во время беременности человека: лонгитюдное исследование у нормальных первородящих и у первобеременных с риском рождения ребенка с задержкой роста. Am J Clin Nutr. 1985;41(5):1032–41.
КАС пабмед Статья ПабМед Центральный Google Scholar
- 20.
Hall MH, Pirani BBK, Campbell D. Причина падения уровня фолиевой кислоты в сыворотке крови при нормальной беременности. Br J Obstet Gynaecol.1976; 83 (2): 132–6.
КАС пабмед Статья Google Scholar
- 21.
Агури С., Гернанд А.Д. Эффективный метод измерения объема плазмы с использованием индоцианинового зеленого красителя. МетодыX. 2019;6:1072–83.
ПабМед ПабМед Центральный Статья Google Scholar
- 22.
Райли А.А., Аракава Ю., Уорли С., Дункан Б.В., Фукамачи К. Объемы циркулирующей крови: обзор методов измерения и метаанализ у детей.АСАИО Дж. 2010;56(3):260–4.
ПабМед Статья Google Scholar
- 23.
Эртл А.С., Дидрих А., Радж С.Р. Методы, используемые для определения объема крови. Am J Med Sci. 2007;334(1):32–6.
ПабМед Статья Google Scholar
- 24.
Хатчинс CJ. Изменения объема плазмы во время беременности у первобеременных в Индии и Европе. Br J Obstet Gynaecol. 1980; 87: 586–9.
КАС пабмед Статья Google Scholar
- 25.
Liberati A, Altman DG, Tetzlaff J, Mulrow C, Gotzsche PC, Ioannidis JP, Clarke M, Devereaux PJ, Kleijnen J, Moher D. Заявление PRISMA для систематических обзоров и метаанализов исследований, оценка медицинских вмешательств: объяснение и разработка. ПЛОС Мед. 2009;6(7):e1000100.
ПабМед ПабМед Центральный Статья Google Scholar
- 26.
Салас С.П., Маршалл Г., Гутьеррес Б.Л., Россо П. Динамика объема материнской плазмы и гормональные изменения у женщин с преэклампсией или задержкой роста плода. Гипертония. 2006;47(2):203–8.
КАС пабмед Статья Google Scholar
- 27.
Мохер Д., Либерати А., Тецлафф Дж., Альтман Д.Г. Предпочтительные элементы отчетности для систематических обзоров и метаанализов: заявление PRISMA. Энн Интерн Мед. 2009;151(4):264–9.
Артикул Google Scholar
- 28.
Чепмен А.Б., Авраам В.Т., Замудио С., Гроб С., Меруани А., Янг Д., Джонсон А., Осорио Ф., Голдберг С., Мур Л.Г. и др. Временные отношения между гормональными и гемодинамическими изменениями на ранних сроках беременности человека. почки инт. 1998;54(6):2056–63.
КАС пабмед Статья Google Scholar
- 29.
Даунс С.Х., Блэк Н. Возможность создания контрольного списка для оценки методологического качества как рандомизированных, так и нерандомизированных исследований медицинских вмешательств.J Эпидемиол общественного здоровья. 1998; 52: 377–84.
КАС пабмед ПабМед Центральный Google Scholar
- 30.
Картер Э.Б., Темминг Л.А., Акин Дж., Фаулер С., Маконес Г.А., Колдитц Г.А., Туули М.Г. Групповой дородовой уход по сравнению с традиционным дородовым уходом: систематический обзор и метаанализ. Акушерство Гинекол. 2016;128(3):551–61.
ПабМед ПабМед Центральный Статья Google Scholar
- 31.
Дерсимониан Р., Лэрд Н. Метаанализ клинических испытаний. Контрольные клинические испытания. 1986; 7: 177–88.
КАС пабмед Статья ПабМед Центральный Google Scholar
- 32.
Абуду О.О., Софола О.А. Объем плазмы у нормальных беременных нигерийских первобеременных. Int J Gynaecol Obstet. 1985; 23: 137–42.
КАС пабмед Статья ПабМед Центральный Google Scholar
- 33.
де Хаас С., Госсейн-Доха С., ван Куйк С.М.Дж., ван Дронгелен Дж., Спаандерман М.А. Физиологическая адаптация объема материнской плазмы во время беременности: систематический обзор и метаанализ. УЗИ Акушерство Гинекол. 2017;49(2):177–87.
ПабМед Статья ПабМед Центральный Google Scholar
- 34.
Higgins JPT, Thompson SG. Количественная неоднородность в метаанализе. Стат мед. 2002;21(11):1539–58.
ПабМед ПабМед Центральный Статья Google Scholar
- 35.
Higgins JPT, Thompson SG, Deeks JJ, Altman DG. Измерение несогласованности в мета-анализах. БМЖ. 2003; 327: 557–60.
ПабМед ПабМед Центральный Статья Google Scholar
- 36.
Эггер М., Смит Г.Д., Шнайдер М., Миндер С. Смещение в метаанализе, обнаруженное с помощью простого графического теста. БМЖ. 1997; 315: 629–34.
КАС пабмед ПабМед Центральный Статья Google Scholar
- 37.
Begg CB, Mazumdar M. Рабочие характеристики теста ранговой корреляции для публикации Bias. Биометрия. 1994; 50(4):1088–101.
КАС пабмед ПабМед Центральный Статья Google Scholar
- 38.
Schwarzer G. meta: пакет R для метаанализа. Р Новости. 2007;3(7):40–5 https://cran. r-project.org/doc/Rnews/Rnews_2007-2003.pdf.
Google Scholar
- 39.
Шварцер Дж., Карпентер Дж. Р., Рюкер Дж.: Метаанализ с помощью R (Используйте-R!). Springer International Publishing, Швейцария . http://www.springer.com/gp/book/97833153; 2015.
Google Scholar
- 40.
Core Team R. R: язык и среда для статистических вычислений. В: R Foundation для статистических вычислений. Вена; 2017. URL https://www.R-project.org/.
- 41.
Taylor DJ, Lind T. Масса эритроцитов во время и после нормальной беременности.Br J Obstet Gynaecol. 1979;86(5):364–70.
КАС пабмед Статья ПабМед Центральный Google Scholar
- 42.
Paintin DB. Размер общего объема эритроцитов при беременности. J Obstet Gynaecol Br Emp. 1962; 69 (5): 719–23.
КАС пабмед Статья ПабМед Центральный Google Scholar
- 43.
Пиварник Дж.М., Мауэр М.Б., Айрес Н.А., Киршон Б., Дилди Г.А., Коттон Д.Б.Влияние хронических упражнений на увеличение объема крови и гематологические показатели во время беременности. Акушерство Гинекол. 1994; 83: 265–9.
КАС пабмед ПабМед Центральный Google Scholar
- 44.
Варгас М., Варгас Э., Джулиан К.Г., Армаза Дж.Ф., Родригес А., Теллез В., Нирмейер С., Уилсон М., Парра Э., Шрайвер М. и др. Детерминанты оксигенации крови во время беременности у жительниц высокогорья Анд и Европы. Am J Physiol Regul Integr Comp Physiol.2007; 293:1303–12.
Артикул КАС Google Scholar
- 45.
Абуду О.О., Маколей К., Олубойде О.А. Серийный ферритин сыворотки и другие гематологические параметры у нормальных нигерийских первобеременных. Int J Gynaecol Obstet. 1988;26(1):33–9.
КАС пабмед Статья ПабМед Центральный Google Scholar
- 46.
Bruinse HW, van den Berg H, Haspels AA. Курение и его влияние на объем материнской плазмы во время и после нормальной беременности.Eur J Obstet Gynecol Reprod Biol. 1985;20(4):215–9.
КАС пабмед Статья ПабМед Центральный Google Scholar
- 47.
Hytten FE, Leitch I. Физиология беременности человека. Оксфорд: Blackwell Scientific Publications Ltd; 1971.
Google Scholar
- 48.
Hytten F. Изменения объема крови при нормальной беременности. Клин Гематол. 1985; 14: 601–12.
КАС пабмед ПабМед Центральный Google Scholar
- 49.
Лецкий Е. Система крови. В: Hytten FE, Chamberlain G, редакторы. Клиническая физиология в акушерстве, стр. 43–78. Оксфорд: Научные публикации Блэквелла; 1980.
Google Scholar
- 50.
Харрисон К.А. Изменения объема крови при нормальной беременности. J Obstet Gynaecol Br Commonw. 1966; 73: 717–23.
КАС пабмед Статья Google Scholar
- 51.
Лунд С.Дж., Донован Д.С.Объем крови во время беременности: значение объемов плазмы и эритроцитов. Am J Obstet Gynecol. 1967; 96 (3): 394–403.
Google Scholar
- 52.
West CA, Sasser JM, Baylis C. Загадка постоянного увеличения объема плазмы при беременности: критическая роль ренин-ангиотензин-альдостероновой системы. Am J Physiol Renal Physiol. 2016;311(6):F1125–34.
КАС пабмед ПабМед Центральный Статья Google Scholar
- 53.
Soma-Pillay P, Nelson-Piercy C, Tolppanen H, Mebazaa A. Физиологические изменения во время беременности. Cardiovasc J Afr. 2016;27(2):89–94.
ПабМед ПабМед Центральный Статья Google Scholar
- 54.
Донкерс Дж., Шолтен Р.Р., Ойен В.Дж., Хопман М.Т., Лотгеринг Ф.К., Спаандерман М.Э. Необъяснимое невынашивание беременности в первом триместре и низкие венозные резервы. Хум Репрод. 2012;27(9):2613–8.
ПабМед Статья Google Scholar
- 55.
CDC: критерии CDC для анемии у детей и женщин детородного возраста. По состоянию на 16 июля 2017 г. Еженедельный отчет о заболеваемости и смертности, Центры по контролю и профилактике заболеваний (CDC), 1989 г., 38(22): 400–404.
- 56.
Бергхофер А., Пишон Т., Рейнхольд Т., Аповян К.М., Шарма А.М., Виллих С.Н. Распространенность ожирения с европейской точки зрения: систематический обзор. Общественное здравоохранение BMC. 2008;8(200). https://doi.org/10.1186/1471-2458-8-200.
- 57.
Флегал К., Кэрролл М., Огден С., Кертин Л.Распространенность и тенденции ожирения среди взрослого населения США, 1999–2008 гг. ДЖАМА. 2010;303(3):235–41.
КАС пабмед Статья ПабМед Центральный Google Scholar
- 58.
Flegal KM, Carroll MD, Kit BK, Ogden CL. Распространенность ожирения и тенденции распределения индекса массы тела среди взрослого населения США, 1999-2010 гг. ДЖАМА. 2012;307(5):491–7.
ПабМед Статья ПабМед Центральный Google Scholar
- 59.
Flegal KM, Carroll MD, Ogden CL, Johnson CL. Распространенность и тенденции ожирения среди взрослого населения США, 1999–2000 гг. ДЖАМА. 2002; 288 (14): 1723–1727.
Артикул Google Scholar
- 60.
Огден С.Л., Кэрролл М.Д., Кертин Л.Р., Макдауэлл М.А., Табак С.Дж., Флегал К.М. Распространенность избыточного веса и ожирения в США, 1999–2004 гг. ДЖАМА. 2006; 295(13):1549–55.
КАС пабмед Статья Google Scholar
- 61.
Ogden CL, Carroll MD, Kit BK, Flegal KM. Распространенность детского и взрослого ожирения в США, 2011–2012 гг. ДЖАМА. 2014;311(8):806–14.
КАС пабмед ПабМед Центральный Статья Google Scholar
- 62.
Вричелла Л.К. Новое понимание и измерение увеличения объема плазмы во время беременности. Am J Clin Nutr. 2017; 106 (Прил.): 1620S–5S.
ПабМед ПабМед Центральный Статья Google Scholar
- 63.
Мэтьюз Т.Дж., Гамильтон, Б.Э. Количество первых родов у пожилых женщин продолжает расти. Краткий обзор данных NCHS. 2014;(152):1–8.
- 64.
Мэтьюз Т.Дж., Гамильтон, Б.Э. Возрастает средний возраст матерей: 2000-2014 гг. Краткий обзор данных NCHS. 2016; 232 (январь): 1–8.
Google Scholar
- 65.
Гернанд А.Д., Кристиан П., Шульце К.Дж., Шейх С., Лабрик А.Б., Шамим А.А., Уэст К.П. Младший. Состояние питания матери на ранних сроках беременности связано с изменениями объема воды и плазмы в организме беременных в сельской местности Бангладеш.

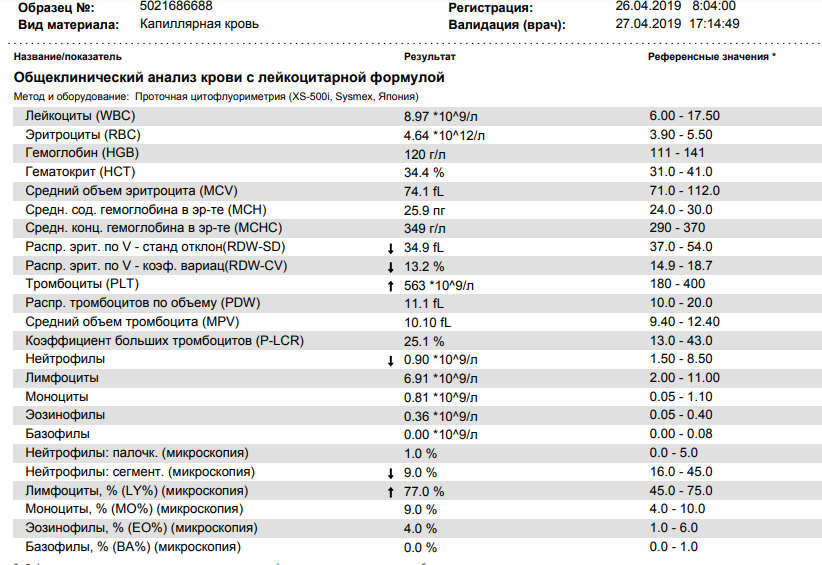
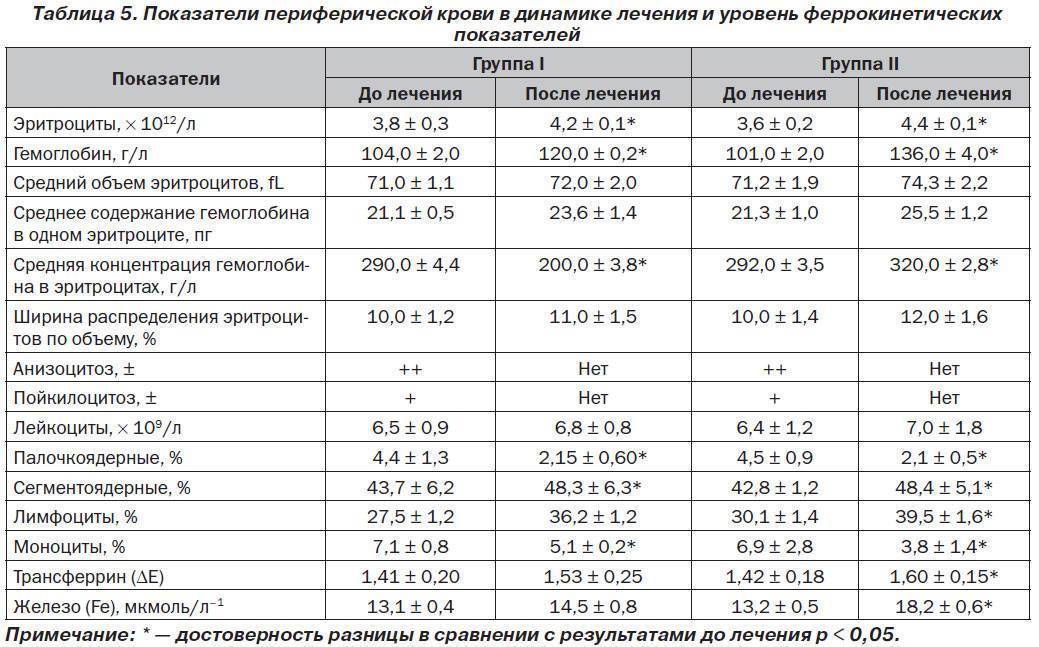
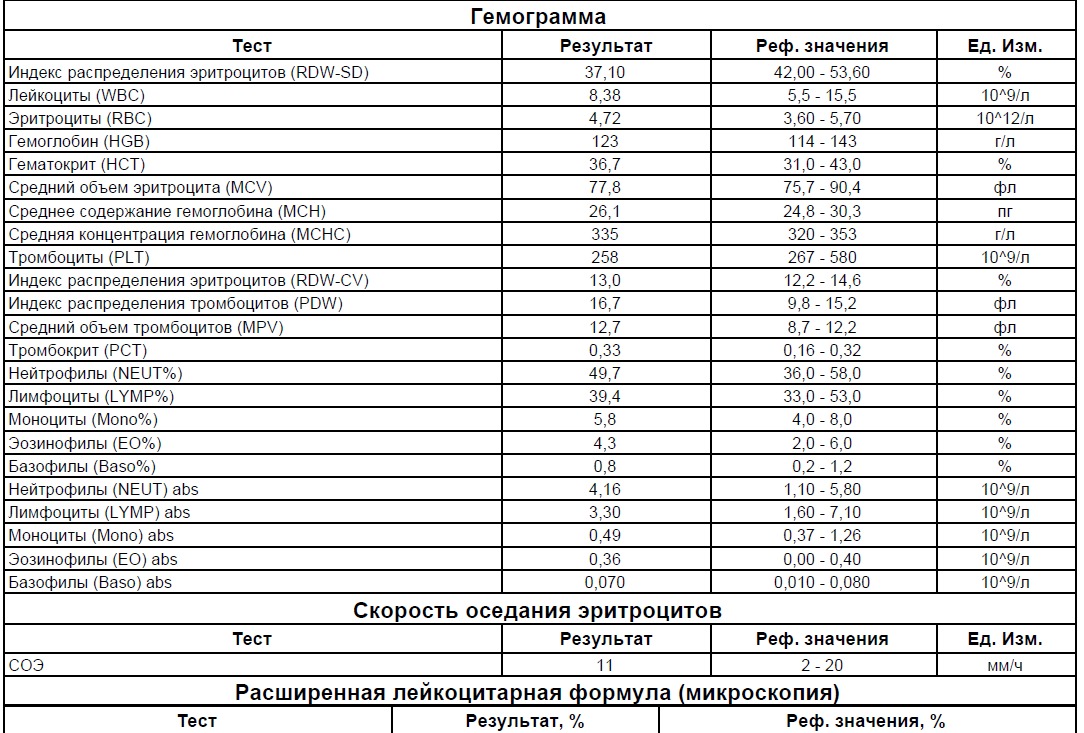 Эта цифра обозначает количество данных клеток в крови человека. При обнаружении в этом показателе отклонений врач может назначить повторное обследование.
Эта цифра обозначает количество данных клеток в крови человека. При обнаружении в этом показателе отклонений врач может назначить повторное обследование.
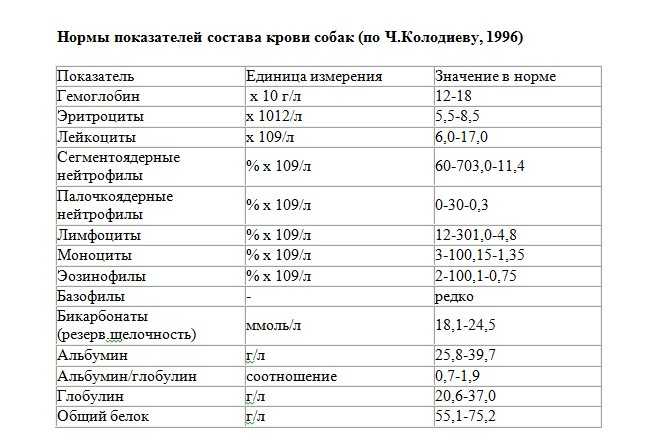
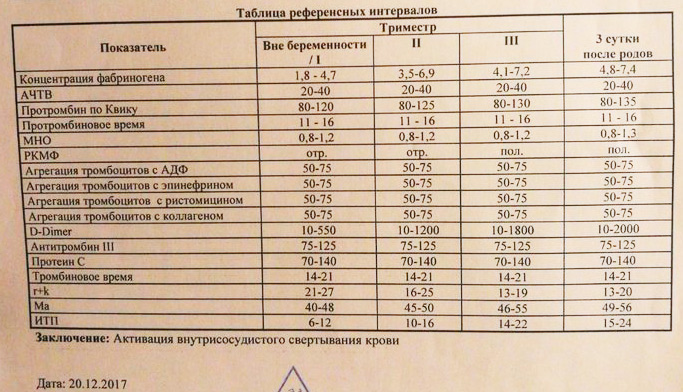 Количество тромбоцитов в периферической крови увеличивается при пневмонии, сепсисе, остеомиелите, а также после хирургических вмешательств и травм. При системных воспалительных заболеваниях соединительной ткани, например при
Количество тромбоцитов в периферической крови увеличивается при пневмонии, сепсисе, остеомиелите, а также после хирургических вмешательств и травм. При системных воспалительных заболеваниях соединительной ткани, например при 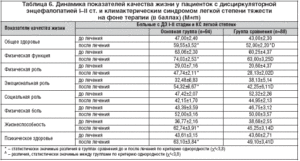

 в сутки.
в сутки.
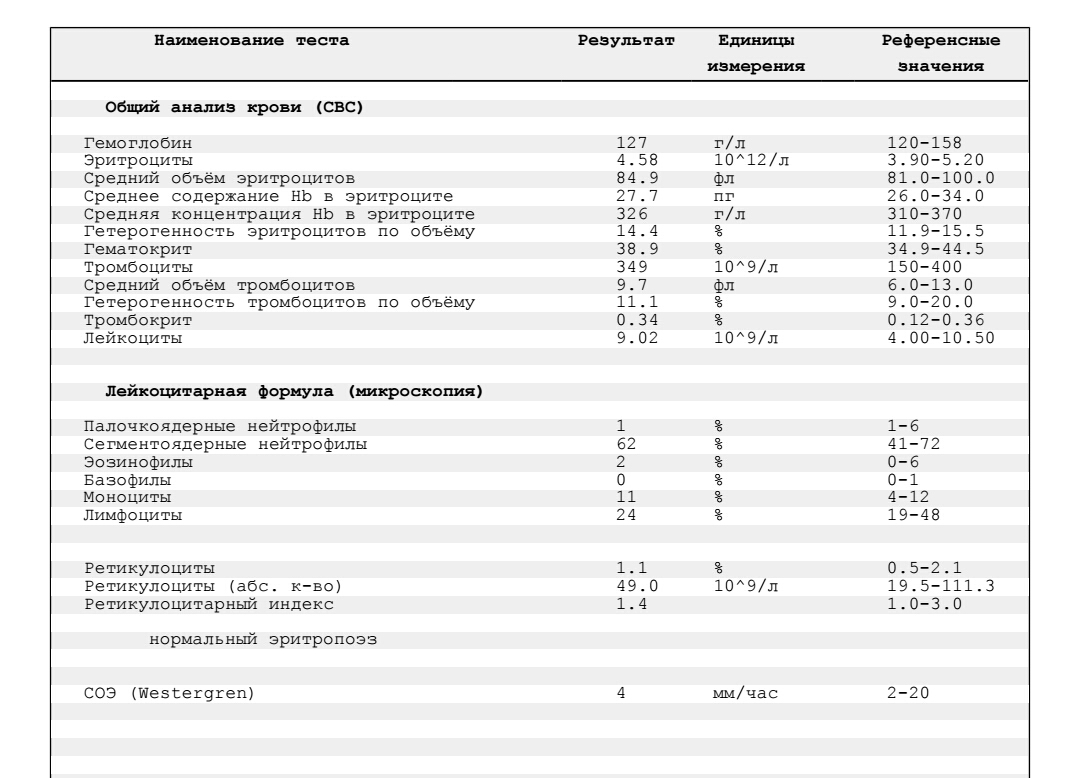
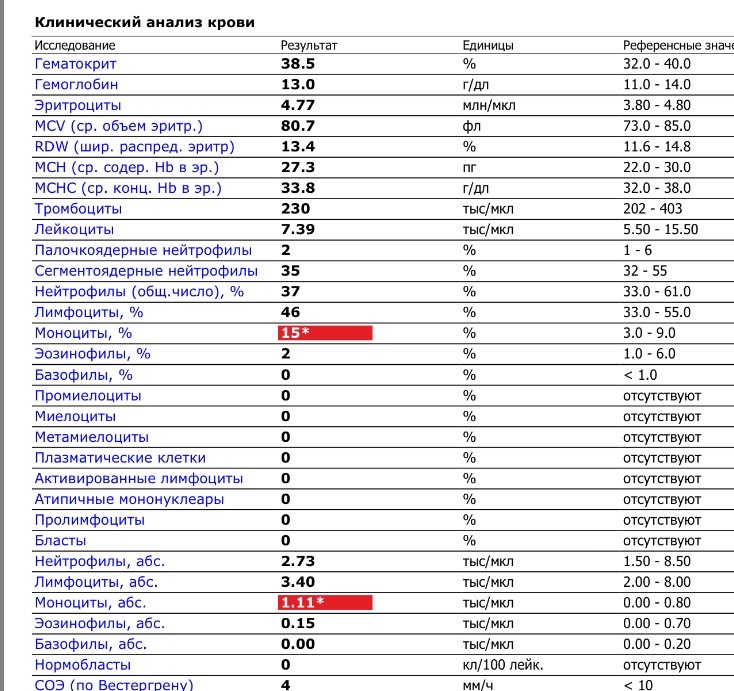
 Однако остается неизвестным, может ли количество тромбоцитов влиять и отражать выживаемость плода на ранних сроках беременности. Мы предполагаем, что аномальный MPV сам по себе или вместе с измененным количеством тромбоцитов связан с ранней гибелью плода.
Однако остается неизвестным, может ли количество тромбоцитов влиять и отражать выживаемость плода на ранних сроках беременности. Мы предполагаем, что аномальный MPV сам по себе или вместе с измененным количеством тромбоцитов связан с ранней гибелью плода. Мы стремимся оценить, связаны ли аномальные количества тромбоцитов с повышенным риском ранней гибели плода.
Мы стремимся оценить, связаны ли аномальные количества тромбоцитов с повышенным риском ранней гибели плода. г. отслойка плаценты, предлежание плаценты или приращение плаценты). Ранее существовавшие нарушения, которые считались связанными с тромбоцитопенией, были зарегистрированы как иммунная тромбоцитопеническая пурпура, системная красная волчанка, вирус иммунодефицита человека и гепатит B или C.
г. отслойка плаценты, предлежание плаценты или приращение плаценты). Ранее существовавшие нарушения, которые считались связанными с тромбоцитопенией, были зарегистрированы как иммунная тромбоцитопеническая пурпура, системная красная волчанка, вирус иммунодефицита человека и гепатит B или C.
 Затем мы попытались оценить связь между риском ранней гибели плода и наличием высокого количества тромбоцитов, используя бинарную логистическую регрессию, оцененную с помощью теста Хосмера-Лемешоу, чтобы принять модели.Все неколлинеарные переменные с p < 0,25 в однофакторном анализе были включены в модель многомерной регрессии. Мы рассчитали отношение шансов (ОШ) с 95% доверительным интервалом (95% ДИ) для основных факторов риска ранней гибели плода. Кроме того, производительность модели оценивалась с помощью 10-кратной перекрестной проверки путем случайного распределения субъектов исследования и связанных с ними данных в 10 дополнительных наборах данных. Девять наборов данных использовались в качестве обучающего набора, а оставшиеся использовались в качестве проверочного набора.Кривые характеристики оператора-приемника (ROC) (AUC) из всех прогонов тестирования, каждая точка которых соответствует конкретным значениям истинно положительного уровня (чувствительности) и истинно отрицательного уровня (специфичности), усреднялись и сообщались.
Затем мы попытались оценить связь между риском ранней гибели плода и наличием высокого количества тромбоцитов, используя бинарную логистическую регрессию, оцененную с помощью теста Хосмера-Лемешоу, чтобы принять модели.Все неколлинеарные переменные с p < 0,25 в однофакторном анализе были включены в модель многомерной регрессии. Мы рассчитали отношение шансов (ОШ) с 95% доверительным интервалом (95% ДИ) для основных факторов риска ранней гибели плода. Кроме того, производительность модели оценивалась с помощью 10-кратной перекрестной проверки путем случайного распределения субъектов исследования и связанных с ними данных в 10 дополнительных наборах данных. Девять наборов данных использовались в качестве обучающего набора, а оставшиеся использовались в качестве проверочного набора.Кривые характеристики оператора-приемника (ROC) (AUC) из всех прогонов тестирования, каждая точка которых соответствует конкретным значениям истинно положительного уровня (чувствительности) и истинно отрицательного уровня (специфичности), усреднялись и сообщались. Все зарегистрированные значения были двусторонними, и p < 0,05 считались статистически значимыми.
Все зарегистрированные значения были двусторонними, и p < 0,05 считались статистически значимыми.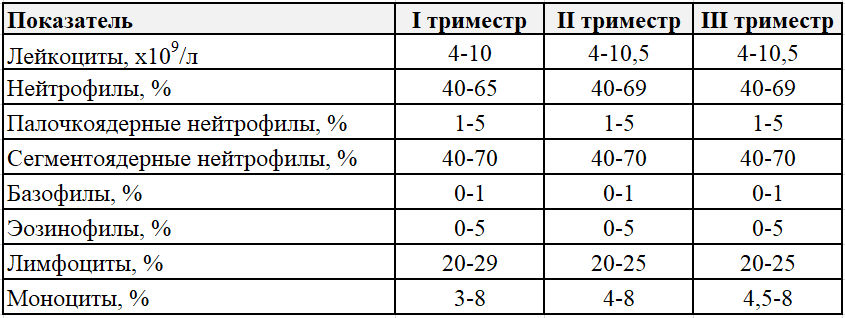 Исходные значения MPV и количества тромбоцитов, полученные у женщин с нормальными родами и у женщин с диагнозом ранней гибели плода, показаны в таблице 1. Мы наблюдали высокую частоту ранней гибели плода на 8-й неделе беременности.
Исходные значения MPV и количества тромбоцитов, полученные у женщин с нормальными родами и у женщин с диагнозом ранней гибели плода, показаны в таблице 1. Мы наблюдали высокую частоту ранней гибели плода на 8-й неделе беременности.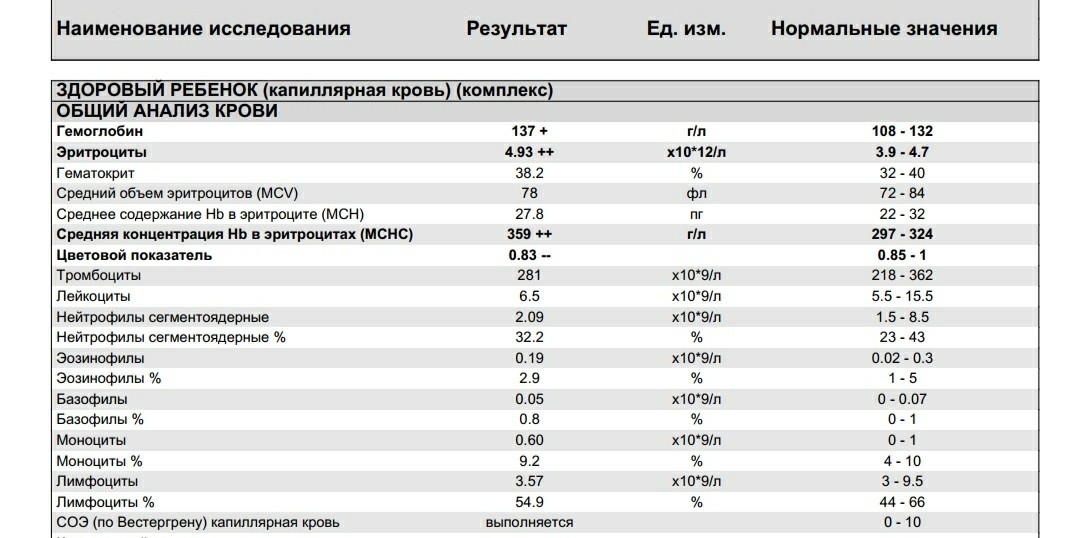 Сто семьдесят данных от оставшихся 425 женщин с неосложненной беременностью подходили для нашего исследования и сравнивались с данными от 99 женщин с выявленной ранней гибелью плода. В таблице 1 показаны исходные характеристики этих женщин в группах с нормальными родами и ранней гибелью плода.
Сто семьдесят данных от оставшихся 425 женщин с неосложненной беременностью подходили для нашего исследования и сравнивались с данными от 99 женщин с выявленной ранней гибелью плода. В таблице 1 показаны исходные характеристики этих женщин в группах с нормальными родами и ранней гибелью плода.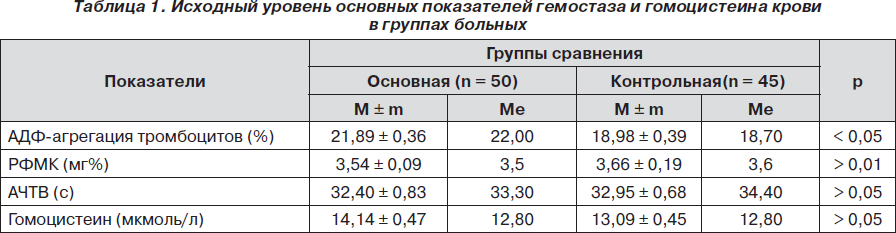 013). Тем не менее, не было существенной разницы MPV между группой с ранней гибелью плода и группой нормальных родов (9,30 fL против 9,25 fL, p = 0,802). Интересно, что результаты теста VerifyNow продемонстрировали более высокую функцию тромбоцитов в группе с нормальными родами (650 ARU), чем в группе с ранней гибелью плода (579 ARU) ( p = ).001) (рис. 2(в)).
013). Тем не менее, не было существенной разницы MPV между группой с ранней гибелью плода и группой нормальных родов (9,30 fL против 9,25 fL, p = 0,802). Интересно, что результаты теста VerifyNow продемонстрировали более высокую функцию тромбоцитов в группе с нормальными родами (650 ARU), чем в группе с ранней гибелью плода (579 ARU) ( p = ).001) (рис. 2(в)).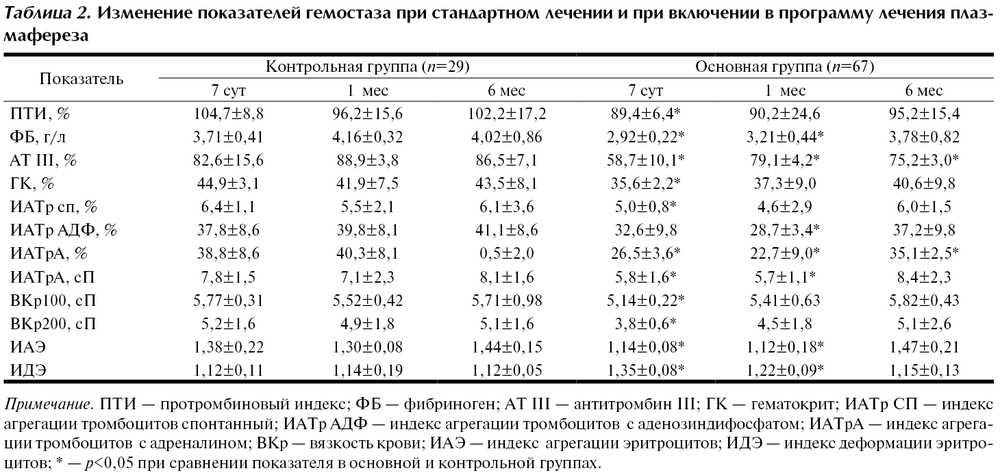 Следовательно, мы попытались оценить связь между риском ранней гибели плода и высоким уровнем тромбоцитов. Все неколлинеарные значимые однофакторные предикторы ранней гибели плода были включены в многопараметрический регрессионный анализ (таблица 2).Наши результаты показали, что высокий уровень тромбоцитов (>231 × 10 9 на литр) был независимо связан с повышенным риском ранней гибели плода с ОШ 2,075 (95% ДИ, 1,215–3,544; p = ,008). ). Более того, в бинарной логистической регрессии с использованием моделей прямой, обратной и пошаговой селекции высокое количество тромбоцитов, паритет и предшествующий выкидыш оставались значимо связанными с ранней гибелью плода. Для оценки общей производительности модели была проведена 10-кратная перекрестная проверка.Средняя точность и точность 10 раз были 66,59% и 56,80% соответственно. Как показано на рисунке 3, среднее значение AUC достигло 0,68.
Следовательно, мы попытались оценить связь между риском ранней гибели плода и высоким уровнем тромбоцитов. Все неколлинеарные значимые однофакторные предикторы ранней гибели плода были включены в многопараметрический регрессионный анализ (таблица 2).Наши результаты показали, что высокий уровень тромбоцитов (>231 × 10 9 на литр) был независимо связан с повышенным риском ранней гибели плода с ОШ 2,075 (95% ДИ, 1,215–3,544; p = ,008). ). Более того, в бинарной логистической регрессии с использованием моделей прямой, обратной и пошаговой селекции высокое количество тромбоцитов, паритет и предшествующий выкидыш оставались значимо связанными с ранней гибелью плода. Для оценки общей производительности модели была проведена 10-кратная перекрестная проверка.Средняя точность и точность 10 раз были 66,59% и 56,80% соответственно. Как показано на рисунке 3, среднее значение AUC достигло 0,68.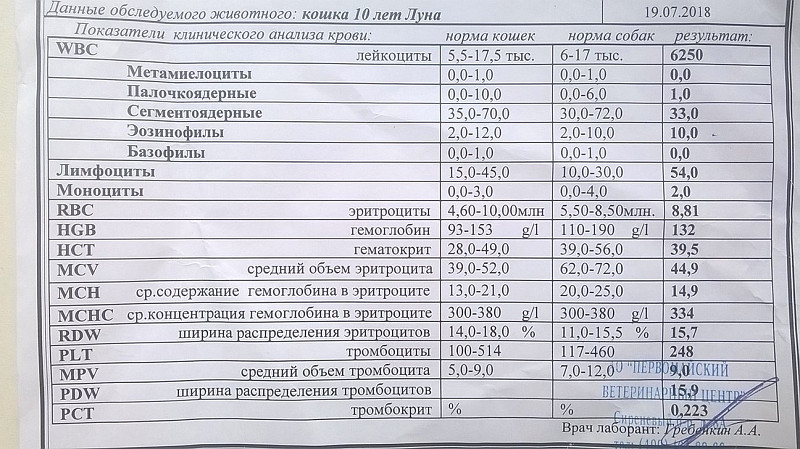 Диагностическая эффективность высокого количества тромбоцитов, паритета и невынашивания беременности.Площадь под кривой (AUC) составила 0,68 ± 0,15.
Диагностическая эффективность высокого количества тромбоцитов, паритета и невынашивания беременности.Площадь под кривой (AUC) составила 0,68 ± 0,15.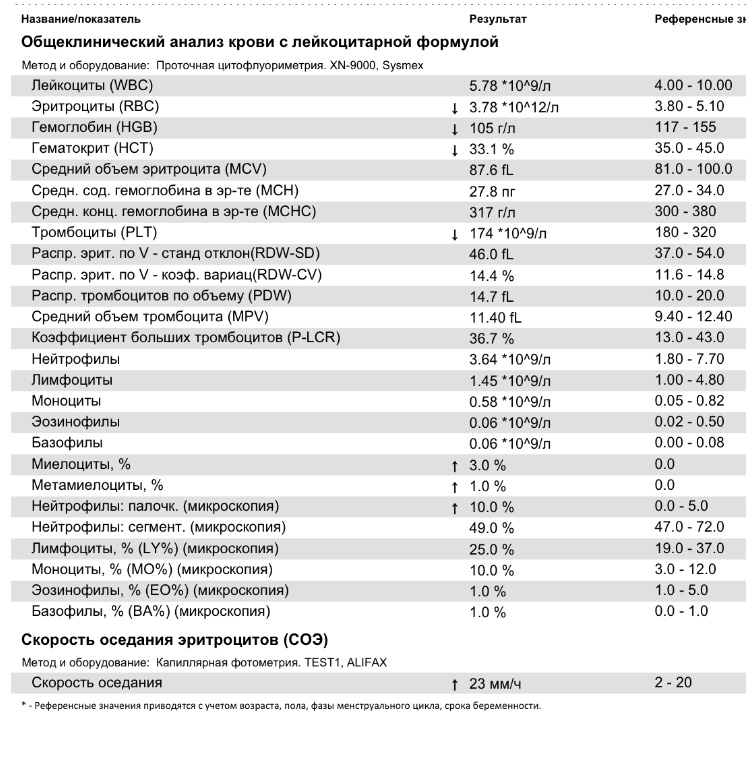 Следовательно, раннее прогнозирование риска ранней гибели плода повысит эффективность репродукции человека.В настоящее время не существует надежного биомаркера или индекса для прогнозирования ранней гибели плода. Здесь мы сообщаем, что высокий уровень тромбоцитов после пропущенной менструации коррелирует с риском ранней гибели плода.
Следовательно, раннее прогнозирование риска ранней гибели плода повысит эффективность репродукции человека.В настоящее время не существует надежного биомаркера или индекса для прогнозирования ранней гибели плода. Здесь мы сообщаем, что высокий уровень тромбоцитов после пропущенной менструации коррелирует с риском ранней гибели плода. Интересно, что количество тромбоцитов в группе ранней гибели плода выше, чем в группе нормальных родов.По сравнению с количеством тромбоцитов на 5–10-й неделе беременности у нормально родивших женщин высокие уровни количества тромбоцитов повышают риск ранней гибели плода.
Интересно, что количество тромбоцитов в группе ранней гибели плода выше, чем в группе нормальных родов.По сравнению с количеством тромбоцитов на 5–10-й неделе беременности у нормально родивших женщин высокие уровни количества тромбоцитов повышают риск ранней гибели плода.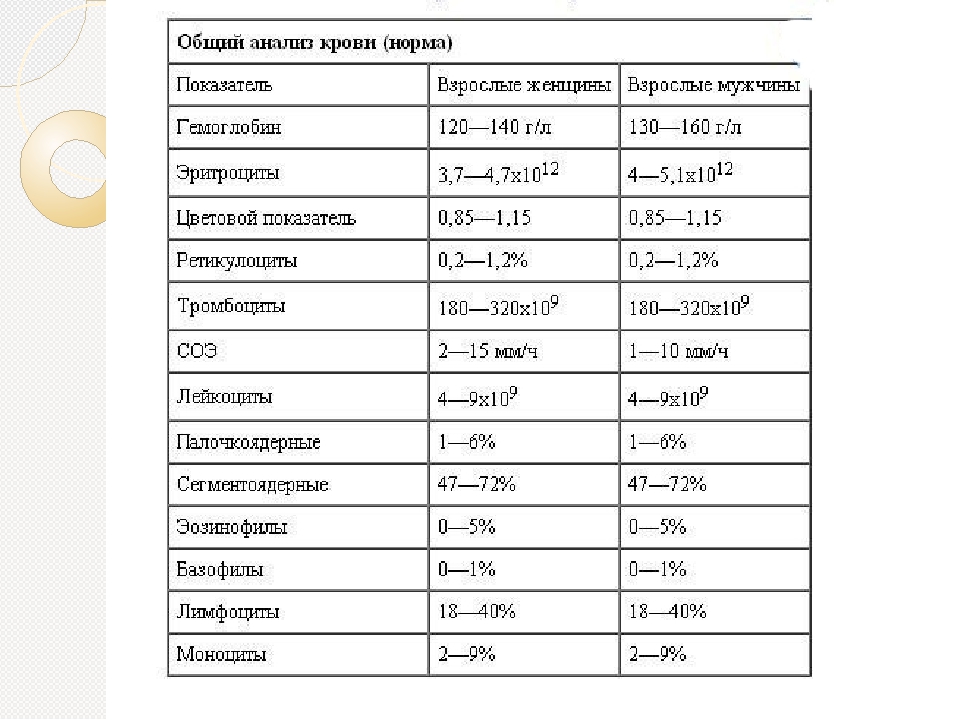
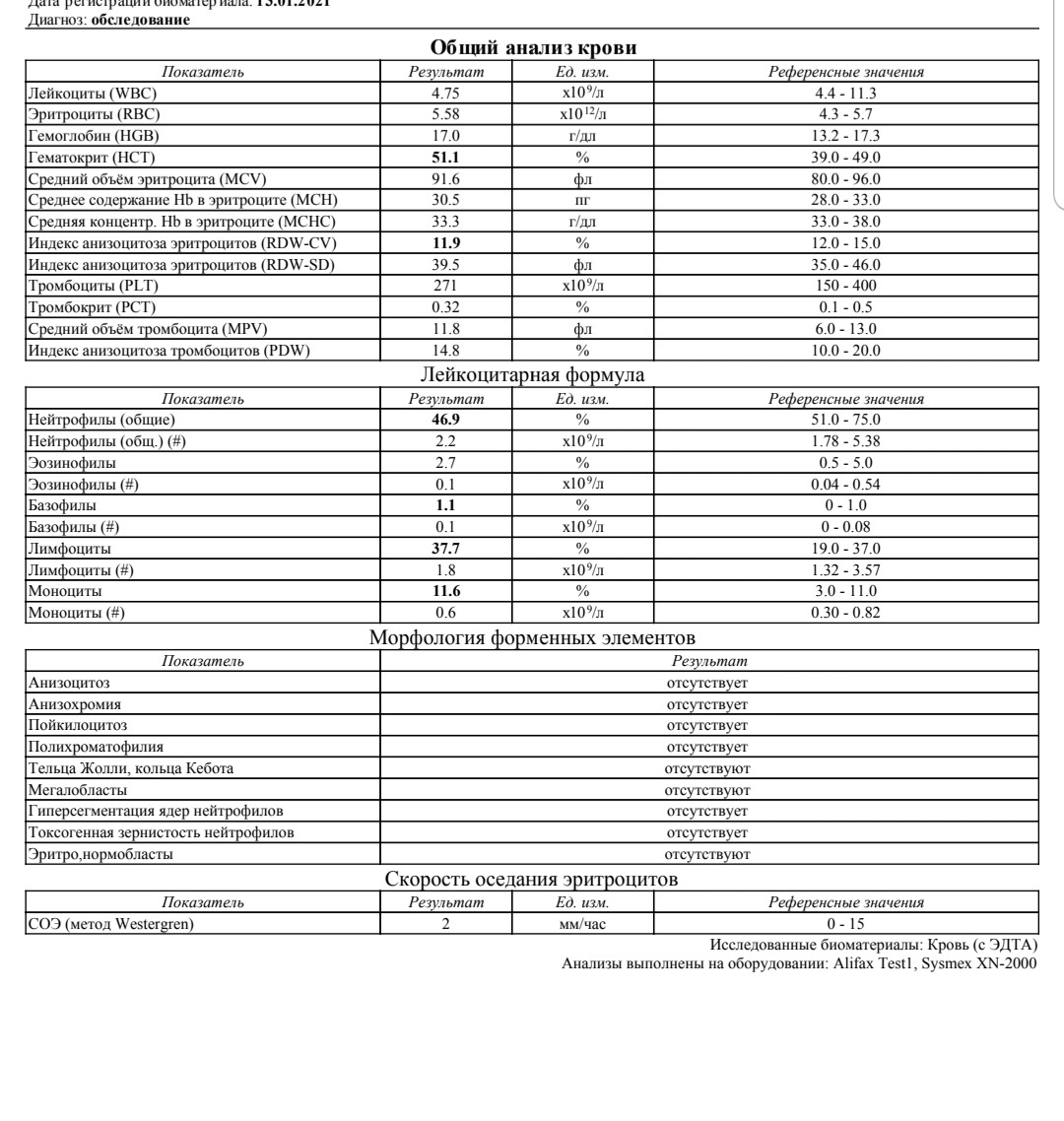 Хотя в нашем исследовании не было различий в MPV между ранней гибелью плода и нормальными родами, мы ожидаем подтверждения такой связи с проспективными исследованиями в будущем. Кроме того, сообщалось, что у одной женщины с эссенциальной тромбоцитемией развилось массивное внутрибрюшное кровотечение после трансвагинального извлечения ооцитов для оплодотворения in vitro (ЭКО) [32].Поэтому следует приложить усилия для оценки функции тромбоцитов перед ЭКО. Ранний мониторинг и лечение всех сопутствующих факторов риска могут быть немедленно осуществлены и иметь положительный эффект, поскольку пациенты с высоким уровнем тромбоцитов могут быть легко идентифицированы во время рутинного гематологического анализа.
Хотя в нашем исследовании не было различий в MPV между ранней гибелью плода и нормальными родами, мы ожидаем подтверждения такой связи с проспективными исследованиями в будущем. Кроме того, сообщалось, что у одной женщины с эссенциальной тромбоцитемией развилось массивное внутрибрюшное кровотечение после трансвагинального извлечения ооцитов для оплодотворения in vitro (ЭКО) [32].Поэтому следует приложить усилия для оценки функции тромбоцитов перед ЭКО. Ранний мониторинг и лечение всех сопутствующих факторов риска могут быть немедленно осуществлены и иметь положительный эффект, поскольку пациенты с высоким уровнем тромбоцитов могут быть легко идентифицированы во время рутинного гематологического анализа.